Screening op Osteoporose en fractuurpreventie
Uitgangsvraag
De module omvat de volgende deelvragen:
- Wanneer is er bij mensen met epilepsie die anti-aanvalsmedicatie gebruiken sprake van verhoogd fractuurrisico; wanneer is er een indicatie voor aanvullend onderzoek en behandeling?
- Wat is het effect van vitamine D suppletie (met of zonder calcium suppletie) op (normalisatie van) vitamine D (25OHD) spiegels, botmineraaldichtheid (BMD) en fracturen bij personen met anti-epileptica gebruik?
Voor uitgangsvraag 1 wordt verwezen naar het onderdeel ‘Personen ≥ 60 jaar met risicofactoren voor een fractuur, zonder recente fractuur en zonder gebruik van glucocorticoïden’ in module 2 van de multidisciplinaire richtlijn (MDR) osteoporose en fractuurpreventie:
Verricht bij mannen en vrouwen ≥ 60 jaar met een fractuurrisicoscore van ≥ 4 punten (zie risicofactoren scorelijst) aanvullend onderzoek conform modules:
- Meerwaarde van aanvullende vertebral fracture assessment (VFA) bij diagnostiek met DXA
- Welk laboratoriumonderzoek bij verhoogd fractuurrisico
- Inschatting valrisico en interventies
Voor de indicatiestelling en het starten met medicatie voor fractuurpreventie wordt verwezen naar module Indicatiestelling medicatie fractuurpreventie en module Starten medicatie voor fractuurpreventie van de MDR:
- Module Indicatiestelling medicatie fractuurpreventie
- Module Starten medicatie voor fractuurpreventie
Uitgangsvraag 2 wordt onderstaand in deze module uitgewerkt
Aanbeveling
Onderstaande aanbevelingen gelden voor mensen met epilepsie en anti-aanvalsmedicatiegebruik (dit is een risicofactor voor fracturen). Voor patiënten die geen ASM gebruiken, wordt verwezen naar de richtlijn Osteoporose en fractuurpreventie.
- Adviseer iedereen die anti-aanvalsmedicatie gebruikt om vitamine D (zelfzorgmedicatie) te gebruiken [zie tabel gezondheidsraad (2012) voor dosering].
- Dagdoseringen van meer dan 75µg (=3000IE) vitamine-D/dag en periodieke hoge doseringen van vitamine-D (zogenaamde bolus regimes ≥ 1500 µg (=60.000IE) vitamine-D per maand) worden afgeraden omdat zij mogelijk een verhoogd valrisico geven.
- Gebruik bij patiënten ≥ 60 jaar met epilepsie, die behandeld worden met anti-aanvalsmedicatie, de risicofactoren scorelijst (uit de multidisciplinaire richtlijn osteoporose en fractuurpreventie) voor het nemen van een beslissing over het verrichten van aanvullend onderzoek in het kader van fractuurrisico
- Overweeg bij patiënten < 50 jaar met (één of meerdere) wervelfracturen of een andere fractuur na een insult zonder ander duidelijk veroorzakend trauma, te bespreken met of te verwijzen naar een (lokale) osteoporose specialist om te bepalen of sprake is van een primaire of secundaire onderliggende oorzaak.
Overwegingen
Balans tussen gewenste en ongewenste effecten
Er zijn drie studies gevonden die het effect van vitamine D suppletie onderzochten bij kinderen met epilepsie die anti-aanvalsmedicatie gebruikten. Er zijn geen studies gevonden die dit effect onderzochten bij volwassenen.
Geen van de studies beschreef de cruciale uitkomstmaten botmineraaldichtheid en fracturen.
Wel beschreven alle studies het effect van de interventie op vitamine D serum spiegels (25OH vitamine D spiegel). Alle studies beschreven een hogere vitamine D spiegel én een lager aantal kinderen met vitamine D tekort in de groep met (hoge) vitamine D suppletie in vergelijking met de groep zonder suppletie of met een lagere dosis.
Er kunnen op basis van de gevonden resultaten geen conclusies worden getrokken over de effectiviteit van vitamine D suppletie bij kinderen en volwassenen op botmineraaldichtheid en fracturen. Hier ligt een kennislacune.
Voor het advies met betrekking tot vitamine D suppletie bij personen met een verhoogd fractuurrisico wordt verwezen naar de aanbevelingen over vitamine D suppletie in de multidisciplinaire richtlijn osteoporose en fractuurpreventie.
Voor het advies met betrekking tot vitamine D suppletie zonder verhoogd fractuurrisico wordt verwezen naar de aanbevelingen in het rapport van de gezondheidsraad (Gezondheidsraad, 2012).
Bij de groep van patiënten < 50 jaar met (meerdere) wervelfracturen of een andere fractuur na een insult (zonder ander duidelijk veroorzakend trauma), kan een primaire of secundaire onderliggende oorzaak een rol spelen. Hier kan aanvullend onderzoek ook geïndiceerd door een osteoporose specialist.
NB: Dagdoseringen van meer dan 75µg (=3000IE) vitamine-D/dag en periodieke hoge doseringen van vitamine-D (zogenaamde bolus regimes ≥ 1500 µg (=60.000IE) vitamine-D per maand) worden afgeraden omdat zij mogelijk een verhoogd valrisico geven. (Zie multidisciplinaire richtlijn osteoporose en fractuurpreventie module: Inname calcium en vitamine D bij verhoogd fractuur risico).
Kwaliteit van bewijs
Er is geen bewijs gevonden voor de cruciale uitkomstmaten. Dit betekent dat we geen informatie hebben over het effect op de cruciale uitkomstmaten.
De kwaliteit van bewijs voor de belangrijke uitkomstmaat vitamine D serum spiegel is zeer laag. Er is afgewaardeerd vanwege zeer ernstige Risk of Bias: methodologische beperkingen door verschil in baselinescores tussen groepen en hoge studie uitval en vanwege imprecisie: onnauwkeurigheid omdat het betrouwbaarheidsinterval de grens van klinische relevantie overschrijdt.
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
Voorlichting
Voor patiënten met epilepsie die anti-aanvalsmedicatie gebruiken (en eventueel hun verzorgers) is het relevant dat zij op de hoogte zijn dat er sprake kan zijn van een verhoogd fractuurrisico vanwege het gebruik van anti-aanvalsmedicatie in combinatie met andere potentiële risicofactoren zoals bij voorbeeld een verhoogd valrisico. De zorgverlener en de patiënten kunnen voor het inschatten van dit risico gebruik maken van de risicofactoren scorelijst.
De in de multidisciplinaire richtlijn osteoporose en fractuurpreventie voorgestelde Risicofactoren scorelijst maakt op een schematische wijze duidelijk welke risicofactoren van belang zijn en hoe de individuele factoren opgeteld kunnen worden tot een totaal aantal punten, en of aanvullend onderzoek aanbevolen wordt (≥ 4 punten) of niet.
Patiënten kunnen hiervoor gebruik maken van de Risicofactoren scorelijst op openbare websites zoals van de Osteoporose Vereniging.
Neem de scorelijst met de patiënt door en geef uitleg bij de verschillende factoren die specifiek van belang zijn. Bedenk dat de term ”fractuurrisico” voor de meeste patiënten geen gangbaar begrip is en dat ook percentages daar weinig aan toevoegen.
Fractuurpreventie zal voor iemand met een recente eenvoudige breuk weinig urgentie oproepen zonder nadere uitleg over het verhoogde risico’s op een nieuwe fractuur en in het bijzonder op ernstige fracturen zoals heup en wervelfracturen.
Behandeling
Voor patiënten (en eventueel hun verzorgers) is het relevant dat zij goed geïnformeerd zijn over de reden van behandeling (de mate waarin fractuurpreventie bereikt kan worden), de eventuele bijwerkingen, de duur van de behandeling en hoe dit zal worden opgevolgd. Een actief betrokken en goed geïnformeerde patiënt heeft betere kansen voor een optimaal ‘disease management’. Voor patiënten die structureel worden geëvalueerd (dus die weten wanneer er een evaluatie moment volgt, hoe dat gedaan wordt en welke factoren een rol spelen bij deze evaluatie) kunnen zelfzorgvaardigheden worden vergroot en ervoor zorgen dat patiënten fractuurpreventieve zorg krijgen die aansluit bij hun behoeften en mogelijkheden, op het juiste moment, in de juiste vorm en gericht op eigen regie over hun gezondheid.
Spiegelcontrole
Er bestaat geen consensus over de toegevoegde waarde van regelmatige spiegelcontroles van 25-OH vitamine D (70% van Nederlanders is in wintermaanden vitamine D deficiënt). De werkgroep is van mening dat het dus niet zinnig is om 25-OH vitamine D spiegels te controleren bij mensen met epilepsie. Maar als je wil doseren op basis van spiegels, kun je overwegen om alsnog de spiegel te controleren.
Kostenaspecten
- Voor de kosten van medicamenteuze behandeling met medicatie voor fractuurpreventie wordt verwezen naar de multidisciplinaire richtlijn osteoporose en fractuurpreventie.
- Vitamine D suppletie: Op advies van Zorginstituut Nederland is besloten dat vitamine D sinds 2023 niet meer vergoed wordt via de zorgverzekering, vanwege de relatief lage kosten en omdat het makkelijk is om vitamine D te kopen.
Vanwege de lage kosten van vitamine D suppletie en de in verhouding daarmee relatief dure Vitamine D lab bepaling (± € 10,-) is het te overwegen om laagdrempelig vitamine D te suppleren conform de aanbevelingen in de multidisciplinaire osteoporose en fractuurpreventie en de gezondheidsraad.
Gelijkheid ((health) equity/equitable)
Met betrekking tot de suppletie van vitamine D kan vermeld worden dat de werkgroep gelet op de lage kosten van Vitamine D tabletten geen problemen voorziet in de haalbaarheid aanvaardbaarheid en implementatie van het advies om laagdrempelig vitamine D te suppleren
Duurzaamheid
Bij de interventie spelen duurzaamheidsaspecten geen rol.
Haalbaarheid
De interventie en diagnostiek lijkt haalbaar.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Er is geen bewijs voor het effect van vitamine D suppletie in vergelijking met placebo op BMD of op het fractuurrisico bij personen met epilepsie die behandeld worden met anti-aanvalsmedicatie. De kwaliteit van bewijs voor het effect van vitamine D suppletie op serum vitamine D spiegels level bij volwassen personen met epilepsie die behandeld worden met anti-aanvalsmedicatie is afwezig en bij kinderen is het bewijs zeer laag.
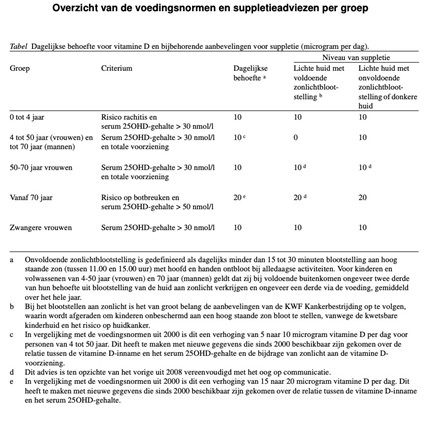
Om die reden worden de aanbevelingen voor vitamine D uit de multidisciplinaire richtlijn multidisciplinaire richtlijn osteoporose en fractuurpreventie en de gezondheidsraad (Gezondheidsraad, 2012) aangehouden. Figuur 1 geeft de adviezen voor suppletie van de gezondheidsraad weer.
Figuur 1. Overzicht van de voedingsnormen en suppletieadviezen per groep
bron: Gezondheidsraad (2012)
Onderbouwing
In the Dutch multidisciplinary guideline osteoporosis and fracture prevention, a systematic review of the literature was performed to answer the following question: Which tools have the best predictive accuracy to identify individuals at high risk of fracture?
Ideally, studies investigating the clinical impact of using a tool would have been included. This clinical impact should be defined as the percentage of patients undergoing additional fracture risk assessment by bone density testing in whom medical treatment is started based on the outcomes of this assessment (high fracture risk).
However, in the MDR, the identification of patients at high fracture risk is the first step to select patients for additional assessment (modules “Meerwaarde van aanvullende vertebral fracture assessment bij diagnostiek met DXA”, “Aanvullend laboratoriumonderzoek”, “Aanvullend onderzoek-Valrisicoschatting”). For men and women ≥ 60 years we have decided to use the Dutch Fracture risk score and defined a score ≥ 4 point as a cutoff for increased risk of fractures.
This risk score can be applied for people with epilepsy who use anti-seizure medication, as this group scores 1 risk point according to the Dutch Fracture risk score.
The impact of vitamin D supplements on vitamin D levels, bone mineral density (BMD), and fractures in people with epilepsy using anti-seizure medications is not well understood. To address these knowledge gaps, a systematic review of the literature was conducted.
|
Outcome Timeframe |
Study results and measurements |
Absolute effect estimates |
Certainty of the evidence (Quality of evidence) |
Summary |
|
Bone mineral density (crucial)
|
-
|
- |
No GRADE (no evidence was found)
|
No evidence was found regarding the effect of vitamin D supplementation on bone mineral density when compared with placebo in patients with epilepsy using anti-seizure medication. |
|
Fractures (crucial)
|
- |
- |
No GRADE (no evidence was found)
|
No evidence was found regarding the effect of vitamin D supplementation on fractures when compared with placebo in patients with epilepsy using anti-seizure medication. |
|
Vitamine D Status (important)
|
Relative risk [95% CI]
|
Due to the differences in inclusion criteria and in cut-off values for deficiency, results were not pooled. |
Very low GRADE Due to very serious risk of bias, Due to serious imprecision4 |
The evidence is very uncertain about the effect of vitamin D supplementation on vitamin D status when compared with placebo in children with epilepsy using anti-seizure medication. (Mishra, 2023; Vichutavate, 2022; Viraraghavan (2018)) |
|
Vitamine D Level (important)
|
Measured by: serum 25 (OH)D level data from 82 participants in 3 studies |
Due to the differences in inclusion criteria and in cut-off values for deficiency, results were not pooled. |
Very low GRADE Due to very serious risk of bias, Due to serious imprecision4 |
The evidence is very uncertain about the effect of vitamin D supplementation on serum 250 (OH)D level when compared with placebo in children with epilepsy using anti-seizure medication. (Mishra, 2023; Vichutavate, 2022; Viraraghavan (2018)) |
1 Viraraghavan (2018) 2 Vichutavate (2022) 3Mishra (2023) 4Risk of Bias: very serious. Missing intention-to-treat analysis; baseline differences in favor of effect; Imprecision: serious. Wide confidence intervals
Description of studies
A total of three studies were included in the analysis of the literature. Important study characteristics and results are summarized in table 1. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Three RCTs reported on the effectiveness of vitamin D supplementation in children using anti-seizure medication (Mishra, 2023; Vichutavate, 2022 and Viraraghavan, 2019). Vichutavate (2022) compared high with standard dose of vitamin D supplementation, whereas the other two studies compared vitamin D supplementation with no supplementation (Mishra, 2023 and Viraraghavan, 2019).
Doses of the vitamin D supplementation in the intervention differed greatly: from 600 IU daily (Mishra, 2023) to 60.000 IU/monthly (Viraraghavan, 2019) to 60.000 IU every 10 days (Vichutavate, 2022).
Inclusion age ranged from two (Mishra, 2023), to 18 years of age (Vichutavate, 2022). Mishra (2023) included children with vitamin D levels above 20 ng/ml whereas Vichutavate (2022) only included children with vitamin D levels below 30 ng/ml. Viraraghavan (2019) did not set an inclusion criterium for vitamin D level. Two studies included children that started on anti-seizure medication (Mishra, 2023; Viraraghavan, 2019) whereas Vichutavate (2022) included children who had been using anti-seizure medication for over 6 months.
No studies were found that reported on vitamin D supplementation in adults using anti-seizure medication.
Table 1. Characteristics of included studies
*For further details, see risk of bias table in the appendix
Results
1. Bone mineral density (crucial), Fractures (crucial)
No studies reported on the crucial outcome measures bone mineral density or fractures.
2. Vitamin D levels (important)
2.1 Serum (OH)D levels
All studies reported on serum (OH)D levels. Results were not pooled due to the differences in inclusion criteria of studies and differences in vitamin D dosage in the intervention group.
Viraraghavan (2018) report a GM [95% CI] serum 25(OH) D at 6 months follow-up of 25.7 [19.6 to 33.8] ng/ml in the group receiving vitamin D supplementation compared to a GM [95% CI] of 12.7 [9.3 to 17.5] ng/ml in the control group.
Vichutavate (2022) report a mean ± SD serum 25(OH)D level after 90 days of 39.0 ± 11.5 ng/ml in the high dose group compared to 27.5 ± 8.6 ng/ml in the low dose group.
Mishra (2023) report a median [IQR] serum vitamin D level after 90 days of 30.12 [28.7 to 32.36] for the group receiving Vitamin D supplementation compared to 19.75 [15.7 to 25.05] in the control group.
2.2 Vitamin D deficiency
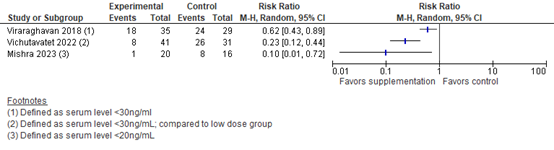
All studies reported on vitamin D deficiency levels. These results are presented in Figure 1. Due to the differences in inclusion criteria, dosage in the intervention group and cut-off values for deficiency, results were not pooled. All studies reported a higher percentage of vitamin D deficiency in the control group. The risk ratio was clinically relevant in all studies.
Figure 1. Vitamin D deficiency
A systematic review of the literature was performed to answer the following question:
What is the effectiveness of vitamin D supplementation with or without calcium supplementation on vitamin D levels (25OHD levels), bone mineral density (BMD) and fractures in people with epilepsy who use anti-seizure medication compared to no supplementation?
| Patients |
P1: Adults with epilepsy who use anti-seizure medication P2: Children with epilepsy who use anti-seizure medication |
| Intervention | Vitamin D supplementation |
| Control | No vitamin D supplementation or usual care |
| Outcomes | Bone Mineral Density; Fractures; Vitamin D levels (250HD levels) |
| Other selection criteria | Study design: systematic reviews and randomized controlled trials |
Relevant outcome measures
The guideline panel considered bone mineral density and fractures as a critical outcome measure for decision making; and vitamin D levels as an important outcome measure for decision making.
A priori, the guideline panel did not define the outcome measures listed above but used the definitions used in the studies. The guideline group considered a 25OHD ≥ 50 nmol/l (20 ng/ml) vitamin D level as a normal vitamin D level.
The guideline panel defined 25% (0.8 ≥ RR ≥ 1.25) for dichotomous outcomes, 0.5 SD for continuous outcomes and standardized mean difference (0.5 ≥ SMD ≥ 0.5) as minimal clinically (patient) important differences.
Search and select (Methods)
In 2012, the first version of this module was based on the Dutch guideline for osteoporosis and fractuurpreventie (Bergh, 2024). Studies from before this date were not included in the literature summary. After this date a yearly search of the literature was conducted to include relevant studies. For the current revision, we searched the databases Medline/Pubmed and Embase with relevant search terms from 01-01-2019 (last search) until 3-1-2024. The detailed search strategy is depicted under the tab Methods. The search was limited to systematic reviews and randomized controlled trials. The systematic literature search resulted in 237 articles. Additionally, we specifically searched for studies on vitamin D supplementation from inception until 8-8-2024. This search resulted in 44 studies, combining a total of 271 articles.
Studies were selected based on the following criteria:
- systematic review (searched in at least two databases, and detailed search strategy, risk of bias assessment and results of individual studies available) or randomized controlled trial;
- full-text English language publication;
- studies according to PICO.
Initially, seven studies were selected based on title and abstract screening. After reading the full text, four studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and three studies were included.
- van den Bergh JP, Geusens P, Appelman-Dijkstra NM, van den Broek HJG, Elders PJM, de Klerk G, van Oostwaard M, Willems HC, Zillikens MC, Lems WF. The Dutch multidisciplinary guideline osteoporosis and fracture prevention, taking a local guideline to the international arena. Arch Osteoporos. 2024 Apr 2;19(1):23. doi: 10.1007/s11657-024-01378-3. PMID: 38564062; PMCID: PMC10987374.
- Gezondheidsraad. Evaluatie van de voedingsnormen voor vitamine D. Den Haag: Gezondheidsraad, 2012; publicatienr. 2012/15. Evaluatie van de voedingsnormen voor vitamine D | Advies | Gezondheidsraad
- Mishra S, Mishra D, Mahajan B, Mantan M, Khan AM. Effect of Daily Vitamin D Supplementation on Serum Vitamin D Levels in Children with Epilepsy Receiving Sodium Valproate Monotherapy: A Randomized, Controlled Trial. Indian J Pediatr. 2023 May;90(5):450-456. doi: 10.1007/s12098-022-04225-w. Epub 2022 Jun 28. PMID: 35763213.
- Vichutavate S, Suwanpakdee P, Likasitthananon N, Numbenjapon N, Nabangchang C, Phatarakijnirund V. Standard and high dose ergocalciferol regimens for treatment of hypovitaminosis D in epileptic children and adolescents. J Pediatr Endocrinol Metab. 2022 Oct 4;35(11):1369-1376. doi: 10.1515/jpem-2022-0197. PMID: 36190481.
- Viraraghavan VR, Seth A, Aneja S, Singh R, Dhanwal D. Effect of high dose vitamin d supplementation on vitamin d nutrition status of pre-pubertal children on anti-epileptic drugs - A randomized controlled trial. Clin Nutr ESPEN. 2019 Feb;29:36-40. doi: 10.1016/j.clnesp.2018.11.007. Epub 2018 Nov 23. PMID: 30661698.
Risk of bias tables
Risk of bias table for intervention studies (randomized controlled trials; based on Cochrane risk of bias tool and suggestions by the CLARITY Group at McMaster University)
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated?
|
Was the allocation adequately concealed?
|
Blinding: Was knowledge of the allocated interventions adequately prevented? |
Was loss to follow-up (missing outcome data) infrequent?
|
Are reports of the study free of selective outcome reporting?
|
Was the study apparently free of other problems that could put it at a risk of bias?
|
Overall risk of bias
LOW Some concerns HIGH
|
|
Vichutavate, 2022 |
Probably yes;
Reason: block randomization. |
No information |
Definitely no;
Reason: the intervention group received more capsules compared to the control group |
Definitely yes;
Reason: no loss to follow-up |
Definitely yes;
Reason: All relevant outcomes were reported |
Definitely yes
Reason: no other problems noted |
LOW
Reason: lack of blinding likely does not affect outcome measures of calcium/vit D. |
|
Viraraghavan, 2019 |
Probably yes;
Reason: block randomization. |
Definitely yes;
Reason: allocation concealment was achieved using sequentially numbered opaque sealed envelopes |
Probably no;
Reason: no description of any placebo given |
Definitely no;
Reason: Loss to follow up was 17% in the intervention group and 29% in the control group. No ITT analysis was performed |
Definitely yes;
Reason: All relevant outcomes were reported |
Definitely no
Reason: baseline differences in outcome parameter in favor of the intervention |
HIGH
Reason: high loss to follow up without intention to treat analysis. Baseline differences in favor of reported outcome. |
|
Mishra, 2023 |
Probably yes;
Reason: permuted block randomization. |
|
Definitely no
Reason: nonblinded trial |
Probably yes;
Reason: loss to follow up was infrequent (4 out of 20) and only in the control group. Reasons for los to follow up are reported. |
Definitely yes;
Reason: All relevant outcomes were reported |
Definitely yes
Reason: no other problems noted |
LOW
Reason: lack of blinding and loss to follow up likely does not affect outcome measures of calcium/vit D. |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
LoPinto-Khoury C, Brennan L, Mintzer S. Impact of carbamazepine on vitamin D levels: A meta-analysis. Epilepsy Res. 2021 Dec;178:106829. doi: 10.1016/j.eplepsyres.2021.106829. Epub 2021 Nov 26. PMID: 34847425. |
Does not comply to PICO; Does not study the effect of Vitamin D supplementation. |
|
Xu Z, Jing X, Li G, Sun J, Guo H, Hu Y, Sun F, Wen X, Chen F, Wang T, Lu XP. Valproate decreases vitamin D levels in pediatric patients with epilepsy. Seizure. 2019 Oct;71:60-65. doi: 10.1016/j.seizure.2019.06.009. Epub 2019 Jun 11. PMID: 31207394. |
Does not comply to PICO; Comparison with healthy controls, and with patients not on VPA.
|
|
Lee RH, Lyles KW, Colón-Emeric C. A review of the effect of anticonvulsant medications on bone mineral density and fracture risk. Am J Geriatr Pharmacother. 2010 Feb;8(1):34-46. doi: 10.1016/j.amjopharm.2010.02.003. PMID: 20226391; PMCID: PMC3570810. |
Wrong study design: review of observational and cohort studies – not RCTs
|
|
Al Khalifah R, Hamad MH, Hudairi A, Al-Sulimani LK, Al Homyani D, Al Saqabi D, Bashiri FA. Prevalence and Related Risk Factors of Vitamin D Deficiency in Saudi Children with Epilepsy. Children (Basel). 2022 Nov 5;9(11):1696. doi: 10.3390/children9111696. PMID: 36360424; PMCID: PMC9688346. |
Wrong study design: prevalence study |
|
Wakeman M. A Literature Review of the Potential Impact of Medication on Vitamin D Status. Risk Manag Healthc Policy. 2021 Aug 14;14:3357-3381. doi: 10.2147/RMHP.S316897. PMID: 34421316; PMCID: PMC8373308. |
Wrong study design: descriptive study |
Beoordelingsdatum en geldigheid
Publicatiedatum : 11-08-2025
Beoordeeld op geldigheid : 04-08-2025
Algemene gegevens
De ontwikkeling van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodules is in 2020 een multidisciplinair cluster ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met epilepsie.
Het cluster Epilepsie bestaat uit meerdere richtlijnen, zie hier voor de actuele clusterindeling. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden worden indien nodig gevraagd om hun expertise in te zetten voor een specifieke richtlijnmodule. Het cluster bestaat uit de volgende personen:
Clusterstuurgroep
- Prof. dr. H.J.M. Majoie (voorzitter), neuroloog, Academisch Centrum voor Epileptologie Kempenhaeghe/ Maastricht UMC+, Heeze en Maastricht
- Dr. C.M. Delsman-van Gelder, kinderneuroloog, RadboudUMC, Nijmegen
- Drs. M.H.G. Dremmen, radioloog, Erasmus MC Rotterdam
- Dr. P. Klarenbeek, neuroloog, Zuyderland Medisch Centrum, Heerlen
- Dr. L. M’Rabet, patiëntvertegenwoordiger, EpilepsieNL, Houten
- Dr. P. van Vliet, neuroloog/intensivist, Haaglanden Medisch Centrum, Den Haag
Clusterexpertisegroep
- Prof. dr. H.J.M. Majoie (voorzitter – zie boven bij stuurgroep)
- Prof. Dr. J.P. van den Bergh, internist-endocrinoloog, VieCurie Medisch Centrum en hoogleraar metabole botaandoeningen Maastricht UMC+, Maastricht
Met ondersteuning van
- Dr. M.M.J. van Rooijen, adviseur Kennisinstituut van de Federatie Medisch Specialisten Utrecht
- Dr. I.J. Blokland, adviseur Kennisinstituut van de Federatie Medisch Specialisten Utrecht
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle clusterstuurgroepleden en actief betrokken expertisegroepsleden (fungerend als schrijver en/of meelezer bij tenminste één van de geprioriteerde richtlijnmodules) hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een richtlijnmodule worden wijzigingen in belangen aan de projectleider doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase. Een overzicht van de belangen van de clusterleden en betrokken expertisegroepsleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Clusterstuurgroep
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Majoie* |
Functie: Neurologie Werkgever: Academisch Centrum voor Epileptologie Kempenhaeghe, Maastricht UMC+ |
Relevante commissies
NB geen betaalde functies |
Lopende onderzoek- en zorginnovatieprojecten (anders dan contract research) worden gefinancierd uit ZonMW, Nationaal epilepsiefonds, stichting vrienden van Kempenhaeghe, en SKMS.
Incidenteel financiële ondersteuning aan stichting Kempenhaeghe voor organisatie refereeravonden en workshops/symposia (telkens volgens geldende wet en regelgeving). |
Geen actie |
|
Delsman |
Kinderneuroloog/kinderarts Werkgever: Maxima MC Veldhoven |
Geen |
Geen |
Geen actie |
|
Dremmen |
Functie: Kinderradioloog met subspecialisatie kinderneuroradiologie Werkgever: ErasmusMC Rotterdam |
Een van de voorzitters van de richtlijn Radiologische diagnostiek acute trauma-opvang bij kinderen Expertisegroep richtlijn Traumatologie Uitgenodigd spreker op meerdere nationale en internationale cursussen en congressen |
Geen |
Geen actie |
|
Klarenbeek |
Functie: Neuroloog (vrijgevestigd) Werkgever: Zuyderland te Heerlen/Sittard |
Geen |
Geen |
Geen actie |
|
Van Vliet |
Functie: Intensivist Werkgever: Haaglanden Medisch Centrum Den Haag |
|
Geen |
Geen actie |
|
M’Rabet |
Functie: MT-lid Kennis en Innovatie Werkgever: EpilepsieNL, Houten |
|
Familielid met epilepsie Lopend onderzoek epilepsie en een verstandelijke beperking Jazz Pharmaceuticals Benelux (werkpakketleider en projectmanager) |
Geen actie |
Betrokken clusterexpertisegroepleden
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Van den Bergh |
Internist-endocrinoloog VieCuri MC Hoogleraar metabole botaandoeningen Maastricht UMC Reguliere aanstelling/betaalde functie |
|
Externe financiering van Novo Nordisk Fonden (Denemarken), Wetenschapsfonds VieCuri MC, Amgen (allen via afdeling) voor onderzoek naar diabetes en bot (internatiotnaal): Metabole botaandoeningen en Glucocorticoid geïnduceerde osteoporose |
Geen restrictie voor epilepsie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door de afvaardiging van EpilepsieNL in het cluster. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptmodule is tevens ter commentaar voorgelegd aan Epilepsie NL en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
|
Module |
Uitkomst raming |
Toelichting |
|
Screening op Osteoporose en fractuurpreventie |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Need-for-update, prioritering en uitgangsvragen
Tijdens de need-for-update fase april 2024 inventariseerde het cluster de geldigheid van de richtlijnmodules binnen het cluster. Naast de partijen die deelnemen aan de stuur- en expertisegroep zijn hier ook andere stakeholders voor benaderd. Per richtlijnmodule is aangegeven of deze geldig is, herzien moet worden, kan vervallen of moet worden samengevoegd. Ook was er de mogelijkheid om nieuwe onderwerpen aan te dragen die aansluiten bij één (of meerdere) richtlijn(en) behorend tot het cluster. De richtlijnmodules waarbij door één of meerdere partijen werd aangegeven herzien te worden, werden doorgezet naar de prioriteringsronde. Ook suggesties voor nieuwe richtlijnmodules werden doorgezet naar de prioriteringsronde. Afgevaardigden vanuit de partijen in de stuur- en expertisegroep werden gevraagd om te prioriteren (zie ‘Samenstelling cluster’ onder ‘Verantwoording’). De uitkomsten (ranklijst) werd gebruikt als uitgangspunt voor de discussie. Voor de geprioriteerde richtlijnmodules zijn door de het cluster concept-uitgangsvragen herzien of opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde het cluster welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. Het cluster waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde het cluster tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd indien mogelijk gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding). GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
Tabel Gradaties voor de kwaliteit van wetenschappelijk bewijs
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in een richtlijnmodule volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door het cluster wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. Het cluster heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Tabel Sterkte van de aanbevelingen
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
Bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de richtlijnmodule Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd voorgelegd aan alle partijen die benaderd zijn voor de need-for-update fase. De commentaren werden verzameld en besproken met het cluster. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door het cluster. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Algemene informatie
|
Richtlijn: Epilepsie |
|
|
Uitgangsvraag: Osteoporose - AED |
|
|
Database(s): Pubmed/Medline, Embase (Ovid) |
Datum: 03-01-2024 |
|
Periode: 2024 |
Talen: Engels |
|
Literatuurspecialist: Irene Gijselhart |
|
|
Toelichting en opmerkingen:
|
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase (Ovid) en Pubmed/Medline is op 03-01-2024 met relevante zoektermen gezocht naar systematische reviews, RCTs en observationele studies over Osteoporose – AED. De literatuurzoekactie leverde 27 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
Pubmed/MEDLINE |
Ontdubbeld |
|
SRs |
18 |
4 |
4 |
|
RCTs |
10 |
2 |
3 |
|
Observationele studies |
75 |
34 |
20 |
|
Overig |
|
|
|
|
Totaal |
103 |
40 |
27 |
Zoekstrategie
Embase (Ovid)
|
# |
Strategy |
Results |
|
1 |
((exp Epilepsy/ or Landau Kleffner Syndrome/ or severe myoclonic epilepsy in infancy/ or Infantile Spasm/ or (epilep* or seizure* or convulsion* or (continuous spikes and waves during sleep) or csws or landau-kleffner syndrome or lennox-gastaut syndrome or infant* spasm* or dravet* or "severe myoclonic epilepsy" or SMEI).ab,ti,kf.) not (pre eclampsia or preeclampsia or eclampsia).ab,ti,kf.) and (exp Acetazolamide/ or (acetazolamide or diamox).ab,ti,kf. or exp corticotropin/ or (acth or adrenocorticotrophin or corticotropin).ab,ti,kf. or anakinra/ or anakinra.ti,ab,kw. or exp brivaracetam/ or (brivaracetam or briviact).ab,ti,kf. or exp Carbamazepine/ or (carbamazepine or tegretol).ab,ti,kf. or cenobamate/ or cenobamate.ab,ti,kf. or exp clobazam/ or (clobazam or frisium).ab,ti,kf. or exp clonazepam/ or (clonazepam or ritrovil).ab,ti,kf. or cvl-865.ab,ti,kf. or exp Diazepam/ or (diazepam or stesolid or valium).ab,ti,kf. or exp eslicarbazepine acetate/ or (eslicarbazepine or zebinix).ab,ti,kf. or exp ethosuximide/ or (ethosuximide or ethymal or zarontin).ab,ti,kf. or exp ezogabine/ or exp felbamate/ or (felba* or taloxa or FBM).ab,ti,kf. or exp fenfluramine/ or (fenfluramine or fintepla).ab,ti,kf. or exp gabapentin/ or (gabapentin or neurontin).ab,ti,kf. or exp Ganaxolone/ or ganaxolone.ab,ti,kf. or exp lacosamide/ or (lacosamide or vimpat).ab,ti,kf. or exp etiracetam/ or (etiracetam or levetiracetam or keppra).ab,ti,kf. or exp lamotrigine/ or (lamotrigine or lamictal).ab,ti,kf. or exp lorazepam/ or (lorazepam or temesta).ab,ti,kf. or exp midazolam/ or (midazolam or dormicum).ab,ti,kf. or exp nitrazepam/ or (nitrazepam or mogadon).ab,ti,kf. or exp oxcarbazepine/ or (oxcarbazepine or trileptal).ab,ti,kf. or exp paraldehyde/ or paraldehyde.ab,ti,kf. or exp perampanel/ or (perampanel or fycompa).ab,ti,kf. or exp pregabalin/ or (pregabalin or lyrica).ab,ti,kf. or exp phenytoin/ or (phenytoin or diphantoine).ab,ti,kf. or exp phenobarbital/ or phenobarbital.ab,ti,kf. or exp rufinamide/ or (rufinamide or inovelon).ab,ti,kf. or exp sulthiame/ or (sulthiame or ospolot).ab,ti,kf. or exp stiripentol/ or (stiripentol or diacomit).ab,ti,kf. or exp topiramate/ or (topiramate or topamax).ab,ti,kf. or exp vigabatrin/ or (vigabatrin or sabril).ab,ti,kf. or exp valproic acid/ or ("valproic acid" or valproate or depakine or depakene or orfiril).ab,ti,kf. or exp zonisamide/ or (zonisamide or zonegran).ab,ti,kf. or exp anticonvulsants/ or exp barbituric acid derivative/ or exp anticonvulsive agent/ or (anticonvulsant* or antiseizure or anti-seizure or antiepileptic* or anti-epileptic).ab,ti,kf.) and (osteoporosis/ or exp bone demineralization/ or exp fracture/ or exp bone density/ or exp fragility fracture/ or exp photon absorptiometry/ or (osteoporos* or bone loss or bone health or bone density or bone mineral or bone demineralization or bone demineralization or fracture*).ab,ti,kf.) |
2387 |
|
2 |
1 not ((exp animal/ or exp animal experiment/ or exp animal model/ or exp nonhuman/) not exp human/) not (conference abstract or conference review or editorial or letter or note).pt. |
1780 |
|
3 |
limit 2 to yr="2022 -Current" |
175 |
|
4 |
limit 3 to english language |
173 |
|
5 |
exp meta analysis/ or exp "meta analysis (topic)"/ or (metaanaly* or meta analy* or metanaly*).ti,ab. or systematic review/ or "cochrane database of systematic reviews".jn. or prisma.ti,ab. or prospero.ti,ab. or ((systemati* or scoping or umbrella or structured literature) adj3 (review* or overview*)).ti,ab. or (systematic* adj1 review*).ti,ab. or ((systemati* or literature or database* or data base*) adj10 search*).ti,ab. or ((structured or comprehensive* or systematic*) adj3 search).ti,ab. or ((literature adj3 review).ti. and (search* or database* or data base*).ab.) or ((data extraction or "data source*") and study selection).ti,ab. or (search strategy and selection criteria).ti,ab. or (data source and data synthesis).ti,ab. or medline.ab. or pubmed.ab. or embase.ab. or cochrane.ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data base*)).ab. or metasynthes*.ti,ab. or meta synthes*.ti,ab. |
983616 |
|
6 |
4 and 5 |
18 |
|
7 |
exp randomized controlled trial/ or random*.ti,ab. or ((pragmatic or practical) adj clinical trial*).ti,ab. or ((non-inferiority or noninferiority or superiority or equivalence) adj3 trial*).ti,ab. |
2133136 |
|
8 |
(4 and 7) not 5 |
10 |
|
9 |
major clinical study/ or clinical study/ or case control study/ or family study/ or longitudinal study/ or retrospective study/ or prospective study/ or cohort analysis/ or cohort*.ab,ti. or (case control adj1 (study or studies)).ab,ti. or (follow up adj1 (study or studies)).ab,ti. or (observational adj1 (study or studies)).mp. or (epidemiologic adj1 (study or studies)).ab,ti. or (cross sectional adj1 (study or studies)).ab,ti. |
7457659 |
|
10 |
case control study/ or exp comparative study/ or control group/ or controlled study/ or controlled clinical trial/ or crossover procedure/ or double blind procedure/ or phase 2 clinical trial/ or phase 3 clinical trial/ or phase 4 clinical trial/ or pretest posttest design/ or pretest posttest control group design/ or quasi experimental study/ or single blind procedure/ or triple blind procedure/ or (((control or controlled) adj6 trial) or ((control or controlled) adj6 (study or studies)) or ((control or controlled) adj1 active) or open label* or ((double or two or three or multi or trial) adj1 (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or sham-control* or ((single or double or triple or assessor) adj1 (blind* or masked))).ti,ab,kw. or nonrandom*.ti,ab,kw. or non-random*.ti,ab,kw. or quasi-experiment*.ti,ab,kw. or crossover.ti,ab,kw. or cross over.ti,ab,kw. or parallel group*.ti,ab,kw. or factorial trial.ti,ab,kw. or (phase adj5 (study or trial)).ti,ab,kw. or (case* adj6 (matched or control*)).ti,ab,kw. or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)).ti,ab,kw. or (propensity adj6 (scor* or match*)).ti,ab,kw. or versus.ti. or vs.ti. or compar*.ti. or (compar* adj1 study).ti,ab,kw. or ((major clinical study/ or clinical study/ or cohort analysis/ or observational study/ or cross-sectional study/ or multicenter study/ or correlational study/ or follow up/ or cohort*.ti,ab,kw. or follow up.ti,ab,kw. or followup.ti,ab,kw. or longitudinal*.ti,ab,kw. or prospective*.ti,ab,kw. or retrospective*.ti,ab,kw. or observational*.ti,ab,kw. or cross sectional*.ti,ab,kw. or cross?ectional*.ti,ab,kw. or multicent*.ti,ab,kw. or multi-cent*.ti,ab,kw. or consecutive*.ti,ab,kw.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kw. or odds ratio*.ab. or relative odds.ab. or risk ratio*.ab. or relative risk*.ab. or rate ratio.ab. or aor.ab. or arr.ab. or rrr.ab. or (rr adj6 ci).ab.)) |
14574624 |
|
11 |
9 or 10 |
16510271 |
|
12 |
(4 and 11) not (5 or 7) |
75 |
Pubmed/Medline
|
# |
Search |
Results |
|
10 |
#4 AND #9 NOT (#5 OR #7) |
34 |
|
9 |
"Epidemiologic Studies"[Mesh] OR cohort[tiab] OR (case[tiab] AND (control[tiab] OR controll*[tiab] OR comparison[tiab] OR referent[tiab])) OR risk[tiab] OR causation[tiab] OR causal[tiab] OR "odds ratio"[tiab] OR etiol*[tiab] OR aetiol*[tiab] OR "natural history"[tiab] OR predict*[tiab] OR prognos*[tiab] OR outcome[tiab] OR course[tiab] OR retrospect*[tiab] |
8644050 |
|
8 |
#4 AND #7 NOT #5 |
2 |
|
7 |
("Randomized Controlled Trial" [Publication Type] OR random*[tiab] OR pragmatic clinical trial*[tiab] OR practical clinical trial*[tiab] OR non-inferiority trial*[tiab] OR noninferiority trial*[tiab] OR superiority trial*[tiab] OR equivalence clinical trial*[tiab]) |
1614255 |
|
6 |
#4 AND #5 |
43 |
|
5 |
("Meta-Analysis" [Publication Type] OR "Meta-Analysis as Topic"[Mesh] OR metaanaly*[tiab] OR meta-analy*[tiab] or metanaly*[tiab] OR "Systematic Review" [Publication Type] OR systematic[sb] OR "Cochrane Database Syst Rev"[Journal] or prisma[tiab] OR preferred reporting items[tiab] OR prospero[tiab] OR ((systemati*[ti] OR scoping[ti] OR umbrella[ti] OR structured literature[ti]) AND (review*[ti] OR overview*[ti])) OR systematic review*[tiab] OR scoping review*[tiab] OR umbrella review*[tiab] OR structured literature review*[tiab] OR systematic qualitative review*[tiab] OR systematic quantitative review*[tiab] OR systematic search and review[tiab] OR systematized review[tiab] OR systematised review[tiab] OR systemic review[tiab] OR systematic literature review*[tiab] OR systematic integrative literature review*[tiab] OR systematically review*[tiab] OR scoping literature review*[tiab] OR systematic critical review[tiab] OR systematic integrative review*[tiab] OR systematic evidence review[tiab] OR Systematic integrative literature review*[tiab] OR Systematic mixed studies review*[tiab] OR Systematized literature review*[tiab] OR Systematic overview*[tiab] OR Systematic narrative review*[tiab] OR ((systemati*[tiab] OR literature[tiab] OR database*[tiab] OR data-base*[tiab] OR structured[tiab] OR comprehensive*[tiab] OR systemic*[tiab]) AND search*[tiab]) OR (Literature[ti] AND review[ti] AND (database*[tiab] OR data-base*[tiab] OR search*[tiab])) OR ((data extraction[tiab] OR data source*[tiab]) AND study selection[tiab]) OR (search strategy[tiab] AND selection criteria[tiab]) OR (data source*[tiab] AND data synthesis[tiab]) OR medline[tiab] OR pubmed[tiab] OR embase[tiab] OR Cochrane[tiab] OR ((critical[ti] OR rapid[ti]) AND (review*[ti] OR overview*[ti] OR synthes*[ti])) OR (((critical*[tiab] OR rapid*[tiab]) AND (review*[tiab] OR overview*[tiab] OR synthes*[tiab]) AND (search*[tiab] OR database*[tiab] OR data-base*[tiab]))) OR metasynthes*[tiab] OR meta-synthes*[tiab]) |
758700 |
|
4 |
#3 AND (2022[pdat]:2023[pdat]) |
52 |
|
3 |
#2 AND English[Language] |
635 |
|
2 |
#1 NOT (("Animals"[Mesh] OR "Animal Experimentation"[Mesh] OR "Models, Animal"[Mesh]) NOT "Humans"[Mesh]) NOT (letter[pt] OR comment[pt] OR editorial[pt]) |
705 |
|
1 |
("Epilepsy"[MeSH] OR epilep*[TW] OR ((continuous[TW] AND spike*[TW] AND wave*[TW] AND sleep[TW])) OR "Landau-Kleffner Syndrome"[Mesh] OR "landau-kleffner syndrome"[TW] OR "Lennox Gastaut Syndrome"[Mesh] OR "lennox-gastaut syndrome"[TW] OR "Spasms, Infantile"[Mesh] OR infantile spasm*[TW] OR dravet*[TW] OR "severe myoclonic epilepsy"[TW] OR SMEI[TW] OR "Seizures"[Mesh] OR seizure*[TW] OR convulsion[TW] OR convulsions[TW]) NOT ("pre eclampsia"[Mesh] OR "pre eclampsia"[TW] OR "preeclampsia"[TW] OR "Eclampsia"[Mesh] OR "eclampsia*"[TW]) AND (("Acetazolamide"[Mesh] OR acetazolamide[TW] OR diamox[TW]) OR ("Adrenocorticotropic Hormone"[Mesh] OR acth[TW] OR adrenocorticotrophin[TW] OR corticotropin[TW]) OR ("brivaracetam" [Supplementary Concept] OR brivaracetam[TW] OR Briviact[TW]) OR ("Carbamazepine"[Mesh] OR carbamazepine[TW] OR Tegretol[TW]) OR ("Cenobamate" [Supplementary Concept] OR cenobamate[TW]) OR ("Clobazam"[Mesh] OR clobazam[TW] OR frisium[TW]) OR ("Clonazepam"[Mesh] OR clonazepam[TW] OR ritrovil[TW]) OR "CVL-865"[TW] OR ("Diazepam"[Mesh] OR diazepam[TW] OR stesolid[TW] OR valium[TW]) OR ("eslicarbazepine acetate"[Supplementary Concept] OR eslicarbazepine[TW] OR zebinix[TW]) OR ("ethosuximide"[Mesh] OR ethosuximide[TW] OR ethymal[TW] OR zarontin[TW]) OR ("Felbamate"[Mesh] OR felba*[TW] OR taloxa[TW] OR FBM[TW]) OR ("Fenfluramine"[Mesh] OR fenfluramine[TW] OR fintepla[TW]) OR ("gabapentin"[Mesh] OR gabapentin[TW] OR neurontin[TW]) OR ("ganaxolone"[Supplementary Concept] OR ganaxolone[TW] OR "CCD 1042"[TW]) OR ("Interleukin 1 Receptor Antagonist Protein"[Mesh] OR "Interleukin 1 Receptor Antagonist Protein"[TW] OR anakinra[TW]) OR ("lacosamide"[Mesh] OR lacosamide[TW] OR vimpat[TW]) OR ("Levetiracetam"[Mesh] OR etiracetam [TW] OR levetiracetam[TW] OR keppra[TW]) OR ("lamotrigine"[Mesh] OR lamotrigine[TW] OR lamictal[TW]) OR ("lorazepam"[Mesh] OR lorazepam[TW] OR temesta[TW]) OR ("midazolam"[Mesh] OR midazolam[TW] OR dormicum[TW]) OR ("nitrazepam"[Mesh] OR nitrazepam[TW] OR mogadon[TW]) OR ("oxcarbazepine"[Mesh] OR oxcarbazepine[TW] OR trileptal[TW]) OR ("paraldehyde"[Mesh] OR paraldehyde[TW]) OR ("perampanel"[Supplementary Concept] OR perampanel[TW] OR fycompa[TW]) OR ("pregabalin"[Mesh] OR pregabalin[TW] OR lyrica[TW]) OR ("phenytoin"[Mesh] OR phenytoin[TW] OR diphantoine[TW]) OR ("phenobarbital"[Mesh] OR phenobarbital[TW]) OR ("rufinamide"[Supplementary Concept] OR rufinamide[TW] OR inovelon[TW]) OR ("sulthiame"[Supplementary Concept] OR sulthiame[TW] OR ospolot[TW]) OR ("stiripentol"[Supplementary Concept] OR stiripentol[TW] OR diacomit[TW]) OR ("Topiramate"[Mesh] OR topiramate[TW] OR topamax[TW]) OR ("vigabatrin"[Mesh] OR vigabatrin[TW] OR sabril[TW]) OR ("valproic acid"[Mesh] OR valproic acid[TW] OR valproate[TW] OR depakine[TW] OR depakene[TW] OR orfiril[TW]) OR ("Zonisamide"[Mesh] OR zonisamide[TW] OR zonegran[TW]) OR "anticonvulsants"[Pharmacological Action] OR "Anticonvulsants"[Mesh] OR anticonvulsant*[TW] OR antiseizure[TW] OR "anti-seizure"[TW] OR antiepileptic*[TW] OR anti-epileptic*[TW]) AND ("osteoporosis"[MeSH] OR "osteoporosis"[TW] OR "osteoporoses"[TW] OR "bone loss"[TW] OR "bone health"[TW] OR "bone density"[TW] OR "bone density"[MeSH] OR "bone mineral "[TW] OR "bone demineralization"[TW] OR "bone demineralisation"[TW] OR "Fractures, Bone"[Mesh] OR "Osteoporotic Fractures"[Mesh] OR "Fractures"[TW] OR "Fracture"[TW] OR "Absorptiometry, photon"[Mesh]) |
751 |
Algemene informatie
|
Richtlijn: Epilepsie |
|
|
Uitgangsvraag: Osteoporose - AED |
|
|
Database(s): Pubmed/Medline, Embase (Ovid) |
Datum: 08-08-2024 |
|
Periode: zonder datalimiet gezocht |
Talen: Engels |
|
Literatuurspecialist: Irene Gijselhart |
|
|
Toelichting en opmerkingen:
|
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase (Ovid) en Pubmed/Medline is op 08-08-2024 met relevante zoektermen gezocht naar systematische reviews, RCTs over vitamin D - Osteoporose – AED. De literatuurzoekactie leverde 44 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
Pubmed/MEDLINE |
Ontdubbeld |
|
SRs |
26 |
7 |
25 |
|
RCTs |
16 |
13 |
19 |
|
Observationele studies |
|
|
|
|
Overig |
|
|
|
|
Totaal |
42 |
20 |
44 |
Zoekstrategie
Embase (Ovid)
|
# |
Search |
Results |
|
1 |
exp meta analysis/ or exp "meta analysis (topic)"/ or (metaanaly* or meta analy* or metanaly*).ti,ab. or systematic review/ or "cochrane database of systematic reviews".jn. or prisma.ti,ab. or prospero.ti,ab. or ((systemati* or scoping or umbrella or structured literature) adj3 (review* or overview*)).ti,ab. or (systematic* adj1 review*).ti,ab. or ((systemati* or literature or database* or data base*) adj10 search*).ti,ab. or ((structured or comprehensive* or systematic*) adj3 search).ti,ab. or ((literature adj3 review).ti. and (search* or database* or data base*).ab.) or ((data extraction or "data source*") and study selection).ti,ab. or (search strategy and selection criteria).ti,ab. or (data source and data synthesis).ti,ab. or medline.ab. or pubmed.ab. or embase.ab. or cochrane.ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data base*)).ab. or metasynthes*.ti,ab. or meta synthes*.ti,ab. |
1049426 |
|
2 |
exp randomized controlled trial/ or random*.ti,ab. or ((pragmatic or practical) adj clinical trial*).ti,ab. or ((non-inferiority or noninferiority or superiority or equivalence) adj3 trial*).ti,ab. |
2228014 |
|
3 |
((exp Epilepsy/ or epilep*.ab,ti,kf.) not (pre eclampsia or preeclampsia or eclampsia).ab,ti,kf.) and (exp Acetazolamide/ or (acetazolamide or diamox).ab,ti,kf. or exp corticotropin/ or (acth or adrenocorticotrophin or corticotropin).ab,ti,kf. or anakinra/ or anakinra.ti,ab,kw. or exp brivaracetam/ or (brivaracetam or briviact).ab,ti,kf. or exp Carbamazepine/ or (carbamazepine or tegretol).ab,ti,kf. or cenobamate/ or cenobamate.ab,ti,kf. or exp clobazam/ or (clobazam or frisium).ab,ti,kf. or exp clonazepam/ or (clonazepam or ritrovil).ab,ti,kf. or cvl-865.ab,ti,kf. or exp Diazepam/ or (diazepam or stesolid or valium).ab,ti,kf. or exp eslicarbazepine acetate/ or (eslicarbazepine or zebinix).ab,ti,kf. or exp ethosuximide/ or (ethosuximide or ethymal or zarontin).ab,ti,kf. or exp ezogabine/ or exp felbamate/ or (felba* or taloxa or FBM).ab,ti,kf. or exp fenfluramine/ or (fenfluramine or fintepla).ab,ti,kf. or exp gabapentin/ or (gabapentin or neurontin).ab,ti,kf. or exp Ganaxolone/ or ganaxolone.ab,ti,kf. or exp lacosamide/ or (lacosamide or vimpat).ab,ti,kf. or exp etiracetam/ or (etiracetam or levetiracetam or keppra).ab,ti,kf. or exp lamotrigine/ or (lamotrigine or lamictal).ab,ti,kf. or exp lorazepam/ or (lorazepam or temesta).ab,ti,kf. or exp midazolam/ or (midazolam or dormicum).ab,ti,kf. or exp nitrazepam/ or (nitrazepam or mogadon).ab,ti,kf. or exp oxcarbazepine/ or (oxcarbazepine or trileptal).ab,ti,kf. or exp paraldehyde/ or paraldehyde.ab,ti,kf. or exp perampanel/ or (perampanel or fycompa).ab,ti,kf. or exp pregabalin/ or (pregabalin or lyrica).ab,ti,kf. or exp phenytoin/ or (phenytoin or diphantoine).ab,ti,kf. or exp phenobarbital/ or phenobarbital.ab,ti,kf. or exp rufinamide/ or (rufinamide or inovelon).ab,ti,kf. or exp sulthiame/ or (sulthiame or ospolot).ab,ti,kf. or exp stiripentol/ or (stiripentol or diacomit).ab,ti,kf. or exp topiramate/ or (topiramate or topamax).ab,ti,kf. or exp vigabatrin/ or (vigabatrin or sabril).ab,ti,kf. or exp valproic acid/ or ("valproic acid" or valproate or depakine or depakene or orfiril).ab,ti,kf. or exp zonisamide/ or (zonisamide or zonegran).ab,ti,kf. or exp anticonvulsants/ or exp barbituric acid derivative/ or exp anticonvulsive agent/ or (anticonvulsant* or antiseizure or anti-seizure or antiepileptic* or anti-epileptic).ab,ti,kf.) and (osteoporosis/ or exp bone demineralization/ or exp fracture/ or exp bone density/ or exp fragility fracture/ or exp photon absorptiometry/ or (osteoporos* or bone loss or bone health or bone density or bone mineral or bone demineralization or bone demineralization or fracture*).ab,ti,kf. or vitamin d/ or 25 hydroxyvitamin d/ or colecalciferol derivative/ or ergocalciferol derivative/ or (vitamin d or 25-hydroxyvitamin d or "25(OH)D" or 25 oh vitamin d or cholecalciferol or colecalciferol or ergocalciferol).ab,ti,kw.) |
2875 |
|
4 |
3 not ((exp animal/ or exp animal experiment/ or exp animal model/ or exp nonhuman/) not exp human/) not (conference abstract or conference review or editorial or letter or note).pt. |
2212 |
|
5 |
limit 4 to english language |
1958 |
|
6 |
5 and 1 |
150 |
|
7 |
(5 and 2) not 1 |
77 |
|
8 |
((exp Epilepsy/ or epilep*.ab,ti,kf.) not (pre eclampsia or preeclampsia or eclampsia).ab,ti,kf.) and (exp Acetazolamide/ or (acetazolamide or diamox).ab,ti,kf. or exp corticotropin/ or (acth or adrenocorticotrophin or corticotropin).ab,ti,kf. or anakinra/ or anakinra.ti,ab,kw. or exp brivaracetam/ or (brivaracetam or briviact).ab,ti,kf. or exp Carbamazepine/ or (carbamazepine or tegretol).ab,ti,kf. or cenobamate/ or cenobamate.ab,ti,kf. or exp clobazam/ or (clobazam or frisium).ab,ti,kf. or exp clonazepam/ or (clonazepam or ritrovil).ab,ti,kf. or cvl-865.ab,ti,kf. or exp Diazepam/ or (diazepam or stesolid or valium).ab,ti,kf. or exp eslicarbazepine acetate/ or (eslicarbazepine or zebinix).ab,ti,kf. or exp ethosuximide/ or (ethosuximide or ethymal or zarontin).ab,ti,kf. or exp ezogabine/ or exp felbamate/ or (felba* or taloxa or FBM).ab,ti,kf. or exp fenfluramine/ or (fenfluramine or fintepla).ab,ti,kf. or exp gabapentin/ or (gabapentin or neurontin).ab,ti,kf. or exp Ganaxolone/ or ganaxolone.ab,ti,kf. or exp lacosamide/ or (lacosamide or vimpat).ab,ti,kf. or exp etiracetam/ or (etiracetam or levetiracetam or keppra).ab,ti,kf. or exp lamotrigine/ or (lamotrigine or lamictal).ab,ti,kf. or exp lorazepam/ or (lorazepam or temesta).ab,ti,kf. or exp midazolam/ or (midazolam or dormicum).ab,ti,kf. or exp nitrazepam/ or (nitrazepam or mogadon).ab,ti,kf. or exp oxcarbazepine/ or (oxcarbazepine or trileptal).ab,ti,kf. or exp paraldehyde/ or paraldehyde.ab,ti,kf. or exp perampanel/ or (perampanel or fycompa).ab,ti,kf. or exp pregabalin/ or (pregabalin or lyrica).ab,ti,kf. or exp phenytoin/ or (phenytoin or diphantoine).ab,ti,kf. or exp phenobarbital/ or phenobarbital.ab,ti,kf. or exp rufinamide/ or (rufinamide or inovelon).ab,ti,kf. or exp sulthiame/ or (sulthiame or ospolot).ab,ti,kf. or exp stiripentol/ or (stiripentol or diacomit).ab,ti,kf. or exp topiramate/ or (topiramate or topamax).ab,ti,kf. or exp vigabatrin/ or (vigabatrin or sabril).ab,ti,kf. or exp valproic acid/ or ("valproic acid" or valproate or depakine or depakene or orfiril).ab,ti,kf. or exp zonisamide/ or (zonisamide or zonegran).ab,ti,kf. or exp anticonvulsants/ or exp barbituric acid derivative/ or exp anticonvulsive agent/ or (anticonvulsant* or antiseizure or anti-seizure or antiepileptic* or anti-epileptic).ab,ti,kf.) and (osteoporosis/ or exp bone demineralization/ or exp fracture/ or exp bone density/ or exp fragility fracture/ or exp photon absorptiometry/ or (osteoporos* or bone loss or bone health or bone density or bone mineral or bone demineralization or bone demineralization or fracture*).ab,ti,kf.) |
2181 |
|
9 |
8 not ((exp animal/ or exp animal experiment/ or exp animal model/ or exp nonhuman/) not exp human/) not (conference abstract or conference review or editorial or letter or note).pt. |
1667 |
|
10 |
limit 9 to english language |
1504 |
|
11 |
10 and 1 |
124 |
|
12 |
(10 and 2) not 1 |
61 |
|
13 |
6 not 11 |
26 |
|
14 |
7 not 12 |
16 |
Pubmed/Medline
|
# |
Search |
Results |
|
14 |
#7 NOT #12 |
13 |
|
13 |
#6 NOT #11 |
7 |
|
12 |
(#10 AND #2) NOT #1 |
15 |
|
11 |
#10 AND #1 |
37 |
|
10 |
#9 AND English[Language] |
577 |
|
9 |
#8 NOT (("Animals"[Mesh] OR "Animal Experimentation"[Mesh] OR "Models, Animal"[Mesh]) NOT "Humans"[Mesh]) NOT (letter[pt] OR comment[pt] OR editorial[pt]) |
643 |
|
8 |
("Epilepsy"[MeSH] OR epilep*[TW]) NOT ("pre eclampsia"[Mesh] OR "pre eclampsia"[TW] OR "preeclampsia"[TW] OR "Eclampsia"[Mesh] OR "eclampsia*"[TW]) AND (("Acetazolamide"[Mesh] OR acetazolamide[TW] OR diamox[TW]) OR ("Adrenocorticotropic Hormone"[Mesh] OR acth[TW] OR adrenocorticotrophin[TW] OR corticotropin[TW]) OR ("brivaracetam" [Supplementary Concept] OR brivaracetam[TW] OR Briviact[TW]) OR ("Carbamazepine"[Mesh] OR carbamazepine[TW] OR Tegretol[TW]) OR ("Cenobamate" [Supplementary Concept] OR cenobamate[TW]) OR ("Clobazam"[Mesh] OR clobazam[TW] OR frisium[TW]) OR ("Clonazepam"[Mesh] OR clonazepam[TW] OR ritrovil[TW]) OR "CVL-865"[TW] OR ("Diazepam"[Mesh] OR diazepam[TW] OR stesolid[TW] OR valium[TW]) OR ("eslicarbazepine acetate"[Supplementary Concept] OR eslicarbazepine[TW] OR zebinix[TW]) OR ("ethosuximide"[Mesh] OR ethosuximide[TW] OR ethymal[TW] OR zarontin[TW]) OR ("Felbamate"[Mesh] OR felba*[TW] OR taloxa[TW] OR FBM[TW]) OR ("Fenfluramine"[Mesh] OR fenfluramine[TW] OR fintepla[TW]) OR ("gabapentin"[Mesh] OR gabapentin[TW] OR neurontin[TW]) OR ("ganaxolone"[Supplementary Concept] OR ganaxolone[TW] OR "CCD 1042"[TW]) OR ("Interleukin 1 Receptor Antagonist Protein"[Mesh] OR "Interleukin 1 Receptor Antagonist Protein"[TW] OR anakinra[TW]) OR ("lacosamide"[Mesh] OR lacosamide[TW] OR vimpat[TW]) OR ("Levetiracetam"[Mesh] OR etiracetam [TW] OR levetiracetam[TW] OR keppra[TW]) OR ("lamotrigine"[Mesh] OR lamotrigine[TW] OR lamictal[TW]) OR ("lorazepam"[Mesh] OR lorazepam[TW] OR temesta[TW]) OR ("midazolam"[Mesh] OR midazolam[TW] OR dormicum[TW]) OR ("nitrazepam"[Mesh] OR nitrazepam[TW] OR mogadon[TW]) OR ("oxcarbazepine"[Mesh] OR oxcarbazepine[TW] OR trileptal[TW]) OR ("paraldehyde"[Mesh] OR paraldehyde[TW]) OR ("perampanel"[Supplementary Concept] OR perampanel[TW] OR fycompa[TW]) OR ("pregabalin"[Mesh] OR pregabalin[TW] OR lyrica[TW]) OR ("phenytoin"[Mesh] OR phenytoin[TW] OR diphantoine[TW]) OR ("phenobarbital"[Mesh] OR phenobarbital[TW]) OR ("rufinamide"[Supplementary Concept] OR rufinamide[TW] OR inovelon[TW]) OR ("sulthiame"[Supplementary Concept] OR sulthiame[TW] OR ospolot[TW]) OR ("stiripentol"[Supplementary Concept] OR stiripentol[TW] OR diacomit[TW]) OR ("Topiramate"[Mesh] OR topiramate[TW] OR topamax[TW]) OR ("vigabatrin"[Mesh] OR vigabatrin[TW] OR sabril[TW]) OR ("valproic acid"[Mesh] OR valproic acid[TW] OR valproate[TW] OR depakine[TW] OR depakene[TW] OR orfiril[TW]) OR ("Zonisamide"[Mesh] OR zonisamide[TW] OR zonegran[TW]) OR "anticonvulsants"[Pharmacological Action] OR "Anticonvulsants"[Mesh] OR anticonvulsant*[TW] OR antiseizure[TW] OR "anti-seizure"[TW] OR antiepileptic*[TW] OR anti-epileptic*[TW]) AND ("osteoporosis"[MeSH] OR "osteoporosis"[TW] OR "osteoporoses"[TW] OR "bone loss"[TW] OR "bone health"[TW] OR "bone density"[TW] OR "bone density"[MeSH] OR "bone mineral "[TW] OR "bone demineralization"[TW] OR "bone demineralisation"[TW] OR "Fractures, Bone"[Mesh] OR "Osteoporotic Fractures"[Mesh] OR "Fractures"[TW] OR "Fracture"[TW] OR "Absorptiometry, photon"[Mesh]) |
682 |
|
7 |
(#5 AND #2) NOT #1 |
28 |
|
6 |
#5 AND #1 |
44 |
|
5 |
#4 AND English[Language] |
911 |
|
4 |
#3 NOT (("Animals"[Mesh] OR "Animal Experimentation"[Mesh] OR "Models, Animal"[Mesh]) NOT "Humans"[Mesh]) NOT (letter[pt] OR comment[pt] OR editorial[pt]) |
1045 |
|
3 |
("Epilepsy"[MeSH] OR epilep*[TW] OR ((continuous[TW] AND spike*[TW] AND wave*[TW] AND sleep[TW])) OR "Landau-Kleffner Syndrome"[Mesh] OR "landau-kleffner syndrome"[TW] OR "Lennox Gastaut Syndrome"[Mesh] OR "lennox-gastaut syndrome"[TW] OR "Spasms, Infantile"[Mesh] OR infantile spasm*[TW] OR dravet*[TW] OR "severe myoclonic epilepsy"[TW] OR SMEI[TW] OR "Seizures"[Mesh] OR seizure*[TW] OR convulsion[TW] OR convulsions[TW]) NOT ("pre eclampsia"[Mesh] OR "pre eclampsia"[TW] OR "preeclampsia"[TW] OR "Eclampsia"[Mesh] OR "eclampsia*"[TW]) AND (("Acetazolamide"[Mesh] OR acetazolamide[TW] OR diamox[TW]) OR ("Adrenocorticotropic Hormone"[Mesh] OR acth[TW] OR adrenocorticotrophin[TW] OR corticotropin[TW]) OR ("brivaracetam" [Supplementary Concept] OR brivaracetam[TW] OR Briviact[TW]) OR ("Carbamazepine"[Mesh] OR carbamazepine[TW] OR Tegretol[TW]) OR ("Cenobamate" [Supplementary Concept] OR cenobamate[TW]) OR ("Clobazam"[Mesh] OR clobazam[TW] OR frisium[TW]) OR ("Clonazepam"[Mesh] OR clonazepam[TW] OR ritrovil[TW]) OR "CVL-865"[TW] OR ("Diazepam"[Mesh] OR diazepam[TW] OR stesolid[TW] OR valium[TW]) OR ("eslicarbazepine acetate"[Supplementary Concept] OR eslicarbazepine[TW] OR zebinix[TW]) OR ("ethosuximide"[Mesh] OR ethosuximide[TW] OR ethymal[TW] OR zarontin[TW]) OR ("Felbamate"[Mesh] OR felba*[TW] OR taloxa[TW] OR FBM[TW]) OR ("Fenfluramine"[Mesh] OR fenfluramine[TW] OR fintepla[TW]) OR ("gabapentin"[Mesh] OR gabapentin[TW] OR neurontin[TW]) OR ("ganaxolone"[Supplementary Concept] OR ganaxolone[TW] OR "CCD 1042"[TW]) OR ("Interleukin 1 Receptor Antagonist Protein"[Mesh] OR "Interleukin 1 Receptor Antagonist Protein"[TW] OR anakinra[TW]) OR ("lacosamide"[Mesh] OR lacosamide[TW] OR vimpat[TW]) OR ("Levetiracetam"[Mesh] OR etiracetam [TW] OR levetiracetam[TW] OR keppra[TW]) OR ("lamotrigine"[Mesh] OR lamotrigine[TW] OR lamictal[TW]) OR ("lorazepam"[Mesh] OR lorazepam[TW] OR temesta[TW]) OR ("midazolam"[Mesh] OR midazolam[TW] OR dormicum[TW]) OR ("nitrazepam"[Mesh] OR nitrazepam[TW] OR mogadon[TW]) OR ("oxcarbazepine"[Mesh] OR oxcarbazepine[TW] OR trileptal[TW]) OR ("paraldehyde"[Mesh] OR paraldehyde[TW]) OR ("perampanel"[Supplementary Concept] OR perampanel[TW] OR fycompa[TW]) OR ("pregabalin"[Mesh] OR pregabalin[TW] OR lyrica[TW]) OR ("phenytoin"[Mesh] OR phenytoin[TW] OR diphantoine[TW]) OR ("phenobarbital"[Mesh] OR phenobarbital[TW]) OR ("rufinamide"[Supplementary Concept] OR rufinamide[TW] OR inovelon[TW]) OR ("sulthiame"[Supplementary Concept] OR sulthiame[TW] OR ospolot[TW]) OR ("stiripentol"[Supplementary Concept] OR stiripentol[TW] OR diacomit[TW]) OR ("Topiramate"[Mesh] OR topiramate[TW] OR topamax[TW]) OR ("vigabatrin"[Mesh] OR vigabatrin[TW] OR sabril[TW]) OR ("valproic acid"[Mesh] OR valproic acid[TW] OR valproate[TW] OR depakine[TW] OR depakene[TW] OR orfiril[TW]) OR ("Zonisamide"[Mesh] OR zonisamide[TW] OR zonegran[TW]) OR "anticonvulsants"[Pharmacological Action] OR "Anticonvulsants"[Mesh] OR anticonvulsant*[TW] OR antiseizure[TW] OR "anti-seizure"[TW] OR antiepileptic*[TW] OR anti-epileptic*[TW]) AND ("osteoporosis"[MeSH] OR "osteoporosis"[TW] OR "osteoporoses"[TW] OR "bone loss"[TW] OR "bone health"[TW] OR "bone density"[TW] OR "bone density"[MeSH] OR "bone mineral "[TW] OR "bone demineralization"[TW] OR "bone demineralisation"[TW] OR "Fractures, Bone"[Mesh] OR "Osteoporotic Fractures"[Mesh] OR "Fractures"[TW] OR "Fracture"[TW] OR "Absorptiometry, photon"[Mesh] OR "Vitamin D"[Mesh] OR "vitamin d"[TW] OR ergocalciferol[TW] OR "25-hydroxyvitamin D"[TW] OR "25(OH)D"[TW] OR "25(OH)"[TW] OR cholecalciferol[TW] OR colecalciferol[TW]) |
1113 |
|
2 |
("Randomized Controlled Trial" [Publication Type] OR random*[tiab] OR pragmatic clinical trial*[tiab] OR practical clinical trial*[tiab] OR non-inferiority trial*[tiab] OR noninferiority trial*[tiab] OR superiority trial*[tiab] OR equivalence clinical trial*[tiab]) |
1676449 |
|
1 |
("Meta-Analysis" [Publication Type] OR "Meta-Analysis as Topic"[Mesh] OR metaanaly*[tiab] OR meta-analy*[tiab] or metanaly*[tiab] OR "Systematic Review" [Publication Type] OR systematic[sb] OR "Cochrane Database Syst Rev"[Journal] or prisma[tiab] OR preferred reporting items[tiab] OR prospero[tiab] OR ((systemati*[ti] OR scoping[ti] OR umbrella[ti] OR structured literature[ti]) AND (review*[ti] OR overview*[ti])) OR systematic review*[tiab] OR scoping review*[tiab] OR umbrella review*[tiab] OR structured literature review*[tiab] OR systematic qualitative review*[tiab] OR systematic quantitative review*[tiab] OR systematic search and review[tiab] OR systematized review[tiab] OR systematised review[tiab] OR systemic review[tiab] OR systematic literature review*[tiab] OR systematic integrative literature review*[tiab] OR systematically review*[tiab] OR scoping literature review*[tiab] OR systematic critical review[tiab] OR systematic integrative review*[tiab] OR systematic evidence review[tiab] OR Systematic integrative literature review*[tiab] OR Systematic mixed studies review*[tiab] OR Systematized literature review*[tiab] OR Systematic overview*[tiab] OR Systematic narrative review*[tiab] OR ((systemati*[tiab] OR literature[tiab] OR database*[tiab] OR data-base*[tiab] OR structured[tiab] OR comprehensive*[tiab] OR systemic*[tiab]) AND search*[tiab]) OR (Literature[ti] AND review[ti] AND (database*[tiab] OR data-base*[tiab] OR search*[tiab])) OR ((data extraction[tiab] OR data source*[tiab]) AND study selection[tiab]) OR (search strategy[tiab] AND selection criteria[tiab]) OR (data source*[tiab] AND data synthesis[tiab]) OR medline[tiab] OR pubmed[tiab] OR embase[tiab] OR Cochrane[tiab] OR ((critical[ti] OR rapid[ti]) AND (review*[ti] OR overview*[ti] OR synthes*[ti])) OR (((critical*[tiab] OR rapid*[tiab]) AND (review*[tiab] OR overview*[tiab] OR synthes*[tiab]) AND (search*[tiab] OR database*[tiab] OR data-base*[tiab]))) OR metasynthes*[tiab] OR meta-synthes*[tiab]) |
8807724 |