Follow-up en verwijderen van perifeer veneuze katheters
Uitgangsvraag
Welke infectiepreventiemaatregelen dienen genomen te worden tijdens de follow-up en bij het verwijderen van een perifeer veneuze katheter?
Deelvraag 1
Wat is de plaats van het routinematig vervangen van perifeer veneuze katheters bij de preventie van katheter-gerelateerde infecties?
Deelvraag 2
Welke overige infectiepreventiemaatregelen dienen genomen te worden tijdens de follow-up en bij het verwijderen van een perifeer veneuze katheter?
Aanbeveling
Aanbeveling 1 – Vervangen en verwijderen
- Vervang een perifeer veneuze katheter niet routinematig.
- Vervang een perifeer veneuze katheter die onder suboptimale omstandigheden (bijv. in een spoedsituatie) is ingebracht binnen 24 tot 48 uur na inbrengen.
- Verwijder een perifeer veneuze katheter wanneer de indicatie voor de katheter vervalt.
- Verwijder een korte of lange perifeer veneuze katheter direct bij tekenen van een katheter-gerelateerde infectie, tenzij er geen alternatieve vaattoegang is; overleg in dat geval met de behandelend arts.
- Verwijder een ‘midline’ katheter bij tekenen van een katheter-gerelateerde infectie alleen in overleg met de behandelend arts.
- Vervang een connector die gebruikt wordt als koppeling tussen de perifeer veneuze katheter en het toedieningssysteem tegelijk met de katheter, tenzij de fabrikant frequenter vervangen voorschrijft.*
- Leg indicaties en afspraken voor het vervangen dan wel verwijderen van perifeer veneuze katheters vast in een lokaal protocol dat gebaseerd is op vigerende nationale en internationale richtlijnen.
- Pas bij het vervangen dan wel verwijderen van een perifeer veneuze katheter de algemene voorzorgsmaatregelen toe conform de richtlijn Handhygiëne en persoonlijke hygiëne medewerker, de richtlijn Persoonlijke beschermingsmiddelen, en de richtlijn Accidenteel bloedcontact.
- Desinfecteer de huid voorafgaand aan het verwijderen van een perifeer veneuze katheter in het geval dat de kathetertip ingestuurd wordt voor kweek.
- Verwijder de katheter pas als de huid volledig aan de lucht gedroogd is.
- Baseer de keuze van het desinfectans en de methode van desinfecteren op de aanbevelingen in de richtlijn Desinfectie huid en slijmvliezen plus puncties.
* Connectoren die worden gebruikt als afsluiter van een extra toegang tot het toedieningssysteem horen bij het toedieningssysteem. Voor het vervangen hiervan wordt verwezen naar de aanbevelingen voor het vervangen van toedieningssystemen (zie module Toedieningssystemen voor intravasculaire katheters).
Aanbeveling 2 – Infectiepreventiemaatregelen tijdens de follow-up
- Evalueer dagelijks of het noodzakelijk is dat de perifeer veneuze katheter nog in situ blijft.
- Controleer de insteekplaats van de perifeer veneuze katheter dagelijks op tekenen van infectie. Registreer de bevinding en meld tekenen van infectie bij de behandelend arts.
- Pas bij het manipuleren van een perifeer veneuze katheter de algemene voorzorgsmaatregelen toe conform de richtlijn Handhygiëne en persoonlijke hygiëne medewerker, de richtlijn Persoonlijke beschermingsmiddelen, en de richtlijn Accidenteel bloedcontact.
- Desinfecteer koppelingen en bijspuitpunten aan een perifeer veneuze katheter voorafgaand aan het uitvoeren van handelingen hieraan.
- Gebruik voor het desinfecteren alcohol 70%.
- Hanteer een contacttijd van tenminste 30 seconden.
- Laat de alcohol volledig aan de lucht drogen.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Deelvraag 1 – Routinematig versus op klinische indicatie vervangen
Er is literatuuronderzoek verricht naar het effect van het routinematig dan wel (alleen) op klinische indicatie vervangen van perifeer veneuze katheters op katheter-gerelateerde infecties bij volwassen patiënten en kinderen (geen neonaten) in de medisch-specialistische zorg. Katheter-gerelateerde bloedbaaninfectie (KRBBI) en katheter-geassocieerde bloedbaaninfectie (KABBI) werden als cruciale uitkomstmaten gedefinieerd. Infecties van de insteekplaats, (trombo)flebitis, mortaliteit door alle oorzaken, en KRBBI/KABBI-gerelateerde mortaliteit werden als belangrijke uitkomstmaten gedefinieerd. Een relatief risico (RR) kleiner dan 0.8 of groter dan 1.25 werd als klinisch relevant beschouwd voor alle uitkomstmaten, met uitzondering van mortaliteit. Voor mortaliteit werd een relatief risico kleiner dan 0.95 of groter dan 1.05 als klinisch relevant beschouwd.
In het literatuuronderzoek is geen onderscheid gemaakt tussen volwassen patiënten en kinderen, omdat de werkgroep voor het effect van het routinematig vervangen van perifeer veneuze katheters op katheter-gerelateerde infecties geen verschil verwacht tussen volwassen patiënten en kinderen.
Er werden acht gerandomiseerde klinische studies geïncludeerd die het routinematig vervangen van (korte of lange) perifeer veneuze katheters na 72 tot 96 uur vergeleken met het (alleen) op klinische indicatie vervangen bij patiënten in het ziekenhuis. ‘Midline’ katheters werden niet onderzocht.
- Er was een niet klinisch relevant verschil voor de cruciale uitkomstmaten KRBBI (3 studies, bewijskracht redelijk) en KRBBI per 1,000 katheterdagen (2 studies; bewijskracht redelijk).
- Er was een klinisch relevant verschil voor de belangrijke uitkomstmaat infectie van de insteekplaats in het voordeel van routinematig vervangen (RR 0.64; 95% CI 0.12 tot 3.33; 5 studies; bewijskracht zeer laag).
- Er was een niet klinisch relevant verschil voor de belangrijke uitkomstmaten (trombo)flebitis (8 studies; bewijskracht laag), en mortaliteit door alle oorzaken (2 studies; bewijskracht zeer laag). Subgroep analyse liet geen belangrijk effect zien van het interval waarop routinematig werd vervangen (72 uur of 96 uur).
- De belangrijke uitkomstmaat KRBBI-gerelateerde mortaliteit werd gerapporteerd, maar het effect van routinematig vervangen van de katheter kon niet worden geschat (1 studie; bewijskracht zeer laag).
De overall bewijskracht, gebaseerd op de cruciale uitkomstmaten KRBBI en KRBBI per 1,000 katheterdagen, was redelijk.
We concluderen dat er voor patiënten in het ziekenhuis met een (korte of lange) perifeer veneuze katheter met redelijke zekerheid geen belangrijk effect is van het routinematig vervangen van de katheter na 72 tot 96 uur op KRBBI en KRBBI per 1,000 katheterdagen; dat er met lage zekerheid geen belangrijk effect is van het routinematig vervangen van de katheter na 72 tot 96 uur op (trombo)flebitis; en dat het bewijs voor een effect van het routinematig vervangen van de katheter na 72 tot 96 uur op infectie van de insteekplaats, mortaliteit door alle oorzaken, en KRBBI-gerelateerde mortaliteit zeer onzeker is.
Er is geen bewijs gevonden voor een effect van het routinematig vervangen van de katheter op katheter-gerelateerde infecties bij patiënten in het ziekenhuis met een ‘midline’ katheter.
Deelvraag 2 – Overige infectiepreventiemaatregelen
Er is geen systematisch literatuuronderzoek verricht naar overige infectiepreventiemaatregelen tijdens de follow-up en bij het verwijderen van perifeer veneuze katheters bij volwassen patiënten en kinderen (geen neonaten) in de medisch-specialistische zorg.
Voor aanbevelingen baseert de werkgroep zich op de eerdere WIP-richtlijn Flebitis en bloedbaaninfecties door intraveneuze infuuskatheters, internationale richtlijnen, ondersteunende literatuur, en expert opinie.
Vervangen en verwijderen
Voor het vervangen en verwijderen van een perifeer veneuze katheter worden de volgende infectiepreventiemaatregelen aanbevolen:
- Vervang een perifeer veneuze katheter die onder suboptimale omstandigheden is ingebracht binnen 24 tot 48 uur na inbrengen. Het door (spoed)omstandigheden niet (volledig) opvolgen van de aanbevolen infectiepreventiemaatregelen kan de kans op een katheter-gerelateerde infectie verhogen.
- Verwijder een perifeer veneuze katheter wanneer de indicatie voor de katheter vervalt.
- Verwijder een korte of lange perifeer veneuze katheter direct bij tekenen van een katheter-gerelateerde infectie, tenzij er geen alternatieve vaattoegang is; overleg in dat geval met de behandelend arts.
- Verwijder een ‘midline’ katheter bij tekenen van een katheter-gerelateerde infectie alleen in overleg met de behandelend arts.
- Manipulaties aan de perifeer veneuze katheter kunnen resulteren in (partiële) dislocatie van de katheter. Om manipulaties aan de katheter te beperken is het advies om een connector die gebruikt wordt als koppeling tussen de perifeer veneuze katheter en het toedieningssysteem tegelijk met de katheter te vervangen, tenzij de fabrikant frequenter vervangen voorschrijft.
Connectoren die gebruikt worden als afsluiter van een extra toegang tot het toedieningssysteem horen bij het toedieningssysteem. Voor het vervangen hiervan wordt verwezen naar de aanbevelingen voor het vervangen van toedieningssystemen (zie module Toedieningssystemen voor intravasculaire kathetersModule is nog in ontwikkeling).
- Er is geen consensus over de indicaties voor het vervangen dan wel verwijderen van perifeer veneuze katheters. Hier ligt een kennisvraag. De werkgroep adviseert om indicaties en afspraken voor het vervangen dan wel verwijderen van perifeer veneuze katheters vast te leggen in een lokaal protocol dat gebaseerd is op vigerende nationale en internationale richtlijnen (Mermel, 2009).
- Pas bij het vervangen dan wel verwijderen van een perifeer veneuze katheter de algemene voorzorgsmaatregelen toe conform de richtlijn Handhygiëne en persoonlijke hygiëne medewerker, de richtlijn Persoonlijke beschermingsmiddelen, en de richtlijn Accidenteel bloedcontact.
- Desinfecteer de huid voorafgaand aan het verwijderen van een perifeer veneuze katheter in het geval dat de kathetertip ingestuurd wordt voor kweek. Op die manier wordt voorkómen dat de kathetertip tijdens het verwijderen besmet raakt met huidbacteriën.
- Verwijder de katheter pas als de huid volledig aan de lucht gedroogd is. Als de katheter wordt verwijderd terwijl de huid nog nat is van het desinfectans, kan het desinfectans de insteekplaats irriteren en tijdens het verwijderen in aanraking komen met de kathetertip, waardoor het kweekresultaat kan worden beïnvloed.
- Voor de keuze van het desinfectans en de methode van desinfecteren wordt verwezen naar de richtlijn Desinfectie huid en slijmvliezen plus puncties.
Follow-up
Voor de follow-up van perifeer veneuze katheters worden de volgende infectiepreventiemaatregelen aanbevolen:
- Evalueer dagelijks of het noodzakelijk is dat de perifeer veneuze katheter nog in situ blijft.
- Controleer de insteekplaats van de perifeer veneuze katheter dagelijks op tekenen van infectie, registreer de bevinding en meld deze bij de behandelend arts.
- Pas bij het manipuleren van een perifeer veneuze katheter de algemene voorzorgsmaatregelen toe conform de richtlijn Handhygiëne en persoonlijke hygiëne medewerker, de richtlijn Persoonlijke beschermingsmiddelen, en de richtlijn Accidenteel bloedcontact.
- Desinfecteer koppelingen en bijspuitpunten aan de perifeer veneuze katheter voorafgaand aan het uitvoeren van handelingen hieraan.
- Gebruik voor het desinfecteren alcohol 70%.
- Hanteer een contacttijd van tenminste 30 seconden.
- Laat de alcohol volledig aan de lucht drogen.
Internationale richtlijnen
De richtlijnen van Centers for Disease Prevention and Control (CDC) (O’Grady, 2017), International Nursing Society (INS) (No authors listed, 2021), en World Health Organization (WHO) (No authors listed, 2024) zijn geraadpleegd (Tabel 1).
INS beveelt aan om perifeer veneuze katheters alleen op klinische indicatie (bij tekenen van flebitis of infectie) te verwijderen. WHO spreekt geen voorkeur uit voor routinematig vervangen dan wel op klinische indicatie vervangen dan wel verwijderen. CDC beveelt aan om op klinische indicatie te vervangen dan wel verwijderen; voor routinematig vervangen wordt aanbevolen dit alleen bij volwassen patiënten te doen en niet vaker dan ieder 72 tot 96 uur.
INS en WHO bevelen daarnaast aan om de perifeer veneuze katheter te vervangen wanneer deze onder suboptimale aseptische of ongecontroleerde condities is ingebracht.
INS beveelt aan dagelijks te evalueren of er nog een indicatie is voor de perifeer veneuze katheter.
CDC en WHO bevelen aan de insteekplaats van perifeer veneuze katheters dagelijks te inspecteren op tekenen van infectie. INS beveelt aan de behandelen arts te informeren bij tekenen van een infectie, vóórdat de katheter wordt verwijderd.
CDC en INS bevelen aan om connectoren bij manipulatie te desinfecteren met chloorhexidine, povidon jodium, jodofoor of 70% alcohol. WHO doet geen aanbeveling over het desinfecteren van connectoren.
Geen van de geraadpleegde richtlijnen doet aanbevelingen over het desinfecteren van de insteekplaats voorafgaand aan het verwijderen van een perifeer veneuze katheter.
Tabel 1. Internationale richtlijnen voor de preventie van katheter-gerelateerde infecties
|
Richtlijn |
Aanbeveling(en) |
|
CDC (O’Grady, 2017) |
|
|
INS (No authors listed, 2021)1,2 |
|
|
WHO (No authors listed, 2024) |
|
CABSI = catheter-associated bloodstream infection (NL: katheter-geassocieerde bloedbaaninfectie); CDC = Centers for Disease Prevention and Control; INS = International Nursing Society; PIVC = peripheral intravenous catheter (NL: perifeer veneuze katheter); VAD = vascular access device (NL: intravasculaire katheter); WHO = World Health Organization.
1 De INS-richtlijn is ontwikkeld met financiële ondersteuning van de industrie; ook waren auteurs niet vrij van persoonlijke financiële belangen.
2 Er wordt niet verwezen naar de in 2024 verschenen update van de INS-richtlijn, omdat deze niet publiek beschikbaar is.
Wettelijke kaders
Niet van toepassing.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Er is geen systematisch literatuuronderzoek verricht naar de waarden en voorkeuren van patiënten met betrekking tot het routinematig dan wel op klinische indicatie vervangen van perifeer veneuze katheters en overige infectiepreventiemaatregelen tijdens de follow-up.
In het algemeen kan gezegd worden dat de preventie van katheter-gerelateerde infecties past binnen de huidige maatstaven voor passende zorg. Standaardisatie en naleving van aanbevelingen over het vervangen en verwijderen van perifeer veneuze katheters en overige infectiepreventiemaatregelen tijdens de follow-up is voor patiënten belangrijk omdat dit de kans op infecties niet wegneemt, maar wel vermindert.
Het vervangen van een perifeer veneuze katheter is een invasieve en voor de patiënt pijnlijke handeling. Daarnaast kunnen patiënten moeilijk prikbaar zijn, en is het aantal inbrenglocaties beperkt. Het onnodig vervangen van een perifeer veneuze katheter is vanuit een patiëntperspectief dan ook niet wenselijk.
Kosten (middelenbeslag)
Er is geen systematisch literatuuronderzoek verricht naar de kosteneffectiviteit van het routinematig dan wel op klinische indicatie vervangen van perifeer veneuze katheters en overige infectiepreventiemaatregelen tijdens de follow-up.
In het algemeen kan gezegd worden dat katheter-gerelateerde infecties gepaard gaan met meer zorgkosten (Drugeon, 2023). Het voorkómen van deze complicaties door standaardisatie en naleving van aanbevelingen over het vervangen en verwijderen van perifeer veneuze katheters en overige infectiepreventiemaatregelen tijdens de follow-up resulteert naar verwachting in een vermindering van zorgkosten.
Het vervangen van perifeer veneuze katheters gaat gepaard met extra kosten op het gebied van materiaal en personele inzet. Het inbrengen van een ‘midline’ katheter vereist bovendien specifieke vaardigheid. Het onnodig vervangen van perifeer veneuze katheters is vanuit kostenperspectief dan ook niet wenselijk.
Gelijkheid ((health) equity)
De werkgroep voorziet voor aanbevelingen over het vervangen en verwijderen van perifeer veneuze katheters en overige infectiepreventiemaatregelen tijdens de follow-up geen effect op de gezondheidsgelijkheid.
Aanvaardbaarheid
Ethische aanvaardbaarheid
De werkgroep voorziet voor aanbevelingen over het vervangen en verwijderen van perifeer veneuze katheters en overige infectiepreventiemaatregelen tijdens de follow-up geen ethische bezwaren.
Duurzaamheid
Er is geen systematisch literatuuronderzoek verricht naar duurzaamheid van het routinematig dan wel op klinische indicatie vervangen van perifeer veneuze katheters en overige infectiepreventiemaatregelen tijdens de follow-up.
Het is belangrijk een afweging te maken tussen de noodzaak van het vervangen van perifeer veneuze katheters enerzijds en duurzaamheid anderzijds. Deze afweging moet vanuit infectiepreventieoogpunt verantwoord gebeuren en kan verschillen per zorgsetting. Uitgangspunt hierbij is dat duurzaamheid niet ten koste mag gaan van patiëntveiligheid.
In het algemeen kan gezegd worden dat de preventie van katheter-gerelateerde infecties leidt tot minder gebruik van medische hulpmiddelen, minder gebruik van antibiotica en de daarmee gepaard gaande ontwikkeling van antibioticaresistentie.
Het onnodig vervangen van perifeer veneuze katheters is vanuit duurzaamheidsperspectief niet wenselijk.
Haalbaarheid
Het op klinische indicatie vervangen van perifeer veneuze katheters sluit aan bij de bestaande klinische praktijk, vraagt minder handelingen en materialen dan het routinematig vervangen van perifeer veneuze katheters en zal daarom gemakkelijker uitvoerbaar zijn.
De werkgroep voorziet voor aanbevelingen over het vervangen en verwijderen van perifeer veneuze katheters en overige infectiepreventiemaatregelen tijdens de follow-up geen belemmeringen voor de uitvoerbaarheid.
Rationale van aanbeveling 1 – Vervangen en verwijderen: weging van argumenten voor en tegen de interventies
De aanbevelingen over het vervangen en verwijderen van perifeer veneuze katheters bij volwassen patiënten en kinderen (geen neonaten) in de medisch-specialistische zorg zijn gebaseerd op systematisch literatuuronderzoek, de eerdere WIP-richtlijn Flebitis en bloedbaaninfecties door intraveneuze infuuskatheters, internationale richtlijnen, ondersteunende literatuur, en expert opinie. Er wordt geen onderscheid gemaakt tussen volwassen patiënten en kinderen.
Wetenschappelijk bewijs van lage tot redelijke kwaliteit liet geen belangrijk effect zien van het routinematig vervangen van (korte of lange) perifeer veneuze katheters na 72 tot 96 uur op katheter-gerelateerde infecties vergeleken met het (alleen) vervangen op klinische indicatie.
Er zijn geen studies gevonden die het effect van routinematig vervangen van ‘midline’ katheters op katheter-gerelateerde infecties hebben onderzocht bij volwassen patiënten en kinderen (geen neonaten) in de medisch-specialistische zorg.
Het vervangen van een perifeer veneuze katheter is een invasieve en voor de patiënt pijnlijke handeling. Het routinematig vervangen van perifeer veneuze katheters gaat gepaard met extra kosten op het gebied van materiaal en personele inzet. Daarnaast kunnen patiënten moeilijk prikbaar zijn, en is het aantal inbrenglocaties beperkt. Het inbrengen van een ‘midline’ katheter vereist bovendien specifieke vaardigheid.
De werkgroep is daarom van mening dat perifeer veneuze katheters alleen op klinische indicatie en bij het vervallen van de indicatie voor de katheter moeten worden verwijderd. Het routinematig vervangen van perifeer veneuze katheters wordt niet aanbevolen. Wel is het advies om een perifeer veneuze katheter die onder suboptimale omstandigheden (bijv. in een spoedsituatie) is ingebracht binnen 24 tot 48 uur na inbrengen te vervangen. Bij tekenen van een infectie adviseert de werkgroep om voorafgaand aan het verwijderen van de katheter altijd te overleggen met de behandelend arts, tenzij het een korte of lange perifeer veneuze katheter betreft waarbij een alternatieve vaattoegang beschikbaar.
Om manipulaties aan de katheter te beperken adviseert de werkgroep om een connector die gebruikt wordt als koppeling tussen de perifeer veneuze katheter en het toedieningssysteem tegelijk met de katheter te vervangen, tenzij de fabrikant frequenter vervangen voorschrijft.
Er is geen consensus over de indicaties voor het vervangen dan wel verwijderen van perifeer veneuze katheters. Hier ligt een kennisvraag. De werkgroep adviseert om indicaties en afspraken voor het vervangen dan wel verwijderen van perifeer veneuze katheters vast te leggen in een lokaal protocol dat gebaseerd is op vigerende nationale en internationale richtlijnen.
Bij het vervangen dan wel verwijderen van een perifeer veneuze katheter dienen de algemene voorzorgsmaatregelen te worden toegepast conform de richtlijn Handhygiëne en persoonlijke hygiëne medewerker, de richtlijn Persoonlijke beschermingsmiddelen, en de richtlijn Accidenteel bloedcontact.
De werkgroep adviseert om, in het geval dat de kathetertip ingestuurd wordt voor kweek, de huid te desinfecteren voorafgaand aan het verwijderen van de katheter. Het is hierbij van belang de katheter pas te verwijderen als de huid volledig aan de lucht gedroogd is. Voor de keuze van het desinfectans en de methode van desinfecteren wordt verwezen naar de richtlijn Desinfectie huid en slijmvliezen plus puncties.
Rationale van aanbeveling 2 – Infectiepreventiemaatregelen tijdens de follow-up: weging van argumenten voor en tegen de interventies
Er is geen systematisch literatuuronderzoek verricht naar infectiepreventiemaatregelen tijdens de follow-up van perifeer veneuze katheters bij volwassen patiënten en kinderen (geen neonaten) in de medisch-specialistische zorg.
De aanbevelingen over infectiepreventiemaatregelen tijdens de follow-up van perifeer veneuze katheters zijn gebaseerd op de eerdere WIP-richtlijn Flebitis en bloedbaaninfecties door intraveneuze infuuskatheters, internationale richtlijnen, ondersteunende literatuur, en expert opinie. Er wordt geen onderscheid gemaakt tussen volwassen patiënten en kinderen.
De werkgroep is van mening dat het vanuit infectiepreventie oogpunt belangrijk is om de noodzaak voor een perifeer veneuze katheter dagelijks te evalueren. Daarnaast is het advies de insteekplaats van de katheter dagelijks te controleren op tekenen van infectie, de bevinding te registreren, en tekenen van infectie te melden bij de behandelend arts.
Bij het manipuleren van een perifeer veneuze katheter dienen de algemene voorzorgsmaatregelen te worden toegepast conform de richtlijn Handhygiëne en persoonlijke hygiëne medewerker, de richtlijn Persoonlijke beschermingsmiddelen, en de richtlijn Accidenteel bloedcontact.
Tot slot adviseert de werkgroep om koppelingen en bijspuitpunten aan een perifeer veneuze katheter te desinfecteren met alcohol 70% voorafgaand aan het uitvoeren van handelingen hieraan.
Onderbouwing
Een perifeer veneuze katheter wordt ingebracht in een perifere vene en reikt niet verder dan de perifere venen.
Een perifeer veneuze katheter wordt gebruikt om (kortdurend) toegang te verkrijgen tot de bloedbaan voor het toedienen van medicatie, vloeistoffen en bloedproducten, en in uitzonderlijk gevallen voor het afnemen van bloed en het toedienen van parenterale voeding.
Er zijn verschillende typen perifeer veneuze katheters: 1) een korte perifeer veneuze katheter (tot 5 cm), die meestal wordt ingebracht in een vene in de hand, onderarm of elleboogplooi, ook wel bekend als ‘perifeer infuus’; 2) een lange perifeer veneuze katheter (6 tot 10 cm), die wordt ingebracht in een vene in de onderarm, elleboogplooi of bovenarm; en 3) een ‘midline’ katheter (vanaf 10 cm), die wordt ingebracht in een grote vene in de bovenarm.
Het gebruik van een perifeer veneuze katheter kan gepaard gaan met infectieuze en niet-infectieuze complicaties, zoals bloedbaaninfecties en trombose. Deze complicaties kunnen belastend zijn voor de patiënt en kunnen resulteren in een afname van de kwaliteit van leven en een toename in zorgkosten.
Deze module beschrijft de infectiepreventiemaatregelen die genomen dienen te worden tijdens de follow-up en bij het verwijderen van perifeer veneuze katheters bij volwassen patiënten en kinderen (geen neonaten) in de medisch-specialistische zorg. De diagnostiek van katheter-gerelateerde infecties valt buiten de scope van deze richtlijn.
In de huidige Nederlandse klinische praktijk worden perifeer veneuze katheters niet routinematig vervangen. Het is onduidelijk wat het effect is van het routinematig vervangen van perifeer veneuze katheters op het optreden van katheter-gerelateerde infecties vergeleken met het vervangen dan wel verwijderen op klinische indicatie; het literatuuronderzoek richt zich op dit aspect.
Subquestion 1 – Routine versus clinically indicated replacement
Table 1. Summary of findings
P: Patients with a peripheral venous catheter
I: Routine catheter replacement based on a predefined schedule
C: Clinically indicated catheter replacement
S: Hospital
|
Outcome |
Number of patients or catheter days (studies) |
Relative effect (95% CI) |
Absolute effect estimate (95% CI)* |
Certainty of the evidence** |
Conclusions |
|
CRBSI (critical) |
7,531 patients (3 RCTs) |
RR not estimable |
Routine: not estimable Clinically indicated: not estimable
RD not estimable |
Moderate1 |
Routine catheter replacement every 72 to 96 hours likely results in little to no difference in CRBSI compared with clinically indicated replacement in in-hospital patients with a peripheral venous catheter.
(Li, 2022; Rickard, 2012; Xu, 2017) |
|
CRBSI per 1,000 catheter days (critical) |
28,359 catheter days (2 RCTs) |
RR not estimable |
Routine: not estimable Clinically indicated: not estimable
RD not estimable |
Moderate2 |
Routine catheter replacement every 72 to 96 hours likely results in little to no difference in CRBSI per 1,000 catheter days compared with clinically indicated replacement in in-hospital patients with a peripheral venous catheter.
(Li, 2022; Rickard, 2012) |
|
Insertion site infection (important) |
8,492 patients (5 RCTs) |
RR 0.64 (95% CI 0.12 to 3.33)
Clinically relevant In favor of routine replacement |
Routine: 0.6 per 1,000 Clinically indicated: 1 per 1,000
RD 0.3 fewer (95% CI 0.8 fewer to 2 more) |
Very low3 |
The evidence is very uncertain about the effect of routine catheter replacement every 72 to 96 hours on insertion site infection compared with clinically indicated catheter replacement in in-hospital patients with a peripheral venous catheter.
(Li, 2022; Rickard, 2012; Webster, 2007; Webster, 2008; Xu, 2017) |
|
(Thrombo)phlebitis (important) |
10,694 patients (8 RCTs) |
RR 0.83 (95% CI 0.66 to 1.03)
Not clinically relevant |
Routine: 83 per 1,000 Clinically indicated: 100 per 1,000
RD 17 fewer (95% CI 34 fewer to 3 more) |
Low4 |
The evidence suggests that routine catheter replacement every 72 to 96 hours results in little to no difference in (thrombo)phlebitis compared with clinically indicated catheter replacement in in-hospital patients with a peripheral venous catheter.
(Li, 2022; Lin, 2021; Lu, 2022; Rickard, 2012; Vendramim, 2018; Webster, 2007; Webster, 2008; Xu, 2017) |
|
All-cause mortality (important) |
6,333 patients (2 RCTs) |
RR 0.98 (95% CI 0.35 to 2.80)
Not clinically relevant |
Routine: 2 per 1,000 Clinically indicated: 2 per 1,000
RD 0 fewer (95% CI 1 fewer to 4 more) |
Very low5 |
The evidence is very uncertain about the effect of routine catheter replacement every 72 to 96 hours on all-cause mortality compared with clinically indicated catheter replacement in in-hospital patients with a peripheral venous catheter.
(Li, 2022; Rickard, 2012) |
|
CRBSI-related mortality (important) |
1,690 patients (1 RCT) |
RR not estimable |
Routine: not estimable Clinically indicated: not estimable
RD not estimable |
Very low6 |
The evidence is very uncertain about the effect of routine catheter replacement every 72 to 96 hours on CRBSI-related mortality compared with clinically indicated catheter replacement in in-hospital patients with a peripheral venous catheter.
(Rickard, 2012) |
CI = confidence interval; CRBSI = catheter-related bloodstream infection; RD = risk difference; RR = risk ratio or rate ratio
* The risk in the routine catheter replacement group was based on the assumed risk in the clinically indicated catheter replacement group and the relative effect of the intervention.
** The level of evidence for RCTs started at high.
1 Downgraded by one level due to lack of blinding and use of coin toss for randomization (risk of bias; -1).
2 Downgraded by one level due to lack of blinding (risk of bias; -1).
3 Downgraded by three levels due to lack of blinding and use of coin toss for randomization (risk of bias; -1), and the 95% confidence interval of the risk ratio crossing both thresholds for clinical relevance (imprecision; -2).
4 Downgraded by two levels due to unclear or insufficient methods for random sequence generation and allocation concealment, lack of blinding, unclear loss to follow-up, and selective outcome reporting (risk of bias; -1), and the 95% confidence interval of the risk ratio crossing the lower threshold for clinical relevance (imprecision; -1).
5 Downgraded by three levels due to lack of blinding (risk of bias; -1), and the 95% confidence interval of the risk ratio crossing both thresholds for clinical relevance (imprecision; -2).
6 Downgraded by three levels due to lack of blinding (risk of bias; -1), and zero events in both study groups with a total sample size <4,000 (imprecision; -2).
Summary of literature – description of studies
Subquestion 1 – Routine versus clinically indicated replacement
Two SRs, describing a total number of eleven studies, and one study that was not described in these SRs were included in the literature summary. The quality assessment of the SRs is summarized in the Quality assessment table.
The review by Chen (2022) is a systematic review on the effects of routine replacement of peripheral intravenous catheters compared with clinically indicated replacement. PubMed, Embase, the Cochrane Library, and ClinicalTrials.gov were searched for RCTs from inception to January 2022. Criteria for inclusion of studies were: 1) RCT; 2) the study included adults with a peripheral intravenous catheter; 3) the study compared clinically indicated replacement of the peripheral intravenous catheters with routine replacement of the peripheral intravenous catheters every 72 to 96 hours; 4) the study reported at least one clinical outcome of interest (phlebitis, occlusion, local infection, infiltration, CRBSI, accidental removal of peripheral intravenous catheters). In total, nine studies were included in the review. The Cochrane Risk of Bias Assessment Tool was used to assess the risk of bias for the following domains: random sequence generation, allocation concealment, blinding of healthcare workers, blinding of outcome assessors, incomplete outcome data, selective outcome reporting, and other bias (Higgins, 2011).
Seven of nine studies were considered eligible to answer the search question of the current module. Two studies were excluded; one was assessed as a possible (partly) duplicate publication (Rickard, 2010), and one was excluded as it was performed in the outpatient (home) setting (van Donk, 2009).
The review by Webster (2019) is the third update of a systematic review first, published in 2010, on the effects of removing and re-siting peripheral venous catheters routinely compared with removing when clinically indicated. The Cochrane Vascular Specialized Register, the Cochrane Central Register of Controlled Trials, Ovid Medline, Ovid Embase, Ebsco CINAHL, Ovid AMED, the World Health Organization International Clinical Trials Registry Platform, ClinicalTrials.gov, and the Australian and New Zealand Clinical Trials Registry were searched for RCTs in April 2018. Criteria for inclusion of studies were: 1) RCT, irrespective of language; 2) the study included any patient in a hospital, nursing home or community setting with a peripheral intravenous catheter to be in situ for at least three days for the administration of intermittent or continuous therapy (no parenteral nutrition); 3) the study included short peripheral intravenous catheters (no midline or long peripheral intravenous catheter) from any type of material, non-coated or coated with any product, and covered by any type of dressing; 4) the study compared any duration of time before routine replacement of the peripheral venous catheter with clinically indicated replacement; 5) the study reported at least one prespecified outcome (CRBSI, all-cause BSI, local infection, thrombophlebitis, mortality, infiltration, catheter occlusion, number of catheters re-sited, pain during infusion, satisfaction, or cost). In total, nine studies were included in the review. The Cochrane Risk of Bias Assessment Tool was used to assess the risk of bias for the following domains: random sequence generation, allocation concealment, blinding of participants and healthcare workers, blinding of outcome assessors, incomplete outcome data, selective outcome reporting, and other bias (Higgins, 2017).
Five of nine studies were considered eligible to answer the search question of the current module. Four studies were excluded; one was assessed as a possible (partly) duplicate publication (Rickard, 2010), one was performed in the outpatient (home) setting (van Donk, 2009), and two investigated a 48-hour schedule for routine catheter replacement (Barker, 2004; Nishanth, 2009).
The literature summary is not presented separately for adults and children because the working group expects the effect of routine replacement of peripheral venous catheters on catheter-related infections not to differ between adults and children.
Eight RCTs compared routine catheter replacement with clinically indicated catheter replacement in in-hospital patients with a peripheral venous catheter. Seven studies included adults (Li, 2022; Lu, 2022; Rickard, 2012; Vendramim, 2018; Webster, 2007; Webster, 2008; Xu, 2017), and one study included children (Lin, 2021). Five studies investigated a 72-hour schedule for routine catheter replacement (Lin, 2021; Rickard, 2012; Webster, 2007; Webster, 2008; Xu, 2017), and three studies a 96-hour schedule (Li, 2022; Lu, 2022; Vendramim, 2018). Midline catheters were not described.
Important study characteristics of the individual studies, including those not described in the SRs, are summarized in the Characteristics of included studies table. The assessment of the risk of bias for the individual studies is summarized in the Risk of bias table.
Subquestion 2 – Other infection control measures
Not applicable.
Summary of literature - results
Subquestion 1 – Routine versus clinically indicated replacement
1. CRBSI (critical)
Three RCTs reported CRBSI as an outcome (Li, 2022; Rickard, 2012; Xu, 2017). The results were pooled in a meta-analysis. The pooled incidence of CRBSI was 1/3,829 (0.03%) in the routine replacement group, compared to 0/3,702 (not estimable) in the clinically indicated replacement group. The risk ratio could not be estimated.
2. CRBSI per 1,000 catheter days (critical)
Two RCTs reported CRBSI per 1,000 catheter days as an outcome (Li, 2022; Rickard, 2012). The results were pooled in a meta-analysis. The pooled incidence rate of CRBSI was 1/13,340 (0.1 per 1,000 catheter days) in the routine replacement group, compared to 0/15,019 (not estimable) in the clinically indicated replacement group. The rate ratio could not be estimated.
3. Insertion site infection (important)
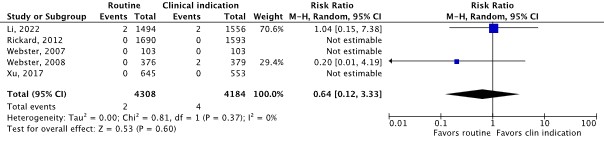
Five RCTs reported insertion site infection as an outcome (Li, 2022; Rickard, 2012; Webster, 2007; Webster, 2008; Xu, 2017). Infections were laboratory-confirmed in two studies (Li, 2022; Rickard, 2012). The results were pooled in a meta-analysis (Figure 1.3). The pooled incidence of insertion site infection was 2/4,308 (0.05%) in the routine replacement group, compared to 4/4,184 (0.1%) in the clinically indicated replacement group. This resulted in a pooled 36% relative risk reduction in favor of routine replacement (RRpooled 0.64; 95% CI 0.12 to 3.33). The relative risk reduction was considered clinically relevant.
Figure 1.3 Forest plot of insertion site infection for routine catheter replacement versus clinically indicated catheter replacement in in-hospital patients with a peripheral venous catheter. Pooled risk ratio, random effects model.
Subgroup analyses – routine catheter replacement schedule
A subgroup analysis according to routine catheter replacement schedule was not feasible due to the small number of studies and events.
4. (Thrombo)phlebitis (important)
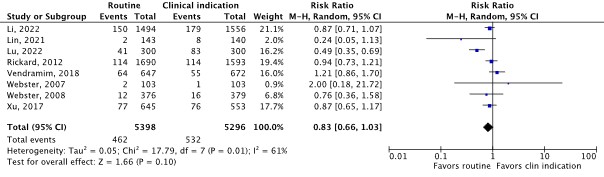
Eight RCTs reported (thrombo)phlebitis as an outcome (Li, 2022; Lin, 2021; Lu, 2022; Rickard, 2012; Vendramim, 2018; Webster, 2007; Webster, 2008; Xu, 2017). The results were pooled in a meta-analysis (Figure 1.4a). The pooled incidence of (thrombo)phlebitis was 462/5,398 (8.6%) in the routine replacement group, compared to 532/5,296 (10.0%) in the clinically indicated replacement group. This resulted in a pooled 17% relative risk reduction in favor of routine replacement (RRpooled 0.83; 95% CI 0.66 to 1.03). The relative risk reduction was considered not clinically relevant.
Figure 1.4a Forest plot of (thrombo)phlebitis for routine catheter replacement versus clinically indicated catheter replacement in in-hospital patients with a peripheral venous catheter. Pooled risk ratio, random effects model.
Subgroup analyses – routine catheter replacement schedule
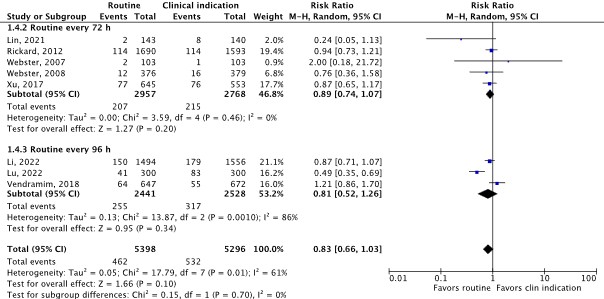
Subgroup analyses were performed according to routine catheter replacement schedule (Figure 1.4b). The effect of routine catheter replacement on (thrombo)phlebitis did not differ statistically significantly between 72-hour and 96-hour schedules (p=0.70).
Figure 1.4b Forest plot of (thrombo)phlebitis for routine catheter replacement versus clinically indicated catheter replacement in in-hospital patients with a peripheral venous catheter, stratified by routine catheter replacement schedule. Pooled risk ratio, random effects model.
5. All-cause mortality (important)
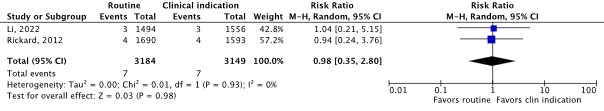
Two RCTs reported all-cause mortality as an outcome (Li, 2022; Rickard, 2012). The results were pooled in a meta-analysis (Figure 1.5). The pooled incidence of all-cause mortality was 7/3,184 (0.2%) in the routine replacement group, compared to 7/3,149 (0.2%) in the clinically indicated replacement group. This resulted in a pooled 2% relative risk reduction in favor of routine replacement (RRpooled 0.98; 95% CI 0.35 to 2.80). The relative risk reduction was considered not clinically relevant.
Figure 1.5 Forest plot of all-cause mortality for routine catheter replacement versus clinically indicated catheter replacement in in-hospital patients with a peripheral venous catheter. Pooled risk ratio, random effects model.
6. CRBSI-related mortality (important)
One RCT reported CRBSI-related mortality as an outcome (Rickard, 2012). The incidence of CRBSI-related mortality was 0/1,690 (not estimable) in the routine replacement group, compared to 0/1,593 (not estimable) in the clinically indicated replacement group. The risk ratio could not be estimated.
Subquestion 2 – Other infection control measures
Not applicable.
Subquestion 1 – Routine versus clinically indicated replacement
A systematic review of the literature was performed to answer the following (search)question:
What is the effect of routine schedule-based catheter replacement compared with clinical indication-based catheter replacement on catheter-related infections for in-hospital patients with a peripheral venous catheter?
Table 1. PICOS
|
Patients |
Patients (non-neonates) with a peripheral venous catheter |
|
Intervention |
Routine catheter replacement based on a predefined schedule |
|
Control |
Clinically indicated catheter replacement (suspected or confirmed complication) |
|
Outcomes* |
CRBSI CABSI** Insertion site infection (Thrombo)phlebitis All-cause mortality CRBSI/CABSI-related mortality |
|
Setting |
Hospital |
|
Other selection criteria |
Study design: systematic review, randomized controlled trial, or comparative observational study |
CABSI = catheter-associated bloodstream infection; CRBSI = catheter-related bloodstream infection
* Per patient and, if reported, per 1,000 catheter days
**If CRBSI is not reported in any of the included studies
Relevant outcome measures
The guideline panel considered catheter-related bloodstream infection (CRBSI) and catheter-associated bloodstream infection (CABSI)* as critical outcome measures for decision-making; and insertion site infection, (thrombo)phlebitis, all-cause mortality, CRBSI (CABSI)-related mortality, insertion failure, and catheter failure for any reason as important outcome measures for decision-making.
* If CRBSI is not reported in any of the included studies
For CRBSI and CABSI, the guideline panel decided to use the definitions as described previously (Maki, 2006; Mermel, 2009; O’Grady, 2011). CRBSI was defined as a primary bloodstream infection with laboratory confirmation of the catheter as the source of the infection. CABSI was defined as a laboratory-confirmed primary bloodstream infection with the catheter in situ or within 48 hours of removal. For all other outcome measures, the guideline panel decided to use the definitions used by the authors of the individual studies.
The guideline panel defined the following thresholds for clinical relevance:
- Mortality: risk ratios of 0.95 and 1.05 (RR<0.95 or RR>1.05)
- Other dichotomous outcomes: risk ratios of 0.8 and 1.25 (RR<0.8 or RR>1.25)
Methods
The literature search for this search question was combined with the similar search question for central venous catheters (see module Follow-up en verwijderen van centraal veneuze katheters) and peripheral arterial catheters (see module Follow-up en verwijderen van perifeer arteriële katheters).
Embase.com and Ovid/Medline databases were systematically searched with relevant search terms from 2000 until April 12, 2024. See Verantwoording for the detailed search strategy. The systematic literature search resulted in 890 unique hits.
Studies were selected based on the following eligibility criteria:
- Systematic review (SR) of randomized controlled trials (RCT) (at least two databases searched, detailed search strategy with search date, in- and exclusion criteria, description of individual study results, risk of bias assessment per study), or RCT; if an SR of RCTs or RCTs were not available, comparative observational studies were selected;
- SR describes at least one RCT that is not described in another selected SR;
- The research question includes all elements of the PICOS;
- The study population is not limited to hemodialysis patients;
- Routine catheter replacement at intervals of at least 72 hours;
- Full paper (i.e., no conference abstract, editorial, letter, or note);
- Full text is available;
- Full text is written in English or Dutch.
The reference lists of excluded systematic reviews were checked for studies that fulfilled the eligibility criteria and were not retrieved in the systematic literature search.
Based on title and abstract screening, 29 studies were initially selected. After reading the full text, twenty studies were excluded (Table of excluded studies), and nine were included. Reference checking of excluded systematic reviews did not result in additional eligible studies.
Subquestion 2 – Other infection control measures
For other infection control measures related to the follow-up and removal of peripheral venous catheters, no systematic literature search was performed.
The recommendations were based on the previous WIP-guideline Flebitis en bloedbaaninfecties door intraveneuze infuuskatheters, international guidelines, supporting literature, and expert opinion.
- •Systematic reviews
- Chen CY, Chen WC, Chen JY, Lai CC, Wei YF. Comparison of clinically indicated replacement and routine replacement of peripheral intravenous catheters: A systematic review and meta-analysis of randomized controlled trials. Front Med (Lausanne). 2022 Aug 12;9:964096. doi: 10.3389/fmed.2022.964096. PMID: 36035414; PMCID: PMC9411788.
- Webster J, Osborne S, Rickard CM, Marsh N. Clinically-indicated replacement versus routine replacement of peripheral venous catheters. Cochrane Database Syst Rev. 2019 Jan 23;1(1):CD007798. doi: 10.1002/14651858.CD007798.pub5. PMID: 30671926; PMCID: PMC6353131.
- •Randomized controlled trials
- Li J, Ding Y, Lu Q, Jin S, Zhang P, Jiang Z, Zhang F, Lyu Y, Lin F. Routine replacement versus replacement as clinical indicated of peripheral intravenous catheters: A multisite randomised controlled trial. J Clin Nurs. 2022 Oct;31(19-20):2959-2970. doi: 10.1111/jocn.16129. Epub 2021 Nov 14. PMID: 34779070.
- Lin SW, Chen SC, Huang FY, Lee MY, Chang CC. Effects of a Clinically Indicated Peripheral Intravenous Replacement on Indwelling Time and Complications of Peripheral Intravenous Catheters in Pediatric Patients: A Randomized Controlled Trial. Int J Environ Res Public Health. 2021 Apr 5;18(7):3795. doi: 10.3390/ijerph18073795. PMID: 33916497; PMCID: PMC8038579.
- Lu H, Yang Q, Nor HM, Lv Y, Zheng X, Xin X, Feng A, Sun Y, Zhou X, Zhang L, Qu Y, Li J, Guo X, Yang Y, Jiao J, Xie N. The safety of clinically indicated replacement or routine replacement of peripheral intravenous catheters: A randomized controlled study. J Vasc Access. 2022 May;23(3):436-442. doi: 10.1177/1129729821998528. Epub 2021 Mar 12. PMID: 33706602.
- Rickard CM, Webster J, Wallis MC, Marsh N, McGrail MR, French V, Foster L, Gallagher P, Gowardman JR, Zhang L, McClymont A, Whitby M. Routine versus clinically indicated replacement of peripheral intravenous catheters: a randomised controlled equivalence trial. Lancet. 2012 Sep 22;380(9847):1066-74. doi: 10.1016/S0140-6736(12)61082-4. PMID: 22998716.
- Vendramim P, Avelar AFM, Rickard CM, Pedreira MDLG. The RESPECT trial-Replacement of peripheral intravenous catheters according to clinical reasons or every 96 hours: A randomized, controlled, non-inferiority trial. Int J Nurs Stud. 2020 Jul;107:103504. doi: 10.1016/j.ijnurstu.2019.103504. Epub 2020 Jan 11. PMID: 32334176.
- Webster J, Lloyd S, Hopkins T, Osborne S, Yaxley M. Developing a Research base for Intravenous Peripheral cannula re-sites (DRIP trial). A randomised controlled trial of hospital in-patients. Int J Nurs Stud. 2007 Jul;44(5):664-71. doi: 10.1016/j.ijnurstu.2006.02.003. Epub 2006 Mar 30. PMID: 16574123.
- Webster J, Clarke S, Paterson D, Hutton A, van Dyk S, Gale C, Hopkins T. Routine care of peripheral intravenous catheters versus clinically indicated replacement: randomised controlled trial. BMJ. 2008 Jul 8;337(7662):a339. doi: 10.1136/bmj.a339. PMID: 18614482; PMCID: PMC2483870.
- Xu L, Hu Y, Huang X, Fu J, Zhang J. Clinically indicated replacement versus routine replacement of peripheral venous catheters in adults: A nonblinded, cluster-randomized trial in China. Int J Nurs Pract. 2017 Dec;23(6). doi: 10.1111/ijn.12595. Epub 2017 Oct 9. PMID: 28990241.
- •Other
- Drugeon B, Guenezan J, Pichon M, Devos A, Fouassin X, Neveu A, Boinot L, Pratt V, Mimoz O. Incidence, complications, and costs of peripheral venous catheter-related bacteraemia: a retrospective, single-centre study. J Hosp Infect. 2023 May;135:67-73. doi: 10.1016/j.jhin.2023.02.012. Epub 2023 Mar 12. PMID: 36918069.
- Higgins JP, Altman DG, Gøtzsche PC, Jüni P, Moher D, Oxman AD, Savovic J, Schulz KF, Weeks L, Sterne JA; Cochrane Bias Methods Group; Cochrane Statistical Methods Group. The Cochrane Collaboration's tool for assessing risk of bias in randomised trials. BMJ. 2011 Oct 18;343:d5928. doi: 10.1136/bmj.d5928. PMID: 22008217; PMCID: PMC3196245.
- Higgins JP, Altman DG, Sterne JA (editors). Chapter 8: Assessing risk of bias in included studies. In: Higgins JP, Churchill R, Chandler J, Cumpston MS (editors), Cochrane Handbook for Systematic Reviews of Interventions Version 5.2.0 (updated June 2017), Cochrane, 2017. 2017.
- Maki DG, Kluger DM, Crnich CJ. The risk of bloodstream infection in adults with different intravascular devices: a systematic review of 200 published prospective studies. Mayo Clin Proc. 2006 Sep;81(9):1159-71. doi: 10.4065/81.9.1159. PMID: 16970212.
- Mermel LA, Allon M, Bouza E, Craven DE, Flynn P, O'Grady NP, Raad II, Rijnders BJ, Sherertz RJ, Warren DK. Clinical practice guidelines for the diagnosis and management of intravascular catheter-related infection: 2009 Update by the Infectious Diseases Society of America. Clin Infect Dis. 2009 Jul 1;49(1):1-45. doi: 10.1086/599376. Erratum in: Clin Infect Dis. 2010 Apr 1;50(7):1079. Dosage error in article text. Erratum in: Clin Infect Dis. 2010 Feb 1;50(3):457. PMID: 19489710; PMCID: PMC4039170.
- O'Grady NP, Alexander M, Burns LA, Dellinger EP, Garland J, Heard SO, Lipsett PA, Masur H, Mermel LA, Pearson ML, Raad II, Randolph AG, Rupp ME, Saint S; Healthcare Infection Control Practices Advisory Committee (HICPAC). Guidelines for the prevention of intravascular catheter-related infections. Clin Infect Dis. 2011 May;52(9):e162-93. doi: 10.1093/cid/cir257. Epub 2011 Apr 1. PMID: 21460264; PMCID: PMC3106269.
- O'Grady NP, Alexander M, Burns LA, Dellinger EP, Garland J, Heard SO, Lipsett PA, Masur H, Mermel LA, Pearson ML, Raad II, Randolph AG, Rupp ME, Saint S; Healthcare Infection Control Practices Advisory Committee (HICPAC). Guidelines for the prevention of intravascular catheter-related infections, 2011. Update 2017. 2017. (https://www.cdc.gov/infection-control/media/pdfs/Guideline-BSI-H.pdf, accessed November 1, 2024).
- No authors listed. 2021 Infusion Therapy Standards of Practice Updates. J Infus Nurs. 2021 Jul-Aug 01;44(4):189-190. doi: 10.1097/NAN.0000000000000436. PMID: 34197345.
- No authors listed. Guidelines for the prevention of bloodstream infections and other infections associated with the use of intravascular catheters: Part 1: peripheral catheters [Internet]. Geneva: World Health Organization; 2024. PMID: 38810002.
Table of quality assessment for systematic reviews
|
Study |
Appropriate and clearly focused question? |
Comprehensive and systematic literature search?
|
Description of included and excluded studies? |
Description of relevant characteristics of included studies? |
Appropriate adjustment for potential confounders in observational studies? |
Assessment of scientific quality of included studies? |
Enough similarities between studies to make combining them reasonable? |
Potential risk of publication bias taken into account? |
Potential conflicts of interest reported? |
|
First author, year |
Yes/no/unclear |
Yes/no/unclear |
Yes/no/unclear |
Yes/no/unclear |
Yes/no/unclear/ not applicable |
Yes/no/unclear |
Yes/no/unclear |
Yes/no/unclear |
Yes/no/unclear |
|
Chen, 2022 |
Yes |
Yes |
No
Excluded studies not described |
Yes |
Not applicable |
Yes |
Yes |
No |
Yes |
|
Webster, 2019 |
Yes |
Yes |
Yes |
Yes |
Not applicable |
Yes |
Yes |
Yes |
Yes |
Characteristics of included studies table
|
Author, year Country Single- or multicenter |
Catheter replacement: clinically indication / predefined schedule |
N patients (baseline); catheters; catheter days Population Ward Device type Follow-up |
Outcomes |
Remarks
|
|
Studies included in SRs (Chen, 2022; Webster, 2019) – randomized controlled trials |
|
|
|
|
|
Li, 2022
China
Multicenter |
G1: phlebitis, infiltration, occlusion, displacement, local infection, CRBSI G2: every 96 hours |
T: 3,050; NR; 10,947
Adults
Medical ward Surgical ward
PVC (not further specified)
Until catheter removal |
CRBSI Insertion site infection Phlebitis1 All-cause mortality |
- |
|
Lu, 2022
China
Single-center |
G1: signs and symptoms of complications G2: every 96 hours |
T: 600; NR; NR
Adults
Medical wards Surgical wards
PVC (not further specified)
Until 48 hours after catheter removal |
Phlebitis1
|
Lost to follow-up: unknown number of patients replaced / distribution unknown |
|
Rickard, 2012
Australia
Multicenter |
G1: phlebitis, infiltration, occlusion, or suspected infection G2: every 72 hours |
T: 3,283; NR; 17,412
Adults
All wards
PVC (not further specified)
Until 48 hours after catheter removal |
CRBSI Insertion site infection Phlebitis2 All-cause mortality CRBSI-related mortality |
- |
|
Vendramim, 2018
Brazil
Multicenter |
G1: phlebitis, infiltration, occlusion, or suspected infection G2: every 96 hours |
T: 1,328*; 2,747; 6,380
Adults
Clinical ward Surgical ward ICU
PVC (not further specified)
Until end of IV therapy or removal of fifth catheter
* Lost to follow-up (allocation mistake): G1: 5; G2: 4 |
Phlebitis1 |
- |
|
Webster, 2007
Australia
Single-center |
G1: clinical indication G2: every 72 hours |
T: 206; NR; NR
Adults
In-hospital
PVC (not further specified)
Until 48 hours after catheter removal or until discharge |
Insertion site infection Phlebitis3 |
- |
|
Webster, 2008
Australia
Single-center |
G1: phlebitis, infiltration, blockage, unexplained fever G2: every 72 hours |
T: 755; NR; 4,411
Adults
In-hospital
PVC (not further specified)
Until end of IV therapy or removal of fifth catheter |
Insertion site infection Phlebitis3 |
- |
|
Xu, 2017
China
Single-center |
G1: clinical indication (occlusion, infiltration, erythema, tenderness, pain at insertion site, suspected infection) G2: every 72 hours |
T: 1,198; NR; NR
Adults
Medical ward Surgical ward
PVC (not further specified)
Until 48 hours after catheter removal |
CRBSI Insertion site infection Phlebitis4
|
- |
|
Additional studies - randomized controlled trials |
|
|
|
|
|
Lin, 2021
Taiwan
Single-center |
G1: infiltration, occlusion, phlebitis G2: every 72 hours |
T: 306; NR; NR
Children
Pediatric ward
PVC (not further specified)
Until catheter removal
* Lost to follow-up: G1: 13; G2: 10 |
Phlebitis1 |
- |
CABSI = catheter-associated bloodstream infection; G = group; ICU = intensive care unit; NR = not reported; PVC = peripheral venous catheter; RCT = randomized controlled trial; T = total number
1 Infusion Nurses Society (INS) phlebitis scale
2 At least two of: pain and/or tenderness, erythema, swelling, purulent discharge, palpable venous cord
3 At least two of: pain, tenderness, erythema, warmth, swelling, palpable venous cord
4 At least two of: erythema, swelling, fever, pain, palpable venous cord
Risk of bias table
Based on Cochrane risk of bias tool and suggestions by the CLARITY Group at McMaster University)
Randomized controlled trials
|
Author, year |
Random sequence generation |
Allocation concealment |
Blinding |
Incomplete outcome data |
Selective outcome reporting |
Other bias |
Overall risk of bias |
|
Was the allocation sequence adequately generated? |
Was the allocation adequately concealed? |
Was knowledge of the allocated interventions adequately prevented?
Were patients, healthcare providers, data collectors, outcome assessors, data analysts blinded? |
Was loss to follow-up (missing outcome data) infrequent? |
Are reports of the study free of selective outcome reporting? |
Was the study apparently free of other problems that could put it at a risk of bias? |
||
|
Li, 2022 |
Definitely yesA1 |
Definitely yesB1 |
Definitely noC1 |
Definitely yesD1 |
Probably yesE1 |
Probably yesF1 |
High (all outcomes) |
|
Lin, 2021 |
Definitely yesA1 |
Probably noB6 |
Definitely noC1 |
Probably yesD2 |
Probably yesE1 |
Probably yesF1 |
High (all outcomes) |
|
Lu, 2022 |
Definitely yesA1 |
Probably noB5 |
Definitely noC1 |
Probably noD3 |
Probably noE2 |
Probably yesF1 |
High (all outcomes) |
|
Rickard, 2012 |
Definitely yesA1 |
Definitely yesB2 |
Definitely noC1 |
Definitely yesD1 |
Probably yesE1 |
Probably yesF1 |
High (all outcomes) |
|
Vendramim, 2018 |
Definitely yesA1 |
Probably yesB4 |
Definitely noC1 |
Definitely yesD1 |
Probably yesE1 |
Probably yesF1 |
High (all outcomes) |
|
Webster, 2007 |
Definitely yesA1 |
Definitely yesB2 |
Definitely noC1 |
Definitely yesD1 |
Probably yesE1 |
Probably yesF1 |
High (all outcomes) |
|
Webster, 2008 |
Definitely yesA1 |
Definitely yesB2 |
Definitely noC1 |
Definitely yesD1 |
Probably yesE1 |
Probably yesF1 |
High (all outcomes) |
|
Xu, 2017 |
Probably noA2 |
Definitely yesB3 |
Definitely noC1 |
Definitely yesD1 |
Probably yesE1 |
Probably yesF1 |
High (all outcomes) |
A1 Randomization using computer-generated random numbers
A2 Randomization using a coin toss
B1 Central randomization using opaque sealed envelopes
B2 Central randomization using a telephone or computer-based service
B3 Randomization using a coin toss
B4 Central randomization using a message app (sequence held by principal investigator)
B5 Patients were ‘divided’ into two groups; concealment was not described
B6 Allocation concealment was not described
C1 No blinding of patients; no blinding of clinicians; no blinding of outcome assessors; blinding of data analysts was not reported
D1 No missing outcome data
D2 Missing outcome data were infrequent (<5%) and non-differential
D3 Lost to follow-up was replaced, but number and distribution are unknown
E1 All outcomes described in the Methods section were reported
E2 Not all secondary outcomes were reported
F1 No funding by industry or conflict of interest
Tables of excluded studies
Systematic search – full text assessment
|
Reference |
Reason for exclusion |
|
Cepkova M, Matthay MA. Reducing risk in the ICU: Vascular catheter-related infections. Infections Medicine. 2006;23(4):141-152. |
Cost-effectiveness study |
|
Cooper AS. Clinically Indicated Replacement Versus Routine Replacement of Peripheral Venous Catheters. Crit Care Nurse. 2019 Aug;39(4):67-68. doi: 10.4037/ccn2019187. PMID: 31371371. |
Summary of systematic review (Webster, 2019) |
|
Farooqi UG, Sabahat M, Akhter AS, Ali MA. Rehman SU, Rahman FU. Incidence, risk factors and prevention related to infusion phlebitis. J Pharmaceutical Negative Results. 2022; 13:2822-2825. |
Insufficient reporting of intervention, comparator and outcome data |
|
Farr BM. Preventing vascular catheter-related infections: current controversies. Clin Infect Dis. 2001 Nov 15;33(10):1733-8. doi: 10.1086/323402. Epub 2001 Oct 5. PMID: 11595992. |
Narrative review |
|
de Jonge RC, Polderman KH, Gemke RJ. Central venous catheter use in the pediatric patient: mechanical and infectious complications. Pediatr Crit Care Med. 2005 May;6(3):329-39. doi: 10.1097/01.PCC.0000161074.94315.0A. PMID: 15857534. |
Narrative review |
|
Ho KH, Cheung DS. Guidelines on timing in replacing peripheral intravenous catheters. J Clin Nurs. 2012 Jun;21(11-12):1499-506. doi: 10.1111/j.1365-2702.2011.03974.x. Epub 2012 Feb 17. PMID: 22340078. |
Critical appraisal of a since-updated systematic review (Webster, 2010; update 2019) |
|
Idvall E, Gunningberg L. Evidence for elective replacement of peripheral intravenous catheter to prevent thrombophlebitis: a systematic review. J Adv Nurs. 2006 Sep;55(6):715-22. doi: 10.1111/j.1365-2648.2006.03962.x. PMID: 16925620. |
Selection criteria for systematic reviews were not fulfilled
|
|
Mermel LA. Prevention of intravascular catheter-related infections. Ann Intern Med. 2000 Mar 7;132(5):391-402. doi: 10.7326/0003-4819-132-5-200003070-00009. Erratum in: Ann Intern Med 2000 Sep 5;133(5):395. PMID: 10691590. |
Narrative review |
|
Morrison K, Holt KE. The Effectiveness of Clinically Indicated Replacement of Peripheral Intravenous Catheters: An Evidence Review With Implications for Clinical Practice. Worldviews Evid Based Nurs. 2015 Aug;12(4):187-98. doi: 10.1111/wvn.12102. Epub 2015 Aug 4. PMID: 26243585. |
Selection criteria for systematic reviews were not fulfilled |
|
Nishanth S, Sivaram G, Kalayarasan R, Kate V, Ananthakrishnan N. Does elective re-siting of intravenous cannulae decrease peripheral thrombophlebitis? A randomized controlled study. Natl Med J India. 2009 Mar-Apr;22(2):60-2. PMID: 19852337. |
I/C didn’t meet PICOS |
|
O'Grady NP. Applying the science to the prevention of catheter-related infections. J Crit Care. 2002 Jun;17(2):114-21. doi: 10.1053/jcrc.2002.34366. PMID: 12096374. |
Selection criteria for systematic reviews were not fulfilled
|
|
O'Grady NP, Alexander M, Dellinger EP, Gerberding JL, Heard SO, Maki DG, Masur H, McCormick RD, Mermel LA, Pearson ML, Raad II, Randolph A, Weinstein RA; Healthcare Infection Control Practices Advisory Committee. Guidelines for the prevention of intravascular catheter-related infections. Infect Control Hosp Epidemiol. 2002 Dec;23(12):759-69. doi: 10.1086/502007. PMID: 12517020. |
CDC guideline / updated in 2017 |
|
O'Grady NP, Alexander M, Dellinger EP, Gerberding JL, Heard SO, Maki DG, Masur H, McCormick RD, Mermel LA, Pearson ML, Raad II, Randolph A, Weinstein RA; Healthcare Infection Control Practices Advisory Committee. Guidelines for the prevention of intravascular catheter-related infections. Am J Infect Control. 2002 Dec;30(8):476-89. doi: 10.1067/mic.2002.129427. PMID: 12461511. |
CDC guideline / updated in 2017 |
|
Pirracchio R, Legrand M, Rigon MR, Mateo J, Lukaszewicz AC, Mebazaa A, Raskine L, Le Pors MJ, Payen D. Arterial catheter-related bloodstream infections: results of an 8-year survey in a surgical intensive care unit. Crit Care Med. 2011 Jun;39(6):1372-6. doi: 10.1097/CCM.0b013e3182120cf7. PMID: 21336106. |
P didn’t meet PICOS |
|
Rickard CM, McCann D, Munnings J, McGrail MR. Routine resite of peripheral intravenous devices every 3 days did not reduce complications compared with clinically indicated resite: a randomised controlled trial. BMC Med. 2010 Sep 10;8:53. doi: 10.1186/1741-7015-8-53. PMID: 20831782; PMCID: PMC2944158. |
Possible (partial) duplicate publication (Rickard, 2012) |
|
Stevens C, Milner KA, Trudeau J. Routine Versus Clinically Indicated Short Peripheral Catheter Replacement: An Evidence-based Practice Project. J Infus Nurs. 2018 May/Jun;41(3):198-204. doi: 10.1097/NAN.0000000000000281. PMID: 29659468. |
Narrative review and quasi-experimental study (before-after study) with insufficient reporting of outcome data |
|
Timsit JF. Scheduled replacement of central venous catheters is not necessary. Infect Control Hosp Epidemiol. 2000 Jun;21(6):371-4. doi: 10.1086/501775. PMID: 10879566. |
Narrative review |
|
Tuffaha HW, Rickard CM, Webster J, Marsh N, Gordon L, Wallis M, Scuffham PA. Cost-effectiveness analysis of clinically indicated versus routine replacement of peripheral intravenous catheters. Appl Health Econ Health Policy. 2014 Feb;12(1):51-8. doi: 10.1007/s40258-013-0077-2. PMID: 24408785. |
Cost-effectiveness study |
|
Ullman A, Keogh S, Marsh N, Rickard C. Routine versus clinically indicated replacement of peripheral catheters. Br J Nurs. 2015 Jan 22-Feb 11;24(2):S14. doi: 10.12968/bjon.2015.24.Sup2.S14. PMID: 25616125. |
Summary of previously published RCT (Rickard, 2012) |
|
Wu MA, Casella F. Is clinically indicated replacement of peripheral catheters as safe as routine replacement in preventing phlebitis and other complications? Intern Emerg Med. 2013 Aug;8(5):443-4. doi: 10.1007/s11739-013-0940-z. Epub 2013 Apr 6. PMID: 23564486. |
Summary of previously published RCT (Rickard, 2012) |
C = comparator; I = intervention; O = outcome; P = population; RCT = randomized controlled trial; S = setting.
In- and excluded systematic reviews – reference lists
|
Reference |
Reason for exclusion |
|
Barker P, Anderson AD, MacFie J. Randomised clinical trial of elective re-siting of intravenous cannulae. Ann R Coll Surg Engl. 2004 Jul;86(4):281-3. doi: 10.1308/147870804317. PMID: 15239872; PMCID: PMC1964197. |
I/C didn’t meet PICOS |
|
Cobb DK, High KP, Sawyer RG, Sable CA, Adams RB, Lindley DA, Pruett TL, Schwenzer KJ, Farr BM. A controlled trial of scheduled replacement of central venous and pulmonary-artery catheters. N Engl J Med. 1992 Oct 8;327(15):1062-8. doi: 10.1056/NEJM199210083271505. PMID: 1522842. |
Published before 2000 |
|
Cook D, Randolph A, Kernerman P, Cupido C, King D, Soukup C, Brun-Buisson C. Central venous catheter replacement strategies: a systematic review of the literature. Crit Care Med. 1997 Aug;25(8):1417-24. doi: 10.1097/00003246-199708000-00033. PMID: 9267959. |
Published before 2000 |
|
Eyer S, Brummitt C, Crossley K, Siegel R, Cerra F. Catheter-related sepsis: prospective, randomized study of three methods of long-term catheter maintenance. Crit Care Med. 1990 Oct;18(10):1073-9. PMID: 2209033. |
Outcome data are not reported by device type |
|
Kerin MJ, Pickford IR, Jaeger H, Couse NF, Mitchell CJ, Macfie J. A prospective and randomised study comparing the incidence of infusion phlebitis during continuous and cyclic peripheral parenteral nutrition. Clin Nutr. 1991 Dec;10(6):315-9. doi: 10.1016/0261-5614(91)90060-p. PMID: 16839938. |
I/C didn’t meet PICOS |
|
May J, Murchan P, MacFie J, Sedman P, Donat R, Palmer D, Mitchell CJ. Prospective study of the aetiology of infusion phlebitis and line failure during peripheral parenteral nutrition. Br J Surg. 1996 Aug;83(8):1091-4. doi: 10.1002/bjs.1800830817. PMID: 8869311. |
I/C didn’t meet PICOS |
|
Nakae H, Igarashi T, Tajimi K. Catheter-related infections via temporary vascular access catheters: a randomized prospective study. Artif Organs. 2010 Mar;34(3):E72-6. doi: 10.1111/j.1525-1594.2009.00960.x. PMID: 20447037. |
I/C didn’t meet PICOS |
|
Uldall PR, Merchant N, Woods F, Yarworski U, Vas S. Changing subclavian haemodialysis cannulas to reduce infection. Lancet. 1981 Jun 20;1(8234):1373. doi: 10.1016/s0140-6736(81)92553-8. PMID: 6113344. |
P didn’t meet PICOS |
|
Van Donk P, Rickard CM, McGrail MR, Doolan G. Routine replacement versus clinical monitoring of peripheral intravenous catheters in a regional hospital in the home program: A randomized controlled trial. Infect Control Hosp Epidemiol. 2009 Sep;30(9):915-7. doi: 10.1086/599776. PMID: 19637959. |
S didn’t meet PICOS |
C = comparator; I = intervention; O = outcome; P = population; S = setting.
Beoordelingsdatum en geldigheid
Publicatiedatum : 12-02-2026
Beoordeeld op geldigheid : 12-02-2026
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd door het ministerie van VWS. De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Werkgroep
- S. (Selma) Bons, Nederlandse Vereniging voor Anesthesiologie (NVA), voorzitter
- Dr. M. (Michelle) Gompelman, Nederlandse Internisten Vereniging (NIV), Nederlandse Vereniging van Internist-Infectiologen (NVII)
- R. (Renze) Jongstra, Verpleegkundigen & Verzorgenden Nederland (V&VN)
- H. (Heidy) Koene, Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg (VHIG)
- M.H.H. (Marc) Königs, Nederlandse Vereniging voor Intensive Care (NVIC)
- Dr. B.J. (Bart) Laan (AIOS), Nederlandse Internisten Vereniging (NIV), Nederlandse Vereniging van Internist-Infectiologen (NVII)
- K. (Kelly) Niggebrugge-Mentink, Nederlandse Vereniging van Ziekenhuisapothekers (NVZA)
- Dr. J.H. (Jan) van Zeijl, Nederlandse Vereniging voor Medische Microbiologie (NVMM)
Klankbordgroep
- Dr. J.R.A. (Jeetindra) Balak, Nederlandse Internisten Vereniging (NIV), Nederlandse Federatie voor Nefrologie (NFN)
- Werkgroep richtlijn Centraal veneuze toegang (NVvH)
- Werkgroep leidraad Infusietechnologie (NVKF)
Met ondersteuning van
- Mw. A. (Alies) Oost, informatiespecialist, Kennisinstituut van Federatie Medisch Specialisten
- Dr. H. (Haitske) Graveland, senior adviseur, Kennisinstituut van Federatie Medisch Specialisten
- Dr. M.F.Q. (Marjolein) Kluijtmans-van den Bergh, senior adviseur, Kennisinstituut van Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
S. (Selma) Bons |
Anesthesioloog, Prinses Maxima Centrum voor kinderoncologie, Utrecht |
Lid werkgroep SRI richtlijnen
Lid bestuur sectie kinderanesthesiologie NVA
Lid SRI |
Geen |
Geen restrictie |
|
Dr. M. (Michelle) Gompelman |
Internist-infectioloog, Elkerliek Ziekenhuis, Helmond |
Lid werkgroep FMS-richtlijn Centraal veneuze toegang
|
Geen |
Geen restrictie |
|
A. (Renze) Jongstra |
Intensive care verpleegkundige |
Vicevoorzitter V&VN afdeling IC (onbetaald)
|
Geen |
Geen restrictie |
|
H. (Heidy) Koene |
Deskundige infectiepreventie, Erasmus MC, Rotterdam |
Geen |
Geen |
Geen restrictie |
|
M.H.H. (Marc) Königs |
Intensivist, Maxima Medisch Centrum. Eindhoven/Veldhoven (100%) |
Duikerarts / duikclubarts
Waarnemer intensivist Aruba en via IC (max. 200 uur/jaar) In het verleden voordrachten op congressen voor 3M en BD (betaald) - ESAIC ( Milaan / München) - WOCOVA ( Athene) - Nordic congres for vasculary acces |
Geen |
Geen restrictie (adviseurschap 3M onbetaald) |
|
Dr. B.J. (Bart) Laan |
AIOS Interne Geneeskunde, Amsterdam UMC, Amsterdam |
Geen |
Geen |
Geen restrictie |
|
K. (Kelly) Niggebrugge-Mentink |
Ziekenhuisapotheker, Hagaziekenhuis, Den Haag |
Gastdocent Fontys Hogeschool (verpleegkundig specialistenopleiding); betaald Gastspreker congres Stichting Vascular Infusion Technology; onbetaald |
Geen |
Geen restrictie |
|
Dr. J.H. (Jan) van Zeijl |
Arts-microbioloog, Certe Medische Diagnostiek & Advies, afdeling Medische Microbiologie (tot april 2024)
Waarnemend arts-microbioloog, Certe Medische Diagnostiek & Advies, afdeling Medische Microbiologie (september t/m december 2025) |
Bestuurslid (sinds januari 2024 voorzitter) Vasculitis Stichting met portefeuille vrijwilligersbeleid en Zorg, Research en Belangenbehartiging; onbetaald |
Geen |
Geen restrictie |
|
Klankbordgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Dr. J.R.A. (Jeetindra) Balak |
Internist, Leids UMC, Leiden |
Geen |
Geen |
Geen restrictie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van Patiëntenfederatie Nederland (PFNL) voor de schriftelijke knelpunteninventarisatie. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan PFNL en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst raming |
Toelichting |
|
Follow-up en verwijderen van perifeer veneuze katheters |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt ook uit de toetsing dat het overgrote deel (±90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II-instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten met betrekking tot infectiepreventiemaatregelen rondom intravasculaire katheters. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere WIP-richtlijn Arteriële katheters en de WIP-richtlijn Flebitis en bloedbaaninfecties door intraveneuze infuuskatheters. Tevens zijn er in de schriftelijke knelpunteninventarisatie knelpunten aangedragen door Inspectie Gezondheidszorg en Jeugd (IGJ), Landelijke Vereniging van Operatieassistenten (LVO), Nederlandse Vereniging van Anesthesiemedewerkers (NVAM), Nederlandse Vereniging van Revalidatieartsen (VRA), Nederlandse Vereniging van Ziekenhuizen (NVZ), Nederlandse Vereniging voor Heelkunde (NVvH), Nederlandse Vereniging voor Medische Microbiologie (NVMM), Rijksinstituut voor Volksgezondheid en Milieu (RIVM), Stichting Kind en Ziekenhuis, Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg (VHIG), Verpleegkundigen & Verzorgenden Nederland (V&VN). Een verslag hiervan is opgenomen onder Verslag schriftelijke knelpunteninventarisatie.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvragen behorende bij de uitgangsvragen inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Ook definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder Zoekverantwoording. Indien mogelijk werden de gegevens uit verschillende studies gepoold in een random-effects-model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de wetenschappelijke bewijskracht wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie https://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nul effect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), duurzaamheid, aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje Overwegingen en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016A; Alonso-Coello 2016B). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling is gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417. A
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494. B
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 3.0 (2023). Adviescommissie Richtlijnen van de Raad Kwaliteit. Available from: https://richtlijnendatabase.nl/uploaded/docs/FMS_MedSpecRicht_2023__v04.pdf?u=1bULOR
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from: https://gdt.gradepro.org/app/handbook/handbook.html.
Zoekverantwoording
|
Richtlijn Intravasculaire katheters |
|
|
Uitgangsvraag: Wat is de plaats van het routinematig vervangen van een perifeer veneuze katheter, een centraal veneuze katheter en een perifeer arteriële katheter bij de preventie van katheter-gerelateerde infecties? Zoekvraag: What is the effect of routine, time schedule-based, catheter replacement compared with clinical indication-based catheter removal/replacement on catheter-related infectious complications in patients requiring a peripheral venous catheter, (non-tunneled) central venous catheter or arterial catheter? |
|
|
Database(s): Embase.com, Ovid/Medline |
Datum: 12 april 2024 |
|
Periode: vanaf 2000 |
Talen: geen restrictie |
|
Literatuurspecialist: Alies Oost |
Rayyan review: https://rayyan.ai/reviews/995636 |
|
BMI-zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Deduplication: voor het ontdubbelen is gebruik gemaakt van http://dedupendnote.nl:9777/ |
|
|
Toelichting: Voor deze vraag is gezocht op de elementen:
|
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SR |
62 |
48 |
62 |
|
RCT |
248 |
184 |
319 |
|
Observationele studies |
384 |
385 |
509 |
|
Totaal |
694 |
617 |
890* |
*in Rayyan
Zoekstrategie
Embase.com
|
No. |
Query |
Results |
|
#1 |
'central venous catheter'/exp OR 'central venous catheterization'/exp OR 'peripherally inserted central venous catheter'/exp OR 'peripheral venous catheter'/exp OR 'artery catheter'/exp OR 'artery catheterization'/exp OR ((peripheral* NEAR/4 (catheter* OR cannula* OR line* OR access* OR infusion OR iv OR ivs)):ti,ab,kw) OR pivc:ti,ab,kw OR pivcs:ti,ab,kw OR 'venous access':ti,ab,kw OR ((('central intravenous' OR 'central vein*' OR 'central venous') NEAR/3 (catheter* OR device* OR line* OR infusion OR iv OR ivs OR access OR cannula*)):ti,ab,kw) OR hickman*:ti,ab,kw OR broviac:ti,ab,kw OR picc*:ti,ab,kw OR 'pic line*':ti,ab,kw OR 'central line*':ti,ab,kw OR 'central catheter*':ti,ab,kw OR cvc:ti,ab,kw OR cvcs:ti,ab,kw OR cvad*:ti,ab,kw OR 'swan ganz':ti,ab,kw OR (((arterial OR artery) NEAR/3 (catheter* OR cannula* OR line* OR access)):ti,ab,kw) |
137284 |
|
#2 |
('catheter removal'/exp OR 'device removal'/de) AND ('time factor'/exp OR 'time'/de OR 'dwell time'/exp OR 'time interval'/de OR 'timeliness'/exp) OR 'catheter removal'/exp/mj OR 'device removal'/mj OR (((remov* OR replac* OR change OR resit* OR 're sit*') NEAR/3 (routin* OR schem* OR schedul* OR timing OR time OR timely OR standard* OR planned OR interval*)):ti,ab,kw) OR (((remov* OR replac*) NEAR/4 routin*):ti,ab,kw) OR (((remov* OR replac* OR resit* OR 're sit*' OR interval*) NEAR/3 ('24 hour*' OR '24 h' OR 24h OR '48 hour*' OR '48 h' OR 48h OR '72 hour*' OR '72 h' OR 72h OR '96 hour*' OR '96 h' OR 96h)):ti,ab,kw) |
103650 |
|
#3 |
#1 AND #2 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
1228 |
|
#4 |
#3 AND [2000-2024]/py |
1082 |
|
#5 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
1018502 |
|
#6 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
4009991 |
|
#7 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
8169857 |
|
#8 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
14987968 |
|
#9 |
#4 AND #5 - SR |
62 |
|
#10 |
#4 AND #6 NOT #9 - RCT |
248 |
|
#11 |
#4 AND (#7 OR #8) NOT (#9 OR #10) - observationeel |
384 |
|
#12 |
#9 OR #10 OR #11 |
694 |
Ovid/Medline
|
# |
Searches |
Results |
|
1 |
exp Central Venous Catheters/ or exp Catheterization, Central Venous/ or exp Catheterization, Peripheral/ or Vascular Access Devices/ or (peripheral* adj4 (catheter* or cannula* or line* or access* or infusion or iv or ivs)).ti,ab,kf. or pivc.ti,ab,kf. or pivcs.ti,ab,kf. or 'venous access'.ti,ab,kf. or (('central intravenous' or 'central vein*' or 'central venous') adj3 (catheter* or device* or line* or infusion or iv or ivs or access or cannula*)).ti,ab,kf. or hickman*.ti,ab,kf. or broviac.ti,ab,kf. or picc*.ti,ab,kf. or 'pic line*'.ti,ab,kf. or 'central line*'.ti,ab,kf. or 'central catheter*'.ti,ab,kf. or cvc.ti,ab,kf. or cvcs.ti,ab,kf. or cvad*.ti,ab,kf. or 'swan ganz'.ti,ab,kf. or ((arterial or artery) adj3 (catheter* or cannula* or line* or access)).ti,ab,kf. |
77952 |
|
2 |
(exp Device Removal/ and (Time/ or Time Factors/)) or ((remov* or replac* or change or resit* or 're sit*') adj3 (routin* or schem* or schedul* or timing or time or timely or standard* or planned or interval*)).ti,ab,kf. or ((remov* or replac*) adj4 routin*).ti,ab,kf. or ((remov* or replac* or resit* or 're sit*' or interval*) adj3 ('24 hour*' or '24 h' or 24h or '48 hour*' or '48 h' or 48h or '72 hour*' or '72 h' or 72h or '96 hour*' or '96 h' or 96h)).ti,ab,kf. |
72387 |
|
3 |
(1 and 2) not (comment/ or editorial/ or letter/) not ((exp animals/ or exp models, animal/) not humans/) |
924 |
|
4 |
limit 3 to yr="2000 -Current" |
781 |
|
5 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
738752 |
|
6 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2712176 |
|
7 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] |
4698772 |
|
8 |
Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) |
5664797 |
|
9 |
4 and 5 - SR |
48 |
|
10 |
(4 and 6) not 9 - RCT |
184 |
|
11 |
(4 and (7 or 8)) not (9 or 10) - observationeel |
385 |
|
12 |
9 or 10 or 11 |
617 |