Orale vocht- en voedingsinname na hoofd-halschirurgie
Uitgangsvraag
Wanneer en op welke wijze kan de orale vocht- en voedingsinname veilig worden opgestart na hoofd-hals oncologische chirurgie?
De uitgangsvraag omvat de volgende deelvragen:
- Wanneer en op welke wijze kan de orale vocht- en voedingsinname veilig worden opgestart na hoofd-hals oncologische chirurgie bij patiënten die een (faryngo) laryngectomie hebben ondergaan, al dan niet met (vrije) lapreconstructie?
- Wanneer en op welke wijze kan de orale vocht- en voedingsinname veilig worden opgestart na uitgebreide hoofd-hals oncologische chirurgie bij patiënten die een mondholteprocedure met (vrije) lapreconstructie hebben ondergaan?
Aanbeveling
PICO 1: Totale (faryngo) laryngectomie met of zonder (vrije) lapreconstructie
- Overweeg om na een primaire of salvage (faryngo) laryngectomie met of zonder (vrije) lapreconstructie vroegtijdig (binnen 24 uur tot 5 dagen postoperatief) te starten met orale vocht- en voedingsinname naast sondevoeding.
- Start alleen als de patiënt klinisch stabiel, helder en instrueerbaar is en een goede integriteit van de lapreconstructie heeft.
- Wees alert op tekenen van fistelvorming; indien er twijfel bestaat, kan aanvullende beeldvorming (zoals een sliktest met methyleenblauw in water of een slikfoto met bijv. Ultravist of Omnipaque) duidelijkheid geven.
- Overweeg om de orale vocht- en voedingsinname uit te stellen om lekkage van drank en voeding naar de hals te voorkomen bij twijfel over de wondgenezing of fistelvorming.
- Houd rekening met beperkte tolerantie voor vastere voeding; betrek altijd een ervaren diëtist bij de start en uitbreiding van orale inname en simultane afbouw van sondevoeding (zie Module GLIM criteria).
- Raadpleeg een ervaren logopedist indien er slikproblemen worden ervaren bij het starten en/of uitbreiden van orale vocht- en voedingsinname.
PICO 2: Excisie met (vrije) lapreconstructie van een uitgebreid mondholtecarcinoom
- Overweeg om na een excisie met een (vrije) lapreconstructie van een uitgebreid mondholtecarcinoom vroegtijdig (na 24 uur en binnen 5 dagen postoperatief) te starten met orale vocht- en voedingsinname naast de sondevoeding.
- Start alleen als de patiënt klinisch stabiel, helder en instrueerbaar is, een goede integriteit van de lapreconstructie heeft en na beoordeling van de slikfunctie door een ervaren logopedist of verpleegkundige en in samenwerking met de mondhygiënist (zie Module Slikfunctiebehoud via prehabilitatie en revalidatie en de Richtlijn Orofaryngeale Dysfagie – Startpagina - Orofaryngeale dysfagie - Richtlijn - Richtlijnendatabase). Betrek ook altijd een ervaren diëtist bij de start en uitbreiding van orale inname en simultane afbouw van sondevoeding (zie Module GLIM criteria).
- Start voorzichtig met orale inname, bijvoorbeeld met een free water protocol en bouw vervolgens geleidelijk op naar dik vloeibare (IDDSI 3) en glad gemalen voeding (IDDSI 4), conform lokale protocollen en afhankelijk van het individuele herstel van de slikfunctie. Eventuele postoperatieve beperkingen zoals een tracheotomie is hierbij geen contra-indicatie. Extra controle op de veiligheid van de slikfunctie wordt bij een tracheotomie wel aanbevolen.
- Wees alert op tekenen van fistelvorming; indien er twijfel bestaat, kan aanvullende beeldvorming (zoals een sliktest met methyleenblauw in water of een slikfoto met bijv. Ultravist of Omnipaque) duidelijkheid geven.
- Overweeg om de orale vocht- en voedingsinname uit te stellen (>5 dagen postoperatief) om lekkage van drank en voeding naar de hals te voorkomen bij twijfel over de wondgenezing of fistelvorming, bij ernstige zwelling in de mond/keelholte, het hebben van een gecuffte tracheacanule en na zeer uitgebreide ingrepen of reconstructies.
- Zorg dat er duidelijke afspraken zijn over het moment van cuff deflatie en het starten van de orale vocht- en voedingsinname.
- Overweeg in geval van ernstige dysfagie een beoordeling middels slikbeeldvorming door een specialist zoals een laryngoloog en/of gespecialiseerd logopedist (zie Module Slikfunctiebehoud via prehabilitatie en revalidatie).
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
In deze module zijn twee deelvragen uitgewerkt. Voor beide deelvragen is een systematische literatuur analyse uitgevoerd. Helaas hadden de geïncludeerde studies relatief kleine steekproefgroottes, onvoldoende externe validiteit en een onvoldoende tot slechte methodologische kwaliteit, wat zorgde voor een verhoogd risico op vertekening van de resultaten en onvoldoende interne validiteit. Voor alle uitkomstmaten geldt dat de kwaliteit van het bewijs zeer laag was. Op basis van de literatuur kan er dus geen richting worden gegeven aan de besluitvorming. Hier ligt een kennislacune. De aanbevelingen in deze richtlijnmodule zijn gebaseerd op de mening van experts.
De eerste uitgangsvraag (PICO 1) van deze module richt zich op de vraag of het vroegtijdig starten van orale vocht- en voedingsinname na een totale (faryngo) laryngectomie met of zonder (vrije) lapreconstructie meer of minder complicaties met zich meebrengt. Voor deze uitgangsvraag werd één systematisch review met meta-analyse gevonden (Milinis, 2021). Het vroegtijdig starten van orale inname kent zowel voor- als nadelen. Een belangrijk voordeel is dat vroegtijdige orale vocht- en voedingsinname geassocieerd is met een kortere ziekenhuisopname, wat blijkt uit twee cohortstudies (n=132) Bulgurcu (2018) en Medina (2001) die binnen de meta analyse van Milinis (2021) gekeken hebben naar ziekenhuis opname duur (MD (dagen) −4.68 (−6.2 tot −3.1, Z = 5.93, p < 0.00001). Daarnaast tonen specifieke bevindingen bij reconstructie met een vrije lap aan dat vroegtijdige orale inname kan bijdragen aan een lager risico op fistelvorming en een verbeterde slikfunctie (paragraaf 1.2). Dit biedt duidelijke voordelen voor het postoperatieve herstel en het verminderen van de zorglast. Toch zijn er enkele mogelijke nadelen en aandachtspunten. Traditioneel wordt verondersteld dat vroegtijdige orale inname het risico op complicaties zoals fistelvorming kan verhogen, hoewel recente data dit niet significant ondersteunen. De kwaliteit van het bewijs voor het vroegtijdig starten van de orale vocht- en voedingsinname is echter laag tot zeer laag, maar met gegevens uit de meta-analyse (Milinis, 2021) en aanvullende cohortstudies (Volling, 2001; Seven, 2003; Sharifian, 2008; Sousa, 2014), die positieve uitkomsten laten zien, lijkt het binnen vijf dagen na de operatie starten van de orale vocht- en voedingsinname verantwoord. Hoewel meer gerichte onderzoeken nodig zijn om optimale richtlijnen met een hogere bewijslast voor specifieke patiëntgroepen te ontwikkelen, bieden de huidige bevindingen voldoende onderbouwing om een vroegtijdige start van orale inname als een veilige en potentieel gunstige interventie te overwegen bij zorgvuldig geselecteerde patiënten die binnen deze uitgangsvraag zijn onderzocht. Hoewel er aanwijzingen zijn dat het vroegtijdig starten van orale inname veilig kan zijn, is er in de literatuur geen duidelijk bewijs beschikbaar met betrekking tot de optimale orale volumina, nutritionele en overige eigenschappen (reologisch, organoleptisch, etc.) van dranken en voeding om de orale inname op te starten. In de praktijk kan overwogen worden om te starten met kleine hoeveelheden water, volgens het het free water protocol[1] (Gillman 2017), onder strikte begeleiding van een logopedist. Na een (faryngo)laryngectomie bestaat er echter geen anatomische verbinding meer tussen de luchtpijp en de slokdarm, waardoor aspiratie (verslikken) niet langer mogelijk is. Wel kunnen er postoperatief slikfysiologische problemen optreden. Bij het begin van de orale intake kan nog niet worden voorspeld of er naadlekkage of fistelvorming ter hoogte van het wondgebied zal optreden. Om deze reden wordt altijd gestart met water. Bij een goede slikfunctie kan de orale vocht- en voedingsinname vervolgens worden uitgebreid naar dik vloeibare consistenties (IDDSI[2] 3) en naar glad gemalen voeding (IDDSI 4) tot wat uiteindelijk functioneel haalbaar is na de operatie (maximaal IDDSI 7; normale voeding). Bij patiënten die een uitgebreide chirurgische ingreep hebben ondergaan zoals een buismaagreconstructie, kan het verstandig zijn pas na de vijfde postoperatieve dag te starten met de inname van water. Indien er problemen worden ervaren bij het starten en/of uitbreiden van orale vocht- en voedingsinname kan een ervaren logopedist ingeschakeld worden.
De tweede uitgangsvraag (PICO 2) van deze module richt zich op de vraag of het vroegtijdig starten van orale vocht- en voedingsinname bij patiënten die een excisie met (vrije) lapreconstructie van een uitgebreid mondholtecarcinoom hebben ondergaan, meer of minder complicaties met zich meebrengt. Voor deze uitgangsvraag werd één systematische review (Dean, 2024) en één gerandomiseerde gecontroleerde studie (RCT) gevonden (Wu, 2022), die verschillende uitkomstmaten hebben onderzocht. Wu en collega’s onderzochten 128 patiënten na een mondholteprocedure met vrije lapreconstructie. Het doel van deze studie was of een versnelde verwijderingsstrategie van de neusmaagsonde veilig en effectief zou zijn. Patiënten werden gerandomiseerd in vier groepen (n=32 per groep): controle- en interventiegroep zonder tracheotomie en controle- en interventiegroep met tracheotomie. De niet-tracheotomie interventiegroep mocht op de eerste postoperatieve dag vijf ml water slikken. Bij afwezigheid van hoesten mochten ze de volgende twee dagen geleidelijk meer water drinken. De neusmaagsonde werd pas verwijderd na het behalen van niveau I/II op de Watian water sliktest (WWST)[3] (geen "natte stem" na het drinken, geen significante daling in de zuurstofsaturatie tijdens en na het drinken, en voldoende dagelijkse orale voedingsinname). De tracheotomie interventiegroep ontving hetzelfde protocol plus een extra Watian water sliktest na verwijdering van de tracheacanule. De niet-tracheotomie controlegroep kreeg het conventionele plan voor het verwijderen van de neusmaagsonde, gebaseerd op de beoordeling van de chirurg over wondgenezing en slikvermogen. Bij de tracheotomie controlegroep moest eerst de tracheacanule verwijderd zijn en daarna hing de timing van het verwijderen van de neusmaagsonde af van de wondgenezing en het slikvermogen. De resultaten van dit onderzoek toonden aan dat de verwijdering van de neusmaagsonde bij de interventiegroepen significant eerder plaatsvond dan in de controlegroepen. Binnen de niet-tracheotomie interventiegroep vond de verwijdering van de neusmaagsonde gemiddeld na 5,0 dagen plaats, vergeleken met 7,8 dagen in de niet-tracheotomie controlegroep (p = 0,001). Voor tracheotomie patiënten was de verwijderingstijd van de neusmaagsonde gemiddeld 9,8 dagen in de interventiegroep, tegenover 16,2 dagen in de controlegroep (p = 0,049). De incidentie van wondcomplicaties en het gemiddelde dagelijks volume van orale inname (in ml) waren vergelijkbaar tussen de groepen, zonder significante verschillen.
Het postoperatieve ziekenhuisverblijf was korter voor patiënten in de tracheotomie interventiegroep dan in de tracheotomie controlegroep (p = 0,005). De auteurs concludeerden dat het vroegtijdig starten van de orale vocht- en voedingsinname bij patiënten na een mondholteprocedure met (vrije) lapreconstructie veilig is. Het vroegtijdig starten van de orale vocht- en voedingsinname gevolgd door een versnelde verwijderingsstrategie van de neusmaagsonde (in de tracheotomie interventiegroep, nadat de tracheacanule verwijderd is) kan het postoperatief herstel bevorderen zonder extra risico’s.
De RCT van Wu (2022) keek onder andere ook naar de vorming van een oro- of faryngocutane fistel. Door het ontbreken van meerdere studies was pooling van data niet mogelijk. De gevonden risk ratio bedroeg 0,50 (95% BI 0,05 tot 5,38) in het voordeel van het vroegtijdig starten van de orale vocht- en voedingsinname. Dit betekent dat het risico op een fistel 50% lager was bij vroegtijdige orale inname. Ondanks het potentieel klinisch relevante effect, is de betrouwbaarheid van het resultaat beperkt door de kleine studiepopulatie en de brede betrouwbaarheidsintervallen. De opnameduur werd eveneens gerapporteerd in de RCT van Wu (2022). De gemiddelde reductie in ziekenhuisopnameduur was -1,45 dagen (95% BI -2,36 tot -0,54) in het voordeel van een vroegtijdige start van orale inname. Hoewel statistisch significant, wordt deze reductie als niet klinisch relevant beschouwd (zie paragraaf ‘Relevant outcome measures’). Ook wonddehiscentie werd bestudeerd in deze RCT van Wu. De risk ratio voor het ontstaan van een wonddehiscentie na de start van orale inname bedroeg 1,00 (95% BI 0,06 tot 15,64), wat duidt op geen verschil in risico tussen het vroeg- en laattijdig starten van de orale vocht- en voedingsinname. Door de brede betrouwbaarheidsintervallen wordt dit resultaat als niet klinisch relevant beschouwd. Lapnecrose werd eveneens gerapporteerd in deze RCT van Wu (2022), met een risk ratio van 1,00 (95% BI 0,15 tot 6,88), wat wederom duidt op geen verschil in risico op lapnecrose tussen het vroeg- en laattijdig starten van de orale vocht- en voedingsinname. De vorming van seroom of hematoom werd beschreven in drie cohortstudies. De risk ratio was 0,74 (95% BI 0,34 tot 1,61) in het voordeel van het vroegtijdig starten van orale inname, met een lage heterogeniteit (I² = 0%), wat wijst op een 26% lager risico op seroom- of hematoomvorming. Dit resultaat wordt als klinisch relevant beschouwd, hoewel de kwaliteit van het bewijs beperkt is. Wondinfectie werd ook onderzocht in de studie van Wu (2022). De risk ratio bedroeg 0,80 (95% BI 0,23 tot 2,84) en liet geen significant verschil in risico op wondinfectie zien tussen het vroeg- en laattijdig starten van de orale vocht- en voedingsinname. Ook dit resultaat wordt als niet klinisch relevant beschouwd (zie paragraaf ‘Relevant outcome measures’). De functionele orale inname (FOIS) werd beschreven in een cohortstudie van Stramiello (2021) en de postoperatieve FOIS-scores op dag 30-60-90 waren beter in de groep die vroegtijdig startte met orale inname. Gegevens over gezondheid-gerelateerde kwaliteit van leven en gewichtsverlies werden niet gerapporteerd. Samenvattend suggereren de beschikbare gegevens dat het vroegtijdig starten van orale vocht- en voedingsinname bij patiënten die een excisie met een (vrije) lapreconstructie van een uitgebreid mondholtecarcinoom hebben ondergaan waarschijnlijk veilig is, zonder verhoogd risico op ernstige complicaties zoals fistelvorming, wonddehiscentie, -necrose of -infecties. Daarnaast kan vroegtijdige orale inname mogelijk het risico op seroom- of hematoomvorming verlagen en bijdragen aan een betere functionele orale vocht- en voedingsinname. De kwaliteit van het bewijs is echter beperkt, waardoor voorzichtigheid en individuele beoordeling noodzakelijk blijven voor het type patiënten dat binnen deze uitgangsvraag werd onderzocht.
Ook bij deze uitgansvraag is er in de literatuur geen duidelijk bewijs beschikbaar met betrekking tot de optimale orale volumina, nutritionele en overige eigenschappen (reologisch, organoleptisch, etc.) van dranken en voeding om de orale inname op te starten. In de praktijk kan overwogen worden te starten met kleine hoeveelheden water volgens het free water protocol[4], onder strikte begeleiding van een logopedist, diëtist en mondhygiënist (preventie aspiratiepneumonie). De onderbouwing voor het starten met water is vergelijkbaar met die van het Free Water Protocol [3], dat kan worden toegepast bij patiënten met dysfagie (Panther, 2005). De patiëntengroep uit PICO 2 bevindt zich in een spanningsveld tussen enerzijds het starten van orale intake en de slikfunctie, en anderzijds het risico op wondcomplicaties na het starten van orale voeding. Bij het begin van de orale intake kan nog niet worden voorspeld of er naadlekkage of fistelvorming ter hoogte van het wondgebied zal optreden. Om deze reden wordt altijd gestart met water. Indien water via wondnaden in de halsweefsels lekt, is dit minder schadelijk dan wanneer dikvloeibare dranken in het wondgebied en diepe halsweefsels terechtkomen. Indien de logopedist vaststelt dat de slikfunctie ernstig beperkt is (bijvoorbeeld door een hoge uitzuigfrequentie via de tracheacanule vanwege speekselaspiratie of een natte stem, etc.), moet de orale inname van water zeer zorgvuldig worden overwogen of zelfs worden uitgesteld, en mogelijk voorafgegaan worden door slikbeeldvorming.
Bij een goede slikfunctie (geen verslikking of beperkte kans op verslikking met goede hoestreflex) kan de orale vocht- en voedingsinname vervolgens worden uitgebreid naar dik vloeibare consistenties (IDDSI[5] 3) en daarna naar glad gemalen voeding (IDDSI 4) tot wat uiteindelijk functioneel haalbaar is na de operatie (maximaal IDDSI 7; normale voeding). Bij patiënten die een uitgebreide chirurgische ingreep van de mondholte hebben ondergaan, zoals een commando operatie, kan het verstandig zijn het free water protocol pas na de vijfde postoperatieve dag te starten, eveneens onder begeleiding van een logopedist, diëtist en mondhygiënist.
Waarden en voorkeuren van patiënten (en evt. hun naasten en/of verzorgers)
Voor patiënten en hun naasten en/of verzorgers zijn het bevorderen van herstel, het verkorten van de ziekenhuisopname en het hervatten van een normaal eetpatroon belangrijke motivaties om vroegtijdig te starten met orale vocht- en voedingsinname na een (faryngo) laryngectomie of uitgebreide mondholteprocedure met (vrije) lapreconstructie. Deze motiverende factoren dragen sterk bij aan het verbeteren van kwaliteit van leven. De prioriteiten kunnen echter verschillen: waar patiënten veelal waarde hechten aan sneller herstel en ontslag, richten zorgprofessionals zich vooral op het voorkomen van complicaties, zoals fistelvorming.
De studie van Wu en collega’s (2022) laat ook zien dat bij een sub-analyse patiënten die een salvage laryngectomie hebben ondergaan dezelfde resultaten laten zien qua fistelvorming dan patiënten die een primaire laryngectomie hebben ondergaan. Hoewel de kwaliteit van het bewijs beperkt is, tonen meta-analyses aan dat vroegtijdige orale inname over het algemeen niet leidt tot een hoger risico op complicaties. Dit ondersteunt de overweging om vroegtijdige orale inname als veilige optie te beschouwen bij patiënten die een totale (faryngo) laryngectomie met of zonder (vrije) lapreconstructie. Verder onderzoek is nodig om aanbevelingen met een hogere bewijslast voor specifieke patiëntgroepen te ontwikkelen.
Kosten (middelenbeslag)
Vroegtijdig starten van orale vocht- en voedingsinname na hoofd-hals oncologische chirurgie kan bijdragen aan het verkorten van de ziekenhuisopnameduur, wat kan resulteren in aanzienlijke kostenbesparingen voor zowel het ziekenhuis als de zorgverzekeraar. Daartegenover staat dat het optreden van complicaties, zoals fistelvorming of wonddehiscentie, kan leiden tot een toename van kosten door verlengde opnames, aanvullende chirurgische ingrepen en intensieve wondzorg.
Bij uitgestelde orale vocht- en voedingsinname is vaak langdurige parenterale of sondevoeding noodzakelijk, wat gepaard gaat met extra materiaalkosten en een grotere inzet van verpleegkundige zorg. Ook kunnen aanvullende diagnostische procedures, zoals endoscopische- of radiologische slikonderzoeken, nodig zijn om het juiste moment voor het hervatten van orale intake te bepalen, wat eveneens de kosten verhoogt.
Een sneller herstel van orale vocht- en voedingsinname kan bovendien de behoefte aan langdurige logopedische (Module Slikfunctiebehoud via prehabilitatie en revalidatie), diëtetische (Module GLIM criteria) en revalidatiezorg verminderen, wat verdere besparing van zorgkosten kan opleveren. Indirect kan vroegtijdige orale vocht- en voedingsinname bijdragen aan een verbeterde kwaliteit van leven en zorgen voor een snellere maatschappelijke re-integratie van patiënten, bijvoorbeeld door een kortere periode van arbeidsongeschiktheid, wat economische voordelen oplevert voor zowel de patiënt als de samenleving.
Aanvaardbaarheid, haalbaarheid en implementatie
Vroegtijdig starten van orale vocht- en voedingsinname na uitgebreide hoofd-halschirurgie met of zonder (vrije) lapreconstructie wordt in toenemende mate als aanvaardbaar beschouwd, mits patiënten worden geïncludeerd die binnen deze uitgangsvraag zijn onderzocht. Echter, over het algemeen gaat men ervan uit dat hoe uitgebreider de reconstructie zal zijn, hoe groter de kans is op wondgenezingproblemen, dus hoe voorzichtiger men moet zijn met het vroegtijdig starten met orale inname. Daarnaast moet de patiënt voldoende helder, coöperatief en instrueerbaar zijn om veilig te kunnen slikken (geen verslikking of beperkte kans op verslikking met goede hoestreflex), mede gezien de mogelijke aanwezigheid van een tracheacanule in de vroege postoperatieve fase. Dit vraagt om goede begeleiding en duidelijke instructies aan en door het behandelteam.
De haalbaarheid van het vroegtijdig starten van orale vocht- en voedingsinname is afhankelijk van een interdisciplinaire aanpak, waarbij tijdige betrokkenheid van logopedisten, diëtisten, mondhygiënisten en verpleegkundigen essentieel is. Scholing van zorgprofessionals in het herkennen van (ver)slikrisico’s en complicaties draagt bij aan een veilige implementatie van het vroegtijdig starten van orale vocht- en voedingsinname.
De implementatie van het vroegtijdig starten van orale vocht- en voedingsinname vraagt daarom om een stapsgewijze opbouw volgens een vooropgesteld protocol (zie IDDSI-levels hierboven). Voorafgaand aan de start moet er voldoende zekerheid zijn over de integriteit van de lapreconstructie (o.a. vitaliteit van de lap), aangezien lekkage van voeding of speeksel langs de lapnaden naar de hals of vaatsteel kan leiden tot ernstige complicaties, zoals wonddehiscentie, infectie of lapnecrose. Indien er twijfel bestaat over het wel of niet aanwezig zijn van een wondfistel in de mond- en keelholte, kan een klinische slikproef met methyleenblauw in water of een slikfoto met wateroplosbaar non-ionisch röntgencontrast (zoals bijv. Ultravist of Omnipaque) worden overwogen, en/of kan het hervatten van orale intake worden uitgesteld. Wanneer er twijfel is over de slikveiligheid en/of -efficiëntie bijvoorbeeld als gevolg van postoperatieve veranderingen (zoals zwelling, veranderde anatomie, etc.) zijn beoordeling en begeleiding door een ervaren logopedist van essentieel belang (zie ook de Richtlijn Orofaryngeale dysfagie: Rol logopedist bij dysfagie - Richtlijn - Richtlijnendatabase). Voor een optimaal postoperatief herstel is een adequate inname van calorieën en eiwitten cruciaal, wat nauwe betrokkenheid van een ervaren diëtist vereist.
Tot slot vereist implementatie van het vroegtijdig starten van orale vocht- en voedingsinname duidelijke protocollen met ruimte voor individuele afwegingen en goede afstemming tussen de intra- en extramurale zorgprofessionals voor een veilige voortzetting van de orale inname na ontslag.
[1] Free water protocol = personen die niet mogen eten of drinken als gevolg van slikproblemen, mogen toch zuiver water drinken, wanneer de mondhygiëne in orde is.
[2] IDDSI= International Dysphagia Diet Standardization Initiative (Home - IDDSI)
[3] WWST: Screeningstest om te onderzoek of iemand moeilijkheden heeft met slikken.
[4] Free water protocol = personen die niet mogen eten of drinken als gevolg van slikproblemen, mogen toch zuiver water drinken, wanneer de mondhygiëne in orde is.
[5] IDDSI= International Dysphagia Diet Standardization Initiative
PICO 1: Totale (faryngo) laryngectomie met of zonder (vrije) lapreconstructie
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Na een (faryngo) laryngectomie wordt vaak gewacht met de start van orale vocht- en voedingsinname uit vrees voor complicaties zoals fistelvorming. Uit de beschikbare literatuur, voornamelijk bestaande uit retrospectieve cohortstudies en een zeer beperkt aantal RCT’s, kon er geen significant verschil in risico op fistelvorming of andere complicaties tussen het vroeg- (binnen 24 uur tot 5 dagen postoperatief) en laattijdig starten van de orale vocht- en voedingsinname worden aangetoond (Volling, 2001; Seven, 2003; Sharifian, 2008; Sousa, 2014). Ook werd geen verschil in ziekenhuisopnameduur gevonden (Medina, 2001; Bulgurcu, 2018).
Op basis hiervan zijn er voldoende argumenten om onder voorwaarden vroegtijdig te starten met orale vocht- en voedingsinname naast de sondevoeding. Daarbij moet worden opgemerkt dat patiënten postoperatief ook doorgaans hun speeksel doorslikken waarbij de wondnaden dus al in contact staan met circa 1 ½ liter waterige en bacterierijke vloeistof per 24 uur. Het vroegtijdig starten van orale inname kan voordelen hebben, zoals behoud en stimulatie van de speekselproductie, behoud van de slikfunctie (‘Use it or Lose it’ theorie – Hutcheson, 2013), verbetering van de mondflora en mondhygiëne en een positieve bijdrage aan de psychosociale revalidatie door het weer kunnen genieten van eten en een snellere verwijdering van de neusmaagsonde. In de praktijk kan overwogen worden te starten met kleine hoeveelheden water volgens het free water protocol[1]. De tolerantie voor vastere voeding kan in de eerste postoperatieve dagen beperkt zijn. De betrokkenheid van een ervaren diëtist is daarom essentieel om te zorgen voor voldoende energie- en eiwitinname, afgestemd op de individuele behoeften en mogelijkheden van de patiënt. Bij een goede slikfunctie en zonder (verdenking op) complicaties kan de orale vocht- en voedingsinname vervolgens worden uitgebreid naar dik vloeibare consistenties (IDDSI[2] 3) en glad gemalen voeding (IDDSI 4) tot wat uiteindelijk functioneel haalbaar is na de operatie (maximaal IDDSI 7; normale voeding). Bij patiënten die een uitgebreide chirurgische ingreep hebben ondergaan zoals een buismaagreconstructie, kan het verstandig zijn pas na de vijfde postoperatieve dag te starten met de inname van water. Indien er problemen worden ervaren bij het starten en/of uitbreiden van orale vocht- en voedingsinname kan een ervaren logopedist ingeschakeld worden.
Indien er twijfel bestaat over het wel of niet aanwezig zijn van een fistel, kan aanvullende beeldvorming (zoals een slikfoto) duidelijkheid geven.
[1] Free water protocol = personen die niet mogen eten of drinken als gevolg van slikproblemen, mogen toch zuiver water drinken, wanneer de mondhygiëne in orde is.
[2] IDDSI= International Dysphagia Diet Standardization Initiative
PICO 2: Excisie met (vrije) lapreconstructie van een uitgebreid mondholtecarcinoom
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Het zo snel mogelijk herstarten van orale vocht- en voedingsinname bij patiënten die een excisie met een (vrije) lapreconstructie van een uitgebreid mondholtecarcinoom hebben ondergaan heeft als voordelen dat de slikfunctie vroegtijdig wordt gestimuleerd en dat sondevoeding sneller kan worden afgebouwd (Use it or Lose it’ theorie – Hutcheson, 2013), wat mogelijk leidt tot een kortere ziekenhuisopname en minder zorgmomenten, ook in de thuissituatie. Het vroegtijdig starten van orale inname kan voordelen hebben, zoals behoud en stimulatie van de speekselproductie, verbetering van de mondflora en mondhygiëne en een positieve bijdrage aan de psychosociale revalidatie door het weer kunnen genieten van eten en een snellere verwijdering van de neusmaagsonde (Hutcheson, 2013). Hoewel er geen overtuigend bewijs is dat vroeg- (<5 dagen) of laattijdig (>5 dagen) postoperatief starten met orale vocht- en voedingsinname een duidelijk voordeel of nadeel oplevert, lijkt uit patiënten perspectief en kostenoverwegingen een zo snel mogelijke afbouw van sondevoeding wenselijk, mits de nutritionele- en energie inname wordt gewaarborgd.
Overweeg om bij patiënten die een excisie met een (vrije) lapreconstructie van een uitgebreid mondholtecarcinoom hebben ondergaan de orale vocht- en voedingsinname vroegtijdig (na 24 uur en binnen 5 dagen postoperatief) te hervatten, startende met kleine slokjes water op de eerste postoperatieve dag, onder begeleiding van een ervaren logopedist, mondhygiënist, diëtist en verpleegkundige gespecialiseerd in hoofd-halskanker. De slikfunctie dient voorafgaand aan de start zorgvuldig beoordeeld te worden om het risico op verslikken, het ontwikkelen van een aspiratiepneumonie en/of wonddehiscentie te minimaliseren (zie Module Slikfunctiebehoud via prehabilitatie en revalidatie en de Richtlijn Orofaryngeale Dysfagie). Indien er twijfel bestaat over het wel of niet aanwezig zijn van een fistel, kan aanvullende beeldvorming (zoals een sliktest met methyleenblauw in water of een slikfoto met bijv. Ultravist of Omnipaque) duidelijkheid geven. Bij aanwezigheid van veel zwelling in de mond- en keelholte, een gecuffte tracheacanule of naadlekkage, dient de orale vocht- en voedingsinname te worden uitgesteld. Start bij voorkeur met een free water protocol en bouw vervolgens geleidelijk op naar dik vloeibare (IDDSI 3) en glad gemalen voeding (IDDSI 4), conform lokale protocollen. Bij het starten van slokjes water volgens het free water protocol is een goede mondzorg belangrijk (preventie aspiratiepneumonie). Hierdoor is betrokkenheid van een mondhygiënist wenselijk.
Bij patiënten met een verhoogd risico op complicaties kan gekozen worden voor een meer voorzichtige, uitgestelde start van orale inname (>5 dagen postoperatief). In geval van ernstige slikdysfunctie kan een beoordeling middels slikbeeldvorming door een specialist zoals een laryngoloog en/of logopedist worden overwogen (zie Module Slikfunctiebehoud via prehabilitatie en revalidatie).
Onderbouwing
The start of oral intake after a total laryngectomy (TLE), pharyngolaryngectomy, or oral cavity intervention with (free) flap reconstruction traditionally begins 10-12 days after surgery (‘late oral intake protocol’) to prevent pharyngocutaneous fistulas.
However, starting oral intake earlier (‘early oral intake protocol’ starts 2-5 days after surgery) may have advantages such as reduced duration of hospital stay, improved nutritional status, maintaining oral hygiene and/or stimulating saliva production, enhance swallowing function (e.g., early stimulation of neuroplasticity; ‘Use it or Lose it’ theory – Hutcheson, 2013), and improved health-related quality of life in the early phase after surgery.
This module will provide recommendations for initiating oral intake in patients who have undergone a TLE or reconstructive surgery of an oral cavity defect using a (free) flap.
PICO 1. Total (pharyngo) laryngectomy with or without (free) flap reconstruction
1.1 Pharyngocutaneous fistula
|
Very low GRADE |
The evidence regarding the effect of early compared to late initiation of oral feeding on fistula formation in patients who have undergone a total (pharyngo) laryngectomy with or without (free) flap reconstruction is very uncertain.
Sources: Volling, 2001; Seven, 2003; Sharifian, 2008; Sousa, 2014 |
1.2 Length of hospital stay
|
Very low GRADE |
The evidence regarding the effect of early compared to late initiation of oral feeding on length of hospital stay in patients who have undergone a total (pharyngo) laryngectomy with or without (free) flap reconstruction is very uncertain.
Source:Medina, 2001; Bulgurcu, 2018 |
1.3 Flap dehiscence, flap necrosis (flap failure), seroma/hematoma formation, wound infection, (health)-related quality of life, functional oral intake and weight loss
|
No GRADE |
No evidence was found regarding the effect of early compared to late initiation of oral feeding on flap dehiscence, flap necrosis, seroma/hematoma formation, wound infection, (health)-related quality of life, functional oral intake, and weight loss in patients who have undergone a total (pharyngo)laryngectomy with or without (free) flap reconstruction.
Source: - |
PICO 2. Reconstructive surgery of an oral cavity defect using a (free) flap
2.1 Oro- or pharyngocutaneous fistula
|
Very low GRADE |
The evidence regarding the effect of early compared to late initiation of oral feeding on fistula formation in patients who have undergone reconstructive surgery of an oral cavity defect using a (free) flap is very uncertain.
Source: Wu, 2022 |
2.2 Length of hospital stay
|
Low GRADE |
The evidence regarding the effect of early compared to late initiation of oral feeding on the length of hospital stay in patients who have undergone reconstructive surgery of an oral cavity defect using a (free) flap is very uncertain.
Source: Wu, 2022 |
2.3 Flap dehiscence
|
Very low GRADE |
The evidence regarding the effect of early compared to late initiation of oral feeding on flap dehiscence in patients who have undergone reconstructive surgery of an oral cavity defect using a (free) flap is very uncertain.
Source: Wu, 2022 |
2.4 Flap necrosis (flap failure)
|
Very low GRADE |
The evidence regarding the effect of early compared to late initiation of oral feeding on flap necrosis in patients who have undergone reconstructive surgery of an oral cavity defect using a (free) flap is very uncertain.
Source: Wu, 2022 |
2.5 Seroma/hematoma formation
|
Very low GRADE |
The evidence regarding the effect of early compared to late initiation of oral feeding on seroma/hematoma formation in patients who have undergone reconstructive surgery of an oral cavity defect using a (free) flap is very uncertain.
Sources: Guidera, 2013; Kerawala, 2021; Le 2022 |
2.6 Wound infection
|
Very low GRADE |
The evidence regarding the effect of early compared to late initiation of oral feeding on wound infection in patients who have undergone reconstructive surgery of an oral cavity defect using a (free) flap is very uncertain.
Source: Wu, 2022 |
2.7 Functional oral intake
|
No GRADE |
The evidence regarding the effect of early compared to late initiation of oral feeding on functional oral intake in patients who have undergone reconstructive surgery of an oral cavity defect using a (free) flap is very uncertain.
Source: Stramiello, 2021 |
2.8 (health)-related quality of life and weight loss
|
No GRADE |
No evidence was found regarding the effect of early compared to late initiation of oral feeding on (health)-related quality of life and weight loss of patients who have undergone reconstructive surgery of an oral cavity defect using a (free) flap.
Source: - |
PICO 1: Total (pharyngo)laryngectomy with or without (free) flap reconstruction
After our literature search one systematic review with a meta-analysis was found for PICO 1. Milinis (2021) performed a systematic review to investigate the effect of early (≤5 days) versus late (>5 days) initiation of oral feeding following total (pharyngo)laryngectomy. The authors searched databases Medline, EMBASE, clinicaltrials.gov, and the Cochrane Library databases until April 2020. Milinis (2021) included both RCTs and cohort studies, that investigated patients who underwent reconstruction with either regional (e.g., pectoralis major flap) or free flaps. Their search was limited to studies reported in the English language. Exclusion criteria of Milinis (2021) were: failure to report the rates of fistula formation, pediatric populations, duplicated and republicated studies and abstracts, inadequate sample size (n < 10), and studies which commenced early oral feeding after day 5. The primary study outcome was the incidence of fistula formation in the early feeding (≤5 days) group compared to the late feeding (>5 days) group. The secondary outcome was the length of hospital stay. For RCTs, the authors used the Cochrane risk of bias tool (RoB 1.0) to perform risk of bias assessment. For cohort studies, the Newcastle-Ottawa tool was used (Wells, 2013). In the review of Milinis (2021) a total of 374 studies were identified, of which 31 full text articles were screened. In total they included 4 RCTs and 10 cohort studies.
For the outcome measure of fistula formation in PICO 1 only the RCTs were included in the analysis, and for the outcome measure length of hospital stay, only two of the ten cohort studies (Bulgurcu, 2018; Medina, 2001) were additionally included since no RCTs reported on length of hospital stay (see Table 1).
Table 1. Characteristics of the included studies for PICO 1 (studies from the systematic review of Milinis, 2021)
|
Study |
Country |
Study design |
Sample size |
Male (%) |
Mean age |
Start of early oral feeding (day) |
Start of late feeding (day) |
Included for outcomes in this analysis |
|
Volling (2001) |
Germany |
RCT |
42 |
34 (80.9) |
NR |
≤5 |
>5 |
Fistula formation |
|
Seven (2003) |
Turkey |
RCT |
65 |
60 (92.3) |
55.7
|
1 |
7 |
Fistula formation |
|
Sharifian (2008) |
Iran |
RCT |
25 |
NR |
66.0 |
3 |
7 |
Fistula formation |
|
Sousa (2014) |
Brazil |
RCT |
89 |
82 (92.1) |
61.0 |
1 |
7 |
Fistula formation |
|
Bulgurcu (2018) |
Turkey |
Retrospective cohort |
62 |
59 (95.0) |
61.7 |
3 |
7 |
Length of hospital stay |
|
Medina (2001) |
United States |
Retrospective cohort |
94 |
NR |
NR |
≤2 |
>7 |
Length of hospital stay |
NR, not reported; RCT, randomized controlled trial
PICO 2: Reconstructive surgery of an oral cavity defect using a (free) flap
Dean (2024) performed a systematic review and meta-analysis to investigate the effect of early (≤5 days) versus late (>5 days) initiation of oral feeding following head and neck reconstructive surgery of the upper aerodigestive tract using (free) flaps. The authors searched the Databases PubMed, Scopus, Cochrane, and Web of Science until 30th August 2022 and 16th August 2023. Inclusion criteria of the systematic review were: RCT, meta-analysis, case-control or cohort studies, including adult (≥18 years) patients undergoing head and neck reconstructive surgery of the upper aerodigestive tract using (free) flaps, reporting length of hospital stay, and availability of full text in English. The outcomes of interest were: incidence of postoperative fistula, flap dehiscence, flap necrosis, seroma/hematoma formation, wound infection, functional oral intake, and length of hospital stay between patients with early versus patients with late initiation of postoperative oral feeding. Dean (2024) used the Newcastle-Ottawa tool for risk of bias assessment (Wells, 2013). In total, 1452 studies were identified, of which 126 full text articles were screened. Of those, 5 studies were included (of which 1 RCT and 4 cohort studies).
For our PICO 2, the RCT of Wu (2022) was included for five of the seven outcome measures. For the outcome measure seroma/hematoma formation 3 cohort studies (Kerawala, 2021; Guidera, 2013; and Le, 2022) were included, and the cohort study of Stramiello (2021) was included based on the subgroup analysis of their secondary outcome on functional oral intake (see Table 2). Subgroup analysis was used to exclude patients who underwent surgical tumor resection and reconstruction at sites other than the oral cavity.
Table 2. Characteristics of the included studies for PICO 2 (studies from the systematic review of Dean, 2024)
|
Study |
Country |
Study design |
Sample size |
Male (%) |
Mean age |
Start of early oral feeding (day) |
Start of late oral feeding (day) |
Included for outcomes in this analysis |
|
Wu (2022) |
China |
RCT |
128 |
76 (59.4) |
51.5
|
1 |
unclear |
Fistula formation, length of hospital stay, flap dehiscence, flap necrosis (flap failure), wound infection |
|
Kerawala (2021) |
United Kingdom |
Prospective cohort |
400 |
228 (57.0) |
62.2 |
1 |
>5 |
Seroma/hematoma formation |
|
Guidera (2013) |
New Zealand |
Retrospective cohort |
54 |
NR |
60.9 |
≤5 |
>5 |
Seroma/hematoma formation |
|
Le (2022) |
United States |
Retrospective cohort |
415 |
253 (61.0) |
58.9 |
≤5 |
>5 |
Seroma/hematoma formation |
|
Stramiello (2021) |
United States |
Retrospective cohort |
104 |
68 (65.3) |
62.3 |
≤5 |
>5 |
Fistula formation/ functional oral intake |
RCT, randomized controlled trial; NR, not reported
Results
PICO 1: Total (pharyngo) laryngectomy with or without (free) flap reconstruction
1.1 Pharyngocutaneous fistula formation
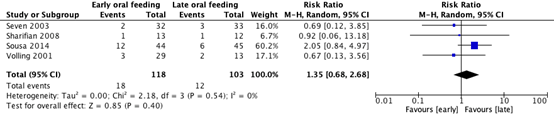
Formation of pharyngocutaneous fistula was reported in four RCTs (see Figure 1). The pooled effect was RR 1.35 (95% CI 0.68 to 2.68), in favor of late initiation of oral feeding (heterogeneity: I2 = 0%).
Figure 1. Forest plot of the RCTs by Seven (2003), Sharifian (2008), Sousa (2024), and Volling (2001) on early versus late initiation of oral feeding in patients with total (pharyngo) laryngectomy regarding the outcome measure formation of pharyngocutaneous fistula
1.2 Length of hospital stay
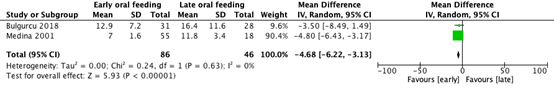
Length of hospital stay was reported in two cohort studies (see Figure 2). The mean difference was -4.68 days (95% CI -6.22 to -3.13), in favor of early initiation of oral feeding (heterogeneity: I2 = 0%). This result is clinically relevant.
Figure 2. Forest plot of the cohort studies by Bulgurcu (2018) and Medina (2001) on early versus late initiation of oral feeding in patients with total (pharyngo) laryngectomy regarding the outcome measure length of hospital stay (days)
The outcome measures flap dehiscence, flap necrosis, seroma/hematoma formation, wound infection, (health)-related quality of life, functional oral intake, and weight loss were not reported for PICO 1.
PICO 2: Reconstructive surgery of an oral cavity defect using a (free) flap.
2.1 Oro- or pharyngocutaneous fistula
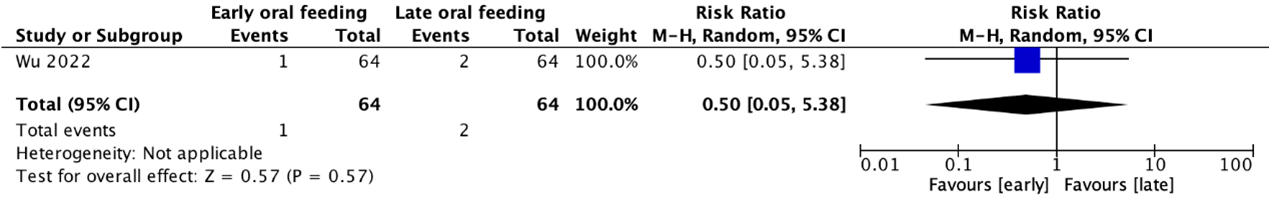
Formation of oro- or pharyngocutaneous fistula was reported in the RCT by Wu (2022) (see Figure 3). Due to the absence of multiple studies, pooling of data was not possible. The risk ratio was 0.50 (95% CI 0.05 to 5.38) in favor of early initiation of oral feeding. This means the risk of oro- or pharyngocutaneous fistula formation is 50% lower in the early versus the late initiation of oral feeding group. This result is clinically relevant.
Figure 3. Forest plot of the RCT by Wu (2022) on early versus late initiation of oral feeding in patients with head and neck reconstructive surgery using (free) flaps regarding the outcome measure oro- or pharyngocutaneous fistula
2.2 Length of hospital stay
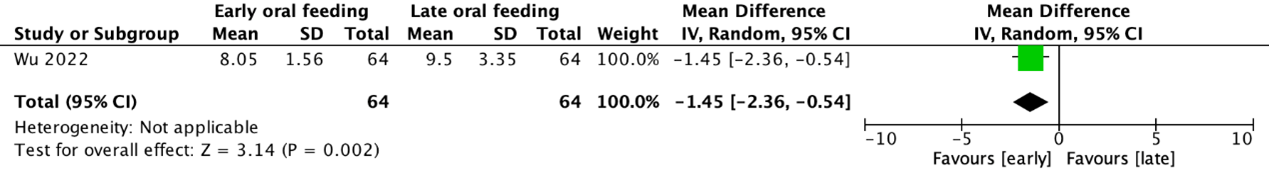
Length of hospital stay was reported in the RCT by Wu (2022) (see Figure 4). Due to the absence of multiple studies, pooling of data was not possible. The mean difference was -1.45 days (95% CI -2.36 to -0.54), in favor of early initiation of oral feeding. This result is not clinically relevant.
Figure 4. Forest plot of the RCT by Wu (2022) on early versus late initiation of oral feeding in patients with head and neck reconstructive surgery using (free) flaps regarding the outcome measure length of hospital stay (days)
2.3 Flap dehiscence
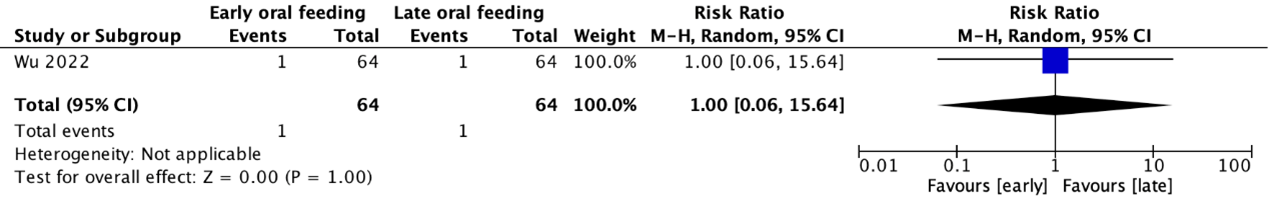
Flap dehiscence was reported in the RCT by Wu (2022) (see Figure 5). Due to the absence of multiple studies, pooling of data was not possible. The risk ratio was 1.00 (95% CI 0.06 to 15.64). This result is not clinically relevant.
Figure 5. Forest plot of the RCT of Wu (2022) on early versus late initiation of oral feeding in patients with head and neck reconstructive surgery using (free) flaps regarding the outcome measure flap dehiscence
2.4 Flap necrosis
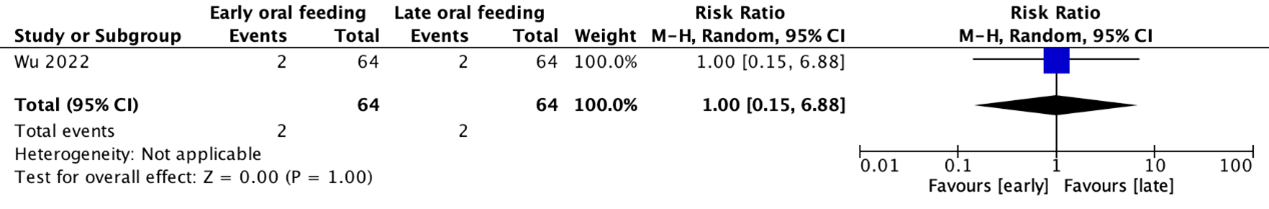
Flap necrosis (flap failure) was reported in the RCT by Wu (2022) (see Figure 6). Due to the absence of multiple studies, pooling of data was not possible. The risk ratio was 1.00 (95% CI 0.15 to 6.88). This result is not clinically relevant.
Figure 6. Forest plot of the RCT by Wu (2022) on early versus late initiation of oral feeding in patients with head and neck reconstructive surgery using (free) flaps regarding the outcome measure flap necrosis
2.5 Seroma/hematoma formation
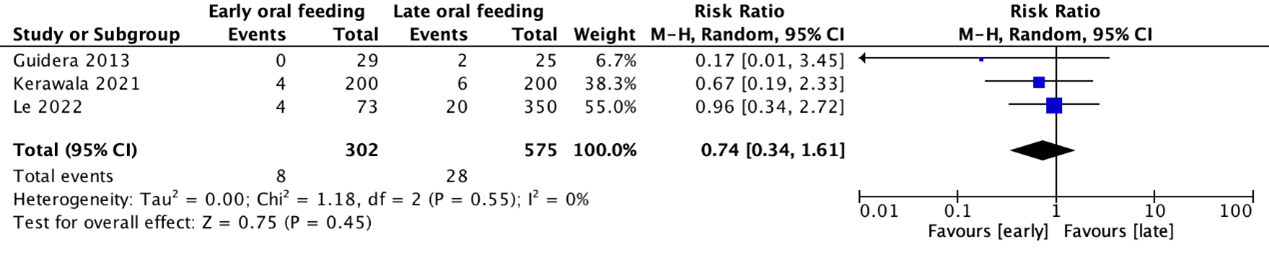
Seroma/hematoma formation was reported in the cohort studies by Guidera (2013), Kerawala (2021), and Le (2022) (see Figure 7). The risk ratio was 0.74 (95% CI 0.34 to 1.61), in favor of early initiation of oral feeding (heterogeneity: I2 = 0%). This means the risk of seroma/hematoma formation is 26% lower in the early versus the late initiation of oral feeding group. This result is clinically relevant.
Figure 7. Forest plot of the cohort studies by Guidera (2013), Kerawala (2021), and Le (2022) on early versus late initiation of oral feeding in patients with head and neck reconstructive surgery using (free) flaps regarding the outcome measure seroma/hematoma formation
2.6 Wound infection
Wound infection was reported in the RCT by Wu (2022) (see Figure 8). Due to the absence of multiple studies, pooling of data was not possible. The risk ratio was 0.80 (95% CI 0.23 to 2.84). This result is not clinically relevant.
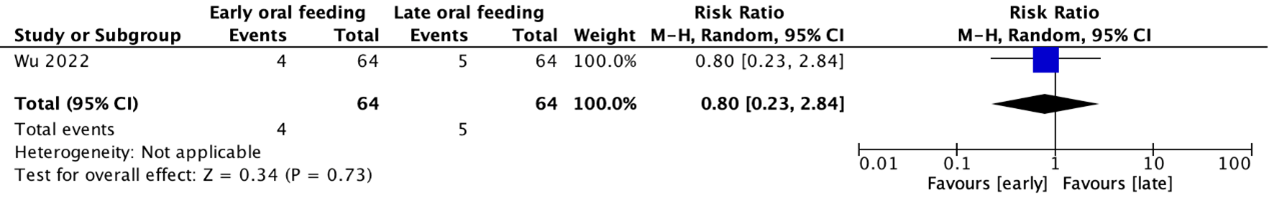 Figure 8. Forest plot of the RCT by Wu (2022) on early versus late initiation of oral feeding in patients with head and neck reconstructive surgery using (free) flaps regarding the outcome measure wound infection
Figure 8. Forest plot of the RCT by Wu (2022) on early versus late initiation of oral feeding in patients with head and neck reconstructive surgery using (free) flaps regarding the outcome measure wound infection
2.7 Functional oral intake
The functional oral intake scale (FOIS) was reported in the cohort study of Stramiello (2021) (Table 2). Subgroup analysis was used to exclude patients who underwent surgical tumor resection and reconstruction at sites other than the oral cavity.
Functional oral intake was assessed using the seven-point FOIS, which measures levels of oral dietary tolerance. FOIS scores range from complete dependence on enteral tube feeding (FOIS 1) to an unrestricted oral diet (FOIS 7). FOIS data were available for 76 patients (97.4%) with oral cavity and mandible reconstruction. Patients were categorized into two groups: the ‘early feeding’ (EF) group, consisting of patients who were fed on or before postoperative day (POD) 5, and the ‘late feeding’ (LF) group, consisting of patients who began oral intake after POD 5. Eight patients (38%) in the EF group were on a full oral diet (FOIS > 3) by POD 30. In the LF group, 19 patients (35%) were on an oral diet by POD 30. There was no statistically significant difference between the EF and LF groups on POD 30 (P = .814), POD 60 (P = .538), and POD 90 (P = .229).
The outcomes (health)-related quality of life and weight loss were not reported.
Level of evidence of the literature
PICO 1: Total (pharyngo) laryngectomy with or without (free) flap reconstruction
1.1 Pharyngocutaneous fistula
The level of evidence regarding the outcome measure pharyngocutaneous fistula formation started at high (due to the randomization in the studies), was downgraded by 3 levels because of study limitations (risk of bias); and because of imprecision (-2, both thresholds for a minimal clinically important difference were crossed) to very low.
1.2 Length of hospital stay
The level of evidence regarding the outcome measure length of hospital stay started at low (due to the observational nature of the studies) and was downgraded by one level because of study limitations (-1 risk of bias) to very low.
1.3 Remaining outcome measures
The outcome measures flap dehiscence, flap necrosis, seroma/hematoma formation, wound infection, (health)-related quality of life, functional oral intake, and weight loss were not reported.
PICO 2: Reconstructive surgery of an oral cavity defect using a (free) flap.
2.1 Oro- or pharyngocutaneous fistula
The level of evidence regarding the outcome measure oro- or pharyngocutaneous fistula formation started at high, was downgraded by 3 levels because of study limitations (-1, risk of bias), and because of imprecision (-2, both thresholds for a minimal clinically important difference were crossed) to very low.
2.2 Length of hospital stay
The level of evidence regarding the outcome measure length of hospital stay started at high, was downgraded by 3 levels because of study limitations (-1, risk of bias); and because of imprecision (-1, one threshold for minimal clinically important difference was crossed) to low.
2.3 Flap dehiscence
The level of evidence regarding the outcome measure flap dehiscence started at high, was downgraded by 3 levels because of study limitations (-1, risk of bias); and because of imprecision (-2, both thresholds for a minimal clinically important difference were crossed) to very low.
2.4 Flap necrosis
The level of evidence regarding the outcome measure flap necrosis (flap failure) started at high, was downgraded by 3 levels because of study limitations (-1, risk of bias); and because of imprecision (-2, both thresholds for a minimal clinically important difference were crossed) to very low.
2.5 Seroma/hematoma formation
The level of evidence regarding the outcome measure seroma/hematoma formation started at low (due to the observational nature of the studies) and was downgraded by one level because of study limitations (-1 risk of bias) to very low.
2.6 Wound infection
The level of evidence regarding the outcome measure wound infection started at high, was downgraded by 3 levels because of study limitations (-1, risk of bias); and because of imprecision (-2, both thresholds for a minimal clinically important difference were crossed) to very low.
2.7 Functional oral intake
The level of evidence regarding the outcome functional oral intake started at low (due to the observational nature of the study) and was downgraded by one level because of risk of bias and of study limitations (-1 risk of bias) to very low.
2.8 (Health)-related quality of life and weight loss
The outcome measures (health)-related quality of life and weight loss were not reported.
A systematic review of the literature was performed to answer the following question:
What is the difference in complications (i.e. pharyngocutaneous fistula (PCF) formation) between early and late oral intake protocols in patients who have undergone 1) a TLE or pharyngolaryngectomy or 2) head and neck reconstructive surgery of an oral cavity defect using (free) flaps.
PICO 1
| P: | Patients who have undergone a (pharyngo)laryngectomy with primary closure, regional flap reconstruction, or free flap reconstruction |
| I: | ‘Early oral intake’ protocol |
| C: | ‘Late oral intake’ protocol |
| O: | Fistula formation, length of hospital stay, flap/wound dehiscence, flap necrosis, seroma/hematoma formation, wound infection (health)-related quality of life, functional oral intake, weight loss |
PICO 2
| P: | Patients who have undergone reconstructive surgery of an oral cavity defect using a (free) flap |
| I: | ‘Early oral intake’ protocol |
| C: | ‘Late oral intake’ protocol |
| O: | Fistula formation, length of hospital stay, flap/wound dehiscence, flap necrosis, seroma/hematoma formation, wound infection, (health)-related quality of life, functional oral intake, weight loss |
Relevant outcome measures
The guideline development group considered fistula formation as a critical outcome measure for decision making; length of hospital stay, flap dehiscence, flap necrosis, seroma/hematoma formation, wound infection, (health)-related quality of life, functional oral intake, and weight loss as important outcome measures for decision making.
A priori, the guideline development group did not predefine the outcome measures listed above but instead used the definitions provided in the studies.
For fistula formation, a 25% relative difference for dichotomous outcomes (present/absent)(RR < 0.8 or > 1.25) was defined as a minimal clinically important difference (MCID).
For length of hospital stay, a mean difference of 2 days was defined as a MCID.
For flap dehiscence, a 25% relative difference for dichotomous outcomes (present/absent)(RR < 0.8 or > 1.25) was defined as a MCID.
For flap necrosis (flap failure), a 25% relative difference for dichotomous outcomes (present/absent)(RR < 0.8 or > 1.25) was defined as a MCID.
For seroma/hematoma formation, a 25% relative difference for dichotomous outcomes (present/absent)(RR < 0.8 or > 1.25) was defined as a MCID.
For wound infection, a 25% relative difference for dichotomous outcomes (present/absent)(RR < 0.8 or > 1.25) was defined as a MCID.
For (health)-related quality of life, a change of 25% in the outcome score (RR < 0.8 or > 1.25) since the MCID is unclear.
For functional oral intake, a change of 1 point in total score (Messing 2017) was defined as a MCID.
For weight loss the working group defined a10% difference in the outcome score (Kg) in six months and 5% in one month as a MCID.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until 29 March 2024. The detailed search strategy is available on request (info@richtlijnendatabase.nl). The systematic literature search resulted in 106 hits in total for PICO 1 and PICO 2. Studies were selected based on the following criteria: systematic reviews (searched in at least two databases, with detailed search strategy, risk of bias assessment, and results of individual studies available), randomized controlled trials (RCTs), and observational (cohort)studies answering the search question.
Results
Twenty studies were initially included based on title and abstract screening. Of those twenty studies, two systematic review studies met the inclusion criteria and were selected (Milinis (2021) for PICO 1 and Dean (2024) for PICO 2). The remaining eighteen articles were further analyzed and excluded if they did not meet the inclusion criteria, had a high risk of bias or if they already were included in the systematic review by Milinis (2021) or Dean (2024) (see Table of excluded studies). No new or more recent studies were included, so a total of 12 articles were included (all included in the reviews by Milinis or Dean). The assessment of the risk of bias is summarized in the risk of bias tables.
- Bulğurcu S, Çukurova İ. Comparison of Early Versus Delayed Oral Feeding After Total Laryngectomy in Terms of Pharyngocutaneous Fistula Development. Turk Arch Otorhinolaryngol. 2018 Dec;56(4):217-220. doi: 10.5152/tao.2018.3605. Epub 2018 Dec 25. PMID: 30701117; PMCID: PMC6340318.
- Dean YE, Motawea KR, Bamousa BAA, Loayza Pintado JJ, Elawady SS, Soffar M, Shah J, Wilcox K, Aiash H. Early oral feeding and its impact on postoperative outcomes in head and neck cancer surgery: a meta-analysis. Maxillofac Plast Reconstr Surg. 2024 Mar 28;46(1):11. doi: 10.1186/s40902-024-00421-0. PMID: 38538984; PMCID: PMC10973317.
- Gillman A, Winkler R, Taylor NF. Implementing the Free Water Protocol does not result in aspiration pneumonia in carefully selected patients with dysphagia: a systematic review. Dysphagia. 2017;32(3):345‑361. doi:10.1007/s00455-016-9761-3.
- Guidera AK, Kelly BN, Rigby P, MacKinnon CA, Tan ST. Early oral intake after reconstruction with a free flap for cancer of the oral cavity. Br J Oral Maxillofac Surg. 2013 Apr;51(3):224-7. doi: 10.1016/j.bjoms.2012.06.005. Epub 2012 Jul 7. PMID: 22776518.
- Hutcheson KA, Bhayani MK, Beadle BM, et al. Eat and Exercise During Radiotherapy or Chemoradiotherapy for Pharyngeal Cancers: Use It or Lose It. JAMA Otolaryngol Head Neck Surg. 2013;139(11):1127–1134. doi:10.1001/jamaoto.2013.4715.
- Kerawala CJ, Riva F, Paleri V. The impact of early oral feeding following head and neck free flap reconstruction on complications and length of stay. Oral Oncol. 2021 Feb;113:105094. doi: 10.1016/j.oraloncology.2020.105094. Epub 2020 Nov 23. PMID: 33242736.
- Le JM, Ying YP, Seri C, Deatherage H, Bourne G, Morlandt AB. Does Early Oral Intake After Microvascular Free Flap Reconstruction of the Oral Cavity Lead to Increased Postoperative Complications? J Oral Maxillofac Surg. 2022 Oct;80(10):1705-1715. doi: 10.1016/j.joms.2022.06.011. Epub 2022 Jun 24. PMID: 35870510.
- Medina JE, Khafif A. Early oral feeding following total laryngectomy. The Laryngoscope. 2001 Mar;111(3):368-72.
- Milinis K, Gaskell P, Lau A, Lancaster J, Jones T. Early versus late oral feeding following total (pharyngo)laryngectomy: Systematic review and meta-analysis. Head Neck. 2021 Apr;43(4):1359-1368. doi: 10.1002/hed.26616. Epub 2021 Feb 4. PMID: 33543554.
- Panther K, The Frazier Free Water Protocol. SIG 13 Perspectives on swallowing and swallowing disorders. Dysphagia. 2005;14(1):4–9.
- Seven H, Calis AB, Turgut S. A randomized controlled trial of early oral feeding in laryngectomized patients. Laryngoscope. 2003 Jun;113(6):1076-9. doi: 10.1097/00005537-200306000-00030. PMID: 12782826.
- Sharifian HA, Najafi M, Khajavi M. Early oral feeding following total laryngectomy. Tanaffos. 2008;123:333-338.
- Sousa AA, Porcaro-Salles JM, Soares JM, Meyer de Moraes G, Souza Silva G, Abreu Sepulcri R, Rezende Carvalho J, Savassi-Rocha PR. Tolerance of early oral feeding in patients subjected to total laryngectomy. Head Neck. 2016 Apr;38 Suppl 1:E643-8. doi: 10.1002/hed.24063. Epub 2015 Jun 15. PMID: 25832556.
- Stramiello J, Nuyen B, Saraswathula A, Blumenfeld L, Divi V, Rosenthal E, Orosco R, Starmer HM. Timing of postoperative oral feeding after head and neck mucosal free flap reconstruction. Laryngoscope Investig Otolaryngol. 2021 Sep 9;6(5):1031-1036. doi: 10.1002/lio2.655. PMID: 34667846; PMCID: PMC8513441.
- Volling P, Singelmann H, Ebeling O. Inzidenz von Speichelfisteln in Abhängigkeit vom Zeitpunkt einer oralen Ernährung nach Laryngektomie [Incidence of salivary fistulas in relation to timing of oral nutrition after laryngectomy]. HNO. 2001 Apr;49(4):276-82. German. doi: 10.1007/s001060050746. PMID: 11382108.
- Wu HY, Shan XF, Cai ZG, Zhang J, Li PJ, Zhang L, Yang Y. Timing of Oral Feeding in Patients Who have Undergone Free Flap Reconstruction for Oral Cancer. Laryngoscope. 2023 Jun;133(6):1382-1387. doi: 10.1002/lary.30435. Epub 2022 Oct 6. PMID: 36200736.
- Wells GA, Shea B, O'Connell D, et al. The Newcastle-Ottawa scale (NOS) for assessing the quality of nonrandomized studies in meta-analyses [Internet]. Ottawa Hosp Res Inst. 2013;(3): 1-4.
Risk of bias tables
For risk of bias analysis of Seven (2003), Sharifian (2008), Sousa (2015), Volling (2001), Bulgurcu (2018) and Medina (2001), see Milinis (2021).
For risk of bias analysis of Guidera (2013), Kerawala (2021), Stramiello (2021), Le (2022) and Wu (2022), see Dean (2024).
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Barlow J, Sragi Z, Rodriguez N, Alsen M, Kappauf C, Ferrandino R, Chennareddy S, Kotz T, Kirke DN, Teng MS, Genden EM, Khan MN, Roof SA. Early feeding after free flap reconstruction of the oral cavity: A systematic review and meta-analysis. Head Neck. 2024 May;46(5):1224-1233. doi: 10.1002/hed.27684. Epub 2024 Feb 27. PMID: 38414175. |
More recent systematic review included (Dean) |
|
Imai, T. and Asada, Y. and Matsuura, K. Enhanced recovery pathways for head and neck surgery with free tissue transfer reconstruction. Auris Nasus Larynx. 2024; 51 (1) :38-50 |
Not a systematic review or RCT (paper desribes the ERAS protocol) |
|
Le, John M. and Ying, Yedeh P. and Seri, Chaitra and Deatherage, Holton and Bourne, Graham and Morlandt, Anthony B. Does Early Oral Intake After Microvascular Free Flap Reconstruction of the Oral Cavity Lead to Increased Postoperative Complications?. Journal of oral and maxillofacial surgery : official journal of the American Association of Oral and Maxillofacial Surgeons. 2022; 80 (10) :1705-1715 |
Included in Dean (2024) |
|
Kerawala, Cyrus J. and Riva, Francesco and Paleri, Vinidh The impact of early oral feeding following head and neck free flap reconstruction on complications and length of stay. Oral oncology. 2021; 113 :105094 |
Included in Dean (2024) |
|
Stramiello, Joshua and Nuyen, Brian and Saraswathula, Anirudh and Blumenfeld, Liza and Divi, Vasu and Rosenthal, Eben and Orosco, Ryan and Starmer, Heather M. Timing of postoperative oral feeding after head and neck mucosal free flap reconstruction. Laryngoscope investigative otolaryngology. 2021; 6 (5) :1031-1036 |
Included in Dean (2024) |
|
Yi, Xuelian and Hu, Chunhong and Peng, Yi and Wen, Zili and Li, Xue and Ye, Linlin and Huang, Qingsong Meta-analysis on the safety and efficacy of early oral feeding after total laryngectomy. Journal of B.U.ON. : official journal of the Balkan Union of Oncology. 2021; 26 (5) :2019-2025 |
Poor quality systematic review (description of studies, description of excluded studies, no risk of bias analysis perforemd, RCTs and observational studies pooled) |
|
Suslu, Nilda and Sefik Hosal, A. Early oral feeding after total laryngectomy: Outcome of 602 patients in one cancer center. Auris, nasus, larynx. 2016; 43 (5) :546-50 |
Included in Milinis (2021) |
|
Aires, Felipe Toyama and Dedivitis, Rogerio Aparecido and Petrarolha, Silvia Migueis Picado and Bernardo, Wanderley Marques and Cernea, Claudio Roberto and Brandao, Lenine Garcia Early oral feeding after total laryngectomy: A systematic review. Head & neck. 2015; 37 (10) :1532-5 |
Poor quality systematic review (study selection unclear), more recent systematic reviews available |
|
Serbanescu-Kele, C. M. C. and Halmos, G. B. and Wedman, J. and van der Laan, B. F. A. M. and Plaat, B. E. C. Early feeding after total laryngectomy results in shorter hospital stay without increased risk of complications: a retrospective case-control study. Clinical otolaryngology : official journal of ENT-UK ; official journal of Netherlands Society for Oto-Rhino-Laryngology & Cervico-Facial Surgery. 2015; 40 (6) :587-92 |
Included in Milinis (2021) |
|
Kishikova, Lyudmila and Fleming, Jason C. Oral feeding following laryngectomy: early or delayed?. International journal of surgery (London, England). 2014; 12 (11) :1137-40 |
Not a systematic review (only one database searched, poor quality search strategy)
|
|
Sousa, A. A. and Porcaro-Salles, J. M. and Soares, J. M. A. and de Moraes, G. M. and Silva, G. S. and Sepulcri, R. A. and Savassi-Rocha, P. R. Does early oral feeding increase the likelihood of salivary fistula after total laryngectomy?. The Journal of laryngology and otology. 2014; :1-7 |
Included in Milinis (2021) |
|
Timmermans, A. Jacqueline and Lansaat, Liset and Kroon, Gertruda V. J. and Hamming-Vrieze, Olga and Hilgers, Frans J. M. and van den Brekel, Michiel W. M. Early oral intake after total laryngectomy does not increase pharyngocutaneous fistulization. European archives of oto-rhino-laryngology : official journal of the European Federation of Oto-Rhino-Laryngological Societies (EUFOS) : affiliated with the German Society for Oto-Rhino-Laryngology - Head and Neck Surgery. 2014; 271 (2) :353-8 |
Included in Milinis (2021) |
|
Guidera, Alice K. and Kelly, Bronwen N. and Rigby, Paul and MacKinnon, Craig A. and Tan, Swee T. Early oral intake after reconstruction with a free flap for cancer of the oral cavity. The British journal of oral & maxillofacial surgery. 2013; 51 (3) :224-7 |
Included in Dean (2024) |
|
Martin, S. K. and Jordan, Z. and Carney, A. S. The effect of early oral feeding compared to standard oral feeding following total laryngectomy: A systematic review. JBI Database of Systematic Reviews and Implementation Reports. 2013; 11 (11) :140-182 |
More recent systematic review available. Low quality systematic review |
|
Aswani, J. and Thandar, M. and Otiti, J. and Fagan, J. Early oral feeding following total laryngectomy. The Journal of laryngology and otology. 2009; 123 (3) :333-8 |
Included in Milinis (2021) |
|
Sharifian, H. A. and Najafi, M. and Khajavi, M. Early oral feeding following total laryngectomy. Tanaffos. 2008; 7 (2) :64-70 |
Included in Milinis (2021) |
|
Seven, Huseyin and Calis, Asli Batur and Turgut, Suat A randomized controlled trial of early oral feeding in laryngectomized patients. The Laryngoscope. 2003; 113 (6) :1076-9 |
Included in Milinis (2021) |
|
Volling, P. and Singelmann, H. and Ebeling, O. [Incidence of salivary fistulas in relation to timing of oral nutrition after laryngectomy]. Inzidenz von Speichelfisteln in Abhangigkeit vom Zeitpunkt einer oralen Ernahrung nach Laryngektomie.. 2001; 49 (4) :276-82 |
Included in Milinis (2021) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 28-01-2026
Beoordeeld op geldigheid : 28-01-2026
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd door de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2023 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met hoofd-halskanker.
Werkgroep
- Prof. dr. L.W.J. (Laura) Baijens, voorzitter, Nederlandse Vereniging van Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied (NVKNO)
- A.C.P. (Anne) Kauerz-de Rooij, Ergotherapie Nederland (EN)
- Dr. C.M. (Caroline) Speksnijder, Koninklijk Nederlands Genootschap Fysiotherapie (KNGF)
- Dr. D.J.M. (Doke) Buurman - Koninklijke Nederlandse Maatschappij tot bevordering der Tandheelkunde (KNMT)
- Dr. K.S. (Kathelijn) Versteeg, Nederlandse Internisten Vereniging (NIV)
- Drs. D. (Desiree) Dona, Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde (NVAB)
- Dr. A. (Annemieke) Kok, Nederlandse Vereniging van Diëtisten (NVD)
- Drs. M. (Marieke) Jacobs, Nederlandse Vereniging voor Klinische Arbeidsgeneeskunde (NVKA)
- Dr L. (Lisette) van der Molen, Nederlandse Vereniging voor Logopedie en Foniatrie (NVLF)
- Dr. L.H.E. (Luc) Karssemakers, Nederlandse Vereniging voor Mondziekten, Kaak- en Aangezichtschirurgie (NVMKA)
- Dr. J. (Jos) Elbers, Nederlandse Vereniging voor Radiotherapie en Oncologie (NVRO)
- R.A. (Rob) Burdorf, Patiëntenvereniging HOOFD-HALS (PvHH)
- P.S. (Petra) Verdouw, Patiëntenvereniging HOOFD-HALS (PvHH)
- Drs. M. (Michael) Brouwers, Nederlandse Vereniging van Revalidatieartsen (VRA)
- Drs. E. (Ellen) Passchier, Verpleegkundigen en Verzorgenden Nederland (V&VN)
- Drs. N. (Narda) Hendriks, Nederlandse Vereniging voor Plastische Chirurgie (NVPC)
Klankbordgroep
- Prof. dr. R. (Remco) de Bree, Nederlandse Vereniging van Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied (NVKNO)
- Dr. P. (Pim) de Graaf, Nederlandse Vereniging voor Radiologie (NVvR)
- Dr. D.S.V.M. (Dominique) Clément, Nederlandse Vereniging van Maag-Darm-Leverartsen (NVMDL)
- J. (Jesmin) Poelstra, Beroepsvereniging van Professionals in Sociaal Werk (BPSW)
- Dr. G. (Gerben) van Hinte, Koninklijk Nederlands Genootschap Fysiotherapie (KNGF)
- Drs. A. (Anne) Arens, Nederlandse Vereniging voor Nucleaire Geneeskunde (NVNG)
- Dr. F. (Femke) Jansen, Nederlandse Vereniging voor Psychosociale Oncologie (NVPO)
Met ondersteuning van
- Dr. L.M. (Lisette) van Leeuwen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. E. (Evelien) Belfroid, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Gemelde (neven)functies en belangen richtlijnwerkgroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Laura Baijens |
KNO-arts/Laryngoloog/Hoofd-hals chirurg Maastricht Universitair Medisch Centrum (MUMC+) |
Consultant for Phagenesis Limited, The Elms Courtyard, Bromesberrow, Ledbury, HR8 1RZ UK. The PhINEST Study – Pharyngeal ICU - Novel Electrical Stimulation Therapy: a prospective, European multi-site, randomised, sham-controlled, single-blind (outcome assessor-blinded) study. August 2018 – 2030 (Consultancy Agreement via the Clinical Trial Center Maastricht) |
Consultant for Phagenesis Limited in the PhINEST Study heeft geen betrekking of relaties met de huidige richtlijn. Het is een Europese multicenter studie over dysfagie bij CVA patiënten waarin ik advies geef. De opbrengsten gaan naar het Clinical Trial Center Maastricht. |
Neen |
Phagenesis Limited Advies geven in een studie over faryngeale elektrostimulatie bij CVA patiënten, MUMC+ is geen site en betreft geen patiënten met hoofd-halskanker.
Michel Keijzer Fonds PVHH Multi-domein screening van hoofd-halskankerpatiënten |
Intellectueel eigendom: Ik ben PI in meerdere lopende niet-WMO studies over dysfagie bij hoofd-halskanker. Ik heb vele internationale W1-publicaties over dysfagie bij hoofd-halskanker. De kans is reëel dat deze publicaties terecht zullen komen in de output van systematic literatuur searches voor deze richtlijn. Er is geen sprake van 'vermarkting' of verwerven van een boegbeeldfunctie bij organisaties. |
Nee |
juli 2025 |
Geen restricties (extern gefinancierd onderzoek heeft geen relatie met het onderwerp van de richtlijn) |
|
Anne Kauerz |
Ergotherapeut UMC Utrecht |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
juli 2025 |
Geen restricties |
|
Desiree Dona |
bedrijfsarts / klinisch arbeidsgeneeskundige oncologie 1.0 fte Radboudumc werkzaamheden: arbeidsgeneeskundige begeleiding in behandelteam van oncologiepatienten, projectmanagement, onderzoek en onderwijs. Alle werkzaamheden zijn betaald. |
vennoot van DELEN ABC (arbeidsdeskundige advisering en coaching) generieke module Arbeidsparticipatie voor medisch specialistische richtlijnen (vacatiegelden) |
Geen |
neen |
Prehabilitatie en werkbegeleiding voor borstkankerpatienten (gefinancierd door MOVIR en Stichting Enjoy the ride, unrestricted grant, geen PI) |
Ik heb een boegbeeldfunctie bij het Radboudumc (Principal Clinician) op de zorginnovatie arbeidsgerichte zorg. Vanuit die functie heb ik een groot netwerk (zorgprofessionals, politiek, ministeries, beroepsverenigingen, patientorganisaties, richtlijn cie's, NZa, ZiNl). Ik ben actief betrokken bij het NKC en in de TF cancersurvivorship care werkgroep werk. We proberen tzt onze innovatie te vermarkten om zodoende de voorinvestering die het Radboudumc doet terug te kunnen verdienen. Dit betreft mn onderwijsmodules. Ik heb meegeschreven aan de generieke module Arbeidsparticipatie voor in medisch specialistische RL. Ik zal een voortrekkersrol hebben in het vervolgtraject: het maken van ene ziektespecifieke module Arbeidsparticipatie voor oncologische RL. En ik ben kerngroeplid van de update van de RL kanker en werk voor bedrijfsartsen |
Ontwikkelen zorgmodel arbeidsgerichte zorg (Janssen Pharma en Radboudumc, in-kind projectondersteuning van Janssen Pharma) |
juli 2025 |
Geen restricties |
|
Ellen Passchier |
Verpleegkundig specialist revalidatie hoofd-hals oncologie tot november 2024 in Antoni van Leeuwenhoek
Heden: - verpleegkundig specialist in de wijk (Buurtzorg Amsterdam) - docent aan de Master ANP (Hogeschool inHolland) - buitenpromovendus afdeling hoofd-hals oncologie (Antoni van Leeuwenhoek) |
Geen |
Geen |
Geen |
Met ingang van november 2016 promotieonderzoek (evaluatie van revalidatieprogramma bij patiënten met een HHT - haalbaarheidsonderzoek naar beweeginterventie, analyses op kwaliteit van leven uitkomsten) |
Door deze richtlijn zal mijn promotie onderzoek (publicaties) meer belangstelling krijgen. |
Geen |
juli 2025 |
Geen restiricties |
|
Jos Elbers |
Radiotherapeut-oncoloog Erasmus MC |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
juli 2025 |
Geen restricties |
|
Kathelijn Versteeg |
internist-oncoloog AmsterdamUMC internist-ouderengeneeskunde AmsterdamUMC |
geen |
geen |
geen |
geen |
geen |
geen |
juli 2025 |
Geen restricties |
|
Lisette van der Molen |
logopedist/senior onderzoek aan het NKI-AVL. |
Het geven van bij/nascholing met betrekking tot de (logopedische) functionele uitkomsten na een behandeling in het HH gebied. Deze scholing kan zowel onbetaald als betaald zijn. |
Geen |
nvt |
ja Atos Medical AB Zweden Unrestricted research grant waardoor er PhD studenten kunnen worden aangenomen
De afdeling hoofd-halsoncologie van het AvL krijgt deze unrestricted research grant van Atos Medical (dus niet op persoonlijke titel van dit werkgroeplid). Ik ben in vaste dienst bij het AvL en ook niet afhankelijk van deze grant.
|
In 2010 heb ik samen met Prof. Hilgers het hoofd-halsrevalidatieprogramma ontwikkeld, welke als (standaard) nazorg binnen het NKI-AVL wordt aangeboden. Mocht dit ook het advies worden van deze richtlijn, dan zal het NKI-AVL een voorsprong hebben op de andere HH centra mbt implementatie.
Als kartrekker van de onderzoekslijn: survivorship rehabilitation and QoL na Hoofd-Halskanker begeleiden van meerdere PhD studenten met o.a. het onderwerp dysfagie. De kans is aanwezig dat er publicaties uit onze onderzoeksgroep terecht zullen komen in de output van de systematische literatuur searches voor deze richtlijn. Er is geen sprake van vermarkting of verwerven van een boegbeeldfunctie bij organisaties. |
nvt |
juli 2025 |
Geen restricties |
|
Luc Karssemakers |
Antoni v Leeuwenhoek Ziekenhuis, afdeling hoofd-hals chirurgie |
Afdeling Kaakchirurgie Slotervaart |
Geen |
Geen |
zie onderstaand STW Craniosafe, ideale implantaat schedelplastieken TKI Sternofix, implantaten sternaal voor laryngectomiepatienten |
Geen |
Geen |
juli 2025 |
Geen restricties (extern gefinancierd onderzoek heeft geen relatie met het onderwerp van de richtlijn) |
|
Marieke Jacobs |
Bedrijfsarts / klinisch arbeidsgeneeskundige, Radboudumc |
Werkzaam als instituutsopleider bedrijfsartsenopleiding bij de SGBO, Radboudumc |
Geen |
Niet van toepassing |
Niet van toepassing |
Niet bewust van |
Nee |
juli 2025 |
Geen restricties |
|
Narda Hendriks-Brouwer |
Medisch Spectrum Twente- plastisch chirurg Ziekenhuisgroep Twente-plastisch chirurg |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
juli 2025 |
Geen restricties |
|
Rob Burdorf |
Patiëntenvertegenwoordiger. Lid van de Wetenschappelijke Advies Commissie van de PVHH. Onbetaald |
geen |
geen |
nvt |
nvt |
nvt |
geen |
juli 2025 |
Geen restricties |
|
Caroline Speksnijder |
Associate professor UMC Utrecht |
Docent: *MSc Oncologie Fysiotherapie; Avans+ *MSc Orofaciale Fysiotherapie SOMT Physiotherapy University Werkgroep Kennisagendaherziening KNO Bestuurstaken: *Koninklijk Genootschap voor Fysiotherapie (KNGF): Bestuurslid Wetenschappelijk College Fysiotherapie (WCF) *Paramedische Werkgroep Hoofdhalstumoren (PWHHT): voorzitter *Dutch Association of Supportive Care in Cancer (DASCC): voorzitter *International Physiotherapy in HIV/Aids, Oncology, and Hospice and Palliative Care (IPT-HOPE part of World Physiotherapy): Vice-president |
Geen |
Nee |
Perioperative nutritional intervention with Fortifit Energy® in combination with exercise versus standard of care in head and neck cancer patients undergoing combined approach resection: a pilot study(gefinancierd door Danone, unrestricted grant, geen PI)
Integrating the Knowledge Agenda Physiotherapy into the science policy of the Royal Dutch Association for Physiotherapy (KNGF) (gefinancierd door ZonMw)
Prehabilitatie fysieke fitheid vooraf aan totale laryngectomie (gefinancierd door Nederlands Fonds tegen Kanker, unrestricted grant) |
nee |
nvt |
juli 2025 |
Restricties ten aanzien van het formuleren van aanbevelingen over het onderwerp op UV6 (nutritionele en excerise interventies ter preventie en behandeling) |
|
Petra Verdouw |
Patiëntenvereniging HOOFD-HALS Directeur |
geen |
geen |
geen |
geen |
geen |
geen |
juli 2025 |
Geen restricties |
|
Annemieke Kok |
Diëtist, onderzoeker |
secretaris PWHHT lid Landelijke Werkgroep Diëtisten Oncologie (tot jan 2024)
Vice-voorzitter van de Landelijke Werkgroep Diëtisten Oncologie (LWDO) (sinds april 2025). |
geen |
nee |
zie onder Ontwikkeling PEG keuzehulp voor hoofd-halskankerpatienten (Michel Keijzer Fonds) Perioperative nutritional intervention with Fortifit Energy® in combination with exercise versus standard of care in head and neck cancer patients undergoing combined approach resection: a pilot study(gefinancierd door Danone, unrestricted grant, geen PI) |
nee |
nee |
juli 2025 |
Restricties ten aanzien van het formuleren van aanbevelingen over het onderwerp op UV5 (nutritionele en excerise interventies ter preventie en behandeling) |
|
Doke Buurman |
Tandarts-MFP bij Maastricht UMC+ (betaald) |
Lid Consilium MFP bij de NVGPT (onbetaald) Lid ROC Mondzorg voor mensen met kanker (in de voorgeschiedenis) van KIMO (vacatieregeling) |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
juli 2025 |
Geen restricties |
|
Michael Brouwers |
Revalidatiearts Anthony van Leeuwenhoek Ziekenhuis Amsterdam |
geen |
geen |
geen |
geen |
geen belangen |
geen belangen |
juli 2025 |
|
Inbreng patiëntenperspectief
De richtlijnwerkgroep besteedde aandacht aan het patiëntenperspectief door het uitnodigen van Patiëntenvereniging Hoofd-Hals voor de schriftelijke invitational conference, en twee afgevaardigde namens deze patiëntenorganisatie in de werkgroep. Het verslag van de invitational conference (zie aanverwante producten) is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntenvereniging en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerde de werkgroep conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
Orale vocht- en voedingsinname na hoofd-halschirurgie |
geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en daarom naar verwachting geen substantiële financiële gevolgen zal hebben voor de collectieve uitgaven.
|