GLIM criteria
Uitgangsvraag
Wat is de plaats van de GLIM criteria voor het diagnosticeren van ondervoeding bij patiënten met hoofd-halskanker?
Aanbeveling
Streef naar de implementatie en het routinematig gebruik van de GLIM criteria als gestandaardiseerde en betrouwbare methode voor de diagnostiek van ondervoeding bij patiënten met hoofd-halskanker die op basis van een gevalideerd screeningsinstrument een verhoogd risico op ondervoeding hebben (zie Module Screening & monitoring voor zorgondersteuning). De richtlijnwerkgroep beveelt het gebruik van een BIA-apparaat aan voor de meting van vetvrije massa (spiermassa), volgens een gestandaardiseerde werkwijze, als onderdeel van de GLIM criteria.
Streef naar de implementatie en toepassing van de GLIM criteria voor het beoordelen en monitoren van het effect van dieetbehandeling bij patiënten met hoofd-halskanker, om zo de (kosten)effectiviteit van voedingsinterventies systematisch te evalueren.
Zorg ervoor dat de metingen binnen de GLIM criteria worden uitgevoerd door daartoe getrainde zorgprofessionals, zoals diëtisten of oncologieverpleegkundigen. Laat het stellen van de diagnose ondervoeding en de opstelling en uitvoering van het dieetbehandelplan verrichten door een diëtist met expertise in hoofd-halskanker.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Tijdens het literatuuronderzoek zijn twee studies geïncludeerd (Orell, 2022; Kaźmierczak-Siedlecka, 2020). Orell vergeleek de GLIM criteria met de PG-SGA. Kaźmierczak-Siedlecka (2020) vergeleek de GLIM criteria met de SGA. Voor alle uitkomstmaten was de kwaliteit van het bewijs zeer laag.
Naast de geïncludeerde studies zijn hieronder ook de resultaten beschreven van drie aanvullende studies, waarin de patiëntenpopulatie niet exclusief bestond uit patiënten met hoofd-halskanker. Deze studies rapporteerden uiteenlopende bevindingen, mogelijk als gevolg van de heterogene samenstelling van de onderzochte patiëntenpopulaties en variaties in prevalentie van ondervoeding tussen de studies.
Ondervoeding bij ziekte kan worden gedefinieerd als "een toestand die het gevolg is van een tekort aan inname of opname van voeding, leidend tot een veranderde lichaamssamenstelling (verminderde vetvrije massa) en celmassa van het lichaam, wat resulteert in een verminderde lichamelijke en mentale functie en een slechter klinisch beloop van ziekte" (Cederholm, 2017). Het betrouwbaar diagnosticeren van ondervoeding aan de hand van één diagnostische test of meetinstrument is niet mogelijk aangezien ondervoeding een multidimensionele en complexe conditie betreft (Rothenberg, 2024). De diagnose ondervoeding kan met grotere betrouwbaarheid worden gesteld op basis van meerdere criteria. Lange tijd bestond er wereldwijd geen consensus over de methoden of criteria die gehanteerd dienen te worden voor de diagnose ondervoeding.
In 2019 werd door vertegenwoordigers van diverse internationale beroepsverenigingen op het gebied van klinische voeding consensus bereikt over de criteria voor de diagnose van ondervoeding (Cederholm, 2019). Er is sprake van ondervoeding wanneer een patiënt voldoet aan ten minste één fenotypische (kenmerkende) factor en ten minste één etiologische (oorzakelijke) factor. Deze GLIM criteria vervangen de basisset van risico-indicatoren die in Nederland in de afgelopen jaren werden gehanteerd voor de vaststelling van ondervoeding bij volwassenen, waaronder een lage BMI en/of onbedoeld gewichtsverlies van >10% in 6 maanden en/of onbedoeld gewichtsverlies >5% in 1 maand (richtlijn ondervoeding).
Met de publicatie van de GLIM criteria deed de GLIM werkgroep tevens de oproep om de relevantie van deze criteria verder te valideren voor de klinische praktijk. Verschillende studies hebben de waarde van de GLIM criteria bij kankerpopulaties aangetoond. Bij patiënten met slokdarmkanker die geopereerd werden, konden postoperatieve uitkomsten beter worden voorspeld aan de hand van preoperatief gebruik van de GLIM criteria dan met de PG-SGA (sensitiviteit 81.6% versus 79.6% en specificiteit 50.4% versus 63.2%) (Liu, 2023). Een recente systematische literatuur review toont aan dat ondervoeding, gediagnosticeerd met de GLIM criteria, consistent geassocieerd is met slechte klinische uitkomsten met betrekking tot opnameduur, overleving en postoperatieve complicaties (Brown, 2023).
Het toepassen van de GLIM criteria in de diëtistische praktijk zal iets meer tijd vergen dan de voorheen gebruikte basisset van risico-indicatoren. Verminderde spiermassa is een fenotypische factor die is opgenomen in de GLIM consensus criteria. Het meten van de spiermassa, hoewel geen verplicht onderdeel van de GLIM, is iets tijdsintensiever dan het meten van het gewicht en vereist specifieke apparatuur. Het GLIM consortium adviseert het gebruik van gevalideerde methoden voor het meten van spiermassa, zoals middels Dual Energy X-Ray Absorptiometry (DEXA), Bio-elektrische Impedantie Analyse (BIA), weefselsegmentatie en kwantificatie m.b.v. Magnetic Resonance Imaging (MRI) of Computed Tomography (CT)-scan (Cederholm, 2019). De BIA is hiervan de meest toegankelijke methode welke door diverse echelons (1e, 2e en 3e lijnszorg) kan worden gebruikt. Een belangrijk voordeel van deze methode is dat zij kostenefficiënt, niet-invasief en het apparaat draagbaar is (Zweers, 2023). Momenteel zijn gevalideerde meetmethoden beschikbaar voor het bepalen van de spiermassa bij patiënten met hoofd-halskanker. De voor deze metingen benodigde CT-scans zijn doorgaans reeds beschikbaar, aangezien zij veelal worden vervaardigd in het kader van de oncologische diagnostiek en stadiering. Hierdoor vormt de meting van de spiermassa een relatief kostenefficiënte methode die geen extra belasting voor de patiënt met zich meebrengt (Bril, 2021). Op basis van het klinische beeld kan ernstige ziekte-gerelateerde inflammatie, een etiologisch criterium van de GLIM, meestal eenvoudig worden vastgesteld. In minder ernstige gevallen, kunnen aanvullende laboratoriummetingen, zoals C-reactief proteïne (CRP), albumine of pre-albumine, trombocyt-lymfocytenratio (PLR), neutrofiel-lymfocytenratio (NLR) en monocyt-lymfocytenratio (MLR) noodzakelijk zijn om de aanwezigheid van ziekte-gerelateerde inflammatie te beoordelen (Cederholm, 2019; Argilés, 2023; Ferrer, 2023). Deze biomarkers kunnen veelal gelijktijdig worden afgenomen met andere routinematige laboratoriumonderzoeken die reeds plaatsvinden in het kader van de oncologische diagnostiek en behandeling, zonder extra belasting voor de patiënt.
Het toepassen van de GLIM criteria voor de diagnostiek van ondervoeding heeft als voordeel dat de diagnose gestandaardiseerd en multidimensioneel kan worden gesteld. Bovendien maakt het een eenduidige evaluatie van het effect van de dieetbehandeling mogelijk, wat bijdraagt aan de standaardisatie van zorg. Het gestandaardiseerd en multidimensioneel in kaart brengen van de voortgang en effectiviteit van dieetbehandeling kan daarnaast een motiverend effect op de patiënt hebben en mogelijk de therapietrouw/dieettrouw bevorderen. De beschikbaarheid van nationale protocollen en richtlijnen voor zowel de diagnostiek en behandeling van ondervoeding als het gestandaardiseerd meten van de spiermassa en het hanteren van referentiewaarden ondersteunt de toepassing van de GLIM criteria (Kenniscentrum ondervoeding, 2021; Nutritional Assessment Platform, 2024). Het gebruik van de GLIM criteria voor een nauwkeurige diagnose van ondervoeding en de systematische rapportage hiervan in het patiëntendossier vergroot bovendien het bewustzijn van andere zorgprofessionals ten aanzien van het probleem ondervoeding. Dit is met name relevant voor patiënten bij wie ondervoeding op het eerste gezicht niet evident is, zoals patiënten met hoofd-halskanker en overgewicht (een hoge BMI gecombineerd met een lage spiermassa), die o.a. een verhoogd risico hebben op wondgenezingscomplicaties. Daarnaast draagt de toepassing van de GLIM criteria bij aan klinische besluitvorming in samenspraak met de patiënt (shared decision-making), zoals de afweging om al dan niet een (preventieve) voedingssonde te plaatsen (zie tevens Module Predictiemodel profylactische gastrotomie).
Toepassing van de GLIM criteria bij andere patiëntengroepen.
Een recente systematische literatuur review toont aan dat de sensitiviteit en specificiteit van de GLIM criteria voor het diagnosticeren van ondervoeding, respectievelijk, 0.72 en 0.82 bedragen, met een area under the curve (AUC) van 0.82 (Huo, 2022). Ondervoeding, gediagnosticeerd op basis van de GLIM criteria, is geassocieerd met ongunstige klinische uitkomsten bij kankerpatiënten, waaronder een verhoogd risico op postoperatieve complicaties, een langere opnameduur en een kortere overleving (Brown, 2023; Peng, 2022). Hoewel de validiteit van de GLIM criteria al uitgebreid is aangetoond, is verdere versterking van de wetenschappelijke bewijslast noodzakelijk voor de toepassing ervan binnen specifieke populaties, zoals patiënten met hoofd-halskanker.
Waarden en voorkeuren van patiënten (en evt. hun naasten en/of verzorgers)
Voeding en hydratatie vormen een essentieel thema voor patiënten met hoofd-halskanker en hun naasten. Wanneer eten en drinken door de tumor of de behandeling niet langer mogelijk is, heeft dit ingrijpende fysieke, sociale en emotionele gevolgen. Hoewel patiënten doorgaans goed worden geïnformeerd over de aard van de medische behandeling, blijft de impact ervan op het dagelijks leven vaak moeilijk te overzien.
Zorgprofessionals richten zich veelal primair op de fysieke gevolgen, met name tijdens de behandeling, maar hebben tevens een belangrijke rol in het erkennen en adresseren van de sociale en emotionele consequenties (zie Module Screening & monitoring voor zorgondersteuning). De GLIM criteria voor de diagnostiek van ondervoeding zijn primair gericht op het objectief en fysiek meten van de voedingsstatus. Het vaststellen van ondervoeding kan echter confronterend zijn voor patiënten. Conform het International Classification of Functioning, Disability and Health (ICF)-model dienen bij het stellen van de diëtistische diagnose en het opstellen van het dieetbehandelplan ook emotionele en sociale aspecten in overweging te worden genomen. Dit is met name relevant voor deze patiëntengroep, die een verhoogd risico heeft op psychosociale kwetsbaarheid.
Een goed geïnformeerde en betrokken patiënt, die actief participeert in de besluitvorming rondom zijn dieetbehandeling (shared decision-making/samen beslissen), vergroot de kans op een succesvolle voedingsinterventie. Door rekening te houden met persoonlijke behoeften, beperkingen, levensovertuigingen en voorkeuren, sluit het dieetbehandelplan beter aan bij de leefstijl, leefomgeving en sociaaleconomische positie van de patiënt.
Binnen de nazorg verdient het aanbeveling de nadruk te verschuiven naar het begeleiden van patiënten bij het omgaan met de chronische gevolgen van de kankerbehandeling. Tegelijkertijd kan onbedoeld gewichtsverlies door sommige patiënten, als er sprake is van overgewicht, als positief worden ervaren. Het meten van de lichaamssamenstelling als onderdeel van de GLIM criteria kan hierin ondersteunend zijn, vooral wanneer verlies van spiermassa zichtbaar wordt. Onderzoek toont aan dat patiënten de meting van spiermassa middels BIA als onderdeel van de GLIM criteria, als weinig belastend ervaren (Roberts, 2023). Om reisbewegingen voor de patiënt te minimaliseren, dienen deze metingen in de nazorg idealiter te worden geïntegreerd in follow-upafspraken bij de behandelend arts. In geval van enkelvoudige voedingsproblematiek kan doorverwijzing naar een eerstelijns diëtist met expertise in hoofd-hals oncologie een passend alternatief zijn.
Kosten (middelenbeslag)
Er zijn geen significante kostenverschillen tussen de verschillende methoden voor het diagnosticeren van ondervoeding. Het meten van de spiermassa kan enkele minuten extra consulttijd vergen, met name wanneer dit nog geen standaardonderdeel is van het diëtistisch consult. Deze meting is echter geen vereiste binnen de GLIM criteria voor de diagnostiek van ondervoeding. Indien sprake is van gewichtsverlies en/of een lage BMI, kan de diagnose ondervoeding ook zonder een spiermassameting worden gesteld. Dit brengt echter het risico met zich mee dat patiënten met een normale BMI en minimale of geen gewichtsafname, maar wel een verlaagde spiermassa, over het hoofd worden gezien.
Voor een nauwkeurige bepaling van de voedingsstatus en het monitoren van de effectiviteit van de dieetbehandeling is het meten van de spiermassa wenselijk. De benodigde apparatuur voor deze metingen is doorgaans al aanwezig in ziekenhuizen. De richtlijnwerkgroep adviseert het gebruik van een BIA apparaat dat geschikt is voor liggende vierpuntsmetingen ter bepaling van de vetvrije massa en spiermassa. De kosten voor single-frequentie BIA-apparaten starten vanaf €1500, terwijl multi-frequentie BIA-apparaten vanaf €3500 verkrijgbaar zijn (Nutritional Assessment Platform, 2022).
De GLIM criteria dienen niet routinematig bij alle patiënten met hoofd-halskanker te worden toegepast, maar enkel bij degenen met een verhoogd risico op ondervoeding, zoals vastgesteld met een gevalideerd screeningsinstrument (zie Module Screening & monitoring voor zorgondersteuning). De totale implementatiekosten van het GLIM proces zijn lastig exact te kwantificeren. Wel is aannemelijk dat implementatie bijdraagt aan de standaardisatie van de diagnostiek van ondervoeding, wat kan resulteren in een betere behandeling. Dit kan op zijn beurt leiden tot kostenbesparingen door een vermindering van complicaties en een lagere toxiciteit van de kankerbehandeling.
Aanvaardbaarheid, haalbaarheid en implementatie
Een internationaal vragenlijstonderzoek naar de implementatie van de GLIM criteria wijst uit dat de eenvoud van de metingen, wetenschappelijke onderbouwing van de effectiviteit en voldoende financiële middelen als belangrijkste bevorderende factoren voor implementatie worden genoemd door GLIM gebruikers. De meest voorkomende belemmeringen bij zorgprofessionals die de GLIM criteria nog niet toepassen, betreffen een gebrek aan prioritering binnen de organisatie, het reeds bestaande gebruik van andere assessmentinstrumenten en onvoldoende kennis of ervaring met implementatiestrategieën. Uit onderzoek blijkt dat ruim 40% van de deelnemende Nederlandse diëtisten (n=42) de GLIM criteria reeds hebben geïmplementeerd of daarmee bezig zijn (Jager-Wittenaar, 2023). Naar verwachting ligt dit percentage hoger binnen academische centra. De implementatie van de GLIM criteria wordt ondersteund door het gebruik van landelijke, openbaar toegankelijke protocollen en standard operating procedures (richtlijnen voor gestandaardiseerde metingen) voor het bepalen van de spiermassa m.b.t. de verschillende, beschikbare methoden. Of de toepassing van de GLIM criteria invloed heeft op gezondheidsongelijkheid bij patiënten met hoofd-halskanker, is vooralsnog onbekend.
Rationale van de aanbeveling: weging van argumenten voor en tegen de diagnostische procedure
De resultaten van het literatuuronderzoek in deze module bieden geen definitieve zekerheid over de diagnostische waarde van de GLIM criteria met betrekking tot het diagnosticeren van ondervoeding bij patiënten met hoofd-halskanker. Tot nu toe ontbreekt echter een algemeen geaccepteerde gouden standaard voor de diagnostiek van ondervoeding. De toepassing van de GLIM criteria brengt slechts minimale extra kosten met zich mee, voornamelijk in de vorm van consulttijd voor metingen. Daarnaast is de benodigde meetapparatuur veelal reeds aanwezig in medische centra, en kunnen de metingen worden uitgevoerd door iedere daartoe getrainde diëtist of andere zorgprofessional. Bovendien wordt de belasting voor de patiënt als gering beschouwd.
Onderbouwing
Malnutrition can be defined as “a state resulting from lack of intake or uptake of nutrition that leads to altered body composition (decreased fat free mass) and body cell mass leading to diminished physical and mental function and impaired clinical outcome from disease” (Cederholm, 2017).
Approximately 20% of patients with head and neck cancer are diagnosed with malnutrition, defined as weight loss >5% in 1 month or >10% in 6 months (Jager-Wittenaar, 2007). Malnutrition and weight loss in these patients are associated with a reduced quality of life, diminished physical function, increased risk of cancer treatment-related toxicity, higher risk of complications, increased mortality, and elevated healthcare costs (Wendrig, 2017; Sealy, 2020).
Diagnosing malnutrition is challenging due to its multidimensional nature involving a range of criteria. Until 2018, there was no global consensus on diagnostic criteria for malnutrition in clinical settings. Malnutrition was diagnosed using validated tools including the full Patient-Generated Subjective Global Assessment (PG-SGA) or the Mini Nutritional Assessment Full Form (MNA-FF). In February 2019, the international GLIM consortium (Global Leadership Initiative on Malnutrition) published a set of consensus-based operational diagnostic criteria for diagnosing malnutrition in adults (Cederholm, 2019). These criteria were designed for global use across various healthcare settings to establish a standardized basis for diagnosis. The GLIM framework involves a two-step process, see figure 1. The first step is malnutrition screening to identify individuals "at risk," using any validated screening tool (see Module Screening & monitoring voor zorgondersteuning). The second step is a nutritional assessment to confirm diagnosis and to determine severity grading of malnutrition. The consensus-based GLIM operational diagnostic criteria include three phenotypic indicators (unintentional weight loss, low body mass index, and reduced muscle mass) and two etiologic criteria (reduced food intake or assimilation, and inflammation or disease burden). For a malnutrition diagnosis, at least one phenotypic and one etiologic criterion must be met. The severity of malnutrition is then graded based on specific thresholds for the three phenotypic criteria (Cederholm, 2015). It is unclear if these criteria are valid for head and neck cancer patients.
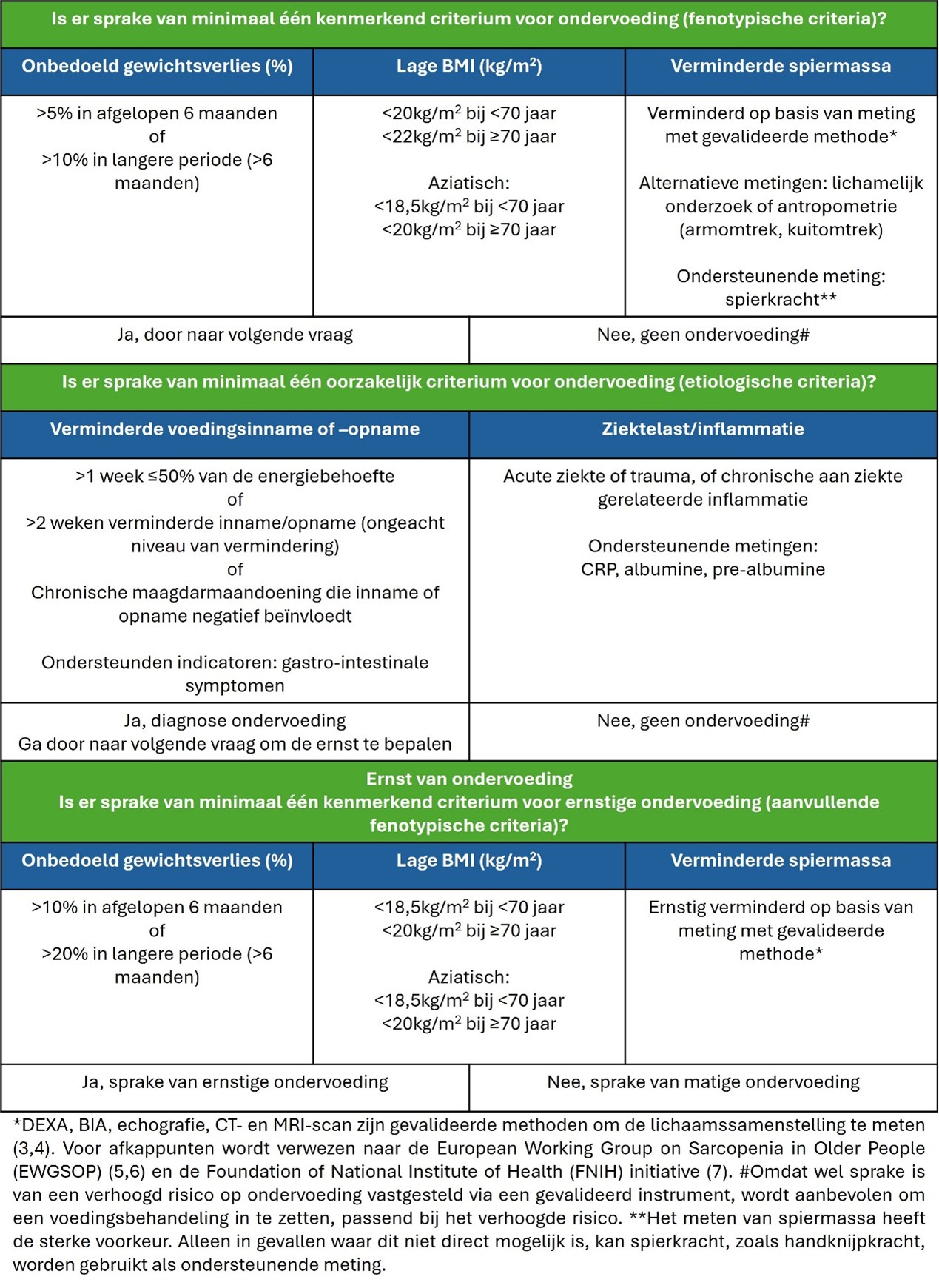
Figuur 1. Bron: Richtlijn ondervoeding. Stuurgroep ondervoeding, 2019
The GLIM criteria versus the PG-SGA
|
Very low GRADE |
The evidence regarding the diagnostic test accuracy of the GLIM criteria compared to the PG-SGA for sensitivity, specificity, positive predictive value, and negative predictive value in patients with head and neck cancer is highly uncertain.
Source: Orell, 2022 |
The GLIM criteria versus the SGA
|
Very low GRADE |
The evidence regarding the diagnostic test accuracy of the GLIM criteria compared to the SGA for sensitivity, specificity, positive predictive value, and negative predictive value in patients with head and neck cancer is highly uncertain.
Source: Kaźmierczak-Siedlecka, 2020 |
Description of studies
Orell (2022) conducted a retrospective study to determine the prevalence of malnutrition in head and neck cancer patients in Finland, comparing the Global Leadership Initiative on Malnutrition (GLIM) criteria with the PG–SGA.
Ambulatory patients aged 18 to 80 with locally advanced squamous cell carcinoma of the oral cavity, oropharynx, hypopharynx, nasopharynx, or larynx were eligible for inclusion.
A total of 65 newly diagnosed patients were included. All patients underwent nutritional surveillance and were offered nutritional treatment when deemed necessary.
Malnutrition was defined as PG-SGA categories B and C and was retrospectively diagnosed using the GLIM criteria in prospectively and systematically collected data (per standardized protocol) at the time of diagnosis before surgery or adjuvant cancer treatment. Nutritional risk screening, nutritional status assessment, and nutritional treatment were conducted by a single investigator during the patients' first hospital outpatient visit.
Kaźmierczak-Siedlecka (2020) evaluated the diagnostic test accuracy of the GLIM criteria compared to the Subjective Global Assessment (SGA) method for diagnosing malnutrition. Thirty-three patients with advanced-stage cancer (including those with head and neck, esophageal, and gastric cancers) from the Nutritional Counselling Centre Copernicus in Gdańsk, and the Department of Surgical Oncology, Medical University of Gdańsk, Poland were included, with 12 patients having head and neck cancer. All patients had advanced-stage head and neck cancer and were not receiving cancer treatment at the time of enrolment. Nutritional status was assessed using the 2019 GLIM criteria alongside the SGA method.
Results
Sensitivity and positive predictive value (critical outcome measures)
Orell (2022)
Out of the 65 patients, 24 (37%) were classified as malnourished according to the GLIM criteria, and 22 (34%) according to the PG–SGA.
Kaźmierczak-Siedlecka (2020)
Out of the 12 patients, one (8.33%) patient scored an A on the SGA, four (33.33%) patients a B and seven (58.33%) a C on the SGA. Three (25%) patients scored stage 1 on the GLIM criteria and 9 (75%) scored Glim 2.
We calculated the diagnostic accuracy of the GLIM criteria using the results of the subgroup of 12 patients with head and neck cancer.
The outcomes sensitivity and positive predictive value of the GLIM criteria are shown in Table 2.
Table 2. Outcomes sensitivity and positive predictive value of the GLIM criteria
|
Study |
Test |
Reference |
N of patients |
Sensitivity (95% CI) |
Positive predictive value (95% CI) |
|
Orell (2022) |
GLIM |
PG-SGA |
65 |
77.3 (57.1 – 90.8) |
70.8 (NR) |
|
Kaźmierczak-Siedlecka (2020) |
GLIM |
SGA |
12 |
81.8 % (48.22 -97.72) |
100 (66.37- 100.00) |
N, number of patients; CI, confidence interval; GLIM, Global Leadership Initiative on Malnutrition; PG-SGA, Patient-Generated Subjective Global Assessment; NR, not reported; SGA, Subjective Global Assessment
Specificity and negative predictive value (important outcome measure and critical outcome measure)
The outcomes specificity and negative predictive value of the GLIM criteria are shown in Table 3.
Table 3. Outcomes specificity and negative predictive value of the GLIM criteria
|
Study |
Test |
Reference |
N of patients |
Specificity (95% CI) |
Negative predictive value (95% CI) |
|
Orell (2022) |
GLIM |
PG-SGA |
65 |
83.7 (70.7 – 92.4) |
87.8 (NR) |
|
Kaźmierczak-Siedlecka (2020) |
GLIM |
SGA |
12 |
100.0 (2.5- 100.0) |
33.3 (12.5- 63.7) |
N, number of patients; CI, confidence interval; GLIM, Global Leadership Initiative on Malnutrition; PG-SGA, Patient-Generated Subjective Global Assessment; NR, not reported; SGA, Subjective Global Assessment
Other supportive studies
The studies of Crestani (2023), Ozorio (2023), and Zhang (2021) were excluded from the literature analysis because they included a heterogeneous cohort of patients rather than focusing exclusively on those with head and neck cancer. Additionally, test performance data were reported for the entire patient cohort, not specifically for patients with head and neck cancer. However, their findings may still support decision-making and are therefore presented in Table 4. These studies were not included in the GRADE-assessment.
Table 4. GLIM test accuracy of studies that are not limited to head and neck cancer patients
|
Study design |
Population |
N |
Test |
Reference |
N of patients |
Sensitivity (95% CI) |
Specificity (95% CI) |
Positive predictive value (95% CI) |
Negative predictive value (95% CI) |
|
Crestani (2023) |
NR** |
68 |
GLIM |
PG-SGA |
183 of which 68 (37%) patients with head and neck cancer |
78.5% (95% CI not reported) |
48.0% (95% CI not reported) |
90.5% (95% CI not reported) |
26.0% (95% CI not reported) |
|
Ozorio (2023) |
NR** |
281 |
GLIM |
SGA |
885 of which 281 (32%) patients with head neck cancer |
GLIM1* 26% GLIM2 12.7% GLIM3 37.0% GLIM4 12.1% GLIM5 66.5%
(95% CI not reported) |
GLIM1* 78.8% GLIM2 94.6 % GLIM3 94.1% GLIM4 97.5% GLIM5 73.8% (95%CI not reported) |
GLIM1* 65.3% GLIM2 66.7% GLIM3 84.2% GLIM4 80.8 % GLIM5 68.5 %
(95% CI not reported) |
GLIM1 * 63.3% GLIM2 55.8% GLIM3 63.5% GLIM4 56.4% GLIM5 72%
(95% CI not reported) |
|
Zhang (2021) |
NR** |
224 |
GLIM |
PS-SGA |
637 of which 224 (35%) patients with head neck cancer |
81.1% (95% CI not reported) |
71.6% (95% CI not reported) |
52.9% (95% CI not reported) |
90.6% (95% CI not reported) |
N, number of patients; CI, confidence interval; NR, not reported; GLIM, Global Leadership Initiative on Malnutrition; PG-SGA, Patient-Generated Subjective Global Assessment; SGA, Subjective Global Assessment.
*GLIM1: weight loss + disease stage
GLIM2: weight loss + low food intake
GLIM3: low body mass index + disease stage
GLIM4: low body mass index + low food intake
GLIM5: weight loss or low body mass index + disease stage or low food intake
** Population characteristics not reported for the subgroup head and neck cancer patients
Level of evidence of the literature
The initial level of evidence for the diagnostic accuracy outcome was rated as high due to the inclusion of diagnostic accuracy studies.
Sensitivity and positive predictive value (critical outcome measures)
The GLIM criteria versus the PG-SGA
The level of evidence for the outcome measures sensitivity and positive predictive value was downgraded by three levels due to the risk of bias (including selection bias and lack of blinding for test results, resulting in a downgrade of 1 level) and imprecision (attributed to very wide confidence intervals, leading to a downgrade of 2 levels). Consequently, the overall level of evidence was graded as very low.
The GLIM criteria versus the SGA
The level of evidence for the outcome measures sensitivity and positive predictive value was downgraded by three levels due to the risk of bias (including selection bias and lack of blinding for test results, resulting in a downgrade of 1 level) and imprecision (attributed to very wide confidence intervals, leading to a downgrade of 2 levels). Consequently, the overall level of evidence was graded as very low.
Specificity and negative predictive value (important outcome measure and critical outcome measure)
The GLIM criteria versus the PG-SGA
The level of evidence for the outcome measures specificity and negative predictive value was downgraded by three levels due to the risk of bias (including selection bias and lack of blinding for test results, resulting in a downgrade of 1 level) and imprecision (attributed to very wide confidence intervals, leading to a downgrade of 2 levels). Consequently, the overall level of evidence was graded as very low.
The GLIM criteria versus the SGA
The level of evidence for the outcome measures specificity and negative predictive value was downgraded by three levels due to the risk of bias (including selection bias and lack of blinding for test results, resulting in a downgrade of 1 level) and imprecision (attributed to very wide confidence intervals, leading to a downgrade of 2 levels). Consequently, the overall level of evidence was graded as very low.
A systematic review of the literature was performed to answer the following question:
What is the validity of the GLIM criteria for diagnosing malnutrition in patients with head and neck cancer?
| P (Patients): | Patients with head and neck cancer |
| I (Index test): | GLIM criteria |
| C (Comparator test): |
In depth nutritional assessment by a trained professional, MNA-FF or SGA/PG-SGA |
| R (Reference): | Diagnostic accuracy: sensitivity, specificity, positive |
| O (Outcome): | Predictive value, negative predictive value |
| T/S (Timing/setting): | Before/during/after cancer treatment, oncology setting |
Relevant outcome measures
The guideline development group considered sensitivity and positive predictive value as critical outcome measures for decision making; and specificity and negative predictive value as important outcome measures for decision making (Table 1).
Table 1. Outcome measures and minimal clinically important values
|
Outcome |
Consequences |
Relevance |
|
True positive (TP), high sensitivity, high positive predictive value |
A patient correctly diagnosed with malnutrition. The patient will be correctly treated for malnutrition. |
Critical |
|
True negative (TN), high specificity, high negative predictive value |
A patient correctly diagnosed without malnutrition. |
Important |
|
False positive (FP), low specificity, low positive predictive value |
A patient incorrectly diagnosed with malnutrition. The patient will be treated for malnutrition, despite not being malnourished. |
Important |
|
False negative, low sensitivity, low negative predictive value |
A patient incorrectly diagnosed without malnutrition. The patient will not be treated for malnutrition, despite being malnourished. |
Critical |
The guideline development group defined 80% as the minimal clinically important value for sensitivity and specificity, and 90% for positive predictive value and negative predictive value.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched using relevant search terms from January 1, 2004, to March 3, 2024. The systematic literature search resulted in 34 hits. Studies were selected based on the following criteria: systematic reviews, randomized controlled trials, and observational studies on the diagnosis of malnutrition in patients with head and neck cancer, in accordance with the PICO framework.
Nine studies were initially selected based on title and abstract screening. After reading the full text, seven studies were excluded (see the Table with reasons for exclusion), leaving two studies to be included.
Results
Two studies were included in the analysis of the literature. The assessment of the risk of bias is summarized in the risk of bias tables.
- Argilés JM, López-Soriano FJ, Stemmler B, Busquets S. Cancer-associated cachexia - understanding the tumour macroenvironment and microenvironment to improve management. Nat Rev Clin Oncol. 2023 Apr;20(4):250-264. doi: 10.1038/s41571-023-00734-5. Epub 2023 Feb 20. PMID: 36806788.
- Bril SI, Chargi N, Wendrich AW, Wegner I, Bol GH, Smid EJ, de Jong PA, Devriese LA, de Bree R. Validation of skeletal muscle mass assessment at the level of the third cervical vertebra in patients with head and neck cancer. Oral Oncol. 2021 Dec;123:105617. doi: 10.1016/j.oraloncology.2021.105617. Epub 2021 Nov 5. PMID: 34749251.
- Brown D, Loeliger J, Stewart J, Graham KL, Goradia S, Gerges C, Lyons S, Connor M, Stewart S, Di Giovanni A, D'Angelo S, Kiss N. Relationship between global leadership initiative on malnutrition (GLIM) defined malnutrition and survival, length of stay and post-operative complications in people with cancer: A systematic review. Clin Nutr. 2023 Mar;42(3):255-268. doi: 10.1016/j.clnu.2023.01.012. Epub 2023 Jan 13. PMID: 36716618.
- Cederholm T, Bosaeus I, Barazzoni R, Bauer J, Van Gossum A, Klek S, Muscaritoli M, Nyulasi I, Ockenga J, Schneider SM, de van der Schueren MA, Singer P. Diagnostic criteria for malnutrition - An ESPEN Consensus Statement. Clin Nutr. 2015 Jun;34(3):335-40. doi: 10.1016/j.clnu.2015.03.001. Epub 2015 Mar 9. PMID: 25799486.
- Cederholm T, Barazzoni R, Austin P, Ballmer P, Biolo G, Bischoff SC, Compher C, Correia I, Higashiguchi T, Holst M, Jensen GL, Malone A, Muscaritoli M, Nyulasi I, Pirlich M, Rothenberg E, Schindler K, Schneider SM, de van der Schueren MA, Sieber C, Valentini L, Yu JC, Van Gossum A, Singer P. ESPEN guidelines on definitions and terminology of clinical nutrition. Clin Nutr. 2017 Feb;36(1):49-64. doi: 10.1016/j.clnu.2016.09.004. Epub 2016 Sep 14. PMID: 27642056.
- Cederholm T, Jensen GL, Correia MITD, Gonzalez MC, Fukushima R, Higashiguchi T, Baptista G, Barazzoni R, Blaauw R, Coats AJS, Crivelli AN, Evans DC, Gramlich L, Fuchs-Tarlovsky V, Keller H, Llido L, Malone A, Mogensen KM, Morley JE, Muscaritoli M, Nyulasi I, Pirlich M, Pisprasert V, de van der Schueren MAE, Siltharm S, Singer P, Tappenden K, Velasco N, Waitzberg D, Yamwong P, Yu J, Van Gossum A, Compher C; GLIM Core Leadership Committee, GLIM Working Group. GLIM criteria for the diagnosis of malnutrition - A consensus report from the global clinical nutrition community. J Cachexia Sarcopenia Muscle. 2019 Feb;10(1):207-217. doi: 10.1002/jcsm.12383. PMID: 30920778; PMCID: PMC6438340.
- Crestani MS, Stefani GP, Scott LM, Steemburgo T. Accuracy of the GLIM criteria and SGA compared to PG-SGA for the diagnosis of malnutrition and its impact on prolonged hospitalization: a prospective study in patients with cancer. Nutrition and cancer. 2023 Apr 21;75(4):1177-88.
- Dewansingh P, Bras L, Ter Beek L, Krijnen WP, Roodenburg JL, Van Der Schans CP, Halmos GB, Jager-Wittenaar H. Malnutrition risk and frailty in head and neck cancer patients: coexistent but distinct conditions. European Archives of Oto-Rhino-Laryngology. 2023 Apr;280(4):1893-902.
- Ferrer M, Anthony TG, Ayres JS, Biffi G, Brown JC, Caan BJ, Cespedes Feliciano EM, Coll AP, Dunne RF, Goncalves MD, Grethlein J, Heymsfield SB, Hui S, Jamal-Hanjani M, Lam JM, Lewis DY, McCandlish D, Mustian KM, O'Rahilly S, Perrimon N, White EP, Janowitz T. Cachexia: A systemic consequence of progressive, unresolved disease. Cell. 2023 Apr 27;186(9):1824-1845. doi: 10.1016/j.cell.2023.03.028. PMID: 37116469; PMCID: PMC11059056.
- Huo Z, Chong F, Yin L, Lu Z, Liu J, Xu H. Accuracy of the GLIM criteria for diagnosing malnutrition: A systematic review and meta-analysis. Clin Nutr. 2022 Jun;41(6):1208-1217. doi: 10.1016/j.clnu.2022.04.005. Epub 2022 Apr 11. PMID: 35504163.
- Jager-Wittenaar H, Dijkstra PU, Vissink A, van der Laan BF, van Oort RP, Roodenburg JL. Critical weight loss in head and neck cancer--prevalence and risk factors at diagnosis: an explorative study. Support Care Cancer. 2007 Sep;15(9):1045-50. doi: 10.1007/s00520-006-0212-9. Epub 2007 Feb 3. PMID: 17277925.
- Kenniscentrum Ondervoeding. Richtlijn Ondervoeding. HERKENNING, DIAGNOSESTELLING EN BEHANDELING VAN ONDERVOEDING BIJ VOLWASSENEN. Januari 2019. URL: https://www.kenniscentrumondervoeding.nl/wp-content/uploads/2022/04/SoV01-Richtlijn-Ondervoeding-februari-2019-met-addendum-september-2021.pdf.
- Kaźmierczak-Siedlecka K, Skonieczna-Żydecka K, Folwarski M, Ruszkowski J, Świerblewski M, Makarewicz W. Influence of malnutrition stage according to GLIM 2019 criteria and SGA on the quality of life of patients with advanced cancer. Nutr Hosp. 2020 Dec 16;37(6):1179-1185. English. doi: 10.20960/nh.03185. PMID: 33119401.
- Liu JC, Egleston BL, Blackman E, Ragin C. Racial survival disparities in head and neck cancer clinical trials. JNCI: Journal of the National Cancer Institute. 2023 Mar 1;115(3):288-94.
- Nutritional Assessment Platform (NAP). Standard operating procedures NAP. https://nutritionalassessment.nl/standard-operating-procedure, 2024.
- Orell HK, Pohju AK, Osterlund P, Schwab US, Ravasco P, Mäkitie A. GLIM in diagnosing malnutrition and predicting outcome in ambulatory patients with head and neck cancer. Front Nutr. 2022 Nov 22;9:1030619. doi: 10.3389/fnut.2022.1030619. PMID: 36483923; PMCID: PMC9724589.
- Ozorio GA, Ribeiro LM, Santos BC, de Sousa Bruzaca WF, da Rocha GD, da Fonseca Marchi LM, Santos FM, de Almeida MM, Kulcsar MA, Junior UR, Correia MI. Exploring the use of the GLIM criteria to diagnose malnutrition in cancer inpatients. Nutrition. 2023 Dec 1;116:112195.
- Peng D, Zong K, Yang H, Huang Z, Mou T, Jiang P, Wu Z. Malnutrition diagnosed by the Global Leadership Initiative on Malnutrition criteria predicting survival and clinical outcomes of patients with cancer: A systematic review and meta-analysis. Front Nutr. 2022 Dec 6;9:1053165. doi: 10.3389/fnut.2022.1053165. PMID: 36562033; PMCID: PMC9763567.
- Roberts S, Nucera R, Dowd T, et al. Prospective validation of the GLIM criteria for identifying malnutrition: a pilot study. 2023. Clin Nutr ESPEN 54 : 463-726.
- Rothenberg E, Tsagari A, Erickson N, Katsagoni CN, Malone A, de van der Schueren M, Shaw C, Steiber A, Vranesic Bender D, Jager-Wittenaar H. Global Leadership Initiative on Malnutrition (GLIM) for the diagnosis of malnutrition - a framework for consistent dietetic practice. Clin Nutr ESPEN. 2024 Apr;60:261-265. doi: 10.1016/j.clnesp.2024.02.009. Epub 2024 Feb 17. PMID: 38479920.
- Sealy MJ, Dechaphunkul T, van der Schans CP, Krijnen WP, Roodenburg JLN, Walker J, Jager-Wittenaar H, Baracos VE. Low muscle mass is associated with early termination of chemotherapy related to toxicity in patients with head and neck cancer. Clin Nutr. 2020 Feb;39(2):501-509. doi: 10.1016/j.clnu.2019.02.029. Epub 2019 Feb 22. PMID: 30846324.
- Wendrich AW, Swartz JE, Bril SI, Wegner I, de Graeff A, Smid EJ, de Bree R, Pothen AJ. Low skeletal muscle mass is a predictive factor for chemotherapy dose-limiting toxicity in patients with locally advanced head and neck cancer. Oral Oncol. 2017 Aug;71:26-33. doi: 10.1016/j.oraloncology.2017.05.012. Epub 2017 Jun 5. PMID: 28688687.
- Zhang Z, Wan Z, Zhu Y, Zhang L, Zhang L, Wan H. Prevalence of malnutrition comparing NRS2002, MUST, and PG-SGA with the GLIM criteria in adults with cancer: A multi-center study. Nutrition. 2021 Mar;83:111072. doi: 10.1016/j.nut.2020.111072. Epub 2020 Nov 19. PMID: 33360034.
- Zweers H. Korzilius H. Kruizenga H, Visser W, Jans I. Standard Operating Procedures. Single frequency bio-elektrische impedantie analyse. Nutritional assessment platform. Versie 8. Aug 2025. NAP-SOP-SFBIA-versie8.
Risk of bias assessment diagnostic accuracy studies (QUADAS II, 2011)
|
Study reference |
Patient selection |
Index test |
Reference standard |
Flow and timing |
Comments with respect to applicability |
|
Orell, 2022 |
Was a consecutive or random sample of patients enrolled? Unclear
Was a case-control design avoided? Yes
Did the study avoid inappropriate exclusions? Unclear |
Were the index test results interpreted without knowledge of the results of the reference standard? Unclear
If a threshold was used, was it pre-specified? Yes |
Is the reference standard likely to correctly classify the target condition? Yes
Were the reference standard results interpreted without knowledge of the results of the index test? Unclear |
Was there an appropriate interval between index test(s) and reference standard? Yes
Did all patients receive a reference standard? Yes
Did patients receive the same reference standard? Yes
Were all patients included in the analysis? Yes |
Are there concerns that the included patients do not match the review question? No
Are there concerns that the index test, its conduct, or interpretation differ from the review question? No
Are there concerns that the target condition as defined by the reference standard does not match the review question? No |
|
CONCLUSION: Could the selection of patients have introduced bias?
RISK: UNCLEAR |
CONCLUSION: Could the conduct or interpretation of the index test have introduced bias?
RISK: HIGH |
CONCLUSION: Could the reference standard, its conduct, or its interpretation have introduced bias?
RISK: HIGH |
CONCLUSION Could the patient flow have introduced bias?
RISK: LOW |
|
|
|
Kaźmierczak-Siedlecka (2020) |
Was a consecutive or random sample of patients enrolled? No
Was a case-control design avoided? Yes
Did the study avoid inappropriate exclusions? Unclear |
Were the index test results interpreted without knowledge of the results of the reference standard? Unclear
If a threshold was used, was it pre-specified? Yes |
Is the reference standard likely to correctly classify the target condition? Yes
Were the reference standard results interpreted without knowledge of the results of the index test? Unclear |
Was there an appropriate interval between index test(s) and reference standard? Unclear
Did all patients receive a reference standard? Yes
Did patients receive the same reference standard? Yes
Were all patients included in the analysis? No (2 refused participation) |
Are there concerns that the included patients do not match the review question? No
Are there concerns that the index test, its conduct, or interpretation differ from the review question? No
Are there concerns that the target condition as defined by the reference standard does not match the review question? No |
|
|
CONCLUSION: Could the selection of patients have introduced bias?
RISK: HIGH |
CONCLUSION: Could the conduct or interpretation of the index test have introduced bias?
RISK: HIGH |
CONCLUSION: Could the reference standard, its conduct, or its interpretation have introduced bias?
RISK: HIGH |
CONCLUSION Could the patient flow have introduced bias?
RISK: LOW |
|
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Crestani, Mariana Scortegagna and Stefani, Giovanna Potrick and Scott, Laura Machado and Steemburgo, Thais Accuracy of the GLIM Criteria and SGA Compared to PG-SGA for the Diagnosis of Malnutrition and Its Impact on Prolonged Hospitalization: A Prospective Study in Patients with Cancer. Nutrition and cancer. 2023; 75 (4) :1177-1188 |
Wrong P, not specified for head and neck cancer patients |
|
Einarsson, Sandra and Laurell, Goran and Tiblom Ehrsson, Ylva Mapping the frequency of malnutrition in patients with head and neck cancer using the GLIM Criteria for the Diagnosis of Malnutrition. Clinical nutrition ESPEN. 2020; 37 :100-106 |
Wrong I/C. Does not compare Glim criteria to other measurement instruments as specified in the PICO |
|
Gascon-Ruiz, Marta and Casas-Deza, Diego and Torres-Ramon, Irene and Zapata-Garcia, Maria and Alonso, Natalia and Sesma, Andrea and Lambea, Julio and Alvarez-Alejandro, Maria and Quilez, Elisa and Isla, Dolores and Arbones-Mainar, Jose M. GLIM vs ESPEN criteria for the diagnosis of early malnutrition in oncological outpatients. Clinical nutrition (Edinburgh, Scotland). 2021; 40 (6) :3741-3747 |
Wrong I/C. Compares GLIM to ESPEN criteria |
|
Ozorio, Gislaine Aparecida and Ribeiro, Lia Mara Kauchi and Santos, Barbara Chaves and Bruzaca, Wannia Ferreira de Sousa and Rocha, Gabriela Del Gallo Vieira da and Marchi, Luani Maria da Fonseca and Santos, Fernando Magri and Alves de Almeida, Maria Manuela Ferreira and Kulcsar, Marco Aurelio Vamondes and Junior, Ulysses Ribeiro and Correia, Maria Isabel Toulson Davisson and Waitzberg, Dan Linetzky Exploring the use of the GLIM criteria to diagnose malnutrition in cancer inpatients. Nutrition (Burbank, Los Angeles County, Calif.). 2023; 116 :112195 |
Wrong P, not specified for head and neck cancer patients |
|
Steer B, Loeliger J, Edbrooke L, Deftereos I, Laing E, Kiss N. Malnutrition Prevalence according to the GLIM Criteria in Head and Neck Cancer Patients Undergoing Cancer Treatment. Nutrients. 2020 Nov 13;12(11):3493. doi: 10.3390/nu12113493. PMID: 33203000; PMCID: PMC7697929. |
Wrong I/C. Does not compare Glim criteria to other measurement instruments specified in the PICO
|
|
Stefani GP, Crestani MS, Scott LM, Soares CH, Steemburgo T. Complementarity of nutritional assessment tools to predict prolonged hospital stay and readmission in older patients with solid tumors: A secondary analysis of a cohort study. Nutrition. 2023 Sep;113:112089. doi: 10.1016/j.nut.2023.112089. Epub 2023 May 22. PMID: 37354653. |
Wrong P, not specified for head and neck cancer patients. Wrong I/C. Studies a combination of tests, and not tests separately. |
|
Zhang Z, Wan Z, Zhu Y, Zhang L, Zhang L, Wan H. Prevalence of malnutrition comparing NRS2002, MUST, and PG-SGA with the GLIM criteria in adults with cancer: A multi-center study. Nutrition. 2021 Mar;83:111072. doi: 10.1016/j.nut.2020.111072. Epub 2020 Nov 19. PMID: 33360034. |
Wrong P, not specified for head and neck cancer patients. |
Beoordelingsdatum en geldigheid
Publicatiedatum : 28-01-2026
Beoordeeld op geldigheid : 28-01-2026
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd door de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2023 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met hoofd-halskanker.
Werkgroep
- Prof. dr. L.W.J. (Laura) Baijens, voorzitter, Nederlandse Vereniging van Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied (NVKNO)
- A.C.P. (Anne) Kauerz-de Rooij, Ergotherapie Nederland (EN)
- Dr. C.M. (Caroline) Speksnijder, Koninklijk Nederlands Genootschap Fysiotherapie (KNGF)
- Dr. D.J.M. (Doke) Buurman - Koninklijke Nederlandse Maatschappij tot bevordering der Tandheelkunde (KNMT)
- Dr. K.S. (Kathelijn) Versteeg, Nederlandse Internisten Vereniging (NIV)
- Drs. D. (Desiree) Dona, Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde (NVAB)
- Dr. A. (Annemieke) Kok, Nederlandse Vereniging van Diëtisten (NVD)
- Drs. M. (Marieke) Jacobs, Nederlandse Vereniging voor Klinische Arbeidsgeneeskunde (NVKA)
- Dr L. (Lisette) van der Molen, Nederlandse Vereniging voor Logopedie en Foniatrie (NVLF)
- Dr. L.H.E. (Luc) Karssemakers, Nederlandse Vereniging voor Mondziekten, Kaak- en Aangezichtschirurgie (NVMKA)
- Dr. J. (Jos) Elbers, Nederlandse Vereniging voor Radiotherapie en Oncologie (NVRO)
- R.A. (Rob) Burdorf, Patiëntenvereniging HOOFD-HALS (PvHH)
- P.S. (Petra) Verdouw, Patiëntenvereniging HOOFD-HALS (PvHH)
- Drs. M. (Michael) Brouwers, Nederlandse Vereniging van Revalidatieartsen (VRA)
- Drs. E. (Ellen) Passchier, Verpleegkundigen en Verzorgenden Nederland (V&VN)
- Drs. N. (Narda) Hendriks, Nederlandse Vereniging voor Plastische Chirurgie (NVPC)
Klankbordgroep
- Prof. dr. R. (Remco) de Bree, Nederlandse Vereniging van Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied (NVKNO)
- Dr. P. (Pim) de Graaf, Nederlandse Vereniging voor Radiologie (NVvR)
- Dr. D.S.V.M. (Dominique) Clément, Nederlandse Vereniging van Maag-Darm-Leverartsen (NVMDL)
- J. (Jesmin) Poelstra, Beroepsvereniging van Professionals in Sociaal Werk (BPSW)
- Dr. G. (Gerben) van Hinte, Koninklijk Nederlands Genootschap Fysiotherapie (KNGF)
- Drs. A. (Anne) Arens, Nederlandse Vereniging voor Nucleaire Geneeskunde (NVNG)
- Dr. F. (Femke) Jansen, Nederlandse Vereniging voor Psychosociale Oncologie (NVPO)
Met ondersteuning van
- Dr. L.M. (Lisette) van Leeuwen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. E. (Evelien) Belfroid, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Gemelde (neven)functies en belangen richtlijnwerkgroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Laura Baijens |
KNO-arts/Laryngoloog/Hoofd-hals chirurg Maastricht Universitair Medisch Centrum (MUMC+) |
Consultant for Phagenesis Limited, The Elms Courtyard, Bromesberrow, Ledbury, HR8 1RZ UK. The PhINEST Study – Pharyngeal ICU - Novel Electrical Stimulation Therapy: a prospective, European multi-site, randomised, sham-controlled, single-blind (outcome assessor-blinded) study. August 2018 – 2030 (Consultancy Agreement via the Clinical Trial Center Maastricht) |
Consultant for Phagenesis Limited in the PhINEST Study heeft geen betrekking of relaties met de huidige richtlijn. Het is een Europese multicenter studie over dysfagie bij CVA patiënten waarin ik advies geef. De opbrengsten gaan naar het Clinical Trial Center Maastricht. |
Neen |
Phagenesis Limited Advies geven in een studie over faryngeale elektrostimulatie bij CVA patiënten, MUMC+ is geen site en betreft geen patiënten met hoofd-halskanker.
Michel Keijzer Fonds PVHH Multi-domein screening van hoofd-halskankerpatiënten |
Intellectueel eigendom: Ik ben PI in meerdere lopende niet-WMO studies over dysfagie bij hoofd-halskanker. Ik heb vele internationale W1-publicaties over dysfagie bij hoofd-halskanker. De kans is reëel dat deze publicaties terecht zullen komen in de output van systematic literatuur searches voor deze richtlijn. Er is geen sprake van 'vermarkting' of verwerven van een boegbeeldfunctie bij organisaties. |
Nee |
juli 2025 |
Geen restricties (extern gefinancierd onderzoek heeft geen relatie met het onderwerp van de richtlijn) |
|
Anne Kauerz |
Ergotherapeut UMC Utrecht |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
juli 2025 |
Geen restricties |
|
Desiree Dona |
bedrijfsarts / klinisch arbeidsgeneeskundige oncologie 1.0 fte Radboudumc werkzaamheden: arbeidsgeneeskundige begeleiding in behandelteam van oncologiepatienten, projectmanagement, onderzoek en onderwijs. Alle werkzaamheden zijn betaald. |
vennoot van DELEN ABC (arbeidsdeskundige advisering en coaching) generieke module Arbeidsparticipatie voor medisch specialistische richtlijnen (vacatiegelden) |
Geen |
neen |
Prehabilitatie en werkbegeleiding voor borstkankerpatienten (gefinancierd door MOVIR en Stichting Enjoy the ride, unrestricted grant, geen PI) |
Ik heb een boegbeeldfunctie bij het Radboudumc (Principal Clinician) op de zorginnovatie arbeidsgerichte zorg. Vanuit die functie heb ik een groot netwerk (zorgprofessionals, politiek, ministeries, beroepsverenigingen, patientorganisaties, richtlijn cie's, NZa, ZiNl). Ik ben actief betrokken bij het NKC en in de TF cancersurvivorship care werkgroep werk. We proberen tzt onze innovatie te vermarkten om zodoende de voorinvestering die het Radboudumc doet terug te kunnen verdienen. Dit betreft mn onderwijsmodules. Ik heb meegeschreven aan de generieke module Arbeidsparticipatie voor in medisch specialistische RL. Ik zal een voortrekkersrol hebben in het vervolgtraject: het maken van ene ziektespecifieke module Arbeidsparticipatie voor oncologische RL. En ik ben kerngroeplid van de update van de RL kanker en werk voor bedrijfsartsen |
Ontwikkelen zorgmodel arbeidsgerichte zorg (Janssen Pharma en Radboudumc, in-kind projectondersteuning van Janssen Pharma) |
juli 2025 |
Geen restricties |
|
Ellen Passchier |
Verpleegkundig specialist revalidatie hoofd-hals oncologie tot november 2024 in Antoni van Leeuwenhoek
Heden: - verpleegkundig specialist in de wijk (Buurtzorg Amsterdam) - docent aan de Master ANP (Hogeschool inHolland) - buitenpromovendus afdeling hoofd-hals oncologie (Antoni van Leeuwenhoek) |
Geen |
Geen |
Geen |
Met ingang van november 2016 promotieonderzoek (evaluatie van revalidatieprogramma bij patiënten met een HHT - haalbaarheidsonderzoek naar beweeginterventie, analyses op kwaliteit van leven uitkomsten) |
Door deze richtlijn zal mijn promotie onderzoek (publicaties) meer belangstelling krijgen. |
Geen |
juli 2025 |
Geen restiricties |
|
Jos Elbers |
Radiotherapeut-oncoloog Erasmus MC |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
juli 2025 |
Geen restricties |
|
Kathelijn Versteeg |
internist-oncoloog AmsterdamUMC internist-ouderengeneeskunde AmsterdamUMC |
geen |
geen |
geen |
geen |
geen |
geen |
juli 2025 |
Geen restricties |
|
Lisette van der Molen |
logopedist/senior onderzoek aan het NKI-AVL. |
Het geven van bij/nascholing met betrekking tot de (logopedische) functionele uitkomsten na een behandeling in het HH gebied. Deze scholing kan zowel onbetaald als betaald zijn. |
Geen |
nvt |
ja Atos Medical AB Zweden Unrestricted research grant waardoor er PhD studenten kunnen worden aangenomen
De afdeling hoofd-halsoncologie van het AvL krijgt deze unrestricted research grant van Atos Medical (dus niet op persoonlijke titel van dit werkgroeplid). Ik ben in vaste dienst bij het AvL en ook niet afhankelijk van deze grant.
|
In 2010 heb ik samen met Prof. Hilgers het hoofd-halsrevalidatieprogramma ontwikkeld, welke als (standaard) nazorg binnen het NKI-AVL wordt aangeboden. Mocht dit ook het advies worden van deze richtlijn, dan zal het NKI-AVL een voorsprong hebben op de andere HH centra mbt implementatie.
Als kartrekker van de onderzoekslijn: survivorship rehabilitation and QoL na Hoofd-Halskanker begeleiden van meerdere PhD studenten met o.a. het onderwerp dysfagie. De kans is aanwezig dat er publicaties uit onze onderzoeksgroep terecht zullen komen in de output van de systematische literatuur searches voor deze richtlijn. Er is geen sprake van vermarkting of verwerven van een boegbeeldfunctie bij organisaties. |
nvt |
juli 2025 |
Geen restricties |
|
Luc Karssemakers |
Antoni v Leeuwenhoek Ziekenhuis, afdeling hoofd-hals chirurgie |
Afdeling Kaakchirurgie Slotervaart |
Geen |
Geen |
zie onderstaand STW Craniosafe, ideale implantaat schedelplastieken TKI Sternofix, implantaten sternaal voor laryngectomiepatienten |
Geen |
Geen |
juli 2025 |
Geen restricties (extern gefinancierd onderzoek heeft geen relatie met het onderwerp van de richtlijn) |
|
Marieke Jacobs |
Bedrijfsarts / klinisch arbeidsgeneeskundige, Radboudumc |
Werkzaam als instituutsopleider bedrijfsartsenopleiding bij de SGBO, Radboudumc |
Geen |
Niet van toepassing |
Niet van toepassing |
Niet bewust van |
Nee |
juli 2025 |
Geen restricties |
|
Narda Hendriks-Brouwer |
Medisch Spectrum Twente- plastisch chirurg Ziekenhuisgroep Twente-plastisch chirurg |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
juli 2025 |
Geen restricties |
|
Rob Burdorf |
Patiëntenvertegenwoordiger. Lid van de Wetenschappelijke Advies Commissie van de PVHH. Onbetaald |
geen |
geen |
nvt |
nvt |
nvt |
geen |
juli 2025 |
Geen restricties |
|
Caroline Speksnijder |
Associate professor UMC Utrecht |
Docent: *MSc Oncologie Fysiotherapie; Avans+ *MSc Orofaciale Fysiotherapie SOMT Physiotherapy University Werkgroep Kennisagendaherziening KNO Bestuurstaken: *Koninklijk Genootschap voor Fysiotherapie (KNGF): Bestuurslid Wetenschappelijk College Fysiotherapie (WCF) *Paramedische Werkgroep Hoofdhalstumoren (PWHHT): voorzitter *Dutch Association of Supportive Care in Cancer (DASCC): voorzitter *International Physiotherapy in HIV/Aids, Oncology, and Hospice and Palliative Care (IPT-HOPE part of World Physiotherapy): Vice-president |
Geen |
Nee |
Perioperative nutritional intervention with Fortifit Energy® in combination with exercise versus standard of care in head and neck cancer patients undergoing combined approach resection: a pilot study(gefinancierd door Danone, unrestricted grant, geen PI)
Integrating the Knowledge Agenda Physiotherapy into the science policy of the Royal Dutch Association for Physiotherapy (KNGF) (gefinancierd door ZonMw)
Prehabilitatie fysieke fitheid vooraf aan totale laryngectomie (gefinancierd door Nederlands Fonds tegen Kanker, unrestricted grant) |
nee |
nvt |
juli 2025 |
Restricties ten aanzien van het formuleren van aanbevelingen over het onderwerp op UV6 (nutritionele en excerise interventies ter preventie en behandeling) |
|
Petra Verdouw |
Patiëntenvereniging HOOFD-HALS Directeur |
geen |
geen |
geen |
geen |
geen |
geen |
juli 2025 |
Geen restricties |
|
Annemieke Kok |
Diëtist, onderzoeker |
secretaris PWHHT lid Landelijke Werkgroep Diëtisten Oncologie (tot jan 2024)
Vice-voorzitter van de Landelijke Werkgroep Diëtisten Oncologie (LWDO) (sinds april 2025). |
geen |
nee |
zie onder Ontwikkeling PEG keuzehulp voor hoofd-halskankerpatienten (Michel Keijzer Fonds) Perioperative nutritional intervention with Fortifit Energy® in combination with exercise versus standard of care in head and neck cancer patients undergoing combined approach resection: a pilot study(gefinancierd door Danone, unrestricted grant, geen PI) |
nee |
nee |
juli 2025 |
Restricties ten aanzien van het formuleren van aanbevelingen over het onderwerp op UV5 (nutritionele en excerise interventies ter preventie en behandeling) |
|
Doke Buurman |
Tandarts-MFP bij Maastricht UMC+ (betaald) |
Lid Consilium MFP bij de NVGPT (onbetaald) Lid ROC Mondzorg voor mensen met kanker (in de voorgeschiedenis) van KIMO (vacatieregeling) |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
juli 2025 |
Geen restricties |
|
Michael Brouwers |
Revalidatiearts Anthony van Leeuwenhoek Ziekenhuis Amsterdam |
geen |
geen |
geen |
geen |
geen belangen |
geen belangen |
juli 2025 |
|
Inbreng patiëntenperspectief
De richtlijnwerkgroep besteedde aandacht aan het patiëntenperspectief door het uitnodigen van Patiëntenvereniging Hoofd-Hals voor de schriftelijke invitational conference, en twee afgevaardigde namens deze patiëntenorganisatie in de werkgroep. Het verslag van de invitational conference (zie aanverwante producten) is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntenvereniging en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerde de werkgroep conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
GLIM criteria |
geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en daarom naar verwachting geen substantiële financiële gevolgen zal hebben voor de collectieve uitgaven.
|
