Medicamenteuze behandeling van agressie en agitatie bij NAH
Uitgangsvraag
Wat is de aanbevolen strategie voor het toepassen van medicamenteuze behandelingen voor agressie of agitatie bij patiënten met neuropsychiatrische gevolgen na NAH?
Aanbeveling
Houd rekening met de volgende aandachtspunten bij medicamenteus beleid bij patiënten met hersenletsel:
- Behandel -indien mogelijk- eerst agitatie of agressie volgens niet-medicamenteus beleid;
- Staak medicatie die agressie kan veroorzaken of verergeren;
- Kies medicatie die ingrijpt op de oorzaak van de agitatie en/of agressie. Zie figuur 1. voor een overzicht van geprefereerde medicamenten;
- Let op de risico’s specifiek voor de patiëntengroep met hersenletsel zoals effect op cognitie, neurologisch herstel, epileptische insulten en valgevaar en op risico’s bij comorbiditeit en polyfarmacie;
- Overweeg in de acute fase medicamenteuze behandeling met medicamenten die de neurotransmitterbeschikbaarheid verlagen, zoals dexmedetomidine (IC-setting) en propranolol; en in de chronische fase voor middelen die de neurotransmitterbeschikbaarheid verhogen, zoals amantadine, methylfenidaat, sertraline, rivastigmine. Naltrexon kan zowel in de acute- als de chronische fase na hersenletsel worden voorgeschreven;
- Zet haloperidol, olanzapine en risperidon alleen in tijdens de acute fase na hersenletsel en met name als “zo nodig” medicatie gezien de potentieel schadelijke effecten op neurologisch herstel;
- Vermijd inzet van medicatie met anticholinerge eigenschappen vanwege het verwachte negatieve effect op cognitieve functies;
- Beperk sederende medicatie in verband met het valrisico bij patiënten met hersenletsel;
- Breng de risico’s in kaart van de inzet van vrijheid beperkende interventies in combinatie met sedatie, minimaliseer de risico’s voordat deze interventies worden ingezet;
- Start low, go slow: begin met een lage dosering en verhoog deze langzaam op geleide van de klachten.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er zijn vanuit de zoekstrategie vier studies naar voren gekomen die het effect van medicamenteuze behandelingen op agressie of agitatie hebben geëvalueerd bij neuropsychiatrische gevolgen na NAH.
Deze studies zijn geselecteerd uit een eerdere search, omdat er bij de update van de search in 2023 geen aanvullende literatuur van hoge kwaliteit is gevonden. De studies betreffen een selectie aan interventies, namelijk sertraline, amantadine en methylfenidaat. Wegens een hoog risico op bias, indirectheid door afwezigheid van agressie en agitatie op baseline en een kleine onderzoekspopulatie, komt de bewijskracht voor de gerapporteerde uitkomstmaten (ernst van agressie en agitatie en bijwerkingen) voor alle drie de medicamenten uit op zeer laag. Hier ligt duidelijk een kennislacune. Daarnaast is het onbekend of andere medicamenteuze behandelingen een positief effect zouden kunnen hebben op agressie en agitatie bij patiënten met niet-aangeboren hersenletsel. Hierom kan er op basis van beschikbare literatuur geen antwoord worden gegeven op de vraag wat de waarde is van medicamenteuze behandelingen voor agressie of agitatie bij patiënten met neuropsychiatrische gevolgen na NAH.
Uit internationale richtlijnen komen geen eenduidige aanbevelingen over medicamenteuze behandeling na hersenletsel naar voren (Block, 2023). Ook een recente INCOG-richtlijn gericht op medicamenteuze behandeling in de PTA-fase (Ponsford, 2023), doet geen aanbeveling ten aanzien van medicamenteuze behandeling bij agitatie en agressie, gezien het gebrek aan bewijs.
Een knelpunt in de dagelijkse zorg voor patiënten met hersenletsel en agitatie of agressie blijft echter de grote heterogeniteit in voorschrijfgedrag bij voornamelijk off-label medicatie (Ponsford, 2023; Block, 2023). Daarnaast hebben enkele medicamenten een tegengesteld of paradoxaal effect en kwam uit de knelpuntenanalyse naar voren dat er onder voorschrijvers onduidelijkheid bestaat over de eventuele schadelijke effecten van medicatie bij patiënten met hersenletsel.
Ten aanzien van paradoxale of schadelijke effecten van medicatie geeft recent onderzoek meer inzicht in het potentieel werkingsmechanisme van medicatie. De laatste 15 jaar is meer kennis ontstaan over de neurocognitieve basis van agitatie en agressie en de werking van het door Blair in 2012 beschreven basale bedreigingssysteem (Basic Threat System). Met behulp van literatuur over het neurologische werkingsmechanisme van agitatie en agressie heeft de werkgroep de beschikbare studies opnieuw beoordeeld. Dit is door de werkgroep vervolgens gecombineerd met literatuur over pathofysiologische mechanismen bij hersenletsel en potentieel schadelijke effecten van medicatie op neurologisch herstel en op lichamelijke of cognitieve gevolgen van hersenletsel.
Hieruit zijn door de werkgroep een aantal aandachtspunten voor medicamenteus beleid gedestilleerd. Per aandachtspunt zijn een aantal medicamenteuze opties beschreven op basis van theoretische kennis, bestaande studies over de effectiviteit van het middel bij agressie en agitatie en expert opinion. Dit is weergegeven in figuur 1. De aandachtspunten zijn opgenomen in de aanbevelingen.
In tabel 1 staan een aantal veelgebruikte medicamenten bij NAH met agressie en agitatie en hun farmacologische aangrijpingspunt beschreven (farmacotherapeutisch kompas; Block, 2023; Williamson, 2019; Hicks, 2019; Rahmani, 2021; Crowley, 2015; Fagan, 2024; Flanigan, 2020; Wardle, 2016; Murugan, 2019; Balan, 2019).
Tabel 1. Farmacologische aangrijpingspunten en effect medicamenten
|
Medicijncategorie |
Middel |
Beschrijving |
|
Benzodiazepine versterkt selectief de remmende werking van GABA (γ-aminoboterzuur) op de benzodiazepinereceptor in het GABAA-receptor-chloride-ionofore complex. |
lorazepam |
Benzodiazepine, toegepast als hypnoticum en anxiolyticum. |
|
temazepam |
Benzodiazepine, toegepast als hypnoticum. Het heeft tevens anxiolytische, sedatieve en mogelijk spierverslappende en anticonvulsieve eigenschappen. |
|
|
oxazepam |
Benzodiazepine, toegepast als anxiolyticum. |
|
|
Klassieke antipsychotica Klassieke antipsychotica blokkeren dopamine type 2 (D2)-receptoren in mesolimbische systeem. |
haloperidol
|
Butyrofenonderivaat met antipsychotische en geringe sederende werking. Blokkeert zowel dopaminerge (D2) als α1-adrenerge receptoren Heeft een sterke centraal antidopaminerge en een zwakke centraal anticholinerge werking. |
|
Atypische antipsychotica Atypische antipsychotica blokkeren de volgende receptoren: postsynaptische dopamine type 2 (D2)-receptoren in het mesocorticale en limbische hersengebied; serotonine type 2 (5HT2)-receptoren in de prefrontale cortex.
|
quetiapine/ laag D2 affiniteit |
brede receptoraffiniteit. Gaat een interactie aan met de volgende receptoren (met afnemende affiniteit): histamine H1 > α1 (adrenerge) > serotonine 5HT2 > dopamine D2 > α2 (adrenerge) > serotonine 5HT1A > dopamine D1. |
|
olanzapine/matig D2 affiniteit |
blokkerende werking op receptoren voor serotonine (o.a. 5HT2A/2C en 5HT₃), dopamine (D1t/m5), muscarine (m1t/m5), adrenerge (α1) en histamine (H1). |
|
|
risperidon/hoge D2 affiniteit |
sterke antiserotoninerge (5HT2) en antidopaminerge (-D2) activiteit en met matige α1-blokkerende eigenschappen. Risperidon heeft een gering α2-blokkerend en antihistaminerg (-H1) vermogen. Het heeft geen affiniteit tot de cholinerge receptor. |
|
|
Dopamine-agonisten
|
bromocriptine |
D2-dopaminereceptor-agonist met D1-receptor-antagonistische werking. Remt de prolactinesecretie, stimuleert direct de dopaminereceptoren. Hoge dosis presynaptisch hoge affiniteit, postsynaptisch lage affiniteit D2 receptor, resulterend in laag Da afgifte, hoge dosis partiele D2 antagonist. |
|
amantadine |
Amantadine. vertraging van de dopamineheropname in de presynaptische zenuwuiteinden, bevordering van de vrijmaking van endogeen dopamine uit de zenuwuiteinden; verder is het een N-methyl-D-aspartaat (NMDA)- antagonist en heeft het mogelijk enige anticholinerge activiteit. |
|
|
levodopa |
Levodopa is een dopamineprecursor die de bloed-hersenbarrière passeert en enzymatisch wordt gedecarboxyleerd tot de werkzame dopamine. |
|
|
methylfenidaat |
Amfetamine: het sympathicomimeticum en lijkt in farmacologische eigenschappen op de amfetaminen. Het werkingsmechanisme is niet helemaal bekend. Verondersteld wordt dat methylfenidaat de heropname van noradrenaline en dopamine in het presynaptische neuron blokkeert (o.a. via blokkade van dopamine transporter) en daardoor de afgifte van de neurotransmitters in de extraneuronale ruimte vergroot. |
|
|
Sympathicus modulerende middelen |
dexmedetomidine
|
selectieve α2-receptoragonist. Remming van de locus caeruleus, een overwegend noradrenerge nucleus in de hersenstam geeft een sedatief effect. Activering van de presynaptische α2-adrenerge receptor remt het vrijkomen van noradrenaline, wat de transmissie van pijnsignalen blokkeert. De activering van postsynaptische α2-adrenerge receptoren in het centrale zenuwstelsel remt de sympathische activiteit, waardoor de bloeddruk en de hartfrequentie dalen. Bij lage dosering heeft dexmedetomidine vooral centrale effecten (daling van de hartslagfrequentie en bloeddruk). |
|
Bètablokkers blokkeren β1 en/of β2-receptoren; hierdoor neemt de gevoeligheid van het weefsel voor adrenerge prikkeling (door endogene of exogene catecholaminen) af. |
propranolol
|
niet-selectieve β-blokker zonder intrinsieke sympathicomimetische activiteit.
|
|
Opiodantagonisten
|
naltrexon |
Opioïdantagonist met minimale antagonistische werking. Naltrexon bindt zich competitief aan opioïdreceptoren, waardoor het effect van endogene en exogene opioïden wordt geblokkeerd. Kappa receptorblokkade leidt waarschijnlijk tot afname van taxatie van dreiging en afname van arousal. |
|
Orexine-antagoninsten |
DORA |
Duale orexine receptor antagonisten, orexine heeft directe werking op VTA, amygdala en BNST. Blokkade werkt anxiolytisch, remt agressie en werkt mogelijk anti-epileptisch. In fase van preklinisch onderzoek. |
|
SSRI
|
sertraline
|
Specifieke serotonineheropnameremmer (SSRI). Het remt de heropname van serotonine in het neuron. |
|
Anti-epileptica
|
valproinezuur (cave teratogeniteit)
|
Anti-epilepticum. Het werkingsmechanisme is onbekend. Vermoedelijk wordt de cerebrale en cerebellaire concentratie van de neurotransmitter γ-aminoboterzuur (GABA) verhoogd, als gevolg van remming van de afbraak en/of beïnvloeding van de GABA-receptor, en is er een effect op de spanningsgevoelige natrium- en kaliumkanalen. |
|
carbamazepine
|
Anticonvulsieve en psychotrope werking. Licht anticholinerg effect. Het remt de herhaaldelijk optredende hoogfrequente neurale ontladingen en vermindert de uitbreiding van synaptische impulsen. Verder remt het de omzetting van catecholaminen en de vrijgifte van glutamaat. |
|
|
Slaapmedicatie |
melatonine
|
Endogeen hormoon geproduceerd door de pijnappelklier en qua structuur verwant aan serotonine. Van de werking op de melatoninereceptoren MT1, MT2 en MT3 wordt aangenomen dat het bijdraagt aan de slaap inducerende eigenschappen ervan, omdat deze receptoren (voornamelijk MT1 en MT2) een rol spelen bij de regulering van het dag-/nachtritme en de slaap. |
|
Acetylcholine modulatoren
|
rivastigmine
|
Remming van acetylcholinesterase, De cholinerge neurotransmissie verbetert door langere aanwezigheid van acetylcholine in de synaptische spleet. |
Het basale bedreigingssysteem
Het basale bedreigingssysteem omvat de amygdala, hypothalamus en substantia grisea centralis/periaqueductale grijze stof (PAG) (Blair 2012; Hashikawa, 2017; Bertsch, 2020; Lischinsky, 2020) en is betrokken bij agressie en aanvallend gedrag (Bertsch, 2020; Lischinsky, 2020). Het ventrale striatum is betrokken bij woede uitgelokt door frustratie (ofwel het uitblijven van een beloning). Multisensore, agressie-uitlokkende stimuli worden verwerkt door de thalamus, waarna het basale bedreigingssysteem wordt geactiveerd (Lischinsky, 2020; Bertsch, 2020). Of uiteindelijk agressief gedrag optreedt hangt af van de taxatie van dreiging, mede op basis van de sociale context (Bertsch 2020), leerervaringen en hiermee de te verwachten dreiging (Bertsch, 2020).
De taxatie vindt plaats door de amygdala; de ventromediale prefrontale cortex (vmPFC) en het salience netwerk (dorsale anterieure insula en cortex cingularis anterior (ACC) (Bertsch, 2020, Menon et al., 2022). Bij verwachte dreiging wordt de bed nucleus van de stria terminalis (BNST) (Zu et al., 2023) actief (Klumpers, 2017). De BNST vormt een schakel met het hypothalamus-hypofyse-bijniersysteem (de HPA-as) (Choi et al, 2007). Het ventrale striatum is (als onderdeel van het mesolimbische systeem) verder betrokken bij leer- en beloningseffecten van agressie (Bertsch, 2020; Wei, 2022; Yamaguchi, 2018).
Agressief gedrag treedt op bij activatie van de PAG. Controle over agressie wordt bereikt door emotieregulatie, oftewel de mogelijkheid om de negatieve angstige emotie te hanteren of af te zwakken via het fronto-parieto-insulaire netwerk (Bertsch, 2020; Li, 2021; Taylor., 2009); en door inhibitie van het agressieve gedrag via de orbitofrontale cortex (Bertsch, 2020).
De gevoeligheid van het bedreigingssysteem is afhankelijk van de interne toestand van de persoon, zoals van de aanwezigheid van honger, stress, het energieniveau, de tijd van de dag en de tijd van het jaar (Todd, 2019; Lischinsky, 2020). Factoren zoals een tekort aan daglicht (Munley, 2022), melatonine (Munley, 2022; Paribello, 2022; Lischinsky, 2020), circulerend dihydroepiandrosteron (DHEA, Munley, 2022, Rendon, 2015), testosteron- en oestrogeenniveau ’s (Munley, 2022; Wei, 2022) en ghreline (Lischinsky, 2020) kunnen het systeem direct of indirect beïnvloeden. Dopamine heeft, via activatie van D2 receptoren, een direct faciliterende rol bij de opwekking van agressie door de ventrale hypothalamus (Yamaguchi, 2018).
Tabel 2. geeft een overzicht van de effecten op het basale bedreigingssysteem bij de middelen beschreven in tabel 1.
Tabel 2. Invloed veel voorgeschreven medicatie op angst en dreigingssysteem
|
Middel: |
Potentieel werkingsmechanisme |
||||
|
Invloed op dreigingssysteem |
Invloed op leerervaringen/ taxatie dreiging/controle agressie |
Invloed op angst/stemming |
Cave |
||
|
Benzodiazepine |
|||||
|
lorazepam |
- |
- |
anxiolyticum |
- |
|
|
temazepam |
- |
- |
- |
- |
|
|
oxazepam |
- |
- |
anxiolyticum |
- |
|
|
Dopamine signalering- Klassieke antipsychotica |
|||||
|
haloperidol |
verminderen activerende werking D2 receptoren hypothalamus (+) |
afname werking DA (-) |
anticholinerge effecten, extrapiramidale verschijnselen en verminderen plasticiteit |
||
|
Dopamine signalering- Atypische antipsychotica |
|||||
|
quetiapine/ laag D2 affiniteit |
afname werking DA (-) |
||||
|
olanzapine/matig D2 affiniteit |
verminderen activerende werking D2 receptoren hypothalamus (+) |
afname werking DA (-) |
|||
|
risperidon/hoge D2 affiniteit |
verminderen activerende werking D2 receptoren hypothalamus (+) |
afname werking DA (-) |
extrapiramidale verschijnselen en verminderen plasticiteit |
||
|
Dopamine signalering- Dopamine-agonisten |
|||||
|
bromocriptine |
afhankelijk van doses D2 agonist of gedeeltelijke antagonist (+/-) |
toename werking DA bij hoge dosis (+) |
|||
|
amantadine |
verhogen activerende werking D2 receptoren hypothalamus? (-?) |
toename werking DA (+) |
anticholinerg effect |
||
|
methylfenidaat |
verhogen activerende werking D2 receptoren hypothalamus? Activatie sympathicus (-) |
toename werking DA (+) |
toename angst? (-?) |
||
|
Sympathicus modulerende middelen |
|||||
|
dexmedetomidine |
remming sympathicus (+) |
afname werking DA (-) |
Anxiolytisch (+) |
||
|
Bètablokkers |
|||||
|
propranolol |
Remming sympathicus input voor taxatie dreiging (+) |
||||
|
Opiodantagonisten |
|||||
|
naltrexon |
minder identificatie van dreiging, Dopamine afname amygdala |
minder taxatie dreiging door minder dopamine via blokkade Kappa receptoren in mesolimbisch systeem (+) |
|||
|
DORA |
|
|
|
||
|
Dual Orexin Receptor Antagonist |
remmende werking hypothalamus (+) |
remmende werking VTA (+) |
Anxiolytisch (+) |
|
|
|
SSRI |
|||||
|
sertraline |
Verhogen serotonine ter plaatse van serotonine receptoren in amygdala, het effect is afhankelijk van upregulatie specifieke 5HT receptoren (+/-) |
Verhogen serotonine ter plaatse van serotonine receptoren in BNST, het effect is afhankelijk van upregulatie specifieke 5HT receptoren (+/-) |
Anxiolytisch (+) |
||
|
Anti-epileptica |
|||||
|
Valproinezuur (cave teratogeniteit) |
verhogen androgenen (-) |
||||
|
carbamazepine |
verlagen testosteron, estradiol, DHEA (+) |
anticholinerge werking |
|||
|
Slaapmedicatie |
|||||
|
melatonine |
directe werking, agressieverhogend (-) |
||||
|
Acetylcholine modulatoren |
|||||
|
rivastigmine |
Verbetering controle (+) |
||||
Voetnoot: middelen hebben positief (+) en negatief (-) effect op het verminderen van agressie per aangrijpingsmechanisme
Verantwoording bij tabel:
a. Hormonen en neurotransmitters -zoals melatonine, ghreline en DHEA- activeren direct het bedreigingssysteem (Lischinsky, 2020; Todd, 2019; Munley, 2022, Rendon, 2015). Afgifte van het hormoon orexine vindt in de laterale hypothalamus plaats. Dit neuropeptide reguleert eetlust en bevordert de waaktoestand, maar is daarnaast ook door interactie met opiaat-receptoren betrokken bij het beloningssysteem. Het heeft een werking op de BNST en amygdala, VMHvL en VTA (Fagan, 2024). Manipulatie van de signaaloverdracht van orexine heeft invloed op agressie bij muizen (Flanigan et al., 2020). Voor de werking van orexine is noradrenerge en GABA-activiteit een voorwaarde. Antagonisten van de orexine-receptor (Dual Orexin Receptor Antagonist/DORA) zijn veelbelovend voor de behandeling van slaapproblemen, epilepsie (Sheibani, 2023), woede/agressie (Flanigan, 2020) en leereffecten van agressief gedrag (Fagan, 2024). Onderzoek naar DORA’s is in de preklinische fase. Dit is een kennislacune.
b. Op afname van angst of de taxatie van dreiging hebben SSRI's, naltrexon (Crowley, 2015; Wardle, 2016) en DORA's (Fagan, 2024) effect. Propranolol en dexmedetomidine hebben wellicht ook dit effect, door remming van de sympathische input op de BSNT (Lebow, 2016). Onderzoek naar het effect van dexmedetomidine op een delier en agitatie bij patiënten met traumatisch hersenletsel op de intensive care liet zien dat patiënten in de dexmedetomidinegroep in vergelijking met de haloperidolgroep kalmer waren en minder verschijnselen toonden van een delier (Soltani, 2021).
c. Het effect op agressie door modulatie van gedragscontrole via ondersteuning van cognitieve functies is aanwezig bij agonisten van dopamine, cholinergica en catecholamines (Schwartz, 2017), zoals amantadine (Zafonte, 2020), methylfenidaat en rivastigmine
d. Vermindering van een zichzelf versterkend effect van agressie middels beloning vindt plaats via beïnvloeding van het mesolimbische systeem, door naltrexon (Valenta, 2013).
Aandachtspunten bij medicatievoorschrift
Indien mogelijk eerst behandeling van agitatie of agressie volgens niet-medicamenteus beleid, daarna pas inzet van medicamenteuze behandeling.
Het is van belang om de interne situatie van patiënt (voedingstoestand, biologische klok) te optimaliseren voor positieve beïnvloeding van het bedreigingssysteem (zie ook module niet-medicamenteuze behandeling van agressie en agitatie bij NAH). Het is goed mogelijk dat agitatie en agressie een bijproduct zijn van natuurlijk herstel (Wang, 2021). Hormonen en neurotransmitters -zoals melatonine, ghreline en DHEA- hebben een anti-inflammatoir effect (Neren, 2016; Bell., 2023), maar activeren ook het bedreigingssysteem (Lischinsky, 2020; Todd, 2019; Munley, 2022, Rendon, 2015). Dit zou theoretisch betekenen dat verbetering van de medische toestand van patiënt leidt tot afname van agitatie en agressie, omdat het gepaard gaat met vermindering van inflammatie en hiermee met afname van lichaamseigen anti-inflammatoire signaalstoffen. Dit zou betekenen dat agressie zelflimiterend kan zijn Voor de voorschrijver is het belangrijk hiervan bewust te zijn, met name in de fase van PTA/confusional state of een delier.
Staken van agressie verhogende middelen.
Hormonen en neurotransmitters -zoals estrogenen, androgenen, melatonine, ghreline, DHEA en dopamineagonisten beïnvloeden direct het bedreigingssysteem (zie tabel 2). Het is van belang om bij agressie middelen te staken of te antagoneren die agressie verhogen. Voor toelichting ten aanzien van middelen die de dopaminereceptor moduleren (zie het kopje “Risico op negatieve effecten van het middel”).
Fase na letsel
Kies direct na het ontstaan van het letsel bij voorkeur voor middelen die de neurotransmitterbeschikbaarheid verlagen en in latere fasen voor middelen die de neurotransmitterbeschikbaarheid verhogen. Zie tabel 3. In de hyperacute fase, binnen enkele uren na letsel, ontstaat er een toename van neurotransmitterafgifte (Hsieh, 2017; Guerriero, 2015); met een verschuiving naar hyperexcitatie in de hersenen en neurotoxiciteit. Neuro-inflammatie, met doorlaatbaarheid van de bloed-hersenbarrière houdt de verstoorde glutamaat/GABA verhouding in stand (Neren, 2016). Glutamaat heeft een duale functie: het is in de hyperacute fase betrokken bij neurotoxiciteit, maar is bevorderd in latere fasen neuronale reparatie en overleving (Godoy 2021). Veranderingen in neurotransmittersystemen in hyperacute (binnen enkele uren), acute (uren tot weken) en chronische (maanden tot jaren) is beschreven door McGuire (2017). Hierbij is er in uren tot weken na letsel effectief een grotere beschikbaarheid van onder andere dopamine, noradrenaline, acetylcholine en serotonine, terwijl die beschikbaarheid na maanden of jaren juist verlaagd is. Ook op het niveau van whole-brain netwerken -zoals het salience netwerk en het default mode netwerk- zijn veranderingen meetbaar na hersenletsel (Sharp, 2014). Over compensatoire en herstelmechanismen is nog relatief weinig bekend.
Delier of inflammatie
Mogelijk is agitatie en agressie bij inflammatie zelflimiterend (Wang, 2021). Wanneer inflammatie op de voorgrond staat (bijv. bij encefalitis, delier of in de acute fase na hersenletsel) kan er theoretisch een plek zijn voor middelen met een anti-inflammatoir effect. Zie tabel 3. Voorzichtigheid is geboden met gebruik van haloperidol en atypische antipsychotica (zie het kopje “Risico op negatieve effecten van het middel”).
Epilepsie
Voorzichtigheid is geboden met middelen tegen agitatie en agressie waarbij insulten als bijwerking zijn beschreven. Anderzijds is het bij patiënt met hersenletsel en epilepsie van belang van de voorgeschreven anti-epileptica het effect op leren en geheugen te evalueren.
Posttraumatische epileptische insulten weerspiegelen veranderingen binnen de hersencircuits in de balans tussen excitatie en inhibitie (de E/I excitatoire balans) (Guerriero, 2015). De sterkte en timing van exciterende en inhiberende signaaloverdracht remmende binnen neurale circuits vormt de activiteit afhankelijke plasticiteit die nodig is voor gedragsaanpassingen aan omgevingsstimuli en voor leren en geheugen (Guerriero, 2015). Verstoring van de E/I balans blijft veranderen gedurende weken, maanden en jaren na hersenletsel.
Tabel 3. geeft de effecten van medicatie op neurotransmitterbeschikbaarheid, inflammatie en hyperexcitatie weer.
Tabel 3. Middelen die biologische beschikbaarheid neurotransmitters stimuleren/remmen en effect op inflammatie
|
Middel: |
Potentieel werkingsmechanisme |
||
|
Invloed neurotransmitter overschot/depletie
|
Invloed op inflammatie
|
Effect op GABA/glutamaatbalans
|
|
|
Benzodiazepine |
|||
|
lorazepam |
- |
- |
versterkt GABA (B+) |
|
temazepam |
- |
- |
versterkt GABA (B+) |
|
oxazepam |
- |
- |
versterkt GABA (B+) |
|
Dopamine signalering- Klassieke antipsychotica |
|||
|
haloperidol |
antidopaminerg, anticholinerg, blokkade α1-adrenerge receptoren (a1-adrenergic receptors binden en activeren NA en reguleren symphaticus) (A+, C-) (N-) |
blokkade noradrenaline-effecten (AI -) |
|
|
Dopamine signalering- Atypische antipsychotica |
|||
|
quetiapine/ lage D2 affiniteit |
afname werking DA, NA (A+, C-), (N-) |
blokkade noradrenaline-effecten (AI-) |
|
|
olanzapine/matig D2 affiniteit |
afname werking DA |
blokkade noradrenaline-effecten (AI-) |
|
|
risperidon/hoge D2 affiniteit |
afname werking DA (A+, C-) (N-) |
geringe blokkade noradrenaline effecten (AI-) |
|
|
Dopamine signalering- Dopamine-agonisten |
|||
|
bromocriptine |
toename werking DA bij hoge dosis (A-, C+) (N+) |
||
|
amantadine |
toename werking DA (A-, C+) (N+) |
mild anti-inflammatoire werking (AI+) |
blokkeert werking glutamaat (NMDA-R antagonist) (B+) |
|
methylfenidaat |
toename werking DA en NA (A-, C+) (N+) |
faciliteren noradrenaline effecten (AI+) |
|
|
Sympathicus modulerende middelen |
|||
|
dexmedetomidine |
remt vrijkomen catecholamines (A+, C-) (N-) |
anti-inflammatoir (AI+) |
|
|
Bètablokkers |
|||
|
propranolol |
remt effect van noradrenaline (A+, C-) (N-) |
remt effect van noradrenaline (AI -) |
|
|
Opiodantagonisten |
|||
|
naltrexon |
|
anti-inflammatoir (AI+) |
afname glutamaat (B+) |
|
DORA |
|
|
|
|
antagonisme adrenerge effecten (A+, C-) (N-) |
|
|
|
|
SSRI |
|||
|
sertraline |
toename serotonine (A-, C+) (N+) |
||
|
Anti-epileptica |
|||
|
Valproinezuur (cave teratogeniteit) |
toename GABA (B+) |
||
|
carbamazepine |
afname omzetting catecholamines (A-, C+) (N+) |
afname anti-inflammatoir effect DHEA (AI-) |
afname glutamaat (B+) |
|
Slaapmedicatie |
|||
|
melatonine |
anti-inflammatoir effect (AI+) |
||
|
Acetylcholine modulatoren |
|||
|
rivastigmine |
toename acetylcholine (A-, C+) (N+) |
anti-inflammatoir (AI+) |
|
Voetnoot: Positief effect in acute (A+) en chronische (C+) fase. Negatief effect acute (A-) en chronische (C-) fase. Toename (N+) en afname (N-) biologische beschikbaarheid neurotransmitters. Anti-inflammatoire werking (AI+), remming anti-inflammatoire werking (AI-). Positief (B+) en negatief (B-) effect op glutamaatbalans, waarbij positief effect wordt gedefinieerd als vermindering van hyperexcitatie.
Toelichting/verantwoording:
Neurotransmitters:
Middelen die neurotransmitterafgifte remmen: dexmedetomidine remt afgifte van catecholamines (farmacotherapeutisch kompas); DORA's remmen adrenerge effecten (Fagan, 2024); antipsychotica hebben blokkerende werking op dopamine en noradrenaline (farmacotherapeutisch kompas).
Middelen die neurotransmitterafgifte stimuleren
Dopamine-agonisten zijn bromocriptine, methylfenidaat, amantadine (Bales et al., 2009). Sertraline vermindert serotonine heropname en rivastigmine vermindert afbraak van acetylcholine (farmacotherapeutisch kompas).
Carbamazepine remt omzetting van catecholamines (farmacotherapeutisch kompas, Hammond et al., 2021).
Inflammatie:
Noradrenaline heeft een anti-inflammatoir effect (Russel., 2019; Neren, 2015), dus alle middelen die noradrenaline blokkeren, remmen het anti-inflammatoire effect.
Carbamazepine remt, door remming van DHEA (Lagana, 2016) het anti-inflammatoir effect (Neren, 2015) van dit hormoon.
Middelen met anti-inflammatoire werking zijn: dexmedetomidine (Soltani, 2021), rivastigmine (Neren, 2015), naltrexon (Younger, 2014), amantadine (Ma, 2020) en noradrenaline-agonisten (Russel, 2019), zoals methylfenidaat. Methylfenidaat heeft daarnaast mogelijk een neuroprotectief effect (Carneiro, 2024)
Hyperexcitatie:
Middelen met een als effect vermindering van glutamaat in de GABA/glutamaatbalans en -hiermee op het verminderen van hyperexcitatie- zijn: lorazepam; temazepam; oxazepam (farmacotherapeutisch kompas); amantadine (Ma, 2020), naltrexon (Younger, 2014); valproinezuur (cave teratogeniteit) en carbamazepine. In een studie naar het effect van carbamazapine op afname van agitatie en agressie meer dan 6 maanden na traumatisch hersenletsel was er geen verschil in effect tussen de interventiegroep en de controlegroep (Hammond, 2021).
Risico op negatieve effecten van het middel
Effect op neurologisch herstel
Dopamine speelt een belangrijke rol bij herstel van plasticiteit, motorisch functioneren en leervermogen (Bales, 2009; Verduzco-Mendoza, 2021). Het is dus belangrijk om specifiek bij patiënten met hersenletsel het gebruik van dopamine-antagonisten te minimaliseren.
De rol van dopamine is complex, met verschillende effecten op D1 en D2 receptoren (Verduzco-Mendoza, 2021); verschillende effecten synaptisch en postsynaptisch (McGuire, 2017); en striataal en extrastriataal (Bales, 2019). Er is hierbij een interactie met glutamaat, omdat glutamaat als aangrijpingspunt striatale dopaminereceptoren heeft, waarbij activatie van D1 receptoren leidt tot verhoogde excitatie en activatie van D2 receptoren tot verlaagde excitatie.
Antipsychotica zijn dopamine- antagonisten. Antipsychotica worden van oudsher voorgeschreven bij agitatie bij bijvoorbeeld schizofrenie of een delier. Dopamine werkt direct agressieverhogend op het dreigingssysteem. Onderzoek naar dieren met hersenletsel heeft een negatief effect laten zien van D2 receptor antagonisten op neurologisch herstel (Race, 2023; Cataford 2024), met name wanneer deze dagelijks werden gegeven. Een intermitterende dosis van haloperidol, risperidon en quetiapine, gestart binnen 24 uur na het letsel, liet geen negatieve effecten op cognitief en motorisch herstel zien (Race, 2023). In recent onderzoek naar de werking van olanzapine bij patiënten in de PTA-fase na traumatisch hersenletsel was er een positief effect van olanzapine op agitatie in 3 van de 5 patiënten. Echter liet deze groep ook een slechtere oriëntatie en geheugenfunctie zien en was er een trend richting een langere PTA-duur dan bij de placebogroep (Phyland, 2023).
Het is dus aan te bevelen om antipsychotica (dopamine-antagonisten) met hoge of matige D2 affiniteit zoals haloperidol, olanzapine en risperidon alleen in te zetten in de fase direct na hersenletsel en met name als “zo nodig” medicatie, gezien de te verwachten schadelijke effecten. Dopamine-antagonisten in het algemeen zijn af te raden bij patiënten met NAH in latere fasen gezien de lage dopaminespiegels in de hersenen en de rol van dopamine bij neuroplasticiteit/leren.
Zoals hierboven beschreven kunnen middelen met effect op de balans tussen excitatie en inhibitie van neurale netwerken, zoals middelen die de GABA/glutamaatbalans veranderen (bijvoorbeeld benzodiazepinen, anti-epileptica) effect hebben op leervermogen en geheugen (Guerriero, 2015).
Acetylcholine speelt een belangrijke rol bij cognitieve functies. Bij patiënten met cognitieve problemen is voorzichtigheid is geboden met middelen die anticholinerge eigenschappen bezitten.
Overige negatieve effecten
Sederende medicamenten zoals haloperidol en benzodiazepines kunnen bij patiënten met motorische problemen leiden tot toename van valincidenten. Er werd bij dierproeven van lorazepam geen schadelijke motorische of cognitieve effecten gevonden (Cheng, 2019). Ook bestaat bij langdurig gebruik van benzodiazepines het risico op verslaving.
Inzet van vrijheidsbeperkende maatregelen kan worden overwogen ter bescherming van patiënt of betrokkenen, wanneer de agressie schadelijk is voor patiënt en/of zorgverleners of het zorgproces in de acute fase ernstig hindert. Hierbij valt te denken aan een hinderend effect van agitatie of agressie op de uitvoer van diagnostiek of op behandeling van de fysieke oorzaak van agressie. (zie ook module wettelijke kaders ten aanzien van gedwongen zorg bij patiënten met niet aangeboren hersenletsel). Een case report beschrijft de inzet van vrijheidsbeperkende maatregelen in combinatie met milde sedatie bij een patiënt met agitatie in de acute fase na traumatisch hersenletsel (Berrol, 1988). Het benadrukt de potentiële schade van inzet van vrijheidsbeperkende maatregelen (bewustzijnsverlies en verstrikt raken in de fixatie met langdurige vegetatieve toestand tot gevolg). De risico’s van inzet van fixatie in combinatie met sedatie moeten daarom per patiënt in kaart gebracht worden en geminimaliseerd voordat men over gaat op dit type maatregelen (Carrier, 2021). Een compleet overzicht van de negatieve bijwerkingen valt buiten het bestek van deze richtlijn. Hoover (2020) en Williamson (2019) geven in hun reviews een overzicht van negatieve effecten van medicatie voor agitatie en agressie bij hersenletsel.
Beoogde aangrijpingspunt binnen het bedreigingssysteem bij medicatiewissel.
Bij de keuze voor een medicament kan men kennis over het dreigingssysteem meewegen. Indien een eerste middel niet effectief is, kan men bij een medicatiewissel kiezen voor een ander aangrijpingspunt.
Theoretisch bestaan de volgende mogelijkheden (zie tabel 4.):
- Directe beïnvloeding van het dreigingssysteem (met als aangrijpingspunt amygdala of de hypothalamus). Voorbeelden zijn sertraline, dopaminereceptor antagonisten, dexmedetomidine, carbamazepine.
- Vermindering van de taxatie van dreiging (door bijvoorbeeld het salience systeem te inhiberen met DORA, sympathische input te verminderen met propranolol of amygdala activiteit te verminderen met anxiolytica zoals sertraline).
- Ondersteuning van corticale gedragsinhibitie (aangrijpingspunt orbitofrontale cortex) met bijvoorbeeld amantadine.
- Vergroting van emotieregulatie (fronto-parieto-insulaire netwerk) en verandering van leerervaringen (mesolimbische systeem) met bijvoorbeeld naltrexon.
Locatie letsel
Indien patiënt geen enkele aanspraak kan doen op de controlefunctie lijken interventies die direct invloed hebben op de hypothalamus of op systemen betrokken bij taxatie van dreiging het meest aangewezen. Zie tabel 4. voor een overzicht. Gebrek aan controle kan optreden bij inprentingsstoornissen tijdens de PTA-fase/confusional state, of wanneer direct na hersenletsel de modulerende systemen van agitatie en agressie zijn aangedaan, zoals de insula (betrokken bij oriëntatie, cognitieve- en cognitief-emotionele processen) (Li et al., 2021; Taylor et al., 2009) of bij frontale schade aan de dmPFC, vmPFC en OFC (betrokken bij controlemechanismen van agressie).
Tabel 4. geeft een overzicht waarin bovenstaande informatie is samengebracht.
Tabel 4.Medicamenteuze opties gegroepeerd naar aangrijpingspunt binnen het dreigingssysteem, rekening houdend met negatieve effecten en kenmerken op casusniveau
|
Middel: |
Potentieel werkingsmechanisme |
Kenmerken casus |
|||
|
Invloed op dreigingssysteem |
Invloed op leerervaringen/ taxatie dreiging/controle agressie |
Invloed op Angst/stemming |
Negatieve effecten gerelateerd aan (gevolgen) van hersenletsel |
Toestand van patiënt/comorbiditeit en fase na letsel |
|
|
Anti-epileptica |
|
||||
|
carbamazepine |
+ |
- |
- |
Anticholinerge werking |
C; E |
|
Dopamine-agonisten |
|||||
|
amantadine |
- |
+ |
Milde anticholinerge werking |
C |
|
|
methylfenidaat |
- |
+ |
- |
Toename angst? |
C |
|
Sympathicus modulerende middelen |
|||||
|
dexmedetomidine |
+ |
- |
+ |
A; D |
|
|
Bètablokkers |
|||||
|
propranolol |
+ |
A |
|||
|
Opiodantagonisten |
|||||
|
naltrexon |
+ |
+ |
A; C; D |
||
|
DORA |
|
|
|
|
|
|
Dual Orexin Receptor Antagonist |
+ |
+ |
+ |
|
A; E |
|
SSRI |
|||||
|
sertraline |
+ |
+ |
C |
||
|
Acetylcholine modulatoren |
|||||
|
rivastigmine |
+ |
C; D |
|||
Voetnoot: positieve werking (+) en negatieve werking (-) op mechanisme. Voorkeur toediening tijdens direct na letsel (A) en in latere fasen na letsel (C). Voorkeur bij hyperexcitatie/epilepsie (E). Voorkeur bij wens tot vermindering inflammatie/delier (D).
Ervaring
Met een aantal medicamenten is in de huidige praktijk ervaring opgedaan. Zo heeft de Nederlandse Vereniging van Spoedeisende Hulp Artsen een handreiking geschreven voor de behandeling van acute gedragsstoornissen op de SEH. De aanbevolen middelen zijn kalmerend en sederend en niet specifiek toegespitst op patiënten met hersenletsel. De beschreven middelen uit de handreiking zijn benzodiazepine-agonisten, dopaminereceptorantagonisten en NMDA-receptor blokker ketamine. Zoals hierboven beschreven is voorzichtigheid geboden bij voorschrift van benzodiazepines en dopaminereceptorantagonisten en worden deze bij voorkeur kortdurend en in de acute fase voorgeschreven. Ketamine is een de NMDA-receptorantagonist met sederende en analgetische werking en wordt in de praktijk regelmatig toegepast bij patiënten met hersenletsel. Een van de indicaties is sedatie. Zanza (2022) beschrijven in hun review dat het veilig is in gebruik bij ernstig traumatisch letsel. Dieronderzoek toonde echter dat een metaboliet van ketamine direct agressief gedrag stimuleert (Ye, 2019). Er is onvoldoende bekend over het effect van ketamine op neurologisch herstel.
De ervaring van de werkgroepleden op de intensive care is dat met het sederen van de patiënten, ook de agitatie en agressie vermindert en dat tijdens het herstel de agitatie ook afneemt. Haloperidol wordt veelvuldig en in hoge doseringen toegepast. Het is van belang om te beoordelen of er bij patiënten op de IC sprake is van hersenletsel en bij deze patiënten in principe geen antipsychotica in te zetten, maar alleen kortdurend en intermitterend. De werkgroep is van mening dat er -na meer generieke inzet van sedatie- in tweede instantie gekozen dient te worden voor gerichte medicatie tegen agitatie of agressie zonder schadelijke bijeffecten voor neurologisch herstel. Een middel dat onderzocht is bij patiënten met hersenletsel op de IC en effectief bleek is de selectieve α2-receptoragonist dexmedetomidine.
Er is voor het schrijven van deze module daarnaast navraag gedaan bij verschillende GGZ instellingen met als specialisatie neuropsychiatrie. Veelal worden binnen deze instellingen patiënten in latere fasen na hersenletsel behandeld. Uit de navraag komt naar voren dat bij agressie regelmatig atypische antipsychotica worden voorgeschreven. Zoals hierboven genoemd moeten positieve en negatieve effecten van deze groep geneesmiddelen worden afgewogen en heeft het de voorkeur om antipsychotica voor te schrijven met een lage affiniteit voor de D2 receptor, zoals bijvoorbeeld quetiapine. Bij prikkelgevoeligheid wordt in de huidige praktijk valproinezuur (cave teratogeniteit) of sertraline toegepast. De ervaring is dat patiënten het gebruik van valproïnezuur als positief ervaren en dat dit de therapietrouw ten goede komt. Aanvullend zijn er positieve ervaringen met het gebruik van mirtazapine vanwege het histaminerge effect en daarmee een positief effect op slaap. Inzet van benzodiazepine-agonisten bij hyperexcitatie wordt afgeraden vanwege de kans op verslaving. Bij cognitieve problemen en agitatie of agressie zijn amantadine (gericht op verbeteren aandacht), rivastigmine en memantine (gericht op verbeteren van het geheugen) middelen van eerste keus bij de voorschrijvers. Een overzicht van geprefereerde middelen, op basis van werkingsmechanisme, veiligheid en expert opinion is weergegeven in figuur 1.
Dosering
Start low, go slow: begin met een lage dosering en verhoog deze langzaam op geleide van klachten.
Evaluatie effecten en bijwerkingen met objectieve schaal.
Evalueer effect en bijwerkingen nauwlettend met een objectieve schaal. Voor inprentingsstoornissen in het kader van PTA is een schaal beschreven door Ponsford (2023) en voor agitatie en agressie door Williamson (2019). Stel zo nodig medicamenteuze beleid bij.
Concluderend
Op basis van beschikbare literatuur kan geen uitspraak worden gedaan over welk medicament het meest effectief is voor behandeling van agressie of agitatie bij patiënten met neuropsychiatrische gevolgen na NAH. Aandachtspunten bij medicatievoorschrift zijn inzet van niet-medicamenteuze behandeling, staken van agressieverhogende medicatie, inzet van middelen die de neurotransmitterbeschikbaarheid verlagen in de acute fase en inzet van middelen in de chronische fase die neurotransmitterbeschikbaarheid verhogen, negatieve effecten van medicatie bij patiënten met hersenletsel, de aanwezigheid van epilepsie of inflammatie, de route van beïnvloeding van het bedreigingssysteem, de startdosering en evaluatie van effecten.
Alle factoren afwegend zijn de volgende middelen in de acute fase geschikt: dexmedetomidine, propranolol, naltrexon en in de toekomst DORA. Kies in acute fase niet voor amantadine, methylfenidaat, sertraline, rivastigmine en carbamazepine omdat deze middelen de beschikbaarheid van neurotransmitters vergroten. Voorzichtigheid is geboden met haloperidol, quetiapine, olanzapine en risperidon vanwege negatieve effecten op neurologisch herstel (anticholinerge effecten, extrapiramidale verschijnselen en verminderen plasticiteit). Deze middelen dienen alleen kortdurend en intermitterend worden ingezet. Verder is voorzichtigheid geboden met benzodiazepine-agonisten vanwege het sederende effect, het risico op vallen en op verslaving. In de chronische fase zijn geprefereerde medicamenten: amantadine, methylfenidaat, sertraline, rivastigmine of naltrexon. Bij epilepsie heeft carbamazapine mogelijk een agressieverlagend effect, maar ook onwenselijke anticholinerge effecten. Kies in chronische fase niet voor haloperidol, quetiapine, olanzapine en risperidon, dexmedetomidine, propranolol of in de toekomst DORA.
In de praktijk is ervaring opgedaan met benzodiazepine-agonisten, dopamine-antagonisten, ketamine (acute fase), atypische antipsychotica, valproinezuur (cave teratogeniteit), sertraline, amantadine, rivastigmine en memantine (subacute en chronische fase). Aanvullend zijn er positieve ervaringen met het gebruik van mirtazapine vanwege het histaminerge effect en daarmee een positief effect op slaap.
De figuren onderaan de aanbevelingen vatten – op basis van werkingsmechanisme en expert opinion - de geprefereerde middelen per specifieke patiëntengroep samen. Interactie met andere middelen en eventuele comorbiditeit dient altijd goed te worden meegewogen in de medicamentkeuze.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Zie module niet-medicamenteuze behandeling van agitatie en agressie bij NAH.
Kosten (middelenbeslag)
Het is te veronderstellen dat het verminderen van agressie op klinische afdelingen leidt tot minder werkdruk bij zorgpersoneel en laat de literatuur bij naasten van patiënten aanwijzingen zien voor een verbeterd welzijn/vermindering van burn-out klachten na interventie. Omdat er geen aanbevelingen worden gedaan ten aanzien van gebruik van specifieke middelen, kan geen uitspraak worden gedaan ten aanzien van eventuele kosten. Wel kunnen aan de hand van de handreikingen in de richtlijn grofweg de effecten op de kosten van agressie worden afgewogen tegen de effecten van een langere duur van de fase van PTA of confusional state.
Aanvaardbaarheid, haalbaarheid en implementatie
Vanwege het gebrek aan evidence worden behandelaren in hun handelen beperkt en zijn zij vaak gedwongen om off-label interventies toe te passen. De handreikingen in deze richtlijn beogen het beslissingsproces te structureren. Uit de conclusie vanuit de literatuur dat er nauwelijks tot geen evidentie is voor een bepaalde interventie in de behandeling van agitatie en agressie na NAH mag niet geconcludeerd worden dat deze interventies niet werkzaam zouden kunnen zijn, want daarvoor ontbreekt ook de bewijskracht.
Ten aanzien van aanvaardbaarheid voor patiënten en naasten is het van belang om te zorgen voor scholing van naasten en voor beschikbaarheid van begrijpelijke informatie(folders) over de gevolgen van hersenletsel. Zie module niet-medicamenteuze behandeling van agitatie en agressie bij NAH voor aanvullende opmerkingen ten aanzien van aanvaardbaarheid, haalbaarheid en implementatie van zorg voor patiënten met een laag IQ, een taalbarrière, lage gezondheidsvaardigheden en patiënten in detentiecentra en voor barrières en facilitatoren van hantering van agressief gedrag door zorgpersoneel.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Er zijn vanuit de zoekstrategie vier studies naar voren gekomen die het effect van medicamenteuze behandelingen op agressie of agitatie hebben geëvalueerd bij neuropsychiatrische gevolgen na NAH. De bewijskracht voor de gerapporteerde uitkomstmaten (ernst van agressie en agitatie en bijwerkingen) komt voor alle drie de medicamenten uit op zeer laag. Op basis van beschikbare literatuur kan dus geen antwoord worden gegeven op de vraag wat de waarde is van medicamenteuze behandelingen voor agressie of agitatie bij patiënten met neuropsychiatrische gevolgen na NAH.
Het klinisch beeld van de patiënt met hersenletsel is uiteenlopend, waarbij deze module de hyperacute tot chronische fase beslaat, waarbij de patiënt zich in een kritische toestand tot een medisch stabiele toestand kan bevinden, neurologisch al dan niet verbeterend is en er comorbiditeit en persoonsfactoren een rol spelen. Omdat daarnaast heterogeniteit in voorschrijfgedrag een groot probleem is, is in deze richtlijn op basis van beschikbare literatuur een overzicht gegeven van pathofysiologische mechanismen van hersenletsel, het werkingsmechanisme van agressie en negatieve effecten van veelvoudig voorgeschreven medicamenten. Aan de hand hiervan zijn aandachtspunten gedestilleerd.
Aandachtspunten bij medicatievoorschrift zijn allereerst inzet van een niet-medicamenteuze behandeling; het staken agressieverhogende medicatie; inzet van middelen die de neurotransmitterbeschikbaarheid verlagen in de acute fase en inzet van middelen in de chronische fase die neurotransmitterbeschikbaarheid verhogen; aanwezigheid van potentieel negatieve effecten van medicatie op (herstel van) hersenletsel; de aanwezigheid van epilepsie of inflammatie; het aangrijpingspunt voor beïnvloeding van het bedreigingssysteem bij beschadigde hersenen; de dosering en evaluatie van effecten.
De werkgroep doet de aanbeveling om antipsychotica (dopamine-antagonisten) met hoge of matige D2 affiniteit zoals haloperidol, olanzapine en risperidon alleen in te zetten in de acute fase na hersenletsel en met name als “zo nodig” medicatie, gezien de te verwachten schadelijke effecten op neurologisch herstel. Dopamine-antagonisten in het algemeen zijn af te raden bij patiënten met NAH in de chronische fase gezien de lage dopaminespiegels in de hersenen en de rol van dopamine bij neuroplasticiteit/leren.
Middelen met effect op de balans tussen excitatie en inhibitie van neurale netwerken, zoals middelen die de GABA/glutamaatbalans veranderen (bijvoorbeeld benzodiazepinen, anti-epileptica) kunnen een negatief effect hebben op leervermogen en geheugen. Daarnaast bestaat het risico op verslaving bij langdurig gebruik van benzodiazepines.
Acetylcholine speelt een belangrijke rol bij cognitieve functies. Bij patiënten met cognitieve problemen is voorzichtigheid is geboden met middelen die anticholinerge eigenschappen bezitten.
Sederende medicamenten zoals haloperidol en benzodiazepines kunnen bij patiënten met motorische problemen leiden tot toename van valincidenten, ook bestaat er bij benzodiazepine-agonisten het risico op verslaving.
Inzet van vrijheidsbeperkende maatregelen kan worden overwogen ter bescherming van patiënt of betrokkenen, wanneer de agressie schadelijk is voor patiënt en/of zorgverleners of het zorgproces in de acute fase ernstig hindert. De risico’s van inzet van fixatie in combinatie met sedatie moeten per patiënt in kaart gebracht worden en geminimaliseerd voordat men over gaat op dit type maatregelen.
De bewijskracht van de gevonden literatuur is te laag om tot een aanbeveling voor een specifiek medicament ter behandeling van agitatie en agressie te komen. Zie figuur 1. voor een overzicht van geprefereerde medicamenten per specifieke patiëntengroep op basis van expert opinion, werkingsmechanisme en beschikbare literatuur over veiligheid van gebruik bij patiënten met hersenletsel.
Onderbouwing
Agitatie en agressie komen voor bij 20-70% van de patiënten met niet-aangeboren hersenletsel. De uiteenlopende prevalentie zoals deze in de literatuur wordt beschreven komt voort uit de gebruikte definitie, de context en is afhankelijk van NAH specifieke kenmerken (Williamson, 2019; Hoover et al., 2020; Pouwels, 2019). Agitatie of agressie kan leiden tot gevaarlijke situaties voor patiënt en naasten, is belastend voor zorgverleners en kan interfereren met het ontvangen van de juiste zorg door patiënt en/of het behalen van behandeldoelen (Alderman, 2007). Vaak is er dringend behandeling nodig, onafhankelijk van de fase waarin dit voorkomt. Met name in de eerste drie maanden na hersenletsel kan er sprake zijn van veranderd of verlaagd bewustzijn met inprentingsstoornissen (vaak in het kader van een Post Traumatische Amnesie of confusional state, zie beneden), waardoor (sneller) geagiteerd gedrag kan ontstaan. In deze richtlijn worden de volgende definities van agitatie en agressie gehanteerd:
Agitatie:
“Agitation is characterized by an excess of behavior, including restlessness, aggression, disinhibition, and emotional lability. (Sandel, 1996 in Phyland, 2021). Agitation is thought to be most common during PTA, a transient period of recovery following emergence from coma characterized by confusion, disorientation, inattention, and impairment in the ability to store and retrieve new memories (Phyland, 2021).
Naast de term PTA wordt in de literatuur de term “confusional state” gebruikt.
Agressie:
Aggressive behavior is an overt act, involving the delivery of noxious stimuli to (but not necessarily aimed at) another organism, object, or self (Patel & Hope, 1992, p21ƒ2 in: Byrne, 2016)
Hoewel agitatie een voorbode kan zijn van agressief gedrag, hoeft dit niet het gevolg te zijn van een interactie met de omgeving. Bij agressie is er wel sprake van interactie met de omgeving. De in de literatuur gebruikte meetinstrumenten maken niet altijd duidelijk onderscheid tussen agitatie en agressie (Volicer, 2017).
Een belangrijk knelpunt in de huidige praktijk bij inzet van medicamenteuze interventies bij agressie en agitatie is de grote heterogeniteit in voorschrijfgedrag door artsen. De werkgroep is van mening dat beperkte kennis over effectiviteit, bijwerkingen of paradoxaal effect van vaak off label beschikbare medicatie hieraan ten grondslag ligt. In de literatuur worden verschillende definities en uitkomstmaten gebruikt, wat het vergelijken van studies lastig maakt.
Deze module beschrijft de medicamenteuze mogelijkheden voor het behandelen van agitatie en agressie voor patiënten met neuropsychiatrische gevolgen na NAH.
Severity of agitation and aggression
|
Very low GRADE |
The evidence is very uncertain about the effect of sertraline 50mg/day on severity of agitation and aggression when compared with placebo in adult patients with agitation/aggression as neuropsychiatric sequelae of aquired brain injury.
Source: Baños , 2010 |
|
Very low GRADE |
The evidence is very uncertain about the effect of amantadine 200mg/day on severity of agitation and aggression when compared with placebo in adult patients with agitation/aggression as neuropsychiatric sequelae of acquired brain injury.
Sources: Hammond, 2014; Hammond, 2015 |
|
Very low GRADE |
The evidence is very uncertain about the effect of methylphenidate 30mg/day on severity of agitation and aggression when compared with placebo in adult patients with agitation/aggression as neuropsychiatric sequelae of acquired brain injury.
Sources: Fleminger, 2006; Mooney, 1993 |
Side effects
|
Very low GRADE |
The evidence is very uncertain about the effect of amantadine 200mg/day on side effects when compared with placebo in adult patients with agitation/aggression as neuropsychiatric sequelae of acquired brain injury.
Sources: Hammond, 2014; Hammond, 2015 |
Description of studies
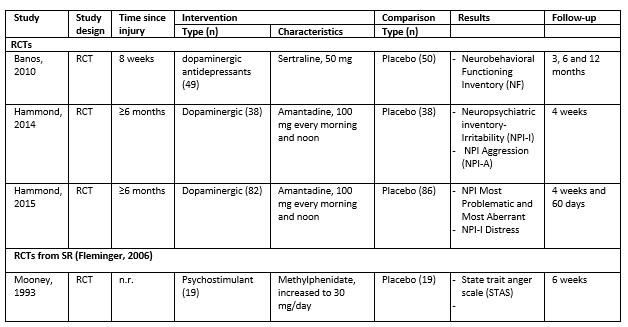
Baňos (2010) conducted a randomized controlled trial (RCT) investigating the efficacy of Sertraline 50mg/day compared to placebo in managing cognitive and behavioral symptoms in 99 hospital inpatients (of whom 49 in the intervention group) with acquired brain injury, all within <8 weeks post-injury. Patients were staying at a level 1 trauma center. The treatment was initiated prophylactically, without specific indication for agitation or aggression. Patients were assessed using the Neurobehavioral Functioning Inventory, including its aggression sub-scale, at three, six-, and twelve-months post-treatment initiation. The NFI is a 5-point Likert scale designed to collect information on behaviors and symptoms commonly associated with traumatic brain injury (TBI).
The RCT Hammond (2014) was conducted in a rehabilitation center. The study investigated the effect of Amantadine 100mg, twice daily versus placebo on irritability in 76 patients (38 in the intervention group, 38 in the control group), all ≥6 months post-brain injury. Patients were treated for 28 days. Aggression and agitation were assessed in both groups via subdomains agitation/aggression (NPI-A) and irritability/lability (NPI-I) of the Neuropsychiatric Inventory. This scale was developed to assess for common behaviors associated with dementia via a structured interview of the caregiver. However, it had been used in TBI populations before. Patients were included only if they scored >2 on the NPI-I before starting treatment with Amantadine or placebo, but there was no requirement for baseline NPI-A scores, meaning there had to be an indication for irritability, not aggression. Furthermore, the study analyzed whether the occurrence of certain side effects was related to either treatment group.
The RCT by Hammond (2015) was a multicenter replication of Hammond (2014) and took place in seven rehabilitation centers. The study examined the effect of twice daily 100 mg Amantadine versus placebo on irritability in 168 patients (82 in the intervention group, 86 in the control group), all ≥6 months post-brain injury. Patients were treated and followed for 60 days. Irritability was measured using the NPI-I, with both the observer and the patient recording this score. The "most problematic" and "most aberrant" scores were determined by multiplying the height of the score by the frequency. The same applied to the NPI-I for emotional resilience. Patients were included only if they scored >5 on the "NPI-I most problematic" before starting treatment with Amantadine or placebo. The study also reported common side effects.
Fleminger (2006) conducted a Cochrane systematic review that included studies examining pharmacological interventions for aggression and agitation in patients with acquired brain injury, and included six RCTs, of which only the study by Mooney (1993) met the selection criteria of this search. Mooney (1993) described a comparison between Methylphenidate 30mg/day and placebo in 38 patients (19 patients per treatment arm) over six weeks regarding various levels of anger, using the State Trait Anger Scale (STAS). The STAS is a precursor of the State trait anger expression inventory (STAXI). The State and Trait Anger subtests of the STAS each have 10 items rated on a four-point scale. Presence of anger or agitation was not a selection criterium for inclusion of subjects.
Results
When not reported in study, the mean difference was calculated based on difference in post-intervention measurements between intervention and control or when not available, based on mean change-from-baseline.
1. Severity of agitation and aggression (crucial)
1.1 Amantadine vs. placebo
In Hammond (2014), presence of anger was not a selection criterium, but for the comparison of amantadine (100mg twice daily) versus placebo, they demonstrated that at 28 days, there was no difference in change in aggression between the amantadine and placebo group. When only selecting patients with a baseline aggression (NPI-A score >2, n = 71, sample size per treatment-arm not reported), there was a bigger decrease in aggression in the amantadine group compared to the control group (amantadine: mean change-from-baseline -4.7 NPI-A; placebo: mean change-from-baseline -2.5 NPI-A.) When assessing all 99 patients (who all had a baseline NPI-I of 2 or higher), both groups showed a reduction of irritability (amantadine: mean change-from-baseline -4.3 NPI-I and placebo: mean change-from-baseline -2.6 NPI-I). Standard deviations and confidence intervals were not reported, so no mean differences could be calculated, and no statements could be made about the clinical relevance of the results found for this study.
The multicenter study by Hammond (2015) examined whether these effects could be replicated and/or were also found in the longer term in 168 patients. This study found no clinically relevant effects for NPI-I Most problematic (agitation) scored by the observer, with at 28 days a mean difference of -0.11 in favor of amantadine (95% CI -1.13 to 0.91), and at 60 days a mean difference of -0.88 (95% CI -1.87 to 0.11). For the observer-scored NPI-I Distress, also no clinically relevant difference was found at 28 days (MD: -0.35, 95% CI -0.77 to 0.07) or 60 days (MD: -0.29, 95% CI -0.70 to 0.12).
For the self-reported scales, at 28 days, no clinically relevant difference was found for either NPI-I Most Problematic (MD -0.69, 95% CI -1.82 to 0.44) or self-reported NPI-I Distress (MD -0.35 95% CI -0.84 to 0.14). However, at 60 days, a small effect was found for NPI-I Distress in favor of amantadine, with a mean difference of -0.52 (95% CI -0.98 to -0.06). This was not a clinically relevant difference. Finally, for self-reported NPI-I most problematic, a clinically relevant difference was found at 60 days, with a mean difference of -1.18 in favor of the amantadine group (95% CI -2.21 to -0.15).
1.2 Sertraline vs. placebo
For the comparison of sertraline 50mg/day versus placebo, Baňos (2010) demonstrated in 99 patients that after six and twelve months, there was a small difference in aggression as measured by the Neurobehavioral Functioning Inventory (aggression item) between the intervention and control group, with a mean difference of -2.2 (95% CI -8.98 to 4.58). This was not a clinically relevant difference.
1.3 Methylphenidate vs. placebo
For the comparison of methylphenidate 30mg/day versus placebo, Mooney (1993) demonstrated in 38 patients that at a follow-up of six weeks, both sub-domains of the STAS Anger trait (MD: -5.0, 95% CI -6.1 to -3.9) and Anger State (MD: -2.0, 95% CI -3.0 to -1.0) were lower in the methylphenidate group than the placebo group. Both are clinically relevant differences.
2. Side effects (important)
2.1 Amantadine vs. placebo
Side effects of different pharmacological interventions were described in both studies by Hammond (2014, 2015), where amantadine was compared to placebo. Hammond (2014) observed 19 out of 38 patients (50%) with any side effect in the amantadine group, and 17 out of 38 patients (45%) with any side effect in the placebo group. For Hammond (2015), no data were provided. In Hammond (2014), one patient required drug termination due to a seizure.
Level of evidence of the literature
1. Severity of agitation and aggression (crucial)
The level of evidence regarding the severity of agitation and aggression started at high because it was based on RCTs. The final level of evidence for this outcome is described separately for each pharmacological intervention below.
1.1 Amantadine versus placebo
The level of evidence when comparing amantadine and placebo was in total downgraded by three levels due to different indication (prophylactic use for aggression/agitation, -1, indirectness), statistical heterogeneity (-1, inconsistency) and crossing the borders of clinical relevance (-1, imprecision). The final level of evidence is very low.
1.2 Sertraline versus placebo
The level of evidence when comparing sertraline with placebo was downgraded by four levels, due to study limitations, including attrition bias (-1, risk of bias), different indication (prophylactic use, -1, indirectness) and number of included patients and crossing the borders of clinical relevance (-2, imprecision). The final level of evidence is very low.
1.3 Methylphenidate versus placebo
The level of evidence when comparing methylphenidate with placebo was in total downgraded by four levels, due to study limitations, including (risk of) selection bias, residual confounding, detection bias, and attrition bias (-2, risk of bias), different indication (prophylactic use, -1, indirectness) and number of included patients (-1, imprecision). The final level of evidence is very low.
2. Side effects (important)
1.1 Amantadine versus placebo
The level of evidence regarding side effects started at high because it was based solely based on RCTs. It was in total downgraded by three levels because of study limitations, including (risk of) selection bias and residual confounding (-2, risk of bias) and number of included patients (-1, imprecision). The final level of evidence is very low.
For the other comparisons of pharmacological interventions, the outcome side effects could not be graded due to lack of evidence.
A systematic review of the literature was performed to answer the following question: What are the effects of pharmacological interventions on severity of agitation and aggression and side effects among patients with neuropsychiatric sequelae of acquired brain injury?
| P: |
Adult patients with agitation/aggression as neuropsychiatric sequelae of acquired brain injury |
| I: | Pharmacological interventions: antipsychotic medication, anticonvulsants, dopaminergic antidepressants, beta-blockers, benzodiazepines |
| C: | No treatment, placebo or comparison between interventions mentioned under ‘I’ |
| O: | Severity of agitation and aggression, side effects |
Relevant outcome measures
The guideline development group considered severity of agitation and aggression as a crucial outcome measure for decision making; and side effects as an important outcome measure for decision making.
Severity of agitation and aggression can be assessed using different validated scales.
The minimum clinically important differences as defined by the working group are reported in table 1, based on expert opinion.
Table 1. Minimum clinically important differences for severity of aggression and agitation
|
Instrument |
Definition |
Minimum clinically important difference |
|
Agitated Behavior Scale (ABS) |
The ABS measures the level of agitation in patient after TBI, with a total score range of 14 to 56. Scores between 14–21 indicate normal behavior, 22–28 indicate mild agitation, 29–35 indicate moderate agitation, and 36–56 indicate severe agitation. |
7.0 points change on the scale |
|
State trait anger expression inventory (STAXI) |
The STAXI measures the intensity of anger as an emotional state (State Anger) and the disposition to experience angry feelings as a personality trait (Trait Anger), along with the expression and control of anger. Each subscale (State Anger, Trait Anger, Anger Expression-Out, Anger Expression-In, Anger Control-Out, and Anger Control-In) typically has a score range from 10 to 40, with higher scores indicating greater anger or less effective anger control. |
2.0 points change per subscale |
|
Other (self-)report scales |
|
1.0 standard deviation change on scale |
Search and select (Methods)
The previous guideline module (from 2017) on this topic has been revised, in which the evidence and literature previously assessed has been reassessed for the (re)formulated PICO, to be supplemented with more recent literature. The process of the search and selection of the more recent literature is described below.
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from January 1st, 2016, until November 9th, 2023. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 595 hits. Studies were selected based on the following criteria:
- Randomized controlled trials, systematic review and/or meta-analysis.
- Included adults with agitation/aggression as neuropsychiatric sequelae of acquired brain injury.
- Described pharmacological interventions, including antipsychotic medication, anticonvulsants, dopaminergic antidepressants, beta-blockers, benzodiazepines.
- Described either no treatment, placebo, or care as usual as a comparison.
- Described at least one of the outcome measures as described in the PICO.
- Included at least 20 subjects.
- Full text publication in Dutch or English available.
From this search, 19 studies were initially selected based on title and abstract screening. After reading the full text, all 19 studies were excluded (see the table with reasons for exclusion under the tab Methods).
The four studies included from the previous guideline module search were reassessed and described below, as no new literature was included. These included three RCTs and one Cochrane systematic review (Fleminger, 2006), and were eventually selected based on screening 426 hits of a similar search in March 2015. The studies included in the systematic review by Fleminger were also reassessed, which resulted in five of the six previously included studies to now be excluded. Thus, additionally to the other three RCTs, only one RCT included in the systematic review by Fleminger (2006) was included in the analysis of literature.
Results
Four studies were included in the analysis of the literature, including one systematic review (with one eligible RCT) and three RCTs. Different types of pharmacological interventions were assessed in the included studies. Table 2 shows the different interventions and corresponding results per included study. The assessment of the risk of bias is summarized in the risk of bias table.
Table 2. Study characteristics
- Alderman N, Wood RL. Neurobehavioral approaches to the rehabilitation of challenging behavior. NeuroRehabilitation. 2013;32:761-770.
- Algemene Rekenkamer (2016), Aanpak van laaggeletterdheid. Den Haag: Algemene Rekenkamer.
- Antonoudiou P, Colmers PLW, Walton NL, et al. Allopregnanolone mediates affective switching through modulation of oscillatory states in the basolateral amygdala. Biol Psychiatry. 2022;91(3):283–293. doi:10.1016/j.biopsych.2021.07.017.
- Balan I, Beattie MC, O’Buckley TK, Aurelian L, Morrow AL. Endogenous neurosteroid (3α,5α)3-hydroxypregnan-20-one inhibits toll-like-4 receptor activation and pro-inflammatory signaling in macrophages and brain. Sci Rep. 2019;9:14.
- Bales, James & Wagner, Amy & Kline, Anthony & Dixon, C. Edward. (2009). Bales JW, Wagner AK, Kline AE, Dixon CE. Persistent cognitive dysfunction after traumatic brain injury: A dopamine hypothesis. Neurosci Biobehav Rev 33:981-1003. Neuroscience and biobehavioral reviews. 33. 981-1003. 10.1016/j.neubiorev.2009.03.011.
- Baños JH, Novack TA, Brunner R, Impact of early administration of sertraline on cognitive and behavioral recovery in the first year after moderate to severe traumatic brain injury. J Head Trauma Rehabil. 2010;25(5):357-61.
- Belelli, D., Lambert, J. Neurosteroids: endogenous regulators of the GABAA receptor. Nat Rev Neuroscience 6, 565–575 (2005). https://doi.org/10.1038/nrn1703.
- Bell, A.; Hewins, B.; Bishop, C.; Fortin, A.; Wang, J.; Creamer, J.L.; Collen, J.; Werner, J.K., Jr. Traumatic Brain Injury, Sleep, and Melatonin— Intrinsic Changes with Therapeutic Potential. Clocks&Sleep 2023, 5, 177-03. https://doi.org/ 10.3390/clockssleep5020016.
- Berrol S. Risks of restraints in head injury. Arch Phys Med Rehabil. 1988 Jul;69(7):537-8. PMID: 3389996.
- Bertsch K, Florange J, Herpertz SC. Understanding Brain Mechanisms of Reactive Aggression. Curr Psychiatry Rep. 2020 Nov 12;22(12):81. doi: 10.1007/s11920-020-01208-6. PMID: 33180230; PMCID: PMC7661405.
- Blair RJR. Considering anger from a cognitive neuroscience perspective. Wiley Interdiscip Rev Cogn Sci. 2012 Jan;3(1):65-74. doi: 10.1002/wcs.154. Epub 2011 Oct 19. PMID: 22267973; PMCID: PMC3260787.
- Block H, Bellon M, Hunter SC, George S. Barriers and enablers to managing challenging behaviours after traumatic brain injury in the acute hospital setting: a qualitative study. BMC Health Serv Res. 2023 Nov 16;23(1):1266. doi: 10.1186/s12913-023-10279-z. PMID: 37974214; PMCID: PMC10655469.
- Block H, Paul M, Muir-Cochrane E, Bellon M, George S, Hunter SC. Clinical practice guideline recommendations for the management of challenging behaviours after traumatic brain injury in acute hospital and inpatient rehabilitation settings: a systematic review. Disabil Rehabil. 2024 Feb;46(3):453-463. doi: 10.1080/09638288.2023.2169769. Epub 2023 Jan 24. PMID: 36694351.
- Boero G, Porcu P, Morrow AL. Pleiotropic actions of allopregnanolone underlie therapeutic benefits in stress-related disease. Neurobiol Stress. 2019 Nov 27;12:100203. doi: 10.1016/j.ynstr.2019.100203. PMID: 31879693; PMCID: PMC6920111.
- Byrne C, Coetzer R. The effectiveness of psychological interventions for aggressive behavior following acquired brain injury: A meta-analysis and systematic review. NeuroRehabilitation. 2016 Jun 30;39(2):205-21. doi: 10.3233/NRE-161352. PMID: 27372357.
- Carneiro P, Ferreira M, Marisa Costa V, Carvalho F, Capela JP. Protective effects of amphetamine and methylphenidate against dopaminergic neurotoxicants in SH-SY5Y cells. Curr Res Toxicol. 2024 Mar 20;6:100165. doi: 10.1016/j.crtox.2024.100165. PMID: 38562456; PMCID: PMC10982568.
- Carrier SL, Hicks AJ, Ponsford J, McKay A. Managing agitation during early recovery in adults with traumatic brain injury: An international survey. Ann Phys Rehabil Med. 2021 Sep;64(5):101532. doi: 10.1016/j.rehab.2021.101532. Epub 2021 Jul 16. PMID: 33933690.
- Cataford G, Monton LA, Karzon S, Livernoche-Leduc C, Saavedra-Mitjans M, Potvin MJ, Bernard F, Burry L, Arbour C, Williamson DR. Cognitive and Motor Function Effects of Antipsychotics in Traumatic Brain Injury: A Systematic Review of Pre-Clinical Studies. Neurotrauma Rep. 2024 Mar 5;5(1):181-193. doi: 10.1089/neur.2023.0108. PMID: 38463417; PMCID: PMC10924062.
- Centraal Bureau voor de Statistiek, Den Haag/Heerlen 3-10-2018.
- Chan V, Estrella MJ, Hanafy S, Colclough Z, Joyce JM, Babineau J, Colantonio A. Equity considerations in clinical practice guidelines for traumatic brain injury and homelessness: a systematic review. EClinicalMedicine. 2023 Aug 24;63:102152. doi: 10.1016/j.eclinm.2023.102152. PMID: 37662521; PMCID: PMC10474365.
- Cheng JP, Leary JB, O'Neil DA, Meyer EA, Free KE, Bondi CO, Kline AE. Spontaneous recovery of traumatic brain injury-induced functional deficits is not hindered by daily administration of lorazepam. Behav Brain Res. 2018 Feb 26;339:215-221. doi: 10.1016/j.bbr.2017.11.039. Epub 2017 Dec 2. PMID: 29203336; PMCID: PMC5734665.
- Choi DC, Furay AR, Evanson NK, Ostrander MM, Ulrich-Lai YM, Herman JP. Bed nucleus of the stria terminalis subregions differentially regulate hypothalamic-pituitary-adrenal axis activity: implications for the integration of limbic inputs. J Neurosci. 2007 Feb 21;27(8):2025-34. doi: 10.1523/JNEUROSCI.4301-06.2007. PMID: 17314298; PMCID: PMC6673539.
- Crowley NA, Kash TL. Kappa opioid receptor signaling in the brain: Circuitry and implications for treatment. Prog Neuropsychopharmacol Biol Psychiatry. 2015 Oct 1;62:51-60. doi: 10.1016/j.pnpbp.2015.01.001. Epub 2015 Jan 12. PMID: 25592680; PMCID: PMC4465498.
- Fagan,H.A. Huneke N.T.M, Domschke, K., Baldwin David S., The role of the orexin system in the neurobiology of anxiety disorders: Potential for a novel treatment target, Neuroscience Applied, Volume 3, 2024.
- Flanigan, M.E., Aleyasin, H., Li, L. et al. Orexin signaling in GABAergic lateral habenula neurons modulates aggressive behavior in male mice. Nat Neurosci 23, 638–650 (2020). https://doi.org/10.1038/s41593-020-0617-7.
- Fleminger S, Greenwood RJ, Oliver DL. Pharmacological management for agitation and aggression in people with acquired brain injury. The Cochrane Library. 2006;(4):CD003299.
- Florentino, S. A., Bawany, M. H., & Ma, H. M. (2022). Acetylcholinesterase inhibitors to enhance recovery from traumatic brain injury: a comprehensive review and case series. Brain Injury, 36(4), 441–454. https://doi.org/10.1080/02699052.2022.2034962.
- Frye CA. Neurosteroids' effects and mechanisms for social, cognitive, emotional, and physical functions. Psychoneuroendocrinology. 2009 Dec;34 Suppl 1(Suppl 1):S143-61. doi: 10.1016/j.psyneuen.2009.07.005. PMID: 19656632; PMCID: PMC2898141.
- Godoy, D.A., Badenes, R., Pelosi, P. et al. Ketamine in acute phase of severe traumatic brain injury “an old drug for new uses?”. Crit Care 25, 19 (2021). https://doi.org/10.1186/s13054-020-03452-x.
- Guerriero RM, Giza CC, Rotenberg A. Glutamate and GABA imbalance following traumatic brain injury. Curr Neurol Neurosci Rep. 2015 May;15(5):27. doi: 10.1007/s11910-015-0545-1. PMID: 25796572; PMCID: PMC4640931.
- Hammond FM, Bickett AK, Norton JH, Effectiveness of amantadine hydrochloride in the reduction of chronic traumatic brain injury irritability and aggression. The Journal of head trauma rehabilitation. 2014;29(5):391-9. doi: 10.1097/01.HTR.0000438116.56228.de.
- Hammond FM, Sherer M, Malec JF, Amantadine Effect on Perceptions of Irritability after Traumatic Brain Injury: Results of the Amantadine Irritability Multisite Study. J Neurotrauma. 2015;32(16):1230-8. PubMed PMID: 25774566.
- Hammond FM, Zafonte RD, Tang Q, Jang JH. Carbamazepine for Irritability and Aggression after Traumatic Brain Injury: A Randomized, Placebo-Controlled Study. J Neurotrauma. 2021 Aug 15;38(16):2238-2246. doi: 10.1089/neu.2020.7530. Epub 2021 Mar 9. PMID: 33563104.
- Hicks AJ, Clay FJ, Hopwood M, James AC, Jayaram M, Perry LA, Batty R, Ponsford JL. The Efficacy and Harms of Pharmacological Interventions for Aggression After Traumatic Brain Injury-Systematic Review. Front Neurol. 2019 Nov 29;10:1169. doi: 10.3389/fneur.2019.01169. PMID: 31849802; PMCID: PMC6895752.
- Hoover GL, Whitehair VC. Agitation after traumatic brain injury: a review of current and future concepts in diagnosis and management. Neurol Res. 2023 Oct;45(10):884-892. doi: 10.1080/01616412.2020.1797374. Epub 2020 Jul 24. PMID: 32706643.
- Hsieh TH, Lee HHC, Hameed MQ, Pascual-Leone A, Hensch TK, Rotenberg A. Trajectory of Parvalbumin Cell Impairment and Loss of Cortical Inhibition in Traumatic Brain Injury. Cereb Cortex. 2017 Dec 1;27(12):5509-5524. doi: 10.1093/cercor/bhw318. PMID: 27909008; PMCID: PMC6075565.
- Klumpers, F., Kroes, M.C.W., Baas, J. & Fernandez, G. How human amygdala and bed nucleus of the stria terminalis may drive distinct defensive responses. J Neurosci 37, 9645–9656 (2017).
- Laganà, A.S., Triolo, O., D’Amico, V. et al. Management of women with epilepsy: from preconception to post-partum. Arch Gynecol Obstet 293, 493–503 (2016). https://doi.org/10.1007/s00404-015-3968-7.
- Li W, Yang P, Ngetich RK, Zhang J, Jin Z, Li L. Differential involvement of frontoparietal network and insula cortex in emotion regulation. Neuropsychologia. 2021 Oct 15;161:107991. doi: 10.1016/j.neuropsychologia.2021.107991. Epub 2021 Aug 12. PMID: 34391808.
- Lischinsky JE, Lin D. Neural mechanisms of aggression across species. Nat Neurosci. 2020 Nov;23(11):1317-1328. doi: 10.1038/s41593-020-00715-2. Epub 2020 Oct 12. PMID: 33046890.
- Lebow, M., Chen, A. Overshadowed by the amygdala: the bed nucleus of the stria terminalis emerges as key to psychiatric disorders. Mol Psychiatry 21, 450–463 (2016). https://doi.org/10.1038/mp.2016.1.
- Ma HM, Zafonte RD. Amantadine and memantine: a comprehensive review for acquired brain injury. Brain Inj. 2020 Feb 23;34(3):299-315. doi: 10.1080/02699052.2020.1723697. Epub 2020 Feb 20. PMID: 32078407.
- McGuire, J. L., Ngwenya, L. B., & McCullumsmith, R. E. (2018). Neurotransmitter changes after traumatic brain injury: an update for new treatment strategies. Molecular Psychiatry. doi:10.1038/s41380-018-0239-6.
- Menon, V., D’Esposito, M. The role of PFC networks in cognitive control and executive function. Neuropsychopharmacol. 47, 90–103 (2022). https://doi.org/10.1038/s41386-021-01152-w.
- Mooney GF, Haas LJ. Effect of methylphenidate on brain injury-related anger. Arch Phys Med Rehabil. 1993 Feb;74(2):153-60. PMID: 8431099.
- Munley KM, Han Y, Lansing MX, Demas GE. Winter madness: Melatonin as a neuroendocrine regulator of seasonal aggression. J Exp Zool A Ecol Integr Physiol. 2022 Dec;337(9-10):873-889. doi: 10.1002/jez.2601. Epub 2022 Apr 22. PMID: 35451566; PMCID: PMC9587138.
- Murugan S, Jakka P, Namani S, Mujumdar V, Radhakrishnan G. The neurosteroid pregnenolone promotes degradation of key proteins in the innate immune signaling to suppress inflammation. J Biol Chem. 2019;294(12):4596–4607. doi:10.1074/jbc.RA118.005543 15.
- Neren D, Johnson MD, Legon W, Bachour SP, Ling G, Divani AA. Vagus Nerve Stimulation and Other Neuromodulation Methods for Treatment of Traumatic Brain Injury. Neurocrit Care. 2016 Apr;24(2):308-19. doi: 10.1007/s12028-015-0203-0. PMID: 26399249.
- Pappadis M.R, Sander A., Juengst S.B., Novelo, L.L., Ngan, E., Bell K.R., Corrigan, J.D., Driver, S., Dreer, L.E., Lequerica, A.H.. The Relationship of Health Literacy to Health Outcomes Among Individuals With Traumatic Brain Injury: A Traumatic Brain Injury Model Systems Study. Journal of Head Trauma Rehabilitation 39(2):p 103-114, March-April 2024. | DOI: 10.1097/HTR.0000000000000912.
- Paribello P, Manchia M, Bosia M, Pinna F, Carpiniello B, Comai S. Melatonin and aggressive behavior: A systematic review of the literature on preclinical and clinical evidence. J Pineal Res. 2022 May;72(4):e12794. doi: 10.1111/jpi.12794. Epub 2022 Mar 10. PMID: 35192237; PMCID: PMC9285357.
- Phyland RK, McKay A, Olver J, Walterfang M, Hopwood M, Ponsford M, Ponsford JL. Use of Olanzapine to Treat Agitation in Traumatic Brain Injury: A Series of N-of-One Trials. J Neurotrauma. 2023 Jan;40(1-2):33-51. doi: 10.1089/neu.2022.0139. Epub 2022 Aug 22. PMID: 35833454.
- Phyland RK, Ponsford JL, Carrier SL, Hicks AJ, McKay A. Agitated Behaviors following Traumatic Brain Injury: A Systematic Review and Meta-Analysis of Prevalence by Post-Traumatic Amnesia Status, Hospital Setting, and Agitated Behavior Type. J Neurotrauma. 2021 Nov 15;38(22):3047-3067. doi: 10.1089/neu.2021.0257. PMID: 34435884.
- Ponsford J, Trevena-Peters J, Janzen S, Harnett A, Marshall S, Patsakos E, Kua A, McIntyre A, Teasell R, Wiseman-Hakes C, Velikonja D, Bayley MT, McKay A; INCOG Expert Panel. INCOG 2.0 Guidelines for Cognitive Rehabilitation Following Traumatic Brain Injury, Part I: Posttraumatic Amnesia. J Head Trauma Rehabil. 2023 Jan-Feb 01;38(1):24-37. doi: 10.1097/HTR.0000000000000840. PMID: 36594857.
- Pouwels CGJG, Wolters Grégorio G, Spauwen PJJ, Bus BAA, Winkens I, Ponds RWHM. Prevalentie en uitingsvormen van agressie bij volwassen patiënten met niet-aangeboren hersenletsel: een literatuuroverzicht [Prevalence and manifestations of aggression in adult patients with acquired brain injury: a review]. Tijdschr Psychiatr. 2019;61(12):862-878. Dutch. PMID: 31907901.
- Race NS, Moschonas EH, Cheng JP, Bondi CO, Kline AE. Antipsychotic Drugs: The Antithesis to Neurorehabilitation in Models of Pre-Clinical Traumatic Brain Injury. Neurotrauma Rep. 2023 Oct 31;4(1):724-735. doi: 10.1089/neur.2023.0082. PMID: 37928134; PMCID: PMC10621671.
- Rahmani E, Lemelle TM, Samarbafzadeh E, Kablinger AS. Pharmacological Treatment of Agitation and/or Aggression in Patients With Traumatic Brain Injury: A Systematic Review of Reviews. J Head Trauma Rehabil. 2021 Jul-Aug 01;36(4):E262-E283. doi: 10.1097/HTR.0000000000000656. PMID: 33656478.
- Rendon, Nikki & Boonstra, Rudy & Albers, H Elliott & Demas, Gregory. (2015). DHEA effects on brain and behavior: Insights from comparative studies of aggression. The Journal of Steroid Biochemistry and Molecular Biology. 261-272. 10.1016/j.jsbmb.2014.05.011.
- Russell, G., Lightman, S. The human stress response. Nat Rev Endocrinol 15, 525–534 (2019). https://doi.org/10.1038/s41574-019-0228-0.
- Schwartz JA, Portnoy J. Lower catecholamine activity is associated with greater levels of anger in adults. Int J Psychophysiol. 2017 Oct;120:33-41. doi: 10.1016/j.ijpsycho.2017.07.005. Epub 2017 Jul 12. PMID: 28711699.
- Sharp DJ, Scott G, Leech R. Network dysfunction after traumatic brain injury. Nat Rev Neurol. 2014 Mar;10(3):156-66. doi: 10.1038/nrneurol.2014.15. Epub 2014 Feb 11. PMID: 24514870.
- Sheibani M, Shayan M, Khalilzadeh M, Ghasemi M, Dehpour AR. Orexin receptor antagonists in the pathophysiology and treatment of sleep disorders and epilepsy. Neuropeptides. 2023 Jun;99:102335. doi: 10.1016/j.npep.2023.102335. Epub 2023 Mar 24. PMID: 37003137.
- Soltani F, Tabatabaei S, Jannatmakan F, Nasajian N, Amiri F, Darkhor R, Moravej M. Comparison of the Effects of Haloperidol and Dexmedetomidine on Delirium and Agitation in Patients with a Traumatic Brain Injury Admitted to the Intensive Care Unit. Anesth Pain Med. 2021 Jul 27;11(3):e113802. doi: 10.5812/aapm.113802. PMID: 34540634; PMCID: PMC8438711.
- Taylor KS, Seminowicz DA, Davis KD. Two systems of resting state connectivity between the insula and cingulate cortex. Hum Brain Mapp. 2009 Sep;30(9):2731-45. doi: 10.1002/hbm.20705. PMID: 19072897; PMCID: PMC6871122.
- Todd WD, Machado NL. A time to fight: Circadian control of aggression and associated autonomic support. Auton Neurosci. 2019 Mar;217:35-40. doi: 10.1016/j.autneu.2018.12.008. Epub 2018 Dec 23. PMID: 30704973; PMCID: PMC6372319.
- Valenta JP, Job MO, Mangieri RA, Schier CJ, Howard EC, Gonzales RA. μ-opioid receptors in the stimulation of mesolimbic dopamine activity by ethanol and morphine in Long-Evans rats: a delayed effect of ethanol. Psychopharmacology (Berl). 2013 Aug;228(3):389-400. doi: 10.1007/s00213-013-3041-9. Epub 2013 Mar 16. PMID: 23503684; PMCID: PMC3707954.
- Verduzco-Mendoza A, Carrillo-Mora P, Avila-Luna A, Gálvez-Rosas A, Olmos-Hernández A, Mota-Rojas D, Bueno-Nava A. Role of the Dopaminergic System in the Striatum and Its Association With Functional Recovery or Rehabilitation After Brain Injury. Front Neurosci. 2021 Jun 24;15:693404. doi: 10.3389/fnins.2021.693404. PMID: 34248494; PMCID: PMC8264205.
- Volicer L, Citrome L, Volavka J. Measurement of agitation and aggression in adult and aged neuropsychiatric patients: review of definitions and frequently used measurement scales. CNS Spectr. 2017 Oct;22(5):407-414. doi: 10.1017/S1092852917000050. Epub 2017 Feb 9. PMID: 2817904.
- Wang Z, Winans NJ, Zhao Z, Cosgrove ME, Gammel T, Saadon JR, Mani R, Ravi B, Fiore SM, Mikell CB and Mofakham S (2021) Agitation Following Severe Traumatic Brain Injury Is a Clinical Sign of Recovery of Consciousness. Front. Surg. 8:627008. doi: 10.3389/fsurg.2021.627008.
- Wardle, M. C., Bershad, A. K., & de Wit, H. (2016). Naltrexone alters the processing of social and emotional stimuli in healthy adults. Social Neuroscience, 11(6), 579–591. https://doi.org/10.1080/17470919.2015.1136355.
- Wei D, Talwar V, Lin D. Neural circuits of social behaviors: Innate yet flexible. Neuron. 2021 May 19;109(10):1600-1620. doi: 10.1016/j.neuron.2021.02.012. Epub 2021 Mar 10. PMID: 33705708; PMCID: PMC8141016.
- Williamson D, Frenette AJ, Burry LD, et al. Pharmacological interventions for agitated behaviours in patients with traumatic brain injury: a systematic review. BMJ Open 2019;9:e029604. doi:10.1136/ bmjopen-2019-029604.
- Willems, A. E. M., Heijmans, M., Brabers, A. E. M., Rademakers, J. Gezondheidsvaardigheden in Nederland: factsheet cijfers 2021. Utrecht, NIVEL, 2021.
- Yamaguchi T, Lin D. Functions of medial hypothalamic and mesolimbic dopamine circuitries in aggression. Curr Opin Behav Sci. 2018 Dec;24:104-112. doi: 10.1016/j.cobeha.2018.06.011. Epub 2018 Jul 3. PMID: 30746430; PMCID: PMC6368185.
- Ye L, Ko CY, Huang Y, Zheng C, Zheng Y, Chou D. Ketamine metabolite (2R,6R)-hydroxynorketamine enhances aggression via periaqueductal gray glutamatergic transmission. Neuropharmacology. 2019 Oct;157:107667. doi: 10.1016/j.neuropharm.2019.107667. Epub 2019 Jun 14. PMID: 31207251.
- Younger J, Parkitny L, McLain D. The use of low-dose naltrexone (LDN) as a novel anti-inflammatory treatment for chronic pain. Clin Rheumatol. 2014 Apr;33(4):451-9. doi: 10.1007/s10067-014-2517-2. Epub 2014 Feb 15. PMID: 24526250; PMCID: PMC3962576.
- Zanza C, Piccolella F, Racca F, Romenskaya T, Longhitano Y, Franceschi F, Savioli G, Bertozzi G, De Simone S, Cipolloni L, La Russa R. Ketamine in Acute Brain Injury: Current Opinion Following Cerebral Circulation and Electrical Activity. Healthcare (Basel). 2022 Mar 17;10(3):566. doi: 10.3390/healthcare10030566. PMID: 35327044; PMCID: PMC8949520.
- Zhu KW, Tao GJ, Huang ZL, Qu WM, Wang L. Whole-brain connectivity to the bed nucleus of the stria terminalis calretinin-expressing interneurons in male mice. Eur J Neurosci. 2023 Aug;58(3):2807-2823. doi: 10.1111/ejn.16068. Epub 2023 Jul 15. PMID: 37452644.
- https://www.farmacotherapeutischkompas.nl.
- https://www.horizonscangeneesmiddelen.nl/geneesmiddelen/brexanolone-neurologische-aandoeningen-depressie/versie2.
|
Study Reference |
Study Characteristics |
Patient Characteristics |
Intervention (I) |
Comparison / Control (C) |
Follow-up |
Outcome Measures and Effect Size |
Comments |
|
Baňos, 2010 |
Type of study: randomized controlled trial
Setting: inpatients
Country: USA
Source of funding: non-commercial |
Inclusion criteria: 1) moderate to severe TBI 2) age ≥16 years 3) recruitment within 8 weeks of injury
Exclusion criteria: 1) neurological problems predating the TBI 2) use of antidepressant medication 3) significant developmental or psychiatric disorders 4) alcohol or drug dependency in the year prior to the TBI 5) administration of antidepressant medication during acute care prior to enrollment
N total at baseline: I: 49 C: 50
Important prognostic factors: age ± SD: I: 35 ± 17, C: 35 ± 16 Sex: I: 79% M, C: 66% M
Groups comparable at baseline? Yes |
Sertraline 50 mg/day |
Placebo (dose frequency NR) |
Length of follow-up:
3, 6, and 12 months Loss-to-follow-up: After 3 months: I: 22 (45%) C: 19 (38%)
After 6 months: I: 27 (55%) C: 20 (40%)
After 12 months: I: 29 (59%) C: 20 (40%)
Incomplete outcome data: As above |
Neurobehavioral Functional Inventory Patient self-report Subscale: aggression
(mean ± SD) 3 months: I: 94 ± 13, C: 96 ± 13
6 months: I: 96 ± 13, C: 95 ± 14
12 months: I: 95 ± 16, C: 97 ± 14
For all p>0.05
Family self-report Subscale: aggression (mean ± SD) 3 months: I: 101 ± 17, C: 99 ± 13
6 months: I: 105 ± 16, C: 99 ± 10 12 months: I: 102 ± 18, C: 107 ± 20
For all p>0.05 |
Sertraline does not appear to prevent development of cognitive and behavioural problems following TBI. This does not negate evidence for treatment role of sertraline for emotional and neurobehavioural problems in TBI. Unclear whether family report was available for all participants, or if there was a difference in loss to follow-up between patient-report and family report. |
|
Hammond, 2014 |
Type of study: Parallel group randomized controlled trial
Setting: outpatients
Country: USA
Source of funding: non-commercial |
Inclusion criteria: 1) age 16-65 years 2) sustained a closed head injury due to trauma at least 6 months prior to enrolment with a score >2 on NPI-irritability domain 3) medical and neurological stability 4) able to give informed consent 5) able to comply with study protocol 6) negative pregnancy test 7) creatinine clearance >60 mg/dL 8) close friend or family member living with patient and able to observe presence of irritability
Exclusion criteria: 1) anticipated surgery or medication change during the study 2) diagnosis of other neurological disorder 3) seizure in the months prior to enrolment 4) concomitant use of neuroleptic agents or monoamine oxidase inhibitors 5) previous allergy or adverse reaction to amantadine ingestion 6) ingestion of amantadine in the month prior to study enrollment
N total at baseline: I: 38 C: 38
Important prognostic factors: age ± SD: I: 35 ± 13, C: 42 ± 14
Sex: I: 66% M, C: 58% M
Groups comparable at baseline? Yes |
Amantadine hydrochloride 2x/day |
Placebo 2x/day |
Length of follow-up: 28 days
Loss-to-follow-up: I: 2/38 (5%)
Reasons: 1 lost to follow-up, 1 withdrew consent C: 2/38 (5%) Reasons: 2 lost to follow-up
Incomplete outcome data: As above |
Neuropsychiatric Inventory Irritability (NPI) NPI-Irritability ≥2 point change
I: 81% C: 44% P=0.0016
Mean change in NPI-irritability I: -4.3 C: -2.6 P=0.0085
Mean change in NPI-irritability distress I: -7.6 C: -5.8 P=0.25
Adverse effects: No significant difference (p>0.05) in incidence of adverse events between I and C |
Amantadine 100mg every morning and at noon appears effective and safe in reducing irritability and aggression in TBI patients with sufficient creatinine clearance. |
|
Hammond, 2015 |
Type of study: Multi-center parallel-group randomized double-blind placebo-controlled trial
Setting: Multi-center (unclear if patients were in care-center or at home)
Country: USA
Source of funding: US Department of Education, Office of Special Education and Rehabilitative Services, National Institute on Disability and Rehabilitation. Dr. Hammond received personal fees from several institutes. No competing financial interests for other authors. |
Inclusion criteria: 1) 16-75 years old 2) sustained a nonpenetrating TBI at least 6 months before enrolment 3) score of ≥6 on Observer-rated NPI-I Most Problematic 4) TBI verified by record review and clinician interview 5) ability to comply with study protocol 6) negative pregnancy test 7) creatinine clearance of >60 8) medical and neurological stability
Exclusion criteria: 1) inability to interact and communicate 2) threat of harm to self or others 3) diagnosis of other neurologic disorder 4) schizophrenia or psychosis 5) seizure in the month before enrolment 6) concomitant use of typical neuroleptic agents or monoamine oxidase inhibitors 7) treatment with amantadine during the month before enrolment 8) enrollment in previous single-site amantadine irritability study
N total at baseline: I: 82 C: 86
Important prognostic factors: Age at enrollment ± SD: I: 40.18±12.67, C: 38.23±12.36
Age at injury ± SD: I: 33.85±12.87, C: 31.88±12.07
Sex: I: 80.5% M, C: 74.4% M (p=0.3473)
Groups comparable at baseline? Yes, except small but significant difference in mean baseline GOS-E (p=0.0492) |
Amantadine, 100 mg twice daily (morning and noon) for 60 days |
Placebo, 100 mg twice daily (morning and noon) for 60 days |
Length of follow-up:
Day 28±3 (primary endpoint) and day 60±3 after baseline (baseline=at least 6 months post-TBI)
Loss-to-follow-up:
28-day follow-up: I: 1 C: 0 60-day follow-up: I: 2 C: 1
Incomplete outcome data: 28-day follow-up: I: n=2 (2.4%) C: n=5 (5.8%)
60-day follow-up: I: n=7 (8.5%) C: n=4 (4.7%) |
Neurobehavioral Functional Inventory rated by Observer
Subdomain I: bad temper, rapid mood changes, sudden anger, impatience, crankiness, argumentative.
Rated: most aberrant, most problematic
% improved by ≥3 points on ‘most problematic’ 28 days: I: 66.3 C: 66.7
% difference (95%CI): -0.4 (-14.7-+13.9) p=0.9554
60 days: I: 74.7 C: 68.3 % difference (95%CI): +6.4% (-7.2- +20%) p=.3777
% improved by ≥3 points on ‘most aberrant’ 28 days: I: 70.4 C: 60.0 % difference (95%CI): -10.4 (-24.7-+3.9) p=0.1672
60 days: I: 68 C: 68.3 % difference (95%CI): -0.3% (-14.4 - +13.8%) p=0.9687
Neurobehavioral Functional Inventory rated by patient
% improved by ≥3 points on ‘most problematic’ 28 days: I: 51.3 C: 40.5 % difference (95%CI): +10.8 (-4.2 - +25.8) p=0.1662
60 days: I: 60.5 C: 48.8 % difference (95%CI): +11.7% (-3.3 - +6.70%) p=0.1373
% improved by ≥3 points on ‘most aberrant’ 28 days: I: 70.4 C: 60.0 % difference (95%CI): -10.4 (-24.7-+3.9) p=0.1672 60 days: I: 60.5 C: 53.6 % difference (95%CI): 6.9% (-8 - +21.8%) p=0.3750
Adverse events: No significant difference in adverse events between I and C |
Observers in both groups reported large improvements, but significant group differences were not found for primary outcome at either day 28 or 60. Amantadine 100 mg every morning and noon may reduce irritability and perceived distress at 60 days post-treatment. Subjective measures used to assess aggressiveness. Some observers appeared more tolerant of irritability. |
|
Mooney, 1993 (SR Fleminger, 2006) |
Type of study: randomized controlled trial
Setting: outpatient
Country: USA
Source of funding: not reported |
Inclusion criteria: 1) serious TBI Other criteria not reported
Exclusion criteria:
N total at baseline: I: 19 C: 19
Important prognostic factors: age ± SD: 29.4 (10.0) Sex: I: 100% male
Groups comparable at baseline? unclear |
methylphenidate increased to 30mg/day |
Placebo (dose frequency NR) |
Length of follow-up:
6 weeks
Loss-to-follow-up: NR
Incomplete outcome data: NR |
State trait anger scale (STAS) difference in change between I and C:
State: -13 lower in I group, p<0.05
Trait: -4 lower in I group, p<0.05 |
|
Risk of Bias
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated? |
Was the allocation adequately concealed?
|
Blinding: Was knowledge of the allocated interventions adequately prevented? |
Was loss to follow-up (missing outcome data) infrequent? |
Are reports of the study free of selective outcome reporting? |
Was the study apparently free of other problems that could put it at a risk of bias? |
Overall risk of bias
|
|
Baňos, 2010 |
Probably no,
no more on procedure reported than it being block randomization, block size unknown |
Not reported
|
Probably no;
blinding not reported |
Definitely no
No intention to treat analysis and high dropout in intervention group |
probably yes;
relevant outcomes were reported |
Probably no
scale used subject to observer bias.
|
high |
|
Hammond, 2014 |
Probably yes;
Blocked randomization with stratification for depression (<13 vs ≥13 on the Beck Depression Inventory–II [BDI-II]) and prior exposure to amantadine was used. |
Probably yes
computer-generated block randomization (central) |
Probably yes
Everyone except the central pharmacist was blinded to group assignment. |
Probably yes
Loss to follow-up was infrequent in intervention and control group. |
Definitely yes
Reason: All relevant outcomes were reported; |
probably no,
measurement instruments and observers subject to observer bias and information bias . |
low
|
|
Hammond, 2015 |
Probably yes;
computer-generated block randomization: Blocked randomization with stratification for depression (<13 vs ≥13 on the Beck Depression Inventory–II |
Probably yes
Allocation through datacentre webpage
Group allocation was concealed. |
Probably yes,
placebo and amantadine pills were identical in taste and appearance. All participants, observers, and personnel were blinded to group assignment. |
Probably no
Loss to follow-up was more frequent in intervention and control group at 60 days than at 30 days, also ‘ITT was followed’ however, outcome data are not measured on all participants. |
Definitely yes
Reason: All relevant outcomes were reported; |
probably no,
measurement instruments and observers subject to observer bias and information bias.
Also, study mainly including white male subjects. |
Some concerns |
|
Mooney, 1993 |
No information; |
No information,
|
Definitely no,
Only subjects were uninformed of their group membership. |
Probably no,
No information about selection and follow up, only analysed subjects described. |
Definitely yes
Reason: All relevant outcomes were reported; |
Probably no,
Little reported on how bias would have been avoided |
high |
Table of excluded studies
Studies from previous guideline (included in the review by Fleminger, 2006)
|
Reference |
Reason for exclusion |
|
Brooke MM, Patterson DR, Questad KA, The treatment of agitation during initial hospitalization after traumatic brain injury. Arch Phys Med Rehabil. 1992;73(10):917-21. PubMed PMID: 1417466. |
Insufficient reporting of results and baseline characteristics |
|
Greendyke RM, Berkner JP, Webster JC,, Treatment of behavioural problems with pindolol. Psychosomatics. 1989;30(2):161-5. PubMed PMID: 2652180. |
Outcome not compared with placebo-group, small sample size |
|
Greendyke RM, Kanter DR, Schuster DB, Propranolol treatment of assaultive patients with organic brain disease: a double-blind crossover, placebo-controlled study. The Journal of nervous and mental disease. 1986;174(5):290-4. |
Sample size too small |
|
Greendyke RM, Kanter DR. Therapeutic effects of pindolol on behavioral disturbances associated with organic brain disease: a double-blind study. Journal of Clinical Psychiatry. 1986;47(8):423-6. |
Outcome not compared with placebo-group, small sample size |
|
Schneider WN, Drew-Cates J, Wong TM,, Cognitive and behavioural efficacy of amantadine in acute traumatic brain injury: an initial double-blind placebo-controlled study. Brain Injury. 1999;13(11):863-72. |
Sample size too small |
Studies from additional search
|
Reference |
Reason for exclusion |
|
Plantier D, Luauté J; SOFMER group. Drugs for behavior disorders after traumatic brain injury: Systematic review and expert consensus leading to French recommendations for good practice. Ann Phys Rehabil Med. 2016 Feb;59(1):42-57. doi: 10.1016/j.rehab.2015.10.003. Epub 2016 Jan 18. PMID: 26797170. |
wrong study design, contains case series and observational studies |
|
Williamson D, Frenette AJ, Burry LD, et alPharmacological interventions for agitated behaviours in patients with traumatic brain injury: a systematic reviewBMJ Open 2019;9:e029604. doi: 10.1136/bmjopen-2019-029604 |
contains non-rcts and studies with children |
|
Barnett M, Reid L. The effectiveness of methylphenidate in improving cognition after brain injury in adults: a systematic review. Brain Inj. 2020;34(1):1-10. doi: 10.1080/02699052.2019.1667538. Epub 2019 Sep 16. PMID: 31526025. |
wrong study design (contains non-RCT studies), wrong outcomes in RCTs |
|
Gao C, Fu Q, Chen P, Liu Z, Zhou Q. The influence of sertraline on depressive disorder after traumatic brain injury: A meta-analysis of randomized controlled studies. Am J Emerg Med. 2019 Sep;37(9):1778-1783. doi: 10.1016/j.ajem.2019.06.050. Epub 2019 Jun 29. PMID: 31326198. |
no new studies included |
|
Hicks AJ, Clay FJ, Hopwood M, James AC, Jayaram M, Batty R, Perry LA, Ponsford JL. Efficacy and Harms of Pharmacological Interventions for Neurobehavioral Symptoms in Post-Traumatic Amnesia after Traumatic Brain Injury: A Systematic Review. J Neurotrauma. 2018 Dec 1;35(23):2755-2775. doi: 10.1089/neu.2018.5738. Epub 2018 Aug 24. PMID: 29969935. |
wrong study design, contains case series and obsevational studies |
|
Hicks AJ, Clay FJ, Hopwood M, James AC, Jayaram M, Perry LA, Batty R, Ponsford JL. The Efficacy and Harms of Pharmacological Interventions for Aggression After Traumatic Brain Injury-Systematic Review. Front Neurol. 2019 Nov 29;10:1169. doi: 10.3389/fneur.2019.01169. PMID: 31849802; PMCID: PMC6895752. |
wrong study design, contains case series |
|
Luauté J, Plantier D, Wiart L, Tell L; SOFMER group. Care management of the agitation or aggressiveness crisis in patients with TBI. Systematic review of the literature and practice recommendations. Ann Phys Rehabil Med. 2016 Feb;59(1):58-67. doi: 10.1016/j.rehab.2015.11.001. Epub 2015 Dec 14. PMID: 26700025. |
Same studie as Plantier D, 2016, double |
|
Mehta S, McIntyre A, Janzen S, Iruthayarajah J, Bateman A, Teasell R. Pharmacological management of agitation among individuals with moderate to severe acquired brain injury: A systematic review. Brain Inj. 2018;32(3):287-296. doi: 10.1080/02699052.2017.1419377. Epub 2018 Jan 23. PMID: 29359952. |
wrong study design, contains case series and obsevational studies |
|
Mohamed, Mona Salah PhD; El Sayed, Iman PhD; Zaki, Adel PhD; Abdelmonem, Sherif MD. Assessment of the effect of amantadine in patients with traumatic brain injury: A meta-analysis. Journal of Trauma and Acute Care Surgery 92(3):p 605-614, March 2022. | DOI: 10.1097/TA.0000000000003363 |
wrong outcome |
|
Nash RP, Weinberg MS, Laughon SL, McCall RC, Bateman JR, Rosenstein DL. Acute Pharmacological Management of Behavioral and Emotional Dysregulation Following a Traumatic Brain Injury: A Systematic Review of the Literature. Psychosomatics. 2019 Mar-Apr;60(2):139-152. doi: 10.1016/j.psym.2018.11.009. Epub 2018 Dec 18. PMID: 30665668; PMCID: PMC8609889. |
contains non-RCTs, no quality appraisal |
|
Ter Mors, B.J., A.P.M. Backx, P. Spauwen, R.W.H.M. Ponds, P.N. Van Harten, and C.M. Van Heugten. “Efficacy of Amantadine on Behavioural Problems Due to Acquired Brain Injury: A Systematic Review.” Brain Injury 33, no. 9 (2019): 1137–50. doi:10.1080/02699052.2019.1631482. |
contains non-RCTS |
|
Wiener J, McIntyre A, Janzen S, Mirkowski M, MacKenzie HM, Teasell R. Opioids and cerebral physiology in the acute management of traumatic brain injury: a systematic review. Brain Inj. 2019;33(5):559-566. doi: 10.1080/02699052.2019.1574328. Epub 2019 Jan 29. PMID: 30696281. |
wrong study design (contains non-RCT studies), wrong outcome in every included RCT |
|
Haddadi, K., Shafizad, M., Elyasi, F., Heidari, F., Fahiminia, F., Alipour, A. (2022). 'Neuroprotective Effects of Methylphenidate on Diffuse Axonal Injury in Acute Traumatic Brain Injury Patients', Trauma Monthly, 27(6), pp. 616-625. doi: 10.30491/tm.2022.328724.1445 |
Outcome measured but results not stated or analysed |
|
Hammond FM, Sherer M, Malec JF, Zafonte RD, Dikmen S, Bogner J, Bell KR, Barber J, Temkin N. Amantadine Did Not Positively Impact Cognition in Chronic Traumatic Brain Injury: A Multi-Site, Randomized, Controlled Trial. J Neurotrauma. 2018 Oct 1;35(19):2298-2305. doi: 10.1089/neu.2018.5767. Epub 2018 Jun 7. PMID: 29742960; PMCID: PMC6157374. |
wrong outcome |
|
Hammond FM, Malec JF, Zafonte RD, Sherer M, Bogner J, Dikmen S, Whitney MP, Bell KR, Perkins SM, Moser EA. Potential Impact of Amantadine on Aggression in Chronic Traumatic Brain Injury. J Head Trauma Rehabil. 2017 Sep/Oct;32(5):308-318. doi: 10.1097/HTR.0000000000000342. PMID: 28891908. |
same trial data as Hammond 2015 |
|
Phyland RK, McKay A, Olver J, Walterfang M, Hopwood M, Ponsford M, Ponsford JL. Use of Olanzapine to Treat Agitation in Traumatic Brain Injury: A Series of N-of-One Trials. J Neurotrauma. 2023 Jan;40(1-2):33-51. doi: 10.1089/neu.2022.0139. Epub 2022 Aug 22. PMID: 35833454. |
wrong design: Not analysed as RCT but as separate studies with n-of-1 design (single case studies) due to recruitment difficulties and small sample size |
|
Soltani F, Tabatabaei S, Jannatmakan F, Nasajian N, Amiri F, Darkhor R, Moravej M. Comparison of the Effects of Haloperidol and Dexmedetomidine on Delirium and Agitation in Patients with a Traumatic Brain Injury Admitted to the Intensive Care Unit. Anesth Pain Med. 2021 Jul 27;11(3):e113802. doi: 10.5812/aapm.113802. PMID: 34540634; PMCID: PMC8438711. |
Wrong population, ICU |
|
Hart T, Whyte J, Watanabe T, Chervoneva I. Effects of dextroamphetamine in subacute traumatic brain injury: A randomized, placebo-controlled pilot study. J Neurosci Res. 2018 Apr;96(4):702-710. doi: 10.1002/jnr.24102. Epub 2017 Jun 27. PMID: 28653428. |
Wrong population, no aggression or agitation at baseline |
|
Chien YJ, Chien YC, Liu CT, Wu HC, Chang CY, Wu MY. Effects of Methylphenidate on Cognitive Function in Adults with Traumatic Brain Injury: A Meta-Analysis. Brain Sci. 2019 Oct 24;9(11):291. doi: 10.3390/brainsci9110291. PMID: 31653039; PMCID: PMC6895997. |
wrong outcome |
Beoordelingsdatum en geldigheid
Publicatiedatum : 14-10-2025
Beoordeeld op geldigheid : 18-09-2025
Algemene gegevens
De ontwikkeling van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire cluster ingesteld. Dit cluster bestaat uit vertegenwoordigers van alle relevante organisaties die betrekking hebben op de zorg rondom acute neurologie inclusief lange termijneffecten.
Het cluster Acute neurologie inclusief lange termijneffecten bestaat uit meerdere richtlijnen, zie hier voor de actuele clusterindeling. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden worden indien nodig gevraagd om hun expertise in te zetten voor een specifieke richtlijnmodule. Het cluster Acute neurologie inclusief lange termijneffecten bestaat uit de volgende personen:
Clusterstuurgroep
- Dhr. drs. H.P. (Paul) Bienfait (voorzitter tot maart 2025), neuroloog, NVN
- Mevr. dr. M.C. (Marieke) Visser (voorzitter vanaf maart 2025), Neuroloog, NVN
- Mevr. dr. I.C. (Irene) Notting, oogarts, NOG
- Dhr. dr. M.H.M. (Mark) Vries, neuroradioloog, NVvR
- Mevr. I.C. (Irene) de Graaf, psychiater, NVvP
Clusterexpertisegroep
- Dhr. drs. I.K. (Iain) Haitsma, neurochirurg, NVvN
- Dhr. dr. W.A. (Wouter) Moojen, neurochirurg, NVvN
- Dhr. drs. M.M. (Mike) Abu Saris, neurochirurg, NVvN
- Mevr. dr. M. (Maayke) Hunfeld, kinderneuroloog, NVN
- Dhr. prof. dr. M.C. (Mathijs) Brouwer, neuroloog, NVN
- Dhr. dr. A. (Anuska) Samkar, neuroloog, NVN
- Dhr. dr. S.F.T.M. (Bas) de Bruijn, neuroloog, NVN
- Dhr. dr. W.M. (Wim) van Mulleners, neuroloog, NVN
- Mevr. prof. dr. J. (Jeannette) Hofmeijer, neuroloog, NVN
- Mevr. prof. dr. J. (Janneke) Horn, neuroloog, NVN
- Dhr. prof. dr. Ing. M.J.A.M. (Michel) van Putten, neuroloog, NVN
- Mevr. dr. K.A. (Kelly) Foks, neuroloog, NVN
- Dhr. mr. M.A.C. (Michiel) Lindhout, patiëntvertegenwoordiger, namens hersenletsel.nl
- Mevr. drs. C.D.E. (Carien) de Jonge, psychiater, NVvP
- Mevr. drs. M. (Monique) van den Berg, psychiater, NVvP
- Mevr. drs. M.Ph.C. (Margit) Klok, psychiater, NVvP
- Mevr. drs. E.C. (Elsbeth) Spakman, revalidatiearts, VRA
- Dhr. dr. J.F. (Jorrit) de Kieviet, revalidatiearts, VRA
- Mevr. drs. J.M. (Janneke) Schuurman, revalidatiearts, VRA
- Mevr. drs. M. (Maartje) Terra, Chirurg, NVvH
- Dhr. drs. I. (Ivar) Spin, fysiotherapeut, KNGF
- Mevr. dr. C.W.E. (Astrid) Hoedemaekers, internist-Intensivist, NVIC
- Dhr. drs. T.F. (Theo) Senden, arbeids- en bedrijfsgeneeskunde, NVAB
- Mevr. H. (Ginie) Wilpshaar, ergotherapeut/handtherapeut, EN
- Dr. drs. T. (Tim) van Grinsven, verslavingsarts, VVGN
- Mevr. prof. dr. J.M. (Joke) Spikman, klinisch neuropsycholoog, NIP
- Dhr. F.A. (Frank) Jonker, klinisch neuropsycholoog, NIP
- Mevr. dr. S.E.L. (Sonja) Leonhard, aio-arts-microbioloog, NVMM
- Mevr. prof. dr. ir. C.E. (Charlotte) Teunissen, hoogleraar neurochemie, NVKC
- Dhr. drs. E.A. (Edwin) Goedhart, sportarts, VSG
- Dhr. dr. L.P.H. (Luuk) van de Rijt, KNO-arts, NVKNO
- Mevr. drs. I. (Ineke) Brümmer, SEH-arts, NVSHA
- Dhr. dr. A.J.B.W. (Arjen) Brouwers, internist, NIV
- Mevr. dr. W.S. (Willemijn) van Erp, specialist ouderengeneeskunde, Verenso
- Dhr. dr. M. (Martijn) Meuwissen, cardioloog, NVVC
Klankbordgroep
- Mevr mr. K. (Katrien) Zetsma, Adviseur gezondheidsrecht bij Artsenfederatie KNMG
Met ondersteuning van
- Mevr. dr. M. (Mirre) den Ouden - Vierwind, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. drs. I. L. (Isabelle) Laseur, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. drs. F. (Florien) Ham, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle clusterstuurgroepleden en actief betrokken expertisegroepsleden (fungerend als schrijver en/of meelezer bij tenminste één van de geprioriteerde richtlijnmodules) hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een richtlijnmodule worden wijzigingen in belangen aan de projectleider doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase. Een overzicht van de belangen van de clusterleden en betrokken expertisegroepsleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Clusterstuurgroep
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Paul Bienfait |
Neuroloog, Gelre Ziekenhuizen |
bestuur MedicALS, bestuur werkgroep acute neurologie NVN, commissie wet- en regelgeving FMS, werkgroep kwaliteit LWNO |
Extern gefinancierd onderzoek: ECO, Profide, Convince, Apache AF, Periscope, Grip |
Geen restricties |
|
Mark Vries |
Neuroradioloog, Amsterdam UMC |
Geen |
Geen |
Geen restricties |
|
Irene Notting |
Oogarts, LUMC Leiden |
Geen |
Subsidie van hartstichting en ZonMw binnen CONTRAST 2. Hartstichting; registratie SAB patienten (CONTRAST 2, WP6). ZonMw; intracerebrale bloedingen trial (DIST). Consultant voor stryker neurovascular, inkomsten worden aan de afdeling Neurochirurgie van het Radboudumc betaald. |
Geen restricties |
|
Irene de Graaf |
Psychiater, Haaglanden Medisch Centrum |
Lid klachtencommissie Parnassiagroep regio Haaglanden (onbetaald behoudens vacatiegelden)
Consulterend psychiater 8 uur per maand bij Basalt revalidatie locatie Den Haag, betaling aan werkgever Haaglanden Medisch Centrum middels detachering. |
Geen |
Geen restricties |
Clusterexpertisegroep
Richtlijn Neuropsychiatrische gevolgen na NAH bij volwassenen
Module Wettelijke kaders na NAH
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Irene de Graaf |
Psychiater, Haaglanden Medisch Centrum |
Lid klachtencommissie Parnassiagroep regio Haaglanden (onbetaald behoudens vacatiegelden)
Consulterend psychiater 8 uur per maand bij Basalt revalidatie locatie Den Haag, betaling aan werkgever Haaglanden Medisch Centrum middels detachering. |
Geen |
Geen restricties |
|
Joke Spikman |
Hoogleraar Klinische Neuropsychologie bij Neurologische Aandoeningen en Klinisch Neuropsycholoog, hoofd onderafdeling Klinische Neuropsychologie, Neurologie, Universitair Medisch Centrum Groningen (UMCG) |
Hoogleraar Klinische Neuropsychologie, Pyschologie, GMW, RUg. |
Geen |
Geen restricties |
|
Katrien Zetsma (klankbordgroep) |
Adviseur gezondheidsrecht bij Artsenfederatie KNMG |
Redactiemedewerker Tijdschrift Gezondheidszorg Jurisprudentie (betaald) |
Geen |
Geen restricties |
Module Niet-medicamenteuze behandeling van agressie en agitatie bij NAH
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Janneke Schuurman |
Revalidatiearts Klimmendaal revalidatiespecialisten |
Werkgroep lid richtlijn Aanhoudende klachten na Licht Traumatisch Hoofd/Hersenletsel |
Geen |
Geen restricties |
|
Ineke Brümmer |
SEH-arts bij Treant zorggroep |
Geen |
Geen |
Geen restricties |
Module Medicamenteuze behandeling van agressie en agitatie bij NAH
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Janneke Schuurman |
Revalidatiearts Klimmendaal revalidatiespecialisten |
Werkgroep lid richtlijn Aanhoudende klachten na Licht Traumatisch Hoofd/Hersenletsel |
Geen |
Geen restricties |
|
Monique van den Berg |
Psychiater, Pro Persona
|
CCE, consulent |
Geen |
Geen restricties |
|
Margit Klok |
Psychiater, Radboudumc Nijmegen |
Bestuurslid NVvP Afdeling Consultatieve-en Ziekenhuispsychiatrie, Redactielid de Psychiater ledentijdschrift NVvP,
|
Geen |
Geen restricties |
Module Behandeling Denk- en/of waarnemingsstoornissen bij NAH
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Carien de Jonge |
Psychiater, Haaglanden Medisch Centrum |
Consult psychiatrie bij Basalt Revalidatie (detachering) |
Geen |
Geen restricties |
|
Willemijn van Erp |
Specialist ouderengeneeskunde en post-doctoraal onderzoeker bij Radboudumc, Accolade Zorg (Bosch en Duin) en Libra Revaldidatie & Audiologie |
Geen |
Lopend: Coördinatie onderzoeksproject Meten in de Keten, gefinancierd door De Hersenstichting (https://www.eennacoma.nl/kennis/projecten/meten-in-de-keten/). |
Geen restricties |
|
Monique van den Berg |
Psychiater, Pro Persona
|
CCE, consulent |
Geen |
Geen restricties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door deelname van relevante patiëntenorganisaties aan de need-for-update en/of prioritering. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De richtlijnmodule is tevens ter commentaar voorgelegd aan alle relevante patiëntenorganisaties in de stuur- en expertisegroep (zie ‘Samenstelling cluster’ onder ‘Verantwoording’) en aan alle patiëntenorganisaties die niet deelnemen aan de stuur- en expertisegroep, maar wel hebben deelgenomen aan de need-for-update (zie ‘Need-for-update’ onder ‘Verantwoording’). De eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Module |
Uitkomst raming |
Toelichting |
|
Medicamenteuze behandeling van agressie en agitatie bij NAH |
Geen financiële gevolgen |
Hoewel er jaarlijks >40.000 patiënten hersenletsel oplopen, hebben de aanbevelingen geen toename in het aantal FTE of toename in kwalificatie tot gevolg. Ook zijn er geen substantiële investeringen met de wijzigingen gemoeid. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Need-for-update, prioritering en uitgangsvragen
Tijdens de need-for-update fase (februari 2023) inventariseerde het cluster de geldigheid van de richtlijnmodules binnen het cluster. Naast de partijen die deelnemen aan de stuur- en expertisegroep zijn hier ook andere stakeholders voor benaderd. Per richtlijnmodule is aangegeven of deze geldig is, herzien moet worden, kan vervallen of moet worden samengevoegd. Ook was er de mogelijkheid om nieuwe onderwerpen aan te dragen die aansluiten bij één (of meerdere) richtlijn(en) behorend tot het cluster. De richtlijnmodules waarbij door één of meerdere partijen werd aangegeven herzien te worden, werden doorgezet naar de prioriteringsronde. Ook suggesties voor nieuwe richtlijnmodules werden doorgezet naar de prioriteringsronde. Afgevaardigden vanuit de partijen in de stuur- en expertisegroep werden gevraagd om te prioriteren (zie ‘Samenstelling cluster’ onder ‘Verantwoording’). Hiervoor werd de RE-weighted Priority-Setting (REPS) – tool gebruikt. De uitkomsten (ranklijst) werd gebruikt als uitgangspunt voor de discussie. Voor de geprioriteerde richtlijnmodules zijn door de het cluster concept-uitgangsvragen herzien of opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde het cluster welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. Het cluster waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde het cluster tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd indien mogelijk gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding). GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
Tabel Gradaties voor de kwaliteit van wetenschappelijk bewijs
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in een richtlijnmodule volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door het cluster wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. Het cluster heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Tabel Sterkte van de aanbevelingen
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
Bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de richtlijnmodule Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd voorgelegd aan alle partijen die benaderd zijn voor de need-for-update fase. De commentaren werden verzameld en besproken met het cluster. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door het cluster. De definitieve richtlijnmodule werd ter autorisatie of goedkeuring voorgelegd aan de partijen die beschreven staan bij ‘Initiatief en autorisatie’ onder ‘Verantwoording’.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 3.0 (2023). Adviescommissie Richtlijnen van de Raad Kwalitieit.
http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html.
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Zoekopbrengst
|
9-11-2023 |
EMBASE |
OVID/MEDLINE |
Ontdubbeld tov 1-8-2023 |
|
SRs |
215 |
37 |
56 |
|
RCTs |
113 |
23 |
21 |
|
Observationele studies |
|
|
|
|
Overig |
|
|
|
|
Totaal |
|
|
336 |
|
1-8-2023 |
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
160 |
33 |
162 |
|
RCTs |
93 |
21 |
97 |
|
Observationele studies |
|
|
|
|
Overig |
|
|
|
|
Totaal |
|
|
259 |
Zoekstrategie
Embase 9-11-2023
|
No. |
Query |
Results |
|
|
#22 |
#7 NOT #21 |
5 |
|
|
#21 |
#7 AND #20 |
2 |
|
|
#20 |
#18 OR #19 |
253 |
|
|
#19 |
#15 AND #17 NOT #18 RCT |
113 |
|
|
#18 |
#15 AND #16 SR |
215 |
|
|
#17 |
'randomized controlled trial'/exp OR random*:ti,ab OR (((pragmatic OR practical) NEAR/1 'clinical trial*'):ti,ab) OR ((('non inferiority' OR noninferiority OR superiority OR equivalence) NEAR/3 trial*):ti,ab) OR rct:ti,ab,kw |
2082419 |
|
|
#16 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
948899 |
|
|
#15 |
#12 AND [2016-2023]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
2135 |
|
|
#14 |
#7 NOT #13 |
0 |
|
|
#13 |
#7 AND #12 |
7 |
|
|
#12 |
#11 NOT (('adolescent'/exp OR 'child'/exp OR adolescent*:ti,ab,kw OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw)) |
5795 |
|
|
#11 |
#8 AND #9 AND #10 |
6735 |
|
|
#10 |
'antidepressant agent'/exp OR 'beta adrenergic receptor blocking agent'/exp OR 'dopamine receptor stimulating agent'/exp OR 'neuroleptic agent'/exp OR 'anticonvulsive agent'/exp OR 'benzodiazepine derivative'/exp OR benzodiazepine*:ti,ab,kw OR 'antidepressant':ti,ab,kw OR 'antidepressants':ti,ab,kw OR 'psychoenergizer':ti,ab,kw OR 'thymoleptic':ti,ab,kw OR 'dopamine agonist':ti,ab,kw OR 'dopamine agonists':ti,ab,kw OR 'dopamine receptor agonist':ti,ab,kw OR 'dopamine receptor stimulating agent':ti,ab,kw OR 'dopamine receptor stimulator':ti,ab,kw OR 'dopaminergics':ti,ab,kw OR 'antipsychotics':ti,ab,kw OR 'butyrophenone tranquilizer*':ti,ab,kw OR 'classical antipsychotic*':ti,ab,kw OR 'major tranquilizer*':ti,ab,kw OR 'major tranquillizer*':ti,ab,kw OR 'neuroleptic':ti,ab,kw OR neuroleptics:ti,ab,kw OR 'phenothiazine tranquilizers':ti,ab,kw OR 'typical antipsychotic*':ti,ab,kw OR 'anticonvulsant*':ti,ab,kw OR 'anti convulsant*':ti,ab,kw OR 'anticonvulsivum':ti,ab,kw OR 'antiepileptic barbiturate*':ti,ab,kw OR ((('anti epilepti*' OR antiepilepti* OR anticonvulsi* OR 'anti convulsi*' OR antipsychotic* OR 'anti depress*' OR antidepress* OR neurothylmoleptic OR dopamin*) NEAR/3 (agent* OR drug*)):ti,ab,kw) OR 'adrenergic beta antagonists':ti,ab,kw OR 'beta adrenergic antagonist':ti,ab,kw OR 'beta adrenolytic':ti,ab,kw OR 'beta antiadrenergic agent':ti,ab,kw OR 'beta sympathicolytic*':ti,ab,kw OR betasympathicolytic*:ti,ab,kw OR ((beta NEAR/3 (block* OR antagonist*)):ti,ab,kw) OR 'amantadine'/exp OR 'amphetamine'/exp OR 'amphetamine derivative'/exp OR 'methylphenidate'/exp OR 'olanzapine'/exp OR 'sertraline'/exp OR 'propranolol'/exp OR 'valproic acid'/exp OR 'oxazepam'/exp OR 'lorazepam'/exp OR 'midazolam'/exp OR 'esketamine'/exp OR 'opiate'/exp OR 'opiate agonist'/exp OR 'morphine'/exp OR 'morphine derivative'/exp OR 'fentanyl'/exp OR 'fentanyl derivative'/exp OR 'sufentanil'/exp OR 'remifentanil'/exp OR 'alfentanil'/exp OR 'phenoperidine'/exp OR 'haloperidol'/exp OR 'droperidol'/exp OR 'droperidol plus fentanyl'/exp OR amphetamin*:ti,ab,kw OR amantadin*:ti,ab,kw OR methyophenidate:ti,ab,kw OR concerta:ti,ab,kw OR ritalin:ti,ab,kw OR equasim:ti,ab,kw OR olanzapin*:ti,ab,kw OR sertralin*:ti,ab,kw OR 'propranolol':ti,ab,kw OR 'valproic acid':ti,ab,kw OR 'oxazepam':ti,ab,kw OR 'lorazepam':ti,ab,kw OR 'midazolam':ti,ab,kw OR 'esketamine':ti,ab,kw OR 'opiate*':ti,ab,kw OR 'morphine':ti,ab,kw OR 'fentanyl':ti,ab,kw OR 'sufentanil':ti,ab,kw OR 'remifentanil':ti,ab,kw OR 'alfentanil':ti,ab,kw OR 'phenoperidine':ti,ab,kw OR 'haloperidol':ti,ab,kw OR 'droperidol':ti,ab,kw |
2040681 |
|
|
#9 |
'aggression'/exp OR 'anger'/exp OR 'agitation'/exp OR 'restlessness'/exp OR 'impulse control disorder'/exp OR 'impulsiveness'/exp OR 'violence'/exp OR 'mental instability'/exp OR 'disruptive behavior'/exp OR 'agitati*':ti,ab,kw OR 'restlessness':ti,ab,kw OR 'impulse control disorder*':ti,ab,kw OR 'dangerous behavior':ti,ab,kw OR 'dangerous behaviour':ti,ab,kw OR 'violen*':ti,ab,kw OR 'anger':ti,ab,kw OR 'tantrum':ti,ab,kw OR aggression:ti,ab,kw OR impulsiv*:ti,ab,kw OR negativism:ti,ab,kw OR irritab*:ti,ab,kw OR hostil*:ti,ab,kw OR violen*:ti,ab,kw OR rage:ti,ab,kw OR (((combative OR destructive OR explosive OR withdrawal OR argument*) NEAR/2 behavio*):ti,ab,kw) OR 'escalating temper':ti,ab,kw OR 'episodic discontrol':ti,ab,kw OR 'verbally abusiv*':ti,ab,kw OR 'assaultive patien*':ti,ab,kw OR disinhibition:ti,ab,kw OR 'catastrophic reaction*':ti,ab,kw OR (((affective OR emotional OR mental OR mood OR psychic OR psychologic*) NEAR/3 (instab* OR labil*)):ti,ab,kw) OR (((combative OR destructive OR aggress* OR withdraw* OR assault*) NEAR/2 (behavior OR behaviour)):ti,ab,kw) OR 'verbally abus*':ti,ab,kw OR disinhibiti*:ti,ab,kw |
532057 |
|
|
#8 |
'brain disease'/de OR 'brain edema'/exp OR 'brain hernia'/exp OR 'brain infection'/exp OR 'brain necrosis'/exp OR 'brain sclerosis'/exp OR 'brain toxicity'/exp OR 'dialysis encephalopathy'/exp OR 'encephalomalacia'/exp OR 'heat stroke'/exp OR 'hemorrhagic encephalopathy'/exp OR 'hydrocephalus'/exp OR 'hypertension encephalopathy'/exp OR 'leukoencephalopathy'/exp OR 'metabolic encephalopathy'/exp OR 'necrotizing encephalopathy'/exp OR 'intracranial hypertension'/exp OR 'organic brain syndrome'/exp OR 'organic psychosyndrome'/exp OR 'pseudobulbar palsy'/exp OR 'sepsis associated encephalopathy'/exp OR 'penetrating head injury'/de OR 'thalamus disease'/exp OR 'head injury'/de OR 'brain injury'/exp OR 'meningitis'/exp OR 'encephalitis'/exp OR 'brain hypoxia'/exp OR 'traumatic coma'/exp OR 'concussion'/de OR 'brain concussion'/exp OR 'brain tumor'/exp OR 'cerebrovascular disease'/exp OR 'stroke patient'/exp OR 'meningeal inflammation':ti,ab,kw OR 'meningitis':ti,ab,kw OR 'perimeningeal infections':ti,ab,kw OR 'brain inflammation':ti,ab,kw OR 'cerebritis':ti,ab,kw OR 'encephalitis':ti,ab,kw OR 'enkephalitis':ti,ab,kw OR 'brain commotion':ti,ab,kw OR 'brain concussion':ti,ab,kw OR 'brain contusion':ti,ab,kw OR 'cerebral concussion':ti,ab,kw OR 'commotio cerebri':ti,ab,kw OR (((brain OR cerebr* OR intracranial OR 'left hemisphere' OR 'right hemisphere' OR craniocerebr*) NEAR/3 (edema OR hernia OR infecti* OR scleros* OR toxic* OR injur* OR accident* OR anoxaemi* OR anoxemi* OR anoxi* OR hypoxi* OR asphyx* OR cancer* OR necros* OR neoplasm* OR carcinom* OR tumor* OR tumour* OR angiopath* OR 'vascular disease*' OR vasculopath* OR 'small vessel disease*' OR 'vascular disorder*' OR 'vascular disturbance*' OR 'vascular lesion*' OR 'vascular damage*' OR 'vascular syndrome*' OR cyst*)):ti,ab,kw) OR (((injur* OR posttrauma* OR trauma*) NEAR/3 coma):ti,ab,kw) OR encephalomalacia:ti,ab,kw OR 'heat stroke':ti,ab,kw OR (((dialysis OR hemorrhag* OR hypertension OR metabol* OR necroti* OR 'sepsis associate*') NEAR/3 encephalopath*):ti,ab,kw) OR ((organic NEAR/3 ('brain syndrome' OR psychosyndrome)):ti,ab,kw) OR 'pseudobulbar palsy':ti,ab,kw OR ((thalam* NEAR/2 disease*):ti,ab,kw) OR leukoencephalopath*:ti,ab,kw OR binswanger:ti,ab,kw OR 'mulitple sclerosis':ti,ab,kw |
2098550 |
|
|
#7 |
#1 OR #2 OR #3 OR #4 OR #5 OR #6 |
7 |
|
|
#6 |
'pharmacological treatment of agitation and/or aggression in patients with traumatic brain injury' |
1 |
|
|
#5 |
'a descriptive analysis of pharmacological management of aggression/ and or agitation in patients with traumatic brain injury in a southwest virginia inpatient population' |
2 |
|
|
#4 |
'amantadine effect on perceptions of irritability after traumatic brain injury: results of the amantadine irritability multisite study' |
1 |
|
|
#3 |
'effectiveness of amantadine hydrochloride in the reduction of chronic traumatic brain injury irritability and aggression' |
1 |
|
|
#2 |
'impact of early administration of sertraline on cognitive and behavioral recovery in the first year after moderate to severe traumatic brain injury' |
1 |
|
|
#1 |
'pharmacological management for agitation and aggression in people with acquired brain injury' AND 2006 |
1 |
|
Embase 1-8-2023
|
No. |
Query |
Results |
|
#22 |
#7 NOT #21 4 sleutelartikelen niet gevonden vanwege tijdslimiet |
4 |
|
#21 |
#7 AND #20 2 sleutelartikelen gevonden |
2 |
|
#20 |
#18 OR #19 RCTs |
253 |
|
#19 |
#15 AND #17 NOT #18 SR |
93 |
|
#18 |
#15 AND #16 |
160 |
|
#17 |
'randomized controlled trial'/exp OR random*:ti,ab OR (((pragmatic OR practical) NEAR/1 'clinical trial*'):ti,ab) OR ((('non inferiority' OR noninferiority OR superiority OR equivalence) NEAR/3 trial*):ti,ab) OR rct:ti,ab,kw |
2082419 |
|
#16 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
948899 |
|
#15 |
#12 AND [2016-2023]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
1564 |
|
#14 |
#7 NOT #13 |
0 |
|
#13 |
#7 AND #12 alle sleutelartikelen gevonden in de basisset |
6 |
|
#12 |
#11 NOT (('adolescent'/exp OR 'child'/exp OR adolescent*:ti,ab,kw OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw)) |
5795 |
|
#11 |
#8 AND #9 AND #10 |
6735 |
|
#10 |
'antidepressant agent'/exp OR 'beta adrenergic receptor blocking agent'/exp OR 'dopamine receptor stimulating agent'/exp OR 'neuroleptic agent'/exp OR 'anticonvulsive agent'/exp OR 'benzodiazepine derivative'/exp OR benzodiazepine*:ti,ab,kw OR 'antidepressant':ti,ab,kw OR 'antidepressants':ti,ab,kw OR 'psychoenergizer':ti,ab,kw OR 'thymoleptic':ti,ab,kw OR 'dopamine agonist':ti,ab,kw OR 'dopamine agonists':ti,ab,kw OR 'dopamine receptor agonist':ti,ab,kw OR 'dopamine receptor stimulating agent':ti,ab,kw OR 'dopamine receptor stimulator':ti,ab,kw OR 'dopaminergics':ti,ab,kw OR 'antipsychotics':ti,ab,kw OR 'butyrophenone tranquilizer*':ti,ab,kw OR 'classical antipsychotic*':ti,ab,kw OR 'major tranquilizer*':ti,ab,kw OR 'major tranquillizer*':ti,ab,kw OR 'neuroleptic':ti,ab,kw OR neuroleptics:ti,ab,kw OR 'phenothiazine tranquilizers':ti,ab,kw OR 'typical antipsychotic*':ti,ab,kw OR 'anticonvulsant*':ti,ab,kw OR 'anti convulsant*':ti,ab,kw OR 'anticonvulsivum':ti,ab,kw OR 'antiepileptic barbiturate*':ti,ab,kw OR ((('anti epilepti*' OR antiepilepti* OR anticonvulsi* OR 'anti convulsi*' OR antipsychotic* OR 'anti depress*' OR antidepress* OR neurothylmoleptic OR dopamin*) NEAR/3 (agent* OR drug*)):ti,ab,kw) OR 'adrenergic beta antagonists':ti,ab,kw OR 'beta adrenergic antagonist':ti,ab,kw OR 'beta adrenolytic':ti,ab,kw OR 'beta antiadrenergic agent':ti,ab,kw OR 'beta sympathicolytic*':ti,ab,kw OR betasympathicolytic*:ti,ab,kw OR ((beta NEAR/3 (block* OR antagonist*)):ti,ab,kw) OR 'amantadine'/exp OR 'amphetamine'/exp OR 'amphetamine derivative'/exp OR 'methylphenidate'/exp OR 'olanzapine'/exp OR 'sertraline'/exp OR 'propranolol'/exp OR 'valproic acid'/exp OR 'oxazepam'/exp OR 'lorazepam'/exp OR 'midazolam'/exp OR 'esketamine'/exp OR 'opiate'/exp OR 'opiate agonist'/exp OR 'morphine'/exp OR 'morphine derivative'/exp OR 'fentanyl'/exp OR 'fentanyl derivative'/exp OR 'sufentanil'/exp OR 'remifentanil'/exp OR 'alfentanil'/exp OR 'phenoperidine'/exp OR 'haloperidol'/exp OR 'droperidol'/exp OR 'droperidol plus fentanyl'/exp OR amphetamin*:ti,ab,kw OR amantadin*:ti,ab,kw OR methyophenidate:ti,ab,kw OR concerta:ti,ab,kw OR ritalin:ti,ab,kw OR equasim:ti,ab,kw OR olanzapin*:ti,ab,kw OR sertralin*:ti,ab,kw OR 'propranolol':ti,ab,kw OR 'valproic acid':ti,ab,kw OR 'oxazepam':ti,ab,kw OR 'lorazepam':ti,ab,kw OR 'midazolam':ti,ab,kw OR 'esketamine':ti,ab,kw OR 'opiate*':ti,ab,kw OR 'morphine':ti,ab,kw OR 'fentanyl':ti,ab,kw OR 'sufentanil':ti,ab,kw OR 'remifentanil':ti,ab,kw OR 'alfentanil':ti,ab,kw OR 'phenoperidine':ti,ab,kw OR 'haloperidol':ti,ab,kw OR 'droperidol':ti,ab,kw |
2040681 |
|
#9 |
'aggression'/exp OR 'anger'/exp OR 'agitation'/exp OR 'restlessness'/exp OR 'impulse control disorder'/exp OR 'impulsiveness'/exp OR 'violence'/exp OR 'mental instability'/exp OR 'disruptive behavior'/exp OR 'agitati*':ti,ab,kw OR 'restlessness':ti,ab,kw OR 'impulse control disorder*':ti,ab,kw OR 'dangerous behavior':ti,ab,kw OR 'dangerous behaviour':ti,ab,kw OR 'violen*':ti,ab,kw OR 'anger':ti,ab,kw OR 'tantrum':ti,ab,kw OR aggression:ti,ab,kw OR impulsiv*:ti,ab,kw OR negativism:ti,ab,kw OR irritab*:ti,ab,kw OR hostil*:ti,ab,kw OR violen*:ti,ab,kw OR rage:ti,ab,kw OR (((combative OR destructive OR explosive OR withdrawal OR argument*) NEAR/2 behavio*):ti,ab,kw) OR 'escalating temper':ti,ab,kw OR 'episodic discontrol':ti,ab,kw OR 'verbally abusiv*':ti,ab,kw OR 'assaultive patien*':ti,ab,kw OR disinhibition:ti,ab,kw OR 'catastrophic reaction*':ti,ab,kw OR (((affective OR emotional OR mental OR mood OR psychic OR psychologic*) NEAR/3 (instab* OR labil*)):ti,ab,kw) OR (((combative OR destructive OR aggress* OR withdraw* OR assault*) NEAR/2 (behavior OR behaviour)):ti,ab,kw) OR 'verbally abus*':ti,ab,kw OR disinhibiti*:ti,ab,kw |
532057 |
|
#8 |
'penetrating head injury'/de OR 'head injury'/de OR 'traumatic coma'/de OR 'brain injury'/exp OR 'meningitis'/exp OR 'encephalitis'/exp OR 'brain hypoxia'/exp OR 'traumatic coma'/exp OR 'concussion'/de OR 'brain concussion'/exp OR 'brain cancer'/exp OR 'cerebrovascular disease'/exp OR 'stroke patient'/exp OR 'meningeal inflammation':ti,ab,kw OR 'meningitis':ti,ab,kw OR 'perimeningeal infections':ti,ab,kw OR 'brain inflammation':ti,ab,kw OR 'cerebritis':ti,ab,kw OR 'encephalitis':ti,ab,kw OR 'enkephalitis':ti,ab,kw OR 'brain commotion':ti,ab,kw OR 'brain concussion':ti,ab,kw OR 'brain contusion':ti,ab,kw OR 'cerebral concussion':ti,ab,kw OR 'commotio cerebri':ti,ab,kw OR (((brain OR cerebr* OR intracranial OR 'left hemisphere' OR 'right hemisphere' OR craniocerebr*) NEAR/3 (injur* OR accident* OR anoxaemi* OR anoxemi* OR anoxi* OR hypoxi* OR asphyx* OR cancer* OR neoplasm* OR carcinom* OR tumor* OR tumour* OR angiopath* OR 'vascular disease*' OR vasculopath* OR 'small vessel disease*' OR 'vascular disorder*' OR 'vascular disturbance*' OR 'vascular lesion*' OR 'vascular damage*' OR 'vascular syndrome*')):ti,ab,kw) OR (((injur* OR posttrauma* OR trauma*) NEAR/3 coma):ti,ab,kw) |
1553457 |
|
#7 |
#1 OR #2 OR #3 OR #4 OR #5 OR #6 sleutelartikelen |
6 |
|
#6 |
'pharmacological treatment of agitation and/or aggression in patients with traumatic brain injury' |
1 |
|
#5 |
'a descriptive analysis of pharmacological management of aggression/ and or agitation in patients with traumatic brain injury in a southwest virginia inpatient population' |
1 |
|
#4 |
'amantadine effect on perceptions of irritability after traumatic brain injury: results of the amantadine irritability multisite study' |
1 |
|
#3 |
'effectiveness of amantadine hydrochloride in the reduction of chronic traumatic brain injury irritability and aggression' |
1 |
|
#2 |
'impact of early administration of sertraline on cognitive and behavioral recovery in the first year after moderate to severe traumatic brain injury' |
1 |
|
#1 |
'pharmacological management for agitation and aggression in people with acquired brain injury' AND 2006 |
1 |
Ovid/Medline 9-11-2023
|
# |
Searches |
Results |
|
11 |
(7 and 9) not 8 RCT |
23 |
|
10 |
7 and 8 SR |
37 |
|
9 |
exp randomized controlled trial/ or randomized controlled trials as topic/ or random*.ti,ab. or rct?.ti,ab. or ((pragmatic or practical) adj "clinical trial*").ti,ab,kf. or ((non-inferiority or noninferiority or superiority or equivalence) adj3 trial*).ti,ab,kf. |
1661152 |
|
8 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
705518 |
|
7 |
limit 6 to yr="2016 -Current" |
237 |
|
6 |
5 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) |
720 |
|
5 |
4 not ((Adolescent/ or Child/ or Infant/ or adolescen*.ti,ab,kf. or child*.ti,ab,kf. or schoolchild*.ti,ab,kf. or infant*.ti,ab,kf. or girl*.ti,ab,kf. or boy*.ti,ab,kf. or teen.ti,ab,kf. or teens.ti,ab,kf. or teenager*.ti,ab,kf. or youth*.ti,ab,kf. or pediatr*.ti,ab,kf. or paediatr*.ti,ab,kf. or puber*.ti,ab,kf.) not (Adult/ or adult*.ti,ab,kf. or man.ti,ab,kf. or men.ti,ab,kf. or woman.ti,ab,kf. or women.ti,ab,kf.)) |
783 |
|
4 |
1 and 2 and 3 |
889 |
|
3 |
exp Antidepressive Agents/ or exp Antipsychotic Agents/ or exp Dopamine Agonists/ or exp Adrenergic beta-Antagonists/ or exp Anticonvulsants/ or exp Benzodiazepines/ or exp Amantadine/ or exp Amphetamines/ or exp Methylphenidate/ or exp Olanzapine/ or exp Sertraline/ or exp Propranolol/ or exp Valproic Acid/ or exp Oxazepam/ or exp Lorazepam/ or exp Midazolam/ or exp Ketamine/ or exp Analgesics, Opioid/ or exp Morphine/ or exp Morphine Derivatives/ or exp Fentanyl/ or exp Sufentanil/ or exp Alfentanil/ or exp Phenoperidine/ or exp Haloperidol/ or exp Droperidol/ or benzodiazepine*.ti,ab,kf. or antidepressant.ti,ab,kf. or antidepressants.ti,ab,kf. or psychoenergizer.ti,ab,kf. or thymoleptic.ti,ab,kf. or dopamine agonist.ti,ab,kf. or dopamine agonists.ti,ab,kf. or dopamine receptor agonist.ti,ab,kf. or dopamine receptor stimulating agent.ti,ab,kf. or dopamine receptor stimulator.ti,ab,kf. or dopaminergics.ti,ab,kf. or antipsychotics.ti,ab,kf. or butyrophenone tranquilizer*.ti,ab,kf. or classical antipsychotic*.ti,ab,kf. or major tranquilizer*.ti,ab,kf. or major tranquillizer*.ti,ab,kf. or neuroleptic.ti,ab,kf. or neuroleptics.ti,ab,kf. or phenothiazine tranquilizers.ti,ab,kf. or typical antipsychotic*.ti,ab,kf. or anticonvulsant*.ti,ab,kf. or anti convulsant*.ti,ab,kf. or anticonvulsivum.ti,ab,kf. or antiepileptic barbiturate*.ti,ab,kf. or ((anti epilepti* or antiepilepti* or anticonvulsi* or anti convulsi* or antipsychotic* or anti depress* or antidepress* or neurothylmoleptic or dopamin*) adj3 (agent* or drug*)).ti,ab,kf. or adrenergic beta antagonists.ti,ab,kf. or beta adrenergic antagonist.ti,ab,kf. or beta adrenolytic.ti,ab,kf. or beta antiadrenergic agent.ti,ab,kf. or beta sympathicolytic*.ti,ab,kf. or betasympathicolytic*.ti,ab,kf. or (beta adj3 (block* or antagonist*)).ti,ab,kf. or amphetamin*.ti,ab,kf. or amantadin*.ti,ab,kf. or methyophenidate.ti,ab,kf. or concerta.ti,ab,kf. or ritalin.ti,ab,kf. or equasim.ti,ab,kf. or olanzapin*.ti,ab,kf. or sertralin*.ti,ab,kf. or propranolol.ti,ab,kf. or valproic acid.ti,ab,kf. or oxazepam.ti,ab,kf. or lorazepam.ti,ab,kf. or midazolam.ti,ab,kf. or esketamine.ti,ab,kf. or opiate*.ti,ab,kf. or morphine.ti,ab,kf. or fentanyl.ti,ab,kf. or sufentanil.ti,ab,kf. or remifentanil.ti,ab,kf. or alfentanil.ti,ab,kf. or phenoperidine.ti,ab,kf. or haloperidol.ti,ab,kf. or droperidol.ti,ab,kf. |
876338 |
|
2 |
exp Aggression/ or Psychomotor Agitation/ or exp Anger/ or "Disruptive, Impulse Control, and Conduct Disorders"/ or exp Impulsive Behavior/ or exp Violence/ or agitati*.ti,ab,kf. or restlessness.ti,ab,kf. or impulse control disorder*.ti,ab,kf. or dangerous behavior.ti,ab,kf. or dangerous behaviour.ti,ab,kf. or violen*.ti,ab,kf. or anger.ti,ab,kf. or tantrum.ti,ab,kf. or aggression.ti,ab,kf. or impulsiv*.ti,ab,kf. or negativism.ti,ab,kf. or irritab*.ti,ab,kf. or hostil*.ti,ab,kf. or violen*.ti,ab,kf. or rage.ti,ab,kf. or ((combative or destructive or explosive or withdrawal or argument*) adj2 behavio*).ti,ab,kf. or escalating temper.ti,ab,kf. or episodic discontrol.ti,ab,kf. or verbally abusiv*.ti,ab,kf. or assaultive patien*.ti,ab,kf. or disinhibition.ti,ab,kf. or catastrophic reaction*.ti,ab,kf. or ((affective or emotional or mental or mood or psychic or psychologic*) adj3 (instab* or labil*)).ti,ab,kf. or ((combative or destructive or aggress* or withdraw* or assault*) adj2 (behavior or behaviour)).ti,ab,kf. or verbally abus*.ti,ab,kf. or disinhibiti*.ti,ab,kf. |
351353 |
|
1 |
Brain Diseases/ or Brain Edema/ or Encephalocele/ or Brain Abscess/ or Multiple Sclerosis/ or exp Brain Injuries/ or exp Heat Stroke/ or exp Intracranial Hypertension/ or Brain Diseases, Metabolic/ or Sepsis-Associated Encephalopathy/ or Encephalomalacia/ or Leukoencephalopathies/ or exp Pseudobulbar Palsy/ or exp Craniocerebral Trauma/ or exp Meningitis/ or exp Hypoxia, Brain/ or exp Brain Neoplasms/ or exp Cerebrovascular Disorders/ or meningeal inflammation.ti,ab,kf. or meningitis.ti,ab,kf. or perimeningeal infections.ti,ab,kf. or brain inflammation.ti,ab,kf. or cerebritis.ti,ab,kf. or encephalitis.ti,ab,kf. or enkephalitis.ti,ab,kf. or brain commotion.ti,ab,kf. or brain concussion.ti,ab,kf. or brain contusion.ti,ab,kf. or cerebral concussion.ti,ab,kf. or commotio cerebri.ti,ab,kf. or ((brain or cerebr* or intracranial or left hemisphere or right hemisphere or craniocerebr*) adj3 (edema or hernia or infecti* or scleros* or toxic* or injur* or accident* or anoxaemi* or anoxemi* or anoxi* or hypoxi* or asphyx* or cancer* or necros* or neoplasm* or carcinom* or tumor* or tumour* or angiopath* or vascular disease* or vasculopath* or small vessel disease* or vascular disorder* or vascular disturbance* or vascular lesion* or vascular damage* or vascular syndrome* or cyst*)).ti,ab,kf. or ((injur* or posttrauma* or trauma*) adj3 coma).ti,ab,kf. or encephalomalacia.ti,ab,kf. or heat stroke.ti,ab,kf. or ((dialysis or hemorrhag* or hypertension or metabol* or necroti* or sepsis associate*) adj3 encephalopath*).ti,ab,kf. or (organic adj3 (brain syndrome or psychosyndrome)).ti,ab,kf. or pseudobulbar palsy.ti,ab,kf. or (thalam* adj2 disease*).ti,ab,kf. or leukoencephalopath*.ti,ab,kf. or binswanger.ti,ab,kf. or mulitple sclerosis.ti,ab,kf. |
1103682 |
Ovid/Medline 1-8-2023
|
# |
Searches |
|
11 |
(7 and 9) not 10 RCT |
|
10 |
7 and 8 SR |
|
9 |
exp randomized controlled trial/ or randomized controlled trials as topic/ or random*.ti,ab. or rct?.ti,ab. or ((pragmatic or practical) adj "clinical trial*").ti,ab,kf. or ((non-inferiority or noninferiority or superiority or equivalence) adj3 trial*).ti,ab,kf. |
|
8 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
|
7 |
limit 6 to yr="2016 -Current" |
|
6 |
5 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) |
|
5 |
4 not ((Adolescent/ or Child/ or Infant/ or adolescen*.ti,ab,kf. or child*.ti,ab,kf. or schoolchild*.ti,ab,kf. or infant*.ti,ab,kf. or girl*.ti,ab,kf. or boy*.ti,ab,kf. or teen.ti,ab,kf. or teens.ti,ab,kf. or teenager*.ti,ab,kf. or youth*.ti,ab,kf. or pediatr*.ti,ab,kf. or paediatr*.ti,ab,kf. or puber*.ti,ab,kf.) not (Adult/ or adult*.ti,ab,kf. or man.ti,ab,kf. or men.ti,ab,kf. or woman.ti,ab,kf. or women.ti,ab,kf.)) |
|
4 |
1 and 2 and 3 |
|
3 |
exp Antidepressive Agents/ or exp Antipsychotic Agents/ or exp Dopamine Agonists/ or exp Adrenergic beta-Antagonists/ or exp Anticonvulsants/ or exp Benzodiazepines/ or exp Amantadine/ or exp Amphetamines/ or exp Methylphenidate/ or exp Olanzapine/ or exp Sertraline/ or exp Propranolol/ or exp Valproic Acid/ or exp Oxazepam/ or exp Lorazepam/ or exp Midazolam/ or exp Ketamine/ or exp Analgesics, Opioid/ or exp Morphine/ or exp Morphine Derivatives/ or exp Fentanyl/ or exp Sufentanil/ or exp Alfentanil/ or exp Phenoperidine/ or exp Haloperidol/ or exp Droperidol/ or benzodiazepine*.ti,ab,kf. or antidepressant.ti,ab,kf. or antidepressants.ti,ab,kf. or psychoenergizer.ti,ab,kf. or thymoleptic.ti,ab,kf. or dopamine agonist.ti,ab,kf. or dopamine agonists.ti,ab,kf. or dopamine receptor agonist.ti,ab,kf. or dopamine receptor stimulating agent.ti,ab,kf. or dopamine receptor stimulator.ti,ab,kf. or dopaminergics.ti,ab,kf. or antipsychotics.ti,ab,kf. or butyrophenone tranquilizer*.ti,ab,kf. or classical antipsychotic*.ti,ab,kf. or major tranquilizer*.ti,ab,kf. or major tranquillizer*.ti,ab,kf. or neuroleptic.ti,ab,kf. or neuroleptics.ti,ab,kf. or phenothiazine tranquilizers.ti,ab,kf. or typical antipsychotic*.ti,ab,kf. or anticonvulsant*.ti,ab,kf. or anti convulsant*.ti,ab,kf. or anticonvulsivum.ti,ab,kf. or antiepileptic barbiturate*.ti,ab,kf. or ((anti epilepti* or antiepilepti* or anticonvulsi* or anti convulsi* or antipsychotic* or anti depress* or antidepress* or neurothylmoleptic or dopamin*) adj3 (agent* or drug*)).ti,ab,kf. or adrenergic beta antagonists.ti,ab,kf. or beta adrenergic antagonist.ti,ab,kf. or beta adrenolytic.ti,ab,kf. or beta antiadrenergic agent.ti,ab,kf. or beta sympathicolytic*.ti,ab,kf. or betasympathicolytic*.ti,ab,kf. or (beta adj3 (block* or antagonist*)).ti,ab,kf. or amphetamin*.ti,ab,kf. or amantadin*.ti,ab,kf. or methyophenidate.ti,ab,kf. or concerta.ti,ab,kf. or ritalin.ti,ab,kf. or equasim.ti,ab,kf. or olanzapin*.ti,ab,kf. or sertralin*.ti,ab,kf. or propranolol.ti,ab,kf. or valproic acid.ti,ab,kf. or oxazepam.ti,ab,kf. or lorazepam.ti,ab,kf. or midazolam.ti,ab,kf. or esketamine.ti,ab,kf. or opiate*.ti,ab,kf. or morphine.ti,ab,kf. or fentanyl.ti,ab,kf. or sufentanil.ti,ab,kf. or remifentanil.ti,ab,kf. or alfentanil.ti,ab,kf. or phenoperidine.ti,ab,kf. or haloperidol.ti,ab,kf. or droperidol.ti,ab,kf. |
|
2 |
exp Aggression/ or Psychomotor Agitation/ or exp Anger/ or "Disruptive, Impulse Control, and Conduct Disorders"/ or exp Impulsive Behavior/ or exp Violence/ or agitati*.ti,ab,kf. or restlessness.ti,ab,kf. or impulse control disorder*.ti,ab,kf. or dangerous behavior.ti,ab,kf. or dangerous behaviour.ti,ab,kf. or violen*.ti,ab,kf. or anger.ti,ab,kf. or tantrum.ti,ab,kf. or aggression.ti,ab,kf. or impulsiv*.ti,ab,kf. or negativism.ti,ab,kf. or irritab*.ti,ab,kf. or hostil*.ti,ab,kf. or violen*.ti,ab,kf. or rage.ti,ab,kf. or ((combative or destructive or explosive or withdrawal or argument*) adj2 behavio*).ti,ab,kf. or escalating temper.ti,ab,kf. or episodic discontrol.ti,ab,kf. or verbally abusiv*.ti,ab,kf. or assaultive patien*.ti,ab,kf. or disinhibition.ti,ab,kf. or catastrophic reaction*.ti,ab,kf. or ((affective or emotional or mental or mood or psychic or psychologic*) adj3 (instab* or labil*)).ti,ab,kf. or ((combative or destructive or aggress* or withdraw* or assault*) adj2 (behavior or behaviour)).ti,ab,kf. or verbally abus*.ti,ab,kf. or disinhibiti*.ti,ab,kf. |
|
1 |
exp Craniocerebral Trauma/ or exp Brain Injuries/ or exp Brain Neoplasms/ or exp Encephalitis/ or exp Hypoxia, Brain/ or exp Cerebrovascular Disorders/ or meningeal inflammation.ti,ab,kf. or meningitis.ti,ab,kf. or perimeningeal infections.ti,ab,kf. or brain inflammation.ti,ab,kf. or cerebritis.ti,ab,kf. or encephalitis.ti,ab,kf. or enkephalitis.ti,ab,kf. or brain commotion.ti,ab,kf. or brain concussion.ti,ab,kf. or cerebral concussion.ti,ab,kf. or brain contusion.ti,ab,kf. or cerebral contusion.ti,ab,kf. or commotio cerebri.ti,ab,kf. or ((brain or cerebr* or intracranial or left hemisphere or right hemisphere or craniocerebr*) adj3 (injur* or accident* or anoxaemi* or anoxemi* or anoxi* or hypoxi* or asphyx* or cancer* or neoplasm* or carcinom* or tumor* or tumour* or angiopath* or vascular disease* or vasculopath* or small vessel disease* or vascular disorder* or vascular disturbance* or vascular lesion* or vascular damage* or vascular syndrome*)).ti,ab,kf. or ((injur* or posttrauma* or trauma*) adj3 coma).ti,ab,kf. |