Opheffen van beschermende maatregelen
Uitgangsvraag
Wanneer kunnen beschermende maatregelen van patiënten en medewerkers worden opgeheven?
Aanbeveling
Aanbevelingen patiënten (zie ook figuur 5.1)
Bewezen MRSA-dragerschap (risicocategorie 1)
- Verlaag MRSA-risicocategorie 1 naar risicocategorie 3 als:
- Minimaal drie opeenvolgende MRSA-testen (sets)* negatief zijn met tussenpozen van minimaal zeven dagen;
én - De patiënt tijdens en minstens 48 uur voorafgaand aan de afname van materiaal voor de MRSA-test* geen antibiotica gebruikte, waarvoor de desbetreffende MRSA-stam gevoelig is zoals vermeld in het antibiogram. Controlekweken kunnen wel worden afgenomen onder gebruik van betalactam-antibiotica, waartegen MRSA-resistent is.
- Minimaal drie opeenvolgende MRSA-testen (sets)* negatief zijn met tussenpozen van minimaal zeven dagen;
- Verklaar de patiënt MRSA-vrij en verwijder risicocategorie 3 uit het patiëntdossier als:
- Minimaal drie opeenvolgende MRSA-testen (sets)* negatief zijn met tussenpozen van minimaal zeven dagen; de MRSA-test* negatief is afgenomen op twee maanden en minimaal één jaar na de eerste MRSA-test*;
én - De patiënt tijdens en minstens 48 uur voorafgaand aan de afname van materiaal voor de MRSA-test* geen antibiotica gebruikte, waarvoor de desbetreffende MRSA-stam gevoelig is zoals vermeld bij het antibiogram. Controlekweken kunnen wel worden afgenomen onder gebruik van betalactam-antibiotica, waartegen MRSA resistent is.
- Minimaal drie opeenvolgende MRSA-testen (sets)* negatief zijn met tussenpozen van minimaal zeven dagen; de MRSA-test* negatief is afgenomen op twee maanden en minimaal één jaar na de eerste MRSA-test*;
Hoog risico op MRSA-dragerschap (risicocategorie 2)
- De voorgeschreven maatregelen kunnen worden beëindigd als de inventarisatiekweken negatief zijn, of als de MRSA-PCR-sneltest van tenminste de neus en één andere locatie negatief zijn.
- Bij persisterend risico blijft de patiënt risicocategorie 3 en zijn de uitslagen geldig gedurende maximaal drie maanden en is het afnemen van een nieuwe MRSA-test binnen deze drie maanden* niet noodzakelijk.
- Na drie maanden (of eerder als dat regionaal zo is afgestemd) valt de patiënt weer in risicocategorie 2 en is het afnemen van nieuwe screeningskweken noodzakelijk.
- Voor een eenduidig beleid naar patiënten is het gewenst om bij een persisterend risico de duur van de geldigheid van een negatieve MRSA-negatieve kweekset af te stemmen binnen de ABR-zorgregio.
Aanbevelingen medewerkers (zie ook figuur 5.1)
- Verklaar de medewerker MRSA-vrij als:
- Minimaal drie opeenvolgende MRSA-testen (sets)* negatief zijn met tussenpozen van minimaal zeven dagen; de MRSA-test* negatief is afgenomen op twee maanden en minimaal één jaar na de eerste MRSA-test*;
én - De medewerker tijdens en minstens 48 uur voorafgaand aan de afname van materiaal voor de MRSA-test* geen antibiotica gebruikte waarvoor de desbetreffende MRSA-stam gevoelig is, zoals vermeld bij het antibiogram. Controlekweken kunnen wel worden afgenomen onder gebruik van betalactam-antibiotica, waartegen MRSA resistent is.
- Minimaal drie opeenvolgende MRSA-testen (sets)* negatief zijn met tussenpozen van minimaal zeven dagen; de MRSA-test* negatief is afgenomen op twee maanden en minimaal één jaar na de eerste MRSA-test*;
- Sta MRSA-dragers toe, na een initieel werkverbod tot de uitslag van de typering bekend is (en na start van dragerschapsbehandeling), om in de directe patiëntenzorg te werken onder de volgende voorwaarden en in overleg met de bedrijfsarts, arts-microbioloog en/of deskundige infectiepreventie:
- De medewerker ondergaat op indicatie (bij afwezigheid van contra-indicaties zoals uitgebreide huidlaesies of persisterende blootstelling) een MRSA-dragerschapsbehandeling.
- De medewerker heeft geen huidafwijkingen, zoals bijvoorbeeld (chronisch/opvlammend) eczeem en/of chronische wonden.
- De medewerker meldt zich bij de bedrijfsarts als er huidafwijkingen ontstaan.
- De medewerker is geen drager van een epidemische stam en/of stam die PVL-positief is.
- De medewerker committeert zich aan bron- en contactonderzoek.
* Voor de afname van kweekmaterialen en het uitvoeren van MRSA-testen verwijst de werkgroep naar de richtlijn Laboratoriumdetectie bijzonder resistente micro-organismen (BRMO).
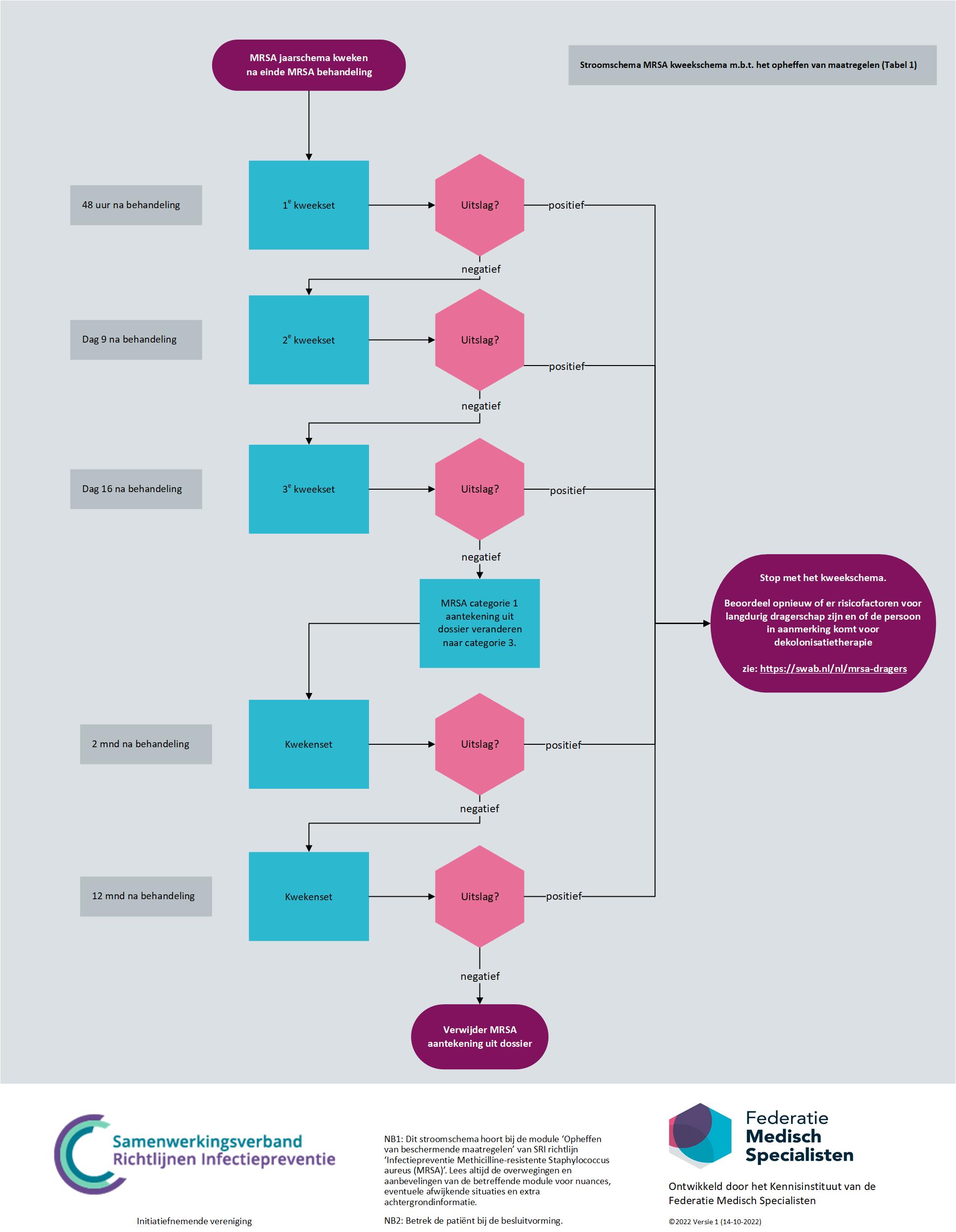
Figuur 5.1: MRSA-kweekschema over het opheffen van maatregelen.
Overwegingen
Zoals beschreven in module Achtergrond en epidemiologie van deze richtlijn wordt er in Nederland voor MRSA een actief ‘search en destroy’ beleid gevolgd. Dit houdt in dat er bij opname in een zorginstelling actief naar MRSA gezocht wordt. Patiënten of medewerkers die mogelijk MRSA bij zich dragen worden op basis van het risico op dragerschap van MRSA ingedeeld in risicocategorieën (zie module Risicocategoriëen). Afhankelijk van deze risicocategorieën worden er ook beschermende maatregelen genomen. Het opheffen van deze maatregelen gebeurt conform een aantal vaste afspraken en dit beleid is succesvol gebleken (Wertheim, 2004; Vos, 2005; Vos, 2009; van Rijen, 2009; Ammerlaan, 2011, Nethmap 2021, Maan, 2021).
Negatieve MRSA-testen
Voor de afname van kweekmaterialen en het uitvoeren van MRSA-testen verwijst de werkgroep naar de richtlijn Laboratoriumdetectie bijzonder resistente micro-organismen. Afhankelijk van het soort antibiotica dat een persoon gebruikt, kan het zo zijn dat de MRSA niet opgepikt wordt in de detectiemethoden als MRSA voor die betreffende antibiotica wel gevoelig is. Als gevolg hiervan zou een patiënt ten onrechte als MRSA-negatief kunnen worden beschouwd. Om een fout-negatieve MRSA-test te voorkomen dient een persoon daarom geen antibiotica gebruiken waarvoor MRSA gevoelig zou zijn tijdens en minstens 48 uur voorafgaand aan de afname van materiaal voor de MRSA-test.
Personen met risico op MRSA-dragerschap
In geval van een hoog risico op MRSA-dragerschap, risicocategorie 2 (zie module Risicocategoriëen ) kunnen de voorgeschreven maatregelen ten aanzien van MRSA worden beëindigd als de kweken negatief blijken te zijn of als de MRSA-PCR-sneltest van tenminste de neus en één andere locatie negatief blijken te zijn (uiteraard zonder positieve resultaten van de sneltest van andere materialen) (Kluytmans-van den Bergh 2013). Voor personen met persisterend hoog risico op MRSA-dragerschap geldt dat een negatieve kweekset een beperkte geldigheidsduur heeft. Het is niet bekend hoe lang een negatieve MRSA-kweekset als geldig kan worden beschouwd. Naar het oordeel van de werkgroep in ieder geval niet langer dan drie maanden. Gedurende deze drie maanden hoeven maatregelen niet te worden genomen. Daarna is een nieuwe negatieve kweekset vereist. Ten behoeve van een eenduidig beleid naar patiënten is het gewenst om de duur van de geldigheid van een negatieve MRSA-negatieve kweekset af te stemmen binnen de ABR-zorgregio. Zie voor groepen met een persisterend verhoogd risico (zie module Risicocategoriëen).
Personen met bewezen MRSA-dragerschap
Als onderdeel van het search en destroy beleid wordt het effect van de dragerschapsbehandeling (eradicatie) bij patiënten met MRSA-dragerschap gecontroleerd door het afnemen van controlekweken. Als gevolg van behandeling bestaat er echter een kans op het terugdringen van MRSA tot onder de detectiegrens, zonder dat er sprake is van volledige eradicatie, zodat na verloop van tijd de MRSA weer kan uitgroeien. Om de kans op een fout-negatieve controlekweek en/of sampling error te verkleinen dienen er na de dragerschapsbehandeling minimaal drie sets kweken te worden afgenomen met een tussenpoos van zeven dagen voor de beschermende maatregelen opgeheven worden. Ter controle volgt nog een set kweken na twee maanden en een set kweken na twaalf maanden. In principe kan na twaalf maanden het label verwijderd worden. Er kunnen echter redenen zijn om bij patiënten met risicofactoren voor langdurig dragerschap het label langer te handhaven.
Om een fout-negatieve-MRSA-test te voorkomen, dient de persoon tijdens en minstens 48 uur voorafgaand aan de afname van materiaal voor de MRSA-tests geen antibiotica te gebruiken waarvoor de desbetreffende MRSA-stam gevoelig is. Zie figuur 5.1.
voor een kweekschema met betrekking tot het opheffen van maatregelen. Voor bekend MRSA-positieve personen zonder risicofactoren voor langdurig dragerschap die langere tijd (langer dan een jaar) uit beeld zijn geweest kan afhankelijk van de omstandigheden gekozen worden om ook dit schema te volgen of in overleg met de deskundige infectiepreventie en/of arts-microbioloog maatwerk te leveren met een ingekort schema.
Medewerkers
Voor medewerkers zonder huidafwijkingen die in een contactonderzoek MRSA-positief testen is een werkverbod in de patiëntenzorg tenminste van toepassing tot de uitslag van typering bekend is, mits direct gestart wordt met MRSA-dekolonisatie therapie. Medewerkers met een huidafwijking ondergaan eerst een behandeling voor de huidafwijking door de bedrijfsarts en starten daarna met dekolonisatietherapie. Dit is doorgaans in overleg met arts-microbioloog (zie SWAB-richtlijn Behandeling MRSA-dragers).
Het werkverbod blijft opgeheven tenzij er sprake is van een van onderstaande kenmerken:
- huidafwijkingen zoals (chronisch/opvlammend) eczeem en/of chronische wonden en/of
- een epidemische of PVL-positieve MRSA-stam is aannemelijk op basis van klinisch epidemiologische informatie en/of
- medewerker is bewezen onderdeel van een MRSA-cluster in de zorg.
In dat geval is er opnieuw sprake van een patiëntgebonden werkverbod dat pas wordt opgeheven als na beëindiging van een dragerschapsbehandeling drie opeenvolgende MRSA-sets met een tussenpoos van minimaal zeven dagen negatief zijn, tenzij de besmettingskans tot zeer gering kan worden teruggebracht, aangezien voldaan wordt aan de hieronder beschreven voorwaarden. Echter, als er sprake is van ongecompliceerd dragerschap en de MRSA-inventarisatiekweken die afgenomen zijn direct voorafgaand aan start van de behandeling uiteindelijk negatief blijken te zijn, dan mag het werkverbod opgeheven worden zodra deze uitslag bekend is. Er kan sprake zijn van een tijdelijke besmetting met MRSA die meestal de volgende dag verdwenen is. Het blijft echter noodzakelijk om driemaal negatief te testen op MRSA na beëindiging van de dragerschapsbehandeling (die wel moet worden uitgevoerd en afgemaakt). Dit geldt ook bij ongecompliceerd dragerschap. Na minimaal twee en twaalf maanden na het opheffen van het patiëntgebonden werkverbod wordt de medewerker opnieuw getest op de aanwezigheid van MRSA.
Het komt echter voor dat MRSA-dekolonisatietherapie bij MRSA-positieve medewerkers, soms na diverse pogingen, niet succesvol is waardoor zij langdurig niet inzetbaar zijn in de directe patiëntenzorg. Het is uiteindelijk aan de zorginstelling om te besluiten of een chronische MRSA-drager onder voorwaarden werkzaam kan blijven in de directe patiëntenzorg, waarbij een afweging gemaakt dient te worden tussen patiëntveiligheid en personeelsbeleid. Bij deze afweging kunnen de volgende argumenten worden meegenomen.
- De besmettingskans kan onder de volgende voorwaarden tot zeer gering worden teruggebracht:
- De medewerker ondergaat op indicatie (bij afwezigheid van contra-indicaties zoals uitgebreide huidlaesies of persisterende blootstelling) een MRSA-dragerschapsbehandeling.
- De medewerker heeft geen huidafwijkingen zoals bijvoorbeeld (chronisch/opvlammend) eczeem en/of chronische wonden.
- De medewerker meldt het bij de bedrijfsarts indien er huidafwijkingen ontstaan.
- De medewerker is geen drager van een epidemische stam en/of stam die PVL-positief is.
- De medewerker committeert zich aan bron- en contactonderzoek.
- Het belang van behoud van personeel dat niet gemist kan worden binnen de directe patiëntenzorg.
- Vergroten van het draagvlak voor het MRSA-beleid, waaronder deelname aan bron en contactonderzoek, onder medewerkers
Hier kan maatwerk worden toegepast in overleg met de bedrijfsarts, arts-microbioloog en/of internist-infectioloog en/of deskundige infectiepreventie.
De prevalentie van MRSA onder de bevolking bedraagt 0.03-0.17% (Weterings, 2019). Dat suggereert dat ook van de zorgverleners een klein deel gekoloniseerd kan zijn met MRSA zonder dat het bekend is en zonder dat gerichte maatregelen genomen worden om transmissie te voorkomen. Dat aantal onbekend MRSA-positieve medewerkers zal waarschijnlijk hoger zijn dan het aantal medewerkers dat ondanks diverse dekolonisatie pogingen MRSA-positief blijft en derhalve een groter risico vormen voor transmissie van MRSA dan de bekend MRSA-positieve medewerkers bij wie een vinger aan de pols gehouden wordt zodat een inschatting van het risico op transmissie kan worden gemaakt. Vanuit principe van proportionaliteit is het niet passend om de zorgverleners met persisterend MRSA-dragerschap per definitie de toegang tot patiëntgebonden zorg te ontzeggen. Maatwerk zoals beschreven is geboden naar de mening van de werkgroep.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers) en medewerkers
Isolatiemaatregelen hebben veel impact op de patiënt en zorgmedewerkers, met name in geval van veel opnames en/of invasieve onderzoeken. Daarnaast kunnen isolatiemaatregelen als stigmatiserend worden ervaren. Het is belangrijk om het draagvlak voor het MRSA-beleid te behouden en de drempel voor medewerkers te verlagen om zich te committeren aan bron- en contactonderzoek. De in deze richtlijn beschreven maatregelen dienen de bescherming en veiligheid van de medepatiënten.
Kosten (middelenbeslag)
Vanwege het actieve zoeken naar MRSA via het screeningsbeleid, en het gematigd toepassen van antibiotica komt MRSA in Nederland weinig voor, vergeleken met andere landen (zie module Achtergrond en epidemiologie). De belasting van de maatregelen uit het nationaal beleid wegen op tegen de beoogde risicoreductie. Het 'search and destroy' beleid blijkt kosteneffectief en draagt bij aan een afname in sterfte door MRSA-infectie (Souverein 2016).
Aanvaardbaarheid, haalbaarheid en implementatie
Het huidige 'search and destroy' beleid wordt al jaren succesvol uitgevoerd en blijkt kosteneffectief. De werkgroep verwacht daarom geen problemen met betrekking tot de aanvaardbaarheid, haalbaarheid en implementeerbaarheid van de aanbevelingen.
Onderbouwing
Achtergrond
Doel van deze module is het beschrijven wanneer beschermende maatregelen met betrekking tot MRSA bij patiënten en medewerkers kunnen worden opgeheven.
Zoeken en selecteren
The WIP-guidelines ’Meticilline-resistente Staphylococcus aureus (MRSA)’, relevant international guidelines and relevant scientific articles were examined in order to answer the clinical question. No systematic literature analysis was performed for this clinical question because the nature of this question does not lend itself well to be an answer by means of a systematic review of original scientific research.
Referenties
- Ammerlaan HS, Kluytmans JA, Berkhout H, Buiting A, de Brauwer EI, van den Broek PJ, van Gelderen P, Leenders SA, Ott A, Richter C, Spanjaard L, Spijkerman IJ, van Tiel FH, Voorn GP, Wulf MW, van Zeijl J, Troelstra A, Bonten MJ; MRSA Eradication Study Group. Eradication of carriage with methicillin-resistant Staphylococcus aureus: effectiveness of a national guideline. J Antimicrob Chemother. 2011 Oct;66(10):2409-17. Doi: 10.1093/jac/dkr243. Epub 2011a Jun 30. PMID: 21719473.
- Kluytmans-van den Bergh MF, Vos MC, Diederen BM, Vandenbroucke-Grauls CM, Voss A, Kluytmans JA; Dutch working group on the laboratory detection of highly resistant microorganisms. Dutch guideline on the laboratory detection of methicillin-resistant Staphylococcus aureus. Eur J Clin Microbiol Infect Dis. 2014 Jan;33(1):89-101. doi: 10.1007/s10096-013-1933-6. Epub 2013 Jul 27. PMID: 23893016.
- Nellums LB, Thompson H, Holmes A, Castro-Sánchez E, Otter JA, Norredam M, Friedland JS, Hargreaves S. Antimicrobial resistance among migrants in Europe: a systematic review and meta-analysis. Lancet Infect Dis. 2018 Jul;18(7):796-811. Doi: 10.1016/S1473-3099(18)30219-6. Epub 2018 May 17. PMID: 29779917; PMCID: PMC6032478.
- NethMap 2021: Consumption of antimicrobial agents and antimicrobial resistance among medically important bacteria in the Netherlands in 2020 / MARAN 2021. Monitoring of Antimicrobial Resistance and Antibiotic Usage in Animals in the Netherlands in 2020.
- Ravensbergen SJ, Berends M, Stienstra Y, Ott A. High prevalence of MRSA and ESBL among asylum seekers in the Netherlands. PloS One. 2017 Apr 25;12(4):e0176481. Doi: 10.1371/journal.pone.0176481. PMID: 28441421; PMCID: PMC5404783.
- Ravensbergen SJ, Louka C, Ott A, Rossen JW, Cornish D, Pournaras S, Bathoorn E, Stienstra Y. Proportion of asylum seekers carrying multi-drug resistant microorganisms is persistently increased after arrival in the Netherlands. Antimicrob Resist Infect Control. 2019 Jan 7;8:6. Doi: 10.1186/s13756-018-0455-5. PMID: 30637100; PMCID: PMC6323800.
- Souverein D, Houtman P, Euser SM, Herpers BL, Kluytmans J, Den Boer JW. Costs and Benefits Associated with the MRSA Search and Destroy Policy in a Hospital in the Region Kennemerland, The Netherlands. PloS One. 2016;11(2):e0148175. Published 2016 Feb 5. Doi:10.1371/journal.pone.0148175.
- van Rijen MM, Bosch T, Heck ME, Kluytmans JA. Meticillin-resistant Staphylococcus aureus epidemiology and transmission in a Dutch hospital. J Hosp Infect. 2009 Aug;72(4):299-306. Doi: 10.1016/j.jhin.2009.05.006. Epub 2009 Jul 10. Erratum in: J Hosp Infect. 2010 Feb;74(2):198. PMID: 19596488.
- Vos MC, Ott A, Verbrugh HA. Successful search-and-destroy policy for methicillin-resistant Staphylococcus aureus in The Netherlands. J Clin Microbiol. 2005 Apr;43(4):2034; author reply 2034-5. Doi: 10.1128/JCM.43.4.2034-2035.2005. PMID: 15815056; PMCID: PMC1081402.
- Vos MC, Behrendt MD, Melles DC, Mollema FP, de Groot W, Parlevliet G, Ott A, Horst-Kreft D, van Belkum A, Verbrugh HA. 5 years of experience implementing a methicillin-resistant Staphylococcus aureus search and destroy policy at the largest university medical center in the Netherlands. Infect Control Hosp Epidemiol. 2009 Oct;30(10):977-84. Doi: 10.1086/605921. PMID: 19712031.
- Wassenberg MW, Hopmans TE, Troelstra A, Kluytmans JA, Bonten MJ. Methicillin-resistant Staphylococcus aureus of livestock origin in Dutch hospitals: high-risk patients need only to be investigated if admitted to hospital. Ned Tijdschr Geneeskd. 2008 Dec 6;152(49):2681-8. Dutch. PMID: 19137969.
- Wertheim HF, Vos MC, Boelens HA, Voss A, Vandenbroucke-Grauls CM, Meester MH, Kluytmans JA, van Keulen PH, Verbrugh HA. Low prevalence of methicillin-resistant Staphylococcus aureus (MRSA) at hospital admission in the Netherlands: the value of search and destroy and restrictive antibiotic use. J Hosp Infect. 2004 Apr;56(4):321-5. Doi: 10.1016/j.jhin.2004.01.026. PMID: 15066745.
- Weterings V, Veenemans J, van Rijen M, Kluytmans J. Prevalence of nasal carriage of methicillin-resistant Staphylococcus aureus in patients at hospital admission in The Netherlands, 2010-2017: an observational study. Clin Microbiol Infect. 2019 Nov;25(11):1428.e1-1428.e5. doi: 10.1016/j.cmi.2019.03.012. Epub 2019 Mar 27. PMID: 30928560.
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 01-07-2025
Beoordeeld op geldigheid : 20-11-2023
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd door het ministerie van VWS. De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met MRSA.
Werkgroep:
- Dr. A.L.M. Vlek (voorzitter), arts-microbioloog, Nederlandse Vereniging voor Medische Microbiologie (NVMM)
- Dr. K.A. Heemstra, arts-microbioloog, Nederlandse Vereniging voor Medische Microbiologie (NVMM)
- Dr. E.M. Mascini, arts-microbioloog, Nederlandse Vereniging voor Medische Microbiologie (NVMM)
- Dr. H. Ammerlaan, internist-infectioloog, Nederlandse Vereniging van Internist-Infectiologen (NIV/NVII)
- Dr. R. Bakx, kinderchirurg, Nederlandse Vereniging voor Heelkunde (NVvH)
- P. Voermans, deskundige infectiepreventie, Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg (VHIG)
- M.B.R. Seijger, deskundige infectiepreventie, Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg (VHIG)
- P. Molenaar, deskundige infectiepreventie, Rijksinstituut voor Volksgezondheid en Milieu (RIVM)
- Drs. G.M.J. Vlasveld, arts verstandelijk gehandicapten, Nederlandse Vereniging Artsen Verstandelijk Gehandicapten (NVAVG)
- Drs. R.J. Naber, bedrijfsarts, Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde (NVAB)
Meelezers:
- Drs. M. Loogman, Huisarts, Nederlands Huisartsen Genootschap (NHG)
Met ondersteuning van:
- Dr. I. van Dusseldorp, literatuurspecialist, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. A.J. Versteeg, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. H. Graveland, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar geen directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Dr. A.L.M. Vlek |
Arts-microbioloog Diakonessenhuis |
Voorzitter stuurgroep ISIS AR |
geen |
Geen actie vereist |
|
Dr. K.A. Heemstra |
Arts-microbioloog Alrijne Zorggroep, MSB Alrijne (laboratorium eigendom van Eurofins clinical diagnostics) |
geen |
geen |
Geen actie vereist |
|
Dr. E. Mascini |
Arts-microbioloog ziekenhuis Rijnstate |
Lid RCT ABR Zorgnetwerk GAIN. |
Geen |
Geen actie vereist |
|
Dr. H. Ammerlaan |
Internist-infectioloog Catharina Ziekenhuis, lid coöperatie MSB |
geen |
geen |
Geen actie vereist |
|
Dr. R. Bakx |
Kinderchirurg, Amsterdam |
CAPP studie, ZonMW behandeling complexe appendicitis. Voorzitter Adviescommissie Richtlijnen FMS, voorzitter Richtlijnencommissie NVvH, Bestuurslid Stichting Spoedeisende Hulp Bij Kinderen, Course Director APLS. |
Geen |
Geen actie vereist |
|
P. Voermans |
Deskundige infectiepreventie |
geen |
geen |
Geen actie vereist |
|
M.B.R. Seijger |
Deskundige infectiepreventie |
Geen |
Geen |
Geen actie vereist |
|
P. Molenaar |
Deskundige infectiepreventie -RIVM- LCI / GGD Amsterdam en ABR zorgnetwerk Noord-Holland |
geen |
geen |
Geen actie vereist |
|
Drs. G.M.J. Vlasveld |
Arts verstandelijk gehandicapten, Amerpoort/Sherpa |
Bestuurslid NVAVG (onbetaald) |
geen |
Geen actie vereist |
|
Drs. R.J. Naber |
Bedrijfsarts, arbodienst Amsterdam UMC |
Secretaris NVAB werkgroep BaZ. Lid NVAB commissie richtlijnontwikkeling en wetenschap. Lid NVAB commissie Intercollegiale toetsing en deskundigheidsbevordering. |
Geen |
Geen actie vereist |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door uitnodigen van Patiëntfederatie Nederland (PFNL) voor de invitational conference. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan PFNL en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Wkkgz & kwalitatieve raming van mogelijke substantiële financiële gevolgen
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er geen substantiële financiële gevolgen zijn. Zie onderstaande tabel.
|
Module |
Uitkomst raming |
Toelichting |
|
Module Opheffen beschermende maatregelen |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er wordt geen toename in voltijdsequivalenten dan wel opleidingsniveau verwacht. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II-instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder ‘Onderbouwing’. Indien mogelijk werden de data uit verschillende studies gepoold in een random-effects-model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie https://www.gradeworkinggroup.org). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt)relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen. (De domeinen voor downgraden zijn: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias. De domeinen voor upgraden zijn: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S,Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 3.0 (2023). Adviescommissie Richtlijnen van de Raad Kwaliteit. https://richtlijnendatabase.nl/werkwijze/richtlijnen_3_0.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin
Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from gdt.gradepro.org/app/handbook/handbook.html