Verwijscriteria voor klinisch genetisch onderzoek bij CRC en genpanelanalyse
Uitgangsvraag
Wat is de rol van genpanelanalyse bij het opsporen van erfelijke vormen van darmkanker (met evt. darmpoliepen), voor verschillende leeftijdsgroepen, met speciale aandacht voor jonge darmkankerpatiënt (onder de 50 jaar)?
De uitgangsvraag omvat de volgende deelvragen:
- Wat is de rol van genpanelanalyse voor de verschillende leeftijdsgroepen, wanneer moeten patiënten met colorectaal carcinoom (CRC) worden verwezen voor genpanelanalyse?
- Wat is de beste samenstelling van het genpanel voor analyse van de diverse CRC-patiëntengroepen?
Aanbeveling
Aanbeveling-1
Verwijs CRC-patiënten jonger dan 40 jaar met een CRC-diagnose standaard door naar de polikliniek Klinische genetica voor erfelijkheidsonderzoek en -advies.
Verwijs CRC- patiënten van ≥40 jaar en < 70 jaar niet standaard naar de polikliniek klinische genetica voor erfelijkheidsonderzoek en advies tenzij:
- Bij MMRd status, zie submodule De detectie van Lynch syndroom middels tumor analyse, zie ook flowchart
- MMRp status en één van de volgende criteria:
- Indien meerdere poliepen en voldaan aan criteria in submodule Verwijscriteria voor klinisch genetisch onderzoek bij adenomateuze polyposis
- 10 of meer adenomen < 60 jaar (cumulatief)
- 20 of meer adenomen <70 jaar (cumulatief
- Indien meerdere poliepen en voldaan aan criteria in submodule Verwijscriteria voor klinisch genetisch onderzoek bij adenomateuze polyposis
- Belaste voorgeschiedenis of familieanamnese verdacht voor een tumor predispositie syndroom
- >1 primaire tumoren bij dezelfde patiënt, waarvan 1 op ongebruikelijk jonge leeftijd; zie tabel 2
- Eerstegraadsfamilieleden met ongebruikelijk jonge kankerdiagnose(s), waarbij deze familieleden niet zelf verwezen kunnen worden;
- Sterke clustering van darmkanker (≥3 eerstegraads <80 jaar of 2 eerstegraads <60 jaar) in de familie)
De criteria zijn algemeen en niet altijd eenduidig. Voor specifieke tumoren zijn verwijscriteria ook te vinden via www.artsengenetica.nl. Bij twijfel of sterke wens van de patiënt kan laagdrempelig met een klinisch geneticus overlegd worden.
N.B. zie voor controle advies voor familieleden FCC submodule Incidentie, risico’s en surveillance bij familiair colorectaal carcinoom
Tabel 2, leeftijden van carcinomen, o.b.v. stoet VKGN en/of incidentie (<100 per jaar) als leidraad voor leeftijd ‘jong’
|
Tumortype |
Leeftijd ‘jong’ bij ≥1 primaire tumor |
|
CRC |
<40 jaar |
|
Endometrium carcinoom |
<50 jaar |
|
Ovarium/tubacarcinoom |
Altijd verwijzen |
|
Pancreascarcinoom |
<50 jaar |
|
Mammacarcinoom |
<40 jaar |
|
Dunne darm carcinoom |
<50 jaar |
|
Maagcarcinoom |
<50 jaar |
|
Urotheelcelcarcinoom hogere urinewegen |
<50 jaar |
|
Urotheelcelcarcinoom blaas |
<40 jaar |
|
Niercelcarcinoom |
<45 jaar |
|
Prostaatcarcinoom |
<50 jaar |
|
Melanoom |
<30 jaar |
NB: dit is niet evidence-based voor de meeste tumoren, eigen beoordeling in combinatie met histologie en familieanamnese blijven van belang.
Aanbeveling-2
Verricht gen panel-analyse bij CRC-patiënten, die in aanmerking komen voor genetische diagnostiek, met behulp van de volgende gen-panels (zie ook Tabel 1):
- Screen darmkankerpatiënten met verdenking op Lynch syndroom volgens onderstaande flowchart met het Lynch syndroom panel: MLH1, MSH2, MSH6, PMS2, EPCAM.
- Screen darmkankerpatiënten met adenomateuze polyposis (>10 adenomen < 60 jaar of > 20 adenomen < 70 jaar) tenminste op de volgende adenomateuze polyposis genen: APC, MUTYH, AXIN2, MLH3, MSH3, MBD4, NTHL1, POLE, POLD1. (Zie evt. ook submodule Genetische testen bij adenomateuze polyposis)
Screen darmkanker patiënten met hamartomateuze poliepen op de genen die geassocieerd zijn met dit type poliepen: PTEN, STK11, SMAD4, BMPR1A (zie evt. ook submodule Genetische testen bij adenomateuze polyposis)
- Genpanels kunnen in de praktijk ook worden gecombineerd
- Indien er een persoonlijke en/of een (familiaire) belasting voor overige tumoren is kan DNA-onderzoek worden aangevuld met andere tumorpredispositie genen zoals aangegeven in Tabel 1. Gebruik hiervoor de consensus gebaseerde criteria voor diagnostiek van de VKGN/StOET (zie www.artsengenetica.nl).
Tabel 1: Aanbevolen genen per patiëntencategorie
|
Indicatie/ aandoening:
|
Core genen |
|
(1) Lynch syndroom |
MLH1, MSH2, MSH6, PMS2, EPCAM (3’ deel) |
|
(2) Adenomateuze polyposis |
APC, MUTYH, AXIN2, MLH3, MSH3, MBD4, NTHL1, POLE, POLD1 (zie ook submodule Genetische testen bij adenomateuze polyposis) |
|
(3) Hamartomateuze polyposis |
BMPR1A, PTEN, SMAD4, STK11 (zie ook submodule Genetische testen bij adenomateuze polyposis) |
|
(4) CRC breed |
Genen geassocieerd met Lynch syndroom + adenomateuze polyposis + hamartomateuze polyposis + serrated polyposis (RNF43) + GREM1 duplicatie + eventueel RPS20/ MCM8/ MCM9 (zie ook submodule Genetische testen bij adenomateuze polyposis) |
|
(5) CRC breed+ aanvullende tumor predispositie genen* |
Het CRC-brede panel + Niet-CRC gerelateerde genen, afhankelijk van de vraagstelling. # met name HBOC-gerelateerd (BRCA1, BRCA2, PALB2, CHEK2, ATM, BRIP1, RAD51C, RAD51D), TP53 en/of CDKN2A |
* WES of WGS-panel erfelijke kanker kan overwogen worden.
# De diagnose ‘erfelijke darmkanker’ is bij het vinden van een pathogene variant in een van deze genen echter NIET bevestigd, er kunnen nog andere genetische factoren een rol spelen; zie tabel 1: genpanelanalyse in verschillende leeftijdsgroepen.
Zie voor een toelichting van de polyposis-geassocieerde genen ook het desbetreffende Module over polyposis (submodule 1.4) **
In de praktijk kan gekozen worden voor losse panels of een groot CRC/polyposis panel
Overwegingen
Balans tussen gewenste en ongewenste effecten
Doorverwijzing van patiënt en van verschillende leeftijdsgroepen voor genpanelanalyse
Door de jaren heen zijn verschillende klinische testcriteria ontwikkeld, zoals de Amsterdam (I en II) criteria en de (gereviseerde) Bethesda criteria. De Amsterdam II-criteria hebben een hoge specificiteit (98%), maar een lage sensitiviteit (27-42%). De gereviseerde Bethesda-criteria (Umar, 2004) zijn breder toepasbaar, met een lagere specificiteit (77-93%), maar een hogere sensitiviteit (82-95%), vergeleken met de Amsterdam-criteria. De rationale achter de Bethesda criteria stammen uit een tijd waar de technische mogelijkheden voor tumordiagnostiek beperkt waren, en de toegang tot deze diagnostiek nog niet gestroomlijnd was. Hierdoor is de huidige diagnostische waarde van de Bethesda criteria in Nederland beperkt. Inmiddels wordt in veel Westerse landen aanbevolen om alle CRC-patiënten onder de 70 jaar te testen, zoals in Nederland, of onafhankelijk van leeftijd (EHTG/ESCP) (Seppälä, 2021). Zie hiervoor submodule De detectie van Lynch syndroom middels tumor analyse met betrekking tot wanneer IHC MMR te verrichten.
Leeftijd en prevalentie van Lynch syndroom
De literatuur bijeengenomen blijkt dat Lynch syndroom wordt vastgesteld bij ongeveer 13% van de CRC-patiënten (waarin nog geen IHC MMR analyse gedaan is) jonger dan 40 jaar, dalend naar 6% in de groep van 40-49 jaar en 3-4% tussen 50-70 jaar. Bij patiënten ouder dan 70 jaar daalt de prevalentie verder naar 1,6% en bij patiënten ouder dan 80 jaar is dit nog slechts 0,7%. Een Nederlandse studie toont aan dat in de groep van 65-70 jarigen de incidentie van nieuwe Lynch syndroom patiënten slechts 0.7% was (Vos, 2020).
Vanwege de dalende detectieratio met toenemende leeftijd wordt standaard MMR-diagnostiek boven de 70 jaar niet aanbevolen, zie submodule De detectie van Lynch syndroom middels tumor analyse. Bij patiënten boven de 70 jaar kan er echter aanleiding zijn voor verwijzing naar de klinische genetica, bijvoorbeeld bij een geïsoleerd verlies van MSH6 of PMS2 kleuring of een belaste familieanamnese of een voorgeschiedenis met Lynch-geassocieerde carcinomen, zie submodule De detectie van Lynch syndroom middels tumor analyse.
Betrouwbaarheid en beperkingen van IHC MMR-analyse
Hoewel IHC MMR in de meeste gevallen betrouwbaar is, zijn er uitzonderingen waarbij eiwitexpressie behouden blijft ondanks MMR-deficiëntie, bijvoorbeeld door missense-varianten. Tot maximaal 6% van de MMRd CRC-patiënten (met somatisch pathogene varianten in een van de MMR genen of een MSI status) vertoont intacte MMR-kleuring (Bou Farhat, 2024; Hechtman, 2020), maar waarschijnlijk is dit een overschatting (Singh 2020). Daarnaast kan verlies van MLH1-expressie veroorzaakt worden door MLH1-promoter methylatie (PM) (meestal sporadisch bij oudere patiënten). Constitutionele MLH1-PM is zeldzaam en komt voornamelijk voor bij jongere patiënten (<55 jaar) (Hitchins, 2023). Daarom wordt kiembaanonderzoek van de MMR genen alsook onderzoek naar constitutionele MLH1-PM aanbevolen bij CRC-patiënten jonger dan 50 jaar met MLH1-PM of een belaste familieanamnese. Zie ook submodule De detectie van Lynch syndroom middels tumor analyse met betrekking tot IHC MMR analyse.
Rol van voorspellende modellen voor Lynch syndroom
Wanneer IHC MMR niet mogelijk is, kan het PREMM5-model worden gebruikt om het risico op Lynch syndroom in te schatten (Kastrinos, 2017). Bij een score van ≥2,5% kan aanvullend DNA-onderzoek worden overwogen, zoals aanbevolen in de NCCN-richtlijnen 2024 (Hodan, 2024). In Nederland is IHC MMR analyse echter bijna altijd mogelijk.
CMMRD-syndroom
Bi-allelische kiembaan MMR gen PV, zogenaamde Congenitaal MMR Deficiëntie Syndroom (CMMRDS) wordt incidenteel gezien bij patiënten met relatief jong CRC en multipele adenomen (Will, 2007; Herkert, 2011). Doorgaans is er dan ook sprake van pigmentafwijkingen en een verhoogd risico op andere tumoren zoals lymforeticulaire maligniteiten, hersentumoren en sarcomen.
Andere erfelijke aanlegfactoren voor CRC
Naast Lynch Syndroom worden de meeste PVs gevonden in APC en MUTYH, welke respectievelijk (Atypische) Familiaire Adenomateuze Polyposis (A)FAP of MUTYH-geassocieerde Polyposis (MAP) veroorzaken. Bij PV in adenomateuze polyposis genen, zijn doorgaans naast CRC multipele (>20) adenomateuze darmpoliepen aanwezig (zie ook: submodule Verwijscriteria voor klinisch genetisch onderzoek bij adenomateuze polyposis).
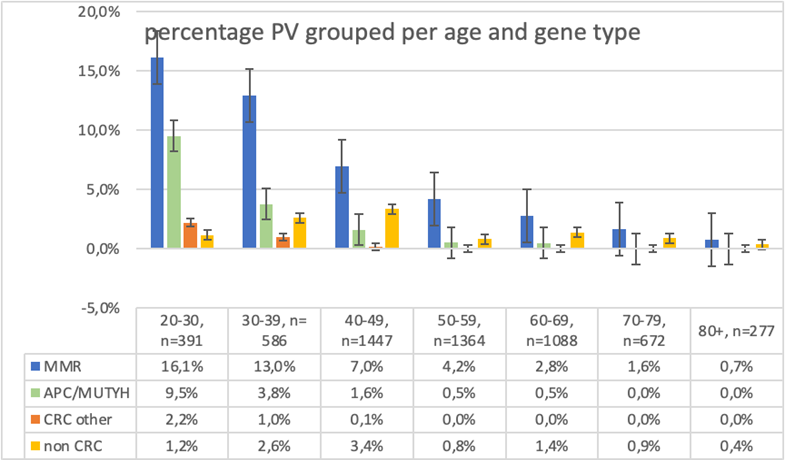
Voor APC- of biallelische MUTYH-mutaties is de opbrengst bij CRC-patiënten, waarbij niet is geselecteerd op poliepen: voor CRC-patiënten jonger dan 30 jaar 10%, 4% tussen 30-40 jaar, 1,5% tussen 40-50 jaar en 0,5% tussen 50-60 jaar (Figuur 1 (submodule Verwijscriteria voor klinisch genetisch onderzoek bij CRC en genpanelanalyse)). Bij CRC-patiënten (zonder poliepen) ouder dan 50 jaar wordt deze genetische aanleg nauwelijks gevonden.
Overige adenomateuze polyposis-genen omvatten onder andere NTHL1, MSH3, MLH3 en MBD4, die geassocieerd zijn met zeldzame autosomaal recessieve polyposissyndromen. Daarnaast spelen pathogene varianten in het exonuclease domein van POLE en POLD1 een rol bij een verhoogd risico op colorectale kanker; deze genen zijn betrokken bij de nauwkeurige replicatie en foutcorrectie van DNA, waardoor de tumoren een hypermutabel fenotype vertonen. AXIN2 is geassocieerd met een erfelijk oligodontie-polyposissyndroom, gekenmerkt door de verstoorde ontwikkeling of het ontbreken van tanden, colorectale (adenomateuze) polyposis en een verhoogd risico op darmkanker. Pathogene varianten in overige CRC-gerelateerde predispositiegenen omvatten ook hamartomateuze polyposis syndromen, zoals SMAD4 en BMPR1A (juveniele polyposis) en STK11 (Peutz-Jeghers-syndroom).
Pathogene varianten in niet-CRC-gerelateerde genen, zoals BRCA1/2, ATM en PALB2, worden infrequent gevonden, vooral bij patiënten tussen 30-49 jaar. In totaal worden er in de cohorten bij zo’n 1,5% (83/5707) PVs gevonden, waarvan het vaakst in BRCA1 of BRCA2 42% (n=35/83), ATM (15/83) en PALB2 (9/83). Dit rechtvaardigt het overwegen van BRCA1/2 en/of HBOC-analyse bij een belaste familieanamnese voor borstkanker, maar de algehele opbrengst is te laag om standaard deze genen in CRC panel-analyses op te nemen. Pearlman beschrijft dat er bij ongeveer 67% (4/6 patiënten met PV BRCA1/2) sprake was van een positieve familie anamnese voor borstkanker (Pearlman, 2017). Dus alleen indien er een persoonlijke en/of een familiaire belasting voor overige tumoren is, kan DNA-onderzoek worden aangevuld met andere tumorpredispositie genen zoals aangegeven in Tabel 1. Gebruik hiervoor de consensus gebaseerde criteria voor diagnostiek van de VKGN/StOET (zie: www.artsengenetica.nl).
De kans op het vinden van een predispositie voor CRC
De kans op het vinden van een erfelijke aanleg voor CRC hangt onder andere af van de leeftijd van diagnose. Figuur 1 (submodule Verwijscriteria voor klinisch genetisch onderzoek bij CRC en genpanelanalyse) geeft een overzicht van de resultaten van DNA-panel analyses uit studies, voornamelijk uitgevoerd in de VS en Europa, bij CRC-patiënten in zowel klinische als populatie-gebaseerde cohorten (Pearlman, 2017; Pearlman, 2021; Terlouw, 2020 PMID 31527860; Mikaeel, 2022; Yurgelun, 2017; Jiang, 2022; Uson 2022; Cercek 2021). Selectiebias in deze studies kan de opbrengst van panel analyses overschatten. In de afgelopen tien jaar zijn meerdere studies uitgevoerd, gericht op verschillende leeftijdsgroepen en aanwezigheid van kiembaan pathogene varianten (PVs) in CRC-, polyposis- en andere predispositie-genen. Ze tonen aan dat veel patiënten met een erfelijke aanleg niet voldoen aan eerder gestelde criteria voor genetisch onderzoek, zoals de Bethesda-criteria voor Lynch syndroom of de polyposiscriteria voor APC en MUTYH. Hoewel grote aantallen patiënten werden getest, zijn er grote verschillen in de opzet van de onderzoeken waardoor het moeilijk is om ze één op één te vergelijken: i) de definitie van CRC op jonge leeftijd varieert van ≤35 tot ≤55 jaar oud, en sommige onderzoeken omvatten patiënten van alle leeftijden; ii) niet in alle studies werden systematisch tumortesten (MSI en/of IHC van de MMR-eiwitten) uitgevoerd; iii) het aantal genen op gebruikte multigenenpanels varieerde van 10 tot 1138 genen; en iv) de beschrijving van het fenotype en de exacte leeftijd van patiënten die drager waren van een pathogene variant was niet altijd beschikbaar. Desalniettemin omvatten deze studies samen meer dan 6.000 patiënten met CRC (op jonge leeftijd). Er is een indeling gemaakt in leeftijdsgroepen en de opbrengst van PV in de MMR-genen, polyposis/CRC genen en andere kanker predispositie genen (non-CRC genen).
Figuur 1 (submodule Verwijscriteria voor klinisch genetisch onderzoek bij CRC en genpanelanalyse): Based on summarized data from DNA panel study in CRC ( Pearlman 2017, Pearlman 2021, Terlouw 2020, Mikaeel 2021, Yurgelun 2017, Jiang 2022 Uson 2022, Cercek 2021) see for more detailed data Table 1a_G (zie bijlage)
De kans op een erfelijke aanleg neemt significant toe bij jongere leeftijd van de patiënten, een belaste familieanamnese voor CRC en/of een voorgeschiedenis met een tweede maligniteit. Daarom zijn deze factoren opgenomen als criteria voor verwijzing naar de Klinische genetica. Op basis van de percentages wordt DNA-onderzoek standaard aanbevolen voor CRC-patiënten jonger dan 40 jaar. Voor patiënten tussen 40 en 60 jaar is dit afhankelijk van de aanwezigheid van poliepen, een belaste familieanamnese of andere tumoren.
Samenstelling genenpanel CRC
Tabel 1: Aanbevolen genen per patiëntencategorie
|
Indicatie/ aandoening:
|
Core genen |
|
(1) Lynch syndroom |
MLH1, MSH2, MSH6, PMS2, EPCAM (3’ deel) |
|
(2) Adenomateuze polyposis |
APC, MUTYH, AXIN2, MLH3, MSH3, MBD4, NTHL1, POLE, POLD1 (zie ook submodule Genetische testen bij adenomateuze polyposis) |
|
(3) Hamartomateuze polyposis |
BMPR1A, PTEN, SMAD4, STK11 (zie ook submodule Genetische testen bij adenomateuze polyposis) |
|
(4) CRC breed |
Genen geassocieerd met Lynch syndroom + adenomateuze polyposis + hamartomateuze polyposis + serrated polyposis (RNF43) + GREM1 duplicatie + eventueel RPS20/ MCM8/ MCM9 (zie ook submodule Genetische testen bij adenomateuze polyposis) |
|
(5) CRC breed+ aanvullende tumor predispositie genen* |
Het CRC-brede panel + Niet-CRC gerelateerde genen, afhankelijk van de vraagstelling. # met name HBOC-gerelateerd (BRCA1, BRCA2, PALB2, CHEK2, ATM, BRIP1, RAD51C, RAD51D), TP53 en/of CDKN2A |
* WES of WGS-panel erfelijke kanker kan overwogen worden.
# De diagnose ‘erfelijke darmkanker’ is bij het vinden van een pathogene variant in een van deze genen echter NIET bevestigd, er kunnen nog andere genetische factoren een rol spelen; zie tabel 1: genpanelanalyse in verschillende leeftijdsgroepen.
Zie voor een toelichting van de polyposis-geassocieerde genen ook het desbetreffende Module over polyposis (submodule 1.4) **
In de praktijk kan gekozen worden voor losse panels of een groot CRC/polyposis panel
Beperkingen van gen panel-analyse
Het gebruik van uitgebreide gen panels brengt het risico met zich mee dat varianten van onbekende klinische significantie (VUS) worden geïdentificeerd, variërend van 29% tot 63%, afhankelijk van de grootte van het genpanel (Yurgelun, 2017; Pearlman, 2021; Jiang, 2022). Dit percentage kan hoger zijn bij patiënten uit bepaalde etnische groepen, wat de interpretatie bemoeilijkt en onzekerheid vergroot (Uson, 2022).
Polygenic risk scores (PRS)
Hoewel PRS mogelijk aanvullende informatie kan bieden bij risicostratificatie, is de klinische bruikbaarheid nog niet aangetoond en blijven verdere validatiestudies noodzakelijk voordat dit in de praktijk ingezet kan worden (Cavestro, 2023).
Rol van tumoronderzoek
Tumortesten kunnen een aanvulling zijn op kiembaantesten en kunnen helpen bij de interpretatie van de resultaten. Bij het vinden van een (waarschijnlijk) pathogene variant in een CRC-geassocieerd gen tijdens tumoranalyse in het kader van een therapeutische vraag, kan gebruikt gemaakt worden van de leidraad voor verwijzing naar de klinische genetica voor kiembaan onderzoek (zie ook: arts en genetica Leidraad voor verwijzing na DNA-diagnostiek in (tumor)weefsel).
Somatische (waarschijnlijk) pathogene varianten in verschillende genen met kiembaanimplicaties komen vaak voor (bijv. TP53, STK11, PTEN, APC), en zal zelden een indicatie zijn van een noodzaak van kiembaanonderzoek, tenzij er klinische/familiekenmerken verdacht voor een pathogene kiembaan variant zijn.
Kwaliteit van bewijs
Er is geen specifieke literatuuranalyse verricht, maar overwegingen zijn gebaseerd op de internationale richtlijnen. Gezien de beschrijvende aard van de studies is er geen GRADE toegepast. De bewijskracht voor doorverwijzing en genpanelanalyse is dan ook niet duidelijk.
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
Gewenste effecten:
Goede verwijscriteria leiden tot optimale detectie van patiënten met een CRC-predispositie met minimale “overbodige” diagnostiek bij patiënten zonder aanleg. Patiënten, die verwezen worden voor erfelijkheidsonderzoek zullen in eerste instantie een informatief gesprek bij de klinisch geneticus krijgen. Zij worden geïnformeerd over de voor- en nadelen van het doen van kiembaan DNA-onderzoek, zodat zij ook zelf een afweging kunnen maken ten aanzien van het verrichten van deze diagnostiek.
Het voordeel van genpanelanalyse is dat dit mogelijk duidelijkheid geeft over een eventueel erfelijke aanleg. Indien een erfelijke aanleg wordt vastgesteld kunnen andere familieleden ook onderzoek laten doen. Het doen van paneldiagnostiek voorkomt dat sequentieel meerdere onderzoeken moeten worden aangevraagd en zorgt voor een doelmatiger diagnostisch proces.
Ongewenste effecten:
Verwijzing voor erfelijkheidsonderzoek naar een CRC-predispositie kan onrust en praktische ongemakken voor de patiënt en/of diens familieleden veroorzaken. Kennis van het hebben van een erfelijke aanleg kan een impact op het psychologische welzijn hebben (Gopie, 2012). Hoewel, een meta-analyse laat zien dat erfelijkheidsonderzoek voor verschillende vormen van kanker geen grote nadelige psychologische gevolgen lijkt te hebben voor patiënten (Yanes, 2019).
Ook moet de kennis van het hebben van een erfelijke aanleg bijvoorbeeld worden gemeld bij het aanvragen van een levensverzekering en arbeidsongeschiktheidsverzekering boven een bepaald bedrag. Het is daarom van belang af te wegen of dit opweegt tegen de kans dat daadwerkelijk een aanleg gevonden wordt en de gezondheidswinst, die hiermee behaald kan worden.
Aangezien een groter panel kan leiden tot de identificatie van variante van onbekende betekenis (variant of unknown significance; VUS), dient goed afgewogen te worden, welk panel in welke situatie het meest doelmatig is.
Kostenaspecten
Het uitvoeren van genpanelanalyses brengt kosten met zich mee, echter het vinden van een erfelijke aanleg kan leiden tot kostenbesparing in de zorg. Screening voor Lynch syndroom en polyposis vormen, zoals voorgesteld in deze richtlijn en door de beroepsvereniging van de Vereniging Klinische Genetica Nederland (VKGN), leidt tot vroege detectie van darmtumoren en andere Lynch geassocieerde tumoren in zowel de betreffende patiënt als mogelijk ook bij familieleden, en dringt daarmee sterfte terug en kan zorgkosten vermijden, die gepaard gaan met kanker in een meer vergevorderd stadium (Kang, 2022; Kastrinos, 2017). De eventuele extra kosten wegen op tegen het verschil in effectiviteit aangezien de aanbevelingen in deze richtlijn niet sterk afwijken ten opzichte van het huidige beleid.
Gelijkheid ((health) equity/equitable)
Het is bekend dat mensen met een lager opleidingsniveau en een taalbarrière minder vaak worden verwezen voor genetisch onderzoek (van der Giessen, 2017; van Riel, 2012). Heldere verwijscriteria, dragen bij aan betere verwijzing, ook van mensen met minder gezondheidsvaardigheden. Definiëring van panels voor specifieke patiëntengroepen, zal de aangeboden diagnostiek in Nederland uniformeren.
Aanvaardbaarheid:
Ethische aanvaardbaarheid
Het aantonen van een (waarschijnlijk) pathogene variant (PV) in een CRC/polyposis geassocieerd gen maakt daaropvolgende cascade onderzoek in de familie en vroege opsporing en preventie van kanker mogelijk. De voorgestelde criteria en diagnostiek lijkt aanvaardbaar voor de betrokkenen. Er zijn geen sterke ethische bezwaren. Er kan wel angst spelen voor de diagnose en zorgen over verzekeringen. Dit kan echter goed worden besproken met de klinisch geneticus en met de aan de afdelingen klinisch genetica verbonden psycholoog en/of maatschappelijk werker. Een deel van de mensen met darmkanker voldoet niet aan de criteria en zal mogelijk onrust ervaren dat er geen erfelijkheidsonderzoek wordt gedaan. In individuele gevallen kan met de MDL-arts en klinisch geneticus worden overlegd hoe deze zorg en angst kan worden gereduceerd.
Ook kunnen familieleden mogelijk zorgen ervaren, omdat zij opeens geconfronteerd worden met de keuze om wel of geen DNA- onderzoek te laten verrichten. Goede verwijscriteria en passende paneldiagnostiek dragen ertoe bij dat deze onrust opweegt tegen de mogelijke gezondheidswinst door mogelijke preventieve maatregelen bij het aantonen van een aanleg.
Duurzaamheid
Het doen van DNA-onderzoek leidt tot CO2 uitstoot. Aan de andere kant kan het vinden van een genetische aanleg in een familie ertoe leiden dat niet alle familieleden darmcontrole hoeven te ondergaan, hetgeen weer tot een reductie van CO2 leidt door minder afspraken in het ziekenhuis, als ook door eerdere en gerichtere behandeling met mogelijk minder agressieve (en minder duurzame) middelen. Door direct een groter panel te testen neemt efficiëntie in laboratoria toe, wat tot minder belasting voor het milieu leidt.
Haalbaarheid
De voorgestelde criteria voor verwijzing en diagnostiek lijken haalbaar. Deze zijn namelijk al grotendeels standaardzorg in de praktijk. In Nederland gaat het om in totaal ongeveer 160 mensen jonger dan 40 jaar met de diagnose darmkanker, en circa 500 mensen tussen 40 en 49 jaar oud. Voor deze groep is er voldoende capaciteit voor afspraken bij de klinische genetica en het doen van DNA-onderzoek.
Rationale van aanbeveling-1: weging van argumenten voor en tegen verwijzing voor de uitvoer van genpanelanalyse bij CRC-patiënt en van diverse leeftijdscategorieën.
Gezien de grote variatie in de praktijk m.b.t. doorverwijzing en uitvoer van genpanelanalyse bij patiënten met CRC heeft de werkgroep adviezen geformuleerd ter bevordering van een uniforme en eenduidige doorverwijzing en analyse. Hierbij is gestreefd naar een zo optimaal mogelijke balans tussen het aanbieden van de meest optimale diagnostiek (om geen patiënten te missen) en haalbaarheid. In de aanbevelingen is hierbij een differentiatie aangebracht voor de verschillende leeftijdsgroepen. De adviezen zijn gebaseerd op aanbevelingen uit (inter-)nationale richtlijnen; (NCCN 2024 (Hodan, 2024), AGA/Delphi 2022 (Cavestro, 2023)) als ook gangbaar gebruik in de klinische praktijk.
Indien patiënt niet voldoet aan genoemde criteria voor doorverwijzing, maar de patiënt een sterke wens tot verwijzing heeft en/of de behandelaar wel meerwaarde ziet van aanvullend testen, is het raadzaam laagdrempelig te overleggen met de klinisch geneticus. Bij verwijzing en uitvoering van analyse dienen uiteraard altijd de wensen van de patiënt mee te worden genomen.
Eindoordeel:
Sterke aanbeveling voor (Doen)
Tabel 2, leeftijden van carcinomen, o.b.v. stoet VKGN en/of incidentie (<100 per jaar) als leidraad voor leeftijd ‘jong’
|
Tumortype |
Leeftijd ‘jong’ bij >1 primaire tumor |
|
CRC |
<40 jaar |
|
Endometrium carcinoom |
<50 jaar |
|
Ovarium/tubacarcinoom |
Altijd verwijzen |
|
Pancreascarcinoom |
<50 jaar |
|
Mammacarcinoom |
<40 jaar |
|
Dunne darm carcinoom |
<50 jaar |
|
Maagcarcinoom |
<50 jaar |
|
Urotheelcelcarcinoom hogere urinewegen |
<50 jaar |
|
Urotheelcelcarcinoom blaas |
<40 jaar |
|
Niercelcarcinoom |
<45 jaar |
|
Prostaatcarcinoom |
<50 jaar |
|
Melanoom |
<30 jaar |
NB: dit is niet evidence-based voor de meeste tumoren, eigen beoordeling in combinatie met histologie en familieanamnese blijven van belang.
Rationale van aanbeveling-2: weging van argumenten voor en tegen samenstelling van het gen panel.
Weinig studies hebben gekeken naar de samenstelling en opbrengst van specifieke genpanelanalyse bij verschillende leeftijden, anders dan de MMR-genen. De werkgroep is van mening dat het belangrijk is om per indicatie een aantal genen sterk te adviseren om praktijkvariatie ten aanzien van zogenaamde “core-genen” te voorkomen. Hiervoor zijn zowel aanbevelingen uit internationale richtlijnen (NCCN 2024 (Hodan, 2024), AGA/Delphi 2022 (Cavestro, 2023)) als standaard gebruik in klinische praktijk als uitgangspunt genomen.
Genpanelanalyses dienen te worden uitgevoerd in een daarvoor toegerust en geaccrediteerd laboratorium om de validiteit te garanderen.
Eindoordeel:
Sterke aanbeveling voor (Doen)
Onderbouwing
Approximately 3-5% of colorectal cancer (CRC) patients have an underlying (high-risk) hereditary predisposition syndrome, primarily Lynch syndrome, but also APC- or MUTYH-associated polyposis. Identifying these genetic predispositions is critical for early cancer detection, prevention, and family cascade testing. Additionally, 10–30% of CRC patients have moderate or mild hereditary risk factors, increasing their risk of secondary malignancies and affecting family members (see chapter 2 on Familial Colorectal Cancer submodule Incidentie, risico’s en surveillance bij familiair colorectaal carcinoom).
A key question is whether DNA analysis, alongside immunohistochemistry (IHC) for mismatch repair (MMR) proteins, is necessary to detect other CRC/polyposis syndromes. This is especially relevant for patients under 50 years, who account for 5.8% of CRC diagnoses in the Netherlands (NKR-cijfers over kanker, 2023) and have higher genetic predisposition rates. While rising CRC incidence in younger populations is largely attributed to non-genetic factors (Spaander, 2023; Sinicrope, 2022), recent gene panel studies in CRC patients under 50 have uncovered additional tumor syndromes beyond Lynch syndrome.
However, uncertainties persist about which genes to include in CRC panels. IHC for MMR proteins may miss some Lynch syndrome cases due to false negatives or undetected germline MLH1 promoter methylation (MLH1-PM) (see submodule De detectie van Lynch syndroom middels tumor analyse). Mosaic predispositions may also contribute to risk.
Both international and local guidelines on gene panel testing for hereditary CRC syndromes lack uniformity, resulting in variation between centers. The current guideline addresses the role of gene panel analysis in identifying hereditary CRC syndromes, particularly in patients with fewer than 10 adenomatous polyps or MMR-proficient CRC, taking into account their age and family history.
Description of studies
Several international guidelines published advice on referral for genetic testing. This included age specific advice and recommendations on which genes to include in CRC panels.
In general, there is agreement between the recommendations in (inter)national guidelines that there should be screened for Lynch syndrome and panel testing should be offered depending on the outcome of this screening, age of cancer diagnosis and/or the amount or type of polyps; but differences can be found in the selection of patients for genetic testing (e.g., age of onset, tumor tests versus prediction tools) and uncertainties persist about which genes to include in CRC panels.
Detecting defective MMR protein expression by high-level immunohistochemistry (IHC) and/or MSI is the gold standard by which mismatch repair deficiency is identified in clinical practice and is recommended for at least all CRC patients under the age of 70 years. IHC for MMR proteins may miss some Lynch syndrome cases due to false negatives, undetected germline MLH1 pathogenic variant (PV) in case of promoter methylation (MLH1-PM) (see submodule De detectie van Lynch syndroom middels tumor analyse) or missense PV in one of the MMR genes. Mosaic predispositions may also contribute to cancer risk.
The NCCN 2024 (Hodan, 2024) and Delphi 2022 (Cavestro, 2023) guidelines recommend germline panel testing for CRC patients under 50 years of age. This is based on a 13.0% prevalence of germline pathogenic variances (gPVs) in this age group when Lynch syndrome is included. However, these guidelines apply when IHC MMR status is unknown and do not address cases with MMR proficient (MMRp) results. The BSG Guideline (Monahan, 2020) specifically recommends multi-gene germline testing for MMRp CRC patients under 30 years of age.
No systematic review of the literature was conducted to answer the following question: What is the yield of DNA testing (CRC/polyposis gene panel) in patients with CRC with different onset ages? This approach was chosen due to the availability of recent international guidelines that specifically address the role of genetic testing in CRC patients of varying ages, with a particular focus on those with early-onset CRC (i.e., under 50 years of age). These included the NCCN 2024 (Hodan, 2024), BSG Guideline 2020 (Monahan, 2020) and AGA/Delphi 2022 (Cavestro, 2023) guidelines. In addition, relevant studies that were published after the publication of these guidelines and were known to the guideline panel were addressed and included in the ‘Overwegingen’.
Relevant outcome measures
The guideline panel considered (guideline based) age-specific advice for genetic testing as critical outcome measure including advice on referral and genes to be included in gene panel analysis for decision making. A priori, the guideline panel did not define the outcome measures listed above but used the definitions used in the studies.
Search and select (Methods)
No systematic literature search was performed. Results from international guidelines including the BSG (Monahan, 2020), NCCN 2024 AGA/ Collaborative Group of the Americas on Inherited Gastrointestinal Cancer (Hodan, 2024); EHTG, and the International Society for Gastrointestinal Hereditary Tumour (Insight, a Delphi-criteria study) 2022 (Cavestro, 2023) as well as recent studies published after publication of these guidelines were summarized.
- Bou Farhat E, Adib E, Daou M, Naqash AR, Matulonis U, Ng K, Kwiatkowski DJ, Sholl LM, Nassar AH. Benchmarking mismatch repair testing for patients with cancer receiving immunotherapy. Cancer Cell. 2024 Jan 8;42(1):6-7. doi: 10.1016/j.ccell.2023.12.001. Epub 2023 Dec 28. Erratum in: Cancer Cell. 2024 Feb 12;42(2):323. doi: 10.1016/j.ccell.2024.01.009. PMID: 38157866.
- Cavestro GM, Mannucci A, Balaguer F, Hampel H, Kupfer SS, Repici A, Sartore-Bianchi A, Seppälä TT, Valentini V, Boland CR, Brand RE, Buffart TE, Burke CA, Caccialanza R, Cannizzaro R, Cascinu S, Cercek A, Crosbie EJ, Danese S, Dekker E, Daca-Alvarez M, Deni F, Dominguez-Valentin M, Eng C, Goel A, Guillem JG, Houwen BBSL, Kahi C, Kalady MF, Kastrinos F, Kühn F, Laghi L, Latchford A, Liska D, Lynch P, Malesci A, Mauri G, Meldolesi E, Møller P, Monahan KJ, Möslein G, Murphy CC, Nass K, Ng K, Oliani C, Papaleo E, Patel SG, Puzzono M, Remo A, Ricciardiello L, Ripamonti CI, Siena S, Singh SK, Stadler ZK, Stanich PP, Syngal S, Turi S, Urso ED, Valle L, Vanni VS, Vilar E, Vitellaro M, You YN, Yurgelun MB, Zuppardo RA, Stoffel EM; Associazione Italiana Familiarità Ereditarietà Tumori; Collaborative Group of the Americas on Inherited Gastrointestinal Cancer; European Hereditary Tumour Group, and the International Society for Gastrointestinal Hereditary Tumours. Delphi Initiative for Early-Onset Colorectal Cancer (DIRECt) International Management Guidelines. Clin Gastroenterol Hepatol. 2023 Mar;21(3):581-603.e33. doi: 10.1016/j.cgh.2022.12.006. Epub 2022 Dec 20. PMID: 36549470; PMCID: PMC11207185.
- Cercek A, Chatila WK, Yaeger R, Walch H, Fernandes GDS, Krishnan A, Palmaira L, Maio A, Kemel Y, Srinivasan P, Bandlamudi C, Salo-Mullen E, Tejada PR, Belanfanti K, Galle J, Joseph V, Segal N, Varghese A, Reidy-Lagunes D, Shia J, Vakiani E, Mondaca S, Mendelsohn R, Lumish MA, Steinruecke F, Kemeny N, Connell L, Ganesh K, Markowitz A, Nash G, Guillem J, Smith JJ, Paty PB, Zhang L, Mandelker D, Birsoy O, Robson M, Offit K, Taylor B, Berger M, Solit D, Weiser M, Saltz LB, Aguilar JG, Schultz N, Diaz LA, Stadler ZK. A Comprehensive Comparison of Early-Onset and Average-Onset Colorectal Cancers. J Natl Cancer Inst. 2021 Nov 29;113(12):1683-1692. doi: 10.1093/jnci/djab124. PMID: 34405229; PMCID: PMC8634406.
- Gopie JP, Vasen HF, Tibben A. Surveillance for hereditary cancer: does the benefit outweigh the psychological burden? --A systematic review. Crit Rev Oncol Hematol. 2012 Sep;83(3):329-40. doi: 10.1016/j.critrevonc.2012.01.004. Epub 2012 Feb 25. PMID: 22366115.
- Hechtman JF, Rana S, Middha S, Stadler ZK, Latham A, Benayed R, Soslow R, Ladanyi M, Yaeger R, Zehir A, Shia J. Retained mismatch repair protein expression occurs in approximately 6% of microsatellite instability-high cancers and is associated with missense mutations in mismatch repair genes. Mod Pathol. 2020 May;33(5):871-879. doi: 10.1038/s41379-019-0414-6. Epub 2019 Dec 19. PMID: 31857677; PMCID: PMC7195218.
- Herkert JC, Niessen RC, Olderode-Berends MJ, Veenstra-Knol HE, Vos YJ, van der Klift HM, Scheenstra R, Tops CM, Karrenbeld A, Peters FT, Hofstra RM, Kleibeuker JH, Sijmons RH. Paediatric intestinal cancer and polyposis due to bi-allelic PMS2 mutations: case series, review and follow-up guidelines. Eur J Cancer. 2011 May;47(7):965-82. doi: 10.1016/j.ejca.2011.01.013. Epub 2011 Mar 4. PMID: 21376568.
- Hitchins MP, Dámaso E, Alvarez R, Zhou L, Hu Y, Diniz MA, Pineda M, Capella G, Pearlman R, Hampel H. Constitutional MLH1 Methylation Is a Major Contributor to Mismatch Repair-Deficient, MLH1-Methylated Colorectal Cancer in Patients Aged 55 Years and Younger. J Natl Compr Canc Netw. 2023 Jul;21(7):743-752.e11. doi: 10.6004/jnccn.2023.7020. PMID: 37433431; PMCID: PMC11578100.
- Hodan R, Gupta S, Weiss JM, Axell L, Burke CA, Chen LM, Chung DC, Clayback KM, Felder S, Foda Z, Giardiello FM, Grady W, Gustafson S, Hagemann A, Hall MJ, Hampel H, Idos G, Joseph N, Kassem N, Katona B, Kelly K, Kieber-Emmons A, Kupfer S, Lang K, Llor X, Markowitz AJ, Prats MM, Niell-Swiller M, Outlaw D, Pirzadeh-Miller S, Samadder NJ, Shibata D, Stanich PP, Swanson BJ, Szymaniak BM, Welborn J, Wiesner GL, Yurgelun MB, Dwyer M, Darlow S, Diwan Z. Genetic/Familial High-Risk Assessment: Colorectal, Endometrial, and Gastric, Version 3.2024, NCCN Clinical Practice Guidelines In Oncology. J Natl Compr Canc Netw. 2024 Dec;22(10):695-711. doi: 10.6004/jnccn.2024.0061. PMID: 39689429.
- Jiang W, Li L, Ke CF, Wang W, Xiao BY, Kong LH, Tang JH, Li Y, Wu XD, Hu Y, Guo WH, Wang SZ, Wan DS, Xu RH, Pan ZZ, Ding PR. Universal germline testing among patients with colorectal cancer: clinical actionability and optimised panel. J Med Genet. 2022 Apr;59(4):370-376. doi: 10.1136/jmedgenet-2020-107230. Epub 2021 Feb 9. PMID: 33563768.
- Kang YJ, Caruana M, McLoughlin K, Killen J, Simms K, Taylor N, Frayling IM, Coupé VMH, Boussioutas A, Trainer AH, Ward RL, Macrae F, Canfell K. The predicted effect and cost-effectiveness of tailoring coloscopic surveillance according to mismatch repair gene in patients with Lynch syndrome. Genet Med. 2022 Sep;24(9):1831-1846. doi: 10.1016/j.gim.2022.05.016. Epub 2022 Jul 9. PMID: 35809086.
- Kastrinos F, Uno H, Ukaegbu C, Alvero C, McFarland A, Yurgelun MB, Kulke MH, Schrag D, Meyerhardt JA, Fuchs CS, Mayer RJ, Ng K, Steyerberg EW, Syngal S. Development and Validation of the PREMM5 Model for Comprehensive Risk Assessment of Lynch Syndrome. J Clin Oncol. 2017 Jul 1;35(19):2165-2172. doi: 10.1200/JCO.2016.69.6120. Epub 2017 May 10. PMID: 28489507; PMCID: PMC5493047.
- Mikaeel RR, Young JP, Li Y, Smith E, Horsnell M, Uylaki W, Tapia Rico G, Poplawski NK, Hardingham JE, Tomita Y, Townsend AR, Feng J, Zibat A, Kaulfuß S, Müller C, Yigit G, Wollnik B, Price TJ. Survey of germline variants in cancer-associated genes in young adults with colorectal cancer. Genes Chromosomes Cancer. 2022 Feb;61(2):105-113. doi: 10.1002/gcc.23011. Epub 2021 Nov 18. PMID: 34761457.
- Monahan KJ, Bradshaw N, Dolwani S, Desouza B, Dunlop MG, East JE, Ilyas M, Kaur A, Lalloo F, Latchford A, Rutter MD, Tomlinson I, Thomas HJW, Hill J; Hereditary CRC guidelines eDelphi consensus group. Guidelines for the management of hereditary colorectal cancer from the British Society of Gastroenterology (BSG)/Association of Coloproctology of Great Britain and Ireland (ACPGBI)/United Kingdom Cancer Genetics Group (UKCGG). Gut. 2020 Mar;69(3):411-444. doi: 10.1136/gutjnl-2019-319915. Epub 2019 Nov 28. PMID: 31780574; PMCID: PMC7034349.
- Olkinuora A, Nieminen TT, Mårtensson E, Rohlin A, Ristimäki A, Koskenvuo L, Lepistö A; Swedish Extended Genetic Analysis of Colorectal Neoplasia (SWEN) Study Group; Gebre-Medhin S, Nordling M, Peltomäki P. Biallelic germline nonsense variant of MLH3 underlies polyposis predisposition. Genet Med. 2019 Aug;21(8):1868-1873. doi: 10.1038/s41436-018-0405-x. Epub 2018 Dec 21. PMID: 30573798; PMCID: PMC6752675.
- Pearlman R, Frankel WL, Swanson B, Zhao W, Yilmaz A, Miller K, Bacher J, Bigley C, Nelsen L, Goodfellow PJ, Goldberg RM, Paskett E, Shields PG, Freudenheim JL, Stanich PP, Lattimer I, Arnold M, Liyanarachchi S, Kalady M, Heald B, Greenwood C, Paquette I, Prues M, Draper DJ, Lindeman C, Kuebler JP, Reynolds K, Brell JM, Shaper AA, Mahesh S, Buie N, Weeman K, Shine K, Haut M, Edwards J, Bastola S, Wickham K, Khanduja KS, Zacks R, Pritchard CC, Shirts BH, Jacobson A, Allen B, de la Chapelle A, Hampel H; Ohio Colorectal Cancer Prevention Initiative Study Group. Prevalence and Spectrum of Germline Cancer Susceptibility Gene Mutations Among Patients With Early-Onset Colorectal Cancer. JAMA Oncol. 2017 Apr 1;3(4):464-471. doi: 10.1001/jamaoncol.2016.5194. PMID: 27978560; PMCID: PMC5564179.
- Pearlman R, Frankel WL, Swanson BJ, Jones D, Zhao W, Yilmaz A, Miller K, Bacher J, Bigley C, Nelsen L, Goodfellow PJ, Goldberg RM, Paskett E, Shields PG, Freudenheim JL, Stanich PP, Lattimer I, Arnold M, Prior TW, Haut M, Kalady MF, Heald B, Paquette I, Draper DJ, Brell JM, Mahesh S, Weeman K, Bastola S, Zangmeister J, Gowda A, Kencana F, Malcolm A, Liu Y, Cole S, Bane C, Li C, Rehmus E, Pritchard CC, Shirts BH, Jacobson A, Cummings SA, de la Chapelle A, Hampel H. Prospective Statewide Study of Universal Screening for Hereditary Colorectal Cancer: The Ohio Colorectal Cancer Prevention Initiative. JCO Precis Oncol. 2021 May 5;5:PO.20.00525. doi: 10.1200/PO.20.00525. PMID: 34250417; PMCID: PMC8232834.
- Seppälä TT, Latchford A, Negoi I, Sampaio Soares A, Jimenez-Rodriguez R, Sánchez-Guillén L, Evans DG, Ryan N, Crosbie EJ, Dominguez-Valentin M, Burn J, Kloor M, Knebel Doeberitz MV, Duijnhoven FJBV, Quirke P, Sampson JR, Møller P, Möslein G; European Hereditary Tumour Group (EHTG) and European Society of Coloproctology (ESCP). European guidelines from the EHTG and ESCP for Lynch syndrome: an updated third edition of the Mallorca guidelines based on gene and gender. Br J Surg. 2021 May 27;108(5):484-498. doi: 10.1002/bjs.11902. PMID: 34043773; PMCID: PMC10364896.
- Sinicrope FA. Increasing Incidence of Early-Onset Colorectal Cancer. N Engl J Med. 2022 Apr 21;386(16):1547-1558. doi: 10.1056/NEJMra2200869. PMID: 35443109.
- Spaander MCW, Zauber AG, Syngal S, Blaser MJ, Sung JJ, You YN, Kuipers EJ. Young-onset colorectal cancer. Nat Rev Dis Primers. 2023 Apr 27;9(1):21. doi: 10.1038/s41572-023-00432-7. PMID: 37105987; PMCID: PMC10589420.
- Terlouw D, Suerink M, Singh SS, Gille HJJP, Hes FJ, Langers AMJ, Morreau H, Vasen HFA, Vos YJ, van Wezel T, Tops CM, Ten Broeke SW, Nielsen M. Declining detection rates for APC and biallelic MUTYH variants in polyposispatients, implications for DNA testing policy. Eur J Hum Genet. 2020 Feb;28(2):222-230. doi: 10.1038/s41431-019-0509-z. Epub 2019 Sep 16. PMID: 31527860; PMCID: PMC6974599.
- Terradas M, Gonzalez-Abuin N, García-Mulero S, Viana-Errasti J, Aiza G, Piulats JM, Brunet J, Capellá G, Valle L. MBD4-associated neoplasia syndrome: screening of cases with suggestive phenotypes. Eur J Hum Genet. 2023 Oct;31(10):1185-1189. doi: 10.1038/s41431-023-01418-5. Epub 2023 Jul 4. PMID: 37402954; PMCID: PMC10545785.
- Umar A, Boland CR, Terdiman JP, Syngal S, de la Chapelle A, Rüschoff J, Fishel R, Lindor NM, Burgart LJ, Hamelin R, Hamilton SR, Hiatt RA, Jass J, Lindblom A, Lynch HT, Peltomaki P, Ramsey SD, Rodriguez-Bigas MA, Vasen HF, Hawk ET, Barrett JC, Freedman AN, Srivastava S. Revised Bethesda Guidelines for hereditary nonpolyposis colorectal cancer (Lynch syndrome) and microsatellite instability. J Natl Cancer Inst. 2004 Feb 18;96(4):261-8. doi: 10.1093/jnci/djh034. PMID: 14970275; PMCID: PMC2933058.
- Uson PLS Jr, Riegert-Johnson D, Boardman L, Kisiel J, Mountjoy L, Patel N, Lizaola-Mayo B, Borad MJ, Ahn D, Sonbol MB, Jones J, Leighton JA, Gurudu S, Singh H, Klint M, Kunze KL, Golafshar MA, Esplin ED, Nussbaum RL, Stewart AK, Bekaii-Saab TS, Jewel Samadder N. Germline Cancer Susceptibility Gene Testing in Unselected Patients With Colorectal Adenocarcinoma: A Multicenter Prospective Study. Clin Gastroenterol Hepatol. 2022 Mar;20(3): e508-e528. Doi: 10.1016/j.cgh.2021.04.013. Epub 2021 Apr 20. PMID: 33857637.
- Van der Giessen JAM, van Riel E, Velthuizen ME, van Dulmen AM, Ausems MGEM. Referral to cancer genetic counseling: do migrant status and patients' educational background matter? J Community Genet. 2017 Oct;8(4):303-310. doi: 10.1007/s12687-017-0326-4. Epub 2017 Sep 4. PMID: 28868568; PMCID: PMC5614888.
- Van Riel E, van Dulmen S, Ausems MG. Who is being referred to cancer genetic counseling? Characteristics of counselees and their referral. J Community Genet. 2012 Oct;3(4):265-74. doi: 10.1007/s12687-012-0090-4. Epub 2012 Mar 17. PMID: 22426886; PMCID: PMC3461220.
- Vos JR, Fakkert IE, Spruijt L, Willems RW, Langenveld S, Mensenkamp AR, Leter EM, Nagtegaal ID, Ligtenberg MJL, Hoogerbrugge N; FINAL Group. Evaluation of yield and experiences of age-related molecular investigation for heritable and nonheritable causes of mismatch repair deficient colorectal cancer to identify Lynch syndrome. Int J Cancer. 2020 Oct 15;147(8):2150-2158. doi: 10.1002/ijc.33117. Epub 2020 Jun 8. PMID: 32510614; PMCID: PMC7496272.
- Will O, Carvajal-Carmona LG, Gorman P, Howarth KM, Jones AM, Polanco-Echeverry GM, Chinaleong JA, Günther T, Silver A, Clark SK, Tomlinson I. Homozygous PMS2 deletion causes a severe colorectal cancer and multiple adenoma phenotype without extraintestinal cancer. Gastroenterology. 2007 Feb;132(2):527-30. doi: 10.1053/j.gastro.2006.11.043. Epub 2006 Nov 29. PMID: 17258725.
- Yanes T, Willis AM, Meiser B, Tucker KM, Best M. Psychosocial and behavioral outcomes of genomic testing in cancer: a systematic review. Eur J Hum Genet. 2019 Jan;27(1):28-35. doi: 10.1038/s41431-018-0257-5. Epub 2018 Sep 11. PMID: 30206354; PMCID: PMC6303287.
- Yurgelun MB, Kulke MH, Fuchs CS, Allen BA, Uno H, Hornick JL, Ukaegbu CI, Brais LK, McNamara PG, Mayer RJ, Schrag D, Meyerhardt JA, Ng K, Kidd J, Singh N, Hartman AR, Wenstrup RJ, Syngal S. Cancer Susceptibility Gene Mutations in Individuals with Colorectal Cancer. J Clin Oncol. 2017 Apr 1;35(10):1086-1095. doi: 10.1200/JCO.2016.71.0012. Epub 2017 Jan 30. PMID: 28135145; PMCID: PMC5455355.
- Zhao ZY, Lei Y, Wang ZM, Han H, Xing JJ, Xu XD, Gao XH, Zhang W, Yu ED. Re-recognition of BMPR1A-related polyposis: beyond juvenile polyposis and hereditary mixed polyposis syndrome. Gastroenterol Rep (Oxf). 2023 Jan 5;11: goac082. doi: 10.1093/gastro/goac082. PMID: 36632626; PMCID: PMC9825710.
Risk of Bias tables
Not applicable
Table of excluded studies
Not applicable
Literature search strategy
Not applicable
Tabel 1 a-g Mutatiedetectie per leeftijdsgroep
1a 20-29 jaar
|
Studie |
N totaal |
MMR-gen PV |
Kiembaan PV in ander CRC gen
|
Kiembaan in non CRC gen |
Specification non-CRC genes |
|
|
Totaal |
Alleen APC/ MUTYH biallelisch |
|||||
|
Pearlman, 2017* |
18 |
2 |
2 |
2 |
0 |
|
|
Yurgelun, 2017 |
14 |
3 |
1 |
1 |
0 |
|
|
Jiang, 2022 |
15 |
4 |
1 |
1 |
|
|
|
Pearlman, 2021 |
33 |
4 |
1 |
1 |
0 |
|
|
Mork 2015# |
193 |
23
|
20 |
18 |
1 |
(Tp53) |
|
Specification Mork |
|
|
20 (2X CMMRD) |
16 APC, 2 biallelic MAP) |
|
|
|
Cercek 2021@ |
118 |
9 |
4 |
3 |
2 |
BRCA2 ATM |
*One patient had a PMS2 and APC combination germline PV
# including all patients aged 17-35 (mean age 29) specification 20-30 and, 30-40 years is missing
@ including all patients aged 18- 35, no specification within this group, nit included CHEK2 heterozygote PV, MITF, MUTYH, APC p.I1307K
1b 30-39 jaar
|
Studie
|
N totaal |
MMR-gen PV |
Kiembaan PV in ander CRC gen
|
Kiembaan PV in non CRC gen
|
Specification non-CRC genes |
|
|
Totaal |
Alleen APC/ MUTYH biallelisch |
|||||
|
Pearlman, 2017 |
98 |
9 |
10 |
7 |
2 |
2x ATM |
|
Terlouw, 2020 |
67 |
|
5 |
5 |
|
|
|
Frostberg 2021@ |
98 |
21 |
2 |
2 |
|
|
|
44 |
3 |
1 |
0 |
2 |
BRCA2 2x
|
|
|
Yurgelun, 2017 |
90 |
12 |
2 |
2 |
1 |
BRCA2 |
|
Jiang, 2022 |
32 |
3 |
0 |
0 |
1 |
BRCA1 |
|
Pearlman, 2021 |
157 |
18 |
7 |
6 |
5 |
4x ATM, 1x CDKN2A |
@ Frostberg et al bevat alle patiënten 18 en 40 jaar, specificatie ontbreekt voor hoeveel onder 30 jaar, vermoedelijk klein aantal.
# Mikaeel et al bevat alle patiënten 18 en 40 jaar, specificatie ontbreekt voor onder 30 jaar, vermoedelijk klein aantal.
Not included MUTYH heterozygotes, ERCC2, BLM heterozygote and CFTR variants
1c 40-49 jaar
|
Studie |
N totaal |
MMR PV |
Kiembaan PV in ander CRC-gen |
Kiembaan in non CRC gen |
Specification non-CRC genes |
|
|
Totaal |
Alleen APC/ MUTYH biallelisch |
|||||
|
Pearlman, 2017 |
333 |
26 |
3 |
3 |
10 |
3x BRCA2 2x BRCA1 2x PALB2 ATM ATM/CHEK2 combined CDKN2A |
|
Pearlman, 2021@ |
529 |
42 |
8 |
7 |
12 |
(7x BRCA1/2, 1 ATM, 1 CDKN2A, 3 PALB2 |
|
Terlouw |
74 |
ND |
4 |
4 |
ND |
|
|
Mikaeel, 2021 # |
56 |
3 |
3 |
2 |
5 |
BRCA1 ATM RAD51C GATA2 BRIP1 |
|
Yurgelun, 2017 |
232 |
6 |
2 |
2 |
4 |
2xBRCA2 2x BRCA1 |
|
Jiang, 2022 |
99 |
4 |
1 |
1 |
1 |
RECQL |
|
Uson, 2022@ |
124 |
9
|
2
|
2
|
6
|
BLM biallelic BRCA2 (2x), BRIP1, PALB2,FH gene |
|
Uson, specification ages |
|
(2< 30 yrs 1 < 40 yrs) |
1<30 |
1<30) |
|
|
|
Cercek, 2021* |
342 |
11 |
2 |
2 |
0 |
1 BRCA2 1 BRCA1 1x PALB2 2x NF1 1x RB1 mosaic PTCH1 SDHA |
# Mikaeel et al bevat alle patiënten 40-54 jaar, specificatie ontbreekt
@ Uson et al cohort includeert 24-50 jaar, meeste ouder dan 40 jaar
- Cercek included 35-49 years, no specification within this group was given.
Not including APC p.I1307K, MUTYH heterozygotes, CHEK2 heterozygotes and other low or non-penetrance genes for CRC such as NBN EGFR, ERCC4, GJB2, MSH3 WRN, HOXb13, SDHA, BLM (heterozygotes)
1d 50-59 jaar
|
Studie |
N totaal |
MMR PV |
Kiembaan PV in ander CRC gen
|
Kiembaan in non CRC gen |
Specification non-CRC genes |
|
|
Totaal |
Alleen APC/ MUTYH biallelisch |
|||||
|
Yurgelun, 2017 |
327 |
8 |
2 |
2 |
3 |
3x BRCA2 |
|
Jiang ,2022 |
160 |
7 |
1 |
1 |
5 |
3x BRCA1/2, 2x RECQL) |
|
Pearlman, 2021 |
877 |
42 |
4 |
4 |
3 |
(ATM 2x? check, Rad51d) |
Not including: BLM, ERCC4, CHEK2, RECQL?, MUTYH heterozygotes
1.e 60-69 jaar
|
Studie |
N totaal |
MMR PV |
Kiembaan PV in ander CRC gen
|
Kiembaan in non CRC gen |
Specification non-CRC genes |
|
|
Totaal |
Alleen APC/ MUTYH biallelic |
|||||
|
Yurgelun, 2017 |
252 |
3 |
1 |
1 |
5 |
1x BRCA1 2xBRCA2 2x PALB2 |
|
Jiang, 2022 |
172 |
1 |
0 |
0 |
5
|
2BRCA1/2,2ATM, 1 RAD51C) |
|
Pearlman, 2021 |
916 |
26 |
4 |
4 |
5
|
(1 POT1, 1 CDKN2A, 1 BRCA1, 1 GALNT12, 1 ATM |
Not including: RAD50, NBN, FANC1, WRN, MRE11A, ERCC2, MUTYH heterozygotes
1.f 70-80 jaar
|
Studie |
N totaal |
MMR PV |
Kiembaan PV in ander CRC gen
|
Kiembaan in non CRC gen |
Specification non-CRC genes |
|
|
Totaal |
Alleen APC/ MUTYH biallelic |
|||||
|
Yurgelun, 2017 |
103 |
1 |
0 |
0 |
2 |
(CDKN2A and TP53) * |
|
Jiang ,2022 |
8 |
0 |
0 |
0 |
0 |
|
|
Pearlman, 2021 |
561 |
10 |
0 |
0 |
4
|
(1 ATM, 2 BRIP1, 1PALB2) |
|
|
|
|
|
|
|
|
* patiënt with TP53 had myelodysplastic syndrome
1.g >80 jaar
|
Studie |
N totaal |
MMR PV |
Kiembaan PV in ander CRC gen
|
Kiembaan in non CRC gen |
Specification non-CRC genes |
|
|
Totaal |
Alleen APC/ MUTYH biallelic |
|||||
|
Yurgelun, 2017 |
40 |
0 |
0 |
0 |
0 |
|
|
Pearlman, 2021 |
237 |
2 |
0 |
0 |
1 |
(BRIP1) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 11-12-2025
Beoordeeld op geldigheid : 11-12-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Belangrijkste wijzigingen t.o.v. vorige versie:
|
Onderwerp |
Wijzigingen meest recente versie |
|
Module 1: Diagnostiek en verwijzing |
|
|
Module 2: Familiair colorectaal carcinoom |
|
|
Module 3: Lynch syndroom |
|
|
Module 4: Adenomateuze polyposis |
|
|
Module 5: Serrated polyposis en overige vormen van polyposis |
|
|
Andere aanpassingen |
|
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met Erfelijke darmkanker.
Werkgroep
- dr. M. (Maartje) Nielsen (voorzitter), Klinisch geneticus, Leids Universitair Medisch Centrum, Leiden, VKGN
- prof. dr. N. (Nicoline) Hoogerbrugge, internist, Radboud UMC, Nijmegen, VKGN
- dr. A. (Anja) Wagner, Klinisch geneticus, Erasmus MC Kanker Instituut, Universitair Medisch Centrum Rotterdam, Rotterdam, VKGN
- dr. S.W. (Sanne) Bajwa – ten Broeke, Klinisch geneticus, Universitair Medisch Centrum Groningen, Groningen, VKGN
- prof. Dr. M.E. (Monique) van Leerdam, MDL-arts, Nederlands Kanker Instituut, Amsterdam, Leiden University Medical Center, NVMDL
- dr. T.M. (Tanya) Bisseling, MDL-arts, Radboud UMC, Nijmegen, NVMDL
- dr. M.C.A. (Mariëtte) van Kouwen, MDL-arts, Radboud UMC, Nijmegen, NVMDL
- prof. Dr. E. (Evelien) Dekker, MDL-arts, Amsterdam UMC, Amsterdam, NVMDL
- drs. H. (Hicham) Bouchiba, Arts-onderzoeker MDL, Amsterdam UMC, Amsterdam, persoonlijke titel
- dr. C.J. (Charlotte) Verberne, Chirurg, Ziekenhuis Amstelland, Amstelveen
- dr. J.M. (Jorien) Woolderink, Gynaecoloog, Martini Ziekenhuis, Groningen, NVOG
- dr. R.S. (Chella) van der Post, Patholoog, Radboud UMC, Nijmegen, NVVP
- dr. J.E. (Jurgen) Seppen, Patiëntvertegenwoordiger, Stichting Lynch Polyposis
- dr. A.R. (Arjen) Mensenkamp, laboratoriumspecialist Klinische genetica, Radboud UMC, Nijmegen, VKGL
- dr. C.M.J. (Carli) Tops, laboratoriumspecialist Klinische genetica, Leids Universitair Medisch Centrum, Leiden, VKGL
- I.J.H. (Ivonne) Schoenaker, Verpleegkundig specialist MDL, Isala Ziekenhuis, Zwolle, V&VN oncologie
- L.J.(Lisette) Saveur, Verpleegkundig specialist MDL, Nederlands Kanker Instituut, Amsterdam, V&VN oncologie
Klankbordgroep:
- Dr. F.J.B. (Fränzel) van Duijnhoven, Universitair hoofddocent voeding, genen en kanker WUR, Wageningen, persoonlijke titel
- Dr. J.A.J. (Job) Verdonschot, AIOS klinische Genetica, Maastricht Universitair Medisch Centrum, Maastricht, persoonlijke titel
- Dr. A.G. (Toine) van der Heijden, Oncologisch uroloog, Radboud UMC, Nijmegen, persoonlijke titel
Met ondersteuning van
- dr. J. (Joppe) Tra, Senior-Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. D. (Dagmar) Nieboer, Senior-Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. J. (Josefien) Buddeke, Senior-Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. M. (Mirre) den Ouden-Vierwind, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. M. (Merel) Wassenaar, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. A.C. (Anniek) van Westing, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. L. (Leanne) Küpers, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. J. (Jing) de Haan- Du, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. S.N. (Sarah) van Duijn, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. M. (Majke) van Bommel, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- drs. E. (Evie) Verweg, Junior Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- D.P. (Diana) Gutierrez, projectsecretaresse, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een (sub-) module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Werkgroepleden |
||||
|
Nielsen |
Klinisch geneticus, volledig betaald door de afdeling. |
2012 - present: the International Society for Gastrointestinal Hereditary Tumors (InSiGHT)
Betaling per bijeenkomst (vacation money for expenses made)
Lid adviesraad Stichting Lynch- Polyposis (onbetaald) |
Lopende subsidiegelden – waar ik bij betrokken bij ben:
|
Geen |
|
Hoogerbrugge – van der Linden |
Medisch specialist en hoogleraar erfelijke kanker
|
Geen |
Geen extern gefinancierd onderzoek in relatie tot deze functie |
Geen |
|
Wagner |
Klinisch geneticus |
Bestuurslid Stichting Opsporing Erfelijke tumoren (onbetaald); |
Extern gefinancierd onderzoek. WP3 leider KWF-project nr: 14976 (Smart measurement of circulating tumour DNA: a tumour-agnostic computational tool to improve CRC-care) |
Geen |
|
Bajwa – ten Broeke |
Klinische geneticus UMCG PI, betaald (vanuit KWF-subsidie) |
Lid European Hereditary Tumor Group (onbetaald), Bestuurslid DCCG |
Ja, subsidie voor onderzoek door KWF (young investigator grant), 2021-2025 |
Geen |
|
Van Leerdam |
MDL-arts Antoni van Leeuwenhoek, Amsterdam (0,6 FTE) betaald
|
Medisch directeur stichting opsporing erfelijke tumoren, Leiden, onbetaald |
Extern gefinancierd onderzoek |
Geen |
|
Bisseling |
MDL-arts Radboud UMC 0.9 fte |
Geen |
Geen |
Geen |
|
Van Kouwen |
Maag-Darm-Leverarts Radboud UMC Nijmegen |
Geen |
Geen |
Geen |
|
Dekker |
Maag-Darm-Leverarts, FT, Amsterdam UMC (betaald)
|
Lid raad van Commissarissen The eNose Company (betaald)
|
I have received honorarium for consultancy* from FujiFilm, Olympus, GI Supply, PAION and Ambu, and speakers' fees from Olympus, GI Supply, Norgine, IPSEN, PAION and FujiFilm. -Studies gefinancierd door KWF, MLDS, TKI, ZonMW, Celtic, FujiFilm. * Single meeting about development, innovation and research |
Geen
Geen deelname aan adviesraden gedurende de richtlijnontwikkeling |
|
Bouchiba |
PhD kandidaat/Arts-onderzoeker maag-darm-leverziekten Amsterdam UMC. |
Geen |
Geen |
Geen |
|
Verberne |
Chirurg in het ziekenhuis Amstelland, Amstelveen |
Geen |
Geen |
Geen |
|
Woolderink |
Gynaecoloog, Martini Ziekenhuis Groningen |
Lid adviesraad Stichting Lynch- Polyposis (onbetaald) |
Geen |
Geen |
|
Van der Post |
Patholoog, Radboud UMC
|
Bestuurslid Stichting Opsporing Erfelijke tumoren (onbetaald) |
Geen extern gefinancierd onderzoek in relatie tot deze functie |
Geen |
|
Seppen |
Universitair hoofddocent, Amsterdam UMC |
Bestuurslid Stichting Lynch Polyposis |
Geen |
Geen |
|
Mensenkamp |
Laboratoriumspecialist klinische genetica, Radboud UMC Nijmegen |
Voorzitter landelijk overleg erfelijke borstkankerdiagnostiek (LOB)
|
-Medewerking verleend aan workshops variantclassificatie en betrokken als assessor bij kwaliteitsrondzendingen BRCA-diagnostiek op tumorweefsel (EMQN/GenQA, gesponsord door AstraZeneca, betaald aan de afdeling Genetica) -VCo-applicant CRAFT project bij KWF. |
Geen |
|
Tops |
Laboratorium specialist klinische genetica, KG, LUMC
|
Geen |
KWF 14469 - Functionele test Lynch genen - Geen projectleider |
Geen |
|
Schoenaker |
Verpleegkundige specialist AGZ (MDL Oncologie) Isala, betaald
|
Geen |
EASIER study; Electronic nose for breath Analysis after curative Surgery to detect dIstant mEtastases or locoregional Recurrence of colon cancer |
Geen |
|
Saveur |
Verpleegkundig specialist Antoni van Leeuwenhoek |
Geen |
Geen |
Geen |
|
|
||||
|
Klankbordgroepleden |
||||
|
Van Duijnhoven |
Associate Professor
|
Geen |
Onderzoeksproject gefinancierd door World Cancer Research Fund/ Wereld Kanker Onderzoek Fonds |
Geen |
|
Verdonschot |
AIOS Klinische Genetica, MUMC+ |
Geen |
Geen |
Geen |
|
Van der Heijden |
Oncologisch uroloog
|
Geen |
ZonMW; BladParadigm; RCT mpMRI versus TURT.Projectleider ja |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door afvaardiging vanuit de patiëntenvereniging Stichting Lynch Polyposis in de werkgroep. De afgevaardigde heeft meebeslist bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen.
De conceptrichtlijn is tevens voor commentaar voorgelegd aan Stichting Lynch Polyposis de Nederlandse Federatie van Kankerpatiëntenorganisaties (NFK). De eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
|
Module |
Uitkomst raming |
Toelichting |
|
Submodule Verwijscriteria voor klinisch genetisch onderzoek bij CRC en gen panel analyse |
Geen mogelijk financiële gevolgen |
Uit de toetsing volgt dat de aanbevelingen niet breed toepasbaar zijn (<5.000 patiënten) en daarom naar verwachting geen substantiële financiële gevolgen zullen hebben voor de collectieve uitgaven. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep schriftelijk de knelpunten in de zorg voor patiënten met Erfelijke darmkanker. Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
er is hoge zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; het is zeer onwaarschijnlijk dat de literatuurconclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Redelijk |
er is redelijke zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; het is mogelijk dat de conclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Laag |
er is lage zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; er is een reële kans dat de conclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Zeer laag |
er is zeer lage zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; de literatuurconclusie is zeer onzeker. |
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Voor- en nadelen van interventies dienen goed met de patiënt te worden doorgenomen.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.