Genetische testen bij adenomateuze polyposis
Uitgangsvraag
Welke genetische testen moeten worden aangeboden voor adenomateuze polyposis?
Aanbeveling
Maak bij patiënten die in aanmerking komen voor genetische diagnostiek voor adenomateuze polyposis gebruik van de aanbevolen gen-panels zoals weergegeven in Tabel 2a, 2b, 2c.
Verricht bij negatief kiembaanonderzoek APC-mozaïek analyse bij patiënten met:
- ≥20 adenomen vóór de leeftijd van 60 jaar of
- ≥30 adenomen vóór de leeftijd van 70 jaar
Overwegingen
Voor het beantwoorden van de vraag ‘Welke genetische testen moeten worden aangeboden voor adenomateuze polyposis’ is geen systematische literatuursearch gedaan. Het antwoord op deze vragen is gezocht in internationale richtlijnen en studies die bekend zijn bij de werkgroep. De kwaliteit van bewijs is dan ook niet gegradeerd.
Genetisch onderzoek bij adenomateuze polyposis
Gen panels
Het gebruik van multi-gen paneltesten is inmiddels standaard in de genetische diagnostiek. Deze benadering kan gebruik maken van fysieke panels of virtuele panels op basis het hele exoom of genoom (WES of WGS).
Onder andere op basis van de studies in Tabel 1 uit submodule Verwijscriteria voor klinisch genetisch onderzoek bij adenomateuze polyposis dienen panels voor gastro-intestinale adenomateuze polyposis in elk geval APC en MUTYH omvatten, die het meest voorkomen. Andere genen, die relevant zijn voor meer zeldzame adenomateuze polyposis syndromen, namelijk AXIN2, MLH3, MSH3, MBD4, NTHL1, POLE (exonuclease domein), en POLD1 (exonucleasedomein), kunnen aan een panel worden toegevoegd (Valle, Weren, Palles, Palles, Aronson, Adam, Olkinuora, Lorca, Terradas).
Daarnaast kan overwogen worden om de MMR-genen (Lynch syndroom) op te nemen en genen die andere polyposis syndromen veroorzaken, zoals STK11 (Peutz-Jeghers syndroom), BMPR1A en SMAD4 (juveniele Polyposis), PTEN (PHTS) en RNF43 (serrated polyposis), vanwege mogelijke fenotypische overlap of misclassificatie van poliepen. De studie van Stanich (2019) laat zien dat in patiënten met adenomateuze polyposis ook MMR-gen PVs gevonden kunnen worden, evenals PVs in genen geassocieerd met hamartomateuze polyposis (STK11, SMAD4, BMPR1A, PTEN). Het is echter niet duidelijk of in die casus een geharmoniseerde pathologische revisie heeft plaatsgevonden en hoeveel van patiënten met een kiembaan MMR PV ook darmkanker hadden (en of hierin IHC MMR was gedaan). Wel wordt beschreven dat in 19% (583/3197) van de geïncludeerde patiënten met adenomateuze poliepen sprake was van darmkanker bij henzelf en in 32% 1024/3197 bij een eerstegraads familielid.
Bij GREM1, dat mixed polyposis kan veroorzaken met name binnen de Ashkenazi-joodse bevolking, zijn alleen duplicaties beschreven die ver 5’ in de promoter liggen (3MB vóór het gen zelf). Mutatie-analyse van het gen zelf is dus niet geïndiceerd (Jaeger, 2012; McKenna, 2019).
Biallelische pathogene varianten in MCM9 en MCM8 zijn geassocieerd met onvruchtbaarheid, maar mogelijk ook met polyposis. Zeker voor MCM9 is deze associatie aannemelijk (Goldberg, 2021; Helderman, 2023).
Het RPS20 gen is recentelijk beschreven in erfelijke darmkanker, maar mogelijk ook polyposis en lijkt zeer zeldzaam met mogelijk hoge penetrantie (Thompson, 2020).
Omdat voor de meer recent beschreven genen het onderscheid tussen CRC en polyposis niet altijd even scherp is, poliepen verkeerd geclassificeerd kunnen zijn of soms niet allemaal pathologisch onderzocht worden en in sommige gevallen polyposis bij darmkanker over het hoofd kan worden gezien, met name als deze atypisch is, kan ter overweging worden genomen om een panel te gebruiken waar zowel darmkanker- als polyposis-geassocieerde genen in worden meegenomen. Ook geeft een panel de mogelijkheid zeldzame of nog onzekere polyposis genen te includeren. Er kan zelfs een breed oncopanel, dat ook kanker predispositie genen bevat voor andere tumor soorten, worden overwogen, bijvoorbeeld indien de persoonlijke of familiegeschiedenis andere tumoren toont.
Het nadeel van grotere panels is echter dat er meer varianten van onbekende betekenis (VUSsen) kunnen worden gevonden. Het is met name bij APC van belang terughoudend te zijn bij de rapportage hiervan. Tot op heden zijn er slechts twee waarschijnlijk pathogene missense varianten in APC beschreven, c.3077A>G p. (Asn1026Ser) en c.3084T>A p. (Ser1028Arg) (InSiGHT/ACMG APC variant classification guideline, (Valle, 2023)). Er zijn twee specifieke varianten in het APC-gen waar extra aandacht voor nodig is. De variant c.3920T>A p. (Ile1307Lys)/(I1307K) komt met name voor in de Ashekenzi-joodse bevolking. Daar wordt deze gerapporteerd als risicofactor: De variant heeft een lage penetrantie met een geschat absoluut risico van 5%-10% op CRC bij personen van Ashkenazisch Joodse afkomst. Er is niet genoeg bewijs om een verhoogd risico op kanker in andere populaties/subpopulaties te ondersteunen. Daarom, totdat/tenzij toekomstig bewijs anders aangeeft, wordt personen van niet-Ashkenazische Joodse afkomst met I1307K geadviseerd deel te nemen aan het nationale bevolkingsonderzoek voor CRC (Valle, 2023). Dit advies geldt ook dragers van Ashkenazisch Joodse afkomst aangezien het risico op CRC niet meer dan 2,5 keer verhoogd is (submodule Incidentie, risico’s en surveillance) De APC-variant c.3949G>C p. (Glu1317Gln)/ E1317Q wordt niet meer beschouwd als een risicovariant (Liang, 2013).
Onderstaande tabel geeft de aanbevolen gen-panels bij polyposis weer
Tabel 2a: Aanbevolen gen-panel bij adenomateuze polyposis
|
Gen |
Beschrijving |
OMIM (ziekte) |
Bewijs |
|
APC (AD) |
Familiaire adenomateuze polyposis (FAP) |
175100 |
Sterk, frequent |
|
MUTYH (AR) |
MUTYH-geassocieerde polyposis (MAP) |
608456 |
Sterk, frequent |
|
AXIN2 (AD) |
Oligodontia-colorectal cancer syndrome |
608615 |
Matig sterk, zeer zeldzaam |
|
MLH3 (AR/AD) |
Polyposis (AR), mogelijk darmkanker (AD) |
614385 |
Matig, zeldzaam |
|
MSH3 (AR) |
Familial adenomatous polyposis |
617100 |
Sterk, zeldzaam |
|
MBD4 (AR) |
Tumor predispositie syndroom |
619975 |
Sterk, zeldzaam |
|
NTHL1 (AR) |
Familiaire adenomateuze polyposis type 3 |
616415 |
Sterk, zeldzaam |
|
POLE (AD) |
Polymerase proofreading-related adenomatous polyposis (PPAP) |
615083 |
Sterk, zeldzaam |
|
POLD1 (AD) |
Polymerase proofreading-related adenomatous polyposis (PPAP) |
612591 |
Sterk, zeldzaam |
Tabel 2b: Aanbevolen gen-panel bij hamartomateuze polyposis
|
Gen |
Beschrijving |
OMIM (ziekte) |
Bewijs |
|
BMPR1A (AD) |
Juveniele polyposis (JPS) |
174900 |
Sterk, zeldzaam |
|
PTEN (AD) |
PTEN-hamartomateus tumor syndroom (PHTS) |
158350 |
Sterk, zeldzaam |
|
SMAD4 (AD) |
Juveniele polyposis (JPS) |
174900 |
Sterk, zeldzaam |
|
STK11 (AD) |
Peutz Jeghers syndroom (PJS) |
175200 |
Sterk, zeldzaam |
Tabel 2c: Genen welke naast de genen in tabel 2a en 2b in een breed CRC-polyposis gen panel-opgenomen kunnen worden
|
Gen |
Beschrijving |
OMIM (ziekte)/ref |
Bewijs |
|
GREM1 (AD) |
Hereditary mixed polyposis syndrome |
PMID: 22561515 |
Matig. Duplicatie 5’ van het gen, m.n. Ashkenazi joodse populatie, zeer zeldzaam |
|
MCM9 (vrnl. AR) |
Onvruchtbaarheid en polyposis |
PMID 34556653 |
Matig |
|
RNF43 (AD) |
Sessile serrated polyposis cancer syndrome |
OMIM 617108 |
Matig, zeer zeldzaam, lage penetrantie |
|
MCM8 (vrnl. AR) |
Onvruchtbaarheid en darmkanker |
PMID: 32841224 |
Laag |
|
RPS20 (AD) |
CRC en polyposis |
PMID:24941021; 32424863 |
Redelijk sterk, zeer zeldzaam |
|
MLH1 (AD) |
Lynch syndroom |
OMIM 609310 |
Sterk, frequent |
|
MSH2 (AD) |
Lynch syndroom |
OMIM 120435 |
Sterk, frequent |
|
MSH6 (AD) |
Lynch syndroom |
OMIM 614350 |
Sterk, frequent |
|
PMS2 (AD) |
Lynch syndroom |
OMIM 614337 |
Sterk, frequent |
|
EPCAM (AD) |
Lynch syndroom |
OMIM 613244 |
Sterk, (alleen deleties van minimaal het laatste exon), zeldzaam |
AD; autosomaal dominante overerving (bij polyposis/darmkanker). AR, autosomaal recessieve overerving.
Valle en Monahan (Valle 2024) hebben een volledig overzicht gepubliceerd over de genetische predispositie voor polyposis. Het gebruik van gen panels wordt nader besproken in submodule Verwijscriteria voor klinisch genetisch onderzoek bij CRC en genpanelanalyse.
APC-mozaïek
Het is inmiddels bekend dat mozaïek APC-varianten in 20-50% van de onverklaarbare gevallen van adenomateuze polyposis kan worden gevonden, vooral in de groep met meer dan 20 colorectale adenomen. (Spier, 2016; Jansen, 2017). Het gaat hierbij dus om patiënten bij wie geen kiembaan pathogene variant(en) (PV werd(en) aangetoond met eerdere diagnostiek en er geen (duidelijk) familieverhaal is van adenomateuze polyposis.
In veel van deze gevallen is het mozaïcisme niet detecteerbaar in uit leukocyten verkregen DNA en vereist dit testen van DNA geïsoleerd uit >2 adenomen. Tumortesten zijn nog steeds een logistieke en financiële uitdaging en daarom zijn duidelijke criteria voor testen wenselijk. Er zijn nog weinig studies die hebben gekeken naar het vóórkomen van APC-mozaïek in de groepen met minder dan 20 adenomen. Hiervoor zijn voorlopige data uit de studie van Terlouw, 2025 (preprint) meegenomen: deze studie laat een detectie van >5% zien in patiënten met milde polyposis (5-19 adenomen) <50 jaar. Pas bij ≥20 adenomen <60 jaar en ≥30 adenomen <70 jaar neemt de detectie toe tot >10%. Het advies is op basis daarvan om APC-mozaïek in ieder geval te onderzoeken in >2 adenomen als sprake is van:
• ≥20 colorectale adenomen vóór de leeftijd van 60 jaar of
• ≥30 colorectale adenomen vóór de leeftijd van 70 jaar
Verder laat deze studie zien dat 24 kinderen van 17 APC mozaïek ouders geen APC PV geërfd. Echter in het semen van een andere patiënt werd de APC-variant wel in 16% aangetoond. Deze patiënt had echter in andere weefsels ook een vrij hoog percentage van de APC-variant (5-10%), dit is slechts zo bij een minderheid van patiënten. Op dit moment lijkt het toch nog van belang, met name als het mozaïcisme zich uitstrekt tot buiten de dikke darm, kinderen vanaf 12 jaar wel DNA-onderzoek aan te bieden. Als er grotere aantallen uitkomsten van DNA-onderzoek bij kinderen beschikbaar zijn, kan dit beleid worden heroverwogen. Voor kinderen tussen de 30 en 40 jaar zonder klachten kan waarschijnlijk terughoudender zijn met het doen van DNA-onderzoek, zeker als de APC-mozaïek PV bij de ouder niet in andere weefsels wordt teruggevonden.
Door onderzoek naar APC-mozaïek werd ook duidelijk dat bij ongeveer een derde van de mensen sprake was van een APC c.835-8A>G variant, die past bij mutatie signaturen die wordt veroorzaakt door het gen toxine colibactine (Terlouw 2020, Terlouw 2024), een vorm van DNA-beschadiging door een toxine van de E. Coli bacterie. Meer onderzoek naar de rol van deze bacterie, die al commensaal vaker voorkomt in een groot deel van de bevolking (Secher 2016), is nodig voordat adviezen kunnen worden gegeven over eventuele (preventieve) behandeling en de gevolgen voor familieleden. Het is voor nu wel aannemelijk dat de aanwezigheid van deze signature/ APC variant wijst op een mogelijk niet-genetische oorzaak en er voor familieleden waarschijnlijk een minder verhoogd risico is om ook poliepen te ontwikkelen. Het is van belang dit punt over 3-5 jaar te herzien.
Balans tussen gewenste en ongewenste effecten
Bij patiënten met polyposis en hun naasten kunnen verschillende overwegingen meespelen in de keuze voor kiembaanonderzoek. Kiembaanonderzoek biedt in de meeste gevallen een beperkte opbrengst, vooral bij patiënten met minder dan 20 adenomateuze poliepen en oudere leeftijd (>50 jaar). Dit kan voor patiënten een reden zijn om af te zien van dit onderzoek, evenals de kosten (eigen risico) en praktische of emotionele belasting. Het niet verwezen worden voor genetisch onderzoek kan onzekerheid en zorgen over genetische risico’s vermijden. Echter, het vinden van een kiembaan variant of mozaïek (afhankelijk van het aantal poliepen varieert deze kans tussen de 5 en 90%) kan daarentegen ook juist duidelijkheid geven voor patiënt en familieleden en de mogelijkheid voor presymptomatisch onderzoek bij familieleden en deelname aan preventieve programma’s. Surveillance bij patiënt en met een hoog risico op poliep vorming en daarmee op CRC leidt tot een sterk verminderd risico op (laat stadium) CRC. Bij patiënten op oudere leeftijd en of met een slechte gezondheid zal DNA-onderzoek voor henzelf niet altijd meer van belang zijn maar dit kan wel van belang zijn voor familieleden. Er zijn geen studies bekend, die naar lange termijn opbrengst in de zin van overlevingswinst of gezondheidswinst hebben gekeken in relatie tot het wel of geen erfelijkheid onderzoek doen bij patiënten met polyposis.
Kostenaspecten
Op dit moment worden er naar verwachting zo’n 300 tot 500 patiënten per jaar verwezen voor erfelijkheidsonderzoek vanwege adenomateuze poliepen in het colorectum. De aanpassingen aan de criteria zullen naar verwachting niet leiden tot een toename van dit aantal. Bij beter toepassen van de criteria, grotendeels gelijk aan die uit 2015, omdat zij beter onderbouwd zijn, zal naar verwachting eerder leiden tot een afname van kosten.
De kosten van genetisch onderzoek (genetische counseling en gen-panel analyse) zijn zo’n 3000 euro. Deze kosten wegen doorgaans wel op tegen de opbrengsten – in geval er een kiembaan variant wordt gevonden kan gericht surveillance en preventieve ingrepen worden aangeboden aan familieleden met de aanleg en kosten voor eventuele kankerbehandeling worden voorkomen. Ook is er een afname van preventieve coloscopieën bij familieleden die een familiaire aanleg niet hebben en mogelijk van onterecht frequente scopieën wanneer geen aanleg in de familie wordt aangetoond.
Het verrichten van een passend gen panel in plaats van sequentieel testen is zowel voor het laboratorium als voor de patiënt doelmatiger en goedkoper. Het voorstel om bij een deel van de polyposis patiënten ook onderzoek te doen in poliepen naar eventueel voorkomen van een APC-mozaïek leidt tot extra werk en kosten. Aan de ander kant leidt het tot een afname van familieleden die controle-adviezen krijgen, omdat als er APC-mozaïek wordt vastgesteld, er geen controles van de darm meer nodig zijn voor familieleden.
Gelijkheid ((health) equity/equitable)
De interventie draagt bij aan gelijkheid in de zorg, omdat het duidelijke indicaties stelt voor genetisch onderzoek bij polyposis patiënten. Waar specifiek aanvullend onderzoek nodig is, wordt dit bepaald op basis van duidelijke klinische indicaties, waardoor een eerlijke en consistente aanpak wordt gehanteerd.
Erfelijkheidsonderzoek valt onder de basis verzekerde zorg, maar mensen zijn wel hun eigen bijdrage en eventueel eigen risico kwijt als zij geen andere medische kosten hebben.
Voor sommige mensen kan het moeten betalen van eventueel eigen risico een reden zijn om af te zien van erfelijkheidsonderzoek, of uit te stellen tot een jaar dat zij meer medische kosten hebben, wat wel ongelijkheid van zorg kan veroorzaken.
Aanvaardbaarheid:
Ethische aanvaardbaarheid
De diagnostiek lijkt aanvaardbaar voor de betrokkenen. Er zijn geen grote ethische bezwaren. Het genetisch onderzoek kan in een klein aantal gevallen tot extra onzekerheid leiden als er sprake is van een variant van onbekende betekenis (VUS). Het huidige beleid in Nederland is echter dat een VUS alleen gemeld wordt indien deze zeer verdacht is en/of nader onderzoek tot her classificatie kan leiden. In praktijk gaat dit om een zeer klein deel van de cases.
De aanbeveling om te werken met een panel voorkomt sequentieel testen en scheelt de zorg en de patiënt tijd en kosten. Als in genetisch testen beperkt wordt tot polyposis en/of CRC-syndromen, dan kan dat leiden tot het missen van andere tumor-predisposities zoals BRCA1/2 of TP53. Echter, de verwachting is dat als het gaat om een van deze genen, het familieverhaal hier vaak ook verdacht voor zal zijn en aanleiding om breder te testen. Het voordeel van restrictief testen is dat daarmee de kans op VUS en matig risico genen waarvoor geen controle adviezen gegeven worden, kleiner is. Bij niet westerse populaties is dit percentage mogelijk nog hoger aangezien er minder grote controle DNA-cohorten voor deze groepen nog beschikbaar zijn (gnomad).
Tenslotte kan het zijn dat een of meerdere familieleden geen DNA-onderzoek wil en andere wel. Dit is een algemeen probleem bij genetisch onderzoek. Patiënten kunnen nooit worden verplicht genetisch onderzoek te doen maar soms kan een uitslag bij een kind ook een uitslag voor een ouder betekenen. In principe gaat het recht in deze gevallen op het wel willen weten voor op niet willen weten.
Duurzaamheid
Bij de interventie spelen de duurzaamheidsaspecten een rol aangezien het doen van genetisch onderzoek een energie intensief onderzoek is. Goede criteria zorgen voor het doelmatig gebruik van genetisch onderzoek. Ook kan de uitslag hiervan leiden tot een verminderde noodzaak van coloscopieën bij familieleden of juist heel gericht aanbieden van controle en preventie en daarmee het voorkomen van kanker en daarbij horende behandelingen.
Haalbaarheid
De geformuleerde verwijscriteria zullen naar verwachting niet leiden tot extra belasting voor de klinisch genetische centra en de gen-panel diagnostiek is over het algemeen al standaard zorg in de klinisch genetische laboratoria. De toevoeging van onderzoek naar APC-mozaïek leidt tot meer werk en kosten, maar moleculaire diagnostiek wordt in toenemende mate al verricht in tumoren in het kader van behandelkeuzes. Ook leidt deze diagnostiek tot een reductie van onnodige coloscopieën bij familieleden als een mozaïek bij een polyposis patiënt wordt aangetoond. Naar verwachting zijn de voorgestelde adviezen in de praktijk dus haalbaar.
Rationale van aanbeveling-1: weging van argumenten voor en tegen de interventie
Eindoordeel: Sterke aanbeveling voor (Doen)
Rationale van aanbeveling-2: weging van argumenten voor en tegen de interventie
Eindoordeel: Sterke aanbeveling voor (Doen)
Onderbouwing
Achtergrond
If genetic testing is decided upon in an individual; with polyposis, submodule Verwijscriteria voor klinisch genetisch onderzoek bij adenomateuze polyposis the question is which DNA test should be offered. Next-generation sequencing (NGS), in which panels of multiple genes can be examined simultaneously, has become the standard. However, the most frequent findings are still APC and MUTYH pathogenic variants; variants in other genes associated with polyposis are rare. Another critical insight of recent years is that high frequency of APC mosaic mutations occurs in a subset of patients, which can only be detected with sensitive NGS in germline (leucocyte derived) DNA or by examining multiple polyps (Jansen, 2017). The question is, therefore, when and to whom additional testing for mosaicism should be offered.
Samenvatting literatuur
Description of the Guidelines
The European Hereditary Tumour Group (EHTG) guideline 2024 (Zaffaroni, 2024) recommends a multigene germline panel in patients with >20 cumulative colorectal adenomas. This guideline also recommends that multi-gene germline testing (for CRC and polyposis syndromes) is performed in patients with gastrointestinal cancers under 50. Finally, they advise that somatic mutation testing for APC mosaic should be considered in patients with unexplained polyposis, who meet the criteria for testing mentioned above.
The British guideline from 2020 (Monahan, 2020) recommends gene panel testing in cases with a lifetime total of ≥10 adenomas <60 years of age, or patients ≥60 years of age with a lifetime ≥20 adenomas, or ≥10 with a family history of multiple adenomas or CRC.
Description of studies
An overview of the outcome of genetic testing in adenomatous polyposis patients is given in Table 1 in submodule Verwijscriteria voor klinisch genetisch onderzoek bij adenomateuze polyposis.
Joo (2025)
This review describes the main autosomal dominant adenomatous polyposis syndromes, including familial adenomatous polyposis (FAP) and polymerase proofreading-associated polyposis (PPAP), which are caused by germline pathogenic variants (PVs) in the APC gene and the POLE and POLD1 genes, respectively. Autosomal recessive syndromes caused by biallelic PVs in the DNA mismatch repair genes (MLH1, MSH2, MSH6, PMS2, MSH3 and MLH3) and in the base excision repair genes (MUTYH, NTHL1, and MBD4) are also described.
Terlouw (2025)
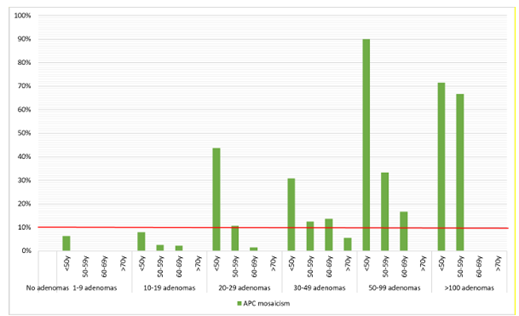
The rate of APC mosaicism was 9.4% in 541 patients with a broad spectrum of polyposis phenotypes. In patients who did not meet the scope of Dutch guidelines, the detection rate was 2.3% (5/219). In patients with ≥20 adenomas before the age of 60 or ≥30 adenomas before the age of 70, the detection rate was ≥10%. Of 34 mosaic patients who underwent an esophagogastroduodenoscopy, 26% were diagnosed with gastroduodenal polyps. In one patient, the mosaic variant was detected in semen, but none of the children tested in this cohort inherited the mosaic variant.
Figuur 1 (submodule Genetische testen bij adenomateuze polyposis): Detection rates of APC mosaicism subdivided in adenoma count groups and stratified for age at first adenoma.
Terlouw 2020 and Terlouw 2024 (PMID: 38238650 en PMID: 32603656)
In a cohort of approximately 400 polyposis patients tested somatically for APC mosaicism, a recurrent splice variant in APC c.835-8A>G was detected in a significant proportion of colorectal lesions. This variant fits a mutation signature caused by the genotoxin colibactin. Further analysis of all APC mutations showed that at least one APC variant was detected in approximately 30% of patients that matched a colibactin-associated mutation signature.
Georgeson 2024 (preprint)
Another recent study of a large cohort of CRCs also describes that occurrence of the signature SBS88 is strongly associated with the presence of the APC splice variant c.835-8A>G and thus further confirmed the association found by Terlouw, in 7.5% (398/5,292) of the intestinal CRCs examined.
Zoeken en selecteren
No systematic review of the literature was performed. To answer the following question, which genetic tests should be offered for adenomatous polyposis?” recent international guidelines were used; the EHTG, British and NCCN guideline (Monahan, 2020; NCCN, Hodan 2024). The EHTG guideline is based on a recent structured literature search (Zaffaroni, 2024). Articles of interest that were published after the publication of this guideline or were otherwise relevant were also included, these include: Terlouw, 2025; Georgeson, 2025; Disel, 2024; Aime, 2015; Joo, 2025.
Referenties
- Aimé A, Coulet F, Lefevre JH, Colas C, Cervera P, Flejou JF, Lascols O, Soubrier F, Parc Y. Somatic c.34G>T KRAS mutation: a new prescreening test for MUTYH-associated polyposis? Cancer Genet. 2015 Jul-Aug;208(7-8):390-5. doi: 10.1016/j.cancergen.2015.04.005. Epub 2015 Apr 23. PMID: 26056087.
- Alexander JL, Johnston BJ, Smith TJ, Yong KK, Marshall SM, Fawkes JDC, Martin JP, Seward EW, Saunders B, Monahan KJ. Low Referral Rates for Genetic Assessment of Patients With Multiple Adenomas in United Kingdom Bowel Cancer Screening Programs. Dis Colon Rectum. 2021 Sep 1;64(9):1058-1063. doi: 10.1097/DCR.0000000000001972. PMID: 34039904.
- Disel U, Sivakumar S, Pham T, Fleischmann Z, Anu RI, Sokol ES, Kurzrock R. Increased KRAS G12C Prevalence, High Tumor Mutational Burden, and Specific Mutational Signatures Are Associated With MUTYH Mutations: A Pan-Cancer Analysis. Oncologist. 2024 Feb 2;29(2):e213-e223. doi: 10.1093/oncolo/oyad230. PMID: 37589222; PMCID: PMC10836311.
- Georgeson P, Steinfelder RS, Harrison TA, Pope BJ, Zaidi SH, Qu C, Lin Y, Joo JE, Mahmood K, Clendenning M, Walker R, Aglago EK, Berndt SI, Brenner H, Campbell PT, Cao Y, Chan AT, Chang-Claude J, Dimou N, Doheny KF, Drew DA, Figueiredo JC, French AJ, Gallinger S, Giannakis M, Giles GG, Goode EL, Gruber SB, Gsur A, Gunter MJ, Harlid S, Hoffmeister M, Hsu L, Huang WY, Huyghe JR, Manson JE, Moreno V, Murphy N, Nassir R, Newton CC, Nowak JA, Obón-Santacana M, Ogino S, Pai RK, Papadimitrou N, Potter JD, Schoen RE, Song M, Sun W, Toland AE, Trinh QM, Tsilidis K, Ugai T, Um CY, Macrae FA, Rosty C, Hudson TJ, Winship IM, Phipps AI, Jenkins MA, Peters U, Buchanan DD. Genotoxic colibactin mutational signature in colorectal cancer is associated with clinicopathological features, specific genomic alterations and better survival. medRxiv [Preprint]. 2024 Jan 30:2023.03.10.23287127. doi: 10.1101/2023.03.10.23287127. PMID: 37090539; PMCID: PMC10120801.
- Goldberg Y, Aleme O, Peled-Perets L, Castellvi-Bel S, Nielsen M, Shalev SA. MCM9 is associated with germline predisposition to early-onset cancer-clinical evidence. NPJ Genom Med. 2021 Sep 23;6(1):78. doi: 10.1038/s41525-021-00242-4. PMID: 34556653; PMCID: PMC8460657.
- Grover S, Kastrinos F, Steyerberg EW, Cook EF, Dewanwala A, Burbidge LA, Wenstrup RJ, Syngal S. Prevalence and phenotypes of APC and MUTYH mutations in patients with multiple colorectal adenomas. JAMA. 2012 Aug 1;308(5):485-492. doi: 10.1001/jama.2012.8780. PMID: 22851115; PMCID: PMC3770297.
- Helderman NC, Terlouw D, Bonjoch L, Golubicki M, Antelo M, Morreau H, van Wezel T, Castellví-Bel S, Goldberg Y, Nielsen M. Molecular functions of MCM8 and MCM9 and their associated pathologies. iScience. 2023 Apr 27;26(6):106737. doi: 10.1016/j.isci.2023.106737. PMID: 37378315; PMCID: PMC10291252.
- Jaeger E, Leedham S, Lewis A, Segditsas S, Becker M, Cuadrado PR, Davis H, Kaur K, Heinimann K, Howarth K; HMPS Collaboration; East J, Taylor J, Thomas H, Tomlinson I. Hereditary mixed polyposis syndrome is caused by a 40-kb upstream duplication that leads to increased and ectopic expression of the BMP antagonist GREM1. Nat Genet. 2012 May 6;44(6):699-703. doi: 10.1038/ng.2263. PMID: 22561515; PMCID: PMC4594751.
- Jansen AM, Crobach S, Geurts-Giele WR, van den Akker BE, Garcia MV, Ruano D, Nielsen M, Tops CM, Wijnen JT, Hes FJ, van Wezel T, Dinjens WN, Morreau H. Distinct Patterns of Somatic Mosaicism in the APC Gene in Neoplasms From Patients With Unexplained Adenomatous Polyposis. Gastroenterology. 2017 Feb;152(3):546-549.e3. doi: 10.1053/j.gastro.2016.10.040. Epub 2016 Nov 2. PMID: 27816598.
- Joo JE, Viana-Errasti J, Buchanan DD, Valle L. Genetics, genomics and clinical features of adenomatous polyposis. Fam Cancer. 2025 Apr 16;24(2):38. doi: 10.1007/s10689-025-00460-0. PMID: 40237887; PMCID: PMC12003455.
- McKenna DB, Van Den Akker J, Zhou AY, Ryan L, Leon A, O'Connor R, Shah PD, Rustgi AK, Katona BW. Identification of a novel GREM1 duplication in a patient with multiple colon polyps. Fam Cancer. 2019 Jan;18(1):63-66. doi: 10.1007/s10689-018-0090-6. PMID: 29804199; PMCID: PMC6261785.
- Monahan KJ, Bradshaw N, Dolwani S, Desouza B, Dunlop MG, East JE, Ilyas M, Kaur A, Lalloo F, Latchford A, Rutter MD, Tomlinson I, Thomas HJW, Hill J; Hereditary CRC guidelines eDelphi consensus group. Guidelines for the management of hereditary colorectal cancer from the British Society of Gastroenterology (BSG)/Association of Coloproctology of Great Britain and Ireland (ACPGBI)/United Kingdom Cancer Genetics Group (UKCGG). Gut. 2020 Mar;69(3):411-444. doi: 10.1136/gutjnl-2019-319915. Epub 2019 Nov 28. PMID: 31780574; PMCID: PMC7034349.
- Stanich PP, Pearlman R, Hinton A, Gutierrez S, LaDuca H, Hampel H, Jasperson K. Prevalence of Germline Mutations in Polyposis and Colorectal Cancer-Associated Genes in Patients With Multiple Colorectal Polyps. Clin Gastroenterol Hepatol. 2019 Sep;17(10):2008-2015.e3. doi: 10.1016/j.cgh.2018.12.008. Epub 2018 Dec 14. PMID: 30557735.
- Terlouw D, Suerink M, Buitelaar Y, van Leerdam ME, Hes FJ, van Egmond D, Ruano D, Wagner A, Groenendijk FH, Meijssen IC, Overwater E, Bajwa-Ten Broeke SW, MensenkampAR, Nagtegaal ID, Tops CM, Langers AMJ, van Wezel T, Morreau H, Nielsen, M. Prevalence and consequences of APC mosaicism in patients with colorectal adenomas. [preprint] doi: https://doi.org/10.1101/2025.02.18.25322465
- Thompson BA, Snow AK, Koptiuch C, Kohlmann WK, Mooney R, Johnson S, Huff CD, Yu Y, Teerlink CC, Feng BJ, Neklason DW, Cannon-Albright LA, Tavtigian SV. A novel ribosomal protein S20 variant in a family with unexplained colorectal cancer and polyposis. Clin Genet. 2020 Jun;97(6):943-944. doi: 10.1111/cge.13757. PMID: 32424863.
- Valle L, Monahan KJ. Genetic predisposition to gastrointestinal polyposis: syndromes, tumour features, genetic testing, and clinical management. Lancet Gastroenterol Hepatol. 2024 Jan;9(1):68-82. doi: 10.1016/S2468-1253(23)00240-6. Epub 2023 Nov 4. PMID: 37931640.
- van Hees F, Saini SD, Lansdorp-Vogelaar I, Vijan S, Meester RG, de Koning HJ, Zauber AG, van Ballegooijen M. Personalizing colonoscopy screening for elderly individuals based on screening history, cancer risk, and comorbidity status could increase cost effectiveness. Gastroenterology. 2015 Nov;149(6):1425-37. doi: 10.1053/j.gastro.2015.07.042. Epub 2015 Aug 4. PMID: 26253304; PMCID: PMC4631390.
- van Puijenbroek M, Nielsen M, Tops CM, Halfwerk H, Vasen HF, Weiss MM, van Wezel T, Hes FJ, Morreau H. Identification of patients with (atypical) MUTYH-associated polyposis by KRAS2 c.34G > T prescreening followed by MUTYH hotspot analysis in formalin-fixed paraffin-embedded tissue. Clin Cancer Res. 2008 Jan 1;14(1):139-42. doi: 10.1158/1078-0432.CCR-07-1705. PMID: 18172263.
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 29-09-2025
Beoordeeld op geldigheid : 15-09-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Belangrijkste wijzigingen t.o.v. vorige versie:
|
Onderwerp |
Wijzigingen meest recente versie |
|
Module 1: Diagnostiek en verwijzing |
|
|
Module 2: Familiair colorectaal carcinoom |
|
|
Module 3: Lynch syndroom |
|
|
Module 4: Adenomateuze polyposis |
|
|
Module 5: Serrated polyposis en overige vormen van polyposis |
|
|
Andere aanpassingen |
|
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met Erfelijke darmkanker.
Werkgroep
- dr. M. (Maartje) Nielsen (voorzitter), Klinisch geneticus, Leids Universitair Medisch Centrum, Leiden, VKGN
- prof. dr. N. (Nicoline) Hoogerbrugge, internist, Radboud UMC, Nijmegen, VKGN
- dr. A. (Anja) Wagner, Klinisch geneticus, Erasmus MC Kanker Instituut, Universitair Medisch Centrum Rotterdam, Rotterdam, VKGN
- dr. S.W. (Sanne) Bajwa – ten Broeke, Klinisch geneticus, Universitair Medisch Centrum Groningen, Groningen, VKGN
- prof. Dr. M.E. (Monique) van Leerdam, MDL-arts, Nederlands Kanker Instituut, Amsterdam, Leiden University Medical Center, NVMDL
- dr. T.M. (Tanya) Bisseling, MDL-arts, Radboud UMC, Nijmegen, NVMDL
- dr. M.C.A. (Mariëtte) van Kouwen, MDL-arts, Radboud UMC, Nijmegen, NVMDL
- prof. Dr. E. (Evelien) Dekker, MDL-arts, Amsterdam UMC, Amsterdam, NVMDL
- drs. H. (Hicham) Bouchiba, Arts-onderzoeker MDL, Amsterdam UMC, Amsterdam, persoonlijke titel
- dr. C.J. (Charlotte) Verberne, Chirurg, Ziekenhuis Amstelland, Amstelveen
- dr. J.M. (Jorien) Woolderink, Gynaecoloog, Martini Ziekenhuis, Groningen, NVOG
- dr. R.S. (Chella) van der Post, Patholoog, Radboud UMC, Nijmegen, NVVP
- dr. J.E. (Jurgen) Seppen, Patiëntvertegenwoordiger, Stichting Lynch Polyposis
- dr. A.R. (Arjen) Mensenkamp, laboratoriumspecialist Klinische genetica, Radboud UMC, Nijmegen, VKGL
- dr. C.M.J. (Carli) Tops, laboratoriumspecialist Klinische genetica, Leids Universitair Medisch Centrum, Leiden, VKGL
- I.J.H. (Ivonne) Schoenaker, Verpleegkundig specialist MDL, Isala Ziekenhuis, Zwolle, V&VN oncologie
- L.J.(Lisette) Saveur, Verpleegkundig specialist MDL, Nederlands Kanker Instituut, Amsterdam, V&VN oncologie
Klankbordgroep:
- Dr. F.J.B. (Fränzel) van Duijnhoven, Universitair hoofddocent voeding, genen en kanker WUR, Wageningen, persoonlijke titel
- Dr. J.A.J. (Job) Verdonschot, AIOS klinische Genetica, Maastricht Universitair Medisch Centrum, Maastricht, persoonlijke titel
- Dr. A.G. (Toine) van der Heijden, Oncologisch uroloog, Radboud UMC, Nijmegen, persoonlijke titel
Met ondersteuning van
- dr. J. (Joppe) Tra, Senior-Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. D. (Dagmar) Nieboer, Senior-Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. J. (Josefien) Buddeke, Senior-Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. M. (Mirre) den Ouden-Vierwind, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. M. (Merel) Wassenaar, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. A.C. (Anniek) van Westing, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. L. (Leanne) Küpers, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. J. (Jing) de Haan- Du, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. S.N. (Sarah) van Duijn, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. M. (Majke) van Bommel, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- drs. E. (Evie) Verweg, Junior Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- D.P. (Diana) Gutierrez, projectsecretaresse, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een (sub-) module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Werkgroepleden |
||||
|
Nielsen |
Klinisch geneticus, volledig betaald door de afdeling. |
2012 - present: the International Society for Gastrointestinal Hereditary Tumors (InSiGHT)
Betaling per bijeenkomst (vacation money for expenses made)
Lid adviesraad Stichting Lynch- Polyposis (onbetaald) |
Lopende subsidiegelden – waar ik bij betrokken bij ben:
|
Geen |
|
Hoogerbrugge – van der Linden |
Medisch specialist en hoogleraar erfelijke kanker
|
Geen |
Geen extern gefinancierd onderzoek in relatie tot deze functie |
Geen |
|
Wagner |
Klinisch geneticus |
Bestuurslid Stichting Opsporing Erfelijke tumoren (onbetaald); |
Extern gefinancierd onderzoek. WP3 leider KWF-project nr: 14976 (Smart measurement of circulating tumour DNA: a tumour-agnostic computational tool to improve CRC-care) |
Geen |
|
Bajwa – ten Broeke |
Klinische geneticus UMCG PI, betaald (vanuit KWF-subsidie) |
Lid European Hereditary Tumor Group (onbetaald), Bestuurslid DCCG |
Ja, subsidie voor onderzoek door KWF (young investigator grant), 2021-2025 |
Geen |
|
Van Leerdam |
MDL-arts Antoni van Leeuwenhoek, Amsterdam (0,6 FTE) betaald
|
Medisch directeur stichting opsporing erfelijke tumoren, Leiden, onbetaald |
Extern gefinancierd onderzoek |
Geen |
|
Bisseling |
MDL-arts Radboud UMC 0.9 fte |
Geen |
Geen |
Geen |
|
Van Kouwen |
Maag-Darm-Leverarts Radboud UMC Nijmegen |
Geen |
Geen |
Geen |
|
Dekker |
Maag-Darm-Leverarts, FT, Amsterdam UMC (betaald)
|
Lid raad van Commissarissen The eNose Company (betaald)
|
I have received honorarium for consultancy* from FujiFilm, Olympus, GI Supply, PAION and Ambu, and speakers' fees from Olympus, GI Supply, Norgine, IPSEN, PAION and FujiFilm. -Studies gefinancierd door KWF, MLDS, TKI, ZonMW, Celtic, FujiFilm. * Single meeting about development, innovation and research |
Geen
Geen deelname aan adviesraden gedurende de richtlijnontwikkeling |
|
Bouchiba |
PhD kandidaat/Arts-onderzoeker maag-darm-leverziekten Amsterdam UMC. |
Geen |
Geen |
Geen |
|
Verberne |
Chirurg in het ziekenhuis Amstelland, Amstelveen |
Geen |
Geen |
Geen |
|
Woolderink |
Gynaecoloog, Martini Ziekenhuis Groningen |
Lid adviesraad Stichting Lynch- Polyposis (onbetaald) |
Geen |
Geen |
|
Van der Post |
Patholoog, Radboud UMC
|
Bestuurslid Stichting Opsporing Erfelijke tumoren (onbetaald) |
Geen extern gefinancierd onderzoek in relatie tot deze functie |
Geen |
|
Seppen |
Universitair hoofddocent, Amsterdam UMC |
Bestuurslid Stichting Lynch Polyposis |
Geen |
Geen |
|
Mensenkamp |
Laboratoriumspecialist klinische genetica, Radboud UMC Nijmegen |
Voorzitter landelijk overleg erfelijke borstkankerdiagnostiek (LOB)
|
-Medewerking verleend aan workshops variantclassificatie en betrokken als assessor bij kwaliteitsrondzendingen BRCA-diagnostiek op tumorweefsel (EMQN/GenQA, gesponsord door AstraZeneca, betaald aan de afdeling Genetica) -VCo-applicant CRAFT project bij KWF. |
Geen |
|
Tops |
Laboratorium specialist klinische genetica, KG, LUMC
|
Geen |
KWF 14469 - Functionele test Lynch genen - Geen projectleider |
Geen |
|
Schoenaker |
Verpleegkundige specialist AGZ (MDL Oncologie) Isala, betaald
|
Geen |
EASIER study; Electronic nose for breath Analysis after curative Surgery to detect dIstant mEtastases or locoregional Recurrence of colon cancer |
Geen |
|
Saveur |
Verpleegkundig specialist Antoni van Leeuwenhoek |
Geen |
Geen |
Geen |
|
|
||||
|
Klankbordgroepleden |
||||
|
Van Duijnhoven |
Associate Professor
|
Geen |
Onderzoeksproject gefinancierd door World Cancer Research Fund/ Wereld Kanker Onderzoek Fonds |
Geen |
|
Verdonschot |
AIOS Klinische Genetica, MUMC+ |
Geen |
Geen |
Geen |
|
Van der Heijden |
Oncologisch uroloog
|
Geen |
ZonMW; BladParadigm; RCT mpMRI versus TURT.Projectleider ja |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door afvaardiging vanuit de patiëntenvereniging Stichting Lynch Polyposis in de werkgroep. De afgevaardigde heeft meebeslist bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen.
De conceptrichtlijn is tevens voor commentaar voorgelegd aan Stichting Lynch Polyposis de Nederlandse Federatie van Kankerpatiëntenorganisaties (NFK). De eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
|
Module |
Uitkomst raming |
Toelichting |
|
Submodule Genetische testen bij adenomateuze polyposis |
Geen mogelijk financiële gevolgen |
Uit de toetsing volgt dat de aanbevelingen niet breed toepasbaar zijn (<5.000 patiënten) en daarom naar verwachting geen substantiële financiële gevolgen zullen hebben voor de collectieve uitgaven. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep schriftelijk de knelpunten in de zorg voor patiënten met Erfelijke darmkanker. Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
er is hoge zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; het is zeer onwaarschijnlijk dat de literatuurconclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Redelijk |
er is redelijke zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; het is mogelijk dat de conclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Laag |
er is lage zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; er is een reële kans dat de conclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Zeer laag |
er is zeer lage zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; de literatuurconclusie is zeer onzeker. |
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Voor- en nadelen van interventies dienen goed met de patiënt te worden doorgenomen.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.