Decompressie van de maag
Uitgangsvraag
Wat is de waarde van decompressie van de maag middels plaatsing van een maaghevel in de behandeling van strengileus?
Aanbeveling
Plaats altijd een maaghevel op afloop indien:
- indicatie voor spoedoperatie;
- persisterend braken ondanks anti-emetica.
Voer maagdecompressie niet standaard uit bij:
- Ervaringsdeskundige patiënt (recidiverend, die goede eigen inschatting kan maken op basis van eerdere ervaringen);
- Beperkte distensie van de maag en misselijkheid die met medicatie te onderdrukken is;
- Patiënten voor wie het plaatsen van een neus/maaghevel traumatisch is [modulerend, met bovenstaand punt].
Overwegingen
Balans tussen gewenste en ongewenste effecten
Er is een systematisch literatuuronderzoek uitgevoerd naar de effectiviteit van het niet toepassen van een maaghevel vergeleken met toepassing van maaghevel in patiënten met strengileus. Er werden drie observationele studies geïncludeerd die deze vergelijking onderzochten, waarvan 2 studies ileus als geheel onderzochten in plaats van specifiek strengileus. De richting van het effect op de gerapporteerde resultaten voor de uitkomstmaten pneumonie, verblijfsduur in het ziekenhuis, operatief ingrijpen, voedingsstatus en mortaliteit was in het voordeel van de patiënten die geen maaghevel ontvingen. Voor de uitkomstmaat frequentie van braken was de richting van het effect (niet significant) in het voordeel van de patiënten die wel een maaghevel ontvingen. Hoewel voor sommige van deze uitkomstmaten klinisch relevante verschillen werden gevonden (zie resultaten), was de bewijskracht voor deze vergelijkingen zeer laag waardoor er geen conclusies getrokken konden worden over verschillen in effectiviteit. De uitkomstmaten terugkeer van darmfunctie, patiënttevredenheid en IC opname werden niet gerapporteerd in de geïncludeerde studies.
De bewijskracht van de vergelijkingen was zeer laag vanwege verschillende redenen. Ondanks dat het aannemelijk is dat het overgrote deel van de geïncludeerde patiënten ASBO (adhesive small bowel obstruction = strengileus) had, werd er afgewaardeerd voor indirectheid omdat er in 2 van de 3 studies patiënten met SBO (small bowel obstruction = ileus) werden geïncludeerd. Daarnaast werd er afgewaardeerd voor imprecisie, vanwege grote betrouwbaarheidsintervallen.
Tevens is er voor alle geïncludeerde studies sprake van beperkingen in studieopzet en -uitvoering (risk of bias), waarvoor afwaardering op zijn plaats is. Er is bijvoorbeeld niet duidelijk wat de reden was dat de ene patiënt een maaghevel kreeg en de ander niet. Het is aannemelijk dat de reden voor maagdecompressie (dus los van daadwerkelijke maagdecompressie zelf) effect heeft gehad op de uitkomstmaten (selectiebias). Het verschil in groepen is onder andere te zien in de studie naar SBO patiënten van Berman (2017) waarbij in de groep met maaghevel significant meer patiënten ouder dan 70 jaar zijn met coronairlijden. Daarnaast zit er in de studie naar ASBO patiënten van Shinohara (2022) een groot verschil tussen beide groepen wat betreft het maagvolume op CT (240ml in decompressie groep vs. 70 ml in de groep zonder decompressie).
Verder valt op dat de gemiddelde opnameduur in de interventiegroep een stuk langer is dan wat hier in Nederland geaccepteerd wordt als maximale duur bij patiënten met conservatieve trial, waardoor men zich kan afvragen in hoeverre de resultaten vertaalbaar zijn naar de Nederlandse praktijk.
Om met zekerheid uitspraken te kunnen doen over gewenste en ongewenste effecten van maagdecompressie middels een maaghevel, is het nodig gerandomiseerd onderzoek te doen onder patiënten met een strengileus (ASBO) zonder indicatie voor een spoedoperatie. Zie ook verderop deze module onder ‘kennisvragen’.
Het plaatsen van maaghevels is geassocieerd met complicaties en significant ongemak (Essenhigh DM. Gastric decompression after abdominal surgery. BMJ 1973;1:547–8.). Voor patiënten met ASBO die een indicatie voor spoedoperatie hebben, is het echter wenselijk dat de maag gedecomprimeerd wordt om meer ruimte ter creëren voor de operateur tijdens de operatie. Op basis van theoretische gronden lijkt het logisch om bij patiënten die persisterend braken ondanks anti-emetica een maaghevel in te brengen met als doel de frequentie van braken en daarmee samenhangend risico op aspiratie te verminderen.
Ondanks de theoretische voordelen van maagdecompressie bij ASBO patiënten, is het gezien het gebrek aan bewijs hiervan te overwegen om maagdecompressie achterwege te laten bij de volgende patiënten: ervaringsdeskundige patiënten met geringe dan wel afwezigheid van complicaties in eerdere episoden, patiënten bij wie het plaatsen van een maaghevel moeizaam/traumatisch is en patiënten met een beperkte maagdistentie en misselijkheid/braken die goed reageert op anti-emetica.
Ondanks dat de literatuur geen uitsluitsel geeft over de effecten is de werkgroep van mening dat het plaatsen van een maaghevel de standaard praktijk moet blijven bij indicatie voor spoedoperatie en persisterend braken en het niet toepassen van een maaghevel overwogen kan worden in specifieke gevallen.
De waarde van wateroplosbaar contrast staat los van deze module en wordt beschreven in module Therapeutische waarde wateroplosbaar contrast.
Over de plaats van maagdecompressie bij zwangere vrouwen met een strengileus is geen literatuur beschikbaar. In principe geldt voor hen dezelfde aanbeveling als niet zwangeren. Voor meer aandachtspunten ten aanzien van zwangere vrouwen wordt verwezen naar module Aandachtspunten voor het herkennen en behandelen van strengileus bij bijzondere groepen.
Kwaliteit van bewijs
De overall kwaliteit van bewijs is zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten.
Er is afgewaardeerd vanwege ernstige:
- Indirectheid: indirectheid van het bewijs, door verschillen in populatie.
- Imprecisie: onnauwkeurigheid, omdat het betrouwbaarheidsinterval de grens/beide grenzen van klinische relevantie overschrijdt.
- Beperkingen in studieopzet en -uitvoering met hoog risico op bias.
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
De resultaten zijn erg onzeker wat betreft gewenste en ongewenste effecten voor patiëntrelevante uitkomstmaten vanwege vertekening van resultaten door selectiebias. Er lijkt in de huidige observationele studies onder andere sprake te zijn van een langere ligduur bij patiënten die maagdecompressie ontvangen. Dit zou effect kunnen hebben op de voorkeur van patiënten met betrekking tot het wel of niet ondergaan van maagdecompressie. Verder is het invoelbaar dat een ervaringsdeskundige patiënt die in het verleden een conservatief behandelde strengileus heeft gehad zonder complicaties, liever niet opteert voor een maaghevel indien dit eerder ook niet nodig was. In verlengde hiervan kan een eerdere traumatische ervaring met het inbrengen van een maaghevel een patiënt ertoe bewegen een nieuwe maaghevel te weigeren.
Kostenaspecten
De interventie levert meer kosten ten opzichte van de controle behandeling. Het is onbekend of dit opweegt tegen het eventuele verschil in effectiviteit. Het inbrengen van een maaghevel brengt an sich meer kosten met zich mee, aangezien hiervoor materialen en geschoold personeel vereist is. De uiteindelijke winst (mogelijk minder operaties/opname dagen/IC opnames/lagere mortaliteit) is niet goed genoeg onderzocht, waardoor over de netto kosten geen zinnige uitspraken gedaan kunnen worden behoudens dat de interventie nu geld kost zonder duidelijk aangetoonde winst.
Gelijkheid ((health) equity/equitable)
De interventie leidt niet tot een mogelijke toe- of afname van gezondheidsgelijkheid omdat iedereen die mogelijk een maaghevel krijgt, toch al opgenomen wordt, daarmee zijn eigen risico kwijt is en dus niet meer kosten zal maken dan iemand die de interventie (maaghevel) niet krijgt.
Aanvaardbaarheid:
Ethische aanvaardbaarheid
De interventie is niet aanvaardbaar voor alle betrokkenen. De werkgroep voorziet ethische bezwaren, namelijk dat het inbrengen van een maaghevel voor patiënten als traumatisch en erg pijnlijk kan worden ervaren. De afwezigheid van duidelijke gezondheidswinst zorgt er voor dat de pijn en traumatische ervaring voor patiënten niet goed gerechtvaardigd kan worden op basis van de huidige observationele onderzoeken. Hooguit dus op basis van fysiologische gronden en expert opinion (zie eerdere overwegingen).
Duurzaamheid
Bij de interventie spelen de volgende duurzaamheidsaspecten een rol.
Het inbrengen van een maaghevel levert meer afval op dan het niet inbrengen van een maaghevel. Hierbij zijn naast steriel verpakte materialen, ook eventuele spuiten om maagretentie te bepalen nodig.
Haalbaarheid
De interventie is haalbaar en is over het algemeen al standaardzorg in de praktijk.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Er is geen gerandomiseerd onderzoek verricht naar de waarde van maagdecompressie bij patiënten met strengileus. Maagdecompressie zou mogelijk kunnen leiden tot minder braken maar is niet significant aangetoond. Daar staat tegenover dat het lijkt alsof maagdecompressie leid tot significant meer pneumonieën en operaties, en een langere opnameduur en tijd tot orale intake. Deze resultaten moeten zeer voorzichtig geïnterpreteerd worden gezien het grote risico op selectiebias. Op basis van expert opinion is het plaatsen van een maaghevel aan te raden bij patiënten met een indicatie voor spoedoperatie omdat dit de operatie vergemakkelijkt. Daarnaast klinkt het logisch om bij patiënten die persisterend braken ondanks anti-emetica ook de maag te decomprimeren.
De overwegingen omtrent de kosten, gelijkheid, aanvaardbaarheid, duurzaamheid en haalbaarheid zijn volgens de werkgroep niet doorslaggevend in de aanbeveling.
Kortom, maagdecompressie bij patiënten met een strengileus is reeds jarenlang standaard, zonder kwalitatief goed bewijs in het voordeel danwel nadeel van decompressie. Gezien de kwaliteit van de evidence zeer matig is ligt hier een kennislacune en is er noodzaak tot gerandomiseerd onderzoek.
Eindoordeel:
Zwakke aanbeveling voor het achterwege laten van maagdecompressie bij geselecteerde patiënten.
Onderbouwing
The current standard of care is that patients receive gastric decompression by means of a gastric tube, with the aim of preventing aspiration and faster recovery from adhesive small bowel obstruction. Inserting a tube is experienced as traumatic and carries a risk of complications (aspiration, epistaxis). The value of using this tube is therefore under discussion.
Summary of Findings table: Nasogastric decompression compared to no nasogastric decompression for ASBO
Population: Patients with ABSO
Intervention: Nasogastric decompression
Comparator: No nasogastric decompression
|
Outcome
|
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence (Quality of evidence) |
Conclusions |
|
|
Nasogastric decompression |
No nasogastric decompression |
||||
|
Pneumonia
|
Based on data of 478 patients from 2 study
|
A pooled risk ratio of 8.44 (95% CI 1.08 to 65.82) was reported, in favor of the patients who did not receive nasogastric decompression. |
Very low Due to serious risk of bias, due to serious circumstantial evidence, due to serious imprecision |
The evidence is very uncertain about the effect of nasogastric decompression on pneumonia when compared with no nasogastric decompression in patients with (A)SBO (Fonseca, 2013; Shinohara, 2022) |
|
|
Length of stay |
Based on data of 759 patients from 3 study
|
Berman (2017) reported a mean difference of 2.8 days, Fonseca (2013) reported a mean difference of 6.98 days, and Shinohara (2022) reported a mean difference of 2 days, in favor of the patients who did not receive nasogastric decompression. |
Very low Due to serious risk of bias, due to serious circumstantial evidence, due to serious imprecision |
The evidence is very uncertain about the effect of nasogastric decompression on length of stay when compared with no nasogastric decompression in patients with (A)SBO (Berman, 2017; Fonseca, 2013; Shinohara, 2022) |
|
|
Need for surgery
|
Based on data of 759 patients from 3 studies
|
A pooled risk ratio of 1.51 (95% CI 1.10 to 2.07) was reported, in favor of the patients who did not receive nasogastric decompression. |
Very low Due to serious risk of bias, due to serious circumstantial evidence, due to serious imprecision |
The evidence is very uncertain about the effect of nasogastric decompression on need for surgery when compared with no nasogastric decompression in patients with (A)SBO (Berman, 2017; Fonseca, 2013; Shinohara, 2022) |
|
|
Return of bowel function |
|
|
No GRADE (no evidence was found) |
No evidence was found regarding the effect of nasogastric decompression on return of bowel function when compared with no nasogastric decompression in patients with (A)SBO |
|
|
Nutritional status |
Based on data of 288 patients from 1 study |
Shinohara (2022) reported a mean difference of 1 day, in favor of the patients who did not receive nasogastric decompression. |
Very low Due to serious risk of bias, due to serious imprecision |
The evidence is very uncertain about the effect of nasogastric decompression on nutritional status when compared with no nasogastric decompression in patients with (A)SBO (Shinohara, 2022) |
|
|
Patient satisfaction |
|
. |
No GRADE (no evidence was found) |
No evidence was found regarding the effect of nasogastric decompression on patient satisfaction when compared with no nasogastric decompression in patients with (A)SBO |
|
|
Mortality |
Based on data of 469 patients from 2 studies |
A pooled risk difference of 0.01 (95% CI -0.01 to 0.03) was reported, in favor of the patients who did not receive nasogastric decompression. |
Very low Due to serious risk of bias, due to serious circumstantial evidence, due to serious imprecision |
The evidence is very uncertain about the effect of nasogastric decompression on mortality when compared with no nasogastric decompression in patients with (A)SBO (Berman, 2017; Shinohara, 2022) |
|
|
ICU admission |
|
|
No GRADE (no evidence was found) |
No evidence was found regarding the effect of nasogastric decompression on ICU admission when compared with no nasogastric decompression in patients with (A)SBO |
|
|
Vomiting frequency |
Based on data of 288 patients from 1 study |
Shinohara (2022) reported a relative risk of 0.68 (95% CI 0.29 to 1.17), in favor of the patients who received nasogastric decompression. |
Very low Due to serious risk of bias, due to serious imprecision |
The evidence is very uncertain about the effect of nasogastric decompression on vomiting frequency when compared with no nasogastric decompression in patients with (A)SBO (Shinohara, 2022) |
|
Description of studies
A total of three studies were included in the analysis of the literature. Important study characteristics and results are summarized in table 2. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Berman (2017) performed a retrospective observational study to determine if nasogastric decompression was associated with the following clinical outcomes: rate of surgery, rate of bowel resection, and hospital length of stay. The study was performed in a single center urban tertiary care hospital associated with a medical school. Patients with all likely ICD-9 codes that may have been linked to SBO, and with a confirmatory CT scan or a CT scan with the likelihood of SBO classified as definite or likely/early were included. Patients who were older than 70 years, patients with a prior history of coronary artery disease (CAD), malignancy or prior SBO were more likely to received nasogastric decompression.
Fonseca (2013) performed a retrospective review to evaluate the use of NGT decompression and potentially identify the presenting characteristics of patients with SBO who could be safely managed without the use of a NGT. The study was performed in a single center. Patients with adhesive or malignant SBOs as well as all other causes of clinical SBO for which the etiology was not clinically evident were included in the analysis. Patients with diabetes, who underwent CT imaging, and CT scan documenting the absence of colonic aire were more likely to receive nasogastric decompression. Abdominal distension and tympany were negatively associated with nasogastric decompression.
Shinohara (2022) performed a retrospective review to examine whether non-NGT decompression for patients with adhesive SBO increased the risk of unfavorable clinical outcomes, that is, vomiting, pneumonia, and the need for surgery. The study was performed in a single center. Patients with the diagnosis of adhesive SBO were included in the analysis. Patients who received nasogastric decompression had a higher gastric volume on CT images.
Table 2. Characteristics of included studies
|
Study |
Participants |
Comparison |
Follow-up |
Outcome measures |
Comments |
Risk of bias (per outcome measure)* |
|
Individual studies |
||||||
|
Berman, 2017 |
N at baseline I: 93 C: 88
Age 18-29 (%) I: 3% C: 10%
Age 20-49 (%) I: 18% C: 30%
Age 50-69 (%) I: 42% C: 41%
Age 70+ (%) I: 37% C: 19%
Sex (male, %) I: 51% C: 57%
Prior SBO: I: 56%
Prior abdominal surgery: I: 88% |
Intervention: Nasogastric decompression
Control: No nasogastric decompression |
NA |
Surgery this hospitalization: I: 29 (31%) C: 20 (23%)
Surgery on Hospital day:
I: 25% C: 30%
I: 38% C: 25%
I: 3% C: 20%
I: 14% C: 10%
I: 7% C: 0%
I: 0% C: 10%
I: 13% C: 5%
Mean hospital length of stay (days): I: 7.0 C: 4.2
Mortality: I: 3% C: 2% |
Patients with SBO1 Funding for medical students provided GWU Gill Fellowship |
HIGH |
|
Fonseca, 2013 |
N at baseline I: 235 C: 55
Age (mean ± SD) I: 58.71 ± 19.58 years C: 54.96 ± 16.74 years
Sex (male, %) I: 95 (40.43%) C: 22 (40%)
Prior SBO: I: 94 (40%)
Prior surgical intervention: I: 211 (89.79%) |
Intervention: Nasogastric decompression
Control: No nasogastric decompression |
NA |
Surgery required: I: 87/235 C: 13/55
Hospital length of stay (days): I: 10.16 C: 3.18
Hospital length of stay excluding patients who needed surgery: I: 9.57 C: 3.13
Pneumonia in patients who were successfully managed non-operatively: I: 16/138 C: 0/52 |
Patients with SBO1 |
HIGH |
|
Shinohara, 2022 |
N at baseline I: 140 C: 148
Age (median, range) I: 76 (17-96) C: 69.5 (30-102)
Sex (male, %) I: 74 (52.9%) C: 61 (41.2%)
Prior SBO: I: 57 (40.7%) C: 80 (54.1%)
Previous gastrointestinal surgery: I: 23 (16.4%) C: 25 (16.9%)
Previous colorectal surgery: I: 82 (58.6%) C: 80 (54.0%) |
Intervention: Nasogastric decompression or long-tube decompression
Control: No nasogastric decompression or long-tube decompression |
NA |
Surgical treatment: I: 18 (12.9%) C: 11 (7.4%)
Hospital length of stay (median, range (days)): I: 10 (2-99) C: 8 (1-55)
Pneumonia after admission: I: 2 (1.4%) C: 0 (0%)
Vomiting after admission: I: 18 (12.9%) C: 28 (18.9%)
Mortality: I: 2 (1.4%) C: 0 (0%)
Time to oral intake (median, range (days)): I: 5 (2-36) C: 4 (1-21) |
Patients with ASBO |
HIGH |
*For further details, see risk of bias table in the appendix
1 It can be expected that the vast majority of included patients with SBO suffers from ASBO
Results
Pneumonia (critical)
Two studies reported the outcome measure pneumonia (Fonseca, 2013; Shinohara, 2022).
Fonseca (2013) reported pneumonia in patients who were successfully managed non-operatively. In total, 16 of 138 patients (11.6%) who received nasogastric decompression had pneumonia, compared with none of the patients (0%) who did not receive nasogastric decompression. The risk ratio (RR) was 12.58 (95% CI 0.77 to 206.02), and the risk difference was 0.12 (95% CI 0.06 to 0.18), in favor of the patients who did not receive nasogastric decompression. This difference is considered clinically relevant.
Shinohara (2022) reported pneumonia after admission. In total, 2 of 140 patients (1.4%) who received nasogastric decompression had pneumonia, compared with none of the patients (0%) who did not receive nasogastric decompression. The risk ratio (RR) was 5.28 (95% CI 1.08 to 65.82), and the risk difference was 0.01 (95% CI -0.01 to 0.04), in favor of the patients who did not receive nasogastric decompression. This difference is not considered clinically relevant.
Length of stay (critical)
Three studies reported the outcome measure length of stay (Berman, 2017; Fonseca, 2013; Shinohara, 2022). The results could not be pooled due to differences in outcome reporting.
Berman (2017) reported mean hospital length of stay. In total, the patients who received nasogastric decompression (n=93) had a mean length of stay of 7.0 days, compared with a mean length of stay of 4.2 days for the patients who did not receive nasogastric decompression (n=88). The mean difference between the two groups was 2.8 days, in favor of the patients who did not received nasogastric decompression. This difference is considered clinically relevant.
Fonseca (2013) reported hospital length of stay. In total, the patients who received nasogastric decompression (n=235) had a mean length of stay of 10.16 days, compared with a mean length of stay of 3.18 days for the patients who did not receive nasogastric decompression (n=55). The mean difference between the two groups was 6.98 days, in favor of the patients who did not receive nasogastric decompression. This difference is considered clinically relevant.
Shinohara (2022) reported hospital length of stay. In total, the patients who received nasogastric decompression (n=140) had a median length of stay of 10 days (range 2-99 days), compared with a median length of stay of 8 days (range 1-55 days) for the patients who did not receive nasogastric decompression (n=148). The mean difference between the two groups was 2 days, in favor of the patients who did not received nasogastric decompression. This difference is considered clinically relevant.
Need for surgery (critical)
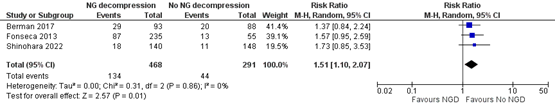
Three studies reported the outcome measure need for surgery (Berman, 2017; Fonseca, 2013; Shinohara, 2022). The results are presented in figure 1. In total, 134 of 468 patients (27.6%) who received nasogastric decompression underwent surgery, compared with 44 of 291 patients (15.1%) who did not receive nasogastric decompression. The RR was 1.51 (95% CI 1.10 to 2.07), in favor of the patients who did not receive nasogastric decompression. This difference is considered clinically relevant.
Figure 1. Need for surgery
Z: p-value of the pooled effect; df: degrees of freedom; I2: statistic heterogeneity; CI: Confidence Interval
Return of bowel function (important)
None of the included studies reported the outcome measure return of bowel function.
Nutritional status (important)
One study reported the outcome measure nutritional status (Shinohara, 2022).
Shinohara (2022) reported time to oral intake. The patients who received nasogastric decompression (n=140) had a median time to oral intake of 5 days (range 2-36 days), compared with a median time to oral intake of 4 days (range 1-21 days) for the patients who did not receive nasogastric decompression (n=148). The median difference between the two groups was 1 day, in favor of the patients that did not receive nasogastric decompression. This difference is considered clinically relevant.
Patient satisfaction (important)
None of the included studies reported the outcome measure patient satisfaction.
Mortality (important)
Two studies reported the outcome measure mortality (Berman, 2017; Shinohara, 2022).
In total, 3 of 93 patients (3%) who received nasogastric decompression died, compared with 2 of 88 patients (2%) who did not receive nasogastric decompression (Berman, 2017). The risk difference was 0.01 (95% CI -0.04 to 0.06), in favor of the patients who did not receive nasogastric decompression. This difference is not considered clinically relevant.
In total, 2 of 140 patients (1.4%) who received nasogastric decompression died, compared with 0 of 148 patients (0%) who did not receive nasogastric decompression (Shinohara, 2022). The risk difference was 0.01 (95% CI -0.01 to 0.04), in favor of the patients who did not receive nasogastric decompression. This difference is not considered clinically relevant.
ICU admission (important)
None of the included studies reported the outcome measure ICU admission.
Vomiting frequency (important)
One study reported the outcome measure vomiting frequency (Shinohara, 2022). In total, 18 of 140 patients (12.9%) who received nasogastric decompression vomited after admission, compared with 28 of 148 patients (18.9%) who did not receive nasogastric decompression. The RR was 0.68 (95% CI 0.39 to 1.17), in favor of the patients who received nasogastric decompression. This difference is considered clinically relevant.
A systematic review of the literature was performed to answer the following question(s):
What are favorable and unfavorable effects of a (naso)gastric decompression tube compared to no tube in patients with ASBO?
Table 1. PICO
|
Patients |
Patients with ASBO |
|
Intervention |
No (naso)gastric decompression tube |
|
Control |
(naso)gastric decompression tube |
|
Outcomes |
pneumonia (aspiration), length of stay, need for surgery, return of bowel function, nutritional status, patient satisfaction, mortality, ICU admission, vomiting frequency |
|
Other selection criteria |
Study design: systematic reviews, randomized controlled trials and observational studies |
Relevant outcome measures
The guideline panel considered pneumonia (aspiration), length of stay, need for surgery as critical outcome measures for decision making; and return of bowel function, nutritional status, patient satisfaction, mortality, ICU admission, vomiting frequency as important outcome measures for decision making.
A priori, the guideline panel did not define the outcome measures listed above but used the definitions used in the studies.
The guideline panel defined the following minimal clinically (patient) important differences:
- Pneumonia (aspiration): 25%: RR <0.8 or >1.25
- Length of stay: 1 day
- Need for surgery: 25%: RR <0.8 or >1.25
- Return of bowel function: 1 day
- Nutritional status: 1 day
- Patient satisfaction: 20%
- Mortality: 10%
- ICU admission: 10%
- Vomiting frequency: 25%: RR <0.8 or >1.25
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until 7 July 2024. The detailed search strategy is listed under the tab ‘Literature search strategy’. The systematic literature search resulted in 679 hits. Studies were selected based on the following criteria systematic reviews, RCTs and observational studies comparing no tube with decompression tube in patients with ASBO. Initially, thirteen studies were selected based on title and abstract screening. After reading the full text, ten studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and three studies were included.
- Berman DJ, Ijaz H, Alkhunaizi M, Kulie PE, Vaziri K, Richards LM, Meltzer AC. Nasogastric decompression not associated with a reduction in surgery or bowel ischemia for acute small bowel obstruction. Am J Emerg Med. 2017 Dec;35(12):1919-1921. doi: 10.1016/j.ajem.2017.08.029. Epub 2017 Aug 15. PMID: 28912083.
- Fonseca AL, Schuster KM, Maung AA, Kaplan LJ, Davis KA. Routine nasogastric decompression in small bowel obstruction: is it really necessary? Am Surg. 2013 Apr;79(4):422-8. PMID: 23574854.
- Shinohara K, Asaba Y, Ishida T, Maeta T, Suzuki M, Mizukami Y. Nonoperative management without nasogastric tube decompression for adhesive small bowel obstruction. Am J Surg. 2022 Jun;223(6):1179-1182. doi: 10.1016/j.amjsurg.2021.11.029. Epub 2021 Dec 2. PMID: 34872712.
Beoordelingsdatum en geldigheid
Publicatiedatum : 09-04-2026
Beoordeeld op geldigheid : 09-04-2026
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd door de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS)
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met schouderinstabiliteit.
Werkgroep richtlijn strengileus
- dr. R.P.G. (Richard) ten Broek, chirurg Radboud UMC, NVvH – voorzitter richtlijnwerkgroep
- dr. C. (Caroline) Andeweg, chirurg St. Jansdal Harderwijk, NVvH
- Prof. dr. M. (Marja) Boermeester, chirurg Amsterdam UMC, NVvH
- Dhr. dr. F.T.J. (Floris) Ferenschild, chirurg Radboud UMC, NVvH
- dr. H.A. (Harmke) Polinder-Bos, klinisch geriater Erasmus MC, NVKG
- Mevr. E. (Elif) Kilicoglu, diëtist, CWZ Nijmegen, NVD
- Mevr. drs. M.W. (Wiesje) Prins, radioloog Maasziekenhuis, NVvR
- drs. T.W. (Thomas) van den Goorbergh, spoedeisende hulp, St. Antonius Ziekenhuis Nieuwegein, NVSHA
- Mevr. S. (Silvie) Dronkers, ervaringsdeskundige en patiëntvertegenwoordiger Stichting Darmkanker Nederland † (in herinnering)
Klankbordgroep richtlijn strengileus
- dr. A. (Sander) van der Beek, internist Ziekenhuis Rivierenland, NIV
- dr. C. (Cor) de Kroon, gynaecoloog LUMC, NVOG
- Mevr. S.D.M. (Sabine) Theuns-Valks, kinderarts Albert Schweitzer Ziekenhuis, NVK
Met ondersteuning van
- dr. L.M. (Lisette) van Leeuwen, adviseur Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. E.R.L. (Evie) Verweg, junior adviseur Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Tabel 1 Gemelde (neven)functies en belangen werkgroep
|
Naam |
Hoofdfunctie |
Neven-werkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Werkgroepleden |
|||||||||
|
Richard Ten Broek |
Chirurg, Post-doctoraal onderzoeker bij Radboud UMC afdeling heelkunde (betaald)
|
Redacteur Wetenschap bij Nederlaqnd Tijdschrift voor Geneeskunde (betaald)
|
geen
|
geen
|
*Radboud Oncologie fonds: MISTIC studie naar gebruik MRI en cineMRI om coloncarcinomen beter te stadiëren *ZonMw/KCE, BENEFIT beurs voor onderzoek naar preventie van recidief ileus, rol als projectleider. |
Speaker and/ or instructor on congres symposia, workshops and courses that have been sponsored by industry: Baxter and PolyMedics Innovations. Courses related to epidemiology, diagnosis and treatment of adhesions, no specific products have been discussed or promoted.
|
geen
|
19-1-2024
|
Geen |
| Floris Ferenschild
|
Kinder- en gastro-intestinaal chirurg Radboudumc |
Chirurg: betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
11-1-2025 |
|
|
Silvie Dronkers (Overleden 18-12-2025) |
Coördinator Patiëntenparticipatie en Belangenbehartiging |
Voorzitter Wooninitiatief Noorderzon
|
Geen |
Geen |
Geen |
Geen |
Geen |
24-11-2023 |
Geen |
|
Harmke Polinder-Bos |
Klinisch geriater, Erasmus MC
|
Geen |
Geen |
Geen |
COOP studie, financiering van ZonMW, lange termijn uitkomsten na COVID bij ouderen. ZonMW: Klinische fellow beurs voor de GRISAILLE study. Intregrating Intrinsic capacity in clinical practice. Studie waarin ik een Intrinsic capacity score ontwikkel en deze toepas in oudere patienten die een intensieve behandeling krijgen zoals een operatie. |
Behoudens dat de inhoud raakt aan mijn expertise in klinisch werk en onderzoek geen belangen. |
Geen |
1-12-2023 |
Geen |
|
Thomas van den Goorbergh |
Arts in opleiding tot spoedeisende hulp arts in het St Antonius Ziekenhuis te Nieuwegein. |
Instructor Advanced Life Support bij QTtime in Nieuwegein, betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
8-12-2023 |
Geen |
|
Elif Kilicoglu |
Diëtist in het Canisius Wilhelmina Ziekenhuis (CWZ) |
Geen |
Geen |
Geen
|
Geen |
Geen |
Geen |
30-12-2023 |
Geen |
|
Wiesje Prins-van Uden |
Radioloog, Maasziekenhuis Pantein |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
12-1-2024 |
Geen |
|
Marja Boermeester |
Amsterdam UMC
|
Medisch Ethische Commissie, Amsterdam UMC, locatie AMC |
Geen |
Geen |
Johnson&Johnson (voorkomen wondinfecties); 3M (voorkomen wondinfecties); New Compliance; Ipsen; ZonMW TelaBio (outcome hernia repair)
|
Speaker and/or instructor for J&J/Ethicon, 3M, BD, Gore, TelaBio, Medtronic, GD Medical, Smith&Nephew, Molnlycke, Angiodynamics. Voorzitter van diverse andere richtlijncommissies bij Kennisinstituut/FMS. Alle adviesraden vallen buiten het onderwerp van de richtlijn. |
Geen |
14-1-2024 |
Geen |
|
Caroline Andeweg
|
Werkzaam als chirurg in St Jansdal ziekenhuis in Hardewijk |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
25-3-2024 |
Geen |
|
Klankbordgroepleden |
|||||||||
|
Cor de Kroon |
LUMC, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
15-12-2023 |
Geen |
|
Sabine Theuns-Valks |
Kinderarts-maag darm leverziekten |
Kinderarts bij Seys centra locatie Zwijndrecht (2,5 u per week)
|
Geen |
Geen |
Geen |
Geen |
Geen |
9-1-2024 |
Geen |
Inbreng patiëntenperspectief
De werkgroep besteedde aandacht aan het patiëntenperspectief door het uitnodigen van de Patiëntenfederatie Nederland en Stichting Darmkanker voor de knelpunteninventarisatie. Daarnaast nam een patiëntvertegenwoordiger van Stichting Darmkanker deel aan de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan Patiëntenfederatie Nederland en Stichting Darmkanker en de eventueel aangeleverde commentaren zijn bekeken en verwerkt
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerde de werkgroep conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
De kwalitatieve raming volgt na de commentaarfase
|
Module |
Uitkomst raming |
Toelichting |
|
Module Decompressie van de maag |
geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële gevolgen hebben voor de collectieve uitgaven. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling van deze richtlijn is hieronder weergegeven.