Therapeutische waarde wateroplosbaar contrast
Uitgangsvraag
Wat is de therapeutische waarde van wateroplosbaar contrast bij patiënten met strengileus?
Aanbeveling
Pas wateroplosbaar contrast toe bij niet-operatieve behandeling van strengileus primair als hulpmiddel in de besluitvorming voor continueren niet-operatieve behandeling of uitgesteld opereren.
Wanneer er een initiële CT-scan gemaakt wordt op de spoed eisende hulp, dient het oraal wateroplosbaar contrast bij voorkeur na de initiële CT scan te worden toegediend, teneinde de beoordeling op CT van de aankleuring van de darmwanden niet te verstoren.
Overwegingen
Balans tussen gewenste en ongewenste effecten
Er is literatuuronderzoek verricht naar het therapeutische effect van wateroplosbaar contrast vergeleken met geen wateroplosbaar contrast in volwassen patiënten met ASBO die zijn geselecteerd voor conservatief beleid (geen indicatie voor spoedoperatie). Voor de cruciale uitkomstmaat noodzaak voor een operatie werd geen verschil gevonden tussen de groep patiënten die wateroplosbaar contrast ontving de groep die geen wateroplosbaar contrast ontving. Echter, de bewijskracht voor deze uitkomstmaat was zeer laag. Voor de cruciale uitkomstmaat duur van het ziekenhuisverblijf (alle patiënten en gecategoriseerd naar alleen niet-chirurgische patiënten) werd een klinisch relevant verschil gevonden, in het voordeel van de patiënten die wateroplosbaar contrast ontvingen. Wateroplosbaar contrast verkort dus mogelijk de verblijfsduur in het ziekenhuis. De belangrijke uitkomstmaat timing van de operatie werd niet gerapporteerd in de geïncludeerde studies. Voor de belangrijke uitkomstmaat timing to resolution werden conflicterende resultaten, met een lage bewijskracht, gevonden.
Uit de literatuur blijkt dat er aanwijzingen zijn dat wateroplosbaar contrast leidt tot sneller herstel en (hierdoor) de opnameduur verkort. Door het gebruik van wateroplosbaar contrast is betere besluitvorming mogelijk. Echter, bestaat de geïncludeerde literatuur uit voornamelijk oudere studies (alle studies zijn minimaal 10 jaar oud) en wordt er geen gebruik gemaakt van CT in de diagnostiek van strengileus. Naast de geïncludeerde literatuur, laat een recente snapshot studie (Krielen, 2023) ook een voordeel zien voor het gebruik van wateroplosbaar contrast, in de Nederlandse setting. Deze studie rapporteert een kortere opnameduur van 1 dag bij patiënten met strengileus die wateroplosbaar contrast ontvingen. In 89% van deze patiënten werd (ongecompliceerde) strengileus aangetoond door middel van CT.
Hoewel deze resultaten veelbelovend zijn, is het van belang dat zorgverleners alert zijn op mogelijke nadelen van het gebruik van wateroplosbaar contrast. Zo moet bij iedere patiënt gecontroleerd worden op een mogelijke allergie voor het contrastmiddel; deze verantwoordelijkheid ligt primair bij de radiologieafdeling. Zo bestaat er een (zeer klein) risico op een allergische reactie bij toediening van contrastmiddel. Contrastmiddel wordt meestal toegediend via de bij opname meestal reeds geplaatste maagsonde van de patiënt. In het uitzonderlijke geval waarin de patiënt geen maagsonde heeft, dan kan de patiënt het contrastmiddel innemen door dit op te drinken.
De grootste potentiële meerwaarde van wateroplosbaar contrast ligt vermoedelijk in de timing van de operatie. Hoewel deze uitkomstmaat niet gerapporteerd is in de geïncludeerde literatuur, wijst klinische ervaring erop dat toediening van contrast kan helpen om tijdig de afweging tot operatief ingrijpen te maken. In de praktijk wordt contrast vaak rond dag 2–3 na opname toegediend; een uitblijvende passage na 24 uur kan dan een extra aanwijzing zijn voor het alsnog inzetten van operatief beleid. Op deze manier kan onnodige vertraging in chirurgisch handelen worden voorkomen. Deze toepassing van wateroplosbaar contrast als beslisondersteunende tool sluit aan bij aanbevelingen in de module 2.1. over conservatief versus operatief beleid bij strengileus. Daarnaast heeft wateroplosbaarcontrast mogelijk ook enige therapeutische werking (laxeren) (Ceresoli, 2016).
Ondanks de potentiële voordelen laat de Nederlandse snapshot studie zien dat slechts een kwart van de niet operatief behandelde patiënten oraal wateroplosbaar contrast krijgt toegediend (Krielen, 2023). Mogelijk heeft dit maken met onzekerheid of methode en timing van toedienen. Het geven van contrast voor de initiële CT scan op de spoed eisende hulp bij opname heeft als nadeel dat enteraal contrast het beoordelen van aankleuren van darmwand lastiger maakt, leidt tot langere wachttijden voor scan, en er bovendien voor het plaatsen van de maaghevel kans is op aspiratie. Het beste wordt contrast toegediend na de initiële scan en plaatsen van de hevel, aangezien het contrast vooral van belang is voor de follow-up (Van Loevezijn, 2018).
Kwaliteit van bewijs
De overall kwaliteit van bewijs is zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten.
Er is afgewaardeerd vanwege ernstige:
- Risk of Bias: methodologische beperkingen (inadequate generatie van volgorde, geen blindering).
- Inconsistentie: inconsistentie van de resultaten.
- Imprecisie: onnauwkeurigheid, omdat het betrouwbaarheidsinterval beide grenzen van klinische relevantie overschrijdt.
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
Er is geen formeel onderzoek verricht naar patiëntvoorkeuren met betrekking tot het gebruik van wateroplosbaar contrast. Bij het overwegen van het gebruik van een wateroplosbaar contrastmiddel voor therapeutische doeleinden is het essentieel om rekening te houden met de waarden en voorkeuren van de patiënt. Een goede informatievoorziening speelt hierin een centrale rol. Patiënten dienen helder geïnformeerd te worden over zowel de voordelen als de mogelijke risico’s van het gebruik van dit middel, zodat zij samen met hun zorgverlener een weloverwogen beslissing kunnen nemen.
De voordelen van het toedienen van wateroplosbaar contrast zijn duidelijk: het kan het herstel van de darmfunctie versnellen en leidt in veel gevallen tot een kortere opnameduur in het ziekenhuis. Voor veel patiënten betekent dit een sneller herstel, minder kans op complicaties en een eerder terugkeren naar de thuissituatie.
Tegelijkertijd moet aandacht worden besteed aan de mogelijke nadelen, zoals hierboven beschreven. In het uitzonderlijke geval waarin de patiënt geen maagsonde heeft, en de patiënt het contrastmiddel inneemtdoor dit op te drinken, kan de patiënt vanwege de vieze smaak van contrastmiddel en de vaak al bestaande misselijkheid bij de patiënt kan dit als onprettig ervaren. De risico’s en nadelen van wateroplosbaar contrast moeten duidelijk worden besproken, vooral bij kwetsbare patiëntengroepen.
Kostenaspecten
De kosten van therapeutisch gebruik van wateroplosbaar contrast zijn minimaal en mogelijk zelfs verwaarloosbaar. Het gebruik van wateroplosbaar contrast leidt hoogstwaarschijnlijk tot een kostenbesparing, aangezien patiënten mogelijk eerder kunnen worden ontslagen uit het ziekenhuis.
Gelijkheid ((health) equity/equitable)
Er zijn geen aanwijzingen voor ongelijkheid in de keuze voor het gebruik van wateroplosbaar contrast.
Aanvaardbaarheid:
Ethische aanvaardbaarheid
Er zijn geen aanwijzingen voor ethische bezwaren in de keuze voor het gebruik van wateroplosbaar contrast.
Duurzaamheid
Het gebruik van wateroplosbaar contrastmiddel heeft invloed op de duurzaamheid, aangezien er meer (wegwerp)materialen worden gebruikt dan bij toepassing zonder contrast. Dit nadeel wordt echter ruimschoots gecompenseerd doordat patiënten die wateroplosbaar contrast krijgen, mogelijk eerder uit het ziekenhuis kunnen worden ontslagen.
Haalbaarheid
Wateroplosbaar contrastmiddel is goed beschikbaar in Nederland. Het gebruik van wateroplosbaar contrastmiddel is over het algemeen al standaardzorg in de praktijk, maar krijgt hiermee een nieuwe toepassing. De werkgroep is van mening dat er geen haalbaarheidsissues zijn.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Hoewel vergelijkende studies verouderd zijn en er twijfel bestaat over de diagnose bij gebrek aan CT-bevestiging, wijzen het overall effect en recente observationele data er toch op dat het gebruik van wateroplosbaar contrast bij volwassen patiënten met een strengileus die conservatief worden behandeld, aanbevolen kan worden. Wateroplosbaar contrast is van waarde als diagnostisch hulpmiddel in de besluitvorming rondom het continueren van niet-operatieve behandeling of uitgesteld opereren. Daarnaast heeft wateroplosbaarcontrast mogelijk ook enige therapeutische werking (laxeren).
Eindoordeel:
Sterke aanbeveling voor het gebruik van wateroplosbaar bij niet-operatieve behandeling van strengileus ter ondersteuning van de besluitvorming over continueren van conservatief beleid of uitgesteld opereren.
Onderbouwing
In most of the international literature, the use of water-soluble contrast is recommended, because it shortens the duration of hospitalization and reduces the delay of surgical treatment. In Dutch practice, oral contrast is only given in about 25% of the patients with ASBO. This may be due to insufficient knowledge about the appropriate method and timing of administering contrast (Snapshot study Krielen).
Summary of Findings
Population: Adult patients with (A)SBO selected for conservative trial treatment (no indication for acute surgery)
Intervention: Water-soluble contrast
Comparator: No water-soluble contrast
|
Outcome Timeframe |
Study results and measurements |
Absolute effect estimates |
Certainty of the evidence (Quality of evidence) |
Summary |
|
|
No water-soluble contrast |
Water-soluble contrast |
||||
|
Need for surgery (critical)
|
Relative risk: 0.98 (CI 95% 0.60 - 1.60) Based on data from 778 participants in 10 studies
|
251 per 1000 |
246 per 1000 |
Very low Due to very serious inconsistency, Due to serious risk of bias1 |
We are uncertain whether water-soluble contrast increases or decreases need for surgery |
|
Difference: 5 fewer per 1000 (CI 95% 100 fewer - 151 more) |
|||||
|
Length of hospital stay (all patients) (critical)
|
Measured by: Scale: - Lower better Based on data from 403 participants in 5 studies
|
Mean |
Mean |
Moderate Due to serious risk of bias2 |
Water-soluble contrast probably decreases length of hospital stay (all patients) |
|
Difference: MD 3.01 lower (CI 95% 4.07 lower - 1.95 lower) |
|||||
|
Length of hospital stay (non-surgical patients) (critical)
|
Measured by: Scale: - Lower better Based on data from 409 participants in 5 studies
|
Mean |
Mean |
Moderate Due to serious risk of bias3 |
Water-soluble contrast probably decreases length of hospital stay (non-surgical patients) |
|
Difference: MD 2.36 lower (CI 95% 2.82 lower - 1.90 lower) |
|||||
|
Timing of surgery (important)
|
- |
- |
- |
No studies were found that looked at timing of surgery |
|
|
Time to resolution (important)
|
- |
The pooled effect of Biondo (2003), Di Saverio (2008) and Haule (2013) showed a mean difference of -33.70 hours (95% CI -72.13 to 4.74), in favor of water-soluble contrast. In addition, Burge (2005) reported a difference in medians of -9 hours, in favor of water-soluble contrast. Choi (2002) reported a difference in medians of -19 hours, in favor of water-soluble contrast. Farid (2010) reported a mean difference of -23.1 hours, in favor of water-soluble contrast. Feigin (1996) reported a mean difference of -3.0 hours, in favor of water-soluble contrast. |
Low Due to serious risk of bias, Due to serious imprecision4 |
Water-soluble contrast may decrease time to resolution |
|
- Risk of Bias: serious. Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias, Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias; Inconsistency: very serious. The direction of the effect is not consistent between the included studies, Point estimates vary widely;
- Risk of Bias: serious. due to measurement of the outcome and selection of the reported result;
- Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, due to selection of the reported result;
- Risk of Bias: serious. due to measurement of the outcome and selection of the reported result; Imprecision: serious. Wide confidence intervals;
Description of studies
A total of one systematic review and two additional individual studies were included in the analysis of the literature. Important study characteristics and results are summarized in table 2. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Klingbeil (2022) performed a systematic review and meta-analysis to evaluate the efficacy of water-soluble contrast in the treatment of adhesive small bowel obstruction. The search was performed for the period of January 1st 1990 to November 1st 2021. Inclusion criteria were: studies reporting the effect of water-soluble contrast on SBO for hospital length of stay and/or operative rates, patients having uncomplicated SBO (secondary to adhesions manifested by abdominal pain and distention, nausea), radiological confirmation of SBO. Eleven randomized controlled trials and nine observational studies were included in the systematic review. In this analysis, only randomized controlled trials were included.
Lee (2004) performed a randomized controlled trial to evaluate the impact of contrast follow-through on clinical outcomes of patients with adhesive SBO. The inclusion criteria were diagnosis of adhesive small bowel obstructions, with a history of previous laparotomies for either benign or malignant conditions. The study was performed in a single center.
Kumar (2009) performed a prospective randomized controlled trial to define the efficacy of an oral water soluble contrast agent in patients with postoperative SBO. The inclusion criteria were postoperative intestinal obstruction, presenting with clinical and radiological evidence of SBO. The study was performed in a single center.
Table 2. Characteristics of included studies
|
Study |
Participants |
Comparison |
Follow-up |
Outcome measures |
Comments |
Risk of bias (per outcome measure)* |
|
Included in systematic review Klingbeil, 2022 |
||||||
|
Assalia, 1994 |
N at baseline Intervention: 54 Control: 45
Age (mean, SD) NR
Sex NR
Center type: Single
Diagnosis: Physical examination and plain XR films
Timing of WSC: NR
Timing of follow-up imaging (abdominal radiograph): 6 hours |
Intervention: water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Operative rate, Time to resolution, Complications, Mortality
|
Funding: NR
Conflicts of interest: No
|
Some concerns |
|
Feigin, 1996 |
N at baseline Intervention: 25 Control: 25
Age (mean, SD) NR
Sex NR
Center type: Single
Diagnosis: Physical examination and plain XR films
Timing of WSC: NR
Timing of follow-up imaging (abdominal radiograph): NR |
Intervention: water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Operative rate, Time to resolution, Complications, Mortality |
Funding: NR
Conflicts of interest: No
|
Some concerns |
|
Choi, 2002 |
N at baseline Intervention: 19 Control: 16
Age (mean, SD) NR
Sex NR
Center type: Single
Diagnosis: Physical examination and plain XR films
Timing of WSC: After 48h of neither clinical nor radiological improvement
Timing of follow-up imaging (abdominal radiograph): Daily |
Intervention: water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Hospital length of stay, Time to resolution, Complications, Mortality |
Funding: NR
Conflicts of interest: No
|
Some concerns |
|
Biondo, 2003 |
N at baseline Intervention: 42 Control:41
Age (mean, SD) NR
Sex NR
Center type: Single
Diagnosis: Physical examination and plain XR films
Timing of WSC: After diagnosis and informed consent and following complete gastric decompression in ED
Timing of follow-up imaging (abdominal radiograph): 24h after GG |
Intervention: water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Hospital length of stay, Operative rate, Time to resolution, Complications, Mortality |
Funding: NR
Conflicts of interest: No
|
Some concerns |
|
Burge, 2005 |
N at baseline Intervention: 18 Control: 17
Age (mean, SD) NR
Sex NR
Center type: Multiple
Diagnosis: Physical examination and plain XR films
Timing of WSC: After NGT placement, resuscitation and stomach emptying
Timing of follow-up imaging (abdominal radiograph): No XRs were taken |
Intervention: water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Hospital length of stay, Operative rate, Time to resolution, Complications, Mortality |
Funding: NR
Conflicts of interest: No
|
HIGH |
|
Di Saverio, 2008 |
N at baseline Intervention: 38 Control: 38
Age (mean, SD) NR
Sex NR
Center type: Multiple
Diagnosis: Physical examination and plain XR films
Timing of WSC: Immediately
Timing of follow-up imaging (abdominal radiograph): 36 and 72 hours after GG administration |
Intervention: water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Hospital length of stay, Operative rate, Time to resolution, Complications, Mortality |
Funding: NR
Conflicts of interest: No
|
Some concerns |
|
Farid, 2010 |
N at baseline Intervention: 55 Control: 55
Age (mean, SD) NR
Sex NR
Center type: Single
Diagnosis: Physical examination and plain XR films
Timing of WSC: After complete suction of gastric fluid
Timing of follow-up imaging (abdominal radiograph): 8 and 24 hours |
Intervention: water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Hospital length of stay, Operative rate, Time to resolution, Complications, Mortality
|
Funding: NR
Conflicts of interest: No
|
HIGH |
|
Rahmani, 2013 |
N at baseline Intervention: 42 Control: 42
Age (mean, SD) NR
Sex NR
Center type: Single
Diagnosis: Physical examination and plain XR films
Timing of WSC: Unclear when it was first given, but states 100cc given daily up to 4 days
Timing of follow-up imaging (abdominal radiograph): NR |
Intervention: water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Hospital length of stay, Operative rate, Complications, Mortality
|
Funding: NR
Conflicts of interest: No
|
Some concerns |
|
Haule, 2013 |
N at baseline Intervention: 25 Control: 25
Age (mean, SD) NR
Sex NR
Center type: Single
Diagnosis: Physical examination and plain XR films
Timing of WSC: After 24 hours of resuscitation
Timing of follow-up imaging (abdominal radiograph): 12 and 24 hours |
Intervention: water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Hospital length of stay, Operative rate, Time to resolution, Complications, Mortality |
Funding: NR
Conflicts of interest: No
|
HIGH |
|
Scotte, 2017 |
N at baseline Intervention: 121 Control: 121
Age (mean, SD) NR
Sex NR
Center type: Multiple
Diagnosis: CT with IV contrast
Timing of WSC: Following 2 hours of decompression
Timing of follow-up imaging (abdominal radiograph): 8, 12, 24, 48 hours after GG |
Intervention: oral water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Hospital length of stay, Operative rate, Mortality
|
Funding: NR
Conflicts of interest: No
|
HIGH |
|
Khorshidi, 2019 |
N at baseline Intervention: 26 Control: 26
Age (mean, SD) NR
Sex NR
Center type: Single
Diagnosis: Physical examination and plain XR films
Timing of WSC: Following 2 hours of decompression
Timing of follow-up imaging (abdominal radiograph): 12, 24, 48 hours |
Intervention: water-soluble contrast Control: no water-soluble contrast (water, saline, or NGT) |
Follow-up radiograph within 6 and 72 hours |
Hospital length of stay for non-surgical patients |
Funding: NR
Conflicts of interest: Yes
|
Some concerns |
|
Individual studies |
||||||
|
Kumar, 2009 |
N at baseline Intervention: 21 Control: 20
Age (mean, SD) Intervention: 40.48 ± 14.96 years Control: 43.40 ± 16.33 years
Sex (male/ female) Intervention: 17/4 Control: 14/6
Diagnosis: Clinical history, examination and abdominal radiograph findings
Timing of WSC: after diagnosis of postoperative SBO
Timing of follow-up imaging (erect and supine abdominal radiographs): after 12 hours and subsequently when necessary |
Intervention: Oral water soluble contrast agent Gastrografin Control: Conventional management |
NR |
Operative rate, Hospital stay |
Funding: NR
Conflicts of interest: NR |
Some concerns |
|
Lee, 2004 |
N at baseline Intervention: 75 Control: 75
Age (mean, SD) Intervention: 64 (range 16-90) Control: 66 (range 17-87)
Sex (male/ female) Intervention: 52/23 Control: 45/30
Diagnosis: Clinical symptoms of abdominal pain, distension and vomiting, supported by the radiological findings of dilated small bowel loops
Timing of WSC: Within 24h of admission (urografin)
Timing of follow-up imaging (supine abdominal X-ray): NR |
Intervention: water-soluble contrast (75% Urografin) Control: no water-soluble contrast (observation) |
16 months |
Operative rate, Observation period, Total hospital stay In-hospital mortality
|
Funding: NR
Conflicts of interest: NR |
LOW |
*For further details, see risk of bias table in the appendix
Results
Length of hospital stay (critical)
Length of hospital stay (all patients)
One systematic review reported the outcome measure length of hospital stay for all patients (Klingbeil, 2022). The mean difference in length of hospital stay between the 202 patients who received water-soluble contrast and the 201 patients who received no water-soluble contrast was -3.01 days (95% CI -4.07 to -1.95), in favor of the patients who received water-soluble contrast (Figure 1). This difference is considered clinically relevant.
Figure 1. Length of hospital stay (all patients) for water-soluble contrast vs. no water-soluble contrast in patients with ASBO
Z: p-value of overall effect; df: degrees of freedom; I2: statistical heterogeneity; CI: confidence interval.
Three studies (two studies included in the systematic review of Klingbeil, 2022) reported median values and ranges for the outcome measure length of hospital stay for all patients (
Burge, 2005; Choi, 2002; Lee, 2004). The results were not pooled.
Burge (2005) reported a median length of hospital stay for the patients who received water-soluble contrast (n=18) of 3 days (range 1-8 days), compared with a median length of hospital stay for the patients who received no water-soluble contrast (n=17) of 4 days (range 2-8 days). The difference in medians was -1 day, in favor of the patients who received water-soluble contrast. This difference is considered clinically relevant.
Choi (2002) reported a median length of hospital stay for the patients who received water-soluble contrast (n=19) of 10 days (range 5-34 days), compared with a median length of hospital stay for the patients who received no water-soluble contrast (n=16) of 10 days (range 5-65 days). Therefore, there was no difference in medians between the groups.
Lee (2004) reported a median length of hospital stay for the patients who received water-soluble contrast (n=25) of 5 days (range 2-54 days), compared with a median length of hospital stay for the patients who received no water-soluble contrast (n=27) of 7 days (range 1-55 days). The difference in medians was -2 days, in favor of the patients who received water-soluble contrast. This difference is considered clinically relevant.
CT-diagnosed ASBO
Scotte (2017) reported a median length of hospital stay for the patients who received water-soluble contrast (n=121) of 3.8 days, compared with a median length of hospital stay for the patients who received no water-soluble contrast (n=121) of 3.5 days. The difference in medians was 0.3 days, in favor of the patients who received no water-soluble contrast. This difference is not considered clinically relevant.
Length of hospital stay (non-surgical patients)
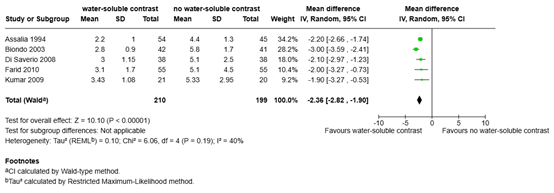
One systematic review and one individual study reported the outcome measure length of hospital stay for non-surgical patients (Klingbeil, 2022; Kumar, 2009). The mean difference in length of hospital stay between the 210 patients who received water-soluble contrast and the 199 patients who received no water-soluble contrast was -2.36 days (95% CI -2.82 to -1.90), in favor of the patients who received water-soluble contrast (Figure 2). This difference is considered clinically relevant.
Figure 2. Length of hospital stay (non-surgical patients) for water-soluble contrast vs. no water-soluble contrast in patients with ASBO
Z: p-value of overall effect; df: degrees of freedom; I2: statistical heterogeneity; CI: confidence interval.
One study (included in the systematic review of Klingbeil, 2022) reported median values and ranges for the outcome measure length of hospital stay for non-surgical patients (Khorshidi, 2019). The patients who received water-soluble contrast (n=26) had a median length of hospital stay of 1.6 days (range 1.2-1.9 days), compared with a median length of hospital stay of 1.9 days (range 1.5-2.5 days) for the patients who received no water-soluble contrast (n=26). The difference in medians was -0.3 days, in favor of the patients who received water-soluble contrast. This difference is not considered clinically relevant.
Need for surgery (critical)
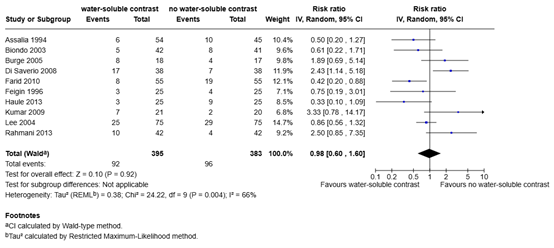
One systematic review and two individual studies reported the outcome measure operative rate (Klingbeil, 2022; Kumar, 2009; Lee, 2004). Of the 395 patients who received water-soluble contrast, 92 patients (23.3%) received surgery, compared with 96 of the 383 patients (25.1%) who received no water-soluble contrast (Figure 3). The risk ratio was 0.98 (95% CI 0.60 to 1.60), in favor of the patients who received water-soluble contrast. This difference is not considered clinically relevant.
Figure 3. Need for surgery for water-soluble contrast vs. no water-soluble contrast in patients with ASBO
Z: p-value of overall effect; df: degrees of freedom; I2: statistical heterogeneity; CI: confidence interval.
CT-diagnosed ASBO
Scotte (2017) reported need for surgery in patients with CT-diagnosed ASBO. In total, 29 of the 121 patients (24.0%) who received water-soluble contrast needed surgery, compared with 24 of the 121 patients (19.8%) who received no water-soluble contrast. The risk ratio was 1.21 (95% CI 0.75 to 1.95), in favor of the patients who received no water soluble contrast. This difference is not considered clinically relevant.
Timing of surgery (important)
None of the included studies reported the outcome measure timing of surgery.
Time to resolution (important)
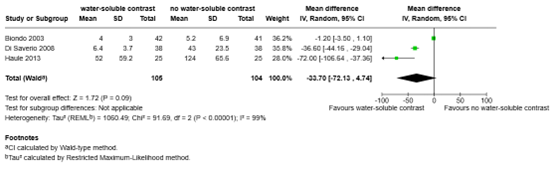
One systematic review reported the outcome measure time to resolution (Klingbeil, 2022). The mean difference in time to resolution between the 105 patients who received water-soluble contrast and the 104 patients who received no water-soluble contrast was -33.70 hours (95% CI -72.13 to 4.74), in favor of the patients who received water-soluble contrast (Figure 4). This difference is considered clinically relevant.
Figure 4. Time to resolution for water-soluble contrast vs. no water-soluble contrast in patients with ASBO
Z: p-value of overall effect; df: degrees of freedom; I2: statistical heterogeneity; CI: confidence interval.
Five studies (included in the systematic review of Klingbeil, 2022) did not report mean values with standard deviations for the outcome measure time to resolution, therefore the results of those studies could not be pooled (Assalia, 1994; Burge, 2005; Choi, 2002; Farid, 2010; Feigin, 1996).
Assalia (1994) reported a mean time to resolution for the patients who received water-soluble contrast (n=54) of 6.2 hours (range 2-20 hours), compared with a mean time to resolution for the patients who received no water-soluble contrast (n=45) of 23.4 hours (range 6-72 hours). The mean difference was -17.2 hours, in favor of the patients who received water-soluble contrast. This difference is considered clinically relevant.
Burge (2005) reported a median time to resolution for the patients who received water-soluble contrast (n=18) of 12 hours (range 6-96 hours), compared with a median time to resolution for the patients who received no water-soluble contrast (n=17) of 21 hours (range 9-96 hours). The difference in medians was -9 hours, in favor of the patients who received water-soluble contrast. This difference is considered clinically relevant.
Choi (2002) reported a median time to resolution for the patients who received water-soluble contrast (n=19) of 41 hours (range 6-80 hours), compared with a median time to resolution for the patients who received no water-soluble contrast (n=16) of 60 hours (range 7-150 hours). The difference in medians was -19 hours, in favor of the patients who received water-soluble contrast. This difference is considered clinically relevant.
Farid (2010) reported a mean time to resolution for the patients who received water-soluble contrast (n=55) of 19.5 hours, compared with a mean time to resolution for the patients who received no water-soluble contrast (n=55) of 42.6 hours. The mean difference was -23.1 hours, in favor of the patients who received water-soluble contrast. This difference is considered clinically relevant.
Feigin (1996) reported a mean time to resolution for the patients who received water-soluble contrast (n=25) of 25.7 hours, compared with a mean time to resolution for the patients who received no water-soluble contrast (n=25) of 28.7 hours. The mean difference was -3.0 hours, in favor of the patients who received water-soluble contrast. This difference is not considered clinically relevant.
A systematic review of the literature was performed to answer the following question(s):
What is the therapeutic value of water soluble contrast (WSC) versus no contrast in patients with a suspicion of SBO selected for conservative trial treatment/without indication for acute surgery?
Table 1. PICO
|
Patients |
Adult patients with (A)SBO selected for conservative trial treatment (no indication for acute surgery) |
|
Intervention |
Water soluble contrast |
|
Control |
No contrast |
|
Outcomes |
Length of hospital stay, need for surgery, timing of surgery, time to resolution |
|
Other selection criteria |
Study design: systematic reviews and randomized controlled trials |
Relevant outcome measures
The guideline panel considered length of hospital stay and need for surgery as critical outcome measures for decision making; and timing of surgery and time to resolution as important outcome measures for decision making.
A priori, the guideline panel did not define the outcome measures listed above but used the definitions used in the studies.
The guideline panel defined the following as minimal clinically (patient) important differences:
- Length of hospital stay: 1 day
- Need for surgery: 25% (RR>0.8, RR<1.25)
- Timing of surgery: 1 day
- Time to resolution: 8 hours
Search and select (Methods)
A systematic literature search was performed by a medical information specialist using the following bibliographic databases: Embase.com and Ovid/Medline. Both databases were searched from December 2004 to eighth of December 2024 (Embase) and eleventh of December 2024 (Ovid/Medline) for systematic reviews, RCTs and observational studies. Systematic searches were completed using a combination of controlled vocabulary/subject headings (e.g., Emtree-terms, MeSH) wherever they were available and natural language keywords. The overall search strategy was derived from two primary search concepts: (1) small bowel obstruction; (2) contrast medium OR water-soluble contrast. Duplicates were removed using EndNote software. After deduplication a total of 724 records were imported for title/abstract screening. Initially, 28 studies were selected based on title and abstract screening. After reading the full text, 25 studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and three studies were included.
- Ceresoli M, Coccolini F, Catena F, Montori G, Di SS, Sartelli M, et al. Water-soluble contrast agent in adhesive small bowel obstruction: a systematic review and meta-analysis of diagnostic and therapeutic value. Am J Surg. 2016;211(6):1114–1125
- Klingbeil KD, Wu JX, Osuna-Garcia A, Livingston EH. The Effect of Hyperosmolar Water- Soluble Contrast for the Management of Adhesive Small Bowel Obstruction: A Systematic Review and Meta-Analysis. Ann Surg. 2022 Dec 1;276(6):981-988. doi: 10.1097/SLA.0000000000005573. Epub 2022 Jul 15. Erratum in: Ann Surg. 2024 Apr 1;279(4):e1-e2. doi: 10.1097/SLA.0000000000006201. PMID: 35837888.
- Krielen P, Kranenburg LPA, Stommel MWJ, Bouvy ND, Tanis PJ, Willemsen JJ, Migchelbrink J, de Ree R, Bormans EMG, van Goor H, Ten Broek RPG; ASBO Snapshot Study Group. Variation in the management of adhesive small bowel obstruction in the Netherlands: a prospective cross-sectional study. Int J Surg. 2023 Aug 1;109(8):2185- 2195. doi: 10.1097/JS9.0000000000000471. PMID: 37288588; PMCID: PMC10442142.
- Kumar P, Kaman L, Singh G, Singh R. Therapeutic role of oral water soluble iodinated contrast agent in postoperative small bowel obstruction. Singapore Med J. 2009 Apr;50(4):360-4. PMID: 19421678.
- Lee, J. F. Y., Meng, W. C. S., Leung, K. L., Yu, S. C. H., Poon, C. M., & Lau, W. Y. (2004). Water soluble contrast follow‐through in the management of adhesive small bowel obstruction: a prospective randomized trial. Annals of the College of Surgeons of Hong Kong, 8(4), 120-126.
- Van Loevezijn, A. A., Smithuis, R. H. M., & van den Bremer, J. (2018). Gastrografin als prognostisch en therapeutisch medium Gastrografin as a prognostic and therapeutic medium; use for small bowel obstruction, but not for closed loop obstruction. Ned Tijdschr Geneeskd, 162, D2408.
Beoordelingsdatum en geldigheid
Publicatiedatum : 09-04-2026
Beoordeeld op geldigheid : 09-04-2026
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd door de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS)
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met schouderinstabiliteit.
Werkgroep richtlijn strengileus
- dr. R.P.G. (Richard) ten Broek, chirurg Radboud UMC, NVvH – voorzitter richtlijnwerkgroep
- dr. C. (Caroline) Andeweg, chirurg St. Jansdal Harderwijk, NVvH
- Prof. dr. M. (Marja) Boermeester, chirurg Amsterdam UMC, NVvH
- Dhr. dr. F.T.J. (Floris) Ferenschild, chirurg Radboud UMC, NVvH
- dr. H.A. (Harmke) Polinder-Bos, klinisch geriater Erasmus MC, NVKG
- Mevr. E. (Elif) Kilicoglu, diëtist, CWZ Nijmegen, NVD
- Mevr. drs. M.W. (Wiesje) Prins, radioloog Maasziekenhuis, NVvR
- drs. T.W. (Thomas) van den Goorbergh, spoedeisende hulp, St. Antonius Ziekenhuis Nieuwegein, NVSHA
- Mevr. S. (Silvie) Dronkers, ervaringsdeskundige en patiëntvertegenwoordiger Stichting Darmkanker Nederland † (in herinnering)
Klankbordgroep richtlijn strengileus
- dr. A. (Sander) van der Beek, internist Ziekenhuis Rivierenland, NIV
- dr. C. (Cor) de Kroon, gynaecoloog LUMC, NVOG
- Mevr. S.D.M. (Sabine) Theuns-Valks, kinderarts Albert Schweitzer Ziekenhuis, NVK
Met ondersteuning van
- dr. L.M. (Lisette) van Leeuwen, adviseur Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. E.R.L. (Evie) Verweg, junior adviseur Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Tabel 1 Gemelde (neven)functies en belangen werkgroep
|
Naam |
Hoofdfunctie |
Neven-werkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Werkgroepleden |
|||||||||
|
Richard Ten Broek |
Chirurg, Post-doctoraal onderzoeker bij Radboud UMC afdeling heelkunde (betaald)
|
Redacteur Wetenschap bij Nederlaqnd Tijdschrift voor Geneeskunde (betaald)
|
geen
|
geen
|
*Radboud Oncologie fonds: MISTIC studie naar gebruik MRI en cineMRI om coloncarcinomen beter te stadiëren *ZonMw/KCE, BENEFIT beurs voor onderzoek naar preventie van recidief ileus, rol als projectleider. |
Speaker and/ or instructor on congres symposia, workshops and courses that have been sponsored by industry: Baxter and PolyMedics Innovations. Courses related to epidemiology, diagnosis and treatment of adhesions, no specific products have been discussed or promoted.
|
geen
|
19-1-2024
|
Geen |
| Floris Ferenschild
|
Kinder- en gastro-intestinaal chirurg Radboudumc |
Chirurg: betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
11-1-2025 |
|
|
Silvie Dronkers (Overleden 18-12-2025) |
Coördinator Patiëntenparticipatie en Belangenbehartiging |
Voorzitter Wooninitiatief Noorderzon
|
Geen |
Geen |
Geen |
Geen |
Geen |
24-11-2023 |
Geen |
|
Harmke Polinder-Bos |
Klinisch geriater, Erasmus MC
|
Geen |
Geen |
Geen |
COOP studie, financiering van ZonMW, lange termijn uitkomsten na COVID bij ouderen. ZonMW: Klinische fellow beurs voor de GRISAILLE study. Intregrating Intrinsic capacity in clinical practice. Studie waarin ik een Intrinsic capacity score ontwikkel en deze toepas in oudere patienten die een intensieve behandeling krijgen zoals een operatie. |
Behoudens dat de inhoud raakt aan mijn expertise in klinisch werk en onderzoek geen belangen. |
Geen |
1-12-2023 |
Geen |
|
Thomas van den Goorbergh |
Arts in opleiding tot spoedeisende hulp arts in het St Antonius Ziekenhuis te Nieuwegein. |
Instructor Advanced Life Support bij QTtime in Nieuwegein, betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
8-12-2023 |
Geen |
|
Elif Kilicoglu |
Diëtist in het Canisius Wilhelmina Ziekenhuis (CWZ) |
Geen |
Geen |
Geen
|
Geen |
Geen |
Geen |
30-12-2023 |
Geen |
|
Wiesje Prins-van Uden |
Radioloog, Maasziekenhuis Pantein |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
12-1-2024 |
Geen |
|
Marja Boermeester |
Amsterdam UMC
|
Medisch Ethische Commissie, Amsterdam UMC, locatie AMC |
Geen |
Geen |
Johnson&Johnson (voorkomen wondinfecties); 3M (voorkomen wondinfecties); New Compliance; Ipsen; ZonMW TelaBio (outcome hernia repair)
|
Speaker and/or instructor for J&J/Ethicon, 3M, BD, Gore, TelaBio, Medtronic, GD Medical, Smith&Nephew, Molnlycke, Angiodynamics. Voorzitter van diverse andere richtlijncommissies bij Kennisinstituut/FMS. Alle adviesraden vallen buiten het onderwerp van de richtlijn. |
Geen |
14-1-2024 |
Geen |
|
Caroline Andeweg
|
Werkzaam als chirurg in St Jansdal ziekenhuis in Hardewijk |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
25-3-2024 |
Geen |
|
Klankbordgroepleden |
|||||||||
|
Cor de Kroon |
LUMC, gynaecoloog |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
15-12-2023 |
Geen |
|
Sabine Theuns-Valks |
Kinderarts-maag darm leverziekten |
Kinderarts bij Seys centra locatie Zwijndrecht (2,5 u per week)
|
Geen |
Geen |
Geen |
Geen |
Geen |
9-1-2024 |
Geen |
Inbreng patiëntenperspectief
De werkgroep besteedde aandacht aan het patiëntenperspectief door het uitnodigen van de Patiëntenfederatie Nederland en Stichting Darmkanker voor de knelpunteninventarisatie. Daarnaast nam een patiëntvertegenwoordiger van Stichting Darmkanker deel aan de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan Patiëntenfederatie Nederland en Stichting Darmkanker en de eventueel aangeleverde commentaren zijn bekeken en verwerkt
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerde de werkgroep conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
De kwalitatieve raming volgt na de commentaarfase
|
Module |
Uitkomst raming |
Toelichting |
|
Module Therapeutische waarde wateroplosbaar contrast |
geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële gevolgen hebben voor de collectieve uitgaven. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling van deze richtlijn is hieronder weergegeven.