Toedieningsvormen van medicatie
Uitgangsvraag
Wat is de aanbevolen toedieningsvorm van medicatie om de milieu-impact zoveel mogelijk te beperken?
Aanbeveling
Kies voor een enterale toediening boven een parenterale toediening bij paracetamol.
Stel bij het gebruik van antibiotica waar mogelijk gestandaardiseerde regels in om een intraveneuze therapie tijdig te veranderen in een enterale therapie.
Kies in het geval van NSAID’s bij voorkeur een enterale boven een topicale toedieningsvorm.
Kies bij een adequate inhalatietechniek voor een poederinhalator of soft mist inhalator in plaats van een dosisaerosol. Indien een dosisaerosol noodzakelijk is, kies de variant met de laagste broeikasgasemissie.
Neem bij elke vorm van toediening de hoeveelheid materiaalgebruik in ogenschouw.
Overwegingen
Kwaliteit van bewijs
Op basis van de beschikbare literatuur is gekeken naar de milieu-impact van verschillende toedieningsvormen van medicatie. Er zijn drie studies gevonden conform de PICO (Davies, 2024; Hermes, 2023; Ponzetti, 2016), waarbij de cruciale uitkomstmaten ‘climate change’ en ‘waste’ zijn gerapporteerd. Davies (2024) en Hermes (2023) rapporteerden de vergelijking tussen enterale en intraveneuze toediening: Davies (2024) vergelijkt enterale versus intraveneuze paracetamol en Hermes (2023) vergelijkt switchtherapie van intraveneuze naar enterale antimicrobiële therapie. Ponzetti (2016) vergeleek twee subtypen van parenterale toediening, namelijk subcutane- en intraveneuze toediening. Er werden geen studies gevonden voor andere vergelijkingen tussen toedieningsvormen of voor de uitkomstmaten ‘eco-toxicity’, ‘human toxicity’, ‘water use’, ‘land use’, ‘acidification’ en ‘eutrophication’.
De globale kwaliteit van bewijs is zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten. Er is afgewaardeerd vanwege (zeer) ernstige risk of bias, indirectheid en imprecisie. Op basis van deze GRADE beoordeling van de literatuur kunnen geen sterke conclusies geformuleerd worden over de precieze mate van milieu-impact van toedieningsmanier van medicatie.
Echter, ondanks de methodologische beperkingen van de gevonden studies, wijzen de resultaten wel dezelfde richting op: Davies (2024) en Hermes (2023) concludeerden dat een enterale toedieningswijze leidt tot een lagere milieu-impact dan intraveneuze toediening. Verder concludeerde Ponzetti (2016) dat een subcutane toedieningswijze leidt tot een lagere milieu-impact dan intraveneuze toediening.
Balans tussen gewenste en ongewenste effecten
Naast dat er aanwijzingen zijn dat enterale toediening minder milieu-impact heeft dan parenterale toediening en dat beide toedieningsvormen een gelijkwaardig klinisch effect kunnen hebben (zie ook leidraad Liever enterale dan parenterale therapie, NVZA, 2025; Santander, 2024; Wald-Dickler, 2022; Mallama, 2021; Osorio, 2024), zijn er andere voordelen te noemen. Zo is de kans op medicatiefouten het kleinst bij toediening van vaste enterale medicatie ten opzichte van andere manieren van toediening (Jessurun, 2023). Daarnaast zijn de kosten voor het gebruik van enteraal toegediende medicatie lager (Hermes, 2023; Sankaranarayanan, 2014; Santander, 2024; Nguyen, 2024) en is enterale toediening minder invasief dan parenterale toediening; zie voor verdere toelichting ‘Kostenaspecten’ en ‘Waarden en voorkeuren van patiënten’.
Het intraveneus toedienen van medicatie is een complexe handeling waarbij strikte hygiëne maatregelen in acht genomen moeten worden om de veiligheid van de patiënt te waarborgen (Voor toediening gereedmaken (VTGM) buiten de apotheek en toediening medicatie Module 2a; SRI, 2024). Door het meer invasieve karakter van intraveneuze medicatie is er een hogere kans op complicaties zoals flebitis, thromboflebitis en extravasatie (Dychter, 2012), waarbij benodigde aanvullende behandeling ook weer tot extra milieu-impact kan leiden.
Een verschil in broeikasgasemissie kan ook binnen eenzelfde toedieningsroute bestaan. Wanneer, bij de behandeling van COPD of astma het aandeel dosisaerosol ten opzichte van poederinhalatoren zou verminderen is er een reductie in de broeikasgasemissie van 67 kiloton CO2-equivalent mogelijk (Bickhardt, 2022; Wichers, 2022; Woodcock, 2022). De mate van CO2 voetafdruk is bij dosisaerosol inhalatoren sterk afhankelijk van het gebruikte drijfgas. In de NHG-Standaard Astma bij volwassenen (NHG, 2020) en de transmurale leidraad Klimaatbewust voorschrijven van inhalatiemedicatie (Zorginstituut Nederland, 2025), is deze CO2-voetafdruk meegenomen in de aanbeveling.
De medicatie uitstoot in het oppervlaktewater is afhankelijk van onder andere de dosering (vergeleken op basis van de defined daily dose), route van toediening, het metabolisme en het zuiveringsrendement van het medicijn in de rioolwaterzuiveringsinstallatie (RWZI) (Faber, 2023). Bij een topicale toepassing van NSAID’s is de mate van onveranderde uitscheiding in het rioolwater, door afspoeling en wassen (81,3% voor ibuprofen en 93,5% voor diclofenac), veel hoger dan na systemische toediening (8,1% voor ibuprofen en 1% voor diclofenac) (Faber, 2023).
Ook medicatie die via inhalatie worden toegediend kunnen gevolgen hebben voor het oppervlaktewater. Een voorbeeld hiervan zijn de inhalatie anesthetica waarbij verschillende degradatie producten, behorende tot de polyfluoroalkyl substanties (PFAS), na gebruik het oppervlaktewater bereiken (Kalmar 2025). Het degradatie product trifluoroazijnzuur (TFA) is exceptioneel resistent tegen verdere omzetting waardoor een duidelijke bio accumulatie in verschillende ecologische compartimenten wordt waargenomen (Freeling 2023)
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
De gewenste effecten op patiëntrelevante uitkomstmaten worden ingeschat als matig tot zeer groot aangezien het enteraal toedienen van medicatie over het algemeen een minder invasief karakter heeft dan parenterale toediening. De ongewenste effecten op patiëntrelevante uitkomstmaten zijn onbekend. Ongewenste effecten bij enterale toediening ten opzichte van parenterale toediening kunnen gelegen zijn in slikstoornissen, darmmotiliteitstoornissen en andere patiëntgerelateerde factoren (zoals prikangst, beperkingen in motoriek) en zullen op individuele basis afgewogen dienen te worden.
Bij andere in deze module genoemde interventies (poederinhalator in plaats van dosisaerosol) is aandacht nodig voor therapietrouw, inhalatietechniek en prikkelvermijding (NHG-Standaard ‘Astma bij volwassenen’, NHG, 2020). Daarbij dient rekening gehouden te worden met patiënt specifieke kenmerken en voorkeuren voor de te kiezen interventie en de uitgangspunten rondom verantwoord wisselen van medicatie, waaronder toedieningsvorm (zie de leidraad Verantwoord Wisselen Medicijnen, Patiëntenfederatie Nederland, 2024).
De lagere systemische absorptie bij topicaal toegepaste NSAID’s, geeft minder kans op systemische bijwerkingen van deze middelen en dient afgewogen te worden tegen de veel hogere aquatische emissie (van Herwaarden, 2021).
Kostenaspecten
De kosten voor het gebruik van enteraal toegediende medicatie zijn lager dan het gebruik van parenteraal toegediende medicatie (Hermes, 2023; Sankaranarayanan, 2014; Santander, 2024). Het verschil in kosten komt voort uit het uitsparen van extra materiaal, het aantal handelingen en de tijdsinvestering bij vaste enteraal toegediende medicatie (van Zanten, 2003). De langere houdbaarheid van vaste enterale medicatie en de hogere kosten van parenteralia spelen hierbij tevens een rol.
Gezondheidsgelijkheid
Het gebruik van enterale in plaats van parenterale toedieningsvormen leidt naar verwachting niet tot directe verschillen in gezondheidsgelijkheid. Ook bij de keuze tussen andere toedieningsvormen worden geen directe effecten op gezondheidsgelijkheid verwacht. Wel kan het verminderen van de milieu-impact van medicatie indirect bijdragen aan gezondheidsgelijkheid, aangezien negatieve milieueffecten wereldwijd relatief zwaar drukken op regio’s met een lagere sociaal-economische status (Chancel, 2022; The Lancet Public Health Editorial Board, 2022; Wilkinson, 2022). Het is daarom belangrijk dat verduurzamingsmaatregelen rondom toedieningsvormen niet leiden tot hogere kosten of verminderde beschikbaarheid, zodat de toegankelijkheid van zorg voor alle patiëntengroepen behouden blijft.
Aanvaardbaarheid
Ethische aanvaardbaarheid
De interventie lijkt aanvaardbaar voor de betrokkenen. De werkgroep voorziet geen ethische bezwaren. Eventuele voordelen van een interventie voor de individu die schade toebrengen aan de ecologie kunnen daarmee ook schade toebrengen aan de maatschappij. Het overgaan van parenteraal op enterale toediening geeft een reductie van risico’s voor de ecologie.
Duurzaamheid
Deze module is volledig gericht op het verlagen van milieu-impact, derhalve speelt duurzaamheid een doorslaggevende- en hoofdrol bij de beschreven vergelijkingen.
Haalbaarheid
De haalbaarheid van de beschreven interventie hangt af van de bewustwording van de voorschrijver en apotheker over de ecologische gevolgen van de verschillende vormen van toediening. Bij elke interventie dient de voorschrijver de beoogde klinische effecten af te wegen tegen de financiële aspecten en milieu-impact van de interventie. Apothekers kunnen hierbij ondersteunen door onder andere tijdens multidisciplinair overleg of na voorschrijven de arts te attenderen op de mogelijkheid tot omzetten van de toedienvorm naar een duurzamer alternatief. Voor antibiotische therapie bestaan er criteria om een tijdige en adequate overstap van intraveneuze naar enterale therapie te maken (iv/orale switch | SwabID, Harvey, 2023; Eii, 2023; Akhloufi, 2017). Ook voor pijnbehandeling heeft bij volwassenen enterale toediening de voorkeur boven parenterale toediening (Mallama, 2021). Echter, bij kinderen in de peri-operatieve periode verdient de parenterale toediening van paracetamol en opioïden de voorkeur boven rectale en enterale toediening. Deze keuze is met name afhankelijk van de inwerkingsduur, de bruikbare toedieningsweg en de kans op postoperatieve misselijkheid en braken (NVA, 2023). Tevens bestaan er geneesmiddelmonografieën voor omzetten van de toedienvorm, zie leidraad Liever enterale dan parenterale therapie (NVZA, 2025), welke ondersteunen in de voorwaarde en overweging om van parenterale naar enterale toedieningsroute te switchen.
Voor een goed behandelresultaat moet in de initiële keuze van de inhalator voorop staan dat de inhalator past bij de patiënt (Hagendoorn, 2016) en dat wanneer een wisseling van inhalator wordt overwogen hierbij de uitgangspunten en werkafspraken uit de leidraad Verantwoord Wisselen Medicijnen, addendum longinhalatie en de transmurale leidraad Klimaatbewust voorschrijven van inhalatiemedicatie worden geadviseerd (Patiëntenfederatie Nederland, 2023; Zorginstituut Nederland, 2025).
Bij deze module is een implementatieplan opgesteld, dat ondersteuning biedt bij het (verder) in de praktijk brengen van de aanbevelingen.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Deze module richt zich op de milieu-impact van de toedieningsvorm van medicatie. Bij een gelijkwaardig klinisch effect heeft een enterale toedieningsvorm de voorkeur boven een parenterale vorm. De mate van broeikasgasemissie en afvalproductie is, in de gevonden studies, in enterale vorm minder dan in parenterale vorm. Hoewel de bewijslast voor de aanbeveling zeer laag is en het niet onmogelijk is dat positieve effecten van een toedieningsroute op de ene uitkomstmaat (afvalproductie) negatieve uitwerking kunnen hebben op een andere (bijvoorbeeld broeikasgasemissie), wil de werkgroep bewustwording creëren voor de ecologische verschillen tussen de verschillende manieren van toediening.
Onderbouwing
There are various methods of administering medications. However, in clinical practice, the most environmentally friendly, efficient, and patient-friendly methods are not always chosen. In hospitals, for example, parenteral administration is relatively often initiated and continued, even though enteral administration could result in less waste and greenhouse gas emissions. Additionally, infusion bags are often used when bolus administration could be just as effective and generate less waste. This module aims to provide recommendations on preferred methods of administration based on environmental considerations.
1. Climate change (critical)
|
Very low GRADE |
The evidence is very uncertain about the effect of enteral administration on climate change compared with intravenous administration in hospitalized patients.
Source: (Davies, 2024) |
2. Waste (critical)
2.1 Enteral versus parenteral
|
Very low GRADE |
The evidence is very uncertain about the effect of enteral therapy on waste compared with intravenous therapy in hospitalized patients.
Source: (Hermes, 2023) |
2.2 Subcutaneous (subtype of parenteral administration) versus intravenous (different subtype of parenteral administration)
|
Very low GRADE |
The evidence is very uncertain about the effect of subcutaneous therapy on drug waste compared with intravenous therapy in hospitalized patients.
Source: (Ponzetti, 2016) |
3. Eco-toxicity (important), human toxicity (important), water use (important), land use (important), acidification (important), eutrophication (important)
|
No GRADE |
Outcome measures ‘eco-toxicity’, ‘human toxicity’, ‘water use’, ‘land use’, ‘acidification’, and ‘eutrophication’ were not reported.
Source: - |
Description of studies
Three studies (Davies, 2024; Hermes, 2023; Ponzetti, 2016) were included in the literature analysis. Important study characteristics and results are summarized in the Evidence table. The risk of bias assessment is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Hermes (2023) conducted a cross-sectional observational study to evaluate the impact of switching from intravenous to oral antimicrobial therapy on hospital waste generation in a teaching hospital in Brazil. The intervention group received switch therapy, thus the drug administration route of the antimicrobials was switched from intravenous (IV) to enteral according to protocol. This protocol recommended switching to enteral administration after 2-3 days of IV administration based on predefined criteria. Inclusion criteria were based on available enteral formulation or a viable alternative, afebrile for at least 48 hours, and improvement in overall clinical status. Exclusion criteria were dysphagia, nausea and vomiting, absorptive and gastrointestinal motility disorder, leukocytosis or leukopenia, tachycardia or tachypnea, acute infectious diseases such as meningitis, endocarditis, and sepsis, as well as specific conditions like osteomyelitis, septic arthritis, deep abscess, and cystic fibrosis. The control group was not clearly described, but was assumed to be continued IV therapy. Data from 2019, 2020, and 2021, provided by the clinical pharmacy service of the hospital, were used. During this period, 275 switch therapy of antimicrobials were performed and analyzed. The reported environmental outcome measure was waste, which was defined as the amount of grams of waste (including needles, syringes, infusion bags, equipment, reconstituted solution bottles, and medication) that was not generated due to switch therapy compared to continued IV therapy.
Davies (2024) assessed the environmental impacts of perioperative paracetamol administration using a life cycle assessment (LCA) framework. The study compared the greenhouse gas (GHG) emissions of intravenous and enteral paracetamol formulations (tablet and liquid) across 26 hospitals in the USA, UK, and Australia. A life cycle inventory (LCI) approach was used, incorporating pharmaceutical production, packaging, transport, administration supplies, and waste disposal. Each input within the defined scope was matched with the corresponding unit process and cumulative LCI from the Ecoinvent 3.6 LCI database (ecoinvent, Zurich, Switzerland). In addition, data were collected retrospectively on perioperative paracetamol prescribing practices over a 12-month period, including the frequency of IV versus enteral administration and associated emissions. The reported environmental outcome measure was climate change (gCO2e).
Ponzetti (2016) conducted an observational study based on a systematic survey across 17 Italian hospitals to evaluate the hospital waste generation of subcutaneous versus intravenous administration of rituximab (for non-Hodgkin’s lymphoma) and trastuzumab (for breast cancer). The comparison focused on subcutaneous administration as the intervention and intravenous administration as the control. As the subcutaneous administration was not yet available in Italy at the time of the study, the analysis was based on theoretical modeling and survey responses rather than actual patient data. Each center provided data for five patients per therapy, comparing current intravenous practices with expected outcomes of subcutaneous administration. Eligibility was based on centers willing to share operational data; no specific patient-level inclusion or exclusion criteria were applied. The reported environmental outcome measure was waste, defined as the amount of drug wastage in micrograms.
Results
1. Climate change (critical)
1.1 Enteral versus parenteral
One study reported on climate change (gCO2e). Davies (2024) performed a cradle-to-grave life-cycle analysis. An overview of the results per country are presented in Table 1. The total life-cycle greenhouse emissions stemming from administering a 1g dose of paracetamol was the lowest for an enteral tablet (38 gCO2e) and the highest for an IV glass vial (628 gCO2e). The gCO2e difference between routes of paracetamol administration was mainly driven by the manufacturing of packaging and supplies. Overall, the estimated carbon emissions that could be saved by replacing intravenous paracetamol doses with enteral tablets was assessed at 5.7 ktCO2e across the USA, UK, and Australia. The guideline panel considered the difference in gCO2e between routes of paracetamol administration as relevant.
|
Location of dose; Brisbane, Australia |
Pharmaceutics |
Packaging & disposal |
Sterilisation |
Transport |
Administration equipment + disposal |
Total |
|
Oral tablet |
36.5 |
0.3 |
0.0 |
0.0 |
1.6 |
36.8* |
|
Enteral Liquid |
36.5 |
85.9 |
0.0 |
0.0 |
28.7 |
151.1* |
|
IV FK Glass |
40.5 |
427.5 |
33.5 |
25.9 |
87.2 |
614.6^ |
|
IV FK Freeflex |
40.5 |
142.7 |
6.3 |
7.8 |
87.2 |
284.4 |
|
IV B-Braun |
40.5 |
197.4 |
13.8 |
2.3 |
87.2 |
341.2 |
|
IV Ofirmez |
40.5 |
473.9 |
37.1 |
28.6 |
87.2 |
667.3^ |
|
Location of dose; London, UK |
Pharmaceutics |
Packaging & disposal |
Sterilisation |
Transport |
Administration equipment + disposal |
Total |
|
Enteral tablet |
36.5 |
0.1 |
0.0 |
0.0 |
1.6 |
38.2* |
|
Enteral Liquid |
36.5 |
85.9 |
0.0 |
0.0 |
28.7 |
151.1* |
|
IV FK Glass |
40.5 |
427.5 |
33.5 |
10.1 |
85.4 |
597.0^ |
|
IV FK Freeflex |
40.5 |
142.7 |
6.3 |
3.1 |
85.4 |
278.0 |
|
IV B-Braun |
40.5 |
197.4 |
13.8 |
0.3 |
85.4 |
337.4 |
|
IV Ofirmez |
40.5 |
473.9 |
37.1 |
10.2 |
85.4 |
647.1^ |
|
Location of dose; New York, USA |
Pharmaceutics |
Packaging & disposal |
Sterilisation |
Transport |
Administration equipment + disposal |
Total |
|
Enteral tablet |
36.5 |
0.3 |
0.0 |
0.0 |
1.6 |
38.4* |
|
Enteral Liquid |
36.5 |
85.9 |
0.0 |
0.0 |
28.7 |
151.1* |
|
IV FK Glass |
40.5 |
427.5 |
33.5 |
14.3 |
85.9 |
601.7^ |
|
IV FK Freeflex |
40.5 |
142.7 |
6.3 |
4.3 |
85.9 |
279.7 |
|
IV B-Braun |
40.5 |
197.4 |
13.8 |
2.3 |
85.9 |
339.9 |
|
IV Ofirmez |
40.5 |
473.9 |
37.1 |
6.2 |
85.9 |
643.6^ |
* lowest total amount of greenhouse gas carbon emissions
^ highest total amount of greenhouse gas carbon emissions
1.2 Other comparisons
No studies were found on other comparisons (parenteral versus topical, topical versus enteral, parenteral versus inhalation, topical versus inhalation, inhalation versus enteral) for outcome measure climate change.
2. Waste (critical)
2.1 Enteral versus parenteral
Hermes (2023) reported on the outcome measure of waste. During the analyzed period of three years (2019, 2020, 2021), the three main classes of antimicrobials for which a switch in route of administration was applied were cephalosporins (25.1%), penicillins (22.55%), and quinolones (17.45%). Over the total study period, 170,631 grams of waste (including needles, syringes, infusion bags, equipment, reconstituted solution bottles, and medication) was not generated due to switch therapy compared to continued IV therapy. The guideline panel considered this difference in waste as relevant.
Table 2. Estimation of the amount of waste that was not generated after antimicrobial switch therapy in 2019, 2020 and 2021 per type of antimicrobial (adopted from Hermes, 2023)
|
|
2019 |
2020 |
2021 |
|
IV-to-PO switches of antimicrobials, in no. of patients (%) |
62 (22.5%) |
85 (31.0%) |
128 (46.5%) |
|
Waste not generated by antimicrobial switch therapy, in grams |
30,066
|
56,301
|
84,264 |
2.2 Subcutaneous (subtype of parenteral administration) versus intravenous (different subtype of parenteral administration)
Ponzetti (2016) reported on the outcome measure of waste. Subcutaneous administration was associated with a decreased estimated drug wastage compared to intravenous administration for both rituximab and trastuzumab (see Table 3).
Table 3. Estimation of drug waste generation for subcutaneous versus intravenous administration of rituximab and trastuzumab
|
Rituximab wastage (for Non-Hodgkin’s lymphoma) |
|||
|
|
Subcutaneous administration |
Intravenous administration |
Difference (95% CI)1; % |
|
Total median wastage (mg) for a full treatment cycle (95% CI) |
13 (95% CI -5 to 38) |
204 (95% CI -85 to 493) |
-191 (95% CI -1350 to 968); -94% |
|
Total median annual wastage wastage (mg) for a full treatment cycle (95% CI) |
159 (95% CI -66 to 384) |
2454 (95% CI -1018 to 5926) |
-2294 (95% CI -16213 to 11623); -94% |
|
Trastuzumab wastage (for breast cancer) |
|||
|
Total median wastage (mg) for a full treatment cycle (95% CI) |
0 |
614 (95% CI 245 to 983) |
-614 (95% CI -1998 to 770); -100% |
|
Total median annual wastage wastage (mg) for a full treatment cycle (95% CI) |
0 |
7376 (95% CI 2937 to 11815) |
-7376 (95% CI -23987 to 9235); -100% |
195% Cis were calculated based on reported data
2.3 Other comparisons
No studies were found on other comparisons (parenteral versus topical, topical versus enteral, parenteral versus inhalation, topical versus inhalation, inhalation versus enteral) for outcome measure waste.
3. Eco-toxicity (important), human toxicity (important), water use (important), land use (important), acidification (important), eutrophication (important)
No studies were found on important outcome measures eco-toxicity, human toxicity, water use, land use, acidification, and eutrophication.
Level of evidence of the literature
1. Climate change (critical)
The level of evidence regarding the outcome measure ‘climate change’ was downgraded with three levels to very low because of risk of bias (-2; limited transparency on impact assessment, sensitivity/uncertainty analyses were lacking, limitations inadequately critically appraised) and indirectness (-1; heterogeneity of interventions).
2. Waste (critical)
2.1 Enteral versus parenteral
The level of evidence regarding the outcome measure ‘waste’ was downgraded with three levels to very low due to risk of bias (-1; lack of adequate adjustment for confounders, no follow-up), indirectness (-1; heterogeneity of interventions, assumptions regarding the control-group, limited generalizability as only one study is included), and imprecision (-1; lacking information on data distribution).
2.2 Subcutaneous (subtype of parenteral administration) versus intravenous (different subtype of parenteral administration)
The level of evidence regarding the outcome measure ‘waste’ was downgraded with three levels to very low because of risk of bias (-1; uncertainty regarding assessment of exposure and outcome due to the use of questionnaire data), indirectness (-1; data solely based on assumptions derived from questionnaire data), and imprecision (-1; due to wide confidence intervals).
3. Eco-toxicity (important), human toxicity (important), water use (important), land use (important), acidification (important), eutrophication (important)
Outcomes were not reported, thus could not be graded.
A systematic review of the literature was conducted to answer the following question:
What is the environmental impact of various ways of applying pharmacological treatment to hospitalized patients?
Table PICO
| Patients | Hospitalized patients receiving pharmaceutical treatment |
| Intervention | Various application methods (parenteral, enteral, topical, inhalation) |
| Control | All comparisons |
| Outcomes | Climate change (CO2 footprint/Global Warming Potential (GWP)), waste, eco-toxicity, human toxicity, water use, land use, acidification, eutrophication |
| Other selection criteria |
Study design: systematic reviews, randomized controlled trials, comparative observational studies (cohort studies, case-control studies), life cycle assessments Period: from 2010 |
Relevant outcome measures
This module focuses specifically on environmental outcomes. Currently, there is no standardized or acknowledged core outcome set available in the field of environmental impact. Therefore, the guideline panel focused on outcomes used in environmental assessments such as life cycle assessments, material flow analyses, waste audits, and footprinting.
The guideline panel considered climate change (CO2 footprint/Global Warming Potential) and waste as critical outcome measures for decision making; and eco-toxicity, human toxicity, water use, land use, acidification, and eutrophication as important outcome measures for decision making.
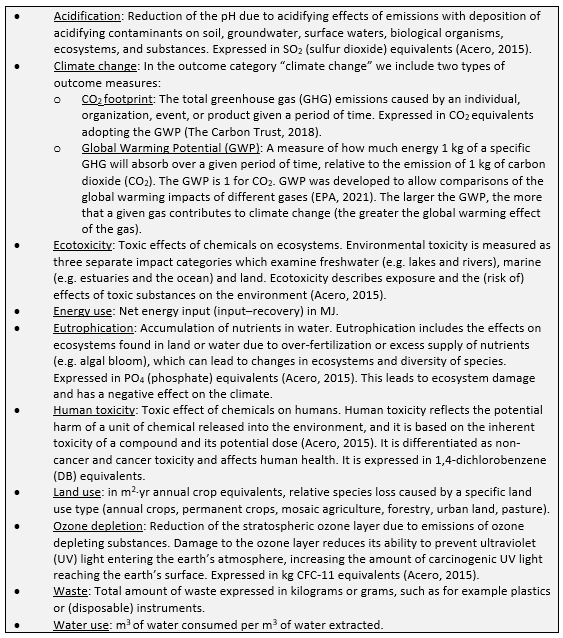
A priori, the guideline panel defined the outcome measures listed above according to the glossary provided in Box 1, which is adapted from leidraad Duurzaamheid in richtlijnen.
Due to the variety of scopes and methods used in studies to perform and report results, the guideline panel did not define the minimal important difference a priori. Differences between the interventions were evaluated by the guideline panel after data extraction.
Box 1. Glossary
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 2010 until 20 August 2024. The detailed search strategy is listed under the tab ‘Literature search strategy’. The systematic literature search resulted in 1863 hits, after deduplication. Due to this large number of hits, the active learning tool ASReview (https://www.asreview.nl) was used to screen the studies on title and abstract.
Studies were selected based on the following criteria:
- Systematic reviews in which searches were performed in at least two databases, with a detailed search strategy, risk of bias assessment and results of individual studies available, randomized controlled trials, (observational) comparative studies, LCA.
- Full-text English or Dutch language publication and
- Studies according to the PICO.
Initially, fifteen studies were selected based on the title and abstract screening in ASReview. After reading the full text, twelve studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’) and three studies were included (Davies, 2024; Hermes, 2023; Ponzetti, 2016).
- Acero, A. P., Rodríguez, C., & Ciroth, A. LCIA methods Impact assessment methods in Life Cycle Assessment and their impact categories. GreenDelta GmbH, Berlin, Germany. 2015. 23.
- Akhloufi H, Hulscher M, Melles DC, Prins JM, van der Sijs H, Verbon A. Development of operationalized intravenous to oral antibiotic switch criteria. J Antimicrob Chemother. 2017 Feb;72(2):543-546. doi: 10.1093/jac/dkw470. Epub 2016 Dec 20. PMID: 27999021.
- Bickhardt J, Czupalla C, Bader U. Reduktion klimaschädlicher Treibhausgase durch Auswahl der Inhalatoren in der Therapie von Patienten mit Asthma und COPD [Reduction of greenhouse gas emissions by inhaler choice in the therapy of asthma and COPD patients]. Pneumologie. 2022 May;76(5):321-329. German. doi: 10.1055/a-1771-5292. Epub 2022 Apr 22. PMID: 35453159.
- Chancel L. Global carbon inequality over 1990–2019. Nat Sustain. 2022 Sep;5:931–938. doi: 10.1038/s41893-022-00955-z.
- Davies JF, McAlister S, Eckelman MJ, McGain F, Seglenieks R, Gutman EN, Groome J, Palipane N, Latoff K, Nielsen D, Sherman JD; TRA2SH, GASP and WAAREN collaborators. Environmental and financial impacts of perioperative paracetamol use: a multicentre international life-cycle assessment. Br J Anaesth. 2024 Dec;133(6):1439-1448. doi: 10.1016/j.bja.2023.11.053. Epub 2024 Jan 30. PMID: 38296752.
- Dychter SS, Gold DA, Carson D, Haller M. Intravenous therapy: a review of complications and economic considerations of peripheral access. J Infus Nurs. 2012 Mar-Apr;35(2):84-91. doi: 10.1097/NAN.0b013e31824237ce. PMID: 22382792.
- Eii MN, Walpole S, Aldridge C. Sustainable practice: Prescribing oral over intravenous medications. BMJ. 2023 Nov 6;383:e075297. doi: 10.1136/bmj-2023-075297. PMID: 37931943.
- Faber M, Montforts MHMM, Roex EWM. Risico’s van pijnstillers in het oppervlaktewater: keuzes voor gebruik op basis van milieueffecten. Bilthoven: Rijksinstituut voor Volksgezondheid en Milieu (RIVM); 2023. RIVM-rapport 2023-0117. [cited 2025 Jul 8]. Available from: https://www.rivm.nl/bibliotheek/rapporten/2023-0117.pdf.
- Freeling F, Maria K. Björnsdotter MK. Assessing the environmental occurrence of the anthropogenic contaminant trifluoroacetic acid (TFA). Current Opinion in Green and Sustainable Chemistry. 2023 Jun;41:100807.doi: 10.1016/j.cogsc.2023.100807.
- Hagendoorn P, de Boer AH, Frijlink HW. Het belang van inhalatietechnologie voor een optimale luchtwegbehandeling. Ned Tijdschr Allergie & Astma 2016;16:130-136.
- Harvey EJ, Hand K, Weston D, Ashiru-Oredope D. Development of National Antimicrobial Intravenous-to-Oral Switch Criteria and Decision Aid. J Clin Med. 2023 Mar 7;12(6):2086. doi: 10.3390/jcm12062086. PMID: 36983089; PMCID: PMC10058706.
- Hermes VC, Loureiro AP, Assis MP, Balbinot F, Frighetto I, Ziembowicz H, Menezes RM, Carneiro M. Pharmacoeconomic and antimicrobial stewardship analysis in waste management: Beyond switching drug administration route. Am J Infect Control. 2023 Dec;51(12):1334-1338. doi: 10.1016/j.ajic.2023.06.003. Epub 2023 Jun 8. PMID: 37295674.
- van Herwaarden N, van den Elsen GAH, de Jong ICA, Kramers CK, Kloppenburg M, van den Bemt BJF. Topicale NSAID’s: ineffectief of ondergewaardeerd? [Topical NSAIDs: ineffective or undervalued?]. Ned Tijdschr Geneeskd. 2021 May 19;165:D5317. Dutch. PMID: 34346575.
- Jessurun JG, Hunfeld NGM, de Roo M, van Onzenoort HAW, van Rosmalen J, van Dijk M, van den Bemt PMLA. Prevalence and determinants of medication administration errors in clinical wards: A two-centre prospective observational study. J Clin Nurs. 2023 Jan;32(1-2):208-220. doi: 10.1111/jocn.16215. Epub 2022 Jan 23. PMID: 35068001; PMCID: PMC10286768.
- Kalmar AF, Rex S, Vereecke H, Teunkens A, Dewinter G, Struys MMRF. Environmental Effects of Propofol Versus Sevoflurane for Maintenance Anesthesia. Anesth Analg. 2025 Mar 1;140(3):740-742. doi: 10.1213/ANE.0000000000007248. Epub 2024 Oct 16. PMID: 39413035.
- Mallama M, Valencia A, Rijs K, Rietdijk WJR, Klimek M, Calvache JA. A systematic review and trial sequential analysis of intravenous vs. oral peri-operative paracetamol. Anaesthesia. 2021 Feb;76(2):270-276. doi: 10.1111/anae.15163. Epub 2020 Jun 18. PMID: 32557588; PMCID: PMC7818191.
- Nguyen CD, Panganiban HP, Fazio T, Karahalios A, Ankravs MJ, MacIsaac CM, Rechnitzer T, Arno L, Tran-Duy A, McAlister S, Ali Abdelhamid Y, Deane AM. A Randomized Noninferiority Trial to Compare Enteral to Parenteral Phosphate Replacement on Biochemistry, Waste, and Environmental Impact and Healthcare Cost in Critically Ill Patients With Mild to Moderate Hypophosphatemia. Crit Care Med. 2024 Jul 1;52(7):1054-1064. doi: 10.1097/CCM.0000000000006255. Epub 2024 Mar 25. PMID: 38537225.
- Nederlands Huisartsen Genootschap (NHG). NHG-Standaard Astma bij volwassenen. Utrecht: NHG; 2020 [cited 2025 Jul 8]. Available from: https://richtlijnen.nhg.org/standaarden/astma-bij-volwassenen.
- Nederlandse Vereniging voor Anesthesiologie (NVA). Richtlijn Postoperatieve pijn. Utrecht: Federatie Medisch Specialisten; 2023 [cited 2025 Jul 8]. Available from: https://richtlijnendatabase.nl/richtlijn/postoperatieve_pijn/startpagina_-_postoperatieve_pijn.html.
- Nederlandse Vereniging van Ziekenhuisapothekers (NVZA). Leidraad ‘Liever enterale dan parenterale therapie’ [Internet]. Utrecht: NVZA; 2025 Oct 10 [cited 2025 Jul 21]. Available from: https://nvza.nl/wp-content/uploads/Leidraad-%E2%80%98liever-enterale-dan-parenterale-therapie.pdf.
- Osorio D, Maldonado D, Rijs K, van der Marel C, Klimek M, Calvache JA. Efficacy of different routes of acetaminophen administration for postoperative pain in children: a systematic review and network meta-analysis. Can J Anaesth. 2024 Aug;71(8):1103-1116. doi: 10.1007/s12630-024-02760-y. Epub 2024 Apr 15. PMID: 38622469; PMCID: PMC11269386.
- Patiëntenfederatie Nederland, NHG, LHV, KNMP, FMS, Zorgverzekeraars Nederland. Leidraad verantwoord wisselen medicijnen. Versie 2024 [Internet]. Utrecht: Federatie Medisch Specialisten; 2024 [cited 2025 Jul 21]. Available from: https://demedischspecialist.nl/sites/default/files/2022-11/Leidraad_Verantwoord_Wisselen_Medicijnen_versie15nov2022.pdf.
- Patiëntenfederatie Nederland, Longfonds, NVALT, NHG, LHV, KNMP, Zorgverzekeraars Nederland. Leidraad verantwoord wisselen medicijnen: addendum longinhalatie medicijnen [Internet]. Utrecht: Federatie Medisch Specialisten; 2023 Aug [cited 2025 Jul 21]. Available from: https://demedischspecialist.nl/sites/default/files/2023-09/Leidraad_verantwoord_wisselen_addendum%20longinhalatie.pdf
- Ponzetti C, Canciani M, Farina M, Era S, Walzer S. Potential resource and cost saving analysis of subcutaneous versus intravenous administration for rituximab in non-Hodgkin's lymphoma and for trastuzumab in breast cancer in 17 Italian hospitals based on a systematic survey. Clinicoecon Outcomes Res. 2016 May 23;8:227-33. doi: 10.2147/CEOR.S97319. Erratum in: Clinicoecon Outcomes Res. 2017 Jan 17;9:75. doi: 10.2147/CEOR.S118835. PMID: 27284260; PMCID: PMC4883807.
- Sankaranarayanan J, Reardon T, Olsen KM. Correlates and economic outcomes of proton pump inhibitor use by routes in intensive care unit patients. Expert Rev Pharmacoecon Outcomes Res. 2014 Oct;14(5):741-9. doi: 10.1586/14737167.2014.940902. Epub 2014 Jul 25. PMID: 25059290.
- Santander S, Le Guennec L, de Maisoncelle I, Liou A, Marois C. Comparison of environmental, economic and professional impacts of levetiracetam according to its administration route in intensive care unit. Intensive Care Med. 2024 Oct;50(10):1708-1710. doi: 10.1007/s00134-024-07575-5. Epub 2024 Sep 2. PMID: 39222138.
- Samenwerkingsverband Richtlijnen Infectiepreventie (SRI). VTGM: Voor Toediening Gereed Maken van medicatie – Module 2a. Utrecht: SRI; 2024 [cited 2025 Jul 8]. Available from: https://www.sri-richtlijnen.nl/vtgm-toediening-medicatie/module-2a.
- The Lancet Public Health Editorial Board. No public health without planetary health. Lancet Public Health. 2022 Apr;7(4):e291. doi: 10.1016/S2468-2667(22)00068-8.
- Wald-Dickler N, Holtom PD, Phillips MC, Centor RM, Lee RA, Baden R, Spellberg B. Oral Is the New IV. Challenging Decades of Blood and Bone Infection Dogma: A Systematic Review. Am J Med. 2022 Mar;135(3):369-379.e1. doi: 10.1016/j.amjmed.2021.10.007. Epub 2021 Oct 27. PMID: 34715060; PMCID: PMC8901545.
- Wichers IM, Pieters LI. Milieu-impact van inhalatoren in Nederland en wereldwijd [Environmental impact of inhalers in the Netherlands and worldwide: the facts at a glance]. Ned Tijdschr Geneeskd. 2022 Oct 4;166:D6718. Dutch. PMID: 36300443.
- Wilkinson JL, Boxall ABA, Kolpin DW, Leung KMY, Lai RWS, Galbán-Malagón C, Adell AD, Mondon J, Metian M, Marchant RA, Bouzas-Monroy A, Cuni-Sanchez A, Coors A, Carriquiriborde P, Rojo M, Gordon C, Cara M, Moermond M, Luarte T, Petrosyan V, Perikhanyan Y, Mahon CS, McGurk CJ, Hofmann T, Kormoker T, Iniguez V, Guzman-Otazo J, Tavares JL, Gildasio De Figueiredo F, Razzolini MTP, Dougnon V, Gbaguidi G, Traoré O, Blais JM, Kimpe LE, Wong M, Wong D, Ntchantcho R, Pizarro J, Ying GG, Chen CE, Páez M, Martínez-Lara J, Otamonga JP, Poté J, Ifo SA, Wilson P, Echeverría-Sáenz S, Udikovic-Kolic N, Milakovic M, Fatta-Kassinos D, Ioannou-Ttofa L, Belušová V, Vymazal J, Cárdenas-Bustamante M, Kassa BA, Garric J, Chaumot A, Gibba P, Kunchulia I, Seidensticker S, Lyberatos G, Halldórsson HP, Melling M, Shashidhar T, Lamba M, Nastiti A, Supriatin A, Pourang N, Abedini A, Abdullah O, Gharbia SS, Pilla F, Chefetz B, Topaz T, Yao KM, Aubakirova B, Beisenova R, Olaka L, Mulu JK, Chatanga P, Ntuli V, Blama NT, Sherif S, Aris AZ, Looi LJ, Niang M, Traore ST, Oldenkamp R, Ogunbanwo O, Ashfaq M, Iqbal M, Abdeen Z, O'Dea A, Morales-Saldaña JM, Custodio M, de la Cruz H, Navarrete I, Carvalho F, Gogra AB, Koroma BM, Cerkvenik-Flajs V, Gombač M, Thwala M, Choi K, Kang H, Ladu JLC, Rico A, Amerasinghe P, Sobek A, Horlitz G, Zenker AK, King AC, Jiang JJ, Kariuki R, Tumbo M, Tezel U, Onay TT, Lejju JB, Vystavna Y, Vergeles Y, Heinzen H, Pérez-Parada A, Sims DB, Figy M, Good D, Teta C. Pharmaceutical pollution of the world's rivers. Proc Natl Acad Sci U S A. 2022 Feb 22;119(8):e2113947119. doi: 10.1073/pnas.2113947119. PMID: 35165193; PMCID: PMC8872717.
- Woodcock A, Janson C, Rees J, et al. Effects of switching from a metered dose inhaler to a dry powder inhaler on climate emissions and asthma control: post-hoc analysis. Thorax. 2022;77(12):1187-1192. doi: 10.1136/thoraxjnl-2021-218088. PMID: 35131893; PMCID: PMC9685707.
- van Zanten AR, Engelfriet PM, van Dillen K, van Veen M, Nuijten MJ, Polderman KH. Importance of nondrug costs of intravenous antibiotic therapy. Crit Care. 2003 Dec;7(6):R184-90. doi: 10.1186/cc2388. Epub 2003 Oct 14. PMID: 14624694; PMCID: PMC374380.
- Zorginstituut Nederland. Transmurale leidraad klimaatbewust voorschrijven van inhalatiemedicatie. Diemen: Zorginstituut Nederland; 2025 Apr 9 [cited 2025 Jul 8]. Available from: https://www.zorginstituutnederland.nl/publicaties/publicatie/2025/04/09/transmurale-leidraad-klimaatbewust-voorschrijven-van-inhalatiemedicatie.
Evidence table for LCA studies
|
Study reference |
Journal |
Study characteristics |
Methods |
Data collection |
Outcomes |
Interpretation |
Comments |
|
Davies, 2024 |
British Journal of Anaesthesia
Journal information: Peer-reviewed journal focused on all branches of anaesthesia, critical care medicine, pain medicine and perioperative medicine including fundamental, translational and clinical sciences, clinical practice, technology, education and training.
Critical review: Peer reviewed article. Not in specific LCA journal. |
Type of study: LCA
Objective: To estimate greenhouse gas (GHG) emissions associated with intravenous and oral formulations of perioperative paracetamol
LCA-method: Not specified
Setting and country: 26 hospitals in USA, UK and Australia
Facility: Large tertiary, specialty, district general, and regional hospitals
Years of data collection: 2020-2021 (audit data), with national surgical encounter data from 2019-2020
Surgical discipline(s): Various elective surgical procedures requiring anaesthesiology care
Funding and conflicts of interest: All authors declare no support from any organization for the submitted work; no financial relationships with any organizations that might have an interest in the submitted work in the previous 3 yr; and no other relationships or activities that could appear to have influenced the submitted work. JS is associate editorial board member and adviser on sustainability of the British Journal of Anaesthesia. |
Goal and scope1: To assess the environmental impact of intravenous versus oral perioperative paracetamol administration. The scope of the LCA included paracetamol (intravenous, oral tablet, and oral liquid formulations), administration supplies (e.g. a paper pill cup, syringe, or an intravenous fluid set), all packaging, transport (from site of production to hospital), and waste disposal management by incineration.
Functional unit(s)2: A single 1 g dose of paracetamol, administered to a patient by either intravenous, oral tablet, or oral liquid routes
System boundaries: Cradle-to-grave
Included stages: Production, formulation, packaging, sterilization, distribution, use, disposal
Stated excluded components: Production and transport of pharmaceutical precursors to production site, hospital or capital equipment production or maintenance, storage, disposal of waste pharmaceutical agent.
Inventory database: Ecoinvent 3.6 LCI database
Allocation: No
Normalization & Weighting: Yes
Impacts reported: No
Contribution analysis: No
Scenario analysis: No
Comparative analysis: No
Sensitivity analysis: No
Uncertainty analysis: No
Variance analysis: No |
Inputs required for API synthesis were modelled following the advanced process calculation. Typical yields, reaction temperatures, and solvent use were derived from Labmonk (open platform of laboratory protocols). Energy calculations in each step included heating and cooling for the reactor, stirring, and pumping. Manufacturing quantities for all non-API formulation ingredients and processing steps of filtration, mixing, and filling (for liquid) or drying and compression (for tablets) were obtained from Sharma et al. The mass of all medication packaging materials required to administer a 1 g dose were broken down and weighed according to composition using scales with a 0.01 g resolution. The quantity of energy required for producing the formulation (including steam sterilization in the case of intravenous formulations) was extrapolated from Sharma et al, and the sterilizing process for intravenous formulations was validated directly with one pharmaceutical company. Steam sterilization data were modelled from previously published LCA data for intravenous morphine 100 ml vials. Shipping distances were calculated from nearest manufacturing sites for each brand to a port located within reasonable proximity to the hospitals studied (ground transport from ports not included). For drug administration, the LCA included a representative intravenous fluid line, a paper pill cup (oral tablet), or a 10ml plastic Luer slip syringe (oral liquid). It was assumed that intravenous fluid lines were used for administering more agents than just paracetamol; therefore, for each dose of intravenous paracetamol, 25% of fluid line was attributed to each dose.
For those surgical patients for whom oral formulations were indicated, CO2e of actual prescribing practices for intravenous or oral doses were compared with optimal oral prescribing based on audit data on perioperative paracetamol prescribing practices. |
Climate change The carbon footprint for a 1 g dose was 38 g CO2e (oral tablet), 151 g CO2e (oral liquid), and 310-628 g CO2e (intravenous dependent on type of packaging and administration supplies). If an additional dedicated plastic tubing set was used to administer intravenous paracetamol instead of using a line already in use, an additional 342 g CO2e was added for an intravenous paracetamol dose.
The estimated carbon emissions that could be saved by replacing intravenous paracetamol doses with oral tablets would be 4.7 kt CO2e in the USA, 923.3 t CO2e in the UK, and 70.4 CO2e in Australia. |
Intravenous paracetamol has significantly more environmental impact than oral formulations.
Glass vials result in higher emissions than plastic vials.
Replacing unnecessary intravenous paracetamol with oral tablets could reduce healthcare emissions by ~5.7 kt CO2e across the USA, UK, and Australia. |
Limitations: * Recycling of pharmaceutical packaging was not modelled, and it is possible that recycling some packaging components could result in fewer GHGs.
Authors conclusion: Replacing intravenous paracetamol with oral tablets where feasible is a safe, cost-effective, and environmentally preferable strategy that should be prioritized in perioperative care.
|
1 Goals and scope: ‘Phase of life cycle assessment in which the aim of the study, and in relation to that, the breadth and depth of the study is established’
2 Functional unit: Quantified description of the function of a product or process that serves as the reference basis for all calculations regarding impact assessment.
Evidence table for intervention studies (RCTs and non-randomized observational studies)
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention |
Comparison/ control |
Follow-up |
Outcome measures and effect size |
Comments |
||||||||||
|
Hermes, 2023 |
Type of study: Observational study
Setting and country: Teaching hospital, Brazil
Funding and conflicts of interest: No information on funding was reported. Authors declared no competing interests. |
No patients involved |
Switch therapy: switching the drug administration route of antimicrobials from intravenous formulation to per-oral formulation |
Continued intravenous therapy: not further described |
No follow-up |
Waste not generated by switch therapy
|
Comment: For the preparation and administration of intravenous drugs, each medicine has a preparation kit that includes: a syringe, needle, distilled water for reconstitution, solution for dilution, equipment, and bottle of the drug. The composition of this kit varies according to the antimicrobial.
Limitations: *The increase in ST intervention between the years 2020 and 2021 resulted in a significant increase in waste not generated. * The in-hospital mortality rate for the years under study, which was not evaluated, despite the pandemic main years.
Authors conclusion: The conversion of intravenous to oral antimicrobial therapy has resulted in a significant reduction in the generation of intravenous therapy waste. |
||||||||||
|
Ponzetti, 2016 |
Type of study: Observational study
Setting and country: 19 clinical centers including both hematology and oncology departments, Italy
Funding and conflicts of interest: Funding from Roche S.p.A. Monica Canciani (MC) and Massimo Farina (MF) are employees of EmmEffe, the consultancy firm that executed the research, and they received funding from Roche S.p.A. Sara Era (SE) is an employee of Roche S.p.A. Stefan Walzer (SW) received funding from Roche S.p.A. for interpretation, analysis, and writing of the research.
|
No patients involved; each center provided information based on five hypothetical patient cases, reflecting typical treatment processes. |
Subcutaneous administration of rituximab and trastuzumab Rituximab (for non-Hodgkin’s lymphoma):
Trastuzumab (for breast cancer):
|
Subcutaneous administration of rituximab and trastuzumab Rituximab (for non-Hodgkin’s lymphoma):
Trastuzumab (for breast cancer):
|
No follow-up |
Waste (difference between subcutaneous and intravenous administration) Rituximab:
Trastuzumab
|
Limitations: *The study was based on a theoreticalc omparison using questionnaires, not on actual patient data or clinical outcomes. *There was no follow-up or monitoring of patients over time. *No hospitals from southern Italy were included, which may limit generalizability. *A few centers contributed disproportionately to the data (e.g., two centers provided over 50% of NHL data), introducing potential center bias. *The results are based on assumptions about standard procedures and may not reflect all real-world variations.
Authors conclusion: Subcutaneous administration significantly reduces drug wastage compared to intravenous administration. |
Risk of Bias tables
Hermes (2023, cross-sectional, observational, and retrospective study); Ponzetti (2016, cross-sectional study using data from questionnaires)
|
Author, year |
Selection of participants
Was selection of exposed and non-exposed cohorts drawn from the same population?
|
Exposure
Can we be confident in the assessment of exposure?
|
Outcome of interest
Can we be confident that the outcome of interest was not present at start of study?
|
Confounding-assessment
Can we be confident in the assessment of confounding factors?
|
Confounding-analysis
Did the study match exposed and unexposed for all variables that are associated with the outcome of interest or did the statistical analysis adjust for these confounding variables? |
Assessment of outcome
Can we be confident in the assessment of outcome?
|
Follow up
Was the follow up of cohorts adequate? In particular, was outcome data complete or imputed?
|
Co-interventions
Were co-interventions similar between groups?
|
Overall Risk of bias
|
|
Hermes, 2023 |
Not applicable
Reason: It applied switch therapy versus continued intravenous therapy
|
Definitely yes
Reason: The two groups were compared in this observational study, data from a clinical pharmacy service were used. |
Definitely no
Reason: Waste was present during whole study period.
|
Definitely no
Reason: No statistical analysis regarding confidence intervals/ uncertainty, confounding was performed. |
Probably no
Reason: See previous comment. |
Probably yes
Reason: Data were provided by the clinical pharmacy service. However, it was not described how the data were collected. |
Definitely no
Reason: The amount of waste was measured cross-sectionally for three years. |
No information
Reason: Not reported. |
HIGH (waste)
|
|
Ponzetti, 2016 |
Not applicable
Reason: no patients were included, as the study compared subcutaneous versus intravenous administration based on data from questionnaires |
Probably no
Reason: The study did not directly observe or measure actual administration of the therapies. Exposure was assessed indirectly through questionnaires completed by hospital staff, based on routine practices and hypothetical scenarios. The subcutaneous administration was not yet available in Italy at the time of the study, so its assessment was based on expectations, not real-world implementation. There may be variation in interpretation across centers, and no validation of the reported data. |
Definitely no
Reason: Waste was present during whole study period.
|
Not applicable
Reason: The study did not collect or analyze patient-level data, so no confounding variables (e.g. age, disease severity, comorbidities) were identified or measured. The analysis was based on hypothetical scenarios and aggregated estimates from hospital staff, not on actual treatment outcomes. Statistical adjustment for confounding was therefore not possible.
|
Not applicable
Reason: See previous comment |
Probably no
Reason: Wastage was not measured directly in clinical practice. The estimates were based on staff-reported data and theoretical assumptions about how much drug would be wasted with intravenous vs. subcutaneous administration. The subcutaneous formulations were not yet in use during the study, so wastage reduction was projected, not observed. Additionally, 12 out of 17 centers reported no wastage for these therapies, suggesting inconsistency in reporting. |
Definitely no
Reason: The study did not involve cohorts or longitudinal follow-up. It was a cross-sectional survey, based on hypothetical scenarios and staff-reported data, not actual patient outcomes.
|
Not applicable
Reason: no actual patient data was used, therefore there was no information regarding co-interventions |
HIGH (waste)
|
Davies (2024, LCA): Critical appraisal of LCAs (based on Drew, 2021)
Drew (2021) developed a critical appraisal pro forma, based on Weidema’s guidelines for critical review of LCA (Weidema, 1997). This scoring system consists of 16 appraisal criteria, which are divided between the different phases of an LCA. It addresses a range of study quality indicators, such as internal validity, external validity, consistency, transparency, and bias. The percentage score provides an indication of the overall study quality. A higher score indicates a higher overall study quality. The points that can be obtained are displayed in the column labeled "appraisal criteria".
|
Appraisal criteria |
Indicator(s) |
Key effect modifiers |
Davies (2024) |
|
Phase 1: Goal & Scope (13 points) |
|
|
|
|
Study goal is clearly stated, including the study's rationale (1), intended application (1), and intended audience (1) |
Transparency |
|
3 |
|
Lifecycle assessment method is clearly stated (1) |
Transparency |
Process-based life-cycle assessment, which is well suited to product-level analysis, may underestimate environmental impacts (i.e. from truncation error); economic input-output lifecycle assessment (EIO-LCA), which uses aggregate data and is well-suited to sector-level analysis, may overestimate environmental impacts |
0 |
|
Functional unit is clearly defined and measurable (1), justified (1), and consistent with the study's intended application (1) |
Consistency |
|
2 |
|
The system to be studied is adequately described with clearly stated system boundaries (1), lifecycle stages (1), and appropriate justification of any omitted stages (1) |
Transparency; bias |
Assessments with narrow system boundaries that exclude a number of lifecycle stages are prone to underestimating life-cycle environmental impacts |
2 |
|
The system covers production (1), use/reuse (1) and disposal (1) of materials and energy (half mark if only for energy and vice versa) |
Internal Validity; completeness |
|
1.5 |
|
Phase 2: Inventory analysis (7 points) |
|
|
|
|
The data collection process is clearly explained, including the source(s) of foreground material weights and energy values (1); the source(s) of reference data (e.g. inventory database; 1); and what data are included (e.g. production and disposal of unit processes; 1) |
Transparency, internal Validity |
|
3 |
|
Representativeness of the data is discussed (1), differences in electricity generating mix are accounted for (1), and the potential significance of exclusions or assumptions is addressed (1) |
Internal validity; external validity |
|
0 |
|
Allocation procedures, where necessary, are described and appropriately justified (1; mark given if no allocation used) |
Transparency; bias |
|
1 |
|
Phase 3: Impact assessment (6 points) |
|
|
|
|
Impact categories (1), characterization method (1), and software used (1) are documented transparently |
Transparency |
|
1 |
|
Results are clearly reported in the context of the functional unit (1) (0.5 if graphically, 0 if only normalized results reported) |
Consistency; transparency |
|
1 |
|
A contribution analysis is performed and clearly reported (1), and hotspots are identified (1) |
|
|
0 |
|
Phase 4: Interpretation (9 points) |
|
|
|
|
Conclusions are consistent with the goal and scope (1) and supported by the impact assessment results (1) |
Internal Validity; consistency |
|
2 |
|
Results are contextualized through the use of sensitivity analysis (1) and uncertainty analysis (1) |
Internal Validity |
|
0 |
|
Limitations are adequately discussed (1), and the potential impact of omissions or assumptions on the study's outcomes are described (1) |
Bias |
|
1 |
|
The assessment has been critically appraised (i.e. peer review if journal article or independent, external critical review if report/thesis; 1) |
Bias |
|
1 |
|
Source(s) of funding and any potential conflict(s) of interest are disclosed (1), and are unlikely to be a source of bias (1) |
Bias |
|
2 |
|
|
Total (/35) |
|
20.5 |
|
|
Percentage score |
|
59% |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Forshay CM, Hansen KN, Eckel SF. Using intravenous pump infusion data to optimize continuous infusion concentrations and reduce drug and fluid waste. Am J Health Syst Pharm. 2020 Sep 4;77(18):1497-1503. doi: 10.1093/ajhp/zxaa199. PMID: 32779706. |
Wrong study design (modelling study) |
|
Gonzalez E, Glick JA, Shan G, Talbot JN. Economic and workload impact of therapeutic interchange of inhaler medications and nebulizer solutions. Am J Health Syst Pharm. 2021 Jan 1;78(1):41-48. doi: 10.1093/ajhp/zxaa343. PMID: 33103194. |
Wrong outcome |
|
Gordon DW. Environmental impact of anesthetic drugs. Curr Opin Anaesthesiol. 2024 Aug 1;37(4):379-383. doi: 10.1097/ACO.0000000000001395. Epub 2024 Jun 4. PMID: 38842001. |
Wrong study design (narrative review) |
|
Hayward A, Huang L, Nagy J, Moretti K. Pushing for IV Push Medications: Cost-Effectiveness Model of Switching from IV Piggyback to IV Push for Frequently Used Emergency Department Medications. R I Med J (2013). 2024 Feb 1;107(2):44-47. PMID: 38285753. |
Wrong outcome |
|
Hernandez C, Rodrigues C, Marques P, Freire F. Life cycle assessment of a large volume parenteral for hospital use. Resour Conserv Recycl. 2023;198:107120. doi: 10.1016/j.resconrec.2023.107120. |
No comparison |
|
LaCrone ME, Buening N, Paul N. A Retrospective Review of an Inhaler to Nebulizer Therapeutic Interchange Program Across a Health System. J Pharm Pract. 2023 Oct;36(5):1211-1216. doi: 10.1177/08971900221101761. Epub 2022 May 21. PMID: 35603944. |
Wrong outcome |
|
Leraut J, Boissinot L, Hassani Y, Bonnet-Zamponi D, Le Gonidec P. Réduire l’impact environnemental des inhalateurs dispensés en ville et à l’hôpital en France. Du diagnostic à l’action durable [Reducing the environmental impact of inhalers dispensed in France. From diagnosis to sustainable action]. Ann Pharm Fr. 2023 Jan;81(1):123-137. French. doi: 10.1016/j.pharma.2022.08.003. Epub 2022 Aug 6. PMID: 35944697. |
Full text unavailable |
|
Mihajlović J, Bax P, van Breugel E, Blommestein HM, Hoogendoorn M, Hospes W, Postma MJ. Microcosting Study of Rituximab Subcutaneous Injection Versus Intravenous Infusion. Clin Ther. 2017 Jun;39(6):1221-1232.e4. doi: 10.1016/j.clinthera.2017.05.342. Epub 2017 Jun 1. PMID: 28579210. |
Wrong outcome |
|
Novosel S, Prangenberg C, Wirtz DC, Burger C, Welle K, Kabir K. Klimawandel: Wie die Chirurgie zur Erderwärmung beiträgt [Climate change: how surgery contributes to global warming]. Chirurgie (Heidelb). 2022 Jun;93(6):579-585. German. doi: 10.1007/s00104-021-01551-1. Epub 2022 Feb 9. PMID: 35138418; PMCID: PMC9133313. |
Article in German |
|
Ten Have P, van Hal P, Wichers I, Kooistra J, Hagedoorn P, Brakema EA, Chavannes N, de Heer P, Ossebaard HC. Turning green: the impact of changing to more eco-friendly respiratory healthcare - a carbon and cost analysis of Dutch prescription data. BMJ Open. 2022 Jun 14;12(6):e055546. doi: 10.1136/bmjopen-2021-055546. PMID: 35701064; PMCID: PMC9198801. |
Wrong setting (primary and secondary care) |
|
Voudrias E, Goudakou L, Kermenidou M, Softa A. Composition and production rate of pharmaceutical and chemical waste from Xanthi General Hospital in Greece. Waste Manag. 2012 Jul;32(7):1442-52. doi: 10.1016/j.wasman.2012.01.027. Epub 2012 Feb 24. PMID: 22365264. |
Wrong comparison |
|
Yang L, Hubert J, Gitundu S, Brovman E, Cobey F. Carbon Footprint of Total Intravenous and Inhalation Anesthesia in the Transcatheter Aortic Valve Replacement Procedure. J Cardiothorac Vasc Anesth. 2024 Jun;38(6):1314-1321. doi: 10.1053/j.jvca.2024.02.027. Epub 2024 Feb 22. PMID: 38490897. |
Wrong comparison |
Beoordelingsdatum en geldigheid
Publicatiedatum : 07-05-2026
Beoordeeld op geldigheid : 07-05-2026
Algemene gegevens
De ontwikkeling/herziening van deze module werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd door de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de leidraad.
Samenstelling werkgroep
Voor het ontwikkelen van de leidraad is in 2024 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij farmaceutisch specialistische zorg.
Werkgroep Inhoud
- Dr. L.J.M. (Loes) van Herpen – Meeuwissen (voorzitter), ziekenhuisapotheker, Radboudumc, NVZA
- Dr. M.E. (Milly) Attema – de Jonge, ziekenhuisapotheker, Meander MC, NVZA
- Dr. C. (Charlotte) Bekker, universitair docent, Radboudumc, persoonlijke titel
- Drs. V. (Vivienne) de Smet, AIOS spoedeisende geneeskunde, Diakonessenhuis, NVSHA
- Dr. N.G.M. (Nicole) Hunfeld, ziekenhuisapotheker, universitair hoofddocent, Erasmus MC, NVIC
- Dr. B.J.A. (Ben) Janssen, farmacoloog, universitair hoofddocent, Maastricht UMC, persoonlijke titel
- Dr. B. (Berber) Kapitein, kinderarts-intensivist, Amsterdam UMC, NVK
- Drs. R. (Remco) Minkhorst, anesthesioloog, UMC Utrecht, NVA
- Drs. J.D. (Joost) Piët, arts-docent en promovendus farmacotherapie, Amsterdam UMC, NVKFB
- Y.H.M. (Yvonne) van Grinsven – Ariaans, (regie)verpleegkundige, Radboudumc, V&VN
- M. (Marga) van Timmeren, kwaliteitsfunctionaris, BModesto, NVFZ
Werkgroep Implementatie
- B.A.P. (Bart) Cramers, apotheker, programmamanager dure geneesmiddelen, NVZ
- Drs. M. (Maarten) Loof, programmamanager dure geneesmiddelen, ZN
- P. (Peter) Roos, adviseur, UMCNL (voorheen NFU; tot december 2024)
- Prof. dr. E.L. (Noortje) Swart, ziekenhuisapother, hoogleraar Klinische Farmacologie en Apotheek, hoofd adeling klinische farmacologie en apotheek, Amsterdam UMC, UMCNL (vanaf maart 2025)
Klankbordgroep
- Dr. P.H.P (Pascal) de Jong, reumatoloog, universitair hoofddocent, Erasmus MC, NVR
- Dr. F. (Femme) Dirksmeier – Harinck, MDL-arts, Franciscus, NVMDL
- Prof. dr. W.J.K. (Wouter) Hehenkamp, gynaecoloog, hoogleraar gynaecologie gericht op doelmatige en duurzame zorg, Amsterdam UMC, NVOG
- Drs. A. (Annemieke) Horikx, apotheker, KNMP
- Dr. J.J.W.M. (Jeroen) Janssen, internist-hematoloog, Radboudumc, NIV
- Dr. P.H.C. (Philip) Kremer, neuroloog, Leids Universitair Medisch Centrum, NVN
- Dr. M. (Maartje) Los, internist-oncoloog, St. Antonius Ziekenhuis, NIV
- Prof. dr. F.M.A.C. (Fabrice) Martens, cardioloog, hoogleraar Preventieve cardiologie, Amsterdam UMC, NVVC
- Drs. N.M.F. (Nikki) Noorda, klinisch geriater, Dijklander Ziekenhuis, NVKG
- Dr. S. (Sam) Schoenmakers, gynaecoloog, Erasmus MC, NVOG
- Drs. D.C. (Dorothée) van Trier, traumachirurg, Diakonessenhuis, NVvH
- P. (Paula) Warmerdam, verpleegkundig specialist, Alrijne Ziekenhuis, V&VN
Met ondersteuning van
- Dr. R. (Renee) Bolijn, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. T. (Thibaut) Dederen, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. C.T.J. (Charlotte) Michels, senior adviseur, Kennisinstituut van de Federatie Medisch Speclisten
- E. (Esther) van der Bijl, Informatiespecialist, Kennisinstituut van de Federatie Medisch Speclisten
Belangenverklaringen
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Gemelde belangen |
Ondernomen actie |
|
Werkgroep Inhoud |
||||
|
Van Herpen – Meeuwissen (voorzitter) |
Ziekenhuisapotheker, Radboudumc, Nijmegen |
NVZA: lid commissie Duurzaamheid |
* ZonMW, Medicatie in eigen beheer 848022007. * Auteur: |
Geen restricties |
|
Attema – de Jonge |
Ziekenhuis apotheker, Meander Medisch Centrum, Amersfoort |
Lid Commissie Duurzaamheid NVZA |
Geen |
Geen restricties |
|
Bekker |
Senior onderzoeker, Radboudumc, Nijmegen |
Voorzitter NFU werkgroep Green deal duurzame zorg thema 5 'medicijnen' |
* ZonMw Heruitgifte orale oncolytica 848018008 * ZonMw RODEO trial 10140021910501 * Transformatieovereenkomst heruitgifte orale oncolytica * VWS Green Deal duurzame zorg thema 5 'medicijnen' * Senior onderzoeker duurzaam geneesmiddelgebruik |
Geen restricties |
|
De Smet |
AIOS SEH, Diakonessenhuis, Utrecht |
* Lid commissie Groene SEH |
Geen |
Geen restricties |
|
Hunfeld |
* Ziekenhuisapotheker, Erasmus MC, Rotterdam (betaald) * Projectleider onderzoek duurzame zorg, Erasmus MC, Rotterdam (betaald) |
* Vice voorzitter en penningmeester KNMP (betaald) * Voorzitter Groene IC NVIC (onbetaald) vVoorzitter commissie ATG (LCG) (betaald) * Toezichthouder VVT Het Maanderzand (betaald) * Lid Commissie Duurzaamheid NVZA |
NWO (geen onderzoek over medicijnen) |
Geen restricties |
|
Janssen (Ben) |
Universitair Hoofddocent Farmacologie, Vakgroep Farmacologie & Toxicologie, Faculty of Health Medicines and Life Sciences Maastricht University. Werk op afdeling Beeldvorming van het Maastrichts Universitair Medisch Centrum. |
Geen |
Geen |
Geen restricties |
|
Kapitein |
Kinderarts-intensivist, Emma Kinderziekenhuis Amsterdam UMC, Amsterdam |
* Lid Groene Kinderarts * NVK Lid wetenschapscommissie |
* MACU-PICU Stichting CJ Vaillant. Multisystem phenotyping of severe ACUte asthma at the Pediatric Intensive Care Unit (macu-pico). Postdoc (geen PI). * AUMC Medewerkersberaad innovatie subsidie "Het AUMC medewerkersberaad: op weg naar duurzaam woon-werkverkeer (studie reeds afgerond). |
Geen restricties |
|
Minkhorst |
Anesthesioloog UMC Utrecht |
Geen |
Geen |
Geen restricties |
|
Piët |
*Fulltime arts-docent en -onderzoeker Farmacotherapie in het AmsterdamUMC (locatie VUmc). *Al het onderwijs betreffende het voorschrijven van medicatie verzorgen voor de opleidingen geneeskunde, tandheelkunde en masteropleidingen voor verpleegkundigen. *Promovendus op gebied van het integreren van milieu-impact door medicatie in het medisch onderwijs. Deze werkzaamheden zijn allen betaald vanuit mijn aanstelling. |
* Klinisch farmacoloog in opleiding * Projectcoördinator Erasmus+ projecten CP4T en PlanED Prescribing |
Erasmus+ projecten: * Planetary Health Education in Prescribing (PlanED Prescribing) * Clinical Pharmacology and Therapeutics Teach The Teacher (CP4T)
Auteur NTvG artikel "Vermindering van de milieu-impact van medicatie; De rol van de voorschrijver" (D7985) (Toekomstige) Uitkomsten (wetenschappelijk) van Erasmus+ project PlanED Prescribing en van eigen PhD. PMID 39303730 |
Geen restricties |
|
Van Grinsven – Ariaans |
* Verpleegkundige Orthopedie Radboudumc (contract 12 uur, betaald) * Kwaliteitsfunctionaris afdeling Orthopedie/KNO/MKA/PCH/Trauma Radboudumc (contract 12 uur, betaald) |
Geen |
Geen |
Geen restricties |
|
Van Timmeren |
Sr Quality Officer, Bmodesto, Lelystad |
Geen |
Geen |
Geen restricties |
|
Werkgroep Implementatie |
||||
|
Cramers |
Programmamanager Dure Geneesmiddelen NVZ Belangenbehartiging ziekenhuizen op dure geneesmiddelen gebied. Gaat over kwaliteit, beschikbaarheid en betaalbaarheid. |
Geen |
Geen |
Geen restricties |
|
Loof |
Programmamanager Dure Geneesmiddelen bij ZN |
Geen |
Geen |
Geen restricties |
|
Roos |
Adviseur binnen NFU |
Geen |
Geen |
Geen restricties |
|
Swart |
Hoofd Afdeling Apotheek en Klinische Farmacologie, AmsterdamUMC |
* Voorzitter Wetenschappelijke Adviesraad Commissie Farmacotherapeutisch Kompas (WAR CFK), Zorginstituut Nederland * Voorzitter NVKFB. * Lid bestuur KNMP |
Echtgenoot werkt bij Pfizer in een niet commerciële functie. Geen relatie met werkgroep
Medicijn voor de Maatschappij: Bereidingen voor zeldzame metabole ziekten. |
Geen restricties |
|
Klankbordgroep |
||||
|
De Jong |
Reumatoloog, Erasmus MC, Rotterdam |
* Lid adviesraad voor Abbvie; AstraZeneca; Bristol-Myers Squibb; Galapagos; Lilly; Novartis; Pfizer; Sanofi Genzyme; UCB * Verzorging van onderwijs voor Abbvie; Galapagos; Lilly; Novartis; Pfizer |
Subsidies voor investigated initiated studies van Abbvie; Dutch Arthritis Foundation; Galapagos; Lilly; Pfizer. 1. Abbvie, ontwikkelen tool voor zorg op afstand, projectleider. 2. Dutch Arthitis Foudation, gecombineerde leefstijlinterventie trial, projectleider. 3. Galapagos: trial naar belandeling op maat. 4. Pfizer: Toediening van medicatie obv chronobiologie, projectleider. 5. Lilly: Implementatieonderzoek gericht op persoonsgerichte zorg, projectleider. |
Geen restricties |
|
Dirksmeier – Harinck |
MDL-arts, Franciscus, Rotterdam |
Geen |
Geen |
Geen restricties |
|
Hehenkamp |
Gynaecoloog, AmsterdamUMC, Amsterdam |
Allen onbetaald: -lid pijlerbestuur gynaecologie -voorzitter Gynae Goes Green (landelijke groen commissie GYN) -lid bestuur SIG anticonceptie -Bestuur Hector Treub stichting |
1. ZonMW: Substitutie van zorg Covid, projectleider. 2. ZonMW: Ulipristal bij myomen., projectleider. 3. Merit Medical: QUESTA trial (adenomyose en hysterectomie danwel embolisatie). 4. ZonMW: Keuzehulp Myomen, projectleider. |
Geen restricties |
|
Horikx |
Apotheker, teamleider Geneesmiddel Informatie Centrum KNMP |
* Bestuurslid Stichting Farmaceutisch Erfgoed. * Commissielid interacterende medicatie VKA's. * Werkgroeplid kritische en kwetsbare geneesmiddelenlijst-NVZA. * Praktijkteamlid palliatieve zorg |
Geen |
Geen restricties |
|
Janssen (Jeroen) |
internist-hematoloog, Afdeling Hematologie, Radboud UMC, Nijmegen, betaald |
* Voorzitter, St. Apps for Care and Science, betaald. * Bestuurslid en penningmeester, Nederlandse Vereniging voor Hematologie, onbetaald |
De St. Apps for Care and Science ontwikkelt de HematologyApp, een smartphone-, tablet- en binnenkort ook web-based applicatie die als doel heeft het werk van hematologen te verbeteren, de kwaliteit van de zorg voor hematologische patienten te verbeteren en klinisch wetenschappelijk onderzoek te bevorderen. Deze stichting zoekt ondersteuning voor het behalen van haar doelen bij farmaceutische bedrijven die initatieven van de stichting kunnen sponsoren. De volgende bedrijven zijn sponsor/donateur van de stichting: Daiichi-Sankyo, Johnson & Johnson, SERB, Sanofi, SOBI, Novo-Nordisk, MSD, Biomea, AstraZeneca, BristolMyersSquibb, Alexion, Kite-Gilead, Pfizer, Abbvie, Astellas,Novartis, Amgen, Takeda en Servier. |
Geen restricties |
|
Kremer |
*Research Director Neurology bij The Centre for Human Drug Research, Leiden * Neuroloog bij het Leids Universitair Medisch Centrum, Leiden |
Geen |
In het CHDR ben ik verantwoordelijk voor ongeveer 10 vroege fase medicijnstudies gefinancierd door veelal Amerikaanse biotech of grote farma. De onderzoeksmiddelen zitten dermate vroeg in het ontwikkeltraject dat er geen belangenverstrengeling is. |
Geen restricties |
|
Los |
internist oncoloog in het St Antonius Ziekenhuis Utrecht/ Nieuwegein |
Geen |
Geen |
Geen restricties |
|
Martens |
Cardioloog, hoogleraar Preventieve Cardiologie bij het Amsterdam UMC, Amsterdam. Namens de NVVC vertegenwoordigend. |
* Adviseur CVRM en medicatie NVVC. * Voorzitter Werkgroep Geneesmiddelen NVVC * Voorzitter DCVA Commissie Preventie * Clinical Valorization Officer Amsterdam UMC *Voorzitter Hartstichting Hart-Vaatagenda-project 'Op tijd ontdekken' Wetenschappelijk nog wel verbonden aan het HartVaatCentrumSalland |
Sprekersvergoeding zonder belangenverstrengeling gezien altijd naar Amsterdam UMC.
Sponsoring GOLDEN-studie: Novartis, Amarin, Novo Nordisk en een Europese IHI-grant. Sponsoring 2-DECIDE-studie: ZoNMW en ZE&GG Sponsoring EUROASPIRE: Hartstichting |
Geen restricties |
|
Noorda |
Klinisch geriater in het Dijklanderziekenhuis |
Geen |
Geen |
Geen restricties |
|
Schoenmakers |
Gynaecoloog, Erasmus MC Universtair Medisch Centrum, Rotterdam |
* Wetenschap-commissielid Strong Babies (onbetaald) * Gezondheidsraad - algemeen / commissie vaccinatie (vacatiegelden) |
ZonMW Open Competitie (2019-2024) - ondewerp Obesitas, microbioom en zwangerschap |
Geen restricties |
|
Van Trier |
(Trauma) Chirurg OLVG en BovenIJ Ziekenhuis |
* Werkgroep Groen OK NVVH. * Tevens lid van de werkgroep Plastic en Circulair van het Landelijk Netwerk Groene OK, onbetaald. |
Geen |
Geen restricties |
|
Warmerdam |
Verpleegkundig specialist werkzaam bij Alrijne |
Presentaties geven aan POH en Huisartsen |
Geen |
Geen restricties |
Inbreng patiëntenperspectief
De werkgroep besteedde aandacht aan het patiëntenperspectief door het uitnodigen van de Patiëntenfederatie Nederland (PFN) voor deelname aan de werkgroep Inhoud en aan twee invitational conferences. Op advies van de PFN heeft de werkgroep de uitkomsten uit het rapport Verduurzaming van de zorg geïntergreerd in de modules. Daarnaast is module 6 Communicatie over milieubewust medicatiegebruik specifiek gericht op communicatie over milieubewust medicatiegebruik met patiënten. De conceptleidraad is tevens voor commentaar voorgelegd aan de PFN en de aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de leidraad voerde de werkgroep conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de leidraad per module op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
Toedieningsvormen van medicatie |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
Voor meer details over de gebruikte methodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze leidraad is hieronder weergegeven.
Zoekverantwoording
Zoekstrategie - 20 augustus 2024
Embase.com
|
No. |
Query |
|
#1 |
'hospital patient'/exp OR 'outpatient'/exp OR 'hospital care'/exp OR 'hospital management'/exp OR ((within NEXT/2 hospital*):ti,ab,kw) OR ((setting* NEAR/2 hospital*):ti,ab,kw) OR 'inpatient*':ti,ab,kw OR 'out patient*':ti,ab,kw OR 'outpatient*':ti,ab,kw OR 'outward patient*':ti,ab,kw OR 'inhospital*':ti,ab,kw OR 'intramural care':ti,ab,kw OR hospital*:ti,ab,kw |
|
#2 |
'drug administration'/de OR 'drug administration route'/exp OR 'oral drug administration'/exp OR 'intravenous drug administration'/exp OR 'parenteral drug administration'/exp OR 'parenteral solution'/exp OR 'bolus injection'/exp OR 'infusion'/exp OR 'infusion bag'/exp OR 'drug packaging'/de OR ('packaging material'/exp AND 'drug'/exp) OR (((iv OR intravenous OR 'intra venous' OR parenteral* OR oral OR 'per os' OR 'p.o.' OR subcutan*) NEAR/3 (drug* OR deliver* OR therap* OR medicat* OR administer* OR dos* OR drip* OR infusion* OR inject* OR therap* OR transfusion* OR infusion* OR treatment* OR administrat* OR applicat* OR rout* OR medicine*)):ti,ab,kw) OR ((bolus* NEAR/3 (inject* OR administrat* OR iv OR intravenous OR 'intra venous' OR intramuscular OR subcutan* OR intradermal OR epidural OR intrathecal)):ti,ab,kw) OR (((inhalation* OR interstitional OR intraabdominal OR 'intra abdominal' OR intraarticular OR 'intra articular' OR intrabilliar* OR intracardia* OR intracartilag* OR intracardal OR intracavernous OR intracavitar* OR intracochlear OR intradermal OR intraductal OR intrahepatic OR intralesional OR intraluminal OR intralymph* OR intramammary OR intraneural OR intraocular OR intraosseous OR intraovarian OR intravenous OR intrapancreatic OR intraperitoneal OR intraplantar OR intraprostatic OR intrarenal OR intrasplen* OR intratendinous OR intratesticul* OR intrathoracic OR intratumoural OR intratumoral OR intratympanic OR intraurethral OR intrauterine OR intravascular OR intraarterial OR intravesical OR 'intra billiar*' OR 'intra cardia*' OR 'intra cartilag*' OR 'intra cardal' OR 'intra cavernous' OR 'intra cavitar*' OR 'intra cochlear' OR 'intra dermal' OR 'intra ductal' OR 'intra hepatic' OR 'intra lesional' OR 'intra luminal' OR 'intra lymph*' OR 'intra mammary' OR 'intra neural' OR 'intra ocular' OR 'intra osseous' OR 'intra ovarian' OR 'intra pancreatic' OR 'intra peritoneal' OR 'intra plantar' OR 'intra prostatic' OR 'intra renal' OR 'intra splen*' OR 'intra tendinous' OR 'intra testicul*' OR 'intra thoracic' OR 'intra tumoural' OR 'intra tumoral' OR 'intra tympanic' OR 'intra urethral' OR 'intra uterine' OR 'intra vascular' OR 'intra arterial' OR 'intra vesical' OR periarticular OR perineural OR periocular OR periodontal OR peritumoral OR 'regional perfusion' OR respiratory OR intrabronch* OR intrapleur* OR intrapulmonar* OR intratracheal OR laryngeal OR oropharyngeal OR transtracheal OR retrobulbar OR 'soft tisuue*' OR subcutan* OR submucosal* OR subplantar OR transplancental OR transtymppanic OR ureteral) NEAR/4 (inject* OR punctur* OR 'drug administrat*' OR 'drug treatment' OR 'drug deliver*' OR infusion* OR biop*)):ti,ab,kw) OR (((vein* OR venous) NEAR/2 (injection* OR drip* OR infusion* OR transfusion* OR administer*)):ti,ab,kw) OR (((infusion* OR iv OR intravenous OR 'intra venous') NEAR/2 bag*):ti,ab,kw) OR 'drip* infusion*':ti,ab,kw |
|
#3 |
#1 AND #2 |
|
#4 |
'biodegradable plastic'/exp OR 'biodiversity'/de OR 'climate change'/exp OR 'climate resilience'/exp OR 'disposable equipment'/exp OR 'ecological diversity'/exp OR 'energy conservation'/exp OR 'environmental aspects and related phenomena'/exp OR 'environmental footprint'/exp OR 'environmental protection'/exp OR 'eutrophication'/exp OR 'life cycle assessment'/exp OR 'pollution and pollution related phenomena'/exp OR 'species diversity'/exp OR 'waste and waste related phenomena'/exp OR 'wastewater'/exp OR 'water management'/exp OR 'water pollution'/exp OR 'global warming potential'/exp OR acidification:ti,ab,kw OR (((water OR land) NEXT/1 use):ti,ab,kw) OR (((air OR organic OR soil OR water OR plastic* OR liquid*) NEAR/4 (pollut* OR contamina* OR wast*)):ti,ab,kw) OR biodivers*:ti,ab,kw OR 'biological divers*':ti,ab,kw OR (((co2 OR 'co 2' OR carbon OR 'nitrous oxide') NEAR/3 (emission* OR footprint OR equival* OR reduct*)):ti,ab,kw) OR (((nature OR environment* OR climat*) NEAR/3 (impact* OR pollut* OR conservat* OR protect* OR preserv* OR effect* OR benefit* OR chang* OR exposure* OR resilien*)):ti,ab,kw) OR disposable*:ti,ab,kw OR ((eco* NEAR/3 (toxic* OR efficien* OR damage)):ti,ab,kw) OR ecotoxic*:ti,ab,kw OR ecoefficien*:ti,ab,kw OR (((emission OR waste) NEAR/3 reduc*):ti,ab,kw) OR environmental*:ti OR (((equipment* OR product* OR waste*) NEAR/3 reus*):ti,ab,kw) OR recycl*:ti,ab,kw OR 'resource recover*':ti,ab,kw OR eutrophicat*:ti,ab,kw OR (((global OR climate) NEAR/2 warming):ti,ab,kw) OR ((green* NEAR/2 (deal OR surger* OR effect* OR gas* OR resource*)):ti,ab,kw) OR (((hospital OR medical OR zero OR product* OR byproduct* OR 'by product*' OR avoid* OR energy OR management OR nuclear OR biomass) NEAR/3 waste*):ti,ab,kw) OR ((('life cycle' OR lifecycle) NEAR/2 (assess* OR inventor*)):ti,ab,kw) OR lca:ti,ab,kw OR lcas:ti,ab,kw OR 'human toxicity potential*':ti,ab,kw OR (((ep OR h+ OR gwp OR faetp OR fatp OR ap OR cfc OR 'kg n' OR 'nox' OR '2.4' OR '2,4' OR pocp OR so2 OR dichlorobenzen* OR ethan* OR po4 OR dcb) NEAR/3 equival*):ti,ab,kw) OR ((ozone NEAR/3 (deplet* OR hole*)):ti,ab,kw) OR (((plastic* OR microplastic* OR 'micro plastic*') NEAR/3 (overuse OR soup OR pollut* OR contaminat*)):ti,ab,kw) OR recycle*:ti,ab,kw OR recycling:ti,ab,kw OR (((refuse OR waste) NEAR/3 disposal):ti,ab,kw) OR reusable*:ti,ab,kw OR reuse*:ti,kw OR reusing:ti,kw OR 'rising sea level*':ti,ab,kw OR 'sea level ris*':ti,ab,kw OR smog:ti,ab,kw OR sustainab*:ti,kw OR ((sustainab* NEAR/3 (development* OR cycle* OR management OR effect* OR environment*)):ti,ab,kw) OR ((water NEAR/3 (purificat* OR sanitat* OR treatment)):ti,ab,kw) OR wastewater:ti,ab,kw OR ((hydrogen NEAR/3 moles NEAR/3 equival*):ti,ab,kw) OR 'circular econom*':ti,ab,kw OR biodegradab*:ti,ab,kw OR (((ecological OR environmental OR water OR energy OR climate OR global) NEAR/2 footprint*):ti,ab,kw) OR waste:ti,ab,kw OR wastes:ti,ab,kw OR reuse:ti,ab,kw OR reusab*:ti,ab,kw OR reprocess*:ti,ab,kw OR pollut*:ti,ab,kw OR greening:ti,ab,kw OR spillage:ti,ab,kw OR spilling:ti,ab,kw OR spoilage:ti,ab,kw OR salinization:ti,ab,kw OR 'cradle to cradle':ti,ab,kw OR 'carbon neutral*':ti,ab,kw OR wastage*:ti,ab,kw |
|
#5 |
#3 AND #4 |
|
#6 |
#5 AND [2010-2024]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) - totaal |
Ovid/Medline
|
# |
Searches |
|
1 |
exp Patients/ or exp Hospitalization/ or (within adj2 hospital*).ti,ab,kf. or (setting* adj2 hospital*).ti,ab,kf. or inpatient*.ti,ab,kf. or out patient*.ti,ab,kf. or outpatient*.ti,ab,kf. or outward patient*.ti,ab,kf. or inhospital*.ti,ab,kf. or intramural care.ti,ab,kf. or hospital*.ti,ab,kf. |
|
2 |
exp Drug Administration Routes/ or exp Administration, Oral/ or exp Administration, Intravenous/ or exp Infusions, Parenteral/ or *Drug Packaging/ or (((iv or intravenous or intra venous or parenteral* or oral or per os or subcutan*) adj3 (drug* or deliver* or therap* or medicat* or administer* or dos* or drip* or infusion* or inject* or therap* or transfusion* or infusion* or treatment* or administrat* or applicat* or rout* or medicine*)) or (bolus* adj3 (inject* or administrat* or iv or intravenous or intra venous or intramuscular or subcutan* or intradermal or epidural or intrathecal)) or ((inhalation* or interstitional or intraabdominal or intra abdominal or intraarticular or intra articular or intrabilliar* or intracardia* or intracartilag* or intracardal or intracavernous or intracavitar* or intracochlear or intradermal or intraductal or intrahepatic or intralesional or intraluminal or intralymph* or intramammary or intraneural or intraocular or intraosseous or intraovarian or intravenous or intrapancreatic or intraperitoneal or intraplantar or intraprostatic or intrarenal or intrasplen* or intratendinous or intratesticul* or intrathoracic or intratumoural or intratumoral or intratympanic or intraurethral or intrauterine or intravascular or intraarterial or intravesical or intra billiar* or intra cardia* or intra cartilag* or intra cardal or intra cavernous or intra cavitar* or intra cochlear or intra dermal or intra ductal or intra hepatic or intra lesional or intra luminal or intra lymph* or intra mammary or intra neural or intra ocular or intra osseous or intra ovarian or intra pancreatic or intra peritoneal or intra plantar or intra prostatic or intra renal or intra splen* or intra tendinous or intra testicul* or intra thoracic or intra tumoural or intra tumoral or intra tympanic or intra urethral or intra uterine or intra vascular or intra arterial or intra vesical or periarticular or perineural or periocular or periodontal or peritumoral or regional perfusion or respiratory or intrabronch* or intrapleur* or intrapulmonar* or intratracheal or laryngeal or oropharyngeal or transtracheal or retrobulbar or soft tisuue* or subcutan* or submucosal* or subplantar or transplancental or transtymppanic or ureteral) adj4 (inject* or punctur* or drug administrat* or drug treatment or drug deliver* or infusion* or biop*)) or ((vein* or venous) adj2 (injection* or drip* or infusion* or transfusion* or administer*)) or ((infusion* or iv or intravenous or intra venous) adj2 bag*) or drip* infusion*).ti,ab,kf. |
|
3 |
1 and 2 |
|
4 |
Biodegradable Plastics/ or exp Biodiversity/ or exp Carbon Footprint/ or exp Environmental Pollution/ or exp Climate Change/ or Disposable Equipment/ or Environment/ or Equipment Reuse/ or exp Eutrophication/ or Greenhouse Gases/ or Greenhouse Effect/ or exp Hazardous Waste/ or exp Medical Waste/ or Ozone Depletion/ or Recycling/ or exp Refuse Disposal/ or Smog/ or Waste Products/ or exp Waste Water/ or acidification.ti,ab,kf. or ((air or organic or soil or water or plastic* or liquid*) adj4 (pollut* or contamina* or wast*)).ti,ab,kf. or (biodivers* or "biological divers*").ti,ab,kf. or ((co2 or "co 2" or carbon) adj3 (emission* or footprint or equival* or reduct*)).ti,ab,kf. or ((nature or environment* or climat*) adj3 (impact* or pollut* or conservat* or protect* or preserv* or effect* or benefit* or chang* or exposure* or resilien*)).ti,ab,kf. or disposable*.ti,ab,kf. or (eco* adj3 (toxic* or efficien* or damage)).ti,ab,kf. or ecotoxic*.ti,ab,kf. or ecoefficien*.ti,ab,kf. or ((waste or emission*) adj3 reduc*).ti,ab,kf. or environmental*.ti. or ((equipment* or product* or waste*) adj3 reus*).ti,ab,kf. or recycl*.ti,ab,kf. or resource recover*.ti,ab,kf. or eutrophicat*.ti,ab,kf. or ((global or climate) adj2 warming).ti,ab,kf. or (("life cycle" or lifecycle) adj2 (assess* or inventor*)).ti,ab,kf. or LCA.ti,ab,kf. or LCAs.ti,ab,kf. or (("life cycle" or lifecycle) adj2 (assess* or inventor* or analys*)).ti,ab,kf. or (green* adj2 (deal or surger* or effect* or gas* or resource*)).ti,ab,kf. or greening.ti,ab,kf. or ((hospital or medical or zero or product* or byproduct* or "by product*" or avoid* or energy or management or nuclear or biomass) adj3 waste*).ti,ab,kf. or "human toxicity potential*".ti,ab,kf. or ((EP or H+ or GWP or FAETP or FATP or AP or CFC or "kg N" or "NOx" or "2.4" or "2,4" or POCP or SO2 or dichlorobenzen* or ethan* or PO4 or DCB) adj3 equival*).ti,ab,kf. or (ozone adj3 (deplet* or hole*)).ti,ab,kf. or ((plastic* or microplastic* or "micro plastic*") adj3 (overuse or soup or pollut* or contaminat*)).ti,ab,kf. or recycle*.ti,ab,kf. or recycling.ti,ab,kf. or ((refuse or waste) adj3 disposal).ti,ab,kf. or reusable*.ti,ab,kf. or reuse*.ti,kf. or reusing.ti,kf. or "rising sea level*".ti,ab,kf. or "sea level ris*".ti,ab,kf. or smog.ti,ab,kf. or sustainab*.ti,kf. or (sustainab* adj3 (development* or cycle* or management or effect* or environment*)).ti,ab,kf. or (water adj3 (purificat* or sanitat* or treatment)).ti,ab,kf. or wastewater.ti,ab,kf. or (hydrogen adj3 moles adj3 equival*).ti,ab,kf. or "circular econom*".ti,ab,kf. or biodegradab*.ti,ab,kf. or ((ecological or environmental or water or energy or global or climat*) adj2 footprint*).ti,ab,kf. or (waste adj3 by product*).ti,ab,kf. or waste.ti,ab,kf. or wastes.ti,ab,kf. or reuse.ti,ab,kf. or reusab*.ti,ab,kf. or reprocess*.ti,ab,kf. or pollut*.ti,ab,kf. or (microplastic* and pollut*).ti,ab,kf. or greening.ti,ab,kf. or spillage.ti,ab,kf. or spoilage.ti,ab,kf. or salinization.ti,ab,kf. or "cradle to cradle".ti,ab,kf. or 'compostable plastic*'.ti,ab,kf. or desertification.ti,ab,kf. or deforestation.ti,ab,kf. or 'algal bloom*'.ti,ab,kf. or eco-friendly.ti,ab,kf. or ecofriendly.ti,ab,kf. or 'global change'.ti,ab,kf. or 'climate change'.ti,ab,kf. or "carbon neutral*".ti,ab,kf. or wastage*.ti,ab,kf. |
|
5 |
3 and 4 |
|
6 |
limit 5 to yr="2010 -Current" - totaal |
