Neuromodulatie bij chronische bekkenpijn
Uitgangsvraag
Wat is de plaats van neuromodulatie als behandeling voor patiënten met chronische bekkenpijn?
Aanbeveling
Aanbeveling-1
Overweeg patiënten met chronische bekkenpijn in een vroege fase van behandeling percutane Posterior Tibial Nerve Stimulation (P-PTNS) aan te bieden.
Pas transcutane PTNS (T-PTNS) alleen toe ter ondersteuning van percutane PTNS (P-PTNS).
Pas andere vormen van neuromodulatie zoals perineale stimulatie en PTNS via een implantaat alleen toe in onderzoekverband.
Aanbeveling-2
Behandel patiënten met chronische bekkenpijn met sacrale neuromodulatie alleen indien alle andere therapieën ineffectief zijn gebleken en indien er tevens therapieresistente urge urine-incontinentie of fecale incontinentie is.
Verwijs patiënten die in aanmerking komen voor sacrale neuromodulatie naar een multidisciplinair expertisecentrum.
Overwegingen
De onderstaande overwegingen en aanbevelingen gelden voor het overgrote deel van de populatie waarop de uitgangsvraag betrekking heeft.
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Sacrale neuromodulatie
Op basis van de literatuur is het onduidelijk wat het effect van sacrale neuromodulatie op de cruciale uitkomstmaat ‘pijnintensiteit’ is bij patiënten met chronische bekkenpijn. De geïncludeerde studies lieten een klinisch relevant verschil in pijn zien na sacrale neuromodulatie, vergeleken met baseline scores. Het vertrouwen in deze conclusie is echter gegradeerd met een GRADE ‘zeer laag’, doordat er louter observationeel vergelijkend onderzoek was gevonden waarin pre- en post-baseline scores werden vergeleken (geen placebo-gecontroleerde studies). Het vóórkomen van complicaties bij sacrale neuromodulatie werd alleen beschrijvend gepresenteerd in deze studies, waardoor de bewijskracht niet kon worden gegradeerd door middel van GRADE. Er werden geen studies over sacrale neuromodulatie geïncludeerd waarin patiënttevredenheid en kwaliteit van leven na sacrale neuromodulatie werden bestudeerd.
Voor sacrale neuromodulatie is het van belang dat dit een operatieve interventie betreft waarin adequate blindering niet toe te passen is aangezien patiënten het voelen wanneer de neuromodulator aan of uit staat. Dit gebrek heeft een direct gevolg op de kwaliteit van het bewijs. Een voordeel van sacrale neuromodulatie is dat er een testfase kan worden geïncludeerd om effectiviteit in de individuele patiënt te evalueren voor het plaatsen van een definitief implantaat. De meeste studies (12) uit de literatuuranalyse betreffen de retrograde techniek die ook in de klinische praktijk het meeste wordt toegepast. Voor de retrograde techniek betreft het in het overgrote merendeel patiënten die een unilaterale electrode hebben gekregen. Maar twee studies beschrijven de antegrade (caudale) techniek. Derhalve zal de aanbevelingen in deze richtlijn zich richten op de retrograde techniek met een unilaterale electrode.
Gezien er meer evidence is voor de toepassing van sacrale neuromodulatie voor de indicaties urge urine-incontinentie en fecale incontinentie in vergelijking met de indicatie chronische bekkenpijn (EAU-guideline Urinary Incontinence, 2019), valt sacrale neuromodulatie te overwegen bij patiënten die naast chronisch bekkenpijn, ook therapieresistente urge urine-incontinentie en/of fecale incontinentie hebben.
Vanwege de aanzienlijk kosten en het invasieve karakter van sacrale neuromodulatie, zal deze therapie pas geïndiceerd zijn bij patiënten bij wie conservatievere therapieën ineffectief zijn.
Perineale zenuwstimulatie
Er zijn geen studies gevonden over perineale zenuwstimulatie voor de behandeling van chronisch bekkenpijn. Er zijn op dit moment meerdere implantaten voor PTNS ontwikkeld die direct de tibiale zenuw kunnen stimuleren. Deze worden nu in meerdere klinische trials onderzocht. Het advies is daarom nu om andere vormen van neuromodulatie zoals perineale stimulatie en PTNS via een implantaat alleen in onderzoeksverband toe te passen.
PTNS
Op basis van de literatuur lijkt het erop dat bij patiënten met chronische bekkenpijn en/of chronische prostatitis de cruciale uitkomstmaat ‘pijnintensiteit’ een klinisch relevante afname laat zien, 3 maanden na behandeling met P-PTNS vergeleken met placebo of usual care. Op een VAS-schaal van 0 tot 10 werd gemiddeld een afname van 3,93 punten gerapporteerd (95%BI -6,22 tot −1,65). De bewijskracht voor deze uitkomstmaat is gegradeerd als ‘laag’, vanwege mogelijk risk of bias in de studies en imprecies (klein aantal deelnemers). Voor de belangrijke uitkomstmaat kwaliteit van leven werd ook een klinisch relevante verbetering gerapporteerd 3 maanden na behandeling met P-PTNS, een afname van 4,60 punten (95%BI -5,27 tot -3,93) op het QoL domein van de NIH-CPSI schaal. Het is onbekend wat het effect van P-PTNS bij patiënten met chronische bekkenpijn is voor de uitkomstmaten patiënttevredenheid en complicaties. Vanwege laag risico op bijwerkingen en geen interactie met farmacologische therapie wordt het toch als een zinnige stap gezien om P-PTNS in een vroege fase aan te bieden.
In tegenstelling tot percutane PTNS (via naald), kan transcutane PTNS zelfstandig in de thuissituatie worden toegepast. Er zijn echter geen geschikte studies gevonden die de effectiviteit van T-PTNS evalueren voor de behandeling van chronische bekkenpijn. Gezien het vergelijkbaar werkingsmechanisme tussen P-PTNS en T-PTNS en de lage invasiviteit, complicatierisico’s en praktische voordelen van T-PTNS, kan overwogen worden om op basis van expert opinion T-PTNS ter ondersteuning aan te bieden bij een P-PTNS-behandeling voor chronische bekkenpijn.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Goede informatie is noodzakelijk om patiënten in te lichten over behandeling met neuromodulatie, de bijbehorende effectiviteit en complicatierisico’s, aangezien er verschillen zijn in werking, invasiviteit en effectiviteit. Hierbij dient de patiënt te worden geïnformeerd over: 1) de verschillende typen neuromodulatie 2) de bijbehorende apparatuur die nodig is voor de therapie 3) bij sacrale neuromodulatie: operatieve procedure, complicatierisico’s, de verwachte batterijduur en verwachte re-operaties. 4) bij P-PTNS: het aantal klinische bezoeken dat nodig zal zijn voor de therapie 5) Bij T-PTNS: dat de werking minder effectief is wanneer het niet in combinatie met P-PTNS wordt uitgevoerd.
Kosten (middelenbeslag)
Er is geen data bekend over kosteneffectiviteit voor verschillende neuromodulatie toepassingen voor de indicatie chronische bekkenpijn. Neuromodulatie is geen curatieve therapie en de kosten hangen sterk af van de techniek die wordt toegepast. P-PTNS is een relatief goedkope behandeling, echter dient deze wel in een klinische setting te worden toegepast door een getrainde zorgverlener. Sacrale zenuwstimulatie is een eenmalige kostbare ingreep. Echter dient ook technisch falen en batterijduur en derhalve re-operatie worden meegenomen in de kosten. Voor andere indicaties zoals urge urine-incontinentie wordt deels vanwege invasiviteit en deels vanwege hoge kosten sacrale neuromodulatie pas als last resort behandeling toegepast bij patiënten die refractair zijn voor andere therapieën. Deze argumenten zijn ook van toepassing voor sacrale neuromodulatie voor de behandeling van chronische bekkenpijn.
Aanvaardbaarheid voor de overige relevante stakeholders
Het is onbekend of er bezwaren zijn van relevante stakeholders.
Haalbaarheid en implementatie
Voor sacrale neuromodulatie voor chronische bekkenpijn geldt dat deze therapie alleen in een expertisecentrum met een multidisciplinaire setting dient te worden uitgevoerd met daarin een getrainde specialist die ervaren is in de operatieve ingreep en de afstelling van de apparatuur. Indien deze kennis niet voorradig is, wordt geadviseerd om te verwijzen naar een expertisecentrum. PTNS kan laagdrempelig klinisch worden aangeboden na adequate scholing.
Rationale/ balans tussen de argumenten voor en tegen de interventie
Aanbeveling-1
Ondanks de lage bewijskracht, is er gezien de lage invasiviteit en beperkte complicatie risico’s van P-PTNS een rationale om deze behandeling laagdrempelig toe te passen bij chronische bekkenpijn. Voor T-PTNS is er geen goed bewijs voor toepassing bij chronische bekkenpijn, echter gezien het vergelijkbare werkingsmechanisme met P-PTNS en de voordelen van toepassing van deze modaliteit in de klinische praktijk, kan het toch overwogen worden T-PTNS toe te passen als aanvulling op P-PTNS. Verder zijn er geen studies gevonden over perineale zenuwstimulatie voor de behandeling van chronisch bekkenpijn. Er zijn meerdere implantaten voor PTNS ontwikkeld die direct de tibiale zenuw kunnen stimuleren en de effectiviteit hiervan wordt nu in meerdere klinische trials onderzocht. Het advies is daarom nu om andere vormen van neuromodulatie zoals perineale stimulatie en PTNS via een implantaat alleen in onderzoeksverband toe te passen.
Aanbeveling-2
Sacrale neuromodulatie wordt bij patiënten met chronische bekkenpijn alleen aanbevolen indien alle andere therapieën ineffectief zijn gebleken. Gezien er meer evidence is voor de toepassing van sacrale neuromodulatie voor de indicaties urge urine-incontinentie en fecale incontinentie in vergelijking met de indicatie chronische bekkenpijn, valt sacrale neuromodulatie te overwegen bij patiënten die naast chronisch bekkenpijn, ook therapieresistente urge urine-incontinentie en/of fecale incontinentie hebben.
Gezien de beperkt in Nederland aanwezige klinische expertise voor het toepassen van sacrale neuromodulatie is het sterk aanbevolen om dit in expertisecentra te laten uitvoeren.
Huidige bewijs laat zien dat veruit de meeste studies, conform de Nederlandse praktijk, bij sacrale neuromodulatie gebruik maken van de retrograde techniek met een unilaterale electrode. Daarbij wordt er standaard een evaluatiefase geïncludeerd met een test electrode voordat het definitieve implantaat wordt ingebracht.
Onderbouwing
Neuromodulatie wordt steeds frequenter klinisch toegepast voor zowel pijnbehandeling als voor dysfunctie van de lage urinewegen. In het bekkengebied wordt het ook op verschillende locaties toegepast en via verschillende modaliteiten en technieken die meer of minder invasief zijn. Chronische bekkenpijn gaat vaak gepaard met dysfunctie van de lage urinewegen en de darm. Aangezien neuromodulatie voor zowel pijn als blaas en darm dysfunctie wordt toegepast, hebben we voor deze richtlijn de uitgangsvraag beperkt tot het beoordelen van de effectiviteit van neuromodulatie behandelingen op het chronische bekkenpijn.
Sacrale neuromodulatie
|
Zeer laag GRADE |
Het is onduidelijk wat het effect van sacrale neuromodulatie op pijnintensiteit bij patiënten met chronische bekkenpijn is.
Bronnen: (Aboseif, 2002; Chai, 2000; Chung, 2007; Comiter, 2003; Falletto, 2009; Ghazwani, 2011; Guardo, 2016; Lavano, 2006; Maher, 2001; Marellucci, 2012; Marinkovi, 2011; Siegel, 2001; Sokal, 2015; Whitmore, 2003) |
|
- GRADE |
Het is onduidelijk wat het effect van sacrale neuromodulatie op complicaties bij patiënten met chronische bekkenpijn is doordat de resultaten alleen beschrijvend werden gepresenteerd.
Bronnen: (Aboseif, 2002; Chai, 2000; Chung, 2007; Comiter, 2003; Falletto, 2009; Ghazwani, 2011; Guardo, 2016; Lavano, 2006; Marellucci, 2012; Marinkovi, 2011; Siegel, 2001; Sokal, 2015; Whitmore, 2003) |
|
- GRADE |
Het is onbekend wat het effect van sacrale neuromodulatie bij patiënten met chronische bekkenpijn is op de uitkomstmaten patiënttevredenheid en kwaliteit van leven. Er werden geen studies gevonden waarin deze uitkomstmaten werden vergeleken tussen patiënten die sacrale neuromodulatie ondergingen en een placebo/geen behandeling ondergingen. |
PTNS
|
Laag GRADE |
Het lijkt erop dat bij patiënten met chronische bekkenpijn en/of chronische prostatitis de pijnintensiteit vermindert 3 maanden na behandeling met P-PTNS vergeleken met placebo of usual care.
Bronnen: (Gokyildiz, 2012; Kabay, 2009) |
|
Laag GRADE |
Het lijkt erop dat bij patiënten met chronische bekkenpijn en/of chronische prostatitis de kwaliteit van leven verbetert 3 maanden na behandeling met P-PTNS vergeleken met placebo of usual care.
Bronnen: (Gokyildiz, 2012; Kabay, 2009) |
|
- GRADE |
Het is onbekend wat het effect van P-PTNS of T-PTNS bij patiënten met chronische bekkenpijn is op de uitkomstmaten patiënttevredenheid en complicaties. Er werden geen studies gevonden waarin deze uitkomstmaten werden vergeleken tussen patiënten die PTNS en een placebo/geen behandeling ondergingen. |
Beschrijving studies
Mahran (2019) voerde een systematische review en meta-analyse uit naar de effecten van sacrale neuromodulatie bij patiënten met chronische bekkenpijn. De search werd verricht in september 2018 in de databases MEDLINE, Embase, Cochrane, Web of Science en Scopus. Er werden in totaal 14 studies geïncludeerd, waarvan 10 prospectieve observationele studies (Aboseif, 2002; Chai, 2000; Comiter, 2003; Falletto, 2009; Guardo, 2016; Lavano, 2006; Maher, 2001; Siegel, 2001; Sokal, 2015; Whitmore, 2003) en 4 retrospectieve observationele studies (Chung, 2007; Ghazwani, 2011; Marellucci, 2012; Marinkovi, 2011). Alle studies beschreven de resultaten voor en na afloop van sacrale neuromodulatie, het was onduidelijk of de metingen op hetzelfde moment plaatsvonden.
In totaal werden 403 patiënten beschreven die percutane zenuwevaluatie (PNE) en/of sacrale neuromodulatie stadium 1 ondergingen. De meeste patiënten waren vrouwen, slechts 7% was man (n=29). Ongeveer de helft van de patiënten kregen uiteindelijk een permanent implantaat (n=221, 54,8%). Interstitiële cystitis en blaaspijnsyndroom waren de meest gerapporteerde diagnoses (n=170, 42,2%). De duur van de pijnklachten werd niet gerapporteerd door Maher (2019). Mahran (2019) includeerde twee verschillende technieken van sacrale neuromodulatie: twaalf studies beschreven een retrograde benadering, waarbij uni- of bilateraal een electrode door het sacrale foramen werd geïntroduceerd (Aboseif, 2002; Chai, 2000; Chung, 2007; Comiter, 2003; Falletto, 2009; Ghazwani, 2011; Lavano, 2006; Maher, 2001; Marellucci, 2012; Marinkovi, 2011; Siegel, 2001; Whitmore, 2003); twee studies beschreven een antegrade (caudale) benadering, waarbij een electrode in het wervelkanaal werd geïntroduceerd via de sacrale hiatus en ter hoogte van sacrale wortels S4, S3 en S2 werd geïmplanteerd (Guardo, 2016; Sokal, 2015). De meeste studies beschreven unilaterale zenuwstimulatie (Aboseif, 2002; Chung, 2007; Comiter, 2003; Falletto, 2009; Ghazwani, 2011; Guardo, 2016; Maher, 2001; Marellucci, 2012; Marinkovi, 2011; Siegel, 2001; Sokal, 2015; Whitmore, 2003); Lavano (2006) implanteerde naast n=3 unilaterale ook n=2 bilaterale implantaten; Chai (2000) rapporteerde deze gegevens niet. Het falen van permanente implantatie (SNM stadium II) varieerde tussen de studies, de meeste studies rapporteerde geen falen (Aboseif, 2002; Lavano, 2006; Maher, 2001; Ghazwani, 2011; Guardo, 2016; Marinkovi, 2011; Marellucci, 2012), twee studies < 10% van de gevallen (Comiter, 2003: n=1 (6%); Falletto, 2009: n= 1 (9%)), bij drie studies betrof dit 25-30% van de gevallen (Siegel, 2001: n=3 (30%); Chung, 2007: n=3 (25%); Sokal, 2015: n=3 (30%)). In twee studies werd dit niet gerapporteerd (Whitmore, 2003)of was het niet van toepassing (Chai, 2000). De gemiddelde duur van follow-up varieerde sterk tussen de studies van enkele maanden tot meerdere jaren, duur van follow-up in Chai (2000) en Maher (2001) was onbekend. Het exacte meetmoment post-baselin werd niet door Mahran (2019).
Tirlapur (2013) voerde een systematische review uit naar de effecten van zenuwstimulatie bij patiënten met chronische bekkenpijn en/of blaaspijnsyndroom. De search werd verricht in juli 2012 in de databases MEDLINE, Embase, Cochrane, Web of knowledge, LILACS en SIGLE. Er werden louter RCT’s en prospectieve quasi-gerandomiseerde gecontroleerde studies geïncludeerd. In totaal werden 3 RCT’s geïncludeerd waarin patiënten door middel van PTNS werden behandeld (Gokyildiz, 2012; Kabay, 2009; O’Reilly, 2004). De eerste twee studies bestudeerde P-PTNS, de studie van O’Reilly (2004) wordt in deze analyse buiten beschouwing gelaten omdat hier door middel van laser werd behandeld. Er zijn geen studies met transcutane techniek (T-PTNS) beschreven in deze studie. Fulltext publicaties van Gokyildiz (2012) en Kabay (2009) werden opgevraagd om data voor de literatuuranalyse te kunnen aanvullen.
Gokyildiz (2012) beschreef een wekelijkse behandeling door middel van P-PTNS van 30 minuten per keer, 12 weken lang bij 24 vrouwen met chronische bekkenpijn. De gemiddelde duur van de pijn was in de interventiegroep (n=13) 3,9 (SD 2.2) jaar en in de controlegroep (n=13) 3,95 (SD 2,3) jaar. In beide groepen viel één vrouw uit tijdens het onderzoek (reden onbekend). Gokyildiz (2012) gebruikte een 34 gauge naald, 3 tot 4 centimeter boven de mediale malleolus van de posterieure tibiale zenuw. De naald was bevestigd aan een 9-V-stimulator met 0,5 tot 10 mA aanpasbare stroom. De controlegroep bestond uit een groep die gewone zorg kreeg, dit was niet nader gedefinieerd. Metingen vonden plaats op baseline en na afloop van 12 weken behandeling.
Kabay (2009) beschreef een wekelijkse behandeling door middel van P-PTNS van 30 minuten per keer, 12 weken lang bij 89 mannen met chronische bekkenpijn en/of chronische bacteriële prostatitis. De gemiddelde duur van de pijn was in de interventiegroep (n=45) 4,5 (SD 6,1) jaar en in de controlegroep (n=44) 3,8 (SD 5,7) jaar. Kabay (2009) gebruikte een 26-gauge naald, 5 centimeter boven de mediale malleolus (aan de posterior zijde van de tibia). Een neutrale elektrode werd geplaatst bij de voetboog. De elektrode en naald waren verbonden met een stimulator met een pulsfrequentie van 20Hz. Controlegroep kreeg een sham device, een apparaat dat niet werkzaam was. Metingen vonden plaats op baseline en na afloop van 12 weken behandeling.
Resultaten
De resultaten uit de 14 studies over sacrale neuromodulatie uit één systematische review en meta-analyse (Maher, 2019) en de 2 studies over PTNS uit de systematische review van Tirlapur (2013) worden hieronder beschreven per uitkomstmaat. Hierbij wordt onderscheid gemaakt in het type zenuwstimulatie (sacrale zenuwstimulatie en PTNS).
1. Pijnintensiteit
1.1. Sacrale zenuwstimulatie
De uitkomstmaat pijn werd beschreven in 14 studies over sacrale zenuwstimulatie (Aboseif, 2002; Chai, 2000; Chung, 2007; Comiter, 2003; Falletto, 2009; Ghazwani, 2011; Guardo, 2016; Lavano, 2006; Maher, 2001; Marellucci, 2012; Marinkovi, 2011; Siegel, 2001; Sokal, 2015; Whitmore, 2003). Pijn werd gemeten op basis van een VAS-schaal 0 tot 10 (geen tot maximale pijn). Pijnintensiteit was gedefinieerd als het verschil in pijnscore na sacrale neuromodulatie ten opzichte van baseline (voor sacrale neuromodulatie).
Pre- en post-baseline pijnscores waren beschikbaar in 210 patiënten (52%). Figuur 1 presenteert het gepoolde, gewogen gemiddelde verschil in de pre- en postbaseline pijnscore. De overall verbetering in pijnscore na sacrale neuromodulatie was -4,36 (95%BI -5,24 tot -3,48); p<0.001). Subgroepanalyses op basis van de benadering (retrograde versus antegrade (caudale) sacrale neuromodulatie) lieten een effect in dezelfde richting zien: in beide groepen werd een afname van de pijnscore waargenomen.
Figuur 1 Forest plot uitkomstmaat ‘pijnintensiteit’ op basis van het gewogen gemiddelde verschil tussen de pijnscore na en vóór sacrale neuromodulatie
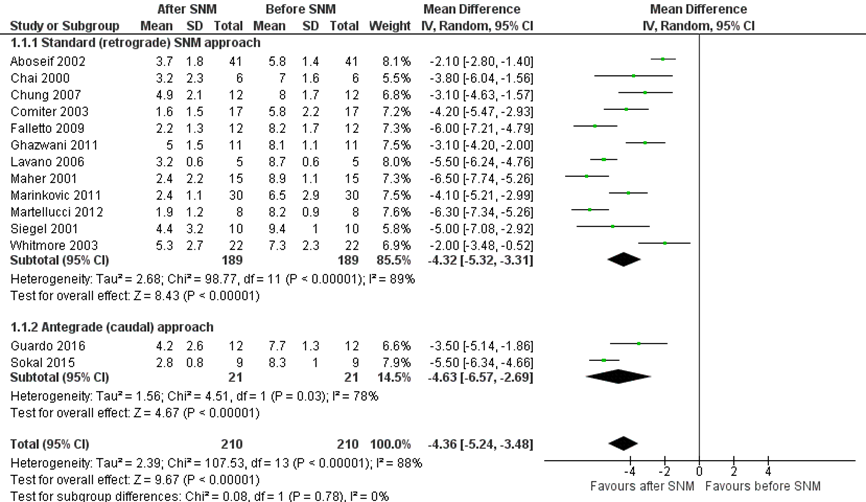
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
1.2. PTNS
De uitkomstmaat pijn werd beschreven in 2 studies over P-PTNS (Gokyildiz, 2012; Kabay, 2009). Pijn werd gemeten op basis van een VAS-schaal 0 tot 10 (geen tot maximale pijn). Pijnintensiteit was gedefinieerd als het verschil in post-treatment pijnscore na PTNS tussen de interventie- en controlegroep.
Post-baseline pijnscores waren beschikbaar in 113 patiënten. Figuur 2 presenteert het gepoolde, gewogen gemiddelde verschil in de postbaseline pijnscore. De overall verbetering in pijnscore na PTNS was -3,93 (95%BI -6,22 tot -1,65); p<0.001).
Figuur 2 Forest plot uitkomstmaat ‘pijnintensiteit’ op basis van het gewogen gemiddelde verschil tussen de interventie en controlegroep bij de behandeling door middel van PTNS
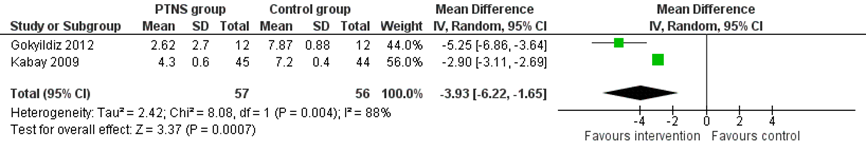
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
2. Patiënttevredenheid
2.1. Sacrale neuromodulatie
Er werden geen studies geïncludeerd waarin patiënttevredenheid werd bestudeerd als uitkomstmaat bij sacrale neuromodulatie.
2.2. PTNS
Er werden geen studies geïncludeerd waarin patiënttevredenheid werd bestudeerd als uitkomstmaat bij PTNS.
3. Complicaties
3.1. Sacrale neuromodulatie
Complicaties of bijwerkingen van de interventie werden gerapporteerd in 13 studies over sacrale neuromodulatie (Aboseif, 2002; Chai, 2000; Chung, 2007; Comiter, 2003; Falletto, 2009; Ghazwani, 2011; Guardo, 2016; Lavano, 2006; Marellucci, 2012; Marinkovi, 2011; Siegel, 2001; Sokal, 2015; Whitmore, 2003), dit werd niet beschreven in de studie van Maher (2001). De resultaten worden alleen beschrijvend gepresenteerd.
Complicaties werden in 30% van de patiënten gerapporteerd (n=67/221). Tabel 1 presenteert het voorkomen van complicaties. Daarnaast werd was er sprake van het falen van het implantaat of het verwijderen van het implantaat bij 11 patiënten (5%), waarbij n=5 wegens infecties geassocieerd met implantatie, n=3 wegens falen van het implantaat zelf en n=2 wegens gevoelloosheid van de ledematen. Daarnaast ondergingen n=23 (10%) patiënten aanpassing of vervanging van het implantaat.
3.2. PTNS
De uitkomstmaat complicaties werd beschreven in 1 studie over PTNS (Gokyildiz, 2012). Gokyildiz (2012). De resultaten worden hieronder beschrijvend gepresenteerd.
Gokyildiz (2012) beschreef dat in de interventiegroep (n=12) 1 hematoom werd gerapporteerd en 2 patiënten rapporteerde kortstondige pijn bij de prikplek van de naald.
Tabel 1 Complicaties voor sacrale zenuwstimulatie gerapporteerd door studies in systematische review van Maher (2019)
|
Complicatie |
n (%) |
|
Wondinfecties |
9 (4%) |
|
Electrode migratie/ disfunctioneren migration/ malfunction (n=1 gedeeltelijk opgelost door herprogrammeren implantaat, n=5 veroorzaakt door trauma). |
17 (8%) |
|
Pijn op plek van implantatie |
12 (5,4%) |
|
Implanteerbare puls generator erosie, zonder infectie |
3 (1,1%) |
|
Spontaan opgeloste seroma |
6 (2,7%) |
|
Verandering in locatie van pijn |
5 (2%) |
|
Urineweginfecties |
2 (<1%) |
|
Gevoel van elektrische shock |
1 (<1%) |
|
Corpus alienum gevoel |
1 (<1%) |
|
Gevoelloze ledematen van het onderlichaam |
2 (<1%) |
4. Kwaliteit van leven
4.1. Sacrale neuromodulatie
Er werden geen studies over sacrale neuromodulatie geïncludeerd waarin kwaliteit van leven werd bestudeerd als uitkomstmaat.
4.2. PTNS
De uitkomstmaat kwaliteit van leven werd beschreven in 2 studies over PTNS (Gokyildiz, 2012; Kabay, 2009). Gokyildiz (2012) bestudeerde kwaliteit van leven via de SF-36 questionnaire. Kabay (2009) rapporteerde de kwaliteit van leven score op basis van de National Institutes of Health Chronic Prostatitis Symptom Index (NIH-CPSI) QoL domein (0 tot 2, waarbij een hogere score meer klachten betekent). De resultaten worden hieronder beschrijvend gepresenteerd.
Gokyildiz (2012) rapporteerde een verbetering op bijna alle SF-36 subschalen, echter waren de patiëntaantallen te klein om een verschil te berekenen en niet gecorrigeerd voor baseline verschillen die op sommige subschalen er leken te zijn.
Kabay (2009) beschreef een gemiddeld verschil in NIH-CPSI QoL domein score van -4,60 (95%BI -5,27 tot -3,93) tussen de interventiegroep en controlegroep. Dit betekent een verbetering in kwaliteit van leven voor patiënten die door middel van PTNS zijn behandeld vergeleken met een placebo.
Bewijskracht van de literatuur
Sacrale neuromodulatie
Observationeel vergelijkend onderzoek begint op een laag niveau van bewijskracht. Het 95% betrouwbaarheidsinterval omvat de waarde van een klinisch relevant effect (gemiddeld verschil: -4,36 (95%BI -5,24 tot -3,48)). De bewijskracht voor de uitkomstmaat pijnintensiteit na sacrale zenuwstimulatie is met één niveau verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias: het was onduidelijk wat de duur van de pijnklachten was en wanneer de metingen plaatsvonden). Hierdoor wordt de bewijskracht gegradeerd als ‘zeer laag’.
De bewijskracht voor de uitkomstmaat patiënttevredenheid na sacrale neuromodulatie kon niet worden gegradeerd door middel van GRADE doordat er geen studies over sacrale neuromodulatie werden geïncludeerd waarin deze uitkomstmaat werd bestudeerd.
De bewijskracht voor de uitkomstmaat complicaties na sacrale neuromodulatie kon niet worden gegradeerd door middel van GRADE doordat er alleen beschrijvende informatie gerapporteerd werd.
PTNS
RCT’s beginnen op een hoog niveau van bewijskracht. Het 95% betrouwbaarheidsinterval omvat de waarde van een klinisch relevant effect (gemiddeld verschil: −3,93 (95%BI -6,22 tot -1,65)). De bewijskracht voor de uitkomstmaat pijnintensiteit na PTNS is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en imprecisie (beperkt aantal deelnemers). Hierdoor wordt de bewijskracht gegradeerd als ‘laag’.
RCT’s beginnen op een hoog niveau van bewijskracht. Het 95% betrouwbaarheidsinterval voor het gemiddeld verschil in de NIH-CPSI QoL domein score omvat de waarde van een klinisch relevant effect (gemiddeld verschil: -4,60 (95%BI -5,27 tot -3,93). De bewijskracht voor de uitkomstmaat kwaliteit van leven na PTNS is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias) en imprecisie (beperkt aantal deelnemers). Hierdoor wordt de bewijskracht gegradeerd als ‘laag’.
De bewijskracht voor de uitkomstmaat complicaties na PTNS kon niet worden gegradeerd door middel van GRADE doordat er alleen beschrijvende informatie gerapporteerd werd.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Wat is de effectiviteit (en veiligheid) van behandeling door middel van neuromodulatie vergeleken met geen behandeling of placebo voor de behandeling van patiënten met chronische bekkenpijn?
P: patiënten met chronische bekkenpijn (duur van de pijn ≥ 6 maanden);
I: behandeling door middel van neuromodulatie;
C: geen behandeling of behandeling door middel van placebo;
O: pijnintensiteit, patiënttevredenheid, complicaties, kwaliteit van leven.
Relevante uitkomstmaten
De werkgroep achtte pijnintensiteit een voor de besluitvorming cruciale uitkomstmaat; en patiënttevredenheid, complicaties, kwaliteit van leven voor de besluitvorming belangrijke uitkomstmaten.
Onder behandeling door middel van neuromodulatie wordt in deze module verstaan sacrale neuromodulatie, percutane posterior tibiale zenuwstimulatie (P-PTNS) en perineale zenuwstimulatie. Voor behandeling met transcutane elektrische neurostimulatie (T-PTNS of TENS) door de bekkenfysiotherapeut wordt verwezen naar (zie de module Bekkenfysiotherapie). Studies over T-PTNS worden wel in deze module beschreven.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
De werkgroep hield de GRADE-default grenzen (25% voor dichotome uitkomstmaten en 0,5 SD voor continue uitkomstmaten) aan als een klinisch (patiënt) relevant verschil (Schüneman, 2013).
Zoeken en selecteren (Methode)
In de databases Medline (via OVID) en Embase (Elsevier) is op 10 juli 2019 met relevante zoektermen gezocht naar systematische reviews, randomized controlled trials (RCT’s) en observationele cohortstudies waarin was gekeken naar de effectiviteit en veiligheid van behandeling van chronische bekkenpijn door middel van neuromodulatie. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 362 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: 1) studie betrof patiënten met chronische bekkenpijn (duur pijn ≥ 6 maanden); 2) studie betrof een vergelijkend onderzoek waarin neuromodulatie werd vergeleken met geen of placebo behandeling; 3) minimaal één van de volgende uitkomstmaten werd gerapporteerd: pijnintensiteit, patiënttevredenheid, complicaties, kwaliteit van leven. Op basis van titel en abstract werden in eerste instantie 45 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 42 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en 3 studies geselecteerd. Dit betroffen 3 systematische reviews en/of meta-analyses (Mahran, 2019; Tirlapur, 2013; Tutolo, 2018). Vergeleken met de andere twee reviews, beschrijft het review van Tutolo (2018) minder gedetailleerd de resultaten van de studies. Er werd daarom voor gekozen om de data uit de reviews van Mahran (2019) en Tirlapur (2013) te extraheren en Tutolo (2018) te gebruiken om te controleren of alle relevante studies waren geïdentificeerd. In totaal werden er dus 2 studies definitief opgenomen in de literatuuranalyse.
Resultaten
Twee systematische reviews werden geïncludeerd in de literatuuranalyse, één over sacrale neuromodulatie (Mahran, 2019) en één over P-PTNS (Tirlapur, 2013).
- F.C. Burkhard, J.L.H.R. Bosch, F. Cruz, G.E. Lemack, A.K. Nambiar, N. Thiruchelvam, A. Tubaro Guidelines Associates: D. Ambühl, D.A. Bedretdinova, F. Farag, R. Lombardo, M.P. Schneider European Association of Urology (EAU) guideline Urinary Incontinence (2019). https://uroweb.org/guideline/urinary-incontinence/#1
- Gokyildiz S, Kizilkaya Beji N, Yalcin O, Istek A. Effects of percutaneous tibial nerve stimulation therapy on chronic pelvic pain. Gynecol Obstet Invest. 2012;73(2):99-105.
- Kabay S, Kabay SC, Yucel M, Ozden H. Efficiency of posterior tibial nerve stimulation in category IIIB chronic prostatitis/chronic pelvic pain: a Sham-Controlled Comparative Study. Urol Int. 2009;83(1):33-8.
- Mahran A, Baaklini G, Hassani D, Abolella HA, Safwat AS, Neudecker M, Hijaz AK, Mahajan ST, Siegel SW, El-Nashar SA. Sacral neuromodulation treating chronic pelvic pain: a meta-analysis and systematic review of the literature. Int Urogynecol J. 2019 Jul;30(7):1023-1035.
- Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
- Tirlapur SA, Vlismas A, Ball E, Khan KS. Nerve stimulation for chronic pelvic pain and bladder pain syndrome: a systematic review. Acta Obstet Gynecol Scand. 2013 Aug;92(8):881-7.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Research question:
Abbreviations: NR not reported, NA not applicable, SNM sacral neuromodulation, IC interstitial cystitis, PNE percutaneous nerve evaluations, BPS bladder pain syndrome, CPP chronic pelvic pain, IPGs implantable pulse generators.
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea, 2007; BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher, 2009; PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Maher, 2019 |
Yes |
Yes |
Yes, see flow chart. |
Yes |
Analyses are within person comparisons, data were therefore only corrected for baseline score. |
Yes, results were provided |
Unclear, heterogeneity is high, subgroup analysis were performed which did not reduce heterogeneity |
Unclear, not reported. |
No |
|
Tirlapur, 2013 |
Yes |
Yes |
Yes, see flow chart |
Yes |
NA (RCTs) |
Yes, results were provided |
Meta-analysis was not performed due to significant heterogeneity |
Unclear, not reported |
No |
- Research question (PICO) and inclusion criteria should be appropriate and predefined..
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table et cetera).
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (for example Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (for example funnel plot, other available tests) and/or statistical tests (for example Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Aboseif, 2002 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Atikin, 2011 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Biemans, 2013 |
systematische review waarin 1 studie zit geïncludeerd die ook door Tirlapur 2013 is meegenomen. |
|
Buffenoir, 2015 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Chaichian 2017 |
voldoet niet aan PICO (geen aparte analyse voor neuromodulatie). |
|
Cohen, 2012 |
voldoet niet aan PICO (interventie met shock wave therapy) |
|
Comiter, 2003 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
De Andres, 2016 |
narrative review |
|
Duddin, 2007 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Dudding, 2013 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Elhilali, 2005 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Everaert, 2001 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Everaert, 2001 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Faletto, 2009 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Fall, 2010 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Gajewski, 2011 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Gaziev, 2013 |
voldoet niet aan PICO (kijkt niet naar onze uitkomstmaten; methodologische kwaliteit matig) |
|
Ghazwani, 2011 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Govaert, 2010 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Hunter, 2018 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Istek, 2014 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Kashif, 2019 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Kessler, 2007 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Levine, 2016 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Magistro, 2016 (2) |
review zonder RoB beoordeling |
|
Maher, 2001 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Marcelissen, 2011 |
narrative review |
|
Martellucci, 2012 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Martellucci, 2012 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Mira, 2018 |
voldoet niet aan PICO (TENS i.p.v. PTNS) |
|
Morgalla, 2017 |
Voldoet niet aan PICO (liespijn) |
|
Peters, 2003 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Peters, 2004 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Peters, 2010 |
voldoet niet aan PICO (geen uitkomstmaten van onze interesse bestudeerd) |
|
Peters, 2013 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Sokal, 2015 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Srivastava 2012 |
review van Mahran 2019 is meer recent over SNM |
|
Tahseen, 2018 |
narrative review |
|
Usmani 2018 |
Voldoet niet aan PICO (behandeling versus. behandeling) |
|
Vancaillie, 2018 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Wang 2017 |
review van Mahran 2019 is meer recent over SNM |
|
Zabihi, 2008 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
|
Aboseif, 2002 |
gepubliceerd binnen search periode van reviews Mahran 2019, Tutolo 2018 en Tirlapur 2013 |
Beoordelingsdatum en geldigheid
Publicatiedatum : 04-08-2021
Beoordeeld op geldigheid : 31-08-2021
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2025 bepaalt het bestuur van de Nederlandse Vereniging voor Urologie (NVU) of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NVU is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module[1] |
Regiehouder(s)[2] |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn[3] |
Frequentie van beoordeling op actualiteit[4] |
Wie houdt er toezicht op actualiteit[5] |
Relevante factoren voor wijzigingen in aanbeveling[6] |
|
Neuromodulatie |
NVU |
2020 |
2025 |
Elke 5 jaar |
NVU |
Nieuwe literatuur |
[1] Naam van de module
[2] Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders)
[3] Maximaal na vijf jaar
[4] (half)Jaarlijks, eens in twee jaar, eens in vijf jaar
[5] regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft
[6] Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
De richtlijn is ontwikkeld in samenwerking met:
- Nederlandse Vereniging van Maag-Darm-Leverartsen
- Nederlandse Vereniging voor Anesthesiologie
- Nederlandse Vereniging voor Obstetrie en Gynaecologie
- Nederlandse Vereniging voor Bekkenfysiotherapie
- Nederlandse Vereniging voor Heelkunde
- Nederlandse Wetenschappelijke Vereniging voor Seksuologie
- Nederlands Instituut van Psychologen
- Landelijke Vereniging Medische Psychologie
- Koninklijke Nederlandse Organisatie van Verloskundigen
- Nederlands Huisartsen Genootschap
- Verpleegkundigen & Verzorgenden Nederland
- Stichting Bekkenbodem4All
- Interstitiële Cystitis Patiëntenvereniging
Doel en doelgroep
Doel
Het ontwikkelen van een evidence based richtlijn over chronische bekkenpijn volgens richtlijnen 2.0.
Doelgroep
Patiënten met chronische bekkenpijn. Alle zorgverleners die betrokken zijn bij de zorg voor patiënten met chronische bekkenpijn.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in december 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met chronische bekkenpijn.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Dr. E.J. (Bert) Messelink, uroloog-seksuoloog NVVS, NVU (voorzitter).
- Dr. A. (Afina) Glas, uroloog, NVU
- Dr. J. (Jacqueline) Groeneweg, gynaecoloog, NVOG
- Dr. D. (Dick) Janssen, arts-onderzoeker urologie, NVU
- Drs. K. (Karlijn) Schweitzer, gynaecoloog, NVOG
- Drs. V. (Wafa) Rezvani, anesthesioloog-pijnbestrijder, NVA
- Dr. R.J.F. (Richelle) Felt-Bersma, maag-darm-leverarts, NVMDL
- Dr. R.J. (Remmie) Hammers, huisarts, kaderarts urogynaecologie, NHG
- Drs. G. (Gidia) Jacobs, gezondheidszorgpsycholoog, pedagoog, seksuoloog NVVS, NVVS, NIP, LVMP.
- Drs. C. (Corine) Adamse, geregistreerd bekkenfysiotherapeut, NVFB
- (Ana) dos Santos, MSc, geregistreerd bekkenfysiotherapeut, NVFB
- H.J. (Henk-Jan) Mulder, verpleegkundig specialist urologie, V&VN
- C.W.L. (Tine) van den Bos, MSPT, belangenbehartiger patiënten namens Stichting Bekkenbodem4All, voorzitter Stichting Bekkenbodem4All, geregistreerd bekkenfysiotherapeut, Stichting Bekkenbodem4All
Klankbordgroep
- Prof. dr. E.J.C. (Esther) Consten, chirurg, NVvH
- B.B.M. (Brigitte) Tebbe, verloskundige, KNOV
- H.M.T. Andriesse-Walhain, patiëntvertegenwoordiger, ICP
Met ondersteuning van
- Dr. I. (Irina) Mostovaya, senior-adviseur en teamleider, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. A (Anne) Bijlsma-Rutte, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J. (Janneke) Hoogervorst-Schilp, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J. (José) Maas, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Y.J. (Yvonne) Labeur, MSc, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- M. (Monique) Wessels, MSc, literatuurspecialist, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
* Messelink |
Uroloog - Seksuoloog NVVS Medisch Centrum Leeuwarden |
Verzorgen onderwijs: SOMT Amersfoort. Opleiding Bekkenfysiotherapeuten, 1,5 dag/jaar. Betaald RINO Utrecht. Opleiding seksuologie, 0,5 dag/jaar. Betaald Opleiding Stomaverpleegkundige Groningen. 2 uur/jaar. Betaald
Europese cursus: Chronic Pelvic Pain, European Association of Urology. Halve dag 1x/jaar. Betaald |
* Voorzitter Pelvic Floor Network, een non-profit organisatie die zich inzet voor het structureren van landelijk onderwijs en het opzetten van een zorg-netwerk betreffende chronische bekkenpijn. * Lid medische adviesraad van de patiëntenverenigingen: BB4All, PVVN. * Vice-chairman EAU Guideline panel Chronic Pelvic Pain. |
Geen |
|
Groeneweg |
gynaecoloog IJsselland ziekenhuis 0,625 fte expert gynaecologie Zorginstituut Nederland 0,2 fte |
bestuurslid werkgroep Bekkenbodem NVOG onbetaald
|
vanuit werkgroep Bekkenbodem ben ik de contactpersoon voor de patiëntenorganisatie BB4all |
Geen |
|
Schaapveld |
Voorzitter Bekkenbodem4all |
Lid cliëntenraad Residentie Molenwijck |
Niet van toepassing |
Geen |
|
Glas |
Uroloog, vrij gevestigd. ZaansMC |
Geen |
Ben betrokken bij opzet onderzoek naar blaasspoelingen bij preventie van urineweginfecties. Dit onderzoek wordt mogelijk gefinancierd (aanvraag unrestricted grant) door bedrijf dat ook blaasspoelingen verkoopt voor indicatie chronische bekkenpijn
Ik hoop dat eerder ontwikkelde standpunt BPS/ic waar ik actief betrokken bij ben geweest een plaats krijgt, qua inhoud, inde de nieuw te ontwikkelen richtlijn bekkenpijn.
Het meehelpen bij ontwikkelen van een dergelijke richtlijn, zal voor mij persoonlijke een intellectueel gewin opleveren. In die zin dat ik er ook iets hoop van te leren.
Het mee ontwikkelen van de richtlijn zal denk ik een gunstige invloed hebben op mijn rol als specialist met affiniteit voor de patiëntengroep en het ziektebeeld. |
Geen actie; NB-blaasspoelingen worden niet besproken in de richtlijn |
|
Adamse |
Bekkenfysiotherapeut en klinisch Epidemiologie Docent EBP en begeleider onderzoekstagiaires Antonius ziekenhuis Sneek |
Bekkenfysiotherapeut: Alle klinische en poliklinische zorg rondom bekken patiënten deelname aan multidisciplinair overleg met gynaecologie, urologie en chirurgie. Deelname aan seksuologisch spreekuur en MDO. samenwerking met MDL-artsen en gespecialiseerde verpleegkundigen. klinisch epidemioloog/ docent EBP/ begeleider onderzoekstherapie lesgeven en ondersteunen van onderzoeksvragen op het gebied van EBP voor zowel fysiotherapeuten als verpleegkundigen. Evidence based practise docent (gastdocent) NHL/stenden hogeschool Leeuwarden |
nee, behalve dat richtlijn mogelijk meer werk/aandacht oplevert voor bekkenfysiotherapie in het ziekenhuis
mogelijk meer aandacht voor bekkenfysiotherapie en de NVFB. Review gedaan naar chronische pijn en effectiviteit van e-health toepassingen en gepubliceerd (2017) |
Geen |
|
Santos |
Geregistreerd bekkenfysiotherapeut MSc bij PelviCentrum- Centrum voor Bekkenfysiotherapie Leiden Eigenaresse van PelviCentrum - Centrum l voor Bekkenfysiotherapie Leiden |
Lid van NVFB Wetenschappelijke Commissie. Vergoeding van de reiskosten en bijwonen van vergaderingen.
In samenwerking met verloskundigenpraktijk en Mamacafe Leiden geef ik workshops aan zwangeren en vrouwen postpartum. Deze werkzaamheden zijn onbetaald. |
Deelname aan het ontwikkelen van de richtlijn kan ervoor zorgen dat collega vaker gaan verwijzen naar mijn praktijk vanwege meer bekendheid. |
Geen |
|
Hammers |
Waarnemend huisarts Kaderhuisarts Urogyneacologie |
Lid medische adviesraad stichting Bekkenbodem4All. Onkostenvergoeding |
Ik ben de afgevaardigde vanuit de UgynHag (kaderhuisartsenartsen urogynaecologie) |
Geen |
|
Jacobs |
Gezondheidszorgpsycholoog, seksuoloog NVVS in vrijgevestigde praktijk: centrum voor psychische, relationele en seksuele gezondheid te Voorschoten. Gezondheidspsycholoog seksuoloog NVVS in deeltijd bij proctosklinkiek te Bilthoven Hoofdopleider post-big-opleiding seksuologie rino te Utrecht |
Lid van Tuchtrechtcommissietucht van de NVVS onbezoldigd. Adviseur van het bestuur van PFN onbezoldigd. Lesgeven bij diverse organisaties bv. SOMT, ZEL. (bezoldigd) |
Adviseur van het bestuur van PFN ik neem deel uit interesse voor het complexe vakgebied met als doelgroep patiëntenzorg te verbeteren. |
Geen |
|
Mulder |
Verpleegkundig specialist urologie Martini Ziekenhuis Groningen |
Lid van Adviesraad Hollister BV. |
|
Geen actie; NB (thuiszorg) hulpmiddelen worden niet besproken in de richtlijn |
|
Rezvani |
Anesthesioloog/pijnbestrijder, werkzaam in het St. Antonius ziekenhuis Nieuwegein/Utrecht in een maatschap |
Lid ledenraad NVA-sectie pijnbestrijding, onbetaald. |
|
Geen |
|
Janssen |
Arts bij Gynos vrouwenkliniek Den Haag, blaaspijn/bps-spreekuur (onderdeel van Andros klinieken)
Arts-onderzoeker, afdeling urologie, Radboudumc
|
Coördinator en docent Technische Geneeskunde Faculteit, Universiteit Twente.
- Medische adviesraad (MAR) patiëntenvereniging ICP |
Te vermelden voor openheid van zaken:
- Werkzaam in 2 medische centra (Radboudumc & Gynos vrouwenkliniek) die patiëntenzorg op dit deelgebied verlenen.
Meegeschreven aan NVU-standpunt BPS 2017 (onbetaald).
- In verleden tegen betaling eenmalig advies gegeven voor Bene Arzneimittel GMBH farmaceuticals, producent van Elmiron, medicijn voor blaaspijn syndroom.
- In 2017 tegen eenmalige vergoeding gesproken op European Association of Urology congres op gesponsorde sessie door IBSA farmaceuticals (producent GAG-therapie voor blaaspijnsyndroom)
- Eigenaar eenmanszaak dr. Dr. D.A.W. Janssen, Urology Science & Healthcare (KvK nr. 77488881). Geen bezit van patenten, geen (incl. toekomstige beloften voor) financieel gewin door participatie aan deze richtlijn commissie.
Deelname aan deze commissie zou impact kunnen hebben op mijn aanzien als klinisch professional binnen mijn vakgebied. De mate van impact kan ik niet overzien |
Geen actie; NB-blaasspoelingen worden niet besproken in de richtlijn |
|
Schweitzer |
Gynaecoloog UMC Utrecht, Bergman Clinics Hilversum vrouwenzorg |
Trainer KNOV-hechtcursus. Trainer hechtcursus Leiderdorp NVOG voor beiden ontvang ik een vergoeding |
Bij Bergman Clinics zien we patiënten met chronische pijn in buik en bekken mogelijk dat er een toename van pte gaat komen
Deelname aan deze het ontwikkelen van de richtlijn kan ervoor zorgen dat collega vaker gaan verwijzen vanwege meer bekendheid |
Geen |
|
Felt - Bersma |
MDL-arts Amsterdam UMC, locatie VUMC |
MDL-arts Proctoskliniek te Bilthoven MDL-arts MCV de Veluwe, Apeldoorn |
ROAD-studie, een studie met een medicament versus placebo ter preventie van recidief diverticulitis |
Geen |
|
Van den Bos |
1. Bekkenfysiotherapeut MSPT (Master of Specialised Physical Therapy) bij AdFysio te De Lier 0.6 fte 2. Bekkenfysiotherapeut MSPT LUMC, afd. urologie 0.2 fte onbezoldigd 3. Voorzitter BB4All (Bekkenbodem4All), vrijwilliger |
Lid MAR (Medische Advies Raad) Lichen Sclerosis Nederland: reiskostenvergoeding Lid MAR Lichen Planus Vereniging Nederland: reiskostenvergoeding Penningmeester zorggroep FEL (Fysiotherapie 1e Lijn) Zuid-Holland West: onkostenvergoeding |
Geen |
Geen |
|
Klankbordgroep |
|
|
|
|
|
Tebbe (klankbordgroep) |
Wetenschappelijk adviseur KNOV (ZZP) verloskundige |
Communicatie + tekstschrijver (ZZP) |
Geen |
Geen |
|
Andriesse (klankbordgroep) |
Voorzitter van de Interstitiële cystitis vereniging, ICP |
Ik ben vrijwilliger niet betaald |
Geen |
Geen |
|
Consten (klankbordgroep) |
chirurg, meander medisch centrum MMC en hoogleraar universitair medisch centrum Groningen UMCG in de chirurgie aandachtsgebied robotica en computer geassisteerde chirurgie |
voorzitter werkgroep coloproctologie opleideer heelkunde mmc |
arts in tertiair bekkenbodem centrum van het meander medisch centrum te Amersfoort |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door middel van een afgevaardigde patiëntenvereniging in de werkgroep en in de klankbordgroep.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden in de bijlagen. Er zijn geen indicatoren ontwikkeld bij deze richtlijn.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door verschillende partijen/vertegenwoordigers van relevante stakeholders via een Invitational conference. Een verslag hiervan is opgenomen in de bijlagen.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Per uitgangsvraag werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen in de bijlagen.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR - voor systematische reviews; Cochrane - voor gerandomiseerd gecontroleerd onderzoek; Newcastle-Ottowa - voor observationeel onderzoek; QUADAS II - voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk* |
|
|
Laag |
|
|
Zeer laag |
|
*in 2017 heeft het Dutch GRADE Network bepaald dat de voorkeursformulering voor de op een na hoogste gradering ‘redelijk’ is in plaats van ‘matig’
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van Zorg.
Indicatorontwikkeling
Er werden geen indicatoren ontwikkeld bij deze richtlijn.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de bijlage Kennislacunes beschreven.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers, M. C., Kho, M. E., Browman, G. P., Burgers, J. S., Cluzeau, F., Feder, G.,... & Littlejohns, P. (2010). AGREE II: advancing guideline development, reporting and evaluation in health care. Canadian Medical Association Journal, 182(18), E839-E842.
Kennisinstituut van de Federatie Medisch Specialisten. Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Utrecht, 2015.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwaliteit. https://richtlijnendatabase.nl/werkwijze/richtlijnen_3_0.html.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann, H. J., Oxman, A. D., Brozek, J., Glasziou, P., Jaeschke, R., Vist, G. E.,... & Bossuyt, P. (2008). Rating Quality of Evidence and Strength of Recommendations: GRADE: Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ: British Medical Journal, 336(7653), 1106.
Wessels, M., Hielkema, L., & van der Weijden, T. (2016). How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. Journal of the Medical Library Association: JMLA, 104(4), 320.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID) |
1 exp pelvic pain/ or dysmenorrhea/ or pelvic girdle pain/ or piriformis muscle syndrome/ or Pelvic Floor Disorders/ or pudendal Neuralgia/ (9520) 2 ((pelvic or pelvis or pudendal) adj3 (pain* or syndrome or neuralgia or myalgia)).ti,ab,kf. (10495) 3 ((prostatitis or prostate or "levator ani" or constipation or puborectalis) adj3 (neuralgia* or pain* or sydrome* or spasm*)).ti,ab,kf. (2735) 4 (prostatalgia or prostatodynia or orchialgia or dyssynergia or Coccydynia or coccygodynia or proctalgia or vestibulodynia or dysmenorrhea* or dysmenorrhoea or vulvodynia or Dyspareunia or "Pyriformis syndrome").ti,ab,kf. (11501) 5 ((bladder or testicular or urethral or scrotal or groin or epididymal or "post vasectom*" or genital or coccyx or sacrococcygeal or anal or anorectal or vestibular or vulvar or "Fissure in Ano" or perineal) adj3 pain*).ti,ab,kf. (8637) 6 (((interstitial or recurrent) adj2 (cystitides or cystitis)) or ((suprapubic or abdominal or endometriosis) adj3 (neuralgia* or pain*))).ti,ab,kf. (61311) 7 ((proctitis or defecation or hemorrhoid* or haemorrhoid* or diverticulitis or PID or "pelvic inflammatory disease*") adj3 (neuralgia* or pain*)).ti,ab,kf. (994) 8 ((voiding or prostat* or menstrual or menstruation or childbirth or vaginal or vulvar or urethral or "cauda equina") adj3 (neuralgia* or pain*)).ti,ab,kf. (5109) 9 ("pelvic floor" adj3 (overactivity or dysfunction or "resting tone" or hypertonicity)).ti,ab,kf. (1029) 10 or/1-9 (91594) 11 exp Chronic Disease/ or (chronic or chronically or persistent or constant* or continuing or sustained or lasting or refractor*).ti,ab,kf. or Chronic Pain/ (2186326) 12 10 and 11 (20209) 13 (Groin/ or exp Testicular Diseases/ or Scrotum/ or Pelvic Floor/) and Chronic Pain/ (140) 14 12 or 13 (20233) 15 limit 14 to english language (17570) 16 limit 15 to yr="1999 -Current" (14458) 17 electric stimulation therapy/ or spinal cord stimulation/ or transcutaneous electric nerve stimulation/ (24270) 18 (((spinal or sacral or nerve) adj3 stimulation) or neuromodulation or PTNS or SNS or TENS).ti,ab,kf. (51254) 19 17 or 18 (68390) 20 16 and 19 (355) 26 ((meta-analysis/ or meta-analysis as topic/ or (metaanaly* or metanaly* or meta-analy* or meta synthes* or metasynthes* or (pooled adj3 analysis)).ti,ab,kf. or ((systematic* or scoping or evidence based) adj3 (review* or overview*)).ti,ab,kf. or ((evidence or research) adj3 synthesis).ti,kf. or systematic review.pt. or (prisma or (("structured literature" or comprehensive or "quantitative literature" or evidence-based) adj2 (search or review)) or "systematic search" or ((systemic or systematized) adj3 review) or "systematic research synthesis" or (review* adj3 independent*))).ti,ab,kf. or (((quantitative or rapid or short or critical* or structured or comparative or comparitive or evidence or comprehensive) adj3 (review* or overview*)).ti. and search.ab.) or "Review Literature as Topic"/ or cochrane.jw. or (cochrane or embase or medline or cinahl or cinhal or cancerlit).ab. or (("selection criteria" or "data extraction").ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (336898) 27 20 and 26 (27) 28 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1875926) 29 20 and 28 (85) 30 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ (Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies) (3219702) 31 20 and 30 (126) 32 29 not 27 (72) 33 27 or 29 (99) > 98 uniek 34 31 not 33 (80) |
362 |
|
Embase (Elsevier) |
(((('pelvic pain'/exp/mj OR 'dysmenorrhea'/exp/mj OR 'pelvic girdle pain'/exp/mj OR 'piriformis syndrome'/exp/mj OR 'pelvic floor disorder'/exp/mj OR 'pudendal neuralgia'/exp/mj OR (((pelvic OR pelvis OR pudendal) NEAR/3 (pain* OR syndrome OR neuralgia OR myalgia)):ti,ab) OR (((prostatitis OR prostate OR 'levator ani' OR constipation OR puborectalis) NEAR/3 (neuralgia* OR pain* OR sydrome* OR spasm*)):ti,ab) OR prostatalgia:ti,ab OR prostatodynia:ti,ab OR orchialgia:ti,ab OR dyssynergia:ti,ab OR coccydynia:ti,ab OR coccygodynia:ti,ab OR proctalgia:ti,ab OR vestibulodynia:ti,ab OR dysmenorrhea*:ti,ab OR dysmenorrhoea:ti,ab OR vulvodynia:ti,ab OR dyspareunia:ti,ab OR 'pyriformis syndrome*':ti,ab OR (((bladder OR testicular OR urethral OR scrotal OR groin OR epididymal OR 'post vasectom*' OR genital OR coccyx OR sacrococcygeal OR anal OR anorectal OR vestibular OR vulvar OR 'fissure in ano' OR perineal) NEAR/3 pain*):ti,ab) OR (((interstitial OR recurrent) NEAR/2 (cystitides OR cystitis)):ti,ab) OR (((suprapubic OR abdominal OR endometriosis) NEAR/3 (neuralgia* OR pain*)):ti,ab) OR (((voiding OR prostat* OR menstrual OR menstruation OR childbirth OR vaginal OR vulvar OR urethral OR 'cauda equina') NEAR/3 (neuralgia* OR pain*)):ti,ab) OR (('pelvic floor' NEAR/3 (overactivity OR dysfunction OR 'resting tone' OR hypertonicity)):ti,ab) OR (((proctitis OR defecation OR hemorrhoid* OR haemorrhoid* OR diverticulitis OR pid OR 'pelvic inflammatory disease*') NEAR/3 (neuralgia* OR pain*)):ti,ab))
AND ('chronic disease'/exp OR 'chronic pain'/exp OR 'chronic inflammatory pain'/exp OR chronic:ti,ab OR chronically:ti,ab OR persistent:ti,ab OR constant*:ti,ab OR continuing:ti,ab OR sustained:ti,ab OR lasting:ti,ab OR refractor*:ti,ab) OR (('inguinal region'/exp/mj OR 'testis disease'/exp/mj OR 'pelvis floor'/exp/mj) AND 'chronic pain'/exp) OR 'chronic scrotal pain'/exp)
AND (english)/lim AND ((embase)/lim OR (pubmed-not-medline)/lim) NOT 'conference abstract':it)
AND (('neuromodulation'/exp OR 'electrotherapy'/de OR 'nerve stimulation'/exp) OR ((((spinal OR sacral OR nerve) NEAR/3 stimulation):ti,ab) OR neuromodulation:ti,ab OR ptns:ti,ab OR sns:ti,ab OR tens:ti,ab)))
AND ((('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp))
OR (('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it)) (203) > 152 uniek
('major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)) > 32 uniek |
|
