Medicamenteuze behandeling van symptomen in de palliatieve fase (exclusief stervensfase)
Uitgangsvraag
Welke medicamenteuze behandeling van symptomen wordt aanbevolen bij mensen met de ziekte van Parkinson tijdens de palliatieve fase?
Aanbeveling
De behandeling in de palliatieve fase is hoofdzakelijk gericht op het bieden van comfort.
Screen in de palliatieve fase op tekenen van intolerantie voor behandeling met levodopa (en andere dopaminerge medicatie), met name op orthostatische hypotensie, sufheid, verwardheid, misselijkheid en psychotische verschijnselen.
Verlaag de levodopa enkel als ‘last resort’, omdat deze verlaging in vrijwel alle situaties gepaard gaat met meer motorische en niet-motore klachten en dus met minder comfort.
Overweeg bij (toename van) neuropsychiatrische klachten te screenen op cognitieve stoornissen en deze te behandelen (zie hiervoor ook de module Behandeling van cognitieve stoornissen bij de ziekte van Parkinson).
Indien er sprake is van orthostatische hypotensie, behandel dan volgens de module Behandeling van autonome disfunctie bij de ziekte van Parkinson, en in aanvulling hierop, met niet-medicamenteuze behandelingen, zoals leefstijladviezen.
Screen op en behandel minder specifieke klachten die kunnen passen bij de palliatieve fase van de ziekte van Parkinson, zoals dyspnoe, pijn, misselijkheid en braken.
Overwegingen
Onderstaande overwegingen hebben betrekking op de zorg in de palliatieve fase voordat de stervensfase intreedt. Zie voor behandeling in de stervensfase de module Medicamenteuze behandeling in de stervensfase.
Algemeen
Als er sprake is van moeilijk behandelbare symptomen en/of complexe problematiek kunnen de richtlijnen palliatieve zorg worden geraadpleegd (https://palliaweb.nl/). Deze richtlijnen hebben betrekking op lichamelijke en psychische symptomen, zorg in de stervensfase, zorg op psychosociaal en spiritueel gebied (mantelzorg, spirituele zorg, rouw) en beslissingen rond het levenseinde (wilsverklaring, euthanasie). Patiënteninformatie voor mensen met de ziekte van Parkinson is te vinden via de Parkinson Vereniging (www.parkinson-vereniging.nl).
Dopaminerge medicatie in de late fase ziekte van Parkinson
Medicamenteuze behandeling van patiënten met de ziekte van Parkinson heeft als doel om klachten en symptomen te verminderen. In de palliatieve fase richt medicamenteuze behandeling zich hoofdzakelijk het bieden van comfort. Als medicamenteuze behandeling heeft vooral levodopa een belangrijke rol. Meerdere kleine studies, met uitsluitend deelnemers in de late-fase, hebben het verschil in symptomen getoond tussen de ON-fase (met levodopa) en de OFF-fase (zonder levodopa). In de ON-fase waren er minder motorische en niet-motorische klachten [Fabbri, 2016; Fabbri, 2017; Rosqvist, 2018; Rosqvist, 2018]. Ook zijn er richting/rond de palliatieve fase duidelijk minder motorische problemen als de diepe hersenstimulator (DBS) aanstaat versus als deze uitstaat [Fabbri, 2020]. De bijwerkingen van levodopa en DBS waren in deze studies bescheiden en wogen niet op tegen het voordeel van de behandeling. In de overtuiging van de werkgroep kunnen er in individuele gevallen situaties ontstaan waarbij de hinderlijke bijwerkingen zodanig ernstig zijn dat reduceren of staken van de medicatie moet worden overwogen. Hieraan kan ook gedacht worden bij een tijdelijke ernstige complicatie, zoals bijvoorbeeld een ernstig delier. In dit geval kan de medicatie in een later stadium herstart of opgehoogd worden. Belangrijk is het om te realiseren dat dit een ‘last resort’ is en in vrijwel alle gevallen gepaard gaat met (forse) verslechtering van de motorische en niet-motorische klachten. Het heeft daarom de voorkeur om hinderlijke bijwerkingen van levodopa te behandelen zonder de dosering te verlagen.
Pas indien mogelijk (niet‐noodzakelijke) medicatie aan voor zover patiënt medicatie gebruikt, in deze volgorde: staak of verlaag anticholinergica, amantadine, MAO‐B remmer, dopamine-agonist, COMT-remmer, levodopa.
Bij patiënten met de ziekte van Parkinson veelgebruikte medicatie met matig tot sterk anti-cholinerge effecten zijn: parasympaticolytica (atropine, scopolamine(butyl), trihexifenidyl en glycopyrronium) spasmolytica (zoals oxybutinine, solifenacine, tolterodine), tricyclische anti-depressiva (clomipramine, amitriptyline en nortriptyline). Voor beoordeling van overige medicatie verdient het de aanbeveling een bij ParkinsonNet aangesloten apotheker te consulteren.
Belangrijk is het om te realiseren dat dit een ‘last resort’ is en in vrijwel alle gevallen gepaard gaat met (forse) verslechtering van de motorische en niet-motorische klachten. Het heeft daarom de voorkeur om hinderlijke bijwerkingen van levodopa te behandelen zonder de dosering te verlagen.
Motorische problemen (vallen, rigiditeit, bradykinesie of (hinderlijke) tremoren)
In de late-fase van de ziekte van Parkinson kan er sprake zijn van ernstige spierrigiditeit, bradykinesie of hinderlijke tremoren. Daarnaast valt 1 op de 5 dagelijks ten gevolge van de ziekte van Parkinson [Schrag, 2016]. De indicaties voor medicatie en uitgangspunten voor behandeling verschillen in de late-fase niet met de vroege fase (zie hiervoor de module Medicamenteuze behandeling van motorische klachten bij de ziekte van Parkinson). Er zijn wel duidelijke accentverschillen. Zo gaat de late-fase vaker gepaard met uitingen van levodopa-intolerantie, zoals orthostatische hypotensie, sufheid, verwardheid, misselijkheid en psychotische klachten [Schrag, 2016]. Dit betekent dat een goede screening op deze klachten vooraf moet gaan aan het starten of aanpassen van behandelingen. Tevens zal de behandeling van de motorische klachten onderdeel moeten zijn van een breder behandelplan waarin deze klachten worden aangepakt. Het gevolg is dat behandeling in de late-fase multimodaal is en vaak wordt vormgegeven door meerdere behandelaren, binnen een multidisciplinaire benadering. Bovendien komen er in de late-fase generieke comorbiditeiten voor, die de motoriek ook belemmeren (bijvoorbeeld cardiovasculaire, pulmonale en reumatische aandoeningen). In dat geval is de inzet van een generalist van toegevoegde waarde. Denk hierbij aan de huisarts, specialist ouderengeneeskunde, klinisch geriater, apotheker aangesloten bij ParkinsonNet of een revalidatiearts.
Neuropsychiatrische klachten
In de palliatieve fase komen neuropsychiatrische klachten zoals een depressie, angstklachten, psychose, delier of gedragsproblemen voor. In de late-fase ziekte van Parkinson heeft nagenoeg iedereen ten minste één psychiatrische klacht [Hommel, 2020; Reid, 2011]. De indicaties voor behandeling en uitgangspunten verschillen niet van de vroege fase, maar er zijn wel accentverschillen:
In de late-fase speelt cognitieve achteruitgang vaak een rol. Na 20 ziektejaren heeft ongeveer 80% parkinson-dementie [Hely, 2008]. Soms zijn neuropsychiatrische symptomen zoals apathie en psychose de eerste uitingen van cognitieve achteruitgang. Het herkennen en vervolgens behandelen van cognitieve achteruitgang is onderdeel van de behandeling van neuropsychiatrische klachten (zie hiervoor de module Behandeling van cognitieve stoornissen bij de ziekte van Parkinson). Bij mensen met gevorderde dementie komen neuropsychiatrische klachten vaak voor. Goede dementiezorg is persoonsgericht en gericht op het bieden van de basale psychologische behoeften, zoals troost, steun en aandacht en waardering. Ondanks deze persoonsgerichte benadering kunnen neuropsychiatrische klachten gepaard gaan met een grote lijdensdruk of gevaarlijk gedrag. Een gerichte multidisciplinaire behandeling door gespecialiseerde deskundigen is dan nodig (zie hiervoor Probleemgedrag bij mensen met dementie, Verenso, 2018).
Ziekteprogressie en verlies van zelfstandigheid kan agitatie, depressie en angstklachten in de hand werken. Zorgdiagnostiek en casemanagement is onderdeel van een goede behandeling van neuropsychiatrische klachten. Psychotische verschijnselen zoals hallucinaties en wanen komen voor in het beloop van de ziekte, maar ook als bijwerking van medicatie [Smit, 2016]. Deze psychotische symptomen kunnen lijken op een delier. Zorgvuldige observatie en zowel psychiatrische (differentieer tussen angst, onrust en een delier) als somatische diagnostiek (bijvoorbeeld uitsluiten urineretentie, constipatie, pijn) is hierbij van belang. Ook bij een delier is een medicatiereview nodig [Delier in de palliatieve fase; IKNL, 2022].
De neuropsychiatrische symptomen zorgen vaak voor een zwaardere belasting voor de mantelzorger dan de motorische verschijnselen. Wees hier bewust van. Veelvoorkomende emotionele labiliteit bij de patiënt maakt de omgang hiermee voor de mantelzorger zwaarder.
Autonome dysfunctie
Bij ongeveer de helft van de mensen in de late-fase ziekte van Parkinson is er sprake van orthostatische hypotensie. Deze klacht gaat bovendien vaak gepaard met postprandiale hypotensie en nachtelijke hypertensie, waardoor een verhoogde diurese en meer nycturie. De behandelindicaties en uitgangspunten verschillen in de niet-terminale palliatieve fase niet van de vroegere fasen. Wel zijn er accentverschillen:
Zo zal er in de late-fase vaker sprake zijn van nadelige effecten van autonome dysfunctie, zoals het vallen/verslikken door sufheid en een hoge mantelzorgbelasting door nachtelijke nycturie. Tijdige inzet van behandelstrategieën is dus nodig. Het inzetten van een medicatiebeoordeling teneinde orthostatische hypotensie uitlokkende medicatie zo mogelijk te staken of therapeutisch te substitueren verdient de aanbeveling. Niet-medicamenteuze strategieën zijn:
- het hoofdeinde te verhogen van het bed met minimaal 5 graden (= minstens 15 cm);
- overdag therapeutische elastische kousen te gebruiken tot het niveau van de heupen (met name wanneer er sprake is van oedeem effectief), minimaal drukklasse 3, bij voorkeur in combinatie met een elastische buikband;
- voorzichtig, in etappes, opstaan vanuit liggende en zittende positie;
- vermijden van manoeuvres die intrathoracale druk verhogen, bijvoorbeeld persen, hoesten;
- vermijden van langdurige bedrust;
- aanleren van contra-manoeuvres bij symptomatische orthostase (lower body muscle tensing): aanspannen van been-, bil-, en buikspieren;
- minimaliseer post-prandiale hypotensie door:
- spreid maaltijden naar meer eetmomenten over de dag;
- beperk koolhydraten.
- drink sterke koffie voor de maaltijd (bijv. dubbele espresso);
- vermijd alcohol;
- inname van 2,0 tot 2,5 l vocht per dag;
- inname van minstens 10 g keukenzout per dag (streef >170 mmol Natrium in 24-uurs urine);
- bij klachten in warm weer: inname van 0,5 liter koud water in 5 tot 15 minuten (bij voorkeur voor de maaltijd indien er sprake is van post-prandiale hypotensie).
Aanvullend kan betrokkenheid van zorgprofessionals (bijvoorbeeld thuiszorg) tijdens risicomomenten, zoals de maaltijd of douchen, risico’s op complicaties verminderen. Indien lisdiuretica in gebruik zijn, is het zinvol deze (deels) rond 15:00 a 16:00 uur in te nemen teneinde de nycturie te reduceren.
Zo nodig kunnen medicamenteuze interventies worden ingezet zoals beschreven in de module Behandeling van autonome disfunctie bij de ziekte van Parkinson [NVN&VRA, 2020].
Minder specifiek maar tevens voorkomende problemen
Dyspnoe
In de palliatieve fase kunnen patiënten met de ziekte van Parkinson toenemende moeilijkheden ervaren met hoesten door rigiditeit, dystonie en/of extreme flexie van het bovenlichaam (camptocormia). Ook kan door spierzwakte een restrictieve longfunctie ontstaan [Group TIPCiPsD, 2016]. Geleidelijk kan sprake zijn van toenemende secretie (afscheiding) in de bovenste luchtwegen. Dit kan leiden tot benauwdheid.
Het is van belang om uitleg te geven over de veranderingen in ademhaling, de (mogelijke) behandeling en beperkingen. Niet-medicamenteuze behandeling zoals zoals het gebruik van een ventilator of respiratoire training door de fysiotherapeut kan overwogen worden. Ook betrokkenheid van de logopedist ter behandeling van onderliggende slikproblemen is een mogelijkheid. Aanbevolen wordt halfzittend te verplegen met kussens in de nek en onder de armen, in een goed geventileerde ruimte, mits dit het comfort van de patiënt verbetert. Bij reutelen wordt zijligging geadviseerd mits patiënt hiervan een positief effect ervaart. Er zijn geen specifieke studies gedaan naar de behandeling van dyspnoe bij mensen met de ziekte van Parkinson. Morfine kan gebruikt worden bij Parkinson. Gebruik van zuurstof is alleen geïndiceerd bij hypoxie [Richtlijn Dyspneu; IKNL, 2015].
Pijn
Pijn komt gedurende de ziekte van Parkinson veelvuldig voor. Het verdient de aanbeveling onderzoek te doen naar de aard van de pijn. Bij aanwijzingen voor pijn als gevolg van onderdosering wordt uiteraard aanpassing en evaluatie van levodopa geadviseerd. Voor de behandeling van pijn wordt verwezen naar de module Behandeling van pijnklachten bij Parkinson.
Misselijkheid en braken
Het is belangrijk om onderliggende oorzaken van misselijkheid en braken in kaart te brengen (bijvoorbeeld dehydratie, obstipatie, maagontledigingstoornis, bijwerking van medicatie, of infectie) en waar mogelijk deze te behandelen. Aanvullende zorg kan bestaan uit het goed ventileren van de ruimte, vermijden van sterke etensluchten en het verplegen van een patiënt halfzittend na inname van vocht/voeding [Richtlijn Misselijkheid en braken; IKNL, 2014]. Misselijkheid is eigenlijk altijd een bijwerking van dopaminerge medicatie als de behandeling net gestart is. Het gaat weliswaar na enkele dagen of weken over, maar het maakt toepassing in de gevorderde fase minder geschikt. Cinnarizine en vele anti-emetica zoals metoclopramide hebben een antagonistische werking op de dopaminereceptoren. Hierdoor is de kans groot dat symptomen/klachten bij de ziekte van Parkinson verergeren (Farmacotherapeutisch kompas). Domperidon geeft deze antagonistische werking in veel mindere mate, en heeft een positief effect op de maagontlediging. Bij het voorschrijven van domperidon dient rekening te worden gehouden met QTc verlenging, maar ook bij QTc verlenging kan in deze fase gefundeerd besloten worden het (kleine) risico op eventuele ritmeproblematiek te accepteren. Een alternatief kan een anti emeticum zijn zoals ondansetron, dit middel gaat door blokkering van 5HT3-receptoren in het maag-darmkanaal en het centrale en perifere zenuwstelsel de braakreflex tegen. Ondansetron heeft geen antagonistische werking op de dopaminereceptoren en is in verschillende toedieningsvormen beschikbaar, echter in de praktijk blijkt het weinig effectief en ook bij ondansetron moet rekening gehouden worden met het QTc verlenging en (verergering van) obstipatie. In uitzonderlijke gevallen kan er plaats zijn voor behandeling met psychofarmaca. In een recente casestudie werd een positief effect gerapporteerd van quetiapine als behandeling tegen misselijkheid bij een persoon met de ziekte van Parkinson [Hindmarsh, 2022].
Onderbouwing
Achtergrond
De palliatieve fase is breder dan enkel de stervensfase. Om pragmatische redenen bakent het kwaliteitskader de palliatieve fase af tot de laatste fase van het leven, waarbij de patiënt naar verwachting van de zorgverlener in de komende twaalf maanden komt te overlijden. In de praktijk is dit bij mensen met de ziekte van Parkinson lastig in te schatten en duurt de palliatieve fase daarom vaak langer dan een jaar.
De stervensfase omvat de laatste dagen (tot zeven dagen) van het leven. Er is sprake van een onomkeerbaar 'fysiologisch' proces dat in gang is gezet, waardoor het overlijden aanstaande is.
Deze module geeft aanbevelingen voor medicamenteuze symptoombehandelingen in de palliatieve fase, maar nog voordat de stervensfase begint. Voor de behandeling in de stervensfase wordt verwezen naar module Medicamenteuze behandeling in de stervensfase.
De medicamenteuze behandeling die in deze module wordt beschreven, is gericht op een aantal symptomen bij de ziekte van Parkinson die in de palliatieve fase geregeld voorkomen. Het gaat hierbij om: vallen, spierrigiditeit, ernstige (hinderlijke) tremor, dyspnoe, misselijkheid en pijn. Er zal in deze module worden teruggevallen op de spaarzame literatuur die inmiddels voor deze doelgroep voorhanden is.
Zoeken en selecteren
Om de uitgangsvraag van deze module te beantwoorden is een systematische analyse van de literatuur gedaan. De onderzoeksvraag die hiervoor is onderzocht is PICO-gestructureerd en luidt:
Wat zijn de (on)gunstige effecten van interventies ter behandeling van klachten in de palliatieve fase bij mensen met de ziekte van Parkinson?
|
P |
Mensen met de ziekte van Parkinson in de palliatieve fase |
|
I |
Alle mogelijke interventies |
|
C |
Geen behandeling/placebo of andere interventie |
|
O |
Effectiviteit/afname van klachten, bijwerkingen, kwaliteit van leven |
Op 27 juni 2022 is in de databases Medline en Embase gezocht naar wetenschappelijke literatuur. De zoekactie leverde na ontdubbelen 306 resultaten op. De volledige zoekactie is beschreven in bijlage 5.
In- en exclusiecriteria
De literatuur is systematisch geselecteerd op basis van vooraf gestelde criteria. Deze criteria luiden als volgt:
- SR’s, RCT’s en observationele studies;
- Mensen met de ziekte van Parkinson in de palliatieve fase;
- De experimentele interventie bestaat uit alle mogelijke interventies ter behandeling van symptomen;
- De controle interventie bestaat uit geen behandeling, placebo of een andere interventie;
Literatuur is geëxcludeerd wanneer het zorg in de stervensfase betrof of zorg voorafgaand aan de palliatieve fase.
De selectiecriteria zijn toegepast op de referenties verkregen uit de zoekactie. In eerste instantie zijn de titel en abstract van de referenties beoordeeld. Hiervan werden zeven referenties geïncludeerd voor de beoordeling op basis van het volledige artikel. Na de beoordeling van de volledige tekst kon geen studie definitief geïncludeerd worden. In de exclusietabel in bijlage 5 is de reden voor exclusie van de referenties toegelicht.
Referenties
- Cooper SD, Ismail HA, Frank C. Case report: successful use of rectally administered levodopa-carbidopa. Can Fam Physician 2001;47:112-113.
- Donnelly RF. Stability of levodopa/ carbidopa rectal suspensions. Hospital Pharmacy 2016;51:915-921.
- Fabbri M, Coelho M, Abreu D, Guedes LC, Rosa MM, Costa N, Antonini A, Ferreira JJ. Do patients with late-stage Parkinson's disease still respond to levodopa? Parkinsonism Relat Disord. 2016 May;26:10-6.
- Fabbri M, Coelho M, Guedes LC, Chendo I, Sousa C, Rosa MM, Abreu D, Costa N, Godinho C, Antonini A, Ferreira JJ. Response of non-motor symptoms to levodopa in late-stage Parkinson's disease: Results of a levodopa challenge test. Parkinsonism Relat Disord. 2017 Jun;39:37-43.
- Fabbri M, Coelho M, Abreu D, Guedes LC, Rosa MM, Godinho C, Cardoso R, Guimaraes I, Antonini A, Zibetti M, Lopiano L, Ferreira JJ. Dysphagia predicts poor outcome in late-stage Parkinson's disease. Parkinsonism Relat Disord. 2019 Jul;64:73-81.
- Fabbri M, Zibetti M, Rizzone MG, Giannini G, Borellini L, Stefani A, Bove F, Bruno A, Calandra-Buonaura G, Modugno N, Piano C, Peppe A, Ardolino G, Romagnolo A, Artusi CA, Berchialla P, Montanaro E, Cortelli P, Luigi R, Eleopra R, Minafra B, Pacchetti C, Tufo T, Cogiamanian F, Lopiano L. Should We Consider Deep Brain Stimulation Discontinuation in Late-Stage Parkinson's Disease? Mov Disord. 2020 Aug;35(8):1379-1387.
- Hely MA, Reid WG, Adena MA, Halliday GM, Morris JG. The Sydney multicenter study of Parkinson's disease: the inevitability of dementia at 20 years. Mov Disord. 2008 Apr 30;23(6):837-44. doi: 10.1002/mds.21956.
- Hindmarsh J, Lee M. The Use of Quetiapine for the Management of Nausea and Vomiting in Idiopathic Parkinson's Disease. J Palliat Care. 2022 Jan;37(1):15-17.
- Hoehn MM, Yahr MD. Parkinsonism: onset, progression and mortality. Neurology. 1967 May;17(5):427-42.
- Hommel ALAJ, Meinders MJ, Lorenzl S, Dodel R, Coelho M, Ferreira JJ, Laurens B, Spampinato U, Meissner W, Rosqvist K, Timpka J, Odin P, Wittenberg M, Bloem PhD BR, Koopmans RT, Schrag A; Care of Late?Stage Parkinsonism Consortium. The Prevalence and Determinants of Neuropsychiatric Symptoms in Late-Stage Parkinsonism. Mov Disord Clin Pract. 2020 May 21;7(5):531-542.
- Ibrahim H, Woodward Z, Pooley J, Richfield EW. Rotigotine patch prescription in inpatients with Parkinsons disease: evaluating prescription accuracy, delirium and end-of-life use. Age Ageing 2021;50:1397401.
- IKNL/Palliactief. Kwaliteitskader palliatieve zorg Nederland. 2017. Geraadpleegd via https://palliaweb.nl/publicaties/kwaliteitskader-palliatieve-zorg-nederland-public.
- IKNL/Palliaweb, richtlijn Delier in de palliatieve fase; 2022. Geraadpleegd via https://palliaweb.nl/richtlijnen-palliatieve-zorg/richtlijn/delier.
- IKNL/Palliaweb, richtlijn Dyspneu in de palliatieve fase, 2021. Geraadpleegd via https://palliaweb.nl/richtlijnen-palliatieve-zorg/richtlijn/dyspneu.
- IKNL/Palliaweb, richtlijn Misselijkheid en braken, 2014. Geraadpleegd via https://palliaweb.nl/richtlijnen-palliatieve-zorg/richtlijn/misselijkheid-braken.
- Reid WG, Hely MA, Morris JG, Loy C, Halliday GM. Dementia in Parkinson's disease: a 20-year neuropsychological study (Sydney Multicentre Study). J Neurol Neurosurg Psychiatry. 2011 Sep;82(9):1033-7.
- Rosqvist K, Horne M, Hagell P, Iwarsson S, Nilsson MH, Odin P. Levodopa Effect and Motor Function in Late Stage Parkinson's Disease. J Parkinsons Dis. 2018;8(1):59-70.
- Rosqvist K, Odin P, Hagell P, Iwarsson S, Nilsson MH, Storch A. Dopaminergic Effect on Non-Motor Symptoms in Late Stage Parkinson's Disease. J Parkinsons Dis. 2018;8(3):409-420.
- Schrag A, Hommel ALAJ, Lorenzl S, Meissner WG, Odin P, Coelho M, Bloem BR, Dodel R; CLaSP consortium. The late stage of Parkinson's -results of a large multinational study on motor and non-motor complications. Parkinsonism Relat Disord. 2020 Jun;75:91-96.
- Smit, Paul; Palliatieve terminale zorg bij de ziekte van Parkinson. Tijdschrift voor Ouderengeneeskunde april 2016 no 2.
- Verenso. Probleemgedrag bij mensen met dementie, 2018. Utrecht: https://www.verenso.nl/richtlijnen-en-praktijkvoering/richtlijnendatabase/probleemgedrag-bij-mensen-met-dementie
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 06-10-2023
Beoordeeld op geldigheid : 26-06-2023
De eigenaars van de richtlijn moeten kunnen aantonen dat de richtlijn zorgvuldig en met de vereiste deskundigheid tot stand is gekomen.
Bij voorkeur beoordelen de eigenaren jaarlijks de (modules van de) richtlijn op actualiteit. Zo nodig wordt de richtlijn tussentijds op onderdelen bijgesteld. De geldigheidstermijn van de richtlijn is maximaal vijf jaar na vaststelling. Indien de inhoud dan nog actueel wordt bevonden, wordt de geldigheidsduur verlengd. De geldigheid van de (modules van de) richtlijn komt eerder te vervallen, indien nieuwe ontwikkelingen aanleiding zijn tot (modulaire) herziening. IKNL draagt gedurende de hele geldigheidsduur zorg voor het beheer en de ontsluiting van deze richtlijn.
Juridische betekenis
Een richtlijn is een kwaliteitsstandaard. Een kwaliteitsstandaard beschrijft wat goede zorg is, ongeacht de financieringsbron (Zorgverzekeringswet (Zvw), Wet langdurige zorg (Wlz), Wet maatschappelijke ondersteuning (Wmo), aanvullende verzekering of eigen betaling door de cliënt/patiënt). Opname van een kwaliteitsstandaard in het Register van Zorginstituut Nederland betekent dus niet noodzakelijkerwijs dat de in de kwaliteitsstandaard beschreven zorg verzekerde zorg is.
De richtlijn bevat aanbevelingen van algemene aard. Het is mogelijk dat deze aanbevelingen in een individueel geval niet van toepassing zijn. Er kunnen zich feiten of omstandigheden voordoen waardoor het wenselijk is dat in het belang van de patiënt van de richtlijn wordt afgeweken. Wanneer wordt afgeweken, dient dit beargumenteerd gedocumenteerd te worden in het dossier van de patiënt. De toepassing van de richtlijnen in de praktijk is de verantwoordelijkheid van elke zorgverlener, zowel BIG-geregistreerd als niet BIG-geregistreerd.
Algemene gegevens
Initiatief
Agendacommissie richtlijnen palliatieve zorg (KNMG/IKNL)
IKNL (Integraal Kankercentrum Nederland)
Regiehouder
De Nederlandse Vereniging voor Neurologie (NVN) en de Nederlandse Vereniging van Revalidatieartsen (VRA) zijn als regiehouders van deze richtlijn de eerstverantwoordelijke voor de actualiteit van (de modules van) de richtlijn en daarmee de eerstverantwoordelijke om bij te houden of de richtlijn geüpdatet moet worden.
Eigenaarschap
Het eigenaarschap van deze richtlijn ligt bij de beroeps- en wetenschappelijke verenigingen die de herziening hebben uitgevoerd en de richtlijn hebben geautoriseerd.
Procesbegeleiding en verantwoording
IKNL (Integraal Kankercentrum Nederland) is het kennis- en kwaliteitsinstituut voor professionals en bestuurders in de oncologische en palliatieve zorg dat zich richt op het continu verbeteren van de oncologische en palliatieve zorg.
IKNL benadert preventie, diagnose, behandeling, nazorg en palliatieve zorg als een keten waarin de patiënt centraal staat. Om kwalitatief goede zorg te waarborgen ontwikkelt IKNL producten en diensten ter verbetering van de oncologische zorg, de nazorg en de palliatieve zorg, zowel voor de inhoud als de organisatie van de zorg binnen en tussen instellingen.
Daarnaast draagt IKNL nationaal en internationaal bij aan de beleidsvorming op het gebied van oncologische en palliatieve zorg.
IKNL rekent het (begeleiden van) ontwikkelen, implementeren en evalueren van multidisciplinaire, evidence based richtlijnen voor de palliatieve zorg tot een van haar primaire taken. IKNL werkt hierbij conform de daarvoor geldende (inter)nationale kwaliteitscriteria. Bij ontwikkeling gaat het in toenemende mate om onderhoud (modulaire revisies) van reeds bestaande richtlijnen.
Financiering
Deze richtlijn(module) is gefinancierd door ZonMW. De inhoud van de richtlijn(module) is niet beïnvloed door de financierende instantie.
Doel en doelgroep
Met de ontwikkeling van evidence-based richtlijnmodules over palliatieve zorg voor mensen met de ziekte van Parkinson wordt beoogd om de kwaliteit van leven en de kwaliteit van sterven voor mensen met de ziekte van Parkinson te verhogen.
Doelpopulatie
De richtlijn beschrijft de zorg voor mensen met de ziekte van Parkinson en hun naasten/mantelzorgers.
Zorg voor mensen met atypische parkinsonismen is beschreven in een kwaliteitstandaard: Kwaliteitstandaard atypische parkinsonismen (VSOP, 2020).
Doelgroep
De richtlijn is bestemd voor alle zorgverleners die betrokken zijn bij de zorg voor mensen met Parkinson in de palliatieve fase. Dit zijn o.a.:
- Diëtisten
- Ergotherapeuten
- Fysio- en oefentherapeuten
- Geestelijk verzorgers
- Huisartsen
- Klinisch geriaters
- Logopedisten
- Maatschappelijk werkers
- Neurologen
- Openbaar apothekers en poliklinische apothekers
- Physician assistants
- Psychologen
- Psychiaters
- Revalidatieartsen
- Specialisten ouderengeneeskunde
- Verzorgenden, verpleegkundigen en verpleegkundig specialisten
Voor huisartsen geldt primair de NHG-Standaard Ziekte van Parkinson. Als de huisarts bij patiënten met de ziekte van Parkinson in de palliatieve fase niet meer met de NHG-Standaard uitkomt, kan de huisarts gebruikmaken van deze IKNL-richtlijn.
Samenstelling werkgroep
Alle werkgroepleden zijn afgevaardigd namens wetenschappelijke en beroepsverenigingen en hebben daarmee het mandaat voor hun inbreng. Bij de samenstelling van de werkgroep is geprobeerd rekening te houden met landelijke spreiding, inbreng van betrokkenen uit zowel academische als algemene ziekenhuizen/instellingen en vertegenwoordiging van de verschillende verenigingen/disciplines.
Het patiëntenperspectief is vertegenwoordigd door middel van afvaardiging van een ervaringsdeskundige en een beleidsmedewerker van de Parkinson Vereniging.
Werkgroepleden
- drs. G. (Gabrielle) Faber, huisarts, NHG
- dr. A.L.A.J. (Danny) Hommel, voorzitter, specialist ouderengeneeskunde, Verenso
- drs. M.M. (Masja) van het Hoofd, beleidsmedewerker, Parkinson Vereniging
- drs. K.C. (Kaie) Klaassen, ervaringsdeskundige, Parkinson Vereniging
- dr. H. (Herma) Lennaerts, verpleegkundig expert en onderzoeker ParkinsonSupport, V&VN/ParkinsonNet
- dr. E.C. (Elsbeth) Littooij, geestelijk verzorger, VGVZ
- dr. M.M. (Mirthe) Ponsen, neuroloog, NVN
- drs. P.H. (Paul) Smit, specialist ouderengeneeskunde, Verenso
- drs. C.C.M. (Clementine) Stuijt, apotheker, clinical pharmacist, KNMP
Klankbordleden
- prof. dr. O.A. (Odile) van den Heuvel, psychiater, NVVP
- drs. J.B. (Joost) Masselink, MSc., ziekenhuisapotheker, NVZA
- drs. E.A. (Eline) Nelissen, revalidatiearts, VRA
- drs. S. (Selma) de Wit, expert logopedie, ParkinsonNet NL
Ondersteuning
- dr. C.A. (Cindy) van den Berg-Verberkt, adviseur (richtlijnen) palliatieve zorg, IKNL (tot 1-8-2022)
- dr. W.A. (Annefloor) van Enst, adviseur richtlijnontwikkeling, IKNL
- L.K. (Jacqueline) Liu, secretaresse, IKNL
- dr. C.H. (Corinne) Stoop, adviseur palliatieve zorg, IKNL (vanaf 1-8-2022)
Belangenverklaringen
Om de beïnvloeding van de richtlijnontwikkeling of formulering van de aanbevelingen door conflicterende belangen te minimaliseren zijn de leden van de werkgroep gemandateerd door de wetenschappelijke en beroepsverenigingen. Alle leden van de richtlijnwerkgroep en klankbordgroep hebben verklaard onafhankelijk gehandeld te hebben bij het opstellen van de richtlijn. Een onafhankelijkheidsverklaring ‘Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling' zoals vastgesteld door onder meer de KNAW, KNMG, Gezondheidsraad, NHG en de Federatie van Medisch Specialisten is door de werkgroepleden bij aanvang en bij afronding van het traject ingevuld. De bevindingen zijn schriftelijk vastgelegd in de belangenverklaring en opvraagbaar via richtlijnen@iknl.nl.
Inbreng patiëntenperspectief
Via Patiëntenfederatie Nederland namen patiëntvertegenwoordigers Parkinson Vereniging zitting in de werkgroep. De Patiëntenfederatie nam als agendalid deel. De input van patiëntvertegenwoordigers is nodig voor de ontwikkeling van kwalitatief goede richtlijnen. Goede zorg voldoet immers aan de wensen en eisen van zowel zorgverlener als patiënt. Door middel van onderstaande werkwijze is informatie verkregen en zijn de belangen van de patiënt meegenomen:
- Bij aanvang van het richtlijntraject hebben de patiëntvertegenwoordigers knelpunten aangeleverd.
- Er is een enquête uitgezet onder patiënten via de Parkinson Vereniging.
- De patiëntvertegenwoordigers hebben de conceptteksten beoordeeld om het patiëntenperspectief in de formulering van de definitieve tekst te optimaliseren.
- Patiëntenfederatie Nederland en Parkinson Vereniging zijn geconsulteerd in de externe commentaarronde.
- Patiëntenfederatie Nederland en Parkinson Vereniging hebben ingestemd met de inhoud van de richtlijn.
- Patiënteninformatie / een patiëntensamenvatting wordt opgesteld en gepubliceerd op de daarvoor relevante sites.
Methode ontwikkeling
Evidence based
Werkwijze
De richtlijnwerkgroep is op 4 oktober 2021 voor de eerste maal bijeengekomen. Op basis van een door de werkgroepleden opgestelde enquête heeft een knelpuntenanalyse plaatsgevonden onder zorgverleners en patiënten(vertegenwoordigers). Na het versturen van de enquête hebben 214 zorgverleners gereageerd en knelpunten geprioriteerd en/of ingebracht (zie bijlage 4). Op basis hiervan is door de werkgroep een keuze gemaakt voor de volgende onderwerpen:
- Starten van palliatieve zorg
- Signaleren van fasen die van belang zijn voor de palliatieve zorg voor mensen met de ziekte van Parkinson
- Proactieve zorgplanning
- Signaleren van zorgbehoeften in de palliatieve fase
- Medicamenteuze behandeling in de palliatieve fase
- Zingeving en spiritualiteit
- Rouw
- Medicamenteuze behandeling in de stervensfase
- Organisatie van zorg
De werkgroep heeft gedurende circa twaalf maanden gewerkt aan de tekst van de conceptrichtlijn. Alle teksten zijn schriftelijk of tijdens plenaire bijeenkomsten besproken en na verwerking van de commentaren door de werkgroep geaccordeerd.
De conceptrichtlijn is op 26 oktober 2022 ter becommentariëring aangeboden aan alle voor de knelpuntenanalyse benaderde wetenschappelijke, beroeps- en patiëntenverenigingen en koepelorganisaties. Het commentaar geeft input vanuit het veld om de kwaliteit en de toepasbaarheid van de richtlijn te optimaliseren en landelijk draagvlak voor de richtlijn te genereren. Alle commentaren werden vervolgens beoordeeld en verwerkt door de richtlijnwerkgroep. Aan de commentatoren is voorafgaand aan de autorisatie teruggekoppeld wat met de reacties is gedaan.
De richtlijn is inhoudelijk vastgesteld op 10 mei 2023. Tenslotte is de richtlijn ter autorisatie/instemming gestuurd naar de betrokken verenigingen/instanties.
Leeswijzer
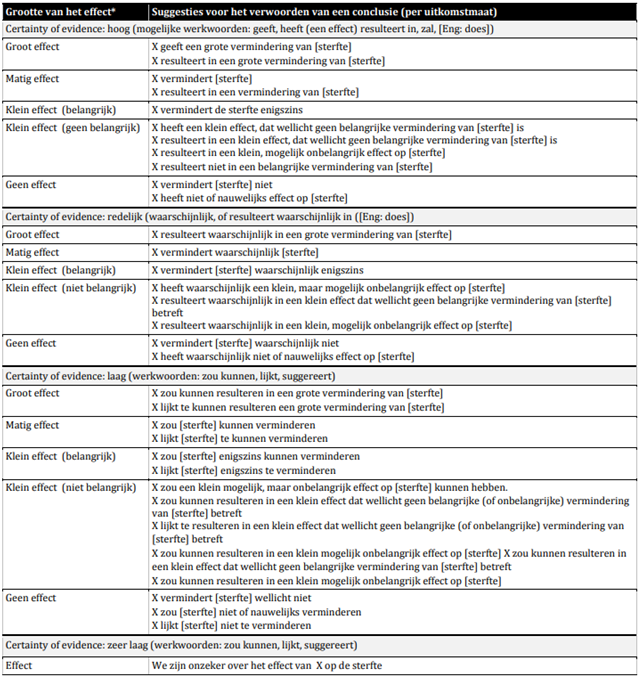
Iedere module of paragraaf in deze richtlijn start met de uitgangsvraag en de bijbehorende aanbevelingen. In tabel 1 is weergegeven wat een sterke of zwakke aanbeveling inhoudt. Een uitgebreide uitleg van de graderingen vindt u in bijlage 4.
Tabel 1. Formulering van aanbevelingen
|
Sterkte van aanbeveling |
Betekenis |
Voorkeursformulering |
|
Sterke aanbeveling voor |
De voordelen zijn groter dan de nadelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
Gebiedende wijs (Geef de patiënt …, Adviseer …) |
|
Zwakke aanbeveling voor |
De voordelen zijn groter dan de nadelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Overweeg [interventie], bespreek de voor- en nadelen. |
|
Neutraal |
… |
… |
|
Zwakke aanbeveling tegen |
De nadelen zijn groter dan de voordelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie niet kiezen. |
Wees terughoudend met [interventie], bespreek de voor- en nadelen. |
|
Sterke aanbeveling tegen |
De nadelen zijn groter dan de voordelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie niet kiezen. |
Gebiedende wijs (Geef niet …, ontraden) |
Voor de evidence-based modules volgt vervolgens de literatuurbespreking. Hierin worden de methode van het literatuuronderzoek, de resultaten, de kwaliteit van het bewijs en de conclusies weergegeven.
Elke module eindigt met de overwegingen.
Bijlagen
Bijlage 5. Zoekverantwoording
Bijlage 6. Evidence tabellen en Risk of bias beoordelingen
Bijlage 7. Kennislacunes
Bijlage 8. Communicatie- en implementatieplan
Bijlage 9. Knelpunteninventarisatie
Bijlage 10. Begrippen en afkortingen
Voor iedere module werd een subgroep uit de richtlijnwerkgroep geformeerd. De modules Proactieve zorgplanning, signaleren van zorgbehoeften en medicamenteuze behandeling in de palliatieve en stervensfase zijn uitgewerkt volgens de evidence-based methodiek GRADE.
Elke module is opgebouwd volgens een vast stramien: uitgangsvraag, aanbevelingen, literatuurbespreking, conclusies, overwegingen en referenties. De antwoorden op de uitgangsvragen (dat zijn de aanbevelingen in deze richtlijn) zijn voor zover mogelijk gebaseerd op gepubliceerd wetenschappelijk onderzoek. Enkele uitgangsvragen zijn zonder systematisch literatuuronderzoek uitgewerkt.
Knelpuntenanalyse
In de voorbereidende fase van de richtlijn is door de werkgroep een overzicht met knelpunten opgesteld. Deze knelpunten zijn middels een enquête voorgelegd aan zorgprofessionals via relevante beroeps- en wetenschappelijke verenigingen. Hierbij werd de respondenten gevraagd de knelpunten te prioriteren. Tevens was er de mogelijkheid om andere knelpunten aan te dragen.
De uitkomsten van de knelpunteninventarisatie ziet u in onze ‘Factsheet knelpuntenenquête de Ziekte van Parkinson: de palliatieve fase: de palliatieve fase (december 2021)’. Deze resultaten zijn door de werkgroep besproken en omgezet in uitgangsvragen.
Ontwikkeling module(s)
Zoeken en selecteren
Bij deze modules is de uitgangsvraag omgezet naar één of meerdere onderzoeksvragen op basis van specifieke zoektermen. Daarnaast zijn door de werkgroep uitkomstmaten aangegeven die voor de patiënt belangrijk zijn. Deze uitkomstmaten zijn gewaardeerd op basis van belang bij de besluitvorming en hierdoor onderverdeeld in cruciale, belangrijke en niet-belangrijke uitkomstmaten.
Aan de hand van deze zoektermen is gezocht in diverse elektronische databases naar wetenschappelijke literatuur. De zoekstrategieën per onderzoeksvraag vindt u in Bijlage 5.
Op basis van vooraf opgestelde in- en exclusiecriteria werd de gevonden literatuur geselecteerd, eerst op basis van de titel en samenvatting en vervolgens op basis van het gehele artikel. Per module zijn de aantallen gevonden artikelen en de aantallen geëxcludeerde studies te vinden in Bijlage 5. Redenen voor exclusie zijn opgenomen in de exclusietabellen in Bijlage 5.
Naast de selectie op relevantie werd tevens geselecteerd op bewijskracht. Hiervoor werd gebruik gemaakt van de volgende hiërarchische indeling van studiedesigns gebaseerd op bewijskracht:
- systematische reviews.
- gerandomiseerde gecontroleerde studies (RCT's).
- niet gerandomiseerde gecontroleerde studies (CCT's).
Kwaliteit van individuele studies
Individuele studies werden beoordeeld door middel van de Cochrane Risk of Bias tool (gerandomiseerde studies) en de AMSTAR Risk of Bias tool (systematische reviews).
Kwaliteit van het bewijs
Vervolgens werd de kwaliteit van het bewijs beoordeeld volgens de GRADE-methodiek. De kwaliteit van bewijs wordt weergegeven in vier categorieën: hoog, matig, laag en zeer laag. Zoals te zien is in tabel 1, starten RCT's hoog en observationele studies laag. Vijf factoren verlagen de kwaliteit van de bewijskracht en drie factoren kunnen de kwaliteit van de evidentie verhogen (zie tabel 1). Op deze manier werd de bewijskracht per uitkomstmaat gegradeerd.
Tabel 1. GRADE-methodiek voor het graderen van bewijs
|
Kwaliteit van bewijs |
Onderzoeksopzet |
Verlagen als |
Verhogen als |
|
Hoog |
Gerandomiseerde studie |
Beperkingen in de onderzoeksopzet -1 ernstig -2 zeer ernstig
Inconsistenties -1 ernstig -2 zeer ernstig
Indirectheid -1 ernstig -2 zeer ernstig
Imprecisie -1 ernstig -2 zeer ernstig
Publicatiebias -1 waarschijnlijk -2 zeer waarschijnlijk |
Sterke associatie + 1 sterk + 2 zeer sterk
Dosis-respons relatie + 1 bewijs voor deze relatie
Aanwezigheid van plausibele residuele confounding + 1 zou een aangetoond effect verminderen, of + 1 zou een onterecht effect suggereren als de resultaten geen effect laten zien |
|
Redelijk |
|
||
|
Laag |
Observationele studie |
||
|
Zeer laag |
|
Algehele kwaliteit van bewijs
Omdat het beoordelen van de kwaliteit van bewijs in de GRADE-methodiek per uitkomstmaat geschiedt, is er behoefte aan het bepalen van de algehele kwaliteit van bewijs. Voor het literatuuronderzoek werd door de richtlijnwerkgroep bepaald welke uitkomstmaten cruciaal, belangrijk en niet belangrijk zijn. Het niveau van de algehele kwaliteit van bewijs wordt in principe bepaald door de cruciale uitkomstmaat met de laagste kwaliteit van bewijs.
Als echter de kwaliteit van het bewijs verschilt tussen de verschillende cruciale uitkomstmaten zijn er twee opties:
- De uitkomstmaten wijzen in verschillende richtingen (zowel gewenst als ongewenste effecten) of de balans tussen gewenste en ongewenste effecten is onduidelijk, dan bepaalt de laagste kwaliteit van bewijs van de cruciale uitkomstmaten de algehele kwaliteit van bewijs;
- De uitkomstmaten wijzen in dezelfde richting (richting gewenst of richting ongewenst effecten), dan bepaalt de hoogste kwaliteit van bewijs van de cruciale uitkomstmaat dat op zichzelf voldoende is om de interventie aan te bevelen van de algehele kwaliteit van bewijs.
Op basis hiervan werden de conclusies geformuleerd (zie tabel 2).
Tabel 2. Formulering conclusies op basis van kwaliteit van bewijs per uitkomstmaat
|
Kwaliteit van bewijs |
Interpretatie |
Formulering conclusie |
|
Hoog |
Er is veel vertrouwen dat het werkelijk effect dicht in de buurt ligt van de schatting van het effect. |
Zie tabel 3 |
|
Redelijk |
Er is redelijk vertrouwen in de schatting van het effect: het werkelijk effect ligt waarschijnlijk dicht bij de schatting van het effect, maar er is een mogelijkheid dat het hier substantieel van afwijkt. |
Zie tabel 3 |
|
Laag |
Er is beperkt vertrouwen in de schatting van het effect: het werkelijke effect kan substantieel verschillend zijn van de schatting van het effect. |
Zie tabel 3 |
|
Zeer laag |
Er is weinig vertrouwen in de schatting van het effect: het werkelijke effect wijkt waarschijnlijk substantieel af van de schatting van het effect. |
Zie tabel 3 |
|
Formulering algehele kwaliteit van bewijs: hoog/redelijk/laag/zeer laag. |
||
Tabel 3. Standaard GRADE conclusies
*Noten:
- Grote en redelijke effecten zijn sowieso belangrijk! Kleine effecten kunnen belangrijk of onbelangrijk zijn.
- Bij het beslissen over de vraag of het een belangrijk of onbelangrijk effect betreft is een leidraad wat de drempelwaarde is waarboven of waarbeneden de beslissing (aanbeveling) zou veranderen.
- Als de richtlijn geen drempelwaarde kan bepalen:
- Continue uitkomstmaten op dezelfde schaal gemeten: in relatie tot MID effectgrootte beoordelen. "Voor sommige uitkomsten is al vastgesteld dat er een specifiek niveau is waarbij het effect belangrijk is voor patiënten (bijvoorbeeld onderzoek laat zien dat 4 punten op de Health Related Quality of Life-schaal belangrijk zijn voor patiënten). In andere gevallen kunnen beoordelaars een drempelwaarde gebruiken (GRADE beveelt aan dat RR < 0,80 of > 1,25), of hun eigen oordeel gebruiken."" klein (0,2 - 0,5 MID), matig (0,5 - 1,5 MID) en groot >1,5 MID. Geen effect: 0 tot 0,2 MID. Indien MID onbekend, omrekenen naar SMD.
- Continue uitkomstmaten op verschillende schalen gemeten: SMD=0,2 (klein); SMD=0,5 (redelijk); SMD=0,8 groot.
- Dichotome uitkomstmaten (absolute effect: NNT = RRR * baseline risico): context gebonden (odds ratio’s converteren naar RR!).
Formuleren van overwegingen
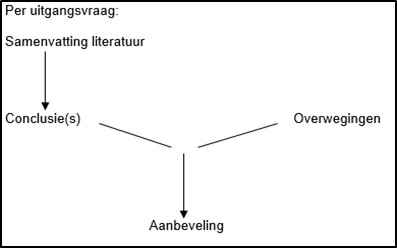
Naast het bewijs uit de literatuur (conclusies) zijn er andere overwegingen die meespelen bij het formuleren van de aanbeveling. Deze aspecten worden besproken onder het kopje ‘Overwegingen' in de module. Hierin worden de conclusies (op basis van de literatuur) geplaatst in de context van de dagelijkse praktijk en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties. De uiteindelijk geformuleerde aanbeveling is het resultaat van de conclusie(s) in combinatie met deze overwegingen (Figuur 1).
Figuur 1. Van bewijs naar aanbeveling
Bij het schrijven van de overwegingen zijn onderstaande zaken in acht genomen:
Kwaliteit van het bewijs
Hoe hoger de algehele kwaliteit van het bewijs, des te waarschijnlijker wordt het formuleren van een sterke (positieve of negatieve) aanbeveling.
Patiëntenperspectief
Beschreven wordt in hoeverre het bewijs aansluit bij de waarde en behoefte van de patiënt. Wat vindt de patiënt het belangrijkste? Of waar loopt de patiënt tegenaan? Is er voldoende bewijskracht voor de voor patiënten relevante uitkomsten? Wat zijn de consequenties voor patiënten (bijv. opnameduur, kosten die zij zelf maken).
Professioneel perspectief
Beschreven wordt in hoeverre het bewijs aansluit bij de inzichten van de professional. Bijvoorbeeld als het gaat om de kennis en ervaring met de interventie, de te verwachten risico’s die de professional loopt en de te verwachten tijdsbesparing/tijdsinvestering.
Aanvaardbaarheid en haalbaarheid
Beschreven wordt in hoeverre de inventie aanvaardbaar is. DenkDenk hierbij aan ethische en juridische overwegingen, maar ook in hoeverre het haalbaar is. Denk daarbij aan voldoende tijd, kennis en mankracht, impact op de organisatie van zorg of bijvoorbeeld beschikbaarheid van medicatie en kosten.
Balans van gewenste en ongewenste effecten
Beschreven wordt in hoeverre de voordelen opwegen tegen de nadelen. Ook de perspectieven van de patiënt en de professional worden belicht, als die verschillend zijn.
Rationale voor de aanbeveling
Optioneel eindigt de overweging met een heel korte samenvatting waarom de aanbeveling voor of tegen de interventie adviseert.
Formuleren van aanbevelingen
Aanbevelingen in richtlijnen geven een antwoord op de uitgangsvraag. De GRADE-methodiek kent twee soorten aanbevelingen: sterke aanbevelingen of conditionele (zwakke) aanbevelingen. De sterkte van de aanbevelingen reflecteert de mate van vertrouwen waarin - voor de groep patiënten waarvoor de aanbevelingen zijn bedoeld - de gewenste effecten opwegen tegen de ongewenste effecten. Zie voor de formulering van sterke en zwakke aanbevelingen Tabel 4.
Tabel 4. Formulering van aanbevelingen
|
Gradering van aanbeveling |
Betekenis |
Voorkeursformulering |
|
Sterke aanbeveling voor |
De voordelen zijn groter dan de nadelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie kiezen. |
Gebiedende wijs (Geef de patiënt …, Adviseer …) |
|
Zwakke aanbeveling voor |
De voordelen zijn groter dan de nadelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie kiezen. |
Overweeg [interventie], bespreek de voor- en nadelen. |
|
Neutraal |
… |
… |
|
Zwakke aanbeveling tegen |
De nadelen zijn groter dan de voordelen voor een meerderheid van de patiënten, maar niet voor iedereen. De meerderheid van geïnformeerde patiënten zal waarschijnlijk deze optie niet kiezen. |
Wees terughoudend met [interventie], bespreek de voor- en nadelen. |
|
Sterke aanbeveling tegen |
De nadelen zijn groter dan de voordelen voor bijna alle patiënten. Alle of nagenoeg alle geïnformeerde patiënten zullen waarschijnlijk deze optie niet kiezen. |
Gebiedende wijs (Geef niet …, ontraden) |
Referenties
- Bouça-Machado R, Titova N, Chaudhuri KR, Bloem BR, Ferreira JJ. Palliative Care for Patients and Families With Parkinson's Disease. Int Rev Neurobiol. 2017;132:475-509.
- Dorsey ER, Sherer T, Okun MS, Bloem BR. The Emerging Evidence of the Parkinson Pandemic. J Parkinsons Dis. 2018;8(s1):S3-S8. doi: 10.3233/JPD-181474. PMID: 30584159; PMCID: PMC6311367.
- IKNL/Palliactief. Kwaliteitskader palliatieve zorg Nederland, 2017.
- Kluger BM. Palliative care for Parkinson's disease and related disorders: stepping into the future. Ann Palliat Med. 2020 Feb;9 (Suppl 1):S3-S5.
- NVN & VRA, 2020. Richtlijn ziekte van Parkinson. Bezocht op 19 oktober 2022 via voor mensen met de ziekte van Parkinson.
- ParkinsonNet, 2018. ParkinsonNet in cijfers, 2020. Bezocht op 6 augustus 2022 via https://www.parkinsonnet.nl/parkinsonnet-in-cijfers
- Richfield EW, Jones EJ, Alty JE. Palliative care for Parkinson's disease: a summary of the evidence and future directions. Palliat Med. 2013 Oct;27(9):805-10.