Behandeling patiënten met een zeldzame mutatie bij NSCLC
Uitgangsvraag
Aanbeveling
Algemeen
Test alle patiënten die in aanmerking komen voor palliatieve systeemtherapie met niet-squameus NSCLC, of met squameuze histologie, die niet of weinig gerookt hebben, op de aberraties in de volgende genen: EGFR, KRAS, ALK, ROS1, BRAF, RET, MET, HER2, NTRK1/2/3 en NRG. Dit is ongeacht de klinische conditie.
Overleg met een ander centrum als niet alle testen in het eigen ziekenhuis kunnen worden uitgevoerd om het predictieve testproces zo gestroomlijnd mogelijk te laten verlopen.
Verwijs patiënten met aberraties in de volgende genen ALK, ROS1, BRAF, RET, MET, HER2, NTRK1/2/3 of NRG, en uncommon EGFR naar een gespecialiseerd centrum (NVALT centrum voor zeldzame driver mutaties).
ALK
Behandel patiënten met een ALK-translocatie met een ALK-TKI in de eerste lijn bij voorkeur met alectinib, andere opties zijn crizotinib, ceritinib en brigatinib.
Behandel patiënten in de tweede lijn en verder afhankelijk van de gegeven TKI in de eerste lijn en het gevonden resistentiepatroon (specifieke ALK-mutatie) met ceritinib, alectinib of brigatinib.
ROS1
Behandel patiënten met een ROS1 translocatie in de eerste lijn met crizotinib.
BRAF V600
Behandel patiënten met een BRAF V600 mutatie in de eerste lijn met de combinatie dabrafenib/trametinib.
RET/ HER2/ MET/ NTRK/ NRG
Bespreek behandelmogelijkheden in de Moleculaire Tumor Board met betrekking tot uncommon EGFR, RET, HER2, MET, NTRK 1/2/3 of NRG afwijkingen als ook combinaties van driver mutaties en bespreek vervolgens met de patiënt indien mogelijk deelname aan een klinische studie.
Behandel met standaard systeemtherapie als een patiënt niet aan een studie deelneemt.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Algemeen: gezien de beschikbare therapieën voor patiënten met een driver aberratie, is de werkgroep van mening dat alle patiënten die in aanmerking komen voor palliatieve systeemtherapie met niet squameus NSCLC, of met squameuze histologie die niet of weinig gerookt hebben, op de volgende predictieve markers getest moeten worden voor genetische tumor-specifieke afwijkingen: mutaties in EGFR, KRAS, BRAF, en MET-skipping en fusies/rearrangements in ALK, ROS, RET, NTRK1/2/3 en NRG. In deze module wordt een onderbouwing gegeven waarom dit zinnig is voor de zeldzame mutaties. De behandeling van patiënten met resistente mutaties ten gevolge van progressie op TKI (zoals mutaties in ALK, ROS, RET) worden besproken in de module 'Bepaling van resistentie bij doelgerichte therapie'; in de module 'Behandeling patienten met activerende EGFR-mutatie' wordt een onderbouwing gegeven waarom dit zinnig is voor EGFR. Voor KRAS bestaat vooralsnog geen veelbelovende doelgerichte therapie, een KRAS mutatie is wel negatief voorspellend voor de effectiviteit van bijvoorbeeld EGFR-TKI.
ALK-fusies/rearrangements/expressie
1e lijn: ORR en PFS zijn significant beter met ALK-TKI (crizotinib danwel ceritinib) dan met platinum-bevattende chemotherapie. De verbetering in mediane PFS is klinisch relevant (HR < 0.7 en verbetering 12 weken of meer). Het percentage graad 3 of hoger bijwerkingen is gelijk tot hoger met ALK-TKIs, het soort bijwerkingen is echter verschillend (met name biochemisch en gastro-intestinaal voor de ALK-TKIs en hematologisch voor de chemotherapie). Echter, ondanks geen evidente verschillen in ernstige bijwerkingen, verbeteren zowel crizotinib als ceritinib de kwaliteit van leven/ patiënt gerapporteerde uitkomsten vergeleken met chemotherapie. Totale overleving verbeterde niet in de studies, waarschijnlijk doordat het merendeel van de patiënten in latere lijnen nog met een ALK-TKI werd behandeld. Belangrijk is verder dat patiënten met hersenmetastasen (niet-significante) betere uitkomsten hebben met ALK-TKIs dan met chemotherapie (zowel ORR als PFS).
De vergelijking van verschillende ALK-TKIs viel buiten de systematische zoekvraag. Echter, in de eerstelijns behandeling zijn recent zowel alectinib als brigatinib met crizotinib vergeleken bij patiënten met een ALK rearrangement. In de fase III ALEX trial zorgde alectinib voor een verbetering in mediane PFS van 10.4 maanden voor crizotinib naar 25.7 maanden voor alectinib (HR 0.50 (95% CI 0.36 to 0.70). Dit effect was zeer uitgesproken bij de patiënten met baseline hersenmetastasen (HR 0.16). Tevens was het percentage patiënten met graad 3 of meer bijwerkingen lager voor alectinib (41% versus 50%) (Peters, 2017). Brigatinib is vergeleken met crizotinib in de ALTA-1L studie. In de eerste geplande interim analyse zorgde brigatinib voor een significant langere progressie vrije overleving op 12 maanden: 67% versus 43%, HR 0.49. ORR was iets hoger voor brigatinib (71% versus 60%), maar met name de intracraniële ORR was hoger met brigatinib (78% versus 29%) (Camidge, 2018). Het is echter nog niet duidelijk of het als eerstelijnsbehandeling in plaats van in latere lijnen inzetten van nieuwere generatie ALK-TKIs zorgt voor een betere overall survival.
Tweedelijns behandeling en verder: voor zowel crizotinib (na progressie op 1e lijn chemotherapie) als ceritinib en alectinib (na progressie op 1e lijn chemotherapie en crizotinib) zijn ORR en PFS beter dan met monotherapie chemotherapie. Ook de resultaten van deze studies zorgen voor een klinisch relevante verbetering in de PFS. Ondanks (behalve voor alectinib) een hoger percentage graad 3 of meer bijwerkingen, zijn kwaliteit van leven / patiënt gerapporteerde uitkomsten beter met crizotinib of ceritinib, vergeleken met chemotherapie (alectinib nog niet gerapporteerd). De opmerkingen over totale overleving en hersenmetastasen in het stuk 1e lijn gelden ook voor latere lijnen. Belangrijk is dat ceritinib een betere bloed-hersenbarrière penetratie heeft dan crizotinib, en dat alectinib weer een betere penetratie heeft dan ceritinib (Remon and Besse, 2018).
Brigatinib is niet vergeleken met chemotherapie of met een andere ALK-TKI in >/=2e lijn, maar wel gerandomiseerd getest (ALTA studie) in 2 doseringen in crizotinib resistente patiënten (74% had ook chemotherapie gehad). ORR was 45% met 90 mg/dag brigatinib, en 54% met 180 mg/dag brigatinib. Mediane PFS was 9.2 en 12.9 maanden respectievelijk. 69% had baseline hersenmetastasen, intracraniële ORR was beter met 180 mg brigatinib (Kim, 2017). De verbeterde intracraniële ORR met 180 mg brigatinib wordt ook gezien in een gepoolde analyse van een fase I/II brigatinib studie gecombineerd met de data van de gerandomiseerde ALTA studie. Bevestigde intracraniele ORR was 53% in de fase I/II studie, 46% in de fase II 90 mg brigatinib arm en 67% in de fase II 180 mg brigatinib arm (Camidge, 2018). Lorlatinib is veelbelovend in fase I en fase II studies(Besse, 2018; Solomon ,2018), maar is nog niet geregistreerd.
Na progressie op nieuwe generatie ALK-TKIs, is afhankelijk van het resistentiepatroon een andere ALK-TKI (te selecteren op basis van de specifieke gevonden ALK-mutatie) danwel (platinum-doublet) chemotherapie, danwel studiedeelname een optie.
ROS1
1e lijn: er zijn geen gerandomiseerde studies die een ROS1-TKI met chemotherapie hebben vergeleken. Gezien de goede ORR in fase I(Shaw, 2014) en fase II studies en in prospectieve series(Mazieres, 2015) van rond de 70%, met een mediane PFS van rond de 10 tot 19 maanden en de goede verdraagbaarheid van crizotinib, is crizotinib (geregistreerd voor ROS1) de eerstelijns behandeling van voorkeur. Ceritinib is veelbelovend in crizotinib-naïeve ROS1 patiënten maar is vooralsnog niet geregistreerd. In een fase II studie was de ORR rond de 70% met een mediane PFS van 19.3 maanden voor crizotinib-naïeve patiënten. Echter, patiënten die al waren behandeld met crizotinib reageerden niet op ceritinib (Lim, 2017).
2e lijn en verder: gezien het ontbreken van geregistreerde tweedelijns middelen specifiek voor ROS1, zijn zowel platinum-bevattende chemotherapie als een ROS1 TKI in studieverband opties.
BRAF V600
BRAF V600 gerichte therapie is zowel in 1e lijn als later getest. Initieel werd monotherapie dabrafenib (BRAF-inhibitor) getest, in een fase II, niet gerandomiseerde open label trial waarbij zowel eerder behandelde als behandeling naïeve patiënten werden geïncludeerd. In totaal werden er 84 patiënten geincludeerd waarvan 6 in de 1e lijn. ORR was 67%, ORR in de voorbehandelde patiënten was 33% (Planchard, Kim, 2016).
De combinatie dabrafenib plus trametinib (MEK-inhibitor) is ook in de 1e lijn en verder getest. In de 1e lijn (single arm fase II studie met 36 patiënten) was de ORR 64% met een mediane PFS van 14.6 maanden (Planchard, 2017). Er zijn echter geen studies die deze behandeling hebben vergeleken met chemotherapie.
2e lijn en verder: er zijn geen geregistreerde BRAF doelgerichte therapieën na progressie op dabrafenib/trametinib. Opties zijn chemotherapie en deelname aan studies. Indien een patiënt in de eerstelijnsbehandeling nog geen dabrafenib/trametinib heeft gekregen, is dit een goede behandeloptie op basis van een single arm fase II studie (59 patiënten) waarin een ORR van 63% werd gevonden, en een mediane PFS van 9.7 maanden (Planchard, Besse, 2016).
Er is een systematisch review plus meta-analyse ten aanzien van behandeling van patiënten met een BRAF mutatie (Li 2018). Tien studies werden geïncludeerd, waarvan 9 met een behandelarm met docetaxel of best-supportive care. Een niet-gecontroleerde trial evalueerde de dabrafenib-trametinib combinatie. De odds ratio om een ORR te krijgen ten opzichte van docetaxel was 13.2 (95% CI 5.5 tot 33.0) voor dabrafenib plus trametinib. Ten opzichte van docetaxel was dabrafenib + trametinib geassocieerd met een 68% lagere hazard ratio voor ziekteprogressie na 12 maanden vergeleken met docetaxel. De geschatte HR voor PFS en OS relatief ten opzichte van docetaxel waren 0.32 (95%CI 0.16 tot 0.59) en 0.41 (95%CI 0.11 tot 1.41).
BRAF niet V600
Er is vrij beperkt data beschikbaar, de data die beschikbaar zijn bij NSCLC laten zien dat targeted therapy geen goede optie is gezien de lage responskans, de korte PFS en OS (Leonetti, 2018).
RET
Er zijn geen geregistreerde RET doelgerichte therapieën en geen gerandomiseerde studies. Tot voor kort waren resultaten van RET doelgerichte therapieën teleurstellend en voor zover te vergelijken niet beter dan met chemotherapie. LOXO-292, een selectieve RET remmer, liet veelbelovende resultaten in een fase I/II studie zien, met een ORR van 77% en een mediane responsduur die nog niet bereikt was (Oxnard, 2018). De ORR met BLU-667 was 50% voor de 19 NSCLC patiënten in een fase I studie (Subbiah, 2018).
MET
MET dysregulatie kan komen door overexpressie, amplificatie, mutatie, exon-14 skipping of gen-herschikking. De vergelijkende studie met doelgerichte MET therapie hebben alleen naar MET overexpressie, maar niet specifiek naar hoge amplificatie of MET exon 14 skipping mutaties gekeken. De laatste twee spelen juist een rol als driver. Meerdere case series en cohorten hebben ORRs van rond de 40 tot 50% laten zien met TKIs die MET targeten, zoals crizotinib, capmatinib en cabozantinib bij METexon 14 skipping mutaties. Een voorbeeld is crizotinib in het PROFILE 1001 MET exon 14 skipping cohort met een ORR van 44%. Retrospectieve series laten een PFS van rond de 7 maanden zien met crizotinib (Drilon, 2016; Awad, 2017).Tepotinib, een selectieve c-MET inhibitor, liet in een single-arm fase II studie een ORR van 60% zien in NSCLC patiënten met een MET exon 14 skipping mutatie (Felip, 2018). Capmatinib, een andere selectieve c-MET inhibitor, liet een ORR van 39% zien in voorbehandelde NSCLC patiënten met een MET exon 14 skipping mutatie, en een ORR van 72% in behandelingsnaïeve NSCLC patiënten (Wolf, 2018).
HER2/ NTRK/ NRG
Ook hier zijn geen vergelijkende studies. HER2 inserties zijn meestal resistent tegen de HER-doelgerichte therapieën afatinib, dacomitinib en neratinib (Mazieres, 2016; Hyman, 2018).In kleine series hebben afatinib (12 weken ziektecontrole: 51%) en poziotinib (ORR 50%, mediane PFS 5 maanden) activiteit laten zien in NSCLC patiënten met een HER2-mutatie (Smit, 2017; Heymach, 2018). Ado-trastuzumab emtansine (TDM-1) heeft redelijke resultaten laten zien in kleine cohorten met een HER2-mutatie: ORR 44% en mediane PFS 5 maanden (Li, 2018). Resultaten bij HER2 amplificatie zijn teleurstellender (Stinchcombe, 2017). Entrectinib is veelbelovend voor NTRK-fusie positieve kankers: in een gepoolde analyse van drie fase I/II trials, waaronder NSCLC patiënten, ORR was 57.4%, mediane PFS was 11.2 maanden, mediane OS 20.9 maanden (Demetri, 2018). Ook larotrectinib laat veelbelovende resultaten zijn bij NTRK-fusie positieve kankers. In een gepoolde analyse van drie fase I/II trials van larotrectinib, waaronder NSCLC patiënten, was de ORR 75%, de mediane PFS nog niet bereikt en de mediane OS eveneens nog niet bereikt (Drilon, 2018)
Alle conclusies hebben een lage bewijskracht, gezien het niveau van de bewijskracht omlaag is gebracht vanwege limitaties in de studie designs, zoals beperkte informatie over de randomisatiemethoden, allocation concealment, open label, en het relatief lage aantal patiënten in de studies. Echter, alle studies wijzen in dezelfde richting (TKI is effectief).
Ten aanzien van ALK-rearrangements: ORR en PFS verbeteren met ALK-TKI vergeleken met chemotherapie. Tevens is kwaliteit van leven beter met ALK-TKI ten opzichte van chemotherapie, ondanks het meestal vergelijkbare (of hogere) percentage graad 3 of meer bijwerkingen.
Voor andere doelgerichte therapieën dan ALK-TKIs, bestaan er geen gerandomiseerde studies, en vaak alleen kleine fase I/II wat het niveau van de bewijskracht verder naar beneden haalt. De reden is dat al deze drivers zeldzaam zijn, tevens is een deel pas relatief recent geïdentificeerd als driver. Echter, zeker bij ROS1 en BRAF V600E zijn ORR en PFS lang bij doelgerichte therapie. Ook bij de andere aberraties zoals MET exon 14 skipping, HER2 mutaties en NTRK1/2/3 fusies zijn er TKIs beschikbaar in studieverband met hoge ORR en relatief lange PFS.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
ALK: voordeel van TKIs is dat deze oraal gegeven worden en dat patiënt dus niet voor een infuus met chemotherapie naar het ziekenhuis moet. Tevens zijn kwaliteit van leven data of patiënt gerapporteerde uitkomsten beter met ALK-TKI dan met chemotherapie.
Overige TKIs; ook hier is het voordeel dat deze oraal gegeven kunnen worden en bij ROS1 en BRAF een hoge ORR en relatief lange PFS hebben.
Kosten (middelenbeslag)
In 2014 is geconstateerd dat crizotinib 1e lijn niet kosten-effectief was in Canada, maar de vraag is of dat nu nog steeds geldt omdat het testen waarschijnlijk goedkoper is geworden. Zie bijvoorbeeld artikel van NICE waar crizotinib waarschijnlijk wel kosteneffectief is. Ceritinib ten opzichte van crizotinib is kosteneffectief. Ceritinib kan kosteneffectief zijn na crizotinib, in ieder geval in Canada. Alectinib versus ceritinib maakt weinig uit in US. Het is de vraag is ook of je dit kunt extrapoleren naar NL. Voor de overige TKIs zijn er voor zover bekend geen kosten berekeningen.
Haalbaarheid en implementatie
Door de NVALT zijn er centra aangewezen voor behandeling van zeldzame aberraties. In deze ziekenhuizen is de expertise aanwezig om patiënten met bovenstaande TKIs te behandelen, en is er toegang tot specifieke studies, expanded access en named patient programma’s en regionale MTB.
Rationale/ balans tussen de argumenten voor en tegen de interventie
Gezien de hoge ORR, lange PFS en vaak goed te hanteren toxiciteit van bovenstaande TKIs en de expertise in de aangewezen centra bestaat er de voorkeur om patiënten met een driver aberratie in een van de aangewezen centra te behandelen, met indien beschikbaar een TKI.
Onderbouwing
Achtergrond
Er worden steeds meer gericht behandelbare driver mutaties en translocaties gevonden bij NSCLC-patiënten, met name bij adenocarcinoom histologie en er komen steeds meer doelgerichte behandelingen beschikbaar in de gemetastaseerde setting voor deze patiënten. Zeker bij de zeldzame DNA-aberraties (gedefinieerd als prevalentie < 5%) zijn gerandomiseerde studies moeilijk uit te voeren. Zeldzame targetable DNA aberraties zijn momenteel anaplastic lymphoma kinase (ALK), c-ros oncogene 1 (ROS1), v-Raf murine sarcoma viral oncogene homolog B (BRAF), rearranged during transfection (RET), MET, Human Epidermal growth factor Receptor 2 (HER2), Neurotrophic receptor tyrosine kinase (NTRK1, NTRK2 en NTRK3) en Neuregulin (NRG). Zeker voor ALK komen steeds meer tyrosine kinase inhibitors (TKIs) beschikbaar. Er is behoefte aan een behandelalgoritme voor deze zeldzame DNA-aberraties, inclusief het sequentieel toepassen van TKIs en/of van chemotherapie. Voor de huidige search is ervoor gekozen de doelgerichte therapie te vergelijken met chemotherapie aangezien dit initieel de standaardtherapie voor NSCLC was. Gezien de lage prevalentie van de aberraties hierboven, gecombineerd met de vaak hoge responspercentages en lange progressievrije overleving met de nieuwe TKIs is het de verwachting dat er weinig tot geen nieuwe gerandomiseerde fase III studies meer komen waarbij een TKI vergeleken wordt met standaard chemotherapie of met een andere TKI. De vergelijkende studies die twee TKI’s vergelijken worden in de overwegingen beschreven, evenals de niet-vergelijkende TKI studies.
Conclusies
ALK-fusions /rearrangements/ expressoins
|
LOW GRADE |
In patients with advanced non-small-cell lung cancer harbouring ALK gene rearrangement (depending on trial tested with FISH or IHC), objective response rate (ORR) is possibly higher (RR=1.8 in case of first line treatment and RR=3.3 in case of second line) and the progression free survival is possibly longer after treatment with crizotinib as compared to treatment with standard chemotherapy (approximately 4 months).
References: (Shaw, 2013; Solomon, 2014; Wu, 2018) |
|
LOW GRADE |
In patients with advanced non-small-cell lung cancer harbouring ALK gene rearrangement (depending on trial tested with FISH or IHC), the overall survival seems comparable for treatment with crizotinib or treatment with standard chemotherapy. The majority of patients initially treated with chemotherapy, however, crossed over to crizotinib after the studies.
References: (Shaw, 2011; Shaw, 2013; Solomon, 2018; Wu, 2018) |
|
LOW GRADE |
The incidence of serious adverse events (grade 3 -5) seems similar in patients with advanced non-small-cell lung cancer harbouring ALK gene rearrangement treated with crizotinib as compared standard chemotherapy.
References: (Shaw, 2013; Solomon, 2014; Wu, 2018) |
|
VERY LOW GRADE |
It is unclear whether treatment with crizotinib as second line treatment results in better quality of life in patients with advanced non-small-cell lung cancer harbouring ALK gene rearrangement as compared to treatment with standard chemotherapy.
References: (Blackhall, 2014) |
|
LOW GRADE |
A higher PFS is likely for patients with advanced non-small-cell lung cancer harbouring ALK gene rearrangement treated with ceritinib as compared to chemotherapy. The overall survival is likely to be comparable for the two treatment options. Most patients initially treated with chemotherapy, however, crossed over to ceritinib after the studies
References: (Soria, 2017; Shaw, 2017) |
|
LOW GRADE |
In patients with advanced non-small-cell lung cancer and an ALK gene rearrangement, serious adverse events (grade 3 or 4) suspected to be related to study drug occurred possibly more frequently in patients treated with ceritinib as compared to patients treated with chemotherapy.
References: (Soria, 2017) |
|
LOW GRADE |
In patients with advanced non-small-cell lung cancer harbouring ALK gene rearrangement, the median progression free survival is possibly higher in patients alectinib as compared to patients treated with chemotherapy (HR 0.32 (95% CI: 0.17 to .59)). The median overall survival seems not to differ between the two treatment groups (HR 0.89 (95% CI: 0.35 to 2.24)). Most patients initially treated with chemotherapy, however, crossed over to alectinib after the study.
References: (Novello, 2018) |
|
LOW GRADE |
The incidence of serious adverse events (grade ≥ 3) is possibly lower in patients treated with alectinib as compared to chemotherapy (ARR = 14%, 95% CI (-5.5%, 33.6%))
References: (Novello, 2018) |
ROS1
|
VERY LOW GRADE |
It is uncertain whether treatment with crizotinib in patients advanced non-small-cell lung cancer and a ROS1 gene rearrangement results in a better median progression free survival and overall response rate.
References: (Mazieres, 2015) |
RET
|
VERY LOW GRADE |
It is unclear whether the median progression free survival and the median overall survival are better or worse in patients with advanced non-small-cell lung cancer and a RET rearrangement who had been treated with a RET inhibitor as compared to patients treated with standard first line platinum-doublet chemotherapy.
References: (Gautschi, 2017) |
MET
|
LOW GRADE |
In patients with advanced non-small-cell lung cancer and a high MET status (defined as MET IHC 2+ or higher), it is unclear whether the progression free survival and the overall survival are better in patients treated with onartuzumab in combination with standard chemotherapy with standard therapy chemotherapy and a placebo. There are no studies comparing a MET inhibitor to chemotherapy in MET exon 14 skipping mutated patients or those with a high MET GCN.
References: (Hirsch, 2017; Wakelee, 2017) |
BRAF/ HER2/ NTRK/ NRG
|
- |
There are no RCTs or observational studies that compared targeted therapy with chemotherapy in patients with NSCLC and a BRAF mutation, HER2 mutation, NTRK fusion or NRG fusion. |
Samenvatting literatuur
A total of fourteen studies that examined the clinical outcome after targeted therapy or chemotherapy in NSCLC patient with a rare mutation were included in this literature analysis.
ALK-fusions/rearrangements/expression
Description of studies
Eight studies were included in which targeted therapy for patients with a ALK rearrangement was investigated (Shaw, 2013; Shaw, 2014; Solomon, 2014; Blackhall, 2014; Shaw, 2017; Novello, 2018; Solomon, 2018; Soria, 2017; Wu; 2018). Of these, 5 studies compared crizotinib with standard chemotherapy (Blackhall, 2014; Shaw, 2013; Solomon, 2014; Solomon, 2018; Wu, 2018). In two studies, treatment with ceritinib was compared with standard chemotherapy (Shaw, 2017; Soria, 2017). Finally, alectinib was compared to chemotherapy in one study (Novello, 2018). All trials were industry sponsored or designed in cooperation with the industry.
Shaw (2013) performed a phase 3, open-label trial comparing crizotinib (n=173) with monotherapy chemotherapy (n=174, either pemetrexed or docetaxel) in patients with locally advanced or metastatic ALK-positive lung cancer, with progressive disease after one prior platinum-based chemotherapy regimen. Outcome measures were progression free survival (PFS), OS, Objective response rate (ORR) and safety. Safety included the number of patients with grade 3 or 4 adverse events and the number of treatment related deaths. The study was designed by the sponsor (Pfizer) together with members of the PROFILE 1007 steering committee.
Blackhall 2014 described the results of a post hoc analysis of the RCT by Shaw (2013). In this article, the results on patients’ quality of life, measured with the EuroQol questionnaire (EQ5D) and EORTC QLQ-C30, were reported.
Solomon (2014) reported on a randomized, open-label, phase 3 study (PROFILE 1014) comparing crizotinib 250 mg twice daily (N=171) with chemotherapy (N=169, pemetrexed plus either cisplatin or carboplatin) in patients with previously untreated advanced ALK-positive NSCLC. Outcomes measures were PFS, objective response rate and safety. In 2018, the authors reported on the long-term effects in overall survival, based on data from the PROFILE 1014 trial (Solomon, 2018). Median follow-up duration for OS was approximately 46 months for both arms.
Wu (2018) reported the results of a phase III RCT (PROFILE 1029) in East Asian Patients with ALK-Positive NSCLC without previous systematic treatment. 104 patients were treated with crizotinib, 250 mg twice daily continuously (3-week cycles). 103 patients treated with chemotherapy (Iv pemetrexed 500 mg/m2 plus cisplatin 75 mg/m2 or carboplatin) every 3 weeks (maximum of six cycles). Patients were treated until RECIST-defined disease progression, development of unacceptable toxicity, withdrawal of consent or death.
Shaw (2017) reported on an open-label, phase 3 RCT (ASCEND-5) in 99 centres across 20 countries. Ceritinib (750 mg per day fasted (in 21-day treatment cycles), N=115) was compared with treatment with chemotherapy (N=116, pemetrexed or docetaxel) in patients with ALK-rearranged stage IIIB or IV NSCLC, previously given chemotherapy and crizotinib. Outcome measures were PFS, OS and ORR. Outcomes were assessed both by investigators and by a masked independent review committee (IRC).
Soria (2017) described the results of an open-label, phase 3 study (ASCEND-4) in 134 centres across 28 countries. Treatment with ceritinib was compared with platinum-based chemotherapy (cisplatin, or carboplatin plus pemetrexed) in patients with untreated ALK-rearranged NSCLC. Outcomes measures were PFS, ORR and safety (number of patients with adverse events requiring dose adjustments and number of patients with grade 3 or 4 adverse events suspected to be related to study drug).
Novello (2018) reported the results of a randomized, open-label, phase III trial (ALUR study) in patients with advanced, recurrent, or metastatic ALK-positive NSCLC; two prior lines of systemic therapy (platinum-based doublet chemotherapy and crizotinib). In the trial alectinib 600 mg twice daily (n=72) and chemotherapy (pemetrexed 500 mg/m2 or docetaxel 75 mg/m2, both every 3 weeks, n=35) were compared. Outcome measures were PFS, OS, ORR, and safety.
Study results
Treatment with crizotinib
Pooled data of the studies comparing treatment with crizotinib versus chemotherapy is shown in Figures 1 to 4.
Solomon (2014) reported a higher median PFS after treatment with ceritinib (10.9 months) as compared to treatment with standard chemotherapy (7.0 months, difference 3,9 months). Wu (2018) also reported higher PFS after crizotinib (median 11,1 months) as compared to chemotherapy (median PFS 6.8 months; difference 4.3 months). The pooled results of the two RCTS concerning crizotinib as first line treatment showed a hazard ratio (HR) of 0.43 (95% confidence interval (CI) 0.35 to 0.53) for PFS favouring targeted therapy (Figure 1). Shaw (2013) reported also a higher PFS for crizotinib compared to chemotherapy in patients with progressive disease after one prior platinum-based chemotherapy (difference median PFS 4.7 months, HR= 0.49; 95% CI, 0.37 to 0.64). In the subgroup of patients with brain metastases, comparable hazard ratios were found (Solomon (2014): HR= 0.57; 95% CI 0.35 to 0.93; Wu (2018): HR= 0.50; 95%CI 0.26 to 0.94))
Figure 1 Forest plot Progression free survival crizotinib versus chemotherapy
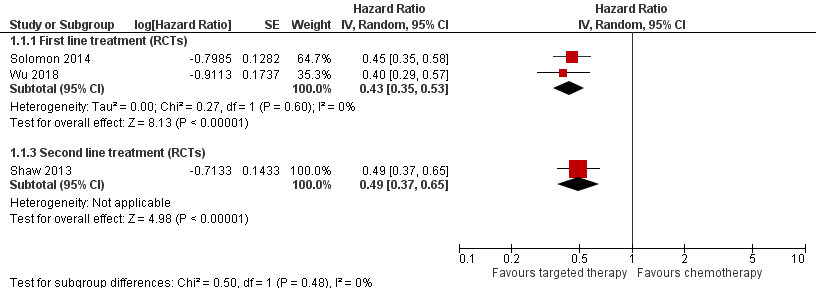
For overall survival, the pooled results of the RCTS investigating first line treatment showed comparable overall survival (hazard ratio of 0.86 (0.69, 1.08) (Figure 2)). In the study by Solomon (2018) the median overall survival was not reached in patients treated with crizotinib. In patients treated with chemotherapy, the median overall survival was 47.5 months. The median follow up duration was 46 months in both groups. Wu (2018) reported comparable median overall survival for patients treated with crizotinib (28.5 months) and chemotherapy (27.7 months). Shaw (2013) reported comparable overall survival for crizotinib compared to chemotherapy in patients with progressive disease after one prior platinum-based chemotherapy (difference median OS 2.5 months, HR=1.02 (95%CI 0.68 to 1.54). However, most patients initially treated with chemotherapy crossed over to crizotinib after discontinuing chemotherapy (64 to 80%).
Figure 2 Forest plot Overall survival Crizotinib versus chemotherapy
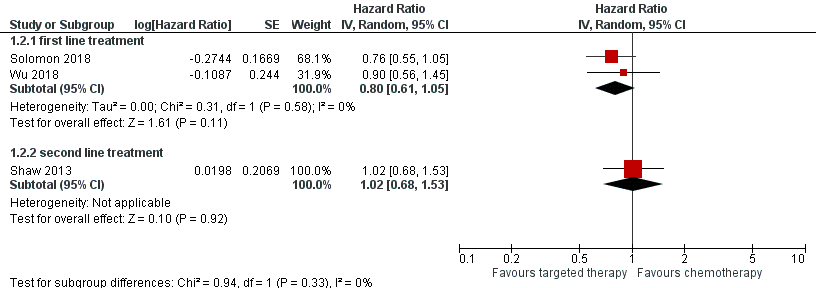
The objective response rate (ORR) was higher in patients treated with crizotinib compared to patients treated with chemotherapy (Figure 3). Combining the results of the two RCTs on first line treatment, resulted in a risk ratio of 1.76 (95%CI 1.52 to 2.03). For second line treatment, Shaw (2013) reported a risk ratio of 3.34 (95%CI 2.43 to 4.61).
Figure 3 Forest plot objective response rate Crizotinib versus chemotherapy
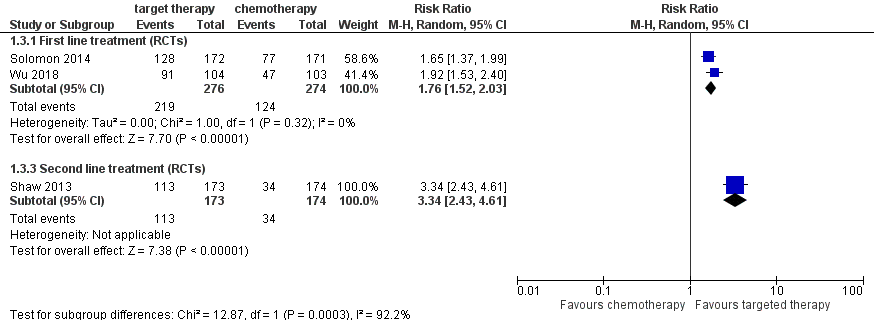
Most studies reported a high number of patients with adverse events. Combining the data from the RCTs, the occurrence of grade 3 or 4 adverse events was 168 in 275 patients treated with crizotinib (61%) and 182 events in 270 patients treated with chemotherapy (67%). In the study by Shaw (2013) (crizotinib as second line treatment) the number of grade 3 or 4 adverse events (all cause) seemed slightly higher in patients treated with crizotinib (83/172=48%) as compared to chemotherapy (68/171=40%) (risk difference =0.08 (95%CI -0.02 to 0.19).
Figure 4 Forest plot Crizotinib versus chemotherapy outcome safety, defined as number of grade 3 or 4 adverse events
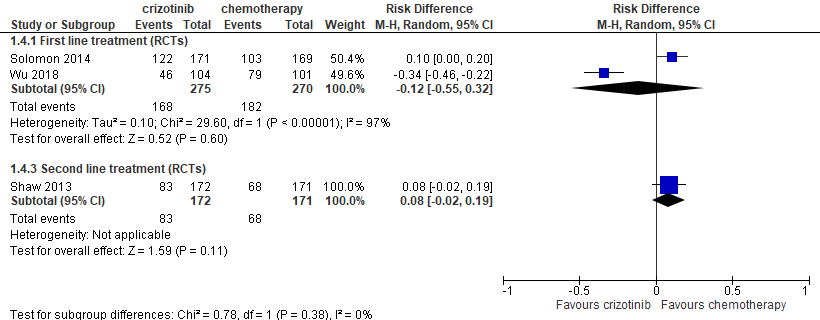
The results on patients’ quality of life were unclear. Blackhall (2014) reported higher mean quality of life scores measured during treatment with crizotinib (mean EuroQol score=0.82, 95%CI (0.79, 0.85)) as compared to chemotherapy (mean EuroQol score =0.73, 95%CI (0.70, 0.77)), but quality of life scores at baseline were also higher in the crizotinib group (Mean EQ5D baseline, crizotinib: 0.73, Chemotherapy 0.70). The mean change in QoL scores per group were not reported. The number of patients with improved quality of life (change 10 points or more) was 73 (42.6%) in the crizotinib group and 35 (12.9%) in the docetaxel group. A change of 10 points is frequently used as a minimally clinical important difference. For the visual analogue scale (VAS) of the EuroQol and the EORTC QLQ-C30 no data per treatment group were reported. The authors concluded “a significant overall improvement from baseline in general health status (EQ-5D VAS) was observed for crizotinib compared with a significant overall deterioration for chemotherapy”. For the EORTC QLQ-C30, they reported “the estimated difference 6.61 (1.81 to 11.39) favouring crizotinib versus pemetrexed and 14.37 (6.19 to 22.54) favouring crizotinib vs docetaxel”. Shaw (2013) and Solomon (2014) suggested a greater reduction from baseline in the symptoms with crizotinib than with chemotherapy. The results, however, were only plotted in a figure. Differences in mean changes in overall quality of life score were not reported.
Treatment with ceritinib
The results of the studies regarding ceritinib versus chemotherapy are shown in Figures 5 to 7. In the study by Soria (2017) the median PFS was 8.5 months longer in patients treated with first line ceritinib as compared to patients treated with chemotherapy (Figure 5) (HR = 0.55 (95% CI 0.42 to 0.73). In the subgroup of patients with brain metastases, no significant difference in PFS was found (HR= 0.70 (95%CI 0.44 to 1.12)) In patients treated with ceritinib as second line treatment (Shaw, 2017), higher PFS were found for ceritinib as compared to chemotherapy (difference in median PFS 3.8 months, HR= 0.49 (95% CI 0.36–0.67)).This difference was also found in the subgroup of patients with brain metastases (HR= 0.50; 95%CI 0.33 to 0.76).
Figure 5 Forest plot Progression free survival ceritinib versus chemotherapy
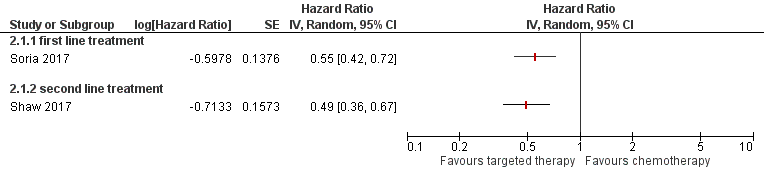
For overall survival, the results showed no difference between the two treatment options (Figure 6). In the study by Soria (2017) the median overall survival was not reached in patients treated with ceritinib. In patients treated with chemotherapy the median overall survival was 26.2 months. Shaw (2017) reported a median overall survival of 18 months in patients treated with ceritinib and 20 months for patients treated with chemotherapy. Many patients initially treated with chemotherapy were treated with ceritinib after discontinuing chemotherapy (65 to 72%).
Figure 6 Forest plot overall survival ceritinib versus chemotherapy
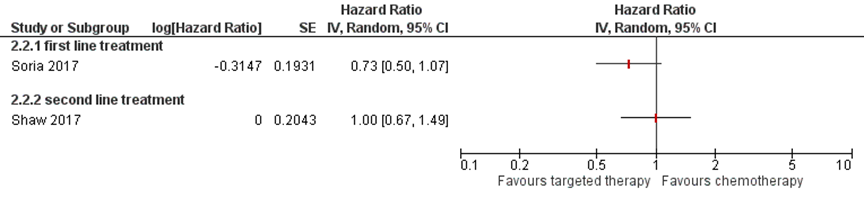
Figure 7 Forest plot objective response rate ceritinib versus chemotherapy

Safety
Adverse events requiring dose adjustment or interruption occurred in 152 (80%) patients treated with ceritinib and in 78 (45%) patients treated with chemotherapy (Soria, 2017) Serious adverse events (grade 3/ 4) suspected to be related to study drug occurred in 123 (65%) patients treated with ceritinib and 70 (40%) patients treated with chemotherapy (Absolute risk increase: 25% 95% CI 15% to 35%; NNH = 4 favouring chemotherapy).
No useful data on patients’ quality of life (QoL) were reported in the included studies. Soria (2017) only reported that lung cancer-specific symptoms and quality of life measures with the EuroQol (EQ-5D-5L) were significantly improved for ceritinib versus chemotherapy. No mean quality of life scores per treatment group were reported; results were only plotted in a figure.
Treatment with alectinib
The median progression free survival (assessed by the Independent Review Committee) was 7.1 months (95% CI: 6.3 to 10.8) in patients treated with alectinib and 1.6 months (95% CI: 1.3 to 4.1) in patients treated with chemotherapy (HR 0.32 (95% CI: 0.17 to 0.59)).
The median overall survival was 12.6 months in the alectinib group (95% CI: 9.7–NR), but was not reached in the chemotherapy group. The hazard ratio showed no difference in overall survival between the two treatment groups (HR 0.89 (95% CI: 0.35 to .24)). 70% of the patients treated with chemotherapy crossed over to alectinib post progression. The investigator-assessed objective response rate (ORR) was 37.5% (27/72 patients;
alectinib) versus 2.9% (1/35 patients; chemotherapy)
Adverse events with grade ≥ 3 occurred in 19 patients treated with alectinib (27.1%) and 14 patients treated with chemotherapy (41.2%) (ARR = 14%, 95% CI (-5.5%, 33.6%); NNT=3, 95%CI (3.0, Infinity))
Level of evidence
There are four levels of evidence: high, moderate, low, and very low. RCTs start at a high level of evidence.
Crizotinib
The levels of evidence for PFS, ORR and OS were downgraded with two levels because of limitations in the study design (Risk of bias, no blinding of patients and physicians and limited information on randomisation method and concealment of allocation) and imprecision (OS: confidence interval crosses threshold for no difference ; PFS/ORR).
The level of evidence for safety was downgraded with two levels because of limitations in the study design (Risk of bias, no blinding and limited information on randomisation method and concealment of allocation) and inconsistency of results (wide variance of point estimates across studies).
The level of evidence for QoL was downgraded with three levels because of limitations in the study design (Risk of bias, no blinding of patients and physicians and limited information on randomisation method and concealment of allocation, unclear report of results) and imprecision (number of patients <2000/ number of events <300).
Ceritinib
The level of evidence for PFS was downgraded with one level because of limitations in the study design (Risk of bias, no blinding of patients and physicians and limited information on concealment of allocation)
The level of evidence for ORR was downgraded with one level because of limitations in the study design (Risk of bias, no blinding of patients and physicians and limited information on concealment of allocation)
The level of evidence for OS was downgraded with two levels because of limitations in the study design (Risk of bias, limited information on randomisation method and concealment of allocation) and imprecision (confidence interval includes no difference)
The level of evidence for safety was downgraded with two levels because of limitations in the study design (Risk of bias, no blinding and limited information on randomisation method) and imprecision (wide variance of point estimates across studies).
Alectinib
The level of evidence for PFS, OS, ORR, safety was downgraded with two levels because of limitations in the study design (Risk of bias, no blinding and limited information on randomisation method and concealment of allocation) and imprecision (number of patients <2000/ number of events <300).
ROS1
Description of studies
There are no prospective randomized controlled trials (RCTs) that compared treatment with targeted therapy and treatment with chemotherapy in NSCLC patients with a ROS1 rearrangement. One retrospective study that compared targeted therapy with chemotherapy was included (Mazieres, 2015). In this study, data from 6 European centers that tested for ROS1 rearrangement were used. Mazieres reported on 31 patients who had received crizotinib use (250 mg two times per day) therapy through an individual off-label for a minimum duration of 2 weeks. The clinical outcome (progression free survival, overall response rate, and toxicity (grade 4 or 5 adverse effects)) during treatment with crizotinib were compared with the outcomes during preceding treatment with chemotherapy. Previous treatments ranged from zero to more than three lines of chemotherapy. 26 patients (84%) had received pemetrexed-based chemotherapy. For toxicity they asked every investigator to retrospectively declare all grade 4 and 5 adverse effects their patients reported while receiving crizotinib.
Study results
The median PFS (months) was 9.1 months (no confidence interval reported) in patients treated with crizotinib and 7.2 (95% CI, 4.8 to 9.6) in patients treated with pemetrexed-based chemotherapy. No statistical testing was reported. The overall response rate was higher in crizotinib treated patients (80%) as compared to patients treated with pemetrexed-based chemotherapy (57.7%, ARR=21.6% (95%CI -2.4% to 45.7%) NNT = 4.6 (95%CI 2.2 to infinity).
No patients treated with crizotinib experienced a grade 4 or 5 adverse event. One patient experienced grade 3 liver toxicity. For chemotherapy no data on toxicity were reported.
Level of evidence
There are four levels of evidence: high, moderate, low, and very low. Observational studies start at a low level of evidence. The level of evidence for all outcome measures was downgraded with 1 level because of limitations in the study design (retrospective design) and imprecision.
RET
Description of studies
There are no prospective randomized controlled trials (RCTs) that compared treatment with targeted therapy and treatment with chemotherapy in NSCLC patients with a RET rearrangement. We included one observational study based on registry data (Gautschi 2017). Data of an international registry of patients with RET rearranged NSCLCs were used. Between Jun2 2015 and April 2016 165 patients from 29 different centers from 12 countries in Europe, Asia, and USA were included. 53 patients used a RET inhibitor (Cabozantinib (n=21), Vandetanib (n=11), Sunitinib (n=10), Sorafenib (n=2), Alectinib (n=2), Lenvatinib (n=2), Nintedanib (n=2), Ponatinib (n=2), Regorafenib (n=1)). 108 patients use first line chemotherapy (Platinum Doublet (n = 84) Platinum + Pemetrexed (n = 66)). Patients treated with a RET inhibitor had on average a higher stage of disease (86% stage IV NSCLC) as compared to the patients not treated with a RET inhibitor (66% stage IV NSCLC) The median line of systemic therapy of the first RET TKI administered was as third line (range, first to eighth line). Data on the response to therapy by RECIST v1.1 were available in 50 patients (94%) treated with a RET inhibitor and 69 (54%) patients treated with chemotherapy.
Study results
The percentage of patients with a complete or partial response to treatment was 26% in the patients treated with targeted therapy and 51% in patients treated with first line platinum-based chemotherapy (95% CI, 38.1 to 63.4). The median progression free survival was 2.3 months (95% CI, 1.6 to 5.0 months) for targeted therapy and 7.8 months for chemotherapy (95% CI, 5.3 to 10.2 months). The HR was not reported. The target therapy, however, was not a first line therapy in many patients. The median line of systemic therapy of the first RET TKI administered was as third line (range, first to eighth line). Therefore, this comparison between target therapy and first line chemotherapy is likely to be biased.
The median overall survival was 6.8 months for targeted therapy (95% CI, 3.9 to 14.3 months) and 24.8 months for chemotherapy (95% CI, 13.6 to 32.3 months). The HR was not reported.
Level of evidence
There are four levels of evidence: high, moderate, low, and very low. Observational studies start at a low level of evidence. The level of evidence for all outcome measures was downgraded with 1 level because of limitations in the study design (retrospective design; patient groups not comparable) and imprecision (small number of patients).
MET
Description of studies
Two RCTs were included in which treatment with the combination of onartuzumab and chemotherapy was compared to treatment with chemotherapy and a placebo (Hirsch, 2017; Wakelee, 2017). The study by Hirsch was a double-blind phase II RCT in patients with stage IIIB or IV NSCLC who were not treated with previous systemic treatment. 55 patients were treated with the combination of onartuzumab plus paclitaxel combined with carboplatin or cisplatin. 27 of these patients had a high MET status, defined as at least 50% of tumor cells stained positive with an intensity of 2+ or greater. 54 patients were treated with placebo plus paclitaxel combined with carboplatin or cisplatin, of whom 27 had high MET status.
The study by Wakelee (2017) was a phase II, randomized, multicenter, double-blind, placebo-controlled study. Both patients with high and low MET status were included but analysed separately. A high MET status was defined as at least 50% of tumour cells stained positive with an intensity of 2+ or greater. Patients received four 3-weekly cycles of either a bevacizumab-based (cohort 1) or a pemetrexed-based (cohort 2) chemotherapy regimen in combination with onartuzumab (15 mg/kg intravenously) or a placebo. Overall, 128 patients were treated with the combination of onartuzumab and chemotherapy, of whom 81 with high MET. 131 patients were treated with chemotherapy and a placebo, of who 81 with high MET.
There are no studies comparing a MET inhibitor to chemotherapy in patients with a MET exon 14 skipping mutation or a high MET gene copy number (GCN).
Study results
The combined results for 108 patients with high MET were treated with onartuzumab + chemotherapy. 108 patients with high MET were treated with chemotherapy and placebo. The pooled progression free survival was not statically significant lower in the subgroup of patients with a high MET status treated with the combination of onartuzumab and chemotherapy as compared to chemotherapy and a placebo (Pooled HR = 1.40, 95%CI 1.00 to 1.95).
Figure 8 Forest plot progression free survival onartuzumab versus chemotherapy in patients with high MET status (IHC 2+ or higher)
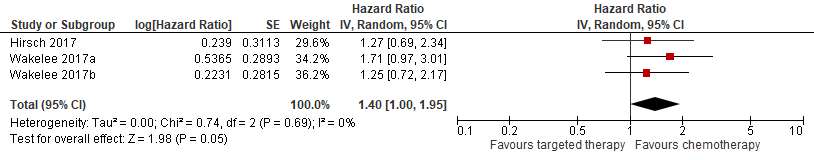
The data for overall survival could not be pooled because hazards ratios were not reported in study by Wakelee (2017). In the study by Hirsch (2017), the median OS was 10.8 months in patients treated with onartuzumab and 7.9 months in patients treated with chemotherapy (HR=0.81, 95%CI 0.40 to 1.64). In the study by Wakelee the median OS was 6 months lower in patients treated with onartuzumab in the first cohort, but comparable in the second cohort of patients. However, data of the uncertainty around these points estimated are not reported.
Level of evidence
There are four levels of evidence: high, moderate, low, and very low. RCTs start at a high level of evidence.
The level of evidence for PFS was downgraded with two levels because of imprecision (confidence interval includes no difference) and limitations in the study design (Risk of bias, no blinding of patients and physicians and limited information on randomisation method and concealment of allocation).
HER2
There are no RCTs or observational studies that compared targeted therapy with chemotherapy in patients with NSCLC and a HER2 mutation.
Zoeken en selecteren
A systematic review of the literature was performed to answer the following question:
Is treatment with targeted therapy preferred above treatment with chemotherapy or best supportive care in patients with advanced NSCLC and a targetable driver mutation?
P (population) patients with non–small-cell lung cancer stage IIIB/IV and a targetable driver mutation/aberration (ALK, ROS1, BRAF, RET, MET, HER2, NTRK or NRG);
I (intervention) targeted therapy (tyrosine kinase inhibitor, crizotinib, ceritinib, alectinib, brigatinib, lorlatinib, entrectinib, dabrafenib, trametinib, vemurafenib, cabozantinib, vandetanib, sunitinib, sorafenib, lenvatinib, nintedanib, ponatinib, regorafenib, capmatinib, afatinib);
C (comparison) chemotherapy or best supportive care;
O (outcome) overall survival, progression free survival, objective response rate, quality of life and adverse events.
Relevant outcome measures
The working group considered overall survival a critical outcome measure for the decision-making process; and progression free survival, response rate, quality of life, safety (adverse events and toxicity) important outcome measures for decision making.
The working group defined clinically relevant difference as follows:
Overall survival: >12 weeks or hazard ratio <0.7
Progression free survival: >12 weeks or hazard ratio <0.7
Adverse events and toxicity: lethal <5%, acute or severe <25%.
For quality of life measured with the EORTC QLQ-C30, a difference of 10 points was considered as a clinical important difference (Fiteni 2016)
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched from 1st of January 2005 up to 10th of July 2018 using relevant search terms for systematic reviews (SRs), randomized controlled trials (RCTs) and observational studies (OBS). The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 793 hits. Studies were selected based on the following criteria: systematic review, randomized trials or cohort studies including patients with non–small-cell lung cancer stage IIIB/IV with one of the selected driver aberrations comparing targeted therapy with chemotherapy. Retrospective studies were excluded, unless no prospective cohort studies or randomised trials were available in a specific population (per aberration). 29 studies were initially selected based on title and abstract. After reading the full text, 18 studies were excluded (see the table with reasons for exclusion under the tab Methods). Four of these excluded studies were systematic reviews (including patients with an ALK or MET aberration) which reported not all relevant data of the individual studies. Therefore, we included the individual studies instead of these four reviews in our own systematic review: two studies concerning patients with a MET aberration and five studies concerning patients with an ALK rearrangement. Finally, four of these additional studies concerning ALK rearrangement were excluded because the study answered another question (Berge, 2013), no comparison with chemotherapy was made (Shaw, 2014), or a retrospective design (Shaw, 2011; Cui, 2016).
Fourteen articles were included in the literature summary. Important study characteristics and results are depicted in the evidence tables. The assessment of the risk of bias is depicted in the risk of bias tables.
Referenties
- 1 - Awad, M. M., G. Leonardi, S. Kravets, and et al. 2017. 'Impact of MET inhibitors on survival among patients (pts) with MET exon 14 mutant (METdel14) non-small cell lung cancer (NSCLC)', J Clin Oncol, 35: 8511.
- 2 - Besse, B., B. Solomon, E. Felip, T. Bauer, S-H. Ignatius Ou, R. Soo, D. Camidge, R. Chiari, S. Gadgeel, G. Riely, E. Tan, H. Hayashi, J. Mazieres, and et al. 2018. 'Lorlatinib in patients (Pts) with previously treated ALK+ advanced non-small cell lung cancer (NSCLC): Updated efficacy and safety.', Journal of Clinical Oncology, 36: abstr 9032.
- 3 - Blackhall, F., Kim D.W., Besse B., et al. Patient-reported outcomes and quality of life in PROFILE 1007: a randomized trial of crizotinib compared with chemotherapy in previously treated patients with ALK-positive advanced non-small-cell lung cancer. J Thorac Oncol. 2014;9(11):1625-33. doi: 10.1097/JTO.0000000000000318.
- 4 - Camidge, D. R., H. R. Kim, M. J. Ahn, J. C. Yang, J. Y. Han, J. S. Lee, M. J. Hochmair, J. Y. Li, G. C. Chang, K. H. Lee, C. Gridelli, A. Delmonte, R. Garcia Campelo, D. W. Kim, A. Bearz, F. Griesinger, A. Morabito, E. Felip, R. Califano, S. Ghosh, A. Spira, S. N. Gettinger, M. Tiseo, N. Gupta, J. Haney, D. Kerstein, and S. Popat. 2018. 'Brigatinib versus Crizotinib in ALK-Positive Non-Small-Cell Lung Cancer', N Engl J Med, 379: 2027-39.
- 5 - Cho B, Drilon A, Doebele R et al. Safety and Preliminary Clinical Activity of Repotrectinib in Patients with Advanced ROS1Fusion-Positive Non-SmallCell Lung Cancer (TRIDENT-1 STUDY), JCO 2019; 37(15):suppl_9011
- 6 - Demetri, G., L. Paz-Ares, A. Farago, Et al. 2018. 'Efficacy and saefty of entrectinib in patients with NTRK fusion-positive tumours: pooled analysis of STARTRK-2, STARTRK-1 and ALKA-372-001', ESMO 2018 conference Munich.
- 7 - Doebele, R., Ahn, M., Siena, S. et al. OA02.01 Efficacy and Safety of Entrectinib in Locally Advanced or Metastatic ROS1 Fusion-Positive Non-Small Cell Lung Cancer (NSCLC). J Thor Oncol 2018; 13(10):S321-322
- 8 - Drilon, A., D. Camidge, S. H. Ou, et al. 2016. 'Efficacy and safety of crizotinib in patients (pts) with advanced MET exon 14-altered non-small cell lung cancer (NSCLC).', J Clin Oncol, 34: 108.
- 9 - Drilon A, Laetsch TW, Kummar S. Efficacy of larotrectinib in TRKfusion-positive cancers in adults and children. N Engl J Med 2018;378:731-9.
- 10 - Felip, E., L. Horn, I. Patel, Et al. 2018. 'Tepotinib in patients with advanced non-small cell lung cancer (NSCLC) harboring MET exon 14-skipping mutations: Phase II trial.', J Clin Oncol, 36: abstr 9016.
- 11 - Fiteni, F., Anota A., Westeel V., Bonnetain F. Methodology of health-related quality of life analysis in phase III advanced non-small-cell lung cancer clinical trials: a critical review. BMC Cancer. 2016 Feb 18;16:122. doi: 10.1186/s12885-016-2152-1.
- 12 - Gautschi, O., Milia J., Filleron T., et al. Targeting RET in Patients With RET-Rearranged Lung Cancers: Results From the Global, Multicenter RET Registry. J Clin Oncol. 2017;35(13):1403-1410. doi: 10.1200/JCO.2016.70.9352.
- 13 - Heymach, J., M. Negrao, J. Robichaux, et al. 2018. 'A phase II trial of poziotinib in EGFR and HER2 exon 20 mutant non-small cell lung cancer (NSCLC).', WCLC, Toronto: Abstract OA02.06.
- 14 - Hirsch, F.R., Govindan R., Zvirbule Z., et al. Efficacy and Safety Results From a Phase II, Placebo-Controlled Study of Onartuzumab Plus First-Line Platinum-Doublet Chemotherapy for Advanced Squamous Cell Non-Small-Cell Lung Cancer. Clin Lung Cancer. 2017;18(1):43-49. doi: 10.1016/j.cllc.2016.05.011.
- 15 - Hyman, D. M., S. A. Piha-Paul, H. Won, J. Rodon, C. Saura, G. I. Shapiro, D. Juric, D. I. Quinn, V. Moreno, B. Doger, I. A. Mayer, V. Boni, E. Calvo, S. Loi, A. C. Lockhart, J. P. Erinjeri, M. Scaltriti, G. A. Ulaner, J. Patel, J. Tang, H. Beer, S. D. Selcuklu, A. J. Hanrahan, N. Bouvier, M. Melcer, R. Murali, A. M. Schram, L. M. Smyth, K. Jhaveri, B. T. Li, A. Drilon, J. J. Harding, G. Iyer, B. S. Taylor, M. F. Berger, R. E. Cutler, Jr., F. Xu, A. Butturini, L. D. Eli, G. Mann, C. Farrell, A. S. Lalani, R. P. Bryce, C. L. Arteaga, F. Meric-Bernstam, J. Baselga, and D. B. Solit. 2018. 'HER kinase inhibition in patients with HER2- and HER3-mutant cancers', Nature, 554: 189-94.
- 16 - Kim, D. W., M. Tiseo, M. J. Ahn, K. L. Reckamp, K. H. Hansen, S. W. Kim, R. M. Huber, H. L. West, H. J. M. Groen, M. J. Hochmair, N. B. Leighl, S. N. Gettinger, C. J. Langer, L. G. Paz-Ares Rodriguez, E. F. Smit, E. S. Kim, W. Reichmann, F. G. Haluska, D. Kerstein, and D. R. Camidge. 2017. 'Brigatinib in Patients With Crizotinib-Refractory Anaplastic Lymphoma Kinase-Positive Non-Small-Cell Lung Cancer: A Randomized, Multicenter Phase II Trial', J Clin Oncol: JCO2016715904.
- 17 - Leonetti, A., Facchinetti, F., Rossi, G. et al. BRAF in non-small cell lung cancer (NSCLC): Pickaxing another brick in the wall. Cancer Treat Rev. 2018 May;66:82-94. doi: 10.1016/j.ctrv.2018.04.006. Epub 2018 Apr 24.
- 18 - Li, B. T., R. Shen, D. Buonocore, Z. T. Olah, A. Ni, M. S. Ginsberg, G. A. Ulaner, M. Offin, D. Feldman, T. Hembrough, F. Cecchi, S. Schwartz, N. Pavlakis, S. Clarke, H. H. Won, E. B. Brzostowski, G. J. Riely, D. B. Solit, D. M. Hyman, A. Drilon, C. M. Rudin, M. F. Berger, J. Baselga, M. Scaltriti, M. E. Arcila, and M. G. Kris. 2018. 'Ado-Trastuzumab Emtansine for Patients With HER2-Mutant Lung Cancers: Results From a Phase II Basket Trial', J Clin Oncol, 36: 2532-37.
- 19 - Li, J., Sasane M., Zhao J., et al. Comparative Efficacy of Treatments for Previously Treated Advanced or Metastatic Non-Small-Cell Lung Cancer: A Network Meta-Analysis. Adv Ther. 2018;35(7):1035-1048. doi: 10.1007/s12325-018-0734-9.
- 20 - Lim, S. M., H. R. Kim, J. S. Lee, K. H. Lee, Y. G. Lee, Y. J. Min, E. K. Cho, S. S. Lee, B. S. Kim, M. Y. Choi, H. S. Shim, J. H. Chung, Y. La Choi, M. J. Lee, M. Kim, J. H. Kim, S. M. Ali, M. J. Ahn, and B. C. Cho. 2017. 'Open-Label, Multicenter, Phase II Study of Ceritinib in Patients With Non-Small-Cell Lung Cancer Harboring ROS1 Rearrangement', J Clin Oncol, 35: 2613-18.
- 21 - Mazières, J., Zalcman G., Crinò L., et al. Crizotinib therapy for advanced lung adenocarcinoma and a ROS1 rearrangement: results from the EUROS1 cohort. J Clin Oncol. 2015;33(9):992-9. doi: 10.1200/JCO.2014.58.3302.
- 22 - Mazieres, J., F. Barlesi, T. Filleron, B. Besse, I. Monnet, M. Beau-Faller, S. Peters, E. Dansin, M. Fruh, M. Pless, R. Rosell, M. Wislez, P. Fournel, V. Westeel, F. Cappuzzo, A. Cortot, D. Moro-Sibilot, J. Milia, and O. Gautschi. 2016. 'Lung cancer patients with HER2 mutations treated with chemotherapy and HER2-targeted drugs: results from the European EUHER2 cohort', Ann Oncol, 27: 281-6.
- 23 - Mazieres, J., G. Zalcman, L. Crino, P. Biondani, F. Barlesi, T. Filleron, A. M. Dingemans, H. Lena, I. Monnet, S. I. Rothschild, F. Cappuzzo, B. Besse, L. Thiberville, D. Rouviere, R. Dziadziuszko, E. F. Smit, J. Wolf, C. Spirig, N. Pecuchet, F. Leenders, J. M. Heuckmann, J. Diebold, J. D. Milia, R. K. Thomas, and O. Gautschi. 2015. 'Crizotinib therapy for advanced lung adenocarcinoma and a ROS1 rearrangement: results from the EUROS1 cohort', J Clin Oncol, 33: 992-9.
- 24 - Novello, S., Mazières J., Oh I.J., et al. Alectinib versus chemotherapy in crizotinib-pretreated anaplastic lymphoma kinase (ALK)-positive non-small-cell lung cancer: results from the phase III ALUR study. Ann Oncol. 2018;29(6):1409-1416. doi: 10.1093/annonc/mdy121
- 25 - Oxnard, G. R., V. subbiah, K. Park, T. Bauer, J. Wirth, V. Velcheti, and et al. 2018. 'OA12.07 - Clinical Activity of LOXO-292, a Highly Selective RET Inhibitor, in Patients with RET Fusion+ Non-Small Cell Lung Cancer ', WCLC, Toronto: abstr OA12.07.
- 26 - Peters, S., D. R. Camidge, A. T. Shaw, S. Gadgeel, J. S. Ahn, D. W. Kim, S. I. Ou, M. Perol, R. Dziadziuszko, R. Rosell, A. Zeaiter, E. Mitry, S. Golding, B. Balas, J. Noe, P. N. Morcos, T. Mok, and Alex Trial Investigators. 2017. 'Alectinib versus Crizotinib in Untreated ALK-Positive Non-Small-Cell Lung Cancer', N Engl J Med.
- 27 - Planchard, D., B. Besse, H. J. M. Groen, P. J. Souquet, E. Quoix, C. S. Baik, F. Barlesi, T. M. Kim, J. Mazieres, S. Novello, J. R. Rigas, A. Upalawanna, A. M. D'Amelio, Jr., P. Zhang, B. Mookerjee, and B. E. Johnson. 2016. 'Dabrafenib plus trametinib in patients with previously treated BRAF(V600E)-mutant metastatic non-small cell lung cancer: an open-label, multicentre phase 2 trial', Lancet Oncol, 17: 984-93.
- 28 - Planchard, D., T. M. Kim, J. Mazieres, E. Quoix, G. Riely, F. Barlesi, P. J. Souquet, E. F. Smit, H. J. Groen, R. J. Kelly, B. C. Cho, M. A. Socinski, L. Pandite, C. Nase, B. Ma, A. D'Amelio, Jr., B. Mookerjee, C. M. Curtis, Jr., and B. E. Johnson. 2016. 'Dabrafenib in patients with BRAF(V600E)-positive advanced non-small-cell lung cancer: a single-arm, multicentre, open-label, phase 2 trial', Lancet Oncol, 17: 642-50.
- 29 - Planchard, D., E. F. Smit, H. J. M. Groen, J. Mazieres, B. Besse, A. Helland, V. Giannone, A. M. D'Amelio, Jr., P. Zhang, B. Mookerjee, and B. E. Johnson. 2017. 'Dabrafenib plus trametinib in patients with previously untreated BRAF(V600E)-mutant metastatic non-small-cell lung cancer: an open-label, phase 2 trial', Lancet Oncol, 18: 1307-16.
- 30 - Remon, J., and B. Besse. 2018. 'Brain Metastases in Oncogene-Addicted Non-Small Cell Lung Cancer Patients: Incidence and Treatment', Front Oncol, 8: 88.
- 31 - Shaw, A. T., S. H. Ou, Y. J. Bang, D. R. Camidge, B. J. Solomon, R. Salgia, G. J. Riely, M. Varella-Garcia, G. I. Shapiro, D. B. Costa, R. C. Doebele, L. P. Le, Z. Zheng, W. Tan, P. Stephenson, S. M. Shreeve, L. M. Tye, J. G. Christensen, K. D. Wilner, J. W. Clark, and A. J. Iafrate. 2014. 'Crizotinib in ROS1-rearranged non-small-cell lung cancer', N Engl J Med, 371: 1963-71.
- 32 - Shaw, A.T., Kim D.W., Nakagawa K., et al. Crizotinib versus chemotherapy in advanced ALK-positive lung cancer. N Engl J Med. 2013;368(25):2385-94. doi: 10.1056/NEJMoa1214886.
- 33 - Shaw, A.T., Kim D.W., Mehra R., et al. Ceritinib in ALK-rearranged non-small-cell lung cancer. N Engl J Med. 2014;370(13):1189-97. doi: 10.1056/NEJMoa1311107.
- 34 - Shaw, A.T., Kim T.M., Crinò L., et al. Ceritinib versus chemotherapy in patients with ALK-rearranged non-small-cell lung cancer previously given chemotherapy and crizotinib (ASCEND-5): a randomised, controlled, open-label, phase 3 trial. Lancet Oncol. 2017;18(7):874-886. doi: 10.1016/S1470-2045(17)30339-X
- 35 - Shaw, A.T., Felip E., Bauer, T.M. et al. Lorlatinib in non-small-cell lung cancer with ALK or ROS1 rearrangement: an international, multicentre, open-label, single-arm first-in-man phase 1 trial. Lancet Oncol. 2017 Dec;18(12):1590-1599. doi: 10.1016/S1470-2045(17)30680-0. Epub 2017 Oct 23
- 36 - Smit, E., S. Peters, R. Dziadziuszko, and et al. 2017. 'A single-arm phase II trial of afatinib in pretreated patients with advanced NSCLC harboring a HER2 mutation: the ETOP NICHE trial', J Clin Oncol, 35: 9070.
- 37 - Solomon, B. J., B. Besse, T. M. Bauer, E. Felip, R. A. Soo, D. R. Camidge, R. Chiari, A. Bearz, C. C. Lin, S. M. Gadgeel, G. J. Riely, E. H. Tan, T. Seto, L. P. James, J. S. Clancy, A. Abbattista, J. F. Martini, J. Chen, G. Peltz, H. Thurm, S. H. Ignatius Ou, and A. T. Shaw. 2018. 'Lorlatinib in patients with ALK-positive non-small-cell lung cancer: results from a global phase 2 study', Lancet Oncol, 19: 1654-67.
- 38 - Solomon, B.J., Mok T., Kim D.W., et al. First-line crizotinib versus chemotherapy in ALK-positive lung cancer. N Engl J Med. 2014 Dec 4;371(23):2167-77. doi: 10.1056/NEJMoa1408440. Solomon B.J., Kim D.W., Wu Y.L., et al. Final Overall Survival Analysis From a Study Comparing First-Line Crizotinib Versus Chemotherapy in ALK-Mutation-Positive Non-Small-Cell Lung Cancer. J Clin Oncol. 2018;36(22):2251-2258. doi: 10.1200/JCO.2017.77.4794.
- 39 - Soria, J.C., Tan D.S.W., Chiari R., et al. First-line ceritinib versus platinum-based chemotherapy in advanced ALK-rearranged non-small-cell lung cancer (ASCEND-4): a randomised, open-label, phase 3 study. Lancet. 2017;389(10072):917-929. doi: 10.1016/S0140-6736(17)30123-X.
- 40 - Stinchcombe, T., R. Stahel, L. Bubendorf, and Et al. 2017. 'Efficacy, safety, and biomarker results of trastuzumab emtansine (T-DM1) in patients (pts) with previously treated HER2-overexpressing locally advanced or metastatic non-small cell lung cancer (mNSCLC).', J Clin Oncol, 35: 8509.
- 41 - Subbiah, V., M. Taylor, J. J. Lin, and et al. 2018. 'Highly potent and selective RET inhibitor, BLU-667, achieves proof of concept in a phase I study of advanced, RET-altered solid tumors', AACR Annual Meeting 2018: Abstract CT043.
- 42 - Wakelee, H., Zvirbule Z., De Braud F., et al. Efficacy and Safety of Onartuzumab in Combination With First-Line Bevacizumab-or Pemetrexed-Based Chemotherapy Regimens in Advanced Non-Squamous Non-Small-Cell Lung Cancer. Clin Lung Cancer. 2017;18(1):50-59. doi: 10.1016/j.cllc.2016.09.013.
- 43 - Wolf, J., T. Seto, J. Han, N. Reguart, and Et al. 2018. 'Results of the GEOMETRY mono-1 phase II study for evaluation of the MET inhibitor capmatinib (INC280) in patients (pts) with MET ex14 mutated advanced NSCLC', ESMO 2018 conference Munich.
- 44 - Wu, Y.L., Lu S., Lu Y., et al. Results of PROFILE 1029, a Phase III Comparison of First-Line Crizotinib versus Chemotherapy in East Asian Patients with ALK-Positive Advanced Non-Small Cell Lung Cancer. J Thorac Oncol. 2018. pii: S1556-0864(18)30721-4. doi: 10.1016/j.jtho.2018.06.012.
Evidence tabellen
Evidence table for intervention studies UV4
PFS=progression free survival, ORR = Objective response rate (=proportion of patients with tumor size reduction of a predefined amount and for a minimum time period., QoL = quality of life; 95%CI=95% confidence interval; AEs = adverse events, HR=hazard ratio
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Kim 2017 |
Original studies included (Limited information on included studies and risk of bias) |
|
Li 2017 |
Original studies included (Limited information on included studies and risk of bias) |
|
Lin 2017 |
Original studies included (Limited information on included studies and risk of bias) |
|
Wang 2017 |
Original studies included (Limited information on included studies and risk of bias) |
|
Ye 2016 |
Meeste geincludeerde studies niet relevant voor PICO; relevante studies originieel geincludeerd |
|
Costa 2018 |
Geen vergelijking |
|
Cui 2016 |
Retrospective study |
|
Fan 2018 |
Geen vergelijking |
|
Hu 2016 |
Geen vergelijking |
|
O’Bryant 2013 |
Narrative review |
|
Pellegrino 2018 |
Geen vergelijking |
|
Qian 2014 |
Geen vergelijking |
|
Verstergaard 2018 |
Zowel vergelijkende als niet vergelijkende studies |
|
Zhang 2017 |
Niet relevante vergelijking voor PICO |
|
Zhu 2017 |
RCTs included but no results reported from the control group |
|
Berge 2013 |
Niet relevant voor PICO (andere vergelijking) |
|
Esfahani 2014 |
Narrative review |
|
Kiura 2018 |
Overlap met Shaw 2017 |
|
Morgan 2017 |
Geen klinische studie |
|
Scagliotti 2015 |
Andere vraagstelling |
|
Shaw 2011 |
Retrospective study |
|
Shaw 2014 |
Geen vergelijkende studie |
|
Solomon 2016 |
Overlap met Solomon 2014 |
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 24-01-2020
Laatst geautoriseerd : 24-01-2020
Geplande herbeoordeling :
Bij het opstellen van de modules heeft de werkgroep een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijnmodule komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten. De geldigheid is per module weergegeven.
|
Module |
Regiehouder(s) |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn |
Frequentie van beoordeling op actualiteit |
Wie houdt er toezicht op actualiteit |
Relevante factoren voor wijzigingen in aanbeveling |
|
Behandeling zeldzame mutaties |
NVALT |
2019 |
2020 |
Jaarlijks |
NVALT |
Nieuwe medicatie gericht op zeldzame mutaties beschikbaar |
Bij ALK zal de komende jaren meer duidelijkheid komen over wat de beste behandelstrategie is, en wat de beste behandeling is per gevonden resistentiepatroon. Voor de overige drivers zullen de komende jaren meer studies beschikbaar komen met next generation TKI, of combinaties van TKIs. Gezien de activiteit in het veld zal de actualiteit van deze module minimaal ieder jaar bekeken moeten worden.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financierder heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Samenstelling werkgroep
Werkgroep
- Dr. I. Bahce, longarts, Nederlandse Vereniging van Artsen voor Longziekten en TBC
- Drs. N.J.M Claessens, longarts, Nederlandse Vereniging van Artsen voor Longziekten en TBC
- Prof. dr. E.F.I. Comans, Nucleaire geneeskundige, Nederlandse Vereniging voor Nucleaire Geneeskunde
- Dr. W.A. Draaisma, chirurg, Nederlandse Vereniging voor Heelkunde (tot 1 december 2018)
- Dr. W.H. van Geffen, longarts, Nederlandse Vereniging van Artsen voor Longziekten en TBC
- Dr. K.J. Hartemink, chirurg, Nederlandse Vereniging voor Heelkunde (vanaf 1 december 2018)
- Dr. L.E.L. Hendriks, longarts, Nederlandse Vereniging van Artsen voor Longziekten en TBC
- Prof. dr. D. de Ruysscher, Radiotherapeut, Nederlandse Vereniging voor Radiotherapie en Oncologie
- Dr. C. Schaefer-Prokop, radioloog, Nederlandse Vereniging voor Radiologie
- Dr. J.H. Schouwink, longarts, Nederlandse Vereniging van Artsen voor Longziekten en TBC (voorzitter)
- Prof. dr. E.M.D. Schuuring, Klinisch Moleculair Bioloog in de Pathologie, Nederlandse Vereniging voor Pathologie
- Dr. E. Thunnissen, patholoog, Nederlandse Vereniging voor Pathologie
- Dr. J.H. von der Thüsen, patholoog, Nederlandse Vereniging voor Pathologie
- Prof. dr. A.F.T.M. Verhagen, cardio-thoracaal chirurg, Nederlandse Vereniging voor Thoraxchirurgie
- Dr. A.J. van der Wekken, longarts, Nederlandse Vereniging van Artsen voor Longziekten en TBC (vice-voorzitter)
Met ondersteuning van
- Dr. M. Moret-Hartman, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. S.N. Hofstede, adviseur, Kennisinstituut van de Federatie Medische Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in de onderstaande tabel met gemelde belangen. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Gezien een substantieel aantal van de werkgroepleden functies of werkzaamheden heeft die een mogelijke verstrengeling van belangen met zich meebrengen, zijn een aantal afspraken gemaakt over de werkwijze. Besproken is of het mogelijk was de deelname aan adviesraden voor de farmaceutische industrie stop te zetten gedurende de looptijd van het project. Dit werd echter onhaalbaar geacht, omdat de informatie uit de bijeenkomsten voor hen belangrijk werd geacht voor goede patiëntenzorg waarbij recente ontwikkelingen worden meegenomen. Aangezien een groot aantal werkgroepleden een potentiele verstrengeling van belangen heeft, bleek het onhaalbaar om tijdens het bespreken van aanbevelingen de werkgroepleden met mogelijke belangen te vragen de zaal te verlaten, omdat er dan slechts een klein aantal werkgroepleden zou overblijven. Daarom is besloten om overwegingen en aanbevelingen te formuleren tijdens een vergadering met de gehele werkgroep. De adviseurs hebben kritisch meegekeken bij de definitieve selectie van abstracts. Tot slot is een nieuwe voorzitter gezocht die geen bezwaar had tegen het opschorten van werkzaamheden voor de farmaceutische industrie gedurende de looptijd van het richtlijnproject. De oorspronkelijk beoogde voorzitter is als vice-voorzitter benoemd.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Bahce |
longarts |
geen |
Participeert incidenteel en op uitnodiging in adviesraden en nascholingen bij diverse farmaceutische bedrijven, te weten Boehringer Ingelheim, AstraZeneca, BMS, Roche.
voert als hoofdonderzoeker investigator-initiated onderzoek uit met sponsoring van Boehringer Ingelheim (18F-Afatinib-PET) en AstraZeneca (89Zr-durvalumab-PET) |
Aangezien een groot aantal werkgroepleden een potentiele verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Hendriks |
longarts |
t/m 31/10/18 postdoc lnstitut Gustave Roussy, Villejuif, Frankrijk |
bezig om een studie op te zetten die veranderingen neurocognitie na cerebrale bestraling concurrent met een tyrosine kinase inhibitor bij niet-kleincellig longkanker patiënten onderzoekt. We zijn bezig funding te zoeken, bedoeling is geld vanuit de industrie te krijgen: voor iedere TKI hebben we de betreffende firma benaderd (industrie heeft geen invloed op het studieprotocol of de analyse/publicatie van de resultaten)
subsidie bij de industrie aangevraagd om psychische belasting te onderzoeken bij patienten die weten dat ze (asymptomatische) hersenmetastasen hebben. Roche heeft een grant toegezegd
funding gekregen van Roche om vermoeidheid na prophylactische schedelbestraling bij SCLC patiënten te onderzoeken (geen bemoeienis met protocol, analyse of publiceren van de resultaten)
neemt af en toe deel aan adviesraad van BMS (nivolumab) en Boehringer lngelheim (afatinib), betaald (instituut); van meerdere industrieen (Pfizer, Amgen, Boehringer lngelheim) in 2016 financiële support gekregen voor drukken proefschrift (hersenmetastasen bij longkanker). Voor AstraZeneca een stukje over mijn proefschrift voor hun website geschreven; voor SMS heb ik een voordracht gehouden. Van Roche, SMS, MSD en AstraZeneca financiele compensatie gekregen voor het houden van lezingen over longkanker |
Aangezien een groot aantal werkgroepleden een potentiele verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Comans |
Nucleaire geneeskundige |
geen |
geen |
geen |
|
Draaisma |
chirurg |
geen |
geen |
geen |
|
Van Geffen |
longarts |
Editorial board Cochrane Airways: Onbetaald
Commisie Bronkhorst Nvalt: Onbetaald
|
Deelname aan een investigator initiated onderzoek naar COPD firma Novartis. financiering is overgemaakt aan UMCG; Voor de bedrijven Chiesi, Boehringer en AstraZeneca deelname aan adviesraden. De hiervoor gebruikelijke CGR vergoeding wordt door geweigerd. Reiskosten worden wel vergoed. |
Aangezien een groot aantal werkgroepleden een potentiele verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Hartemink |
chirurg |
"Faculty NVALT cursus oncologie voor de longarts Bestuurslid tumorwerkgroep thoracale oncologie AvL commissielid "Kwaliteit" longchirurgijn Nederland Specialisten adviesraad longkanker Nederland Commissielid Wetenschap DLCA-S Bestuurslid PLCRG (research longkanker)" |
Diverse studies die de rol van neo adjuvante immunotherapie bij stadium I, II en III NSCLC onderzoeken |
Aangezien een groot aantal werkgroepleden een potentiele verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Claessens |
longarts |
Lid sectie oncologie NVALT - onbetaald Incidenteel adviesraad Astra Zeneca - betaald Gelegenheidsredacteur iPulmonologist - betaald Bestuurslid Holland-Stellenbosch Medical Foundation - onbetaald |
Binnen ons ziekenhuis nemen wij deel en hebben wij deelgenomen aan verscheidende industrie-gedreven klinische trials, onder andere van Astra Zeneca, MSD, BMS, Eli-Lilly en regeneron. Hierbij bestond er onzerzijds geen persoonlijk financieel belang. |
Aangezien een groot aantal werkgroepleden een potentiele verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
De Ruysscher |
radiotherapeut |
Hoogleraar Radiotherapie-Oncologie KU Leuven, België. Betaald. |
Onderzoek gefinancierd door Bristol-Myers-Squibb (principal investigator). |
Aangezien een groot aantal werkgroepleden een potentiele verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Schaefer-Prokop |
radioloog |
|
geen |
geen |
|
Schouwink |
longarts |
Voorzitter bestuur Emil starkenstein Stichting, onbezoldigd |
Hij heeft in het verleden (2015, 2016) tweemaal deelgenomen aan een adviesraad. |
Afgesproken om gedurende het project deelname aan adviesraden stop te zetten. |
|
Schuuring |
Klinisch Moleculair Bioloog in de Pathologie |
"Adviseur/KMBP voor Moleculaire Pathologie voor de Stichting Pathologie Friesland in Leeuwarden (onbetaald)
Adviseur/KMBP voor Moleculaire Pathologie voor Martini Ziekenhuis te Groningen (onbetaald)
Adviseur/KMBP voor Moleculaire Pathologie voor Treant Zorggroep Bethesda ziekenhuis in Hoogeveen (onbetaald)
Adviseur/KMBP voor Moleculaire Pathologie voor Pathologie van Isala in Zwolle (onbetaald)
Bestuurslid van de NVVP (Nederlandse Vereniging voor Pathologie) (onbetaald)
Bestuurslid/voorzitter van de NVVP-sectie Klinische Moleculaire Experimentele Pathologie (onbetaald)
Lid stuurgroep ZONMW-PATH: “Optimising Access to Personalised Cancer Therapy in the Netherlands; from Tissue to Therapy” (https://www.netwerk-path.nl/) (onbetaald)
Scientific Advisory Board. ESP-Quality Control committee (onbetaald)" |
Adviseur/consultant met betrekking tot (moleculaire) diagnostiek voor longkanker (en andere maligniteiten) voor de firma's AstraZeneca, Roche, Pfizer, Bayer, Novartis, BMS, BioRad, Amgen, Illumina, Ageno BioSciences, Janssen Cilag (Johnson&Johnson), BioCartis (honoraria komen op een rekening op UMCG) Adviseur/scientific expert voor organisatie van (inter)nationale ringstudies voor weefsel en plasma tbv diagnostiek van longkanker (External Quality Assessment) voor de European Society of Pathology (ESP) en overkoepelende IQNPATH
lezingen, onderwijs, nascholing op het gebied van de moleculaire pathologie van longkanker deels tegen vergoeding van firma zoals AstraZeneca, Roche, Pfizer, Novartis, BioRad, Illumina, BioCartis (honoraria komen op een rekening op UMCG)
financiële ondersteuning voor onderzoek ontvangen van (als PI verantwoordelijk voor een workpackage (onderdeel) van het project) betaald aan UMCG: Boehringer Ingelheim, Avenio/Roche/Cancer-ID, BMS (CA209-759), BioRad and Avenio - |
Aangezien een groot aantal werkgroepleden een potentiele verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Thunnissen |
patholoog |
histogenex, consultant long pathologie; training onder andere PD-L1. bezoldigd |
Investigator initiated research Pfizer naar ALK IHC+ m+ NSCLC (principal investigator)
advisory board bij farmaceutische industrie in verleden (MSD, Pfizer, Clovis, BMS, AstraZeneca, Amgen, Diaceutics, Abbvie,) bezoldigd tegen standaard tarief.
Adviseur UKNEQAS= organisation for external quality assurance in UK (onbezoldigd)" |
Aangezien een groot aantal werkgroepleden een potentiele verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Von der Thüsen |
patholoog |
|
deelname advisory boards: AbbVie BMS MSD Roche" |
Aangezien een groot aantal werkgroepleden een potentiele verstrengeling van belangen heeft, is besloten dat het niet werkbaar is het werkgroeplid uit te sluiten als trekker of uit te sluiten bij het formuleren van overwegingen en aanbevelingen. Besloten is aanbevelingen zoveel mogelijk te formuleren tijdens een werkgroepvergadering. |
|
Verhagen |
Cardio-thoracaal chirurg |
|
geen |
geen |
|
van der Wekken |
longarts |
|
Deelname aan eenmalige adviesraden voor: AstraZeneca, BMS, Roche, MSD, Pfizer, Boehringer-Ingelheim (geld gaat naar UMCG)
lectures voor AstraZeneca, Roche, BMS, Novartis, Pfizer, Boehringer-Ingelheim (geld gaat naar UMCG)
"Research grant voor investigator initiated study door AstraZeneca voor indicatie die niets met de huidige richtlijn ontwikkeling te maken heeft (geld gaat naar UMCG)
De afdeling longoncologie doet mee aan verschillende internationale onderzoeken, die betaald worden aan het UMCG door BMS, MSD, Roche, Novartis, AbbVie, Boehringer-Ingelheim, Pfizer, ARIAD (Takeda)." |
In verband met gemelde belangen is gezocht naar een nieuwe voorzitter zonder potentiële verstrengeling van belangen. Van de Wekken is vice-voorzitter die onder andere vergaderingen leidt. Schouwink zal onder andere zorgvuldigheid tijdens proces van formuleren van aanbevelingen bewaken. |
|
Moret-Hartman |
adviseur richtlijnontwikkeling |
geen |
getrouwd met praktijkhoudend huisarts |
geen |
|
Hofstede |
adviseur richtlijnontwikkeling |
geen |
geen |
geen |
Inbreng patiëntenperspectief
Er is een focusgroepbijeenkomst georganiseerd om knelpunten en aandachtspunten voor goede zorg te inventariseren bij patiënten met niet-kleincellig longcarcinoom. Een verslag hiervan (zie aanverwante producten) is besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de module. Longkanker Nederland heeft ook deelgenomen aan de Invitational conference. De conceptmodules zijn tevens voor commentaar voorgelegd aan de deelnemers van de focusgroep en de patiëntenvereniging Longkanker Nederland.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van het ontwikkelproces is rekening gehouden met de implementatie van de richtlijnmodule en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de module in de praktijk kunnen bevorderen of belemmeren. De implementatietabel is te vinden bij de aanverwante producten. De werkgroep heeft geen interne kwaliteitsindicatoren ontwikkeld, omdat dit proces reeds is verankerd in de kwaliteitsregistratie longkanker (https://dica.nl/).
Werkwijze
AGREE
Deze module is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based module tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Uit de inventarisatie van de knelpunten door Sectie oncologie van de NVALT (SON) dat er een noodzaak was voor de herziening van de richtlijn niet-kleincellig longcarcinoom. Tijdens een invitational conference zijn er knelpunten aangedragen door Longkanker Nederland, de Inspectie Gezondheidszorg en Jeugd (IGJ), de Nederlandse Associatie Physician Assistants (NAPA), de Vereniging Innovatieve Geneesmiddelen (VIG) en de Nederlandse Vereniging van Ziekenhuisapothekers (NVZA). Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvraag en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse is door de werkgroepleden en de adviseur een uitgangsvraag opgesteld. Vervolgens inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden. Bij het vaststellen van welke verschil klinisch relevant is, heeft de werkgroep zich laten inspireren door de PASKWIL-criteria. De werkgroep is zich ervan bewust dat deze criteria zijn ontwikkeld voor de beoordeling van geneesmiddelen in de palliatieve setting en niet voor een curatieve setting.
Strategie voor zoeken en selecteren van literatuur
Aan de hand van specifieke zoektermen werd gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De geselecteerde databases waarin is gezocht en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie is opvraagbaar bij de Richtlijnendatabase, zie het tabblad ‘Zoekverantwoording’ voor verdere details.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration:
- AMSTAR – voor systematische reviews.
- Cochrane – voor gerandomiseerd gecontroleerd onderzoek.
- ACROBAT-NRS – voor observationeel onderzoek.
- QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Indien van toepassing: Bij voldoende studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, matig, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt, kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
Bij de ontwikkeling van de module is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag, randvoorwaarden die van invloed zijn op de implementatie van de aanbeveling zijn opgenomen in de implementatietabel.
Kennislacunes
Tijdens de ontwikkeling van deze module is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvraag. Er is nagegaan of (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Mocht dit bij deze module het geval zijn, dan is er een aanbeveling voor het doen van onderzoek opgenomen in de Kennislacunes. Deze zijn te vinden onder de aanverwante producten.
Commentaar- en autorisatiefase
De conceptmodules zijn aan de betrokken (wetenschappelijke) verenigingen, instanties en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren zijn de conceptmodules aangepast en definitief vastgesteld door de werkgroep. De definitieve modules zijn aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd. De commentaartabel is op te vragen bij het Kennisinstituut via secretariaat@kennisinstituut.nl
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site.html
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van de Federatie Medisch Specialisten.
Zoekverantwoording
Zoekacties zijn opvraagbaar. Neem hiervoor contact op met de Richtlijnendatabase.
