Op- en afschaling binnen chronische pijn zorg
Uitgangsvraag
Welke criteria kunnen gebruikt worden bij de opschaling en afschaling binnen de eerste, tweede en derdelijn van patiënten met chronische pijn?
Aanbeveling
Bied de meest effectieve behandeling aan op de juiste plaats, passend bij de aard en ernst van het probleem en context. Pas zo veel mogelijk de principes van ‘samen beslissen’ toe.
Overweeg in samenspraak met de patiënt opschaling naar een hoger echeleon bij één of meer van deze factoren:
- De juiste pijndiagnose of verklaring kan niet worden gesteld of worden gevonden en aanvullend onderzoek, advies en/of expertise is nodig (inclusief second en third opinion);
- De complexiteit van de klachten van de patiënt is te hoog (teveel onderhoudende beïnvloedende factoren die de pijn en functioneren negatief beïnvloeden en niet zelf kunnen worden behandeld);
- Verwachte reductie in pijn en verhoging van functioneren blijven uit/ ingezette therapie niet effectief en geen alternatieve mogelijkheden binnen huidige echelon;
- Er is geen aansluiting bij de hulpvraag, behoefte en/of waarde van de patiënt.
Overweeg in samenspraak met de patiënt de zorg af te schalen naar een lager echeleon indien er sprake is van één of meer van deze factoren:
- er is een adequate pijndiagnose gesteld, er is inzicht in de onderhoudende beïnvloedende factoren (bio-psycho-sociaal; en
- er is een effectieve, minder belastende, goedkopere of korte vorm van behandeling mogelijk in een lagere lijn; of
- de ingezette therapie is niet effectief en er is geen alternatief binnen competenties; of
- er is geen aansluiting bij de hulpvraag, behoefte of waarden van de patiënt.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er werden zeven publicaties die vijf RCTs beschreven geïncludeerd. Deze studies vergeleken uitkomsten na risico-gestratificeerde zorg (waarbij in de meeste gevallen de STarT Back voor risicostratificatie werd gebruikt) met uitkomsten na standaard zorg. Het is mogelijk dat de resultaten ook afhankelijk zijn van de eventueel ingezette behandeling na risicostratificatie.
De studies werden uitgevoerd bij patiënten met aspecifieke lage rugpijn (Cherkin, 2018; Hill, 2011 & Whitehurst, 2012; Jamal, 2020), bij patiënten met ischias (Foster, 2020 & Konstantinou, 2020) en bij patiënten met musculoskeletale pijn (Hill, 2020). Er werden geen studies gevonden die opschaling en afschalingscriteria op een andere manier toepasten dan risico-stratificering op baseline of in andere patiëntengroepen. Patiënten met psychiatrische en/of somatische comorbiditeit waren in veel van de studies uitgesloten van deelname.
De cruciale uitkomstmaten ‘kwaliteit van leven’ en ‘patiënttevredenheid’ werden beschreven door de geïncludeerde studies. Er werden geen klinisch relevante verschillen gevonden in de risico-gestratificeerde groep in vergelijking met standaard zorg. Vanwege beperkingen in studieopzet, het relatief lage aantal patiënten en inconsistente studieresultaten was de bewijskracht zeer laag. Op basis van de cruciale uitkomstmaten kan geen voorkeur worden gegeven voor risico-gestratificeerde zorg of standaard zorg.
De belangrijke uitkomstmaten ‘fysiek functioneren’ en ‘kosteneffectiviteit’ werden beschreven door de geïncludeerde studies. De bewijskracht werd verlaagd gezien de beperkingen in de onderzoeksopzet, inconsistente studieresultaten en het geringe aantal patiënten. Ook voor deze uitkomstmaten is de bewijskracht zeer laag.
Enkele studies rapporteerden subgroep resultaten voor laag- matig- en hoog-risicogroepen zoals ingedeeld op baseline. De resultaten in hoog-risicopatiënten wijzen erop dat fysiek functioneren (op basis van de rug-gerelateerde RMDQ-score) mogelijk beter is na risico-gestratificeerde zorg dan na standaard zorg. De resultaten in de laag- en matig-risicogroepen wisselden, waardoor op basis van de literatuur geen uitspraak gedaan kan worden over het effect van risico-gestratificeerde zorg in vergelijking met standaard zorg op fysiek functioneren in deze subgroepen.
De belangrijke uitkomstmaat ‘duur van de behandeling’ werd niet beschreven door de geïncludeerde studies.
Op basis van de gevonden literatuur is het onduidelijk of het toepassen van specifieke op- en afschalingcriteria bij patiënten met chronische pijn meerwaarde heeft. Naast de in de literatuuranalyse beschreven resultaten, zijn er in Nederland eerder experimenten binnen de Health Deal Chronische Pijn (Wolff, 2018) geweest waarin werd onderzocht of stepped care op kleinere schaal georganiseerd kon worden. In de diverse living labs heeft de health deal geleid tot intensievere samenwerking. Echter alle deelnemende regio’s ervaarden ook diverse belemmeringen die de implementatie van de Zorgstandaard Chronische pijn (Dutch Pain Society en Vereniging Samenwerkingsverband Pijnpatiënten naar één stem, 2017) vertraagde en op sommige punten zelfs onmogelijk maakte. Denk hier bij aan silowerking binnen de zorg (financiering, beroepskaders en eigen belang boven algemeen belang) en de huidige rol van de huisartsen in de keten. Op- en afschalingscriteria konden zo niet ontwikkeld en onderzocht worden. Uit het rapport lage rugpijn van ZIN blijkt dat slechts circa 5% van de patiënten wordt doorverwezen naar de 2e lijn. Echter binnen de 2e lijn wordt vaak toch onderling doorverwezen met veel diagnostiek en behandelingen. Mogelijk bestaat hier verbeterruimte d.m.v. meer afschaling of of meer en vroegere (multidisciplinaire) afstemming ten behoeve van juiste zorg op de juiste plek.
Gezien bovenstaande, zijn de aanbevelingen in deze module geformuleerd op basis van expert opinion van de werkgroep en de eerder in de Zorgstandaard Chronische Pijn opgenomen omschrijving van het stepped care principe.
Stepped care
In de Zorgstandaard Chronische Pijn wordt het proces van stepped care als volgt omschreven: ‘aan een patiënt wordt altijd de meest effectieve, minst belastende, goedkoopste en kortste vorm van behandeling aangeboden die mogelijk is gezien de aard en de ernst van de problematiek. Hierbij wordt rekening gehouden met de behoeftes van de patiënt en wordt passende zorg geboden op basis van de benodigde zorgzwaarte. Als de minimaal noodzakelijke interventie onvoldoende effect heeft, wordt naar een intensievere interventie overgegaan.’ (Zorgstandaard Chronische pijn, p. 6, regel 41-46; Dutch Pain Society en Vereniging Samenwerkingsverband Pijnpatiënten naar één stem, 2017). Op basis van deze omschrijving van stepped care, is het mogelijk om waar mogelijk de tweede lijn over te slaan. De werkgroep is van mening, analoog aan de omschrijving in de Zorgstandaard, dat er gestreefd moet worden om passende zorg bij de benodigde zorgzwaarte te bieden: Voor iedere patiënt wordt een op maat gemaakte behandeling aangeboden, waarbij geldt: zo licht als mogelijk en zo intensief als nodig (matched care). Belangrijk aandachtspunt is daarbij wel dat er optimale mogelijkheden worden gecreëerd binnen de eerste lijn in de vorm van multidisciplinaire eerstelijnszorg. De onderstaande op- en afschalingscriteria zijn gebaseerd op deze visie.
Voorgestelde kernvragen voor zelf behandelen of verwijzen en op- of afschalen
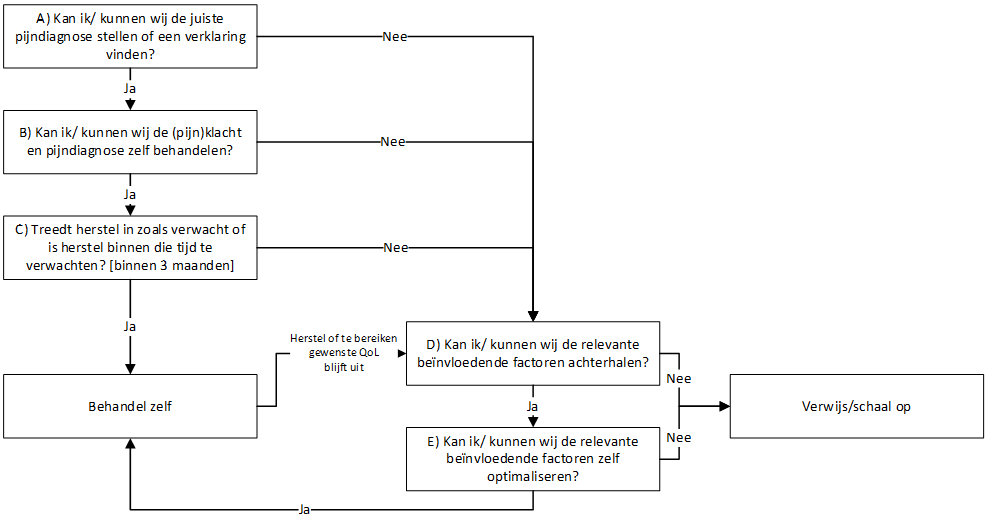
Het grootste deel van de patiënten zal in de nabije toekomst in de eerste (en anderhalve) lijn behandeld worden. Daar waar nodig kan echter aanvullende expertise, advies of onderzoek in de tweede lijn of derde lijn aangevraagd worden. Ook indien de complexiteit van de patiënt te hoog is, de ingezette therapie niet effectief is gebleken, er geen alternatieve adequate interventies binnen de competenties van de zorgprofessional zijn en/of er onvoldoende aansluiting is bij de hulpvraag of behoefte van de patiënt, moet opschaling overwogen worden. Figuur 3.1 geeft de kernvragen en globale stappen voor opschaling weer in geval aanhoudende pijn en/of toenemende afname van functioneren een probleem vormt.
Zoals in de module ‘Organisatie van zorg’ is beschreven, wordt er momenteel te weinig gebruik gemaakt van de mogelijkheid om af te schalen naar een lagere lijn. Voor professionals in de tweede of derde lijn adviseert de werkgroep afschaling te overwegen indien er een effectieve, minder belastende, goedkopere en/of korte vorm van behandeling mogelijk is in bijvoorbeeld de nulde of eerste lijn (juiste zorg op juiste plek), de ingezette therapie niet effectief is en geen alternatief is binnen competenties van de zorgverlener/organisatie en/of er geen aansluiting is bij de hulpvraag of behoefte van de patiënt. Het afschalen betreft niet alleen minder belastend, goedkoper of korter (in plaats van) maar vooral passende zorg na een andere (hier dus 2e of 3e lijns) interventie. Als voorbeeld kan je denken aan eerstelijns behandeling na MSR om verkregen vaardigheden in zelfmanagement met pijn verder te integreren en te bestendigen in het dagelijkse functioneren.
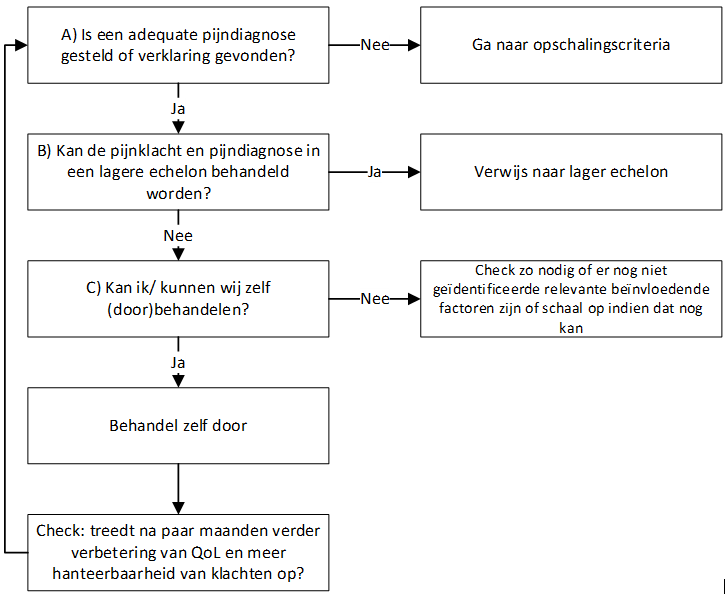
Figuur 3.1 geeft de vijf kernvragen en stappen weer om op te schalen wanneer pijnklachten aanhouden. Figuur 3.2 geeft de 3 globale vragen en stappen om af te schalen weer wanneer aanhoudende pijn vermindert en/of hanteerbaar wordt.
Figuur 3.1 Vijf kernvragen voor opschalen (5J’s)
Figuur 3.2 Drie kernvragen om af te schalen
Waarden en voorkeuren van patiënten (en evt. hun naasten)
Voor elke patiënt heeft het leven met chronische pijn een andere betekenis. Het is voor de patiënt belangrijk dat hij/zij passende zorg krijgt op basis van de benodigde zorgzwaarte en waarden. De behoefte die iemand heeft kan echter veranderen gedurende de tijd. Dit door veranderde leefomstandigheden, bepaalde levensfase of het doorlopen van een eigen (acceptatie) proces. Deze wisselende behoeften vragen om goede afstemming tussen de patiënt en de zorgprofessional. Kan deze zorgprofessional het behandelaanbod of de begeleiding (nog) geven die passend is? Sluit het aan bij de hulpvraag en de waarden van de patiënt? Voor de patiënt is het belangrijk dat de keuzes omtrent op- en afschaling worden gemaakt in samenspraak tussen patiënt en zorgprofessional (samen beslissen). Het antwoord op de vraag of de behandeling nog aansluit bij de behoeften van de patiënt van dat moment is een logisch criterium om op te schalen of af te schalen.
Het is de verwachting van de werkgroep dat op- en afschalingscriteria en het toepassen van het stepped care en Matched care principe zoals beschreven in de Zorgstandaard, bijdragen aan patiënttevredenheid. In zijn algemeenheid zal de patiënt het waarderen indien de zorgverlener duidelijk aangeeft waar de behandelmogelijkheden liggen, en waar de behandelmogelijkheden ophouden en verwijzing naar een andere discipline nodig is. Matched care bevordert dat patiënten sneller de zorg krijgen die zij nodig hebben. Daarnaast is het voor de patiënt belangrijk om de zorg zo dicht mogelijk bij huis te ontvangen. Tijdige afschaling maakt dit mogelijk.
Kosten (middelenbeslag)
De evidence is onzeker over de kosteneffectiviteit van gestratificeerde zorgpaden bij patiënten met chronische pijn. Verder is er geen informatie over de kosteneffectiviteit van het inzetten van specifieke op- en afschalingcriteria beschikbaar. De werkgroep verwacht echter dat door het inzetten van de voorgestelde op- en afschalingscriteria, alsmede de toepassing van het stepped care principe zoals beschreven in de Zorgstandaard, de zorg goedkoper en efficiënter wordt. Door betere samenwerking en tijdige inzet van elkaars expertise (als onderdeel van netwerkzorg) krijgt de patiënt eerder de passende zorg.
Aanvaardbaarheid, haalbaarheid en implementatie
Een mogelijke barrière voor zorgprofessionals om patiënten te verwijzen naar een andere zorgverlener is dat hij/zij de patiënt dan ‘kwijtraakt’ (en dus omzet mist). Duidelijke criteria voor op- en afschaling zullen helpend zijn bij het vormgeven van de samenwerking en het maken van keuzes.
De aanbevelingen met betrekking tot op- en afschaling zijn eenvoudig en makkelijk in de praktijk toe te passen. Een valkuil bij toepassing van het stepped care model is dat ook een vaste volgorde wordt aangehouden waar dit niet zinvol is. In het geval van complexe problematiek leidt dit tot uitstel van de juiste zorg en daarmee tot verminderde kwaliteit van leven en toename van directe en indirecte kosten (zie ook elders de betreffende literatuur over wachtlijst problematiek). Op indicatie moet de patiënt direct naar de juiste zorg op de juiste plek kunnen worden verwezen (matched care).
Een ander ervaringsvoorbeeld uit de praktijk waarom toepassing van stepped care momenteel nog problematisch is, is dat vergoeding voor een belangrijk deel productie gedreven is en onderlinge afstemming, intensieve analyse en advisering onvoldoende gestimuleerd wordt. Afstemming, zeker bij patiënten met een hoge complexiteit, tussen en binnen de lijnen en stappen (steps) is van groot belang.
Er zijn ten aanzien van de aanvaardbaarheid, haalbaarheid en implementatie geen overwegingen die van invloed zijn op de besluitvorming omtrent de aanbevelingen.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
De werkgroep onderschrijft de omschrijving van stepped care en matched care in de Zorgstandaard en het belang van ‘samen beslissen’. Ze kiest daarom om de eerste aanbeveling als ‘sterke’ aanbevelingen te formuleren. Ten aanzien van de voorgestelde op- en afschalingscriteria, hoewel gerelateerd aan stepped care, is er zeer beperkte evidence, daarom heeft de werkgroep hier gekozen voor een zwakke aanbeveling.
Onderbouwing
Achtergrond
Zorg voor patiënten met chronische pijn is vaak complex en vraagt om betrokkenheid van verschillende zorgverleners. Samenwerking en afstemming in het netwerk “horizontaal en in de keten” en tussen de diverse lijnen en zorgverleners is belangrijk om te zorgen dat 1. de patiënt zo spoedig mogelijk op de juiste plek komt en 2. er op tijd wordt ingespeeld bij een veranderde situatie. De diversiteit en complexiteit van chronische pijnzorg vraagt om handvatten voor op- en afschaling. In deze module willen we komen tot een instrument of handvatten die zorgprofessionals kunnen gebruiken om te zien of opschaling nodig is of afschaling gewenst is. Daarnaast wordt aandacht besteed aan de relatie met en invulling van het stepped and matched care principe.
Conclusies / Summary of Findings
Kwaliteit van leven (cruciaal)
|
Zeer laag GRADE |
Het bewijs is onzeker over het effect van gestratificeerde zorgpaden in vergelijking met standaard zorg op kwaliteit van leven bij patiënten met chronische pijn.
Bronnen: Foster (2020) & Konstantinou (2020), Hill (2020), Whitehurst (2012) |
Patienttevredenheid (cruciaal)
|
Zeer laag GRADE |
Het bewijs is onzeker over het effect van gestratificeerde zorgpaden in vergelijking met standaard zorg op patiënttevredenheid bij patiënten met chronische pijn.
Bronnen: Cherkin (2018), Foster (2020) & Konstantinou (2020), Hill (2011), Hill (2020) |
Fysiek functioneren (belangrijk)
|
Zeer laag GRADE |
Totale groep patiënten Het bewijs is onzeker over het effect van gestratificeerde zorgpaden in vergelijking met standaard zorg op fysiek functioneren bij patiënten met chronische pijn
Bronnen: Cherkin (2018), Foster (2020) & Konstantinou (2020), Hill (2011), Hill (2020), Jamal (2019) |
|
Laag GRADE |
Het bewijs suggereert dat gestratificeerde zorgpaden in vergelijking tot standaard zorg mogelijk resulteren in een beter fysiek functioneren bij hoog-risico patiënten met chronische pijn.
|
|
Zeer laag GRADE |
Het bewijs is onzeker over het effect van gestratificeerde zorgpaden in vergelijking met standaard zorg op fysiek functioneren bij laag- en matig-risico patiënten met chronische pijn
Bronnen: Cherkin (2018), Hill (2011)
|
Duur van de behandeling (belangrijk)
|
geen GRADE |
Er was geen literatuur beschikbaar waarin de duur van de behandeling van zorg met gestratificeerde zorgpaden werd vergeleken met standaard zorg bij patiënten met chronische pijn.
Bronnen: - |
Kosteneffectiviteit (belangrijk)
|
Zeer laag GRADE |
Het bewijs is onzeker over het effect van gestratificeerde zorgpaden in vergelijking met standaard zorg op de kosteneffectiviteit bij patiënten met chronische pijn.
Bronnen: Foster (2020) & Konstantinou (2020), Hill (2011) & Whitehurst (2012) |
Samenvatting literatuur
Beschrijving studies
Cherkin (2018) beschrijft een cluster RCT in huisartsenpraktijken (primary care clinics) in Engeland bij patiënten met aspecifieke lage rugpijn. In de interventiepraktijken werd de STarT Back tool voor risico stratificatie geïmplementeerd, werden de zorgverleners voorzien van informatie over de aanbevolen behandeling volgens de risicoclassificering (STarT Back tool) en werden de eerstelijnszorgverleners en fysiotherapeuten getraind in het gebruik van deze aanpak. De uitkomsten van de interventie werden vergeleken met standaard zorg.
Zes praktijken werden gerandomiseerd en via de medische dossiers werden alle volwassen patiënten met een primaire diagnose van aspecifieke lage rugpijn geïdentificeerd en uitgenodigd voor het onderzoek. In totaal kwamen er 2138 patiënten in de interventie klinieken en 2571 in de controle klinieken. 36% daarvan gaf toestemming voor deelname. Patiënten die deelnamen waren gemiddeld 57,1 jaar oud en iets meer dan de helft vrouw. Het percentage patiënten dat deelnam aan de follow-up metingen was 93% voor de meting na 2 maanden en 91% na 6 maanden.
Relevante uitkomstmaten waren effect van behandeling (rug-gerelateerd fysiek functioneren, pijn), patiënttevredenheid en zorggebruik.
Foster (2020) en Konstantinou (2020) beschrijven de SCOPiC trial, een RCT in huisartsenpraktijken in het Verenigd Koninkrijk, bij patiënten met ischias. Volwassenen die zorg zochten vanwege rug of been-klachten, onafhankelijk van de duur en waarbij de huisarts sciatica vermoedde, kwamen in aanmerking voor de studie. In de interventiepraktijken werd gerichte behandeling gegeven op basis van risicostratificering (STarT Back Tool en aanvullende klinische karakteristieken). Op basis van deze risicoclassificering werd richting gegeven aan het behandelplan (zie evidence table voor details). Uiteindelijk werden er 476 deelnemers van 42 praktijken geïncludeerd en werden aan elk van de behandelgroepen 238 patiënten toegewezen. Patiënten in de interventiegroep waren gemiddeld 50,7 (SD 14,5) jaar oud, vergeleken met 53,3 (SD 13,5) jaar in de controlegroep. Beide groepen bestonden voor 50% uit vrouwen.
Relevante uitkomsten waren effect van behandeling (rug-gerelateerd fysiek functioneren), kwaliteit van leven, patiënttevredenheid, zorggebruik en kosteneffectiviteit.
Hill (2011) beschrijft de STarT Back trial, een RCT in huisartspraktijken (general practices) in Engeland, bij patiënten met lage rugpijn. Volwassenen die zorg zochten voor lage rugpijn, met of zonder gerelateerde pijn in het been, kwamen in aanmerking voor deelname. In de interventiepraktijken werd gerichte behandeling gegeven op basis van risicostratificering (STarT Back Tool). Patiënten met een laag risico ontvangen geen aanvullende zorg, patiënten met een matig en hoog risico ontvingen aanvullende gerichte zorg (zie evidence table voor details). Tien praktijken werden gerandomiseerd en in totaal werden er 568 patiënten geïncludeerd in interventiepraktijken en 283 in controlepraktijken. Patiënten waren gemiddeld 50 jaar (range 18-87) en 500 (59%) was vrouw. Relevante uitkomsten waren effect van behandeling (rug-gerelateerd fysiek functioneren, perceptie van verandering in rugpijn), kwaliteit van leven, patiënttevredenheid en zorggebruik. Aanvullend beschrijft Whitehurst (2012) een kosteneffectiviteit studie.
Hill (2020) beschrijft een cluster RCT in huisartspraktijken (general practices) in Engeland, bij patiënten met musculoskeletale pijn. Volwassenen die zorg zochten voor musculoskeletale pijn, als nieuwe of terugkerende patiënt, kwamen in aanmerking voor deelname. Patiënten die op basis van ‘rode vlaggen’ mogelijk urgente medische interventie nodig hadden, werden geëxcludeerd. In de interventiepraktijken werd gerichte behandeling gegeven op basis van risicostratificering (STarT Back Tool). Op basis van de locatie van de pijn en de risicoclassificering, werd het behandelplan opgesteld (zie evidence table voor details).
Acht praktijken werden gerandomiseerd en in totaal werden er 231 patiënten geïncludeerd in interventiepraktijken en 293 in controlepraktijken. Patiënten waren gemiddeld 61,1 jaar (SD 14,8) en 318 (60; 7%) was vrouw. Relevante uitkomsten waren effect van behandeling (rug-gerelateerd fysiek functioneren, perceptie van verandering in rugpijn), kwaliteit van leven, patiënttevredenheid en zorggebruik.
Jamal (2020) beschrijft een RCT in 93 huisartspraktijken in Nederland, bij patiënten met lage rugpijn. Volwassenen van 18 tot 45 jaar waar minimaal 12 weken een registratie bij openstond voor ICPC code L03 (LBP zonder uitstraling) kwamen in aanmerking voor de studie. In de interventiepraktijken werden patiënten op basis van de Case Finding Axial Spondyloarthritis (CaFaSpA) verwijzing strategie verwezen. Uiteindelijk namen 140 huisartsen uit de 93 praktijken deel en werden er 333 patiënten binnen de interventiegroep gezien en 346 binnen de controlegroep. Patiënten waren gemiddeld 36.2 jaar oud en 64% van de patiënten was vrouw. De relevante uitkomst was effect van behandeling.
Resultaten
Kwaliteit van leven (cruciaal)
Kwaliteit van leven werd beschreven door vijf publicaties over drie studies, die allen de EQ-5D score rapporteerden. Dit is een generieke maat voor kwaliteit van leven. De maximale score is 1, waarbij een hogere score wijst op een hoger kwaliteit van leven.
Foster (2020) en Konstantinou (2020) rapporteerden dat de gemiddelde baseline EQ-5D score 0,5168 (SD 0,2109) was in de interventiegroep en 0,5201 (SD 0,2300) in de controlegroep. Na vier maanden was de EQ-5D score 0,6710 (SD 0,2006) in de interventiegroep en 0,6806 (SD 0,1955) in de controlegroep. De MD was -0,009 (95% BI -0,046 tot 0,026), ten gunste van de controlegroep.
Na 12 maanden was de EQ-5D score in de interventiegroep 0,7138 (SD 0,2137)
en 0,7320 (SD 0,1879) in de controlegroep. De MD was -0,018 (95% BI -0,054 tot 0,0176), ten gunste van de controlegroep.
Deze verschillen waren niet klinisch relevant (< 0,03).
Whitehurst (2012) rapporteerde de kwaliteit van leven apart voor de laag, matig en hoog-risico groepen. De gemiddelde baseline EQ-5D scores voor interventie- en controlegroep waren: laag-risico: 0,725 (SD 0,19) en 0,733 (SD 0,15); matig-risico: 0,540 (SD 0,27) en 0,573 (SD 0,27); hoog-risico: 0,325 (SD 0,33) en 0,252 (SD 0,35).
Voor de laag-risicogroep werd na vier maanden een EQ-5D score van 0,799 (SD 0,21) in de interventiegroep en 0,821 (SD 0,18) in de controlegroep gerapporteerd. De MD was −0,022 (95%BI −0,07 tot 0,03), ten gunste van de controlegroep.
Na 12 maanden was de EQ-5D score 0,787 (SD 0,20) in de interventiegroep en 0,773 (SD 0,24) in de controlegroep. De MD was 0,014 (95%BI −0,05 tot 0,08), ten gunste van de interventiegroep. Deze verschillen waren niet klinisch relevant (< 0,03).
Voor de matig-risicogroep werd na vier maanden een EQ-5D score van 0,702 (SD 0,28) in de interventiegroep en 0,674 (SD 0,28) in de controlegroep gerapporteerd. De MD was 0,028 (95% BI -0,03 tot 0,09), ten gunste van de interventiegroep. Dit was geen klinisch relevant verschil (< 0,03). Na 12 maanden was de EQ-5D score 0,687 (SD 0,32) in de interventiegroep en 0,635 (SD 0,31) in de controlegroep. De MD was 0,052 (95% BI −0,01 tot 0,12), ten gunste van de interventiegroep. Dit verschil was klinisch relevant (> 0,03).
Voor de hoog-risicogroep werd na vier maanden een EQ-5D score van 0,585 (SD 0,35) in de interventiegroep en 0,474 (SD 0,38) in de controlegroep gerapporteerd. De MD was 0,111 (95% BI 0,02 tot 0,20), ten gunste van de interventiegroep. Na 12 maanden was de EQ-5D score 0,541 (SD 0,37) in de interventiegroep en 0,458 (SD 0,38) in de controlegroep. De MD was 0,083 (95% BI −0,01 tot 0,18) ten gunste van de interventiegroep. Dit waren klinisch relevante verschillen (> 0,03).
Gezien het geringe aantal patiënten in deze groepen is de bewijskracht voor de studies zeer laag tot laag en is er geen aparte conclusie opgesteld specifiek voor matig- en hoog-risicogroepen.
Hill (2020) rapporteerde een EQ-5D score op baseline van 0,55 (SD 0,25; n = 226) in de interventiegroep en 0,57 (SD 0,22; n = 287) in de controlegroep. Na 6 maanden was de EQ-5D score 0,65 (SD 0,26; n = 208) in de interventiegroep en 0,63 (SD 0,25; n = 258) in de controlegroep. De MD was 0,02 (95% CI -0,03 tot 0,07), ten gunste van de interventiegroep. Dit was geen klinisch relevant verschil (< 0,03).
Cherkin (2018) en Jamal (2019) beschreven geen resultaten voor kwaliteit van leven.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat begon hoog, omdat het gebaseerd werd op RCTs. De bewijskracht is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias, -1), inconsistentie tussen studieresultaten (inconsistentie, -1) en het geringe aantal patiënten (imprecisie, -1). De bewijskracht komt daarmee op zeer laag.
Patiënttevredenheid (cruciaal)
Voor vier studies werd de patiënttevredenheid beschreven. De schalen en items waarmee dit gebeurde, varieerde tussen studies. De resultaten zijn samengevat in onderstaande tabel.
Het varieerde of de scores voor patiënttevredenheid ten gunste waren van de interventiegroep of controlegroep. Enkele resultaten waren klinisch relevant, maar ook hier zien we een inconsistent beeld.
|
Studie |
Item |
Follow-up |
Interventie groep |
Controle groep |
RR (95% BI) of anders |
Ten gunste van |
Klinisch relevant |
|
Cherkin, 2018 |
Very satisfied with care
|
6M |
OR pre-post 1,01 (0,63 tot 1,61) |
OR 1,27 (0,83 tot 1,94) |
OR interventie vs. control 0,79 (0,42 tot 1,49) |
Controle
|
|
|
|
Very satisfied with treatment
|
|
OR 1,15 (0,68 tot 1,95) |
OR 0,91 (0,57 tot 1,44) |
OR 1,26 (0,63 tot 2,54) |
Interventie |
|
|
|
Very satisfied with information about cause of pain |
|
OR 1,29 (0,76 tot 2,20) |
OR 1,52 (0,94 tot 2,46) |
OR 0,85 (0,41 tot 1,740) |
Controle |
|
|
Foster, 2020 Konstantinou, 2020 |
Satisfaction with care – Very satisfied |
4M |
65/153 (43%) |
57/158 (36%) |
1,18 (0,89 tot 1,55) |
Interventie |
Ja |
|
|
Quite satisfied |
4M |
42/153 (27%) |
48/158 (30%) |
0,90 (0,64 tot 1,28) |
Controle |
Nee |
|
|
Not satisfied |
4M |
24/153 (16%) |
26/158 (16%) |
0,95 (0,57 tot 1,58) |
Geen |
Nee |
|
|
Satisfaction with care – Very satisfied |
12M |
42/123 (34%) |
50/132 (38%) |
0,90 (0,65 tot 1,25) |
Controle |
Nee |
|
|
Quite satisfied |
12M |
32/123 (26%) |
36/132 (27%) |
0,95 (0,63 tot 1,43) |
Controle |
Nee |
|
|
Not satisfied |
12M |
17/123 (14%) |
18/132 (14%) |
1,01 (0,55 tot 1,88) |
Geen |
Nee |
|
|
Satisfaction with results of care – Very satisfied |
4M |
62/153 (41%) |
42/158 (27%) |
1,52 (1,10 tot 2,10) |
Interventie |
Ja |
|
|
Quite satisfied |
4M |
43/153 (28%) |
58/158 (37%) |
0,77 (0,55 tot 1,06) |
Controle |
Ja |
|
|
Not satisfied |
4M |
27/153 (18%) |
28/158 (18%) |
1,00 (0,62 tot 1,61) |
Geen |
Nee |
|
|
Satisfaction with results of care – Very satisfied |
12M |
37/123 (30%) |
49/132 (37%) |
0,81 (0,57 tot 1,15) |
Controle |
Ja |
|
|
Quite satisfied |
12M |
36/123 (30%) |
37/132 (28%) |
1,04 (0,71 tot 1,54) |
Interventie |
Nee |
|
|
Not satisfied |
12M |
16/123 (13%) |
19/132 (14%) |
0,90 (0,49 tot 1,68) |
Interventie |
Nee |
|
Hill, 2011 |
Satisfaction with care- Very satisfied |
4M |
166/416 (40%) |
46/197 (23%) |
1,71 (1,29 tot 2,26) |
Interventie |
Ja |
|
|
Quite satisfied |
4M |
139/416 (33%) |
81/197 (41%) |
0,81 (0,66 tot 1,01) |
Controle |
Ja |
|
|
Not satisfied |
4M |
111/416 (27%) |
70/197 (36%) |
0,75 (0,59 tot 0,96) |
Interventie |
Ja |
|
Hill, 2020
|
Satisfaction with GP care for MSK pain – Very satisfied |
6M |
48/200 (24,2%) |
58/158 (22,8%) |
1,07 (0,76 tot 1,49) |
Interventie |
Nee |
|
|
Quite satisfied |
6M |
71/200 (35,9%) |
89/258 (34,9%) |
1,03 (0,80 tot 1,32) |
Interventie |
Nee |
|
|
Not very satisfied |
6M |
25/200 (12,6%) |
44/258 (17,3%) |
0,73 (0,47 tot 1,16) |
Interventie |
Ja |
|
|
Not at all satisfied |
6M |
8/200 (4,0%) |
4/258 (1,6%) |
2,58 (0,79 tot 8,45) |
Controle |
Ja |
Jamal (2019) beschreef geen resultaten voor patiënttevredenheid.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat begon hoog, omdat het gebaseerd werd op RCTs. De bewijskracht is met 3 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias, -1), inconsistentie tussen studieresultaten (inconsistentie, -1) en het geringe aantal patiënten (imprecisie, -1). De bewijskracht komt daarmee op zeer laag.
Fysiek functioneren (belangrijk)
Alle vijf de studies rapporteerden met de Roland-Morris Disability Questionnaire (RMDQ) resultaten voor rug-gerelateerd fysiek functioneren. Vanwege de vergelijkbaarheid tussen de studies werd deze maat gekozen als weergave voor rug-gerelateerd fysiek functioneren. De RMDQ heeft een schaal van 0 tot 24, waarbij een hogere score duidt op meer beperkingen.
Cherkin (2018) beschrijft dat de baseline RMDQ score 11,8 (SD 6,1) was in de interventiegroep en 11,8 (SD 6,3) in de controlegroep. In vergelijking met de score op baseline was het verschil op zes maanden follow-up −0,05 (95% BI −0,83, 0,73) in de interventiegroep en −0,55 (95% BI −1,26 tot 0,15) in de controlegroep. Het gemiddelde verschil tussen de groepen was 0,50 (95% BI −0,55 tot 1,55), ten gunste van de controlegroep. Dit is geen klinisch relevant verschil (<10%). Gesplitst voor risicoscore op baseline was het effect in de laag-risico en hoog-risico groepen ten gunste van de controlegroep en in de matig-risico groep ten gunste van de interventiegroep (MD: laag-risico 0,56 (95% BI − 0,71 tot 1,82), hoog-risico 1,76 (95% BI −1,10 tot 4,62) en matig-risico −0,06 (95% BI −1,94 tot 1,81). Dit verschil was klinisch relevant voor de hoog-risico patiënten (> 10%), maar niet voor de laag- en matig-risico patiënten (< 10%).
Foster (2020) en Konstantinou (2020) beschreven dat de baseline scores 11,1 (SD 5,2) in de interventiegroep en 11,3 (5,4) in de controlegroep waren. Op vier maanden was de RMDQ-score in de interventie groep 6,5 (SD 6,3) en 6,2 (SD 6,0) in de controlegroep. Het gemiddeld verschil tussen de groepen was 0,43 (95% BI –0,69 tot 1,54), ten gunste van de controlegroep. Op 12 maanden was de RMDQ-score in de interventiegroep 5,0 (SD 6,2) en in de controlegroep 5,5 (SD 6,0). Het gemiddelde verschil was -0,53 (95% BI –1,84 tot 0,78), ten gunste van de interventiegroep. De verschillen na vier en 12 maanden (resp. 0,43 en -0,53) waren niet klinisch relevant (< 10%).
Hill (2011) beschreef de RMDQ-verschilscore na vier maanden en 12 maanden, gecorrigeerd voor leeftijd, geslacht, baseline RMDQ en duur van rugpijn. De baseline scores waren 9,8 (SD 5,6) in de interventiegroep en 9,7 (SD 5,8) in de controlegroep. Na vier maanden was de RMDQ-verschilscore in de interventiegroep 4,7 (SD 5,9) en in de controlegroep 3,0 (SD 5,9). Het verschil was 1,81 (95% BI 1,06 tot 2,57), ten gunste van de interventiegroep.
Na 12 maanden was de RMDQ-verschilscore in de interventiegroep 4,3 (SD 6,4) en in de controlegroep 3,3 (SD 6,2). Het verschil was 1,06 (95% BI 0,25 tot 1,86), ten gunste van de interventiegroep. Dit zijn klinisch relevante verschillen (> 10%).
De scores werden ook beschreven voor de subgroepen op basis van baseline risico-stratificering. De verschilscore was in alle drie de risicogroepen groter in de interventiegroep, ten gunste van de interventiegroep. Het verschil tussen de groepen was op vier maanden: laag-risico: 0,66 (95% BI –0,41 tot 1,74), matig-risico: 1,99 (95% BI 0,75 tot 3,22); hoog-risico 2,53 (95% BI 0,90 tot 4,16); en op 12 maanden: laag-risico: 0,12 (95% BI –1,13 tot 1,38); matig-risico: 1,33 (95% BI 0,15 tot 2,52); hoog-risico: 1,22 (95% BI –0,47 tot 2,91). Deze verschillen waren klinisch relevant voor de matig- en hoog-risico patiënten (> 10%), maar niet voor de laag-risico patiënten (< 10%).
Hill (2020) beschreef dat de RMDQ score op baseline 9,84 (SD 5,40) was in de interventiegroep en 9,38 (SD 5,57) in de controlegroep. Na zes maanden was de RMDQ score 6,90 (SD 6,52) in de interventiegroep en 6,44 (SD 5,80) in de controlegroep. De MD was 0,46 (95% BI -1,64 tot 2,56), ten gunste van de controlegroep. Dit was geen klinisch relevant verschil.
Hill (2020) includeerde naast patiënten met rugpijn ook patiënten met andere musculoskeletale pijn. Daarom werden er naast de RMDQ op zes maanden ook andere functievragenlijsten ingevuld. De algemene musculoskeletale gezondheid werd gemeten met de Musculoskeletal Health Questionnaire (MSK-HQ; schaal 0 tot 56; hogere score wijst op betere gezondheidsstatus. De baseline MSK-HQ waren 29,9 (SD 10,5) in de interventiegroep en 29,4 (SD 10,4) in de controlegroep. De MSK-HQ score op zes maanden was 37,5 (SD 12,8) in de interventiegroep en 37,3 (SD 11,8) in de controlegroep. De MD was 0,20 (95% BI -2,13 tot 2,53), ten gunste van de interventiegroep. Dit verschil was niet klinisch relevant (< 10%).
Jamal (2019) beschreef dat de baseline mediaan RMDQ score 8 (IKR 4-12) was in de interventiegroep en 8 (4-12) in de controlegroep. Na vier maanden was de gemiddelde RMDQ score 7,65 (95% BI 6,79 tot 8,50) in de interventiegroep en 8,15 (95% BI 7,34 tot 8,96) in de controlegroep. De MD was -0,50 (95% CI -1,68 tot 0,68), ten gunste van de interventiegroep. Dit was geen klinisch relevant verschil (< 10%).
Bewijskracht van de literatuur
Totale groep patiënten
De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ begon hoog, omdat het gebaseerd werd op RCTs. De bewijskracht is met 3 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias, -1), inconsistente resultaten tussen studies (inconsistentie, -1) en het geringe aantal patiënten (imprecisie, -1). De bewijskracht komt daarmee op zeer laag.
Hoog-risico patiënten
De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ in hoog-risicopatiënten begon hoog, omdat het gebaseerd werd op RCTs. De bewijskracht is met 2 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias, -1) en het geringe aantal patiënten (imprecisie, -1). De bewijskracht komt daarmee op laag.
Laag- en matig-risico patiënten
De bewijskracht voor de uitkomstmaat ‘fysiek functioneren’ in laag- en matig-risico patiënten begon hoog, omdat het gebaseerd werd op RCTs. De bewijskracht is met 3 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias, -1), inconsistente resultaten (inconsistentie, -1) en het geringe aantal patiënten (imprecisie, -1). De bewijskracht komt daarmee op zeer laag.
Duur van behandeling (belangrijk)
Duur van behandeling werd in de geïncludeerde studies niet vergeleken tussen de interventiegroep en controlegroep.
Bewijskracht van de literatuur
Er was geen literatuur beschikbaar waarin de duur van behandeling van de interventiegroep werd vergeleken met de duur van behandeling van de controlegroep.
Kosteneffectiviteit (belangrijk)
Twee studies beschreven het verschil in totale zorgkosten en de kosteneffectiviteit. Bij de bepaling van de kosteneffectiviteit werd uitgegaan van de EuroQol-5D. Het is belangrijk om bij de interpretatie van deze resultaten mee te nemen dat het zorgstelsel en de zorgkosten per element verschillen van de situatie in Nederland.
Foster (2020) en Konstantinou (2020) rapporteerden over de SCOPiC trial, een studie bij patiënten in het Verenigd Koninkrijk. In de totale zorgkosten werden zowel zorgkosten die vergoed werden meegenomen, als kosten die berekend werden aan de patiënten, zoals over-the-counter medicatie en private zorg.
De zorgkosten voor de patiënten in de interventiegroep waren gemiddeld £743.23 (SD 764.05) en in de controlegroep £665.55 (SD978.15). Dat is een verschil van £77.67 (95% BI –70.49 tot 232.94), ten gunste van de controlegroep. De gemiddelde QALY’s van de interventiegroep waren met een verschil van –0.011 (95% BI –0.035 tot 0.013) lager dan de gemiddelde QALY’s van de controle groep. Dit zijn geen klinisch relevante verschillen.
Hill (2011) en Whitehurst (2012) rapporteerden over de STarT Back trial, een studie in patiënten het Verenigd Koninkrijk. In de totale kosten werden diverse zorgkosten (eerstelijnszorg, tweedelijnszorg, andere zorg, over-the-counter middelen en medicatie op recept) opgenomen. De zorgkosten voor de patiënten in de interventiegroep waren gemiddeld £240.01 (SD 356.3) en in de controlegroep £274.40 (SD 350.8). Dat is een verschil van £-34.39 (95% BI -80.3 tot 11.5), ten gunste van de interventiegroep. De interventie leverde gemiddeld 0.039 (95% BI 0.01 tot 0.07) QALY’s op voor de patiënten in de interventiegroep ten opzichte van de controlegroep. Dit verschil is niet klinisch relevant.
|
Studie |
Variabele |
Gestratificeerde zorg |
Standaard zorg |
Gemiddelde verschil (95% BI) |
|
SCOPiC trial (Foster (2020), Konstantinou (2020)) |
Gemiddelde kosten (SD), £ |
743.23 (764.05) |
665.55 (978.15) |
77.67* (–70.49 tot 232.94)
|
|
|
Gemiddelde QALYs (SD) |
0.6599 (0.1731) |
0.6713 (0.1685) |
–0.011* (–0.035 tot 0.013) |
|
|
|
|
|
|
|
STarT Back trial (Hill (2011) en Whitehurst (2012)) |
Gemiddelde kosten (SD), £ |
240.01 (356.3) |
274.40 (350.8) |
-34.39 (-80.3 tot 11.5) |
|
|
Gemiddelde QALYs (SD) |
niet gespecificeerd |
niet gespecificeerd |
0.039 (0.01 tot 0.07) |
|
*: gecorrigeerd voor waarden op baseline |
||||
Kosteneffectiviteit werd niet beschreven door Cherkin (2018), Hill (2020) en Jamal (2019).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat begon hoog, omdat het gebaseerd werd op RCTs. De bewijskracht is met 3 niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias, -1), brede betrouwbaarheidsintervallen (imprecisie, -1) en de indirectheid van de resultaten gezien het verschil in zorgstelsel (indirectheid, -1). De bewijskracht komt daarmee op zeer laag.
Zoeken en selecteren
Er zijn verschillende benaderingen mogelijk om deze uitgangsvraag te beantwoorden. Het is bijvoorbeeld mogelijk om een beschrijving van de mogelijke criteria te geven zonder verdere analyse wat de beste criteria zijn, te focussen op kwalitatieve studies of een volledige literatuursamenvatting waarin onderzocht wordt of de toepassing van specifieke op- en afschalingscriteria effectief is op voor patiënt belangrijke uitkomstmaten. De werkgroep heeft gekozen voor de laatste optie.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag: wat is het effect van het toepassen van specifieke op- en afschalingcriteria in vergelijking met standaard zorg op het effect van behandeling, kwaliteit van leven, patiënttevredenheid, de duur van behandelingen, en kosteneffectiviteit bij patiënten met chronische pijn?
P: Patiënten met chronische pijn
I: Toepassing van specifieke op- en afschalingcriteria
C: Standaard zorg
O: Kwaliteit van leven, patiënttevredenheid, fysiek functioneren, duur van behandeling, kosteneffectiviteit.
Relevante uitkomstmaten
De werkgroep achtte kwaliteit van leven en patiënttevredenheid voor de besluitvorming cruciale uitkomstmaten; en fysiek functioneren, duur van de behandeling en kosteneffectiviteit voor de besluitvorming belangrijke uitkomstmaten.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Kwaliteit van leven en fysiek functioneren kunnen met veel verschillende instrumenten gemeten worden. De werkgroep definieerde de kleinste minimal important difference (MID) zoals gerapporteerd voor het specifieke instrument als klinisch (patiënt) relevant verschil. Indien deze onbekend is, hanteerde de werkgroep op basis van consensus een grens van 10%.
De werkgroep definieerde voor de kosteneffectiviteit zoals bepaald met behulp van de EQ-5D een verschil van 0,03 (Soer, 2012) als een klinisch (patiënt) relevant verschil.
De uitkomstmaat ‘patiënttevredenheid’ kan op verschillende manieren gescoord worden. De werkgroep acht een relatief verschil van 10% als klinisch relevant verschil.
Voor de duur van de behandeling werd niet a priori vastgesteld welk verschil in behandelduur als klinisch relevant verschil werd gezien. Bij deze uitkomstmaat moet opgemerkt worden dat een kortere of langere behandelduur niet per se gunstig is voor de patiënt, maar dat de interpretatie bij deze uitkomstmaat afhankelijk is van de gevonden resultaten op de overige patiëntrelevantie uitkomstmaten. Deze weging wordt, waar relevant, gemaakt in de overwegingen.
Zoeken en selecteren (Methode)
In de databases Medline (via OVID) en Embase (via Embase.com) is op 25 januari 2021 met relevante zoektermen gezocht naar studies naar op- en afschalingcriteria voor zorg bij patiënten met chronische pijn. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 1952 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: RCT waarin methoden van op- en afschaling of stratificatie met elkaar vergeleken worden bij patiënten met chronische pijn. Op basis van titel en abstract werden in eerste instantie 38 artikelen voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 31 publicaties geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording), en zeven publicaties over vijf studies definitief geselecteerd.
Resultaten
Er zijn zeven publicaties gevonden die resultaten van vijf RCTs beschrijven opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidencetabellen. De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
Op basis van de RCTs zijn voor elk van de cruciale uitkomstmaten resultaten beschikbaar. Aangezien observationele vergelijkende studies ten opzichte van RCTs op een lager niveau van bewijskracht beginnen (laag in plaats van hoog), is het minder waarschijnlijk dat inclusie van observationele studies zou bijdragen aan een hogere bewijskracht. Er is daarom gekozen om alleen RCT’s te includeren.
Referenties
- Cherkin, D., Balderson, B., Wellman, R., Hsu, C., Sherman, K. J., Evers, S. C., . . . Foster, N. E. (2018). Effect of Low Back Pain Risk-Stratification Strategy on Patient Outcomes and Care Processes: the MATCH Randomized Trial in Primary Care. Journal of General Internal Medicine, 33(8), 1324-1336. https://doi.org/10.1007/s11606-018-4468-9
- Dutch Pain Society en Vereniging Samenwerkingsverband Pijnpatiënten naar één stem. (2017). Zorgstandaard Chronische Pijn. https://www.zorginzicht.nl/binaries/content/assets/zorginzicht/kwaliteitsinstrumenten/Zorgstandaard+Chronische+Pijn.pdf
- Foster, N. E., Konstantinou, K., Lewis, M., Ogollah, R., Saunders, B., Kigozi, J., . . . Dunn, K. M. (2020). Stratified versus usual care for the management of primary care patients with sciatica: the SCOPiC RCT. Health Technology Assessment, 24(49), 1-130. https://doi.org/10.3310/hta24490
- Hill, J. C., Whitehurst, D. G., Lewis, M., Bryan, S., Dunn, K. M., Foster, N. E., . . . Hay, E. M. (2011). Comparison of stratified primary care management for low back pain with current best practice (STarT Back): a randomised controlled trial. The Lancet, 378(9802), 1560-1571. https://doi.org/10.1016/s0140-6736(11)60937-9
- Hill, J. C., Garvin, S., Chen, Y., Cooper, V., Wathall, S., Saunders, B., Lewis, M., Protheroe, J., Chudyk, A., Dunn, K. M., Hay, E., van der Windt, D., Mallen, C., & Foster, N. E. (2020). Stratified primary care versus non-stratified care for musculoskeletal pain: findings from the STarT MSK feasibility and pilot cluster randomized controlled trial. BMC family practice, 21(1), 30. https://doi.org/10.1186/s12875-019-1074-9
- Jamal, M., Korver, A. M., Kuijper, M., Lopes Barreto, D., Appels, C., Spoorenberg, A., Koes, B.W., Hazes, J., Hoeven, L. V., & Weel, A. (2020). The IMPACT study: A clustered randomized controlled trial to assess the effect of a referral algorithm for axial spondyloarthritis. PloS one, 15(1), e0227025. https://doi.org/10.1371/journal.pone.0227025
- Konstantinou, K., Lewis, M., Dunn, K. M., Ogollah, R., Artus, M., Hill, J. C., . . . Foster, N. E. (2020). Stratified care versus usual care for management of patients presenting with sciatica in primary care (SCOPiC): a randomised controlled trial. The Lancet Rheumatology, 2(7), e401-e411. https://doi.org/10.1016/s2665-9913(20)30099-0
- Wolff, A., Thomassen, I., Jong de, E., Engelbart, D., Niendieker, H., & Oosting, H. (2018). De Health Deal Chronische Pijn. NTTP , 14-19.
Evidence tabellen
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies [cohort studies, case-control studies, case series])1
Risk of bias table for intervention studies (randomized controlled trials)
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Cherkin, 2018 |
Web-based
Prior to the intervention, the trial biostatistician randomly assigned one clinic in each of the three geographic and sociodemographic matched pairs of clinics to the intervention by computer-generated random number. All eligible patients seen in the intervention clinics were considered to have received the intervention. |
Unlikely
Adequate, randomized before participation of patients and providing the intervention. |
Unlikely
Researchers did not inform patients that their clinics were participating in an intervention.
|
Likely
Care providers were aware of the allocation as they were trained or not trained. This might have induced an (unaware) difference in contact with the patient, on top of the difference in provided intervention.
|
Unlikely
Interviewers were blinded to patients’ clinics. |
Likely
Trial registration present: NCT02286141. Registered November 5, 2014.
Unclear Satisfaction was measured at a 10-item instrument among three dimensions; in this report only 3 dichotomous outcomes are presented |
Likely
The numbers of patients that consented and provided baseline data do not correspond with patients numbers of the results. Unclear for which patients the baseline characteristics were provided. |
Likely
No intention-to-treat analysis, high rate of missing data |
|
Foster, 2020
& Konstantinou, 2020
SCOPiC trial |
Computerised
At the research clinic, eligible patients who gave written informed consent were randomly assigned by a computer-generated code, to either stratified care or usual care. Randomisation was done with a web-based service from Keele Clinical Trials Unit, and was stratified by centre and sciatica group allocation (sciatica groups 1, 2, and 3), by use of random permuted blocks of varying size (2, 4, and 6). |
Unlikely
Allocation not known before inclusion; computerized strategy by external service |
Likely
Patients were told that the trial was comparing two approaches for the treatment of sciatica, one based on matching patients to treatment by use of a simple tool that helps to decide on the treatment pathway, and one based on treatment needed as discussed and agreed between the patient and physiotherapist. |
Unlikely
To further help with allocation concealment, participants randomised to the UC arm of the trial were seen by physiotherapists who had not carried out their detailed clinical assessment and eligibility screen for the trial. Therefore, physiotherapists in the UC arm remained blinded to both the details of the stratification algorithm and the individual patient’s sciatica group status, hence avoiding contamination between the two trial arms. |
Unlikely
Statisticians and outcome assessors were masked to treatment allocation. |
Unlikely
Outcomes consistent with protocol; relevant sub group reporting |
Likely
% of non-responders s 12% and 10% for the primary outcome and 19% and 16% for the secondary outcomes. This is quite a high percentage and could induce a bias in the results. Costs and EQ-5D data were imputed to minimise bias. |
Likely
Not all patients were included in analysis; up to data available for 75% of the patients for the physical function (RMDQ) at 12 months. |
|
Hill, 2011 & Whitehurst 2012 |
Computerized
A clinic administrator telephoned a remote clinical trials unit (Keele University), which assigned participants to intervention and control groups by use of computer-generated stratified block randomisation (block sizes of three) in a 2:1 ratio to enable future secondary analysis of targeted treatment mechanisms. |
Unlikely
Administrator randomly assigned the patients; clinicians and research nurse no insight in allocation |
Likely
Participants, administrator, or physiotherapists could not be masked to randomisation […], however, we ensured that the therapists administering the control treatment were not made aware of the details of the stratified model of care during the trial, and that patients were made aware that they would be treated according to one of two primary care management models. |
Likely
Participants, administrator, or physiotherapists could not be masked to randomisation because therapists were administering the active intervention; however, we ensured that the therapists administering the control treatment were not made aware of the details of the stratified model of care during the trial, and that patients were made aware that they would be treated according to one of two primary care management models. |
Unlikely
The research nurse who retrieved outcome data was masked to randomisation, and the concealment strategies were that the nurse was in a separate office during clinic, the administrator randomly assigned the patients, and the use of a masked follow-up database. |
Unlikely
Elaborate protocol; announced outcomes reported; no questionable sub-group analyses |
Likely
In total, quite high rate of missing data / withdrawal (I: 22.5%, C: 26.1%), plus slight imbalance in attrition between the groups |
Unlikely
Analysis performed according to intention-to-treat analysis; missing data was imputed |
|
Hill, 2020 |
Computerised
Randomisation used stratified block randomisation based on GP practice list size to allocate the 8 practices in a ratio of 1:1 (4 intervention, 4 control). Keele Clinical Trials Unit (CTU) computer-generated the random sequence and ensured concealment by providing each practice with an anonymised code.
|
Unlikely
Keele Clinical Trials Unit (CTU) computer-generated the random sequence and ensured concealment by providing each practice with an anonymised code. |
Unlikely
Blinding for participating GPs was obviously not possible, however, patients were unaware of the RCT and the differences between consultations in intervention and control practices, and instead were informed about, and consented to, providing questionnaire data for a study investigating the Treatment of Aches and Pains (TAPs) |
Likely
Blinding for participating GPs was obviously not possible [..]
Allocation (at cluster and individual level) was shared with the study team (except for the trial statistician and outcome data collectors who were blinded until the analysis was finalised). |
Unlikely
Allocation (at cluster and individual level) was shared with the study team (except for the trial statistician and outcome data collectors who were blinded until the analysis was finalised). |
Unlikely
Outcomes consistent with trial, registered before study onset. |
Unlikely
Numbers provided per outcome; follow-up rate of > 75% with less than 5% missing items in participant questionnaires |
Likely
No intention-to-treat analysis, no data imputed; rate of missing data 9.1% (intervention) and 8.2% (control). |
|
Jamal, 2019 |
Computerised
The block randomization schedule was computer generated and conducted by an independent person, who was not involved in patient care. Randomization was stratified for the number of GPs working in the general practices (one or two vs. more than two) to ensure a similar number of patients in both groups. |
Unclear
Concealment of allocation not described and unclear at which moment allocation was known. |
Likely
Patients and GPs were unblinded, because of the nature of the intervention. |
Likely
Patients and GPs were unblinded, because of the nature of the intervention. |
Unlikely
Online questionnaire, by patient |
Likely
Outcomes not consistent or incomplete compared to protocol paper (effect on quality of life and costs not described) |
Likely
Percentage of missing data is relatively high and unequal between groups. Baseline: I: 18.9%, C: 11.3%; 4 months: I 35.1%, C: 22.5%.
|
Likely
No intention-to-treat analysis performed; linear mixed model allows for patients to have a missing outcome at either baseline visit or after 4 months (but not all (both) visits), but yields unbiased estimates in case the data is missing at random. |
Exclusietabel
|
Auteur en jaartal |
Redenen van exclusie |
|
Karran, 2017 |
Sluit niet aan bij PICO (P) |
|
Peterson, 2018 |
Sluit niet aan bij PICO (I) |
|
Van Der Windt, 2013 |
Studie design |
|
Van Hooff, 2014 |
Sluit niet aan bij PICO (I) |
|
Smink, 2013 |
Sluit niet aan bij PICO (I) |
|
Bair, 2009 |
Studie design |
|
Bier, 2018 |
Sluit niet aan bij PICO (I) |
|
Azevedo, 2013 |
Studie design |
|
Foster, 2017 |
Type publicatie |
|
Nicholas (2020) |
sluit niet aan bij PICO (P) |
|
Murphy, 2016 |
Studie design |
|
Morso, 2018 |
Type publicatie |
|
Murphy, 2013 |
Type publicatie |
|
Cherkin, 2016 |
Type publicatie |
|
Rebbeck, 2016 |
Type publicatie |
|
Rua, 2020 |
Type publicatie |
|
Suri, 2018 |
Studie design |
|
Schedlbauer, 2019 |
Type publicatie |
|
Kroenke, 2013 |
Type publicatie |
|
Lipton, 200 |
Sluit niet aan bij PICO (I) |
|
Knoop, 2020 |
Type publicatie |
|
Saunders, 2020 |
Studie design; |
|
Maselli, 2020 |
Studie design |
|
Taneja, 2014 |
Sluit niet aan bij PICO (P, I) |
|
Hussenbux, 2015 |
Sluit niet aan bij PICO (I) |
|
Button, 2019 |
Sluit niet aan bij PICO (P, I, C) |
|
Petit, 2015 |
Type publicatie |
|
Meyer, 2018 |
Revelante studies zijn individueel geïncludeerd |
|
Babatunde, 2020 |
Revelante studies zijn individueel geïncludeerd |
|
Smith, 2011 |
Type publicatie |
|
van Hooff, 2018 |
Studie design; Sluit niet aan bij PICO (I, O) |
|
Bishop, 2015 |
Sluit niet aan bij PICO (I, C) |
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 12-02-2026
Beoordeeld op geldigheid : 12-02-2026
Algemene gegevens
Goedgekeurd door:
- Nederlands Huisartsen Genootschap
- Samenwerkingsverband Pijnpatiënten naar één stem
- Nederlandse Vereniging van Rugpatiënten ‘de Wervelkolom‘
- Patiëntenfederatie Nederland
De ontwikkeling/herziening van deze leidraad werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de leidraad.
Samenstelling werkgroep
Voor het ontwikkelen van de leidraad zijn in 2020 een multidisciplinaire werkgroep en klankbordgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met chronische pijn. De werkgroep heeft de leidraad opgesteld, de leden uit de klankbordgroep hebben deze kritisch meegelezen. Naast deze groepen is in 2021 een werkgroep Haalbaarheid & Implementatie gevormd, welke: 1. Input heeft gegeven met betrekking tot de haalbaarheid, implementatie en randvoorwaarden voor toepassing van de leidraad; en 2. Het disseminatie- en implementatieplan heeft ontwikkeld.
Werkgroep leidraad
- Prof. dr. A. Wolff, anesthesioloog, NVA (voorzitter)
- Dr. H.R. Schiphorst Preuper, revalidatiearts, VRA (vicevoorzitter)
- Drs. Z. Damen, huisarts niet praktiserend en senior wetenschappelijk medewerker, NHG
- P. de Haan, ergotherapeut, EN
- E. de Jong, oefentherapeut, VvOCM
- Dr. B.C. ter Meulen, neuroloog, NVN
- Drs. C.J. van Oort, anesthesioloog, NVA
- Prof. dr. R.J.E.M. Smeets, revalidatiearts, VRA
- Drs. I.L. Thomassen-Hilgersom, patiëntvertegenwoordiger, Samenwerkingsverband pijnpatiënten naar één stem
- Dr. L.P. Voogt, lector complexe pijn, fysiotherapeut en manueel therapeut, KNGF
- Dr. L.N.L. Zonneveld, klinisch psycholoog, NIP
Meelezers leidraad
- G. Fennis-de Vries, MSc, pijnverpleegkundige, V&VN
- Drs. M.E. Havinga, orthopedisch chirurg, NOV
- Drs. J. Heering, huisarts en senior beleidsmedewerker, LHV
- G.R.M van Hoof, arts M&G, medisch adviseur, ZN
- Prof. dr. F.J.P.M. Huygen, anesthesioloog, pijnspecialist, NvNN
- Dr. P. van den Munckhof, neurochirurg, NVvN
-
J.F.A. van Kessel, Physician Assistant, NAPA
- Dr. A.J.A. Köke, senior onderzoeker en fysiotherapeut/bewegingswetenschapper KNGF
- Drs. R.L. Kriekaart, klinisch geriater, NVKG
- Dr. M.M. Lipvsky, internist en psychotherapeut, NIV
- Drs. C.H. Lunter, psychiater, NVvP
- H. Macleane, MPA, bedrijfskundig zorgmanager en physician assistant, NAPA
- R. Mali, oefentherapeut NCP, VvOCM
- R. van der Noord, MSc, fysiotherapeut, psychosomatisch fysiotherapeut en EFIC pijnfysiotherapeut, KNGF
-
K. Roeleveld, oefentherapeut NCP, psychosomatisch oefentherapeut, VvOCM
- V.M. Schoorlemmer, MSc, geriatrie oefentherapeut, VvOCM
- Dr. A.C.L.P.J. Verhoeven, bedrijfsarts, NVAB
- B.L. van der Vossen, MSc, chiropractor, NCA
- L. Voogt, patiëntvertegenwoordiger, NVVR
- H.W.A. Walravens, MANP, verpleegkundig specialist, V&VN
- Dr. T.R. Zijlstra, reumatoloog, NVR
Werkgroep haalbaarheid & implementatie
- Dr. L. Timmerman, NVA (Voorzitter)
-
R. Mali, oefentherapeut NCP, VvOCM
- M.P.G.J. Berkhout, VRA
- I. Bruaset, NVZ
- A. van der Gaag, NVA
- M. Horn, ZIN (toehoorder)
- G.R.M van Hoof, arts M&G, medisch adviseur, ZN
- M. Liedorp, ZKN
- Drs. M.J. Oostindiër, FMCC
- Drs. C. Ritoe, ZN (toehoorder)
- Dr. H.R. Schiphorst Preuper, revalidatiearts, VRA
- V.M. Schoorlemmer, MSc, geriatrie oefentherapeut, VvOCM
- Drs. J. Smale, VRA/RN
- Drs. I.L. Thomassen-Hilgersom, patiëntvertegenwoordiger, Samenwerkingsverband pijnpatiënten naar één stem
- Dr. L.P. Voogt, lector complexe pijn, fysiotherapeut en manueel therapeut, KNGF
- Prof. Dr. A. Wolff, anesthesioloog, NVA
- Dr. L.N.L. Zonneveld, klinisch psycholoog, NIP (meelezer)
Met ondersteuning van Kennisinstituut van de Federatie Medisch Specialisten:
- Dr. L.M.P. Wesselman, adviseur
- Dr. L.M. van Leeuwen, adviseur (vanaf maart 2023)
- Dr. S.N. Hofstede, senior adviseur (vanaf september 2022)
- Dr. D.H.H. Dreesens, senior adviseur (van april 2022 tot maart 2023)
- Dr. S. Persoon, senior adviseur (tot maart 2022)
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werk- en klankbordgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling van de leidraad zijn wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring zijn opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Werkgroep leidraad
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Wolff (Voorzitter) |
Anesthesioloog-pijnspecialist, medisch hoofd UMCG Pijncentrum Universitair Medisch Centrum Groningen Hoogleraar Anesthesiologie i.h.b. Pijngeneeskunde Rijksuniversiteit Groningen |
Bestuurslid stichting Helpelandsdoorn (onbetaald)
Beleidsadviseur VOLT (onbetaald) Co-voorzitter PA!N (onbetaald) Counsilor EFIC (onbetaald)klankbordgroep RL pijnrevalidatie (onbetaald) |
Extern gefinancierd onderzoek: ZonMw; AAL; Philips; Grünenthal; (investigator initiated onderzoek).
Consultancy of vergoedingen: Pfizer QPS, Equip, Novartis; NVA, NPZF, Overprikkeling |
Geen actie, alle subsidiegevers hebben geen belang bij adviezen uit de leidraad. |
|
Schiphorst Preuper |
Revalidatiearts, Universitair docent Afdeling Revalidatiegeneeskunde UMCG |
Voorzitter Werkgroep Pijnrevalidatie Nederland (WPN) van de VRA tot 2022 onbetaald; per 2022 lid WPN; Secretaris van de Pijnalliantie in Nederland (PA!N); van 2022 t/m 2023 lid algemeen bestuur PA!N, onbetaald; Lid van kernredactie NTPP t/m 2023, onbetaald; Lid van congrescommissie PA!N congres 2022 (08-12-2022), onbetaald; Lid van congrescommissie 18th International Forum on Back and Neck Pain Research in Primary Care 2023; (onbezoldigd) Werkgroeplid Richtlijn Pijnrevalidatie; vacatiegelden naar CvR UMCG; Per 2023 WECO van de VRA (lid); onbezoldigd. |
Geen |
Geen actie nodig |
|
Damen |
Senior wetenschappelijk medewerker/huisarts niet praktiserend bij het NHG |
Geen |
Betrokken bij de herziening van de NHG-standaard Pijn, op het gebied van toepassing opioïden bij chronische niet-oncologische pijn. |
Geen actie nodig |
|
De Haan |
Ergotherapeut Praktijkhouder ErgoAnders (gespecialiseerd in chronische pijn en vermoeidheid). Daarnaast 27,5 contracturen Roessingh Revalidatiecentrum |
Docent Pro-Education (NCOI) (betaald). Verzorging cursussen (betaald) Teamondersteuner RC Roessingh – betaald Lid Overleggroep Chronische pijn Ergotherapie Nederland (onbetaald).
|
|
Geen actie nodig |
|
De Jong |
Werkzaam als Oefentherapeut Cesar/Mensedieck in praktijk Isokin Training & Therapie voor 24 uur per week |
Bestuurslid Landelijk Netwerk Oefentherapeuten Chronische Pijn, (deels betaald, deels onbetaald) |
Bestuurslid bij Landelijk Netwerk Oefentherapeuten Chronische Pijn |
Geen actie nodig |
|
Smeets |
Hoogleraar Revalidatiegeneeskunde, Universiteit Maastricht (0,5 fte) Revalidatiearts, CIR revalidatie (0,6 fte) |
Lid van Wetenschappelijke Advies Raad patiëntenvereniging de Wervelkolom. Lid van Wetenschappelijk Advies Raad patiëntenvereniging HME/MO |
Geen |
Geen actie nodig |
|
Ter Meulen |
Neuroloog OLVG |
Raad van advies Nederlandse Vereniging van Rugpatiënten ‘de Wervelkolom’ |
Geen |
Geen actie nodig |
|
Thomassen-Hilgersom |
Vrijwilliger Samenwerkingsverband Pijnpatiënten naar één stem (onbetaald) |
Voorzitter patiëntenvereniging CRPS, vrijwilliger (onbetaald) |
Geen |
Geen actie nodig |
|
Van Oort |
Anesthesioloog-pijnbestrijder; Ikaziaziekenhuis en van Weel Bethesda ziekenhuis Dirksland |
Centraal Medisch Tuchtcollege (onkostenvergoeding) adviseur NVA (onkostenvergoeding) Medisch coördinator OK tot 1 juli 2021 (betaald) |
Geen |
Geen actie nodig |
|
Voogt |
Lector ‘Complexe pijn’ Hogeschool Rotterdam |
Visiting professor Vrije Universiteit Brussel. Lid commissie Zorgstandaard Chronische Pijn (KNGF). |
Geen |
Geen actie nodig |
|
Zonneveld |
Klinisch psycholoog, Amsterdam UMC, locatie AMC (Poli pijngeneeskunde) |
Voorzitter werkgroep ‘Somatisch-symptoomstoornis en verwante stoornissen’ van de Landelijke Vereniging Medische Psychologie (LVMP) (onbetaald) Voorzitter commissie ‘Financiering van het NIP en de LVMP’ (onbetaald) Bestuurslid PA!N (onbetaald) |
ZonMw, Amsterdams Universiteitsfonds |
|
Klankbordgroep leidraad
|
Klankbordgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Fennis-de Vries |
Verpleegkundig Specialist pijnkliniek
|
lid congrescommissie V&VN pijn (onbetaald) |
Geen |
Geen actie nodig |
|
Havinga |
Orthopedisch chirurg OCON |
Lid beroepsbelangen commissie NOV (onbetaald) |
Geen |
Geen actie nodig |
|
Heering |
beleidsadviseur Landelijke Huisartsen Vereniging |
huisarts (betaald) |
Geen |
Geen actie nodig |
|
Huygen |
Hoogleraar Anesthesiologie Erasmusmc (0,9 fte) Hoogleraar Anesthesiologie UMCU (0,1 fte) |
Lid Centraal tucht college (vacatiegeld). Lid wetenschappelijke adviesraad Patiëntenvereniging voor CRPS (Nederland en USA) (onbezoldigd). Director International Research Consortium CRPS (onbezoldigd). Lid Advisory Board Abbott, Boston Scientific, Saluda, Medtronic (bezoldigd). Voorzitter Vereniging voor Neuromodulatie Nederland (onbezoldigd). |
Geen |
Geen actie nodig. De leidraad richt zich niet op medicatie/medische technologie. |
| Van Kessel
|
Physician Assistant Libra revalidatie&audiologie locatie Blixembosch Eindhoven |
Geen |
Geen actie nodig |
Geen actie nodig |
|
Köke |
Senior onderzoeker, vakgroep revalidatiegeneeskunde Universiteit Maastricht 0,5 fte. Coordinator innovatie Kenniscentrum Adelante Hoensbroek 0,5 fte. |
Hoofdredacteur Nederlands Tijdschrift Pijn en Pijnbestrijding, (onbetaald). Vertegenwoordiger KNGF bij Pijn Alliantie Nederland, (onbetaald). |
Geen |
Geen actie nodig |
|
Kriekaart |
Tot oktober 2021: Klinische geriater Radboudumc. Klinisch geriater Sint Maartenskliniek. Waarnemend klinisch geriater Propersona, locatie Marie McKenzie, ouderenpsychiatrie. Vanaf oktober 2021: Klinisch geriater werkzaam in Gelre ziekenhuis Apeldoorn/Zutphen. |
Geen |
|
Geen actie nodig |
|
Lipovsky |
Internist en psychotherapeut, boegbeeld TOPGGZ, Altrecht Psychosomatiek Eikenboom |
Gastdocentschappen SOLK-communicatie voor medisch specialisten en AIOS, deels betaald, (ism Erasmus Medisch Centrum), deels onbetaald (UMCU e.a.). |
Geen |
Geen actie nodig |
|
Lunter |
Psychiater en boegbeeld TOPGGZ, Altrecht Psychosomatiek Eikenboom |
Bestuurslid landelijk Netwerk Aanhoudende Lichamelijke Klachten (NALK) – (onbetaald) Bestuurslid Pijn Alliantie In Nederland (PA!N) – (onbetaald) Enkele docentschappen – (betaald) |
Geen |
Geen actie nodig |
|
Macleane |
Physician assistant bij Excellent Klinieken, 85% Bestuurder bij Ecxellent Klinieken, 15% |
Geen |
Geen |
Geen actie nodig |
|
Van den Munckhof |
Neurochirurg Amsterdam UMC |
Geen |
Geen |
Geen actie nodig |
|
Van Hoof |
Medisch adviseur bij zorgverzekeraar bij CZ |
Lid commissie EEK van ZonMw |
Geen |
Geen actie nodig |
|
Schoorlemmer |
Geriatrie oefentherapeut, praktijk Oefentherapie in Kampen en in Lemmer. |
Ketenpartner vanuit Netwerk Oefentherapeuten Chronische Pijn bij Regionaal Pijncentrum Zwolle (onbetaald) |
Geen |
Geen actie nodig |
|
Van der Noord |
Praktijkeigenaar Interfysio, fysiotherapiepraktijk voor chronische pijn en psychosomatiek |
Wetenschappelijke Advies Raad (WAR) Psychosomatiek namens de Nederlandse vereniging voor Fysiotherapie volgens de Psychosomatiek (NFP) – alleen vergaderingen betaald. - Projectgroep Psychosomatische fysiotherapie binnen de GGZ (een NFP project) – Betaald - Projectgroep Visie op (chronische) pijn voor de fysiotherapeut, voor de Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF) – Betaald - Scholingen voor fysiotherapeuten op het gebeid van pijn diagnostiek en pijneducatie – betaald. |
Geven van scholingen op het gebied van diagnostiek en educatie bij chronische pijn voor fysiotherapeuten |
Geen actie nodig |
|
Roeleveld |
Praktijkeigenaar oefentherapie voor chronische pijn en neurologische aandoeningen BeweegBewust in Aalsmeer |
Regiocoördinator/voorzitter Parkinsonnet regio Amsterdam/Amstelland (onbetaald) |
Geen |
Geen actie nodig |
|
Van der Vossen |
Chiropractor, Chiropractie Epe |
Bestuurslid Stichting Chiropractie (onbetaald) |
Geen |
Geen actie nodig |
|
Verhoeven |
Instituutsopleider, bedrijfsarts en verzekeringsarts (0,8fte) |
Adviseur en docent via eigen bedrijf 'carco consult & medische advies' (betaald) |
Geen |
Geen actie nodig |
|
Voogt |
Voorzitter NVVR de Wervelkolom |
Geen |
Geen |
Geen actie nodig |
|
Walravens |
Verpleegkundig specialist, polikliniek Pijnbehandeling UMC Utrecht |
Incidenteel consultancy voor Grunenthal gericht op scholing neuropathische pijn |
Geen |
Geen actie nodig |
|
Zijlstra |
Reumatoloog, Isala, Zwolle |
Geen |
Geen |
Geen actie nodig |
Werkgroep haalbaarheid & implementatie
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Timmerman (voorzitter) |
Anesthesioloog-pijnspecialist St Antonius Ziekenhuis, Utrecht-Nieuwegein |
Hoofd afdeling R&D anesthesiologie, coördinatie wetenschappelijk onderzoek op gebied van anesthesiologie, IC en pijngeneeskunde. Onbetaald. |
Lid maatschap anesthesiologie, intensive care en pijngeneeskunde. |
Geen actie nodig |
|
Mali |
Oefentherapeut NCP, Praktijkeigenaar Haarlem Centrum & Velserbroek |
Voorzitter Platform Psychosomatiek & Netwerk Chronische Pijn VvOCM (bestuursvergoeding) Algemeen Bestuurslid PA!N (Pijn Alliantie in Nederland), als afgevaardigde namens de oefentherapeuten (onbetaald) Lid Congrescommissie PA!N (Pijn Alliantie in Nederland) (onbetaald) Voorzitter Regionaal Netwerk Chronische Pijn Haarlem/Haarlemmermeer e.o. (onbetaald) Voorzitter Patform oefentherapie Kennemerland & Haarlemmermeer (POKH) (onkostenvergoeding) |
Geen |
Geen actie nodig |
|
Berkhout |
Directeur Nederlandse Vereniging van Revalidatieartsen |
Bestuurslid stichting Revalidatie Impact. Onbetaald |
Geen |
Geen actie nodig |
|
Bruaset |
Medisch Manager Anesthesiologie en pijnbestrijding |
Geen |
Geen |
Geen actie nodig |
|
Van der Gaag |
Medisch Specialist Anesthesioloog - pijnspecialist |
Bestuurslid sectiebestuur pijn en pallitatieve geneeskunde Nederlandse Vereniging voor Anesthesiologie |
Geen |
Geen actie nodig |
|
Horn (toehoorder) |
Adviseur, Zorginstituut Nederland.
|
Geen |
Geen |
Geen actie nodig |
|
Van Hoof |
Medisch adviseur bij zorgverzekeraar bij CZ |
Lid commissie EEK van ZonMw |
Geen |
Geen actie nodig |
|
Liedorp |
Lid commissie - vertegenwoordiger ZKN |
lid MR basisschool IKC de Piramide (onbetaald) |
Geen |
Geen actie nodig |
|
Oostindiër |
Maxima Medisch Centrum (MMC): Beleidsadviseur huisartsenzorg w.o. secretaris bestuur FMCC |
Mede-eigenaar van medisch kwartier Eindhoven (onbezoldigd) 1e lijns gezondheidscentrum
|
Geen |
Geen actie nodig |
|
Ritoe |
Medisch Adviseur - Zorgverzekeraars Nederland |
Geen |
Geen |
Geen actie nodig |
|
Schoorlemmer |
Geriatrie oefentherapeut, praktijk Oefentherapie in Kampen en in Lemmer. |
Ketenpartner vanuit Netwerk Oefentherapeuten Chronische Pijn bij Regionaal Pijncentrum Zwolle (onbetaald) |
Geen |
Geen actie nodig |
|
Schiphorst Preuper |
Revalidatiearts, Universitair docent Afdeling Revalidatiegeneeskunde UMCG |
Voorzitter Werkgroep Pijnrevalidatie Nederland (WPN) van de VRA tot 2022 onbetaald; per 2022 lid WPN; Secretaris van de Pijnalliantie in Nederland (PA!N); van 2022 t/m 2023 lid algemeen bestuur PA!N, onbetaald; Lid van kernredactie NTPP t/m 2023, onbetaald; Lid van congrescommissie PA!N congres 2022 (08-12-2022), onbetaald; Lid van congrescommissie 18th International Forum on Back and Neck Pain Research in Primary Care 2023; (onbezoldigd) Werkgroeplid Richtlijn Pijnrevalidatie; vacatiegelden naar CvR UMCG; Per 2023 WECO van de VRA (lid); onbezoldigd. |
Geen |
Geen actie nodig |
|
Smale |
Beleidsadviseur |
Geen |
Geen |
Geen actie nodig |
|
Thomassen-Hilgersom |
Vrijwilliger Samenwerkingsverband Pijnpatiënten naar één stem (onbetaald) |
Voorzitter patiëntenvereniging CRPS, vrijwilliger (onbetaald) |
Geen |
Geen actie nodig |
|
Voogt |
Lector ‘Complexe pijn’ Hogeschool Rotterdam |
Visiting professor Vrije Universiteit Brussel. Lid commissie Zorgstandaard Chronische Pijn (KNGF). |
Geen |
Geen actie nodig |
|
Wolff |
Anesthesioloog-pijnspecialist, medisch hoofd UMCG Pijncentrum Universitair Medisch Centrum Groningen Hoogleraar Anesthesiologie i.h.b. Pijngeneeskunde Rijksuniversiteit Groningen |
Bestuurslid stichting Helpelandsdoorn (onbetaald)
Beleidsadviseur VOLT (onbetaald) Co-voorzitter PA!N (onbetaald) Counsilor EFIC (onbetaald)klankbordgroep RL pijnrevalidatie (onbetaald) |
Extern gefinancierd onderzoek: ZonMw; AAL; Philips; Grünenthal; (investigator initiated onderzoek).
Consultancy of vergoedingen: Pfizer QPS, Equip, Novartis; NVA, NPZF, Overprikkeling |
Geen actie, alle subsidiegevers hebben geen belang bij adviezen uit de leidraad. |
|
Zonneveld |
Klinisch psycholoog, Amsterdam UMC, locatie AMC (Poli pijngeneeskunde) |
Voorzitter werkgroep ‘Somatisch-symptoomstoornis en verwante stoornissen’ van de Landelijke Vereniging Medische Psychologie (LVMP) (onbetaald) Lid commissie ‘Financiering van de LVMP’ (onbetaald) Bestuurslid PA!N (onbetaald) |
ZonMw, Amsterdams Universiteitsfonds |
Geen actie nodig |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door het uitnodigingen de Nederlandse Vereniging van Rugpatiënten ‘de Wervelkolom’ (NVVR) en het Samenwerkingsverband pijnpatiënten naar één stem voor de invitational conference en de deelname van een afgevaardigde namens het Samenwerkingsverband in de werkgroep en van de NVVR in de klankbordgroep. De conceptleidraad is tevens voor commentaar voorgelegd aan het Samenwerkingsverband, de NVVR en Patiëntenfederatie Nederland en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase). Uit de kwalitatieve raming blijkt dat er geen substantiële financiële gevolgen zijn: het merendeel van de kosten van chronische pijn wordt niet veroorzaakt door medische kosten maar door indirecte maatschappelijke kosten door ziekteverzuim en presenteïsme. De verwachting is dat bij een betere organisatie van de pijnzorg deze kosten zullen afnemen. Een overzicht van uitkomsten van de kwalitatieve raming met bijbehorende toelichting vindt u in onderstaande tabel.
|
Module |
Uitkomst raming |
Toelichting |
|
Module Organisatie van de chronische pijnzorg |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt ook uit de toetsing dat het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht. |
|
Module Versterking eerste lijn |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt ook uit de toetsing dat het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht. |
|
Module Op- en afschalingscriteria |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt ook uit de toetsing dat het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Ten aanzien van de aanbevelingen
De voorgestelde aanbevelingen sluiten aan bij de wens van de overheid om meer in te zetten op taakherschikking en -verschuiving en de juiste zorg op de juiste plek. De implementatie zal echter veel aandacht vragen. Waar we in deze leidraad op landelijk niveau de grote lijnen beschrijven, zal de invulling vooral regionaal moeten gebeuren. De werkgroep acht het bijvoorbeeld belangrijk dat er regionaal/lokaal afspraken worden gemaakt over welke zorgprofessional(s) de verschillende taken op zich gaan nemen. Afhankelijk van de invulling zullen er ook afspraken moeten worden gemaakt over supervisie en de juridische aansprakelijkheid. Er zijn op dit moment nog een aantal algemene barrières voor implementatie, te weten:
- Financiering voor de inzet van de zorgprofessionals met expertise in pijnzorg.
- Er zijn op dit moment landelijk gezien te weinig – in chronische pijn geschoolde – professionals beschikbaar die in de eerste lijn kunnen worden ingezet. Voor de uitvoering van de beschreven taken bestaat nog geen specifieke opleiding. Als startpunt acht de werkgroep het gewenst dat de zorgprofessional minimaal is opgeleid in alle componenten zoals beschreven in het curriculum van de International Association for Study of Pain (IASP). In de toekomst zou het wenselijk zijn als voor de zorgprofessionals die deze taken gaan oppakken een beroepsprofiel, kwaliteitscriteria en opleiding beschikbaar komen.
Het veld zal tijd nodig hebben om deze barrières te overkomen. Met betrekking tot haalbaarheid en implementatie en randvoorwaarden daarvoor wordt verwezen naar het bijgaande Haalbaarheid & Implementatieplan.
Werkwijze
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de organisatie en werkwijze van de zorg voor patiënten met chronische pijn. Tevens zijn er knelpunten aangedragen door de NVA, VRA, KNMP, KNGF, NAPA, NCA, PA!N, Samenwerkingsverband pijnpatiënten naar één stem, VVOCM, VVGN, ZiNL, ZKN, NVVR en twee personen op eigen titel tijdens een invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep drie concept uitgangsvragen opgesteld en definitief vastgesteld. Deze drie vragen worden in afzonderlijke modules beantwoord. In de eerste module worden de knelpunten en gewenste situatie omschreven in de organisatie van chronische pijn zorg. In de laatste twee modules wordt er respectievelijk ingezoomd op twee specifieke aspecten binnen de organisatie van de pijnzorg: de versterking van de eerste lijn en de op- en afschalingscriteria. Bij de ontwikkeling van deze modules is de gangbare richtlijnmethodiek gevolgd. Deze methodiek voldoet aan de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit, welke is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010). De methodiek wordt in de onderstaande paragrafen toegelicht. De gehanteerde werkwijze wordt in de overwegingen van de deze module verder toegelicht.
Voor de modules ‘Organisatie van de chronische pijnzorg’ en ‘Op- en afschalingscriteria’
Er zijn zorgpaden uitgewerkt die beschrijven en visueel weergeven welk traject de patiënt doorloopt wanneer er sprake is van (een vermoeden van) chronische pijn. Hiervoor werden vier werksessies en een focusgroep georganiseerd. De vier werksessies werden gehouden bij verschillende lokale samenwerkingsverbanden voor chronische pijn (regio’s Maastricht, Sneek, Eindhoven en Zwolle). Hierbij waren verschillende zorgverleners en patiëntvertegenwoordigers aanwezig. Daarnaast is een focusgroep gehouden met patiënten. Naast het uitwerken van de zorgpaden werden beïnvloedende factoren voor het doorlopen van de zorgpaden geïnventariseerd, en werden mogelijke oplossingsrichtingen om de beïnvloedende factoren te overwinnen in het zorgpad besproken. Tevens werden op- en afschalingscriteria besproken.
Voor de modules ‘Versterking van de eerste lijn’ en ‘Op- en afschalingscriteria’
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep (inclusief patiëntvertegenwoordiger) welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep (waaronder de patiëntvertegenwoordiger) tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch relevant (voor de patiënt) vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in kwaliteitsstandaarden volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Voor alle modules
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende gebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van de chronische pijnzorg. Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag zijn genoemd bij de overwegingen.
Commentaar- en autorisatiefase
De concept leidraad werd schriftelijk aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep, waarna een tweede commentarenronde volgde. Daarna is de aangepaste leidraad besproken tijdens een tweede invitational conference. Naar aanleiding van de twee commentaarrondes en de input tijdens de tweede invitational conference werd de conceptleidraad aangepast en definitief vastgesteld door de werkgroep. De definitieve leidraad werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwaliteit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Zoekverantwoording
Algemene informatie
|
Richtlijn: Leidraad Organisatie en werkwijze zorg voor patiënten met chronische pijn |
|
|
Uitgangsvraag: Wanneer is escalatie en de-escalatie binnen de chronische pijnzorg geïndiceerd? |
|
|
Database(s): Ovid/Medline, Embase |
Datum: 25-01-2021 |
|
Periode: 2000 - heden |
Talen: Engels, Nederlands |
|
Literatuurspecialist: Miriam van der Maten |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting en opmerkingen:
|
|
|
Te gebruiken voor richtlijnen tekst: In de databases Embase.com en Ovid/medline is op 25-01-2021 met relevante zoektermen gezocht naar systematische reviews, randomized controlled trials en observationele studies over escalatie en de-escalatie criteria binnen de chronische pijnzorg. De literatuurzoekactie leverde 1952 unieke treffers op. |
|
Zoekopbrengst
|
|
Embase |
OVID/MEDLINE |
Ontdubbeld |
|
SRs |
114 |
72 |
186 |
|
RCT |
357 |
276 |
633 |
|
Observationeel |
558 |
575 |
1133 |
|
Totaal |
1040 |
1575 |
1952 |
Zoekstrategie
Embase
|
No. |
Query |
Results |
|
#13 |
#10 OR #11 OR #12 |
1040 |
|
#12 |
#6 AND #9 NOT (#10 OR #11) = observationeel |
563 |
|
#11 |
#6 AND #8 NOT #10 = RCT |
360 |
|
#10 |
#6 AND #7 = SR |
117 |
|
#9 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'cohort analysis'/de OR cohort*:ab,ti OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
5861214 |
|
#8 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
3212295 |
|
#7 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
700542 |
|
#6 |
#1 AND (#2 OR #3 OR #4 OR #5) AND ([english]/lim OR [dutch]/lim) AND [2000-2021]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) |
1576 |
|
#5 |
'patient referral'/exp/mj OR gatekeep*:ti,ab,kw OR referring:ti,kw OR referral:ti,kw |
43277 |
|
#4 |
'integrated health care system'/exp OR (((integrated OR network) NEAR/3 ('health care' OR medicine OR healthcare)):ti,ab,kw) |
21813 |
|
#3 |
'interdisciplinary communication'/exp OR (((interdisciplinary OR 'inter-disciplinary' OR 'cross-disciplinary' OR 'multi-disciplinary' OR multidisciplinary OR 'trans-disciplinary' OR transdisciplinary) NEAR/1 communication*):ti,ab,kw) |
13345 |
|
#2 |
'stratified medicine'/exp OR 'stepped care'/exp OR ((care NEAR/3 (stepped OR stratified OR matched)):ti,ab,kw) OR 'risk stratification':ti,ab,kw OR ((criteria NEAR/2 (referring OR referral OR escalation OR 'de-escalation')):ti,ab,kw) |
62296 |
|
#1 |
'chronic pain'/exp OR 'complex regional pain syndrome'/exp/mj OR 'low back pain'/exp/mj OR 'fibromyalgia'/exp/mj OR 'rheumatic disease'/exp/mj OR 'whiplash injury'/exp OR 'neuropathic pain'/exp OR 'headache'/exp/mj OR 'abdominal pain'/exp/mj OR 'visceral pain'/exp/mj OR 'pelvic pain'/exp/mj OR 'pelvic girdle pain'/exp/mj OR 'neuralgia'/exp/mj OR 'musculoskeletal pain'/exp/mj OR 'fibromyalgia':ti,ab,kw OR 'rheuma*':ti,ab,kw OR 'whiplash*':ti,ab,kw OR 'headache*':ti,ab,kw OR 'head ache*':ti,ab,kw OR neuralgia:ti,ab,kw OR ((chronic NEAR/3 pain):ti,ab,kw) OR (((longterm OR 'long term') NEAR/2 pain):ti,ab,kw) OR 'complex regional pain':ti,ab,kw OR 'musculoskeletal pain':ti,ab,kw |
723661 |
Ovid/Medline
|
# |
Searches |
Results |
|
14 |
11 or 12 or 13 |
1575 |
|
13 |
(7 and 10) not (11 or 12) = observationeel |
951 |
|
12 |
(7 and 9) not 11 = RCT |
475 |
|
11 |
7 and 8 = SR |
149 |
|
10 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort*.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ |
3781407 |
|
9 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2262917 |
|
8 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
502056 |
|
7 |
limit 6 to (english language and yr="2000 -Current") |
2723 |
|
6 |
1 and (2 or 3 or 4 or 5) |
3590 |
|
5 |
exp "Referral and Consultation"/ or gatekeep*.ti,ab,kf. or referring.ti,kf. or referral.ti,kf. |
89022 |
|
4 |
exp "Delivery of Health Care, Integrated"/ or ((integrated or network) adj3 ('health care' or medicine or healthcare)).ti,ab,kf. |
20276 |
|
3 |
exp *Interdisciplinary Communication/ or ((interdisciplinary or 'inter-disciplinary' or 'cross-disciplinary' or 'multi-disciplinary' or multidisciplinary or 'trans-disciplinary' or transdisciplinary) adj1 communication*).ti,ab,kf. |
7320 |
|
2 |
((care adj3 (stepped or stratified or matched)) or 'risk stratification' or (criteria adj2 (referring or referral or escalation or 'de-escalation'))).ti,ab,kf. |
36347 |
|
1 |
exp Chronic Pain/ or exp *"Complex Regional Pain Syndromes"/ or *"Low Back Pain"/ or *Fibromyalgia/ or exp *"Rheumatic Diseases"/ or exp *"Whiplash Injuries"/ or exp *Neuralgia/ or exp *Headache/ or exp *"Abdominal Pain"/ or exp *"Visceral Pain"/ or exp *"Pelvic Pain"/ or exp *"Pelvic Girdle Pain"/ or exp *"Musculoskeletal Pain"/ or 'fibromyalgia'.ti,ab,kf. or 'rheuma*'.ti,ab,kf. or 'whiplash*'.ti,ab,kf. or 'headache*'.ti,ab,kf. or 'head ache*'.ti,ab,kf. or neuralgia.ti,ab,kf. or (chronic adj3 pain).ti,ab,kf. or ((longterm or 'long term') adj2 pain).ti,ab,kf. or 'complex regional pain'.ti,ab,kf. or 'musculoskeletal Pain'.ti,ab,kf. |
497567 |