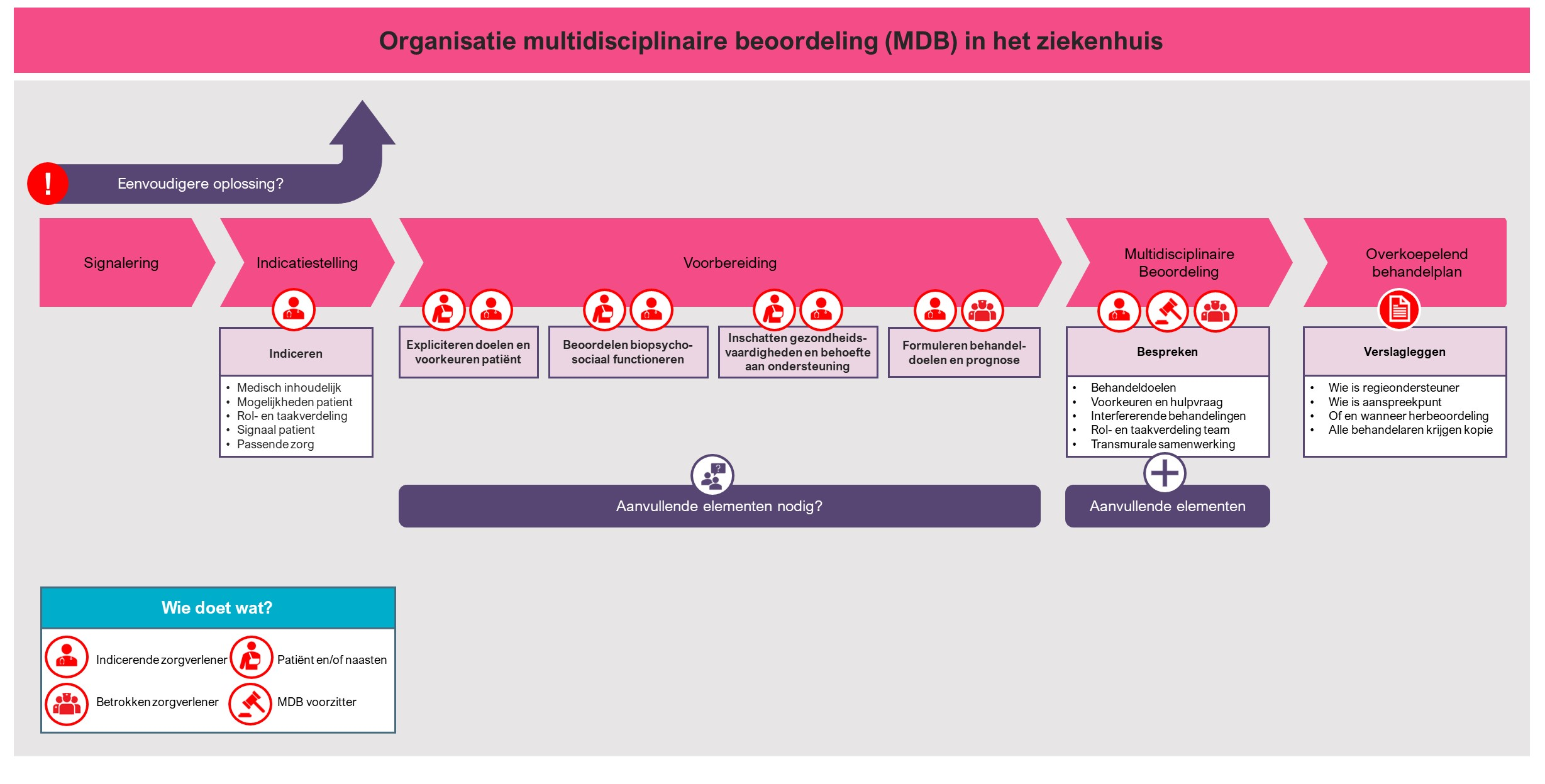
Organisatie van een multidisciplinaire beoordeling
Uitgangsvraag
Hoe geef je de multidisciplinaire beoordeling vorm in het ziekenhuis?
Aanbeveling
Aanbeveling-1
Streef naar maatwerk bij de organisatie van een MDB:
- Stel een overkoepelend en afgestemd behandelplan op in een basis MDB en laat hierbij de doelen, voorkeuren en mogelijkheden van de patiënt leidend zijn
- Voeg aanvullende elementen, afgestemd op de problematiek en biopsychosociale context van de individuele patiënt, toe aan de basis om tot een uitgebreider MDB te komen
Aanbeveling-2
Kies een model voor het opzetten van de MDB die past bij de lokale situatie in eigen ziekenhuis.
Overweeg de volgende opties:
- Vraag leidend: afhankelijk van de problematiek wordt per individuele patiënt gekozen voor een basis MDB of aangevuld met aanvullende elementen
- Initieel uitgebreid: starten met de meest complexe patiënten in het ziekenhuis en voor hen een uitgebreid MDB organiseren
- Stepped care: starten met een basis MDB voor alle patiënten zonder aanvullende elementen. Wanneer dit niet toereikend is, in een latere fase een tweede MDB organiseren met aanvullende elementen.
Overwegingen
In de literatuur wordt gesteld dat de patiënt met meerdere chronische aandoeningen gebaat is bij een behandeling waarbij de behandelaren de zorg onderling afstemmen, en de behandeling afgestemd is op de doelen, voorkeuren en mogelijkheden van de patiënt (35–37). Echter, de literatuur biedt maar beperkt handvatten hoe dit in de praktijk, in de spreekkamer óf op organisatieniveau, vorm te geven (zie Bijlage C). De voorbeelden die er zijn, zijn behoorlijk arbeidsintensief. Gezien de heterogeniteit van de patiënten met meerdere chronische aandoeningen, is het goed voor te stellen dat de intensiteit van de beoordeling mede afhankelijk is van de ernst van de problematiek, het aantal chronische aandoeningen en behandelaren, en het algemeen, cognitief en sociaal functioneren van de patiënt. Wat in de ene situatie noodzakelijk is, is in de andere situatie niet doelmatig. Om een beweging naar patiëntgerichte zorg bij multimorbiditeit op gang te krijgen, heeft de werkgroep drie doelen voor ogen: 1) een beoordeling op maat die aansluit bij de individuele patiënt met meerdere chronische aandoeningen, 2) aansluiten bij de huidige dagelijkse praktijk in het ziekenhuis, en 3) aansluiten bij de beweging naar maatschappelijk verantwoorde passende zorg.
Om te waarborgen dat de adviezen van de werkgroep aansluiten bij de dagelijkse praktijk werd hier uitgebreid aandacht aan besteed tijdens de focusgroepen met behandelaren in de tweede lijn (zie Bijlage B), en tijdens de focusgroep met huisartsen (zie Bijlage E). Ook werd er zorgvuldig gezocht naar kwaliteitsdocumenten over het multidisciplinair overleg om te verzekeren dat wij alle elementen in deze leidraad beschrijven.
Tijdens de focusgroepen en het bespreken van casuïstiek kwam naar voren dat de huidige werkwijze tekort kan schieten voor een groep complexe patiënten. De MDB introduceren wij als een nieuwe manier van multidisciplinaire samenwerking, die niet in alle scenario’s nodig zal zijn maar in sommige ook nadrukkelijk wel.
Wanneer er problematiek op meerdere vlakken speelt, zoals medische complexiteit i.e. (zoals interfererende behandelingen), onduidelijke rolverdeling van het behandelteam, en (mogelijk) disproportionele zorg, en er ook meerdere uitkomsten worden beoogd zoals het incorporeren van doelen, voorkeuren en mogelijkheden van de patiënt en het verminderen van zorggebruik, dan lijkt een MDB een doelmatige interventie. Omdat patiënten met meerdere chronische aandoeningen een heterogene groep zijn, is er geen ‘one MDB fits all’. Om maatwerk te kunnen bieden wordt er dus gekozen om een basis MDB te beschrijven, die is uit te breiden met aanvullende elementen tot een uitgebreide vorm. Voor een basis MDB is een minimale set aan gegevens noodzakelijk, die altijd vooraf geïnventariseerd en in de MDB besproken moet worden. Daarnaast zijn er nog aanvullende elementen, die de behandelaar kan toevoegen aan de basis MDB op geleide van de behoefte van patiënt en behandelaar. Zo biedt de MDB maatwerk voor de individuele patiënt. De uitgebreide vorm bestaat dus uit zowel de basis- als de facultatieve elementen. Zie figuur 3 voor een visuele weergave van dit proces.
In dit hoofdstuk worden de volgende onderdelen van de organisatie van een MDB in meer detail beschreven: signaleren en verwijzen, indicatiestelling en voorbereiding, inhoud, setting, team, het betrekken van de patiënt en diens naasten, en de verslaglegging. Bij het toelichten van de verschillende onderdelen wordt ook aangegeven waar er verschillen zijn tussen de basis en de uitgebreide MDB. Daarnaast beschrijft de werkgroep een aantal randvoorwaarden waaraan moet worden voldaan om een MDB te kunnen organiseren. Tot slot beschrijven wij een aantal modellen waaruit gekozen kan worden om de MDB binnen de eigen ziekenhuisorganisatie te introduceren.
Signaleringsfunctie
In hoofdstuk 2 werd toegelicht hoe de patiënt herkend kan worden die mogelijk gebaat is bij het opstellen van een overkoepelend en afgestemd behandelplan. Omdat de negatieve gevolgen van gefragmenteerde zorg zich kunnen uiten op verschillende vlakken, kunnen deze dus ook herkend worden door verschillende partijen. De werkgroep is daarom van mening dat alle betrokken zorgverleners van de patiënt, inclusief de huisarts, verpleegkundigen en paramedici, maar ook de patiënt en diens naasten zelf, een signaleringsfunctie bekleden.
Huisarts, verpleegkundigen, paramedici, patiënten en naasten kunnen het verzoek voor een MDB neerleggen bij ieder betrokken medisch specialist, ziekenhuisarts, VS of PA, in de tweede lijn. Een patiënt hoeft dus niet verwezen te worden voor een MDB, omdat dit verzoek neergelegd wordt bij een reeds betrokken behandelaar. Er zijn verschillende routes denkbaar om het verzoek te doen voor een MDB (bijvoorbeeld digitale brief, telefonisch contact), en het is belangrijk dat er heldere lokale afspraken gemaakt worden hoe dit het beste in te vullen. Als het een behandelaar in de tweede lijn is die signaleert, dan gaat deze behandelaar zelf over tot de indicatiestelling.
Indicatiestelling en voorbereiding
De indicatiestelling en voorbereiding kan door ieder betrokken medisch specialist, VS of PA worden gedaan in de tweede lijn. Het heeft wel de voorkeur dat dit gedaan wordt door een behandelaar met generalistische competenties. Onder generalistische competenties verstaat de werkgroep het vermogen om een patiënt in kaart te brengen volgens het biopsychosociale model (38) of een beoordeling over meerdere assen, zoals bij een geriatrisch assessment (anders dan het Comprehensive Geriatric Assessment) (39), het herkennen van interfererende behandelingen en/of interventies, discipline-overstijgend denken, en consultvoering volgens het model Samen Beslissen (40,41). Zie infobox 1 voor meer uitleg over deze competenties. De werkgroep benadrukt dat het beschikken over deze generalistische competenties niet is voorbehouden voor enkele beschouwende specialismen, maar juist competenties zijn die gedeeld kunnen worden door medisch specialismen. Wel zal dit voor de ene medisch specialist meer natuurlijk en passend zijn, dan voor de andere. Bij de keuze voor regieondersteuning mag daar ook aandacht voor zijn.
De behandelaar die een indicatie voor MDB signaleert of het verzoek binnenkrijgt voor een MDB beoordeelt allereerst of er een eenvoudige oplossing bestaat zoals (telefonisch) overleg met een collega, of dat er binnen de huidige werkwijze een oplossing te vinden is, zonder direct extra behandelaren te betrekken. Een eenvoudige oplossing heeft uiteraard de voorkeur. Bestaat die oplossing niet, en is een overkoepelende en afgestemde behandeling het antwoord op de hulpvraag, dan is de indicatie voor een MDB gesteld.
Infobox 1. Generalistische competenties
|
Biopsychosociale model: in dit model, ontwikkeld door internist-psychiater George Engel, worden gezondheid, ziekte en functioneren benaderd vanuit zowel de biologische (o.a. pathofysiologie en epidemiologie), en psychologische, als sociale, spirituele/zingevings- en culturele componenten van gezondheidsklachten of symptomen. Meer informatie vindt u in hoofdstuk 1 van dit document.
(Comprehensive) Geriatric Assessment ((C)GA): Bij een geriatric assessment (GA) brengt een behandelaar (niet geriater of internist-ouderengeneeskunde) zelf de kwetsbaarheden globaal in kaart op de vier verschillende domeinen (somatisch, psychisch, functioneel en sociaal). Dit is anders dan het comprehensive geriatric assessment (CGA).Het CGA is een uitgebreid geriatrisch onderzoek. Tijdens dit onderzoek worden de vier assen uitgebreid beoordeeld door een klinisch geriater of internist ouderengeneeskunde. Meer informatie vindt u hier.
Samen Beslissen: een proces waarin zorgprofessional en patiënt samen bespreken welke behandeling of zorg het beste bij de patiënt past. Hierbij worden alle opties, voor- en nadelen, voorkeuren en omstandigheden van de patiënt meegenomen. Meer informatie vindt u hier. Een aangepast model voor kwetsbare ouderen vindt u hier, welke ook zeer toepasbaar is voor de patiënt met multimorbiditeit omdat in dit model meer aandacht is voor de doelen van de patiënt. |
Als de behandelaar in het ziekenhuis de noodzaak voor een MDB signaleert, maar zich niet bekwaam voelt in het indiceren van de MDB, dan kan deze verantwoordelijkheid in overleg belegd worden bij een collega die reeds deel uitmaakt van het behandelteam van de patiënt. Mocht er geen behandelaar betrokken zijn die over generalistische competenties beschikt, dan kan daar eventueel naar verwezen worden maar dat heeft niet de voorkeur.
De voorbereiding wordt gedaan door degene die de indicatie stelt. Door de voorbereiding te treffen zal ook de indicatie steeds scherper worden. Afhankelijk van de problematiek die speelt zal de basis MDB wel of niet toereikend zijn. Deze afweging wordt gemaakt door degene die de indicatie stelt. Tabel 3 geeft de verschillende onderdelen weer die horen bij de voorbereiding, en welke van die onderdelen deel uitmaken van de voorbereiding van een basis MDB.
Degene die de basis MDB voorbereidt is er verantwoordelijk voor dat, met de patiënt en eventuele naasten, o.a. in kaart is gebracht wat de behandel- en functionele doelen zijn van de patiënt, en inzicht is verkregen in het biopsychosociaal functioneren. Dit kan uitgevoerd worden door een medisch specialist, ziekenhuisarts, physician assistant of verpleegkundig specialist.
De werkgroep raadt aan om tijdens de voorbereiding de verbinding te zoeken met de eerste lijn. In de focusgroep gaven huisartsen ook aan graag informatie aan te willen leveren voorafgaand aan een MDB zoals de hulpvraag van de patiënt, informatie met betrekking tot de sociale kaart (wie staan er om de patiënt heen, is mantelzorg mogelijk, etc.), aanvullen van de voorgeschiedenis, en afspraken met betrekking tot Advance Care Planning. Bij voorkeur leveren zij deze informatie digitaal aan via ZorgDomein. Er kunnen ook vragenlijsten opgesteld worden die meegegeven worden aan patiënten om op die manier aanvullende informatie te verzamelen.
|
Algemene doelen: deze doelen geven weer hoe de patiënt in het leven staat. Staat kwaliteit van leven voorop, of verlenging van het leven? Maar ook: wat betekent kwaliteit van leven voor de patiënt? Wat draagt daaraan bij? Voorbeeld: zo lang mogelijk thuis wonen en in de tuin kunnen werken
Functionele doelen: deze doelen hebben betrekking op het verminderen van functionele beperkingen, en wat daarin belangrijk is. Is het belangrijk om zelfstandig nog boodschappen te kunnen doen, of om zichzelf zelfstandig om te kunnen kleden? Wat zijn belangrijke prioriteiten voor de patiënt? Voorbeeld: de knieën kunnen buigen om een algemeen doel, in de tuin werken, te kunnen bereiken
Ziekte-specifieke doelen: deze doelen hebben betrekking op de behandeldoelen voor een specifieke ziekte of symptoom. Wat willen arts en patiënt samen bereiken in de behandeling, en wat heeft de patiënt daarvoor over en wat vindt diegene belangrijk? Bijvoorbeeld: wil de patiënt regelmatig naar het ziekenhuis komen voor controles, of niet? Wil de patiënt een diagnostisch traject door, of geeft diegene de voorkeur aan symptoomreductie zonder diagnostiek?
Voorbeeld: pijnbestrijding bij artrose op een zo min mogelijk invasieve manier, om zo het functionele doel en algemene doel te kunnen bereiken. |
Infobox 2. Expliciteren van doelen (40)
Mocht deze informatie grotendeels ontbreken, dan is het waardevol om de patiënt uit te nodigen op de polikliniek. In andere gevallen kan het mogelijk volstaan op telefonisch een aantal aanvullende vragen te stellen aan de patiënt en/of naasten.
Bij het in kaart brengen van algemene behandeldoelen en functionele doelen (37,42), zijn belangrijke vragen o.a.: Staat zelfredzaamheid centraal, of is symptoomreductie belangrijk? Staat kwaliteit van leven of levensduur voorop? Het expliciteren van doelen is belangrijk bij keuzes in de aanpak van multiproblematiek (43). Zie infobox 2 voor meer informatie over het expliciteren van doelen. Ook voorkeuren worden in kaart gebracht door de initiatiefnemer ten aanzien van de te maken beslissingen tijdens de MDB zoals wie is de regieondersteuner en het aanspreekpunt. Tevens is het belangrijk om te achterhalen welk resultaat de patiënt graag behaald ziet na de MDB én, als het lukt, een kernprobleem te identificeren. Daarna brengt diegene de patiënt globaal in kaart met betrekking tot algemeen en psychosociaal functioneren door het bundelen van de beschikbare informatie uit het (EPD) en vult dit aan met informatie van de patiënt en naasten. Dit geeft een indruk van de mogelijkheden van de patiënt (draagkracht t.a.v. behandelingen, uitvoeren van leefstijladviezen, etc.). Alle andere betrokken behandelaren zijn ieder verantwoordelijk om informatie aan te dragen over hun eigen medische domein (ziekte-specifieke behandelplan en -doel) tijdens de MDB.
Tijdens de voorbereiding van de MDB, kan het zijn dat de behandelaar op specifieke problemen stuit die maken dat de patiënt vastloopt in de zorg die geleverd werd. Bijvoorbeeld, er ontstaat een vermoeden op nog niet onderkende cognitieve problemen, die wél meegenomen moeten worden in de overwegingen m.b.t. toekomstige behandelplannen. Of er speelt problematiek op financieel gebied die, zonder de juiste ondersteuning, behandeling belemmert. Tabel 5 geeft een overzicht van voorbeelden van facultatieve elementen die kunnen worden toegevoegd aan de hand van de problematiek die speelt. Dit is geen uitputtende tabel maar geeft een indruk van waar men aan kan denken. Met behulp van deze elementen wordt het uitgebreidere MDB ingericht op maat. Deze werkwijze sluit aan bij het adviesrapport ‘Multimorbiditeit en Regie in het ziekenhuis’(7), waarin beschreven staat dat regievoering een glijdende schaal is, waarbij de intensiteit van de interventie toeneemt als de problematiek toeneemt.
Tabel 3. Voorbereiding basis MDB
|
Onderwerp |
Taak/Uitleg |
Bron |
|
Personalia |
Leeftijd, geslacht |
EPD |
|
Relevante voorgeschiedenis (ook uit andere ziekenhuizen) en actieve diagnosen |
Maak een op logische wijze en overzichtelijk gegroepeerd overzicht van de voorgeschiedenis met daarin verwerkt:
|
EPD |
|
Psychiatrische comorbiditeit |
Noteer actuele psychische klachten en psychiatrische comorbiditeit. |
EPD |
|
Medicatielijst |
Maak een medicatieoverzicht met daarin verwerkt:
|
EPD, LSP |
|
Actuele behandelaren, behandelingen (inclusief behandeldoel) |
Maak een overzicht van de betrokken behandelaren en hun behandelingen. Geef aan voor welke behandelaren betrokkenheid bij een MDB cruciaal is (ook niet medisch specialisten). Vraag hen een ziekte specifiek behandeldoel en prognose ten aanzien van hun eigen behandeltraject te formuleren. |
EPD Betrokken behandelaren |
|
Doelen, voorkeuren en hulpvraag van patiënt |
Vraag na bij de patiënt:
|
Patiënt (evt. mantelzorger) |
|
Behoefte regieondersteuning |
Maak een inschatting van gezondheidsvaardigheden en de behoefte aan ondersteuning. |
Patiënt (evt. mantelzorger) |
|
Functionele beperkingen en psychische klachten |
Verzamel beschikbare gegevens ten aanzien van:
|
EPD |
|
Andere relevante zaken |
Denk bv aan
|
EPD |
Inhoud
Tabel 4 geeft een volledig overzicht van de verschillende elementen die deel uitmaken van een basis MDB. Tijdens deze afstemming wordt o.a. zorg gedragen dat 1) de behandeldoelen van de behandelaren aansluiten bij de behandeldoelen van de patiënt 2) de behandelingen aansluiten bij het biopsychosociaal functioneren en prognose van de patiënt 3) het behandelregime zo optimaal mogelijk is 4) er een proactief behandelplan is met aandacht voor preventie van acute escalaties 5) heldere rol en taakverdeling met het afschalen van zorg waar dat mogelijk is.
Tabel 5 geeft voorbeelden van verschillende elementen die deel kunnen uitmaken van een uitgebreider MDB, weergegeven aan de hand van domeinen (somatisch, functioneren, psychisch, sociaal). Elementen kunnen worden toegevoegd aan de hand van problemen die worden gesignaleerd tijdens de voorbereiding. Zo kan er sprake zijn van farmacotherapie gerelateerde problemen en kan een ziekenhuisapotheker of openbaar apotheker worden betrokken om een medicatiereview te doen. Er kan een vermoeden bestaan op kwetsbaarheid omdat er veel complicaties optreden van behandelingen waardoor een (comprehensive) geriatric assessment (CGA) geïndiceerd kan zijn. Ook kan er een vermoeden zijn op een overbelaste patiënt of steunsysteem waardoor er behoefte is aan ondersteuning. Door alert te zijn op problematiek die speelt op biopsychosociaal vlak, en hier de juiste ondersteuning in te zetten (vaak met behulp van de eerste lijn en paramedici), kan problematiek (en zorggebruik) op langere termijn worden voorkomen.
Zie bijlage I voor casuïstiek voor een illustratie van een basis MDB.
Tabel 4. Basiselementen van een MDB bespreking
|
Elementen |
Doel |
|
De aanleiding van de beoordeling en door wie dit werd gesignaleerd |
Indicatie voor de MDB is helder |
|
Doelen, voorkeuren en hulpvraag van patiënt |
Doelen van de patiënt zijn voor het hele behandelteam helder, daarbij worden ook de (on)mogelijkheden besproken die voortvloeien uit de beoordeling van het biopsychosociaal functioneren |
|
De actuele klachten en problemen aan de hand van prioritering door patiënt (niet limiterend tot het somatische domein) |
Prioritering van klachten en problemen zijn helder |
|
Behandeldoelen en verwachtingen van alle behandeltrajecten t.a.v. mogelijkheden en prognose |
Het doel en prognose van iedere behandeling is besproken en beoordeeld of dit past binnen de doelen, voorkeuren en mogelijkheden van de patiënt |
|
Interferentie van behandelingen, ziekten, medicatie, dieet- en leefstijladviezen |
Optimaal en zo eenvoudig mogelijk behandelregime voor de patiënt, waarbij leefstijladviezen geïntegreerd zijn en medicatieschema’s in het dagritme passen |
|
De voor- en nadelen van (toekomstige) behandelingen |
Duidelijk proactief behandelplan voor de nabije toekomst met aandacht voor preventie van acute escalaties |
|
Taak- en rolverdeling van het behandelteam in de tweede lijn |
Heldere afspraken onderling, én een aangewezen regieondersteuner en aanspreekpunt voor de patiënt. Streef naar een beperking van het aantal afspraken en aantal behandelaren. Streef naar zoveel mogelijk gecombineerde diagnostiek en zorg. Behandel zoveel mogelijk in de thuissituatie en in de eerste lijn. |
|
Transmurale samenwerking |
Afgestemde behandeling met de huisarts, specialist ouderengeneeskunde, medewerker GGZ, psychiater, apotheker en/of andere betrokken zorgverleners |
|
Herbeoordeling en bespreking |
Een MDB heeft geen vaste frequentie. Een herbeoordeling kan op maat worden afgesproken |
Tabel 5. Aanvullende elementen voor een MDB
|
SOMATISCH |
||||
|
Probleem |
Element |
Bron/betrokkenen |
Taken |
Doel |
|
Medicatiereview |
Ziekenhuisapotheker, openbaar apotheker en/of poliklinisch apotheker. Zie richtlijn ‘Polyfarmacie bij ouderen’ |
Medicatiereview met behulp van Systematic Tool to Reduce Inappropriate Prescribing (STRIP) |
Optimaal en zo eenvoudig mogelijk medicatieschema met een begrijpelijk overzicht voor patiënt en gepaste ondersteuning voor medicatiebeheer |
|
Cardiovasculair risicomanagement |
Leefstijlloket, huisarts |
Maak een overzicht van betrokken paramedici Optimaliseren leefstijl, voeding en beweging |
Optimaal cardiovasculair risicomanagement passend bij doelen, voorkeuren en mogelijkheden |
|
FUNCTIONEREN |
||||
|
Probleem |
Element |
Bron/betrokkenen |
Taken |
Doel |
|
Geriatrisch assessment
|
Zorgverlener met geriatrische/ revalidatiegeneeskundige competenties Zie richtlijn 'Comprehensive geriatric assessment (CGA)’ cq ICF |
Breng functioneren op functioneel en psychosociaal domein in kaart of via ICF Breng prioritering aan de klachten/problemen samen met de patiënt. Probeer een kernprobleem te identificeren |
Inzicht in kwetsbaarheden en mogelijkheden van patiënt |
|
Inventarisatie enkelvoudig functioneren |
Huisarts, audicien, opticien |
Via 1e lijn in kaart brengen |
Patiënt ondersteunen met de juiste hulpmiddelen |
|
PSYCHISCH |
||||
|
Probleem |
Element |
Bron/betrokkenen |
Taken |
Doel |
|
Inventarisatie cognitief functioneren |
Verpleegkundige met geriatrische expertise |
Heteroanamnese, screenende geheugentest |
Heldere diagnose, beleid en begeleiding voor cognitief functioneren |
|
Inventarisatie psychische problematiek |
Psycholoog |
Screening en eventueel aanvullend onderzoek |
Diagnosticeren en behandelen |
|
SOCIAAL |
||||
|
Probleem |
Element |
Bron/betrokkenen |
Taken |
Doel |
|
Ontlasten patiënt of zorgsysteem |
Verpleegkundige, thuiszorg |
Vraag coping strategieën uit, exploreer de behoefte aan psychosociale ondersteuning. Meet mantelzorgbelasting Professionele en informele hulp/begeleiding nagaan |
Voldoende ondersteuning op psychosociaal, maatschappelijk, financieel vlak |
|
Advance Care Planning |
Huisarts, regieondersteuner Zie leidraad ‘Leidraad proactieve zorgplanning’
|
Gesprek over persoonlijke doelen, voorkeuren en beperkingen, en de medische haalbaarheid ervan |
(On)mogelijkheden t.a.v. ziekenhuisopnames, IC opnames, beademing en reanimatie zijn besproken. Afspraken rondom Proactief Zorg Plan worden gedeeld met het behandelteam. |
|
Relatieproblematiek, eenzaamheid |
Inventarisatie relationele problematiek |
Huisarts, geestelijke verzorging, psycholoog, maatschappelijk werk |
In kaart brengen |
Ondersteuning op psychosociaal gebied |
|
Woonproblematiek |
Inventarisatie problematiek m.b.t. huisvesting |
Huisarts, maatschappelijk werk, andere sociale instanties |
In kaart brengen |
Ondersteuning op maatschappelijk/financieel vlak |
|
Financiële problematiek |
Inventarisatie problematiek m.b.t. financiën |
Huisarts, maatschappelijk werk |
|
Ondersteuning op maatschappelijk/financieel vlak |
Deelnemers en rollen
De deelnemers van een basis MDB bestaan uit:
- Degene die de indicatie heeft gesteld en de voorbereiding heeft uitgevoerd
- Alle betrokken medische behandelaren die aangemerkt zijn als cruciaal tijdens de voorbereiding, denk hierbij ook aan behandelaren uit andere ziekenhuizen
- Voorzitter
De behandelaar die de indicatiestelling en voorbereiding heeft gedaan is degene die de casus voorlegt aan de andere behandelaren. Diegene is tevens de belangenbehartiger van de patiënt en draagt zorg dat de doelen, voorkeuren en mogelijkheden van de patiënt centraal staan tijdens de bespreking.
Bij voorkeur bestaan de deelnemers zoveel mogelijk uit behandelaren die een directe behandelrelatie hebben met de patiënt. Mocht dit binnen het organiserende ziekenhuis niet haalbaar zijn, dan kan er ook gekozen worden om een aantal medisch specialisten vanuit de beschouwende specialismen (algemene interne geneeskunde en geriatrie in het bijzonder) als vaste deelnemers aan de MDB aan te wijzen. Zij zijn dan onderdeel van de vaste kern, en per MDB wordt deze vaste kern dan aangevuld met een flexibele schil van betrokken behandelaren uit de andere specialismen die bij voorkeur wel een directe behandelrelatie met de patiënt hebben. Iedereen vertegenwoordigt de eigen discipline. Iedereen draagt verantwoording voor het afstemmen van de behandeling(en) op de doelen, voorkeuren en mogelijkheden van de patiënt.
De werkgroep geeft ter overweging om één of meerdere personen aan te wijzen binnen het ziekenhuis die afwisselend de rol van voorzitter op zich kunnen nemen tijdens de MDB. Dit zijn generalisten (medisch specialist, ziekenhuisarts, VS of PA) die dus wel inhoudelijk expert zijn, maar de voorbereiding niet hebben gedaan. Door een vaste groep aan te wijzen die afwisselend het voorzitterschap op zich neemt, wordt er ervaring opgebouwd met het richting geven aan een MDB en het efficiënt komen tot een overkoepelende en afgestemde behandeling. De voorzitter houdt de belangrijke doelen van de MDB, zoals beschreven in Tabel 4 en 5, daarbij voor ogen. Deze manier van werken is succesvol gebleken binnen de best practice van het COBRA-MDO (zie Bijlage D).
Afhankelijk van de toegevoegde elementen en de benodigde expertise kan het team uitgebreid worden met:
- Andere betrokken medisch specialisten of verpleegkundigen/ verpleegkundig specialisten/ Physician Assistants
- Paramedici: diëtist, maatschappelijk werk, fysiotherapeut, ergotherapeut, logopedist
- Behandelaren uit de eerste lijn: specialist ouderengeneeskunde, huisarts, kaderhuisarts ouderen, kaderapotheker (indien aanwezig in de regio), openbaar apotheker
- Ziekenhuisapotheker, poliklinisch apotheker
- Geestelijk verzorgers
- Psychologen
De werkgroep adviseert hierbij om zoveel mogelijk gebruik te maken van de expertise van de reeds betrokken behandelaren, en waar mogelijk geen behandelaren toe te voegen aan het team. Zo is, afhankelijk van de situatie, het niet noodzakelijk om altijd te verwijzen naar een geriater of internist-ouderengeneeskunde voor een CGA maar kan een korter Geriatric Assessment door een andere zorgverlener in bepaalde situaties ook volstaan (zie richtlijn CGA). Dit kan ook door een daartoe opgeleide verpleegkundige of Praktijk Ondersteuner Huisarts Ouderenzorg. Soms kan het wel efficiënt en doelmatig zijn om een behandelaar toe te voegen aan het team waardoor er op een later moment juist weer zorg afgeschaald kan worden.
Tijdens de MDB worden er twee rollen vastgesteld: een regieondersteuner en een aanspreekpunt. Dit kan dezelfde persoon zijn, maar hoeft niet. De regieondersteuner bespreekt ook de adviezen van de MDB met de patiënt, volgens het model Samen Beslissen. De regieondersteuner informeert de uitkomst van dit gesprek, het overkoepelende en afgestemde behandelplan, met de overige behandelaren, inclusief de huisarts (zie verslaglegging). Het aanspreekpunt is de primaire contactpersoon voor de patiënt, en voor het MDB-team wanneer zij organisatorische vragen willen stellen. Het aanspreekpunt hoeft niet de rol van medisch-inhoudelijk expert te vervullen, maar moet wel aan deze informatie kunnen komen.
Modaliteit
Voor een eerste MDB is de modaliteit van een multidisciplinair overleg het meest geschikt. Er zal immers in overleg gekomen worden tot afstemming, gezamenlijke kernproblemen en overkoepelende behandeldoelen (43). Het uitnodigen van de patiënt en/of diens naasten is hierbij een mogelijkheid, maar geen verplichting. In sommige gevallen kan dit een passende en doelmatige vorm zijn, zoals gebleken in de eerste lijn ouderenzorg. Ook hier is ruimte voor maatwerk.
Er kan gekozen worden voor een fysiek of een virtueel multidisciplinaire beoordeling. Indien zorgverleners buiten het ziekenhuis betrokken zijn of de huisarts een belangrijke rol speelt, dan is een hybride vorm wenselijk. Het heeft hierbij de voorkeur dat alle betrokkenen aanwezig zijn maar er kan ook uitgeweken worden naar een asynchroon overleg, waarbij de regieondersteuner de continuïteit bewaakt.
Bij het vervolgoverleg van een MDB zou eventueel een schriftelijk overleg kunnen volstaan, maar dat is afhankelijk van de individuele casus en ter beoordeling aan de regieondersteuner.
Een MDB voor een specifieke patiënt heeft geen vaste frequentie. De regieondersteuner bepaalt op maat wanneer een herbeoordeling nodig is, waarbij alle behandelaren de behoefte hiervoor kunnen aangeven bij de regieondersteuner. Wel is het verstandig voor de implementatie het overleg organisatorisch een vaste structuur en ritme te geven, waarop dan een MDB voor een specifieke patiënt kan plaats hebben.
Verslag en afspraken
De elementen van de basis MDB dienen allen kort en bondig terug te komen in de verslaglegging en een centrale plek te krijgen in het EPD. Het spreekt daarbij voor zich dat wanneer er elementen worden toegevoegd die voor de individuele patiënt van toepassing zijn, dit ook wordt meegenomen in de verslaglegging. Alle betrokken behandelaren, inclusief behandelaren uit de eerste lijn, ontvangen dit verslag. Stel ook een overzicht van de zorg- en behandelafspraken op voor de patiënt, in begrijpelijke taal (zie Bijlage F). Elke behandelaar neemt de bijgestelde zorg en afspraken op in het eigen behandelplan in het EPD.
Iedere discipline houdt zich in principe aan het vastgestelde beleid en aan de behandeldoelen die vastgesteld zijn in de MDB en stelt het eigen team hiervan in kennis. Indien een behandelaar in overleg met de patiënt afwijkt van het advies, wordt dit zo mogelijk besproken met de regieondersteuner en beargumenteerd vastgelegd in het EPD. Terugkoppeling vindt plaats aan de huisarts en de regieondersteuner.
Mogelijkheden voor invoering MDB in eigen ziekenhuis
Voor de invoering van een MDB in het ziekenhuis kunnen verschillende modellen gekozen worden (zie Figuur 4). Het model wat gekozen wordt, hangt af van factoren zoals de specifieke doelpopulatie waar de MDB voor ingezet wordt en de mogelijkheden van het ziekenhuis. Ook de (on)ervarenheid met deze nieuwe zorgactiviteit kan de keuze bepalen voor een bepaald model. Het is zinvol om binnen de organisatie een MDB te laten plaatsvinden met een vaste frequentie. Afhankelijk van de uitgebreidheid van de populatie is een frequentie van wekelijks tot maandelijks voor de hand liggend.
De voor- en nadelen van de verschillende vormen worden hieronder nader toegelicht.
Model 1: Vraag leidend
In het eerste model is per individuele patiënt de inhoud leidend. Vanuit de hiervoor gestelde vragen wordt vooraf gekozen voor basis MDB of een uitgebreide vorm met toevoegen van elementen. In geval van zeer complexe problematiek, die zich over domeinen danwel instellingen heen begeeft en interacteert op verschillende assen wordt gekozen voor een uitgebreid MDB, waarbij de verschillende elementen afhangen van de specifieke problematiek.
Ook als de problematiek meer gaat over de mogelijkheden van de patiënt (past de ingezette zorg bij de prognose van de patiënt, Advance Care Planning), de rol- en taakverdeling van het behandelteam, of door een signaal van de patiënt of diens naaste(n) waardoor het evident wordt dat er geen coördinatie van zorg ervaren wordt lijkt dit meer voor de hand te liggen.
Als de problematiek vooral medisch inhoudelijk complex is, of interfererende behandelingen spelen, ligt het meer voor de hand om te kiezen voor een basis MDB.
In het algemeen is de verwachting dat voor dit model gekozen wordt, als er enige ervaring is met het doen van een MDB en als een belangrijk deel van de patiënten met uitgebreide multimorbiditeit en veel behandelaren in kaart is gebracht. Er kan dan veel gerichter gekozen worden voor maatwerk.
Model 2: Initieel uitgebreid
Zeker in het begin zal niet direct duidelijk zijn, wanneer professionals moeten kiezen voor welke vorm. Een organisatie kan er dan voor kiezen om te starten met de meest complexe patiënten. Deze patiënten worden dan allen besproken in een uitgebreid MDB. Nadeel kan zijn dat dit wellicht veel tijd en organisatiekracht vergt. Zeker zolang niet helemaal duidelijk is hoe het precies in te richten, is de efficiëntie minder groot. Anderzijds, als men kiest voor de meest complexe patiënten (“het laaghangend fruit”) is de kans daarop kleiner.
Model 3: Stepped care
Een ander model is het stepped care-model. Er wordt dan primair bij alle patiënten voor de basis MDB zonder facultatieve elementen toe te voegen. Zeker bij aanvankelijke implementatie van de MDB kan dit een zinvol model zijn. De tijdsinvestering die de voorbereiding kost is beperkter en ook de MDB zelf vermoedelijk korter van duur. Dit maakt het gemakkelijker om te implementeren. Voor de patiëntengroep waarbij de basis MDB niet toereikend blijkt, kan een aanvullende MDB georganiseerd waarin de facultatieve elementen aan bod komen.
Randvoorwaarden
Hoewel het nog zoeken is naar de juiste aanpak, laten ervaringen in de geriatrie en oncologie zien dat goede afstemming en samenwerking leiden tot beter passende en integrale zorg en meer tevreden patiënten. Ervaringen leren ook dat het een bepaalde tijd duurt voor er een doelmatige vorm is ontwikkeld. Als deze aanpak ook voor multimorbiditeit wordt gevolgd is een vrij zekere verwachting dat dit leidt tot een betere zorg voor patiënten met multimorbiditeit en meer tevredenheid bij patiënten en behandelaren. Echter, gezien de diffuusheid van het probleem en het groot aantal betrokken, wisselende behandelaren is de verwachting dat dit een complexe uitdaging zal zijn. Desalniettemin zijn stappen op dit pad noodzakelijk in het kader van het integraal zorgakkoord. Het evalueren van de effectiviteit moet onderdeel uitmaken van het proces. Wij stimuleren het delen van ervaring onderling, en verwijzen naar het platform voor multimorbiditeit (Nederlands Platform voor Multimorbiditeit | (multimorbidity.nl)) voor het faciliteren hiervan.
Er zijn meerdere randvoorwaarden te identificeren waaraan voldaan moet worden om de aanbevelingen in de praktijk te kunnen brengen. Er zijn concrete acties te benoemen die door verschillende partijen (de zorgprofessional zelf, de ziekenhuisorganisatie en beleidsmakers in de zorg) opgepakt zullen moeten worden. Wij verwijzen naar Bijlage G voor een uitgebreide uiteenzetting van randvoorwaarden en gekoppelde acties. In dit hoofdstuk zullen wij de drie belangrijkste pijlers uitlichten die essentieel zijn om de MDB te kunnen implementeren in de praktijk: tijd, financiering en integratie van het patiëntendossier.
Tijd en Financiering
Hoewel de verwachting is dat het inzetten op een MDB als onderdeel van de zorg uiteindelijk zal leiden tot minder (acute) escalaties met SEH-bezoeken, acute opnames in het ziekenhuis en crisisopnames in de ouderenzorg en tot minder zorgcontacten met verschillende behandelaren/ effectief minder behandelaren, is er nog weinig wetenschappelijk bewijs. Aanvankelijk zal dit een praktische zoektocht zijn, waarbij voorbereiding en bespreking tijdsintensief zullen zijn. Er moet ruimte gecreëerd worden voor de zorgprofessional om tijd te investeren in de patiënt, wat zich later zal terugbetalen.
Idealiter verplaatsen financieringsstromen zich van opvang van escalaties en veel zorgtrajecten naast elkaar, naar afgestemde en geïntegreerde zorg. Deze zorg zal naar verwachting efficiënter zijn door het streven naar minder betrokken zorgverleners en het voorkomen van acuut zorggebruik (zie bijlage I voor een illustratie hiervan). Voorbereiding van een MDB kost tijd, zonder dat daar op dit moment een verrichting tegenover staat. Dit geldt eveneens voor de MDB zelf. Omdat dit een majeure wijziging betreft, met potentieel een grote groep (kwetsbare) patiënten, zal aparte financiering geregeld moeten worden.
Om de daadwerkelijke financiële impact van de MDB in kaart te brengen, is een Budget Impact Analyse (BIA) wenselijk. Het uitvoeren valt buiten de opdracht en begroting van de huidige leidraad. De werkgroep is bereid om mee te werken aan initiatieven om deze uit te voeren.
EPD
In het EPD moeten een aantal zaken geregeld zijn, waarbij dit niet alleen voor alle zorgverleners beschikbaar, maar ook centraal inzichtelijk moet zijn. Dit zijn de volgende zaken:
- Een tabblad multidisciplinaire beoordeling met een passend format;
- Een gemakkelijke verslaglegging vanuit dit tabblad naar de huisarts;
- De mogelijkheid om in het centrale dossier vast te leggen wie de regieondersteuner is en wie het aanspreekpunt is van de patiënt met bij voorkeur een minimaal aantal afspraken;
- Gestandaardiseerde vragenlijsten, zo mogelijk vooraf in te vullen door de patiënt;
- Koppeling naar Patiënt Gebonden Omgeving (PGO) voor patiënten beschrijving.
Onderbouwing
Referenties
- 1. van Oostrom S, Gijsen R, Stirbu I, Korevaar J, Schellevis FG, Picavet S, et al. Toename in chronische ziekten en multimorbiditeit. NTVG [Internet]. 2017 Aug 24 [cited 2023 Mar 21]; Available from: https://www.ntvg.nl/artikelen/toename-chronische-ziekten-en-multimorbiditeit
- 2. Integrated care models: an overview. World Health Organization; 2016.
- 3. Nolte E, Knai C, Hofmarcher M, Conklin A, Erler A, Elissen A, et al. Overcoming fragmentation in health care: chronic care in Austria, Germany and The Netherlands. Health Econ Policy Law. 2012 Jan;7(1):12546.
- 4. Wallace E, Salisbury C, Guthrie B, Lewis C, Fahey T, Smith SM. Managing patients with multimorbidity in primary care. BMJ. 2015 Jan 20;350:h176.
- 5. Rapport Leven met meerdere aandoeningen [Internet]. Patiëntenfederatie Nederland; 2022 Nov p. 55. Available from: https://www.patientenfederatie.nl/downloads/rapporten/1274-rapportage-multimorbiditeit/file
- 6. Basisset MSZ Risicoprofiel 2022-2027. IGJ;
- 7. Multimorbiditeit en regie in het ziekenhuis [Internet]. Richtlijnendatabase; [cited 2023 Mar 21]. Available from: https://richtlijnendatabase.nl/richtlijn/multimorbiditeit_en_regie_in_het_ziekenhuis/startpagina_-_multimorbiditeit_en_regie_in_het_ziekenhuis.html
- 8. Verantwoordelijkheidsverdeling bij samenwerking in de zorg [Internet]. KNMG; 2022. Available from: https://www.knmg.nl/advies-richtlijnen/dossiers/verantwoordelijkheidsverdeling
- 9. Leefstijl bij patiënten met een ernstige psychische aandoening (richtlijn 2015) [Internet]. GGZ Standaarden; 2015. Available from: https://www.ggzstandaarden.nl/richtlijnen/leefstijl-bij-patienten-met-een-ernstige-psychische-aandoening-richtlijn-2015/introductie
- 10. Kwaliteitsstandaard Psychosociale zorg bij somatische aandoeningen [Internet]. WSPZisa; 2019 Nov. Available from: https://richtlijnendatabase.nl/richtlijn/kwaliteitsstandaard_psychosociale_zorg_bij_somatische_aandoeningen/startpagina_-_psychosociale_zorg_bij_somatische_aandoeningen.html
- 11. DE Hert M, Correll CU, Bobes J, Cetkovich-Bakmas M, Cohen D, Asai I, et al. Physical illness in patients with severe mental disorders. I. Prevalence, impact of medications and disparities in health care. World Psychiatry Off J World Psychiatr Assoc WPA. 2011 Feb;10(1):5277.
- 12. Schorr S. Drug safety in patients with psychotic disorders. University of Groningen; 2010.
- 13. van Hasselt FM, Thier CSM, van Rijswijk E, Loonen AJM. Is somatic health screening in patients with severe mental illness of added value? Perspect Psychiatr Care. 2014 Jul;50(3):186-92.
- 14. Osborn DPJ, Nazareth I, King MB. Physical activity, dietary habits and Coronary Heart Disease risk factor knowledge amongst people with severe mental illness: a cross sectional comparative study in primary care. Soc Psychiatry Psychiatr Epidemiol. 2007 Oct;42(10):787-93.
- 15. Oud MJT, Meyboom-de Jong B. Somatic diseases in patients with schizophrenia in general practice: their prevalence and health care. BMC Fam Pract. 2009 May 9;10:32.
- 16. KNMG. Handreiking Verantwoordelijkheidsverdeling bij samenwerking in de zorg [Internet]. 2022. Available from: https://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=&ved=2ahUKEwiF4pSM-pCCAxVW_7sIHdQ4BpoQFnoECBIQAQ&url=https%3A%2F%2Fwww.knmg.nl%2Fdownload%2Fhandreiking-verantwoordelijkheidsverdeling-bij-samenwerking-in-de-zorg&usg=AOvVaw0lmeGgjWxbXC3GVhsUaVQz&opi=89978449
- 17. Onderzoek Interprofessionale identiteit [Internet]. Federatie Medisch Specialisten; 2021 May. Available from: https://demedischspecialist.nl/sites/default/files/2021-12/fms_factsheet_interprofessionele_identiteit_210x297_def.pdf
- 18. Berkman ND, Chang E, Seibert J, Ali R, Porterfield D, Jiang L, et al. Management of High-Need, High-Cost Patients: A Best Fit Framework Synthesis, Realist Review, and Systematic Review [Internet]. Rockville (MD): Agency for Healthcare Research and Quality (US); 2021 [cited 2023 Apr 25]. (AHRQ Comparative Effectiveness Reviews). Available from: http://www.ncbi.nlm.nih.gov/books/NBK575200/
- 19. de Ruijter UW, Kaplan ZLR, Bramer WM, Eijkenaar F, Nieboer D, van der Heide A, et al. Prediction Models for Future High-Need High-Cost Healthcare Use: a Systematic Review. J Gen Intern Med. 2022 May;37(7):176370.
- 20. Wammes JJG, van der Wees PJ, Tanke MAC, Westert GP, Jeurissen PPT. Systematic review of high-cost patients characteristics and healthcare utilisation. BMJ Open. 2018 Sep 8;8(9):e023113.
- 21. Van Calster B, Vickers AJ. Calibration of risk prediction models: impact on decision-analytic performance. Med Decis Mak Int J Soc Med Decis Mak. 2015 Feb;35(2):1629.
- 22. Wynants L, van Smeden M, McLernon DJ, Timmerman D, Steyerberg EW, Van Calster B, et al. Three myths about risk thresholds for prediction models. BMC Med. 2019 Oct 25;17(1):192.
- 23. Johnson TL, Rinehart DJ, Durfee J, Brewer D, Batal H, Blum J, et al. For many patients who use large amounts of health care services, the need is intense yet temporary. Health Aff Proj Hope. 2015 Aug;34(8):1312-9.
- 24. Vogeli C, Spirt J, Brand R, Hsu J, Mohta N, Hong C, et al. Implementing a hybrid approach to select patients for care management: variations across practices. Am J Manag Care. 2016 May;22(5):358-65.
- 25. Davis AC, Osuji TA, Chen J, Lyons LJL, Gould MK. Identifying Populations with Complex Needs: Variation in Approaches Used to Select Complex Patient Populations. Popul Health Manag. 2021 Jun;24(3):393-402.
- 26. Clegg A, Bates C, Young J, Ryan R, Nichols L, Ann Teale E, et al. Development and validation of an electronic frailty index using routine primary care electronic health record data. Age Ageing. 2016 May;45(3):353-60.
- 27. Heins M, Korevaar J, Schellevis F, Rijken M. Identifying multimorbid patients with high care needs - A study based on electronic medical record data. Eur J Gen Pract. 2020 Dec;26(1):189-95.
- 28. Verhoeff M, de Groot J, Burgers JS, van Munster BC. Development and internal validation of prediction models for future hospital care utilization by patients with multimorbidity using electronic health record data. PloS One. 2022;17(3):e0260829.
- 29. Hippisley-Cox J, Coupland C. Predicting risk of emergency admission to hospital using primary care data: derivation and validation of QAdmissions score. BMJ Open. 2013 Aug 19;3(8):e003482.
- 30. Hopman P, Heins MJ, Korevaar JC, Rijken M, Schellevis FG. Health care utilization of patients with multiple chronic diseases in the Netherlands: Differences and underlying factors. Eur J Intern Med. 2016 Nov;35:44-50.
- 31. Rosella LC, Kornas K, Yao Z, Manuel DG, Bornbaum C, Fransoo R, et al. Predicting High Health Care Resource Utilization in a Single-payer Public Health Care System: Development and Validation of the High Resource User Population Risk Tool. Med Care. 2018 Oct;56(10):e61-9.
- 32. Rosella LC, Kornas K, Sarkar J, Fransoo R. External Validation of a Population-Based Prediction Model for High Healthcare Resource Use in Adults. Healthc Basel Switz. 2020 Dec 4;8(4):537.
- 33. Ng SHX, Rahman N, Ang IYH, Sridharan S, Ramachandran S, Wang DD, et al. Characterising and predicting persistent high-cost utilisers in healthcare: a retrospective cohort study in Singapore. BMJ Open. 2020 Jan 6;10(1):e031622.
- 34. Berkman ND, Chang E, Seibert J, Ali R. Characteristics of High-Need, High-Cost Patients?: A "Best-Fit" Framework Synthesis. Ann Intern Med. 2022 Dec;175(12):1728-41.
- 35. Multimorbidity: clinical assessment and management [Internet]. NICE guideline; 2016 Sep [cited 2023 Mar 21]. Available from: https://www.nice.org.uk/guidance/ng56
- 36. Rijken M, Korevaar J. Goede zorg voor mensen met multimorbiditeit. Nivel; 2021.
- 37. Boyd C, Smith CD, Masoudi FA, Blaum CS, Dodson JA, Green AR, et al. Decision Making for Older Adults With Multiple Chronic Conditions: Executive Summary for the American Geriatrics Society Guiding Principles on the Care of Older Adults With Multimorbidity. J Am Geriatr Soc. 2019 Apr;67(4):665-73.
- 38. Engel GL. The need for a new medical model: a challenge for biomedicine. Science. 1977 Apr 8;196(4286):129-36.
- 39. Comprehensive Geriatric Assessment (CGA) [Internet]. Richtlijnendatabase; 2021. Available from: https://richtlijnendatabase.nl/richtlijn/comprehensive_geriatric_assessment_cga/startpagina_-_comprehensive_geriatric_assessment_cga.html
- 40. Elwyn G, Frosch D, Thomson R, Joseph-Williams N, Lloyd A, Kinnersley P, et al. Shared Decision Making: A Model for Clinical Practice. J Gen Intern Med. 2012 Oct;27(10):1361-7.
- 41. Pel-Littel RE, van de Pol M, de Boer M, Delmee L. Infographic Samen beslissen met kwetsbare ouderen [Internet]. Available from: https://www.zorgvoorbeter.nl/zorgvoorbeter/media/documents/thema/persoonsgerichte-zorg/infographic-samen-beslissen-kwetsbare-ouderen.pdf
- 42. Vermunt NP, Harmsen M, Elwyn G, Westert GP, Burgers JS, Olde Rikkert MG, et al. A three?goal model for patients with multimorbidity: A qualitative approach. Health Expect Int J Public Particip Health Care Health Policy. 2018 Apr;21(2):528-38.
- 43. Fried TR, Tinetti ME, Iannone L, O'Leary JR, Towle V, Van Ness PH. Health Outcome Prioritization as a Tool for Decision Making Among Older Persons With Multiple Chronic Conditions. Arch Intern Med. 2011 Nov 14;171(20):1856-8.
- 44. Handreiking Implementatie Passende zorg [Internet]. Federatie Medisch Specialisten; 2023 Jul p. 50. Available from: https://demedischspecialist.nl/sites/default/files/2023-07/handreiking_implementatie_passende_zorg.pdf
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 08-04-2024
Algemene gegevens
In samenwerking met: verpleegkundigen & verzorgenden, en patientenfederatie nederland.
De ontwikkeling van deze leidraad werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de leidraad.
Samenstelling werkgroep
Voor het ontwikkelen van de leidraad is in 2021 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met multimorbiditeit.
Werkgroep
Prof. B.C. (Barbara) van Munster, Nederlandse Internisten Vereniging
Dr. S.K. (Sven) Schiemanck, Nederlandse Vereniging van Revalidatieartsen
I. (Ilse) van Ee, Patiëntenfederatie Nederland
Drs. A.J. (Arend) Arends, Nederlandse Vereniging voor Klinische Geriatrie
Drs. E.M. (Eefje) Meulenberg, Nederlandse Vereniging voor Klinische Geriatrie
N. (Niels) Jongejan, Nederlandse Vereniging voor Cardiologie
Dr. J.E.H. (Jeroen) Ponten, Nederlandse Vereniging voor Heelkunde
Prof. dr. P.M.L.A. (Patricia) van den Bemt, Nederlandse Vereniging van ZiekenhuisApothekers
Prof. dr. I. (Indira) Tendolkar, Nederlandse Vereniging voor Psychiatrie
W.M.E. (Mieke) Bil MANP, Verpleegkundigen & Verzorgenden Nederland
Dr. H. (Henk) Kramer, Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose
Drs. Y.M. (Yolande) Vermeeren, Nederlandse Internisten Vereniging
Drs. U.W. (Ursula) de Ruijter, persoonlijke titel
Agendaleden
Drs. L. (Lucie) van Iersel, Vereniging van Specialisten Ouderengeneeskunde
Drs. E. (Eline) Okel, Koninklijke Nederlandse Maatschappij ter bevordering der Pharmacie
Meeleeslid
Prof. Dr. J. (Jako) Burgers, strategisch-medisch adviseur bij de NHG, en werkzaam als huisarts reflecteerde op persoonlijke titel op de leidraad
Met ondersteuning van
Drs. E.A. (Emma) Gans, adviseur Kennisinstituut van de Federatie Medisch Specialisten
Dr. J.F. (Janke) de Groot, senior adviseur Kennisinstituut van de Federatie Medisch Specialisten
Drs. L.A.M. (Liza) van Mun, junior adviseur Kennisinstituut van de Federatie Medisch Specialisten
Y. (Yvonne) van Kempen, projectsecretaresse, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Achternaam werkgroeplid |
Functie |
Nevenfuncties |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Ondernomen actie |
|
* Voorzitter werkgroep Munster, Van |
12/2020 - present Head of Alzheimer Center Groningen (5%)
2021: Voorzitter Commissie Kwetsbare Ouderen 11/2022: internist-geriater |
Onbetaalde nevenwerkzaamheden: 2021 - heden Lid Stuurgroep Richtlijn Cluster cognitieve stoornissen 2021 - heden Voorzitter Nederlands Platform voor multimorbiditeit 2021 - heden Member multimorbidity working group European Federation of Internal Medicine 2020 - heden Board member ‘European Academy of Medicine of Ageing’ 2017 - heden Gemandateerd Lid platform kwaliteit NIV namens kerngroep ouderengeneeskunde 2015 - heden Lid werkgroep wetenschap Nederlandse Vereniging Klinische Geriatrie 2015 - heden Member Multimorbidity Working Group, Guideline International Network 2016 - 2023 Voorzitter (2019 lid) werkgroep kwaliteit en richtlijnen, kerngroep ouderengeneeskunde 2020 - 2021 Afgevaardigde NIV DHFA 2019 - 2021 Expertgroep ‘Aging Academy' 2016 - 2021 Redacteur 'Tijdschrift gerontologie en geriatrie'
2022- heden Voorzitter leidraad multimorbiditeit (NIV) 2021 - heden Voorzitter werkgroep multidisciplinaire beoordeling (NIV) 2018 - 2021 Voorzitter werkgroep 'Regievoering bij multimorbiditeit' (NIV) 2016 - 2019 Voorzitter werkgroep 'shared decision making in behandelbeperkingen' (NIV) 2016 - 2019 Lid landelijke werkgroep 'zorgpad kwetsbare ouderen' (NIV) |
Geen |
Iedereen heeft baat bij de uitkomsten dus ook de directe omgeving |
ZONMw: Young Onset Dementia- INCLUDED: Advance care planning (projectleider)
ZEGG/ZONMw: "The impact of a comprehensive geriatric assessment including advance care planning in acutely hospitalized frail patients with cognitive disorders: the GOAL study" (projectleider)
Innovatiesubsidie ONO: ‘Regieondersteuning bij multimorbiditeit’ (projectleider)
ABOARD: A Personalized Medicine Approach for Alzheimer’s Disease (projectleider van deelproject)
Wetenschapsfonds Gelre Ziekenhuizen: ‘Esophagogastric Cancer in the elderly patient’ (geen projectleider)
Wetenschapsfonds Gelre Ziekenhuizen: ‘Perioperatieve mobiliteit’ (projectleider)
Hersenstichting ‘No guts no glory’ (1 miljoen) (geen projectleider)
ZonMw Wetenschap voor de praktijk: ‘Eigen huis als polikliniek: de ervaren kwaliteit van beeldbel zorg bij kwetsbare ouderen met multi-morbiditeit en hun families’
Methodiekontwikkeling geïntegreerd Richtlijn gebruik bij Multimorbiditeit (geen projectleider)
SKMS: ‘Leidraad multimorbiditeit’ (geen projectleider)
Wetenschapsfonds Gelre Ziekenhuizen: ‘Gezondheidsvaardigheden van patiënten met multimorbiditeit en meerdere betrokken behandelaars in het ziekenhuis’ (projectleider)
Wetenschapsfonds Gelre Ziekenhuizen: 'PREsurgery Thoughts’ (projectleider)
KMS: ‘Leidraad multidisciplinaire beoordeling’ (geen projectleider) |
Regievoering bij multimorbiditeit is een van mijn aandachtsgebieden binnen de zorg en mijn onderzoekslijn. |
Geen |
Geen restricties |
|
Ponten |
Gastro-intestinaal en oncologisch chirurg, Groene Hart Ziekenhuis te Gouda. |
Bariatrisch chirurg, Nederlandse Obesitas Kliniek. |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restricties |
|
Bemt, van den |
Hoofd Sectie Patiëntenzorg - Klinische Farmacie en Farmacologie - UMCG - fulltime |
Voorzitter bestuur Stichting ANNA (Academisch Netwerk Noordelijke Apotheken) -
Voorzitter redactieraad NPFO (Ned Platform Farmaceutisch Onderzoek) – onbetaald Docentbegeleider Masteropleiding Kwaliteit en veiligheid RadboudUMC/NFU – betaald. Commissie Duurzaamheid NVZA – onbetaald NFU werkgroep Green Deal Duurzame Zorg Medicijnen Werkgroep schoon water UMCG - onbetaald |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restricties |
|
Arends |
Klinisch geriater Maasstadziekenhuis; medisch manager geriatrie |
Secretaris DHFA (vacatiegelden) Bestuurslid stichting mentorschap Rotterdam en omstreken (onbetaald). |
Geen |
Geen |
Geen |
Voorzitter NVKG |
Geen |
Geen restricties |
|
Kramer |
Longarts, Martini Ziekenhuis Groningen; 1.0 FTE. |
Lid adviesraad Longfibrose Patiëntenvereniging: medisch inhoudelijk advies omtrent patiëntenzorg en vragen van patiënten; onbetaald. |
Ik heb geen belangen (financieel noch anderszins) bij de deelname en/of de uitkomst van deze werkgroep en/of het advies van de werkgroep. |
Geen |
Geen |
Geen |
Geen |
Geen restricties |
|
Schiemanck |
Revalidatiearts, Spaarne Gasthuis Hoofddorp (sinds 1-2-2023)
|
Zelfstandig revalidatiearts, parttime (Revalidatie Advies), sinds 1-10-23
Lid algemeen bestuur, Vereniging van Revalidatieartsen (VRA) tot 11-2021 (onbetaald) |
Geen |
Geen |
Hermes studie: onderzoek naar een ‘negatieve veer’ ter vermindering van spasticiteitsklachten bij lopen. Financier is Health Holland/ ZonMw/NWOttw. Geen rol als projectleider. |
Geen |
De afdeling revalidatiegeneeskunde LUMC heeft een spreekuur voor ‘bewegingsstoornissen bij multimorbiditeit’ (pas sinds kort op zordomein)
|
Geen restricties |
|
Tendolkar |
Afdelingshoofd Psychiatrie, Radboudumc Hoogleraar psychiatrie. |
Geen |
Geen |
Geen |
Onderzoek: Transcrantiaal Electrical Stimulation as treatment for delirium, financier is ZonMw open competitive. Geen projectleider. Onderzoek: TMS for treatment obsessive-compulsive disorder (OCD): bridging the gap between 1st line treatment and invasive brain surgery. Financier is ZonMw, geen projectleider. |
Geen |
Geen |
Geen restricties |
|
Ee, van |
Adviseur patientenbelang - patientenfederatie.nl - fulltime |
Patient-advocate- psoriasispatiënten Nederland - onbetaald |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restricties |
|
Meulenberg |
Geriater ETZ |
Kwaliteitszaken NVKG, (onkosten) vergoeding Commissie Behandeling van multimorbiditeit (NIV), vacatiegelden. |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restricties |
|
Bil |
Verpleegkundig specialist AGZ, afd. Klinische geriatrie OLVG |
Gastdocent (betaald) |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restricties |
|
Jongejan |
PA Ouderengeneeskunde en 'stafarts' Stichting QuaRijn, Doorn, fulltime |
NVVC lid: Congrescommissie, parttime |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restricties |
|
Vermeeren |
Werkgroep multidisciplinaire beoordeling bij multimorbiditeit |
Lyme centrum Apeldoorn, onderdeel van Gelre ziekenhuizen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restricties |
|
Ruijter |
Arts-onderzoeker Noordwest Ziekenhuisgroep en Erasmus universitair Medisch centrum (betaald) |
Lid Nederlands Platform voor Multimorbiditeit (onbetaald) Onderzoeksstagiair Coöperatie VGZ (onbetaald) |
Geen |
Geen |
Ja, Erasmus MC Efficiencybeurs Advance Care Planning (ACP) bij multimorbide ouderen en Foreest Wetenschapsbeurs Noordwest Ziekenhuisgroep, High Utilizing Patient Prediction (HUPP) mode |
Een deel van mijn onderzoek richt zich op regieondersteuning voor patiënten die fragmentatie van zorg ervaren. |
Geen |
Geen restricties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van de Patiëntenfederatie Nederland voor het rondetafelgesprek en een afgevaardigde van de Patiëntenfederatie Nederland in de werkgroep. Het verslag hiervan (zie bijlage A) is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen en bij het opstellen van de overwegingen.
Gedurende de ontwikkeling van deze leidraad is er een survey van Patiëntenfederatie Nederland en haar leden onder dertienduizend mensen gepubliceerd. Van hen hadden er meer dan zevenduizend twee of meer aandoeningen. Het Onderzoek Leven met Meerdere Aandoeningen geeft onder andere inzichten in de gevolgen van het hebben van meerdere chronische aandoeningen op kwaliteit van leven en mentale gezondheid, de behoefte aan multidisciplinaire samenwerking tussen zorgverleners en regievoering, en of de deelnemers zorg krijgen gericht op individuele aandoeningen of het totaalplaatje. De inzichten uit dit onderzoek zijn meegenomen in de ontwikkeling van deze leidraad.
De leidraad is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland en de aangeleverde commentaren zijn bekeken en verwerkt.
Wkkgz & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz.
Bij de leidraad is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn leidraadhoofdstukken op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Hoofdstuk |
Uitkomst raming |
Toelichting |
|
Hoofdstuk 1 |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Hoofdstuk 2 |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Hoofdstuk 3 |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Hoofdstuk 4 |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
De modules zijn tot stand gekomen door middel van verschillende methoden: literatuursearch, focusgroepen, interviews en rondetafelgesprekken.
Literatuur
Er is door middel van een systematische search op 08-07-2021 gezocht naar nationale en internationale literatuur ten aanzien van de multidisciplinaire beoordeling bij multimorbiditeit bij volwassenen. De zoekvraag was gericht op het vinden van verschillende methoden om een multidisciplinaire beoordeling vorm te geven met meerdere medisch specialisten óf organisaties, waarbij de tweede lijn ten minste betrokken was. De methode en bevindingen van deze systematisch search zijn opgenomen in Bijlage C.
Daarnaast is er uitgebreide inventarisatie gedaan van kwaliteitsdocumenten over het multidisciplinair overleg en samenwerking in de zorg. Via de werkgroep werden verschillende documenten aangeleverd, er werd niet-systematisch gezocht (google), en Webinars (o.a. Oncologienetwerken ‘optimaliseren van het MDO’ bijgewoond.
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling.
Focusgroepen
Behandelaren van patiënten met multimorbiditeit in het ziekenhuis
Er werden 7 focusgroepen gehouden met behandelaren van patiënten met multimorbiditeit in het ziekenhuis. Tijdens deze focusgroepen werd o.a. een recente, lokale casus met multimorbiditeit besproken.
De discussiegids bestond uit drie hoofdvragen:
- Wat is de ervaring van behandelaren m.b.t. de onderlinge afstemming van zorg voor patiënten met multimorbiditeit in het ziekenhuis?
- Wat zijn de gedachtes van behandelaren op de werkdefinitie en doelgroep van een MDB, zoals deze is vormgegeven door de werkgroep?
- Hoe zou je een multidisciplinaire beoordeling kunnen vormgeven in de praktijk?
De focusgroepen werden geanalyseerd volgens de grounded theory methode door E. Gans en U. de Ruijter en de bevindingen staan uitgebreid beschreven in Bijlage B.
Huisartsen
Er werd 1 focusgroep gehouden met huisartsen. Zij waren ook uitgenodigd voor de focusgroepen met behandelaren in de tweede lijn, maar dit bleek niet haalbaar.
De discussiegids bestond uit de volgende hoofdvragen:
- Wat is de mogelijke rol voor de huisarts in een MDB?
- Hoe kunnen we de juiste afstemming met de eerste lijn bewaken (in de context van de MDB)?
De bevindingen van deze focusgroep staan beschreven in Bijlage E.
Daarnaast reflecteerde Prof. Dr. Jako Burgers, huisarts, op de leidraad en zijn overwegingen werden meegenomen.
Identificatie en interviews met best practices
Via de werkgroep werd er een uitvraag gedaan over best practices die raken aan de MDB. Er waren twee voorbeelden: het COBRA-MDO (Amsterdam-UMC) en de Intensieve Samenwerkingsafdeling (Jeroen Bosch Ziekenhuis). Beide initiatieven leveren zorg voor de patiënt met multimorbiditeit op een innovatieve wijze, waar wij leerpunten uit hebben getrokken.
De verslaglegging van de interviews die wij gedaan hebben met vertegenwoordigers van deze initiatieven staan beschreven in Bijlage D.
Interviews met auteurs
Op basis van de systematische literatuursearch die wij verricht hebben, waren er nog twee aanvullende vragen die wij aan alle auteurs wilden stellen:
1. Is it possible to give an estimation of the time investment required for the different elements of your care intervention? [deze vraag werd alleen gesteld wanneer het antwoord niet te vinden was in het artikel]
2. Is the care intervention still in practice today? Why/why not?
Met deze vragen wilden wij meer inzicht krijgen in de belemmerende en bevorderende factoren voor het oprichten van een MDB. De samenvatting van de antwoorden die wij verkregen hebben staan beschreven in Bijlage H.
Rondetafelgesprek met belanghebbende partijen
Het rondetafelgesprek vond plaats met belanghebbende partijen rondom de zorg van patiënten met multimorbiditeit. Het doel was om de conceptleidraad te bespreken en verbeteren en aanpassingen op te halen. Dit gesprek vond plaats nadat de conceptteksten waren geschreven en de werkgroep hiermee akkoord was, maar voordat de commentaarfase werd gestart.
Commentaar- en autorisatiefase
De conceptleidraad werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptleidraad aangepast en definitief vastgesteld door de werkgroep. De definitieve leidraad werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.