Anamnese en lichamelijk onderzoek bij infantiele hemangiomen
De meeste IH kunnen over het algemeen moeiteloos worden onderscheiden van (andere) vaattumoren en -malformaties door hun typische groei- en regressiepatroon. Toch is het van groot belang te realiseren dat een snelgroeiende vaatafwijking in de neonatale fase mogelijk een ándere snelgroeiende tumor/ afwijking kan betreffen die in eerste instantie op een IH kan lijken. Het is dus cruciaal andere, benigne afwijkingen of mogelijk maligne tumoren uit te sluiten. In de meeste gevallen kan de diagnose IH gesteld worden op basis van de voorgeschiedenis, anamnese en het lichamelijk onderzoek. Hierbij zijn de volgende onderwerpen van belang:
Anamnese
Risicofactoren voor een IH (zie ook risicofactoren in voorgaande module)
- Laag geboortegewicht
- Vroeggeboorte, neonatale complicaties
- Gecompliceerde zwangerschap
- IH in de familieanamnese
Kenmerken van een IH
- Karakteristiek groeipatroon
- Het IH is afwezig bij de geboorte. Bij ongeveer 65% van de kinderen met een IH is een precursor aanwezig, bij de andere kinderen is er geen laesie aanwezig bij de geboorte, zie ook ‘Lichamelijk onderzoek’
- Het IH ontstaat in enkele dagen tot weken na de geboorte
- Groeifase met disproportionele groei in de eerste levensweken-maanden
- Plateaufase met stagnatie groei tussen de leeftijd van 7 en 12 maanden
- Spontane involutie meestal gezien tussen de leeftijd van 2 en 6 jaar (proces van jaren)
Lichamelijk onderzoek
- Een precursor laesie (voorloper laesie van IH) kan bestaan uit een bleek gebied, teleangiëctastieën of een paars-rode macula met daaromheen een halo
- De locatie van het IH (zie ook alarmsymptomen)
- Bepaal het type en patroon van het IH (zie Definities voor beschrijving van het klinisch beeld)
- Meten van het IH (in mm), meet de oppervlakkige component
- Overweeg om (bij elke controle) een foto te maken van het IH (met een centimeter ‘’normale’’ huid ernaast)
- Inspectie van de hele huid (incl. slijmvliezen oraal en genitaal) naar aanwezigheid van andere IH
- Het onderzoeken van de lever kan een aanwijzing geven over de aanwezigheid van hepatische IH (meestal in samenhang met meerdere (>10) IH van de huid)
Alarmsymptomen
- Tekenen van ulceratie. Naast een duidelijke wond in het IH kan er ook sprake zijn van subtielere tekenen van ulceratie, zoals zwart/grijze gebieden of crustae (zie ook ‘Ulceratie’ in de module behandelmogelijkheden en uitgangsvraag (UV) 1. Bloeden kan ook een teken van ulceratie zijn.
- Zeer grote IH kunnen gepaard gaan met high output hartfalen. Let op tekenen van vochtretentie, zoals pulmonale crepitaties, perifeer oedeem en verhoogde centraalveneuze druk (CVD)
- Multipele IH kunnen geassocieerd zijn met hepatische (en/of viscerale) IH. Dit geldt met name voor kinderen jonger dan 6 maanden met 10 of meer cutane IH (zie ook UV1 en UV2)
- Subglottische IH worden gekenmerkt door een niet bij de geboorte aanwezige maar progressieve stridor die ontstaat tussen de 6-12 weken, soms gepaard gaande met een blafhoest. In 50% van de gevallen is sprake van een IH elders op het lichaam; met name lokalisatie in het baardgebied is geassocieerd met een subglottisch IH (Zie Figuur 1).
In geval van stridor en verdenking subglottische IH dient er beoordeling plaats te vinden door de KNO-arts; het liefst met flexibele scopie indien de kliniek dit toestaat. - Segmentale en oppervlakkige of minimal-growth type IH in het gelaat of in het lumbo-sacrale/peri-anale/ genitale gebied kunnen geassocieerd zijn met structurele afwijkingen of syndromen, zoals PHACES syndroom en LUMBAR syndroom (zie ook UV1)
Wanneer moet getwijfeld worden aan de diagnose IH
- Aanwezigheid bij de geboorte
- Ontstaan op leeftijd >12 weken
- Uitblijven van disproportionele groei
- Uitblijven van spontane involutie/regressie
- Snelle involutie (binnen het eerste levensjaar)
- Fors (recidiverend) bloeden
- Thrill voelen en/of souffle horen bij lichamelijk onderzoek
- Comprimeerbaar of leeg te drukken tumor
- Vast aanvoelende tumor
- Houdingsafhankelijk veranderen van de vaatafwijking
- Bleke halo rondom de tumor
- Doorgroei in onderliggend spierweefsel
Verwijsindicaties vanuit de 0e en 1e lijn
Verwijs (of overleg) bij voorkeur binnen één week naar een dermatoloog/kinderarts met expertise of gespecialiseerd centrum bij:
- Twijfel aan de diagnose IH
- IH centraal in het gelaat (zie Figuur 2)
- IH buiten het hoofdhalsgebied groter dan 4 cm
- IH in de mammaregio bij meisjes
- IH in een doorgaans zichtbaar gebied, in overleg met de ouders
- Genitale en/of lumbosacrale (midline) lokalisatie
- Meer dan 10 IH op het lichaam*
- Snel groeiend IH (NB indien een afwachtend beleid gehanteerd wordt: controleer in weken naar de leeftijd in maanden; dus bij 1 maand oud: controle na 1 week, etc.)
- Ulcererend IH, ook indien er alleen necrotische korstjes zichtbaar zijn
- Bij het ontstaan van een stridor (vanaf een leeftijd van 5-6 weken)
- In overleg met de ouders, bij wens tot behandeling of niet wegneembare zorgen
Indien er voor een afwachtend beleid wordt gekozen, controleer in ieder geval volgens ‘leeftijd kind in maanden’ = ‘controle interval in weken’ (1 maand oud à controle na 1 week, 2 maanden oud à controle na 2 weken). Bied ouders en goed vangnet aan met duidelijk uitleg over alarmsymptomen. Meet het IH en neem foto’s.
*: Als leidraad voor verwijzing vanuit de 0e/1e lijn kan er ook gebruik gemaakt worden van de recent verschenen Infantile Hemangioma Referral Score (IHRes); (https://www.ihscoring.com/wp-content/uploads/2020/01/PFD-PDF-RESULTATS_NL.pdf).
Een kanttekening hierbij is dat het nieuwe advies vanuit deze richtlijn luidt om bij meer dan 10 IH te verwijzen.
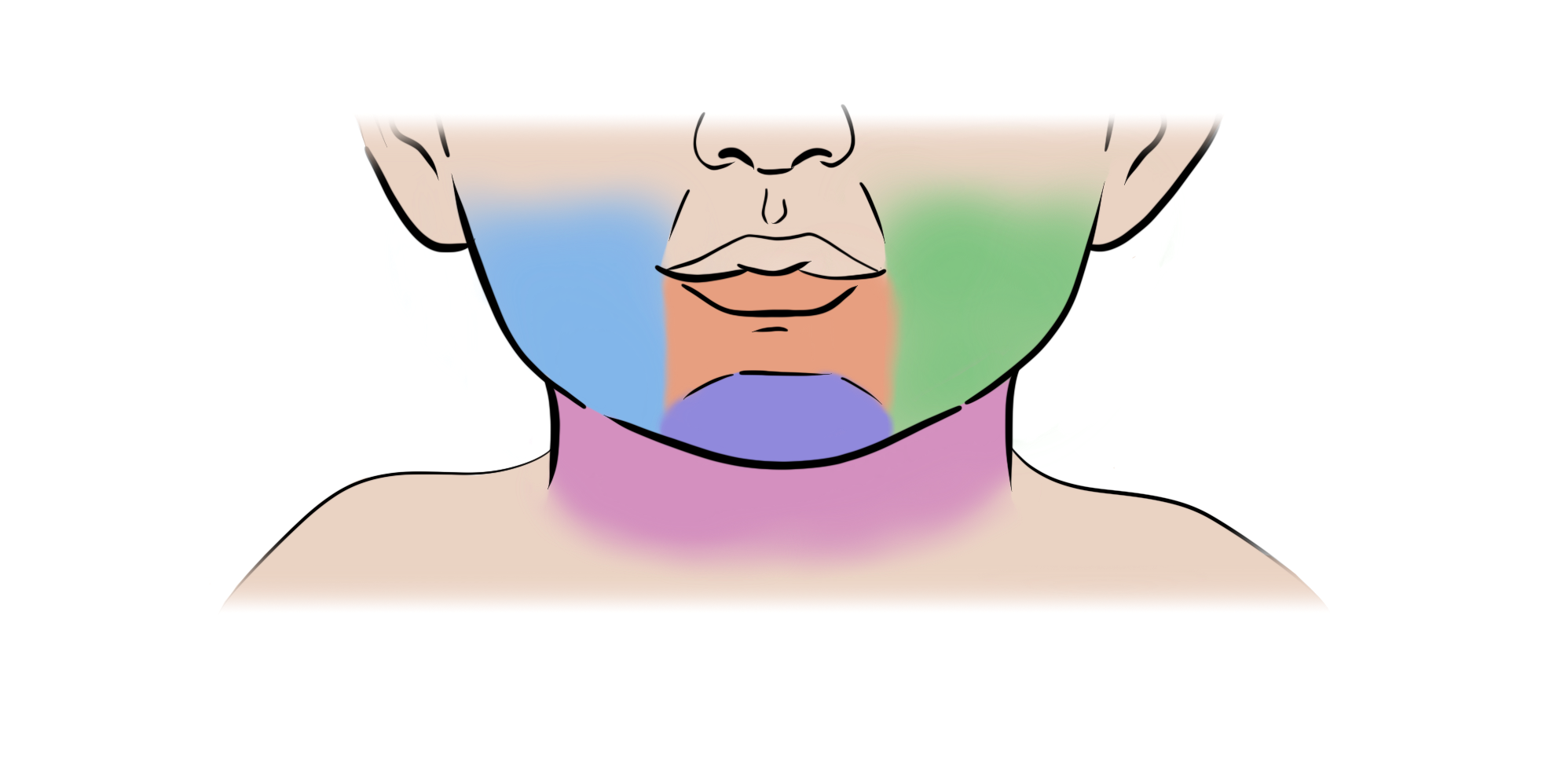
Figuur 1: IH in baardregio
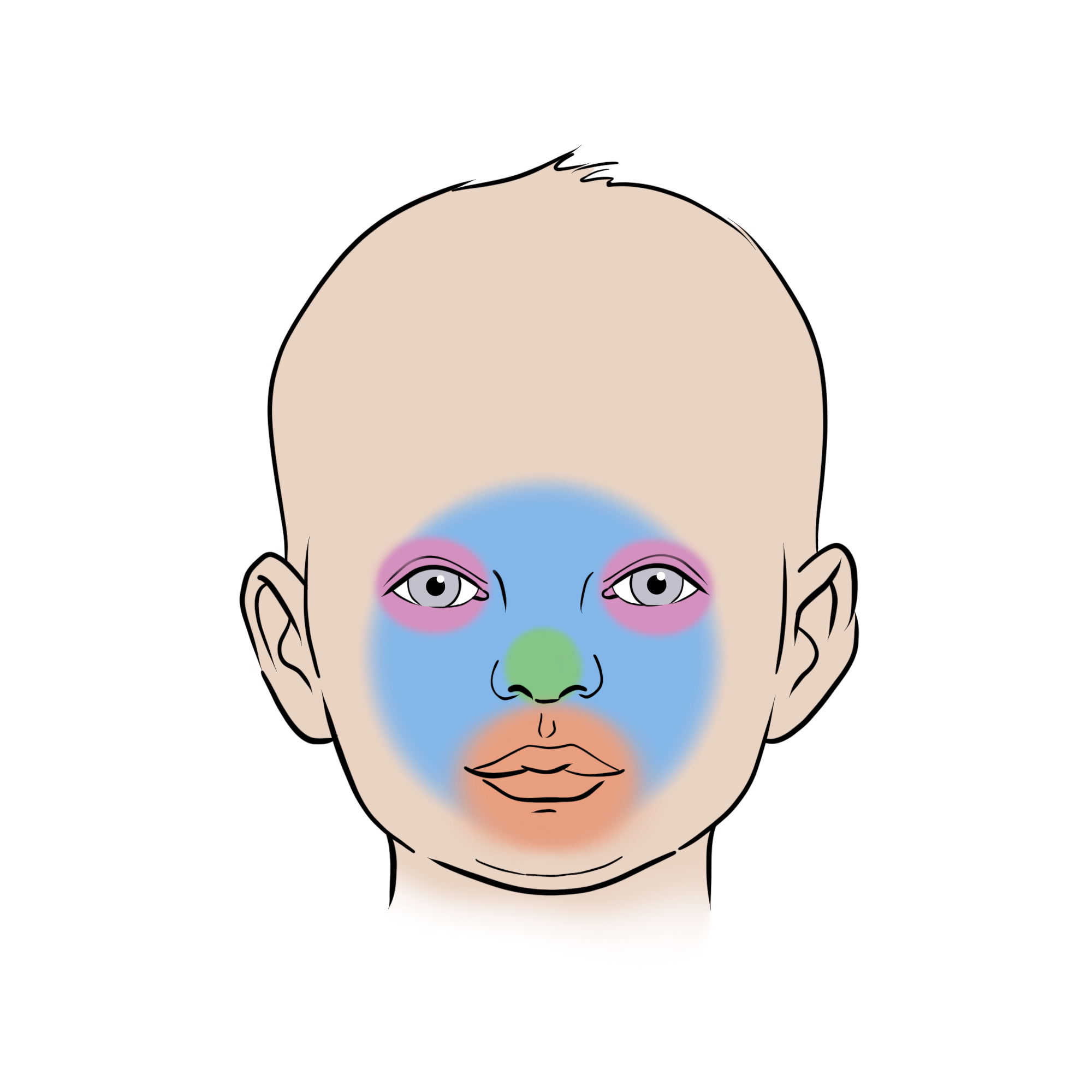
Figuur 2: IH centraal in het gelaat
Beoordelingsdatum en geldigheid
Publicatiedatum : 19-04-2021
Beoordeeld op geldigheid : 11-01-2021
Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update).
De Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) is regiehouder van deze richtlijnen eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn(modules). De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door arts-onderzoekers van de NVDV en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Deze richtlijn over infantiele hemangiomen is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering. De richtlijn berust op de resultaten van wetenschappelijk onderzoek en aansluitende meningsvorming gericht op het vaststellen van goed medisch handelen. De richtlijn geeft aanbevelingen voor de diagnostiek, behandeling en follow-up van patiënten met een infantiel hemangioom.
Doelgroep
De richtlijn is bestemd voor alle zorgverleners die betrokken zijn bij de zorg voor patiënten met infantiele hemangiomen zoals dermatologen, kinderartsen, plastisch chirurgen, kinderchirurgen, KNO-artsen, radiologen, oogartsen, pathologen, huisartsen en jeugdartsen. Voor (de ouders van) patiënten zal aparte informatie worden opgesteld, beschikbaar via de website van de NVDV (www.nvdv.nl) en www.thuisarts.nl.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met infantiele hemangiomen en patiëntenvertegenwoordiger(s) vanuit Hevas (zie hiervoor het overzicht van de werkgroepleden de tabel hieronder). Wetenschappelijke verenigingen zoals NVK, NVPC, NVVH, NVKNO, NOG, NVvR, NVVP, NHG, NVZA en de AJN en stakeholders zoals VIG, NVZ, V&VN, NFU, ZN, ZiNL en de patiëntenfederatie werden voor de knelpunten analyse en commentaarronde uitgenodigd.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroepleden – versie 2020
|
Werkgroeplid |
Affiliatie en vereniging |
|
Mw. Dr. C.J.M. van der Vleuten, dermatoloog, (voorzitter) |
Radboudumc, Nijmegen, NVDV |
|
Dhr. Z. Çiftçi, arts-onderzoeker (secretaris) (vanaf februari 2020) |
Bureau NVDV, Utrecht, NVDV |
|
Mw. C.T. van den Bosch, patientvertegenwoordiger |
Bestuur HEVAS |
|
Dhr. Dr. C.C. Breugem, plastisch chirurg |
Amsterdam UMC, NVPC |
|
Dhr. L.M.A. Favié, ziekenhuisapotheker |
UMC Utrecht, NVZA |
|
Dhr. S.W. Genders, oogarts (vanaf september 2019) |
LUMC, Amsterdam UMC, NOG |
|
Mw. Dr. M. de Graaf, dermatoloog |
UMC Utrecht, NVDV |
|
Dr. J.J.E. van Everdingen, dermatoloog n.p. |
Directeur NVDV |
|
Mw. Dr. D.J.J. Hermans, dermatoloog |
Jeroen Bosch ziekenhuis, NVDV |
|
Mw. M.F. Hofhuis, arts-onderzoeker (secretaris) (tot november 2019) |
Bureau NVDV, Utrecht, NVDV |
|
Dhr. T. Boere, arts-onderzoeker (secretaris) (tot februari 2020) |
Bureau NVDV, Utrecht, NVDV |
|
Dhr. Dr. J. Honings, KNO-arts / Hoofd-hals chirurg |
Radboudumc, NVKNO |
|
Mw. Prof. Dr. C.M.A.M. van der Horst, plastisch chirurg |
Amsterdam UMC, NVPC |
|
Mw. M.P. Jongma, patientvertegenwoordiger |
Bestuur HEVAS |
|
Mw. K. Kamphuis – van Ulzen, radioloog |
Radboudumc, NVvR |
|
Dhr. Dr. P.C.J. de Laat, kinderarts |
Erasmus MC, NVK |
|
Mw. M. Marinkovic, oogarts (tot september 2019) |
LUMC, NOG |
|
Mw. Dr. E. Mendels, dermatoloog |
Erasmus MC, NVDV |
|
Mw. M. Mul, huisarts n.p. |
NHG |
|
Mw. Dr. M.F. Raphael, kinderarts-oncoloog |
Amsterdam UMC, NVK |
|
Dhr. Dr. B.H. Verhoeven, kinderchirurg |
Radboudumc, NVVH |
|
Dhr. A.C. van der Wal, patholoog |
Amsterdam UMC, NVVP |
|
Ondersteuning werkgroep |
Affiliatie en vereniging |
|
Mw. I. Tissen, jeugdarts |
AJN |
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben bij aanvang van en na het afronden van de richtlijn schriftelijk verklaard of zij in de laatste 3 jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen is hieronder opgenomen. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van de NVDV.
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van de Nederlandse Vereniging voor Dermatologie en Venereologie.
|
Werkgroeplid |
Nevenfunctie |
Gemelde belangen (firma en activiteit) |
Ondernomen actie (indien van toepassing) |
|
Dr. C.J.M. van der Vleuten, dermatoloog, (voorzitter) |
Geen |
Consultatie/advisering Pierre Fabre |
Treedt terug in de rol van voorzitter, indien er in de werkgroep discussie is over onderwerpen die gerelateerd zijn aan het advies wat gegeven wordt aan Pierre Fabre. |
|
Dhr. Z. Çiftçi, arts-onderzoeker (secretaris) |
Geen |
Geen |
Geen |
|
Dhr. T. Boere, arts-onderzoeker (secretaris) |
Geen |
Geen |
Geen |
|
Mw. C.T. van den Bosch, patientvertegenwoordiger |
Geen |
Geen |
Geen |
|
Dhr. Dr. C.C. Breugem, plastisch chirurg |
Geen |
Geen |
Geen |
|
Dhr. L.M.A. Favié, ziekenhuisapotheker |
Geen |
Geen |
Geen |
|
Dhr. S.W. Genders, oogarts |
Geen |
Geen |
Geen |
|
Mw. Dr. M. de Graaf, dermatoloog |
Geen |
Geen |
Geen |
|
Dr. J.J.E. van Everdingen, directeur NVDV, dermatoloog n.p. |
Geen |
Geen |
Geen |
|
Mw. Dr. D.J.J. Hermans, dermatoloog |
Geen |
Geen |
Geen |
|
Mw. M.F. Hofhuis, arts-onderzoeker (secretaris) |
Geen |
Geen |
Geen |
|
Dhr. Dr. J. Honings, KNO-arts |
Geen |
Geen |
Geen |
|
Mw. Prof. Dr. C.M.A.M. van der Horst, plastisch chirurg |
Geen |
Geen |
Geen |
|
Mw. M.P. Jongma, patientvertegenwoordiger |
Geen |
Geen |
Geen |
|
Mw. K. Kamphuis – van Ulzen, radioloog |
Geen |
Geen |
Geen |
|
Dhr. Dr. P.C.J. de Laat, kinderarts |
Geen |
|
|
|
Mw. M. Marinkovic, oogarts |
Geen |
Geen |
Geen |
|
Mw. Dr. E. Mendels, dermatoloog |
Geen |
Geen |
Geen |
|
Mw. M. Mul, huisarts |
Geen |
Geen |
Geen |
|
Mw. Dr. M.F. Raphael, kinderarts |
Geen |
Geen |
Geen |
|
Dhr. Dr. B.H. Verhoeven, kinderchirurg |
Geen |
Geen |
Geen |
|
Dhr. A.C. van der Wal, patholoog |
Geen |
Geen |
Geen |
Inbreng patiëntenperspectief
Er is aandacht besteed aan het patiëntenperspectief door deelname van de patiëntenvereniging Hevas (Nederlandse ouder- en patiëntenvereniging voor hemangiomen en vasculaire malformaties) in de richtlijnwerkgroep. Zij zijn inhoudelijk betrokken geweest bij het opstellen van de projectaanvraag en in de richtlijnwerkgroep. De conceptrichtlijn is tevens voor commentaar en autorisatie voorgelegd aan patiëntenvereniging Hevas.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn(module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren, zoals de invoering van nieuwe systemische middelen. Omdat er mogelijk een grote maatschappelijke impact te verwachten zou zijn bij een grote toename in het gebruik van propranolol (Hemangiol) werd er in 2020 een doorrekening van de gewijzigde kosten bij integrale implementatie van de richtlijn gerealiseerd in een zogenaamde Budget Impact Analyse (BIA). De volledige rapportage is opgenomen in de separate bijlage ‘Budget impact analyse’.
Werkwijze
De werkgroep Infantiele Hemangiomen heeft in 2018-2021 de vraag- en doelstellingen van deze richtlijn met elkaar afgestemd en uitgewerkt. De ontwikkeling van deze richtlijn is gebaseerd op het ‘consensusdocument voor de behandeling van infantiele hemangiomen’ welke in 2017 werd vastgesteld door 4 samenwerkende (door de minister van VWS erkende) expertisecentra[1] op het gebied van aangeboren vaatafwijkingen samen met patiëntenvereniging Hevas. [Consensusdocument 2017] Naast de 4 expertisecentra zijn er nog enkele andere ziekenhuizen in Nederland waar multidisciplinaire teams (met onder andere dermatologen, (plastisch) chirurgen, kinderartsen en radiologen) zorg leveren aan kinderen met infantiele hemangiomen.
Hieronder wordt de werkwijze van de richtlijn 2021 verder toegelicht.
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. [Medisch Specialistische Richtlijnen] Dit rapport is gebaseerd op het AGREE II-instrument (Appraisal of Guidelines for Research & Evaluation II), dat een internationaal breed geaccepteerd instrument is. [Brouwers 2010] Voor een stap-voor-stapbeschrijving hoe een evidence-based richtlijn tot stand komt, wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften maar wetenschappelijk onderbouwde en breed gedragen inzichten en aanbevelingen waaraan zorgverleners zouden moeten voldoen om kwalitatief goede zorg te verlenen. Aangezien richtlijnen uitgaan van ‘gemiddelde patiënten’, kunnen zorgverleners in individuele gevallen zo nodig afwijken van de aanbevelingen in de richtlijn. Afwijken van richtlijnen is, als de situatie van de patiënt dat vereist, soms zelfs noodzakelijk. Een richtlijn beschrijft wat goede zorg is, ongeacht de financieringsbron (Zorgverzekeringswet (Zvw), Wet langdurige zorg (Wlz), Wet maatschappelijke ondersteuning (Wmo), aanvullende verzekering of eigen betaling door de cliënt/patiënt). Opname van een richtlijn in een register betekent dus niet noodzakelijkerwijs dat de in de richtlijn beschreven zorg verzekerde zorg is. Informatie over kosten zoals beschreven in de richtlijn is gebaseerd op beschikbare gegevens ten tijde van schrijven.
Knelpuntenanalyse
In de eerste vergadering zijn knelpunten en wensen ten aanzien van de richtlijn geïnventariseerd door de werkgroepleden.Tevens zijn er knelpunten aangedragen door de betrokken verenigingen NVK, NOG, NVvH, NVKNO, NVvP, NVPC, NVvR, patiëntenvereniging Hevas, NVZA, VIG en ZN in een knelpuntenanalyse.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep uitgangsvragen opgesteld. Per uitgangsvraag zijn klinisch relevante uitkomstmaten opgesteld, waarbij zowel naar gewenste als ongewenste effecten is gekeken (op bladzijde 18 staat een overzicht van de uitgangsvragen en uitkomstmaten). De werkgroep heeft deze uitkomstmaten gewaardeerd volgens hun relatieve klinisch belang bij de besluitvorming rondom aanbevelingen.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen is aan de hand van specifieke zoektermen een systematische zoekstrategie uitgevoerd in (verschillende) elektronische databases Embase en MEDLINE. In eerste instantie is gezocht naar studies met de hoogste mate van bewijs. De aldus gevonden studies zijn per uitgangsvraag door twee tot drie werkgroepleden/auteurs van de modules (CvdV, EM, PdL, DH, MdG, MR en CvdH) onafhankelijk van elkaar geselecteerd op basis van titel en abstract en vooraf opgestelde selectiecriteria. Bij discrepantie is een derde persoon gevraagd (MH). De beoordeling en uiteindelijke selectie op basis van volledige tekst is gedaan door arts-onderzoeker(s) van de NVDV. De geselecteerde studies zijn gebruikt om de uitgangsvraag te beantwoorden. De zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de zoekverantwoording.
Kwaliteits beoordeling individuele studies
De beoordeling van de kwaliteit van het wetenschappelijk bewijs/onderzoeksgegevens is in de richtlijn tot stand gekomen met de GRADE-methode.
Bij de GRADE-methode (Grading Recommendations Assessment, Development and Evaluation) worden individuele studies systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB)-tabellen, deze zijn op te vragen via de NVDV. Hiervoor is gebruikgemaakt van de Cochrane risk of bias tool. [Higgins 2011]
Tabel 1 geeft een kort overzicht van de indeling van methodologische kwaliteit van individuele studies volgens GRADE. Een volledige uitleg over de GRADE-methode valt buiten het bestek van deze richtlijn, zie hiervoor het ‘GRADE handbook’. [Schünemann 2013, https://www.gradeworkinggroup.org/]
Tabel 1. Indeling van kwaliteit van wetenschappelijk bewijs volgens GRADE
|
GRADE-systeem |
||
|
Kwaliteitsindeling bewijs |
|
|
|
|
|
|
|
|
|
|
|
|
Startkwalificatie |
- Gerandomiseerd onderzoek = hoog - Observationele studie = laag |
|
|
Factoren die de kwaliteit van bewijs kunnen verlagen* |
- Ernstige of zeer ernstige beperkingen in de kwaliteit van de studie - Indirectheid van het bewijs - Belangrijke inconsistentie tussen studies - Imprecisie - Grote kans op ‘publicatiebias’ |
|
|
Factoren die de kwaltiteit van bewijs kunnen verhogen** |
- Sterk bewijs voor een associatie – significant relatief risico van > 2 (< 0,5) gebaseerd op consistent bewijs uit twee of meer observationele studies, zonder plausibele ‘confounders’ (+1) - Zeer sterk bewijs voor een associatie – significant relatief risico van > 5 (< 0,2) gebaseerd op direct bewijs zonder belangrijke bedreigingen voor de validiteit (+2) - Bewijs voor een dosis respons gradiënt (+1) - Alle plausibele ‘confounders’ zonder het effect te hebben verminderd (+1) |
|
* Elk criterium kan de kwaliteit verminderen met 1 stap of bij zeer ernstige beperkingen met 2 stappen.
** Verhogen kan alleen indien er geen beperkingen zijn t.a.v. de studiekwaliteit, imprecisie, inconsistentie, indirectheid en publicatiebias
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde studies zijn overzichtelijk weergegeven als ‘karakteristieken en resultaten van geïncludeerde studies’ in de evidence tabellen. De belangrijkste bevindingen uit de literatuur met betrekking op de vooraf opgestelde uitkomstmaten zijn beschreven in de samenvatting van de literatuur.
Formuleren van conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methode. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten werden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overige overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn met behulp van de GRADE-methodiek gebaseerd op het beschikbare wetenschappelijke bewijs, de belangrijkste overige overwegingen en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht of het niveau van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling.
Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling beschreven (zie de bijlage ‘Kennislacunes’).
Commentaar- en autorisatiefase
De conceptrichtlijn is aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren zijn verzameld in een commentaarformulier/tabel en besproken met de werkgroep. Naar aanleiding van de commentaren is de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn is aan de betrokken (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd ter autorisatie en door hen geautoriseerd dan wel geaccordeerd. Zie daarvoor paragraaf ‘Autorisatie’.
Literatuur
- Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
- Consensusdocument voor de behandeling van infantiele hemangiomen, HEVAS. 5 juli 2017
- Higgins JPT, Green S (editors). Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0 [updated March 2011]. The Cochrane Collaboration, 2011. Available from http://www.handbook.cochrane.org.
- Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit.. Online beschikbaar op http://richtlijnendatabase.nl/ Laatst geraadpleegd op [DATUM geraadpleegd voor concepttekst]
- Van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum 2004.
- Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from.
[1] Het Radboudumc te Nijmegen, het Amsterdam UMC/Emmakinderziekenhuis te Amsterdam, het ErasmusMC/Sophia Kinderziekenhuis te Rotterdam en het UMCU/Wilhelmina Kinderziekenuis te Utrecht.
