HCL bij zwangerschap met diabetes mellitus type 1
Uitgangsvraag
Wat is de rol van een hybrid closed loop bij vrouwen met diabetes mellitus type 1 (DM1) die zwanger zijn of een zwangerschapswens hebben?
Aanbeveling
Bespreek met alle vrouwen met DM1 in de vruchtbare levensfase tijdig preconceptioneel, en ten laatste in de vroege zwangerschap, de voordelen voor glucoseinstelling (TiR), zonder nadelen voor hypoglycemien, en de reductie in het aantal te grote neonaten (LGA) en de nadelen (toename SGA) van HCL systemen ten opzichte van de andere glucose regulatie systemen.
Maak de keuze voor het type HCL systeem voor gebruik in de zwangerschap op basis van pompeigenschappen, algoritmes, streefwaarden en wensen van de zwangere met DM1.
Overwegingen
Balans tussen gewenste en ongewenste effecten
De literatuuranalyse is gebaseerd op vijf interventie studies (Stewart, 2016; Stewart, 2018; Lee, 2023; Benhalima, 2024; Polsky, 2024). De cruciale uitkomstmaten ‘tijd binnen bereik’ (Time in Range, TiR) ernstige hypoglykemie en maternale hypoglykemie zijn gerapporteerd in alle vijf de studies. De cruciale uitkomstmaten Diabetische Keto Acidose (DKA) en ‘groot voor de zwangerschapsduur ‘neonaten (Large for gestational age, LGA) zijn beide gerapporteerd in drie van de vijf studies (Lee, 2023; Benhalima, 2024; Polsky, 2024). De verschillen in de uitkomstmaten TiR en LGA zijn mogelijk klinisch relevant, en waren beide ten gunste van de interventie groep (HCL systeem). De bewijskracht voor deze uitkomstmaten is echter van zeer lage kwaliteit. Voor de overige cruciale uitkomstmaten is geen klinisch relevant effect gevonden.
De belangrijke uitkomstmaten levendgeborenen, PE, vroeggeboorte, opname op de NICU, en ernstige groeiachterstand zijn gerapporteerd in drie van de vijf studies (Lee, 2023; Benhalima, 2024; Polsky, 2024). De belangrijke uitkomstmaten PIH, HELLP en aangeboren afwijkingen, zijn enkel gepubliceerd in Benhalima (2024). HCL heeft mogelijk een klinisch relevant effect op het verlagen van de incidentie van aangeboren afwijkingen en de incidentie van pre-eclampsie in vergelijking met andere technieken. HCL heeft mogelijk wel een nadelig klinisch relevant effect op de incidentie van vroeggeboortes (<37 weken) en de incidentie van ‘Klein voor zwangerschapsduur’ in vergelijking met andere technieken. Echter is de bewijskracht voor deze uitkomsten van lage of zelfs zeer lage kwaliteit. Voor de andere belangrijke uitkomstmaten zijn geen klinisch relevante effecten gevonden.
Kwaliteit van bewijs
De overall kwaliteit van bewijs is zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten.
Er is afgewaardeerd vanwege:
- Risk of Bias: methodologische beperkingen aangezien de interventie niet goed geblindeerd kon worden.
- Inconsistentie: inconsistentie van de resultaten.
- Imprecisie: onnauwkeurigheid, omdat het betrouwbaarheidsinterval de grens of beide grenzen van klinische relevantie overschrijdt. Daarnaast was er bij sommige dichotome uitkomstmaten een zeer laag aantal events.
Aanvullende argumenten
Uit onze literatuuranalyse blijkt dat de puntschatter voor de gekozen cruciale zwangerschapsuitkomst (LGA) wijst op klinisch relevante verbeteringen bij gebruik van HCL ten opzichte van andere glucose regulatie systemen. Echter zijn we zeer onzeker over dit effect. De ‘trade-off’ die wordt gezien in de meeste diabetes in zwangerschap studies, waarbij iedere verbetering op LGA, een toename van small for gestational age (SGA) laat zien, is ook in onze literatuuranalyse zichtbaar. Het feit dat in de CONCEPTT trial – een studie van voldoende grootte om geboorte uitkomsten bij gebruik van CGM te vergelijken met andere methodes van glucosemonitoring - een kleine reductie van LGA te zien was, maar een nog veel grotere reductie van NICU opnames, laat zien dat SGA in deze context niet noodzakelijkerwijs op meer pathologie wijst (Feig, 2017). Het feit dat er 13% meer vroeggeboorte wordt waargenomen na HCL wordt door de werkgroep niet goed begrepen, ook al omdat er geen verschil in NICU opnames werd gezien (Feig, 2017). De auteurs van de individuele trials bespreken de uitkomst vroeggeboorte niet. Uit correspondentie naar aanleiding van de AiDAPT-publicatie (Lee, 2023) blijkt dat het hogere aantal vroeggeboorten in de groep met HCL waarschijnlijk niet te wijten is aan de technologie zelf, maar aan meerdere andere factoren (Grzych, 2024). Ten eerste hadden vrouwen in de groep met automated insulin delivery (AID) vaker eerdere zwangerschappen en een geplande keizersnede, wat kan hebben bijgedragen aan een (niet klinisch relevante) kleine reductie van de zwangerschapsduur. Ten tweede had de controlegroep juist opvallend weinig vroeggeboortes, wat mogelijk berust op toeval en is het percentage vroeggeboorte in de interventie groep (45%) ongeveer gelijk aan het populatie risico voor zwangeren met DM1. Belangrijk is dat er geen toename was van neonatale complicaties (Lee, 2023).
De studies besproken in de literatuuranalyse in deze module zijn alle begonnen met HCL eind eerste trimester of begin tweede trimester. Hoewel dit een goed argument is ten gunste van de voordelen van wisselen naar een HCL in dit deel van de zwangerschap, is daarmee een harde conclusie over de meerwaarde van introductie van HCL in preconceptie om daarmee betere perinatale uitkomsten te bereiken, niet te trekken. Met name uitkomsten die beïnvloed worden door eerste trimester glucose instelling, zoals miskraam, live birth en congenitale afwijkingen, zouden in potentie kunnen verbeteren door vroege (preconceptionele) implementatie.
Hoewel het bewijs uit de hierboven genoemde literatuuranalyse voor betere zwangerschapsuitkomsten met HCL systemen beperkt is, zijn er indirecte aanwijzingen dat het gebruik ervan in de preconceptieperiode gunstig is: aangezien HCL buiten de zwangerschap leidt tot aanzienlijke TiR-verbetering (Fan 2024), kan dit een aanwijzing zijn dat ook preconceptioneel gebruik van HCL bijdraagt aan betere uitkomsten. Daarnaast is in bestaande netwerkanalyses aannemelijk gemaakt dat HCL (voor de zwangerschap) leidt tot een lager HbA1c dan andere systemen (Asgharzadeh, 2024). Dit sluit aan bij de aanbevelingen voor glucose zelfmanagement bij patiënten met DM1. Een lage preconceptionele HbA1c is geassocieerd met een aanzienlijke verlaging van het risico op ongunstige uitkomsten, waaronder congenitale afwijkingen en doodgeboorte (Evers, 2004). HCL-systemen zijn effectiever dan oudere therapieën in het bereiken van die streefwaarden (Thivolet, 2021; Boughton, 2022; Carlson, 2022). Daarnaast laten eerdere CGM-data zien dat een verbetering van 5% in time-in-range (TiR) al geassocieerd is met circa 50% reductie in uitkomsten zoals LGA en pre-eclampsie (Sobhani, 2024). Hiermee is vroege inzet van HCL een ondersteunende strategie ter verbetering van de zwangerschapsuitkomsten bij vrouwen met DM1.
Het was reeds aangetoond dat de continue glucose sensor (CGM) in de zwangerschap aanzienlijke voordelen biedt boven de conventionele vingerprik glucose monitoring voor perinatale uitkomsten (Feig, 2017; Jones, 2019), waarbij een opvallend grote mate van verbetering van de perinatale uitkomsten, gelet op de relatief geringe verbetering in glycemische instelling, geldt. De CGM is in Nederland snel en breed ingevoerd in de zwangerschap en preconceptiefase. Andere technologische mogelijkheden, zoals de toediening van insuline via een insulinepomp, lijken juist géén groter voordeel te bieden dan insuline toediening meermaals per dag (MDI) met een insulinepen voor zwangerschapsuitkomsten (Farrar, 2016). De keuze voor insulinepomp wordt daarmee vooral bepaald door gebruikersvoorkeur van de zwangere met DM1.
De perinatale uitkomsten van kinderen van moeders met pre-existente diabetes zijn aanzienlijk slechter dan die van kinderen van moeders zonder diabetes: er treedt vaker een miskraam, congenitale afwijking, vroeggeboorte, perinatale sterfte, macrosomie, schouderdystocie en neonatale hypoglycemie op (Wahabi, 2012). Ook wat betreft maternale uitkomsten geldt dat moeders met pre-existente diabetes slechter af zijn: vaker hypotensieve zwangerschapsaandoeningen en vaker een sectio caesarea, ook kan pre-existente nefro- of retinopathie door de zwangerschap tijdelijk of permanent verslechteren (Cavero-Redondo, 2018; Piccoli, 2013). Het doel van zorg voor diabetes in de zwangerschap is in belangrijke mate het streven naar de best mogelijke perinatale uitkomst- en heeft daarmee duidelijk een ander focus dan de gebruikelijke zorg buiten de zwangerschap, die gericht is op preventie van korte- en lange termijn diabetes gerelateerde complicaties. Daarmee kunnen beleidskeuzes in de zwangerschap of preconceptie fase afwijken van de gebruikelijke zorg voor mensen met diabetes. Een voorbeeld is dat lagere ‘time in range’ (TiR) targets in de zwangerschap op basis van de veronderstelde positieve effecten op perinatale uitkomsten werden geïmplementeerd (Battelino, 2019).
Subgroepen
Het was op basis van de beschikbare data niet mogelijk om een onderscheid te maken in de relatieve voordelen van HCL voor zwangeren met DM1 op basis van de mate van preconceptionele glucose instelling. De AiDAPT trial heeft relatief slechter ingestelde zwangeren met DM1 geïncludeerd (gemiddelde baseline HbA1c 7.7% ± 1.2%) (Lee, 2023) dan de CRISTAL studie (gemiddelde baseline HbA1c = 6.5% ± 0.6%) (Benhalima, 2024). Beide studies laten voordelen zien voor TiR. Op basis van de beschikbare data is de werkgroep van mening dat er geen reden is om bepaalde zwangeren met DM1 op basis van instellingskenmerken uit te zonderen van het aanbieden van HCL systemen in de zwangerschap (Lee, 2025).
Intrapartum en postpartum gebruik HCL systemen
Tijdens de partus zijn door een sterk veranderd eetpatroon en inspanningsniveau, en door verlies van de insulineresistentie na de geboorte van de placenta, grote oscillaties te zien in de insulineresistentie. Sommige clinici waren bezorgd over het voldoende snel kunnen reageren op dergelijke verschillen van HCL algoritmes, en gaven de voorkeur voor continue glucose/insuline infusie durante partu. Ten aanzien van het gebruik van HCL systemen intrapartum/ peripartum zijn inmiddels, buiten de strikte scope van deze richtlijn module, een aantal studies verschenen (Beunen, 2024). Deze observationele data laten zien dat HCL intrapartum veilig leidt tot lagere intrapartum TiR, en geen toename geeft van hypoglycemien. De werkgroep is daarom van mening dat wanneer men voor een HCL heeft gekozen in de zwangerschap, deze in de meeste gevallen ook gedurende de partus op automodus kan blijven functioneren. Ook tijdens lactatie kan de HCL veilig worden voort gebruikt (Lee, 2025).
Verschillende HCL systemen
Er is een snelle ontwikkeling geweest in de laatste decennia op het gebied van diabetes technologie, waarbij met name de algoritmes die de dosering insuline berekenen tussen de momenteel beschikbare systemen verschillen. Het feit dat de insuline gevoeligheid snel verandert in de zwangerschap en postpartum, en de lagere TiR streefwaarden in de zwangerschap zijn twee voorbeelden van verschillende uitdagingen voor dergelijke algoritmes. De in de studies onderzochte systemen zijn CamAPS (compatibel met DANA-i of Ypsomed) (Lee, 2023); Medtronic 670G (Polsky, 2024) en Medtronic 780G (Benhalima, 2024). In de studies van Steward (Stewart, 2016; Stewart, 2018) wordt gebruik gemaakt van DANA-i pomp i.c.m. eigen ontwikkelde software. Verschillen in uitkomsten tussen studies kunnen gerelateerd zijn aan verschillende (software-) systemen, waarbij Medtronic 780G technisch geavanceerder is ten opzichte van 670G, met een adaptiever algoritme (drie vaste streefwaarden in plaats van één) en meer autonomie. CamAPS hanteert verschillende streefwaarden, waaronder de flexibele streefwaarde voor zwangeren (5,5mmol/l) en functioneert zeer autonoom. De mate van autonomie verschilt dus binnen verschillende HCL systemen waarbij de verwachting is dat nieuwere systemen waarschijnlijk nog meer “closed” worden en er daarmee steeds minder input en correctie vragen van de gebruiker.
Hoewel pomp specifieke voorkeuren van de zwangere met DM1 ook een rol spelen in de keuze voor systemen zijn niet alle pomp systemen (bv pod vs losse pomp) te combineren met iedere sensor voor HCL. Daarnaast kan de tijd en moeite die er nodig zijn om een eventuele overstap naar een ander systeem te maken soms interfereren met de zwangerschapsplanning. Er is voor deze module geen formele sensitiviteitsanalyses uitgevoerd op basis van de verschillende systemen, maar het loont toch de moeite om naar de karakteristieken van deze systemen te kijken alvorens een conclusie te trekken. Voor toepassing in de zwangerschap is het belangrijk dat deze systemen de zwangerschapsspecifieke range kunnen bedienen. Daarnaast kan het een voordeel zijn om de streefwaarde manueel in te kunnen stellen en een eventuele extra insuline-injectie zelf te kunnen invoeren.
Waarden en voorkeuren van zwangeren met DM1 (en eventueel hun naasten/verzorgers)
Voor zwangeren met DM1 kan gelden dat vertrouwdheid/ ervaring met het glucose regulerend systeem van grote waarde is, naast de voorlichting van de zorgverlener omtrent effectiviteit en veiligheid van de verschillende systemen. Het toepassen van een nieuw glucose regulerend systeem terwijl men ook nog kampt met een jonge zwangerschap, met daarbij horende klachten en mogelijk verminderde of veranderde voedselintake kan voor sommige zwangeren met DM1 een te grote uitdaging zijn. Overstappen lijkt op basis van de studies echter niet nadelig te zijn: HCL is hierin juist geïnitieerd tijdens de zwangerschap.
Op het moment van het schrijven van deze module hadden enkele systemen nog niet compatibiliteit met alle operating systemen voor mobiele telefoons- ook deze factor, en de bereidheid om van telefoon te wisselen kan bepalend zijn voor de keuze.
Buiten de zwangerschap wordt een afname in diabetes distress gerapporteerd bij gebruik van een HCL systeem. Tijdens de zwangerschap is dit effect echter nog niet systematisch aangetoond; enkel anekdotisch wordt erover gerapporteerd — een bevinding die, gezien de verhoogde druk om strikte glykemische regulatie te realiseren, plausibel lijkt (Halliday, 2024; Lawton, 2023).
Sommige zwangeren met DM1 hebben een sterke voorkeur voor insulinetoedieningssystemen zonder los infuussysteem, hierbij geldt dat men dan beperkter is in de keuze voor (type) HCL.
Het is gezien de bovengenoemde verschillen derhalve van belang de diverse systemen bij vrouwen met een zwangerschapswens al in een vroeg stadium te bespreken. Hierbij moeten specifieke voorkeuren van de patiënt, compatibiliteit van de systemen, autonomie van de HCL én zwangerschap specifieke streefwaarden meegenomen worden.
Kostenaspecten
Het aantal ongeplande en totale ziekenhuisbezoeken was in de AIDAPT trial groter in de standaard zorg groep dan in de HCL groep. De CRISTAL trial liet in een kosteneffectiviteit analyse zien dat HCL minder kostte (€232) met name vanwege minder frequente en kortere ziekenhuisbezoeken (Lee, 2023; Benhalima, 2024).
Samengenomen is er weinig literatuur m.b.t. de kosteneffectiviteit van het gebruik van HCL systemen bij zwangere vrouwen met DM1. Desondanks suggereren genoemde studies dat het mogelijk is dat een HCL systeem in de zwangerschap kosten effectiever is ten opzichte van andere systemen.
Gelijkheid ((health) equity/equitable)
In een ‘high resource’ gezondheidszorgsysteem als het Nederlandse, is (dure) diabetes zorg en de bijbehorende technologie voor iedereen toegankelijk, mits wordt voldaan aan sensor vergoedingscriteria voor sensoren. Wel vereist het veilig zelfstandig gebruik van deze technologie een basis gezondheidsvaardigheid, en toegang tot mobiele telefoon. Het feit dat, in Nederland, HCL systemen als eerste voor kinderen werd geïmplementeerd, laat zien dat HCL (met goede supervisie) juist toepasbaar is en voordelen kent dan conventionele behandeling voor personen met laaggeletterdheid of intellectuele beperkingen. Eveneens is HCL superieur ten opzicht van andere technieken in zwangeren met DM1 die uitdagingen ervaren bij het volgen van hun diabetesbehandeling.
Verzekeringsaspecten, waarbij bv technologie voor een periode van een aantal jaren wordt vastgelegd, kunnen een barrière vormen voor toegankelijkheid van technologie die specifiek gericht is op vrouwen in de periconceptie of zwangerschapsfase. Indien met bestaande (niet HCL) techniek de glycemische streefwaarden niet gehaald worden is het op dit moment niet mogelijk contracten open te breken en vervroegd over te stappen op een HCL, wanneer de gecontracteerde pomp niet uitgebreid kan worden tot HCL. Dit kan resulteren in de situatie dat de zwangerschapswens moet worden uitgesteld.
Anderzijds kunnen vrouwen al jaren preconceptioneel volgens aanbeveling van de Nederlandse richtlijn tijdens de zwangerschapswens een CGM vergoed krijgen teneinde een optimale glucose instelling te verkrijgen. Bij een vrije keus voor een insulinepomp betekent dit dat een aanzienlijk deel van de vrouwen met zwangerschapswens al preconceptioneel is ingesteld op HCL. Deze situatie is niet meegenomen in deze module, omdat veel van de onderzochte zwangeren met DM1 pas in het eerste trimester op HCL overstapten. Hoewel de zoekvraag ook preconceptionele behandeling omvatte zijn geen geschikte studies over gevonden die deze vraag separaat onderzochten, en is er dus alleen indirect bewijs meegenomen in de overwegingen.
Geen van de RCTs (AIDAPT, CRISTAL) rapporteerde etnische of socio-economische data van de deelnemers, het is daarom niet goed te zeggen of deze factoren een rol spelen in het wel of niet voordelig zijn van de HCL systemen ten opzichte van de andere systemen.
Samengevat leiden HCL toepassing in de zwangerschap naar verwachting niet tot een verandering in gezondheidsgelijkheid
Aanvaardbaarheid:
De HCL lijkt aanvaardbaar voor de betrokkenen. De verschillende sensoren zijn niet onderling vergeleken, daarmee geniet het de voorkeur om van de sensor die patiente al heeft te continueren, uiteraard mits deze voldoende in staat is om de pregnancy specific target range te behalen. Er zijn geen ethische bezwaren te verwachten.
Duurzaamheid
Bij de HCL in vergelijking met conventionele pomp/ sensor combinaties spelen de volgende duurzaamheidsaspecten een rol: de belasting van de productie van disposable materialen die nodig zijn voor het systeem, de belasting op het verwerken van de afvalstromen die ontstaan na gebruik van de disposable artikelen (pomp, insuline vulling, sensor, infuussysteem, pleisters), en de reiskosten van ziekenhuisbezoeken, alsook ziekenhuisverblijfsimpact. Omdat een HCL, in vergelijking met conventionele CGM en insulinepomp, geen additionele productiekosten of afvalstromen veroorzaakt, maar wel bijdraagt aan een reductie aan ziekenhuisbezoeken, zou HCL een duurzamere keuze kunnen zijn.
Haalbaarheid
De inzet van HCL lijkt haalbaar, omdat deze reeds beschikbaar is. Wel voorziet de werkgroep mogelijke belemmeringen rondom periodiek slechte leverbaarheid van bepaalde onderdelen/ systemen. Verder voorziet de werkgroep mogelijke beperkingen door verzekeringstechnische bepalingen. Ondanks vergoeding van sensoren voor vrouwen met zwangerschap(-swens) is niet iedere pomp compatibel te gebruiken als HCL. De haalbaarheid van de inzet van HCL hangt derhalve af van de bereidwilligheid van verzekeraars om een andere pomp te vergoeden wanneer een huidig systeem niet als HCL kan functioneren.
Rationale van aanbeveling-1: weging van argumenten voor en tegen de interventies
Hybrid closed loop systemen (HCL) zorgen bij zwangere voor een klinisch relevante toename in de tijd binnen doelbereik en klinisch relevante afname van LGA, zonder toename van (ernstige) hypoglykemie, Daarnaast doet zich een toename in SGA voor, zonder daaraan gerelateerde toename van NICU opnames.
Omdat HCL in verschillende groepen leidt tot lagere HbA1c en een preconceptioneel lager HbA1c leidt tot een reductie in congenitale afwijkingen of miskramen, zijn er - hoewel geen directe bewijzen - sterke indirecte bewijzen de HCL preconceptioneel in te zetten.
De werkgroep is van mening dat wanneer men voor een HCL heeft gekozen in de zwangerschap, deze in de meeste gevallen ook gedurende de partus op automodus kan blijven functioneren. Ook tijdens lactatie kan de HCL veilig worden voort gebruikt.
Bespreek met alle vrouwen met DM1 in de vruchtbare levensfase regelmatig of er sprake is van een zwangerschapswens. Mocht er een zwangerschapswens zijn, dan is het belangrijk om bij het aanbevelen van een systeem naast de afweging op basis van patiënt specifieke wensen en technisch vlak ook de verzekeringstechnische aspecten mee in overweging te nemen.
Eindoordeel:
[Sterke aanbeveling voor (Doen)]
Rationale van aanbeveling-2: weging van argumenten voor en tegen de interventies
De werkgroep is van mening dat, op basis van de thans beschikbare data, geen conclusie kan worden getrokken ten aanzien van welk HCL systeem prevaleert boven andere systemen. Naar verwachting komen in de komende jaren HCL systemen met zwangerschap specifieke en lagere glucose targets breder beschikbaar. Gezien het besproken indirecte bewijs voor HCL tijdens de zwangerschap is het aannemelijk om systemen te selecteren op eigenschappen en niet per definitie voor iedere pomp de RCT af te wachten.
Eindoordeel:
[Sterke aanbeveling voor (Doen)]
Onderbouwing
Achtergrond
Introduction
After rapidly increased uptake, use of continuous glucose sensor (CGM) in preconception and pregnancy in diabetes mellitus type 1 (DM1) is now commonplace. CGM’s popularity is explained by its ability to achieve better diabetes specific outcomes and its user friendliness. Moreover, compared to other methods of glucose monitoring, CGM has been shown to lead to improved pregnancy outcomes.
Insulin pump use, with or without the option of hybrid closed loop (the sensor and pump are paired), is similarly widespread, although there is no clear evidence base for a preference over insulin pen (MDI) in terms of improved perinatal outcomes.
This guideline aims to evaluate the role of Hybrid Closed Loop (HCL) systems during pregnancy.
Conclusies / Summary of Findings
Population: Pregnant women or women wishing to become pregnant with DM1
Intervention: Hybrid Closed Loop
Comparator: Other techniques for glucose regulation
|
Outcome Timeframe |
Study results and measurements |
Absolute effect estimates |
Certainty of the evidence (Quality of evidence) |
Summary |
|||||
|
HCL |
Other techniques |
||||||||
|
Time in range
|
Measured by: Percentage of time in range within 63 – 140 mg/dL Scale: - High better Based on data from 277 participants in 5 studies
|
|
|
Very low Due to serious risk of bias, inconsistency and imprecision7 |
We are uncertain whether HCL improves or worsens time in range |
||||
|
Difference: MD 5.9 higher (CI 95% 2.46 lower - 14.25 higher) |
|||||||||
|
Diabetic keto acidosis
|
Relative risk: 1.04 (CI 95% 0.78 - 1.40) Based on data from 237 participants in 3 studies
|
17 Per 1000 |
16 Per 1000 |
Low Due to serious risk of bias and serious imprecision9 |
HCL may result little or no difference on the incidence of diabetic keto acidosis |
||||
|
Difference: 1 more per 1000 (CI 95% 4 fewer - 6 more) |
|||||||||
|
Severe diabetic dysregulation - Hypoglycemia
|
Measured by: Percentage of time below 63 mg/dL Scale: - Lower better Based on data from 277 participants in 5 studies
|
Difference: MD 0.62 lower (CI 95% 1.54 lower - 0.29 higher) |
Moderate Due to serious risk of bias9 |
HCL probably has little or no difference the percentage of time spent in hypoglycemia |
|||||
|
Large for gestational age
|
Relative risk: 0.84 (CI 95% 0.64 - 1.1) Based on data from 236 participants in 3 studies
|
420 per 1000 |
500 per 1000 |
Very low Due to serious risk of bias, inconsistency, and imprecision1 |
We are uncertain whether HCL increases or decreases the incidence of being large for gestational age |
||||
|
Difference: 80 fewer per 1000 (CI 95% 180 fewer - 50 more) |
|||||||||
|
Live birth
|
Relative risk: 1.0 (CI 95% 0.89 - 1.12) Based on data from 234 participants in 3 studies
|
979 per 1000 |
979 per 1000 |
Very low Due to inconsistency and very serious imprecision,2 |
We are uncertain whether HCL increases or decreases the incidence of live birth |
||||
|
Difference: 0 fewer per 1000 (CI 95% 106 fewer - 116 more) |
|||||||||
|
Preeclampsia
|
Relative risk: 0.83 (CI 95% 0.08 - 8.2) Based on data from 230 participants in 3 studies
|
166 per 1000 |
200 per 1000 |
Very low Due to serious risk of bias and very serious imprecision3 |
We are uncertain whether HCL increases or decreases the incidence of preeclampsia |
||||
|
Difference: 34 fewer per 1000 (CI 95% 184 fewer - 1440 more) |
|||||||||
|
Preterm birth
|
Relative risk: 1.61 (CI 95% 0.69 - 3.74) Based on data from 235 participants in 3 studies
|
376 per 1000 |
233 per 1000 |
Very low Due to very serious imprecision and inconsistency4 |
We are uncertain whether HCL increases or decreases the incidence of preterm birth |
||||
|
Difference: 143 more per 1000 (CI 95% 72 fewer - 638 more) |
|||||||||
|
NICU admission
|
Relative risk: 1.14 (CI 95% 0.63 - 2.07) Based on data from 229 participants in 3 studies
|
285 per 1000 |
250 per 1000 |
Very low Due to serious risk of bias, serious imprecision, and inconsistency5 |
We are uncertain whether HCL increases or decreases the NICU admission |
||||
|
Difference: 35 more per 1000 (CI 95% 92 fewer - 268 more) |
|||||||||
|
Severe hypoglycemia
|
Relative risk: 1.22 (CI 95% 0.59 - 2.5) Based on data from 306 participants in 5 studies
Absolute effect estimates derived from two approaches. Continuity correction or excluding zero-events (results in brackets) |
49 (138) per 1000 |
40 (113) per 1000 |
Very low Due to serious risk of bias and very serious imprecision. |
We are uncertain whether HCL increases or decreases the incidence of severe hypoglycemia. |
||||
|
Difference: 9 (25) more per 1000 (CI 95% 16 (46) fewer – 60 (170) more) |
|||||||||
|
Pregnancy-induced hypertension
|
Based on data from 89 participants in 1 studies
|
Four women in the HCL group compared to six women in the other techniques group experienced gestational hypertension. |
Very low Due to serious risk of bias and very serious imprecision10 |
We are uncertain whether HCL increases or decreases the incidence of pregnancy-induced hypertension |
|||||
|
HELLP syndrome
|
Based on data from 88 participants in 1 studies
|
One woman in the HCL group (n=42) compared to zero women in the other techniques group (n=46) experienced the HELLP syndrome. |
Very low Due to serious risk of bias and very serious imprecision11 |
We are uncertain whether HCL increases or decreases the incidence of HELLP syndrome |
|||||
|
Congenital abnormalities
|
Based on data from 87 participants in 1 studies
|
Two women in the HCL group compared to four women in the other techniques group delivered a baby with congenital malformations. |
Very low Due to serious risk of bias and very serious imprecision12 |
We are uncertain whether HCL increases or decreases the incidence of congenital abnormalities |
|||||
|
Small for gestational age
|
Relative risk: 3.12 (CI 95% 0.51 – 19.11) Based on data from 231 participants in 3 studies
Absolute effect estimates derived from two approaches. Continuity correction or excluding zero-events (results in brackets) |
|
Very low Due to serious risk of bias and very serious imprecision13 |
We are uncertain whether HCL increases or decreases the incidence of severe growth retardation (small for gestational age) |
|||||
- Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias; Inconsistency: serious. The direction of the effect is not consistent between the included studies; Imprecision: serious. Wide confidence intervals;
- Inconsistency: serious. The direction of the effect is not consistent between the included studies; Imprecision: very serious. Wide confidence intervals, Low number of events;
- Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias; Imprecision: very serious. Wide confidence intervals;
- Inconsistency: serious. The direction of the effect is not consistent between the included studies; Indirectness: no serious. Direct comparisons not available; Imprecision: serious. Wide confidence intervals;
- Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias; Inconsistency: serious. The direction of the effect is not consistent between the included studies; Imprecision: serious. Wide confidence intervals;
- Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias; Imprecision: very serious. Wide confidence intervals;
- Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias. In addition, inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias; Inconsistency: serious. The direction of the effect is not consistent between the included studies; Imprecision: serious. Wide confidence intervals;
- Risk of Bias: serious. Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias, Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias; Imprecision: very serious. Low number of patients;
- Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias;
- Risk of Bias: serious. Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias, Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias; Imprecision: very serious. Wide confidence intervals, Low number of patients;
- Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias; Imprecision: very serious. Wide confidence intervals, Low number of patients;
- Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias; Imprecision: very serious. Wide confidence intervals, Low number of patients;
- Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias; Imprecision: very serious. Wide confidence intervals, Low number of patients;
Samenvatting literatuur
Description of studies
A total of five studies were included in the analysis of the literature. Important study characteristics and results are summarized in table 2. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Stewart (2016) conducted an open-label, multicenter, randomized, two-period crossover trial. Participants were recruited from three U.K. National Health Service (NHS) sites (Cambridge, Norwich, and Ipswich). The study included women 18-45 years of age who had a history of DM1 for at least 12 months, and a pregnancy between 8 and 24 weeks of gestation.
Stewart (2018) conducted open-label, randomized, two-period crossover study. Participants were recruited from three U.K. National Health Service (NHS) sites (Cambridge, Norwich, and Ipswich). Inclusion criteria were pregnant women who had DM1 for at least 1 year before pregnancy. They were age 18–45 years and had a singleton pregnancy with ultrasound confirmed gestational age between 8 and 24 weeks.
Benhalima (2024) conducted a double-arm, parallel-group, open-label, randomized controlled trial. The trial was conducted in secondary and tertiary care specialist endocrinology centers at 11 hospitals in Belgium and one hospital in the Netherlands. Inclusion criteria were pregnant women who had a history of DM1 for at least 12 months. Women were recruited until 11 weeks and 6 days’ gestation.
Lee (2023) conducted an open-label, multicenter, randomized, controlled trial in nine sites in the United Kingdom. The inclusion criteria were pregnant women, 18 to 45 years of age, who had had DM1 for at least 12 months. Women were recruited as soon as possible after confirmation by ultrasonography of a viable pregnancy and before 14 weeks’ gestation.
Polsky (2024) conducted a pilot feasibility investigator-initiated, single-blind, randomized controlled trial at two sites in Colorado and Ohio. The study included women 18–45 years old with DM1 >1 year and ≤11 weeks’ gestation.
Table 2. Characteristics of included studies (Vergroot tabel)
|
Study |
Participants |
Comparison |
Follow-up |
Outcome measures |
Comments |
Risk of bias (per outcome measure)* |
|
Stewart, 2016 |
N at baseline: 20
Age (mean, SD): 34.1 ± 4.6
BMI: 29.7 ± 5.7 Duration of DM1 in years: 23.6 ± 7.2
|
Intervention: Overnight Sensor-augmented pump therapy with closed-loop system (4 weeks).
Control: Sensor-augmented pump therapy (4 weeks)
Note: After completion of the randomly assigned interventions, participants could choose to continue sensor-augmented pump therapy or the day-and-night closed-loop system with manually administered boluses before meals until delivery. |
Run-in period: 2 – 4 weeks (for device training and optimization of insulin doses)
Intervention/control: 4 weeks
Washout period: 2-4 weeks (participants were asked finger-stick testing, with or without continuous glucose monitoring or pump therapy, but could not use the closed-loop system.) |
Time in range and hypoglycemia (both only overnight) |
Of the 20 participants, three withdrew during the run-in training phase and 17 underwent randomization. One participant withdrew during her first study phase (sensor-augmented pump therapy) because of termination of pregnancy for trisomy 13.
During the washout period all participants choose to continue the study continuous glucose monitoring and insulin pump devices. |
Moderate RoB (all outcomes) |
|
Stewart, 2018 |
N at baseline: 17
Age (mean, SD): 32.8 ± 5.0
BMI: 26.6 ± 4.4
Duration of DM1 in years: 19.4 ± 10.2
|
Intervention: day-and-night closed-loop insulin delivery (4 weeks)
Control: Sensor-augmented pump therapy (4 weeks)
Note: After the randomized trial, participants could choose to resume their previous intensive insulin therapy or continue to use the study devices (any combination of CGM, pump, or closed-loop) throughout pregnancy and delivery and for up to 6 weeks postpartum. |
Run-in period: 2 – 4 weeks (for device training and optimization of insulin doses)
Intervention/control: 4 weeks
Washout period: 1-2 weeks |
Time in range and hypoglycemia |
Of the 19 participants, two dropped out during training phase. One participant withdrew during her first study phase (sensor-augmented pump therapy) as a result of preterm preterm rupture of membranes, severe oligohydramnios, and termination of pregnancy because of poor fetal prognosis. |
Moderate RoB (all outcomes) |
|
Benhalima, 2024 |
N at baseline Intervention: 46 Control: 49
Age (mean, SD) Intervention: 30.8 ± 4.6 Control: 30.3 ± 3.9
BMI: Intervention: 26.0 ±3.6 Control: 26.9 ± 5.4
Duration of DM1 in years: Intervention: 17.0 ± 9.2 Control: 30.3 ± 3.8
|
Intervention: Advanced hybrid closed loop therapy. MiniMed 780G AHCL combined with CGM
Control: Standard insulin therapy with multiple daily injections, standalone insulin pumps, or sensor-augmented pump therapy with predictive suspension of insulin infusion before or at low sensor glucose concentration, combined with CGM. |
Run-in phase: 10 days (for baseline glycaemic assessment with a CGM)
Women started at a median of 10.1 (IQR 8.6–11.6) weeks of gestation, until delivery. |
Time in range, hypoglycemia, Diabetes ketoacidosis (defined as: pH 7.30 or lower, bicarbonate 18 mmol/L or lower, anion gap higher than 10, and ketones positive in urine or serum), large for gestational age, live birth, PE, PIH, HELLP, preterm birth, NICU admission, and congenital abnormalities |
Of the women included in the intervention, 43 gave birth. Of the women included in the control, 46 gave birth. |
Low RoB (live birth and preterm birth)
Moderate RoB (all other outcomes) |
|
Lee, 2023 |
N at baseline Intervention: 61 Control: 63
Age (mean, SD) Intervention: 32.0 ± 5.0 Control: 30.2 ± 5.5
BMI: Intervention: 27.9 ± 5.9 Control: 26.9 ± 4.8
Duration of DM1 in years: Intervention: 18.8 ± 8 Control: 16 ± 7 |
Intervention: Automated hybrid closed-loop therapy in combination with continuous glucose monitoring.
Control: Standard insulin therapy (by means of multiple daily injections or an insulin pump) in combination with continuous glucose monitoring. |
Run-in period: 4-to-10 days (to provide a baseline glycemic assessment (≥96 hours of glucose values, including 24 hours overnight) and to ensure that continuous glucose monitoring was not associated with unacceptable effects.
Started > 16 weeks’ gestation until delivery. |
Time in range, hypoglycemia, Diabetes ketoacidosis (defined as ketosis with acidosis that resulted in treatment with fixed-rate intravenous insulin infusion), large for gestational age, live birth, PE, preterm birth, and NICU admission. |
Differences in baseline characteristics: Participants in the closed-loop group had more previous pregnancies, whereas those in the standard-care group reported more previous diabetic ketoacidosis events. |
Low RoB (live birth and preterm birth)
Moderate RoB (all other outcomes) |
|
Polsky, 2024 |
N at baseline Intervention: 11 Control: 12
Age (mean, SD) Intervention: 30.7 ± 3.5 Control: 31.5 ± 4.9
BMI: Intervention: 27.4 ± 4.4 Control: 30.5 ± 5.9
Duration of DM1 in years: Intervention: 18.0 ± 6.7 Control: 20.6 ± 8.6 |
Intervention: Hybrid closed loop therapy
Control: Sensor-augmented pump therapy |
Run-in period: 1 week
Started between 14 and 18 weeks gestation, continued until 4-6 weeks postpartum (however, HCL was stopped for hospital admissions (including labor and delivery [L&D]). HCL was resumed between 3 and 7 days postpartum.) |
Time in range, hypoglycemia, Diabetes ketoacidosis, large for gestational age, live birth, PE, preterm birth, and NICU admission. |
Funded by industry but disclosure states: The content of this publication is the authors’ sole responsibility and does not necessarily represent official JDRF, Medtronic MiniMed, Inc., Children’s Diabetes Foundation, University of Colorado Denver, or NIH views. |
Low RoB (live birth and preterm birth)
Moderate RoB (all other outcomes) |
AID: Automated insulin delivery; CGM: continuous glucose monitoring; HCL: Hybrid closed loop; PE: preeclampsia; PIH: pregnancy-induced hypertension; HELLP: hemolysis, elevated liver enzymes, and low platelet count
*For further details, see risk of bias table under Evidence tables
Results
Time in range (critical)
All five studies reported the outcome Time in range, defined as the 24-h percentage of time spent in the target glucose range of 63 – 140 mg/dL (Stewart, 2016; Stewart, 2018; Lee, 2023; Benhalima, 2024; Polsky, 2024).
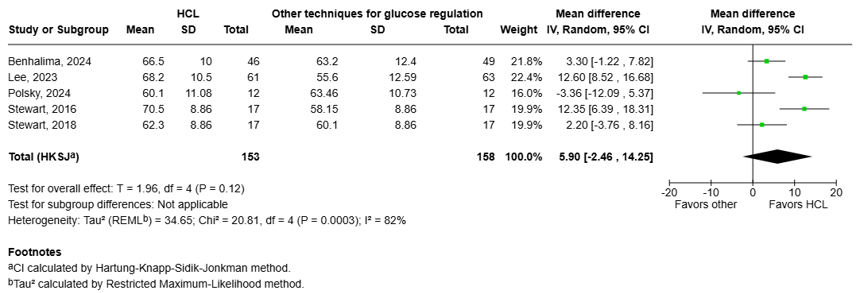
The pooled data shows a mean difference (MD) of 5.90% (95% CI: -2.46% to 14.25%, I2 = 82%) in favor of the HCL system (figure 1.1). This difference was considered clinically relevant.
Figure 1.1 Time in range: Forest plot of the Mean Difference on the effect of HCL system versus other techniques for glucose regulation.
Severe diabetic dysregulation (critical)
Severe hypoglycemia
All five studies reported severe hypoglycemia (Stewart, 2016; Stewart, 2018; Lee, 2023; Benhalima, 2024; Polsky, 2024), defined as hypoglycemia requiring third-party assistance.
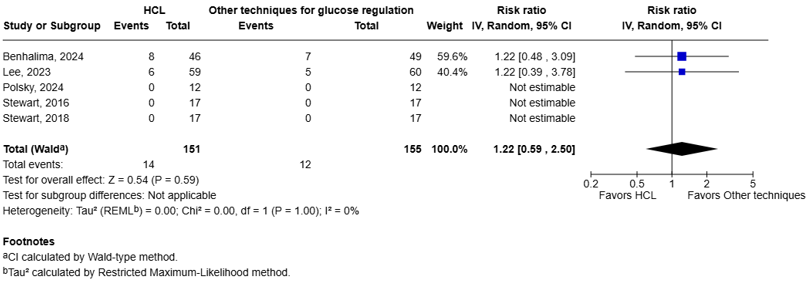
Three studies reported zero events in both arms (Stewart, 2016; Stewart, 2018; Polsky, 2024). The pooled data shows a RR of 1.22 (95%CI 0.59 to 2.50, I2 = 0%), in favor of other techniques (figure 1.2). Because of the zero-event studies, risk differences (RDs) and baseline risks were derived using two approaches. Using a continuity correction (adding 0.5 to the number of events and total of the control group of the non-events in the zero-event studies), the RD was 0.009 (95% CI −0.016 to 0.06). With a baseline risk of 0.04, the MID of RR < 0.75 or > 1.25 resulted in a MID of RD < -0.01 or > 0.01. Therefore, this RD is not clinically relevant. Alternatively, excluding the zero-event studies and using only Benhalima (2024) and Lee (2023), the RD was 0.025 (95% CI −0.046 to 0.17). With a baseline risk of 0.11, the MID of RR < 0.75 or > 1.25 resulted in a MID of RD < -0.03 or > 0.03, and the RD is again not clinically relevant. The potential RD ranged from 0.0009 to 0.025. Overall, both approaches lead to the same conclusion: HCL shows no clinically relevant effect on severe hypoglycemia compared with other glucose regulation techniques.
Figure 1.2 Severe hypoglycemia: Forest plot of the RR on the effect of HCL system versus other techniques for glucose regulation.
Maternal Hypoglycemia
All five studies reported the outcome maternal hypoglycemia defined as the 24-h percentage of time spent below the glucose concentration of 63 mg/dL (Stewart, 2016; Stewart, 2018; Lee, 2023; Benhalima, 2024; Polsky, 2024).
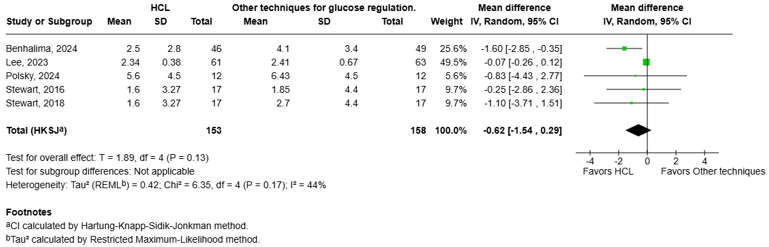
The pooled data shows a MD of -0.62% (95%CI -1.54% to 0.29%, I2 = 44%) in favor of the HCL systems (figure 1.3). This difference was not considered clinically relevant.
Figure 1.3 Hypoglycemia <63 mg/dL: Forest plot of the Mean Difference on the effect of HCL system versus other techniques for glucose regulation.
Diabetic Keto Acidosis
Three studies reported the outcome diabetic keto acidosis (Lee, 2023; Benhalima, 2024; Polsky, 2024). However, in Polsky, 2024 there was no diabetic keto acidosis event.
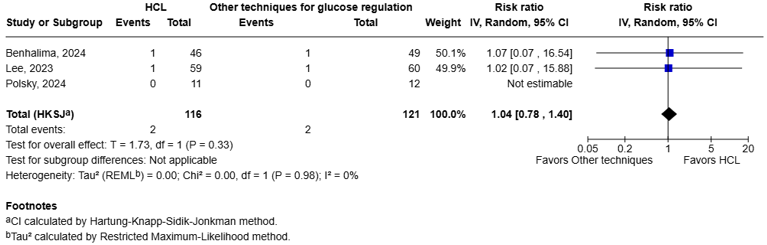
Two women in the HCL group (n=116, incidence: 1.7%) compared to two women in the other techniques group (n=121, incidence: 1.65%) experienced diabetic keto acidosis (figure 1.4). The pooled data shows a RR of 1.04 (95%CI 0.78 to 1.40). The RD is 0.0007 (95%CI: -0.004 to 0.007). With a baseline risk of 0.017, the MID of RR < 0.90 or > 1.10 resulted in a MID of RD < -0.002 or > 0.002 Therefore, the corresponding RD is not considered clinically relevant.
Figure 1.4 Diabetic keto acidosis: Forest plot of the RR on the effect of HCL system versus other techniques for glucose regulation.
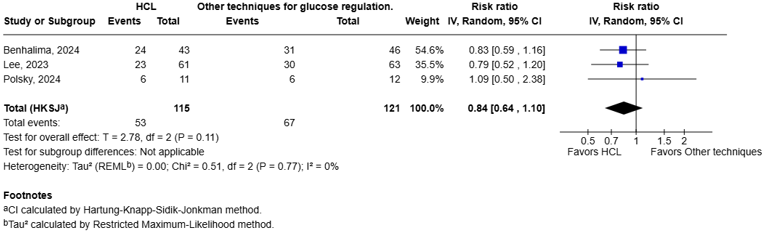
Large for gestational age (LGA) (critical)
Three studies reported the outcome Large for gestational age (Lee, 2023; Benhalima, 2024; Polsky, 2024). Lee (2023) defined this outcome as weight higher than the 90th percentile. Benhalima (2024) and Polsky (2024) did not define the outcome Large for gestational age.
The pooled data shows a RR of 0.84 (95%CI: 0.64 to 1.10, I2 = 0%) in favor of the HCL system (figure 1.5). The corresponding RD is -0.08 (95%CI: -0.18 to 0.05). With a baseline risk of 0.5, the MID of RR < 0.92 or > 1.08 resulted in a MID of RD < -0.050 or > 0.050 Therefore, the corresponding RD is considered clinically relevant.
Figure 1.5 Large for gestational age: Forest plot of the RR on the effect of HCL system versus other techniques for glucose regulation.
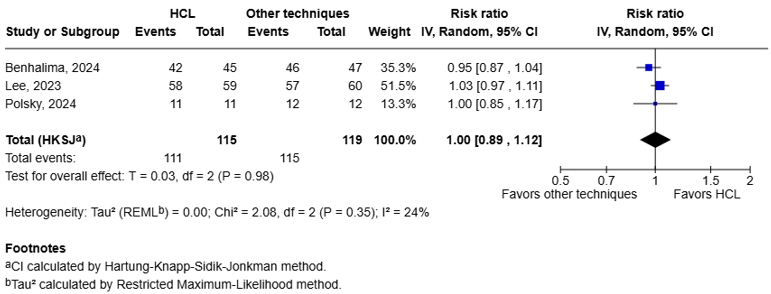
Live birth (important)
Three studies reported the outcome live birth, as they reported the incidence of miscarriages and stillbirth (Lee, 2023; Benhalima, 2024; Polsky, 2024).
The pooled data shows a RR of 1.00 (95%CI: 0.89 to 1.12, I2 = 24%) (figure 1.6). The corresponding RD is 0.00 (95%CI: -0.11 to 0.12). With a baseline risk of 0.98, the MID of RR < 0.90 or > 1.10 resulted in a MID of RD < -0.1 or > 0.1 Therefore, the corresponding RD is not considered clinically relevant.
Figure 1.6 Live birth: Forest plot of the RR on the effect of HCL system versus other techniques for glucose regulation.
Hypertensive disorders of pregnancy (important)
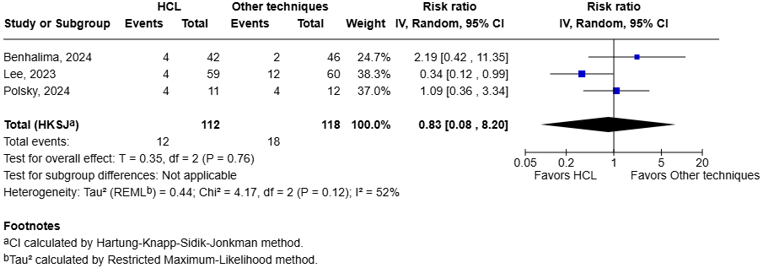
Preeclampsia (PE)
Three studies reported the incidence pregnant women with DM1 suffered from preeclampsia (Lee, 2023; Benhalima, 2024; Polsky, 2024).
The pooled data shows a RR of 0.83 (95%CI: 0.08 to 8.20, I2 = 52%), in favor of the HCL system (figure 1.7). The corresponding RD is -0.03 (95%CI: -0.18 to 1.44). With a baseline risk of 0.2, the MID of RR < 0.85 or > 1.15 resulted in a MID of RD < -0.03 or > 0.03 Therefore, the corresponding RD is considered clinically relevant.
Figure 1.7 Preeclampsia: Forest plot of the RR on the effect of HCL system versus other techniques for glucose regulation.
Pregnancy-induced hypertension (PIH)
Benhalima (2024) reported the incidence of gestational hypertension. Four women in the HCL group (n=43, incidence: 9.3%) compared to six women in the other techniques group (n=46, incidence: 13%) experienced gestational hypertension.
HELLP (hemolysis, elevated liver enzymes, and low platelet count) syndrome
Benhalima (2024) reported the incidence of the HELLP syndrome. One woman in the HCL group (n=42, incidence: 2.4%) compared to zero women in the other techniques group (n=46, incidence: 0%) experienced the HELLP syndrome.
Fetal complications (important)
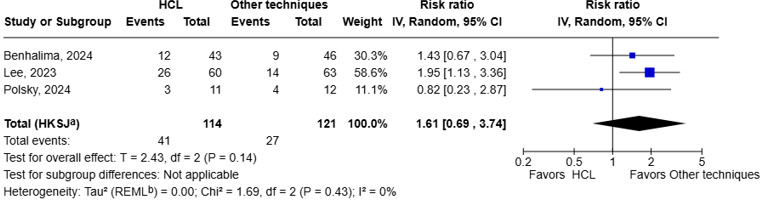
Preterm birth (<37 wk)
Three studies reported the incidence of preterm delivery, at < 37 weeks (Lee, 2023; Benhalima, 2024; Polsky, 2024).
The pooled data shows a RR of 1.61 (95%CI: 0.69 to 3.74, I2 = 0%), in favor of other techniques (figure 1.8). The corresponding RD is 0.14 (95%CI: -0.07 to 0.64). With a baseline risk of 0.23, the MID of RR < 0.85 or > 1.15 resulted in a MID of RD < -0.035 or > 0.035. Therefore, the corresponding RD is considered clinically relevant.
Figure 1.8 Preterm birth: Forest plot of the RR on the effect of HCL system versus other techniques for glucose regulation.
NICU admission
Three studies reported the incidence of neonatal intensive care unit (NICU) stay ≥ 1 day (Lee, 2023; Benhalima, 2024; Polsky, 2024).
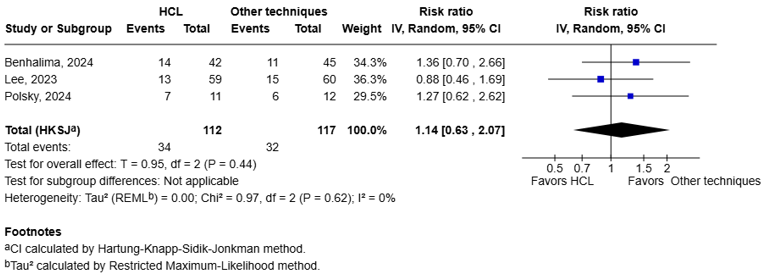
The pooled data shows a RR of 1.14 (95%CI: 0.63 to 2.07, I2 = 0%), in favor of other techniques (figure 1.9). The corresponding RD is 0.035 (95%CI: -0.09 to 0.27). With a baseline risk of 0.25, the MID of RR < 0.85 or > 1.15 resulted in a MID of RD < -0.038 or > 0.038. Therefore, the corresponding RD is not considered clinically relevant.
Figure 1.9 NICU admission: Forest plot of the RR on the effect of HCL system versus other techniques for glucose regulation.
Congenital abnormalities
Benhalima, 2024 reported the incidence of congenital malformation. Two women in the HCL group (n=41, incidence: 4.9%) compared to four women in the other techniques group (n=46, incidence: 8.7%) delivered a baby with congenital malformations.
Small for gestational age
Three studies reported the incidence of small for gestational age (Lee, 2023; Benhalima, 2024; Polsky, 2024). Lee (2023) defined this outcome as weight less than the 10th percentile. Benhalima (2024) and Polsky (2024) did not define the outcome small for gestational age.
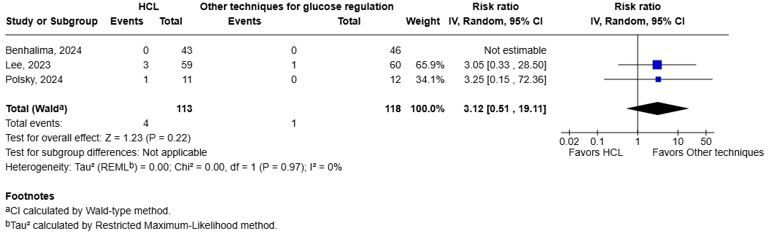
Two studies reported zero events in the control arm (Benhalima, 2024; Polsky, 2024). The pooled data shows a RR of 3.12 (95%CI 0.51 to 19.11, I2 = 0%), in favor of other techniques (figure 1.10). Because of the zero-event studies, risk differences (RDs) and baseline risks were derived using two approaches. Using a continuity correction (adding 0.5 to the number of events and total of the control group of the non-events in the zero-event studies), the RD was 0.035 (95% CI −0.008 to 0.30). With a baseline risk of 0.02, the MID of RR < 0.85 or > 1.15 resulted in a MID of RD < -0.003 or > 0.003. Therefore, this RD is clinically relevant. Alternatively, excluding the zero-event studies and using only Lee (2023), the RD was 0.035 (95% CI −0.008 to 0.30). With a baseline risk of 0.17, the MID of RR < 0.75 or > 1.25 resulted in a MID of RD < -0.003 or > 0.003, and the RD is again clinically relevant. Overall, both approaches lead to the same conclusion: HCL shows a clinically relevant effect on the incidence of small for gestational age compared with other glucose regulation techniques.
Figure 1.10 Small for gestational age: Forest plot of the RR on the effect of HCL system versus other techniques for glucose regulation.
Sensitivity analyses
For all crucial outcome measures, sensitivity analyses (not reported) were performed with the study by Polsky (2024) excluded as a HCL system was used that is not used in Dutch health care anymore. These analyses resulted in the same conclusions (partially due to the small number of events and study size).
Zoeken en selecteren
A systematic review of the literature was performed to answer the following question(s):
What is the effect of a hybrid closed loop in women with DM1 who are pregnant or wish to become pregnant?
Table 1. PICO
|
Patients |
Pregnant women or women wishing to become pregnant with DM1 |
|
Intervention |
Hybrid Closed Loop |
|
Comparison |
Other techniques for glucose regulation |
|
Outcomes |
Time in range, Severe diabetic dysregulation (hypoglycemia, Diabetic keto acidosis), Large for gestational age (LGA), Live birth, Hypertensive disorders of pregnancy (Preeclampsia (PE), Pregnancy-induced hypertension (PIH), HELLP (hemolysis, elevated liver enzymes, and low platelet count) syndrome), and Fetal-neonatal complications (preterm birth (<37 wk), NICU admission, congenital abnormalities, fetal growth restriction) |
|
Other selection criteria |
Study design: systematic reviews, randomized controlled trials, and observational studies |
Relevant outcome measures
The guideline panel considered Time in range, Severe diabetic dysregulation (hypoglycemia, Diabetic keto acidosis), and Large for gestational age (LGA) as a critical outcome measure for decision making; and Live birth, Hypertensive disorders of pregnancy (PE, PIH, HELLP), and Fetal complications (preterm birth (<37 wk), NICU admission, congenital abnormalities, severe growth retardation) as an important outcome measure for decision making.
A priori, the guideline panel did not define the outcome measures listed above but used the definitions used in the studies.
The guideline panel defined the following thresholds as minimal clinically (pregnant woman with DM1) important differences:
- Time in range: 5 – 10% difference
- Severe hypoglycemia: Relative risk of ≥ 25%
- Maternal hypoglycemia: -0.5 SD > MD > 0.5 SD
- Diabetic keto acidosis: Relative risk of ≥ 10%
- Large for gestational age: Relative risk of ≥ 8%
- Live birth: Relative risk of ≥ 10%
- Preeclampsia/HELLLP syndrome/ hypertensive disorders of pregnancy: Relative risk of ≥ 15%
- Preterm birth: Relative risk of ≥ 15%
- NICU admission: Relative risk of ≥ 15%
- Congenital abnormalities: Relative risk of ≥ 10%
- Small for gestational age: Relative risk of ≥ 15%
Search and select (Methods)
A systematic literature search was performed by a medical information specialist using the following bibliographic databases: Embase.com and Ovid/Medline. Both databases were searched from 2014 to January 13th 2025 for systematic reviews, RCTs and observational studies. Systematic searches were completed using a combination of controlled vocabulary/subject headings (e.g., Emtree-terms, MeSH) wherever they were available and natural language keywords. The overall search strategy was derived from three primary search concepts: (1) Diabetes mellitus type 1; (2) Pregnancy/ pregestational; (3) Hybrid Closed Loop. Duplicates were removed using EndNote software. After deduplication a total of 146 records were imported for title/abstract screening. Initially, 33 studies were selected based on title and abstract screening. Since there was a sufficient number of RCTs, it was decided to exclude the observational studies. After reading the full text, 28 studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and five studies were included.
Referenties
- Asgharzadeh, Asra et al. “Hybrid closed-loop systems for managing blood glucose levels in type 1 diabetes: a systematic review and economic modelling.” Health technology assessment (Winchester, England) vol. 28,80 (2024): 1-190. doi:10.3310/JYPL3536
- Battelino T, Danne T, Bergenstal RM, Amiel SA, Beck R, Biester T, Bosi E, Buckingham BA, Cefalu WT, Close KL, Cobelli C, Dassau E, DeVries JH, Donaghue KC, Dovc K, Doyle FJ 3rd, Garg S, Grunberger G, Heller S, Heinemann L, Hirsch IB, Hovorka R, Jia W, Kordonouri O, Kovatchev B, Kowalski A, Laffel L, Levine B, Mayorov A, Mathieu C, Murphy HR, Nimri R, Nørgaard K, Parkin CG, Renard E, Rodbard D, Saboo B, Schatz D, Stoner K, Urakami T, Weinzimer SA, Phillip M. Clinical Targets for Continuous Glucose Monitoring Data Interpretation: Recommendations From the International Consensus on Time in Range. Diabetes Care. 2019 Aug;42(8):1593-1603. doi: 10.2337/dci19-0028. Epub 2019 Jun 8. PMID: 31177185; PMCID: PMC6973648.
- Benhalima K, Beunen K, Van Wilder N, Ballaux D, Vanhaverbeke G, Taes Y, Aers XP, Nobels F, Marlier J, Lee D, Cuypers J, Preumont V, Siegelaar SE, Painter RC, Laenen A, Gillard P, Mathieu C. Comparing advanced hybrid closed loop therapy and standard insulin therapy in pregnant women with type 1 diabetes (CRISTAL): a parallel-group, open-label, randomised controlled trial. Lancet Diabetes Endocrinol. 2024 Jun;12(6):390-403. doi: 10.1016/S2213-8587(24)00089-5. Epub 2024 Apr 30. PMID: 38697182.
- Beunen, Kaat et al. “Advanced Hybrid Closed-Loop Therapy Compared With Standard Insulin Therapy Intrapartum and Early Postpartum in Women With Type 1 Diabetes: A Secondary Observational Analysis From the CRISTAL Randomized Controlled Trial.” Diabetes care vol. 47,11 (2024): 2002-2011. doi:10.2337/dc24-1320
- Boughton CK, Hartnell S, Thabit H, Mubita WM, Draxlbauer K, Poettler T, Wilinska ME, Hood KK, Mader JK, Narendran P, Leelarathna L, Evans ML, Hovorka R. Hybrid closed-loop glucose control compared with sensor augmented pump therapy in older adults with type 1 diabetes: an open-label multicentre, multinational, randomised, crossover study. Lancet Healthy Longev. 2022 Mar;3(3):e135-e142. doi: 10.1016/S2666-7568(22)00005-8. Epub 2022 Mar 7. PMID: 35359882; PMCID: PMC8967297.
- Carlson AL, Sherr JL, Shulman DI, Garg SK, Pop-Busui R, Bode BW, Lilenquist DR, Brazg RL, Kaiserman KB, Kipnes MS, Thrasher JR, Reed JHC, Slover RH, Philis-Tsimikas A, Christiansen M, Grosman B, Roy A, Vella M, Jonkers RAM, Chen X, Shin J, Cordero TL, Lee SW, Rhinehart AS, Vigersky RA. Safety and Glycemic Outcomes During the MiniMed™ Advanced Hybrid Closed-Loop System Pivotal Trial in Adolescents and Adults with Type 1 Diabetes. Diabetes Technol Ther. 2022 Mar;24(3):178-189. doi: 10.1089/dia.2021.0319. Epub 2021 Nov 16. PMID: 34694909; PMCID: PMC8971997.
- Cavero-Redondo I, Martínez-Vizcaíno V, Soriano-Cano A, Martínez-Hortelano JA, Sanabria-Martínez G, Álvarez-Bueno C. Glycated haemoglobin A1c as a predictor of preeclampsia in type 1 diabetic pregnant women: A systematic review and meta-analysis. Pregnancy Hypertens. 2018 Oct;14:49-54. doi: 10.1016/j.preghy.2018.04.004. Epub 2018 Apr 7. PMID: 30527118.
- Evers IM, de Valk HW, Visser GH. Risk of complications of pregnancy in women with type 1 diabetes: nationwide prospective study in the Netherlands. BMJ. 2004 Apr 17;328(7445):915. doi: 10.1136/bmj.38043.583160.EE. Epub 2004 Apr 5. PMID: 15066886; PMCID: PMC390158.
- Fan, Wenqi et al. “Efficacy and Safety of Automated Insulin Delivery Systems in Patients with Type 1 Diabetes Mellitus: A Systematic Review and Meta-Analysis.” Diabetes & metabolism journal vol. 49,2 (2025): 235-251. doi:10.4093/dmj.2024.0130
- Farrar, Diane et al. “Continuous subcutaneous insulin infusion versus multiple daily injections of insulin for pregnant women with diabetes.” The Cochrane database of systematic reviews vol. 2016,6 CD005542. 7 Jun. 2016, doi:10.1002/14651858.CD005542.pub3
- Feig DS, Donovan LE, Corcoy R, Murphy KE, Amiel SA, Hunt KF, Asztalos E, Barrett JFR, Sanchez JJ, de Leiva A, Hod M, Jovanovic L, Keely E, McManus R, Hutton EK, Meek CL, Stewart ZA, Wysocki T, O'Brien R, Ruedy K, Kollman C, Tomlinson G, Murphy HR; CONCEPTT Collaborative Group. Continuous glucose monitoring in pregnant women with type 1 diabetes (CONCEPTT): a multicentre international randomised controlled trial. Lancet. 2017 Nov 25;390(10110):2347-2359. doi: 10.1016/S0140-6736(17)32400-5. Epub 2017 Sep 15. Erratum in: Lancet. 2017 Nov 25;390(10110):2346. doi: 10.1016/S0140-6736(17)32712-5. PMID: 28923465; PMCID: PMC5713979.
- Grzych, Guillaume, and Isabelle Kim. “Automated Insulin Delivery during Pregnancy Complicated by Type 1 Diabetes.” The New England journal of medicine vol. 390,2 (2024): 183-184. doi:10.1056/NEJMc2313410
- Halliday, Jennifer A et al. “Six months of hybrid closed-loop therapy improves diabetes-specific positive well-being, and reduces diabetes distress and fear of hypoglycemia: secondary analysis of a randomized controlled trial.” BMJ open diabetes research & care vol. 12,6 e004428. 22 Dec. 2024, doi:10.1136/bmjdrc-2024-004428
- Jones LV, Ray A, Moy FM, Buckley BS. Techniques of monitoring blood glucose during pregnancy for women with pre-existing diabetes. Cochrane Database Syst Rev. 2019 May 23;5(5):CD009613. doi: 10.1002/14651858.CD009613.pub4. PMID: 31120549; PMCID: PMC6532756.
- Lawton, Julia et al. “Listening to Women: Experiences of Using Closed-Loop in Type 1 Diabetes Pregnancy.” Diabetes technology & therapeutics vol. 25,12 (2023): 845-855. doi:10.1089/dia.2023.0323
- Lee TTM, Collett C, Bergford S, Hartnell S, Scott EM, Lindsay RS, Hunt KF, McCance DR, Barnard-Kelly K, Rankin D, Lawton J, Reynolds RM, Flanagan E, Hammond M, Shepstone L, Wilinska ME, Sibayan J, Kollman C, Beck R, Hovorka R, Murphy HR; AiDAPT Collaborative Group. Automated Insulin Delivery in Women with Pregnancy Complicated by Type 1 Diabetes. N Engl J Med. 2023 Oct 26;389(17):1566-1578. doi: 10.1056/NEJMoa2303911. Epub 2023 Oct 5. PMID: 37796241.
- Lee, Tara T M et al. “Automated insulin delivery during the first 6 months postpartum (AiDAPT): a prespecified extension study.” The lancet. Diabetes & endocrinology vol. 13,3 (2025): 210-220. doi:10.1016/S2213-8587(24)00340-1
- Piccoli GB, Clari R, Ghiotto S, Castelluccia N, Colombi N, Mauro G, Tavassoli E, Melluzza C, Cabiddu G, Gernone G, Mongilardi E, Ferraresi M, Rolfo A, Todros T. Type 1 diabetes, diabetic nephropathy, and pregnancy: a systematic review and meta-study. Rev Diabet Stud. 2013 Spring;10(1):6-26. doi: 10.1900/RDS.2013.10.6. Epub 2013 May 10. PMID: 24172695; PMCID: PMC3932068.
- Polsky S, Buschur E, Dungan K, Garcetti R, Nease E, Malecha E, Bartholomew A, Johnson C, Pyle L, Snell-Bergeon J. Randomized Trial of Assisted Hybrid Closed-Loop Therapy Versus Sensor-Augmented Pump Therapy in Pregnancy. Diabetes Technol Ther. 2024 Aug;26(8):547-555. doi: 10.1089/dia.2024.0012. Epub 2024 Mar 18. PMID: 38386437.
- Sobhani NC, Goemans S, Nguyen A, Chambers ME, Richley M, Gabby LC, Field N, Han CS, Ramos GA. Continuous glucose monitoring in pregnancies with type 1 diabetes: small increases in time-in-range improve maternal and perinatal outcomes. Am J Obstet Gynecol. 2024 Oct;231(4):467.e1-467.e8. doi: 10.1016/j.ajog.2024.01.010. Epub 2024 Jan 17. PMID: 38242337.
- Stewart ZA, Wilinska ME, Hartnell S, Temple RC, Rayman G, Stanley KP, Simmons D, Law GR, Scott EM, Hovorka R, Murphy HR. Closed-Loop Insulin Delivery during Pregnancy in Women with Type 1 Diabetes. N Engl J Med. 2016 Aug 18;375(7):644-54. doi: 10.1056/NEJMoa1602494. PMID: 27532830.
- Stewart ZA, Wilinska ME, Hartnell S, O'Neil LK, Rayman G, Scott EM, Barnard K, Farrington C, Hovorka R, Murphy HR. Day-and-Night Closed-Loop Insulin Delivery in a Broad Population of Pregnant Women With Type 1 Diabetes: A Randomized Controlled Crossover Trial. Diabetes Care. 2018 Jul;41(7):1391-1399. doi: 10.2337/dc17-2534. Epub 2018 Mar 13. PMID: 29535135.
- Thivolet C, Gaudilliere M, Villar Fimbel S, Bendelac N, Mestre B, Protsenko N, Brunot S, Nicolino M. Hybrid closed Loop improved glucose control compared to sensor-augmented pumps in outpatients with type 1 diabetes in real-life conditions with telehealth monitoring. Acta Diabetol. 2022 Mar;59(3):395-401. doi: 10.1007/s00592-021-01820-9. Epub 2021 Nov 1. PMID: 34725723; PMCID: PMC8559915.
- Wahabi HA, Alzeidan RA, Esmaeil SA. Pre-pregnancy care for women with pre-gestational diabetes mellitus: a systematic review and meta-analysis. BMC Public Health. 2012 Sep 17;12:792. doi: 10.1186/1471-2458-12-792. PMID: 22978747; PMCID: PMC3575330.
Evidence tabellen
Risk of Bias tables
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated?
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented?
Were patients blinded?
Were healthcare providers blinded?
Were data collectors blinded?
Were outcome assessors blinded?
Were data analysts blinded?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measure
LOW Some concerns HIGH
|
|
Stewart, 2016 |
Probably yes;
Reason: participants were randomly assigned in permuted blocks of 4 |
Probably no
Reason: no information provided |
Definitely no
Reason: Open-label trial (patients and health care providers not blinded). Blinding of outcome assessors, data collectors and analysts is not reported. |
Definitely yes;
Reason: Only one loss to follow up after randomization. Drop-out as a result of chromosomal anomaly (trisomy 13) unrelated to diabetes and subsequent termination of pregnancy. |
Definitely yes;
Reason: All relevant outcomes were reported |
Definitely yes;
Reason: No other problems noted |
Some concerns (all outcomes) |
|
Stewart, 2018 |
Definitely yes:
Reason: The randomization schedule was created with an automated Web-based program that used a permuted four-block schedule. |
Definitely yes:
Reason: The four-block schedule maintained in a secure database, ensuring that allocation was concealed from trial staff and participants.
|
Definitely no:
Reason: Open-label trial (patients and health care providers not blinded). Blinding of outcome assessors, data collectors and analysts is not reported. |
Definitely yes;
Reason: Only one loss to follow up after randomization. Drop-out as a result unrelated to diabetes and subsequent termination of pregnancy. |
Definitely yes;
Reason: All relevant outcomes were reported |
Definitely yes;
Reason: No other problems noted |
Some concerns (all outcomes) |
|
Benhalima, 2024 |
Definitely yes:
Reason: Participants were randomly assigned with the central software randomisation algorithm performed by I Biostat. Permuted block randomisation was performed on the first four participants. bsequently, deterministic minimisation of variation was applied. The minimisation procedure and randomisation were done by the statistician (AL). |
Definitely yes:
Reason: The outcome of the randomisation was sent digitally to the study centres and communicated to each participant by the local study teams. |
Definitely no:
Reason: Participants, investigators, and study teams were not masked to group allocation. |
Probably yes
Reason: Loss to follow-up was not high or infrequent in intervention (n=3) and control group (n=5). |
Definitely yes;
Reason: All relevant outcomes were reported |
Definitely yes;
Reason: Funding from industry. Industry provided devices and an unrestricted grant for academic research. But no role of the funding body. |
Low concerns (live birth) Some concerns (all other outcomes)
|
|
Lee, 2023 |
Definitely yes:
Reason: Randomized in a 1:1 ratio by means of a Web-based system that used a computer-generated randomization list with permuted block sizes of 2 and 4 and with stratification by clinical site.
|
Probably no:
Reason: no information. |
Definitely no:
Reason: Open-label trial (patients and health care providers not blinded). Blinding of outcome assessors, data collectors and analysts is not reported. |
Definitely no:
Reason: Loss to follow-up was frequent but high in intervention and control. |
Definitely yes;
Reason: All relevant outcomes were reported |
definitely yes:
Reason: funding body had no influence on study outcomes |
Low concerns (live birth) Some concerns (all other outcomes)
|
|
Polsky, 2024 |
Definitely yes:
Reason: randomized 1:1, stratified within center. |
Probably no:
Reason: no information. |
Definitely no:
Reason: Open-label trial (patients and health care providers not blinded). Statisticians were blinded for data analyses, but investigators managing pump settings were not |
Definitely yes:
Reason: Only one loss to follow-up due to fetal death in control group. |
Definitely yes;
Reason: All relevant outcomes were reported |
Definitely yes:
Reason: Funded by industry but the disclosure states: The content of this publication is the authors’ sole responsibility and does not necessarily represent official JDRF, Medtronic MiniMed, Inc., Children’s Diabetes Foundation, University of Colorado Denver, or NIH views. |
Low concerns (live birth) Some concerns (all other outcomes)
|
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Nandam N, Thung S, Venkatesh KK, Gabbe S, Ma J, Peng J, Dungan K, Buschur EO. Tandem T:Slim X2 Insulin Pump Use in Clinical Practice Among Pregnant Individuals With Type 1 Diabetes: A Retrospective Observational Cohort Study. Cureus. 2024 Jan 16;16(1):e52369. doi: 10.7759/cureus.52369. PMID: 38361690; PMCID: PMC10868538. |
Wrong study design (observational) |
|
Medina AMG, Carrillo DCH, Macías MNS, Chávez MJS, Gómez MAR, Parra D, González JAG, Grassi B, Imitola A, Cob A, Rondón M, García M, Velandia OMM. Time in range and mean glucose cut-off points for reduction of fetal outcomes in pregnant women with type 1 diabetes using automated insulin delivery systems. Diabetes Res Clin Pract. 2024 Nov;217:111902. doi: 10.1016/j.diabres.2024.111902. Epub 2024 Oct 21. PMID: 39442806. |
Wrong study design (prospective cohort) |
|
Akturk HK, Giordano D, Champakanath A, Brackett S, Garg S, Snell-Bergeon J. Long-term real-life glycaemic outcomes with a hybrid closed-loop system compared with sensor-augmented pump therapy in patients with type 1 diabetes. Diabetes Obes Metab. 2020 Apr;22(4):583-589. doi: 10.1111/dom.13933. Epub 2020 Jan 3. PMID: 31789447. |
Wrong study design (observational) |
|
Lee TTM, Collett C, Bergford S, Hartnell S, Scott EM, Lindsay RS, Hunt KF, McCance DR, Barnard-Kelly K, Rankin D, Lawton J, Reynolds RM, Flanagan E, Hammond M, Shepstone L, Wilinska ME, Sibayan J, Kollman C, Beck R, Hovorka R, Murphy HR. Automated closed-loop insulin delivery for the management of type 1 diabetes during pregnancy: the AiDAPT RCT. Southampton (UK): National Institute for Health and Care Research; 2024 Apr. PMID: 38718153. |
AiDAPT trial: Data already included through Lee, 2023 |
|
Beunen K, Gillard P, Van Wilder N, Ballaux D, Vanhaverbeke G, Taes Y, Aers XP, Nobels F, Van Huffel L, Marlier J, Lee D, Cuypers J, Preumont V, Siegelaar SE, Painter RC, Laenen A, Mathieu C, Benhalima K. Advanced Hybrid Closed-Loop Therapy Compared With Standard Insulin Therapy Intrapartum and Early Postpartum in Women With Type 1 Diabetes: A Secondary Observational Analysis From the CRISTAL Randomized Controlled Trial. Diabetes Care. 2024 Nov 1;47(11):2002-2011. doi: 10.2337/dc24-1320. PMID: 39331059. |
CRISTAL study: Data already included through Benhalima, 2024 |
|
Donovan LE, Feig DS, Lemieux P, Murphy HR, Bell RC, Sigal RJ, Ho J, Virtanen H, Crawford S, Yamamoto JM. A Randomized Trial of Closed-Loop Insulin Delivery Postpartum in Type 1 Diabetes. Diabetes Care. 2023 Dec 1;46(12):2258-2266. doi: 10.2337/dc23-0882. PMID: 37824779; PMCID: PMC10698209. |
Wrong P (postpartum) |
|
Ozaslan B, Levy CJ, Kudva YC, Pinsker JE, O'Malley G, Kaur RJ, Castorino K, Levister C, Trinidad MC, Desjardins D, Church MM, Plesser M, McCrady-Spitzer S, Ogyaadu S, Nelson K, Reid C, Deshpande S, Kremers WK, Doyle FJ , III, Rosenn B, Dassau E. Feasibility of Closed-Loop Insulin Delivery with a Pregnancy-Specific Zone Model Predictive Control Algorithm. Diabetes Technol Ther. 2022 Jul;24(7):471-480. doi: 10.1089/dia.2021.0521. Epub 2022 Apr 26. PMID: 35230138; PMCID: PMC9464083. |
No comparison and intervention only lasted 2 days. |
|
Quirós C, Herrera Arranz MT, Amigó J, Wägner AM, Beato-Vibora PI, Azriel-Mira S, Climent E, Soldevila B, Barquiel B, Colomo N, Durán-Martínez M, Corcoy R, Codina M, Díaz-Soto G, Márquez Pardo R, Martínez-Brocca MA, Rebollo Román Á, López-Gallardo G, Cuesta M, García Fernández J, Goya M, Vega Guedes B, Mendoza Mathison LC, Perea V. Real-World Evidence of Off-Label Use of Commercially Automated Insulin Delivery Systems Compared to Multiple Daily Insulin Injections in Pregnancies Complicated by Type 1 Diabetes. Diabetes Technol Ther. 2024 Aug;26(8):596-606. doi: 10.1089/dia.2023.0594. Epub 2024 May 24. PMID: 38417014. |
Wrong study design (observational) |
|
Stewart ZA, Yamamoto JM, Wilinska ME, Hartnell S, Farrington C, Hovorka R, Murphy HR. Adaptability of Closed Loop During Labor, Delivery, and Postpartum: A Secondary Analysis of Data from Two Randomized Crossover Trials in Type 1 Diabetes Pregnancy. Diabetes Technol Ther. 2018 Jul;20(7):501-505. doi: 10.1089/dia.2018.0060. PMID: 29958022; PMCID: PMC6025695. |
Wrong study design (observational) |
|
Farrington C, Stewart ZA, Barnard K, Hovorka R, Murphy HR. Experiences of closed-loop insulin delivery among pregnant women with Type 1 diabetes. Diabet Med. 2017 Oct;34(10):1461-1469. doi: 10.1111/dme.13406. Epub 2017 Jul 21. PMID: 28631849. |
Wrong O: psychosocial response |
|
Lei M, Chen D, Ling P, Wang C, Yang D, Deng H, Yang X, Xu W, Yan J. Effect of artificial pancreas system use on glycaemic control among pregnant women with type 1 diabetes mellitus: A meta-analysis of randomized controlled trials. Diabetes Obes Metab. 2024 Feb;26(2):673-681. doi: 10.1111/dom.15357. Epub 2023 Nov 12. PMID: 37953389. |
Systematic review; studies already included separately in this literature review |
|
Teixeira T, Godoi A, Romeiro P, Novaes JVLC, de Freitas Faria FM, Pereira S, Lamounier RN. Efficacy of automated insulin delivery in pregnant women with type 1 diabetes: a meta-analysis and trial sequential analysis of randomized controlled trials. Acta Diabetol. 2024 Jul;61(7):831-840. doi: 10.1007/s00592-024-02284-3. Epub 2024 May 3. PMID: 38700546. |
Systematic review; studies already included separately in this literature review |
|
Sieradzki, J., Cyganek, K., Cypryk, K., Wender-Ożegowska, E., Skoczylas, K., Runzis, S., & Shin, J. (2018). Objectives and methods of the ORCHESTRA FOUNDATION Registry study: a multicenter observational study of the use of insulin pump therapy in pregnant women with type 1 diabetes mellitus in Poland. Clinical Diabetology, 7(3), 136-144. |
Wrong study design (observational) |
|
Stamati A, Christoforidis A. Automated insulin delivery in pregnant women with type 1 diabetes mellitus: a systematic review and meta-analysis. Acta Diabetol. 2025 Jan 10. doi: 10.1007/s00592-025-02446-x. Epub ahead of print. PMID: 39792171. |
Systematic review; studies already included separately in this literature review |
|
Gómez AM, Marín Carrillo LF, Arévalo Correa CM, Muñoz Velandia OM, Rondón Sepúlveda MA, Silva Herrera JL, Henao Carrillo DC. Maternal-Fetal Outcomes in 34 Pregnant Women with Type 1 Diabetes in Sensor-Augmented Insulin Pump Therapy. Diabetes Technol Ther. 2017 Jul;19(7):417-422. doi: 10.1089/dia.2017.0030. PMID: 28731823. |
Wrong study design (observational) and wrong intervention (no HCL) |
|
Cindy, G., Guerci, B., Morel, O., Solange, P., Bourgeois, C., & Langbour-Remy, C. (2024). Grossesse chez la patiente atteinte d’un diabète de type 1: résultats métaboliques et obstétricaux avant l’utilisation de la boucle fermée hybride. Médecine des Maladies Métaboliques, 18(2), 120-129. |
Wrong language (Spanish) and wrong intervention (no HCL) |
|
Perea V, Quirós C, Herrera-Arranz MT, Azriel-Mira S, Wägner AM, Beato-Vibora P, Soldevila B, Barquiel B, Pardo RM, Díaz-Soto G, Picón MJ, Colomo N, Amigó J, Climent E, Durán-Martínez M, Corcoy R, Codina M, Cuesta M, Guedes BV, Vinagre I. Pregnancy outcomes with the pregestational use of Minimed 780G compared to Minimed 640G: findings from a multicenter cohort study. Acta Diabetol. 2024 Dec 4. doi: 10.1007/s00592-024-02430-x. Epub ahead of print. PMID: 39630235. |
Wrong study design (observational) |
|
Levy CJ, Kudva YC, Ozaslan B, Castorino K, O'Malley G, Kaur RJ, Levister CM, Church MM, Desjardins D, McCrady-Spitzer S, Ogyaadu S, Trinidad MC, Reid C, Rizvi S, Deshpande S, Zaniletti I, Kremers WK, Pinsker JE, Doyle FJ, Dassau E; LOIS-P Diabetes and Pregnancy Consortium. At-Home Use of a Pregnancy-Specific Zone-MPC Closed-Loop System for Pregnancies Complicated by Type 1 Diabetes: A Single-Arm, Observational Multicenter Study. Diabetes Care. 2023 Jul 1;46(7):1425-1431. doi: 10.2337/dc23-0173. PMID: 37196353; PMCID: PMC10300516. |
Wrong study design (observational) |
|
Guibert C, Amoura L, Rakotoarisoa L, Plat F, Sonnet E, Lablanche S, Tréglia C, Sarde E, Leca V, Rimareix F, Melki V, Baucher F, Betari B, Meyer L, Kessler L. MiniMedTM 780G Advanced Hybrid Closed-Loop System Study in Pregnant Women with Type 1 Diabetes. Diabetes Technol Ther. 2023 Dec;25(12):893-901. doi: 10.1089/dia.2023.0267. Epub 2023 Nov 14. PMID: 37956265. |
Wrong study design (observational) |
|
Kaur RJ, Smith BH, Ozaslan B, Pinsker JE, Trinidad MC, O'Malley G, Desjardins D, Castorino KN, Levister C, Reid C, McCrady-Spitzer S, Ogyaadu SJ, Church MM, Piper M, Kremers WK, Rosenn B, Doyle FJ 3rd, Dassau E, Levy CJ, Kudva YC. Hypoglycemia in Prospective Multicenter Study of Pregnancies with Pre-Existing Type 1 Diabetes on Sensor-Augmented Pump Therapy: The LOIS-P Study. Diabetes Technol Ther. 2022 Aug;24(8):544-555. doi: 10.1089/dia.2021.0479. PMID: 35349353; PMCID: PMC9353990. |
Wrong study design (observational) |
|
Benhalima K, Yamamoto JM. Use of continuous glucose monitoring and hybrid closed-loop therapy in pregnancy. Diabetes Obes Metab. 2024 Dec;26 Suppl 7:74-91. doi: 10.1111/dom.15999. Epub 2024 Oct 16. PMID: 39411880. |
Wrong study design (narrative review) |
|
Benhalima K, van Nes F, Laenen A, Gillard P, Mathieu C. Risk for ketonaemia in type 1 diabetes pregnancies with sensor-augmented pump therapy with predictive low glucose suspend compared with low glucose suspend: a crossover RCT. Diabetologia. 2021 Dec;64(12):2725-2730. doi: 10.1007/s00125-021-05589-y. Epub 2021 Oct 13. PMID: 34647140. |
Wrong intervention (no HCL) |
|
Donovan LE, Bell RC, Feig DS, Lemieux P, Murphy HR, Sigal RJ, Ho J, Virtanen H, Crawford S, Yamamoto JM. Glycaemic patterns during breastfeeding with postpartum use of closed-loop insulin delivery in women with type 1 diabetes. Diabetologia. 2024 Oct;67(10):2154-2159. doi: 10.1007/s00125-024-06227-z. Epub 2024 Jul 19. PMID: 39028360; PMCID: PMC11447145. |
Wrong P (postpartum) |
|
Dickens LT, Gonzalez MG. Approach to the Patient using Diabetes Technology in Pregnancy. J Clin Endocrinol Metab. 2025 Jan 7:dgae914. doi: 10.1210/clinem/dgae914. Epub ahead of print. PMID: 39775858. |
Wrong study design (narrative review) |
|
Benhalima K, Jendle J, Beunen K, Ringholm L. Automated Insulin Delivery for Pregnant Women With Type 1 Diabetes: Where Do We Stand? J Diabetes Sci Technol. 2024 Nov;18(6):1334-1345. doi: 10.1177/19322968231223934. Epub 2024 Jan 10. PMID: 38197363; PMCID: PMC11535386. |
Wrong study design (narrative review) |
|
Farrington C, Stewart Z, Hovorka R, Murphy H. Women's Experiences of Day-and-Night Closed-Loop Insulin Delivery During Type 1 Diabetes Pregnancy. J Diabetes Sci Technol. 2018 Nov;12(6):1125-1131. doi: 10.1177/1932296818800065. Epub 2018 Oct 5. PMID: 30288999; PMCID: PMC6232744. |
Wrong intervention (no HCL) and wrong outcomes |
|
Chillakanti M, Young E, Hopcroft A, Bellini N, Smith J, Isaacs D. Use of Automated Insulin Delivery in Pregnancies Complicated by Type 1 Diabetes. touchREV Endocrinol. 2024 Oct;20(2):110-118. doi: 10.17925/EE.2024.20.2.14. Epub 2024 Oct 9. PMID: 39526053; PMCID: PMC11548357. |
Wrong study design (narrative review) |
|
Eberle C, Loehnert M, Stichling S. Clinical Effectiveness of Different Technologies for Diabetes in Pregnancy: Systematic Literature Review. J Med Internet Res. 2021 Apr 28;23(4):e24982. doi: 10.2196/24982. PMID: 33908894; PMCID: PMC8116994. |
Systematic review. Wrong intervention (too broad, and the two studies that do match PICO are already included). |
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 02-05-2026
Beoordeeld op geldigheid : 02-05-2026
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2023 een multidisciplinaire cluster ingesteld. Het cluster Diabetes Mellitus bestaat uit meerdere richtlijnen, zie hier voor de actuele clusterindeling. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden geven hun expertise in, indien nodig. De volgende personen uit het cluster zijn betrokken geweest bij de herziening van deze module:
Clusterstuurgroep
- Dr. E.H. (Erik) Serné, internist in het AUMC te Amsterdam, NIV, voorzitter cluster
- Dr. L.P.F. (Luc) Janssens, kinderarts in het Isala te Zwolle, NVK
- Dr. W.J. (Wouter) de Waal, kinderarts in het Sint Antonius Ziekenhuis te Nieuwegein, NVK
- Dr. R.C. (Rebecca) Painter, gyneaocoloog in het AUMC te Amsterdam, NVOG
- Dr. B.E. (Bastiaan) de Galan, internist in het MUMC te Maastricht, NIV
- T.M. (Ties) Obers, patiëntvertegenwoordiger, Diabetesvereniging Nederland
Betrokken clusterexpertisegroepleden
- Dr. R.C. (Rebecca) Painter, gyneaocoloog in het AUMC te Amsterdam, NVOG
- Dr. M.A.R. (Mechteld) Vermeulen, internist-endocrinoloog in het CWZ te Nijmegen, NIV
- S.J.D.M. (Siska) Verburgh-Post, verloskundige 1e lijn en Verloskundigen Etten-Leur, KNOV
- Dr. K. (Koen) Verdonk, vasculair internist en obstetrisch internist in het Erasmus MC te Rotterdam, NIV
- Dr. L (Liselotte) van Bloemendaal, internist ouderengeneeskunde in het OLVG te Amsterdam, NIV
Met ondersteuning van
- Dr. A.N. (Anh Nhi) Nguyen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten.
- Dr. L.K. (Leanne) Küpers, adviseur, Kennisinstituut van de Federatie Medisch Specialisten.
- Drs. J.M.H. (Harm-Jan) van der Hart, adviseur, Kennisinstituut van de Federatie Medisch Specialisten.
- Drs. F.A. (Fieke) Pepping, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten.
Belangenverklaringen
Een overzicht van de belangen van de clusterleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Clusterstuurgroepleden
Tabel 1 Gemelde (neven)functies en belangen stuurgroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Restrictie |
|
Dr. E.H. (Erik) Serné |
Internist-Vasculaire Geneeskunde binnen Amsterdam UMC, locatie VUmc |
Clustervertegenwoordiger (NIV, NVK, NHG) binnen bestuur Nederlandse Diabetes Federatie (betaald) Lid van Rondetafel Diabeteszorg (onbetaald) Hoofdredacteur Nederlands Tijdschrift voor Diabetologie (betaald) Redactielid platform Diabetesgeneeskunde.nl (betaald) Medisch directeur van Diabeter Centrum Amsterdam, een joint venture tussen Amsterdam UMC en Diabeter; aangesteld via een detacheringscontract vanuit Amsterdam UMC (betaald). Medtronic is deels eigenaar van Diabeter. |
Geen |
Doelmatigheidsproject ZonMw betreffende behandeling patiënten met 'hypoglycemia unawareness' met 'stepped care' bestaande uit cursus HypoBewust en vervolgens evetueel continueglucose monitoring (CGM) versus directe start CGM
Veelbelovende zorg ZonMw-project betreffende Bi-hormonale kunstalvleesklier bij volwassen patiënten met diabetes type 1 die hun behandeldoelen niet halen; Automated blood glucose control in type 1 diabetes: effectiveness of the artificial pancreas (DARE-study)
Doelmatigheidsproject ZonMw betreffende LOFIT: Lifestyle front Office For Integrating lifestyle medicine in the Treatment of patients: a novel care-model towards community-based options for lifestyle change |
Advisering binnen Ronde Tafel Diabeteszorg betreffende doelmatige inzet nieuwe behandelingen toont belangrijke parallellen met richtlijnvorming. Beide maken gebruik van 'evidence-based medicine' en GRADE om de beschikbare data te duiden. Hierbij is dus geen sprake van belangenverstrengeling, maar van synergie. |
Restrictie t.a.v. besluitvorming bij modules HCl bij zwangerschap met DM1 en Preventie hypoglykemie met sensor bij diabetes mellitus type 2. |
|
Dr. L.P.F. (Luc) Janssens |
Kinderarts Isala |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Dr. W.J. (Wouter) de Waal |
Kinderarts Diakonessenhuis Utrecht |
Kinderarts Diabetes Centraal |
Geen |
Geen |
Geen |
Geen |
|
Dr. R.C. (Rebecca) Painter |
Gynaecoloog-perinatoloog Amsterdam UMC, hoogleraar verloskunde Vrije Universiteit Per 1 sept: Gynaecoloog-perinatoloog Erasmus MC, Hoogleraar Erasmus Universiteit |
Wetenschappelijk Adviseur Stichting ZEHG (onbetaald) Voorzitter werkgroep NVOG Richtlijn "schildklier en zwangerschap" (vacatiegelden) Lid werkgroep NVOG Richtlijn "Hyperemesis gravidarum" (vacatiegelden) Lid Koepel Wetenschap NVOG, namense Pijler FMG (onbetaald) Vice voorzitter NVOG Pijler FMG Wetenschapscommissie (onbetaald) Voorzitter NVOG SIG Diabetes en Zwangerschap (onbetaald) Lid Stadscoaltie Amsterdam Kansrijke Start (onbetaald) Projectleider en lid kernteam Netwerk Geboortezorg Noordwest Nederland (onbetaald) Bestuurslid NRCG, Nederlandse Regionale Consortia Geboortezorg (onbetaald) Lid Bestuurd Verloskundig Samenwerkingsverband Amsterdam UMC (onbetaald) Projectleider en hoofdonderzoeker SugarDip, TANGO-DM, PI NL RCTs (onbetaald) |
Geen |
ZonMW: SugarDip, projectleider PI NL, projectleider Netwerk Geboortezorg Noordwest Nederland, projectleider VSV stimulering implementatie basiskader, projectleider Minder dieren, meer kennis: Metformine in diermodellen systematic review, project leider NRCG, nationale regionale geboorteconsortia, geen projectleider
Diabetes Fonds: Register Diabetes en Zwangerschap, geen projectleider
Leading the Change: Tango DM, projectleider
Toegevoegd tijdens vergadering: CRISTAL studie (HCL bij zwangeren met DM1). Deze studie is niet gefinancierd door een farmaceut maar Medtronic heeft wel middelen geleverd. |
Projectleider TANGO DM, onderzoekt de afkapwaarden die gebruikt worden voor de diagnose diabetes gravidarum.
Medeprojectleider van SugarDip, over de medicamenteuze behandeling van diabetes gravidarum (insuline vs orale therapie). |
Geen |
|
Dr. B.E. (Bastiaan) de Galan |
Internist, MUMC+, Maastricht (0,6 fte) Hoogleraar interne geneeskunde/diabetologie, UM, Maastricht (0,2 fte) Internist, Radboudumc, Nijmegen (0,2 fte) |
Docent/cursusleider DESG cursus voor aios interne geneeskunde en kindergeneeskunde (betaald; naar MUMC+) Associate editor Diabetologia (betaald; naar MUMC) Bestuurslid Nederlandse Vereniging voor Endocrinologie (NVE; onbetaald) Voozitter accreditatiecommissie NIV (vacatiegelden) Voorzitter Commissie van Uitvoering voor het Accreditatieoverleg (onbetaald) Organisatie nascholingsreeks Diabetes Overleg (betaald, naar MUMC) Organisatie nascholingsreeks Dutch Diabetes Academy (betaald, naar MUMC) Secretaris International Hypoglycaemia Study Group (onbetaald) |
Geen |
Horizon Europe Framework Programme: Hypo-RESOLVE (Hypoglycaemia - redefining solutions for better lives) 2018-2023 (afgerond). Novo Nordisk, Lilly, Medtronic en Abbott betrokken als research partners, projectleider: ja
MELISSA (mobile artificial intelligence solution for diabetes adaptive care) 2022-2026. Novo Nordisk levert insuline, projectleider: ja
REDDIE (Real-world evidence for decisions in diabetes) 2023-2027. Novo Nordisk betrokken als research partner, projectleider: nee
Novo Nordisk: ADREM study (investigator initiated trial naar aanpassing van degludec bij sport bij mensen met type 1 diabetes, unrestricted grant) 2021-2022 (afgerond). |
Geen |
Geen |
|
T.M. (Ties) Obers |
Beleidsadviseur Belangenbehartiging (0,6 FTE) Diabetesvereniging Nederland
Directeur (0,2 FTE) Stichting Knowledge for Children Nederland
Freelance Adviseur Non-Profit (0,2 FTE) Groei voor Goed |
Geen |
Geen |
Geen |
Bescherming van de reputatie/positie van Diabetesvereniging Nederland. Boegbeeldfunctie bij patiëntenorganisatie Diabetesvereniging Nederland. |
Geen |
Betrokken clusterexpertisegroepleden
Tabel 2 Gemelde (neven)functies en belangen betrokken clusterexpertisegroepleden
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Restrictie |
|
Dr. R.C. (Rebecca) Painter |
Zie tabel 1 |
|||||
|
Dr. M.A.R. (Mechteld) Vermeulen |
Internist-endocrinoloog, Canisius Wilhelmina Ziekenhuis |
Medisch Decaan Wetenschap en Innovatie, Canisius Wilhelmina Ziekenhuis |
Geen |
Onderstaande studies zijn uitgevoerd als lokale PI. |
Geen |
Geen |
|
S.J.D.M. (Siska) Verburgh-Post |
Verloskundige 1e lijn - maatschapslid - Verloskundigen Etten-Leur (betaald) |
Echoscopiste pretecho&zo - betaald tot 31dec2024 |
Geen |
Geen |
Geen |
Geen |
|
Dr. K. (Koen) Verdonk |
Vasculair internist, obstetrisch internist, Erasmus MC |
Geen |
Geen |
Geen |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door inbreng van de Diabetesvereniging Nederland.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerden de clusterleden conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
HCL bij zwangerschap met diabetes mellitus type 1 |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze.
Zoekverantwoording
Literature search strategy
Embase.com
|
No. |
Query |
Results |
|
#1 |
'insulin dependent diabetes mellitus'/exp OR (((diabet* OR dm) NEAR/3 ('type 1' OR 'type i' OR 'type one' OR 'insulin depend*' OR 'insulin treat*' OR 'intensive insulin*' OR brittle)):ti,ab,kw) OR dm1:ti,ab,kw OR 'dm 1':ti,ab,kw OR iddm:ti,ab,kw OR t1d*:ti,ab,kw OR 'juvenile diabet*':ti,ab,kw OR 'juvenile dm':ti,ab,kw OR 'juvenile onset diabet*':ti,ab,kw OR 'juvenile onset dm':ti,ab,kw OR 'early onset diabetes':ti,ab,kw |
224481 |
|
#2 |
'pregnancy'/exp OR 'pregnant woman'/exp OR 'pregnancy complication'/exp OR 'family planning'/exp OR 'perinatal period'/exp OR 'perinatal care'/exp OR 'puerperium'/exp OR 'childbirth'/exp OR pregnan*:ti,ab,kw OR gravidit*:ti,ab,kw OR gestation*:ti,ab,kw OR perinatal*:ti,ab,kw OR peripartum:ti,ab,kw OR intrapartum:ti,ab,kw OR 'family planning':ti,ab,kw OR 'child bearing':ti,ab,kw OR childbearing:ti,ab,kw OR 'child birth*':ti,ab,kw OR childbirth*:ti,ab,kw OR labor:ti,ab,kw OR labour:ti,ab,kw OR prepregnan*:ti,ab,kw OR pregestation*:ti,ab,kw OR preconcept*:ti,ab,kw OR 'pre concept*':ti,ab,kw OR 'before conception*':ti,ab,kw OR puerperal*:ti,ab,kw OR puerperium:ti,ab,kw OR postpartum:ti,ab,kw OR 'post partum':ti,ab,kw OR maternal:ti,ab,kw |
1970456 |
|
#3 |
'hybrid closed loop system'/exp OR 'glucose monitoring/insulin pump system'/exp OR 'artificial pancreas'/exp OR 'clos* loop':ti,ab,kw OR hcl:ti,ab,kw OR ahcl:ti,ab,kw OR ((automat* NEAR/3 insulin*):ti,ab,kw) OR ((artificial NEAR/3 pancreas):ti,ab,kw) OR camaps:ti,ab,kw OR minimed:ti,ab,kw OR 780g:ti,ab,kw OR 670g:ti,ab,kw OR ypsopump*:ti,ab,kw OR 'patch pump*':ti,ab,kw |
77256 |
|
#4 |
#1 AND #2 AND #3 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) NOT (('adolescent'/exp OR 'child'/exp OR adolescent*:ti,ab,kw OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw)) |
187 |
|
#5 |
#4 AND [2014-2025]/py |
153 |
|
#6 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR 'systematic review'/exp OR 'systematic review (topic)'/exp OR 'scoping review'/exp OR 'rapid review'/exp OR 'umbrella review'/exp OR 'cochrane database of systematic reviews'/jt OR 'network meta-analysis'/exp OR 'networkmeta analy*':ti,ab,kw OR 'networkmetaanaly*':ti,ab,kw OR metaanaly*:ti,ab,kw OR 'meta analy*':ti,ab,kw OR metanaly*:ti,ab,kw OR prisma:ti,ab,kw OR prospero:ti,ab,kw OR metaanali*:ti,ab,kw OR 'meta anali*':ti,ab,kw OR metanali*:ti,ab,kw OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab,kw) OR (((structured OR systemic*) NEAR/3 (review* OR overview* OR synth*) NEAR/3 literature):ti,ab,kw) OR ((systemic* NEAR/1 review*):ti,ab,kw) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab,kw) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab,kw) OR (((literature NEAR/3 (review* OR overview*)):ti,ab,kw) AND (search*:ti,ab,kw OR database*:ti,ab,kw OR 'data base*':ti,ab,kw)) OR (('data extraction*':ti,ab,kw OR 'data source*':ti,ab,kw) AND ('study selection*':ti,ab,kw OR 'studies selection*':ti,ab,kw)) OR ('search strateg*':ti,ab,kw AND 'selection criteria*':ti,ab,kw) OR ('data source*':ti,ab,kw AND 'data synth*':ti,ab,kw) OR medline*:ti,ab,kw OR pubmed*:ti,ab,kw OR 'pub med*':ti,ab,kw OR embase:ti,ab,kw OR cochrane*:ti,ab,kw OR (((critical* OR rapid*) NEAR/2 (review* OR overview* OR synth*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synth*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynth*:ti,ab,kw OR 'meta synth*':ti,ab,kw OR 'review* of review*':ti,ab,kw |
1112629 |
|
#7 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
4185387 |
|
#8 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
8594640 |
|
#9 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
15711877 |
|
#10 |
#5 AND #6 |
24 |
|
#11 |
#5 AND #7 NOT #10 |
37 |
|
#12 |
#5 AND (#8 OR #9) NOT (#10 OR #11) |
27 |
|
#13 |
#10 OR #11 OR #12 |
88 |
Ovid/Medline
|
# |
Searches |
Results |
|
1 |
exp Diabetes Mellitus, Type 1/ or ((diabet* or dm) adj3 ('type 1' or 'type i' or 'type one' or 'insulin depend*' or 'insulin treat*' or 'intensive insulin*' or brittle)).ti,ab,kf. or dm1.ti,ab,kf. or 'dm 1'.ti,ab,kf. or iddm.ti,ab,kf. or t1d*.ti,ab,kf. or 'juvenile diabet*'.ti,ab,kf. or 'juvenile dm'.ti,ab,kf. or 'juvenile onset diabet*'.ti,ab,kf. or 'juvenile onset dm'.ti,ab,kf. or 'early onset diabetes'.ti,ab,kf. |
135568 |
|
2 |
exp Pregnancy/ or exp Pregnant Women/ or exp Pregnancy Complications/ or exp Pregnancy Trimesters/ or exp Perinatal Care/ or exp Preconception Care/ or exp Prenatal Care/ or exp Postpartum Period/ or pregnan*.ti,ab,kf. or gravidit*.ti,ab,kf. or gestation*.ti,ab,kf. or perinatal*.ti,ab,kf. or peripartum.ti,ab,kf. or intrapartum.ti,ab,kf. or 'family planning'.ti,ab,kf. or 'child bearing'.ti,ab,kf. or childbearing.ti,ab,kf. or 'child birth*'.ti,ab,kf. or childbirth*.ti,ab,kf. or labor.ti,ab,kf. or labour.ti,ab,kf. or prepregnan*.ti,ab,kf. or pregestation*.ti,ab,kf. or preconcept*.ti,ab,kf. or 'pre concept*'.ti,ab,kf. or 'before conception*'.ti,ab,kf. or puerperal*.ti,ab,kf. or puerperium.ti,ab,kf. or postpartum.ti,ab,kf. or 'post partum'.ti,ab,kf. or maternal.ti,ab,kf. |
1556910 |
|
3 |
exp Insulin Infusion Systems/ or exp Pancreas, Artificial/ or 'clos* loop'.ti,ab,kf. or hcl.ti,ab,kf. or ahcl.ti,ab,kf. or (automat* adj3 insulin*).ti,ab,kf. or (artificial adj3 pancreas).ti,ab,kf. or camaps.ti,ab,kf. or minimed.ti,ab,kf. or 780g.ti,ab,kf. or 670g.ti,ab,kf. or ypsopump*.ti,ab,kf. or 'patch pump*'.ti,ab,kf. |
63728 |
|
4 |
(1 and 2 and 3) not (comment/ or editorial/ or letter/) not ((exp animals/ or exp models, animal/) not humans/) |
340 |
|
5 |
limit 4 to yr="2014 -Current" |
181 |
|
6 |
exp Meta-Analysis/ or exp "Meta-Analysis as Topic"/ or exp Network Meta-Analysis/ or exp Systematic Review/ or exp "Systematic Reviews as Topic"/ or (networkmeta analy* or networkmetaanaly* or metaanaly* or meta analy* or metanaly* or prisma or prospero or metaanali* or meta anali* or metanali*).ti,ab,kf. or ((systemati* or scoping or umbrella or structured literature) adj3 (review* or overview*)).ti,ab,kf. or ((structured or systemic*) adj3 (review* or overview* or synth*) adj3 literature).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 (review* or overview*)) and (search* or database* or data base*)).ti,ab,kf. or ((data extraction* or data source*) and (study selection* or studies selection*)).ti,ab,kf. or (search strateg* and selection criteria*).ti,ab,kf. or (data source* and data synth*).ti,ab,kf. or (medline* or pubmed* or pub med* or embase or cochrane*).ti,ab,kf. or cochrane.jw. or ((critical* or rapid*) adj2 (review* or overview* or synth*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synth*)) and (search* or database* or data base*)).ab. or metasynth*.ti,ab,kf. or meta synth*.ti,ab,kf. |
805779 |
|
7 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2831115 |
|
8 |
Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) |
5882782 |
|
9 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] |
4934047 |
|
10 |
5 and 6 |
19 |
|
11 |
(5 and 7) not 10 |
47 |
|
12 |
(5 and (8 or 9)) not (10 or 11) |
48 |
|
13 |
10 or 11 or 12 |
114 |