Antidepressiva bij dementie
Uitgangsvraag
Wat is de rol van antidepressiva in de behandeling van depressiesymptomen bij patiënten met dementie?
De uitgangsvraag omvat de volgende twee deelvragen:
- Wat is de effectiviteit van antidepressiva in de behandeling van depressiesymptomen bij patiënten met dementie?
- Wat is het meest effectieve antidepressivum als behandeling van depressiesymptomen bij patiënten met dementie?
Aanbeveling
Bespreek en overweeg het starten van antidepressiva voor depressieve symptomen bij dementie alleen wanneer deze klachten ernstig zijn en wanneer niet-farmacologische interventies afdoende zijn geprobeerd en onvoldoende werkzaam zijn.
Gebruiken van antidepressiva
- Start een antidepressivum bij dementie uitsluitend na vastleggen van doelsymptomen en behandelduur. Gebruik hiervoor een gevalideerde vragenlijst (zoals de Cornell Scale for Depression in Dementia CSDD of de Hamilton Depression Rating Scale HDRS).
- Gebruik als eerste keuze een SSRI. De aanbevolen SSRI’s bij ouderen zijn (es-)citalopram en sertraline op grond van het gunstiger bijwerkingenprofiel, ervaring, minder kans op interacties, beperkte risico’s bij overdosering en het gebruikersgemak.
- Evalueer na maximaal zes weken de symptomen met behulp van dezelfde vragenlijst als voorafgaand aan het starten is gebruikt (zoals CSDD of HDRS).
- Indien het middel na zes weken niet of onvoldoende werkt, en wel goed verdragen wordt: overweeg de dosering verder op te hogen tot de maximale dosering zoals beschreven in het Farmacotherapeutisch Kompas, of om te wisselen naar een ander antidepressivum. Volg hierbij de richtlijnmodule ‘Farmacotherapie van eerste keuze bij ouderen (≥60 jaar)’ (NVvP-richtlijn ‘Depressie’).
Stoppen van antidepressiva
- Om onttrekkingsverschijnselen te voorkomen wordt geadviseerd het antidepressivum in stappen af te bouwen. Bij nog steeds bestaande indicatie: wissel naar een ander antidepressivum conform de NVvP Richtlijn ‘Depressie’.
- Stop of verlaag de dosering van antidepressiva bij onacceptabele bijwerkingen in overleg met patiënt/ mantelzorger.
Overwegingen
Vergelijking 1 ‘Antidepressiva versus placebo’
Kwaliteit van bewijs
Het doel van deze uitgangsvraag was om de toegevoegde waarde van antidepressiva als behandeling tegen depressieve symptomen bij dementie te evalueren. Bij de eerste deelvraag (PICO 1) werd specifiek gekeken naar de effectiviteit van antidepressiva ten opzichte van placebo. Als cruciale uitkomstmaat werd vermindering in depressieve symptomen en bijwerkingen gedefinieerd.
De overall kwaliteit van bewijs is zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten. Er is afgewaardeerd vanwege ernstige:
- Risk of Bias: methodologische beperkingen (ontbrekende informatie over de randomisatie procedure, gebrek aan/ontbrekende informatie over blindering, selective outcome reporting, ontbrekende uitkomstdata door loss to follow-up).
- Indirectheid: indirectheid van het bewijs, door verschillen in interventies (in één studie kreeg de interventiegroep rivastigmine naast het antidepressivum wat kan leiden tot vertekende resultaten).
- Imprecisie: onnauwkeurigheid (brede betrouwbaarheidsintervallen, en omdat het betrouwbaarheidsinterval de grens van klinische relevantie overschrijdt).
Balans tussen gewenste en ongewenste effecten
Er zijn in totaal twee systematische reviews geïncludeerd (Dudas, 2018; Zhang, 2023), waarbij uiteindelijk twaalf RCT’s in de analyse ten aanzien van reductie in depressieve symptomen en bijwerkingen zijn meegenomen in de literatuuranalyse (totaal: 807 patiënten).
Gezien de zeer lage overall bewijskracht, kunnen er op basis van literatuur geen sterke aanbevelingen geformuleerd worden over de waarde van antidepressiva bij oudere patiënten met dementie en depressieve symptomen.
Depressieve symptomen
In de meeste studies betrof het patiënten met een milde tot matige dementie (grotendeels van het Alzheimer type) in een poliklinische setting, met een wisselende ernst van depressieve symptomen, waarbij de gemiddelde leeftijd 75-78 jaar was. Vanuit de intention-to-treat analyse (lage bewijskracht voor effect van antidepressiva op depressieve symptomen, acht studies, 596 patiënten), wordt een niet-klinisch relevant en niet-statistisch significant verschil gevonden ten faveure van medicamenteuze behandeling.
Vanuit de completers-analyse (zeer lage bewijskracht voor effect van antidepressiva op depressieve symptomen, vier studies, 154 patiënten) wordt een klinisch relevant maar niet-statistisch significant verschil gevonden ten faveure van medicamenteuze behandeling.
Het cluster plaatst enkele kanttekeningen bij de interpretatie van deze resultaten. In de geïncludeerde studies was de ernst en type van dementie wisselend en werd niet altijd de ernst van de depressie eenduidig vastgesteld.
De vragenlijsten die gebruikt werden waren de Cornell Scale of Depression in Dementia (CSDD), de Hamilton Depression Rating Scale (HDRS) en de Montgomery-Asberg Depression Rating Scale (MADRS). De onderzochte studiepopulaties waren relatief jong voor een geriatrische setting, en het onderscheid tussen fragiele en fitte patiënten is veelal onduidelijk. Daarnaast waren er geen secundaire uitkomstmaten gerapporteerd (e.g. cognitief functioneren, ADL-zelfstandigheid, kwaliteit van leven).
Onderzochte medicatie
Een aantal van de onderzochte middelen worden weinig gebruikt in de Nederlandse praktijk, zoals moclobemide, clomipramine of imipramine. Veelgebruikte middelen zoals citalopram, duloxetine en nortriptyline werden niet onderzocht. Verder varieerden de doseringen sterk en loopt de range in sommige studies tot boven of onder de in Nederland gangbare klinische doseringen. Daarnaast stelt het cluster dat een langere follow-up gewenst is (nu slechts 6-13 weken) om langetermijneffecten vast te kunnen stellen.
Bijwerkingen
Vanuit de beoordeling van bijwerkingen (lage bewijskracht voor uitkomstmaat ‘bijwerkingen’, vier studies, 1147 patiënten) wordt een klinisch relevant en statistisch significant verschil gevonden ten faveure van placebo, waarbij dit effect voornamelijk wordt veroorzaakt door de studie die placebo vergeleek met moclobemide, en in mindere mate door de studie naar sertraline. Mirtazapine, clomipramine en escitalopram geven in de individuele studies niet significant meer bijwerkingen dan placebo. Voor fluoxetine zijn de bijwerkingen niet gerapporteerd.
Er moet worden opgemerkt dat relatief hoge doseringen worden genoemd in de geanalyseerde studies (escitalopram tot 20mg/dag, mirtazapine tot 45mg/dag). Bijwerkingen van antidepressiva zijn vrijwel altijd dosisgebonden. In deze module zijn geen studies gevonden die naar andere veelgebruikte middelen kijken, zoals citalopram (wel bijvoorbeeld aangeraden in de NHG-standaard 2019 en de NVvP-richtlijn Depressie 2024), nortriptyline, venlafaxine en duloxetine.
Vergelijking 2 ‘Antidepressiva onderling vergeleken’
Kwaliteit van bewijs
Het doel van deze uitgangsvraag was om de toegevoegde waarde van antidepressiva als behandeling tegen depressieve symptomen bij dementie te evalueren. Bij de tweede deelvraag werd specifiek gekeken naar de meest effectieve antidepressiva als behandeling van depressie symptomen (i.e. een onderlinge vergelijking). Als cruciale uitkomstmaat werd vermindering in depressieve symptomen en bijwerkingen gedefinieerd. De overall kwaliteit van bewijs is zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten. Er is afgewaardeerd vanwege ernstige:
- Risk of Bias: methodologische beperkingen (ontbrekende informatie over de randomisatie procedure, selective outcome reporting, attrition bias).
- Imprecisie: onnauwkeurigheid (brede betrouwbaarheidsintervallen, het feit dat er geen effectmaten konden worden berekend en omdat het betrouwbaarheidsinterval de grenzen van klinische relevantie overschrijdt).
Balans tussen gewenste en ongewenste effecten
In totaal zijn twee systematische reviews geïncludeerd in deze literatuuranalyse (Dudas, 2018; Zhang, 2023), waarbij vier RCT’s ten aanzien van reductie in depressieve symptomen en bijwerkingen werden meegenomen (Banerjee, 2011; Katona, 1998; Mokhber, 2014; Taragano, 1997: totaal 620 patiënten). Deze resultaten konden niet gepoold worden omdat verschillende meetinstrumenten zijn gebruikt en/of er geen effect sizes zijn gerapporteerd.
In de studies hadden de meeste patiënten een milde tot matig ernstige dementie (meestal van het Alzheimer type), met MMSE-scores uiteenlopend van 10 tot 24, of een DSM-diagnose. Depressieve klachten werden gemeten met de HDRS, MADRS of CSDD, waarbij de ernst varieerde van dysthymie, een minimale CSDD-score van 8/38, tot een depressie die voldoet aan de criteria in de DSM. Samenvattend laten de vier RCTs het volgende zien:
- Banerjee (2011) vergeleek mirtazapine met sertraline en vond geen significant of klinisch relevant verschil in afname op de CSDD.
- Katona (1998) rapporteerde een MADRS-scorevermindering van ±12 punten voor zowel paroxetine als imipramine, maar zonder standaarddeviatie (i.e. klinische relevantie kon niet beoordeeld worden).
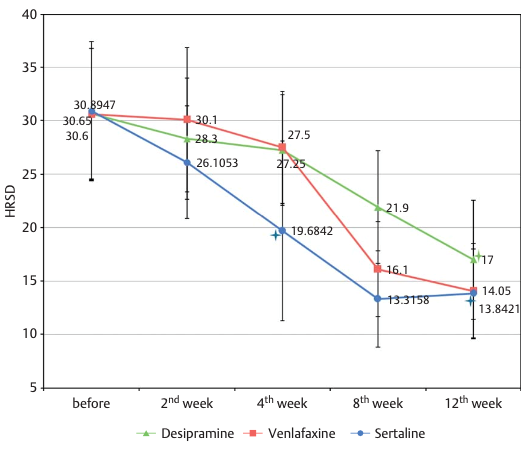
- Mokhber (2014) vond een grotere daling op de HDRS in de desipramine-groep (17 punten) in vergelijking met de venlafaxine-groep en sertraline-groep (14 punten).
- Taragano (1997) vond geen significant of klinisch relevant verschil tussen fluoxetine en amitriptyline op de HDRS.
In de vier bovengenoemde studies wordt geen verschil in effectiviteit gevonden tussen de verschillende middelen wanneer deze onderling worden vergeleken. Hierbij moet worden opgemerkt dat paroxetine, imipramine en amitriptyline nauwelijks tot niet worden gebruikt in de Nederlandse klinische praktijk voor de behandeling van depressieve symptomen bij dementie.
In verschillende richtlijnen voor ouderen met depressie komt ook citalopram naar voren als middel van eerste keuze (hier niet onderzocht). Daarnaast zijn duloxetine en nortriptyline in andere richtlijnen beschreven als effectief en voldoende veilig bevonden (maar in de populatie met dementie niet onderzocht).
Klinische overwegingen
Wel of niet starten met antidepressiva
Samenvattend is er geen klinisch relevant verschil tussen placebo en antidepressiva voor de behandeling van depressieve symptomen bij patiënten met dementie.
Er is geen antidepressivum dat overtuigend aangetoond het meest effectief is bij depressieve symptomen bij dementie, of het meest gunstige bijwerkingenprofiel heeft.
In lijn met andere richtlijnen formuleert het cluster derhalve het advies om de start van antidepressiva alleen te overwegen voor depressieve symptomen bij dementie wanneer deze klachten ernstig zijn en wanneer niet-farmacologische interventies afdoende zijn geprobeerd en onvoldoende werkzaam zijn.
Voorbeelden van niet-farmacologische interventies zijn elders in deze richtlijn uitgewerkt; lichaamsbeweging is te adviseren (bijvoorbeeld in de vorm van 30 minuten wandelen meerdere malen per week) voor personen met dementie ter verbetering van cognitie, conditie en stemming (module 4.3.5). Daarnaast is conform de Verenso richtlijn een breed gedeelde visie op zorg voor mensen met dementie dat deze persoonsgericht dient te zijn. Voor verdere (niet medicamenteuze) adviezen zie de richtlijn ‘probleemgedrag bij mensen met dementie’ Verenso (2018).
Keuze voor een middel
Op basis van de gevonden studies voor ouderen met dementie komt geen voorkeursmiddel duidelijk naar voren. In enkele studies (Lyketsos et al. 2003; Munro et al. 2004) komt sertraline naar voren als effectiever dan placebo, maar in de studie van Banerjee et al. (2011) is sertraline niet effectiever dan placebo, en geeft wel significant meer bijwerkingen.
Het cluster adviseert om bij het starten de richtlijn ‘Depressie’ te volgen van de Nederlandse Vereniging voor Psychiatrie (2024). Bij ouderen vanaf 60 jaar adviseert deze richtlijn om (es)citalopram, sertraline, duloxetine of mirtazapine als eerste-stapbehandeling te gebruiken, met aandacht voor valpreventie en (sedatieve) bijwerkingen. Bij uitblijvende respons na 4-6 weken wordt overstappen naar een ander middel uit deze groep of een andere SSRI aanbevolen. Dit is voornamelijk gebaseerd op een systematic review met netwerk meta-analyse (Krause, 2019) waarbij citalopram en sertraline niet als effectief naar voren komen (<50% symptoomreductie). Deze bevinding is echter gebaseerd op slechts 4 RCT's (Krause, 2019).
De Verenso-richtlijn ‘Behandeling van depressief gedrag’ adviseert om de NVvP-richtlijn Depressie te volgen. Hierbij is een SSRI het middel van eerste keuze, en bij uitblijven van effect na zes weken een therapeutische dosering, kan worden gewisseld naar een ander niet-tricyclisch antidepressivum of nortriptyline. De richtlijn adviseert antidepressiva alleen te overwegen bij ernstige (therapieresistente) depressies met bijvoorbeeld weigering van medicatie en vocht/voeding en een duidelijke grote lijdensdruk bij de patiënt (Verenso 2018). Verder wordt opgemerkt in de Verenso-richtlijn dat algehele ontrading van antidepressiva te drastisch is ondanks dat er uit onderzoek geen overtuigend resultaat komt (Verenso, 2018): antidepressiva geven namelijk pas bij ernstige depressies een klinisch relevant effect (Kirsch, 2008), en patiënten met dementie en ernstige depressies worden waarschijnlijk niet geïncludeerd in RCT’s.
In de NHG-standaard ‘Depressie’ zijn de SSRI’s citalopram en sertraline middelen van eerste keuze voor depressie bij ouderen vanwege het relatief gunstige bijwerkingenprofiel (NHG-standaard Depressie, 2019). Mirtazapine heeft als nadeel dat het sterker sedatief is dan de andere middelen door de antihistaminerge werking (Farmacotherapeutisch Kompas).
De internationale NICE richtlijn ‘Dementia’ concludeert op basis van 10 RCT’s geen significant voordeel van antidepressiva boven placebo bij dementie-gerelateerde depressieve symptomen voor milde tot matige depressie bij milde tot matige dementie (NICE guideline [NG97], 2018).
Tevens is er klinische consensus om een middel te kiezen met zo min mogelijk anticholinerge bijwerkingen vanwege het verwachte negatieve effect op de cognitie, maar dit is niet onderzocht. Nortriptyline is ook niet onderzocht bij deze doelgroep maar heeft bij ouderen met een depressie een plaats bij ernstige depressies (na bovengenoemde middelen), waarbij anticholinerge bijwerkingen goed moeten worden gemonitord.
Depressieve symptomen bij dementie versus een klinische depressie
In de klinische praktijk probeert men onderscheid te maken tussen patiënten met depressieve symptomen bij dementie en patiënten die naast hun dementie een primaire, klinische depressie hebben. Het is nog onduidelijk of dit verschil nog bestaat bij een (gevorderde) dementie of dat de behandeling uiteindelijk hetzelfde moet zijn. De richtlijn ‘Depressie’ van de NVvP (2024) adviseert onder andere verschillende augmentatiestappen en neuromodulatie, wat bij ouderen zonder dementie goed is onderzocht, maar bij ouderen met dementie niet tot nauwelijks. Ook adviseert Verenso om ECT alleen te overwegen bij levensbedreigende situaties, waar de NVvP ECT ook adviseert bij therapieresistentie. Daarnaast verschilt het advies over de behandelduur: waar Verenso adviseert bij probleemgedrag bij mensen met dementie om na drie maanden een afbouwpoging te doen met als doel te stoppen, schrijft de NVvP dat in de praktijk vaak een duur van zes maanden wordt gehanteerd bij een eerste depressieve episode, en langer (één tot meerdere jaren) bij recidiverende episoden.
Aanwijzingen die in de praktijk gebruikt worden om de depressieve klachten te beschouwen als een primaire stoornis (en niet als neuropsychiatrisch symptoom bij dementie) zijn onder andere een voorgeschiedenis met recidiverende depressies, en een positieve familie-anamnese (vooral voor bipolaire stoornis gezien de hoge erfelijkheid).
Daarnaast is het van belang om onderliggende en bijdragende problematiek zoals bijvoorbeeld psychotrauma, persoonlijkheidsproblematiek en somatische stoornissen mee te nemen. Zie voor verdere adviezen de NvvP richtlijn module 2 diagnostiek, hoofdstuk 16 ‘specifiek voor ouderen’ en de Verenso richtlijn probleemgedrag bij dementie.
Hoewel er geen klinisch significant effect in het voordeel van antidepressiva gevonden werd in de huidige search, zijn er toch overwegingen die het starten van antidepressiva voor individuele patienten kunnen rechtvaardigen. Conform ook de NICE richtlijn volgt het cluster de lijn dat in het geval van een ernstige depressie er een (urgente) reden voor het starten van medicamenteuze behandeling kan zijn. Ook kan een voorgeschiedenis met een goede reactie op antidepressiva doorslaggevend zijn om een herstart daarvan te proberen.
Starten van medicamenteuze behandeling
Voorafgaand aan het starten van antidepressiva dienen de depressieve symptomen te worden gescoord middels een gevalideerde vragenlijst, zoals de CSDD of de HDRS (Atchison, 2024). Voor start- en streefdoseringen kunnen evidence based rapporten worden geraadpleegd, beschikbaar op www.ephor.nl. Besteed hierbij aandacht aan valpreventie en monitor het optreden van (sedatieve) bijwerkingen. Verricht op indicatie een ECG of natrium controle.
Monitoren van medicamenteuze behandeling
Uiterlijk zes weken na starten dient de behandeling te worden geëvalueerd. De evaluatie vindt plaats middels anamnese, heteroanamnese (naasten en/ of verzorging/ verpleging/ leden van het multidisciplinaire team indien patiënt in een instelling verblijft) en wederom dient de vragenlijst te worden afgenomen die ook voorafgaand aan het starten afgenomen worden (zoals de CSDD of HDRS). Zowel het effect als de bijwerkingen moeten worden geëvalueerd en worden meegewogen in de beslissing om wel of niet te continueren. Indien de behandeling wordt voortgezet is het wenselijk om elke zes weken te evalueren.
Verlagen en stoppen van medicamenteuze behandeling
Bij geen of onvoldoende werkzaamheid na zes weken: overweeg de dosering verder op te hogen tot de maximale dosering zoals beschreven in het Farmacotherapeutisch Kompas, of om te wisselen naar een ander antidepressivum. Volg hierbij de richtlijnmodule ‘Farmacotherapie van eerste keuze bij ouderen (≥60 jaar)’ (NVvP-richtlijn ‘Depressie’).
Indien effect uitblijft en/ of het middel wordt niet goed verdragen, adviseert het cluster om de dosering te verlagen (bij bijwerkingen) of weer te stoppen. Bij (ernstige) bijwerkingen is het advies om de dosering eerst te verlagen, maar als dit onvoldoende helpt of het effect verdwijnt hiermee, kan het middel ook gestopt worden. Momenteel is nog onvoldoende onderzoek gedaan naar het afbouwen van antidepressiva in het algemeen, en bij dementie in het bijzonder, om een wetenschappelijk onderbouwd stappenplan te kunnen adviseren (Sørensen, 2022). In de praktijk worden antidepressiva in meerdere weken tot een maand stapsgewijs verlaagd en uiteindelijk volledig gestaakt. Zie ook het kennisdocument van Ephor ‘afbouw en minderen van antidepressiva’. Bij het stoppen van de volledige dosering in één keer worden voor alle middelen ontwenningsverschijnselen beschreven, voor SSRI’s sterker dan voor TCA’s (Gastaldon, 2022).
Overig
Het onderwerp ‘medicamenteuze behandeling van neuropsychiatrische symptomen’ wordt uitgewerkt in verschillende modules, gefocust en onderverdeeld op de behandeling per farmacotherapeutische groep (zie Medicatie neuropsychiatrische symptomen). Een bepaald doelsymptoom kan dus in meerdere modules zijn uitgewerkt, waarbij per module een aanbeveling wordt gedaan voor een keuze binnen deze farmacotherapeutische groep. Er kan hiermee geen uitspraak worden gedaan over een vergelijking van de effecten tussen de verschillende farmacotherapeutische groepen.
Algemeen: Antidepressiva (vergelijking 1 en 2)
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
Het onderzoek naar het effect van behandeling op depressieve klachten beperkt zich tot reductie van depressieve symptomen, en het optreden van bijwerkingen. Andere uitkomstmaten zoals kwaliteit van leven voor de patiënt en/ of de mantelzorger, zorgvraag, of (somatische) comorbiditeit zijn niet onderzocht. Indien medicamenteuze behandeling geïndiceerd is zal het gesprek met patiënten en de naasten hierover moeten worden aangegaan om samen de afweging te maken of de patiënt medicatie zou willen en wat het doel van de behandeling wordt.
Een depressie geeft per definitie (hoge) lijdensdruk, niet alleen voor patiënten maar vaak ook voor de omgeving. Naasten herkennen de persoon niet in de somberheid, de mantelzorg wordt zwaarder, de gedeelde kwaliteit van leven verslechtert, en het geheugen van de patiënt verslechtert verder onder invloed van de depressie.
Voor naasten voelt behandeling vaak prangender dan voor patiënten. Dit is omdat depressie zich kenmerkt door onverschilligheid en hopeloosheid, waardoor patiënten denken dat behandeling toch geen zin heeft. De patiënt moet altijd gehoord worden en er moet worden meegewogen dat het behandeleffect van depressieve symptomen bij dementie onzeker is. Maar als er een hoge lijdensdruk is, én als een wens tot niet behandelen lijkt te worden ingegeven door de gekleurde beleving vanuit de depressie zelf, is het te verdedigen om toch behandeling met psychofarmaca voor te stellen.
Kostenaspecten
Bij het cluster is weinig bekend of behandeling met antidepressiva meer kosten oplevert dan controle behandeling. In 2013 toonde een Britse kosten-effectiviteitsstudie aan dat mirtazapine en sertraline beiden niet kosteneffectief waren voor depressie bij dementie. Mirtazapine verminderde echter de mantelzorgtijd en -kosten aanzienlijk, waardoor dit middel de hoogste waarschijnlijkheid van kosteneffectiviteit had (Banerjee, 2013; Romeo, 2013).
De kosten van de onderlinge middelen zijn nagenoeg vergelijkbaar in Nederland (www.medicijnkosten.nl; geraadpleegd 9 februari 2025): Sertraline €0,04/ stk (50mg);
Mirtazepine €0,05/ stk (15mg); Citalopram €0,03/ stk (20mg); Escitalopram €0,10/ stk (10mg); en Nortriptyline €0,06/ stk (10mg). Citalopram is op de maximale dosering dus het goedkoopste, maar het cluster verwacht geen grote kostenverschillen op nationaal vlak.
Gelijkheid ((health) equity/equitable)
De interventie leidt tot een (mogelijke) toename van gezondheidsgelijkheid. Antidepressiva worden vergoed door iedere basisverzekering, evenals medisch-specialistische zorg. Depressie wordt bij Nederlanders met een niet-westerse migratieachtergrond vaak minder goed herkend door een andere presentatie, beperkte herkenning door westerse artsen, of lagere zorgzoekende bereidheid. Ook is onduidelijk of vragenlijsten als de Hamilton en de CSDD ook depressieve klachten kunnen diagnosticeren bij patiënten met een niet-westerse migratieachtergrond met dementie.
Aanvaardbaarheid
Gezien de aanbevelingen overeenkomen met de huidige zorg en bestaande richtlijnen (NVvP, 2024; Verenso, 2018; NHG, 2019; NICE, 2018) zullen deze aanbevelingen al breed geïmplementeerd zijn. Het cluster voorziet dan ook geen grote barrières op het gebied van aanvaardbaarheid, haalbaarheid en implementatie.
Ethische aanvaardbaarheid
De interventie lijkt wel aanvaardbaar voor de betrokkenen. Het cluster voorziet dan ook geen ethische bezwaren.
Duurzaamheid
Duurzaamheidsoverwegingen spelen bij de formulering en richting van de aanbevelingen geen doorslaggevende rol.
Haalbaarheid
De haalbaarheid van de beschreven interventie hangt met name af van de kennis van de zorgverlener en binnen het interdisciplinaire team. Indien deze de depressieve symptomen herkent en middels shared decision making met de patiënt en de naasten zou starten met een antidepressivum, is dit een gemakkelijk te implementeren interventie. De meeste ouderen gebruiken dagelijks één of meer medicijn(en) en het antidepressivum kan dan worden toegevoegd aan bijvoorbeeld de weekdoos of de Baxter. De geadviseerde middelen zijn niet duur, in elke Nederlandse apotheek te verkrijgen, en er zijn de laatste jaren geen tekorten beschreven.
‘Antidepressiva versus placebo’ EN ‘Antidepressiva onderling vergeleken’
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Er is geen klinisch relevant verschil tussen placebo en antidepressiva voor de behandeling van depressieve symptomen bij patiënten met dementie. Het cluster formuleert – in lijn met al bestaande richtlijnen – een zwakke aanbeveling vóór het gebruik van antidepressiva.
Er is geen antidepressivum dat overtuigend aangetoond het meest effectief is bij depressieve symptomen bij dementie, of het meest gunstige bijwerkingenprofiel heeft. Op basis van bestaande richtlijnen wordt een voorkeur voor de SSRI’s uitgesproken.
Eindoordeel: Zwakke aanbeveling voor.
Onderbouwing
The use of antidepressants in dementia accompanied by depressive symptoms is widespread, but their clinical efficacy is uncertain. Therefore, this module aims to assess to which extent antidepressants treatment is effective, and to determine the most effective antidepressants treatment for managing depressive symptoms in patients with dementia.
PICO 1 Summary of Findings table: Antidepressants compared to placebo in patients with dementia and depressive symptoms
Population: Patients with dementia and depressive symptoms
Intervention: Antidepressants
Comparator: Placebo
|
Outcome |
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence (Quality of evidence) |
Summary |
|
|
Antidepressants |
Placebo |
||||
|
Reduction in depression (critical) ITT analysis
|
Measured by CSDD, HRSD and MADRS. Based on data from 596 participants in 7 studies. |
Difference: SMD 0.13 lower (CI 95% 0.31 fewer – 0.05 higher) |
Low Due to serious risk of bias, due to serious imprecision1 |
Antidepressants may reduce depression when compared with placebo in patients with dementia and depressive symptoms.
(Dudas, 2018; Zhang, 2023) |
|
|
Reduction in depression (critical) Completers |
Measured by CSDD and HRSD. Based on data from 154 participants in 4 studies. |
Difference: SMD 0.81 lower (CI 95% 1.82 fewer – 0.20 higher) |
Very low Due to serious risk of bias, due to serious indirectness, due to serious imprecision2 |
The evidence is very uncertain about the effect of antidepressants on depression when compared with placebo in patients with dementia and depressive symptoms.
(Dudas, 2018; Zhang, 2023) |
|
|
Adverse events (critical) |
Based on data from 1147 participants in 4 studies. |
479 per 1000* |
380 per 1000* |
Low Due to serious risk of bias, due to serious imprecision3 |
Antidepressants may increase adverse events when compared with placebo in patients with dementia and depressive symptoms.
(Dudas, 2018; Zhang, 2023) |
|
Difference: 99 more per 1000 (CI 95% 38 more - 167 more) |
|||||
|
Quality of life (important) |
- |
- |
No GRADE (no evidence was found) |
No evidence was found regarding the effect of antidepressants on quality of life when compared with placebo in patients with dementia and depressive symptoms. |
|
|
Patient satisfaction (important)
|
- |
- |
No GRADE (no evidence was found) |
No evidence was found regarding the effect of antidepressants on patient satisfaction when compared with placebo in patients with dementia and depressive symptoms. |
|
|
Carer satisfaction (important) |
- |
- |
No GRADE (no evidence was found) |
No evidence was found regarding the effect of antidepressants on carer satisfaction when compared with placebo in patients with dementia and depressive symptoms. |
|
1 Risk of Bias: serious. Due to missing information about the randomization procedure, selective outcome reporting, missing information about/lack of blinding. Imprecision: serious. Due to wide confidence intervals of the individual studies.
2 Risk of Bias: serious. Due to missing information about the randomization procedure, missing outcome data, selective outcome reporting. Indirectness: serious. Due to intervention group of one study that received rivastigmine in addition to fluoxetine (Mowla, 2007). Imprecision: serious. Due to overlap of confidence interval with border of clinical relevance.
3 Risk of Bias: serious. Due to missing information about the randomization procedure, selective outcome reporting, incomplete outcome data. Imprecision: serious. Due to overlap of confidence interval with border of clinical relevance. *Baseline/comparator Control arm of reference used for intervention.
PICO 2 Summary of Findings table: Head-to-head comparison of antidepressants in patients with dementia and depressive symptoms
Population: Patients with dementia and depressive symptoms
Intervention: Antidepressants
Comparator: Antidepressants
|
Outcome |
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence (Quality of evidence) |
Summary |
|
|
Antidepressants |
Antidepressants |
||||
|
Reduction in depression (critical) |
Measured by CSDD, HRSD, and MADRS. Based on data from 451 participants in 4 studies. |
Results could not be pooled due to the variety in reporting of the outcome measure, and because of missing effect sizes (SD/SE). |
Very low Due to serious risk of bias, due to very serious imprecision1 |
The evidence is very uncertain about the effect of antidepressants on depression when compared with other antidepressants in patients with dementia and depressive symptoms.
(Banerjee, 2011; Katona, 1998; Mokhber, 2014; Taragano, 1997) |
|
|
Adverse events (critical) |
Based on data from 257 participants in 2 studies. |
Results could not be pooled because results were obtained from two studies only. |
Very low Due to serious risk of bias, due to very serious imprecision2 |
The evidence is very uncertain about the effect of antidepressants on adverse events when compared with other antidepressants in patients with dementia and depressive symptoms.
(Katona, 1998; Mokhber, 2014) |
|
|
Quality of life (important) |
- |
- |
No GRADE (no evidence was found) |
No evidence was found regarding the effect of antidepressants on quality of life when compared with other antidepressants in patients with dementia and depressive symptoms. |
|
|
Patient satisfaction (important)
|
- |
- |
No GRADE (no evidence was found) |
No evidence was found regarding the effect of antidepressants on patient satisfaction when compared with other antidepressants in patients with dementia and depressive symptoms. |
|
|
Carer satisfaction (important) |
- |
- |
No GRADE (no evidence was found) |
No evidence was found regarding the effect of antidepressants on carer satisfaction when compared with other antidepressants in patients with dementia and depressive symptoms. |
|
|
1 Risk of Bias: serious. Due to unclear risk of sequence generation, selective outcome reporting, allocation concealment and attrition bias, and high risk of attrition bias. Imprecision: very serious. Due to wide confidence intervals of the individual studies and the inability to calculate effect measures. 2 Risk of Bias: serious. Due to unclear risk of sequence generation, selective outcome reporting, allocation concealment and attrition bias. Imprecision: very serious. Due to overlap of confidence interval with both borders of clinical relevance. |
|||||
PICO 1: Description of studies
Two systematic reviews were included in the analysis of the literature. Important study characteristics and results are summarized in Table 1. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Dudas (2018) aimed to determine the efficacy and safety of antidepressants for patients with dementia and depression. ALOIS, the Cochrane Dementia and Cognitive Improvement Group’s Specialized Register was searched on 16 August 2017. Studies in ALOIS are identified from international healthcare databases (Medline, Embase, CINAHL, PsycINFO, Lilacs), trial registers, the Cochrane Library’s Central Register of Controlled Trials (CENTRAL), and grey literature sources. All relevant double-blind RCTs comparing any antidepressant drug with placebo for patients diagnosed as having dementia and depression were included. The Cochrane risk of bias tool was used to assess risk of bias. The review included 10 RCTs with a total of 1592 participants.
Zhang (2023) aimed to assess the effects of selective serotonin reuptake inhibitors (SSRIs) on the alleviation of depressive symptoms in patients with Alzheimer’s disease (AD). Five international databases (Medline via PubMed, Scopus, Web of Science, Google Scholar, PsycINFO) were searched from inception until October 2022. Additionally, reference screening of each obtained article was used to look for further pertinent studies. Studies that assessed the effects of SSRIs on the attenuation of depressive symptoms in patients with a diagnosis of AD were included. Risk of bias was assessed using the Cochrane risk of bias assessment technique. The review included 13 RCTs with a total of 1033 subjects with AD, including 513 in the experimental group and 520 in the placebo group. Eventually, 4 out of 13 RCTs were included in the current analysis because five overlapped with Dudas (2018), three RCTs did not have a placebo control group, and one RCT did not report any outcome measure of interest.
PICO 2: Description of studies
One systematic review was included in the analysis of the literature. Important study characteristics are summarized in Table 2. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
He (2021) aimed to assess the efficacy of antidepressants in the treatment of depression in AD patients. Three international databases (Cochrane Central Register of Controlled Trials, PubMed, Embase) and one Chinese database (Chinese National Knowledge Infrastructure) were searched until May 2020. The Cochrane Risk of Bias tool was used for quality assessment. The study included 25 RCTs comparing 14 antidepressants or placebo. Twelve studies (An, 2017; Chen, 2014; de Vasconcelos, 2007; Fuchs, 1993; Lyketsos, 2003; Magai, 2000; Nyth, 1990; Passeri, 1985; Petracca, 1996; Petracca, 2001; Rosenberg, 2010; Teri, 1991) were placebo trails, eight studies were published in Chinese (Fei, 2010; Liu, 2011; Su, 2007; Wang, 2006; Wu, 2007; Zhao, 2015; Zhou, 2012; Zhu, 2006), and one study (Ren,2004) was not available full text. Thus, four studies were included in the literature analysis (Banerjee, 2011; Katona, 1998; Mokhber, 2014; Taragano, 1997).
Table 1. Characteristics of included studies in Dudas (2018) and Zhang (2023)
|
Abbreviations: AD = Alzheimer’s disease; CSDD = Cornell scale for depression in dementia; GDS = global depression scale; HRSD = Hamilton rating scale for depression; MADRS = Montgomery-Asberg depression rating scale; NR = not reported. a Median age is presented. b Mean daily dose is presented. c N is only reported for the total study population. d Participants in the intervention group received fluoxetine in addition to rivastigmine. |
|||||||
Table 2. Characteristics of includes studies in He (2021)
Results
1. Subquestion - placebo
1.1 Reduction in depression
Eight studies included in Dudas (2018), and three studies included in Zhang (2023) reported on the outcome measure reduction in depression, assessed by using the Cornell scale for depression in dementia (CSDD) (n=6) (range: 0-38), the Hamilton rating scale for depression (HRSD) (n=4) (range: 0-52), and the Montgomery-Asberg depression rating scale (MADRS) (n=1) (range: 0-60). For all instruments, a higher score indicates greater depression severity.
Two separate analyses were conducted because four studies reported only completers’ data (Reifler, 1989; Petracca, 1996; Mowla, 2007; Munro, 2004), whereas the other studies reported intention-to-treat data. Standardized mean difference (SMD) was used due to the usage of different instruments to assess depression.
Results of Fuchs (1993) and Roth (1996) could not be included in the analysis, because they did not include/report the numbers in each treatment group who had completed the study.
Intention-to-treat analysis
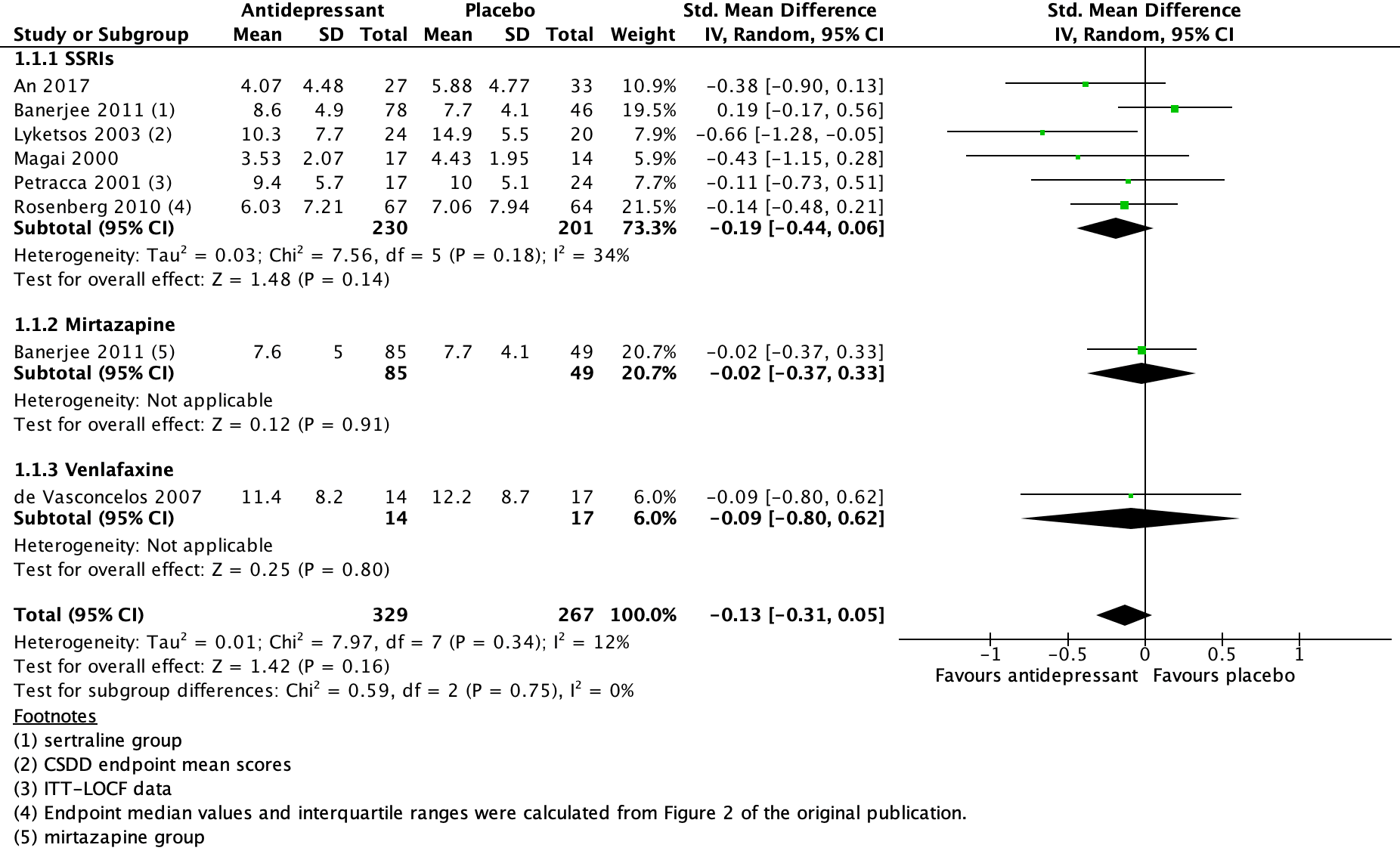
The pooled data show a SMD of -0.13 (95%CI -0.31 to 0.05) in favour of antidepressants (figure 1). This difference is considered not clinically relevant.
Figure 1. The effect of antidepressants on depression endpoint mean scores at 6-13 weeks - ITT
Z: p-value of the pooled effect; df: degrees of freedom; I2: statistic heterogeneity; CI: confidence interval
Completer data analysis
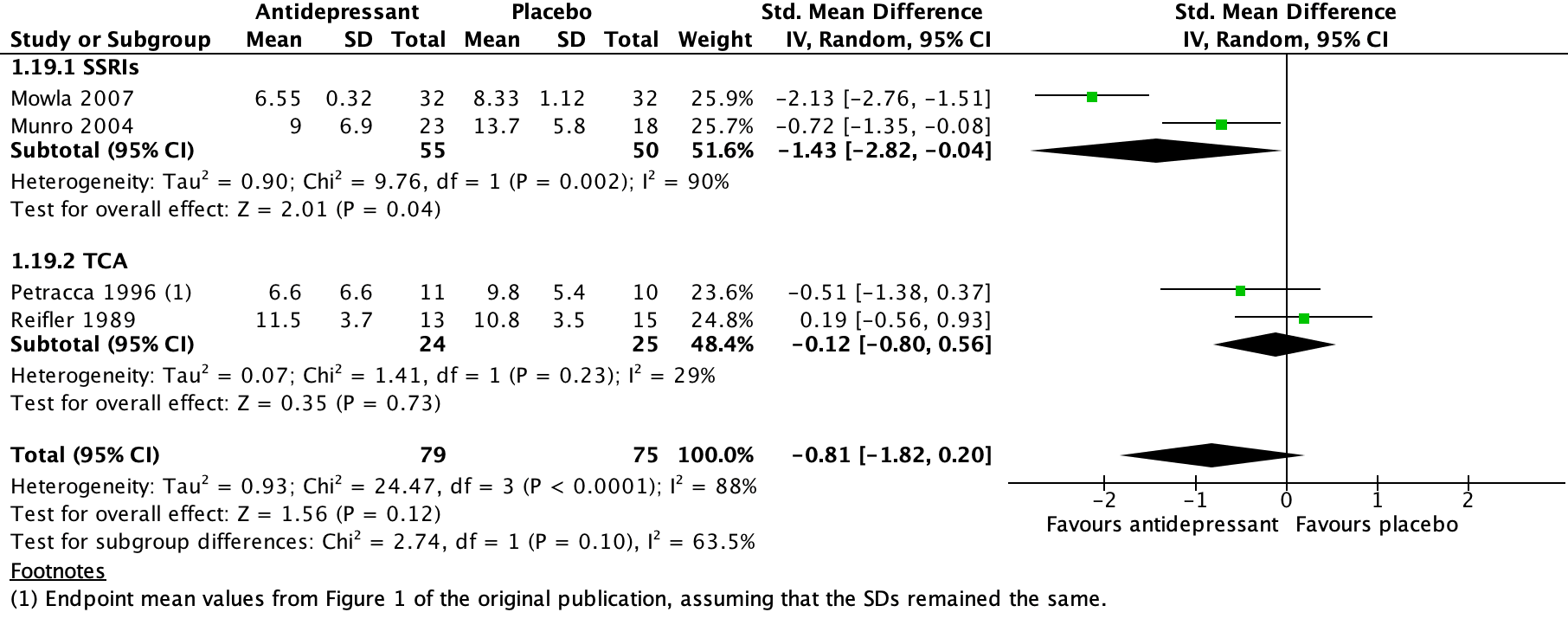
The pooled data show a SMD of -0.81 (95%CI -1.82 to 0.20) in favour of antidepressants (figure 2). This difference is considered a large clinically relevant effect.
Figure 2. The effect of antidepressants on depression endpoint mean scores at 6-13 weeks - completers’ data
Z: p-value of the pooled effect; df: degrees of freedom; I2: statistic heterogeneity; CI: confidence interval
1.2 Adverse events
Three studies included in Dudas (2018), and one study included in Zhang (2023) reported on the outcome measure adverse events, defined as the number of participants experiencing at least one adverse event.
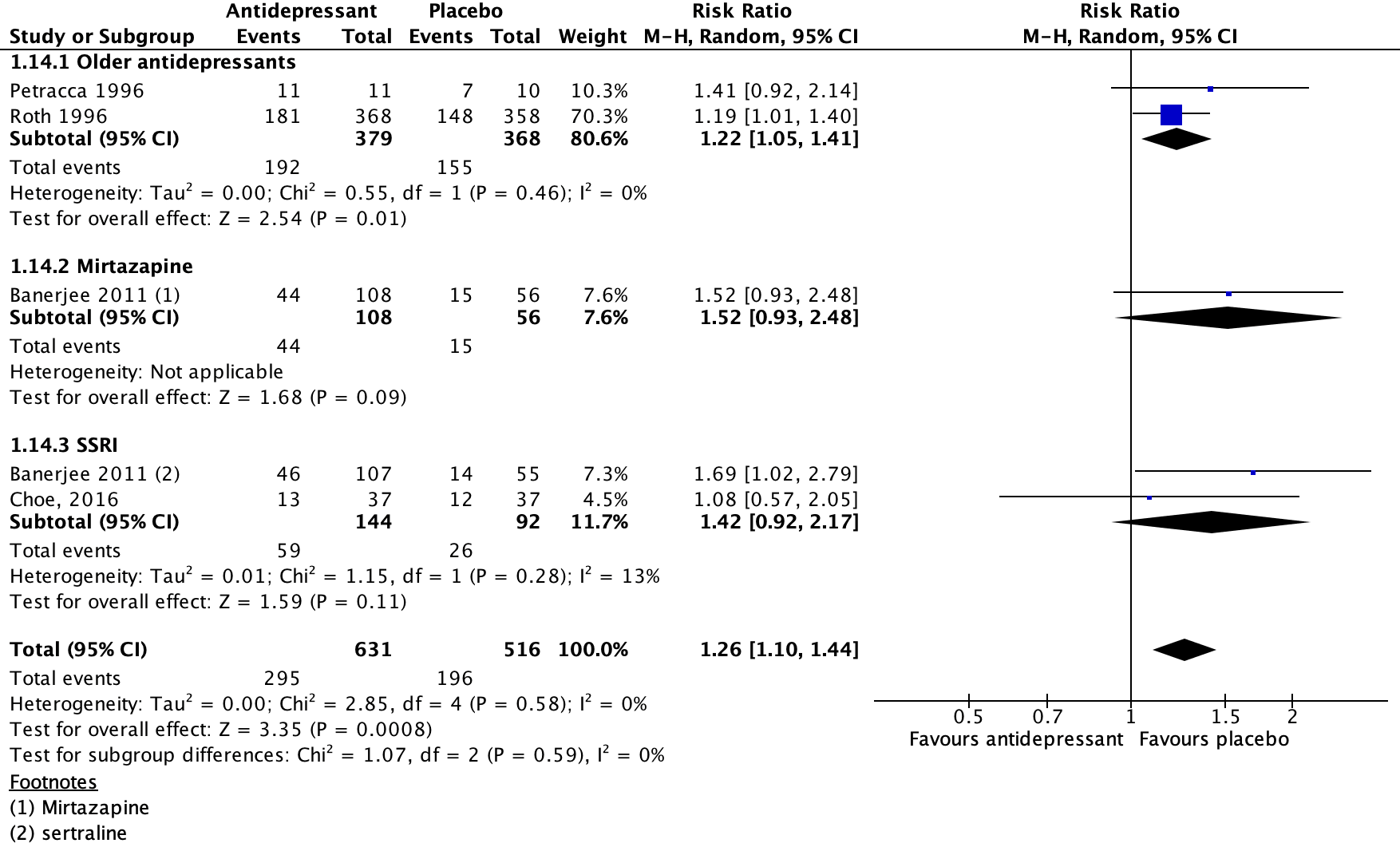
The pooled data show a risk ratio of 1.26 (95%CI 1.10 to 1.44) in favour of placebo (figure 3). This difference is considered clinically relevant.
Figure 3. The effect of antidepressants on adverse events
Z: p-value of the pooled effect; df: degrees of freedom; I2: statistic heterogeneity; CI: confidence interval
1.3 Quality of life, 1.4. Patient satisfaction, 1.5. Carer satisfaction
Dudas (2018) and Zhang (2023) did not report on the outcome measures quality of life, patient satisfaction, and carer satisfaction.
2. Subquestion - Head-to-head comparison
2.1 Reduction in depression
Four studies included in He (2021) reported on the outcome measure reduction in depression, assessed by using the CSDD (n=1) (range: 0-38), the HRSD (n=2) (range: 0-52), and the MADRS (n=1) (range: 0-60). For all instruments, a higher score indicates greater depression severity. Results could not be pooled, or effect sizes (mean difference/risk ratio) could not be calculated (Katona, 1998; Mokhber, 2014) due to the variety in reporting of the outcome measure, and because of missing effect sizes (SD/SE).
Banerjee (2011) reported a mean (SD) CSDD score after 13 weeks of follow-up in ITT population of 8.6 (4.9) for the sertraline group (n=78), and 7.9 (5.0) for the mirtazapine group (n=85). Mean difference is 0.70 (95%CI -0.82 to 2.22) in favour of mirtazapine. This difference is considered not clinically relevant.
Katona (1998) reported a mean change (SD) in MADRS score (baseline compared to endpoint in ITT population) of -12.6 (10.0) for the paroxetine group (n=96), and -11.8 (10.0) for the imipramine group (n=96).
Mokhber (2014) reported a mean HRSD score after 12 weeks of treatment of 17.0 in the desipramine group (n=19), 14.1 in the venlafaxine group (n=20), and 13.8 in the sertraline group (n=20).
Taragano (1997) reported a mean (SD) HRSD score after 6 weeks of treatment of 16.7 (2.9) for the fluoxetine group (n=18), and 15.6 (3.2) for the amitriptyline group (n=19). Mean difference is 1.10 (95%CI -0.87 to 3.07) in favour of amitriptyline. This difference is considered not clinically relevant.
2.2 Adverse events
Two studies included in He (2021) reported on the outcome measure adverse events.
Katona (1998) reported on the number of participants experiencing at least one treatment-emergent adverse event (TEAE). The authors reported at least one TEAE in 51/99 (51.5%) of participants in the paroxetine group, and in 50/99 (50.5%) of participants in the imipramine group. Risk ratio was 1.02 (95%CI 0.78 to 1.34) in favour of imipramine. This difference was considered not clinically relevant.
Mokhber (2014) reported on the number of participants experiencing headaches, restlessness, and nausea. The results are displayed in Table 3.
Table 3. Frequency of adverse events (Mokhber, 2014)
|
|
Group |
Frequency (n) |
Percentage (%) |
|
Headaches |
Sertraline |
5 |
16.6 |
|
Venlafaxine |
1 |
3.3 |
|
|
Desipramine |
0 |
0 |
|
|
Restlessness |
Sertraline |
3 |
10.0 |
|
Venlafaxine |
3 |
10.0 |
|
|
Desipramine |
0 |
0 |
|
|
Nausea |
Sertraline |
2 |
6.6 |
|
Venlafaxine |
6 |
20.0 |
|
|
Desipramine |
3 |
10.3 |
2.3 Quality of life, 2.4 Patient satisfaction, 2.5 Carer satisfaction
None of the studies reported on the outcome measures quality of life, patient satisfaction, and carer satisfaction.
A systematic review of the literature was performed to answer the following question(s):
- What is the effectiveness of antidepressants in comparison to placebo in patients with dementia and depressive symptoms?
- What is the effectiveness of various antidepressants in patients with dementia and depressive symptoms?
| Patients | Patients with dementia (e.g. Alzheimer, Vascular, Parkinson, LBD) and depressive symptoms |
| Intervention | Antidepressants (e.g. * TCAs: Amitriptyline, Clomipramine, Dosulepine, Doxepine, Imipramine, Maprotiline, Nortriptyline. * SSRIs: Citalopram, Escitalopram, Fluoxetine, Fluvoxamine, Paroxetine, Sertraline. * NSRIs: Duloxetine, Venlafaxine) |
| Control 1 | Placebo |
| Control 2 | Comparison between antidepressants |
| Outcomes | Reduction in depression, adverse events, quality of life, patient satisfaction, (informal) carer satisfaction |
| Other selection citeria | Study design: systematic reviews |
Relevant outcome measures
The guideline panel considered reduction in depression and adverse events as critical outcome measures for decision making; and quality of life, patient satisfaction, and (informal) carer satisfaction as important outcome measures for decision making.
A priori, the guideline panel did not define the outcome measures listed above but used the definitions used in the studies.
For all outcome measures the guideline panel defined a 25% difference for dichotomous outcomes (0.8 ≥ RR ≥ 1.25) and 0.5 SD for continuous outcomes as a minimal clinically (patient) important difference.
If studies used different rating instruments (e.g. reduction in depression could be measured with the validated scales CSDD, HRSD, MADRS) to measure the same outcome measure, then the standardized mean difference (SMD) is calculated. According to Cohen, SMD values of 0.2-0.5 represent a small clinically relevant effect, values of 0.5-0.8 a medium clinically relevant effect, and values >0.8 represent a large clinically relevant effect (Cohen, 1988).
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 2010 until 21 August 2024. The detailed search strategy is listed under the tab ‘Literature search strategy’. The systematic literature search resulted in 4194 hits. Studies were selected based on the following criteria:
- Systematic reviews in which searches were performed in at least two databases, with a detailed search strategy, risk of bias assessment and results of individual studies available.
- Full-text English or Dutch language publication and
- Studies according to the PICO.
Initially, 16 studies were selected based on title and abstract screening. After reading the full text, thirteen studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and three systematic reviews were selected for inclusion:
- Subquestion 1 Placebo comparison: Dudas (2018), Zhang (2023).
- Subquestion 2 Head-to-head comparison: He (2021).
- Atchison K, Nazir A, Wu P, Seitz D, Watt J, Goodarzi Z. Depression detection in dementia: A diagnostic accuracy systematic review and meta analysis update. Health Sci Rep. 2024 Nov 11;7(11):e70058. Doi: 10.1002/hsr2.70058. PMID: 39530065. PMCID: PMC11551879.
- Banerjee S, Hellier J, Romeo R, Dewey M, Knapp M, Ballard C, Baldwin R, Bentham P, Fox C, Holmes C, Katona C, Lawton C, Lindesay J, Livingston G, McCrae N, Moniz-Cook E, Murray J, Nurock S, Orrell M, O'Brien J, Poppe M, Thomas A, Walwyn R, Wilson K, Burns A. Study of the use of antidepressants for depression in dementia: the HTA-SADD trial--a multicentre, randomised, double-blind, placebo-controlled trial of the clinical effectiveness and cost-effectiveness of sertraline and mirtazapine. Health Technol Assess. 2013 Feb;17(7):1-166. doi: 10.3310/hta17070. PMID: 23438937; PMCID: PMC4782811.
- Dudas R, Malouf R, McCleery J, Dening T. Antidepressants for treating depression in dementia. Cochrane Database Syst Rev. 2018 Aug 31;8(8):CD003944. doi: 10.1002/14651858.CD003944.pub2. PMID: 30168578; PMCID: PMC6513376.
- Gastaldon C, Schoretsanitis G, Arzenton E, Raschi E, Papola D, Ostuzzi G, Moretti U, Seifritz E, Kane JM, Trifirò G, Barbui C. Withdrawal Syndrome Following Discontinuation of 28 Antidepressants: Pharmacovigilance Analysis of 31,688 Reports from the WHO Spontaneous Reporting Database. Drug Saf. 2022 Dec;45(12):1539-1549. doi: 10.1007/s40264-022-01246-4. Epub 2022 Nov 18. PMID: 36400895; PMCID: PMC9676852.
- He Y, Li H, Huang J, Huang S, Bai Y, Li Y, Huang W. Efficacy of antidepressant drugs in the treatment of depression in Alzheimer disease patients: A systematic review and network meta-analysis. J Psychopharmacol. 2021 Aug;35(8):901-909. doi: 10.1177/02698811211030181. Epub 2021 Jul 9. PMID: 34238048.
- NHG, 2019. Depressie. NHG-Standaard (M44). Gepubliceerd: april 2019, laatste aanpassing: januari 2024. Geraadpleegd via: https://richtlijnen.nhg.org/standaarden/depressie.
- NICE, 2018. Dementia: Assessment, management and support for people living with dementia and their carers. NICE Guideline 97. Published: 20 June 2018. Link: https://www.nice.org.uk/guidance/ng97.
- NVvP, 2024. Richtlijn Depressie. Geautoriseerd op 01-03-2024. Geraadpleegd via: https://richtlijnendatabase.nl/richtlijn/depressie/startpagina_-_richtlijn_depressie_2024.html.
- Romeo R, Knapp M, Hellier J, Dewey M, Ballard C, Baldwin R, Bentham P, Burns A, Fox C, Holmes C, Katona C, Lawton C, Lindesay J, Livingston G, McCrae N, Moniz-Cook E, Murray J, Nurock S, O'Brien J, Poppe M, Thomas A, Walwyn R, Wilson K, Banerjee S. Cost-effectiveness analyses for mirtazapine and sertraline in dementia: randomised controlled trial. Br J Psychiatry. 2013 Feb;202:121-8. doi: 10.1192/bjp.bp.112.115212. Epub 2012 Dec 20. PMID: 23258767.
- Sørensen A, Juhl Jørgensen K, Munkholm K. Clinical practice guideline recommendations on tapering and discontinuing antidepressants for depression: a systematic review. Ther Adv Psychopharmacol. 2022 Feb 11;12:20451253211067656. doi: 10.1177/20451253211067656. PMID: 35173954; PMCID: PMC8841913.
- Verenso, 2018. Richtlijn Probleemgedrag bij mensen met dementie. Utrecht, 2018. Geraadpleegd via: https://www.verenso.nl/kwaliteit/richtlijnen-en-praktijkvoering/richtlijnendatabase/probleemgedrag-bij-mensen-met-dementie.
- Zhang J, Zheng X, Zhao Z. A systematic review and meta-analysis on the efficacy outcomes of selective serotonin reuptake inhibitors in depression in Alzheimer's disease. BMC Neurol. 2023 May 31;23(1):210. doi: 10.1186/s12883-023-03191-w. PMID: 37259037; PMCID: PMC10230772.
Risk of Bias tables
PICO 1: Risk of Bias (Dudas, 2018; Zhang, 2023)
For further details about the risk of bias assessment, see
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated?
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented? Were patients, healthcare providers, data collectors, outcome assessors, data analysts blinded?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measure
LOW Some concerns HIGH
|
|
Choe, 2016 |
Definitely yes
Reason: Block randomization with block sizes of 4 or 6 was performed using a web-based randomization system. |
Definitely yes
Reason: All investigators and participants were blind to the intervention allocation. |
Definitely yes
Reason: Double-blinded trial: All investigators and participants were blind throughout the study. |
Probably yes
Reason: 8 (22%) participants withdrew from the intervention group, and 3 (8%) from the placebo group. ITT analyses were conducted and included all participants that had suitable data from baseline assessment and at least one post-baseline assessment. |
Probably yes
Reason: No protocol available or trial registration mentioned. But there is no reason to doubt that the study is free of selective outcome reporting. |
Probably yes
Reason: Not reported |
Low |
|
Magai, 2000 |
No information |
No information |
Probably yes
Reason: Double-blind trial: all personnel associated with the study were blind to treatment condition. Not mentioned if participants were actually blinded. |
Probably yes
Reason: 2 (12%) participants withdrew from the intervention group, and 2 (14%) from the placebo group. LOCF analysis was performed. |
Probably yes
Reason: No protocol available or trial registration mentioned. But there is no reason to doubt that the study is free of selective outcome reporting. |
Probably yes
Reason: Not reported. |
Some concerns |
|
Mowla, 2007 |
Definitely yes
Reason: Computer-generated randomization was used. Participants were randomized in a 1:1:1 ratio. |
No information |
Definitely yes
Reason: Double-blind trial: Researchers and participants were blinded (same number of similar pills). |
Probably no
Reason: 9 (21%) participants withdrew from the intervention group, and 8 (20%) from the placebo group. No imputation methods were used. |
Probably yes
Reason: No protocol available or trial registration mentioned. But there is no reason to doubt that the study is free of selective outcome reporting. |
Probably yes
Reason: Not reported. |
Some concerns |
|
Munro, 2004 |
No information
Reason: It is mentioned that participants were randomly assigned, but nothing about the procedure. |
No information |
Definitely yes
Reason: Double-blind trial: Patients, caregivers, and investigators were blinded to treatment condition. |
Probably no
Reason: In total, 7 participants of the original 44 withdrew from the study. No imputation methods were used. |
Definitely no
Reason: No protocol available or trial registration mentioned. Not all outcomes as specified in the methods are reported. |
Probably yes
Reason: Not reported. |
High |
PICO 2. Risk of Bias (He, 2021)
|
Study ID |
Sequence generation |
Allocation concealment |
|||
|
An et al., 2017 |
Unclear |
Unclear |
Low |
Low |
High |
|
Banerjee et al., 2011 |
Low |
Low |
Low |
Low |
Low |
|
Chen, 2014 |
High |
Unclear |
High |
Low |
Low |
|
de Vasconcelos et al., 2007 |
Unclear |
Low |
Low |
High |
|
|
Fei et al., 2010 |
Low |
Low |
Unclear |
Low |
Low |
|
Fuchs et al., 1993 |
Low |
Unclear |
Low |
Low |
Low |
|
Katona et al., 1998 |
Unclear |
Low |
Low |
Unclear |
Low |
|
Lyketsos et al., 2003 |
Low |
Low |
Low |
Low |
Low |
|
Liu et al., 2011 |
Unclear |
Unclear |
Unclear |
Low |
Unclear |
|
Magai et al., 2000 |
Unclear |
Low |
Low |
Unclear |
Low |
|
Mokhber et al., 2014 |
Unclear |
Unclear |
Low |
Low |
Unclear |
|
Nyth and Gottfries, 1990 |
Unclear |
Unclear |
Low |
Low |
Low |
|
Passeri et al., 1985 |
Unclear |
Unclear |
Unclear |
Low |
Unclear |
|
Petracca et al., 1996 |
Unclear |
Unclear |
Unclear |
Low |
High |
|
Petracca et al., 2001 |
Unclear |
Low |
Low |
Low |
|
|
Ren et al., 2004 |
Unclear |
Unclear |
Unclear |
Low |
Low |
|
Rosenberg et al., 2010 |
Low |
Low |
Low |
Unclear |
Low |
|
Su et al., 2007 |
Unclear |
High |
High |
Low |
Low |
|
Taragano et al., 1997 |
Low |
Low |
Low |
Unclear |
High |
|
Teri et al., 1991 |
Unclear |
Low |
Low |
Unclear |
Low |
|
Wang et al., 2005 |
Unclear |
Unclear |
High |
Low |
Low |
|
Wu and Zhang, 2007 |
Unclear |
High |
High |
Low |
Unclear |
|
Zhao et al., 2015 |
Unclear |
Unclear |
Unclear |
High |
Low |
|
Zhou and Chi, 2012 |
Unclear |
Unclear |
Unclear |
Low |
Low |
|
Zhu et al., 2006 |
Unclear |
Unclear |
Unclear |
Low |
Low |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Henry G, Williamson D, Tampi RR. Efficacy and tolerability of antidepressants in the treatment of behavioral and psychological symptoms of dementia, a literature review of evidence. Am J Alzheimers Dis Other Demen. 2011 May;26(3):169-83. doi: 10.1177/1533317511402051. Epub 2011 Mar 23. PMID: 21429956; PMCID: PMC10845558. |
Wrong design (literature/narrative review; results are descriptively reported and not pooled). |
|
Mischel N, Rakesh G, Gupta S, Muzyk A, Masand P. Pharmacological agents to treat severe neuropsychiatric symptoms in major neurocognitive disorders. Ann Clin Psychiatry. 2020 May;32(2):128-141. PMID: 32343284. |
Full text is not available. |
|
Hsu TW, Stubbs B, Liang CS, Chen TY, Yeh TC, Pan CC, Chu CS. Efficacy of serotonergic antidepressant treatment for the neuropsychiatric symptoms and agitation in dementia: A systematic review and meta-analysis. Ageing Res Rev. 2021 Aug;69:101362. doi: 10.1016/j.arr.2021.101362. Epub 2021 May 14. PMID: 34000464. |
Includes only two studies with patients with depression. Studies are included in Zhang (2023) as well. |
|
Lenouvel E, Tobias S, Mühlbauer V, Dallmeier D, Denkinger M, Klöppel S, Schönfeldt-Lecuona C. Antidepressants for treating depression among older adults with dementia: A systematic review and meta-analysis. Psychiatry Res. 2024 Oct;340:116114. doi: 10.1016/j.psychres.2024.116114. Epub 2024 Jul 31. PMID: 39163819. |
Included studies are in Zhang (2023) and Dudas (2018) as well. |
|
Leong C. Antidepressants for depression in patients with dementia: a review of the literature. Consult Pharm. 2014 Apr;29(4):254-63. doi: 10.4140/TCP.n.2014.254. PMID: 24704894. |
Wrong design (narrative review). |
|
Nelson JC, Devanand DP. A systematic review and meta-analysis of placebo-controlled antidepressant studies in people with depression and dementia. J Am Geriatr Soc. 2011 Apr;59(4):577-85. doi: 10.1111/j.1532-5415.2011.03355.x. Epub 2011 Mar 31. PMID: 21453380. |
Less recent and complete compared to Dudas (2018) and Zhang (2023). |
|
Orgeta V, Tabet N, Nilforooshan R, Howard R. Efficacy of Antidepressants for Depression in Alzheimer's Disease: Systematic Review and Meta-Analysis. J Alzheimers Dis. 2017;58(3):725-733. doi: 10.3233/JAD-161247. PMID: 28505970; PMCID: PMC5467718. |
Less recent and complete compared to Dudas (2018) and Zhang (2023). |
|
Seibert M, Mühlbauer V, Holbrook J, Voigt-Radloff S, Brefka S, Dallmeier D, Denkinger M, Schönfeldt-Lecuona C, Klöppel S, von Arnim CAF. Efficacy and safety of pharmacotherapy for Alzheimer's disease and for behavioural and psychological symptoms of dementia in older patients with moderate and severe functional impairments: a systematic review of controlled trials. Alzheimers Res Ther. 2021 Jul 16;13(1):131. doi: 10.1186/s13195-021-00867-8. PMID: 34271969; PMCID: PMC8285815. |
P and I are too broad. |
|
Sepehry AA, Lee PE, Hsiung GY, Beattie BL, Jacova C. Effect of selective serotonin reuptake inhibitors in Alzheimer's disease with comorbid depression: a meta-analysis of depression and cognitive outcomes. Drugs Aging. 2012 Oct;29(10):793-806. doi: 10.1007/s40266-012-0012-5. PMID: 23079957. |
Less recent and complete compared to Dudas (2018) and Zhang (2023). |
|
Sultan S. Treating Depression in Dementia Patients: A Risk or Remedy-A Narrative Review. Geriatrics (Basel). 2024 May 15;9(3):64. doi: 10.3390/geriatrics9030064. PMID: 38804321; PMCID: PMC11130822. |
Wrong design (narrative review). |
|
Trieu C, Gossink F, Stek ML, Scheltens P, Pijnenburg YAL, Dols A. Effectiveness of Pharmacological Interventions for Symptoms of Behavioral Variant Frontotemporal Dementia: A Systematic Review. Cogn Behav Neurol. 2020 Mar;33(1):1-15. doi: 10.1097/WNN.0000000000000217. PMID: 32132398. |
PICO is too broad. |
|
Siarkos KT, Katirtzoglou EA, Politis AM. A Review of Pharmacological Treatments for Depression in Alzheimer's Disease. J Alzheimers Dis. 2015;48(1):15-34. doi: 10.3233/JAD-148010. PMID: 26401925. |
Wrong design (narrative review). |
|
Watt JA, Goodarzi Z, Veroniki AA, Nincic V, Khan PA, Ghassemi M, Lai Y, Treister V, Thompson Y, Schneider R, Tricco AC, Straus SE. Comparative efficacy of interventions for reducing symptoms of depression in people with dementia: systematic review and network meta-analysis. BMJ. 2021 Mar 24;372:n532. doi: 10.1136/bmj.n532. PMID: 33762262; PMCID: PMC7988455. |
I and C are too broad. |
Beoordelingsdatum en geldigheid
Publicatiedatum : 03-11-2025
Beoordeeld op geldigheid : 23-10-2025
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinair cluster ingesteld. Het cluster Cognitieve stoornissen en dementie bestaat uit meerdere richtlijnen (zie hier de actuele clusterindeling). De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden brengen hun expertise in, indien nodig. De volgende personen uit het cluster zijn betrokken geweest bij de herziening van deze module:
Clusterstuurgroepleden
- Dhr. prof. dr. M.G.M. (Marcel) Olde Rikkert (voorzitter), klinisch geriater; NVKG
- Dhr. prof. dr. A.R. (Tony) Absalom, anesthesioloog; NVA
- Dhr. dr. J.H.J.M. (Jeroen) de Bresser, radioloog; NVvR
- Mevr. dr. I.K. (Indrag) Lampe, psychiater; NVvP
- Mevr. R. (Renske) Leistra, patiëntvertegenwoordiger; Alzheimer Nederland
- Mevr. prof. dr. B.C. (Barbara) van Munster, internist; NIV
- Dhr. prof. dr. E. (Edo) Richard, neuroloog; NVN
- Mevr. prof. dr. Ir. C. (Charlotte) Teunissen, klinisch chemicus; NVKC
- Dhr. dr. R.A.W. (Ronald) Verhagen, orthopedisch chirurg; NOV
Betrokken clusterexpertisegroepleden
- Dhr. dr. A.P.A. (Auke) Appelman, radioloog; NVvR
- Mevr. dr. R.L. (Rozemarijn) van Bruchem-van Visser, internist ouderengeneeskunde; NIV
- Dhr. drs. B.P.H. (Bas) ter Brugge, specialist ouderengeneeskunde; Verenso
- Dhr. dr. J.A.H.R. (Jurgen) Claassen, klinisch geriater; NVKG
- Dhr. dr. P.L.J. (Paul) Dautzenberg, klinisch geriater; NVKG
- Mevr. dr. M.E.A. (Marlise) van Eersel, internist; NIV
- Mevr. drs. C.M. (Christa) de Geus, neurogeneticus; NVKG
- Mevr. dr. E.M. (Elsmarieke van de Giessen), radioloog; NVNG
- Mevr. drs. M. (Marjolein) Groeneveld, verpleegkundig Consulent Geriatrie, klinisch epidemioloog; V&VN
- Mevr. drs. H. (Hiltsje) Heemskerk, klinisch geriater; NVKG
- Dhr. dr. R.B. (Rients) Huitema, klinisch neuropsycholoog; NIP
- Dhr. drs. A. (Ali) Lahdidioui, internist; NIV
- Dhr. dr. J. (Jules) Lavalaye, nucleair geneeskundige; NVNG
- Mevr. drs. L. (Lieke) Mitrov, ziekenhuisapotheker; NVZA
- Mevr. dr. M. (Marieke) Perry, huisarts/onderzoeker; NHG
- Dhr. dr. G. (Gerwin) Roks, neuroloog; NVN
- Mevr. dr. T.R. (Rikje) Ruiter, internist; NIV
- Mevr. A.J.B.P. (Astrid) Schoonbrood, ergotherapeut; EN
- Mevr. dr. N. (Niki) Schoonenboom, neuroloog; NVN
- Dhr. dr. H. (Harro) Seelaar, neuroloog; NVN
- Dhr. dr. K.S. (Koen) Simons, intensivist-internist; NVIC
- Mevr. drs. M.M.E. (Marlies) Sleegers-Kerkenaar, klinisch geriater; NVKG
- Mevr. drs. VCJ (Vera) van Stek-Smits, neuropsycholoog-gezondheidszorgpsycholoog; NIP
- Mevr. dr. E.M. (Eveline) Veltman, psychiater; NVvP
- Dhr. drs. D. (Dave) Verkaik, AIOS geriatrie; NVKG
- Mevr. prof. dr. M. (Meike) Vernooij, radioloog; NVvR
- Dhr. dr. E.G.B. (Jort) Vijverberg, neuroloog; NVN
- Mevr. dr. M.A. (Marjolein) Wijngaarden, internist; NIV
Met ondersteuning van
- Mevr. dr. C.T.J. (Charlotte) Michels, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. dr. L.C. (Lotte) Houtepen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. drs. L.C. (Laura) van Wijngaarden, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van de clusterleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Clusterstuurgroepleden
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Olde Rikkert* |
Hoogleraar Geriatrie, Radboudumc, Nijmegen |
Hoofdredacteur Nederlands Tijdschrift voor Geneeskunde |
Geen; uitsluitend ZonMw gefinancierd onderzoek dat overheidsbelang centraal stelt. Sinds 2017 geen farma-onderzoek meer. |
Geen restrictie |
|
Absalom |
Hoogleraar Anesthesiologie, UMCG, Groningen |
Consultancy werkzaamheden (betaald, alle betalingen aan UMCG) 6. Consultancy werk voor Becton Dickinson (Eysins, Switzerland) en Terumo (Tokyo, Japan) – technische advies over spuitpompen. Niet gerelateerd aan dementie/ MCI/ delier. |
Extern gefinancierd onderzoeken, maar financier heeft geen belangen bij de richtlijn. * Rigel Pharmaceuticals (San Francisco, USA) (PAST) * The Medicines Company (Parsippany, NJ, USA)(PAST) |
Geen restricties, omdat adviseurswerk niet gerelateerd is aan de afbakening van het cluster |
|
De Bresser |
- Neuroradioloog 1.0fte, LUMC, Leiden |
Geen |
Mijn onderzoek wordt mede gesponsord door Alzheimer Nederland. Deze financier heeft geen belang bij bepaalde uitkomsten van de richtlijn. |
Geen restrictie |
|
Lampe |
Psychiater, OLVG Ziekenhuis, Amsterdam |
Geen |
Geen |
Geen restrictie |
|
Leistra |
Belangenbehartiger, Alzheimer Nederland |
Casemanager Dementie bij de King Arthur Groep |
Geen |
Geen restrictie |
|
Richard |
Hoogleraar neurologie: * afdeling neurologie Radboudumc (0.8fte) * afdeling Public and Occupational Health Amsterdam UMC (0.2 fte) |
- Neuroloog-onderzoeker AmsterdamUMC, locatie AMC, gastvrijheidsaanstelling. - Hoofdredacteur Leerboek Neurologie (Bohn Staffleu van Loghem) |
Geen, uitsluitend onderzoek financiering van non-profit instellingen (e.g. ZonMw, Europese Commissie). |
Geen restrictie |
|
Teunissen |
Hoofd Neurochemisch laboratorium, Afdeling Klinische Chemie, AmsterdamUMC, lokatie VUmc, Amsterdam |
*Adviseur voor educatief blad: Mednet Neurologie (betaald). * Alle betalingen zijn aan het AmsterdamUMC. |
*Wetenschappelijke samenwerking met ADxNeurosciences, Olink, Quanterix, Roche in kader van o.a. Marie Curie subsidie. Het doel van het Marie Curie project is om een nieuwe generatie van onderzoekers in het biomarker veld op te leiden, tot experts in alle aspecten van biomarker onderzoek. Aan het einde van de ontwikkeling van biomarkers zullen deze via bedrijven op de markt moeten komen, en omdat niet alle wetenschappers uiteindelijk in de academische wereld blijven, is het belangrijk dat jonge onderzoekers ervaring opdoen met de manier van onderzoek doen in het bedrijfsleven. In marie curie projecten gebeurt dat door een deel van het onderzoek bij een bedrijf uit te voeren. *Het Neurochemisch laboratorium doet contractresearch voor Acumen, ADx Neurosciences, AC-Immune, Alamar, Aribio, Axon Neurosciences, Beckman-Coulter, BioConnect, Bioorchestra, Brainstorm Therapeutics, Celgene, Cognition Therapeutics, EIP Pharma, Eisai, Eli Lilly, Fujirebio, Instant Nano Biosensors, Novo Nordisk, Olink, PeopleBio, Quanterix, Roche, Toyama, Vivoryon. Dit zijn meestal biomarker-analyses voor hun trials, bij inclusies en als uitkomstmaten. *Grants: Research of CET is supported by the European Commission (Marie Curie International Training Network, grant agreement No 860197 (MIRIADE) and TAME, Innovative Medicines Initiatives 3TR (Horizon 2020, grant no 831434) EPND ( IMI 2 Joint Undertaking (JU), grant No. 101034344) and JPND (bPRIDE, CCAD), European Partnership on Metrology, co-financed from the European Union’s Horizon Europe Research and Innovation Programme and by the Participating States ((22HLT07 NEuroBioStand), CANTATE project funded by the Alzheimer Drug Discovery Foundation, Alzheimer Association, Michael J Fox Foundation, Health Holland, the Dutch Research Council (ZonMW), Alzheimer Drug Discovery Foundation, The Selfridges Group Foundation, Alzheimer Netherlands. CT is recipient of ABOARD, which is a public-private partnership receiving funding from ZonMW (#73305095007) and Health~Holland, Topsector Life Sciences & Health (PPP-allowance; #LSHM20106). CT is recipient of TAP-dementia, a ZonMw funded project (#10510032120003) in the context of the Dutch National Dementia Strategy. |
Geen restrictie |
|
Van Munster |
* Hoogleraar Interne Geneeskunde, Ouderengeneeskunde/Geriatrie, UMCG, Groningen. *Plaatsvervangend opleider Geriatrie, UMCG, Groningen. |
- 2020 – heden Voorzitter Alzheimer Centrum Groningen (alle functies zijn onbetaald) |
*2022 ZONMw: Young Onset Dementia- INCLUDED: Advance care planning. 2022 ZEGG/ZONMw: "The impact of a comprehensive geriatric assessment including advance care planning in acutely hospitalized frail patients with cognitive disorders: the GOAL study" |
Geen restrictie |
|
Verhagen |
Orthopedisch chirurg/opleider in Tergooi MC |
Geen |
Geen |
Geen restrictie |
Clusterexpertisegroepleden
Richtlijn Dementie: Module ‘Antipsychotica bij dementie’
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Mitrov |
Ziekenhuisapotheker, Flevoziekenhuis, Almere |
Special Interest Group Farmacotherapie bij ouderen (NVKG/NVZA), onbetaald |
Geen |
Geen restrictie |
|
Verkaik |
Aios geriatrie, betaalde functie. In opleiding vanuit Gelre ziekenhuizen Apeldoorn en Zutphen. |
Deelname pvc commissie als aios lid voor kwaliteits visitaties (onbetaald) |
Geen |
Geen restrictie |
Richtlijn Dementie: Module ‘Antidepressiva bij dementie’
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Heemskerk |
Klinisch geriater, Arkin Ouderen (GGZ, Amsterdam) |
NVKG, commissie ouderenpsychiatrie |
Geen |
Geen restrictie |
|
Veltman |
Psychiater, UMCU |
Geen |
Geen |
Geen restrictie |
Richtlijn MCI: Module 'Biomarkers’
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Van de Giessen |
Radioloog (aandachtsgebeid nucleaire geneeskunde), Amsterdam UMC |
- NVNG, commissie onderwijs en themagroep neuro |
Beoordelingen PET scans voor Ixico (betaald aan instituut) Contract research voor Roche (betaald aan instituut) Onderzoeksfinanciering van non-profit instelingen (o.a. ZonMw, Alzheimer Nederland, Hersenstichting, Health~Holland, KWF) |
Geen restrictie |
|
Richard |
Hoogleraar neurologie: * afdeling neurologie Radboudumc (0.8fte) * afdeling Public and Occupational Health Amsterdam UMC (0.2 fte) |
- Neuroloog-onderzoeker AmsterdamUMC, locatie AMC, gastvrijheidsaanstelling. - Hoofdredacteur Leerboek Neurologie (Bohn Staffleu van Loghem) |
Geen, uitsluitend onderzoek financiering van non-profit instellingen (e.g. ZonMw, Europese Commissie). |
Geen restrictie |
Richtlijn MCI: Module ‘Leefstijladviezen’
|
Clusterlid
|
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Groeneveld |
Verpleegkundig consulent geriatrie (16 uur) Verpleegkundig onderzoeker Waardengedreven zorg (16 uur) |
Geen
|
Extern gefinancieerd onderzoek: * Catharina onderzoeksfonds: Prestatie en acceptatie van een predictiemodel voor vallen in het ziekenhuis (rol als projectleider) *KIPZ subsidie t/m 31 december: Prestatie en acceptatie van een predictiemodel voor vallen in het ziekenhuis (ja) |
Geen restrictie |
|
Ruiter |
*Internist ouderen geneeskunde en klinische farmacologie Maasstad Ziekenhuis 0,8fte *Post-doctoraal onderzoeker & Epidemioloog B Erasmus MC dept. Epidemiologie 0,1 fte * Lid van het College ter beoordeling van geneesmiddelen |
*Lid raad van toezicht Stichting Landelijk Wonen Klein Houtdijk (Onbetaald). *Secretaris Forum Visitatorum NIV (Onbetaald). *Redactielid Tijdschrift Geriatrie en Gerontologie (Onbetaald). * Voorzitter commissie beroepsbelangen kerngroep ouderengeneeskunde NIV. |
Geen |
Geen restrictie |
|
Claassen |
Universitair hoofddocent en klinisch geriater (1.0 fte), Radboudumc, Nijmegen |
Geen |
*Fase 3 onderzoek Novo Nordisk (EVOKE, NCT04777396. Wereldwijde geneesmiddelenstudie (semaglutide) over Alzheimer. Rol als lokale PI. Middel komt niet aan bod in huidige vijf modules. *MOCIA-project, gefinancierd door ZonMW (www.mocia.nl). *ABOARD onderzoek (gefinancierd door ZonMW en Health Holland, projectnummer: 73305095007) |
Geen restrictie |
Richtlijn MCI: Module ‘Follow-up’
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Claassen |
Universitair hoofddocent en klinisch geriater (1.0 fte), Radboudumc, Nijmegen |
Geen |
*Fase 3 onderzoek Novo Nordisk (EVOKE, NCT04777396. Wereldwijde geneesmiddelenstudie (semaglutide) over Alzheimer. Rol als lokale PI. Middel komt niet aan bod in huidige vijf modules. *MOCIA-project, gefinancierd door ZonMW (www.mocia.nl). *ABOARD onderzoek (gefinancierd door ZonMW en Health Holland, projectnummer: 73305095007) |
Geen restrictie |
|
Perry |
* Huisarts, Huisartsenpraktijk Velp, 0.5 fte * Senior-onderzoeker afdelingen eerstelijnsgeneeskunde en Geriatrie van het Radboudumc en bij het Radboud Alzheimer Centrum, 0.5 fte |
Auteur hoofdstuk Vergeetachtigheid in Álledaagse klachten 2020 (onkostenvergoeding) Commissielid werkgroep multidisciplinaire richtlijn Dementie 2018 - 2020 (onkostenvergoeding) Commissielid werkgroep heziening NHG standaard Dementie 2017 - 2020 (onkostenvergoeding) Commissielid werkgroep Addendum MCI bij multidisciplinaire richtlijn Dementie 20 1 6-20 1 B (onkostenvergoeding) Auteur online nascholing dementie Accredidact huisartsen 2016 en doktersassistenten 2017 (betaald) Auteur twee boekhoofdstukken dementie (palliatieve zorg en diagnostische verrichtingen) 2017 en 2018 in opdracht van het NHG (onkostenvergoeding) Auteur hoofdtsuk Vergeetachtigheid (Alledaagse klachten in de huisartsgeneeskunde) 2020 Onkostenvergoeding Expert bij www.dementie.nl tot heden (vrijwillig) Columnist Alz (donateursblaadje Alzheimer Nederland) tot 2016 (vrijwillig) |
Projectleider DementieNet (financiering door Giekes-Strijbis fonds, Alzheimer Nederland en ZonMw) Andere ZonMw/Memorabel projecten: - Decidem (anticiperende besluitvorming met mensen met dementie door huisartsen), medeprojectleider - Crisisreductie in de dementiezorg, medeaanvrager - SHiMMy en SHARED (relatie sociale gezondheid en ontstaan en progressie van dementie), medeaanvrager - S-Decided (gezamelijke besluitvorming bij diagnostiek bij geheugenklachten), medeaanvrager
Diverse projecten omtrent transmurale/interprofessionele aanpak van advance care planning van Zorginstituut Nederland, Stoffels-Hornstra fonds, ZonMw EPOS: Extramurale praktijkontwikkeling specialist ouderengeneeskunde UNICITY: dementie op jonge leeftijd, oa signalering door huisartsen en onderscheid met depressie, burn-out
*DementieNet aanpak, generieke benadering voor lokale eerstelijns netwerkzorg *Expert bij www.dementie.nl, website van Alzheimer Nederland (vrijwillig) *Columnist Alz (donateursblaadje Alzheimer Nederland) tot 2016 (vrijwillig) *Diverse malen gastspreker bij verschillende Alzheimer Cafés (vrijwillig) |
Geen restrictie |
|
Roks |
Neuroloog ETZ Tilburg |
METC Brabant, lid en vice voorzitter (onkostenvergoeding) |
Geen |
Geen restrictie |
Algemene herziening: Nieuwe concept indeling (richtlijn Dementie en richtlijn MCI)
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Lampe |
Psychiater, OLVG ziekenhuis |
Geen |
Geen |
Geen restrictie |
|
Olde Rikkert* |
Hoogleraar Geriatrie, Radboudumc, Nijmegen |
Hoofdredacteur Nederlands Tijdschrift voor Geneeskunde |
Geen; uitsluitend ZonMw gefinancierd onderzoek dat overheidsbelang centraal stelt. Sinds 2017 geen farma-onderzoek meer. |
Geen restrictie |
|
Perry |
* Huisarts, Huisartsenpraktijk Velp, 0.5 fte * Senior-onderzoeker afdelingen eerstelijnsgeneeskunde en Geriatrie van het Radboudumc en bij het Radboud Alzheimer Centrum, 0.5 fte |
Auteur hoofdstuk Vergeetachtigheid in Álledaagse klachten 2020 (onkostenvergoeding) Commissielid werkgroep multidisciplinaire richtlijn Dementie 2018 - 2020 (onkostenvergoeding) Commissielid werkgroep heziening NHG standaard Dementie 2017 - 2020 (onkostenvergoeding) Commissielid werkgroep Addendum MCI bij multidisciplinaire richtlijn Dementie 20 1 6-20 1 B (onkostenvergoeding) Auteur online nascholing dementie Accredidact huisartsen 2016 en doktersassistenten 2017 (betaald) Auteur twee boekhoofdstukken dementie (palliatieve zorg en diagnostische verrichtingen) 2017 en 2018 in opdracht van het NHG (onkostenvergoeding) Auteur hoofdtsuk Vergeetachtigheid (Alledaagse klachten in de huisartsgeneeskunde) 2020 Onkostenvergoeding Expert bij www.dementie.nl tot heden (vrijwillig) Columnist Alz (donateursblaadje Alzheimer Nederland) tot 2016 (vrijwillig) |
Projectleider DementieNet (financiering door Giekes-Strijbis fonds, Alzheimer Nederland en ZonMw) Andere ZonMw/Memorabel projecten: - Decidem (anticiperende besluitvorming met mensen met dementie door huisartsen), medeprojectleider - Crisisreductie in de dementiezorg, medeaanvrager - SHiMMy en SHARED (relatie sociale gezondheid en ontstaan en progressie van dementie), medeaanvrager - S-Decided (gezamelijke besluitvorming bij diagnostiek bij geheugenklachten), medeaanvrager
Diverse projecten omtrent transmurale/interprofessionele aanpak van advance care planning van Zorginstituut Nederland, Stoffels-Hornstra fonds, ZonMw EPOS: Extramurale praktijkontwikkeling specialist ouderengeneeskunde UNICITY: dementie op jonge leeftijd, oa signalering door huisartsen en onderscheid met depressie, burn-out
*DementieNet aanpak, generieke benadering voor lokale eerstelijns netwerkzorg *Expert bij www.dementie.nl, website van Alzheimer Nederland (vrijwillig) *Columnist Alz (donateursblaadje Alzheimer Nederland) tot 2016 (vrijwillig) *Diverse malen gastspreker bij verschillende Alzheimer Cafés (vrijwillig) |
Geen restrictie |
|
Richard |
Hoogleraar neurologie: * afdeling neurologie Radboudumc (0.8fte) * afdeling Public and Occupational Health Amsterdam UMC (0.2 fte) |
- Neuroloog-onderzoeker AmsterdamUMC, locatie AMC, gastvrijheidsaanstelling. - Hoofdredacteur Leerboek Neurologie (Bohn Staffleu van Loghem) |
Geen, uitsluitend onderzoek financiering van non-profit instellingen (e.g. ZonMw, Europese Commissie). |
Geen restrictie |
Inbreng patiëntenperspectief
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerden de clusterleden conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
| Module |
Uitkomst raming |
Toelichting |
|
Antidepressiva bij depressiesymptomen bij dementie |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het overgrote deel van de zorgverleners al aan de norm voldoet, het geen nieuwe manier van zorgverlening betreft, het geen toename in het aantal voltijdsequivalenten of wijziging in het opleidingsniveau van zorgverleners betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.
Zoekverantwoording
Algemene informatie
|
Cluster/richtlijn: Cluster Cognitieve stoornissen en Dementie |
|
|
Uitgangsvraag/modules: UV2 Wat is de rol van antidepressiva in de behandeling van depressie symptomen bij patiënten met dementie? |
|
|
Database(s): Embase.com, Ovid/Medline, Ovid/PsycInfo |
Datum: 27 augustus 2024 |
|
Periode: vanaf 2010 |
Talen: geen restrictie |
|
Literatuurspecialist: Alies Oost |
|
|
BMI-zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Deduplication: voor het ontdubbelen is gebruik gemaakt van http://dedupendnote.nl:9777/ |
|
|
Toelichting: Voor deze vraag is gezocht op de elementen:
→De sleutelartikelen worden gevonden met deze search. →Er is besloten om in eerste instantie alleen de SRs te screenen. |
|
|
Te gebruiken voor richtlijntekst: In de databases Embase.com, Ovid/Medline en Ovid/PsycInfo is op 27 augustus 2024 systematisch gezocht naar systematische reviews RCTs en observationele studies vanaf 2010 over antidepressiva bij de behandeling van depressie symptomen bij patiënten met dementie. De literatuurzoekactie leverde 924 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
OVID/PSYCINFO |
Ontdubbeld |
|
SR |
823 |
150 |
143 |
924* |
|
RCT |
1322 |
269 |
112 |
1395 |
|
Observationele studies |
1817 |
351 |
168 |
1875 |
|
Totaal |
3962 |
770 |
423 |
4194 |
*in Rayyan
Zoekstrategie
Embase.com
|
No. |
Query |
Results |
|
#1 |
'dementia'/exp OR 'parkinson disease'/exp OR dement*:ti,ab,kw OR parkinson*:ti,ab,kw OR alzheimer*:ti,ab,kw OR ((lewy* NEAR/2 bod*):ti,ab,kw) OR dlbd:ti,ab,kw OR lbd:ti,ab,kw OR ftd:ti,ab,kw OR ftld:ti,ab,kw OR ((pick* NEAR/3 (complex OR disease* OR syndrome*)):ti,ab,kw) |
763962 |
|
#2 |
'depression'/exp OR 'mood disorder'/exp OR depress*:ti,ab,kw OR (((mood OR affective) NEAR/3 (disorder* OR disturbance*)):ti,ab,kw) OR melanchol*:ti,ab,kw OR dysthym*:ti,ab,kw |
1102505 |
|
#3 |
'antidepressant agent'/exp OR (((antidepress* OR 'anti depress*' OR thymoleptic OR thymolytic) NEAR/3 (agent* OR drug* OR medicine* OR medicat* OR pharmacother* OR atypical)):ti,ab,kw) OR antidepressants:ti,ab,kw OR 'anti depressants':ti,ab,kw OR psychoenergiz*:ti,ab,kw OR thymoleptics:ti,ab,kw OR thymoanaleptics:ti,ab,kw OR 'tricyclic antidepressant agent'/exp OR 'tricyclic antidepress*':ti,ab,kw OR 'tricyclic anti depress*':ti,ab,kw OR tca:ti,ab,kw OR 'amitriptyline'/exp OR 'amitriptylin*':ti,ab,kw OR 'clomipramine'/exp OR 'clomipramin*':ti,ab,kw OR 'dosulepin'/exp OR 'dosulepin*':ti,ab,kw OR dothiepin:ti,ab,kw OR 'doxepin'/exp OR 'doxepin*':ti,ab,kw OR 'imipramine'/exp OR 'imipramin*':ti,ab,kw OR 'maprotiline'/exp OR 'maprotilin*':ti,ab,kw OR 'nortriptyline'/exp OR 'nortriptylin*':ti,ab,kw OR 'serotonin uptake inhibitor'/exp OR (((serotonin OR '5 ht' OR '5 hydroxytryptamin*') NEAR/4 (uptake OR reuptake OR 're uptake') NEAR/4 inhibit*):ti,ab,kw) OR ssri:ti,ab,kw OR ssris:ti,ab,kw OR 'citalopram'/exp OR 'citalopram':ti,ab,kw OR 'escitalopram'/exp OR 'escitalopram':ti,ab,kw OR 'fluoxetine'/exp OR 'fluoxetin*':ti,ab,kw OR 'fluvoxamine'/exp OR fluvoxamin*:ti,ab,kw OR 'paroxetine'/exp OR 'paroxetin*':ti,ab,kw OR 'sertraline'/exp OR 'sertralin*':ti,ab,kw OR 'serotonin noradrenalin reuptake inhibitor'/exp OR (((noradrenalin* OR norepinephrin*) NEAR/4 serotonin NEAR/4 inhibit*):ti,ab,kw) OR snri:ti,ab,kw OR snris:ti,ab,kw OR ssnri:ti,ab,kw OR nsri:ti,ab,kw OR nsris:ti,ab,kw OR 'duloxetine'/exp OR 'duloxetin*':ti,ab,kw OR 'venlafaxine'/exp OR 'venlafaxin*':ti,ab,kw |
683995 |
|
#4 |
#1 AND #2 AND #3 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) AND [2010-2024]/py |
7013 |
|
#5 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
1056327 |
|
#6 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
4095000 |
|
#7 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
8377707 |
|
#8 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
15342315 |
|
#9 |
#4 AND #5 - SR |
823 |
|
#10 |
#4 AND #6 NOT #9 - RCT |
1322 |
|
#11 |
#4 AND (#7 OR #8) NOT (#9 OR #10) - observationeel |
1817 |
|
#12 |
#9 OR #10 OR #11 |
3962 |
Ovid/Medline
|
# |
Searches |
Results |
|
1 |
exp Dementia/ or Parkinsonian Disorders/ or dement*.ti,ab,kf. or parkinson*.ti,ab,kf. or alzheimer*.ti,ab,kf. or (lewy* adj2 bod*).ti,ab,kf. or dlbd.ti,ab,kf. or lbd.ti,ab,kf. or ftd.ti,ab,kf. or ftld.ti,ab,kf. or (pick* adj3 (complex or disease* or syndrome*)).ti,ab,kf. |
477354 |
|
2 |
exp Depression/ or exp Depressive Disorder/ or exp Mood Disorders/ or depress*.ti,ab,kf. or ((mood or affective) adj3 (disorder* or disturbance*)).ti,ab,kf. or melanchol*.ti,ab,kf. or dysthym*.ti,ab,kf. |
698008 |
|
3 |
exp Antidepressive Agents/ or ((antidepress* or 'anti depress*' or thymoleptic or thymolytic) adj3 (agent* or drug* or medicine* or medicat* or pharmacother* or atypical)).ti,ab,kf. or antidepressants.ti,ab,kf. or 'anti depressants'.ti,ab,kf. or psychoenergiz*.ti,ab,kf. or thymoleptics.ti,ab,kf. or thymoanaleptics.ti,ab,kf. or exp Antidepressive Agents, Tricyclic/ or 'tricyclic antidepress*'.ti,ab,kf. or 'tricyclic anti depress*'.ti,ab,kf. or tca.ti,ab,kf. or exp Amitriptyline/ or 'amitriptylin*'.ti,ab,kf. or exp Clomipramine/ or 'clomipramin*'.ti,ab,kf. or exp Dothiepin/ or 'dosulepin*'.ti,ab,kf. or dothiepin.ti,ab,kf. or exp Doxepin/ or 'doxepin*'.ti,ab,kf. or exp Imipramine/ or 'imipramin*'.ti,ab,kf. or exp Maprotiline/ or 'maprotilin*'.ti,ab,kf. or exp Nortriptyline/ or 'nortriptylin*'.ti,ab,kf. or exp Selective Serotonin Reuptake Inhibitors/ or ((serotonin or '5 ht' or '5 hydroxytryptamin*') adj4 (uptake or reuptake or 're uptake') adj4 inhibit*).ti,ab,kf. or ssri.ti,ab,kf. or ssris.ti,ab,kf. or exp Citalopram/ or 'citalopram'.ti,ab,kf. or exp Escitalopram/ or 'escitalopram'.ti,ab,kf. or exp Fluoxetine/ or 'fluoxetin*'.ti,ab,kf. or exp Fluvoxamine/ or fluvoxamin*.ti,ab,kf. or exp Paroxetine/ or 'paroxetin*'.ti,ab,kf. or exp Sertraline/ or 'sertralin*'.ti,ab,kf. or exp "Serotonin and Noradrenaline Reuptake Inhibitors"/ or ((noradrenalin* or norepinephrin*) adj4 serotonin adj4 inhibit*).ti,ab,kf. or snri.ti,ab,kf. or snris.ti,ab,kf. or ssnri.ti,ab,kf. or nsri.ti,ab,kf. or nsris.ti,ab,kf. or exp Duloxetine Hydrochloride/ or 'duloxetin*'.ti,ab,kf. or exp Venlafaxine Hydrochloride/ or 'venlafaxin*'.ti,ab,kf. |
228338 |
|
4 |
(1 and 2 and 3) not (comment/ or editorial/ or letter/) not ((exp animals/ or exp models, animal/) not humans/) |
2667 |
|
5 |
limit 4 to yr="2010 -Current" |
1337 |
|
6 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
770083 |
|
7 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2769217 |
|
8 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] |
4811329 |
|
9 |
Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) |
5769612 |
|
10 |
5 and 6 - SR |
150 |
|
11 |
(5 and 7) not 10 - RCT |
269 |
|
12 |
(5 and (8 or 9)) not (10 or 11) - observationeel |
351 |
|
13 |
10 or 11 or 12 |
770 |
Ovid/PsycInfo
|
# |
Searches |
Results |
|
1 |
exp Dementia/ or exp Alzheimer Disease/ or exp Parkinsons Disease/ or dement*.ti,ab,id. or parkinson*.ti,ab,id. or alzheimer*.ti,ab,id. or (lewy* adj2 bod*).ti,ab,id. or dlbd.ti,ab,id. or lbd.ti,ab,id. or ftd.ti,ab,id. or ftld.ti,ab,id. or (pick* adj3 (complex or disease* or syndrome*)).ti,ab,id. |
160879 |
|
2 |
exp Major Depression/ or exp Persistent Depressive Disorder/ or exp "Depression (Emotion)"/ or exp Affective Disorders/ or depress*.ti,ab,id. or ((mood or affective) adj3 (disorder* or disturbance*)).ti,ab,id. or melanchol*.ti,ab,id. or dysthym*.ti,ab,id. |
408902 |
|
3 |
exp Thymoleptic Drugs/ or ((antidepress* or 'anti depress*' or thymoleptic or thymolytic) adj3 (agent* or drug* or medicine* or medicat* or pharmacother* or atypical)).ti,ab,id. or antidepressants.ti,ab,id. or 'anti depressants'.ti,ab,id. or psychoenergiz*.ti,ab,id. or thymoleptics.ti,ab,id. or thymoanaleptics.ti,ab,id. or exp Tricyclic Antidepressant Drugs/ or 'tricyclic antidepress*'.ti,ab,id. or 'tricyclic anti depress*'.ti,ab,id. or tca.ti,ab,id. or exp Amitriptyline/ or 'amitriptylin*'.ti,ab,id. or exp Clomipramine/ or 'clomipramin*'.ti,ab,id. or 'dosulepin*'.ti,ab,id. or dothiepin.ti,ab,id. or exp Doxepin/ or 'doxepin*'.ti,ab,id. or exp Imipramine/ or 'imipramin*'.ti,ab,id. or exp Maprotiline/ or 'maprotilin*'.ti,ab,id. or exp Nortriptyline/ or 'nortriptylin*'.ti,ab,id. or exp Selective Serotonin Reuptake Inhibitors/ or ((serotonin or '5 ht' or '5 hydroxytryptamin*') adj4 (uptake or reuptake or 're uptake') adj4 inhibit*).ti,ab,id. or ssri.ti,ab,id. or ssris.ti,ab,id. or exp Citalopram/ or 'citalopram'.ti,ab,id. or 'escitalopram'.ti,ab,id. or exp Fluoxetine/ or 'fluoxetin*'.ti,ab,id. or exp Fluvoxamine/ or fluvoxamin*.ti,ab,id. or exp Paroxetine/ or 'paroxetin*'.ti,ab,id. or exp Sertraline/ or 'sertralin*'.ti,ab,id. or exp Serotonin Norepinephrine Reuptake Inhibitors/ or ((noradrenalin* or norepinephrin*) adj4 serotonin adj4 inhibit*).ti,ab,id. or snri.ti,ab,id. or snris.ti,ab,id. or ssnri.ti,ab,id. or nsri.ti,ab,id. or nsris.ti,ab,id. or 'duloxetin*'.ti,ab,id. or exp Venlafaxine/ or 'venlafaxin*'.ti,ab,id. |
100459 |
|
4 |
1 and 2 and 3 |
1629 |
|
5 |
limit 4 to yr="2010 -Current" |
817 |
|
6 |
((literature review or systematic review or meta analysis).md. or "literature review"/ or meta analysis/ or (((meta adj2 analy*) or metaanaly* or (synthes* adj2 (literature* or research* or studies or data)) or (pooled and analys*) or ((data adj1 pool*) and studies) or medline or medlars or embase or cinahl or scisearch or psychlit or psyclit or cinhal or cancerlit or cochrane or bids or pubmed or ovid or ((hand or manual or database* or computer*) adj1 search*) or (electronic adj1 (database* or data base or data bases))).ti,ab,id. or (review* or overview).ti. or (bibliograph* or relevant journals or ((review* or overview*) adj9 (systematic* or methodologic* or quantitativ* or research* or literature* or studies or trial* or effective*))).ab.)) not (((retrospective* or record* or case* or patient*) adj1 review*) or ((patient* or review*) adj1 chart*)).ti,ab,id. |
500903 |
|
7 |
exp clinical trial/ or randomized controlled trial/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
306565 |
|
8 |
Epidemiologic studies/ or case control studies/ or exp Cohort Analysis/ or Controlled Before-After Studies/ or Case control.tw. or cohort*.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ |
492829 |
|
9 |
5 and 6 - SR |
143 |
|
10 |
(5 and 7) not 9 - RCT |
112 |
|
11 |
(5 and 8) not (9 or 10) - observationeel |
168 |
|
12 |
9 or 10 or 11 |
423 |