Leidraad chirurgische behandeling van CMN
Uitgangsvraag
Leidraad chirurgische behandeling (bij behandelindicatie) van congenitale melanocytaire naevi (CMN).
Aanbeveling
De werkgroep is van mening dat indien er een indicatie bestaat voor behandeling in principe excisie (evt met reconstructie) de voorkeur heeft. Pas in tweede instantie dient ‘partial thickness’ behandeling te worden overwogen, indien excisie niet mogelijk of niet wenselijk is.
Het advies van de Nederlandse Vereniging voor Anesthesiologie luidt: liefst geen electieve ingrepen voor de leeftijd van 3 jaar. Kleinere CMN kunnen in principe op elke leeftijd behandeld worden, maar voor grotere CMN kan de leeftijd een belangrijke rol spelen (liefst jong). Verwacht resultaat en risico op complicaties dienen goed met de patiënt/ouders te worden doorgesproken. Vroegtijdige voorlichting is van belang voor het openhouden van alle behandelopties.
Na verwijdering met alle chirurgische technieken geldt dat in uitgebreidere CMN levenslange follow-up nodig blijft, omdat de verwijdering van alle naevuscellen niet gegarandeerd is (ook bij excisie) en er een (laag) risico blijft bestaan op neurologische complicaties.. Of hierbij zelfonderzoek kan volstaan of follow-up in een ziekenhuis aangewezen is is afhankelijk van het risicofenotype (zie follow-up schema in de module ‘Organisatie van zorg bij CMN’).
Onderbouwing
Expert opinion
De optimale chirurgische behandeling van grotere CMN is een uitdaging. Geen van de huidige technieken is toepasbaar voor alle CMN. Vaak zijn meerdere, ingrijpende operaties en een combinatie van technieken nodig. Individuele benadering is van groot belang. In kleinere CMN is het dilemma minder groot en kunnen naevi <5cm (afhankelijk van de lokalisatie) in het algemeen succesvol in één etappe worden geëxcideerd [Kruk-Jeromin 1998].
Het doel van chirurgische verwijdering is het zo volledig mogelijk verwijderen van alle naevuscellen met zo min mogelijk complicaties, en met een minimaal zichtbaar litteken, behoud van de anatomische structuur en behoud van functie.
In principe geldt met de nieuwe inzichten ten aanzien van een lager melanoomrisico, met het grootste risico in de allergrootste CMN, en de niet bewezen rol van profylactische chirurgie hierbij, dat de noodzaak van volledige verwijdering van CMN meer naar de achtergrond verdwijnt [Arad 2014, Kinsler 2009] al zijn de meningen hierover verdeeld [Bauer 2014]. Cosmetische indicatie voor behandeling treedt meer op de voorgrond.
Het is lastig op basis van de literatuur een uitspraak te doen over cosmetisch resultaat en veiligheid van de behandelingen, en behandelingen te vergelijken (welke heeft de voorkeur?). De studies over chirurgische behandeling van CMN (alle technieken) zijn van lage methodologische kwaliteit: vooral retrospectieve caseseries met een groot risico op selectiebias, met slechts summiere beschrijving van uitkomsten, niet gevalideerde uitkomstmaten en complicaties zonder objectieve, kwantitatieve beoordelingen. Tevens zijn de patiëntkarakteristieken niet altijd duidelijk (grootte, lokalisatie CMN), en vaak erg heterogeen tussen studies. Ook zijn er geen (gecontroleerde) vergelijkende studies.
Op basis van expert opinion komt de werkgroep tot de volgende leidraad:
Keuze voor behandeling
De werkgroep komt tot de aanbeveling dat indien chirurgische verwijdering gewenst is, excisie in principe de voorkeur heeft. Met excisie wordt de naevus in de diepte (zo goed als) geheel verwijderd, en geeft daarmee de beste reductie van het risico op melanoom. Tevens is de pigmentatie daarmee geheel verwijderd. Wel bestaat er een klein risico op repigmentatie in en rondom het litteken, waarvan niet duidelijk is waarom deze ontstaat. Excisie liefst met primaire sluiting, indien dit niet mogelijk is kunnen andere reconstructietechnieken worden toegepast [zie de module ‘Invasieve behandelingen bij CMN’]. Als de CMN te groot is voor complete (seriële) excisie kan eventueel ook met partiële excisie worden volstaan (van het meest onrustige of cosmetisch storende deel).
Indien excisie niet mogelijk is kunnen superficiële technieken worden overwogen, indien:
- de CMN te groot is voor excisie
- excisie niet wenselijk is (waarschijnlijk zeer ontsierende littekens of functieverlies geeft).
Bij de oppervlakkige therapieën kan niet al het pigment in de diepte worden verwijderd en treedt er repigmentatie op. Deze technieken hebben tevens geen effect op de hypertrichose (behoudens enkele typen lasertherapie). Voor oppervlakkige technieken geldt overigens wel dat nadien nog excisie zou kunnen plaatsvinden. Deze behandelingen kunnen ook gecombineerd worden (in eenzelfde sessie) met excisie. Bij een keuze voor oppervlakkige technieken wordt op basis van de huidige ervaring in grotere CMN eerder curettage of lasertherapie (Er:YAG) dan dermabrasie geadviseerd, in kleinere CMN lasertherapie [zie de module ‘Invasieve behandelingen bij CMN’]. De werkgroep benadrukt dat het van belang is dat de toepassing van deze technieken in ervaren handen gebeurt.
Leeftijd van behandelen
Kleinere CMN kunnen in principe op elke leeftijd behandeld worden, maar voor grotere CMN kan de leeftijd een belangrijke rol spelen waarbij ingrijpen op jonge leeftijd vaak de voorkeur heeft, hoewel er geen bewijs is in de literatuur dat dit ook beter is.
Argumenten voor ingrijpen op jonge leeftijd zijn:
- de elasticiteit van de huid is op jongere leeftijd vele malen hoger (tot ongeveer de leeftijd van 4 jaar) waardoor per sessie grotere delen naevushuid kunnen worden verwijderd, of beter kunnen worden opgerekt bij ‘tissue expansion’ [Fujiwara 2008, Paul 1998]Vooral in de eerste maanden na de geboorte kan een laesie bijv op het behaard hoofd geëxcideerd worden waarvoor vaak op latere leeftijd meerdere ingrepen nodig zijn.
- het subcutane vet is op jonge leeftijd het dikste [Fujiwara 2008, Paul 1998]
- bij operaties op de jonge kinderleeftijd kunnen kinderen zich er later vaak niet meer veel van herinneren, bovendien is de CMN dan verwijderd vóór de schoolgaande leeftijd [Bellier-Waast 2008]
- sommige technieken zijn alleen mogelijk op zeer jonge leeftijd (curettage 1~3 maanden)
- het melanoomrisico, in grotere CMN is dit het hoogst op de kinderleeftijd (maar actueel niet meer de hoofdindicatie).
Nadelen van opereren op jonge leeftijd zijn dat de patiënt hier zelf geen keuze in heeft (de keuze wordt gemaakt door de ouders). Tevens bestaat de mogelijkheid dat de CMN spontaan lichter zou zijn geworden in de loop der jaren [Kinsler 2009].
Een ander belangrijk aandachtspunt bij de keuze van leeftijd van behandelen is de toepassing van anesthesie. Er zijn zorgen ontstaan rondom de toepassing van algehele anesthesie bij jonge kinderen, vanwege een mogelijk verhoogd risico op complicaties (hartstilstand bij zeer jonge kinderen, mogelijke invloed op neurologische, cognitieve en sociale ontwikkeling) [Rappaport 2011]. Verder onderzoek hiernaar is nodig. Globaal hebben jongere kinderen meer risico’s en complicaties dan ouderen, en kinderen meer dan volwassenen. Kinderen >3 jr hebben het laagste risico, dan categorie kinderen 1-2 jaar, dan zuigelingen (1maand-1jaar) en dan neonaten/ex-prematuren (hoogste risico). Momenteel hanteert de Nederlandse Vereniging voor Anesthesiologie als leidraad: electieve ingrepen indien mogelijk pas vanaf de leeftijd van 3 jaar (www.anesthesiologie.nl/kwaliteit/richtlijnen). De werkgroep volgt deze richtlijn.
Op basis van chirurgische expertise en ervaring kan in uitzonderingsgevallen van bovenstaande richtlijn worden afgeweken. Indien met een enkele ingreep op babyleeftijd de naevus geheel kan worden weggehaald, en met wachten alleen middels (meerdere) complexe ingrepen heeft jong ingrijpen toch de voorkeur. Ook indien voor curettage wordt gekozen is behandeling in de eerste drie maanden geïndiceerd. Indien er meerdere ingrepen op jonge leefijd nodig zullen zijn (bv meerdere rondes ‘tissue expansion’) dient er eerst uitgebreid overleg te volgen met ouders. Iindien het gaat om een kleinere, relatief onschuldige naevus kan prima worden afgewacht tot de leeftijd van 3 jaar.
Follow-up
In de postoperatieve periode is met alle technieken goede follow-up van belang om optimale wondcondities te creëren, en mogelijke complicaties (zoals littekenvorming) in een tijdig stadium te herkennen en wellicht nog te kunnen behandelen.
Daarnaast is blijvende follow-up na behandeling van belang. Bij alle verwijderingstechnieken blijft er immers een risico op maligne ontaarding bestaan. Zeker bij de superficiële technieken, waar slechts een reductie van de naevusload wordt bereikt terwijl in de diepere huidlagen naevuscellen aanwezig blijven. In principe gaat men bij excisie uit van volledige verwijdering, maar ook hier blijven mogelijk bij excisie van uitgebreidere CMN er nog naevuscellen achter, deze kunnen zeer diep infiltreren. Om deze reden blijft het van belang ook het litteken na chirurgie op pigmentatie te blijven controleren, repigmentatie is bekend. Verder hebben patiënten met uitgebreidere CMN een risico op maligne manifestaties in het centraal zenuwstelsel waarvoor blijvende follow-up nodig is.
- Alikhan A, Ibrahimi OA, Eisen DB. Congenital melanocytic nevi: where are we now? Part I. Clinical presentation, epidemiology, pathogenesis, histology, malignant transformation, and neurocutaneous melanosis. J Am Acad Dermatol. 2012;67(4):495 e1-17; quiz 512-4.
- Arad E, Zuker RM. The shifting paradigm in the management of giant congenital melanocytic nevi: review and clinical applications. Plast Reconstr Surg. 2014;133(2):367-76.
- Arons MS, Hurwitz S. Congenital nevocellular nevus: a review of the treatment controversy and a report of 46 cases. Plast Reconstr Surg. 1983;72(3):355-65.
- Bauer BS, Dickie SR, Marghoob AA. Reply: The shifting paradigm in the management of giant congenital melanocytic nevi: review and clinical applications. Plast Reconstr Surg. 2014 Oct;134(4):659e-60e.
- Fujiwara M, Nakamura Y, Fukamizu H. Treatment of giant congenital nevus of the back by convergent serial excision. J Dermatol 2008;35:608-10
- Kovalyshyn I, Braun R, Marghoob A. Congenital melanocytic naevi. Australas J Dermatol. 2009;50(4):231-40; quiz 41-2.
- Krengel S, Marghoob AA. Current management approaches for congenital melanocytic nevi. Dermatol Clin. 2012;30(3):377-87.
- Paul AA, Cole TJ, Ahmed EA, Whitehead RG. The need for revised standards for skinfold thickness in infancy. Arch Dis Child 1998;78:354-8
- Rappaport B, Mellon RD, Simone A, Woodcock J. Defining safe use of anesthesia in children. N Engl J Med 2011;364: 1387-90.
- Sweren RJ. Management of congenital nevocytic nevi: a survey of current practices. J Am Acad Dermatol. 1984;11(4 Pt 1):629-34.
- Tromberg J, Bauer B, Benvenuto-Andrade C, Marghoob AA. Congenital melanocytic nevi needing treatment. Dermatol Ther. 2005;18(2):136-50.
Beoordelingsdatum en geldigheid
Publicatiedatum : 21-02-2018
Beoordeeld op geldigheid : 17-11-2017
Een richtlijn heeft alleen zeggingskracht als op continue basis onderhoud plaatsvindt, op grond van systematische monitoring van zowel de medisch wetenschappelijke literatuur als praktijkgegevens en door gebruikers van de richtlijn aangeleverde commentaren. Voor deze richtlijn is afgesproken één keer per jaar de literatuur te evalueren om nieuwe ontwikkelingen te volgen. Bij essentiële ontwikkelingen kan besloten worden om een gehele richtlijnwerkgroep bij elkaar te roepen en tussentijdse elektronische amendementen te maken en deze onder de verschillende beroepsgroepen te verspreiden. Om de richtlijn ‘levend’ te houden is modulaire herziening mogelijk, waarbij slechts een deel of delen van de richtlijn kunnen worden gereviseerd.
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Deze richtlijn is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering in de begeleiding van patiënten met congenitale melanocytaire naevi (CMN) en hun directe omgeving. De richtlijn berust op de resultaten van wetenschappelijk onderzoek en aansluitende meningsvorming, door experts, gericht op het vaststellen van goed medisch handelen. De financiering van deze richtlijn is tot stand gekomen met gelden die de NVDV uit zijn SKMS-programma heeft vrijgemaakt.
Doelgroep
De richtlijn is bestemd voor leden van de medische en paramedische beroepsgroepen, waartoe tenminste behoren: dermatologen, plastisch chirurgen, pathologen, kinderartsen, neurologen, huisartsen, verpleegkundigen en huidtherapeuten. Tevens is in een samenwerking tussen patiëntenvereniging NNN en de VSOP een huisartsbrochure ontwikkeld.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn werd een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordiging van de bij CMN betrokken disciplines. Bij het samenstellen van de werkgroep is getracht rekening te houden met de geografische spreiding van de werkgroepleden en met een evenredige vertegenwoordiging van academische en niet-academische werkgroepleden. De werkgroepleden hebben onafhankelijk gehandeld en geen enkel werkgroeplid ontving gunsten met het doel de richtlijn te beïnvloeden.
|
Werkgroepleden |
Vereniging |
|
Prof.dr. Suzanne Pasmans (voorzitter) |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Drs. Céline Eggen (secretaris) |
Promovendus kinderdermatologie Erasmus MC (NVDV)
|
|
Prof.dr. Wilma Bergman |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Nicole Kukutsch |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Albert Wolkerstorfer |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Simone Stadhouders-Keet |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Marianne Crijns |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Drs. Annelies Lommerts
|
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Prof.dr. Chantal van der Horst |
Nederlandse Vereniging voor Plastische Chirurgie (NVPC) |
|
Dr. Corstiaan Breugem |
Nederlandse Vereniging voor Plastische Chirurgie (NVPC) |
|
Prof.dr. Wolter Mooi |
Nederlandse Vereniging voor Pathologie (NVVP) |
|
Dr. Hanneke Rijk-van Gent |
Nederlandse Vereniging voor Kindergeneeskunde (NVK) |
|
Prof.dr. Michèl Willemsen |
Nederlandse Vereniging voor Neurologie (NVN) en Nederlandse Vereniging voor Kinderneurologie (NVKN) |
|
Mw. Anja Ebus |
Verpleegkundigen en Verzorgenden Nederland Verpleegkundig Specialist (V&VN VS) en V&VN Dermatologie. |
|
Mw. Marjolein van Kessel |
Nevus Netwerk Nederland (NNN)
|
Verder hebben aan deze richlijn meegewerkt drs. Joep Wijnand en drs. Michéle Hennekam.
Inbreng patiëntenperspectief
Reeds sinds de start van het richtlijntraject is de patiëntenvereniging Nevus Netwerk Nederland (NNN) zeer betrokken geweest bij de totstandkoming van deze richtlijn, door afvaarding van een bestuurslid in de werkgroep. Zij zijn in deze hoedanigheid tijdens het gehele richtlijntraject betrokken geweest, door actieve participatie tijdens werkgroepvergaderingen, en het aandragen van knelpunten die vanuit patiëntenperspectief van groot belang zijn, evenals het deelgenoot maken van lopende initiatieven in het veld. Nevus Netwerk Nederland heeft ook zijn fiat verleend aan de inhoud van de richtlijn.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de ontwikkeling van de conceptrichtlijn is zoveel mogelijk rekening gehouden met de implementatie van de richtlijn en de daadwerkelijke uitvoerbaarheid van de aanbevelingen. De richtlijn wordt gepubliceerd op de website van de NVDV, de website van de richtlijnen database en wordt tevens verspreid onder alle bij CMN betrokken beroepsgroepen. Ook wordt een samenvatting van de richtlijn gepubliceerd en er zal in verschillende specifieke vaktijdschriften aandacht aan worden besteed. Daarnaast wordt de richtlijn onder de aandacht gebracht via de betrokken patiëntenvereniging. De richtlijn is ondergebracht in huidhuis.nl (vanuit de NVDV) en gekoppeld aan het persoonlijk gezondheidsdossier van Patient1 in huidhuis.nl voor mensen met een huidafwijking en de betrokken professionals.
Werkwijze
De richtlijn congenitale melanocytaire naevi is een geheel nieuwe richtlijn. In de richtlijn melanoom (goedgekeurd op 13.08.2012) wordt reeds verwezen naar de in wording zijnde richtlijn CMN. De richtlijnwerkgroep is opgestart in het najaar van 2011, maar heeft tussendoor enkele malen stil gelegen onder andere vanwege een andere prioritering op de richtlijnagenda van de NVDV.
In de eerste vergadering(en) werden de knelpunten en wensen ten aanzien van het onderwerp CMN geïnventariseerd binnen de werkgroep. De werkgroep formuleerde aan de hand hiervan in de richtlijn vermelde uitgangsvragen. Ook werd aan de start van het traject een enquête uitgezet onder dermatologen en plastisch chirurgen in Nederland om het huidige beleid omtrent CMN te inventariseren. De doelen van deze enquête waren het vastleggen van de uitgangssituatie om tot een richtlijn te komen die aansluit op de werkvloer, en het identificeren van aanvullende knelpunten.
De uitgangsvragen werden op het bureau van de Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) uitgewerkt tot PICO-zoekvragen. Via systematische zoekopdrachten en reference checking is bruikbare literatuur verzameld. De secretaris van de richtlijn en studenten hebben samen met de werkgroepleden de literatuur beoordeeld op inhoud en kwaliteit. Vervolgens zijn er teksten geschreven waarin de beoordeelde literatuur werd verwerkt. Deze teksten, op basis van de evidencetabellen met de verwerkte literatuur, zijn tijdens een tweedaagse vergadering besproken en van nuances en aanbevelingen voorzien. Na verdere discussie binnen de gehele richtlijnwerkgroep is de tekst verder afgestemd.
De uiteindelijke tekst werd in september 2016 aan alle betrokken wetenschappelijke verenigingen aangeboden. Men is in staat gesteld om via websites van de betrokken verenigingen commentaar op de richtlijn te geven. De commentaren zijn in de definitieve versie van de richtlijn verwerkt.
Wetenschappelijke bewijsvoering
De aanbevelingen uit deze richtlijn zijn, voor zover mogelijk, gebaseerd op bewijs uit gepubliceerd wetenschappelijk onderzoek.
Relevante artikelen zijn gezocht via een systematische, oriënterende zoekopdracht in Pubmed, overkoepelend voor het onderwerp congenitale melanocytaire naevi (van 1987 tot november 2014, talen Nederlands, Engels, Frans, Duits). Voor specifieke uitgangsvragen werd nog een aanvullende systematische search verricht met meer specifieke zoektermen voor de desbetreffende vraag, en in aanvullende databases (zoals Embase, CENTRAL, Cochrane library etc). Tevens is voor enkele uitgangsvragen en passages de search meer recent herhaald (2014~2016). Zie ook de zoekstrategie.
De zoekacties zijn met behulp van de PICO-systematiek opgebouwd. Dit houdt in dat voor elke uitgangsvraag een zoekvraag is geformuleerd waarbij zoveel mogelijk de volgende structuur is gehanteerd: Patiënt-Interventie-Controle-Outcome. De zoekvragen hebben de P als gemeenschappelijk onderdeel, de overige onderdelen van de PICO zijn geformuleerd op basis van de uitgangsvraag. Het merendeel van de zoekcriteria is afhankelijk van de uitgangsvraag.
Algemeen werden de volgende zoek- en selectiecriteria opgesteld:
|
Taal |
Engels, Nederlands, Duits, Frans |
|
Populatie |
Congenitale melanocytaire naevi (in alle synoniemen), alle groottes, alle leeftijden (exclusie van verworven melanocytaire naevi, of als niet gespecifieerd was of de naevi congenitaal waren) |
|
level of evidence |
Literatuurselectie volgens piramide van bewijs (EBRO-methode). Vanwege het veelal ontbreken van studies van goede kwaliteit (gerandomiseerd of prospectief) is er niet beperkt op de fundamentele opzet van de studie |
|
grootte van de studies |
Hier is in het algemeen geen limiet aangesteld, omdat voor de meeste uitgangsvragen slechts caseseries met enkele patiënten beschikbaar zijn. Wel zijn bij meerdere uitgangsvragen casereports en caseseries met <5 patiënten geëxcludeerd, omdat deze een nog grotere selectiebias geven en daarmee een mogelijk te vertekend beeld van de werkelijkheid. |
Van de geselecteerde referenties op basis van titel en/of abstract werd de full-text aangevraagd. Op basis van full-text artikelen is vervolgens verder geselecteerd en zijn artikelen zonder informatie over de betreffende uitgangsvraag geëxcludeerd. De overgebleven artikelen zijn full-text beoordeeld op kwaliteit en inhoud.
Tijdens de search werden geen (buitenlandse) richtlijnen over dit onderwerp geïdentificeerd, maar wel enkele relevante en betrouwbare ‘learning articles’, waarin op gedegen wijze relevante literatuur over het onderwerp CMN in zijn totaliteit is samengebracht. Deze artikelen vormen deels de basis voor de enkele richtlijnteksten [Alikhan 2012, Ibrahimi 2012, Viana 2013], aangevuld met andere relevante literatuur.
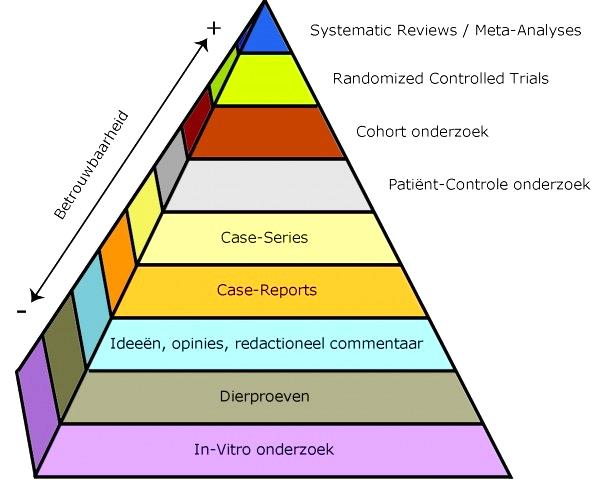
Fig. 1: Piramide van wetenschappelijk bewijs
Methode van literatuurbeoordeling
De richtlijn is ontwikkeld volgens de EBRO-methode (Evidence-based Richtlijn Ontwikkeling). Per deelonderwerp is van de relevante artikelen een ‘evidencetabel’ opgesteld, waarin de literatuur is samengevat en beoordeeld op kwaliteit. De beschrijving en beoordeling van de artikelen staan in de verschillende module onder het kopje ‘wetenschappelijke onderbouwing’, en de literatuur is vervolgens samengevat in ‘conclusies’. De kwaliteit van de artikelen en het niveau van het relevante bewijs is volgens de EBRO-methode gegradeerd, aan de hand van de indeling in tabel 1.
Daarnaast is voor de beoordeling van uitgangsvraag 12 gekozen voor de GRADE methodiek (Grading of Recommendations Assessment, Development and Evaluation), waarbij per uitkomstmaat het beschikbare bewijs is ‘gepooled’ en beoordeeld op de kwaliteit van het bewijs, zie tabel 2. De toepassing van GRADE voor deze richtlijn was lastig omdat er alleen observationele studies zijn, geen vergelijkende studies, en de studies erg heterogeen zijn qua patiënt- en naevuskenmerken. Deze methodiek is daarom alleen toegepast bij behandelmodaliteiten waarbij ‘pooling’ van resultaten volgens de werkgroep mogelijk was.
Tabel 1: EBRO methode; A. niveau van conclusies volgens EBRO; B. Indeling van methodologische kwaliteit van individuele studies
A.
|
niveau |
Conclusie gebaseerd op |
|
1 |
Onderzoek van niveau A1 of tenminste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A2 |
|
2 |
1 onderzoek van niveau A2 of tenminste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
1 onderzoek van niveau B of C |
|
4 |
Mening van deskundigen |
B.
|
Kwaliteit |
Interventie |
Diagnostisch accuratesse onderzoek |
Schade / bijwerkingen*, etiologie, prognose |
|
A1 |
Systematische review van tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van A2-niveau |
||
|
A2 |
Gerandomiseerd dubbelblind vergelijkend klinisch onderzoek van goede kwaliteit van voldoende omvang |
Onderzoek ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
Prospectief cohortonderzoek van voldoende omvang en follow-up, waarbij adequaat gecontroleerd is voor ‘confounding’ en selectieve follow-up voldoende is uitgesloten. |
|
B |
Vergelijkend onderzoek, maar niet met alle kenmerken als genoemd onder A2 (hieronder valt ook patiënt-controle onderzoek, cohortonderzoek) |
Onderzoek ten opzichte van een referentietest, maar niet met alle kenmerken die onder A2 zijn genoemd |
Prospectief cohortonderzoek, maar niet met alle kenmerken als genoemd onder A2 of retrospectief cohortonderzoek of patiënt-controle onderzoek |
|
C |
Niet-vergelijkend onderzoek |
||
|
D |
Mening van deskundigen |
||
* Deze classificatie is alleen van toepassing in situaties waarin om ethische of andere redenen gecontroleerde trials niet mogelijk zijn. Zijn die wel mogelijk dan geldt de classificatie voor interventies.
Tabel 2: GRADE methode; A. niveau van bewijs volgens GRADE; C. wijze van beoordelen niveau van bewijs per uitkomstmaat
A.
|
GRADE Working Group grades of quality of evidence |
|
|
High |
We are very confident that the true effect lies close to that of the estimate of the effect |
|
Moderate |
We are moderately confident in the effect estimate: The true effect is likely to be close to the estimate of the effect, but there is a possibility that it is substantially different |
|
Low |
Our confidence in the effect estimate is limited: The true effect may be substantially different from the estimate of the effect |
|
Very low |
We have very little confidence in the effect estimate: The true effect is likely to be substantially different from the estimate of effect |
B.
|
Startpunt van beoordelen kwaliteit van bewijs |
|
|
RCT’s |
Beginnen als ‘high quality’ |
|
Observationele studies |
Beginnen als ‘low quality’ |
|
Per uitkomstmaat over de studies heen evt quality of evidence één of twee niveaus downgraden (1-5) of upgraden (6-8) |
|
|
1. |
risk of bias |
|
2. |
inconsistency |
|
3. |
indirectness |
|
4. |
imprecision |
|
5. |
publication bias |
|
6. |
large effect |
|
7. |
plausible confounding |
|
8. |
dose response gradient |
Totstandkoming van de aanbevelingen
Voor het komen tot een aanbeveling zijn er naast het wetenschappelijke bewijs vaak andere aspecten van belang, bijvoorbeeld: patiëntvoorkeuren, beschikbaarheid van speciale technieken of expertise, organisatorische aspecten, maatschappelijke consequenties of kosten. Deze aspecten worden besproken na de conclusie(s) onder ‘overige overwegingen’. Hierin wordt de conclusie op basis van de literatuur geplaatst in de context van de dagelijkse praktijk en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties. De uiteindelijk geformuleerde aanbeveling is het resultaat van het beschikbare bewijs in combinatie met deze overwegingen vanuit expert opinion. Het volgen van deze procedure en het opstellen van de richtlijn in dit format heeft als doel de transparantie van de richtlijn te verhogen.
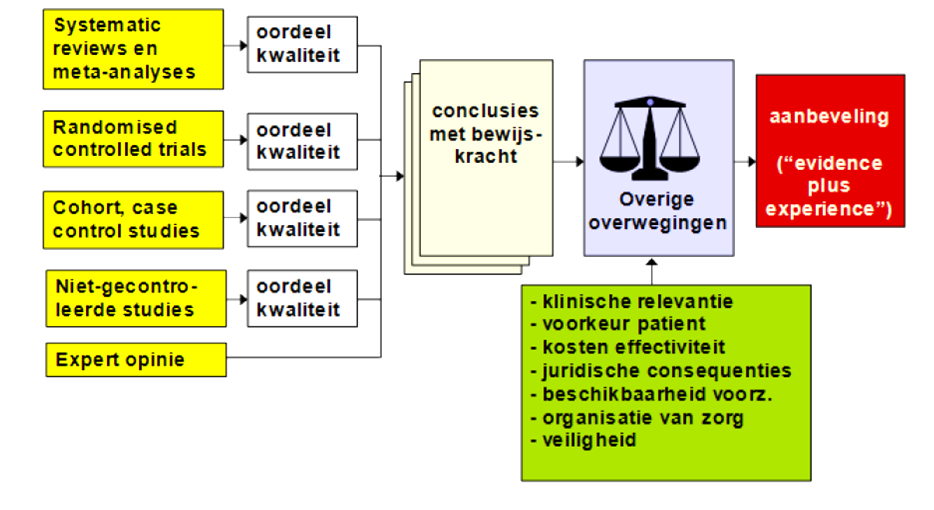
Fig. 2: Schematisch weergave methodiek van evidence-based richtlijnontwikkeling
Innovatie
Het veld van de congenitale melanocytaire naevi is in beweging. Enerzijds wordt langzamerhand de moleculaire signatuur van CMN ontrafeld, hetgeen belangrijke nieuwe aanknopingspunten geeft voor nieuwe (genetische) diagnostiek en (niet-chirurgische) therapieën. Daarnaast is er in de loop der jaren een verschuiving opgetreden van invasief en agressief behandelen om zoveel mogelijk naevusweefsel te verwijderen in het kader van een vermeend hoog melanoomrisico, naar minder agressief en meer oppervlakkig of partieel ingrijpen met meer oog voor het cosmetisch resultaat. Verder is er in het verleden veelal slechts retrospectief onderzoek verricht met een hoog risico op bias. Er zijn inmiddels enkele prospectieve studies verschenen over melanoomrisico, maar nog niet over therapie in CMN.
Advies voor onderzoek
Over de gehele linie ontbreekt het aan goed uitgevoerde studies op het gebied van CMN. Veelal zijn er alleen caseseries en casereports verschenen, met een hoog risico op bias. Dit is ergens inherent aan het onderwerp, waarbij met name grotere CMN zeldzaam zijn, en CMN daarnaast nog in grote mate interindividueel verschillen. Met name op het gebied van therapieën ontbreekt het aan betrouwbaar onderzoek. Bijna alle auteurs meten verschillende of niet-gevalideerde uitkomstmaten, en ‘patient-important outcomes’, zoals kwaliteit van leven, patiënttevredenheid maar ook veiligheid, worden vrijwel niet onderzocht. In de studies over melanoomrisico ontbreekt het aan studies in volwassen patiënten en kleinere CMN, en studies met langere follow-up duur (>10 jaar). Dit geldt ook voor studies naar het risico op NCM, hierbij zijn tevens veel verschillende definities voor NCM gehanteerd.
Onderzoek naar CMN zou moeten bestaan uit prospectief onderzoek, met nauwkeurige en gestandaardiseerde registratie van patiëntkenmerken, en gevalideerde en gestandaardiseerde registratie van uitkomsten, over een lange tijd. Hierbij moet er ten aanzien van behandeling ook meer aandacht komen voor voor de patiënt belangrijke uitkomsten en veiligheid. Op het gebied van melanoomrisico is dit internationaal reeds opgepakt, door het in diverse landen opzetten van (nationale) prospectieve registries. De werkgroep is van plan op korte termijn een dergelijke registry op te zetten in Nederland (via huidhuis.nl vanuit de NVDV), waarbij ook de uitkomsten van therapieën zullen worden meegenomen. Later zal deze gekoppeld worden aan internationale registries.
Daarnaast is meer en beter onderzoek nodig naar diagnostische modaliteiten bij CMN, zoals dermatoscopie en MRI, en diagnostische technieken om melanoom in CMN te ontdekken en te kunnen onderscheiden van benigne naevusweefsel of proliferaties.
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften, maar wetenschappelijk onderbouwde en breed gedragen inzichten en aanbevelingen waaraan zorgverleners zouden moeten voldoen om kwalitatief goede zorg te verlenen. Aangezien richtlijnen uitgaan van ‘gemiddelde patiënten’, kunnen zorgverleners in individuele gevallen zo nodig afwijken van de aanbevelingen in de richtlijn. Afwijken van richtlijnen is, als de situatie van de patiënt dat vereist, soms zelfs noodzakelijk. Wanneer bewust van de richtlijn wordt afgeweken, moet dit echter beargumenteerd, gedocumenteerd en waar nodig in overleg met de patiënt worden gedaan.
Zoekverantwoording
Search richtlijn overkoepelend
Zoekstrategie voluit:
(nevi OR naevi OR nevus OR naevus OR mole OR moles OR birthmark* OR “Nevus”[MESH] OR “Nevus, pigmented”[MESH])
AND
((congenita* OR inborn OR hereditary OR newborn OR “congenital”[Subheading]) OR
(giant OR garment OR Tierfell OR gigantic OR ‘bathing trunk’))
NOT
connective tissue OR anaemicus OR elasticus OR inelasticus OR depigmentosus OR mucinosis OR lipomatosus OR sebaceus OR blue OR comedonicus OR spindle OR sponge OR woolly OR spilus OR spider OR flammeus OR Jadassohn OR Ota OR Becker OR Sutton OR Unna OR neurofibromatosis OR pancreas* OR placenta
Filters: taal: NL, EN, DU; jaar: vanaf 1987
Gezocht op 22.11.2014: 1934 hits (PubMed)
Tussentijds (2014~2016) op specifieke uitgangsvragen geupdate.
Search fotografie
Zoekstrategie voluit:
("congenital naevus".ti,ab OR "congenital naevi".ti,ab OR "congenital nevus".ti,ab OR "congenital nevi".ti,ab OR "congenital melanocytic naevus".ti,ab OR "congenital melanocytic naevi".ti,ab OR "congenital melanocytic nevus".ti,ab OR "congenital melanocytic nevi".ti,ab OR (("naevus".ti,ab OR "naevi".ti,ab OR "nevus".ti,ab OR "nevi".ti,ab OR "melanocytic naevus".ti,ab OR "melanocytic naevi".ti,ab OR "melanocytic nevus".ti,ab OR "melanocytic nevi".ti,ab) AND congenital*.ti,ab)) AND (Photography/ OR medical photography/ OR Photograph*.ti,ab) AND (english.la OR dutch.la)
Gezocht op 07.05.2014: 44 hits (34 Pubmed, 37 Embase waarvan 10 uniek)
Search dermatoscopie
Zoekstrategie voluit:
("congenital naevus".ti,ab OR "congenital naevi".ti,ab OR "congenital nevus".ti,ab OR "congenital nevi".ti,ab OR "congenital melanocytic naevus".ti,ab OR "congenital melanocytic naevi".ti,ab OR "congenital melanocytic nevus".ti,ab OR "congenital melanocytic nevi".ti,ab OR (("naevus".ti,ab OR "naevi".ti,ab OR "nevus".ti,ab OR "nevi".ti,ab OR "melanocytic naevus".ti,ab OR "melanocytic naevi".ti,ab OR "melanocytic nevus".ti,ab OR "melanocytic nevi".ti,ab) AND congenital*.ti,ab)) AND (Dermoscopy/ OR Dermascopy/ OR dermatosc*.ti,ab) AND (english.la OR dutch.la OR german.la)
Filters: taal: NL, EN, DU (zie searchtermen) en jaar vanaf 1990
Gezocht in mei/juni 2014: 243 hits (Pubmed, Embase) >> na ontdubbeling 171; met reference checking 2 extra artikelen
Search chirurgie
Chirurgische ingrepen (excision, tissue expansion, skin grafting)
((nevus/de AND ('congenital disorder'/de OR congenital:lnk OR (congent* OR unacquir* OR 'not acquired' OR 'non acquired'):ab,ti)) OR 'congenital nevus'/de OR 'pigmented nevus'/de OR 'melanocytic nevus'/de OR (((congenit* OR unacquir* OR 'not acquired' OR 'non acquired' OR pigment* OR melanocyt* OR nevocell* OR naevocell* OR 'nevo cellular' OR 'naevo cellular' OR giant OR gigantic OR medium OR large* OR multiple OR small* OR pilos* OR hair* OR divided) NEAR/3 (nevus OR naevus OR nevi OR naevi OR mole OR moles OR birthmark* OR nævi OR nævus)) OR nevocyt* OR nevomelanocyt* OR naevocyt* OR naevomelanocyt* OR ((nevocell* OR naevocell* OR 'nevo cellular' OR 'naevo cellular') NEAR/3 (lesion* OR laesion*)) OR tierfell* OR (bathing NEXT/1 trunk*) OR (((pigment* NEAR/3 (lesion* OR laesion*))) AND (nevus OR naevus OR nevi OR naevi OR mole OR moles OR birthmark*) AND (melanom* OR pseudomelanom*))):ab,ti) AND (surgery/de OR 'surgical technique'/de OR excision/de OR 'local excision'/de OR surgery:lnk OR 'minor surgery'/de OR 'major surgery'/de OR 'pediatric surgery'/exp OR 'plastic surgery'/exp OR dermatome/de OR 'skin surgery'/exp OR autograft/de OR allograft/de OR transplantation/de OR (surg* OR dermatosurg* OR excis* OR resect* OR remov* OR dermatome* OR shaving OR shave OR shaved OR ((skin OR tissue) NEAR/3 (flap* OR expan* OR stretch* OR transplant* OR replace*)) OR graft* OR autograft* OR allograft* OR reconstruct* OR resurfac*):ab,ti)
Gezocht in juli 2014: 4609 hits na ontdubbelen
|
Embase.com |
3134 |
|
Medline (OvidSP) |
393 |
|
Web-of-science |
304 |
|
Scopus |
618 |
|
PubMed publisher |
35 |
|
Cochrane |
0 |
|
Google scholar |
125 |
|
Total |
4609 |
Curettage, dermabrasie
Uit bovenstaande search kwamen ook artikelen over curettage en dermabrasie naar boven. Met reference checking en een korte search op synoniemen voor ‘congenital n(a)evi, dermbrasion, curettage) is gekeken of de gevonden artikelen voor dit onderwerp compleet waren.
Search lasertherapie
(((nevus[tiab] OR nevi[tiab] OR naevus[tiab] OR naevi[tiab] OR CMNs[tiab] OR SCMN[tiab] OR MCMN[tiab] OR LCMN[tiab] OR LCMNs[tiab] OR GCMN[tiab] OR GCMNs[tiab] OR CNNs[tiab] OR SCNN[tiab] OR MCNN[tiab] OR MCNNs[tiab] OR GCNN[tiab] OR Tierfell*[tiab] OR bathing-trunk*[tiab] OR garment-like[tiab] OR ((CNN[tiab] OR CMN[tiab] OR mole[tiab] OR moles[tiab] OR birthmark*[tiab]) AND (giant[tiab] OR gigantic[tiab] OR medium[tiab] OR large[tiab] OR multiple[tiab] OR pilos*[tiab] OR hairy[tiab] OR melanocytic[tiab] OR naevocytic[tiab] OR nevocytic[tiab] OR naevocell*[tiab] OR nevocell*[tiab] OR naevomelanocytic[tiab] OR nevomelanocytic[tiab] OR congenital*[tiab] OR unacquired[tiab] OR non-acquired[tiab]))) AND (laser[tiab] OR lasers[tiab] OR yttrium[tiab] OR erbium[tiab] OR neodymium[tiab] OR aluminum oxide[tiab] OR QSRL*[tiab] OR QSNYL*[tiab] OR QSND[tiab] OR FDQS*[tiab] OR NMRL*[tiab] OR NM-QS*[tiab] OR ND-QS*[tiab] OR Q-switch*[tiab] OR Qswitch*[tiab] OR YAG*[tiab] OR NDYAG*[tiab] OR ND-YAG*[tiab] OR ERYAG*[tiab] OR ER-YAG*[tiab] OR Neodymi*[tiab] OR Erbium*[tiab] OR Yttrium*[tiab] OR Alexandrit*[tiab] OR UCO2*[tiab] OR UltraPulse[tiab])) NOT ota[ti])
Gezocht in November 2015: 683 hits
|
Medline (OvidSP) |
330 |
|
Embase.com |
554 |
|
Central |
33 |
|
PubMed publisher |
7 |
|
Total (na ondubb.) |
683 |
