Organisatie van zorg bij CMN
Uitgangsvraag
Welke zorg is aanbevolen, door wie en waar?
Aanbeveling
Indeling in “risicoklassen”
De werkgroep heeft o.a. ten aanzien van het risico op complicaties (melanoom, neurocutane melanocytose) een indeling gemaakt in solitaire (één enkele) vs. mulitipele CMN (CMN >20cm PAS met één of meer satellietnaevi of alleen ≥3 middelgrote laesies al dan niet met multipele kleine laesies). Patiënten met multipele CMN hebben uitgebreidere zorg nodig.
Beleid ten aanzien van follow-up
Patiënten met multipele CMN (CMN >20cm PAS met satellietnaevi of ≥3 CMN 1,5-20cm PAS) dienen tenminste jaarlijks te worden gezien in een expertisecentrum. Aanvullende zorg of controles tussendoor kunnen ook dichtbij huis. Patiënten met solitaire CMN kunnen indien geïndiceerd in de periferie gevolgd worden.
Bij alle patiënten met chirurgisch complexe CMN (arbitraire indeling >10cm PAS, maar bij lastige lokalisatie evt kleiner) wordt tenminste éénmalig voorlichting over behandeling in een expertisecentrum geadviseerd.
De expertisecentra zijn bekend bij de patiëntenvereniging Nevus Netwerk Nederland (NNN).
In de zorg voor patiënten met CMN is de dermatoloog veelal de hoofdbehandelaar en adviseert de plastisch chirurg ten aanzien van de behandelopties.
Reguliere follow-up
Aandachtspunten bij de reguliere follow-up (anamnese, lichamelijk onderzoek, classificatie) zijn samengebracht in figuur 2.
Neurologische follow-up
Bij patiënten met multipele CMN wordt 1-2 jaarlijkse neurologische follow-up door een kinderarts-erfelijke aangeboren afwijkingen en/of een kinderneuroloog geadviseerd om de ontwikkeling van het kind goed in de gaten te houden. Bij problemen contacteert de kinderarts de kinderneuroloog.
Standaard follow-up schema
De werkgroep heeft een follow-up schema opgesteld voor de standaard zorg voor de patiënt met CMN per risicoklasse, te vinden in figuur 3 (welk specialisme, in welke frequentie, in expertisecentrum of perifeer).
Onderbouwing
In deze richtlijn wordt beschreven dat het risico op complicaties van CMN en de complexiteit van behandeling afhankelijk zijn van het fenotype. Mede op basis van de literatuur en internationale expert opinion is de werkgroep tot aanbevelingen voor zorg gekomen. Deze worden in deze module uiteengezet. Bij de aanverwante producten is een ‘Spreekkamerprotocol’ te vinden met daarin de belangrijkste punten (schema’s) uit deze module.
Indeling in “risicoklassen”
De werkgroep heeft een indeling gemaakt in groepen patiënten die meer of minder standaard zorg nodig hebben.
Risico op complicaties: het risico op cutaan melanoom lijkt in CMN over alle groottes niet duidelijk verhoogd ten opzichte van de algehele bevolking (<1%). Wel is elke CMN in feite een precursor laesie voor melanoom. De mogelijkheid van betrokkenheid van het centraal zenuwstelsel (neurocutane melanocytose, symptomatische melancoytaire deposities in het CZS) is gelegen in de embryologie: ‘timing’ van de oorzakelijke postzygotische mutatie bepaalt zowel de mogelijkheid van betrokkenheid van het CZS als de uitgebreidheid van het huidfenotype. NCM kan een relatief ‘mild’ beloop hebben, maar er kunnen ook maligne complicaties optreden (progressieve leptomeningeale melanocytose, melanoom in het CZS). Tevens zijn bij CMN zeer sporadisch andere maligne associaties beschreven (bv rhabdomyosarcoom).
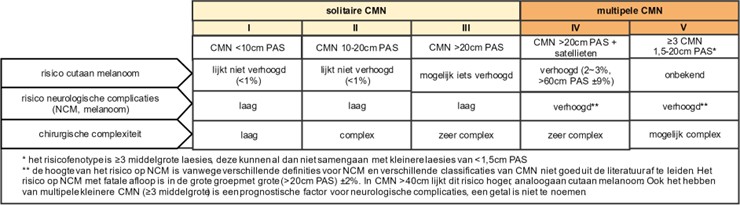
Op basis van de huidige literatuur legt de werkgroep een scheidingslijn voor verhoogd risico op complicaties (melanoom, NCM) bij CMN >20cm PAS met satellietnaevi of ≥3 middelgrote laesies (1,5~20cm PAS) zonder ‘moederlaesie’, al dan niet met multipele kleinere CMN. Hierbij heeft de werkgroep overkoepelend gekozen voor een indeling in solitaire vs multipele CMN, waarbij de patiënten met multipele CMN meer standaard zorg nodig hebben (zie figuur 1.).
Het risico op maligne complicaties (cutaan melanoom, CZS melanoom, progressieve leptomeningeale melanocytose) lijkt met name verhoogd te zijn in grotere, uitgebreidere CMN (reuze CMN >40cm of zelfs >60cm PAS met satellietnaevi of multipele kleinere CMN). Zie de module ‘Risico op melanoom en NCM’ en fig. 1 voor de hoogte van het risico op complicaties en de risicofenotypen.* Een ander afkappunt dan bovenstaande kan echter niet met zekerheid worden gegeven vanwege de verschillende classificaties voor grootte die zijn gehanteerd in de literatuur.
*Bij het inschatten van de hoogte van het complicatierisico moet wel worden opgemerkt dat de follow-up duur van de meeste studies beperkt is (meeste ±5 jaar, enkele 10 jaar) en de geïncludeerde patiënten veelal jong waarbij mogelijke complicaties in volwassenen worden gemist. Dit is van belang in de follow-up van patiënten met CMN: we geven in de richtlijn een leidraad, we kunnen geen absolute risico’s geven.
Chirurgische complexiteit: ook deze speelt een belangrijke rol in de zorg die nodig is voor de patiënt met CMN. De werkgroep heeft op basis van de grootte een arbitraire indeling gemaakt in chirurgische complexiteit, op individuele basis (o.a. lokalisatie) kan een patiënt in categorie opschuiven.
Deze twee tezamen (risico op complicaties en chirurgische complexiteit) komt de werkgroep tot de volgende indeling in risicoklassen (zie figuur 1.):
Figuur 1. Indeling fenotypen CMN in risicoklassen ten behoeve van voorlichting en standaard zorg
Behandeladvies
Voorheen was de beleving veelal: als mogelijk verwijder je de CMN vanwege het onzekere risico op maligniteit. Het risico op melanoom lijkt nu (op basis van de huidige literatuur) lager dan voorheen gedacht, bovendien lijkt melanoom vooral te ontstaan in grotere CMN (>40cm P.A.S.). Het verwijderen van grote CMN is complex, en indien puur uit profylactisch oogpunt te betwijfelen omdat je niet weet waar het melanoom gaat ontstaan (en ook extracutaan kan ontstaan). Bovendien zijn grotere CMN soms alleen te verwijderen met oppervlakkige technieken, waarbij niet alle naevuscellen kunnen worden verwijderd en het risico op maligne ontaarding blijft bestaan. De indicatie voor ingrijpen verschuift daarom nu meer naar (ook) cosmetisch.
Het advies van de werkgroep is daarom in principe géén profylactische excisie, wél excideren als*:
- Verdacht (gebied)
- Moeilijk te vervolgen
- Gevoel ‘moet eruit’
- Cosmetische indicatie”
Bovenstaand advies geldt voor alle ‘risicoklassen’.
Beleid ten aanzien van follow-up
Zorg in expertisecentra vs. periferie
In hoeverre kan worden volstaan met zorg in de periferie of in het expertisecentrum, is afhankelijk van het fenotype (‘risicoklasse’).
Expertisecentrum
De risicofenotypen van CMN zijn zeldzaam en de literatuur is van slechts matige kwaliteit. De kennis en ervaring omtrent de aandoening zit met name bij de experts (in de expertisecentra). Daarnaast zijn de experts als eerste op de hoogte van nieuwe ontwikkelingen in het veld, en hebben laagdrempelig de mogelijkheid tot contact met internationale collegae.
Tevens is gezien de verscheidene mogelijke manifestaties van de aandoening een multidisciplinaire benadering gewenst (zie tabel 1). Deze disciplines zijn of alle in het expertisecentrum aanwezig, of deze samenwerking kan (gezien het beperkte aantal specialisten in Nederland op dit gebied) transmuraal plaatsvinden. Het is in de zorg voor patiënten met complexere CMN daarbij van belang dat een hoofdbehandelaar wordt aangesteld. Deze inventariseert en onderzoekt of er zorgen zijn, zet zo nodig aanvullend onderzoek in, consulteert eventueel andere specialisten en/of regelt aanvullende zorg indien gewenst. In de praktijk zal de hoofdbehandelaar veelal de dermatoloog zijn.
De werkgroep is op grond van bovenstaande van mening dat patiënten met een risicofenotype voor complicaties (multipele CMN, IV+V) voor zorg blijvend in een expertisecentrum thuishoren, en tenminste jaarlijks in het expertisecentrum dienen te worden gezien voor algehele follow-up.
De werkgroep is daarnaast van mening dat alle patiënten met een chirurgisch complexe CMN (risicoklassen II-V) op jonge leeftijd tenminste éénmalig in een expertisecentrum voorlichting dienen te krijgen over de mogelijke behandelopties door de plastisch chirurg. Expertise t.a.v. lasertherapie bevindt zich vaker bij dermatologen. In een expertisecentrum waarin wordt gewerkt met een multidisciplinair team is gewaarborgd dat alle mogelijk opties worden meegewogen.
De expertisecentra zijn bekend bij de patiëntenvereniging NNN.
Tabel 1. Multidisciplinair team mogelijk betrokken bij zorg CMN en NCM*
|
(kinder)dermatoloog |
|
(kinder)plastisch chirurg |
|
kinderarts |
|
(kinder)neuroloog |
|
(kinder)oncoloog |
|
patholoog |
|
radioloog |
|
psycholoog |
|
huidtherapeut |
* in hoeverre deze disciplines betrokken zijn bij de zorg is mede afhankelijk van het fenotype van de CMN en of er complicaties optreden.
Perifeer centrum
De standaard (dermatologische) zorg voor patiënten met solitaire CMN (risicofenotypen I, II, III) kan in de periferie plaatsvinden.
Naast de jaarlijkse controle in het expertisecentrum, kan voor een deel van de patiënten met multipele CMN (IV, V) tevens reguliere zorg en frequentere controles tussendoor door clinici dichterbij huis plaatsvinden. Voor patiënten/ouders kan het prettig zijn ook een aanspreekpunt dichtbij te hebben. Dit geldt voor een dermatoloog en mogelijk kinderarts, maar ook voor de mogelijke begeleiding door psycholoog of huidtherapeut. Bij zorgen of vragen omtrent de patiënt dient wel de hoofdbehandelaar in het expertisecentrum (transmuraal) te worden gecontacteerd.
Reguliere follow-up
Het belangrijkste bij de follow-up is medisch gezien eventuele veranderingen op het spoor te komen die zouden kunnen wijzen op cutane of neurologische complicaties, en daarnaast aandacht te hebben voor de patiënt in zijn geheel (o.a. psychologische consequenties, andere zorgen/vragen). Activiteiten tijdens reguliere follow-up van CMN van alle groottes zijn samengebracht in figuur 2.
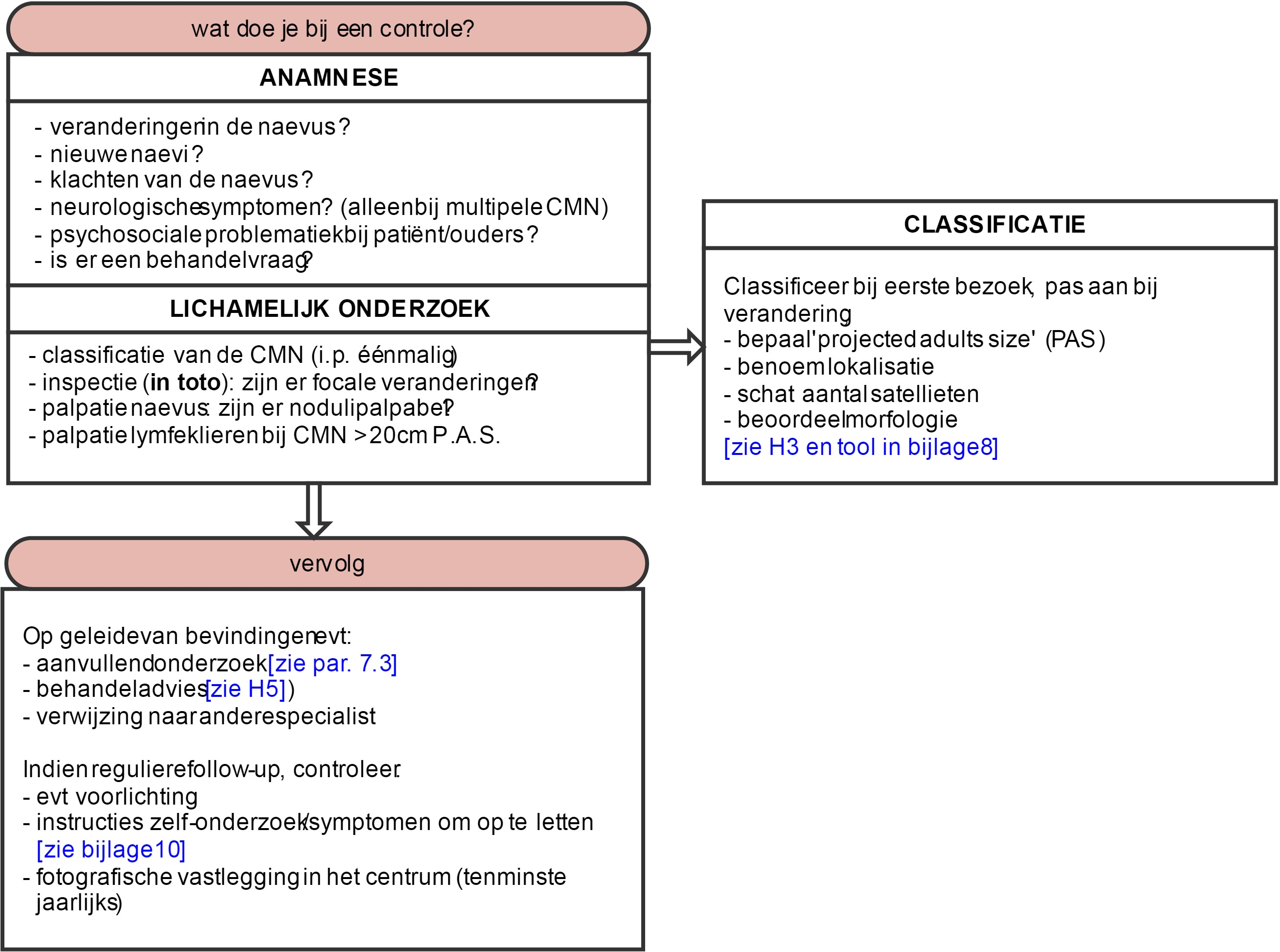 Figuur 2. Handelingen bij follow-up van CMN
Figuur 2. Handelingen bij follow-up van CMN
Neurologische follow-up
Het verrichten van een jaarlijkse screenende MRI bij alle patiënten met een risicofenotype voor neurologische complicaties wordt niet aanbevolen (zie de module ‘MRI hersenen/ruggenmerg bij CMN en neurologische follow-up’). Indien er echter aanwijzingen zijn voor neurologische manifestaties, zoals verhoogde intracraniële druk (hoofdpijn, braken, bewustzijnsstoornissen), focale afwijkingen (zoals epilepsie, hersenzenuwuitval) of tekenen van ruggenmergcompressie dient een MRI inclusief series met contrasttoediening te worden verricht. Bij bovenstaande (alarm)symptomen bestaat er een spoedindicatie voor MRI. Ook bij andere onverklaarbare symptomen, zoals een achterstand in de ontwikkeling etc. bestaat er een indicatie voor MRI (niet spoed). De MRI kan overlegd worden met een centrum met expertise.
Om eventuele neurologische complicaties tijdig op het spoor te komen acht de werkgroep het van belang dat kinderen met een verhoogd risico op NCM (multipele CMN, risicoklassen IV+V) routinematig (1-2 maal per jaar) op neurologische ontwikkeling en symptomen worden onderzocht. NCM kan zich in eerste instantie met zeer subtiele afwijkingen openbaren. De werkgroep is van mening dat follow-up van de ontwikkeling goed op zijn plaats is bij de perifere kinderarts. Bij de kinderarts is nauwkeurige follow-up gewaarborgd, de perifere kinderarts bevindt zich dicht bij huis en kan laagdrempelig door ouders worden gecontacteerd. Bij zorgen neemt de kinderarts contact op met de kinderneuroloog in het expertisecentrum.
Standaard follow-up schema
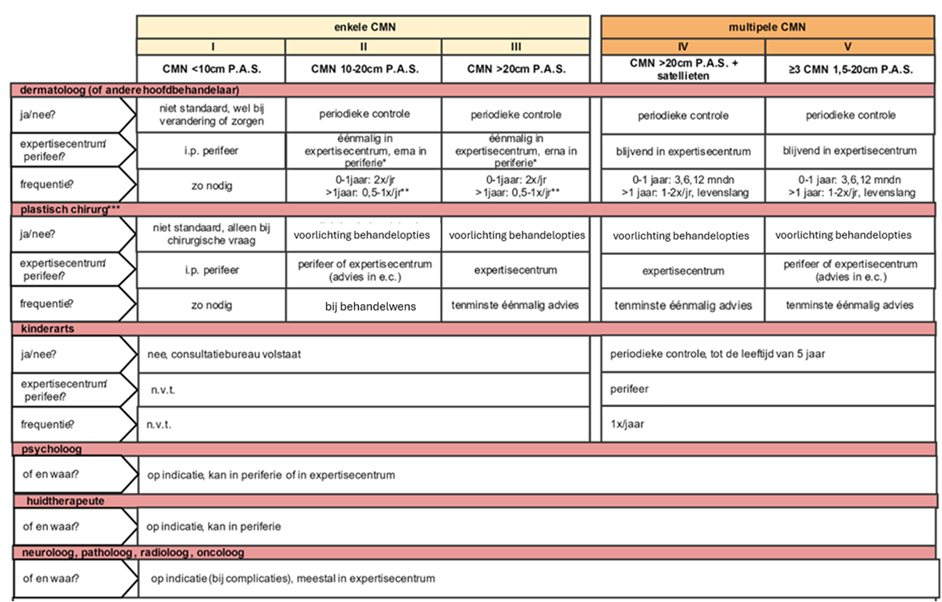
De werkgroep heeft onderstaande leidraad voor een follow-up schema opgesteld (figuur 3).
Hierin zijn de overwegingen uit de vorige paragrafen samengebracht.
Figuur 3. Standaard follow-up schema bij CMN
* Tenzij lastige lokalisatie/aspect, dan eventueel centrum met expertise
** Periodieke controle in principe niet altijd nodig in risicoklasse II, advies over follow-up na eenmalige beoordeling door het centrum met expertise afhankelijk van klinisch beeld. Volledige voorlichting geven zoals in de module ‘voorlichting en zelfmanagement’. Bij verandering, wanneer er mogelijk aanvullende diagnostiek gewenst is of behandelwens: controle in centrum met expertise.
***Indien een CMN zich op een lastige lokalisatie bevindt (zoals het gelaat, behaarde hoofd, genitaalstreek, etc.) schuift een patiënt een klasse omhoog qua chirurgische complexiteit
In dit schema wordt naast voor patiënten met multipele CMN tevens standaard dermatologische controle aanbevolen voor patiënten met solitaire CMN van >10cm PAS, hoewel op basis van de huidige literatuur het risico op melanoom in deze groep niet duidelijk verhoogd lijkt ten opzichte van de algehele bevolking. Binnen de groep met solitaire CMN kan de clinicus het van het klinisch beeld laten afhangen of reguliere follow-up nodig is, of dat goede instructie voor zelf-onderzoek volstaat. De werkgroep heeft voor in principe periodieke follow-up gekozen om reden dat er toch een risico bestaat op melanoom in solitaire CMN, en CMN van deze groottes (>10cm PAS) door hun morfologie vaak lastiger te vervolgen zijn. Bovendien kan er op deze manier worden ingespeeld op de veelvoorkomende zorgen bij patiënten/ouders. De werkgroep geeft een leidraad (zie schema), goed gemotiveerd mag van dit schema worden afgeweken.
Er wordt geadviseerd om patiënten minimaal één keer naar een centrum met expertise te verwijzen voor een eerste consult (vanaf risicogroep II). Patiënten dienen bij voorkeur zo snel mogelijk doorverwezen te worden (binnen een maand na geboorte). Het eerste consult dient bij voorkeur voor de leeftijd van 3 maanden plaats te vinden.
Beleid bij afwijkende bevindingen
Indien er zorgwekkende bevindingen zijn die mogelijk zouden kunnen wijzen op complicaties van CMN (melanoom, neurocutane melanocytose), verricht men aanvullend onderzoek zoals samengebracht in figuur 4. Het vervolg is op geleide van de bevindingen. Indien het gaat om mogelijke maligne complicaties is spoed geboden bij het inzetten van aanvullend onderzoek (binnen 2 weken).
Voor de routing in de beoordeling van histopathologisch materiaal wordt verwezen naar de module ‘Follow-up van CMN’. Indien na aanvullend onderzoek cutaan melanoom wordt gevonden geldt de landelijke richtlijn melanoom voor het verdere beleid (richtlijn melanoom 2024). De richtlijn melanoom richt zich niet specifiek op melanomen bij kinderen, daar is op dit moment geen aparte evidence voor. Het is van belang dat kinderen met een melanoom in CMN in een expertisecentrum voor melanomen (voor kinderen) terechtkomen met kennis van CMN voor uitgebreide follow-up. Ook patiënten met een melanoom in grotere CMN (alle leeftijden) horen in een expertisecentrum thuis met kennis van CMN en melanoom, deze patiënten zijn als het goed is reeds in zorg in een expertisecentrum voor CMN.
Indien er neurologische symptomen zijn en er afwijkingen worden gevonden bij MRI-onderzoek stelt de (kinder)neuroloog in een expertisecentrum het vervolgbeleid op. Ook indien géén afwijkingen worden gezien op de MRI is bij duidelijke neurologische symptomen strikte controle in een (kinder)neurologisch centrum van belang in verband met (onverklaarde) gevonden klinische afwijkingen.
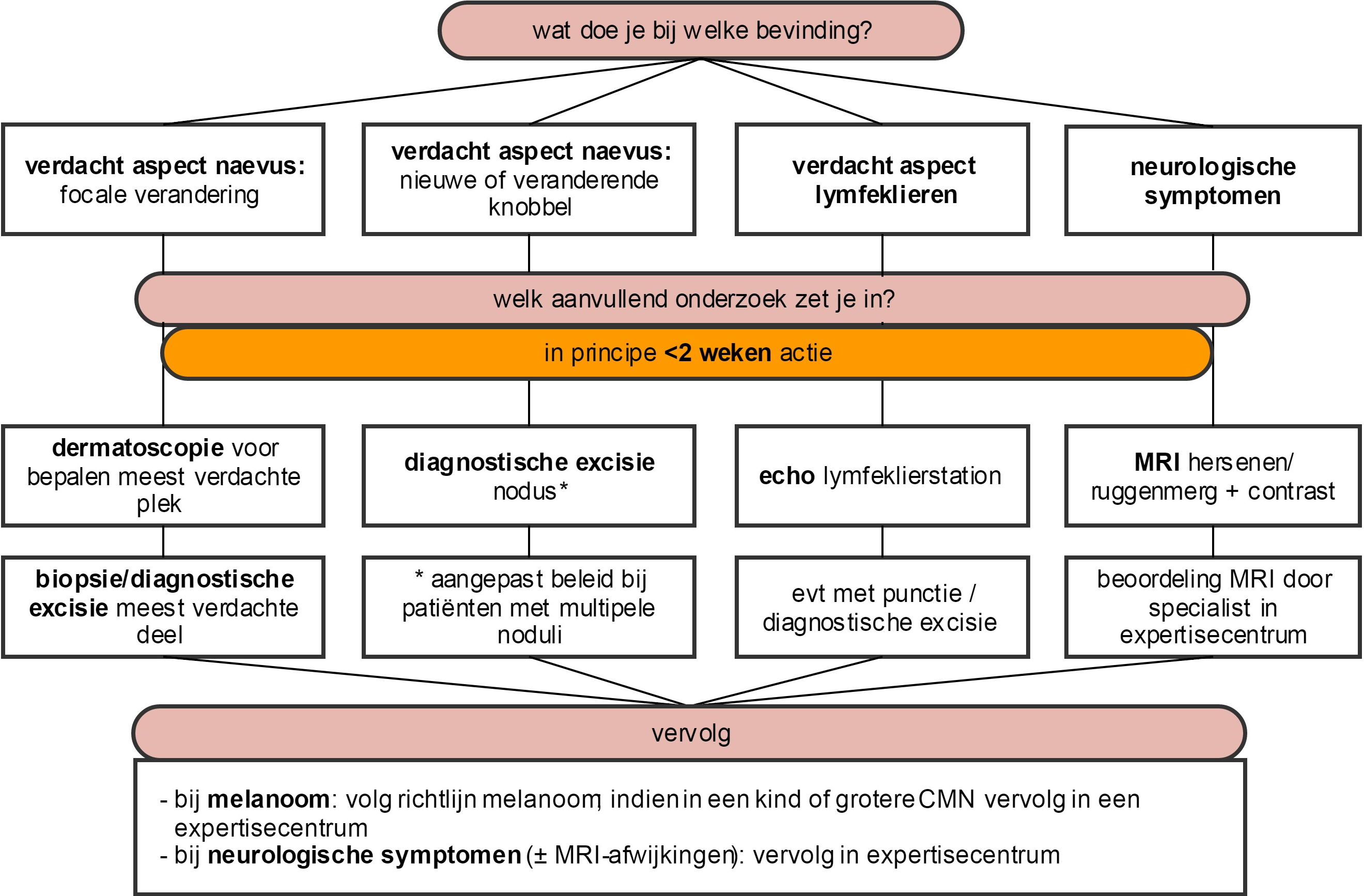
Figuur 4. Beleid bij afwijkende bevindingen tijdens follow-up van CMN
Samenwerking met eerste lijn
Voor de professionals in de 0e en 1e lijn geldt dat zij een signalerende, doorverwijzende en ondersteunende rol hebben.
Voor de 0e lijn geldt dat doorverwezen wordt wanneer de moedervlek groter dan een handpalm van het kind is (±10cm PAS), of wanneer een kleinere moedervlek een onrustig aspect heeft, klachten geeft of wanneer er een positieve familie-anamnese is voor melanoom (JGZ richtlijn Huid, 2012). Praktische handvatten voor de huisartsgeneeskundige behandeling en begeleiding van de patiënt en zijn/haar omgeving zijn samengebracht in de huisartsenbrochure over CMN (www.nhg.org/thema/zeldzameziekten/Congenitalemelanocytairenaevi), ontwikkeld door de NHG in samenwerking met NNN, de VSOP en de NVDV. Voor het doorverwijsbeleid naar de 2e lijn wordt verwezen naar figuur 3. in deze richtlijn.
In de brochure vindt u praktische handvatten voor de huisartsgeneeskundige behandeling en begeleiding van de patiënt en zijn/haar naasten. Het heeft de voorkeur dat de coördinatie in overleg met een gespecialiseerde behandelaar en patiënt afgestemd wordt op de behoefte van die patiënt. In deze brochure en bij de patiëntenvereniging NNN zijn de adressen van gespecialiseerde behandelcentra te vinden.
Bij patiënten met een congenitale naevus die intensievere begeleiding nodig hebben kan de huisarts een belangrijke ondersteunende rol vervullen samen met de specialisten.
Nationale werkgroep CMN
De multidisciplinaire richtlijnwerkgroep CMN blijft actief als werkgroep ook na het afronden van de richtlijn, met naast de huidige werkgroepleden toevoeging van andere experts in Nederland op het gebied van CMN. De werkgroep heeft tevens contacten het een internationaal netwerk van experts binnen en buiten de European Reference Network SKIN. Deze nieuwe, meer permanente werkgroep zal zich blijven buigen over vraagstukken omtrent CMN. Bij problematiek rondom patiënten met CMN kunnen leden van de werkgroep laagdrempelig worden benaderd.
Vanwege de matige kwaliteit van de literatuur is het verrichten van grote prospectieve studies van belang, om meer betrouwbaardere uitspraken te kunnen doen over de hoogte van het risico op complicaties, het natuurlijk beloop van CMN en de resultaten van therapie. De richtlijnwerkgroep werkt aan het opzetten van een (inter)nationale registry via de ERN-SKIN voor patiënten met CMN. De registry is te vinden zijn via www.huidhuis.nl/huidaandoening/moedervlek-aangeboren. Tevens is de richtlijn ondergebracht in huidhuis.nl.
Actuele ontwikkelingen CMN/NCM
De recente ontdekkingen ten aanzien van de pathofysiologie van CMN veranderen langzaam aan het beeld hoe we naar CMN kijken (zie ook de module ‘Achtergrond van CMN’), we zitten nu in feite middenin dat proces.
Vanwege het risico op extracutane complicaties hebben Kinsler et al. de term CMN syndroom geïntroduceerd voor patiënten met multipele CMN. Vooralsnog denken we dan voornamelijk aan de combinatie van een cutane naevus met mogelijke betrokkenheid van het centraal zenuwstelsel, maar mogelijk zijn ook andere organen/systemen aangedaan die ook neuroectodermaal van oorsprong zijn (Waelchli, 2015; Kinsler, 2012).
De bevinding dat een postzygotische somatische mutatie in NRAS of BRAF (MAPK pathway) aanleiding kan geven tot CMN én NCM én melanoom, en identieke mutaties worden gevonden in de aangedane weefsels in eenzelfde patiënt, geeft een aangrijpingspunt voor therapie.
Ten eerste zouden MEK- en BRAF-remmers kunnen worden ingezet in de behandeling van melanoom in CMN. Voor melanomen bij volwassenen is deze ‘targeted therapy’ recent geregistreerd. Vanwege het ontwikkelen van resistentie lijkt de effectduur van deze middelen beperkt (onderzocht in volwassenen zonder CMN). In CMN is echter onvoldoende ervaring om hier iets over te kunnen zeggen, er wordt gesuggereerd dat de werking mogelijk iets anders (beter) is in CMN patiënten omdat in melanomen in CMN minder genetische veranderingen worden aangetroffen (Pawlikowksi, 2015).
Verder zou theoretisch remming van NRAS/BRAF mogelijk progressieve leptomeningeale melanocytose in patiënten met CMN kunnen remmen. Recent is dit in Nederland geprobeerd met MEK162 op ‘compassionate use’ basis in een kind (Küsters-Vandevelde, 2014). Dit patiëntje overleed 5 dagen na start van de MEK-remmer, maar op weefsel verkregen bij obductie werd op eiwit/biomarker niveau wel een effect gezien. MEK-remming zou daarmee een belangrijk therapeuticum kunnen zijn voor progressieve leptomeningeale melanocytose met slechte prognose waar nu geen therapie voor voorhanden is.
Op het moment van verschijnen van de richtlijn zijn deze middelen (MEK-remmer, BRAF-remmer) nog niet geregistreerd voor melanoom in kinderen, en nog niet geregistreerd voor behandeling van NCM, maar wel kan worden geprobeerd deze middelen op ‘compassionate use’ basis of in trialverband te verkrijgen. Bij de behandeling van melanomen in CMN moet verder wel ook worden gedacht aan de mogelijkheid van andere therapieën (zoals immuunmodulerende therapie).
Het veld is enorm in beweging met name op moleculair/genetisch gebied, hetgeen inzicht geeft in prognostische factoren, en aanleiding tot betere diagnostiek en behandeling. Indien er op basis van nieuwe inzichten en ontwikkelingen essentiële wijzingen nodig zijn in follow-up en beleid bij CMN patiënten zal de richtlijn hierop (modulair) worden herzien.
- Nederlandse Melanoom Werkgroep (NMW), Integraal Kankercentrum Nederland (IKNL). Evidence-based richtlijn melanoom, versie 2.0. Datum goedkeuring 13.08.2012
- T&O, GGD. JGZ-richtlijn huidafwijkingen. JGZ Tijdschrift voor jeugdgezondheidszorg, June 2013, Volume 45, Issue 3, pp 55-56
- Kinsler V, Shaw AC, Merks JH, Hennekam RC. The face in congenital melanocytic nevus syndrome. Am J Med Genet A. 2012;158A(5):1014-9.
- Kusters-Vandevelde HV, Willemsen AE, Groenen PJ, Kusters B, Lammens M, Wesseling P, et al. Experimental treatment of NRAS-mutated neurocutaneous melanocytosis with MEK162, a MEK-inhibitor. Acta Neuropathol Commun. 2014;2:41.
- Pawlikowski JS, Brock C, Chen SC, Al-Olabi L, Nixon C, McGregor F, et al. Acute Inhibition of MEK Suppresses Congenital Melanocytic Nevus Syndrome in a Murine Model Driven by Activated NRAS and Wnt Signaling. J Invest Dermatol. 2015;135(11):2902.
- Waelchli R, Williams J, Cole T, Dattani M, Hindmarsh P, Kennedy H, et al. Growth and hormone profiling in children with congenital melanocytic naevi. Br J Dermatol. 2015;173(6):1471-8.
Beoordelingsdatum en geldigheid
Publicatiedatum : 03-11-1111
Beoordeeld op geldigheid : 17-11-2017
Een richtlijn heeft alleen zeggingskracht als op continue basis onderhoud plaatsvindt, op grond van systematische monitoring van zowel de medisch wetenschappelijke literatuur als praktijkgegevens en door gebruikers van de richtlijn aangeleverde commentaren. Voor deze richtlijn is afgesproken één keer per jaar de literatuur te evalueren om nieuwe ontwikkelingen te volgen. Bij essentiële ontwikkelingen kan besloten worden om een gehele richtlijnwerkgroep bij elkaar te roepen en tussentijdse elektronische amendementen te maken en deze onder de verschillende beroepsgroepen te verspreiden. Om de richtlijn ‘levend’ te houden is modulaire herziening mogelijk, waarbij slechts een deel of delen van de richtlijn kunnen worden gereviseerd.
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Deze richtlijn is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering in de begeleiding van patiënten met congenitale melanocytaire naevi (CMN) en hun directe omgeving. De richtlijn berust op de resultaten van wetenschappelijk onderzoek en aansluitende meningsvorming, door experts, gericht op het vaststellen van goed medisch handelen. De financiering van deze richtlijn is tot stand gekomen met gelden die de NVDV uit zijn SKMS-programma heeft vrijgemaakt.
Doelgroep
De richtlijn is bestemd voor leden van de medische en paramedische beroepsgroepen, waartoe tenminste behoren: dermatologen, plastisch chirurgen, pathologen, kinderartsen, neurologen, huisartsen, verpleegkundigen en huidtherapeuten. Tevens is in een samenwerking tussen patiëntenvereniging NNN en de VSOP een huisartsbrochure ontwikkeld.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn werd een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordiging van de bij CMN betrokken disciplines. Bij het samenstellen van de werkgroep is getracht rekening te houden met de geografische spreiding van de werkgroepleden en met een evenredige vertegenwoordiging van academische en niet-academische werkgroepleden. De werkgroepleden hebben onafhankelijk gehandeld en geen enkel werkgroeplid ontving gunsten met het doel de richtlijn te beïnvloeden.
|
Werkgroepleden |
Vereniging |
|
Prof.dr. Suzanne Pasmans (voorzitter) |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Drs. Céline Eggen (secretaris) |
Promovendus kinderdermatologie Erasmus MC (NVDV)
|
|
Prof.dr. Wilma Bergman |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Nicole Kukutsch |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Albert Wolkerstorfer |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Simone Stadhouders-Keet |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Marianne Crijns |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Drs. Annelies Lommerts
|
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Prof.dr. Chantal van der Horst |
Nederlandse Vereniging voor Plastische Chirurgie (NVPC) |
|
Dr. Corstiaan Breugem |
Nederlandse Vereniging voor Plastische Chirurgie (NVPC) |
|
Prof.dr. Wolter Mooi |
Nederlandse Vereniging voor Pathologie (NVVP) |
|
Dr. Hanneke Rijk-van Gent |
Nederlandse Vereniging voor Kindergeneeskunde (NVK) |
|
Prof.dr. Michèl Willemsen |
Nederlandse Vereniging voor Neurologie (NVN) en Nederlandse Vereniging voor Kinderneurologie (NVKN) |
|
Mw. Anja Ebus |
Verpleegkundigen en Verzorgenden Nederland Verpleegkundig Specialist (V&VN VS) en V&VN Dermatologie. |
|
Mw. Marjolein van Kessel |
Nevus Netwerk Nederland (NNN)
|
Verder hebben aan deze richlijn meegewerkt drs. Joep Wijnand en drs. Michéle Hennekam.
Inbreng patiëntenperspectief
Reeds sinds de start van het richtlijntraject is de patiëntenvereniging Nevus Netwerk Nederland (NNN) zeer betrokken geweest bij de totstandkoming van deze richtlijn, door afvaarding van een bestuurslid in de werkgroep. Zij zijn in deze hoedanigheid tijdens het gehele richtlijntraject betrokken geweest, door actieve participatie tijdens werkgroepvergaderingen, en het aandragen van knelpunten die vanuit patiëntenperspectief van groot belang zijn, evenals het deelgenoot maken van lopende initiatieven in het veld. Nevus Netwerk Nederland heeft ook zijn fiat verleend aan de inhoud van de richtlijn.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de ontwikkeling van de conceptrichtlijn is zoveel mogelijk rekening gehouden met de implementatie van de richtlijn en de daadwerkelijke uitvoerbaarheid van de aanbevelingen. De richtlijn wordt gepubliceerd op de website van de NVDV, de website van de richtlijnen database en wordt tevens verspreid onder alle bij CMN betrokken beroepsgroepen. Ook wordt een samenvatting van de richtlijn gepubliceerd en er zal in verschillende specifieke vaktijdschriften aandacht aan worden besteed. Daarnaast wordt de richtlijn onder de aandacht gebracht via de betrokken patiëntenvereniging. De richtlijn is ondergebracht in huidhuis.nl (vanuit de NVDV) en gekoppeld aan het persoonlijk gezondheidsdossier van Patient1 in huidhuis.nl voor mensen met een huidafwijking en de betrokken professionals.
Werkwijze
De richtlijn congenitale melanocytaire naevi is een geheel nieuwe richtlijn. In de richtlijn melanoom (goedgekeurd op 13.08.2012) wordt reeds verwezen naar de in wording zijnde richtlijn CMN. De richtlijnwerkgroep is opgestart in het najaar van 2011, maar heeft tussendoor enkele malen stil gelegen onder andere vanwege een andere prioritering op de richtlijnagenda van de NVDV.
In de eerste vergadering(en) werden de knelpunten en wensen ten aanzien van het onderwerp CMN geïnventariseerd binnen de werkgroep. De werkgroep formuleerde aan de hand hiervan in de richtlijn vermelde uitgangsvragen. Ook werd aan de start van het traject een enquête uitgezet onder dermatologen en plastisch chirurgen in Nederland om het huidige beleid omtrent CMN te inventariseren. De doelen van deze enquête waren het vastleggen van de uitgangssituatie om tot een richtlijn te komen die aansluit op de werkvloer, en het identificeren van aanvullende knelpunten.
De uitgangsvragen werden op het bureau van de Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) uitgewerkt tot PICO-zoekvragen. Via systematische zoekopdrachten en reference checking is bruikbare literatuur verzameld. De secretaris van de richtlijn en studenten hebben samen met de werkgroepleden de literatuur beoordeeld op inhoud en kwaliteit. Vervolgens zijn er teksten geschreven waarin de beoordeelde literatuur werd verwerkt. Deze teksten, op basis van de evidencetabellen met de verwerkte literatuur, zijn tijdens een tweedaagse vergadering besproken en van nuances en aanbevelingen voorzien. Na verdere discussie binnen de gehele richtlijnwerkgroep is de tekst verder afgestemd.
De uiteindelijke tekst werd in september 2016 aan alle betrokken wetenschappelijke verenigingen aangeboden. Men is in staat gesteld om via websites van de betrokken verenigingen commentaar op de richtlijn te geven. De commentaren zijn in de definitieve versie van de richtlijn verwerkt.
Wetenschappelijke bewijsvoering
De aanbevelingen uit deze richtlijn zijn, voor zover mogelijk, gebaseerd op bewijs uit gepubliceerd wetenschappelijk onderzoek.
Relevante artikelen zijn gezocht via een systematische, oriënterende zoekopdracht in Pubmed, overkoepelend voor het onderwerp congenitale melanocytaire naevi (van 1987 tot november 2014, talen Nederlands, Engels, Frans, Duits). Voor specifieke uitgangsvragen werd nog een aanvullende systematische search verricht met meer specifieke zoektermen voor de desbetreffende vraag, en in aanvullende databases (zoals Embase, CENTRAL, Cochrane library etc). Tevens is voor enkele uitgangsvragen en passages de search meer recent herhaald (2014~2016). Zie ook de zoekstrategie.
De zoekacties zijn met behulp van de PICO-systematiek opgebouwd. Dit houdt in dat voor elke uitgangsvraag een zoekvraag is geformuleerd waarbij zoveel mogelijk de volgende structuur is gehanteerd: Patiënt-Interventie-Controle-Outcome. De zoekvragen hebben de P als gemeenschappelijk onderdeel, de overige onderdelen van de PICO zijn geformuleerd op basis van de uitgangsvraag. Het merendeel van de zoekcriteria is afhankelijk van de uitgangsvraag.
Algemeen werden de volgende zoek- en selectiecriteria opgesteld:
|
Taal |
Engels, Nederlands, Duits, Frans |
|
Populatie |
Congenitale melanocytaire naevi (in alle synoniemen), alle groottes, alle leeftijden (exclusie van verworven melanocytaire naevi, of als niet gespecifieerd was of de naevi congenitaal waren) |
|
level of evidence |
Literatuurselectie volgens piramide van bewijs (EBRO-methode). Vanwege het veelal ontbreken van studies van goede kwaliteit (gerandomiseerd of prospectief) is er niet beperkt op de fundamentele opzet van de studie |
|
grootte van de studies |
Hier is in het algemeen geen limiet aangesteld, omdat voor de meeste uitgangsvragen slechts caseseries met enkele patiënten beschikbaar zijn. Wel zijn bij meerdere uitgangsvragen casereports en caseseries met <5 patiënten geëxcludeerd, omdat deze een nog grotere selectiebias geven en daarmee een mogelijk te vertekend beeld van de werkelijkheid. |
Van de geselecteerde referenties op basis van titel en/of abstract werd de full-text aangevraagd. Op basis van full-text artikelen is vervolgens verder geselecteerd en zijn artikelen zonder informatie over de betreffende uitgangsvraag geëxcludeerd. De overgebleven artikelen zijn full-text beoordeeld op kwaliteit en inhoud.
Tijdens de search werden geen (buitenlandse) richtlijnen over dit onderwerp geïdentificeerd, maar wel enkele relevante en betrouwbare ‘learning articles’, waarin op gedegen wijze relevante literatuur over het onderwerp CMN in zijn totaliteit is samengebracht. Deze artikelen vormen deels de basis voor de enkele richtlijnteksten [Alikhan 2012, Ibrahimi 2012, Viana 2013], aangevuld met andere relevante literatuur.
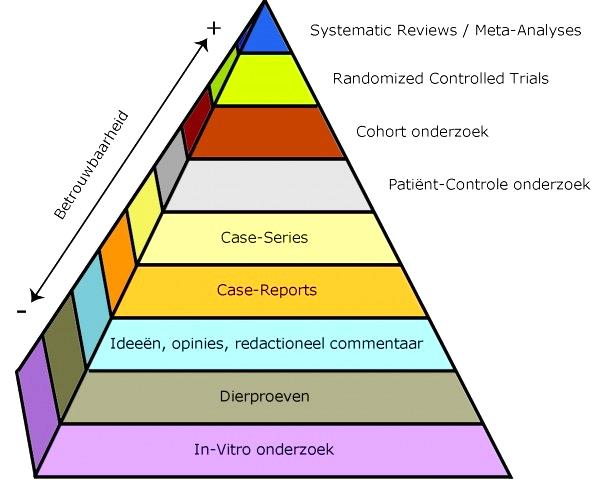
Fig. 1: Piramide van wetenschappelijk bewijs
Methode van literatuurbeoordeling
De richtlijn is ontwikkeld volgens de EBRO-methode (Evidence-based Richtlijn Ontwikkeling). Per deelonderwerp is van de relevante artikelen een ‘evidencetabel’ opgesteld, waarin de literatuur is samengevat en beoordeeld op kwaliteit. De beschrijving en beoordeling van de artikelen staan in de verschillende module onder het kopje ‘wetenschappelijke onderbouwing’, en de literatuur is vervolgens samengevat in ‘conclusies’. De kwaliteit van de artikelen en het niveau van het relevante bewijs is volgens de EBRO-methode gegradeerd, aan de hand van de indeling in tabel 1.
Daarnaast is voor de beoordeling van uitgangsvraag 12 gekozen voor de GRADE methodiek (Grading of Recommendations Assessment, Development and Evaluation), waarbij per uitkomstmaat het beschikbare bewijs is ‘gepooled’ en beoordeeld op de kwaliteit van het bewijs, zie tabel 2. De toepassing van GRADE voor deze richtlijn was lastig omdat er alleen observationele studies zijn, geen vergelijkende studies, en de studies erg heterogeen zijn qua patiënt- en naevuskenmerken. Deze methodiek is daarom alleen toegepast bij behandelmodaliteiten waarbij ‘pooling’ van resultaten volgens de werkgroep mogelijk was.
Tabel 1: EBRO methode; A. niveau van conclusies volgens EBRO; B. Indeling van methodologische kwaliteit van individuele studies
A.
|
niveau |
Conclusie gebaseerd op |
|
1 |
Onderzoek van niveau A1 of tenminste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A2 |
|
2 |
1 onderzoek van niveau A2 of tenminste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
1 onderzoek van niveau B of C |
|
4 |
Mening van deskundigen |
B.
|
Kwaliteit |
Interventie |
Diagnostisch accuratesse onderzoek |
Schade / bijwerkingen*, etiologie, prognose |
|
A1 |
Systematische review van tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van A2-niveau |
||
|
A2 |
Gerandomiseerd dubbelblind vergelijkend klinisch onderzoek van goede kwaliteit van voldoende omvang |
Onderzoek ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
Prospectief cohortonderzoek van voldoende omvang en follow-up, waarbij adequaat gecontroleerd is voor ‘confounding’ en selectieve follow-up voldoende is uitgesloten. |
|
B |
Vergelijkend onderzoek, maar niet met alle kenmerken als genoemd onder A2 (hieronder valt ook patiënt-controle onderzoek, cohortonderzoek) |
Onderzoek ten opzichte van een referentietest, maar niet met alle kenmerken die onder A2 zijn genoemd |
Prospectief cohortonderzoek, maar niet met alle kenmerken als genoemd onder A2 of retrospectief cohortonderzoek of patiënt-controle onderzoek |
|
C |
Niet-vergelijkend onderzoek |
||
|
D |
Mening van deskundigen |
||
* Deze classificatie is alleen van toepassing in situaties waarin om ethische of andere redenen gecontroleerde trials niet mogelijk zijn. Zijn die wel mogelijk dan geldt de classificatie voor interventies.
Tabel 2: GRADE methode; A. niveau van bewijs volgens GRADE; C. wijze van beoordelen niveau van bewijs per uitkomstmaat
A.
|
GRADE Working Group grades of quality of evidence |
|
|
High |
We are very confident that the true effect lies close to that of the estimate of the effect |
|
Moderate |
We are moderately confident in the effect estimate: The true effect is likely to be close to the estimate of the effect, but there is a possibility that it is substantially different |
|
Low |
Our confidence in the effect estimate is limited: The true effect may be substantially different from the estimate of the effect |
|
Very low |
We have very little confidence in the effect estimate: The true effect is likely to be substantially different from the estimate of effect |
B.
|
Startpunt van beoordelen kwaliteit van bewijs |
|
|
RCT’s |
Beginnen als ‘high quality’ |
|
Observationele studies |
Beginnen als ‘low quality’ |
|
Per uitkomstmaat over de studies heen evt quality of evidence één of twee niveaus downgraden (1-5) of upgraden (6-8) |
|
|
1. |
risk of bias |
|
2. |
inconsistency |
|
3. |
indirectness |
|
4. |
imprecision |
|
5. |
publication bias |
|
6. |
large effect |
|
7. |
plausible confounding |
|
8. |
dose response gradient |
Totstandkoming van de aanbevelingen
Voor het komen tot een aanbeveling zijn er naast het wetenschappelijke bewijs vaak andere aspecten van belang, bijvoorbeeld: patiëntvoorkeuren, beschikbaarheid van speciale technieken of expertise, organisatorische aspecten, maatschappelijke consequenties of kosten. Deze aspecten worden besproken na de conclusie(s) onder ‘overige overwegingen’. Hierin wordt de conclusie op basis van de literatuur geplaatst in de context van de dagelijkse praktijk en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties. De uiteindelijk geformuleerde aanbeveling is het resultaat van het beschikbare bewijs in combinatie met deze overwegingen vanuit expert opinion. Het volgen van deze procedure en het opstellen van de richtlijn in dit format heeft als doel de transparantie van de richtlijn te verhogen.
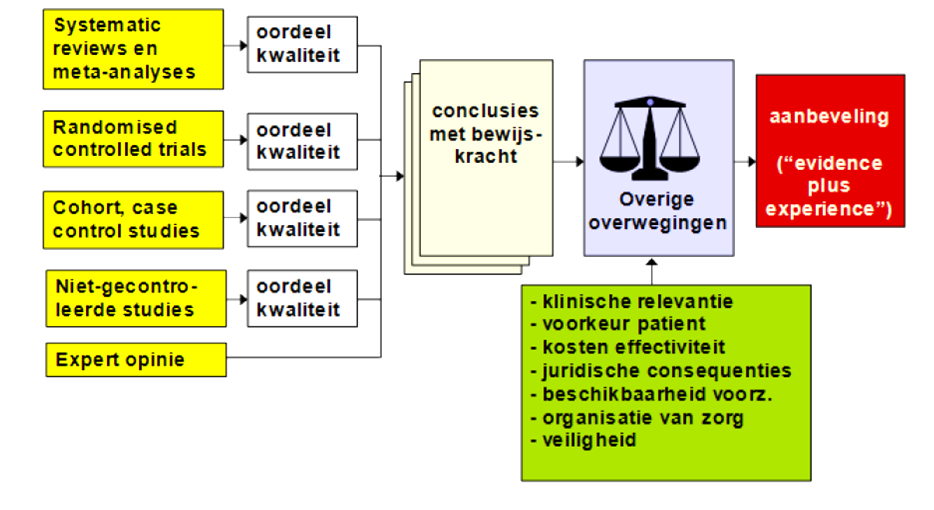
Fig. 2: Schematisch weergave methodiek van evidence-based richtlijnontwikkeling
Innovatie
Het veld van de congenitale melanocytaire naevi is in beweging. Enerzijds wordt langzamerhand de moleculaire signatuur van CMN ontrafeld, hetgeen belangrijke nieuwe aanknopingspunten geeft voor nieuwe (genetische) diagnostiek en (niet-chirurgische) therapieën. Daarnaast is er in de loop der jaren een verschuiving opgetreden van invasief en agressief behandelen om zoveel mogelijk naevusweefsel te verwijderen in het kader van een vermeend hoog melanoomrisico, naar minder agressief en meer oppervlakkig of partieel ingrijpen met meer oog voor het cosmetisch resultaat. Verder is er in het verleden veelal slechts retrospectief onderzoek verricht met een hoog risico op bias. Er zijn inmiddels enkele prospectieve studies verschenen over melanoomrisico, maar nog niet over therapie in CMN.
Advies voor onderzoek
Over de gehele linie ontbreekt het aan goed uitgevoerde studies op het gebied van CMN. Veelal zijn er alleen caseseries en casereports verschenen, met een hoog risico op bias. Dit is ergens inherent aan het onderwerp, waarbij met name grotere CMN zeldzaam zijn, en CMN daarnaast nog in grote mate interindividueel verschillen. Met name op het gebied van therapieën ontbreekt het aan betrouwbaar onderzoek. Bijna alle auteurs meten verschillende of niet-gevalideerde uitkomstmaten, en ‘patient-important outcomes’, zoals kwaliteit van leven, patiënttevredenheid maar ook veiligheid, worden vrijwel niet onderzocht. In de studies over melanoomrisico ontbreekt het aan studies in volwassen patiënten en kleinere CMN, en studies met langere follow-up duur (>10 jaar). Dit geldt ook voor studies naar het risico op NCM, hierbij zijn tevens veel verschillende definities voor NCM gehanteerd.
Onderzoek naar CMN zou moeten bestaan uit prospectief onderzoek, met nauwkeurige en gestandaardiseerde registratie van patiëntkenmerken, en gevalideerde en gestandaardiseerde registratie van uitkomsten, over een lange tijd. Hierbij moet er ten aanzien van behandeling ook meer aandacht komen voor voor de patiënt belangrijke uitkomsten en veiligheid. Op het gebied van melanoomrisico is dit internationaal reeds opgepakt, door het in diverse landen opzetten van (nationale) prospectieve registries. De werkgroep is van plan op korte termijn een dergelijke registry op te zetten in Nederland (via huidhuis.nl vanuit de NVDV), waarbij ook de uitkomsten van therapieën zullen worden meegenomen. Later zal deze gekoppeld worden aan internationale registries.
Daarnaast is meer en beter onderzoek nodig naar diagnostische modaliteiten bij CMN, zoals dermatoscopie en MRI, en diagnostische technieken om melanoom in CMN te ontdekken en te kunnen onderscheiden van benigne naevusweefsel of proliferaties.
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften, maar wetenschappelijk onderbouwde en breed gedragen inzichten en aanbevelingen waaraan zorgverleners zouden moeten voldoen om kwalitatief goede zorg te verlenen. Aangezien richtlijnen uitgaan van ‘gemiddelde patiënten’, kunnen zorgverleners in individuele gevallen zo nodig afwijken van de aanbevelingen in de richtlijn. Afwijken van richtlijnen is, als de situatie van de patiënt dat vereist, soms zelfs noodzakelijk. Wanneer bewust van de richtlijn wordt afgeweken, moet dit echter beargumenteerd, gedocumenteerd en waar nodig in overleg met de patiënt worden gedaan.
Zoekverantwoording
Search richtlijn overkoepelend
Zoekstrategie voluit:
(nevi OR naevi OR nevus OR naevus OR mole OR moles OR birthmark* OR “Nevus”[MESH] OR “Nevus, pigmented”[MESH])
AND
((congenita* OR inborn OR hereditary OR newborn OR “congenital”[Subheading]) OR
(giant OR garment OR Tierfell OR gigantic OR ‘bathing trunk’))
NOT
connective tissue OR anaemicus OR elasticus OR inelasticus OR depigmentosus OR mucinosis OR lipomatosus OR sebaceus OR blue OR comedonicus OR spindle OR sponge OR woolly OR spilus OR spider OR flammeus OR Jadassohn OR Ota OR Becker OR Sutton OR Unna OR neurofibromatosis OR pancreas* OR placenta
Filters: taal: NL, EN, DU; jaar: vanaf 1987
Gezocht op 22.11.2014: 1934 hits (PubMed)
Tussentijds (2014~2016) op specifieke uitgangsvragen geupdate.
Search fotografie
Zoekstrategie voluit:
("congenital naevus".ti,ab OR "congenital naevi".ti,ab OR "congenital nevus".ti,ab OR "congenital nevi".ti,ab OR "congenital melanocytic naevus".ti,ab OR "congenital melanocytic naevi".ti,ab OR "congenital melanocytic nevus".ti,ab OR "congenital melanocytic nevi".ti,ab OR (("naevus".ti,ab OR "naevi".ti,ab OR "nevus".ti,ab OR "nevi".ti,ab OR "melanocytic naevus".ti,ab OR "melanocytic naevi".ti,ab OR "melanocytic nevus".ti,ab OR "melanocytic nevi".ti,ab) AND congenital*.ti,ab)) AND (Photography/ OR medical photography/ OR Photograph*.ti,ab) AND (english.la OR dutch.la)
Gezocht op 07.05.2014: 44 hits (34 Pubmed, 37 Embase waarvan 10 uniek)
Search dermatoscopie
Zoekstrategie voluit:
("congenital naevus".ti,ab OR "congenital naevi".ti,ab OR "congenital nevus".ti,ab OR "congenital nevi".ti,ab OR "congenital melanocytic naevus".ti,ab OR "congenital melanocytic naevi".ti,ab OR "congenital melanocytic nevus".ti,ab OR "congenital melanocytic nevi".ti,ab OR (("naevus".ti,ab OR "naevi".ti,ab OR "nevus".ti,ab OR "nevi".ti,ab OR "melanocytic naevus".ti,ab OR "melanocytic naevi".ti,ab OR "melanocytic nevus".ti,ab OR "melanocytic nevi".ti,ab) AND congenital*.ti,ab)) AND (Dermoscopy/ OR Dermascopy/ OR dermatosc*.ti,ab) AND (english.la OR dutch.la OR german.la)
Filters: taal: NL, EN, DU (zie searchtermen) en jaar vanaf 1990
Gezocht in mei/juni 2014: 243 hits (Pubmed, Embase) >> na ontdubbeling 171; met reference checking 2 extra artikelen
Search chirurgie
Chirurgische ingrepen (excision, tissue expansion, skin grafting)
((nevus/de AND ('congenital disorder'/de OR congenital:lnk OR (congent* OR unacquir* OR 'not acquired' OR 'non acquired'):ab,ti)) OR 'congenital nevus'/de OR 'pigmented nevus'/de OR 'melanocytic nevus'/de OR (((congenit* OR unacquir* OR 'not acquired' OR 'non acquired' OR pigment* OR melanocyt* OR nevocell* OR naevocell* OR 'nevo cellular' OR 'naevo cellular' OR giant OR gigantic OR medium OR large* OR multiple OR small* OR pilos* OR hair* OR divided) NEAR/3 (nevus OR naevus OR nevi OR naevi OR mole OR moles OR birthmark* OR nævi OR nævus)) OR nevocyt* OR nevomelanocyt* OR naevocyt* OR naevomelanocyt* OR ((nevocell* OR naevocell* OR 'nevo cellular' OR 'naevo cellular') NEAR/3 (lesion* OR laesion*)) OR tierfell* OR (bathing NEXT/1 trunk*) OR (((pigment* NEAR/3 (lesion* OR laesion*))) AND (nevus OR naevus OR nevi OR naevi OR mole OR moles OR birthmark*) AND (melanom* OR pseudomelanom*))):ab,ti) AND (surgery/de OR 'surgical technique'/de OR excision/de OR 'local excision'/de OR surgery:lnk OR 'minor surgery'/de OR 'major surgery'/de OR 'pediatric surgery'/exp OR 'plastic surgery'/exp OR dermatome/de OR 'skin surgery'/exp OR autograft/de OR allograft/de OR transplantation/de OR (surg* OR dermatosurg* OR excis* OR resect* OR remov* OR dermatome* OR shaving OR shave OR shaved OR ((skin OR tissue) NEAR/3 (flap* OR expan* OR stretch* OR transplant* OR replace*)) OR graft* OR autograft* OR allograft* OR reconstruct* OR resurfac*):ab,ti)
Gezocht in juli 2014: 4609 hits na ontdubbelen
|
Embase.com |
3134 |
|
Medline (OvidSP) |
393 |
|
Web-of-science |
304 |
|
Scopus |
618 |
|
PubMed publisher |
35 |
|
Cochrane |
0 |
|
Google scholar |
125 |
|
Total |
4609 |
Curettage, dermabrasie
Uit bovenstaande search kwamen ook artikelen over curettage en dermabrasie naar boven. Met reference checking en een korte search op synoniemen voor ‘congenital n(a)evi, dermbrasion, curettage) is gekeken of de gevonden artikelen voor dit onderwerp compleet waren.
Search lasertherapie
(((nevus[tiab] OR nevi[tiab] OR naevus[tiab] OR naevi[tiab] OR CMNs[tiab] OR SCMN[tiab] OR MCMN[tiab] OR LCMN[tiab] OR LCMNs[tiab] OR GCMN[tiab] OR GCMNs[tiab] OR CNNs[tiab] OR SCNN[tiab] OR MCNN[tiab] OR MCNNs[tiab] OR GCNN[tiab] OR Tierfell*[tiab] OR bathing-trunk*[tiab] OR garment-like[tiab] OR ((CNN[tiab] OR CMN[tiab] OR mole[tiab] OR moles[tiab] OR birthmark*[tiab]) AND (giant[tiab] OR gigantic[tiab] OR medium[tiab] OR large[tiab] OR multiple[tiab] OR pilos*[tiab] OR hairy[tiab] OR melanocytic[tiab] OR naevocytic[tiab] OR nevocytic[tiab] OR naevocell*[tiab] OR nevocell*[tiab] OR naevomelanocytic[tiab] OR nevomelanocytic[tiab] OR congenital*[tiab] OR unacquired[tiab] OR non-acquired[tiab]))) AND (laser[tiab] OR lasers[tiab] OR yttrium[tiab] OR erbium[tiab] OR neodymium[tiab] OR aluminum oxide[tiab] OR QSRL*[tiab] OR QSNYL*[tiab] OR QSND[tiab] OR FDQS*[tiab] OR NMRL*[tiab] OR NM-QS*[tiab] OR ND-QS*[tiab] OR Q-switch*[tiab] OR Qswitch*[tiab] OR YAG*[tiab] OR NDYAG*[tiab] OR ND-YAG*[tiab] OR ERYAG*[tiab] OR ER-YAG*[tiab] OR Neodymi*[tiab] OR Erbium*[tiab] OR Yttrium*[tiab] OR Alexandrit*[tiab] OR UCO2*[tiab] OR UltraPulse[tiab])) NOT ota[ti])
Gezocht in November 2015: 683 hits
|
Medline (OvidSP) |
330 |
|
Embase.com |
554 |
|
Central |
33 |
|
PubMed publisher |
7 |
|
Total (na ondubb.) |
683 |