Complementerende oncologische resectie na lokale excisie van pT1-2 coloncarcinoom
Uitgangsvraag
Wat is de optimale behandelstrategie na lokale resectie van een coloncarcinoom, afhankelijk van oncologisch risico, concurrerende gezondheidsrisico’s en andere factoren zoals kwaliteit van leven en kosten?
Deze uitgangsvraag omvat de volgende deelvragen
- Zijn er bruikbare risicogroepen te definiëren voor het bepalen van de behandelstrategie, en welke (combinatie van) kenmerken van het pT1-T2 coloncarcinoom corresponderen met deze risicogroepen?
- Wanneer is follow-up met salvage chirurgie in het geval van locoregionaal recidief een beter of gelijkwaardig alternatief voor complementerende chirurgie?
- Wat bepaalt de keuze voor lokale littekenexcisie en follow-up in plaats van complementerende chirurgie bij een R1/Rx lokale excisie?
Aanbeveling
Algemeen
Bespreek de histologische uitslag van de lokale excisie in een multidisciplinair overleg (MDO) met tenminste een patholoog, maag-darm-leverarts en een chirurg. Formuleer in dit MDO een voorkeursbehandeling en ook eventuele alternatieven.
Verricht een complete stadiering (CT-thorax/abdomen) na lokale excisie van een pT1 coloncarcinoom met een of meer histologische risicofactoren of een pT2 coloncarcinoom.
Schat de kans op lokaal intramuraal recidief en/of lymfekliermetastasen in op basis van:
• pT categorie (T1 vs. T2);
• poliep morfologie (gesteeld vs. niet-gesteeld);
• radicaliteit (R0 met marge >0,1 mm, R1 ≤ 0,1 mm, Rx);
• (lymf-)angioinvasie;
• hooggradige tumor budding (Bd2-3);
• slechte differentiatie
• beoordeelbaarheid van histologische risicofactoren (fragmentatie en/of cauterizatie)
Maak hierbij eventueel gebruik van online beschikbare risicocalculators.
Betrek in de keuze voor complementerende chirurgie of actieve follow-up (module 9.2) naast de recidief risico’s ook de kans op postoperatieve mortaliteit en morbiditeit, concurrerende gezondheidsrisico’s functionele uitkomst en kwaliteit van leven, en de kans op succesvolle curatieve behandeling bij actieve follow-up. Bespreek deze afwegingen met de patiënt.
Voer bij een complementerende colon resectie een oncologische segmentresectie uit met centrale vasculaire ligatie en een D2 lymfklierdissectie.
Voer actieve follow-up uit met een combinatie van CEA, CT- Thorax/Abdomen en endoscopie (module Follow-up na lokale behandeling T1 coloncarcinoom).
Complementerende chirurgie of follow-up met salvage chirurgie
Verricht alleen endoscopische follow-up bij een geschat lymfkliermetastase risico <5%, zoals voor een radicaal verwijderd pT1 coloncarcinoom zonder risico factoren.
Kies voor actieve follow-up bij patiënten met een geschat lymfkliermetastase risico van 5-15% na lokale excisie van een pT1-2 coloncarcinoom.
Overweeg actieve follow-up als alternatief voor complementerende chirurgie bij een geschat risico op lymfkliermetastasen van 15-25%.
Beschouw complementerende chirurgie als voorkeursbehandeling bij patiënten met een geschat risico op lymfekliermetastasen van >25%.
Littekenexcisie bij R1/Rx pT1 coloncarcinoom zonder risicofactoren
Overweeg een aanvullende littekenexcisie als alternatief voor complementerende chirurgie voor een R1/Rx resectie van een pT1 coloncarcinoom zonder aanwezigheid van andere histologische risicofactoren ((lymf-)angioinvasie, hooggradige tumor budding (Bd2-3), en slechte differentiatie). Voorwaarde is wel dat alle histologische risicofactoren voldoende betrouwbaar te beoordelen zijn door de patholoog.
Overwegingen
Aanvullende beeldvorming
Indien een lokale excisie is verricht van een pT1 coloncarcinoom met histologische risicofactoren (zie module Histologische risicofactoren bij T1 CRC) of een pT2 coloncarcinoom, waarbij wordt gekozen voor een complementerende resectie of actieve follow-up, dan wordt geadviseerd een CT-thorax-abdomen te verrichten ter detectie van synchrone metastasen (mocht dit nog niet gedaan zijn). Het risico op synchrone metastasen bij een pT1 coloncarcinoom is betrekkelijk klein (3/647; 0.5%) (Huisman, 2023) maar bepaalt het beleid aanzienlijk (Backes, 2017). Bovendien kan deze beeldvorming gebruikt worden als uitgangssituatie voor de follow-up nadien.
Het maken van een keuze voor complementerende chirurgie dan wel actieve follow-up
De keuze om wel of geen complementerende chirurgie te verrichten is afhankelijk van de ingeschatte kans op lokaal recidief en lymfekliermetastasen, de kans op succesvolle curatieve behandeling indien het recidief optreedt, de kans op terugkeer van ziekte na complementerende chirurgie, de verwachte kans op mortaliteit van chirurgie, de korte- en lange termijn morbiditeit van chirurgie, en de levensverwachting van de kwetsbare patiënt. Daarnaast speelt de kwaliteit van leven, en de persoonlijke wensen van de patiënt een belangrijke rol, evenals kosten en duurzaamheid (Govaert, 2017 ; Sandberg, 2024). Met name in de situaties waarbij er geen duidelijke voorkeursbehandeling is, is het derhalve belangrijk dat de patiënt in een proces van gedeelde besluitvorming een geïnformeerde beslissing kan nemen voor een specifieke behandelstrategie.
Inschatten van het risico op lymfkliermetastasen
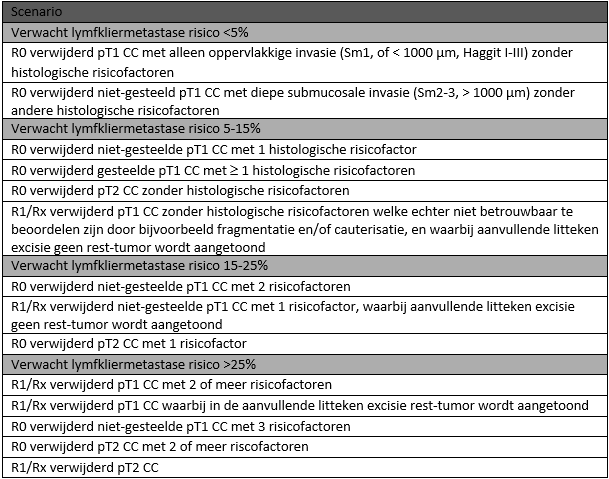
De kans op lymfekliermetastasen is afhankelijk van de aan- of afwezigheid van histologische risicofactoren ((lymf-)angioinvasie, hooggradige tumor budding en slechte differentiatie) en ook poliepkarakteristieken (gesteeld versus niet gesteeld), waarbij een positieve resectie marge bijdraagt aan een hogere kans op lokaal recidief. De kans op lymfkliermetastase kan nog niet per individu exact worden bepaald. Wel zijn er specifieke subgroepen identificeerbaar. In tabel 5.2.2, wordt een overzicht gegeven van de scenario’s die vallen in de groepen met <5%, 5-15%, 15-25%, en >25% risico op lymfkliermetastasen.
Tabel 5.2.2. Overzicht met scenario’s en de bijbehorende kans op regionale lymfkliermetastasen (LNM)
Legenda: De toepassing van histologische risicofactoren wordt beschreven in module Histologische risicofactoren bij T1 CRC
CC coloncarcinoom
De beschreven risico’s zijn tot stand gekomen op basis van verschillende gepubliceerde risicomodellen (Kaijwara, 2023; Guo, 2020, Naffouie, 2022; Oh, 2019; Ozeki, 2022; Yan, 2021; Backes, 2018; Wang, 2024; Ichimasa, 2022; Kudo, 2020). Voor gesteelde poliepen is het risicomodel van Backes et al, nu gevalideerd en terug te vinden op T1CRC.com/calculator. Voor niet gesteelde poliepen bestaat er geen gevalideerde en in de Nederlandse populatie getest model. Echter, gezien de kwaliteit zijn het normogram van Kajiwara en Yan het best te gebruiken.
Ten eerste dient onderscheid te worden gemaakt tussen gesteelde en niet-gesteelde poliepen met een carcinoom. Van alle T1 coloncarcinomen (CCs) heeft 20 tot 35% een gesteelde morfologie, en komen ze voornamelijk voor in het linkszijdige colon (Kessels, 2018). Gesteelde pT1 coloncarcinomen hebben een lager risico op een lokaal recidief en lymfekliermetastasen dan niet-gesteelde poliepen (Hassan, 2005; Kessels, 2018). Een risicoanalyse van alleen gesteelde poliepen werd een risico variërend van 0.3 tot 36.8% berekend, afhankelijk van de aanwezigheid van 1 of meerdere histologische risicofactoren, waarbij de meerderheid een risico had tussen de 3 en 8.5% (Backes, 2018). Gesteelde pT1 CCs met Haggit 4 invasie worden nooit R0 verwijderd. Desondanks is ook bij aanwezigheid hiervan het risico op LNM altijd kleiner dan 15%. De calculator voor de gesteelde T1 CCs is inmiddels door middel van de PATCH-studie gevalideerd voor de Nederlandse situatie.
De meta-analyse van Dang (2020) toonde aan dat het risico op lymfkliermetastase slechts 0.7% betreft wanneer alle risicofactoren, inclusief een submucosale invasie >1000 µm/Sm2-3, negatief zijn in niet-gesteelde poliepen (Dang, 2020). Een meta-analyse van Zwager (2022) toonde aan dat het risico 2.6% betrof voor niet-gesteelde poliepen, wanneer er sprake was van alleen diepe invasie in de submucosa (> 1000 µm/Sm2-3). In een meta-analyse van Dang (2020) werd specifiek gekeken naar de cumulatieve incidentie van lokale recidieven en/of recidieven of afstand, in de groep die alleen een lokale excisie heeft ondergaan (Dang, 2020). CRC recidieven werden waargenomen bij 209/5167 patiënten (3.3%; 95% CI 2.6 tot 4.3%). CRC gerelateerde mortaliteit werd geobserveerd in 42/2519 (1.7%; 95% CI1.2 tot 2.2%) patiënten. CRC gerelateerde mortaliteit wanneer een recidief was opgetreden was 42/103 (41%). Dit was bijna volledig te wijten aan het ontstaan van metastasen. Gedifferentieerd voor patiënten met een hoog risico (een of meerdere histologische risicofactoren) versus laag risico (afwezigheid van histologische risicofactoren) op recidief betrof dit 82/1023 (7.0%; 95%CI 4.9 tot 9.9%) en 10/1499 (0.7%; 95%CI 0.4 tot 1.2%). In de hoog risicogroep was de kans op een afstandsmetastase 3.5% (95% CI, 1.9% tot 6.1%), en de gepoolde CRC-gerelateerde mortaliteit 4.5%. Omdat het een meta-analyse op vooral retrospectieve studies betreft, is het onduidelijk in hoeverre er een selectie heeft plaatsgevonden naar patiënten met een hoog risico op post-chirurgische mortaliteit, slechte ASA score, dan wel een relatief lager (5-15%) risico op lokaal recidief of lymfekliermetastasen. Daarnaast zijn zowel rectum als colon samengenomen, waarbij het rectum een veel hogere kans had op recidief (locoregionaal + afstandsmetastasen) dan colon (0.8 versus 5.7%). Het is derhalve onduidelijk of deze getallen op alle hoog risico T1 coloncarcinomen van toepassing zijn.
De kans op lymfkliermetastasen neemt toe met de aanwezigheid van multipele risicofactoren. Mogelijk is het risico op lokaal recidief of lymfekliermetastasen bij de aanwezigheid van slechts 1 risicofactor ook beperkt bij niet-gesteelde pT1 coloncarcinomen, alhoewel betrouwbare data hierover ontbreken (Hassan, 2005; Williams, 2013; Kawachi, 2015; Yasue, 2019). Het wordt nu ingeschat dat wanneer alleen hooggradige tumor budding, slechte differentiatie of (lymf-)angioinvasie aanwezig is, het risico op recidief 5 tot 15% betreft. Hierbij is (lymf-)angioinvasie geassocieerd met een hoger risico dan hooggradige tumor budding of slechte differentiatie.
Kans op intramuraal recidief/residu
Het lokaal recidief wordt ook bepaald door de aanwezigheid van zowel histologische risicofactoren, (hooggradige tumor budding of lymf-angioinvasie) (Gijsbers, 2022), en de toegepaste lokale resectie techniek. De kans op een intramuraal recidief na lokale excisie met een positieve resectiemarge is ongeveer 12-15% (Backes 2017, Gibson 2022, Gijsbers 2020, Gauci 2024). Voor ESD blijkt de laterale resectiemarge niet voorspellend, de diepe resectie marge echter wel (Oh, 2024). Betrouwbare getallen over de kans op intramuraal recidief na een R1 met eFTR of CAL-WR verwijderde T1-T2 coloncarcinoom zijn nog niet beschikbaar. De kans op intramuraal recidief bij een R0 resectie is uitermate klein.
Oncologische uitkomsten na actieve follow-up en complementerende chirurgie
Overlijden ten gevolge van recidief ziekte is secundair aan de gevolgen van gemetastaseerde ziekte dan wel complicaties ten gevolge van de behandeling ter preventie van metastasen. De kans op recidief ziekte na een complementerende chirurgie is gemiddeld 3.2%, waarbij rectum mogelijk een hoger risico kent (4%) op recidief dan colon (2.5%) (van Oostendorp, 2020; Yeh, 2020; Nian, 2021). Recidief na chirurgie gaat vaak gepaard met metastasen op afstand (Yeh, 2020, Tian, 2021). Recidief na complementerende chirurgie is geassocieerd met een <10 verwijderde lymfeklieren, de aanwezigheid van lymfkliermetastasen en de aanwezigheid van histologische risicofactoren zoals (lymf-)angio invasie, slechte differentiatie en hooggradige tumor budding. Bij de laatste neemt de kans op post-chirurgische recidieven toe met het aantal risicofactoren die aanwezig zijn. In principe geldt dat bij het verrichten van een complementerende resectie een formele oncologische segmentresectie dient plaats te vinden (module 5.3: Uitgebreidheid colonresectie) (Backes, 2017). Bertelsen et al. toonde namelijk niet alleen voor stadium 2 en 3, maar ook voor stadium 1 een betere locoregionale controle aan bij het toepassen van complete mesocolische excisie (Bertelsen, 2019).
Kans op geslaagde salvage chirurgie na een lokaal recidief na actieve follow-up
In de studie van Dang (2020) bleek 40% van de recidieven gepaard te gaan met CRC specifieke mortaliteit, en kon 60% alsnog curatief worden behandeld. In twee andere Nederlandse studies bleek dit percentage curatieve behandeling 65 tot 67% te betreffen (Backes, 2017; Gijsbers, 2022). Er zijn echter ook lagere succeskansen voor salvage chirurgie gerapporteerd (50% Levic, 2019). De follow-up in de bestudeerde cohorten was echter wisselend van intensief naar minder intensief, hetgeen mogelijk een impact heeft gehad op een vroege detectie, en daarmee kans op het ontdekken van afstandsmetastasen. Het is echter te verwachten dat een actieve follow-up strategie gepaard zal gaan met een hoger percentage afstandsmetastasen, in vergelijking met een strategie met complementerende chirurgie. Hoe groot deze stijging precies is, en of dit opweegt tegen chirurgie in een groep met co-morbiditeit zal verder moeten worden onderzocht.
Indicatiestelling voor actieve follow-up of complementerende chirurgie
Binnen de Nederlandse T1 CRC werkgroep is consensus verkregen om een stratificatie voor de kans op lymfkliermetastasen toe te passen, om daarmee meer differentiatie aan te brengen in het vervolgbeleid na lokale excisie van een pT1-2 coloncarcinoom. In plaats van de laag vs. hoog risico onderverdeling is nu een stratificatie in 4 categorieën gemaakt (<5%, 5-15%, 15-25% en > 25% kans op lymfkliermetastasen), zie tabel 5.2.2.
De indicatiestelling voor complementerende chirurgie is internationaal nog steeds ruim, gebaseerd op de veronderstelling dat met het direct verwijderen van eventueel aanwezige lymfkliermetastasen voorkomen wordt dat er afstandsmetastasen ontstaan. Maar afstandsmetastasen ontstaan voor een groot deel bij patiënten zonder lymfkliermetastasen (60-70%), en daarmee lijkt complementerende chirurgie in beperkte mate de kans op metastasering op afstand te beïnvloeden. Uit de cohort series met actieve follow-up blijkt ook dat de kans op regionaal lymfklierrecidief lager lijkt te zijn dan het percentage lymfkliermetastasen wat bij complementerende chirurgie wordt gevonden bij een vergelijkbare patiëntengroep (Dang, 2020; Oka, 2024). Dat suggereert dat niet alle lymfkliermetastasen uitgroeien tot een mesocolisch recidief. Tenslotte blijkt de meerderheid van de locoregionale recidieven nog met salvage chirurgie behandeld te kunnen worden op het moment dat dit recidief gedurende actieve follow-up wordt gediagnosticeerd. Dat is de reden dat in toenemende mate ingezien wordt dat de additionele waarde van complementerende chirurgie waarschijnlijk beperkt is, en dat er een relatief hoog a priori oncologisch risico moet zijn om dit te rechtvaardigen, zeker als de postoperatieve mortaliteit, en korte- en lange termijn morbiditeit wordt meegerekend.
Met deze kennis in het achterhoofd kunnen we dan komen tot aanbevelingen voor vervolgbeleid voor de verschillende risico strata.
A <5% kans op regionale lymfkliermetastase
Voor de groep met lymfkliermetastase risico <5% geldt al lange tijd de aanbeveling om alleen endoscopische follow-up te doen, dus zonder CEA/CT. Verschillende studies hebben aangetoond dat de kans op afstandsmetastasen heel erg klein is. Het is zeer onwaarschijnlijk derhalve dat actieve follow-up impact zal hebben op de kanker-specifieke overleving, maar wel gepaard zal gaan met veel kosten en belasting voor de patiënt en het zorgsysteem (Oka, 2024).
B 5-15% kans op regionale lymfkliermetastasen
Er zijn 4 studies die met een statistische methode hebben gecorrigeerd voor baseline verschillen tussen een cohort met actieve follow-up versus complementerende chirurgie (Corre 2023, Levic 2019, Nilsson 2024, Ouchi 2023). Vervolgens hebben deze cohorten gekeken naar de kans op afstandsmetastasen en kanker-specifieke overleving. Geen van deze 4 studies toonde een verschil aan in de kanker-specifieke overleving of de kans op afstandsmetastasen. Het Zweedse cohort (n= 488 actieve surveilance vs 1317 complementerende chirurgie), betrof alleen coloncarcinomen, waar de andere cohorten ook rectum carcinomen includeerden. Na correctie voor leeftijd, geslacht, locatie, en aanwezigheid van histologische risicofactoren, werd geen verschil in ziekte-vrije interval aangetoond (gecorrigeerde Hazard ratio 1.03, 95%CI 0.56-1.91). Een Deense studie waarin gecorrigeerd werd met propensity score matching (n=152 vs n=152) toonde geen verschil aan in ziektevrije overleving. Een Frans cohort (n=90 actieve follow-up v.s. 107 complementerende chirurgie) heeft gecorrigeerd voor confounders met een gewogen analyse, en toonde ook geen verschil aan (weighted hazard ratio 0.95; 95% CI, 0.52-1.75). Het Japanse cohort toonde geen verschil aan in 5-jaar kanker-specifieke overleving na propensity matching van alleen cases met 1 of meerdere risicofactoren (n=178 vs n=178 cases).
Het is bekend dat het grootste gedeelte van hoog risico pT1 coloncarcinomen slechts 1 risicofactor hebben, en in een minderheid 2 of meer. Om deze reden wordt aangenomen dat de kennis die voortkomt uit deze 4 cohorten vooral toepasbaar is op de groep met een LNM risico van 5-15%. Actieve follow-up biedt dan de voordelen van orgaansparende behandeling, zonder operatieve risico’s en met betere functionele uitkomst. Op basis van deze studies wordt aangenomen dat actieve follow-up de voorkeursstrategie is voor patiënten met een risico van 5-15% op lymfkliermetastasen.
C 15-25% kans op regionale lymfkliermetastasen
Voor de groep met een geschat lymfkliermetastase risico van 15-25% is nog niet duidelijk of actieve follow-up een gelijkwaardig alternatief is voor complementerende chirurgie, maar zou je deze twee opties wel beide met een patiënt die fit voor chirurgie is kunnen bespreken. In een proces van gedeelde besluitvorming kan dan tot een behandelkeuze worden gekomen.
D >25% kans op regionale lymfkliermetastasen
Voor patiënten met een lymfkliermetastase risico van >25% moet een complementerende resectie nog steeds beschouwd worden als standaardbehandeling, tenzij een patiënt niet fit is voor chirurgie. De aanwezigheid van een lymfkliermetastase is geassocieerd met een verhoogd risico op het post-operatief optreden van afstandsmetastasen. Herkenning van deze lymfkliermetastasen kan aanleiding zijn tot het starten van adjuvante chemotherapie ten einde dit risico te verlagen. Daarnaast zijn er geen studies beschikbaar voor deze specifieke subgroep die aantoont dat actieve follow-up mogelijk een vergelijkbaar alternatief is t.o.v. complementerende chirurgie.
Aanvullende littekenexcisie na een lokaal potentieel irradicale resectie (R1/Rx) van een pT1 coloncarcinoom.
Na een potentieel irradicale resectie (zoals na een piecemeal EMR) bestaat er een kans op lokaal recidief (Butte, 2012; Backes, 2017). Indien er geen andere histologische risicofactoren aanwezig zijn, zou de kans op lymfekliermetastasen klein zijn, en betreft het vooral het risico op een lokaal recidief. Het is echter gebleken dat door fragmentatie, tangentiele aansnijding, en cauterisatie histologische risicofactoren niet altijd goed te beoordelen zijn. In deze subgroep persisteert een risico op lymfekliermetastasen van 8% (Gijsbers, 2020). Het is derhalve niet alleen belangrijk om te bepalen of de risicofactoren wel of niet aanwezig zijn, maar ook of ze betrouwbaar zijn te bepalen, bij voorkeur door een 2e onafhankelijke beoordeling (zie module Histologische risicofactoren bij T1 CRC). In een grote Nederlandse studie bleek bij herbeoordeling van R1/Rx verwijderde pT1 coloncarcinomen dat in ongeveer 50% alsnog een risicofactor kon worden aangetoond in de groep afgegeven als R1/Rx maar zonder histologische risicofactoren. In de groep die geen risicofactoren vertoonde ontstond slechts 1 recidief (Gijsbers, 2022). Alle andere 7 recidieven toonden wel een histologische risicofactor. Al met al bleek bij deze strategie ondanks een 9% recidiefkans in de groep met een aanvullende lokale littekenexcisie, dat de totale-, en metastasevrije overleving gelijk was (OS; 95.6% 94.4% en MFS 96.8% versus 92.1%) (Gijsbers, 2022). eFTR is een veilige en effectieve techniek gebleken om het litteken te verwijderen (Kuellmer, 2019; Zwager, 2022) van poliepen die bij oorsprong <30 mm waren, met een litteken diameter <15 mm. Voor littekens van poliepen > 30 mm, of litteken > 15 mm is het beter CELS te gebruiken om het litteken te verwijderen. Ook hierbij is het aan te bevelen om de indicatie te beperken tot een < 50% circumferent litteken.
Er zijn omstandigheden waarin een aanvullende litteken excisie niet is te verrichten, zoals wanneer het litteken niet betrouwbaar is terug te vinden, of als een litteken excisie als te risicovol wordt ingeschat. Het is helaas dan niet mogelijk om verder onderscheid te maken tussen de aan-, of afwezigheid van residu in het litteken hetgeen invloed heeft op de prognose. Residu wordt aangetoond in 11-12% van de patiënten met een R1/Rx resectie zonder risicofactoren. Bij aanwezigheid van residu in het litteken bleek er een 11-18% kans op lymfkliermetastasen te bestaan (Gijsbers, 2021), hetgeen aanzienlijk hoger is dan wanneer geen residu werd aangetoond. Deze onzekerheid rond deze schatting is echter groot door de kleine aantallen patiënten met residu in het litteken. Dit moet worden meegewogen wanneer wordt gekozen voor actieve follow-up zonder litteken excisie.
Het is belangrijk te beseffen dat deze informatie is gebaseerd op retrospectieve cohorten, met tevens een zeer heterogene follow-up, en mogelijk een significante kans op selectiebias. Het is derhalve dan ook sterk aan te bevelen patiënten bij wie wordt gekozen voor de strategie met een lokale littekenexcisie gevolgd door follow-up te laten participeren in de LOCAL-studie zodat ook hoog kwalitatieve informatie wordt verkregen over de oncologische uitkomsten van deze strategie op de lange termijn.
Balans tussen gewenste en ongewenste effecten
De voordelen van een oncologische resectie betreft de toegenomen zekerheid dat de lymfklieren, met potentieel metastasen zijn weggehaald, waarmee de kans op afstandsmetastasen mogelijk wordt verlaagd. Daarnaast zal indien er geen lymfkliermetastasen worden aangetoond, de follow-up zeer beperkt zijn, en dus minder belastend voor de patiënt. Daar tegenover staat dat een oncologische resectie schade kan veroorzaken die ook op de lange termijn de kwaliteit van leven kan beïnvloeden, kostbaar is, en ook in 1-2% kan leiden tot behandeling gerelateerde mortaliteit. Actieve follow-up heeft als voordeel dat er geen beschadiging wordt aangebracht en derhalve de kwaliteit van leven wordt behouden, minder geld kost en minder behandeling gerelateerde mortaliteit kent. Nadelen zijn echter de frequente noodzaak tot endoscopie en beeldvorming, angst voor terugkeer van ziekte die dit kan veroorzaken, en een onzekerheid dat terugkeer van ziekte ook leidt tot een toegenomen risico op afstandsmetastasen. Voor situaties met een zeer lage kans op lymfkliermetastasen en afstandsmetastasen lijkt de keuze voor een aanvullende behandeling heel duidelijk. Maar juist bij de groep met 15-25% kans op lymfkliermetastasen is dat veel minder duidelijk en moet dit worden afgewogen tegen de wensen van de patiënt, de aanwezige co-morbiditeit, operatierisico’s, en verwachtte levensverwachting.
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
Het is belangrijk om patiënten te betrekken in de keuze voor of een oncologische resectie dan wel actieve follow-up. Het kan per patiënt verschillen welk belang zij hechten aan oncologische zekerheid versus lange termijneffecten van een oncologische resectie. Ook eventuele angst voor terugkeer, en het stresserende effect van herhaalde beeldvorming bij actieve follow-up kan leidend zijn in het maken van een behandelkeuze. Al deze aspecten dienen dan ook met patiënt te worden besproken.
Kostenaspecten
Actieve follow-up zal zeer waarschijnlijk goedkoper zijn dan complementerende chirurgie voor de groep met een lage kans op lymfkliermetastasen (<5% en 5-15% kans). Voor de groep met 15-25% kans op lymfkliermetastasen is dit echter onduidelijk. Voor de groep met een > 25% kans speelt dit niet, omdat actieve follow-up niet als een valide alternatief wordt gezien. De noodzaak tot minder opname dagen, minder behoefte tot algehele sedatie, en OK-capaciteit speelt ook een rol de capaciteit.
Gelijkheid ((health) equity/equitable)
Voor het maken van een keuze is goede voorlichting van alle behandelaspecten essentieel. Mogelijk dat de huidige voorlichting veel vraagt aan de patiënt, complex is om te doorgronden, en veel tijd kost. Een taalbarrière, als ook verschillen in culturele achtergrond, kunnen een sterke invloed hebben in het verkrijgen en tevens het waarderen van deze informatie.
Aanvaardbaarheid
Ethische aanvaardbaarheid
De keuze om voor de groep met 5-15% kans op lymfkliermetastasen actieve follow-up als eerste behandelkeuze te verkiezen op basis van cohortstudies, komt voort uit het totale bewijs aan studies, die het onwaarschijnlijk maakt dat er een groot effect op kanker-specifieke overleving zal worden verkregen met een oncologische resectie in deze specifieke subgroep. Daarentegen geeft een oncologische resectie wel morbiditeit op de lange termijn, is kostbaar en maakt gebruik van gezondheidscapaciteit. Juist om het nadeel van deze ingreep op de grote groep te beperkten wordt een aanvaardbaar risico genomen op een zeer beperkte stijging in het aantal afstandsmetastasen.
Duurzaamheid
Er zijn geen studies die specifiek gekeken hebben naar de verschillen in duurzaamheid van beide strategieën. Alhoewel het wel te verwachten is dat de carbon-footprint van actieve follow-up lager zal zijn dan van complementerende chirurgie. Hier is echter in deze context niet specifiek onderzoek naar verricht. Wel zal actieve follow-up minder gebruik maken van kostbare en schaarse gezondheidscapaciteit zoals ligduur in het ziekenhuis, OK-capaciteit en noodzaak tot sedatie.
Haalbaarheid
Bij een eerdere inventarisatie van de capaciteit is gebleken dat zowel de NVvR en de NVMDL denken dat de toegenomen ingrepen (beeldvorming en endoscopie ter inspectie van het litteken) opgevangen kunnen worden binnen de bestaande capaciteit.
Onderbouwing
Achtergrond
Wat is nieuw?
- Na lokale excisie van een pT1-T2 coloncarcinoom worden de patiënten nu onderverdeeld in 4 subgroepen: <5%, 5-15%, 15-25% en > 25% kans op lymfkliermetastasen. De behandeling van voorkeur verschilt per subgroep
- Voor de <5% subgroep geldt dat alleen endoscopische follow-up nog steeds de aanbevolen behandeling is
- Voor de 5-15% subgroep is actieve follow-up de aanbevolen behandeling geworden
- Voor de 15-25% subgroep wordt geadviseerd samen met de patiënt te kiezen voor òf complementerende chirurgie, òf actieve follow-up op basis van de wensen van de patiënt, concurrerende gezondheidsrisico’s, operatierisico, en kwaliteit van leven
- Voor de >25% subgroep is nog steeds complementerende chirurgie de aanbevolen behandeling
Achtergrond
Na een macroscopisch radicale lokale excisie van een pT1-2 coloncarcinoom moet de kans op recidief worden ingeschat om de noodzaak voor aanvullende behandeling te bepalen. Recidief ziekte kan worden onderverdeeld in locoregionaal recidief (lokaal intramuraal recidief of regionale lymfekliermetastasen/tumor deposities) en afstandsmetastasen. Een aanvullende oncologische resectie binnen enkele weken na de lokale excisie wordt een complementerende oncologische segmentresectie genoemd (complementerende chirurgie). Met deze resectie worden een eventueel aanwezig lokaal intramuraal residu en/of lymfekliermetastasen verwijderd, met als doel het verlagen van de kans op recidief ziekte. Indien tijdens follow-up na lokale excisie een intramuraal recidief of lymfekliermetastase wordt gedetecteerd, en hiervoor wordt een oncologische colonresectie gedaan, dan wordt dit een salvage resectie genoemd (salvage chirurgie).
De kans op een lokaal intramuraal of regionaal recidief in het mesocolon op basis van achtergebleven lymfekliermetastasen/ tumor deposities zijn na de lokale excisie niet exact te bepalen. Derhalve moet op basis van tumor karakteristieken (gesteeld versus niet-gesteelde morfologie) en de histologische risicofactoren (lymf)angioinvasie, slechte (hooggradige) differentiatie, hooggradige tumor budding, en positieve resectiemarge (zie module Histologische risicofactoren bij T1 CRC) de kans op beide worden ingeschat. Deze risico inschatting is een belangrijk discussiepunt in de dagelijkse praktijk.
Er zijn verschillende strategieën beschreven voor aanvullende behandeling van een lokale excisie van een coloncarcinoom. Indien er sprake is van de aanwezigheid van 1 of meerdere risicofactoren voor lymfkliermetastasen (lymf)angioinvasie, slechte (hooggradige) differentiatie, of hooggradige tumor budding) bestaat de keuze uit complementerende oncologische resectie of een strategie met actieve follow-up (module Follow-up na lokale behandeling T1 coloncarcinoom) gevolgd door salvage chirurgie indien een locoregionaal recidief optreedt. Indien er alleen sprake is van een potentieel irradicale resectie (R1/Rx), maar zonder de aanwezigheid van de andere histologische risicofactoren, bestaat de keuze uit complementerende chirurgie, een strategie bestaande uit een aanvullende littekenexcisie gevolgd door actieve follow-up (module Follow-up na lokale behandeling T1 coloncarcinoom) indien de litteken excisie geen residuaal carcinoom aantoont, of alleen actieve follow-up (bijvoorbeeld indien litteken excisie technisch niet mogelijk is als het litteken niet betrouwbaar wordt teruggevonden, of als een litteken excisie als risicovol wordt ingeschat). De keuze voor een bepaalde strategie is afhankelijk van het ingeschatte risico op recidief coloncarcinoom, maar ook morbiditeit en mortaliteit van complementerende chirurgie, concurrerende gezondheidsrisico’s en kwaliteit van leven. Er is een toenemende tendens naar orgaansparende behandeling, omdat de oncologische winst van complementerende chirurgie kleiner lijkt dan voorheen gedacht, en ook duidelijke nadelen heeft.
Samenvatting literatuur
Samenvatting van internationale richtlijnen en consensusdocumenten
Veel van de richtlijnen maken geen onderscheid tussen colon en rectum. Derhalve is zoveel mogelijk gekeken naar specifieke aanbevelingen voor colon, maar kan dit ook rectum betreffen.
Er zijn verschillende internationale richtlijnen die een advies geven over de keuze tot complementerende chirurgie. pT1 CRCs worden ingedeeld als hebbende een laag risico op recidief CRC (zonder risicofactoren), en hebbende een hoog risico op recidief CRC bij aanwezigheid van 1 of meerdere histologische risicofactoren. Een overzicht van de geadviseerde risicofactoren wordt weergegeven in tabel 5.2.1.
Tabel 5.2.1
|
Risk factor |
ASGE |
ESGE |
ESMO |
APCGBI |
JSCCR |
|
Lymphovascular invasion |
X |
X |
X |
X |
X |
|
High grade tumor budding1 |
X |
X |
X |
X |
X |
|
Deep Submucosal Invasion (> 1 mm) |
X |
X |
|
X* |
X |
|
Poor/mucinous differentiation2 |
X |
X |
X |
X |
X |
|
Resection margin <1 mm |
X |
X |
|
X |
|
|
Resection margin (< 0.1 mm) |
|
|
X |
|
X |
1 High grade tumor budding is Bd2+Bd3
2 Mucinous differentiation is only considered a risk factor in the JSCCR guideline
*Only Sm3 invasion is considered a risk factor
De richtlijn van de American Society of Gastrointestinal Endoscopy (ASGE), European Society of Gastrointestinal Endoscopy (ESGE), Japanese Society for cancer of the colon and rectum (JSCCR), The Association of Coloproctology of Great Britain and Ireland (APCGBI) maken geen onderscheid tussen rectum en colon. Alleen de European Society for Medical Oncology (ESMO) heeft een aparte richtlijn voor colon en rectum.
De ASGE stelt dat de aanwezigheid van een histologische risicofactor in principe een indicatie is voor een complementerende oncologische resectie (Shaukat, 2020). Dit geldt ook voor T1 CRCs die piecemeal zijn verwijderd, en niet optimaal zijn te beoordelen door de patholoog ten gevolge van gebrek aan oriëntatie en fragmentatie. De keuze voor een complementerende resectie moet worden gewogen ten opzichte van het operatierisico van de patiënt. De ASGE adviseert dat de keuze voor wel of geen complementerende oncologische resectie via een multidisciplinair overleg, en via gedeelde besluitvorming met de patiënt tot stand komt.
De ESGE (Pimentel-Nunes, 2015; Ferlitsch, 2017; Hassan, 2019) stelt dat er bij aanwezigheid van een van de risicofactoren er een indicatie bestaat voor een complementerende oncologische resectie. Hierbij wordt diepe submucosale invasie ook gezien als risicofactor i.t.t. de Nederlandse CRC richtlijn (module 4.7). Bij afwezigheid van deze risicofactoren is het advies patiënt endoscopisch te vervolgen conform de CRC richtlijn (colonoscopie 1 en 3 jaar na resectie) (Hassan, 2019). De ESGE adviseert het gebruik van de 1 mm marge voor een radicale resectie. Wel stelt de richtlijn dat bij alleen diepe invasie, afhankelijk van de morbiditeit en wensen van de patiënt er voor actieve follow-up kan worden gekozen.
De ESMO stelt dat er bij patiënten met een laag of gemiddeld operatierisico er een indicatie bestaat voor een complementerende oncologische resectie bij aanwezigheid van een risicofactor (Glynne-Jones, 2017; Argiles, 2020).
De ACPGBI stelt dat het onduidelijk is of chirurgie een betere optie is dan afwachten in patiënten met 1 of meer risicofactoren (Williams, 2013). De keuze voor een complementerende oncologische resectie is een keuze van de patiënt na uitleg van de risico’s en meerwaarde van elke strategie. Met een gemiddeld percentage van 10% lymfekliermetastasen in de groep geclassificeerd als hoog risico, zal bij veel patiënten geen residuaal CRC meer worden aangetoond in het resectiepreparaat.
De ACPGBI adviseert follow-up bij een risico < 5%, en een discussie met de patiënt over intensief vervolgen versus complementerende chirurgie bij een risico tussen de 5 en 10%. Bij een risico > 10% wordt chirurgie geadviseerd, indien patiënt voldoende fit is voor chirurgie (Williams, 2013).
De JSCCR geeft aan dat een complementerende resectie dient plaats te vinden indien er een van de risicofactoren aanwezig is (Hashiguchi, 2020). De JSCCR maakt wel de kanttekening dat bij alleen diepe invasie, het risico op een lokaal recidief of lymfekliermetastasen waarschijnlijk erg laag is.
Een internationaal consensus document geïnitieerd door de World Endoscopy Organization (WEO) en uitsluitend bestaand uit Maag-Darm-Leverartsen stelt dat bij aanwezigheid van alleen diepe submucosale invasie, via gedeelde besluitvorming, kan worden gekozen tussen complementerende chirurgie dan wel actieve follow-up (Djinbachian, 2024). Bij aanwezigheid van een andere risicofactor dient chirurgie of andere oncologische behandeling plaats te vinden.
Samenvatting van systematische reviews en meta-analyses
In de beschikbare literatuur wordt niet altijd onderscheid gemaakt tussen rectum en colon. Het is derhalve niet altijd mogelijk om separaat voor colon of rectum de specifieke getallen te extraheren. Waar mogelijk is dit gespecificeerd. Indien dit niet mogelijk bleek is gekozen voor colorectaal carcinoom (CRC).
Tian (2021) vergeleek 7 studies waarin 1205 CRC patiënten met lokale excisie gevolgd door complementerende chirurgie werden vergeleken met 993 patiënten met lokale excisie gevolgd door actieve follow-up (Tian, 2021). Complementerende chirurgie werd geassocieerd met een klinisch relevant verschil voor algehele overleving (OR 0.29; 95%CI 0.08 tot 0.53) en bijna significant lagere kans op een lokaal recidief (OR 0.29; 95%CI 0.08 tot 1.01). Er werd geen verschil waargenomen in CRC specifieke overleving (OR 0.68; 95% CI 0.27-1.69; I2 = 22%)), recidief vrije overleving (OR 1.27; CI 0.72-2.25; I2 = 0%)) en afstandmetastasen (OR 0.99; CI 0.49-2.01). De betere algehele overleving na complementerende chirurgie zou heel goed kunnen passen bij een selectie van patiënten met een hoog operatierisico voor een afwachtend beleid. Ten gevolge van deze co-morbiditeiten is er een hogere kans op concurrerende doodsoorzaken in de groep die alleen een lokale excisie heeft ondergaan.
Chen (2023) rapporteerde een meta-analyse met random effects modellen en een Kaplan-Meier analyse voor totale overleving, ziektevrije overleving, en kanker-specifieke overleving op basis van studies, met in totaal 831 CRC-patiënten die lokale resectie met actieve follow-up en 2130 patiënten die complementerende operatie ondergingen. Vijf studies werden ook geïncludeerd in de meta-analyse van Tian (2021). De 5-jaar algehele overleving (10 studies) was lager in de groep met actieve follow-up vergeleken met de groep met operatie (86.3% vs 94.5%; HR 2.50, 95%CI 1,52-4,10). Actieve follow-up werd ook geassocieerd met een lagere 5-jaar ziektevrije overleving op basis van 9 studies (89.9% vs 96,9%; HR 2.44; 95%CI 1,27-4,70). Er was geen verschil in CRC specifieke overleving op basis van 7 studies (96.7% vs 98.3%; HR 1.09; 95%CI 0,48-2,45). De bewijskracht van deze studie is zeer laag. Dit heeft te maken met imprecisie, het includeren van observationele studies en heterogeniteit tussen de studies.
Zoeken en selecteren
Uitkomstmaten
- Totale overleving
- Coloncarcinoom specifieke overleving
- Recidief vrije overleving.
- Metastase vrije overleving
- Curatief te behandelen recidief
- Proportie afstandmetastasen
- Orgaansparende behandeling
- Postoperatieve morbiditeit en mortaliteit van complementerende chirurgie.
- Kwaliteit van leven
- Functionele uitkomst
- Kosten
- Duurzaamheid
PICO(s)
Voor deelvraag 1 werd geen PICO opgesteld
PICO 2 Follow-up met salvage chirurgie versus complementerende chirurgie
| P: | patiënt met status na lokale excisie van een pT1-2 coloncarcinoom en bepaalde oncologische en niet-oncologische risico’s; |
| I: | complementerende chirurgie; |
| C: | actieve follow-up met salvage chirurgie bij recidief |
| O: | totale overleving, coloncarcinoom specifieke overleving, ziektevrije overleving, metastasevrije overleving, curatief te behandelen recidief, proportie afstandsmetastasen, postoperatieve mortaliteit en morbiditeit, kwaliteit van leven, functionele uitkomsten, kosten en duurzaamheid. |
PICO 3 Indicatie lokale littekenexcisie
| P: | patiënt met een R1/Rx lokale excisie van een pT1 coloncarcinoom zonder histologische risicofactoren; |
| I: | complementerende chirurgie; |
| C: | lokale littekenexcisie gevolgd door actieve follow-up met salvage chirurgie bij recidief; |
| O: | totale overleving, coloncarcinoom specifieke overleving, ziektevrije overleving, metastasevrije overleving, curatief te behandelen recidief, proportie afstandsmetastasen, postoperatieve mortaliteit en morbiditeit, kwaliteit van leven, functionele uitkomsten, kosten en duurzaamheid |
Referenties
- Argilés G, Tabernero J, Labianca R, Hochhauser D, Salazar R, Iveson T, et al. Localised colon cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2020;31(10):1291-305.
- Backes Y, Elias SG, Bhoelan BS, Groen JN, van Bergeijk J, Seerden TCJ, et al. The prognostic value of lymph node yield in the earliest stage of colorectal cancer: a multicenter cohort study. BMC Med. 2017;15(1):129.
- Backes Y, Elias SG, Groen JN, Schwartz MP, Wolfhagen FHJ, Geesing JMJ, et al. Histologic factors associated with need for surgery in patients with pedunculated T1 colorectal carcinomas. Gastroenterology. 2018;154(6):1647-59.
- Backes Y, de Vos Tot Nederveen Cappel WH, van Bergeijk J, Ter Borg F, Schwartz MP, Spanier BWM, et al. Risk for incomplete resection after macroscopic radical endoscopic resection of T1 colorectal cancer: a multicenter cohort study. Am J Gastroenterol. 2017;112(5):785-96.
- Butte JM, Tang P, Gonen M, Shia J, Schattner M, Nash GM, et al. Rate of residual disease after complete endoscopic resection of malignant colonic polyp. Dis Colon Rectum. 2012;55(2):122-7.
- Djinbachian R, Rex DK, Chiu HM, Fukami N, Aihara H, Bastiaansen BAJ, et al. International consensus on the management of large (≥20 mm) colorectal laterally spreading tumors: World Endoscopy Organization Delphi study. Dig Endosc. 2024.
- Dang H, Dekkers N, le Cessie S, van Hooft JE, van Leerdam ME, Oldenburg PP, et al. Risk and time pattern of recurrences after local endoscopic resection of T1 colorectal cancer: a meta-analysis. Clin Gastroenterol Hepatol. 2020;18(4):716-28.
- Ferlitsch M, Moss A, Hassan C, Bhandari P, Dumonceau JM, Paspatis G, et al. Colorectal polypectomy and endoscopic mucosal resection (EMR): European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline. Endoscopy. 2017;49(3):270-97.
- Gijsbers KM, Laclé MM, Elias SG, Backes Y, Bosman JH, van Berkel AM, et al. Full-thickness scar resection after R1/Rx excised T1 colorectal cancers as an alternative to completion surgery. Am J Gastroenterol. 2022;117(4):647-53.
- Glynne-Jones R, Wyrwicz L, Tiret E, Brown G, Rödel C, Cervantes A, et al. Rectal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2017;28(suppl_4)
- Govaert JA, van Hazebroek EJ, Buis CI, et al. Multicenter Stratified Comparison of Hospital Costs Between Laparoscopic and Open Colorectal Cancer Resections: Influence of Tumor Location and Operative Risk. Ann Surg. 2017;266(6):1021-8.
- Guo K, Feng Y, Yuan L, Wasan HS, Sun L, Shen M, et al. Risk factors and predictors of lymph nodes metastasis and distant metastasis in newly diagnosed T1 colorectal cancer. Cancer Med. 2020;9(14):5095-113.
- Hassan C, Wysocki PT, Fuccio L, Seufferlein T, Dinis-Ribeiro M, Brandao C, et al. Endoscopic surveillance after surgical or endoscopic resection for colorectal cancer: ESGE and ESDO Guideline. Endoscopy. 2019;51(3):266-77.
- Huisman JF, Dang H, Moons LMG, Backes Y, Dik VK, Groen JN, et al. Diagnostic value of radiological staging and surveillance for T1 colorectal carcinomas: a multicenter cohort study. United European Gastroenterol J. 2023;11(6):551-63.
- Ichimasa K, Nakahara K, Kudo SE, Misawa M, Bretthauer M, Shimada S, et al. Novel "resect and analysis" approach for T2 colorectal cancer with use of artificial intelligence. Gastrointest Endosc. 2022;96(4):665-72.e1.
- Kawachi H, Eishi Y, Ueno H, Nemoto T, Fujimori T, Iwashita A, et al. A three-tier classification system based on the depth of submucosal invasion and budding/sprouting can improve the treatment strategy for T1 colorectal cancer: a retrospective multicenter study. Mod Pathol. 2015;28(6):872-9.
- Kajiwara Y, Oka S, Tanaka S, Nakamura T, Saito S, Fukunaga Y, et al. Nomogram as a novel predictive tool for lymph node metastasis in T1 colorectal cancer treated with endoscopic resection: a nationwide, multicenter study. Gastrointest Endosc. 2023;97(6):1119-28.e5.
- Kudo SE, Ichimasa K, Villard B, Mori Y, Misawa M, Saito S, et al. Artificial intelligence system to determine risk of T1 colorectal cancer metastasis to lymph node. Gastroenterology. 2020;158(3):744-53.e4.
- Naffouje SA, Lauwers G, Klapman J, Dam A, Pena L, Friedman M, et al. Malignant colon polyps: predicting lymph node metastasis following endoscopic excision. Int J Colorectal Dis. 2022;37(2):393-402.
- Oka S, Tanaka S, Kajiwara Y, Saito S, Fukunaga Y, Takamatsu M, et al. Treatment decision for locally resected T1 colorectal carcinoma-verification of the Japanese guideline criteria for additional surgery based on long-term clinical outcomes. Am J Gastroenterol. 2024.
- Ozeki T, Shimura T, Ozeki T, Ebi M, Iwasaki H, Kato H, et al. The risk analyses of lymph node metastasis and recurrence for submucosal invasive colorectal cancer: novel criteria to skip completion surgery. Cancers (Basel). 2022;14(3):557.
- Sandberg K, Holm T, Olsson I, et al. Bowel Dysfunction After Colon Cancer Surgery: A Prospective, Longitudinal, Multicenter Study. Dis Colon Rectum. 2024;67(1):85-94.
- Shaukat A, Kaltenbach T, Dominitz JA, Robertson DJ, Anderson JC, Cruise M, et al. Endoscopic recognition and management strategies for malignant colorectal polyps: recommendations of the US Multi-Society Task Force on Colorectal Cancer. Gastrointest Endosc. 2020;92(5):997-1015.e11.
- Tian Y, Rong L, Ma Y. Surgical resection after endoscopic resection in patients with T1 colorectal cancer: a meta-analysis. Int J Colorectal Dis. 2021;36(3):457-66.
- Van Oostendorp SE, Smits LJH, Vroom Y, Detering R, Heymans MW, Moons LMG, et al. Local recurrence after local excision of early rectal cancer: a meta-analysis of completion TME, adjuvant (chemo) radiation, or no additional treatment. J Br Surg. 2020;107(13):1719-30.
- Wang K, He H, Lin Y, Zhang Y, Chen J, Hu J, et al. A new clinical model for predicting lymph node metastasis in T1 colorectal cancer. Int J Colorectal Dis. 2024;39(1):46.
- Yan S, Ding H, Zhao X, Wang J, Deng W. Development and validation of a nomogram for further decision of radical surgery in pT1 colorectal cancer after local resection. Int J Colorectal Dis. 2021;36(7):1499-506.
Evidence tabellen
Samenvattingstabel van bevindingen uit systematische reviews en meta-analyses
|
Summary of findings: |
||||||
|
Additional surgical resection (ASR) after endoscopic resection compared to endoscopic resection only for patients with T1 colorectal cancer |
||||||
|
Patient or population: patients with T1 colorectal cancer |
||||||
|
Outcomes |
Anticipated absolute effects* (95% CI) |
Relative effect |
№ of participants |
Certainty of the evidence |
Comments |
|
|
Risk with endoscopic resection only |
Risk with additional surgical resection (ASR) after endoscopic resection |
|||||
|
Overall survival |
59 per 1.000 |
19 per 1.000 |
OR 0.31 |
1587 |
⨁◯◯◯ |
The evidence is very uncertain about the effect of additional surgical resection (ASR) after endoscopic resection on overall survival. |
|
Disease-specific survival |
20 per 1.000 |
14 per 1.000 |
OR 0.68 |
1045 |
⨁◯◯◯ |
The evidence is very uncertain about the effect of additional surgical resection (ASR) after endoscopic resection on disease-specific survival. |
|
Recurrence |
57 per 1.000 |
44 per 1.000 |
OR 0.76 |
1994 |
⨁◯◯◯ |
Additional surgical resection (ASR) after endoscopic resection may reduce/have little to no effect on recurrence but the evidence is very uncertain. |
|
Distant metastasis |
29 per 1.000 |
29 per 1.000 |
OR 0.99 |
1063 |
⨁◯◯◯ |
Additional surgical resection (ASR) after endoscopic resection may reduce/have little to no effect on distant metastasis but the evidence is very uncertain. |
|
Postoperative complications |
0 per 1.000 |
0 per 1.000 |
not estimable |
( studies) |
- |
No data available regarding postoperative complications from this systematic review. |
|
*The risk in the intervention group (and its 95% confidence interval) is based on the assumed risk in the comparison group and the relative effect of the intervention (and its 95% CI). |
||||||
|
GRADE Working Group grades of evidence |
||||||
Explanations
a. We downgraded the certainty of the evidence with two levels due to very serious risk of bias (methodological limitations).
b. We downgraded the certainty of the evidence with one level due to indirectness (patient population consists of both colon cancer patients and rectal cancer patients and patient population not restricted to those carrying factors of poorer prognosis (e.g., deeper invasion, positive lymph nodes).
c. We downgraded the certainty of the evidence with one levels due to imprecision (few events).
|
Summary of findings: |
||||||
|
Local resection versus surgical resection for high-risk T1 colorectal cancer |
||||||
|
Patient or population: patients with (high-risk) T1 colorectal cancer |
||||||
|
Outcomes |
Anticipated absolute effects* (95% CI) |
Relative effect |
№ of participants |
Certainty of the evidence |
Comments |
|
|
Risk with endoscopic resection only |
Risk with additional surgical resection (ASR) after endoscopic resection |
|||||
|
Overall survival |
59 per 1.000 |
111 per 1.000 |
HR 1.93 |
2560 |
⨁◯◯◯ |
The evidence is very uncertain about the effect of additional surgical resection (ASR) after endoscopic resection on overall survival. |
|
5-year overall survival |
59 per 1.000 |
49 per 1.000 |
HR 2.50 |
2560 |
⨁◯◯◯ |
The evidence is very uncertain about the effect of additional surgical resection (ASR) after endoscopic resection on 5-year overall survival. |
|
Disease-specific overall survival |
20 per 1.000 |
46 per 1.000 |
HR 2.31 |
2121 |
⨁◯◯◯ |
The evidence is very uncertain about the effect of additional surgical resection (ASR) after endoscopic resection on disease-specific overall survival. |
|
5-year disease specific overall survival |
20 per 1.000 |
22 per 1.000 |
HR 1.09 |
2121 |
⨁◯◯◯ |
The evidence is very uncertain about the effect of additional surgical resection (ASR) after endoscopic resection on 5-year disease-specific overall survival. |
|
Recurrence free survival |
57 per 1.000 |
186 per 1.000 |
HR 3.51 |
2674 |
⨁◯◯◯ |
The evidence is very uncertain about the effect of additional surgical resection (ASR) after endoscopic resection on recurrence free survival. |
|
5-year recurrence |
57 per 1.000 |
133 per 1.000 |
OR 2.44 |
2671 |
⨁◯◯◯ |
The evidence is very uncertain about the effect of additional surgical resection (ASR) after endoscopic resection on 5-year recurrence free survival. |
|
Distant metastasis |
0 per 1.000 |
0 per 1.000 |
not estimable |
( studies) |
- |
No data available regarding distant metastasis from this systematic review. |
|
Postoperative complications |
0 per 1.000 |
0 per 1.000 |
not estimable |
( studies) |
- |
No data available regarding postoperative complications from this systematic review. |
|
*The risk in the intervention group (and its 95% confidence interval) is based on the assumed risk in the comparison group and the relative effect of the intervention (and its 95% CI). |
||||||
|
GRADE Working Group grades of evidence |
||||||
Explanations
a. We downgraded the certainty of the evidence with two levels due to very serious risk of bias (methodological limitations).
b. We downgraded the certainty of the evidence with one level due to indirectness (patient population consists of both colon cancer patients and rectal cancer patients and patient population not restricted to those carrying factors of poorer prognosis (e.g., deeper invasion, positive lymph nodes).
c. We downgraded the certainty of the evidence with one levels due to imprecision (few events).
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 24-03-2025
Beoordeeld op geldigheid : 18-03-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodules werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodules.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met colorectaal carcinoom. Deze werkgroep is ingesteld in het kader van het cluster oncologie onderste tractus digestivus.
De huidige samenstelling van de werkgroep
- Prof. dr. P.J. (Pieter) Tanis, gastrointestinaal en oncologisch chirurg, Erasmus MC, Rotterdam, NVvH (voorzitter)
- Dr. T.S. (Tjeerd) Aukema, chirurg, HagaZiekenhuis, Den Haag, NVvH
- Dr. J.W.A. (Pim) Burger, chirurg, Catharina Ziekenhuis, Eindhoven, NVvH
- Dr. M. (Myriam) Chalabi, internist, Antoni van Leeuwenhoek, Amsterdam, NIV/NVMO
- S. (Silvie) Dronkers, stichting Darmkanker
- S. Dokter (Simone) MSc., verpleegkundig specialist, Antoni van Leeuwenhoek, Amsterdam, V&VN
- Dr. D.J.A. (Derk Jan) de Groot, internist-oncoloog, UMC Groningen, Groningen, NIV/NVMO
- Dr. E.C. (Elske) Gootjes, internist-oncoloog, Radboud UMC, Nijmegen, NIV/NVMO
- Dr. M.P.W. (Martijn) Intven, radiotherapeut, UMC Utrecht, Utrecht, NVRO
- Dr. M. (Miranda) Kusters, colorectaal chirurg, AmsterdamUMC, Amsterdam, NVvH
- Dr. M.M. (Miangela) Laclè, patholoog, UMC Utrecht, Utrecht, NVvP
- Dr. M.M. (Marilyne) Lange, patholoog, AmsterdamUMC, Amsterdam, NVvPathologie
- Dr. H.A.A.M. (Huub) Maas, klinisch geriater, Elisabeth-TweeSteden Ziekenhuis, Tilburg, NVKG
- Dr. M. (Monique) Maas, radioloog, Nederlands Kanker Instituut, Amsterdam, NVvR (vice-voorzitter)
- Dr. L. (Leon) Moons, MDL-arts, UMC Utrecht, Utrecht, NVMDL
- Prof. dr. I.D. (Iris) Nagtegaal, patholoog, Radboud UMC, Nijmegen, NVvP
- Dr. J.M.L. (Jeanine) Roodhart, internist-oncoloog, UMC Utrecht, Utrecht, NIV/NVMO
- Dr. M. (Mark) Roef, nucleair geneeskundige, Catharina Ziekenhuis, Eindhoven, NVNG
- Dr. M. (Maarten) Smits, radioloog, UMC Utrecht, Utrecht, NVvR
- I. (Iris) van der Veeken MSc., coloncare verpleegkundige, Flevoziekenhuis, Almere, V&VN
- Prof. dr. C. (Kees) Verhoef, oncologisch chirurg, Erasmus MC, Rotterdam, NVvH
- Dr. K.S. (Kathelijn) Versteeg, internist-oncoloog, AmsterdamUMC, Amsterdam, NIV/NVMO
- Dr. M. (Marianne) de Vries, abdominaal radioloog, Erasmus MC, Rotterdam, NVvR
- Dr. M.L. (Miriam) Wumkes, internist, Jeroen Bosch Ziekenhuis, ’s-Hertogenbosch, NIV/NVMO
Voormalig betrokken werkgroepleden
- Dr. M.E. (Marije) Hamaker, klinisch geriater, Diakonessenhuis, Utrecht, NVKG
- Dr. P. (Petur) Snaebjornsson, patholoog, Nederlands Kanker Instituut, Amsterdam, NVvP
- Dr. H.M.W. (Henk) Verheul, internist-oncoloog, Radboudumc, Nijmegen, NIV/NVMO
- Dr. H.L. (Erik) van Westreenen, chirurg, Isala Zwolle/ Isala Diaconessenhuis, Zwolle/Meppel, NVvH
Met ondersteuning van
- Dr. D. (Dagmar) Nieboer, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. R.J.S. (Rayna) Anijs, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- I. (Ingeborg) van Dusseldorp, medisch informatiespecialist, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoek financiering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Er is vastgesteld dat het niet mogelijk was werkgroepleden af te vaardigen met voldoende expertise zonder potentiële belangenverstrengeling. Het gaat daarbij met name om werkgroepleden die deelnemen aan de aanvraag voor de CROSSROADS-studie. Gedurende de ontwikkeling van de module 5.2 (complementerende oncologische resectie na lokale excisie van pT1-T2 coloncarcinoom) heeft daarom afstemming plaatsgevonden tussen de werkgroepvoorzitter, de belangencommissie van het Kennisinstituut van de Federatie Medisch Specialisten over passende acties naar aanleiding van de gemelde belangen.
Restricties voor de module over het onderwerp Module 5.2 Complementerende oncologische resectie na lokale excisie van pT1-2 coloncarcinoom waar de directe belangen (onderzoek aanvraag CROSSROADS) betrekking op hebben:
- Werkgroep lid werkt niet als enige inhoudsdeskundige aan de module;
- Werkgroep lid werkt tenminste samen met een werkgroep lid met een vergelijkbare expertise in alle fasen (zoeken, studieselectie, data-extractie, evidence synthese, Evidence-to-decision, aanbevelingen formuleren) van het ontwikkelproces. Indien nodig worden meer werkgroepleden geworven;
- In alle fasen van het ontwikkelproces is een onafhankelijk methodoloog betrokken;
- Overwegingen en aanbevelingen worden besproken en vastgesteld tijdens een werkgroep vergadering onder leiding van een onafhankelijk voorzitter (zonder gemelde belangen).
Wellicht ten overvloede willen wij erop wijzen dat medisch specialistische richtlijnen niet worden vastgesteld door de betreffende richtlijnwerkgroep maar door de besturen/ledenvergadering van de betrokken verenigingen.
Een overzicht van de belangen van werkgroep leden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke Financiële Belangen |
Persoonlijke Relaties |
Extern gefinancierd onderzoek |
Intell. belangen en reputatie |
Overige belangen |
Ondernomen acties |
|
Prof. Dr. P.J. (Pieter) Tanis |
Chirurg, Erasmus MC |
Lid clinical audit board Dutch ColoRectal Audit, onbetaald |
Geen te vermelden. |
Geen |
Meerdere klinische multicenter trials: |
Geen |
Geen |
Deelname aan de CROSSROADS studie, zie ‘werkwijze ent oelichting van belangen’ |
|
dr. M. (Miranda) Kusters |
Colorectaal chirurg, Amsterdam UMC |
Geen |
Geen |
Geen |
KWF - Snapshot rectumcarcinoom - Projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. H.L. (Erik) van Westreenen |
Chirurg, Isala Zwolle |
Geen |
Geen |
Geen |
* KWF - Complex Colon Carcinoom - Projectleider |
Geen |
Geen |
Deelname aan de CROSSROADS studie, zie ‘werkwijze ent oelichting van belangen’ |
|
Prof. Dr. C. (Kees) Verhoef |
Hoofd Gastro-Intestinale en Oncologische Chirurgie, Erasmus MC |
Bestuur Familiehuis, onbetaald |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
dr. J.W.A. (Pim) Burger
|
Chirurg in het Catharina Ziekenuis Eindhoven, vrijgevestigd, full time |
Geen |
Geen |
Geen |
* ZonMW - Multidisiplinaire zorg - Geen Projectleider |
Ik werk in een tertair verwijscentrum voor patienten met lcoally advanced rectumcarcinoom en patienten met peritoneale metastasen. Hieronder valt ook het anuscarcinoom. |
Geen |
Geen acties ondernomen |
|
dr. K.S. (Kathelijn) Versteeg |
Internist-oncoloog en ouderengeneeskunde |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M.L. (Miriam) Wumkes
|
Internist-oncoloog Jeroen Bosch ziekenhuis (vrijgevestigd, betaald) |
Voorzitter oncologiecommissie JBZ, betaald |
Niet van toepassing |
Niet van toepassing |
Lokale PI van onderzoek in JBZ, geen projectleider. |
niet van toepassing. |
2019 Advies raad maagcarcinoom, Servier |
Geen acties ondernomen |
|
dr. M. (Myriam) Chalabi |
Internist-oncoloog, Antoni van Leeuwenhoek |
Geen |
Geen |
Geen |
* BMS - neoadjuvante * roche - neoadjuvante radiotherapie,immuuntherapie en bevacizumab bijrectumcarcinoom (Projectleider JA) * agenus - neoadjuvante immuuntherapie pan-cancer (Projectleider, ) * roche - neoadjuvante immuuntherapie bij * MSD - neoadjuvante
|
Geen |
Geen actie |
Geen acties ondernomen |
|
Dr. D.J.A. (Derk-Jan) de Groot |
Internist oncoloog, UMC Groningen |
Geen |
Geen |
Geen |
zie onder: |
Geen |
Geen |
Geen acties ondernomen |
|
dr. J.M.L. (Jeanine) Roodhart |
internist-oncoloog, UMC Utrecht |
ONCODE clinical advisory board |
geen persoonlijke; geen betalingen aan mij als persoon voor deelname adviesraden, wel betalingen aan afdeling voor adviesraden/spreken door diverse farma en onderzoeksprojecten betaald door farma. |
nee |
ja: |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M.E. (Marije) Hamaker |
Klinisch geriater Diakonessenhuis |
NTVG sectieredacteur - onbetaald |
Geen |
Geen |
Europese Commissie - Nieuw zorgpad voor ouderen met kanker - Geen projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Prof. Dr. M.P.W. (Martijn) Intven |
Radiotherapeut-Oncoloog UMC Utrecht |
- Voorzitter Nederlandse Vereniging voor radiotherapie en Oncologie, onbetaald |
Geen |
Geen |
KWF - Pancreascarcinoom - Projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. M. (Mark) Roef |
Nucleair geneeskundige, Catharina Ziekenhuis Eindhoven |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. M. (Monique) Maas |
Radioloog bij NKI-AVL |
Redacteur nascholingsblad 'Imago'; hiervoor ontvang ik een vergoeding 1x per jaar |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M.L.K. (Maarten) Smits |
Interventieradioloog, UMC Utrecht |
- Voorzitter wetenschapscommissie Nederlandse Vereniging voor Interventieradiologie (onbetaald) |
Geen |
Geen |
* Terumo / Quirem Medical - HEPAR primary study, radioembolization for patients with hepatocellular carcinoma - Geen projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M. (Marianne) de Vries |
Erasmus MC Radiologie Rotterdam: Radioloog (betaald) |
colorectale richtlijn meeschrijven en lezen (betaald) |
Geen |
Geen (niet dat ik weet) |
Alleen meewerken aan multicenter studies maar niet als hoofdonderzoeker en krijg daar geen geld voor (bijvoorbeeld SNAPshot studie AVL of PELVEX studie) |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. L.M.G. (Leon Moons) |
MDL arts, UMC Utrecht |
Geen |
consultant voor Boston Scientific |
Geen persoonlijke relaties met een belang |
Alleen KWF, ZonMW en MLDS gesponsorde onderzoeken: ZonMw CROSSROADS: behandelstrategie na lokale excisie pT1-2 coloncarcinoom, gestratificeerd voor lymfkliermetastase risico- projectleider |
Voorzitter T1 CRC werkgroep |
Geen |
Deelname aan de CROSSROADS studie, zie ‘werkwijze ent oelichting van belangen’ |
|
Prof. Dr. I.D. (Iris) Nagtegaal |
Hoogleraar Pathologie, Radboudumc |
Voorzitter Stichting Palga (detachering) |
Geen |
Geen |
ja diverse wetenschappelijke projecten van verschillende fondsen: |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M.M. (Marilyne) Lange |
Patholoog Amsterdam UMC |
Geen betaalde nevenwerkzaamheden |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
I. (Iris) van Veeken |
verpleegkundige - Flevoziekenhuis |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
S.Y.A. (Silvie) Dronkers MA |
Stichting Darmkanker |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Deelname aan de CROSSROADS studie, zie ‘werkwijze ent oelichting van belangen’ |
|
prof. dr. P. (Petur) Snaebjornsson |
Patholoog Antoni van Leeuwenhoek en professor aan de Universiteit van Ijsland |
Bestuur Expertisegroep GE pathologie van NVVP sinds 2021 (sectie lower GI, onbetaald), bestuur DCCG 2018-2022 (onbetaald), les pathasseropleiding in Hogeschool van Leiden sinds 2019 (betaald), Richtlijncommissie PTO sinds 2022 (voorzitter, vacatiegelden), bestuur CUPP-NL sinds 2021 (onbetaald) |
Geen |
Geen |
Betrokken bij diverse projecten door KWF geinanficeerde (niet PI), waaronder COLOPEC 1 en 2, CAIRO5, CAIRO6, snapshot complex colon cancer, FAPI/PET bij peritoneale metastasen. Betrokken bij onderzoeken gefinanceerd door RANNIS (Ijslands fonds) voor studies (mutaties in normaal darnmslijmvlies, als PI) en mutaties in Lynch syndroom tumoren (niet PI). Betrokken bij DISCO trial gefinanceerd door Zonmw (niet PI). |
Geen |
Op 28-09-2022: deelname als expert aan nascholing Colorectaal carcinoom (talkshow). Georganiseerd door MEDtalks. Hiervoor betaling aan ALV. |
Geen acties ondernomen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door het uitnodigen van Stichting Darmkanker en de Nederlandse Federatie van Kankerpatiëntenorganisaties (NFK) voor de invitational conferences in 2017 en 2023. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. Daarnaast zijn deze patiëntenorganisaties in de commentaarfase uitgenodigd om modules mee te lezen, te becommentariëren en de werkgroep van feedback vanuit het patiënten perspectief voorzien.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
|
Module |
Uitkomst raming |
Toelichting |
|
n.v.t. |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling niet breed toepasbaar is (<5.000 patiënten) en daarom naar verwachten geen substantiële financiële gevolgen zal hebben voor de collectieve uitgaven. |
|
Alle modules |
Geen financiële gevolgen |
Hoewel het niet duidelijk is of de aanbeveling breed toepasbaar is, volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodules zijn opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase in 2017 inventariseerde de werkgroep knelpunten en de werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (NVRO, 2014) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door verschillende partijen via een invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Medio 2023 is het grootste deel van de richtlijn herzien en worden nieuwe modules of herzieningen door de werkgroep besproken indien de werkgroep:
- Signalen krijgt van (nieuwe) knelpunten in de zorg voor patiënten met colorectaal carcinoom die geadresseerd dienen te worden in de richtlijn;
- Signaleert dat er nieuwe onderzoeksresultaten zijn die relevant zijn voor de richtlijn;
- Constateert dat er tekstuele verbeteringen of aanvullingen nodig zijn in de richtlijn om de bruikbaarheid of volledigheid van de richtlijn te verbeteren.
De werkgroep bespreekt welke aanvullingen of herzieningen geprioriteerd dienen te worden en stelt evt. passende (nieuwe) uitgangsvragen op. De werkroep bepaalt de prioriteit van aanvullingen of herzieningen op basis van: (1) klinische relevantie, (2) de beschikbaarheid van nieuwe evidence, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten.
Uitkomstmaten
De werkgroep inventariseerde per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij men zowel naar gewenste als ongewenste effecten keek. De werkgroep baseerde de keuze voor uitkomstmaten mede op basis van de “core outcome set” gepubliceerd door Zerillo (2017). De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden. Hiervoor sloot de werkgroep zich, waar mogelijk, aan bij de grenzen voor klinische besluitvorming volgens de PASKWIL criteria uit 2023. Wanneer er geen grenzen voor klinische besluitvorming conform de PASKWIL criteria geformuleerd konden worden (bijvoorbeeld bij non-inferioriteitsvraagstukken) werden de standaard GRADE grenzen gehanteerd, tenzij anders vermeld.
Strategie voor zoeken en selecteren van literatuur
De werkgroep raadpleegde voor de afzonderlijke uitgangsvragen reeds gepubliceerde systematische reviews (SRs). SRs kwamen in aanmerking indien: i) systematisch was gezocht in één of meerdere databases; ii) transparante in- en exclusiecriteria zijn toegepast en iii) idealiter de kwaliteit van de geïncludeerde literatuur was beoordeeld. De voor de uitgangsvragen relevante internationale richtlijnen en consensusdocumenten werden eveneens geraadpleegd. Overige literatuur, waar niet systematisch naar werd gezocht, is als bewijsvoering in de overwegingen opgenomen.
Relevante beschikbare populatiegegevens uit Nederland in de periode 2000-2022 werden gebruikt voor het bepalen van knelpunten, praktijkvariatie en externe validiteit van internationale richtlijnen en gepubliceerde literatuur.
Kwaliteitsbeoordeling individuele studies
De (risk of bias) kwaliteitsbeoordelingen van de individuele studies uit de gebruikte SRs werden gebruikt, tenzij deze afwezig waren of onbruikbaar waren voor het beoordelen van de kracht van het wetenschappelijke bewijs. Indien afwezig of onbruikbaar werd aangenomen dat er een risico op bias aanwezig zou kunnen zijn. In enkele gevallen, wanneer studies informatie verschaften over de cruciale uitkomstma(a)t(en), werd er een nieuwe kwaliteitsbeoordeling van individuele studies uitgevoerd.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van de geselecteerde SRs werden weergegeven in ‘Summary of Findings’ tabellen. De belangrijkste bevindingen uit de literatuur werden kort beschreven onder “Samenvatting literatuur” (kopjes “Samenvatting van internationale richtlijnen en consensusdocumenten” en “Samenvatting van systematische reviews en meta-analyses”) en onder “Overwegingen”. Bestaande meta-analyses uit de gebruikte systematische reviews werden beschreven. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek (te vinden in de ‘Summary of Findings’ tabellen). De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling beargumenteerd hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Indicatorontwikkeling
De werkgroep conformeert zich aan de SONCOS normen en de DICA-DCRA indicatoren. De werkgroep ontwikkelde geen interne kwaliteitsindicatoren om het toepassen van de richtlijn in de praktijk te volgen en te versterken.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule wordt aan de betrokken wetenschappelijke verenigingen en (patiënt)organisaties voorgelegd ter commentaar. De commentaren worden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren wordt de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule wordt aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zerillo JA, Schouwenburg MG, van Bommel ACM, Stowell C, Lippa J, Bauer D, Berger AM, Boland G, Borras JM, Buss MK, Cima R, Van Cutsem E, van Duyn EB, Finlayson SRG, Hung-Chun Cheng S, Langelotz C, Lloyd J, Lynch AC, Mamon HJ, McAllister PK, Minsky BD, Ngeow J, Abu Hassan MR, Ryan K, Shankaran V, Upton MP, Zalcberg J, van de Velde CJ, Tollenaar R; Colorectal Cancer Working Group of the International Consortium for Health Outcomes Measurement (ICHOM). An International Collaborative Standardizing a Comprehensive Patient-Centered Outcomes Measurement Set for Colorectal Cancer. JAMA Oncol. 2017 May 1;3(5):686-694. doi: 10.1001/jamaoncol.2017.0417. PubMed PMID: 28384684.