Locoregionale stadiëring coloncarcinoom
Uitgangsvraag
Welke beeldvorming dient gebruikt te worden voor locoregionale stadiëring van het coloncarcinoom?
De uitgangsvraag omvat de volgende deelvragen:
- Wat is de accuratesse van preoperatieve beeldvorming voor de differentiatie tussen wel of geen lokaal gevorderd (T3cd-T4) coloncarcinoom en de aanwezigheid van positieve lymfklieren in het algemeen en in het D3 gebied in het bijzonder?
- Met welke beeldvorming dient de aanwezigheid van positieve lymfklieren in het algemeen en in het D3 gebied in het bijzonder bepaald te worden?
- Wat dient gerapporteerd te worden in het radiologisch verslag?
Aanbeveling
Gebruik CT voor de locoregionale stadiëring van het coloncarcinoom, maar verricht geen CT- scan na lokale excisie van een laag risico T1 carcinoom.
Benoem centraal gelegen lymfeklieren rondom de a. mesenterica inferior bij linkszijdig coloncarcinoom als D3 locoregionale lymfklieren, en niet als para-aortale lymfklieren.
Beoordeel de volgende items bij locoregionale stadiering van een coloncarcinoom: locatie, lengte, morfologie ((semi)circulair, poliep), cT-stadium, cN-stadium (cN0 of cN+ en bij cN+ aan- of afwezigheid van pathologische D3 klieren), relatie tot de mesocolische fascie bij T3 (MCF+, MCF-), EMVI, tumor deposities, en complicaties van de tumor.
Overwegingen
De gezamenlijke specificiteit van 70% voor het T3cd-4 stadium bij stadiëring met CT (Nerad, 2016) wil dus zeggen dat de kans op overstadiëring middels CT bij bijna 1/3 van de patiënten optreedt. Dit probleem van vals positieve resultaten wordt vermoedelijk veroorzaakt doordat minimale pericolische desmoplastische vet stranding lastig te onderscheiden is van tumor en daarom door radiologen wordt geïnterpreteerd als tumor doorgroei. Sommige (kleinere) studies die MRI gebruiken laten wel veelbelovende resultaten zien, al blijft het ook voor MRI uitdagend om desmoplastische reactie te onderscheiden van echte tumor doorgroei.
In de literatuur is veel informatie beschikbaar over cTN status, echter er zijn weinig studies die hebben gekeken naar cT3cd-T4 status. Verder zijn er weinig studies die MRI met CT bij coloncarcinoom hebben vergeleken. De relatief grotere studie van 116 patiënten van Liu uit 2019 die MR met CT heeft vergeleken voor lokale stadiëring van sigmoïd en colon descendens carcinoom heeft gekeken naar cT3-4, EMVI+, N+ (Liu, 2019). Zij laten wel zien dat MRI beter is dan CT om het cT-stadium te bepalen: sensitiviteit van 69,8 % voor MRI (bij 81 van 116 patiënten) versus 56,9 % voor CT. Zij hebben niet gekeken naar cT3cd-T4 status, ook hadden ze geen multi-planar reconstructies voor CT beschikbaar (dit laatste zou de kwaliteit voor CT verbeteren). Mogelijk kan het cT-stadium nauwkeuriger op een CT colonografie worden bepaald door betere distensie van het colon (Nerad, 2016; Horvat, 2019). Voor cT3 tumoren is het van belang om de relatie tot de mesocolische fascie posterieur te rapporteren. Dit wordt ook wel de retroperitoneale chirurgische marge of circumferentiele resectie marge genoemd. In analogie aan het rectumcarcinoom wordt hiervoor ook de afkapwaarde van ≤ 1 mm gebruikt, waarbij voor CT een accuratesse van 80% wordt gerapporteerd (Seo, 2023). Een positieve mesocolische fascie is een onafhankelijke voorspeller voor een slechtere ziektevrije overleving (HR 3,36; 95% CI 1,71- 6,59). Eveneens conform het rectumcarcinoom, moet bij een bedreigde of positieve mesocolische fascie de indicatie voor een multiviscerale resectie worden beoordeeld, waarbij omliggend weefsel (bijvoorbeeld buikwand, fascie van Gerota, psoas, segment ureter) en bloc moet worden meegenomen voor een radicale resectie.
In de literatuur is het nog niet eenduidig wat de beste radiologische criteria zijn om pathologische klieren op te sporen aangezien de meest gebruikte criteria vorm en diameter niet nauwkeurig genoeg zijn. Er zijn veel studies die verschillende criteria uitgeprobeerd hebben (heterogene aankleuring, ADC-waarde op MRI, heterogene begrenzing, korte as, lengte as, clusters van klieren, radiomics). Daarbij zijn er ook geen diagnostische studies die gekeken hebben naar exacte locatie van de klieren (D1-D3). In het standaard verslag colon tumor is de definitie van pathologische klieren daarom niet exact bepaald. Opvallend is dat er ook in de literatuur/richtlijnen zeer weinig/geen radiologische gestructureerde standaardverslagen over colon tumoren zijn (Pedersen, 2020). Er zijn vooral gestructureerde verslagen van de MRI bij rectum tumoren gepubliceerd. Ten aanzien van de locatie wordt geadviseerd om bij cN+ alleen aan te geven of er al dan niet pathologische D3 lymfklieren aanwezig zijn, omdat dit consequenties heeft voor de uitgebreidheid van de resectie. Pathologische lymfklieren in het D3 gebied zijn zeldzaam; een cohortstudie vond dit bij 3 van 197 patiënten met als criteria korte-as diameter ≥ 8 mm, interne heterogeniteit of irregulaire begrenzing (Sammour, 2020). Maar indien deze aanwezig zijn, moet de resectie worden uitgebreid van een standaard CME-D2 resectie naar een CME-D3 dissectie (module 5.3), wat ook een reden kan zijn voor verwijzing naar een expertise centrum.
CT heeft een lage diagnostische accuratesse voor het bepalen van lymfkliermetastasering op basis van diameter (cN+). In een systematische review en meta-analyse van Nerad (2016) waren de sensitiviteit, specificiteit en OR respectievelijk 71% (95% CI, 59 tot 81%), 67% (95% CI, 46 tot 83%), en 4,8 (95% CI, 2,5 tot 9,4). Dit laat zien dat de diameter geen betrouwbare indicator is om pathologische versus niet- pathologische klieren te onderscheiden (Nerad, 2016). Andere parameters kunnen worden meegenomen in de beoordeling (zoals vorm, begrenzing en heterogeniteit), maar zijn evenmin betrouwbaar voor klierdiagnostiek. Om te streven naar meer uniformiteit in de beoordeling van het cN stadium, heeft de werkgroep besloten om toch een afkapwaarde voor de korte as van zichtbare lymfklieren in het mesocolon in te voeren voor cT3-4 tumoren, waarbij suspect gedefinieerd is als ≥8mm. Wees terughoudend bij de beoordeling van kliermetastasen bij T2 tumoren, aangezien kliermetastasen in deze groep veel minder vaak voorkomen. Ook bij gevorderde tumoren kan er sprake zijn van reactieve benigne klieren gezien, waardoor overstadiering kan voorkomen. Gezien het relatief frequent voorkomen van overstadiering en de daardoor matige accuratesse, wordt analoog aan het rectumcarcinoom geadviseerd om de klierstatus te rapporteren als cN0 of cN+ en niet te subclassificeren in cN1 en cN2.
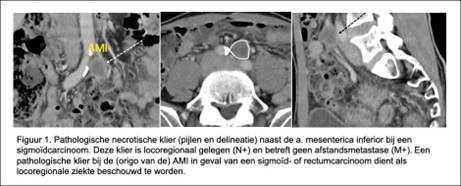
Een belangrijke valkuil bij sigmoïdtumoren (evenals bij rectumcarcinoom) is om klieren rond de origo van de arteria mesenterica inferior foutief te interpreteren als para-aortaal gelegen (met als consequentie het foutief stadieren van M1-ziekte). Het is daarom belangrijk om goed te beoordelen wat de locatie is van dergelijke klieren en klieren bij de origo van de AMI als locoregionaal te beschouwen (zie Figuur 1), (Storm, 2019).
Ook in geval van andere locaties van coloncarcinoom liggen klieren in het D3 compartiment soms dichtbij de aorta en in deze gevallen moet de radioloog ook locoregionale klieren onderscheiden van daadwerkelijke para-aortale (M1) klieren. De prevalentie van geïsoleerde para-aortale lymfadenopathie is laag (<2%, Kim 2019) en de consequenties zijn groot indien een D3 klier als M1 ziekte wordt gestadieerd.
Daarnaast is het onderscheid tussen wel of geen pathologische D3 klieren van belang voor de uitgebreidheid van de chirurgie: een D3 dissectie vindt niet routinematig plaats, maar op indicatie indien op beeldvorming maligne D3 klieren gezien worden. Hierbij geldt wederom dat de prevalentie laag is en overstadiering veel voorkomt, waar de radioloog rekening mee dient te houden in de beoordeling.
Naast de TNM-stadiëring kan ook naar de extramurale veneuze invasie (EMVI) en tumor deposities gekeken worden als eventuele prognostische ongunstige kenmerken die de behandelkeuze zouden kunnen bepalen. Dit blijkt onder andere bij een grote studie van 400 patiënten met sigmoïd carcinoom de sterkste prognostische voorspeller voor slechtere ziektevrije overleving vergeleken met TNM-stadium (D'Souza, 2019). Dit wordt ook gezien in een review van MRI bij het rectumcarcinoom (Lord, 2019). Accuratesse van CT voor tumor deposities en EMVI was 88% en 73% in een studie van Karahacioglu et al. (Karahacioglu, 2024). In een Nederlandse studie werd gevonden dat bij CT gedetecteerde EMVI en tumor deposities, er in 96% sprake was van een lokaal gevorderde tumor (van den Berg, 2024).
Stadiëring bij T1 coloncarcinoom
Een CT-abdomen heeft geen meerwaarde bij het inschatten van de mogelijkheid tot een lokale excisie in het colon (Module Endoscopische of chirurgische lokale excisie vroegcarcinoom colon). Bij de selectie van T1 coloncarcinomen voor een lokale excisie is optische diagnostiek tijdens endoscopie leidend.
Gezien de lage kans op lymfkliermetastasen en synchrone afstandsmetastasen bij het T1 coloncarcinoom zonder histologische risicofactoren (Dang, 2020), wordt geadviseerd alleen een CT te verrichten ter stadiering bij een coloncarcinoom met een of meer histologische risicofactoren voor lymfkliermetastasen (zie module Histologische risicofactoren bij T1 CRC), of wanneer besloten wordt tot een primaire oncologische segmentresectie. Voor volledige stadiëring wordt dan een CT thorax/abdomen geadviseerd. Na een lokale excisie is er bovendien kans op vergrote reactieve klieren die foutief voor pathologische klieren kunnen worden aangezien. Daarom wordt geadviseerd om geen CT te doen na lokale excisie van een laag risico T1 coloncarcinoom.
Samenvatting van nationale data en populatiestudies
Er zijn geen relevante populatiestudies gevonden die betrekking hebben op de PICO.
Onderbouwing
Stadiëring van het coloncarcinoom wordt gedaan middels CT thorax/abdomen. Echter lokaal gevorderde coloncarcinomen komen mede sinds de FOxTROT (Fluoropyrimidine, Oxaliplatin and Targeted-Receptor pre-Operative Therapy) studie steeds meer in aanmerking voor neoadjuvant chemo(radio)therapie. Er is daarnaast analoog aan het rectumcarcinoom toenemend aandacht voor extramurale veneuze invasie (EMVI) en tumor deposities, als slecht prognostische factoren die mogelijk behandel consequenties zouden kunnen hebben.
Voor T3 tumoren is het van belang voor de uitgebreidheid van de resectie of de tumor al dan niet doorgroeit tot aan de mesocolische fascie (MCF) posterieur. Daarnaast speelt de discussie over uitgebreidheid van de verticale lymfklierdissectie bij het coloncarcinoom. Een complete mesocolische excisie (CME) met centrale vasculaire ligatie (CVL optimale D2 lymfklierdissectie) is de standaard, maar selectieve D3 (=centrale) lymfklierdissectie zou kunnen worden overwogen indien er klinisch verdachte centrale lymfklieren aanwezig zijn op de preoperatieve beeldvorming. Daarom wordt het steeds belangrijker om zo nauwkeurig mogelijk het exacte stadium en hoog risico kenmerken pre-operatief te bepalen.
Samenvatting van internationale richtlijnen en consensusdocumenten
SIGN, NICE, en EURECCA geven in het algemeen aan om coloncarcinoom preoperatief te stadiëren middels CT. Zij maken geen onderscheid tussen lokaal gevorderd T3cd-T4 of niet. De Japanse Society voor colon- en rectumcarcinoom (JSCCR) richtlijn 2016 raadt aan om de uitgebreidheid van lymfeklier resectie te bepalen op basis van de preoperatieve klinische gegevens, uitgebreidheid van lymfekliermetastase(n) en de tumor doorgroei die intra- operatief wordt bepaald. Als er lymfklier metastasering op beeldvorming/peroperatief is gezien, dan raden zij aan een D3 dissectie te doen (Watanabe, 2017).
Samenvatting van systematische reviews en meta-analyses
cT stadium
De meta-analyse over CT van Nerad (2016) toont een sensitiviteit, specificiteit en diagnostische odds ratio (OR) voor detectie van tumordoorgroei door de wand van 5 mm of meer (T3cd–T4) van, respectievelijk, 77% (95% CI, 66 tot 85%), 70% (95% CI, 53 tot 83%), en 7.8 (95% CI, 4.2 tot 14.2).
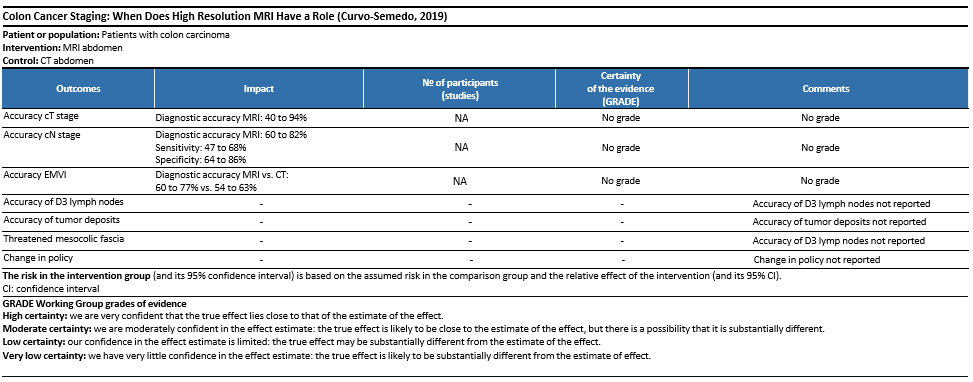
De review van Curvo-Semedo (2019) laat zien dat de rol van MRI bij stadiëring van het coloncarcinoom beperkt is. De diagnostische accuratesse voor identificatie van T3cd-T4
tumoren middels MRI varieert sterk:40 tot 93% (Curvo-Semedo, 2019).
cN stadium
CT heeft een lage diagnostische accuratesse voor het bepalen van lymfklier metastasering op basis van diameter (cN+). De sensitiviteit, specificiteit en OR waren respectievelijk 71% (95% CI, 59 tot 81%), 67% (95% CI, 46 tot 83%) en 4.8 (95% CI, 2.5 tot 9.4) (Nerad 2016). Andere parameters kunnen worden meegenomen in de beoordeling (zoals vorm, begrenzing en heterogeniteit), maar zijn evenmin betrouwbaar voor klierdiagnostiek.
De review van Curvo-Semedo (2019) toont dat de diagnostische accuraatheid van MRI voor detectie van pathologische lymfeklieren (cN+) ongeveer 60 tot 82% bedraagt. Een studie van deze review toonde een sensitiviteit en specificiteit van 47 tot 68% en 64 tot 86 %. Criteria voor pathologische klieren varieerden tussen deze studies: korte as ≥ 8mm, en/of cluster van 3 of meer klieren met diameter van > 5 mm, anderen gebruikten 10 mm of irregulaire begrenzing of heterogeen signaal. Geen enkele van deze studies maakte onderscheid in de locatie van de klieren (D1-D3) (Figuur 1).
In de literatuur zijn er geen systematische review van studies die CT direct met MRI vergelijken.
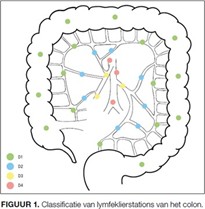
Figuur 1. Classificatie van lymfeklierstations van het colon (Storm NTVO, 2019)
D1 betreft klieren lokaal vlak bij de tumor. D3 klieren liggen centraal langs de oorsprong van de vaatwortels (arteria mesenterica superior en inferior). D2 lymfeklieren liggen mesenteriaal dus tussen D1 en D3 in. D4 zijn para-aortale klieren en deze worden geclassificeerd als afstandsmetastasen (M1 ziekte). D3 voor linkszijdige tumoren zijn lymfeklieren centraal langs de origo van de a. mesenterica inferior/of a. colica sinistra. Voor rechtszijdige tumoren zijn dit lymfeklieren langs de a. en v. mesenterica superior. Let op: pathologische klieren van het sigmoïd die bij de inmonding van de arteria mesenterica inferior zijn gelegen moeten nog wel locoregionaal worden beschouwd en niet als para-aortale klieren worden benoemd (dus geen M1 ziekte)
Extramurale vene invasie (EMVI)
In de literatuur is er een trend dat EMVI iets beter op de MRI kan worden beoordeeld dan op CT: de diagnostische accuratesse voor MRI bedraagt 60 tot 77 % versus 54 tot 63 % voor CT. Gezien de relatief lage accuratesse blijft het dus lastig om het verschil te maken tussen daadwerkelijke veneuze invasie en desmoplastische of inflammatoire veranderingen (Curvo- Semedo, 2019). Impact van radiologische EMVI op de ziektevrije uitkomst en eventuele verandering in het behandelplan is nog niet bekend.
Tumor deposities
Er zijn geen systematische reviews over de accuratesse van CT of MRI ten aanzien van tumor deposities.
Bedreigde mesocolische fascie (MCF)
Er zijn geen systematische reviews over de accuratesse van CT of MRI ten aanzien van het vaststellen van de relatie van de tumor tot de mesocolische fascie posterieur richting het retroperitoneum bij T3 tumoren.
Te beoordelen items coloncarcinoom:
Voor het opstellen van het beste behandelplan is het belangrijk om gestructureerde beoordeling te doen, waarbij de volgende items als handvat dienen te worden gebruikt:
- Locatie colontumor: (sigmoid, colon descendens, flexura lienalis, colon transversum, flexura hepatica, colon ascendens, ceacum).
- Lengte tumor: …… cm.
- Circulair/ semicirculair/ poliep:
- Tumor doorgroei door de wand:
- cT1/ T2:
- c T3ab: < 5mm.
- cT3cd: > 5mm.
- cT4a: ingroei in peritoneum.
- cT4b: ingroei in andere structuren/organen.
- Relatie van de tumor tot de mesocolische fascie (MCF+ofMCF-), waarbij een afstand ≤ 1 mm als positief wordt geclassificeerd (zie figuur 2).
- cN0 = geen pathologische klieren cN+= 1 of meer pathologische klieren; benoem hierbij specifiek of er al dan niet pathologische klieren aanwezig zijn in het D3 gebied (ventraal van de v. en a. mesenterica inferior van para aortale lymfeklieren (D4, M-status).
- Tumor depositie(s): ja/nee.
- EMVI (extra murale vene invasie): ja/nee.
- Complicatie: Obstructie dunne of dikke darm/abces/fisteling/perforatie.
- Conclusie: in TNM met benoemen relatie tot de mesocolische fascie in geval van T3, eventuele pathologische D3 lymfklieren in geval cN+, en toevoeging van extra aanwezige risicofactoren.
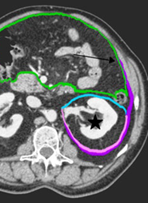
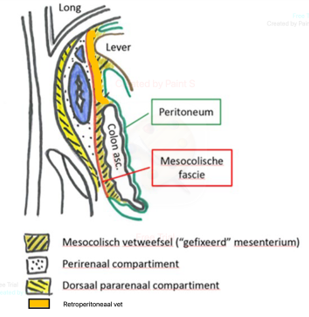
Figuur 2a. Anatomie retroperitoneale ruimte (referentie: Coffin, 2015)
Groene lijn = peritoneum parietale en viscerale. Blauwe lijn = mesocolische fascie en anterieure renale fascie (samen 1 structuur op CT). Lateroconale fascie (paars) loopt door in de posterieure renale fascie (roze)
Figuur 2b Sagittale anatomie
Bij groei tot aan de mesocolische fascie (wat op CT niet te onderscheiden is van anterieure renale fascie) is er sprake van T3 stadium met een bedreigde marge; als de tumor door de mesocolische fascie groeit (en zich dus in een andere ruimte bevindt, is het T4b)
| P: | Patiënt met coloncarcinoom |
| I: | MRI abdomen |
| C: | CT abdomen |
| O: |
Accuratesse cT stadium, accuratesse cN stadium, accuratesse D3 lymfklieren, accuratesse EMVI, accuratesse tumor deposities, bedreigde mesocolische fascie, verandering in beleid |
- Coffin A, Boulay-Coletta I, Sebbag-Sfez D, Zins M. Radioanatomy of the retroperitoneal space. Diagn Interv Imaging. 2015 Feb;96(2):171-86. doi: 10.1016/j.diii.2014.06.015. Epub 2014 Dec 26. PMID: 25547251.
- Curvo-Semedo, L. Colon Cancer Staging: When Does High Resolution MRI Have a Role?. Curr Colorectal Cancer Rep 15, 170–174 (2019). https://doi.org/10.1007/s11888-019-00444-0.
- Dang H, Dekkers N, le Cessie S, van Hooft JE, van Leerdam ME, Oldenburg PP, et al. Risk and Time Pattern of Recurrences After Local Endoscopic Resection of T1 Colorectal Cancer: A Meta-analysis. Clin Gastroenterol Hepatol. 2020 Dec 1:S1542-3565(20)31622-0. doi: 10.1016/j.cgh.2020.11.032. Epub ahead of print. PMID: 33271339.
- DʼSouza N, de Neree Tot Babberich MPM, d'Hoore A, Tiret E, Xynos E, Beets-Tan RGH, etal. Definition of the Rectum: An International, Expert-based Delphi Consensus. Ann Surg. 2019 Dec;270(6):955-959. doi:10.1097/SLA.0000000000003251. PMID: 30973385.
- Horvat N, Raj A, Liu S, Matkowskyj KA, Knezevic A, Capanu M, et al. CT Colonography in Preoperative Staging of Colon Cancer: Evaluation of FOxTROT Inclusion Criteria for Neoadjuvant Therapy. AJR Am J Roentgenol. 2019 Jan;212(1):94-102. doi: 10.2214/AJR.18.19928. Epub 2018 Nov 13. PMID: 30422707; PMCID: PMC7959265.
- Karahacioglu D, Taskin OC, Esmer R, Armutlu A, Saka B, Ozata IH, Rencuzogullari A, Bugra D, Balik E, Adsay V, Gurses B. Performance of CT in the locoregional staging of colon cancer: detailed radiology-pathology correlation with special emphasis on tumor deposits, extramural venous invasion and T staging. Abdom Radiol (NY). 2024 Jun;49(6):1792-1804. doi: 10.1007/s00261-024-04203-0. Epub 2024 Mar 6. PMID: 38446179.
- Kim HJ, Choi GS. Clinical Implications of Lymph Node Metastasis in Colorectal Cancer: Current Status and Future Perspectives. Ann Coloproctol. 2019 Jun;35(3):109-117. doi: 10.3393/ac.2019.06.12. Epub 2019 Jun 30. PMID: 31288500; PMCID: PMC6625771.
- Liu LH, Lv H, Wang ZC, Rao SX, Zeng MS. Performance comparison between MRI and CT for local staging of sigmoid and descending colon cancer. Eur J Radiol. 2019 Dec;121:108741. doi:10.1016/j.ejrad.2019.108741. Epub 2019 Nov 10. PMID: 31743882.
- Nerad E, Lahaye MJ, Maas M, Nelemans P, Bakers FC, Beets GL, Beets-Tan RG. Diagnostic Accuracy of CT for Local Staging of Colon Cancer: A Systematic Review and Meta-Analysis. AJR Am J Roentgenol. 2016 Nov;207(5):984-995. doi: 10.2214/AJR.15.15785. Epub 2016 Aug 4. PMID: 27490941.
- Pedersen MRV, Dam C, Loft M, Rafaelsen SR. Reporting colon cancer staging using a template. Eur J Radiol Open. 2020 Jan 29;7:100213. doi: 10.1016/j.ejro.2020.01.002. PMID: 32021880; PMCID: PMC6994830.
- Sammour T, Malakorn S, Thampy R, Kaur H, Bednarski BK, Messick CA, Taggart M, Chang GJ, You YN. Selective central vascular ligation (D3 lymphadenectomy) in patients undergoing minimally invasive complete mesocolic excision for colon cancer: optimizing the risk-benefit equation. Colorectal Dis. 2020 Jan;22(1):53-61. doi: 10.1111/codi.14794. Epub 2019 Aug 18. PMID: 31356721.
- Seo N, Lim JS, Chung T, Lee JM, Min BS, Kim MJ. Preoperative computed tomography assessment of circumferential resection margin in retroperitonealized colon cancer predicts disease-free survival. Eur Radiol. 2023 Apr;33(4):2757-2767. doi: 10.1007/s00330-022-09222-3. Epub 2022 Nov 10. PMID: 36355197.
- Storm SL, Boer FC. De waarde van D3 –lymfadenectomie en complete mesocolische excisie bij een colonresectie wegens coloncarcinoom. NTVO (Nederlands Tijdschrift voor Oncolgie). 2019 Juli; 16(5);176-185.
- van den Berg K, Wang S, Willems JMWE, Creemers GJ, Roodhart JML, Shkurti J, Burger JWA, Rutten HJT, Beets- Tan RGH, Nederend J. The diagnostic accuracy of local staging in colon cancer based on computed tomography (CT): evaluating the role of extramural venous invasion and tumour deposits. Abdom Radiol (NY). 2024 Feb;49(2):365-374. doi: 10.1007/s00261-023-04094-7. Epub 2023 Nov 29. PMID: 38019283.
- Watanabe T, Muro K, Ajioka Y, Hashiguchi Y, Ito Y, Saito Y, et al. Japanese Society for Cancer of the Colon and Rectum (JSCCR) guidelines 2016 for the treatment of colorectal cancer. Int J Clin Oncol. 2018 Feb;23(1):1-34. doi: 10.1007/s10147-017-1101-6. Epub 2017 Mar 27. PMID: 28349281; PMCID: PMC5809573.
Beoordelingsdatum en geldigheid
Publicatiedatum : 13-03-2026
Beoordeeld op geldigheid : 13-03-2026
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodules werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodules.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met colorectaal carcinoom. Deze werkgroep is ingesteld in het kader van het cluster oncologie onderste tractus digestivus.
De huidige samenstelling van de werkgroep
- Prof. dr. P.J. (Pieter) Tanis, gastrointestinaal en oncologisch chirurg, Erasmus MC, Rotterdam, NVvH (voorzitter)
- Dr. M. (Myriam) Chalabi, internist, Antoni van Leeuwenhoek, Amsterdam, NIV/NVMO
- Dr. E.C. (Elske) Gootjes, medisch oncoloog, Radboud UMC, Nijmegen, NIV
- Dr. D.J.A. (Derk Jan) de Groot, internist-oncoloog, UMC Groningen, Groningen, NIV/NVMO
- Dr. M.P.W. (Martijn) Intven, radiotherapeut, UMC Utrecht, Utrecht, NVRO
- Dr. M. (Miranda) Kusters, colorectaal chirurg, Amsterdam UMC, Amsterdam, NVvH
- Dr. M. M. (Miangela) Laclè, patholoog, UMC Utrecht, Utrecht, NVVPathologie
- Dr. M.M. (Marilyne) Lange, patholoog, Amsterdam UMC, Amsterdam, NVvPathologie
- Dr. M. (Monique) Maas, radioloog, Nederlands Kanker Instituut, Amsterdam, NVvR (vice-voorzitter)
- Dr. L. (Leon) Moons, MDL-arts, UMC Utrecht, Utrecht, NVMDL
- Prof. dr. I.D. (Iris) Nagtegaal, patholoog, Radboud UMC, Nijmegen, NVvPathologie
- Dr. M. (Mark) Roef, nucleair geneeskundige, Catharina Ziekenhuis, Eindhoven, NVNG
- Dr. J.M.L. (Jeanine) Roodhart, internist-oncoloog, UMC Utrecht, Utrecht, NIV/NVMO
- Dr. M. (Maarten) Smits, radioloog, UMC Utrecht, Utrecht, NVvR
- (Iris) van der Veeken Msc., coloncare verpleegkundige, Flevoziekenhuis, Almere, V&VN
- Prof. dr. C. (Kees) Verhoef, oncologisch chirurg, Erasmus MC, Rotterdam, NVvH
- Dr. K.S. (Kathelijn) Versteeg, internist-oncoloog, Amsterdam UMC, Amsterdam, NIV/NVMO
- Dr. M. (Marianne) de Vries, abdominaal radioloog, Erasmus MC, Rotterdam, NVvR
- Dr. M.L. (Miriam) Wumkes, internist, Jeroen Bosch Ziekenhuis, ’s-Hertogenbosch, NIV/NVMO
- S. (Silvie) Dronkers, stichting Darmkanker † (in herinnering)
Voormalig betrokken werkgroepleden
- Dr. M.E. (Marije) Hamaker, klinisch geriater, Diakonessenhuis, Utrecht, NVKG
- Dr. H.M.W. (Henk) Verheul, internist-oncoloog, Radboudumc, Nijmegen, NIV/NVMO
- Dr. H.L. (Erik) van Westreenen, chirurg, Isala Zwolle/ Isala Diaconessenhuis, Zwolle/Meppel, NVvH
- Dr. P. (Petur) Snaebjornsson, patholoog, Nederlands Kanker Instituut, Amsterdam, NVvP
Met medewerking van
- Dr. H.M.U. (Heike) Peulen, radiotherapeut-oncoloog, Catharina Ziekenhuis, Eindhoven
- Drs. F. (Floor) Piquer, PhD kandidaat, Catharina ziekenhuis
- dr. J.W.A. (Pim) Burger, chirurg, Catharina Ziekenhuis, Eindhoven, NVvH
Met ondersteuning van
- dr. D. (Dagmar) Nieboer, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. R.J.S. (Rayna) Anijs, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- I. (Ingeborg) van Dusseldorp, medisch informatiespecialist, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke Financiële Belangen |
Persoonlijke Relaties |
Extern gefinancierd onderzoek |
Intell. belangen en reputatie |
Overige belangen |
Ondernomen acties |
|
Prof. Dr. P.J. (Pieter) Tanis |
Chirurg, Erasmus MC |
Lid clinical audit board Dutch ColoRectal Audit, onbetaald Bestuurslid Stichting Opsporing Erfelijke Tumoren, onbetaald Lid medische adviesraad Lynch Polyposis vereniging, onbetaald Associate Editor Colorectal Disease, onbetaald |
Geen |
Geen |
Meerdere klinische multicenter trials: * KWF - COLOPEC-2: vroegdetectie peritoneale metastasen CRC - Projectleider * KWF - BIOPEX-2: transpositielap voor sluiting perineale wond APR voor rectumcarcinoom - Projectleider * KWF - IMARI: preventie en optimale behandeling naadlekkage na rectumcarcinoom resectie - Projectleider * KWF - Predicitiemodel longlaesies bij CRC - Projectleider * KWF - Snapshot complex coloncarcinoom - Geen projectleider KWF-COLOPEC-2: vroegdetectie peritoneale metastasen CRC-projectleider KWF-CAIRO-6: perioperatieve chemotherapie bij CRS-HIPEC voor peritoneale metastasen van CRC-geen projectleider KWF-BIOPEX-2: transpositielap voor sluiting perineale wond APR voor rectumcarcinoom- projectleider KWF- IMARI: preventie en optimale behandeling naadlekkage na rectumcarcinoom resectie-projectleider KWF-AI voor karakterisatie / predictie van longlaesies bij CRC-projectleider KWF-Snapshot complex coloncarcinoom-projectleider KWF-Snapshot rectumcarcinoom 2016-geen projectleider ZonMw CROSSROADS: behandelstrategie na lokale excisie pT1-2 coloncarcinoom, gestratificeerd voor lymfkliermetastase risico- geen projectleider Zorgverzekeraars (ZN)-DICA 2.0, pilot DCRA: verdiepingsmodules, videoregistratie-projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. M. (Myriam) Chalabi |
Internist-oncoloog, Antoni van Leeuwenhoek |
Geen |
Geen |
Geen |
* BMS - neoadjuvante immuuntherapie bij coloncarcinoom (Projectleider JA) * roche - neoadjuvante radiotherapie,immuuntherapie en bevacizumab bijrectumcarcinoom (Projectleider JA) * agenus - neoadjuvante immuuntherapie pan-cancer (Projectleider, ) * roche - neoadjuvante immuuntherapie bij slokdarm/maagcarcinoom (Projetleider JA) * MSD - neoadjuvante immuuntherapie bij lokaal irresectabele colorectale (Projectleider JA) carcinomen
|
Geen |
Geen |
Geen acties ondernomen |
|
Dr. E.C. (Elske) Gootjes |
Medisch oncoloog, Radboud UMC |
Geen |
Geen |
Geen |
* KWF - ORCHESTRA, lokale behandeling bij mCRC - Geen projectleider * Roche - ORCHESTRA, lokale behandeling bij MCRC - Geen projectleider * Stichting Blokker Verwer - ORCHESTRA, lokale behandeling bij mCRC - Geen projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
S.Y.A. (Silvie) Dronkers MA (overleden 18-12-2025)
|
Stichting Darmkanker Coördinator Patiënten Participatie Onderzoek en Belangenbehartiging
onbetaald |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. D.J.A. (Derk-Jan) de Groot |
Internist oncoloog, UMC Groningen |
Geen |
Geen |
Geen |
zie onder: * Hoffman-La Roche - Fase 2 klinische geneesmiddelen studie - Projectleider * GE - Fase 2 klinische studie - Geen projectleider * Siemens - Beurs om PET onderzoek te doen |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. E.C. (Elske) Gootjes
|
Medisch oncoloog RadboudUMC |
Geen |
Geen |
Geen |
* KWF - ORCHESTRA, lokale behandeling bij mCRC - Geen projectleider * Roche - ORCHESTRA, lokale behandeling bij MCRC - Geen projectleider * Stichting Blokker Verwer - ORCHESTRA, lokale behandeling bij mCRC - Geen projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Prof. Dr. M.P.W. (Martijn) Intven |
Radiotherapeut-Oncoloog UMC Utrecht |
- Voorzitter Nederlandse Vereniging voor radiotherapie en Oncologie, onbetaald - Lid redactieraad NTVO, onbetaald |
Geen |
Geen |
KWF - Pancreascarcinoom - Projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M. (Miranda) Kusters |
Colorectaal chirurg, Amsterdam UMC |
Geen |
Geen |
Geen |
KWF - Snapshot rectumcarcinoom - Projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. M.M. (Miangela) Laclè
|
Patholoog, UMC Utrecht |
Geen |
Geen |
Geen |
KWF - PATCH (validatie studie predictiemodel gesteelde T1 CRCs) - Projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M.M. (Marilyne) Lange |
Patholoog Amsterdam UMC |
Geen betaalde nevenwerkzaamheden |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. M. (Monique) Maas |
Radioloog bij NKI-AVL |
Redacteur nascholingsblad 'Imago'; hiervoor ontvang ik een vergoeding 1x per jaar |
Geen |
Geen |
KWF – Near complete response in rectal cancer – projectleider/PI |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. L.M.G. (Leon Moons) |
MDL arts, UMC Utrecht |
Geen |
Consultant voor Boston Scientific |
Geen persoonlijke relaties met een belang |
Alleen KWF, ZonMW en MLDS gesponsorde onderzoeken: * KWF - MATILDA-studie: EMR vs ESD voor grote linkszijdige poliepen - Projectleider * KWF - STAR-studie: cluster gerandomiseerde studie naar het effect van training in EMR in het verlagen - Projectleider * MLDS - STONE-studie: risicofactoen voor lymfkliermetastasen bij T1 CRCs * ZonMW - TRIASSIC-studie: ESD vs TAMIS voor rectum poliepenoor - Geen projectleider ZonMw CROSSROADS: behandelstrategie na lokale excisie pT1-2 coloncarcinoom, gestratificeerd voor lymfkliermetastase risico- projectleider |
Voorzitter T1 CRC werkgroep bestuurslid DCCG Voorzitter richtlijn Poliepectomie in het rectum en colon |
Geen |
Geen acties ondernomen |
|
Prof. Dr. I.D. (Iris) Nagtegaal |
Hoogleraar Pathologie, Radboudumc |
Voorzitter Stichting Palga (detachering) Expert patholoog BVO darmkanker (detachering) Onbetaalde functies: |
Geen |
Geen |
ja diverse wetenschappelijke projecten van verschillende fondsen: * KWF - Microbiome and metastases - Geen projectleider * Hanarth Foundation - Cancer of unknown primary - Projectleider * KWF - Implementation Al in pathology * ZonMW - Covid19 and cancer - Geen projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
Dr. M. (Mark) Roef |
Nucleair geneeskundige, Catharina Ziekenhuis Eindhoven |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
dr. J.M.L. (Jeanine) Roodhart |
internist-oncoloog, UMC Utrecht |
ONCODE clinical advisory board KWF wetenschappelijke raad, exploratie kamer bestuurslid stichting Hubrecht Organoid Biobank
allen onbetaald. |
Geen persoonlijke; geen betalingen aan mij als persoon voor deelname adviesraden, wel betalingen aan afdeling voor adviesraden/spreken door diverse farma en onderzoeksprojecten betaald door farma. |
nee |
ja: * KWF - ACTOR studie, organoids anuscarcinoom als predictieve biomarker en platform voor ontwikkelen nieuwe - Projectleider * GSK - MIRROR, analyse behandeling en uitkomsten MSI vs MSS rectumcarcinoom - Projectleider * HUB - OPTIC studie, voorspellende waarde organoids - Projectleider * Xilis - POSTED, MOS screeningsplatform als predictieve biomarker - Projectleider * Pierre Fabre - BRIDGE, real life treatment patterns en uitkomsten per moleculaire subgroep - Projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M.L.K. (Maarten) Smits |
Interventieradioloog, UMC Utrecht |
- Voorzitter wetenschapscommissie Nederlandse Vereniging voor Interventieradiologie (onbetaald) - Lid kernwerkgroep Kwaliteitsnormen in de Interventieradiologie - Consultant voor Philips (begunstigde UMC Utrecht) - Consultant voor Terumo / Quirem Medical (begunstigde UMC Utrecht) - Consultant voor Medtronic (begunstigde UMC Utrecht) - Consultant voor Swedish Orphan Biovitrum (eenmalige zitting in advisory board in 2021, begunstigde UMC Utrecht) |
Geen |
Geen |
* Terumo / Quirem Medical - HEPAR primary study, radioembolization for patients with hepatocellular carcinoma - Geen projectleider * Zorginstituut Nederland - CAIRO7-studie: radioembolisation for frail or elderly patients with colorectal liver metastases - Geen projectleider |
Geen |
Geen |
Geen acties ondernomen |
|
I. (Iris) van Veeken |
verpleegkundige - Flevoziekenhuis |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
Prof. Dr. C. (Kees) Verhoef |
Hoofd Gastro-Intestinale en Oncologische Chirurgie, Erasmus MC |
Bestuur Familiehuis, onbetaald Bestuur DCCG, onbetaald Ass Editor Sarcoma, Cancers and Digestive Surgery, onbetaald Dagvoorzitter expertmeeting Johnson en Johnon, betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
dr. K.S. (Kathelijn) Versteeg |
Internist-oncoloog en ouderengeneeskunde Amsterdam UMC |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M. (Marianne) de Vries |
Erasmus MC Radiologie Rotterdam: Radioloog (betaald) |
Geen |
Geen |
Geen |
Alleen meewerken aan multicenter studies maar niet als hoofdonderzoeker en krijg daar geen geld voor (bijvoorbeeld SNAPshot studie AVL of PELVEX studie) |
Geen |
Geen |
Geen acties ondernomen |
|
dr. M.L. (Miriam) Wumkes
|
Internist-oncoloog Jeroen Bosch ziekenhuis (vrijgevestigd, betaald) |
Voorzitter oncologiecommissie JBZ, betaald LId netwerkoncologiecommissie EMBRAZE, betaald Lid Regiocommissie Onco-oost, betaald Lid wetenschappelijke commissie DPCG, niet betaald Lid werkgroep organisatie van zorg DRPC, niet betaald Moleculaire diagnostiek per augustus, Zorginstituut Nederland, niet betaald. |
Geen |
Geen |
Lokale PI van onderzoek in JBZ, geen projectleider. Overigens onderzoeken niet binnen de lower tract * Overheid (vergoeding vanuit basispakket) - Periscope 2, beperkt gemetastaseerd maagcarcinoom, chemo vs chemo met CRS/HIPEC - Geen projectleider * KWF - Preopanc 3, resectabel pancreascarcinoom - Geen projectleider |
niet van toepassing. |
2019 Advies raad maagcarcinoom, Servier 2019 Adviesraad pancreascarcinoom, Servier 2020 Consensus expert Groep NTRK genfusie gerelateerde kanker. 2021: Programmacommissie en voordracht indian Summerschool voor jonge klaren, Servier
Vanaf 2022: Wetenschappelijk comite Waddenworkshop MDL, sponsoring verschillende farma (beschreven op de site welke farma voor welk jaar, https://www.waddenworkshoponcologie.nl/mdl-tumoren )
Voordracht masterclass GE oncologie stichting oncowijs |
Geen acties ondernomen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van Stichting Darmkanker en de Nederlandse Federatie van Kankerpatiëntenorganisaties (NFK) voor de invitational conferences in 2017 en 2023. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. Daarnaast zijn deze patiëntenorganisaties in de commentaarfase uitgenodigd om modules mee te lezen, te becommentariëren en de werkgroep van feedback vanuit het patiëntenperspectief voorzien.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
|
Module |
Uitkomst raming |
Toelichting |
|
Locoregionale stadiëring coloncarcinoom |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodules zijn opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase in 2017 inventariseerde de werkgroep knelpunten en de werkgroep beoordeelde de aanbevelingen uit de eerdere richtlijn (NVRO, 2014) op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door verschillende partijen via een invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten. Medio 2023 is het grootste deel van de richtlijn herzien en worden nieuwe modules of herzieningen door de werkgroep besproken indien de werkgroep:
- Signalen krijgt van (nieuwe) knelpunten in de zorg voor patiënten met colorectaal carcinoom die geadresseerd dienen te worden in de richtlijn.
- Signaleert dat er nieuwe onderzoeksresultaten zijn die relevant zijn voor de richtlijn.
- Constateert dat er tekstuele verbeteringen of aanvullingen nodig zijn in de richtlijn om de bruikbaarheid of volledigheid van de richtlijn te verbeteren.
De werkgroep bespreekt welke aanvullingen of herzieningen geprioriteerd dienen te worden en stelt evt. passende (nieuwe) uitgangsvragen op. De werkroep bepaalt de prioriteit van aanvullingen of herzieningen op basis van: (1) klinische relevantie, (2) de beschikbaarheid van nieuwe evidence, (3) en de te verwachten impact op de kwaliteit van zorg, patiëntveiligheid en (macro)kosten.
Uitkomstmaten
De werkgroep inventariseerde per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij men zowel naar gewenste als ongewenste effecten keek. De werkgroep baseerde de keuze voor uitkomstmaten mede op basis van de “core outcome set” gepubliceerd door Zerillo (2017). De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden. Hiervoor sloot de werkgroep zich, waar mogelijk, aan bij de grenzen voor klinische besluitvorming volgens de PASKWIL criteria uit 2023. Wanneer er geen grenzen voor klinische besluitvorming conform de PASKWIL criteria geformuleerd konden worden (bijvoorbeeld bij non-inferioriteitsvraagstukken) werden de standaard GRADE grenzen gehanteerd, tenzij anders vermeld.
Strategie voor zoeken en selecteren van literatuur
De werkgroep raadpleegde voor de afzonderlijke uitgangsvragen reeds gepubliceerde systematische reviews (SRs). SRs kwamen in aanmerking indien: i) systematisch was gezocht in één of meerdere databases; ii) transparante in- en exclusiecriteria zijn toegepast en iii) idealiter de kwaliteit van de geïncludeerde literatuur was beoordeeld. De voor de uitgangsvragen relevante internationale richtlijnen en consensusdocumenten werden eveneens geraadpleegd. Overige literatuur, waar niet systematisch naar werd gezocht, is als bewijsvoering in de overwegingen opgenomen.
Relevante beschikbare populatiegegevens uit Nederland werden gebruikt voor het bepalen van knelpunten, praktijkvariatie en externe validiteit van internationale richtlijnen en gepubliceerde literatuur.
Kwaliteitsbeoordeling individuele studies
De (risk of bias) kwaliteitsbeoordelingen van de individuele studies uit de gebruikte SRs werden gebruikt, tenzij deze afwezig waren of onbruikbaar waren voor het beoordelen van de kracht van het wetenschappelijke bewijs. Indien afwezig of onbruikbaar werd aangenomen dat er een risico op bias aanwezig zou kunnen zijn. In enkele gevallen, wanneer studies informatie verschaften over de cruciale uitkomstma(a)t(en), werd er een nieuwe kwaliteitsbeoordeling van individuele studies uitgevoerd.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van de geselecteerde SRs werden weergegeven in ‘Summary of Findings’ tabellen. De belangrijkste bevindingen uit de literatuur werden kort beschreven onder “Samenvatting literatuur” (kopjes “Samenvatting van internationale richtlijnen en consensusdocumenten” en “Samenvatting van systematische reviews en meta-analyses”) en onder “Overwegingen”. Bestaande meta-analyses uit de gebruikte systematische reviews werden beschreven. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek (te vinden in de ‘Summary of Findings’ tabellen). De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE- methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling beargumenteerd hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Indicatorontwikkeling
De werkgroep ontwikkelde geen interne kwaliteitsindicatoren om het toepassen van de richtlijn in de praktijk te volgen en te versterken. De werkgroep conformeert zich aan de SONCOS normen en de DICA-DCRA indicatoren.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule wordt aan de betrokken wetenschappelijke verenigingen en (patiënt)organisaties voorgelegd ter commentaar. De commentaren worden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren wordt de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule wordt aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi:
10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol.
2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html.
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi:10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zerillo JA, Schouwenburg MG, van Bommel ACM, Stowell C, Lippa J, Bauer D, Berger AM, Boland G, Borras JM, Buss MK, Cima R, Van Cutsem E, van Duyn EB, Finlayson SRG, Hung-Chun Cheng S, Langelotz C, Lloyd J, Lynch AC, Mamon HJ, McAllister PK, Minsky BD, Ngeow J, Abu Hassan MR, Ryan K, Shankaran V, Upton MP, Zalcberg J, van de Velde CJ, Tollenaar R; Colorectal Cancer Working Group of the International Consortium for Health Outcomes Measurement (ICHOM). An International Collaborative Standardizing a Comprehensive Patient-Centered Outcomes Measurement Set for Colorectal Cancer. JAMA Oncol. 2017 May 1;3(5):686-694. doi: 10.1001/jamaoncol.2017.0417. PubMed PMID: 28384684.