Opioïdrotatie
Uitgangsvraag
Hoe wordt opioïdrotatie zinvol toegepast in de behandeling van oncologische pijn?
Aanbeveling
Pas opioïdrotatie toe als er sprake is van onvoldoende effect en eerdere ophogingen van het opioïd niet hebben geleid tot verbetering van de klachten.
Pas opioïdrotatie toe als er sprake is van onacceptabele bijwerkingen of als ophoging tot onacceptabele bijwerkingen leidt.
Pas opioïdrotatie toe als de dosering van het huidige opioïd al hoog is, om zeer hoge doses te voorkomen.
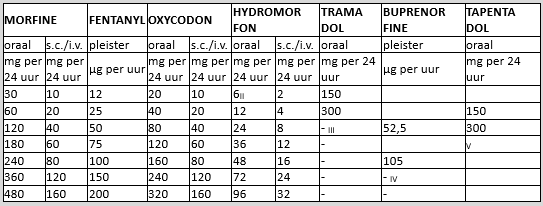
Maak bij opioïdrotatie gebruik van de onderstaande conversiefactoren, zie ook de omrekentabel:
- oraal morfine:oraal oxycodone = 1,5:1
- oraal morfine:oraal hydromorfon = 5:1
- oraal morfine:transdermaal fentanyl = 100:1
- oraal morfine:transdermaal buprenorphine = 100:1
- oraal morfine:oraal methadon = variabel tussen 5:1 en 10:1
- oraal oxycodone:oraal hydromorfon = 3,3:1
- oraal morfine:oraal tramadol = 1:10
- oraal morfine: tapentadol = 1:2,5
Omrekentabel opioïdenI, VI
[I] Bij het overgaan van het ene opioïd naar het andere (opioïdrotatie) vanwege bijwerkingen wordt geadviseerd om 75% van de equi-analgetische dosis te geven
[II] Deze dosering kan in de praktijk niet gegeven worden omdat de laagste dagdosering van het slow releasepreparaat 4 mg is en het middel 2x per dag moet worden gegeven
[III] De maximale dagdosering van tramadol is 400 mg/24 uur
[IV] Hogere doseringen buprenorfine dan 140 μg per uur worden niet geadviseerd
[V] De maximaal onderzochte dosis is 500 mg/dag. Over hogere doses kunnen geen uitspaken worden gedaan
[VI] vanaf een dosering van 240 mg morfine equivalent per dag dient rotatie altijd overwogen te worden om zeer hoge doseringen (> 480mg morfine equivalent per dag) te voorkomen
Overwegingen
Balans tussen gewenste en ongewenste effecten
Er is een systematisch onderzoek verricht naar de rol van opioïdrotatie bij patiënten met pijn door kanker of door een kankerbehandeling. Hierbij is enerzijds gekeken naar de meerwaarde van een opioïdrotatie, en anderzijds naar de effectiviteit van opioïdrotatie naar methadon. Er werd slechts een studie gevonden die geïncludeerd werd (Corli, 2019). Deze studie vergeleek pijnintensiteit en bijwerkingen voor en na een opioïdrotatie, en vond dat een opioïdrotatie tot een gemiddelde pijnafname van 31,2% leidde. In geval van rotatie in verband met bijwerkingen, verdwenen deze in 43,5% van de patiënten. Omdat het slechts één kleine open-label post-hoc analyse betreft, kan er op basis van deze literatuur geen conclusie getrokken worden over de gewenste en ongewenste effecten van een opioïdrotatie.
Er zijn daarnaast studies gevonden met betrekking tot opioïdrotatie naar methadon, die niet aan de inclusiecriteria voldeden, maar wellicht enige richting kunnen geven voor de aanbeveling. Er zijn geen literatuurconclusies voor deze studies beschreven.
Kwaliteit van bewijs
Wanneer we kijken naar de vergelijking voor en na een opioïdrotatie, is de overall kwaliteit van bewijs zeer laag voor pijnintensiteit en bijwerkingen. Dit betekent dat we geen uitspraak kunnen doen over het gevonden geschatte effect van de cruciale uitkomstmaten. Kwaliteit van leven en patiënttevredenheid werden niet gerapporteerd.
Voor de effectiviteit van opioïdrotatie naar methadon is de kwaliteit van bewijs niet beschreven, omdat de studies niet aan de inclusiecriteria voldeden.
De studies die in de literatuuranalyse zijn beschreven, voor beide vergelijkingen, hebben bepaalde methodologische beperkingen. Veelal waren studies niet geblindeerd of inadequaat gerandomiseerd. Er is behoefte aan goed opgezette, randomized controlled trials (RCT’s), die de effectiviteit van opioïdrotatie of switch en de rol van methadon onderzoeken bij patiënten met pijn door kanker of pijn door een kankerbehandeling.
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
Bespreek of de gewenste effecten die op groepsniveau zijn onderzocht opwegen tegen de ongewenste effecten die op groepsniveau zijn onderzocht (voor zover gerapporteerd) en hoe die zich verhouden tot de waarden en voorkeuren van de individuele patiënt en diens naaste(n). De afweging is voor iedereen anders. Bijvoorbeeld: weegt de grotere kans op overleving (gewenst effect) bij een bepaalde behandeling bij een individuele patiënt op tegen de kans op ernstigere complicaties van de behandeling (ongewenst effect)? Maak hierbij gebruik van de beschikbare uitkomsten op groepsniveau en pas dit toe op de individuele patiënt door middel van samen-beslis instrumenten. De waarden en voorkeuren verschillen per patiënt.
Opioïdrotatie laat een afname van pijnintensiteit en bijwerkingen zien in wetenschappelijke studies (Corli, 2019; Good, 2014; Mercadante, 2001; Mercadante, 2012) maar deze studies hebben een lage bewijskracht omdat er beperkingen in studieopzet bestaan (ontbreken van blindering, ontbreken van controlegroep). Niet uitgesloten is dat de gevonden effecten kunnen berusten op een placebo-effect of dat hetzelfde effect bereikt had kunnen worden met verhoging van het bestaande opioïd.
Er wordt in de literatuur geen voorkeur voor rotatie naar een specifiek opioïd beschreven. Ook worden er geen aanbevelingen voor specifieke patiëntengroepen gedaan. Met betrekking tot bijwerkingen lijken braken en sufheid het beste te reageren op een opioïdrotatie, terwijl obstipatie en een droge mond meestal blijven bestaan.
Naar methadonrotatie is er geen gecontroleerd onderzoek gedaan. Er zijn enkel studies beschreven waarbij alle patiënten een rotatie ondergingen. Een toevoeging van een lage dosis methadon aan huidig opioïdgebruik (zogenaamd add-on) wordt niet in de literatuur beschreven. Uit dit literatuuronderzoek is dan ook geen duidelijke aanbeveling af te leiden. Wel laten de beschreven studies allen een positief effect zien van methadonrotatie, waarbij bijwerkingen wisselend aanwezig zijn (zowel toename als afname) en langzame rotatie over enkele dagen minder bijwerkingen en betere pijncontrole geeft dan snelle rotatie.
In de spreekkamer zullen naast bovengenoemde overwegingen andere factoren van invloed zijn op de besluitvorming met betrekking tot opioïdrotatie. Vanuit het perspectief van de patiënt valt hierbij te denken aan ervaring met eerder gebruikte opioïden, eerdere gevoeligheid voor bijwerkingen, toedieningsvorm (bijvoorbeeld pleister, drank) en ernstige nierfunctiestoornissen (zie submodule Patiënten met nierfunctiestoornissen).
Vanuit het perspectief van de arts kan de hoogte van de dosering van het huidige opioïd ook een rol spelen. Een rotatie naar ongeveer equivalente dosis van een ander opioïd voorkomt namelijk dat er zeer hoge doses gegeven (moeten) worden. Als handvat hiervoor kan onderstaande omrekentabel gebruikt worden: overweeg altijd opioïdrotatie vanaf 180-240 mg morfine-equivalent per dag (halverwege de tabel) om zeer hoge doseringen die buiten de omrekentabel vallen (>480mg morfine-equivalent per dag) te voorkomen. Dat maakt afbouw bij pijnvermindering door ziektegerichte therapie (in het perspectief van verantwoord opioïdgebruik, zie elders in deze module) of eventuele rotatie naar een andere toedieningsvorm in de palliatieve fase eenvoudiger.
Ook ervaring met een specifiek opioïd kan van invloed zijn, waarbij dit vooral geldt voor methadon gezien het complexe farmacokinetische en farmacodynamische profiel. Er dient onder andere aandacht te zijn voor de lange halfwaardetijd (19-55 uur) bij opbouw en effectevaluatie, en voor gelijktijdig gebruik van QTc-verlengende medicatie (zoals anti-emetica ten tijde van chemotherapie).
Tot slot bestaat er met betrekking tot methadon soms een negatieve associatie met verslavingszorg, die dan aanvullende uitleg behoeft. In de praktijk is merkbaar dat deze associatie er steeds minder is, omdat meer artsen ervaring met methadon opdoen en de effecten gunstig zijn.
Conversiefactoren
Bij orale en transdermale toediening kunnen de volgende conversiefactoren gehanteerd worden (Mercadante, 2011):
- oraal morfine: oraal oxycodon=1,5:1;
- oraal morfine: oraal hydromorfon=5:1;
- oraal morfine: transdermaal fentanyl=100:1;
- oraal morfine: transdermaal buprenorfine=100:1
- oraal morfine: oraal methadon = variabel tussen 5:1 en 10:1;
- oraal oxycodon: oraal hydromorfon=4:1;
- oraal morfine: oraal tapentadol=1:2,5 (gegevens fabrikant).
Hoewel de conversiefactor van morfine naar buprenorfine door Mercadante als 75:1 wordt gesteld, acht het cluster het bewijs hiervoor van dermate lage kwaliteit dat de door de fabrikant gehanteerde conversiefactor van 100:1 wordt gehandhaafd.
Omrekentabel opioïdenI, VI
|
MORFINE |
FENTANYL |
OXYCODON |
HYDROMORFON |
TRAMADOL |
BUPRENORFINE |
TAPENTADOL |
|||
|
oraal |
s.c./i.v. |
pleister |
oraal |
s.c./i.v. |
oraal |
s.c./i.v. |
oraal |
pleister |
oraal |
|
mg per 24 uur |
mg per 24 uur |
μg per uur |
mg per 24 uur |
mg per 24 uur |
mg per 24 uur |
mg per 24 uur |
mg per 24 uur |
μg per uur |
mg per 24 uur |
|
30 |
10 |
12 |
20 |
10 |
6II |
2 |
150 |
|
|
|
60 |
20 |
25 |
40 |
20 |
12 |
4 |
300 |
|
150 |
|
120 |
40 |
50 |
80 |
40 |
24 |
8 |
- III |
52,5 |
300 |
|
180 |
60 |
75 |
120 |
60 |
36 |
12 |
- |
|
V |
|
240 |
80 |
100 |
160 |
80 |
48 |
16 |
- |
105 |
|
|
360 |
120 |
150 |
240 |
120 |
72 |
24 |
- |
- IV |
|
|
480 |
160 |
200 |
320 |
160 |
96 |
32 |
- |
- |
|
[I] Bij het overgaan van het ene opioïd naar het andere (opioïdrotatie) vanwege bijwerkingen wordt geadviseerd om 75% van de equi-analgetische dosis te geven
[II] Deze dosering kan in de praktijk niet gegeven worden omdat de laagste dagdosering van het slow releasepreparaat 4 mg is en het middel 2x per dag moet worden gegeven
[III] De maximale dagdosering van tramadol is 400 mg/24 uur
[IV] Hogere doseringen buprenorfine dan 140 μg per uur worden niet geadviseerd
[V] De maximaal onderzochte dosis is 500 mg/dag. Over hogere doses kunnen geen uitspaken worden gedaan.
[VI] vanaf een dosering van 240 mg morfine equivalent per dag dient rotatie altijd overwogen te worden om zeer hoge doseringen (> 480mg morfine equivalent per dag) te voorkomen
Kostenaspecten
De interventie levert gelijke kosten als de controlebehandeling.
Gelijkheid ((health) equity/equitable)
De interventie heeft geen verwachte invloed op gezondheidsgelijkheid. De toegang tot zorg blijft gelijk.
Aanvaardbaarheid:
Ethische aanvaardbaarheid
De interventie lijkt aanvaardbaar voor de betrokkenen. Er zijn geen ethische bezwaren.
Duurzaamheid
Bij de interventie spelen duurzaamheidsaspecten een beperkte rol. Het eerste voorschrift van het opioïd waarnaar geroteerd wordt dient kort te zijn, om medicijnverspilling bij een niet-succesvolle rotatie te voorkomen.
Haalbaarheid
De interventie lijkt haalbaar. De interventie is over het algemeen al standaardzorg in de praktijk.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Er is een gunstig effect te verwachten van opioïdrotatie op pijn en bijwerkingen. De bewijskracht is beperkt door het ontbreken van gerandomiseerde studies. Er is geen voorkeur uit te spreken voor rotatie naar een specifiek opioïd: eerdere ervaringen van patiënt en zorgverlener (met name in het geval van voorschrift van methadon) zijn hierin leidend.
Eindoordeel:
Conditionele aanbeveling voor opioïdrotatie wanneer er sprake is van onvoldoende effect van ophoging, onacceptabele bijwerkingen of bij zeer hoge dosering van het opioïd.
Onderbouwing
The management of chronic cancer pain often involves the long-term administration of strong (i.e. pure mu-receptor agonist) opioids. Due to tolerance and / or cancer pain progression, dosage increasement is often necessary over time. Opioid rotation is a treatment strategy that can be applied in order to optimize analgesia and minimize side effects. Although concisely accounted for in the current guideline, literature support was scarce at time of writing due to the lack of randomized studies (2020, very low grade).
In recent years the administration of and rotation to methadone has become more common. A more profound embedding of this drug in the guideline is considered necessary from a clinical perspective, with concurrent revision of literature supporting opioid rotation including but not limited to methadone.
Summary of Findings
Click here to see these tables in a document
PICO 1. Efficacy of opioid switch
|
Outcome
|
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence (Quality of evidence) |
Conclusions |
|
|
Before switch |
After switch |
||||
|
Pain intensity (critical) |
Based on data from 1 study (Corli, 2019) |
Average pain intensity (API) was measured using the numeric rating scale (NRS, 0-10). The API decreased on average by 31.2%. The worst pain intensity (WPI) had a 13.3% decrease. Pain reduction was adequate (defined as decrease >30% of API) after 51.45% of switches. |
Very low Due to serious risk of bias, due to serious indirectness, due to serious imprecision6 |
The evidence is very uncertain regarding the effect of opioid switching when compared with no opioid rotation or opioid switching in patients with pain due to cancer (treatment). |
|
|
Adverse effects (AE) |
Based on data from 1 study (Corli, 2019) |
AE were measured by the number of points of the Therapy Impact Questionnaire. The control of opioid side effects was adequate (AE disappeared or decreased ≥2 points) after switching in 43.5% of patients. The relief of AE varied among AE and within each patient. |
Very low Due to serious risk of bias, due to serious indirectness, due to serious imprecision7 |
The evidence is very uncertain regarding the effect after opioid switch when compared with before in patients with pain due to cancer (treatment). |
|
|
Quality of life |
- |
- |
No GRADE (No evidence was found)
|
No evidence was found regarding the effect after opioid switch when compared with before in patients with pain due to cancer (treatment). |
|
|
Patient satisfaction |
- |
- |
No GRADE (no evidence was found)
|
No evidence was found regarding the effect after opioid switch when compared with before in patients with pain due to cancer (treatment). |
|
1. Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias; Indirectness: serious. Due to the design of the study, the study made an indirect comparison of the intervention and control group. Imprecision: serious. Low number of patients.
2. Risk of Bias: serious. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias Indirectness: serious. Due to the design of the study, the study made an indirect comparison of the intervention and control group. Imprecision: serious. Low number of patients.
PICO 2. Efficacy of Methadone Rotation and Comparison Between Different Methods of Rotation to Methadone
Since none of the studies met the inclusion criteria, no quality of evidence (GRADE) and conclusions based on literature could be drawn.
|
Outcome
|
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence (Quality of evidence) |
Conclusions |
|
All outcomes
|
- |
- |
No GRADE (no evidence was found)
|
No evidence was found regarding the effect of opioid rotation or opioid switching when compared with no opioid rotation or opioid switch in patients with pain due to cancer (treatment). |
|
All outcomes
|
- |
- |
No GRADE (no evidence was found)
|
No evidence was found regarding the effect of opioid rotation to methadone when compared with methadone as an add-on in patients with pain due to cancer (treatment). |
Description of studies
For PICO 1, one study (Corli, 2019) was included that compared an opioid switch to no switch.
Corli (2019) conducted a post-hoc analysis from a multicenter, randomized, four-arm, controlled, phase IV clinical trial. They analyzed the impact of opioid switching in a cancer pain population treated with strong opioids for pain (N=498). Patients with advanced/ metastatic solid tumors were randomized in equal groups to receive either oral morphine (active comparator) or transdermal buprenorphine or oral oxycodone or transdermal fentanyl. Patients were eligible with persistent moderate to severe cancer pain [average pain intensity (API) in the last 24 h ≥4 points measured on a 0 to 10 Numerical Rating Scale (NRS) ranging from no pain to the worst imaginable pain] and the prescription of strong opioids never previously given.
Since this would lead to limited evidence, we decided to describe three additional studies (one systematic review and two additional non-randomized studies) in the summary of the literature, that did not meet the inclusion criteria. These additional studies describe further evidence on opioid rotation and the role of methadone and could therefore potentially support the recommendation. These studies will not be graded for their level of evidence (no clinical relevance is assessed). Important study characteristics and results are summarized in table 2. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Good (2014) conducted a systematic literature search for randomized controlled trials (RCTs) published post the 2007 Cochrane review of methadone in cancer pain. They included four randomized trials (272 participants). Two RCTs (Mercadante, 2008; Lauretti, 2013) compared the efficacy and safety of methadone with placebo or active control and two studies investigated rotation to methadone from other opioids (Moksnes, 2011; Cubero, 2010). The studies used different routes of administration, dosing, initiation, and titration of methadone and distinct pain scoring tools. In this analysis, Lauretti (2013) was excluded as they administered methadone epidurally, which was not relevant to the current research question.
In addition, two non-randomized studies were described (Mercadante 2001; 2012) that were not included in the systematic review by Good. They described a switch from an opioid to methadone in patients with cancer related pain. Table 3 depicts further details regarding the studies.
Table 3. Characteristics of included studies
|
Study |
Participants |
Comparison |
Follow-up |
Outcome measures |
Risk of bias (per outcome measure)* |
|
PICO 1: Efficacy of Opioid Rotation |
|||||
|
Corli, 2019 |
N at baseline Total: 498
Age, mean (SD)
Sex (m/f) 277/221
|
The opioid was switched in 79 patients (15.9%) 87 times, mainly for uncontrolled pain (52.3%), adverse opioid reactions (22.1%), both of these (4.8%), and dysphagia (20.8%). The starting opioid varied (oral morphine, oral oxycodone, transdermal fentanyl, transdermal buprenorphine; similar population size)
Comparison: before and after switch |
4 weeks |
Pain intensity, adverse effects |
HIGH (pain intensity, adverse effects) |
|
PICO 2a: Efficacy of Methadone Rotation |
|||||
|
Mercadante, 2008 |
N at baseline Total: 108
Age (mean) a) morphine: 59 y b) fentanyl: 57 y c) methadone: 61 y
Sex Not reported
|
Cancer patients, no longer responsive to opioids for moderate pain, were selected to randomly receive one of the following interventions:
initial doses: sustained-release morphine 60 mg/day, transdermal fentanyl 0.6 mg/day, oral methadone 15 mg/day followed by individual dose titration oral morphine for breakthrough pain (1/6 of the oral morphine equivalent requirement in 24 hours)
Comparison: Across the three intervention groups |
4 weeks |
Adverse effects, pain intensity, quality of life |
HIGH (all outcomes) |
|
Cubero, 2010 |
N at baseline: Total: 50
Age (median) a) Methadone + acetaminophen: 58.1 y b) methadone + placebo: 59 y
Sex Not reported
|
All patients switched from morphine to methadone and were randomized to receive either acetaminophen (750 mg PO q6h) or placebo for one week. Extra methadone (25% of daily methadone) was allowed for pain.
Comparison: before and after switch across the two intervention groups |
1 week |
Adverse effects, pain intensity, quality of life, satisfaction (preference) |
MODERATE (all outcomes) |
|
Additional studies |
|||||
|
Mercadante 2012 |
N at baseline: Total: 345
Age (mean) 62.5 y (range 34–82)
Sex (m/f) 198/147
|
Comparison: Before and after switch from different opioids (mostly oral morphine) to methadone. Reason of switch: poor pain relief in the presence of adverse effects. After the initial oral dose, the subsequent doses were flexible and were changed timely to fit the patients’ needs in an attempt to find the best balance between pain and opioid-related symptoms. |
1 week |
Pain intensity |
HIGH (all outcomes; design: retrospective chart review) |
|
Mercadante 2001 |
N at baseline: Total: 50
Age (mean) 60.7 y (95% CI 57-63)
Sex (m/f) 28/22 |
Comparison: Before and after switch from oral morphine to oral methadone administered every 8 hours using different dose ratios |
Until stable opioid dose was reached (mean 3.6 days) |
Pain intensity, adverse events |
HIGH (all outcomes; design: prospective non-randomized study) |
|
PICO 2b: Comparison Between Different Methods of Rotation to Methadone |
|||||
|
Moksnes, 2011 |
N at baseline: Total: 42
Age (mean) a) Stop-and-go: 61 b) 3-day switch: 58
Sex Not reported
|
Intervention: All patients were switched to methadone. Randomized to two different rotation strategies: “Stop-and-Go” or “3-Day Switch” Rescue opioid 1/6 of the baseline opioid dose
Comparison: Before and after morphine-to-methadone switch across the two intervention groups |
2 weeks |
Adverse effects, pain intensity |
HIGH (all outcomes) |
*For further details, see risk of bias table in the appendix
Results
PICO 1: Efficacy of Opioid Switch
Pain intensity (crucial)
Corli (2019) reported that 45 patients switched due to previous analgesic inefficacy. In those patients, the mean API score (measured on NRS 0-10) ranged from 5.0 (± 2.0) to 3.7 (± 1.6) before and after the switches, thus decreasing on average by 31.2%. The worst pain intensity (WPI) varied from 6.4 (± 2.6) to 5.4 (± 1.7) with a 13.3% decrease. Pain reduction was adequate (defined as decrease >30% of API) after 51.45% of switches. Pain reported was mostly breakthrough pain (46.8%), or neuropathic or mixed pain (24.1%).
Adverse effects
Corli (2019) reported that 23 patients switched due to opioid toxicity.
For each adverse event, the responders, poor responders and non-responders after opioid switch were reported (Table 4). Responders were defined as adverse drug reaction (ADR) disappeared or decreased ≥2 points as reported on Therapy Impact Questionnaire (TIQ). Poor responders had a decrease of 1 point and non-responders had an unchanged or worse intensity for ADRs.
Table 4. Responses after switch for adverse events (Corli, 2019)
|
Opioid adverse events, n (%) |
Responders |
Poor responders |
Non-responders |
|
Nausea |
6 (46.2) |
0 (0) |
7 (58.3) |
|
Vomiting |
6 (60) |
1 (10) |
3 (30) |
|
Constipation |
5 (41.7) |
0 (0) |
7 (58.3) |
|
Dry mouth |
3 (30) |
1 (10) |
6 (60) |
|
Drowsiness |
4 (36.4) |
3 (27.3) |
4 (36.4) |
|
Confusion |
5 (50) |
1 (10) |
4 (40) |
|
Hallucinations |
1 (50) |
0 (0) |
1 (50) |
|
Myoclonus |
0 (0) |
0 (0) |
1 (100) |
|
Total |
30 (43.5) |
6 (8.7) |
33 (47.8) |
In summary, there were ≥50% of responders among patients with vomiting and confusion, whereas non-responders prevailed in the case of constipation and dry mouth. The control of opioid side effects was adequate (responders) after switching in 43.5% of patients.
Quality of life
Not reported.
Patient satisfaction
Not reported.
PICO 2a: Efficacy of Methadone Rotation
Pain intensity (crucial)
Mercadante (2008) showed no clinically relevant difference in pain intensity among the groups. Mean pain intensity after 4 weeks (scale 0-10): 2.5 (morphine), 2.4 (fentanyl) 3.4 (methadone). No standard deviations were reported. Pain reported was a mix of nociceptive-neuropathic pain.
Cubero (2010) reported a lower pain intensity (numerical scale 0-10) after switching to methadone compared to baseline, although adding paracetamol did not enhance the effect.
Both groups (methadone rotation with and without paracetamol) went from score 5.0 at baseline to 3.5 after 7 days.
Pain intensity scored with the Faces pain scale gave similar results. Both groups went from score 6 at baseline to 4 after 7 days. Pain was mostly non-neuropathic. No standard deviations were reported.
Mercadante (2012) retrospectively observed that in 267 out of 345 patients (77.3%) substitutions with methadone were considered successful, presenting a decrease in pain intensity and/or symptoms intensity expressed as DS of more than 33%. No average pain scores were reported. The majority of patients had mixed nociceptive-neuropathic pain.
Mercadante (2001) reported a clinically relevant reduction in pain intensity in patients who switched to methadone. VAS scores (scale 0-10) went from 6.15 (95% CI 5.5 to 6.7) at time of opioid switching from 3.06 (95% CI 2.5 to 3.6) at time of stable opioid dose. Patients had most often somatic or mixed somatic-neuropathic or somatic-visceral pain.
Adverse effects
Mercadante (2008) reported several adverse effects for the comparison of methadone with morphine and fentanyl.
Adverse effects were measured using a scale from 0 to 3 (not at all, slight, a lot, severe). Nausea, vomiting, drowsiness, constipation, and confusion were similar across groups.
Central side effects (such as confusion and drowsiness) were slightly more pronounced with methadone and morphine than with fentanyl.
Distress score (sum of symptom intensities) increased during the first two weeks with methadone, but these symptoms did not require discontinuation of treatment and no differences in consumption of drugs used to manage opioid-induced adverse effects and non-opioid-analgesics were found.
Cubero (2010) reported adverse effects for the comparison of methadone with and without acetaminophen:
After switching from morphine to methadone, side effects decreased.
Significant reduction in constipation (P < .001) and dry mouth (P = .03) were observed after 7 days. No absolute data were available, and clinical relevance could not be judged.
Mercadante (2001) reported that in the 32 patients switching because of uncontrolled pain and morphine-related adverse effects, significant improvement was found in nausea and vomiting (P < .03), constipation (P < .001), and drowsiness (P < .01), but a significant increase in the methadone dose of an average of 20% (P < .004) was required. No absolute data were available, and clinical relevance could not be judged.
Quality of life
Mercadante (2008) used the Spitzer QoL Index rated on a Likert 3-point scale (0–2) in five areas (activity, daily life, health perceptions, social support, and behavior). There was no difference in QoL among the groups. QoL remained stable during 4 weeks of follow-up. No absolute data were available, and clinical relevance could not be judged.
Cubero (2010) used a standardized QoL questionnaire for cancer patients (QLQ-C30 version 3.0) before and after completion of the intervention period. QoL improved significantly after switching from morphine to methadone. There was no enhanced effect in the group with add-on paracetamol. No absolute data were available, and clinical relevance could not be judged.
Patient satisfaction
This outcome was not explicitly reported as a score in the studies. However, Cubero (2010) reported that 71% of patients preferred methadone over morphine.
PICO 2b: Comparison Between Different Methods of Rotation to Methadone
Pain intensity
Moksnes (2011) reported mean pain intensity on Brief Pain Inventory (BPI, 0-10) at baseline and after 14 days.
The Stop-and-Go group reported 5.4 at baseline and a slight increase after 14 days.
The 3-Day Switch group reported 5.5 at baseline and a decrease after 14 days. No absolute change in scores was available, and clinical relevance could not be judged.
Quality of life
Not reported.
Adverse effects
Moksnes (2011) reported adverse effects for the comparison of Stop-and-Go versus 3-Day Switch for methadone rotation.
No significant differences in side effects such as drowsiness, nausea, loss of appetite, or dry mouth were observed.
The mean differences between groups day 3 were for drowsiness 0.0 (95% CI -1.3–1.6), for nausea 0.1 (95% CI -1.0 to 1.0), for loss of appetite 1.2 (95% CI -1.1 to 3.5) and for dry mouth 0.6 (95% CI -1.2 to 2.3). This differences were not clinically relevant. Regarding QTc prolongation (risk of cardiac arrhythmias): in the Stop-and-Go group the QTc interval increased, while in the 3-Day Switch the QTc interval decreased.
A systematic review of the literature was performed to answer the following questions:
What is the effect of opioid rotation or switch compared to no opioid rotation or switch in patients with pain due to cancer (treatment)?
Table 1. PICO 1
| Patients | Patients with pain due to cancer (treatment) |
| Intervention | Opioid rotation or opioid switch |
| Control | No opioid switch or increased dose |
| Outcomes | Adverse effects, pain intensity, quality of life, patient satisfaction |
| Other selection criteria | Study design: systematic reviews and randomized controlled trials |
What is the effect of opioid rotation or switch to methadone compared to adding methadone to an opioid in patients with pain due to cancer (treatment)?
| Patients | Patients with pain due to cancer (treatment) |
| Intervention | Opioid rotation or switch to methadone |
| Control | Add-on (adding methadone to opioid) |
| Outcomes | Adverse effects, pain intensity, quality of life, patient satisfaction |
| Other selection criteria | Study design: systematic reviews and randomized controlled trials |
Relevant outcome measures
The guideline panel considered pain intensity and adverse events as a critical outcome measure for decision making; and quality of life and patient satisfaction as an important outcome measure for decision making.
A priori, the guideline panel did not define the outcome measures listed above but used the definitions used in the studies.
The guideline panel defined the following as a minimal clinically (patient) important difference:
- Adverse effects: 10% difference.
- Pain intensity (scale 0-10): MD <-1 or > 1.
- Quality of life: SMD < -0.5 or > 0.5.
- Patient satisfaction: SMD < -0.5 or > 0.5.
Search and select (Methods)
A systematic literature search was performed by a medical information specialist using the following bibliographic databases: Embase.com and Ovid/Medline. Both databases were searched from 2000 to 2024 for systematic reviews, RCTs and observational studies. Systematic searches were completed using a combination of controlled vocabulary/subject headings (e.g., Emtree-terms, MeSH) wherever they were available and natural language keywords. The overall search strategy was derived from three primary search concepts: (1) cancer; (2) pain; (3) opioid rotation. Duplicates were removed using EndNote software. After deduplication a total of 395 records were imported for title/abstract screening. Initially, 26 studies were selected based on title and abstract screening. After reading the full text, 25 studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and 1 study was included.
- Corli O, Roberto A, Corsi N, Galli F, Pizzuto M. Opioid switching and variability in response in pain cancer patients. Support Care Cancer. 2019 Jun;27(6):2321-2327. doi: 10.1007/s00520-018-4485-6. Epub 2018 Oct 24. PMID: 30357556.
- Good P, Afsharimani B, Movva R, Haywood A, Khan S, Hardy J. Therapeutic challenges in cancer pain management: a systematic review of methadone. J Pain Palliat Care Pharmacother. 2014 Sep;28(3):197-205. doi: 10.3109/15360288.2014.938883. Epub 2014 Aug 7. PMID: 25102037.
- Mercadante S, Casuccio A, Fulfaro F, Groff L, Boffi R, Villari P, Gebbia V, Ripamonti C. Switching from morphine to methadone to improve analgesia and tolerability in cancer patients: a prospective study. J Clin Oncol. 2001 Jun 1;19(11):2898-904. doi: 10.1200/JCO.2001.19.11.2898. PMID: 11387363.
- Mercadante S, Caraceni A. Conversion ratios for opioid switching in the treatment of cancer pain: a systematic review. Palliat Med 2011;25:504-515.
- Mercadante S. Switching methadone: a 10-year experience of 345 patients in an acute palliative care unit. Pain Med. 2012 Mar;13(3):399-404. doi: 10.1111/j.1526-4637.2012.01334.x. Epub 2012 Feb 23. PMID: 22360828.
Risk of Bias tables
Risk of bias table for intervention studies (randomized controlled trials; based on Cochrane risk of bias tool and suggestions by the CLARITY Group at McMaster University)
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated?
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented?
Were patients blinded?
Were healthcare providers blinded?
Were data collectors blinded?
Were outcome assessors blinded?
Were data analysts blinded?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measure
LOW Some concerns HIGH
|
|
Corli (2019) |
Probably yes
The study describes an adequate randomization method, likely using computer-generated sequences or sealed envelopes, ensuring allocation concealment |
Probably yes
Allocation was concealed from participants and investigators until assignment, preventing foreknowledge of treatment allocation |
Definitely no
The study was open-label due to the nature of the intervention. This may have influenced participant behavior and treatment administration. |
Probably yes
The study adequately accounted for dropouts and missing data, with an intention-to-treat analysis applied. |
Probably yes
All pre-specified outcomes appear to have been reported in the results section without evidence of omission or selective reporting. |
Probably yes
No conflicts of interest reported, no mention of additional biases. |
HIGH (pain intensity, adverse effects) |
|
Mercadante (2008) |
Probably no
Randomized, but the method is not described in detail. |
No information |
Definitely no
No blinding of participants, personnel or outcome assessors |
Definitely no
35% loss to follow-up |
No information
No protocol available |
Probably yes |
HIGH (all outcomes) |
|
Mercadante (2001) |
Definitely no
Not randomized |
Definitely no
|
Definitely no
No blinding |
Probably yes
Barely loss to follow up |
Probably yes
All predefined outcomes were reported |
Probably yes |
HIGH (all outcomes) |
|
Mercadante (2012) |
Definitely no
Not randomized |
Definitely no
|
Definitely no
No blinding |
Probably yes
Barely loss to follow up |
Probably yes
All predefined outcomes were reported |
Probably yes |
HIGH (all outcomes) |
|
Cubero & del Giglio |
Probably yes
Randomized, but the method is not described in detail. |
No information |
Probably no
Double blind design with placebo-controlled arm, outcome assessment probably blinded as well |
Probably yes
16% loss to follow-up, probably no significant impact on the results |
Probably yes
Outcomes are complete |
Probably yes |
Some concerns (all outcomes) |
|
Moksnes et al. |
Probably no
Randomization is mentioned, but there is no detailed description of the procedure. |
No information |
Definitely no
Open-label design, with no blinding |
Definitely no 33% loss to follow-up |
Probably yes
Outcomes are complete |
Probably yes |
HIGH (all outcomes) |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Auret K, Roger Goucke C, Ilett KF, Page-Sharp M, Boyd F, Oh TE. Pharmacokinetics and pharmacodynamics of methadone enantiomers in hospice patients with cancer pain. Ther Drug Monit. 2006 Jun;28(3):359-66. doi: 10.1097/01.ftd.0000211827.03726.e4. PMID: 16778720. |
no comparison
|
|
Benítez-Rosario MA, Salinas-Martín A, Aguirre-Jaime A, Pérez-Méndez L, Feria M. Morphine-methadone opioid rotation in cancer patients: analysis of dose ratio predicting factors. J Pain Symptom Manage. 2009 Jun;37(6):1061-8. doi: 10.1016/j.jpainsymman.2008.05.016. Epub 2009 Jan 25. PMID: 19171458. |
wrong outcome: morphine-methadone dose ratio |
|
Khoo SY, Aziz FA, Nambbiar P. Opioid Rotation to Methadone for Refractory Cancer Pain: A Case Series. J Pain Palliat Care Pharmacother. 2019 Sep-Dec;33(3-4):125-130. doi: 10.1080/15360288.2019.1666956. Epub 2019 Oct 22. PMID: 31638444. |
no comparison
|
|
Clemens KE, Klaschik E. Clinical experience with transdermal and orally administered opioids in palliative care patients--a retrospective study. Jpn J Clin Oncol. 2007 Apr;37(4):302-9. doi: 10.1093/jjco/hym017. Epub 2007 May 22. PMID: 17519302. |
wrong route of administration
|
|
Leppert W. The role of methadone in opioid rotation-a Polish experience. Support Care Cancer. 2009 May;17(5):607-12. doi: 10.1007/s00520-008-0537-7. Epub 2008 Nov 29. PMID: 19043743. |
no comparison
|
|
Tse DM, Sham MM, Ng DK, Ma HM. An ad libitum schedule for conversion of morphine to methadone in advanced cancer patients: an open uncontrolled prospective study in a Chinese population. Palliat Med. 2003 Mar;17(2):206-11. doi: 10.1191/0269216303pm696oa. PMID: 12701853. |
no comparison
|
|
Sugiyama Y, Sakamoto N, Ohsawa M, Onizuka M, Ishida K, Murata Y, Iio A, Sugano K, Maeno K, Takeyama H, Akechi T, Kimura K. A Retrospective Study on the Effectiveness of Switching to Oral Methadone for Relieving Severe Cancer-Related Neuropathic Pain and Limiting Adjuvant Analgesic Use in Japan. J Palliat Med. 2016 Oct;19(10):1051-1059. doi: 10.1089/jpm.2015.0303. Epub 2016 Jul 12. PMID: 27404399. |
Wrong study design |
|
Poulain P, Berleur MP, Lefki S, Lefebvre D, Chvetzoff G, Serra E, Tremellat F, Derniaux A, Filbet M; EQUIMETH2 Study Group. Efficacy and Safety of Two Methadone Titration Methods for the Treatment of Cancer-Related Pain: The EQUIMETH2 Trial (Methadone for Cancer-Related Pain). J Pain Symptom Manage. 2016 Nov;52(5):626-636.e1. doi: 10.1016/j.jpainsymman.2016.05.022. Epub 2016 Sep 30. PMID: 27693901. |
wrong intervention/comparison: stop and go vs progressive
|
|
O'Bryant CL, Linnebur SA, Yamashita TE, Kutner JS. Inconsistencies in opioid equianalgesic ratios: clinical and research implications. J Pain Palliat Care Pharmacother. 2008;22(4):282-90. doi: 10.1080/15360280802537241. PMID: 21923312. |
wrong study design: cases
|
|
Michael N, Sulistio M, Wojnar R, Gorelik A. Methadone rotation versus other opioid rotation for refractory cancer induced bone pain: protocol of an exploratory randomised controlled open-label study. BMC Palliat Care. 2023 Apr 15;22(1):42. doi: 10.1186/s12904-023-01160-1. PMID: 37059995; PMCID: PMC10105403. |
wrong comparison: methadone rotation versus other opioid |
|
Sande TA, Laird BJA, Fallon MT. The Management of Opioid-Induced Nausea and Vomiting in Patients with Cancer: A Systematic Review. J Palliat Med. 2019 Jan;22(1):90-97. doi: 10.1089/jpm.2018.0260. Epub 2018 Sep 21. PMID: 30239277. |
wrong outcome: opioid-induced nausea and vomiting
|
|
Mercadante S, Bruera E. The effect of age on opioid switching to methadone: a systematic review. J Palliat Med. 2012 Mar;15(3):347-51. doi: 10.1089/jpm.2011.0198. Epub 2012 Feb 21. PMID: 22352334. |
wrong outcome: effect of age
|
|
Mercadante S, Bruera E. Opioid switching: a systematic and critical review. Cancer Treat Rev. 2006 Jun;32(4):304-15. doi: 10.1016/j.ctrv.2006.03.001. Epub 2006 Apr 19. PMID: 16624490. |
SR bevat geen RCTs
|
|
Fredheim OM, Moksnes K, Borchgrevink PC, Skurtveit S. Opioid switching to methadone: a pharmacoepidemiological study from a national prescription database. Palliat Med. 2012 Sep;26(6):804-12. doi: 10.1177/0269216311412415. Epub 2011 Jun 22. PMID: 21697266. |
wrong population: variety of different patients, not strictly oncology
|
|
Leppert W. The own study of methadone in cancer pain treatment. ONKOLOGIA POLSKA. 2005;8(3):134. |
wrong language: polish
|
|
Rhondali W, Tremellat F, Ledoux M, Ciais JF, Bruera E, Filbet M. Methadone rotation for cancer patients with refractory pain in a palliative care unit: an observational study. J Palliat Med. 2013 Nov;16(11):1382-7. doi: 10.1089/jpm.2013.0222. Epub 2013 Oct 12. PMID: 24116946. |
wrong study design: observational, no comparison
|
|
Okayama S, Matsuda Y, Yoshikawa Y. A Comparative Study of Opioid Switching to Methadone for Cancer Pain Control in Successful and Unsuccessful Cases. J Palliat Med. 2019 Jul;22(7):844-847. doi: 10.1089/jpm.2018.0490. Epub 2019 Feb 4. PMID: 30716000. |
wrong comparison: sorted into unsuccessful and successful
|
|
Mercadante S, Ferrera P, Villari P, Adile C, Casuccio A. Switching from oxycodone to methadone in advanced cancer patients. Support Care Cancer. 2012 Jan;20(1):191-4. doi: 10.1007/s00520-011-1259-9. Epub 2011 Sep 7. PMID: 21901297. |
wrong study design: prospective, no comparison
|
|
Mercadante S, Ferrera P, Villari P, Casuccio A, Intravaia G, Mangione S. Frequency, indications, outcomes, and predictive factors of opioid switching in an acute palliative care unit. J Pain Symptom Manage. 2009 Apr;37(4):632-41. doi: 10.1016/j.jpainsymman.2007.12.024. PMID: 19345298. |
wrong population: variety of different patients, not strictly oncology
|
|
Mercadante S, Porzio G, Ferrera P, Fulfaro F, Aielli F, Verna L, Villari P, Ficorella C, Gebbia V, Riina S, Casuccio A, Mangione S. Sustained-release oral morphine versus transdermal fentanyl and oral methadone in cancer pain management. Eur J Pain. 2008 Nov;12(8):1040-6. doi: 10.1016/j.ejpain.2008.01.013. Epub 2008 Mar 18. PMID: 18353696. |
wrong intervention: transdermal fentanyl
|
|
Moksnes K, Kaasa S, Paulsen Ø, Rosland JH, Spigset O, Dale O. Serum concentrations of opioids when comparing two switching strategies to methadone for cancer pain. Eur J Clin Pharmacol. 2012 Aug;68(8):1147-56. doi: 10.1007/s00228-012-1228-3. Epub 2012 Feb 29. PMID: 22374345. |
Wrong outcome: pharmacological aspects |
|
Benítez-Rosario MA, Feria M, Salinas-Martín A, Martínez-Castillo LP, Martín-Ortega JJ. Opioid switching from transdermal fentanyl to oral methadone in patients with cancer pain. Cancer. 2004 Dec 15;101(12):2866-73. doi: 10.1002/cncr.20712. PMID: 15529307. |
wrong intervention: transdermal fentanyl to oral methadone, wrong study design: clinical trial
|
|
Mercadante S, Bruera E. Methadone as a First-Line Opioid in Cancer Pain Management: A Systematic Review. J Pain Symptom Manage. 2018 Mar;55(3):998-1003. doi: 10.1016/j.jpainsymman.2017.10.017. Epub 2017 Nov 1. PMID: 29101087. |
wrong intervention: methadone as first line opioid, not rotation
|
|
Nicholson AB. Methadone for cancer pain. Cochrane Database Syst Rev. 2004;(2):CD003971. doi: 10.1002/14651858.CD003971.pub2. Update in: Cochrane Database Syst Rev. 2007 Oct 17;(4):CD003971. doi: 10.1002/14651858.CD003971.pub3. PMID: 15106230. |
Wrong population, children included |
|
Dale O, Moksnes K, Kaasa S. European Palliative Care Research Collaborative pain guidelines: opioid switching to improve analgesia or reduce side effects. A systematic review. Palliat Med. 2011 Jul;25(5):494-503. doi: 10.1177/0269216310384902. PMID: 21708856. |
Outdated systematic review. More recent one available and included. |
Beoordelingsdatum en geldigheid
Publicatiedatum : 12-03-2026
Beoordeeld op geldigheid : 12-03-2026
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinair cluster ingesteld. Het cluster pijnmanagement bestaat uit meerdere richtlijnen, zie hier voor de actuele clusterindeling. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden brengen hun expertise in, indien nodig. De volgende personen uit het cluster zijn betrokken geweest bij de herziening van deze module:
Clusterstuurgroep
- Dr. J.W. (Jan Willem) Kallewaard, anesthesioloog-pijnspecialist, NVA (voorzitter)
- Drs. M.O. (Maarten) Mensink, kinderanesthesioloog en pijnarts, NVA
- Drs. E.M. (Esther) Boot, neuroloog, NVN
- Dr. K.B. (Kim) Gombert-Handoko, ziekenhuisapotheker, NVZA
- Dr. J.L. (Loes) Swaan, revalidatiearts, VRA
- Drs. S.J. (Stijn) Westerbos, kinderorthopeed, NOV
- Ddrs. P.J.W.J. (Hans) van Dongen, patiëntvertegenwoordiger, Samenwerkingsverband Pijnpatiënten naar één stem
Clusterexpertisegroep
- Prof. dr. M.A.H. (Monique) Steegers, anesthesioloog-pijnspecialist, NVA
- Dr. K.T.E. (Kim) Olde Dubbelink, anesthesioloog-pijnspecialist, NVA
- E.J.H. (Elle) van Dijk – van Oort MSc, physician assistant, NAPA
- Drs. I.L. (Ilona) Thomassen-Hilgersom, patiëntvertegenwoordiger, Samenwerkingsverband Pijnpatiënten naar één stem
- Drs. T.G. (Thomas) Knuijver, verslavingsarts, VVGN
- Prof. dr. F.G.A. (Frank) Jansman, ziekenhuisapotheker-klinisch farmacoloog, NVZA
- M. (Manon) Immerzeel, verpleegkundig specialist AGZ, V&VN
- Dr. E.J.M. (Evelien) Kuip, internist-oncoloog, NIV
Met ondersteuning van
- Dr. F. Willeboordse, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. I. van Dijk, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van de clusterleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Gemelde (neven)functies en belangen stuurgroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Restrictie |
|
Jan Willem Kallewaard |
Anesthesioloog-pijnspecialist Rijnstate en AMC |
Beroepsbelangencie NVA sectie pijn nva anesthesioloog in rijnstate en aumc |
Geen |
Geen |
Onderzoek gesponsord door industrie neuromodulatie: boston scientific 50.000 euro; onderzoek naar de effecten van neuromodulatie op pijn bij endometriose 2022-2023. Dhr. Kallewaard is hierbij PI. Neuromodulatie is een klein onderdeel van dit cluster, bij enkele modules is dit of kan dit in de toekomst één van de last-resort behandelopties zijn.Geen |
Geen |
Geen |
Besluit: Wanneer onderwerpen rondom neuromodulatie binnen het cluster worden ontwikkeld (of wanneer er discussie plaats vindt over de prioritering) zal Dhr. Kallewaard niet deelnemen aan de vergadering en zal een vice-voorzitter (Dhr. Mensink) waarnemen als voorzitter. |
|
Maarten Onno Mensink |
kinderanesthesioloog - pijnspecialist bij Prinses Máxima Centrum voor kinderoncologie |
Beroepsbelangencie NVA sectie pijn nva anesthesioloog in rijnstate en aumc |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restrictie |
|
Stijn Westerbos |
Fellow (oncologische) kinder orthopedie Prinses Maxima centrum Utrecht Cello Kinder orthopedie Wilhelmina kinder ziekenhuis Utrecht |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restrictie |
|
Esther Boot |
Neuroloog, Rijnstate |
Lid van werkgroep pijn NVN |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restrictie |
|
Kim Gombert-Handoko |
Lid werkgroep |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restrictie |
|
Loes Swaan |
Revalidatiearts in dienst van Rijndam Revalidatie te Rotterdam. |
- Lid van de Werkgroep Pijnrevalidatie Nederland van de VRA Onbetaald. - Lid van de Commissie Onderzoek en Onderwijs van het Netwerk Pijnrevalidatie Nederland (onbetaald) - Gastdocent Hogeschool Rotterdam (incidenteel, betaald). - Lid redactie nieuw uit te geven boek over pijnrevalidatie bij Bohn Stafleu van Loghum (onbetaald). |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restrictie |
|
Hans van Dongen |
- gepensioneerd -Vereniging samenwerkingsverband pijnpatiënten naar één stem - penningmeester, vrijwillige functie,
|
- adviserend lid Projectgroep van het project spiegelprogramma voor het reduceren voorschrijven sterkwerkende opioïden door huisartsen, project van het Academisch Huisartsennetwerk van U MC Amsterdam, vrijwillige functie - adviserend lid bij de subsidieaanvraag van het project "Esketamine-infusies voor refractaire chronische pijn bij patiënten met depressieve en niet-depressieve symptomen, met vacatiegeld (is afgerond); - Stichting Pijn-Hoop, interim-voorzitter en penningmeester, vrijwillige functie, algemene patiëntenorganisatie gericht op chronische pijn; - voorzitter Adviesraad Sociaal Domein Noordwijk, met vacatiegeld; - Stichting Sociale Projekten, voorzitter, vrijwillig |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restrictie |
Gemelde (neven)functies en belangen expertisegroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Restrictie |
|
Monique Steegers |
Anesthesioloog-pijnspecialist Amsterdam UMC |
Geen |
Geen |
Geen |
PI bij: 1) OMAMA (ZonMw) - onderwerp: effectiviteit laxeermiddelen bij patiënten met ver gevorderde kanker en obstipatie en 2) duloxetine versus qutenza (Grunenthal) - onderwerp: effectiviteit van de 2 geneesmiddelen bij pijnlijke chemotherapie geïnduceerde perifere neuropathie Beiden zijn lopende studies |
Geen |
Geen |
Monique Steegers |
|
Kim Olde Dubbelink |
Anesthesioloog-pijnspecialist Radboudumc |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
|
E. Dijk-Van van Oort |
MSc Physician Assistant Anesthesie - Pijngeneeskunde |
Geen |
Geen |
Geen |
Ja |
Geen |
Geen |
Geen restrictie |
|
Ilona Thomassen-Hilgersom |
voorzitter Samenwerkingsverband Pijnpatiënten naar één stem |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restrictie |
|
Thomas Knuijver |
Verslavingsarts en klinisch farmacoloog bij IrisZorg. Tevens docent en plaatsvervangend hoofdopleider bij NOVA, ELG, RadboudUMC. |
-Onderzoeker (8uur) betaald, onderzoek binnen de verslavingszorg, naar veiligheid en toepasbaarheid van ibogaïne, GHB en patiënt karakteristieken bij opiaatafhankelijkheid. -Docent (4uur) Onderwijs over verslavingsgeneeskunde en pharmacotoxicologie aan zorgprofeesional, oa over opioïden, de werking, bijwerking en intrapersoonlijke interacties tussen patiënt en arts. (standaard vergoeding of vrijwillig) |
Geen |
Geen |
Geen |
Deelname aan de werkgroep vergroot mijn kennis en netwerk, waardoor ik in een meer prominente positie kom en mogelijk meer onderwijs kan geven.
|
Geen |
Geen restrictie |
|
Frank Jansman |
Ziekenhuisapotheker-klinisch farmacoloog Deventer Teaching Hospital |
Hoogleraar Klinische farmacie, in het bijzonder in de oncologie, Rijksuniversiteit Groningen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen restrictie |
|
Manon Immerzeel |
Verpleegkundig specialist. AGZ. aandachtsgebied pijn. Reinier de Graaf. |
Voorzitter bestuur Afdeling pijnverpleegkundigen,V&VN (vrijwilligersvergoeding) |
Geen |
Geen |
Amsterdam UMC/ LUMC leiden Comparison between Qutenza and duloxetine for the treatment of painful chemotherapy-induced peripheral neuropathy. Coördinerend onderzoeker locatie delft.Subsidieverstekker: Grünenthal. The study is investigator initiated and no data will be shared with the subsidising party |
Voorzitter in het bestuur van V&VN pijnverpleegkundigen |
Geen |
Geen restrictie |
|
Kuip |
Internist -oncoloog, arts palliatief team, Radboud UMC Nijmegen |
palliatief consulent IKNL (vanuit Radboud UMC) |
geen |
nee |
nee |
Het zou kunnen opleveren dat we gevraagd worden voor volgende (aanverwante) richtlijnen en/of het geven van praatjes. |
Geen |
Geen restrictie |
Inbreng patiëntenperspectief
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerden de clusterleden conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
Sterkwerkende opioïden bij pijn bij patiënten met kanker - Submodule Opioïdrotatie |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt ook uit de toetsing dat het overgrote deel (±90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet OF het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betref]. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.
Zoekverantwoording
Algemene informatie
|
Cluster/richtlijn: Cluster pijnmanagement - Richtlijn pijn bij kanker |
|
|
Uitgangsvraag/modules: Module 2 Hoe wordt opioidrotatie zinvol toegepast in de behandeling van oncologische pijn?/ Wat is de rol van opioidrotatie bij patiënten met kanker en pijn? |
|
|
Database(s): Embase.com, Ovid/Medline |
Datum: 8 juli 2024 |
|
Periode: vanaf 2000 |
Talen: geen restrictie |
|
Literatuurspecialist: Alies Oost |
Rayyan review: https://rayyan.ai/reviews/1080855 |
|
BMI-zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Deduplication: voor het ontdubbelen is gebruik gemaakt van http://dedupendnote.nl:9777/ |
|
|
Toelichting: Voor deze vraag is gezocht op de elementen:
Het sleutelartikel wordt gevonden met deze search. |
|
|
Te gebruiken voor richtlijntekst: In de databases Embase.com en Ovid/Medline is op 8 juli 2024 systematisch gezocht naar systematische reviews, RCTs en observationele studies vanaf 2000 over opioïdrotatie bij patiënten met kanker en pijn. De literatuurzoekactie leverde 395 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SR |
42 |
33 |
45 |
|
RCT |
151 |
95 |
183 |
|
Observationele studies |
168 |
152 |
167 |
|
Totaal |
361 |
280 |
395* |
*in Rayyan
Zoekstrategie
Embase.com
|
No. |
Query |
Results |
|
#1 |
'neoplasm'/exp OR 'oncology'/exp OR 'cancer therapy'/exp OR 'cancer patient'/exp OR 'oncologist'/exp OR neoplasm*:ti,ab,kw OR tumor*:ti,ab,kw OR tumour*:ti,ab,kw OR carcinoma*:ti,ab,kw OR neoplastic:ti,ab,kw OR cancer*:ti,ab,kw OR oncolog*:ti,ab,kw OR oncotherap*:ti,ab,kw OR oncotreatment*:ti,ab,kw OR malignan*:ti,ab,kw OR metastas*:ti,ab,kw |
7609201 |
|
#2 |
'pain'/exp OR 'pain parameters'/de OR 'pain intensity'/exp OR 'pain severity'/exp OR 'pain assessment'/exp OR 'pain measurement'/exp OR 'nociception'/exp OR pain*:ti,ab,kw OR nocicept*:ti,ab,kw OR nocipercept*:ti,ab,kw |
2330513 |
|
#3 |
((opioid* OR analges* OR morphin* OR morfin* OR fentanyl OR fentanil OR phentanyl OR buprenorphin* OR buprenorfin* OR oxycodon* OR methadon*) NEAR/4 (rotat* OR switch* OR conversion*)):ti,ab,kw |
2222 |
|
#4 |
#1 AND #2 AND #3 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) NOT (('adolescent'/exp OR 'child'/exp OR adolescent*:ti,ab,kw OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw)) |
641 |
|
#5 |
#4 AND [2000-2024]/py |
584 |
|
#6 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
1043538 |
|
#7 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
4065280 |
|
#8 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
|
|
#9 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
|
|
#10 |
#5 AND #6 - SR |
42 |
|
#11 |
#5 AND #7 NOT #10 - RCT |
151 |
|
#12 |
#5 AND (#8 OR #9) NOT (#10 OR #11) - observationeel |
168 |
|
#13 |
#10 OR #11 OR #12 |
361 |
Ovid/Medline
|
# |
Searches |
Results |
|
1 |
exp Neoplasms/ or exp Medical Oncology/ or Integrative Oncology/ or exp Oncologists/ or (neoplasm* or tumor* or tumour* or carcinoma* or neoplastic or cancer* or oncolog* or oncotherap* or oncotreatment* or malignan* or metastas*).ti,ab,kf. |
5342457 |
|
2 |
exp Pain/ or Pain Measurement/ or Pain Management/ or exp Pain Perception/ or pain*.ti,ab,kf. or nocicept*.ti,ab,kf. or nocipercept*.ti,ab,kf. |
1094667 |
|
3 |
((opioid* or analges* or morphin* or morfin* or fentanyl or fentanil or phentanyl or buprenorphin* or buprenorfin* or oxycodon* or methadon*) adj4 (rotat* or switch* or conversion*)).ti,ab,kf. |
1324 |
|
4 |
(1 and 2 and 3) not (comment/ or editorial/ or letter/) not ((exp animals/ or exp models, animal/) not humans/) not ((Adolescent/ or Child/ or Infant/ or adolescen*.ti,ab,kf. or child*.ti,ab,kf. or schoolchild*.ti,ab,kf. or infant*.ti,ab,kf. or girl*.ti,ab,kf. or boy*.ti,ab,kf. or teen.ti,ab,kf. or teens.ti,ab,kf. or teenager*.ti,ab,kf. or youth*.ti,ab,kf. or pediatr*.ti,ab,kf. or paediatr*.ti,ab,kf. or puber*.ti,ab,kf.) not (Adult/ or adult*.ti,ab,kf. or man.ti,ab,kf. or men.ti,ab,kf. or woman.ti,ab,kf. or women.ti,ab,kf.)) |
499 |
|
5 |
limit 5 to yr="2000 -Current" |
450 |
|
6 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
758106 |
|
7 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2747317 |
|
8 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] |
4769045 |
|
9 |
Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) |
5730136 |
|
Mercadante S, Casuccio A, Fulfaro F, Groff L, Boffi R, Villari P, Gebbia V, Ripamonti C. Switching from morphine to methadone to improve analgesia and tolerability in cancer patients: a prospective study. J Clin Oncol. 2001 Jun 1;19(11):2898-904. doi: 10 |
5 and 6 - SR |
33 |