Achtergrond (pathofysiologie)
Inleiding
Kennis van de lymfologische basisbegrippen is noodzakelijk voor iedere hulpverlener die betrokken is bij de zorg voor patiënten met (risico op) lymfoedeem. In deze module wordt de achtergrond voor de volgende modules in de richtlijn geschetst. De basisbegrippen m.b.t. de lymfologie en organisatie van de lymfologische zorg worden besproken. Achtereenvolgend komen de volgende punten aan bod: de (patho)fysiologie, de verschillende vormen (classificatie), de (vroege) klinische kenmerken, het natuurlijk beloop (de stadia), de (moeilijkheden rondom) de diagnostiek, de behandelingsmogelijkheden/ strategieën van lymfoedeem en de terminologie rondom chronische (lymfologische) zorg. In deze richtlijn wordt vooral gefocust op secundair lymfoedeem omdat deze vorm het vaakst voorkomt.
Onderbouwing
Basisbegrippen in de lymfologische zorg werden verzameld uit leerboeken, recente richtlijnen en consensus documenten (Verdonk 2021, Pascal 2021, Vignes 2021).
(Patho)fysiologie van lymfoedeem
Het lymfatisch systeem bestaat uit lymfvaten, lymfeklieren en lymfatische organen (Oliver 2020). Het lymfsysteem is een eenrichtingsverkeer: er is geen centrale pomp en de lymfvaten beginnen als kleine, endotheel zakjes (initiële capillairen) in de intercellulaire ruimte van alle weefsels, met uitzondering van de avasculaire structuren, zoals haar, nagels, kraakbeen en de retina. Van daaruit komen collectoren en lymfvaten die draineren op de lymfeklieren die de lymfe al voor 40-50% concentreren. Vandaaruit gaan de lymfevaten naar de ductus thoracicus die middels meerdere anatomische variaties in de linker en rechter vena jugularis of vena subclavia uitkomt. Als interstitieel vocht in de lymfevaten komt spreken we van lymfe.
De functies van het lymfatisch systeem zijn:
- Regulatie van het interstitiële vocht (homeostasis) en afvloed van al het interstitiële vocht (100%) (Levick 2010). Hierdoor is oedeem in het algemeen te beschouwen als een gevolg van lymfogene dysfunctie.
- Vetabsorptie van de darmen.
- Immunologische functie voor afweer en immunologische respons bij o.a. infecties of metastasering van tumoren.
Lymfoedeem wordt veroorzaakt door het tekortschieten van het lymfatisch systeem. Gebaseerd op (patho)fysiologische overwegingen is lymfinsufficiëntie relatief of absoluut. Indien de zwelling het gevolg is van een te groot lymfaanbod bij een normaal afvloedsysteem, spreekt men van 'dynamische insufficiëntie' ('high-output insufficiëntie/verhoogde preload’); indien er lymfvat obstructie of functionele dysfunctie is, spreekt men van 'mechanische of statische lymfvatinsufficiëntie' ('low-output insufficiëntie/verhoogde afterload'). In de praktijk is vaak een combinatie van beide vormen van lymfafvloedinsufficiëntie aanwezig (Verdonk 2021). De mate van preload of afterload bepaalt mede het behandelplan. Lymfoedeem is geen diagnose maar een symptoom.
Vormen (classificatie)
Op basis van etiologie kan er onderscheid gemaakt worden tussen primair en secundair lymfoedeem (Damstra 2022). Primair (hereditair) lymfoedeem is gerelateerd aan een aangeboren ontwikkelings- of functiestoornis van de lymfvaten en/of de lymfeklieren. Secundair lymfoedeem wordt veroorzaakt door een verworven verstoring van het lymfafvloedsysteem en/of een pathologisch verhoogd lymfaanbod door diverse oorzaken (Martin-Almedina 2021).
Over het algemeen vormt het onderscheid tussen primaire en secundaire oorzaak de basis van gerichte diagnostiek en behandeling van lymfoedeem (Rockson 2010). Dit onderscheid is echter arbitrair, omdat een gecompenseerd primair lymfoedeem vaak pas manifest wordt na gebeurtenissen zoals trauma of infectie, waardoor het ten onrechte als secundair gezien kan worden (Damstra 2008).
Zo zijn er bij borstkanker gerelateerd lymfoedeem aanwijzingen dat pre-existente factoren in het lymfafvloedsysteem kunnen bepalen welke patiënt wel en welke patiënt geen lymfoedeem zal ontwikkelen (Stanton 2009, Wolf 2022). Met de groeiende kennis over de pathogenetische achtergrond van lymfafvloedstoornissen en lymfoedeem worden momenteel steeds gedetailleerdere en completere classificatiesystemen geformuleerd waarin bijvoorbeeld ook genetische kenmerken worden meegenomen om onderliggende afwijkingen in te delen. Deze aspecten kunnen invloed hebben op hoe en bij wie secundaire preventie wordt gegeven.
Primair lymfoedeem
Bij primair lymfoedeem is er een ontwikkelings- of functiestoornis van de lymfvaten en/of de lymfeklieren (Brouillard 2021). Vroeger sprak men over 3 categorieën van primair lymfoedeem gebaseerd op leeftijd van het ontwikkelen van zwelling: congenitaal lymfoedeem (aangeboren), lymfoedeem praecox (patiënten <35 jaar) en lymfoedeem tarda (patiënten >35 jaar). Deze indeling is verouderd.
Nieuwe inzichten zijn gericht op klinische fenotypering en op identificatie van eventuele genetische oorzaken van primair lymfoedeem. Het aantal bekende genen in relatie tot lymfoedeem stijgt snel. Lymfoedeem blijkt dan ook bij een zeer heterogene groep van aandoening voor te komen. Sinds 2013 ontwikkelde het St. Georges Hospital in het Verenigd Koninkrijk een classificatiemodel en flowchart om de achtergrond van primair lymfoedeem te analyseren op grond van klinische fenotypering. Deze is nu algemeen aanvaard door de Europese werkgroep voor pediatrisch en Primair Lymfoedeem (PPL) (Gordon 2020).
Secundair lymfoedeem
Secundair lymfoedeem komt veel vaker voor dan primair lymfoedeem en wordt veroorzaakt door een verstoring van het lymftransportsysteem al dan niet gecombineerd met een pathologisch verhoogd lymfaanbod (Rockson 2010). Vroeger werd vaak gedacht dat er bij secundair lymfoedeem sprake is van een ‘blokkade’ (de obstructieve theorie). Er zijn meerdere aanwijzingen dat er sprake is van een lymfepomp falen door langdurige overbelasting van een resterend lymfsysteem waardoor de lymfvaten uitzetten, minder effectief zijn en tenslotte niet meer pompen. Er is dan en beeld van dermale backflow (Thomis 2020). Deze nieuwe inzichten vormen mede de onderbouwing van nieuwe therapeutische inzichten.
Oorzaken van secundair lymfoedeem zijn er velen. Uit meerdere literatuurbronnen waaronder het International Lymphedema Framework (2012) consensus document en andere bronnen (Verdonk 2021, Greene 2015) kan een indeling worden gemaakt voor oorzaken van secundair lymfoedeem. Deze zijn beschreven in tabel 1.
Tabel 1: Indeling van secundair lymfoedeem naar oorzaak van het lymfoedeem.
|
Oorzaak |
Specificatie |
|
Trauma en weefselschade |
|
|
Maligniteiten en geassocieerde behandelingen |
|
|
Veneuze pathologie |
|
|
Infectie |
|
|
Inflammatoire processen |
|
|
Cardiaal |
|
|
Endocriene aandoeningen |
|
|
Dependency oedeem |
|
|
Overige |
|
Lymfoedeem na (behandeling voor) kanker
In de westelijke landen is lymfoedeem na behandeling voor kanker de meest voorkomende vorm van secundair lymfoedeem. In de module risicofactoren wordt de incidentie van lymfoedeem bij de diverse soorten van kanker besproken.
Lymfoedeem en infectie
Wereldwijd is filariasis, met zo’n 120 miljoen individuen met lymfoedeem, de belangrijkste oorzaak van secundair lymfoedeem (World Health Organization 2013). Omdat lymfoedeem veroorzaakt door filariasis in Nederland bijna niet voorkomt, wordt hier in deze richtlijn niet dieper op in gegaan. In het westen is cellulitis of erysipelas de meest bekende oorzaak van infectie bij lymfoedeem (Vignes 2021).
Een onderzoek toont aan dat 80% van de patiënten die zich presenteren met een eerste episode van erysipelas aan één been vaak ook scintigrafisch tekenen hebben van pre-existent (subklinische) lymfatische dysfunctie aan het niet aangedane been. Infectie (erysipelas) kan waarschijnlijk dus zowel een pre-existent, gecompenseerd lymfeafvloedsysteem doen decompenseren als een bestaand lymfoedeem verergeren (Damstra 2008).
Lymfoedeem en veneuze pathologie
Afwijkingen in het veneuze systeem kunnen zowel acuut als langzaam ontstaan. Bij een acute insufficiëntie is er sprake van een snel ontstane afvloedbelemmering zoals bijvoorbeeld bij trombose in het diepe veneuze systeem (trombosebeen). Wanneer het trombotisch proces optreedt in een van de oppervlakkige aderen, wordt gesproken van een oppervlakkig veneuze trombose (eigenlijk foutief “tromboflebitis”).
Meestal zal een veneuze pathologie zich langzaam ontwikkelen en spreekt men van een chronische veneuze insufficiëntie (CVI). De term chronisch veneuze insufficiëntie wordt vooral gebruikt om een functionele afwijking (reflux) van het veneuze systeem aan te duiden en wordt gewoonlijk gereserveerd voor een meer gevorderde ziekte met tekenen van oedeem, huidveranderingen en soms veneuze ulcera. Dit kan zowel door varices ontstaan (oppervlakkige CVI) dan wel bij doorgemaakt trombose (diepe insufficiëntie of posttrombotisch syndroom) (Chiesa 2007).
Door de langdurige veneuze hypertensie ontstaat er een verhoogde filtratie in de interstitiële weefsels waardoor het lymfsysteem overbelast kan raken met oedeem als gevolg (verhoogde preload). Het lymfsysteem is aanvankelijk niet defect maar kan dat door langdurige overbelasting wel raken. Men spreekt soms van flebo-lymfoedeem of lymfoedeem door CVI en hierbij is sprake van een dynamische lymfinsufficiëntie die zelfs na jaren nog reversibel kan zijn mits goed behandeld. Onbehandeld raken uiteindelijk de lymfvaten ook (deels) irreversibel beschadigd en kan er zelfs lymfostatische verrucosis ontstaan.
Bij lymfoedeem door CVI komen door de verhoogde filtratie ook plasmabestanddelen en zelfs erytrocyten in het interstitium. Hierdoor ontstaan de klassieke verschijnselen van chronisch veneuze insufficiëntie, zoals oedeem, verkleuringen en uiteindelijk ulcera. Bij deze vorm van lymfoedeem vormt de veneuze insufficiëntie het belangrijkste aangrijpingspunt voor de behandeling.
(Vroege) klinische kenmerken
Lymfoedeem is geen diagnose maar een symptoom. Het is geen statische aandoening die wel of niet aanwezig is, maar een dynamisch proces waarbij de balans tussen lymfaanbod en lymfafvloed in samenhang met compenserende mechanismen tekortschiet. Vroege tekenen van lymfstasis, bijvoorbeeld aan te tonen met indocyanine groen lymfografie, kunnen zeker bij risicogroepen, de eerste tekenen zijn van een tekortschietend lymfafvloedsysteem, nog voordat er zwelling of klachten ontstaan (Thomis 2021).
Vroegtijdige diagnostiek gericht op klachten en/of zwelling kunnen tot een vroegtijdige behandeling leiden. Vroege symptomen die worden gerapporteerd bij zowel primair als secundair lymfoedeem zijn onder andere passagiere zwelling, een stuwend gevoel, pijn, tintelingen, gevoel van een zware extremiteit, functiebeperking (International Lymphedema Framework 2012) en volumeverandering.
Lymfoedeem na een oncologische ingreep door beschadiging van het lymfsysteem ontwikkelt zich meestal geleidelijk, varieert soms gedurende de dag in omvang en is vaak gerelateerd aan afname van fysieke inspanning, overgewicht of bijkomende infecties. Ook spelen psychomotore componenten een rol.
Een andere vorm van lymfoedeem die een andere benadering behoeft is lymfoedeem dat ontstaat door actieve ingroei en obstructie door (recidief)kanker (‘maligne lymfoedeem’). Dit ontstaat vaak snel, kent geen fluctuatie over de dag en gaat vaak gepaard met uitstralende pijn en/of sensibiliteit uitval en tekenen van veneuze stuwing. Belangrijk is dat bij lymfoedeem dat ontstaat waarbij een behandeling voor kanker in het verleden heeft plaats gevonden, een recidief tumor wordt uitgesloten voordat met de therapie wordt begonnen.
In de latere stadia van lymfoedeem (stadium 3) is er een karakteristiek beeld van non-pitting oedeem met hypertrofie van vetweefsel, fibrose door interstitiële ontsteking. Dit ontstaat bij langer bestaand (onbehandeld) lymfoedeem en stuwing (Escobedo 2017).
Het teken van Stemmer, voor het eerst gepubliceerd door Robert Stemmer in 1976, wordt internationaal gezien als een bewezen klinisch fenomeen om lymfoedeem vast te stellen. Het Stemmer teken is positief als het niet lukt om met behulp van een handgreep een huidplooi van de voetrug op te tillen ter hoogte van de basisfalanx tussen de tweede en derde teen. Het teken van Stemmer is zeer bruikbaar voor lymfoedeem aan het been (Stemmer 1999). Voor vroegdiagnostiek van lymfoedeem (secundair aan oncologische behandeling aan de armen, genitale regio, hoofd-hals regio) is het teken van Stemmer niet bruikbaar. Afwezigheid van het teken van Stemmer sluit lymfoedeem niet uit. Bij lymfoedeem ten gevolge van een verhoogde preload kan het teken van Stemmer afwezig zijn.
Beloop en stadiëring
Gezien het (natuurlijk) beloop wordt lymfoedeem beschouwd als een chronische aandoening die vaak progressief is en meestal sluipend begint. Onderverdeling van het beloop in stadia draagt bij aan de communicatie tussen de verschillende zorgprofessionals die betrokken zijn bij patiënten met (risico op) lymfoedeem en is daarmee belangrijk voor multidisciplinaire afstemming van de zorg. Daarnaast biedt het mogelijkheden om verschillende zorgbehoeften in de verschillende fases van lymfoedeem in kaart te brengen. Het is tevens relevant voor het verrichten van wetenschappelijk onderzoek.
Een veel gebruikt stadiëringssysteem van de International Society of Lymphology (ISL) onderscheidt in de ontwikkeling van lymfoedeem drie klinische stadia (stadium 1-3) (International Society of Lymphology 2020):
- Stadium 1: vroege opeenhoping van interstitieel vocht, wat verdwijnt na hoog legging van de extremiteit. Het oedeem fluctueert. Pitting kan aanwezig zijn.
- Stadium 2a: pitting oedeem dat zelden verdwijnt met hoog legging van arm of been. In de late fase van stadium 2b: verdwijnt het pitting karakter deels door vetophoping en fibrose.
- Stadium 3: lymfoedeem met vooral non-pitting en soms lymfostatische verrucosis. Soms zijn er aan de voeten epidermale verschijnselen zoals acanthosis, papillomatosis, verrucosis. In de subcutis treedt proliferatie van vetweefsel op.
Het beloop van lymfoedeem wordt in sterke mate bepaald door risicofactoren zoals toename van gewicht/overgewicht, minder bewegen (ongezonde levensstijl) en recidief infecties. Verder zal een onbehandeld of onvoldoende behandeld lymfoedeem ook vaak neigen tot verergering van klachten en vervetting (stadium 3). Helaas betekent het dragen van een kous niet dat er al een goede onderhoudsfase is: vaak wordt een TEK aangemeten als het oedeem nog niet onder controle is. Indien dit na zes tot twaalf weken het geval is, dient de diagnose en/of het behandelplan te worden heroverwogen en is misschien een second opinion gewenst. Zie de module organisatie van zorg.
De differentiaal diagnostiek bij lymfoedeem
Lymfoedeem is geen diagnose maar een symptoom. Om de ontwikkeling van verder gevorderde stadia te voorkomen is secundaire en tertiaire preventie belangrijk samen met tijdige diagnosestelling en behandeling. De oorzaken van (chronisch) oedeem zijn weergegeven in de tabel 2 ’Differentiaal diagnostiek van (chronisch) oedeem verdeeld naar pathofysiologie’.
Tabel 2. Differentiaal diagnostiek van (chronisch) oedeem verdeeld naar pathofysiologie.
|
Toename veneuze druk (hoge preload) |
Afname van lymfafvloed (hoge afterload) |
Toename weefseldruk (hoge preload) |
Afname capillair-osmotische druk (hoge preload) |
|
Primair lymfoedeem: Medicamenteus op lymfefunctie (bv Amlodipine)
Secundair lymfoedeem:
|
|
|
Als de diagnose lymfoedeem is vastgesteld moet men behandeling starten voor zowel het lymfoedeem maar ook voor de eventuele onderliggende oorzaak.
De diagnose kanker-gerelateerd lymfoedeem wordt in principe gesteld wanneer er sprake is van klinisch aantoonbaar/relevant oedeem waarbij het lymfsysteem is gecompromitteerd. Er is internationaal echter geen consensus over het (meet)punt vanaf wanneer men spreekt van lymfoedeem en over het punt vanaf wanneer men behandeling moet starten.
Zo is de mate van zwelling die hiermee gepaard gaat onder andere afhankelijk van de karakteristieken/nauwkeurigheid van de gebruikte meetmethoden maar ook van de eventuele aanwezigheid van bijkomende klachten voortkomend uit het gezondheidsprofiel.
Patiënten na lymfeklierdissectie hebben allen een risico op lymfoedeem maar hoeven dat zeker niet te ontwikkelen. Zo is de incidentie van borstkanker gerelateerd lymfoedeem variërend van 5% tot 30% afhankelijk van de gekozen therapie en bijkomende risicofactoren (Monleon 2015). Bij cervixkanker varieert dit van 0% tot 69% (Bona 2020). Voor vulva kanker zijn percentages beschreven van 0% tot 73%, mede afhankelijk van of alleen de oppervlakkig of ook de diepe lymfklieren zijn verwijderd (Mattson 2022, Huang 2017).
Radiotherapie beschadigt weefsels, maar dit als monotherapie leidt vaak niet tot de ontwikkeling van lymfoedeem. Radiotherapie in de adjuvante setting volgend op eerdere chirurgische interventies leidt wel vaker tot de ontwikkeling van lymfoedeem dan radiotherapie als enige modaliteit. Ten gevolge van voortgaande fibrosering door slechtere doorbloeding van weefsels na radiotherapie, kan lymfoedeem eventueel nog vele jaren later ontstaan. Er lijkt hierbij overigens wel een dosis-effect relatie te bestaan, wat betekend dat een hogere dosis radiotherapie een verhoogd risico geeft op het ontwikkelen van lymfoedeem (Allam 2020)
Het systematisch monitoren van deze patiënten met een verhoogd risico op lymfoedeem is in ieder geval belangrijk. Ook is er plaats voor risicostratificatie op het ontstaan van lymfoedeem en daaruit voortvloeiende preventieve maatregelen zoals leefstijlnterventies (Wang 2021).
Behandelingsmodaliteiten en –strategieën
Preventief en therapeutisch
Behandelingsmodaliteiten zijn zowel gericht op het voorkomen van progressie (de preventie) als op vermindering van lymfoedeem (de therapeutische behandeling).
Met betrekking tot preventie onderscheidt men bij lymfoedeem interventies gericht op patiënten met verhoogd risico op lymfoedeem, zoals voorlichting, vermijding van risicofactoren (met name gewichtstoename/overgewicht en verminderde activiteiten/ongezonde levensstijl) en monitoring na oncologische ingrepen (secundaire preventie). Daarnaast is tertiaire preventie belangrijk bij patiënten die daadwerkelijk lymfoedeem ontwikkelen om naast de therapie verergering te voorkomen (voor definities van de verschillende vormen van preventie zie figuur 1).
|
Primaire preventie omvat in de geneeskunde de naam van maatregelen die ten doel hebben een eerste ziekte-episode te voorkomen, waarbij dus in principe gezonde mensen, vaak zelfs zonder klachten, worden behandeld.
Secundaire preventie omvat alle maatregelen die ten doel hebben het opsporen en behandelen van een beginnend gezondheidsprobleem. Monitoring van patiënten met verhoogd risico op lymfoedeem om de diagnose te kunnen stellen in een vroeg stadium is hiervan een voorbeeld.
Tertiaire preventie omvat alle maatregelen die bij een patiënt met een ziekte worden genomen op te voorkomen dat er een recidief optreedt of een verergering (bijvoorbeeld bij patiënten met lymfoedeem voorkomen dat er elefantiasis ontstaan). |
Figuur 1. Definities van de verschillende vormen van preventie
Conservatieve en chirurgische behandeling
Bij de behandeling van lymfoedeem wordt het onderscheid gemaakt tussen conservatieve en chirurgische behandeling. De conservatieve behandeling omvat meerdere modaliteiten. Deze worden vaak niet afzonderlijk maar gecombineerd met elkaar toegepast. Deze gecombineerde (niet operatieve) behandeling wordt decongestieve lymfatische therapie (DLT) of complexe lymfoedeemtherapie genoemd. In deze richtlijn wordt in dit verband de term DLT gebruikt. DLT bestaat uit:
- Compressietherapie (CT): zwachtels, therapeutisch elastische kousen (TEK) en intermitterende pneumatische compressietherapie (IPC);
- Weefsel/fascie release technieken;
- Oefentherapie gecombineerd met activeren/beweging;
- Manuele lymfdrainage (MLD);
- Voorlichting en ondersteunende zorg gericht op: leefstijladviezen, risicoreductie (waaronder actief beleid om een ‘voor een patiënt gezonde BMI’ te behouden of verkrijgen), huidzorg, begeleiding naar het gewenste niveau van activiteiten en participatie en (stimulatie tot) zelfmanagement.
Er bestaan ook chirurgische behandelingsmogelijkheden, die in de praktijk veelal worden gezien als secundaire optie indien de conservatieve behandeling niet of onvoldoende slaagt. Objectieve beoordeling waarom een conservatieve therapie faalt is essentieel en berust vaak op de aard van het behandelplan en de uitvoer daarvan.
Behandelfases: ‘stepped care’ principe
Vóór de diagnosestelling (bij patiënten met risico op lymfoedeem) bestaat de behandeling voornamelijk uit voorlichting en ondersteunende zorg gericht op: leefstijladviezen, risicoreductie (waaronder actief beleid om een ‘voor de patiënt gezonde BMI’ te behouden of verkrijgen), huidzorg en begeleiding naar het gewenste niveau van activiteiten en participatie (zie module leefstijlinterventies)
Na diagnosestelling wordt er onderscheid gemaakt in een initiële kortdurende (intensieve) fase en een (langdurige) onderhoudsfase. De eerste fase is vooral therapeutisch, expliciet gericht op actieve behandeldoelen zoals volumereductie. Wanneer het behandeldoel (bijna) is bereikt, volgt de langdurige onderhoudsfase. Deze fase is meer gericht op (tertiaire) preventie zoals het toepassen zelfmanagement technieken en kennis en behoud van de verkregen verbeteringen en op het verminderen van de impact op het algehele menselijk functioneren van de patiënt. De twee fases gaan meestal geleidelijk in elkaar over waarbij soms sprake is van een één tot twee maanden durende overgangsfase. Wanneer een verergering van zwelling en/of klachten plaatsvindt tijdens de onderhoudsfase, dan kan worden overwogen een nieuwe initiële behandelfase te starten. Mocht een herhaalde initiële behandeling onvoldoende effect hebben in de ambulante setting, dan valt doorverwijzing naar een centrum voor intensievere therapie of een operatieve lymfoedeembehandeling te overwegen (‘stepped care’ principe).
Terminologie (chronische) lymfologische zorg
De term lymfologische zorg omvat het gehele traject van (vroegtijdige) diagnostiek, behandeling en follow-up van alle patiënten met lymfoedeem of met risico op lymfoedeem. Omdat lymfoedeem een niet te genezen chronische aandoening is, vormt preventie een zeer belangrijk aspect van de lymfologische zorg.
De overheid stelt een pragmatische aanpak van chronische zorg voor. Deze gaat uit van goed afgestemde multidisciplinaire zorg waarbij een patiënt eigen regie en verantwoordelijkheid ontwikkelt en aangeleerd krijgt, voor zover dat voor de patiënt mogelijk is. Deze visie op chronische zorg omsluit de concepten van het ’chronic care model (CCM)’ van de Amerikaan Edward Wagner (Wagner 1998). Daarnaast is voor deze richtlijn gekozen om de aandoening ‘lymfoedeem’ niet alleen te zien in een biomedische context, maar binnen het bio-psycho-sociaal model van de ‘International Classification of Functioning, disability and health (ICF)’ van de WHO (World Health Organization 2001).
Een derde concept dat inzicht kan geven in het totaal functioneren is ‘positieve gezondheid’ (IPH instituut, 2020). Dit geeft een bredere kijk op de gezondheid en focust zich op zes dimensies, te weten lichaamsfuncties, mentaal welbevinden, zingeving, kwaliteit van leven, meedoen en dagelijks functioneren. Met deze brede benadering wordt bijgedragen aan het vermogen van patiënten om met fysieke, emotionele en sociale uitdagingen in het leven om te gaan. Hierbij geldt meer de mogelijkheid van een individu om zich aan te passen aan nieuwe omstandigheden (adaptief model), waarbij zelfmanagement een belangrijke rol speelt.
Naar deze concepten wordt in deze richtlijn regelmatig gerefereerd. De aspecten uiten zich onder meer in zelfmanagement, eigen regie, aanpassen en aandacht voor de ICF domeinen.
Het chronic care model
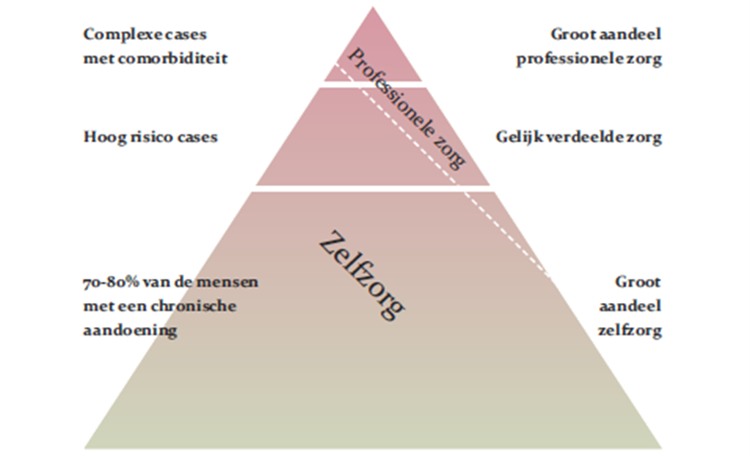
Het CCM is een model voor het ontwikkelen en verbeteren van zorg voor chronisch zieken (Wagner 1998). Uitgangspunt is dat patiënten met een chronische ziekte hun gedrag pas zullen veranderen wanneer zij in dit proces een leidende rol krijgen. In dit model wordt ‘zelfmanagement’ gezien als een essentieel onderdeel van de zorg voor chronisch zieken. Van patiënten wordt verwacht dat zij – samen met hun zorgverleners – een actieve bijdrage leveren aan hun behandeling en algemene gezondheid (NIVEL 2011). Er zijn veel initiatieven om zelfmanagement te bevorderen. Ondersteuning van zelfmanagement vraagt enerzijds een andere rol van zorgverleners. Zij moeten een meer coachende rol kunnen vervullen. Anderzijds hebben patiënten ondersteuning nodig om zelf de regie te kunnen voeren (NIVEL 2011). In dit verband wordt ook steeds vaker over “ samenmanagement” gesproken. Zie ook figuur 2.
Figuur 2. Aandeel van zelfzorg en professionele zorg naar complexiteit van de gezondheidssituatie van patiënten met chronische ziekten (NIVEL 2011).
Het International Classification of Functioning, Disability and Health (ICF) model
Het ICF-model is een bio-psycho-sociaal classificatiemodel dat zowel symptomen van een ziekte of aandoening beschrijft als het vermogen van de patiënt om te functioneren (World Health Organization 2001).
Met de ICF kan het menselijk functioneren worden beschreven vanuit drie verschillende perspectieven:
- Het perspectief van het menselijk organisme;
- Het perspectief van het menselijk handelen;
- Het perspectief van de mens als deelnemer aan het maatschappelijk leven.
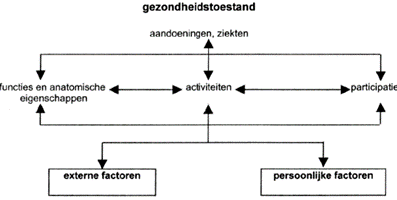
Het eerste perspectief is uitgewerkt in twee afzonderlijke classificaties: de classificatie van functies van het organisme en de classificatie van anatomische eigenschappen. Het tweede en derde perspectief zijn uitgewerkt in de classificaties van activiteiten en participatie. De term ´menselijk functioneren´ verwijst naar functies, anatomische eigenschappen, activiteiten en participatie; de term ´functioneringsprobleem´ verwijst naar stoornissen, beperkingen en participatieproblemen. De ICF ordent op systematische wijze verschillende domeinen betreffende aspecten van het menselijk functioneren die verband kunnen houden met een gezondheidsprobleem. De ICF kent daarnaast een rol toe aan persoonlijke en omgevingsfactoren (‘externe factoren’), die van invloed zijn op elk domein van het menselijk functioneren. Persoonlijke factoren zijn kenmerken zoals leeftijd, opleiding, persoonlijkheid en karakter, doorgemaakte ervaringen en bekwaamheden. Omgevingsfactoren betreffen zowel de sociale als de fysieke omgeving waarin mensen leven, bijvoorbeeld de houding van andere mensen, normen, wetgeving, faciliteiten, externe hulpbronnen, en de werk en leefomgeving (NIVEL 2011). Op deze manier kan een zinvol beeld verkregen worden van iemands functioneren en de problemen die daarin kunnen optreden. Zie ook figuur 3.
Figuur 3. De wisselwerking tussen de verschillende aspecten van de gezondheidstoestand en externe en persoonlijke factoren.
Klinimetrie
Bij het werken met modellen als ICF en CCM is het belangrijk dat de betrokkenen onderling afstemmen hoe de verschillende aspecten van het menselijk functioneren en problemen daarin ‘gemeten’ kunnen worden in alle fasen van een aandoening. Klinimetrie (zijnde: het meten van klinische verschijnselen), wordt gebruikt om bij te dragen aan het vaststellen van de zorgbehoefte van de patiënt vanuit alle perspectieven van het menselijk functioneren. Het doel is tweeledig, inventariserend/diagnostisch en evaluatief. Klinimetrie dient te worden toegepast in zowel de diagnostische fase, de behandelfase als ook de onderhoudsfase. Hierbij wordt veel aandacht besteed aan functionele fysieke eigenschappen. In de onderhoudsfase worden de intervallen tussen de metingen groter, krijgt zelfmanagement (zelfstandig onder controle houden van een aandoening en daar zelfmonitoring/zelfinterventies op toepassen) over alle ICF-domeinen de overhand en is de benadering van een hulpverlener veelal hands-off (uitgezonderd patiënten die door een bepaalde oorzaak kampen met terugval/toename van lymfoedeem).
Er worden voor steeds meer chronische aandoeningen internationaal geaccepteerde lijsten ontwikkeld (zogenoemde ICF core sets) met daarin een complete uiteenzetting van problemen (hulpvraagdomeinen) die relevant zijn voor het algehele menselijk functioneren van patiënten met die aandoening. Zo’n core set biedt aanknopingspunten voor het vaststellen van een afgestemd klinimetrisch instrumentarium, behandelprotocol en voor gerichte voorlichting en (psychosociale) ondersteuning (Viehoff, 2015). Er is een core set voor lymfoedeem beschikbaar, echter wordt deze naast onderzoeksdoeleinden nog niet veel gebruikt.
Wel zijn er meerdere kwaliteit van leven vragenlijsten ontwikkeld op basis van de ICF-methodiek LYMF-ICF arm en been die in de dagelijkse praktijk erg nuttig zijn (Devoogdt, 2014; Devoogdt, 2011).
Europees Reference Netwerk (ERN) voor pediatrisch en primair lymfoedeem (PPL-WG)
De Europese Gemeenschap is in 2015 een project gestart om de kennis en vaardigheden voor patiënten met zeldzame ziekten in Europa te bundelen. Via een netwerk kunnen alle Europese patiënten met een zeldzame ziekte de beste zorg krijgen, ook al is deze zorg niet in hun eigen land aanwezig (‘Crossborder healthcare’). Dit wordt het European Reference Network (ERN) genoemd.
Een zeldzame ziekte is gedefinieerd als een ziekte die bij minder dan 1:2000 mensen voorkomt. Primair lymfoedeem komt hiervoor in aanmerking. Van elk land is in principe 1 expertisecentrum vertegenwoordigd in het ERN en dat centrum kan in het eigen land zelf weer een satelliet netwerk opbouwen. Om expertisecentrum te worden zijn er zeer strenge criteria gesteld. De erkenning wordt door het ministerie van volksgezondheid in het betreffende land verleend.
In Europa zijn 24 netwerken opgericht voor verschillende groepen aandoeningen, waaronder een netwerk voor de multi-systemische VASCulaire ziekten (VASCERN) die uit 5 werkgroepen bestaat waaronder de pediatrisch en primair lymfoedeem werkgroep (PPL-WG).
Binnen de werkgroep PPL werken centra uit België, Engeland, Nederland, Finland, Duitsland, Denemarken, Slovenië en Frankrijk samen.
Voor nadere informatie over de Europese expertisecentra en de ERN’s, raadpleeg www.vascern.eu. Voor advies rond een complexe casus binnen pediatrische en primaire lymfoedeem kan altijd contact opgenomen worden met het Expertise Centrum voor Lymfo-vasculaire geneeskunde (ECL) in Drachten dat aangesloten is bij de ERN.
Onderbouwing
Referenties
- Allam, O., Park, K. E., Chandler, L., Mozaffari, M. A., Ahmad, M., Lu, X., & Alperovich, M. (2020). The impact of radiation on lymphedema: a review of the literature. Gland surgery, 9(2), 596-602. https://doi.org/10.21037/gs.2020.03.20
- Bates DO. An interstitial hypothesis for breast cancer related lymphoedema. Pathophysiology. 2010 Sep;17(4):28994.
- Bona AF, Ferreira KR, Carvalho RBM, Thuler LCS, Bergmann A. Incidence, prevalence, and factors associated with lymphedema after treatment for cervical cancer: a systematic review. Int J Gynecol Cancer. 2020 Nov;30(11):1697-1704.
- Chiesa R, Marone EM, Limoni C, et al. Chronic venous disorders: correlation between visible signs, symptoms, and presence of functional disease. J Vasc Surg 2007;46(2):322-30.
- Damstra, R. J., Hendrickx, A. A., Duinen, K. van, Klinkert, P. & Dickinson-Blok, J. L. [Diagnosis and treatment of primary and secondary lymphedema]. Ned Tijdschr Genees 166, (2022).
- Damstra RJ, Halk A-B, Dutch Working Group on Lymphedema. The Dutch lymphedema guidelines based on the International Classification of Functioning, Disability, and Health and the chronic care model. Journal of Vascular Surgery: Venous and Lymphatic Disorders. 2017;5(5):756-65.
- Damstra RJ, van Steensel MA, Boomsma JH, Nelemans P, Veraart JC. Erysipelas as a sign of subclinical primary lymphoedema: a prospective quantitative scintigraphic study of 40 patients with unilateral erysipelas of the leg. Br J Dermatol. 2008b;158(6):1210-5.
- Damstra RJ, van Steensel MAM, Boomsma JHB, Nelemans P, Veraart JCJM. Erysipelas as a sign of subclinical primary lymphoedema: a prospective quantitative scintigraphic study of 40 patients with unilateral erysipelas of the leg. Br J Dermatol. 2008;158(6):1210-5.
- Devoogdt N, De Groef A, Hendrickx A, Damstra R, Christiaansen A, Geraerts I, Vervloesem N, Vergote I, Van Kampen M. Lymphoedema Functioning, Disability and Health Questionnaire for Lower Limb Lymphoedema (Lymph-ICF-LL): reliability and validity. Phys Ther. 2014 May;94(5):705-21.
- Devoogdt N, Van Kampen M, Geraerts I, Coremans T, Christiaens MR. Lymphoedema Functioning, Disability and Health questionnaire (Lymph-ICF): reliability and validity. Phys Ther. 2011 ;91(6):944-57.
- Escobedo N, Oliver G. The Lymphatic Vasculature: Its Role in Adipose Metabolism and Obesity. Cell Metab 2017;26(4):598-609.
- Executive committee ISL. The diagnosis and treatment of peripheral lymphedema: 2020 Consensus Document of the International Society of lymphology.Lymphology 2020;53(1): 3-19
- Gezondheidsraad. Beweegrichtlijnen 2017. Den Haag: Gezondheidsraad, 2017; publicatienr. 2017/08
- Gordon K, Varney R, Keeley V, Riches K, Jeffery S, van Zanten M, et al. Update and audit of the St George's classification algorithm of primary lymphatic anomalies: a clinical and molecular approach to diagnosis. J Med Genet. 2020;14(26):17.
- Greene AK, Grant FD, Maclellan RA. Obesity-induced Lymphedema Nonreversible following Massive Weight Loss. Plast Reconstr Surg Glob Open. 2015 Jul 8;3(6):e426.
- Huang J, Yu N, Wang X, Long X. Incidence of lower limb lymphedema after vulvar cancer: A systematic review and meta-analysis. Medicine (Baltimore). 2017 Nov;96(46):e8722.
- Instiute for positive health - 'Wat is positieve gezondheid?', 2020. Beschikbaar via: https://www.iph.nl/kennisbank/wat-is-positieve-gezondheid/ Geraadpleegd op 23-05-2023.
- Levick JR, Michel CC. Microvascular fluid exchange and the revised Starling principle. Cardiovasc Res. 2010;87(2):198-210.
- Martin-Almedina S, Mortimer PS, Ostergaard P. Development and physiological functions of the lymphatic system: insights from human genetic studies of primary lymphedema. Physiol Rev 2021;101:1809-1871.
- Mattson J, Emerson J, Underwood A, Sun G, Mott SL, Kulkarni A, Robison K, Hill EK. Superficial versus deep inguinal nodal dissection for vulvar cancer staging. Gynecol Oncol. 2022 Jun 30:S0090-8258(22)00428-0.
- Monleon S, Murta-Nascimento C, Bascuas I, Macià F, Duarte E, Belmonte R. Lymphedema Predictor Factors after Breast Cancer Surgery: A Survival Analysis. Lymphat Res Biol. Lymphatic Research and Biology 2015;13:268-274.
- NIVEL Overzichtsstudies: zorg voor chronisch zieken. 2011(ISBN 978 94 61221 08 7
- O'Donnell, T. F., Allison, G. M. & Iafrati, M. D. A systematic review of guidelines for lymphedema and the need for contemporary intersocietal guidelines for the management of lymphedema. Journal of Vascular Surgery: Venous and Lymphatic Disorders 2020;8:676-684.
- Oliver G, Kipnis J, Randolph GJ, Harvey NL. The Lymphatic Vasculature in the 21st Century: Novel Functional Roles in Homeostasis and Disease. Cell. 2020:23;182(2):270-96.
- Pascal Brouillard, Marlys H. Witte, Robert P. Erickson, Robert J. Damstra, Corinne Becker, Isabelle Quéré, Miikka Vikkula. Primary lymphoedema. Nat Rev Dis Primers. 2021;7(1):77.
- Rockson SG. The physiology of lymphatic pump therapeutics. Lymphat Res Biol. 2010;8(3):141.
- Stanton AW, Modi S, Bennett Britton TM, Purushotham AD, Peters AM, Levick JR, Mortimer PS. Lymphatic drainage in the muscle and subcutis of the arm after breast cancer treatment. Breast Cancer Res Treat. 2009;117(3):549-57.
- Stemmer R. Das Stemmersche Zeichen--Möglichkeiten und Grenzen der klinischen Diagnose des Lymphödems [Stemmer's sign--possibilities and limits of clinical diagnosis of lymphedema]. Wien Med Wochenschr. 1999;149(2-4):85-6.
- Stout NL, Brantus P, Moffatt C. Lymphoedema management: an international intersect between developed and developing countries. Similarities, differences and challenges. Glob Public Health. 2012;7(2):107-23. doi: 10.1080/17441692.2010.549140. Epub 2011 May 24. PMID: 21360379.
- Thomis S, Dams L, Fourneau I, et al. Correlation Between Clinical Assessment and Lymphofluoroscopy in Patients with Breast Cancer-Related Lymphedema: A Study of Concurrent Validity. Lymphat Res Biol 2020;18(6):539-548.
- Thomis S, Devoogdt N, De Vrieze T, Bechter-Hugl B, Heroes AK, Fourneau I. Relation Between Early Disturbance of lymphatic transport Visualized With Lymphofluoroscopy and Other Clinical Assessment Methods in Patients With Breast Cancer. Clin Breast Cancer. 2022 Jan;22(1):e37-e47.
- Verdonk HPM, Devoogdt N, Damstra RD (2021). Oedeem en oedeemtherapie. Houten Bohn Stafleu van Loghum. (ISBN 978-90-368-2589-4)
- Viehoff PB, Heerkens YF, van Ravensberg CD, Hidding J, Damstra RJ, Ten Napel H, Neumann HAM. Development of consensus International Classification of Functioning, Disability and Health (ICF) Core Sets for Lymphedema. Lymphology 2015, 48: 38-50.
- Vignes S, Poizeau F, Dupuy A. Cellulitis risk factors for patients with primary or secondary lymphedema. J Vasc Surg Venous Lymphat Disord. 2022 Jan;10(1):179-185.e1.
- Vignes, S. et al. Primary lymphedema French National Diagnosis and Care Protocol (PNDS; Protocole National de Diagnostic et de Soins). Orphanet Journal of Rare Diseases 2021;16:18-12.
- Wagner EH. Chronic disease management: what will it take to improve care for chronic illness? Eff Clin Pract. 1998 Aug-Sep;1(1):2-4.
- Wang K, Tepper JE. Radiation therapy-associated toxicity: Etiology, management, and prevention. CA Cancer J Clin. 2021 Sep;71(5):437-454.
- World Health Organization (2001). International Classification of Functioning, Disability and Health: ICF (1st ed., Vol. 2nd): Geneva: World Health Organization.
- Wolf S, von Atzigen J, Kaiser B, Grünherz L, Kim BS, Giovanoli P, Lindenblatt N, Gousopoulos E. Is Lymphedema a Systemic Disease? A Paired Molecular and Histological Analysis of the Affected and Unaffected Tissue in Lymphedema Patients. Biomolecules. 2022 Nov 11;12(11):1667.
Verantwoording
Autorisatiedatum en geldigheid
Laatst beoordeeld : 28-12-2023
Laatst geautoriseerd : 28-12-2023
Geplande herbeoordeling :
Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update).
De Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) is regiehouder van deze richtlijn lymfoedeem en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
Aanleiding
Op initiatief van de Nederlandse Vereniging voor Dermatologie en Venereologie is de richtlijn lymfoedeem in 2020-2023 herzien. Ten opzichte van de richtlijn van 2014 zijn er nieuwe inzichten rondom chronisch oedeem, alsmede vragen rond de effectiviteit van nieuwe en bestaande behandeltechnieken zoals lymfchirurgie en MLD. De benadering van diagnostiek en behandeling is meer in een holistische benadering geplaatst met accent op functioneren van de patiënt in al zijn aspecten (participatie/activiteiten niveau/persoonlijke en omgevingsfactoren).
De benadering van de patiënt hierbij berust meer op een co-activiteit met aandacht voor shared decision making, “ samenmanagement” en coaching.
Afbakening onderwerp
In deze richtlijn worden adviezen gegeven ten aanzien van de diagnostiek en behandeling van lymfoedeem en begeleiding bij lymfoedeem en dient als leidraad voor de dermatoloog en andere zorgprofessionals die in aanraking komen met patiënten met lymfoedeem.
Definities
Oedeemtherapeut
Wanneer in de richtlijn de term ‘oedeemtherapeut’ wordt gebruikt, bedoelt de werkgroep alle
zorgverleners die bevoegd zijn oedeemtherapie te praktiseren. In Nederland zijn hiertoe twee
beroepsgroepen bevoegd: de huid- en oedeemtherapeut en de oedeemfysiotherapeut.
Compressietherapie
Compressietherapie betekent letterlijk drukbehandeling. In deze richtlijn wordt hiermee bedoeld het aanbrengen van drukmiddelen die de veneuze en lymfatische afvloed bevorderen. In de praktijk wordt vaak gesproken van ambulante compressie, omdat het samengaan van de comprimerende werking van het aangelegde verband en de pompwerking van de spieren het beoogde resultaat tot stand brengt. Men onderscheidt verschillende compressiemiddelen, waaronder diverse types zwachtels (niet-elastische compressie), therapeutisch elastische kousen (TEK), intermitterende pneumatische compressie (IPC) pompen en adjustable compression devices (ACD).
Aanmeter
De aanmeter is in deze richtlijn de zorgprofessional die TEK en/of andere compressiehulpmiddelen aanmeet en levert. In Nederland mogen compressiehulpmiddelen alleen aangemeten worden na het behalen van een erkend diploma. Dit is een discipline met aantekening voor compressietherapeut, dit kan bijvoorbeeld een oedeemtherapeut zijn. Het verdient sterk de voorkeur dat de aanmeter direct bij het behandelproces betrokken is om een adequaat compressiehulpmiddel te kunnen verstrekken. Vaak zal de betrokken oedeemtherapeut (huidtherapeut of oedeemfysiotherapeut) uit service oogpunt ook de gewenste compressiehulpmiddelen aanmeten en leveren. In dit geval heeft die persoon ook de functie van aanmeter en wordt die ook zo genoemd.
Overige inleidende teksten
Lymfoedeem is een vorm van de verzamelnaam ‘chronisch oedeem’: oedeem dat langer dan 3 maanden bestaat. Vroeger werd lymfoedeem vaak als diagnose gezien maar dat is niet juist. Het betreft een symptoom van zwelling door lymfstasis met (non) pitting oedeem en/of weefselverandering. Lange tijd werden in epidemiologische studies vooral gelet op chronische zwelling na bijvoorbeeld kanker waarbij de eventueel bijkomende oorzaken van chronisch oedeem niet vermeld worden. Echter, de groep is heterogeen waarbij vele factoren een rol spelen die deels gerelateerd zijn aan de initiële factoren die het lymfesysteem hebben beschadigd (bijvoorbeeld een operatie en bestraling) maar vaak spelen persoons- en omgevingsfactoren een erg belangrijke rol (bijvoorbeeld overgewicht en gebrek aan mobiliteit/spierkracht/conditie).
Deze benadering maakt een goede medische diagnose van het chronische oedeem en een gezondheidsprofiel van de patiënt essentieel voordat een behandelplan wordt gesteld. Een multidisciplinaire samenwerking is hiervoor zeer belangrijk.
De prevalentie van chronisch oedeem wisselt sterk binnen de volgende groepen:
- Veneus oedeem;
- Primair en secundair lymfoedeem;
- Dependency oedeem;
- Chronisch oedeem door vergevorderde kanker;
- Chronische zwelling door obesitas;
- Chronische zwelling bij vasculaire malformaties.
Dit maakt dat als er naar studies rond prevalentie wordt gekeken, het bredere perspectief van chronisch oedeem/lymfoedeem en de complexe oorzaken daarvan dient mee te worden genomen (Moffatt 2019).
Doel en doelgroep
Doel
Deze richtlijn is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering. De richtlijn berust op de resultaten van wetenschappelijk onderzoek en aansluitende meningsvorming gericht op het vaststellen van goed medisch handelen. De richtlijn geeft aanbevelingen over begeleiding en behandeling van patiënten met lymfoedeem.
Doelgroep
De richtlijn is bestemd voor leden van de medische en paramedische beroepsgroep. Daartoe behoren onder andere: NVDV, NVPC, NVOG, NVNG, NVRO, NVvH, NVH, V&VN, NIP, NVFL, KNGF, NVD en andere betrokkenen i.e. dermatologen, huisartsen, verpleegkundig specialisten, physician assistants, fysiotherapeuten, huidtherapeuten en (dermatologie) verpleegkundigen. Voor patiënten is informatie op thuisarts.nl en een patiënten folder ontwikkeld.
Samenstelling werkgroep
|
Werkgroepleden – versie 2023 |
Vereniging |
||
|
Dr. R.J. Damstra (voorzitter) |
NVDV |
||
|
Dr. C. van Montfrans |
NVDV |
||
|
Dr. C.J.M. van der Vleuten |
NVDV |
||
|
Dr. S.S. Qiu Shao |
NVPC |
||
|
Dr. M.E.E. Bröker |
NVVH |
||
|
Drs. E.B.L. van Dorst |
NVOG |
||
|
Drs. N. Groen |
NVNG |
||
|
Dr. B. Kreike |
NVRO |
|
|
|
Mevr. C. Alberts-Hoeben |
NVH |
|
|
|
Mevr. S. van Beusekom |
NVH |
|
|
|
Mevr. W. den Hollander |
V&VN |
|
|
|
Mevr. J.E.W.M. van Dongen-Melman |
NIP |
|
|
|
Mevr. F. Potijk |
NVFL en KNGF |
|
|
|
Mevr. B. Pinkert |
NVD |
|
|
|
Mevr. C. Hovenier |
Stichting Olijf |
|
|
|
Mevr. A Diepstraten |
Stichting Olijf |
|
|
|
Drs. J.M.G. Fijn |
Borstkankervereniging Nederland (BVN) |
|
|
|
Drs. M. Velting |
Borstkankervereniging Nederland (BVN) |
|
|
|
Drs. W.F. Hoelen |
NLNet |
|
|
|
Drs. P.A.M. van den Broek |
Huid Nederland |
|
|
|
Dr. J.J.E. van Everdingen |
NVDV |
|
|
|
Dr. A. van Enst |
NVDV |
|
|
|
Drs. E. de Booij Start t/m juni 2021 |
Arts-onderzoeker NVDV |
|
|
|
Drs. E. van der Veen Sep 2021 t/m apr 2022 |
Arts-onderzoeker NVDV |
|
|
|
Drs. S.L. Wanders Jul 2021 t/m dec 2022 |
Arts-onderzoeker NVDV |
|
|
|
Drs. A.C. de Waal Apr 2022 t/m dec 2022 |
Arts-onderzoeker NVDV |
|
|
|
Drs. C. Smit Dec 2022 t/m heden |
Arts-onderzoeker NVDV |
|
|
* Zie toelichting in ‘Tabel: Overzicht betrokken partijen (modulaire herziening) 2023’
|
Werkgroepleden - versie 2014 |
Vereniging |
|
|
Dr. R.J. Damstra (voorzitter) |
NVDV |
|
|
Drs. A.B. Halk (secreatris) |
NVDV |
|
|
Dr. J.P. van den Berg |
VRA |
|
|
Mevr. Y. Born |
NVH |
|
|
Mevr. E.S.F.A. Butter |
V&VN oncologie |
|
|
Drs. E.B.L. van Dorst |
NVOG |
|
|
Dr. J.J.E. van Everdingen |
NVDV |
|
|
mevr. C. Feenstra |
NVH |
|
|
Drs. P. Gielink |
NVFL |
|
|
Drs. M.J. de Haas |
NVNG |
|
|
Dhr. A. Hendrickx |
Kon. Nederlandse Gen. voor Fysiotherapie |
|
|
Drs. J.T. Hidding |
NVFL |
|
|
Drs. J.B. Storm van Leeuwen |
NVPC |
|
|
Mevr. S. Nijland |
V&VN dermatologie |
|
|
Mevr. E. Oskam |
Borstkankervereniging Nederland (BVN) |
|
|
Mevr. I. Paulusma |
V&VN oncologie |
|
|
Dr. N. Russell |
NVRO |
|
|
Mevr. K. Rutgers- van Wijlen |
BPSW |
|
|
Mevr. I. Sissingh |
VATEK / NVOS-Orthobanda |
|
|
Dr. L.J.A. Strobbe |
NVVH |
|
|
Drs. C.J.A. Verhoeff-Braat |
Nederlands netwerk voor lymfoedeem en lipoedeem |
|
|
Dhr. R. Verwaard |
NVOS |
|
|
Dr. C.J.M. van der Vleuten |
NVDV |
|
|
Drs. H.G.J.M. Voesten |
NVVV |
|
|
Drs. A. Hartog |
Arts-onderzoeker NVDV |
|
|
Drs. M.C. Urgert |
Arts-onderzoeker NVDV |
|
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van de Nederlandse Vereniging voor Dermatologie en Venereologie.
|
Werk-groeplid |
Hoofdfunctie(s) |
Nevenfunctie(s) |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Getekend op |
|
Dhr. R.J. Damstra (voorzitter) |
|
Medisch manager zorgverantwoordelijke eenheid in ziekenhuis Nij Smellinghe (1e dag/week). |
n.v.t. |
n.v.t. |
n.v.t. |
De lymfologie is een klein vakgebied en primair lymfoedeem is internationaal als "Rare disease" erkend(Orphanet). Vanuit de samenwerking op Europees niveau zijn meerdere leden lid van landelijke organisaties op het gebied van lymfoedeem. Ik beschouw dat vooral als bundelen van expertise en kennis wat uiteindelijk de zorg voor de patiënt verbeterd. |
n.v.t. |
02-06-2020 |
|
Mw. C. van Montfrans |
|
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
25-07-2020 |
|
Mw. C. van der Vleuten |
Dermatoloog RadboudUMC (0.8 fte) |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
22-06-2020 |
|
Mw. S.S. Qiu Shao |
|
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
03-06-2020 |
|
Mw. M.E.E. Bröker |
Oncologisch chirurg Franciscus Gasthuis en Vlietland, Rotterdam |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
01-12-2022 |
|
Mw. E.B.L van Dorst |
Staflid gynaecologische oncologie UMC Utrecht |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
18-06-2020 |
|
Dhr. N. Groen |
Nucleair geneeskundige, Amphia ziekenhuis |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
19-06-2020 |
|
Dhr. B. Kreike |
Radiotherapeut, radiotherapie-groep, locatie Arnhem/Ede |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
04-06-2020 |
|
Mw. C. Alberts-Hoeben |
Huid- en oedeemtherapeut Huidtherapie Limburg |
Lid Expertgroep Oedeem NVH (vrijwilligers- en onkostenvergoeding) |
Dienstverband van een bedrijf met doelgroep oedeem-patiënten (Huidtherapie Limburg) |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
15-06-2020 |
|
Mw. S. Beusekom |
Huid- en oedeemtherapeut Heerlen |
NPI zelfmanagement cursus, advies functie bij de NVH, novomundo: examinator opleiding TEK |
Ik werk in een oedeempraktijk; maar conformeer mij aan de richtlijn. Ik verwacht geen toename van financiële stromen door de uitkomst van de richtlijn |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
12-11-2022 |
|
Mw. W. den Hollander |
Verpleegkundig specialist Jeroen Bosch Ziekenhuis, expertisegebied: Mamma-oncologie |
Consulent transmuraal Palliatief Advies Team |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
11-09-2023 |
|
Mw. F. Potijk |
|
Wetenschap Oncologie en Oedeem (WOO) commissie NVFL (vrijwillig met gedeeltelijke vergoeding) |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
18-06-2020 |
|
Mw. B. Pinkert |
Diëtist, Additief voiding diet & leefstijl (zelfstandige praktijk) |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
Ik vertegenwoordig de Nederlandse Vereniging van Diëtisten (NVD) in deze werkgroep. |
n.v.t. |
23-06-2020 |
|
Mw. C. Hovenier |
Volledig arbeidsongeschikt, formeel tot 15-08-2020 in dienst bij EMMA Communicatie te Den Haag als senior redacteur |
Stichting Olijf (vrijwilliger, onbezoldigd). |
n.v.t. |
n.v.t. |
n.v.t. |
Ik ben vrijwilliger bij stichting Olijf. Wij hebben er baat bij dat er een goede richtlijn komt, waarin ook de ervaringen uit de praktijk aan de orde komen, zover dat kan gegeven de stand der wetenschap en praktijk. Daarvoor zijn we gevraagd. Los daarvan hebben Olijf, BVN en onze koepelorganisatie NFK, noch haar vertegenwoordigers, enig gewin bij deze deelname. |
n.v.t. |
23-06-2020 |
|
Mw. A. Diepstraten |
Zelfstandig ondernemer en eigenaar Praktijk ‘de Vormende Hand: consulent hulpverlener & beeldend therapeut. |
n.v.t. |
n.v.t. |
Ik ben betrokken naaste van een persoon met lymfoedeem n.a.v. kankerbehandeling. We hebben ons echter allebei te houden aan het zorgvuldig behandelen van ontvangen informatie via Stichting Olijf, omdat we beiden bij Stichting Olijf zijn aangesloten. |
n.v.t. |
Ik ben vanuit mijn eigen bedrijf ingehuurd als coördinator Kwaliteit van Zorg bij stichting Olijf. Wij hebben er baat bij dat er een goede richtlijn komt, waarin ook de ervaringen uit de praktijk aan de orde komen, zover dat kan gegeven de stand der wetenschap en praktijk. Los daarvan hebben Olijf, BVN en onze koepelorganisatie de NFK, noch haar vertegenwoordigers, enig gewin bij deze deelname. |
n.v.t. |
22-06-2020 |
|
Mw. J.M.G. Fijn |
Gepensioneerd |
Ervaringsdeskundige bij de Expertgroep late Gevolgen bij Borstkankervereniging Nederland (vrijwilligerswerk) |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
16-09-2020 |
|
Mw. M. Velting |
Belangenbehartiger borstkankervereniging Nederland (24 uur). |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
16-11-2022 |
|
Dhr. W.F. Hoelen |
|
(Inter)nationaal docent oedeem en oncologie fysiotherapie, voorzitter oncologisch netwerk (KM) Onco in balans, Vicepresident Casley Smith international adviseur Medi, bestuurslid NLNet. |
Adviseur Medi (compressie hulpmiddelen) en opleidings-directeur Berekuyl Academy |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
12-11-2022 |
|
Dhr. P.A.M. van den Broek |
|
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
21-09-2020 |
|
Mw. E. de Booij |
Arts-onderzoeker NVDV |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
02-06-2020 |
|
Mw. E. van Veen |
Arts-onderzoeker NVDV |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
01-09-2021 |
|
Mw. S.L. Wanders |
Arts-onderzoeker NVDV |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
01-07-2021 |
|
Mw. A.C. de Waal |
Arts-onderzoeker NVDV |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
01-04-2022 |
|
Mw. C. Smit |
Arts-onderzoeker NVDV |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
06-12-2022 |
Inbreng patiëntenperspectief
Er is aandacht besteed aan het patiëntenperspectief door de zitting neming van verschillende patiënten van meerdere patiëntenverenigingen (stichting Olijf, BVN, NLNet, Huid Nederland) in de werkgroep en de opname van informatie over patiëntenvoorlichting. De conceptrichtlijn is tevens voor commentaar voorgelegd aan betreffende patiëntenverenigingen.
Wkkgz & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (gebaseerd op het stroomschema ontwikkeld door FMS).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst Raming |
Toelichting |
|
Achtergrond (pathofysiologie) (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Risicofactoren (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Indocyanine groen lymfografie (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Conservatieve behandeling (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Zwachtelen en bandageren (2014) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Intermitterende Pneumatische Compressie (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Therapeutische Elastische Kousen (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Manuele lymfedrainage (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Oefentherapie (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Reductiechirurgie (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Reconstructieve (micro)chirurgie (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Therapeutische Elastische Kousen (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Leefstijlinterventies: preventie, ondersteunende zorg en voorlichting (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
|
Organisatie van zorg (2023) |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn(module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. De richtlijn wordt via het internet verspreid onder alle relevante beroepsgroepen en ziekenhuizen en er zal in verschillende specifieke vaktijdschriften aandacht worden besteed aan de richtlijn. Tevens zal een samenvatting worden gemaakt. De voorlichtingsfolder van de NVDV zal worden afgestemd op de richtlijn. Het volledige implementatieplan is opgenomen in het bijlagedocument.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Onderstaand is de methode stapsgewijs beschreven.
Knelpuntenanalyse
In de voorbereidingsfase heeft een bijeenkomst plaatsgevonden waarvoor alle belanghebbenden zijn uitgenodigd. In deze bijeenkomst zijn knelpunten aangedragen door de werkgroepleden; NVDV, NVPC, NVVH, NVOG, NVNG, NVRO, NVH, V&VN, NVFL, NVD, NIP, Stichting Olijf, BVN, NLNet, Huid Nederland. Tevens werden uitgenodigd Zorgverzekeraars Nederland (ZN), Nederlandse Vereniging Ziekenhuizen (NVZ), Zorginstituut Nederland (ZiNL) en de Nederlandse Federatie van Universitair Medische Centra (NFU).
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse heeft de werkgroep uitgangsvragen opgesteld. Daarbij inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen en consultatie van experts. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. Literatuur is geselecteerd op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in bijlage 4.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR - voor systematische reviews; Cochrane - voor gerandomiseerd gecontroleerd onderzoek; Newcastle-Ottowa - voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen zijn overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs (2021)
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE
|
Definitie
|
|
Hoog
|
|
|
Redelijk
|
|
|
Laag
|
|
|
Zeer laag
|
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
C) Voor vragen over de waarde van meet- of classificatie-instrumenten (klinimetrie)
Deze instrumenten werden beoordeeld op validiteit, intra- (test-hertest) en inter-beoordelaarsbetrouwbaarheid, responsiviteit (alleen bij meetinstrumenten) en bruikbaarheid in de praktijk. (naar keuze: optie-1 ‘Bij ontbreken van een gouden standaard, werd een beoordeling van de bewijskracht van literatuurconclusies achterwege gelaten.’ Of optie-2 ‘De kracht van het wetenschappelijk bewijs werd bepaald met de generieke GRADE-methode’).
Beoordelen van het niveau van het wetenschappelijke bewijs (oude modules)
Bij de EBRO-methode (Evidence Based RichtlijnOntwikkeling) wordt een andere classificatie voor de beoordeling van de kwaliteit van studies aangehouden (van Everdingen 2004). Hierbij ligt de belangrijkheid van de uitkomstmaten niet van tevoren vast en is er geen vastgelegde procedure voor upgraden en downgraden van bewijs, zoals die bij GRADE geldt.
|
Kwaliteit |
Interventie |
Diagnostisch accuratesse-onderzoek |
Schade/bijwerkingen*, etiologie, prognose |
|
A1 |
Systematische review van ten minste twee onafhankelijk van elkaar uitgevoerde onderzoeken van A2-niveau |
||
|
A2 |
Gerandomiseerd dubbelblind vergelijkend klinisch onderzoek van goede kwaliteit van voldoende omvang |
Onderzoek ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
Prospectief cohortonderzoek van voldoende omvang en follow-up, waarbij adequaat gecontroleerd is voor ‘confounding’ en selectieve follow-up voldoende is uitgesloten. |
|
B |
Vergelijkend onderzoek, maar niet met alle kenmerken als genoemd onder A2 (hieronder valt ook patiënt-controleonderzoek, cohortonderzoek) |
|
|
|
C |
Niet-vergelijkend onderzoek |
||
|
D |
Mening van deskundigen |
||
* Deze classificatie is alleen van toepassing in situaties waarin om ethische of andere redenen gecontroleerde trials niet mogelijk zijn. Zijn die wel mogelijk dan geldt de classificatie voor interventies.
Bij het werken volgens de EBRO-methode zijn op basis van de beschikbare literatuur een of meerdere conclusies geformuleerd. Afhankelijk van het aantal onderzoeken en de mate van bewijs is een niveau van bewijskracht toegekend aan de conclusie (van Everdingen 2004).
|
Niveau |
Conclusie gebaseerd op |
|
1 |
Onderzoek van niveau A1 of ten minste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A2 |
|
2 |
1 onderzoek van niveau A2 of ten minste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
1 onderzoek van niveau B of C |
|
4 |
Mening van deskundigen |
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in één of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overkoepelende bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overkoepelende conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk. Door gebruik te maken van de Guideline Development Tool werd het Evidence to decision framework conform GRADE methodiek toegepast. Alle werkgroepleden hebben systematisch antwoord gegeven op vragen over de grootte van het effect en grootte van negatieve consequenties, waarden en voorkeuren van de patiënt, kosten en kosteneffectiviteit, beschikbaarheid van voorzieningen, aanvaardbaarheid, en overwegingen voor subgroepen in de patiëntenpopulatie. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Indicatorontwikkeling
Er werden geen indicatoren ontwikkeld voor deze richtlijn.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling beschreven (zie bijlage 11).
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften maar wetenschappelijk onderbouwde en breed gedragen inzichten en aanbevelingen waaraan zorgverleners zouden moeten voldoen om kwalitatief goede zorg te verlenen. Aangezien richtlijnen uitgaan van ‘gemiddelde patiënten’, kunnen zorgverleners in individuele gevallen zo nodig afwijken van de aanbevelingen in de richtlijn. Afwijken van richtlijnen is, als de situatie van de patiënt dat vereist, soms zelfs noodzakelijk. Een richtlijn beschrijft wat goede zorg is, ongeacht de financieringsbron (Zorgverzekeringswet (Zvw), Wet langdurige zorg (Wlz), Wet maatschappelijke ondersteuning (Wmo), aanvullende verzekering of eigen betaling door de cliënt/patiënt). Opname van een richtlijn in een register betekent dus niet noodzakelijkerwijs dat de in de richtlijn beschreven zorg verzekerde zorg is. Informatie over kosten zoals beschreven in de richtlijn is gebaseerd op beschikbare gegevens ten tijde van schrijven.
Commentaar- en autorisatiefase
De conceptrichtlijn is aan de betrokken (wetenschappelijke) verenigingen, (patiënt) organisaties en stakeholders voorgelegd ter becommentariëring. De commentaren zijn verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren is de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn is aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter autorisatie.
Literatuur
- Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
- Higgins JPT, Green S (editors). Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0 [updated March 2011]. The Cochrane Collaboration, 2011. Available from www.handbook.cochrane.org.
- Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit.. Online beschikbaar op http://richtlijnendatabase.nl/
- Van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum 2004.
- Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html