Prednisolon bij alcoholische hepatitis
Uitgangsvraag
Wat is de plek voor prednisolon bij patiënten met een alcoholische hepatitis?
Aanbeveling
Overweeg een patiënt met voorspeld ernstige alcoholische hepatitis met prednisolon te behandelen, na uitsluiting van een (intercurrente) onderliggende infectie. De volgende factoren kunnen hierbij meegewogen worden: mogelijk betere overleving op korte termijn; klinische voor- en nadelen van de behandeling voor de patiënt en het klinisch beloop in de eerste dagen na opname.
Voeg geen pentoxifylline toe aan een behandeling met prednisolon, vanwege het ontbreken van toegevoegde waarde ten aanzien van overleving.
Wees terughoudend met het toevoegen van N-acetylcysteïne aan een behandeling met prednisolon.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Voor deze module zijn tien RCT’s gevonden die het effect van prednisolon, of het op een gelijke manier werkende methylprednisolon, op de uitkomstmaten korte- en/of langetermijnoverleving hebben onderzocht in patiënten met alcoholische hepatitis in vergelijking met placebo. Eén studie hiervan heeft eveneens gekeken naar het effect van prednisolon in combinatie met pentoxifylline. Er zijn geen placebogecontroleerde studies gevonden met betrekking tot het effect van prednisolon in combinatie met N-acetyl cysteïne.
De gebundelde resultaten laten met betrekking tot kortetermijnoverleving een klinisch relevant positief effect zien van prednisolon ten opzichte van placebo. Voor de combinatie van prednisolon met pentoxifylline werd geen klinisch relevant verschil gevonden. Ook voor langetermijnoverleving werd geen klinisch relevant verschil gevonden van prednisolon of de combinatie ervan met pentoxifylline ten opzichte van placebo. De bewijskracht van de resultaten werd gelimiteerd door imprecisie en mogelijke risico op bias in met name de oudere studies. Diverse studies rapporteren geen of incomplete informatie over het randomisatieproces en de blindering van dit proces. Ook werd in een aantal studies gebruik gemaakt van een per-protocol analyse. Voor de cruciale uitkomstmaten kortetermijnoverleving en langetermijnoverleving is de bewijskracht laag voor zowel het effect van prednisolon als het effect van prednisolon in combinatie met pentoxifylline. De totale bewijskracht is laag.
Met betrekking tot het effect van prednisolon in combinatie met N-acetylcysteïne op overleving, heeft Nguyen-Khac (2011) een open-label trial uitgevoerd met 174 patiënten met ernstig alcoholische hepatitis. Deze studie is niet meegenomen in de literatuursamenvatting vanwege een incorrecte controlegroep (alleen prednisolon en geen placebo). In totaal kregen 85 patiënten prednisolon toegediend voor vier weken plus intraveneuze N-acetylcysteïne voor vijf dagen (zie studie voor details over dosering). De controlegroep, 89 patiënten, kreeg prednisolon toegediend volgens hetzelfde protocol plus placebo. Het aantal overlijdens na zes maanden was 23/85 (38%) in de interventiegroep, vergeleken met 34/89 (27%) in de controlegroep. Het gemiddelde aantal dagen tot overlijden was 54 ± 37 in de interventiegroep, vergeleken met 40 ± 35 dagen in de controlegroep. Hoewel deze studie op de korte termijn (28 dagen) een positief effect laat zien van prednisolon met N-acetylcysteïne aan een behandeling met prednisolon, dienen de resultaten met voorzichtigheid te worden geïnterpreteerd vanwege het ontbreken van een placebogroep, de beperkte studieomvang en ontbreken van resultaten over langetermijnoverleving. De richtlijn van de American College of Gastroenterology uit 2024 adviseren op basis van onder meer deze studie om te starten met een combinatie van prednisolon en N-acetylcysteïne in patiënten met ernstige alcoholische hepatitis. De werkgroep is echter van mening dat ook hier enige terughoudendheid geboden dient te worden, vanwege de bovengenoemde beperkingen in de studie van Nguyen-Khac (2011). Grotere studies (liefst met drie armen) met een langere follow-uptijd zijn noodzakelijk om definitieve conclusies te kunnen geven over de toevoeging van N-acetylcysteïne aan een behandeling met prednisolon.
Overige alternatieve behandelingen zoals prednisolon in combinatie met pentoxifylline lieten geen verbeterde overleving zien op korte- en of langetermijnoverleving en hebben dan ook geen toegevoegde waarde.
Corticosteroïden worden al sinds 40 jaar intensief bestudeerd in de behandeling van alcoholische hepatitis. De literatuursamenvatting met tien placebogecontroleerde onderzoeken laten wisselende resultaten zien. Dit geeft onder clinici al decennialang discussie over het nut van prednisolon. De ernst van de alcoholische hepatitis (hoogte van Maddrey Score of MELD-score) zou daarbij mogelijk ook mee moeten spelen, maar bewijs daarvoor ontbreekt vooralsnog. Wat de interpretatie van de studieresultaten eveneens bemoeilijk is dat het lijkt dat de overleving van patiënten met alcoholische hepatitis in de loop der tijd verbeterd is. De 28-dagen sterfte in de oudere studies uit de literatuursamenvatting varieerde tussen 30%-50%, terwijl deze in meer recente studies 8%-28% was (Thursz, 2015; Nguyen-Khac, 2011). Samenvattend moet toch gesteld worden dat deze studies ondanks de lage bewijslast een bescheiden ondersteuning bieden voor prednisolon op de kortetermijnoverleving en derhalve overwogen zou moeten worden bij de patiënten met een ernstige alcoholische hepatitis (MDF > 32 en een gevorderde MELD-score (e.g. tussen 25-39))(Arab, 2021). Wel is het van evident belang eerst eventueel onderliggende infecties op te sporen en te behandelen en zeker te zijn van de diagnose na uitsluiten van differentiaal diagnostische overwegingen voor het klinische beeld van de acute hepatitis (middels monitoren van het klinische beloop in de eerste dagen na opname). Een studie van Louvet (2009) liet namelijk zien dat 26% van de patiënten een infectie hebben bij opname en nog eens 24% een infectie oplopen tijdens prednisolon behandeling. Vanuit dit oogpunt zou een evaluatieperiode van drie totvijf dagen na dag van opname wenselijk zijn alvorens te starten met prednisolon.
Een uitspraak over het effect van corticosteroïden op de lange termijn is moeilijker te geven. Terugval in alcoholgebruik speelt hier waarschijnlijk de belangrijkste factor in (Jophlin, 2024). Slechts één studie heeft hiernaar gekeken, tevens de grootste gerandomiseerde studie bij ernstige alcoholische hepatitis, namelijk de STOPAH-studie (Thursz, 2015). Op basis van deze studie is met lage bewijskracht te concluderen dat er niet of nauwelijks verschil in langetermijnoverleving is. Meer onderzoek over de overleving op de lange termijn (en vooral met meenemen van de huidige multidisciplinaire benadering) moet hier meer uitsluitsel gaan geven.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Het gebruik van prednisolon bij patiënten met een alcoholische hepatitis kent enkele belangrijke bijwerkingen die met de patiënt of mantelzorger besproken dienen te worden. Meest voorkomende bijwerkingen zijn verlaagde koolhydraattolerantie, waardoor diabetes mellitus (DM) ontregelt kan worden of latente DM manifest kan worden. Daarnaast heeft prednisolon effect op de psyche, wat met name kan leiden tot stemmingsveranderingen, euforie, angst, prikkelbaarheid, depressie of slapeloosheid (Farmacotherapeutisch Kompas, n.d.). Prednisolon kan ook resulteren in wazig zien, het optreden van een tremor, toegenomen eetlust en een stijging in het aantal witte bloedlichaampjes (leukocytose). Dit laatste kan een eventuele detectie van een infectie bemoeilijken, omdat er een verdere verhoging van gevoeligheid voor infecties ontstaat (cirrose zorgt al voor een verminderde immuun response) en klinische verschijnselen van een infectie gemarkeerd worden. Het profylactisch toevoegen van breedspectrum antibiotica heeft aangetoond dat het aantal infecties verminderde, maar dit had geen effect op de overleving (Louvet, 2021). Vanwege het risico op resistentie en het uitselecteren van gisten wordt dan ook niet geadviseerd om naast prednisolon breedspectrum antibiotica te geven.
Kosten (middelenbeslag)
De kosten voor een behandeling met prednisolon zijn zeer laag (Farmacotherapeutisch Kompas, n.d.) en spelen daarom geen rol in de besluitvorming.
Aanvaardbaarheid, haalbaarheid en implementatie
In de praktijk wordt verschillend omgegaan met het toedienen van prednisolon bij patiënten met alcoholische hepatitis. Vanuit de literatuur kan met lage bewijskracht worden geconcludeerd dat prednisolon de kortetermijnoverleving kan verbeteren. De werkgroep doet dan ook de aanbeveling om prednisolon te overwegen bij patiënten met een voorspeld ernstige alcoholische hepatitis, tenzij gecontra-indiceerd.
Er zijn verder geen problemen bekend met betrekking tot de beschikbaarheid van prednisolon.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Na samenvoegen van alle placebogecontroleerde studies mag geconcludeerd worden dat prednisolon de korte termijn overleving zou kunnen verbeteren. De werkgroep adviseert dan ook bij een voorspeld ernstige alcoholische hepatitis prednisolon te overwegen. Het kan echter niet uitgesloten worden dat betere hedendaagse behandelopties ook een rol spelen in de overleving van patiënten met een ernstige alcoholische hepatitis. Er zijn twee contra-indicaties voor het starten van prednisolon. Daarnaast dient men bewust te zijn dat de behandeling niet zonder complicaties is. Een onderliggende (intercurrente) infectie is een absolute contra-indicatie voor het starten van prednisolon. Daarom dient dit voor aanvang uitgesloten en eventueel behandeld te worden. De werkgroep stelt dan ook voor op z’n vroegst drie dagen na opname te starten met prednisolon om zeker te zijn dat er geen sprake is van een gedecompenseerde cirrose op basis van infectie. Ook tijdens de behandeling met prednisolon dient men bedacht te zijn op het ontstaan van infecties. Een relatieve contra-indicatie voor het starten van prednisolon is de leverfunctie uitgedrukt in MELD-score. De ideale MELD-score ligt tussen de 25 en 39. Hierboven of hieronder kan het geven van prednisolon schadelijk zijn en moet dit vermeden worden. Het toevoegen van pentoxifylline is gebleken niet effectiever te zijn en dient niet gegeven te worden. Over het toevoegen van N-acetylcysteïne is meer onduidelijkheid. Hoewel de ACG-richtlijn uit 2024 dit middel wel adviseert, is de werkgroep van mening dat terughoudendheid geboden is vanwege beperkt bewijs over de toegevoegde waarde.
Onderbouwing
Achtergrond
Wetenschappelijke data over het nut van het geven van prednisolon bij ernstige alcoholische hepatitis zijn tegenstrijdig. Meerdere studies suggereren dat prednisolon gunstige effecten heeft op de korte termijn overleving, maar geen of weinig effect heeft op de lange termijn. Er zijn scoringsmodellen beschikbaar om de kans op gunstige response op prednisolon op de korte termijn in te schatten, maar deze modellen zijn er niet om de gunstige effecten op langere termijn te kunnen voorspellen. Daarnaast is het geven van prednisolon bij deze ernstig zieke patiëntenpopulatie niet zonder risico, met name in geval van infectieuze complicaties. In de huidige situatie wordt in Nederland per centrum verschillend omgegaan met het wel of niet geven van prednisolon, waarbij eveneens onduidelijkheid is over de selectie van patiënten hiervoor.
Conclusies / Summary of Findings
Short-term survival
|
Low GRADE
No GRADE
|
Prednisolone may increase short-term survival when compared with placebo in patients with alcoholic hepatitis.
Prednisolone in combination with pentoxifylline may result in little to no difference in short-term survival when compared with placebo in patients with alcoholic hepatitis.
No evidence was found regarding the effect of prednisolone in combination with N-acetyl cysteine on short-term survival compared with placebo in patients with alcoholic hepatitis.
Source: Blitzer, 1977; Carithers, 1989; Depew, 1980; Maddrey, 1978; Porter, 1971; Ramond, 1992; Shumaker, 1978; Theodossi, 1982; Thursz, 2015 |
Long-term survival
|
Low GRADE
No GRADE |
Prednisolone may result in little to no difference in long-term survival when compared with placebo in patients with alcoholic hepatitis.
Prednisolone in combination with pentoxifylline may result in little to no difference in long-term survival when compared with placebo in patients with alcoholic hepatitis.
No evidence was found regarding the effect of prednisolone in combination with N-acetyl cysteine on long-term survival compared with placebo in patients with alcoholic hepatitis.
Source: Mendenhall, 1984; Thursz, 2015 |
Samenvatting literatuur
Description of studies
Buzzetti (2017) conducted a systematic review and meta-analysis for the effect of different pharmacological interventions in the management of alcohol-related liver disease. The database Cochrane Central Register of Controlled Trials (CENTRAL), MEDLINE, Embase, Science Citation Index Expanded, World Health Organization International Clinical Trials Registry Platform and multiple randomized controlled trials registers were searched until February 2017. Inclusion criteria included: RCTs involving patients with alcohol-related liver disease (broader compared to PICO of current literature analysis) and pharmacological interventions with target on the liver, compared with each other either alone or in combination or with placebo or no intervention. A total of 81 RCTs were included in the study. Of these, twelve RCTs studied the effect of (methyl)prednisolone (alone or in combination with pentoxifylline) compared with placebo in patients with alcoholic hepatitis. Two studies did not report on short-term survival (30-days) or long-term survival (1-2 years) (Campra, 1973; Helman, 1971) and were excluded in the current summary of literature. The remaining ten RCTs are further considered (Blitzer, 1977; Carithers, 1989; Depew, 1980; Maddrey, 1978; Mendenhall, 1984; Porter, 1971; Ramond, 1992; Shumaker, 1978; Theodossi, 1982; Thursz, 2015), with a total of 1728 patients.
Of the ten relevant studies in Buzzetti (2017), six studies tested the effect of prednisolone (Blitzer, 1977; Depew, 1980; Maddrey, 1978; Mendenhall, 1984; Ramond, 1992; Thursz, 2015) and four studies tested the effect of methylprednisolone (Carithers, 1989; Porter, 1971; Shumaker, 1978; Theodossi, 1982) compared with placebo (Table 1). Because methylprednisolone is similar to prednisolone, these studies are also included. One study also tested the effect of prednisolone in combination with pentoxifylline (Thursz, 2015). The dosage for the intervention products ranged from 5-60 mg/day for prednisolone, with most studies using a dosage of 40 mg/day. For methylprednisolone, dosages ranged from 32-120 mg/day with one study (Theodossi, 1982) using a dosage of 1 g for three days. Thursz (2015) used a dosage of 400 mg pentoxifylline for the study arm receiving prednisolone and pentxofylline. Except for the study of Theodossi (2015), duration of the intervention was 26-30 days, with multiple studies including a tapering period within the intervention duration (Blitzer, 1977; Depew, 1980; Mendenhall, 1984; Porter 1971; Shumaker, 1978). The total number of patients in the included studies is 1641, although Thursz (2015) also included a study group receiving pentoxifylline only (n = 273), while Mendenhall (1984) included a study group receiving oxandrolone (n = 85). These study groups will not be further considered. Follow-up period ranged between one-three months, up to one year in the study of Thursz (2015). The studies were similar with respect to mean age (41-51 years), although it was not reported in the study of Theodossi (1982). Proportion of males ranged between 31-65%, with only males involved in the studies of Blitzer (1977) and Mendenhall (1984). Risk of bias was assessed via the Cochrane method, with all twelve RCTs containing high risk of bias, in most cases due to insufficient information on randomization and blinding method, funding by pharmaceutical companies, disease history and use of a per protocol-analysis.
Table 4. Interventions used in relevant, included studies of Buzzetti (2017).
|
Study |
Intervention |
Dosage |
Duration of intervention |
|
Blitzer, 1977 |
Prednisolone |
40 mg/day |
Two weeks (followed by 12 days tapering) |
|
Depew, 1980 |
Prednisolone |
40 mg/day |
28 days (followed by 14 days tapering) |
|
Maddrey, 1978 |
Prednisolone |
5 mg/day |
28-32 days |
|
Mendenhall, 1984 |
Prednisolone |
60 mg/day, tapered to 5 mg |
30 days |
|
Ramond, 1992 |
Prednisolone |
40 mg/day |
28 days |
|
Thursz, 2015 |
Prednisolone |
40 mg/day |
28 days |
|
Prednisolone + pentoxifylline |
40 mg/d prednisolone + pentoxifylline 400 mg/day |
28 days |
|
|
Carithers, 1989 |
Methylprednisolone |
32 mg/day |
28 days |
|
Porter, 1971 |
Methylprednisolone |
120 mg/day |
Ten days or until clinical improvement |
|
Shumaker, 1978 |
Methylprednisolone |
80 mg/day |
Four to seven days, followed by 21-24 days tapering |
|
Theodossi, 1982 |
Methylprednisolone |
1 g/day |
Three days |
Results
Short-term survival
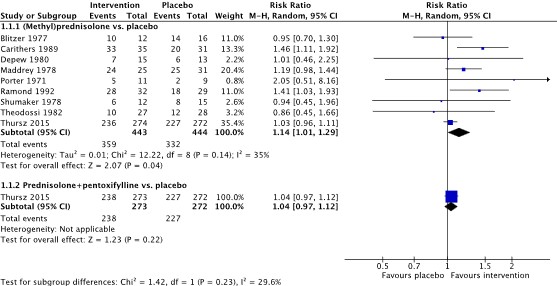
All included studies, except for the study by Mendenhall (1984) reported on the outcome measure short-term survival defined as 30-day mortality (Blitzer, 1977; Carithers, 1989; Depew, 1980; Maddrey, 1978; Porter, 1971; Ramond, 1992; Shumaker, 1978; Theodossi, 1982; Thursz, 2015). With recalculation, a total of 359/443 patients (81%) who received (methyl)prednisolone were alive 30 days after start of treatment, compared to 332/444 patients (75%) in the control group. The corresponding risk ratio is 1.14 (95%CI 1.01 to 1.29) in favor of the intervention group, which is considered clinically relevant.
In the study of Thursz (2015), 238/273 patients (87%) who received a combination of prednisolone and pentoxifylline were alive 30 days after start of treatment, compared to 332/444 patients (75%) in the control group. The corresponding risk ratio is 1.04 (95%CI 0.97 to 1.12) in favor of the intervention group, which is not considered clinically relevant.
Figure 4. Forest plot showing the comparison between (methyl)prednisolone and placebo on short-term survival (30-day survival). Subgroup analysis was performed for the comparison between prednisolone + pentoxifylline compared with placebo. Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; SD: standard deviation; I2; statistical heterogeneity; CI: confidence interval.
Long-term survival
Two studies reported on the outcome measure long-term survival. Both Mendenhall (1984) and Thursz (2015) reported on one-year survival, defined as one-year mortality. In the study by Mendenhall (1984), 35/90 patients (39%) who received prednisolone were alive one year after start of treatment, compared to 38/88 patients (43%) in the control group. The corresponding risk ratio is 0.90 (95%CI 0.63 to 1.28) in favor of the control group, which is considered clinically relevant. In the study by Thursz (2015), 164/274 patients (60%) who received prednisolone were alive one year after start of treatment, compared to 166/272 patients (61%) in the control group. The corresponding risk ratio is 0.98 (95%CI 0.85 to 1.12) in favor of the control group, which is not considered clinically relevant.
In the study by Thursz (2015) a total of 173/273 patients (63%) who received a combination of prednisolone and pentoxifylline were alive one year after start of treatment, compared to 166/272 patients (61%) in the control group. The corresponding risk ratio is 1.04 (95%CI 0.91 to 1.18) in favor of the intervention group, which is not considered clinically relevant.
Level of evidence of the literature
The level of evidence came from RCTs and therefore started as high.
Short-term survival
The level of evidence regarding the outcome measure short-term survival for the effect of prednisolone solely was downgraded by 2 levels to low because of risk of bias (infrequent loss to follow-up in several included studies with use of per-protocol analysis, lack of information on allocation concealment in several studies) and number of included patients (effect estimate (95%CI) crosses the upper threshold for clinical relevance, -1 level for imprecision).
The level of evidence regarding the outcome measure short-term survival for the effect of prednisolone in combination with pentoxifylline was downgraded by 2 levels to low because of number of included patients (effect estimate (95%CI) crosses the upper threshold for clinical relevance, only one study included with low number of participants, -2 levels for imprecision).
Long-term survival
The level of evidence regarding the outcome measure long-term survival for the effect of prednisolone solely was downgraded by 2 levels to low because of number of included patients (effect estimate (95%CI) crosses the lower and upper threshold for clinical relevance in both included studies, -2 levels for imprecision).
The level of evidence regarding the outcome measure long-term survival for the effect of prednisolone in combination with pentoxifylline was downgraded by 2 levels to low because of number of included patients (effect estimate (95%CI) crosses the upper threshold for clinical relevance, only one study included with low number of participants, -2 levels for imprecision).
Short-term survival and long-term survival (prednisolone + N-acetyl cysteine)
No evidence was found regarding the outcome measures short-term survival and long-term survival for the effect of prednisolone in combination with N-acetyl cysteine, compared with placebo. Therefore, the level of evidence could not be assessed.
Zoeken en selecteren
A systematic review of the literature was performed to answer the following question:
What are the effects of prednisolone (alone or in combination with pentoxifylline or N-acetyl cysteine) compared to placebo on short- and long-term survival in adult patients with acute alcoholic hepatitis?
P (Patients): adult patients with alcoholic hepatitis
I (Intervention): prednisolone (solely or in combination with N-acetyl cysteine or pentoxifylline)
C (Comparison): placebo or standard care
O (Outcomes): long-term survival, short-term survival
Relevant outcome measures
The guideline development group considered long-term survival and short-term survival as critical outcome measures for decision making.
The working group defined the outcome measures as follows:
- Short-term survival: Survival at 30-days
- Long-term survival: Survival at 1-2 years
The working group defined a 10% difference (RR < 0.91 or > 1.10) as a minimal clinically (patient) important difference for all outcomes.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until March 17, 2023. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 367 hits. Studies were selected based on the following criteria: systematic reviews or RCTs involving adult patients with alcoholic hepatitis. Ten studies were initially selected based on title and abstract screening. After reading the full text, nine studies were excluded (see the table with reasons for exclusion under the tab Methods), and one study was included (Buzzetti, 2017).
Results
One systematic review (Cochrane review) was included in the analysis of the literature (Buzzetti, 2017). Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
Referenties
- Arab JP, Díaz LA, Baeza N, Idalsoaga F, Fuentes-López E, Arnold J, Ramírez CA, Morales-Arraez D, Ventura-Cots M, Alvarado-Tapias E, Zhang W, Clark V, Simonetto D, Ahn JC, Buryska S, Mehta TI, Stefanescu H, Horhat A, Bumbu A, Dunn W, Attar B, Agrawal R, Haque ZS, Majeed M, Cabezas J, García-Carrera I, Parker R, Cuyàs B, Poca M, Soriano G, Sarin SK, Maiwall R, Jalal PK, Abdulsada S, Higuera-de la Tijera MF, Kulkarni AV, Rao PN, Guerra Salazar P, Skladaný L, Bystrianska N, Prado V, Clemente-Sanchez A, Rincón D, Haider T, Chacko KR, Cairo F, de Sousa Coelho M, Romero GA, Pollarsky FD, Restrepo JC, Castro-Sanchez S, Toro LG, Yaquich P, Mendizabal M, Garrido ML, Narvaez A, Bessone F, Marcelo JS, Piombino D, Dirchwolf M, Arancibia JP, Altamirano J, Kim W, Araujo RC, Duarte-Rojo A, Vargas V, Rautou PE, Issoufaly T, Zamarripa F, Torre A, Lucey MR, Mathurin P, Louvet A, García-Tsao G, González JA, Verna E, Brown RS, Roblero JP, Abraldes JG, Arrese M, Shah VH, Kamath PS, Singal AK, Bataller R. Identification of optimal therapeutic window for steroid use in severe alcohol-associated hepatitis: A worldwide study. J Hepatol. 2021 Nov;75(5):1026-1033. doi: 10.1016/j.jhep.2021.06.019. Epub 2021 Jun 21. PMID: 34166722.
- Buzzetti E, Kalafateli M, Thorburn D, Davidson BR, Thiele M, Gluud LL, Del Giovane C, Askgaard G, Krag A, Tsochatzis E, Gurusamy KS. Pharmacological interventions for alcoholic liver disease (alcohol-related liver disease): an attempted network meta-analysis. Cochrane Database Syst Rev. 2017 Mar 31;3(3):CD011646. doi: 10.1002/14651858.CD011646.pub2. PMID: 28368093; PMCID: PMC6464309.
- Crabb DW, Im GY, Szabo G, Mellinger JL, Lucey MR. Diagnosis and Treatment of Alcohol-Associated Liver Diseases: 2019 Practice Guidance From the American Association for the Study of Liver Diseases. Hepatology. 2020 Jan;71(1):306-333. doi: 10.1002/hep.30866. PMID: 31314133.
- Farmacotherapeutisch Kompas n.d., Prednisolon (systemisch), Zorginstituut Nederland, accessed January 8 2024., < https://www.farmacotherapeutischkompas.nl/bladeren/preparaatteksten/atc/H02AB06#kosten>
- Jophlin LL, Singal AK, Bataller R, Wong RJ, Sauer BG, Terrault NA, Shah VH. ACG Clinical Guideline: Alcohol-Associated Liver Disease. Am J Gastroenterol. 2024 Jan 1;119(1):30-54. doi: 10.14309/ajg.0000000000002572. Epub 2023 Sep 1. PMID: 38174913.
- Louvet A, Labreuche J, Dao T, Thévenot T, Oberti F, Bureau C, Paupard T, Nguyen-Khac E, Minello A, Bernard-Chabert B, Anty R, Wartel F, Carbonell N, Pageaux GP, Hilleret MN, Moirand R, Nahon P, Potey C, Duhamel A, Mathurin P. Effect of Prophylactic Antibiotics on Mortality in Severe Alcohol-Related Hepatitis: A Randomized Clinical Trial. JAMA. 2023 May 9;329(18):1558-1566. doi: 10.1001/jama.2023.4902. PMID: 37159035; PMCID: PMC10170332.
- Louvet A, Wartel F, Castel H, Dharancy S, Hollebecque A, Canva-Delcambre V, Deltenre P, Mathurin P. Infection in patients with severe alcoholic hepatitis treated with steroids: early response to therapy is the key factor. Gastroenterology. 2009 Aug;137(2):541-8. doi: 10.1053/j.gastro.2009.04.062. Epub 2009 May 13. PMID: 19445945.
- Mathurin P, Moreno C, Samuel D, Dumortier J, Salleron J, Durand F, Castel H, Duhamel A, Pageaux GP, Leroy V, Dharancy S, Louvet A, Boleslawski E, Lucidi V, Gustot T, Francoz C, Letoublon C, Castaing D, Belghiti J, Donckier V, Pruvot FR, Duclos-Vallée JC. Early liver transplantation for severe alcoholic hepatitis. N Engl J Med. 2011 Nov 10;365(19):1790-800. doi: 10.1056/NEJMoa1105703. PMID: 22070476.
- Nguyen-Khac E, Thevenot T, Piquet MA, Benferhat S, Goria O, Chatelain D, Tramier B, Dewaele F, Ghrib S, Rudler M, Carbonell N, Tossou H, Bental A, Bernard-Chabert B, Dupas JL; AAH-NAC Study Group. Glucocorticoids plus N-acetylcysteine in severe alcoholic hepatitis. N Engl J Med. 2011 Nov 10;365(19):1781-9. doi: 10.1056/NEJMoa1101214. PMID: 22070475.
Evidence tabellen
Evidence table for systematic review of RCTs and observational studies (intervention studies)
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size |
Comments |
|
Buzzetti, 2017
[individual study characteristics deduced from [Buzzetti, 2017]] |
SR and meta-analysis of RCTs
Literature search up to February 2017]
A: Blitzer, 1977 B: Carithers, 1989 C: Depew, 1980 D: Maddrey, 1978 E: Mendenhall, 1984 F: Porter, 1971 G: Ramond, 1992 H: Shumaker, 1978 I: Theodossi, 1982 J: Thursz, 2015
Study design: All studies: RCT, parallel groups
Setting and Country: A: USA B: USA C: USA D: USA E: USA F: USA G: France H: USA I: United Kingdom J: United Kingdom
Source of funding and conflicts of interest: A: Funding of intervention products by pharmaceutical company. B: Non-commercial funding C: Unknown D: Non-commercial funding E: Funding of intervention products by pharmaceutical company. F: Non-commercial funding G: Non-commercial funding H: Funding of intervention products by pharmaceutical company. I: Unknown J: Non-commercial funding |
Inclusion criteria SR: RCTs involving patients with alcohol-related liver disease. Pharmacological intervention that are possible treatments for alcohol-related liver disease with the liver as target of treatment, compared with each other either alone or in combination or with placebo or no intervention
Exclusion criteria SR: RCTs involving patients with previous liver transplantation or other causes of chronic liver disease (e.g. hepatitis C).
Ten relevant studies with focus on (methyl)prednisolone and short-term (30-day) or long-term (1-2 years) survival as outcomes are reported in this table.
Important patient characteristics at baseline:
N, mean age A: 33, 48 years B: 67, 43 years C: 28, 49 years D: 57, 41 years E: 178, 51 years F: 23, 47 years G: 65, 48 years H: 27, 45 years I: 60, mean age not stated J: 1103, 49 years
Sex (n, % male): A: 100% B: 51 (61.2%) C: 16 (57.1%) D: 57 (37 (64.3%) E: 100% F: 16 (65%) G: 23 (31.1%) H: 16 (59.3%) I: 36 (56.4%) J: 696 (62.8%)
Age groups among studies largely similar. Two studies only included male participants. |
A: Prednisolone, 10 mg; four times daily (total 40 mg/day) for 14 days, then tapering (20 mg for four days, 10 mg for four days, 5 mg for four days). B: Methylprednisolone, 32 mg/day for 28 days C: Prednisolone, 40 mg, once daily for 28 days, followed by 14 days tapering. D: Prednisolone, 5 mg/day for 28-32 days E: Prednisolone, 60 mg/day, tapered to 5 mg/day in one month. F: Methylprednisolone, 40 mg, thrice daily. Tapered after ten days if clinically improvement was seen. G: Prednisolone, 40 mg, once daily for 28 days H: Methylprednisolone, 80 mg for 4-7 days, then tapering for the next 21-24 days I: Methylprednisolone 1 g/daily, intravenously for three days J: Two intervention groups: a) Prednisolone 40 mg once daily, plus pentoxifylline 400 mg thrice daily for 28 days b) Prednisolone 40 mg once daily for 28 days
|
A: Placebo B: Placebo C: Placebo D: Placebo E: Placebo F: Placebo G: Placebo H: Placebo I: Placebo J: Placebo
|
Endpoint of follow-up: A: Nine weeks B: 30 days C: 42 days D: 28-32 days E: One year F: 30 days G: Three months H: 30 days I: 30 days J: One year
For how many participants were no complete outcome data available? A: 5 (15.2%) B: None C: None D: 1 (1.8%) E: None F: 3 (13%) G: 4 (6.2%) H: None I: 5 (8.3%) J: 11 (1%)
|
30-day mortality OR, Fixed effects model [95% CI] A: 1.4 [0.17 to 11.68] B: 0.11 [0.02 to 0.55] C: 0.98 [0.22 to 4.34] D: 0.17 [0.02 to 1.55] F: 0.34 [0.05 to 2.46] G: 0.23 [0.06 to 0.85] H: 1.14 [0.25 to 5.22] I: 1.27 [0.43 to 3.76] J: a) 0.81 [0.51 to 1.3] b) 0.74 [0.46 to 1.2]
Pooled effect (fixed effects model), excluding Jb: OR 0.59 [95% CI 0.34 to 1.04] favoring intervention. Heterogeneity (I2): 36.47%
Mortality at maximum follow-up Only studies who reported results for follow-up of at least one year. OR [95% CI] E: 1.19 [0.66 to 2.17] L: a) 1.05 [0.75 to 1.48] b) 0.91 [0.64 to 1.28]
|
Risk of bias (high, some concerns or low): Tool used by authors: Cochrane method
A: High B: High C: High D: High E: High F: High G: High H: High I: High J: High
Facultative: The authors conclude that the overall quality of evidence is low with high risk of bias in the included studies. There is no evidence that glucocorticoids (prednisolone and methylprednisolone) alone or in combination with pentoxifylline reduce the risk of mortality after three or more months. However, 30-day mortality might be reduced, although certainty is very limited.
Personal remarks: Except for Mendenhall (1984) and Thursz (2015), all included studies are relatively small. Intervention doses and follow-up times range widely. Clear inconsistency in results.
|
Risk of bias table for intervention studies (randomized controlled trials; based on Cochrane risk of bias tool and suggestions by the CLARITY Group at McMaster University)
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated?
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented?
Were patients blinded?
Were healthcare providers blinded?
Were data collectors blinded?
Were outcome assessors blinded?
Were data analysts blinded?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measure
LOW Some concerns HIGH
|
|
Blitzer, 1977 |
Probably yes
Reason: No information on randomization method, although correct allocation concealment method used. |
Probably yes
Reason: Sealed envelopes randomly assigned to participants. |
Definitely yes
Reason: Double-blind study, only pharmacist aware of type of therapy. Placebo tablets similar appearance compared to intervention product. |
Definitely no
Reason: Five of 18 patients in the intervention group stopped the study within five days, compared to no patients in the control group. Use of a per-protocol analysis. |
Definitely yes
Reason: All relevant outcomes were reported |
Definitely yes
Reason: No other problems noted |
Some concerns (all outcomes)
Reason: Use of per-protocol analysis with high number dropouts in intervention group. |
|
Carithers, 1989 |
Probably yes
Reason: Method for preparation of random code not stated. Random code sequence kept by an independent source. |
No information |
Probably yes
Reason: ‘double-blind trial’, no further information stated. |
Definitely yes
Reason: Only one patient lost to follow-up. All patients included in analysis. |
Definitely yes
Reason: All relevant outcomes were reported |
Definitely yes
Reason: No other problems noted |
Some concerns (all outcomes)
Reason: No information on allocation concealment. Limited details on blinding process. |
|
Depew, 1980 |
Probably yes
Reason: Unclear, very limited details on allocation concealment
|
Probably yes
Reason: Drugs provided were coded, not further information stated. |
Definitely yes
Reason: Patients, principal investigator and outcome assessors were blinded. |
Definitely yes
Reason: No loss to follow-up in both study groups. |
Definitely yes
Reason: All relevant outcomes were reported |
Definitely yes
Reason: No other problems noted |
Some concerns (all outcomes)
Reason: Limited information on randomization process and allocation concealment. |
|
Maddrey, 1978 |
No information
|
No information
|
Definitely yes
Reason: Double-blind study design; principal investigators were blinded. Intervention products had similar appearance. |
Probably no
Reason: One patient stopped with before treatment, another patient stopped with prednisolone due to complications. Use of per-protocol analysis. |
Definitely yes
Reason: All relevant outcomes were reported |
Definitely yes
Reason: No other problems noted |
Some concerns (all outcomes)
Reason: No information on randomization process and allocation concealment. Use of per-protocol analysis of minor detail, due to low dropout rate. |
|
Mendenhall, 1984 |
Probably yes
Reason: Randomization was balanced within each hospital, according to disease severity. |
No information |
Definitely yes
Reason: Patients, physicians and staff of hospital pharmacy were unaware of the specific medication use. |
Probably yes
Reason: Loss to follow-up was infrequent in intervention and control group. Use of ITT-analysis, although exact method used is not stated. |
Definitely yes
Reason: All relevant outcomes were reported |
Definitely yes
Reason: No other problems noted |
Some concerns (all outcomes)
Reason: No information on allocation concealment. |
|
Porter, 1971 |
Definitely yes
Reason: Randomization achieved by numbers drawn from a pool. |
Probably yes
Reason: Both intervention and placebo products were coded by numbers. No further information on similarity. |
Probably yes
Reason: Patients and physicians were blinded until end of study. Not clearly stated what role of physician is and to what extent other disciplines were involved. |
Probably no
Reason: Three of 23 patients (study group unclear) died within 36 hours after start of therapy, not included in analysis. |
Definitely yes
Reason: All relevant outcomes were reported |
Definitely yes
Reason: No other problems noted |
Some concerns (all outcomes)
Reason: Use of per-protocol analysis with high dropout rate. Study group to which dropouts belonged not reported. |
|
Ramond, 1992 |
Definitely yes
Reason: Computer generated randomization sequence, stratified by gender. |
Probably yes
Reason: Randomization procedure was blinded for principal investigator and associates. |
Probably no
Reason: Pharmacist was aware of type of drugs given to patients. |
Probably no
Reason: Loss to follow-up was infrequent in both study groups, although dropouts were not included in the analysis. |
Definitely yes
Reason: All relevant outcomes were reported |
Definitely yes
Reason: No other problems noted |
Some concerns MELD-score) LOW (short and long-term survival
Reason: Inadequate blinding method. |
|
Shumaker, 1978 |
Probably yes
Reason: Method for preparation of random code not stated. Random code sequence kept by an independent source. |
No information |
Probably yes
Reason: Physician assistants that performed clinical evaluations were blinded. Number of placebo tablets was equal to number of intervention tablets. |
Definitely yes
Reason: One patient from the intervention group voluntarily withdrew from the study but was included in statistical analysis. |
Definitely yes
Reason: All relevant outcomes were reported |
Definitely yes
Reason: No other problems noted |
Some concerns (all outcomes)
Reason: No information on allocation concealment. |
|
Theodossi, 1982 |
Probably yes
Reason: No information on randomization method, although correct allocation concealment method used. |
Definitely yes
Reason: Allocation with random, sealed envelopes. |
Probably no
Reason: No information stated on blinding. Intervention product was given intravenously, unclear for placebo product. |
Definitely no
Reason: With study groups equal in number, one of 28 patients from intervention groups withdrew compared to four of 32 patients from the control group. Use of per-protocol analysis. |
Definitely yes
Reason: All relevant outcomes were reported |
Definitely yes
Reason: No other problems noted |
Some concerns (MELD-score) LOW (short and long-term survival)
Reason: No information on blinding method. Use of per-protocol analysis of minor detail due to low dropout rate. |
|
Thursz, 2015 |
Definitely yes
Reason: Computer-generated randomization with block size four. |
Definitely yes
Reason: Treatment allocation blinded to staff and patients. |
Probably yes
Reason: All involved personnel and patients were blinded, except for statisticians for analysis purposes. |
Definitely yes
Reason: All study groups had similar an infrequent loss to follow up, apart from deaths (outcome). Use of ITT-analysis. |
Definitely yes
Reason: All relevant outcomes were reported |
Definitely yes
Reason: No other problems noted |
LOW (all outcomes) |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Hmoud BS, Patel K, Bataller R, Singal AK. Corticosteroids and occurrence of and mortality from infections in severe alcoholic hepatitis: a meta-analysis of randomized trials. Liver Int. 2016 May;36(5):721-8. doi: 10.1111/liv.12939. Epub 2015 Sep 14. PMID: 26279269. |
Specific study population (encephalopathy), more recent review available. |
|
Lee YS, Kim HJ, Kim JH, Yoo YJ, Kim TS, Kang SH, Suh SJ, Joo MK, Jung YK, Lee BJ, Seo YS, Yim HJ, Yeon JE, Kim JS, Park JJ, Um SH, Bak YT, Byun KS. Treatment of Severe Alcoholic Hepatitis With Corticosteroid, Pentoxifylline, or Dual Therapy: A Systematic Review and Meta-Analysis. J Clin Gastroenterol. 2017 Apr;51(4):364-377. doi: 10.1097/MCG.0000000000000674. PMID: 27636406. |
Specific study population (severe intoxication). |
|
Louvet A, Thursz MR, Kim DJ, Labreuche J, Atkinson SR, Sidhu SS, O'Grady JG, Akriviadis E, Sinakos E, Carithers RL Jr, Ramond MJ, Maddrey WC, Morgan TR, Duhamel A, Mathurin P. Corticosteroids Reduce Risk of Death Within 28 Days for Patients With Severe Alcoholic Hepatitis, Compared With Pentoxifylline or Placebo-a Meta-analysis of Individual Data From Controlled Trials. Gastroenterology. 2018 Aug;155(2):458-468.e8. doi: 10.1053/j.gastro.2018.05.011. Epub 2018 May 5. PMID: 29738698. |
Search only performed in Medline, relevant articles missing. |
|
Njei B, Do A, McCarty TR, Fortune BE. Corticosteroids Versus Pentoxifylline for Severe Alcoholic Hepatitis: A Sequential Analysis of Randomized Controlled Trials. J Clin Gastroenterol. 2016 Nov/Dec;50(10):871-881. doi: 10.1097/MCG.0000000000000585. PMID: 27404293; PMCID: PMC5065367. |
More recent review available |
|
Pavlov CS, Varganova DL, Casazza G, Tsochatzis E, Nikolova D, Gluud C. Glucocorticosteroids for people with alcoholic hepatitis. Cochrane Database Syst Rev. 2017 Nov 2;11(11):CD001511. doi: 10.1002/14651858.CD001511.pub3. Update in: Cochrane Database Syst Rev. 2019 Apr 09;4:CD001511. PMID: 29096421; PMCID: PMC6491283. |
No clear/full outcome data reported |
|
Singal AK, Kodali S, Vucovich LA, Darley-Usmar V, Schiano TD. Diagnosis and Treatment of Alcoholic Hepatitis: A Systematic Review. Alcohol Clin Exp Res. 2016 Jul;40(7):1390-402. doi: 10.1111/acer.13108. Epub 2016 Jun 2. PMID: 27254289; PMCID: PMC4930399. |
Systematic review with narrative output, no statistic analysis
|
|
Singh S, Murad MH, Chandar AK, Bongiorno CM, Singal AK, Atkinson SR, Thursz MR, Loomba R, Shah VH. Comparative Effectiveness of Pharmacological Interventions for Severe Alcoholic Hepatitis: A Systematic Review and Network Meta-analysis. Gastroenterology. 2015 Oct;149(4):958-70.e12. doi: 10.1053/j.gastro.2015.06.006. Epub 2015 Jun 16. PMID: 26091937. |
More recent review available
|
|
Yu CH, Xu CF, Ye H, Li L, Li YM. Early mortality of alcoholic hepatitis: a review of data from placebo-controlled clinical trials. World J Gastroenterol. 2010 May 21;16(19):2435-9. doi: 10.3748/wjg.v16.i19.2435. PMID: 20480532; PMCID: PMC2874151. |
More recent review available
|
|
Akriviadis E, Sinakos E. Treatment of alcoholic hepatitis: is this a "dead-end"? Ann Gastroenterol. 2016 Apr-Jun;29(2):236-7. doi: 10.20524/aog.2016.0023. PMID: 27065743; PMCID: PMC4805751. |
Narrative review
|
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 30-09-2025
Beoordeeld op geldigheid : 10-09-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit [de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met somatische complicaties als gevolg van risicovol alcoholgebruik.
Werkgroep
- Dr. H. van Soest, MDL-arts, Haaglanden MC, NVMDL (voorzitter)
- Dr. M.A. Lantinga, MDL-arts, Amsterdam UMC, NVMDL (vice-voorzitter)
- Dr. R.B. Takkenberg, MDL-arts, Amsterdam UMC, NVMDL
- Dr. H.J.M. de Jonge, MDL-arts, Jeroen Bosch Ziekenhuis, NVMDL
- Prof. dr. A.F.A. Schellekens, psychiater, Radboudumc, NVVP
- Drs. T. van Grinsven, verslavingsarts, Novadic Kentron, VVGN
- Dr. M. van Loon, spoedeisende hulparts, Haaglanden MC, NVSHA
- Drs. H. Lam, levertransplantatiechirurg, LUMC, NVvH (vanaf 2024)
- Drs. J.A. Willemse, directeur, Nederlandse Leverpatienten Vereniging
- Drs. P.J. van Dongen, ervaringsdeskundige en vrijwilliger, Hersenletsel.nl (tot 2023)
- H.M. Luttikhuis Msc, ziekenhuisapotheker, Slingeland Ziekenhuis, NVZA (vanaf 2023)
- Dr. R.A. Weersink, ziekenhuisapotheker, Deventer Ziekenhuis (tot 2024), NVZA (vanaf 2023)
- Dr. J. Blokzijl, MDL-arts, UMCG, NTV/LOL (vanaf 2025, specifiek voor module levertransplantatie)
Klankbordgroep
- J.E. de Haan, intensivist, Erasmus MC, NVIC
- Drs. A.T. Timmer, klinisch geriater, Tjongerschans Ziekenhuis, NVKG
- Dr. J.M.W. van den Ouweland, klinische chemie en endocrinologie, Canisius Wilhelmina Ziekenhuis, NVKC
- Dhr. A. van den Berg, ervaringsdeskundige, Stichting het Zwarte Gat (vanaf 2024)
Met ondersteuning van
- H. Olthuis-van Essen MSc, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- J.M.H. van der Hart MSc, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Tabel 1 Gemelde (neven)functies en belangen werkgroep
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Dr. H. van Soest (voorzitter) |
MDL-arts, Haaglanden MC |
Voorzitter commissie hepatologie NVMDL; Voorzitter richtsnoer hepatitis C; Lid richtsnoer commissie hepatitis B; Lid medisch advies raad NLV; Lid visitatiecommissie NVMDL; Lid adviesraad MLDS/NAFLD-NL (initiation of a Dutch NAFLD consortium), lid werkgroep portale hypertensie |
Geen |
Geen restricties |
|
Dr. M.A. Lantinga (vice-voorzitter) |
MDL-arts, Amsterdam UMC, locatie VUmc |
Post Doc, Radboudumc (onbetaald), copromotor. Co-voorzitter portale hypertensie werkgroep, Nederlandse Vereniging van Hepatologie (NVH), onbetaald. Advisory Board - ERN RARE-LIVER // Training and Education Committee, onbetaald. |
Geen |
Geen restricties |
|
Dr. R.B. Takkenberg |
MDL-arts, Amsterdam UMC |
Deelname werkgroep tweede lijn, lid alcoholalliantie, gesprekken in het kader van nationaal preventieakkoord, deelname adviesraad over hepatitis Delta, Gilead |
ZonMw, Prevention of hepatic Encephalopathy by Administration of in patients with l, projectleider; Fonds-LVC, Neurofilament light chain and glial fibrillary acidic protein for hepatic encephalopathy, projectleider; KWF, Validation of a Short and Effective MRI Surveillance protocol for Hepatocellular Carcinoma Scr; MLDS, Initiation of a Dutch NAFLD consortium, geen projectleider |
Geen restricties (adviesraad betreft onderwerp dat niet relevant is voor deze richtlijnmodules) |
|
Dr. H.J.M. de Jonge |
MDL-arts, Jeroen Bosch Ziekenhuis |
Lid AIH werkgroep, lid werkgroep portale hypertensie, deelname werkgroep tweede lijn |
Geen |
Geen restricties |
|
Prof. dr. A.F.A. Schellekens |
Psychiater, Radboudumc |
Nationaal rapporteur verslavingen, adviescommissie alcohol van Gezondheidsraad |
ZonMw, onderzoek over verslaving, projectleider; NWO, onderzoek over verslaving, geen projectleider |
Geen restricties |
|
Drs. T. van Grinsven |
Verslavingsgeneeskundige, Novadic-Kentron |
Geen |
Dienstverband bij verslavingszorg Novadic-Kentron |
Geen restricties |
|
Dr. M. van Loon |
SEH-arts in Haaglanden MC; onderzoeker bij LUMC, afdeling Public Health en Eerstelijnsgeneeskunde |
Promotieonderzoek naar effectiviteit screening/haalbaarheid op SEH (afgerond); lid werkgroep 2e Lijn, samenwerkingsverband Vroegsignalering Alcoholstoornissen, onbetaald; Lid sectie Geriatrische Spoedzorg, NVSHA, scholing geven aan collega's m.b.t. acute geriatrie, betaald; de NVSHA vertegenwoordigen op landelijke bijeenkomsten, waarbij gesproken en beleid gemaakt wordt over geriatrische zorg in de acute keten, onbetaald; Instructeur voor aantal medische cursussen. |
Geen |
Geen restricties |
|
Drs. J.A. Willemse |
Directeur Nederlandse Leverpatienten Vereniging (betaald, tot 2024); bestuurslid/penningmeester Liver Patients International (onbetaald); bestuurslid ERN RARE LIVER (onbetaald) |
Deelname diverse commissies op gebied van leverziekten (onbetaald) |
Geen |
Geen restricties |
|
Drs. P.J. van Dongen (tot 2023) |
Patiëntenvertegenwoordiger bij Hersenletsel.nl (onbetaald) |
Geen |
Geen |
Geen restricties |
|
H.M. Luttikhuis Msc (vanaf 2023) |
Ziekenhuisapotheker in Slingelandziekenhuis |
Mede-eigenaar bij cooperatie Herenboerderij De Groote Modderkolk |
Geen |
Geen restricties |
|
Dr. R.A. Weersink (vanaf 2023) |
Ziekenhuisfarmacie, Deventer Ziekenhuis (tot 2024) |
Geen |
Geen |
Geen restricties |
|
Drs. H. Lam (vanaf 2024) |
Levertransplantatiechirurg, LUMC |
Geen |
Geen |
Geen restricties |
|
Dr. J. Blokzijl (vanaf 2025) |
MDL-arts, UMCG |
Geen |
Geen |
Geen restricties |
|
Klankbordgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
J.E. de Haan |
Internist-intensivist |
Geen |
Geen |
Geen restricties |
|
Drs. A.T. Timmer |
Klinisch geriater in het Tjongerschans Ziekenhuis |
Geen |
Geen |
Geen restricties |
|
Dr. J.M.W. van den Ouweland |
Klinisch chemicus Dicoon, locatie Canisius-Wilhelmina Ziekenhuis, Nijmegen |
Geen |
Geen |
Geen restricties |
|
Lid algemeen bestuur Stichting het Zwarte Gat |
Lid cliëntenraad verslavingszorg; Lid werkgroepen Verslavingskunde Nederland; Lid expertcommissie MIND/LpGgz; Cliëntdeskundige bij twee zorgstandaarden, twee werkwijzers/richtlijnen voor alcohol/verslaving en werk en/of leefstijl, etc. |
Bij werken aan herstel van verslaving is er baat voor familie vanwege werk aan herstel. Verder zijn de uitkomsten altijd van nut bij naasten (b.v. cliënten die ik vertegenwoordig) |
Geen restricties |
Inbreng patiëntenperspectief
De werkgroep besteedde aandacht aan het patiëntenperspectief door het uitnodigen van patiëntenverenigingen voor de invitational conference, focusgroep en afgevaardigde patiëntenverenigingen in de werkgroep. Het verslag van de invitational conference is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan Hersenletsel.nl, de Nederlandse Leverpatienten Vereniging en Stichting het Zwarte Gat en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Module |
Uitkomst raming |
Toelichting |
|
Module Prednisolon bij alcoholische hepatitis |
geen financiële gevolgen |
Uit de toetsing volgt dat de aanbevelingen niet breed toepasbaar zijn (<5.000 patiënten) en daarom naar verwachting geen substantiële financiële gevolgen zullen hebben voor de collectieve uitgaven. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.
Zoekverantwoording
Literature search strategy
|
Richtlijn: Somatische complicaties van alcoholstoornissen |
|
|
Uitgangsvraag: UV7 Wat is de plek voor prednison bij patiënten met een alcohol-geïnduceerde hepatitis? |
|
|
Database(s): Embase.com, Medline(Ovid) |
Datum:13-3-2023, 17-3-2023 |
|
Periode: 1990-heden |
Talen: nvt |
|
Literatuurspecialist: Eugenie Delvaux |
|
|
BMI zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting en opmerkingen:
Er is gezocht met de volgende elementen: ‘alcohol hepatitis’ EN ‘prednison’ OF corticosteroids EN volwassenen. Alle 2 de artikelen komen uit de search.
|
|
|
Te gebruiken voor richtlijnen tekst:
In de databases Medline(Ovid) en Embase.com is op met relevante zoektermen eerst gezocht naar Systematic Reviews en RCT’s en Observationele studies over ‘alcohol hepatitis’ EN ‘prednison’ OF corticosteroids EN volwassenen. De literatuurzoekactie leverde 367 unieke treffers op.
|
|
|
|
EMBASE |
OVID/Medline |
Ontdubbeld |
|
SRs |
82 |
11 |
88 |
|
RCTs |
83 |
53 |
62 |
|
OBS |
297 |
38 |
217 |
|
Totaal |
|
|
367 |
Embase
|
No. |
Query |
Results |
|
#18 |
#10 AND #15 |
297 |
|
#17 |
#10 AND #12 |
83 |
|
#16 |
#10 AND #11 |
82 |
|
#15 |
#13 OR #14 |
15726957 |
|
#14 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
13920783 |
|
#13 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
7541415 |
|
#12 |
'randomized controlled trial'/exp OR random*:ti,ab OR (((pragmatic OR practical) NEAR/1 'clinical trial*'):ti,ab) OR ((('non inferiority' OR noninferiority OR superiority OR equivalence) NEAR/3 trial*):ti,ab) OR rct:ti,ab,kw |
2027652 |
|
#11 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
909446 |
|
#10 |
#9 AND [1-1-1990]/sd |
734 |
|
#9 |
#8 NOT (('adolescent'/exp OR 'child'/exp OR adolescent*:ti,ab,kw OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw)) |
824 |
|
#8 |
#7 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
840 |
|
#7 |
#1 AND #6 |
1429 |
|
#6 |
#4 OR #5 |
1196474 |
|
#5 |
'corticosteroid'/exp OR 'adrenal cortex hormone*':ti,ab,kw OR 'adrenal cortical hormone*':ti,ab,kw OR 'adrenal cortical steroid*':ti,ab,kw OR 'adrenal steroid*':ti,ab,kw OR 'adrenal steroid hormone*':ti,ab,kw OR 'adreno cortical steroid*':ti,ab,kw OR 'adreno corticosteroid*':ti,ab,kw OR 'adrenocortical hormone*':ti,ab,kw OR 'adrenocortical steroid*':ti,ab,kw OR 'adrenocorticosteroid*':ti,ab,kw OR 'cortical steroid*':ti,ab,kw OR 'cortico steroid*':ti,ab,kw OR 'corticoid*':ti,ab,kw OR 'corticosteroid*':ti,ab,kw OR 'corticosteroid agent*':ti,ab,kw OR 'corticosteroid calcium':ti,ab,kw OR 'corticosteroid hormone*':ti,ab,kw OR 'corticosteroids, inhalation':ti,ab,kw OR 'dermocorticosteroid*':ti,ab,kw OR 'fluorinated corticosteroid*':ti,ab,kw |
1188192 |
|
#4 |
#2 OR #3 |
355730 |
|
#3 |
'prednisone'/exp OR '1, 2 dehydrocortisone':ti,ab,kw OR '1, 4 pregnadiene 17alpha, 21 diol 3, 11, 20 trione':ti,ab,kw OR '1, 4 pregnadiene 3, 11, 20 trione 17, 21 diol':ti,ab,kw OR '17 hydroxy 17 (2 hydroxyacetyl) 10, 13 dimethyl 6, 7, 8, 9, 12, 14, 15, 16 octahydrocyclopenta [a] phenanthrene 3, 11 dione':ti,ab,kw OR '17, 21 dihydroxypregna 1, 4 diene 3, 11, 20 trione':ti,ab,kw OR 'ancortone':ti,ab,kw OR 'apo-prednisone':ti,ab,kw OR 'biocortone':ti,ab,kw OR 'colisone':ti,ab,kw OR 'cortan':ti,ab,kw OR 'cortidelt':ti,ab,kw OR 'cortiprex':ti,ab,kw OR 'cutason':ti,ab,kw OR 'dacorten':ti,ab,kw OR 'de cortisyl':ti,ab,kw OR 'decortancyl':ti,ab,kw OR 'decortin':ti,ab,kw OR 'decortin e merck':ti,ab,kw OR 'decortine':ti,ab,kw OR 'decortisyl':ti,ab,kw OR 'dehydrocortisone':ti,ab,kw OR 'dekortin':ti,ab,kw OR 'delitisone':ti,ab,kw OR 'dellacort a':ti,ab,kw OR 'delta 1 dehydrocortisone':ti,ab,kw OR 'delta cortelan':ti,ab,kw OR 'delta cortisone':ti,ab,kw OR 'delta dome':ti,ab,kw OR 'delta e':ti,ab,kw OR 'delta prenovis':ti,ab,kw OR 'delta-dome':ti,ab,kw OR 'deltacorten':ti,ab,kw OR 'deltacortene':ti,ab,kw OR 'deltacortisone':ti,ab,kw OR 'deltacortone':ti,ab,kw OR 'deltasone':ti,ab,kw OR 'deltison':ti,ab,kw OR 'deltisona':ti,ab,kw OR 'deltra':ti,ab,kw OR 'di adreson':ti,ab,kw OR 'di-adreson':ti,ab,kw OR 'diadreson':ti,ab,kw OR 'drazone':ti,ab,kw OR 'encorton':ti,ab,kw OR 'encortone':ti,ab,kw OR 'enkorton':ti,ab,kw OR 'fernisone':ti,ab,kw OR 'hostacortin':ti,ab,kw OR 'insone':ti,ab,kw OR 'liquid pred':ti,ab,kw OR 'lodotra':ti,ab,kw OR 'me-korti':ti,ab,kw OR 'meprison':ti,ab,kw OR 'metacortandracin':ti,ab,kw OR 'meticorten':ti,ab,kw OR 'meticortine':ti,ab,kw OR 'nisona':ti,ab,kw OR 'nsc 10023':ti,ab,kw OR 'nsc10023':ti,ab,kw OR 'orasone':ti,ab,kw OR 'orb 101':ti,ab,kw OR 'orb101':ti,ab,kw OR 'orisane':ti,ab,kw OR 'panafcort':ti,ab,kw OR 'paracort':ti,ab,kw OR 'pehacort':ti,ab,kw OR 'precort':ti,ab,kw OR 'precortal':ti,ab,kw OR 'prednicen-m':ti,ab,kw OR 'prednicorm':ti,ab,kw OR 'prednicot':ti,ab,kw OR 'prednidib':ti,ab,kw OR 'prednison':ti,ab,kw OR 'prednisone':ti,ab,kw OR 'prednisone alcohol':ti,ab,kw OR 'prednisone intensol':ti,ab,kw OR 'prednisone test':ti,ab,kw OR 'prednitone':ti,ab,kw OR 'pregna 1, 4 diene 3, 11, 20 trione 17, 21 diol':ti,ab,kw OR 'pronison':ti,ab,kw OR 'pronisone':ti,ab,kw OR 'pronizone':ti,ab,kw OR 'pulmison':ti,ab,kw OR 'rayos':ti,ab,kw OR 'rectodelt':ti,ab,kw OR 'servisone':ti,ab,kw OR 'steerometz':ti,ab,kw OR 'sterapred':ti,ab,kw OR 'sterapred ds':ti,ab,kw OR 'ultracorten':ti,ab,kw OR 'urtilone':ti,ab,kw OR 'winpred':ti,ab,kw |
209975 |
|
#2 |
'prednisolone'/exp OR '1, 2 dehydro hydrocortison':ti,ab,kw OR '1, 4 pregnadien 11beta, 17alpha, 21 triol 3, 20 dion':ti,ab,kw OR '1, 4 pregnadiene 11beta, 17alpha, 21 triol 3, 20 dione':ti,ab,kw OR '1, 4 pregnadiene 3, 20 dione 11beta, 17alpha, 21 triol':ti,ab,kw OR '11, 17 dihydroxy 17 (2 hydroxyacetyl) 10, 13 dimethyl 7, 8, 9, 11, 12, 14, 15, 16 octahydro 6h cyclopenta [a] phenanthren 3 one':ti,ab,kw OR '11beta, 17, 21 trihydroxypregna 1, 4 diene 3, 20 dione':ti,ab,kw OR '11beta, 17alpha, 21 trihydroxy 1, 4 pregnadien 3, 20 dion':ti,ab,kw OR '11beta, 17alpha, 21 trihydroxypregna 1, 4 diene 3, 20 dione':ti,ab,kw OR '14, 17 dihydroxy 14 (2 hydroxyacetyl) 2, 15 dimethyltetracyclo [8.7.0.0 (2, 7) .0 (11, 15)] heptadeca 3, 6 dien 5 one':ti,ab,kw OR '3, 20 dioxo 11beta, 17alpha, 21 trihydroxy 1, 4 pregnadiene':ti,ab,kw OR 'adelcort':ti,ab,kw OR 'antisolon':ti,ab,kw OR 'antisolone':ti,ab,kw OR 'aprednislon':ti,ab,kw OR 'aprednislone':ti,ab,kw OR 'benisolon':ti,ab,kw OR 'benisolone':ti,ab,kw OR 'berisolon':ti,ab,kw OR 'berisolone':ti,ab,kw OR 'caberdelta':ti,ab,kw OR 'capsoid':ti,ab,kw OR 'co hydeltra':ti,ab,kw OR 'codelcortone':ti,ab,kw OR 'compresolon':ti,ab,kw OR 'cortadeltona':ti,ab,kw OR 'cortadeltone':ti,ab,kw OR 'cortalone':ti,ab,kw OR 'cortelinter':ti,ab,kw OR 'cortisolone':ti,ab,kw OR 'cotolone':ti,ab,kw OR 'dacortin':ti,ab,kw OR 'dacortin h':ti,ab,kw OR 'dacrotin':ti,ab,kw OR 'decaprednil':ti,ab,kw OR 'decortin h':ti,ab,kw OR 'decortril':ti,ab,kw OR 'dehydro cortex':ti,ab,kw OR 'dehydro hydrocortison':ti,ab,kw OR 'dehydro hydrocortisone':ti,ab,kw OR 'dehydrocortex':ti,ab,kw OR 'dehydrocortisol':ti,ab,kw OR 'dehydrocortisole':ti,ab,kw OR 'dehydrohydrocortison':ti,ab,kw OR 'dehydrohydrocortisone':ti,ab,kw OR 'delcortol':ti,ab,kw OR 'delta 1 17 hydroxycorticosterone 21 acetate':ti,ab,kw OR 'delta 1 hydrocortisone':ti,ab,kw OR 'delta cortef':ti,ab,kw OR 'delta cortril':ti,ab,kw OR 'delta ef cortelan':ti,ab,kw OR 'delta f':ti,ab,kw OR 'delta hycortol':ti,ab,kw OR 'delta hydrocortison':ti,ab,kw OR 'delta hydrocortisone':ti,ab,kw OR 'delta ophticor':ti,ab,kw OR 'delta stab':ti,ab,kw OR 'delta-cortef':ti,ab,kw OR 'delta1 dehydrocortisol':ti,ab,kw OR 'delta1 dehydrohydrocortisone':ti,ab,kw OR 'delta1 hydrocortisone':ti,ab,kw OR 'deltacortef':ti,ab,kw OR 'deltacortenolo':ti,ab,kw OR 'deltacortil':ti,ab,kw OR 'deltacortoil':ti,ab,kw OR 'deltacortril':ti,ab,kw OR 'deltaderm':ti,ab,kw OR 'deltaglycortril':ti,ab,kw OR 'deltahycortol':ti,ab,kw OR 'deltahydrocortison':ti,ab,kw OR 'deltahydrocortisone':ti,ab,kw OR 'deltaophticor':ti,ab,kw OR 'deltasolone':ti,ab,kw OR 'deltastab':ti,ab,kw OR 'deltidrosol':ti,ab,kw OR 'deltisilone':ti,ab,kw OR 'deltisolon':ti,ab,kw OR 'deltisolone':ti,ab,kw OR 'deltolasson':ti,ab,kw OR 'deltolassone':ti,ab,kw OR 'deltosona':ti,ab,kw OR 'deltosone':ti,ab,kw OR 'depo-predate':ti,ab,kw OR 'dermosolon':ti,ab,kw OR 'dhasolone':ti,ab,kw OR 'di adreson f':ti,ab,kw OR 'di adresone f':ti,ab,kw OR 'di-adreson-f':ti,ab,kw OR 'diadreson f':ti,ab,kw OR 'diadresone f':ti,ab,kw OR 'dicortol':ti,ab,kw OR 'domucortone':ti,ab,kw OR 'encortelon':ti,ab,kw OR 'encortelone':ti,ab,kw OR 'encortolon':ti,ab,kw OR 'equisolon':ti,ab,kw OR 'fernisolone-p':ti,ab,kw OR 'glistelone':ti,ab,kw OR 'hefasolon':ti,ab,kw OR 'hostacortin h':ti,ab,kw OR 'hostacortin h vet':ti,ab,kw OR 'hydeltra':ti,ab,kw OR 'hydeltrone':ti,ab,kw OR 'hydrelta':ti,ab,kw OR 'hydrocortancyl':ti,ab,kw OR 'hydrocortidelt':ti,ab,kw OR 'hydrodeltalone':ti,ab,kw OR 'hydrodeltisone':ti,ab,kw OR 'hydroretrocortin':ti,ab,kw OR 'hydroretrocortine':ti,ab,kw OR 'inflanefran':ti,ab,kw OR 'insolone':ti,ab,kw OR 'keteocort h':ti,ab,kw OR 'key-pred':ti,ab,kw OR 'key-pred sp':ti,ab,kw OR 'lenisolone':ti,ab,kw OR 'leocortol':ti,ab,kw OR 'liquipred':ti,ab,kw OR 'lygal kopftinktur n':ti,ab,kw OR 'mediasolone':ti,ab,kw OR 'meprisolon':ti,ab,kw OR 'meprisolone':ti,ab,kw OR 'metacortalon':ti,ab,kw OR 'metacortalone':ti,ab,kw OR 'metacortandralon':ti,ab,kw OR 'metacortandralone':ti,ab,kw OR 'metacortelone':ti,ab,kw OR 'meti derm':ti,ab,kw OR 'meti-derm':ti,ab,kw OR 'meticortelone':ti,ab,kw OR 'metiderm':ti,ab,kw OR 'morlone':ti,ab,kw OR 'mydrapred':ti,ab,kw OR 'nanocort':ti,ab,kw OR 'neo delta':ti,ab,kw OR 'nisolon':ti,ab,kw OR 'nisolone':ti,ab,kw OR 'nsc 9120':ti,ab,kw OR 'nsc9120':ti,ab,kw OR 'opredsone':ti,ab,kw OR 'panafcortelone':ti,ab,kw OR 'panafcortolone':ti,ab,kw OR 'panafort':ti,ab,kw OR 'paracortol':ti,ab,kw OR 'phlogex':ti,ab,kw OR 'pre cortisyl':ti,ab,kw OR 'preconin':ti,ab,kw OR 'precortalon':ti,ab,kw OR 'precortancyl':ti,ab,kw OR 'precortisyl':ti,ab,kw OR 'pred-ject-50':ti,ab,kw OR 'predacort 50':ti,ab,kw OR 'predaject-50':ti,ab,kw OR 'predalone 50':ti,ab,kw OR 'predartrina':ti,ab,kw OR 'predartrine':ti,ab,kw OR 'predate-50':ti,ab,kw OR 'predeltilone':ti,ab,kw OR 'predisole':ti,ab,kw OR 'predisyr':ti,ab,kw OR 'predne dome':ti,ab,kw OR 'prednecort':ti,ab,kw OR 'prednedome':ti,ab,kw OR 'prednelan':ti,ab,kw OR 'predni coelin':ti,ab,kw OR 'predni h tablinen':ti,ab,kw OR 'predni-helvacort':ti,ab,kw OR 'prednicoelin':ti,ab,kw OR 'prednicort':ti,ab,kw OR 'prednicortelone':ti,ab,kw OR 'prednifor drops':ti,ab,kw OR 'predniment':ti,ab,kw OR 'predniretard':ti,ab,kw OR 'prednis':ti,ab,kw OR 'prednisil':ti,ab,kw OR 'prednisolon':ti,ab,kw OR 'prednisolona':ti,ab,kw OR 'prednisolone':ti,ab,kw OR 'prednisolone alcohol':ti,ab,kw OR 'prednisolone h':ti,ab,kw OR 'prednisolone oleosae sr 82':ti,ab,kw OR 'prednisolone, topical':ti,ab,kw OR 'prednivet':ti,ab,kw OR 'prednorsolon':ti,ab,kw OR 'prednorsolone':ti,ab,kw OR 'predonine':ti,ab,kw OR 'predorgasolona':ti,ab,kw OR 'predorgasolone':ti,ab,kw OR 'pregna 1, 4 diene 11beta, 17alpha, 21 triol 3, 20 dione':ti,ab,kw OR 'prelon':ti,ab,kw OR 'prelone':ti,ab,kw OR 'prenilone':ti,ab,kw OR 'prenin':ti,ab,kw OR 'prenolone':ti,ab,kw OR 'preventan':ti,ab,kw OR 'prezolon':ti,ab,kw OR 'rubycort':ti,ab,kw OR 'scherisolon':ti,ab,kw OR 'scherisolona':ti,ab,kw OR 'serilone':ti,ab,kw OR 'solondo':ti,ab,kw OR 'solone':ti,ab,kw OR 'solupren':ti,ab,kw OR 'soluprene':ti,ab,kw OR 'spiricort':ti,ab,kw OR 'spolotane':ti,ab,kw OR 'sterane':ti,ab,kw OR 'sterolone':ti,ab,kw OR 'supercortisol':ti,ab,kw OR 'supercortizol':ti,ab,kw OR 'taracortelone':ti,ab,kw OR 'walesolone':ti,ab,kw OR 'wysolone':ti,ab,kw |
160023 |
|
#1 |
'alcoholic hepatitis'/exp OR ((alcohol* NEAR/4 hepati*):ti,ab,kw) |
15233 |
Ovid/Medline
|
# |
Searches |
Results |
|
12 |
6 and 9 |
38 |
|
11 |
6 and 8 |
53 |
|
10 |
6 and 7 |
11 |
|
9 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort*.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ |
4429383 |
|
8 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2565166 |
|
7 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
655317 |
|
6 |
limit 5 to yr="1990-Current" |
133 |
|
5 |
4 not (child* or schoolchild* or infan* or adolescen* or pediatri* or paediatr* or neonat* or boy or boys or boyhood or girl or girls or girlhood or youth or youths or baby or babies or toddler* or childhood or teen or teens or teenager* or newborn* or postneonat* or postnat* or puberty or preschool* or suckling* or picu or nicu or juvenile?).tw. |
169 |
|
4 |
3 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) |
174 |
|
3 |
1 and 2 |
205 |
|
2 |
exp prednisolone/ or exp prednisone/ or exp methylprednisolone/ or exp methylprednisolone hemisuccinate/ or prednisolone.ti,ab,kf. or prednison.ti,ab,kf. or methylprednisolone.ti,ab,kf. or prednimustine.ti,ab,kf. |
113578 |
|
1 |
exp Hepatitis, Alcoholic/ or (alcohol* adj4 hepati*).ti,ab,kf. |
9206 |