Verlaging valrisico ouderen in verpleeghuis
Uitgangsvraag
Welke (multifactoriële) valpreventieve interventies zijn effectief bij ouderen met een matig of hoog valrisico in het verpleeghuis?
Deelvraag: Wat zijn de effectieve interventiecomponenten en welke componenten zouden minimaal overwogen moeten worden in multicomponent of multifactoriële interventies?
Aanbeveling
Voer bij ouderen in het verpleeghuis met een hoog valrisico een multifactoriële valpreventieve interventie*, gebaseerd op de geïdentificeerde valrisicofactoren vanuit de multidisciplinaire, multifactoriële valrisicobeoordeling.
Verwerk in de multifactoriële valpreventieve interventie de positief gescoorde valrisicofactoren en overweeg minimaal de volgende items (zie voor het volledige overzicht en details per interventiecomponent zie tabel Aanbevelingen valpreventie interventies ouderen in het verpleeghuis):
Startend met de interventie met de hoogste bewijskracht
- Management van orthostatische hypotensie (conform de module valpreventie bij orthostatische hypotensie)
- Vitamine D-suppletie
- Afbouw van valrisicoverhogende medicatie via een gestructureerde medicatieoptimalisatie (zie hiervoor de module beoordeling valrisicoverhogende medicatie)
- Gecombineerde beweeginterventie gericht op kracht en balans, afgestemd op het individu, met voldoende uitdaging en intensiteit.
Betrek mantelzorgers bij de besluitvorming over valpreventieve maatregelen, met aandacht voor zowel de mogelijkheden als de beperkingen van de bewoner binnen de verpleeghuissetting.
*Multicomponent: alle patiënten krijgen dezelfde combinatie van interventiecomponenten; Multifactorieel: de combinatie van interventiecomponenten wordt afgestemd op de individuele patiënt.
Overwegingen
Balans tussen gewenste en ongewenste effecten
Er is literatuuronderzoek gedaan naar de effectiviteit van valpreventieve interventies bij ouderen in verpleeghuis. Als deelvraag werd geformuleerd: Wat zijn de effectieve deelinterventies en welke componenten moeten er minimaal in een multifactoriële interventie zitten?
In de systematische literatuur analyse werd gefocust op multicomponent en multifactoriële valpreventie interventies (hierna: multifactoriële interventies). Multicomponent interventies worden hierbij gedefinieerd als een interventie waarbij alle deelnemers dezelfde combinatie van deelinterventies ontvangen. Bij multifactoriële interventies wordt de combinatie van deelinterventies aangepast naar de individuele patiënt. De Cochrane review van Cameron (2018) werd als basis gebruikt voor het literatuuronderzoek en de literatuursamenvatting. Daarnaast werden er nog twee gerandomiseerde studies geïncludeerd (Kerse, 2009; Logan, 2021)
Als uitkomstmaten werden, conform de Cochrane review van Cameron (2018), valrisico, valfrequentie en het risico op valgerelateerde fracturen gedefinieerd. Hierbij werd valrisico gedefinieerd als het aantal patiënten dat (éénmalig of herhaaldelijk) valt in de interventiegroep, vergeleken met het aantal patiënten dat valt in de controlegroep. Valfrequentie werd gedefinieerd als het totaal aantal valincidenten per eenheid van tijd. Het risico op valgerelateerde fracturen verwijst naar het aantal patiënten met fracturen ten gevolge van een val.
Op basis van de RCTs over multicomponent interventies die geïncludeerd zijn in Cameron (2018), kunnen geen conclusies worden getrokken over de effectiviteit van dit type interventie. Er waren slechts twee studies naar multicomponent interventies, die beiden verschillende typen interventies onderzochten (een studie naar zonlicht en calcium en een studie naar management van urine-incontinentie). Vanwege de heterogeniteit tussen deze twee studies, en mogelijk mede daardoor de brede betrouwbaarheidsintervallen rond het gepoolde effect (imprecisie), zijn we zeer onzeker over het daadwerkelijke effect van multicomponent interventies op de valrisico, valfrequentie en risico op fracturen (GRADE zeer laag).
De meerderheid van de geïncludeerde studies onderzocht het effect van multifactoriële interventies de gevonden effecten zijn eenduidiger dan de resultaten over multicomponent interventies. Multifactoriële interventies lijken in vergelijking met standaard zorg, zowel het valrisico als de valfrequentie te verlagen. De bewijskracht van dit gevonden effect is redelijk/laag (GRADE moderate/low). Vanwege het doorkruizen van het 95% betrouwbaarheidsinterval, met de onderste grens van klinische relevantie, zou er ook sprake kunnen zijn van géén effect.
Om de deelvraag wat zijn de effectieve deelinterventies en welke componenten moeten er minimaal in een multifactoriële interventie zitten? te kunnen beantwoorden is er gekeken naar de interventiecomponenten van de multicomponent en multifactoriële interventies die beschreven werden in de literatuursamenvatting (Tabel 3). Interventiecomponenten die in meerdere studies onderdeel zijn van de multicomponent of multifactoriële interventie zijn:
- Beweeginterventies, gericht op het verbeteren van conditie, kracht en balans.
- Medicatie interventies
- Omgevingsinterventies
- Ondersteunende technologie, zoals bewegingssensoren en indicatoren voor patiënten met hoog valrisico
- Educatie van personeel
Bovenstaande deelinterventies vormen belangrijke componenten in een multifactoriële interventie.
Naar aanleiding van de geadviseerde multifactoriële valanalyse gericht op de geïdentificeerde risicofactoren van vallen, kan worden opgemaakt welke onderdelen op individueel niveau toegepast kunnen worden.
Ook is er gekeken naar de resultaten uit het Cochrane review van Cameron (2018) over enkelvoudige interventies. De belangrijkste bevindingen over enkelvoudige interventies waren staan beschreven in Tabel 5.
Tabel 5: resultaten van enkelvoudige interventies op de vooraf gedefinieerde uitkomstmaten, afkomstig van Cameron, 2018.
|
|
Valrisico (aantal patiënten dat valt) |
Valfrequentie |
Risico op botbreuken |
|
Lichamelijke beweging |
RR: 1.02 (95% BI: 0.88 tot 1.18) N = 2090, 10 studies GRADE: low |
RaR: 0.93 (95% BI: 0.72 tot 1.20) N = 2002, 10 studies GRADE: very low |
RR: 0.88 (95% BI: 0.25 tot 3.14) N = 183, 1 studie GRADE: very low |
|
Medicatie review |
RR: 0.92 (95% BI: 0.80 tot 1.09) N = 5138, 6 studies GRADE: low |
RaR: 0.93 (95% BI: 0.64 tot 1.23) N = 2409, 6 studies GRADE: low |
RR: 1.60 (95% BI: 0.28 tot 9.16) N = 93, 1 studie GRADE: very low |
|
Vitamine D |
RR: 0.92 (95% BI: 0.76 tot 1.12) N = 4512, 4 studies GRADE: Moderate |
RaR: 0.72 (95% BI: 0.55 tot 0.95) N = 4512, 4 studies GRADE: Moderate |
RR: 1.09 (95% BI: 0.58 tot 2.03) N = 4464, 3 studies GRADE: very low
|
RR = Risk Ratio; RaR = Rate Ratio; 95% BI = 95% betrouwbaarheidsinterval
Deze resultaten geven enkel bewijslast voor het feit dat vitamine D valfrequentie waarschijnlijk verlaagt, wanneer vergeleken met standaard zorg (GRADE redelijk). Veel patiënten in het verpleeghuis hebben vitamine D deficiëntie, waardoor zij baat zullen hebben bij het toedienen van vitamine D. Gezien de lage individuele belasting die het gebruik van vitamine D met zich meebrengt, raadt de werkgroep het aan om in principe alle bewoners in het verpleeghuis deze vitamine voor te schrijven.
Voor het effect van lichamelijke beweging en de inzet van een medicatie review, werden geen klinisch relevante effecten gevonden. Dit suggereert dat de inzet van lichamelijke beweging en medicatie reviews als enkelvoudige interventie, geen effect hebben op het valrisico en de valfrequentie bij oudere patiënten in verpleeghuizen. Deze resultaten laten zich verklaren door het feit dat bij de meeste kwetsbare ouderen in het verpleeghuis een verhoogd valrisico een multifactoriële origine heeft en daardoor vaak niet door een enkelvoudige interventie op te lossen is. Het feit dat een enkelvoudige interventie op zichzelf geen klinisch relevant effecten laten zien, betekent overigens niet dat deze in een combinatie met andere interventies ook niet effectief zijn.
Lichamelijke beweging vormt een belangrijk uitgangspunt in de meerderheid van de multifactoriële interventies. Om na te gaan aan welke voorwaarden deze lichamelijke beweging moet voldoen om effectief te zijn, voerden Dawson (2024) naar aanleiding van de laatste Cochrane update een interventie component analyse uit. Zij concluderen dat valpreventie het meest gebaat is bij beweeginterventies die balans en kracht trainen op een matige intensiteit en aangepast aan het niveau van het individu. Daarnaast suggereren zij dat dergelijke interventies een grotere kans van slagen hebben wanneer deze structureel, onder getrainde supervisie en in groepsverband worden aangeboden. Dit sluit aan bij de ervaring van de werkgroep, zijnde een succesvolle manier om extrinsieke motivatie en participatie van kwetsbare ouderen in het verpleeghuis te faciliteren.
Het uitvoeren van een medicatiereview wordt overigens tegenwoordig beschouwd als standaard zorg in het verpleeghuis en reikt verder dan alleen de doelstelling valpreventie. De werkgroep acht het zeer bijdragend om in het kader van de medicatiereview een orthostatische bloeddrukmeting te doen. Orthostatische hypotensie kan als bijwerking van verschillende geneesmiddelen een belangrijke factor vormen bij frequent vallen. Indien het fenomeen zich presenteert zonder dat dit te herleiden is tot medicatiegebruik, dan kunnen aanvullende maatregelen getroffen worden om het valrisico te reduceren (zie valpreventie bij orthostatische hypotensie)
Naast boven genoemde interventies, worden adviezen omtrent het verbeteren van gehoor, visus en looppatroon, door een bezoek aan respectievelijk de opticien, audicien en hulpmiddelenwinkel of orthopedische schoenmaker gezien als voor de hand liggende onderdelen in een multifactoriële interventie.
In het verpleeghuis is onderzoek gedaan naar de inzet van heupbeschermers om het valrisico te reduceren. Nemeth (2022) toont voorzichtig positieve resultaten van deze heupbeschermers, de incidentie van heup- en bekkenfracturen door het dragen van de WOLK hip airbag nam af met een IRR van 0.55. De studie is mogelijk onderhevig aan selectiebias, aangezien het zelfstandig afdoen van de heupbeschermers een exclusiecriterium was. Dit gegeven gaat mogelijk op voor een deel van de populatie van ouderen in het verpleeghuis met dementie, naast het gegeven dat ouderen mogelijk niet ’s nachts willen slapen met de airbag om en alsnog kunnen vallen bij de nachtelijke toiletgang.
Om te bepalen welke eigenschappen van multifactoriële interventies bijdragen aan een verlaging van het valrisico, deed Suen (2023) interventie component analyse en een kwalitatieve vergelijkende analyse naar de studies in Cameron (2018) die keken naar de effectiviteit van multifactoriële interventies in het verpleeghuis. Naast deze studies uit Cameron (2018), was de RCT van Logan (2021) toegevoegd aan de meta-analyse. Op basis van de thematische interventie component analyse werd geconcludeerd dat de volgende thema’s een rol spelen in de effectiviteit van een multifactoriële interventie:
- Interventie co-design met managers en personeel: het betrekken van managers om personeel van het verpleeghuis te ondersteunen met de noodzakelijke training en gezamenlijke besluitvorming over het interventie protocol. Aanwezig in 6/7 effectieve trials.
- Gepersonaliseerde interventie (aanpassen van de interventie naar intrinsieke factoren van verpleeghuisbewoners): de mogelijkheid om een interventie aan te passen, o.b.v. een individuele valrisico beoordeling, zodat deze aansluit bij persoonlijk en omgevingsfactoren van verpleeghuisbewoners. Aanwezig in 7/7 effectieve trials. Het aanpassen van een interventie naar het individu werd met name belangrijk geacht bij patiënten met cognitieve beperkingen.
Voor een juiste interpretatie van deze resultaten, is het goed om een aantal belangrijke kanttekeningen te benoemen over de populatie patiënten in het verpleeghuis. Enerzijds kan worden gesteld dat lichamelijke beweging in algemene zin goed is voor patiënten. Bovendien kunnen veel factoren die worden geanalyseerd als onderdeel van een multifactoriële interventie in potentie bijdragen aan de afname van het valrisico en valfrequentie. Anderzijds dient er rekening te worden met het feit dat de implementatie in de praktijk voor patiënten in het verpleeghuis soms lastig is. Niet alleen vormt de grote mate van afhankelijkheid, (cognitieve) kwetsbaarheid en vergevorderde achteruitgang in mobiliteit een obstakel in deelname aan bewegingsinterventies. Ook bevindt het merendeel van de patiënten in het verpleeghuis zich in de palliatieve of terminale fase van hun degeneratieve ziekteproces. Dit kan mogelijk de beperkte effectiviteit van bewegingsinterventies, zoals in het Cochrane Review van Cameron (2018) verklaren (Tabel 5). In het kader van toenemende kwetsbaarheid, is het afbouwen of staken van medicatie niet altijd zonder risico. Een medicatiereview dient daarom vergezeld te worden door een orthostatische bloeddrukmeting, om na te gaan of afbouwen of staken van antihypertensiva vanuit het kader van valpreventie bijdragend is, of dat dit mogelijk risico’s met zich meebrengt (Bogaerts, 2024)
Frequent vallen en een verhoogd valrisico kunnen symptomen zijn van een vergevorderd stadium van dementie, de ziekte van Parkinson, of andere complexe neurologische aandoeningen. Daardoor is frequent vallen of een verhoogd valrisico niet eenvoudig als een losstaand probleem te behandelen. Behandeling van patiënten in het verpleeghuis is maatwerk. Zelfs als dit wordt erkend en er diverse multifactoriële interventies worden ingezet volgens de hoogste wetenschappelijke standaarden, komt er nog geen eenduidige conclusie dat deze effectief zijn. Dit neemt niet weg dat er grote aantallen patiënten met een verhoogd valrisico zijn die wel baat hebben bij dergelijke interventies, maar de gemiddelde verpleeghuisbewoner niet. Valpreventie is – naar inzicht van de werkgroep – een belangrijke pijler van preventieve zorg, die zich hoofdzakelijk buiten het verpleeghuis dient af te spelen, bij de groepen ouderen (en volwassenen) die nog leerbaar en trainbaar zijn en bij wie ernstige geriatrische pathologie nog niet gezorgd heeft voor onherroepelijke achteruitgang. Overigens is er op individueel niveau altijd ruimte om te zoeken naar passende verbetermogelijkheden, binnen handbereik.
Kwaliteit van bewijs
De overall kwaliteit van bewijs is laag tot redelijk. Dit betekent dat we onzeker tot redelijk zeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten. Er is afgewaardeerd vanwege ernstige:
- Risk of Bias: methodologische beperkingen, waaronder gebrek aan blindering
- Imprecisie: onnauwkeurigheid, omdat het betrouwbaarheidsinterval de grens van klinische relevantie overschrijdt
Waarden en voorkeuren van patiënten (en eventueel hun naasten/ verzorgers)
Zoals hierboven beschreven kenmerkt de populatie ouderen in een verpleeghuis zich door een aantal factoren. Zo kan er sprake zijn van een grote mate van afhankelijkheid, cognitieve kwetsbaarheid en/of vergevorderde achteruitgang in mobiliteit. Daarnaast zijn er vaak comorbiditeiten, bijvoorbeeld dementie, de ziekte van Parkinson of andere complexe neurologische aandoeningen, die het risico op vallen kunnen verhogen. Het betreft een periode van het leven die zich kenmerkt door toenemende passiviteit, met daarbij soms ook initiatiefverlies als symptoom in het geval van vorderende dementie. Goede zorg voor deze populatie kenmerkt zich door aandacht voor waardig ouder worden en kwaliteit van leven. De belasting van bijvoorbeeld een (meervoudige) beweeginterventie is binnen de populatie ouderen in het verpleeghuis groter, dan dat die voor een zelfstandig wonende oudere is. Iedere interventie dient daarom gewogen te worden naar de belasting die het met zich meebrengt, tegenover de potentiële winst die hiermee te behalen valt. Het verdient de aandacht om bij opname in het verpleeghuis al met patiënt en zijn vertegenwoordiger te spreken over het belang van valpreventie en welke interventies haalbaar zijn en welke geboden worden op de betreffende locatie. Daarnaast is het goed om na te gaan tot op welk niveau intrinsieke motivatie nog is te verwachten en welk belang er door patiënt en zijn vertegenwoordiger wordt gehecht aan valpreventie.
Onder de wet Zorg en Dwang is er in de afgelopen jaren meer aandacht gekomen over de toepassing van vrijheidsbeperkende maatregelen en is er meer bewustwording dat deze bij ouderen in het verpleeghuis zo weinig mogelijk ingezet dienen te worden. Enerzijds is hierdoor meer aandacht voor maatregelen die minder ingrijpend zijn en daardoor minder vaak tot vallen zouden kunnen leiden, bijvoorbeeld de inzet van een laag-laag bed en een sensor naast het bed. Anderzijds krijgen bewoners meer bewegingsvrijheid in hun eigen leefruimte met daarbij meer kans om te vallen.
Kostenaspecten
De interventie levert meer kosten ten opzichte van de controle behandeling. Dit betreft bijvoorbeeld materiële uitgaven en extra inzet van het personeel. De meest kostbare component betreft waarschijnlijk de beweeginterventies, vanuit de gedachte dat deze op wekelijkse basis gefaciliteerd moeten worden door een terzake kundige professional. Daarbij is de vraag hoe dit opweegt tegen frequent vallen, wanneer dat niet tot gevolg heeft dat iemand wordt ingestuurd naar het ziekenhuis, omdat dit in het kader van behandelbeleid is afgesproken. Veel ouderen in het verpleeghuis spreken af dat zij bij calamiteiten (zoals bijvoorbeeld een heupfractuur) niet meer ingestuurd willen worden naar het ziekenhuis, en in het verpleeghuis behandeld willen worden, soms ook uitdrukkelijk zonder het doel het leven verder te verlengen.
Logan (2021) deed een kosteneffectiviteitsanalyse van de inzet van een multifactoriële interventie vergeleken met standaard zorg bij patiënten in het verpleeghuis. De analyse laat zien dat de kosten per afgewende val 191 pond zijn. Invoering van de interventie leidde tot een reductie in het aantal vallen in een periode van 3 maanden, waarna dit effect overigens verdween na 6 maanden. Het heeft geen effect gehad op mortaliteit, afhankelijkheid of activiteit onder bewoners, noch vonden de onderzoekers een verbetering in kwaliteit van leven als gevolg van de interventie. Wel hebben zij aangetoond dat hun programma valt binnen de conventionele grens van kosteneffectiviteit valt, wanneer gelet wordt op de gezondheidsgerelateerde kwaliteit van leven, gemeten middels de EQ-5D-5L, terwijl dit niet geconcludeerd kon worden als de DEMQOL-P-U resultaten werden gebruikt in de analyse. De daadwerkelijke kosteneffectiviteit van het programma kan daarom als twijfelachtig worden beschouwd.
Gelijkheid ((health) equity/equitable)
Het feit dat interventies worden aangeboden in een verpleeghuissetting, maakt dat deze in theorie niet toegankelijk zijn voor iedereen. De werkgroep is echter van mening dat dit niet leidt tot een toename van gezondheidsongelijkheid, omdat er ook interventies worden aangeboden voor thuiswonende ouderen of ouderen in het ziekenhuis
Mogelijk dat voor bepaalde interventies verschillende resultaten behaald kunnen worden afhankelijk van de individuele patiënt. Denk aan verschil in opleidingsniveau, culturele opvattingen en taalachterstand.
Aanvaardbaarheid:
Ethische aanvaardbaarheid
Het inzetten van vrijheidsbeperkende maatregelen, zoals het gebruik van een bewegingssensor kent mogelijk ethische bezwaren. Echter wordt in de praktijk gezien dat zowel patiënten als mantelzorgers weinig bezwaren hebben tegen de inzet van valsensoren. Voor de andere (deel)interventies, voorziet de werkgroep geen ethische bezwaren.
Duurzaamheid
Aangezien er bij de interventie meer middelen zullen moeten worden ingezet dan in bij standaard zorg, is dit een minder duurzame keuze. Echter wegen deze overwegingen niet op tegen de effectiviteit van de interventie en duurzaamheidsoverwegingen spelen daarmee geen rol.
Haalbaarheid
De haalbaarheid van de beschreven interventie hangt af van een aantal factoren. In het verpleeghuis speelt de beschikbare capaciteit een cruciale rol bij de implementatie van multicomponent of multifactoriële interventies. De aanwezigheid van personeel is niet alleen belangrijk om de interventies uit te voeren, maar ook om de patiënt in de gaten te houden. Belangrijk voor de effectiviteit is de betrokkenheid van een multidisciplinair behandelteam, bestaand uit minstens een (geriatrie)fysiotherapeut, ergotherapeut en een arts, verpleegkundig specialist of physician assistant. Daarnaast is het belangrijk dat een specialist ouderengeneeskunde beschikbaar is voor intercollegiale consulatie. De specialist ouderengeneeskunde heeft daarnaast een belangrijke rol in het uitvoeren van de multifactoriële valanalyse. Voor de uitvoering van een interventie is de expertise van een (geriatrie)fysiotherapeut en eventueel ergotherapeut zeer gewenst. Een deel van de genoemde (deel)interventies, zoals het voorschrijven van vitamine D, zijn eenvoudig te implementeren in de praktijk of behoren al tot de standaard zorg.
Betrokkenheid van een multidisciplinair team is cruciaal, bijvoorbeeld bij het signaleren van potentieel gevaarlijke situaties en bij het uitvoeren van interventies. Het betrekken van een (geriatrie)fysiotherapeut die betrokken is in desbetreffend verpleeghuis is van meerwaarde, echter er is een sterk tekort aan (geriatrie)fysiotherapeuten in de verpleeghuissetting.
De toegang tot opticien, audicien en hulpmiddelen is in de verpleeghuissetting minder eenvoudig, zeker in het geval dat de patiënt niet meer mobiel instrueerbaar is. Dit kan de haalbaarheid van bepaalde valpreventieve interventies in de weg staan.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Het uitvoeren van een multifactoriële, multidisciplinaire valanalyse is noodzakelijk bij alle patiënten wanneer zij worden opgenomen in het verpleeghuis en bij toename van de valfrequentie, met als doel om gericht een multifactoriële interventie in te zetten indien dit nog wenselijk en haalbaar is. In het verpleeghuis hoort kwaliteit van leven een belangrijke pijler voor behandeling te zijn. Valpreventieve interventies staan soms haaks op deze visie. Laagdrempelig in te zetten diagnostiek en interventies, zoals gebruik van vitamine D en het uitvoeren van een orthostatische bloeddrukmeting lijken daadwerkelijk bij te dragen aan een hogere kwaliteit van leven en dienen daarom toegepast te worden waar mogelijk. Een beweeginterventie kan bijdragen wanneer de patiënt in voldoende mate en voor langere tijd in staat is om deel te nemen. De uitvoering van een medicatiereview kan onderdeel zijn van een valpreventieve interventie, maar kan ook gebruikt worden om in bredere zin polyfarmacie terug te dringen en verdient follow-up wanneer wordt besloten om medicatie af te bouwen of te staken. Gezien de wankele balans en afnemende compensatiemechanismen in verschillende tracti dient voorzichtigheid en waakzaamheid betracht te worden.
Eindoordeel:
Sterke aanbeveling voor multifactoriële valpreventie interventies bij ouderen in het verpleeghuis.
Onderbouwing
In the Netherlands, the target population of nursing home residents seems to have changed in recent years due to societal developments, even though we do not have clear population comparisons available. In this module, we rely on available literature that considers the nursing home environment, including in-house rehabilitation settings. The target group for Geriatric Rehabilitation Care is more comparable to the community-dwelling population; therefore, it is recommended to apply the interventions used for this community-dwelling population to individual treatments.
Treatment
Fall prevention within the nursing home environment is important to reduce fall-related morbidity, mortality, loss of independence, and hospital admissions. Hip fractures are a significant cause of these hospital admissions, morbidity, and mortality. Given that the etiology is determined by multiple factors, it is crucial to develop a comprehensive treatment plan. It may be useful to divide the interventions within the treatment plan into intrinsic, modifiable risk factors versus environmental factors. Additionally, it is important that the treatment plan is developed and implemented in a multidisciplinary manner within the organization.
This guideline does not include interventions where there is insufficient evidence (based on comparative research and/or observational studies), and where no new studies are expected to investigate these interventions/treatments. As a result, interventions such as restrictive measures and bed alarm systems are no longer addressed in this guideline.
The original Dutch guideline on fall prevention originates from 2017. This module presents an update of this guideline. Various (inter)national guidelines on fall prevention have been published, including the World Falls Guideline (Montero-Odasso, 2022). Both the original version of the Dutch guideline and the World Falls Guideline concluded that multifactorial interventions should be applied to patients with an increased risk of falls in hospital settings. This module further investigates the effectiveness of multifactorial interventions. To gain comprehensive insight into the effectiveness of multifactorial interventions, it is also important to examine the effectiveness of individual (single component) interventions.
The following definitions were used for the different intervention types, similar to the definitions used in Hopewell (2018)
- Multiple component interventions: all participants receiving the same combination of interventions.
- Multifactorial interventions: the combination of interventions that is delivered, is tailored towards each individual participant.
Population: Older patients in care facilities
Intervention: multiple component and multifactorial interventions for fall prevention
Comparator: Usual care, no intervention or another (single-component) interventions (with no or limited effectiveness)
|
Outcome
|
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence (Quality of evidence) |
Conclusions |
|
|
Intervention |
Control |
||||
|
Multiple component interventions |
|||||
|
Fall risk (number of patients who fell once or more)
|
Risk Ratio: 0.83 (CI 95%: 0.55 to 1.24) Based on data from 602 participants in 2 studies
|
Absolute effect estimates can’t be calculated as only Log (RR) and SE’s were provided in Cameron 2018 |
Very Low Due to serious risk of bias, due to serious inconsistency, due to very serious imprecision, serious imprecision1
|
The evidence is very uncertain about the effect of multiple component interventions on fall risk when compared with usual care in older patients in care facilities.
(Sambrook, 2012; Schnelle, 2003) |
|
|
Rate of falls (falls per person time)
|
Rate Ratio: 0.84 (CI 95%: 0.52 – 1.37) Based on data from 602 participants in 2 studies
|
Absolute effect estimates can’t be calculated as only Log (RR) and SE’s were provided in Cameron 2018 |
Very Low Due to serious risk of bias, due to serious inconsistency, due to very serious imprecision, serious imprecision2
|
The evidence is very uncertain about the effect of multiple component interventions on rate of falls when compared with usual care in older patients in care facilities.
(Sambrook, 2012; Schnelle, 2003) |
|
|
Fractures |
Risk Ratio: 1.33 (CI 95%: 0.28 – 6.22) Based on data from 3757 participants in 6 studies
|
Absolute effect estimates can’t be calculated as only Log (RR) and SE’s were provided in Cameron 2018 |
Very Low Due to serious risk of bias, due to serious inconsistency, due to very serious imprecision, serious imprecision3
|
The evidence is very uncertain about the effect of multiple component interventions on rate of falls when compared with usual care in older patients in care facilities.
(Sambrook, 2012; Schnelle, 2003) |
|
|
Multifactorial interventions |
|||||
|
Fall risk (number of patients who fell once or more)
|
Risk Ratio: 0.90 (CI 95%: 0.80 to 1.01) Based on data from 4557 participants in 11 studies
|
Absolute effect estimates can’t be calculated as only Log (RR) and SE’s were provided in Cameron 2018 |
Low Due to serious imprecision4 Due to serious risk of bias
|
Multifactorial interventions may reduce the number of patients with fall incidents when compared with usual care in older patients in care facilities.
(Becker, 2003; Dyer, 2004; Jensen, 2002; Kerse, 2004; Kerse, 2009; Logan, 2021; McMurdo, 2000; Rubenstein, 1990; Salva, 2016; Shaw, 2003; Whitney, 2017) |
|
|
Rate of falls (falls per person time)
|
Rate Ratio: 0.87 (CI 95%: 0.69 – 1.10) Based on data from 4843 participants in 12 studies
|
Absolute effect estimates can’t be calculated as only Log (RR) and SE’s were provided in Cameron 2018 |
Low Due to serious imprecision5 Due to serious risk of bias |
Multifactorial interventions may to reduce the rate of falls when compared with usual care in older patients in care facilities.
(Becker, 2003; Dyer, 2004; Jensen, 2002; Kerse, 2004; Kerse, 2009; Logan, 2021; McMurdo, 2000; Neyes, 2009; Rubenstein, 1990; Salva, 2016; Shaw, 2003; Whitney, 2017) |
|
|
Fractures |
Risk Ratio: 0.76 (CI 95%: 0.42 – 1.39) Based on data from 3757 participants in 6 studies
|
Absolute effect estimates can’t be calculated as only Log (RR) and SE’s were provided in Cameron 2018 |
Very Low Due to serious risk of bias and very serious imprecision6
|
The evidence is very uncertain about the effect of multifactorial interventions on fractures in older patients in the hospital.
(Becker, 2003; Jensen, 2002; Logan, 2021; Salva, 2016; Shaw, 2003; Whitney, 2017) |
|
| 1. |
Risk of bias: serious. Due to lack of blinding, unclear allocation procedure Inconsistency: serious. Due to heterogeneity in interventions and effect Imprecision: very serious. Due to overlap of both limits of the 95% confidence interval with the minimal clinically important difference. |
| 2. |
Risk of bias: serious. Due to lack of blinding, unclear allocation procedure Inconsistency: serious. Due to heterogeneity in interventions and effect Imprecision: very serious. Due to overlap of both limits of the 95% confidence interval with the minimal clinically important difference. |
| 3. |
Risk of bias: serious. Due to lack of blinding, unclear allocation procedure Inconsistency: serious. Due to heterogeneity in interventions and effect Imprecision: very serious. Due to overlap of both limits of the 95% confidence interval with the minimal clinically important difference. |
| 4. |
Risk of bias: serious. Due to unclear randomization and allocation procedures, lack of blinding. Imprecision: serious. Due to overlap of the lower limit of the 95% confidence interval with the minimal clinically important difference. |
| 5. |
Risk of bias: serious. Due to unclear randomization and allocation procedures, lack of blinding. Imprecision: serious. Due to overlap of the lower limit of the 95% confidence interval with the minimal clinically important difference. |
| 6. |
Risk of Bias: serious. Due to unclear randomization and allocation procedures, lack of blinding Imprecision: very serious. Due to overlap of both limits of the 95% confidence interval with the minimal clinically important difference |
Description of studies
In an earlier version of this guideline (2017) was recommended to use multifactorial interventions to in patients in care facilities with high fall risk. Therefore, in the update of the guideline, focus of the summary of literature was on studies on multiple component and multifactorial interventions. Additionally, to be able to answer the sub-question of this module (“what are the effective intervention components and which intervention components should minimally be considered in multicomponent or multifactorial interventions?”) information from systematic reviews on single-component interventions is also summarized under ‘considerations’.
One systematic review, including eleven relevant trials, and two additional RCTs were included in the analysis of the literature. Important study characteristics and results are summarized in table 2. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Cameron (2018) performed a Cochrane systematic review to assess the effects of interventions designed to reduce the incidence of falls in older people in care facilities and in hospitals. The systematic review was an update of the Cochrane review from Cameron (2012). For this update, the Cochrane Database, MEDLINE, EMBASE and CINAHL were searched for relevant papers published until August 2017. Trials on interventions to prevent falls in older people (mean age > 65 years) in care facilities and hospitals were included. Studies on interventions that took place in emergency departments, outpatient clinics or the community were excluded. The intervention had to be any intervention designed to reduce falls in older people, compared with any other intervention, usual care, or placebo. Study designs: randomized trials, including quasi-randomised trials, cluster randomized trials, and trials in which treatment allocations was inadequately concealed. Outcomes included rate of falls, number of fallers and number of patients sustaining fall-related fractures. For the purpose of this guideline, only studies on multiple component and multifactorial interventions executed in care facilities were considered relevant. In total 3 studies investigated the effect of multiple component interventions (Huang, 2016; Sambrook, 2012; Schnelle, 2003) and 13 studies investigated multiple component or multifactorial interventions (Beck, 2016; Becker, 2003; Dyer, 2004; Jensen, 2002; Kerse, 2004; McMurdo, 2000; Neyens, 2009; Ray, 1997; Rubenstein, 1990; Salvà, 2016; Shaw, 2003; Walker, 2015; Whitney, 2017). Beck (2016) and Ray (1997) did not report one of the predefined outcomes measures and were therefore excluded from the summary of literature. Huang (2016) was also excluded from the summary of literature, as falls in the intervention period were excluded.
An overview the baseline characteristic of the relevant studies is presented in Table 2. Table 3 presents an overview of the different intervention components that were included in the multifactorial interventions. In Cameron (2018) 54 studies were included in which the effect single component interventions was tested. A summary of the results of these studies is presented under the tab ‘considerations’
Table 2: overview of the studies on multiple component and multifactorial interventions in care facilities included in Cameron (2018)
|
Author |
Year |
Participants |
Multifactorial intervention |
|
Becker |
2003 |
Resident of long-term care facility. Able to stand while holding a chair, able to lift one foot (high-level nursing care) Mean age: 83.5 years Fall risk: no information |
Fall prevention program for staff and residents. Staff training on risk factors and preventive measures, check list of environmental hazards, resident education, group exercise program, hip protectors. Residents chose to participate in any combination of interventions for any length of time. Those choosing to participate in fall registration only also received environmental modification and modification of nursing care
|
|
Dyer |
2004;
|
Residents (aged ≥60) of residential care home not specializing in mental illness, without nursing services. (intermediate-level care) Fall risk: no information |
Multifactorial, multidisciplinary intervention: exercise, staff education, medical review, environmental modification |
|
Jensen |
2002 |
Residents (aged ≥65) of residential care facilities (intermediate care) Fall risk: no information |
Multidisciplinary program: general and resident specific tailored interventions for 11 weeks: supervised exercises, medication review, modifying environmental hazards, supplying and repairing aids, hip protectors, education of staff, post fall problem solving conferences and staff guidance. |
|
Kerse |
2004 |
Residents of mixed-level dependency residential homes (intermediate- and high-level care). Mean age: 83.2 years Fall risk: no information |
Fall risk management program: fall coordinator in residential care home, evidence-based risk assessment tool + detailed management strategies (relating to mobility impairments, mental impairments, medications, continence, sensory impairment) tailored care plan based on assessment, logo on high-risk resident walls, manual containing the risk assessment form. |
|
McMurdo |
2000 |
Residents (aged ≥70), of residential care facilities (intermediate-level care) Fall risk: no information
|
Multifactorial, multidisciplinary intervention: fall risk assessment and modification, including medication review. Recommendations sent to the participants GP, optometrist review if indicated, review of lighting levels, supervised exercises. |
|
Neyens |
2009 |
Residents of nursing homes, psychogeriatric wards (high-level nursing care). Fall risk: wards not using a fall-prevention protocol. |
Multifactorial, multidisciplinary intervention: General medical assessment, assessment with fall risk evaluation tool, team decisions about individually tailored fall-prevention activities (medication review, exercise programs, assessing and providing assistive and protective aids), environmental hazards check, general fall prevention activities for the nursing home team. |
|
Rubenstein |
1990 |
Residents of long-term care facility (intermediate- and high-level nursing care). Mean age: 86.8 years Fall risk: no information |
Comprehensive post fall assessment within 7 days of fall. Physical examination including visual screening, extended pulse and blood pressure assessments, assessment of footwear and foot problems, gait and balance assessment, laboratory tests, ECG, 24-hour holter monitoring, environmental assessment |
|
Salvà |
2016 |
Resident (aged ≥65) with or without cognitive impairment living indefinitely in a nursing home place (mixed-level care). Fall risk defined: yes |
Multifactorial falls prevention program: mini falls assessment instrument and implementation of a multifactorial tailored program to prevent falls. Interventions addressed individual risk factors including: gait and balance impairment, cognitive impairment, polypharmacy, assistance with ADLs, lower limb pain, urinary incontinence, weakness, symptomatic heart disease, fear of falling, neuroleptics/psychotropic drugs, problems in feet, dizziness, visual impairment, depressive symptoms
|
|
Sambrook |
2012 |
Residents (aged ≥70), ambulant and likely to survive for 12 months or more, living in care facilities (intermediate care). Fall risk: not reported |
Multiple component intervention. Increased sunlight exposure to face, hands and arms, 30 to 40 minutes, 5 days/week and additionally calcium carbonate 600 mg daily; or increased sunlight exposure alone.
|
|
Schnelle |
2003 |
Residents, incontinent, no in-dwelling catheter and occupying a long stay bed in 4 nursing homes (high-level nursing care) |
Multiple component program FIT: incontinence care and functional exercises delivered by research staff. Every 2 hours from 08.00 to 16.00, 5 days a week for 8 months. At each session patients prompted to toilet and changed if wet; encouraged to walk (or mobilise in wheel chair if not ambulatory); carried out sit-to-stand exercises with minimal assistance; offered fluids to drink before and after each episode. Upper body resistance training (arm curls and arm raises) at one episode per day. Individually tailored to meet weekly goals (up to 8 sit-to-stands, and up to 10 minutes walking (wheeling) per episode)
|
|
Shaw |
2003 |
Patients presenting to accident and emergency departments after a fall (aged ≥65). 79% of participants lived in high- and intermediate nursing care facilities. |
Multifactorial, multidisciplinary assessment and intervention to manage risk factors: Assessment of feet and footwear, gait and balance (physiotherapist), medical intervention, cardiovascular review and advice or treatment on identified risk factors, assessment of environmental fall hazards and hazard modification if indicated. |
|
Walker |
2015 |
Residents (aged ≥50), high risk, of residential care facilities (mixed-level care) Fall risk: fallen at least once in the past year. |
Implementation of the Guide to Action Care Home Tool (a checklist of fall risk factors with suggested actions). |
|
Whitney
|
2017 |
Resident (aged ≥65) of nursing homes (mixed-level care), 97% cognitively impaired. Fall risk: no information |
Multifactorial intervention: exercise, dementia related behaviour management, comprehensive geriatric assessment including medication review, staff training, movement sensor. Fall risk assessment and management, including medical interventions, environmental modifications, equipment modifications, cognitive and behavioural treatment, family guidance. Mobility restrictions and optimizing location for high-risk patients. For moderate risk patients mobility was done only. Under supervision and/or assistance of a professional staff member. |
Additional RCTs
Kerse (2008)* performed a multicentre cluster randomized trial to assess the effectiveness of an activity program in improving function, quality of life and falls in older people in residential care. The trial was executed in 41 low level dependency residential care homes in New-Zealand. 330 residents were offered a goal-setting and individualized activities program by a gerontology nurse, reinforced by usual healthcare assistants, 352 residents received usual care (two social visits). Eligible residents were aged 65 years and over, able to engage in a conversation about a goal remember the goal, and able to participate in program to achieve the goal.
*While the publication date from Kerse (2009) was before the search date, of this guideline, the guideline development panel identified this trial and considered it relevant for the purpose of this guideline. Therefore it was decided to include this study.
Logan (2021) performed a multicentre parallel cluster randomized controlled trial to determine the clinical and cost-effectiveness of a multifactorial fall prevention program compared with usual care in long term care homes in the UK. The study was executed in long term care homes registered to care for older people or those with dementia.
In total 39 nursing homes (n = 775 patients) were randomized to the multifactorial intervention and 45 nursing homes to usual care (n = 882 patients). All residents in the recruited homes were eligible to participate, including those who lacked mental capacity to provide consent. Residents who the care home staff determined to be in the last few days of life, of who were receiving short term care or rehabilitation were not included.
Table 3. Characteristics of included studies
|
Study |
Participants |
Comparison |
Follow-up |
Outcome measures |
Comments |
Risk of bias (per outcome measure)* |
|
Kerse, 2009 |
N at baseline Intervention: 30 Control: 32
Age, mean (SD) Intervention: - Control: -
Sex, % female Intervention: - Control: -
|
Intervention: UpRight exercise program, group exercise program including strength, balance, sensory integration and dual tasks exercises, 2 times/week (60 min/session)
Comparison: control seated exercise |
1 year follow-up |
Time to fall over 12 months |
Information retrieved from systematic review (not published) |
|
|
Logan, 2021 |
N at baseline Intervention: 775 (39 nursing homes) Control: 882 (45 nursing homes)
Age, mean (SD) Intervention: 86, (8.6) Control: 84.2 (9.7)
Sex, % female Intervention: 70.2 Control: 65.9
Patients with dementia, % Intervention: 65.4 Control: 68.4
|
Intervention: Multifactorial fall prevention program (GtACH program) Control: usual care |
Outcomes were assessed at 3, 6, 9 and 12 monts post-randomisation
At 91-180 days, data was available for 630 patients in the intervention group and 712 patients in the usual care group (no data available because patients died of moved to a new care home, or because patients withdrew from care home) |
Fall rate (at 91-180 days after randomization)
Number of fallers (at 91-180 days after randomization)
Fractures (0 – 180 days) |
Economic evaluation was also performed |
|
Table 4: overview of the intervention components included in the multiple component and multifactorial interventions studied in the included trials
|
|
Exercise |
Medication int. |
Vitamin D supplemen-tation |
Environmental int. |
Assistive technology* |
Social environment |
Staff education |
Resident education |
Fall risk assessment |
Psycho- logical int. |
Other |
|
Becker (2003) |
X |
|
|
X |
X |
|
X |
|
|
|
|
|
Dyer (2004) |
X |
X |
|
X |
|
|
X |
|
|
|
|
|
Jensen (2002) |
X |
X |
|
X |
X |
|
X |
|
|
|
Post-fall problem solving conferences |
|
Kerse (2004) |
|
X |
|
|
X |
|
|
|
X |
|
Fall coordinator in residential care home, continence |
|
Kerse (2008) |
X |
|
|
|
|
|
x |
|
|
|
Goal setting |
|
Logan (2021) |
|
|
|
|
|
|
|
|
|
|
Implementation of the Guide to Action Care Home Tool |
|
McMurdo (2000) |
X |
X |
|
|
|
|
|
|
X |
|
Recommendations sent to the participants GP. optometrist review if indicating, review of lighting levels. |
|
Neyens (2009) |
X |
X |
|
X |
X |
|
|
|
X |
|
|
|
Rubenstein (1990) |
|
|
|
|
|
|
|
|
|
|
Physical examination including visual screening, assessment of: - extended pulse and blood pressure footwear - foot problems, - gait and balance - environement laboratory tests, ECG, 24-hour holter monitoring, |
|
Salvà (2016) |
|
X |
|
|
X |
|
|
|
X |
|
Interventions addressed individual risk factors including: - gait and balance impairment - cognitive impairment, - assistance with ADLs, - lower limb pain, - urinary incontinence - weakness, - symptomatic heart diseas - fear of falling, - problems in feet, - dizziness - visual impairment, - depressive symptoms |
|
Sambrook (2012) |
|
|
X |
|
|
|
|
|
|
|
Sunlight Exposure, Calcium carbonate |
|
Schnelle (2003) |
X |
|
|
|
|
|
|
|
|
|
Incontinence care |
|
Shaw (2003) |
X |
X |
|
X |
X |
|
|
|
|
|
|
|
Walker (2015) |
|
|
|
|
|
|
|
|
|
|
Implementation of the Guide to Action Care Home Tool |
|
Whitney (2017) |
X |
X |
|
X |
X |
X |
X |
|
X |
X |
Dementia related behaviour management, CGA. |
*including hip-protectors, walking aids, footwear, movement sensors; Int = interventioon
Results
Multiple component interventions
Fall risk (number of patients who fell once or more)
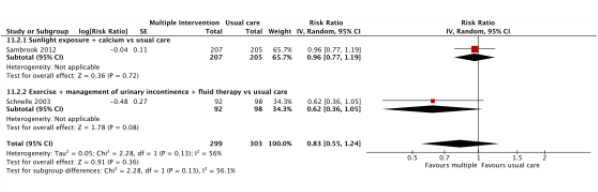
Two studies reported the effects of multiple component interventions on fall risk (Sambrook, 2012; Schnelle, 2003). See Figure 1.
Sambrook (2012) investigated the effects of a multiple component intervention with sunlight exposure and calcium (n = 207) compared to usual care (n = 205). A Risk Ratio (RR) of 0.96 (95% CI: 0.77 to 1.19) was reported. Schnelle (2003) investigated the effects of an exercise + urinary incontinence management and fluid therapy intervention (n = 92) with usual care (n = 98). A RR of 0.62 (95% CI: 0.36 to 1.05) was reported.
The pooled risk ratio between multiple component interventions and usual care in care facilities was 0.83 (95% CI 0.55 to 1.24).
Figure 1. Forest plot showing the comparison multiple component interventions versus usual care for the outcome fall risk (number of patients who fell once or more) Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; SD: standard deviation; I2; statistical heterogeneity; CI: confidence interval.
Rate of falls (falls per person time)
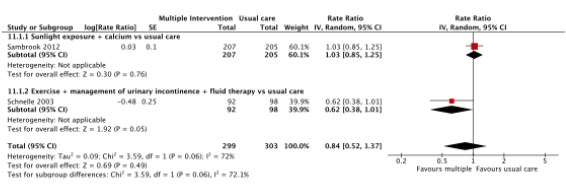
Two studies reported the effects of multiple component interventions on rate of falls (Sambrook, 2012; Schnelle, 2003). See Figure 2.
Sambrook (2012) investigated the effects of a multiple component intervention with sunlight exposure and calcium (n = 207) compared to usual care (n = 205). A Rate ratio (RaR) of 1.03 (95% CI: 0.85 to 1.25) was reported.
Schnelle (2003) investigated the effects of an exercise + urinary incontinence management and fluid therapy intervention (n = 92) with usual care (n = 98). A RR of 0.62 (95% CI: 0.38 to 1.01) was reported.
The pooled rate ratio between multiple component interventions and usual care in care facilities was 0.84 (95% CI 0.52 to 1.37).
Figure 2. Forest plot showing the comparison multiple component interventions versus usual care for the outcome rate of falls. Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; SD: standard deviation; I2; statistical heterogeneity; CI: confidence interval.
Fall related fracture risk
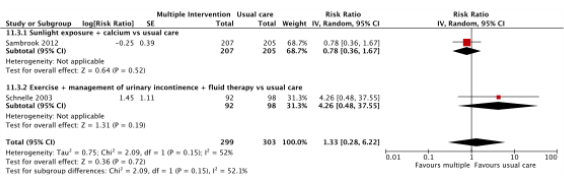
Two studies reported the effects of multiple component interventions on rate of falls (Sambrook, 2012; Schnelle, 2003). See Figure 3.
Sambrook (2012) investigated the effects of a multiple component intervention with sunlight exposure and calcium (n = 207) compared to usual care (n = 205). A RR of 0.78 (95% CI: 0.36 to 1.67) was reported.
Schnelle (2003) investigated the effects of an exercise + urinary incontinence management and fluid therapy intervention (n = 92) with usual care (n = 98). A RR of 4.26 (95% CI: 0.48 to 37.55) was reported.
The pooled rate ratio between multiple component interventions and usual care in care facilities was 1.33 (95% CI 0.28 to 6.22).
Figure 3. Forest plot showing the comparison multiple component interventions versus usual care for the outcome fracture risk Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; SD: standard deviation; I2; statistical heterogeneity; CI: confidence interval.
Multifactorial interventions
Fall risk (number of patients who fell once or more)
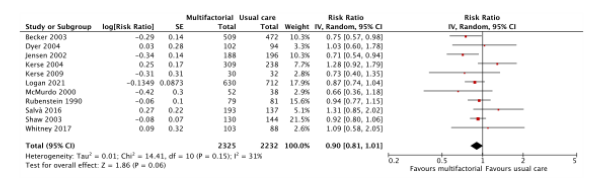
Eleven studies reported the effects of multifactorial interventions on fall risk (Becker, 2003; Dyer, 2004; Jensen, 2002; Kerse, 2004; Kerse 2009; Logan, 2021; McMurdo, 2000; Rubenstein, 1990; Salva, 2016; Shaw, 2003; Whitney, 2017). The risk ratio between patients who received a multifactorial intervention (n = 2325) compared to patients who received usual care (n = 2232) was RR: 0.90 (95% CI: 0.81 to 1.01). See Figure 4.
Figure 4. Forest plot showing the comparison multifactorial interventions versus usual care for the outcome fall risk. Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; SD: standard deviation; I2; statistical heterogeneity; CI: confidence interval.
Rate of falls (falls per person time)
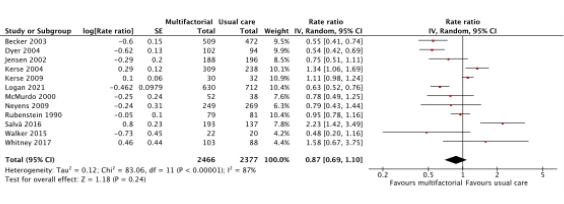
Twelve studies reported the effects of multifactorial interventions on fall risk (Becker, 2003; Dyer, 2004; Jensen, 2002; Kerse, 2004; Kerse, 2009; Logan, 2021; McMurdo, 2000; Neyes, 2009; Rubenstein, 1990; Salva, 2016; Shaw, 2003; Whitney, 2017). The rate ratio between patients who received a multifactorial intervention (n = 2466) compared to patients who received usual care (n = 2377) was RaR: 0.87 (95% CI: 0.69 to 1.10). See Figure 5.
Figure 5. Forest plot showing the comparison multifactorial interventions versus usual care for the outcome falls rate. Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; SD: standard deviation; I2; statistical heterogeneity; CI: confidence interval.
Fracture risk
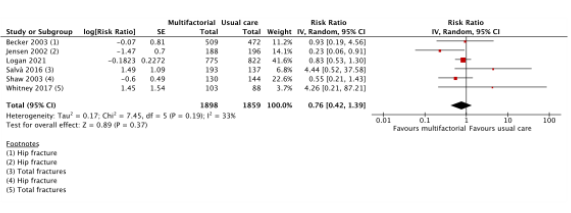
Six studies reported the effects of multifactorial interventions on fall risk (Becker, 2003; Jensen, 2002; Logan, 2021; Salva, 2016; Shaw, 2003; Whitney, 2017). The difference between patients who received a multifactorial intervention (n = 1898) compared to patients who received usual care (n = 1859) was RR: 0.76 (95% CI: 0.42 to 1.39). See Figure 6.
Figure 6. Forest plot showing the comparison multifactorial interventions versus usual care for the outcome fracture risk. Pooled relative risk ratio, random effects model. Z: p-value of overall effect; df: degrees of freedom; SD: standard deviation; I2; statistical heterogeneity; CI: confidence interval.
A systematic review of the literature was performed to answer the following question: What is the effectiveness of multiple component and multifactorial interventions for fall prevention in care facilities, compared to usual care, no intervention or another (single component) intervention?
Table 1. PICO
|
Patients |
Older patients in care facilities |
|
Intervention |
Multiple component or Multifactorial interventions for fall prevention |
|
Control |
Usual care, no intervention or another (single component) interventions |
|
Outcomes |
|
|
Other selection criteria |
Study design:
|
Relevant outcome measures
A priori, the guideline panel defined the outcomes as follows:
- Falls risk: The risk of being a faller; the number of people who fell once or more (fallers) in the intervention and control group.
- Rate of falls: falls per unit of person time (such as bed days), presented as the rate ratio
- Fall related fracture risk: the risk of fall related fractures in the intervention group, compared to the control group.
The guideline panel considered falls risk and rate of falls as a critical outcome measure for decision making; and fall related fracture risk as an important outcome measure for decision making.
The guideline panel defined a difference of 10% as a minimal clinically (patient) important difference, RR < 0.90 and RR > 1.10 for the outcomes falls risk, rate of falls and fall related fracture risk.
Search and select (Methods)
To answer this question, the Cochrane systematic review from Cameron (2018) was used as a basis for this literature analysis. In Cameron (2018), the Cochrane Bone, Joint and Muscle trauma group Register, the Cochrane Central register of Controlled trials (CENTRAL), OVID/MEDLINE, Embase and CINAHL were searched with relevant search terms, until 12-06-2017. We performed an update of this Cochrane Systematic review with similar search terms as used in Cameron (2018). The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms for articles published between 12-06-2017 until 09-08-2024. A combined search for older persons in the hospital, older persons in the community and older persons living in nursing homes was performed, as the specific research setting was not always specified in the title/abstract. The detailed search strategy is depicted under the tab Methods. The systematic literature search resulted in 6510 hits. Studies were selected based on the criteria described in Table 1. Titles and abstracts were screened using the ASReview software version 1.6.2. The settings TF-IDF and Naïve bayes were used. Morris (2022) was used as prior knowledge for inclusion. Park (2021), Borreli (2021), Verrusio (2018) were used as prior knowledge for exclusions.
The first 10% of references were screened by the working group and the guideline methodologist. The remaining articles were subsequently screened by the guideline methodologist, using the following stopping rule: stop after 200 subsequent exclusions.
Initially, nine studies were selected based on title and abstract screening using ASreview software. After reading the full text, 101 studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and three studies were included.
- Bogaerts JMK, Gussekloo J, de Jong-Schmit BEM, Le Cessie S, Mooijaart SP, van der Mast RC, Achterberg WP, Poortvliet RKE. Effects of the discontinuation of antihypertensive treatment on neuropsychiatric symptoms and quality of life in nursing home residents with dementia (DANTON): a multicentre, open-label, blinded-outcome, randomised controlled trial. Age Ageing. 2024 Jul 2;53(7):afae133. doi: 10.1093/ageing/afae133. PMID: 38970547; PMCID: PMC11227112.
- Cameron ID, Dyer SM, Panagoda CE, Murray GR, Hill KD, Cumming RG, Kerse N. Interventions for preventing falls in older people in care facilities and hospitals. Cochrane Database Syst Rev. 2018 Sep 7;9(9):CD005465. doi: 10.1002/14651858.CD005465.pub4. PMID: 30191554; PMCID: PMC6148705.
- Dawson R, Suen J, Sherrington C, Kwok W, Pinheiro MB, Haynes A, McLennan C, Sutcliffe K, Kneale D, Dyer S. Effective fall prevention exercise in residential aged care: an intervention component analysis from an updated systematic review. Br J Sports Med. 2024 May 31;58(12):641-648. doi: 10.1136/bjsports-2023-107505. PMID: 38658135; PMCID: PMC11187368.
- Logan PA, Horne JC, Gladman JRF, Gordon AL, Sach T, Clark A, Robinson K, Armstrong S, Stirling S, Leighton P, Darby J, Allen F, Irvine L, Wilson ECF, Fox C, Conroy S, Mountain G, McCartney K, Godfrey M, Sims E. Multifactorial falls prevention programme compared with usual care in UK care homes for older people: multicentre cluster randomised controlled trial with economic evaluation. BMJ. 2021 Dec 7;375:e066991. doi: 10.1136/bmj-2021-066991. PMID: 34876412; PMCID: PMC8649897.
- Nemeth B, van der Kaaij M, Nelissen R, van Wijnen JK, Drost K, Blauw GJ. Prevention of hip fractures in older adults residing in long-term care facilities with a hip airbag: a retrospective pilot study. BMC Geriatr. 2022 Jun 30;22(1):547. doi: 10.1186/s12877-022-03221-1. Erratum in: BMC Geriatr. 2022 Jul 27;22(1):624. doi: 10.1186/s12877-022-03267-1. PMID: 35773627; PMCID: PMC9245388.
- Rezola-Pardo C, Irazusta J, Mugica-Errazquin I, Gamio I, Sarquis-Adamson Y, Gil SM, Ugartemendia M, Montero-Odasso M, Rodriguez-Larrad A. Effects of multicomponent and dual-task exercise on falls in nursing homes: The AgeingOn Dual-Task study. Maturitas. 2022 Oct;164:15-22. doi: 10.1016/j.maturitas.2022.06.006. Epub 2022 Jun 20. PMID: 35763894.
- Suen J, Kneale D, Sutcliffe K, Kwok W, Cameron ID, Crotty M, Sherrington C, Dyer S. Critical features of multifactorial interventions for effective falls reduction in residential aged care: a systematic review, intervention component analysis and qualitative comparative analysis. Age Ageing. 2023 Nov 2;52(11):afad185. doi: 10.1093/ageing/afad185. PMID: 37993405; PMCID: PMC10665139.
Beoordelingsdatum en geldigheid
Publicatiedatum : 30-04-2026
Beoordeeld op geldigheid : 30-04-2026
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinair cluster ingesteld. Het cluster Duizeligheid, Vallen en Syncope bestaat uit meerdere richtlijnen, zie hier voor de actuele clusterindeling. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden geven hun expertise, indien nodig. De volgende personen uit het cluster zijn betrokken geweest bij de herziening van deze module:
Clusterstuurgroep
- Prof. dr. T.D. (Tjasse) Bruintjes, voorzitter cluster Duizeligheid, Vallen en Syncope, NVKNO, KNO-arts, Gelre Ziekenhuizen
- Prof. dr. N. (Nathalie) van der Velde, NVKG, klinisch geriater, Amsterdam UMC
- Dr. R.B. (Roeland) van Leeuwen, NVN, neuroloog, Gelre Ziekenhuizen
- Dr. J.H.W. (Joost) Rutten, NIV, internist, Radboud UMC
- Drs. S. (Simon) Geerse, NVKNO, KNO-arts, Treant Ziekenhuizen
- Dr. W.P.A. (Willem) Kelders, NVKNO, KNO-arts, Franciscus Gasthuis & Vlietland
- Drs. J.O. (Judella) Daal, NVKG, klinisch-geriater, Dijklander Ziekenhuis
Clusterexpertisegroep
- Drs. C.M. (Margreet) Aalten, NVKG klinisch geriater, St. Jansdal Ziekenhuis
- Ir. R.M. (Renske) Hoeben, NVKF, Klinisch Fysicus, Bernhoven
- Drs. B.S. (Birgit) Jacobs, NVZA, ziekenhuisapotheker, Catharina Ziekenhuis
- Dr. E.C.A. (Evert) Kaal, NVN, neuroloog, Maasstad Ziekhuis
- Dr. W.F. (Linde) Kok, Verenso, specialist ouderengeneeskunde bij GeriCall
- Dr. E.P. (Eveline) van Poelgeest, NIV, NVKG, internist-ouderengeneeskunde, Amsterdam UMC
- Dr. V.A. (Vincent) van Vugt, NHG, huisarts, Amsterdam UMC
- B.J.F.M. (Bart) Zwaneveld, KNGF, orofaciaal en manueel therapeut
Met ondersteuning van
- Dr. R. Zwarts - van de Putte, adviseur, Kennisinstituut van Medisch Specialisten
- Drs. D.G. Ossendrijver, adviseur, Kennisinstituut van Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van de clusterleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Cluster stuurgroepleden
Tabel 1 Gemelde (neven)functies en belangen stuurgroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Tjasse Bruintjes*
|
- KNO-arts (vrijgevestigd) Gelre ziekenhuizen Apeldoorn (0,8 fte) |
- lid beroepsgenoot Regionaal Tuchtcollege voor de Gezondheidszorg Zwolle (onkostenvergoeding) |
Geen |
Geen |
In 2022 toegekende ZonMW-subsidie voor de zgn. Predmentrial |
Geen |
Geen |
07-01-2021
18-05-2025 herbevestigd |
Geen |
|
Nathalie Van der Velde |
Staflid en hoogleraar onderafdeling Geriatrie Amsterdam UMC, locatie AMC |
Onbetaald: |
Geen |
Geen |
Nee; alleen subsidies van onafhankelijke subsidieverstrekkers (NWO, ZonMW, Amsterdams Universiteitsfonds) |
Geen |
Geen |
07-10-2020
06-06-2025 herbevestigd |
Geen |
|
Roeland Van Leeuwen |
Neuroloog, Gelre ziekenhuizen Apeldoorn |
Lid Scheidsgerecht Gezondheidszorg. Betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
11-10-2020
18-05-2025 herbevestigd |
Geen |
|
Joost Rutten |
Internist-Vasculair Geneeskunde 0.9 FTE/Radboudumc, Nijmegen |
Consultant op projectbasis voor Volw Interna–ional – project ontwikkeling screeningstool ter opsporing patiënten met lipodystrofie |
Geen |
Geen |
Principle Investigator Radboudumc CALM DIEM en CALM START studies, sponsor Vascular Dynamics (studies naar effect van specifiek type carotisstent ter verlaging van de bloeddruk) |
Geen |
Geen |
21-01-2021
23-05-2025 herbevestigd |
|
|
Simon Geerse |
KNO-arts (vrijgevestigd) Treant ziekenhuizen (0.8 fte) |
Voorzitter kerngroep Vestibulologie KNO-vereniging (vacatievergoeding) |
Geen |
Geen |
Geen |
Geen |
Geen |
21-01-2021
26-5-2025 herbevestigd |
Geen |
|
Willem Kelders |
- KNO-arts (vrijgevestigd) Franciscus Gasthuis en Vlietland Rotterdam (0,8 fte) |
- lid kerngroep vestibulogie KNO-vereniging (vacatievergoeding) |
Geen |
Geen |
Geen |
Geen |
Geen |
10-01-2021
17-5-2025 herbevestigd |
Geen |
|
Judella Daal |
NVKG als vereniging |
Voorzitter SIG Valpreventie NVKG/Landelijke netwerk valklinieken |
Geen |
Geen |
Geen |
Geen |
Geen |
10-04-2025
21-5-2025 herbevestigd |
Geen |
Betrokken cluster expertisegroepleden
Tabel 2 Gemelde (neven)functies en belangen expertisegroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Margreet Aalten |
Klinisch geriater Ziekenhuis St. Jansdal Harderwijk 0,6 FTE |
Lid accreditatie beoordelingscommissie NVKG onbezoldigd. |
Geen |
Geen |
Geen |
Geen |
Geen |
13-10-2021
20-05-2025 herbevestigd |
Geen |
|
Evert Kaal |
Neuroloog Maasstad Ziekenhuis 0,8 FTE |
Voorzitter Werkgroep voor Syncope en Autonome Aandoeningen, onbetaald |
Geen |
Geen |
Geen |
Geen |
Geen |
15-10-2021
18-06-2025 herbevestigd |
Geen |
|
Linde Kok |
Specialist Ouderengeneeskunde bij GeriCall, momenteel in de 1e lijn |
Geen |
Geen |
Geen relaties met belangen |
Geen |
Geen |
Geen |
10-10-2023
16-5-2025 herbevestigd |
Geen |
|
Eveline Van Poelgeest |
Internist ouderengeneeskunde AUMC, betaald |
Kernlid Expertisecentrum farmacotherapie bij ouderen (Ephor), betaald |
Geen |
Geen |
Geen |
Geen |
Geen |
15-06-2023
16-5-2025 herbevestigd
|
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door deelname van de Patiëntenfederatie Nederland in de richtlijncommissie.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerden de clusterleden conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
Module verlaging valrisico bij thuiswonende ouderen |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.