Laboratoriumonderzoek bij bekende risicofactor van polyneuropathie
Uitgangsvraag
Is laboratoriumonderzoek naar een bijkomende oorzaak van een chronische polyneuropathie geïndiceerd wanneer een patiënt al een bekende risicofactor heeft?
Aanbeveling
Bepaal (voor zover niet eerder is verricht) bij iedere patiënt met een chronische polyneuropathie het basislaboratorium pakket, ook wanneer de patiënt al bekend is met een risicofactor voor polyneuropathie.
Overwegingen
De resultaten van het literatuuronderzoek tonen dat de kans op het vinden van een tweede risicofactor reëel is (ongeveer 9% van de patiënten met chronische polyneuropathie). Nagenoeg alle verschillende oorzaken kwamen in combinatie met andere oorzaken voor. Om die reden is ervoor gekozen bij iedere patiënt met een nieuw gediagnosticeerde chronische polyneuropathie laboratoriumonderzoek te verrichten, ondanks de hogere kosten die dit met zich meebrengt. In geval van afwezigheid van alarmsymptomen kan worden volstaan met het basislaboratoriumpakket. Het laboratoriumonderzoek hoeft slechts eenmaal ten tijde van het diagnosticeren van de polyneuropathie te worden verricht.
Onderbouwing
In de richtlijn Polyneuropathie uit 2005 wordt geadviseerd geen verder aanvullend laboratoriumonderzoek te doen bij patiënten met een chronische polyneuropathie die al een bekende risicofactor hebben (diabetes mellitus, nierinsufficiëntie, overmatig alcoholgebruik en het gebruik van bepaalde geneesmiddelen).
Diabetes mellitus en overmatig alcoholgebruik hebben een hoge prevalentie in de algemene populatie. Daarnaast komen bij patiënten met deze risicofactoren relatief vaker co-morbiditeiten (onder anderen nierfunctiestoornissen of vitaminedeficiënties) voor. Het is van belang om inzicht te hebben in het vóórkomen van meerdere risicofactoren/ mogelijke oorzaken van polyneuropathie bij één persoon, opdat geen mogelijk behandelbare oorzaken worden gemist.
In deelvraag 2 wordt beschreven of bij patiënten met een chronische polyneuropathie met een bekende risicofactor aanvullend laboratoriumonderzoek naar een andere, bijkomende oorzaak van de polyneuropathie geïndiceerd is.
Naar schatting heeft ongeveer 9% van de patiënten met een chronische polyneuropathie meer dan één mogelijke oorzaken voor de polyneuropathie. Diabetes mellitus, overmatig alcoholgebruik, vitaminedeficiënties worden het vaakst gevonden in combinatie met nog een andere risicofactor.
Bewijskracht van de literatuur
Gezien de aard van de uitgangsvraag is er geen GRADE beoordeling uitgevoerd.
Bovenstaande resultaten zijn gebaseerd op observationeel onderzoek in relatief heterogene populaties. Derhalve is de bewijskracht laag.
Beschrijving studies
De resultaten van deelvraag 2 zijn gebaseerd op negen publicaties. Zeven van de negen studies kwamen overeen met de zoekresultaten van deelvraag 1 en zijn reeds beschreven onder Beschrijving studies bij die deelvraag.
Daarnaast werden twee hospital-based studies van Gorson (2006) en Dyck (1993) gevonden die cohorten van 103 en 171 volwassen patiënten met diabetes mellitus beschrijven. In de studie van Gorson (2006) werd de diagnose polyneuropathie gesteld op basis van anamnese en lichamelijk onderzoek, in de studie van Dyck (1993) werd de diagnose in de meerderheid van de patiënten bevestigd middels EMG.
Resultaten
Het aantal patiënten dat meer dan één risicofactor heeft voor de chronische polyneuropathie varieerde in de diverse studies van 0-53% met een mediaan van 9% (zie ook evidencetabel). In zes van de negen geïncludeerde studies lag het aantal patiënten met meerdere risicofactoren tussen 5-11%. Nagenoeg alle verschillende risicofactoren werden gevonden in combinatie met andere risicofactoren, hoewel de frequentie sterk verschilde per oorzaak. In totaal werden 378 risicofactoren gevonden bij 181 patiënten. De meest voorkomende binnen deze 334 risicofactoren waren diabetes mellitus (37%), overmatig alcoholgebruik (14%), vitamine deficiënties (11%), en metabole oorzaken (nier-, schildklier- en leverlijden, 11%). Infectieuze oorzaken, maligniteiten en immuungemedieerde en erfelijke neuropathieën werden veel minder frequent gevonden in combinatie met een andere risicofactor (0-6%). Een compleet overzicht van alle voorkomende combinaties van risicofactoren wordt gegeven in de evidencetabel.
Zoekvraag 2: Bij welk percentage patiënten met polyneuropathie en diabetes mellitus worden er nog andere (additionele) risicofactoren voor polyneuropathie gevonden?
Flow-chart literatuursearch deelvraag 2
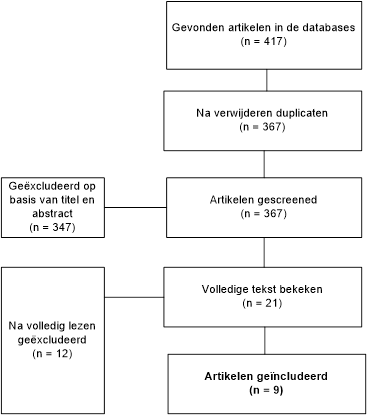
In de databases Medline (via OVID en Pubmed) en Embase (via EMbase.com) is met relevante zoektermen systematisch gezocht naar publicaties naar patiënten met polyneuropathie en diabetes mellitus, met als uitkomst het vóórkomen van meerdere risicofactoren voor een chronische polyneuropathie. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 417 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: systematische analyse in cohorten met meer dan 10 patiënten naar het vóórkomen van oorzaken van een chronische polyneuropathie in de Westerse populatie, in combinatie met de zoekterm diabetes mellitus.
Op basis van titel en abstract werden in eerste instantie 21 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 12 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en zijn er 9 studies geselecteerd, die definitief zijn opgenomen in de literatuuranalyse. De belangrijkste studiekarakteristieken en resultaten zijn opgenomen in de evidence tabel. Indien beschreven werd ook het voorkomen van meerdere oorzaken bij andere categorieën patiënten dan diabetes mellitus patiënten opgenomen in de evidence tabel gezien de relevantie voor het beantwoorden van de uitgangsvraag.
- Hanewinckel R, Ikram MA, van Doorn PA. Assessment scales for the diagnosis of polyneuropathy. J Peripher Nerv Syst. 2016 Jun;21(2):61-73. doi: 10.1111/jns.12170. Review. PubMed PMID: 26968746.
- Rudolph T, Farbu E. Hospital-referred polyneuropathies--causes, prevalences, clinical- and neurophysiological findings. Eur J Neurol. 2007 Jun;14(6):603-8. PubMed PMID: 17539935.
- Gallagher G, Rabquer A, Kerber K, Calabek B, Callaghan B. Value of thyroid and rheumatologic studies in the evaluation of peripheral neuropathy. Neurol Clin Pract. 2013;3(2):90-8. PMID: 23914318
- Vrancken AF, Kalmijn S, Buskens E, Franssen H, Vermeulen M, Wokke JH, Notermans NC. Feasibility and cost efficiency of a diagnostic guideline for chronic polyneuropathy: a prospective implementation study. J Neurol Neurosurg Psychiatry. 2006 Mar;77(3):397-401. Erratum in: J Neurol Neurosurg Psychiatry. 2006 May;77(5):710. PubMed PMID: 16484653; PubMed Central PMCID: PMC2077697.
- Gorson KC, Ropper AH. Additional causes for distal sensory polyneuropathy in diabetic patients. J Neurol Neurosurg Psychiatry. 2006 Mar;77(3):354-8. PubMed PMID: 16484643; PubMed Central PMCID: PMC2077706.
- Rosenberg NR, Portegies P, de Visser M, Vermeulen M. Diagnostic investigation of patients with chronic polyneuropathy: evaluation of a clinical guideline. J Neurol Neurosurg Psychiatry. 2001 Aug;71(2):205-9. PubMed PMID: 11459893; PubMed Central PMCID: PMC1737522.
- Johannsen L, Smith T, Havsager AM, Madsen C, Kjeldsen MJ, Dalsgaard NJ, Gaist D, Schrøder HD, Sindrup SH. Evaluation of patients with symptoms suggestive of chronic polyneuropathy. J Clin Neuromuscul Dis, 2001. 3(2): p. 47-52. PMID: 19078654
- Beghi E, Monticelli ML. Chronic symmetric symptomatic polyneuropathy in the elderly: a field screening investigation of risk factors for polyneuropathy in two Italian communities. Italian General Practitioner Study Group (IGPST). J Clin Epidemiol. 1998 Aug;51(8):697-702. PubMed PMID: 9743318.
- Dyck PJ, Kratz KM, Karnes JL, Litchy WJ, Klein R, Pach JM, Wilson DM, O'Brien PC, Melton LJ 3rd, Service FJ. The prevalence by staged severity of various types of diabetic neuropathy, retinopathy, and nephropathy in a population-based cohort: the Rochester Diabetic Neuropathy Study. Neurology. 1993 Apr;43(4):817-24. Erratum in: Neurology 1993 Nov;43(11):2345. PubMed PMID: 8469345.
Evidence-table UV 4b, multipele risicofactoren bij patiënten met polyneuropathie en diabetes mellitus
|
Referentie |
Studie karakteristieken |
Patiënt karakteristieken
|
Inclusie en exclusie criteria |
Diagnostische criteria |
Proportie patiënten met tweede etiologie |
Etiologie |
Opmerkingen |
|
Hanewinckel (2016) |
Studie type Population-based
Setting Prospectief cohort 2013-2015
Land Nederland
Financiering Prinses Beatrix Spierfonds, Janivo foundation, NOW, ZonMW. |
Aantal deelnemers n = 1310, waarvan n = 72 diagnose polyneuropathie
Leeftijd Gemiddeld 70 jaar
Geslacht 55% vrouw
|
Inclusie ≥ 45 jaar
Exclusie onvoldoende data om de diagnose PNP te kunnen stellen |
Definite PNP 1. eerder gediagnosticeerd door neuroloog na volledige work-up;
2. consensus door expert panel over afwijkend neurologisch onderzoek, typische symptomen, en passend geleidingsonderzoek; 3. consensus door expert panel over afwijkend neurologisch onderzoek en zeer typische symptomen
EMG bevestigd n = 65
|
Meerdere risicofactoren: n = 16 (22%)
2 risicofactoren: n = 13 (18%)
3 risicofactoren: n = 2 (3%)
4 risicofactoren: n = 1 (1%)
In 72 patiënten werden 92 oorzaken gevonden (128%) |
Diabetes mellitus en: -alcohol n = 2 -nierfunctiestoornis n = 3 -nierfunctiestoornis + vit B12 deficiëntie n = 1 -nierfunctiestoornis + schildklier n = 1 -toxisch n = 1 -vit B12 deficiëntie n = 3 -paraproteïnemie n = 2
Overig: -toxisch + systeemziekte n = 1 -toxisch + vit B12 deficiëntie + schildklier + paraproteïnemie n = 1 -toxisch + schildklier n = 1
|
Niet-gepubliceerde data
|
|
Gallagher (2013) |
Studie type Hospital-based
Setting Retrospectief statusonderzoek, tertiair centrum, 2007-2008
Land Verenigde Staten
Financiering Geen |
Aantal deelnemers n = 225
Leeftijd Gemiddeld 63 jaar (51-72 jaar)
Geslacht
|
Inclusie criteria Diagnose polyneuropathie gesteld door een neuromusculair arts
Exclusie criteria -compressie neuropathie -traumatische neuropathie -radiculopathie |
Diagnose PNP gesteld door neuromusculair arts
EMG bevestigd n = 175 (78%) |
Meerdere risicofactoren: n = 24 (11%) |
Risicofactoren die in combinatie met andere factoren voorkwamen: -diabetes n = 4 -erfelijk n = 6 -toxisch/chemotherapie n = 4 -reumatologische aandoening n = 3 -auto-immuun n = 2 -MGUS/anti-MAG n = 2 -alcohol n = 5 -nierinsufficientie n = 1 -vitamine B12 deficientie n = 4 -schildklier n = 3 |
Niet vermeld welke combinaties van risicofactoren voorkwamen
|
|
Rudolph (2007) |
Studie type Hospital-based
Setting Retrospectief, status-onderzoek 2000-2005
Land Noorwegen
Financiering Niet vermeld
|
Aantal deelnemers n = 226
Leeftijd Gemiddeld 65 jaar (9-92 jaar)
Geslacht 40% vrouw
|
Inclusie Alle patiënten met zowel klinische als neurofysiologische karakteristieken passend bij PNP
Exclusie asymmetrisch aangedane zenuwen bij EMG onderzoek (mononeuritis multiplex)
|
‘Definite PNP’ Diagnose op basis van zowel klinische symptomen, neurologisch onderzoek en EMG afwijkingen van minimaal 2 aangedane zenuwen (nn. medianus, radialis, peroneus, tibialis, suralis)
EMG bevestigd n = 226
|
Meerdere risicofactoren: n = 21 (9%)
2 risicofactoren: n = 20 (9%) 3 risicofactoren: n = 1 (<1%)
|
Diabetes mellitus in combinatie met: -hypothyreoidie n = 7 -alcohol n = 7 -toxische medicatie n = 1 -vit B12 deficiëntie n = 1
Alcohol en hypothyreoidie n =1
Overig: -Vit B12 deficientie + infectie n = 1 -Maligniteit en toxische medicatie n = 1 -Collagenose en hypothyreoidie n = 1 -vit B12 deficientie + sarcoidose + hypothyreoidie n = 1
|
Bij 2/3 van de patiënten met meerdere risicofactoren was diabetes mellitus één van de risicofactoren ( n = 14) |
|
Originele data uit studie Vrancken (2006) |
Studie type Hospital-based
Setting Prospectief multi-center (zowel algemene ziekenhuizen als UMC), 1999-2002
Land Nederland
Financiering CVZ/VAZ doelmatigheidsproject “doelmatigheid academische ziekenhuizen”
|
Aantal deelnemers n = 308
Leeftijd ≥ 18 jaar
Geslacht Niet beschreven
|
Inclusie -Leeftijd ≥ 18 jaar -klachten en NO passend bij PNP -EMG bevestiging -Work-up op de polikliniek - Eerste analyse voor PNP
Exclusie Niet voldaan aan de criteria van de richtlijn PNP |
Symptomen en neurologisch onderzoek passend bij PNP, met EMG bevestiging
EMG bevestigd: n = 308 |
Meerdere risicofactoren: n = 34 (11%)
2 risicofactoren: n = 31 (10%) 3 risicofactoren: n = 3 (1%)
|
Diabetes mellitus en: -alcohol n = 8 -nierfunctiestoornis n = 3 -schildklier n = 1 -CIDP n = 1 - vit B1 def n = 1 -erfelijk n = 2 -systeemziekte n = 1 -toxisch n = 1 -nierfunctiestoornis + CIDP n = 1 - nierfunctiestoornis + alcohol n = 1
Alcohol en: -vit B1 deficientie n = 3 -nierfunctiestoornis n = 2 -nierfunctiestoornis + toxisch n = 1
MGUS en: -CIDP n = 1 -maligniteit n = 2 -vit B12 deficientie n = 1
Toxisch en: -maligniteit n = 2 -vit B12 deficientie n = 1 -nierfunctiestoornis n = 1
|
Niet-gepubliceerde data
|
|
Gorson (2006) |
Studie type Hospital-based
Setting Retrospectieve studie van diabetes patienten met PNP 1999-2004
Land USA
Financiering Niet vermeld
|
Aantal deelnemers n= 103
Leeftijd Gemiddeld 64 jaar (26-92 jaar)
Geslacht 56% man
|
Inclusie -diabetes mellitus met PNP -Symptomen zijn 3 of meer maanden aanwezig, stabiel of langzaam progressief. -sensibele klachten of milde zwakte van teen extensoren of -flexoren
Exclusie -MRC 4 of minder van de benen -Heup of armzwakte -Mononeuropathie of multipele mononeuropathieen -Plexopathie, radiculopathie of asymmetrie |
Diabetes: Serum glucose van >126 mg/dl of >200 mg/dl na 2 uur glucose tolerantie test
Symptomen en NO (vibratiezin, positiezin, aanraking en pinprick) passend bij een symmetrische PNP
EMG bevestigd: n = 103 |
Extra risicofactor naast diabetes mellitus: n = 55 (53%)
1 risicofactor: n = 29 (28%) 2 risicofactoren: n = 18 (17%) 3 risicofactoren: n = 4 (4%) 4 risicofactoren: n = 4 (4%)
|
Diabetes mellitus en: -vit B1 deficiëntie n= 10 -vit B6 deficiëntie n = 11 -monoclonale gammopathie n = 8 -hypertriglyceridemie n = 8 -toxisch (medicatie) n = 7 -alcohol n = 6 -systeemziekte n = 6 -vit B12 deficiëntie n = 4 -vit B6 intoxicatie n = 2 -nierfunctiestoornis n = 4 -infectieus n = 0 -CIDP n = 9
|
Studiecohort bestaande uit diabetes mellitus patiënten |
|
Rosenberg (2001) |
Studie type Hospital-based
Setting Statusonderzoek 1993-1997
Land Nederland
Financiering Niet vermeld
|
Aantal deelnemers n=172
Leeftijd 26–93 jaar
Geslacht Niet beschreven
|
Inclusie Nieuwe verdenking PNP bij de neuroloog, op basis van symptomen of neurologisch onderzoek passend bij PNP, na introductie van de nieuwe richtlijn.
Exclusie 2nd opinion, al eerder (gedeeltelijk) onderzocht op PNP, reeds gestelde PNP diagnose, en ‘missing follow-up data’
|
Diagnose op basis van anamnese, NO en EMG bevestiging
EMG onderzoek volgens de richtlijn, in ten minste 2 armzenuwen en 1 zenuw in het been.
EMG bevestigd n = 172 |
Extra risicofactor naast diabetes mellitus n = 0 (0%) |
nvt
|
NB onderzoek uitgevoerd in tertiair verwijzingscentrum voor HIV
|
|
Johannsen (2000) |
Studie type Hospital based
Setting KNF afdeling 1993-1999
Land Denemarken
Financiering Niet vermeld
|
Aantal deelnemers n = 135
Leeftijd Mediaan 52 jaar (20-69 jaar)
Geslacht 36.7% |
Inclusie 18-70 jaar oud, verwezen met vraagstelling PNP
Exclusie Eerder gediagnosticeerd met PNP |
‘Definite polyneuropathy’ Passend geleidingsonderzoek
EMG bevestigd n = 135
|
2 risicofactoren: n = 10 (7%)
|
Diabetes mellitus en alcohol n = 10 |
NB n = 147, echter n = 12 uitsluitend dunnevezel neuropathie, deze geëxcludeerd |
|
Beghi (1998) |
Studie type Population-based
Setting Prospectief 1990-1993
Land Italië
Financiering Consiglio Nazionale delle Richerche, Rome, and Regine Lombardia, Milan; en Telethon Italian Comittee
|
Aantal deelnemers n = 734, waarvan n = 151 diagnose ‘probable polyneuropathy’
Leeftijd Niet vermeld
Geslacht 72% vrouw
‘Probable polyneuropathy’ n = 151 Leeftijd gemiddeld 70 jaar 67% vrouw
|
Inclusie criteria ≥ 55 jaar, twee of meer symptomen van PNP
Exclusie criteria nvt |
‘Probable polyneuropathy’ Passende symptomen en ≥ 2 passende bevindingen bij neurologisch onderzoek door neuroloog
EMG bevestigd n = 0
|
Meerdere risicofactoren: n = 13 (8%)
2 risicofactoren: n = 11 (7%) 3 risicofactoren: n = 2 (1%)
|
Diabetes mellitus en: -leverziekte (niet gerelateerd aan alcohol) n = 3 -maligniteit n = 2 -alcohol n = 2 -hypothyroeïdie n = 2 -nierfunctiestoornis n = 1 -toxisch (allopurinol) n = 1 -alcohol en maligniteit n = 1 -maligniteit + toxisch (allopurinol) n = 1 |
|
|
Dyck (1993)
|
Studie type Hospital-based
Setting Cohort studie 1986
Land USA
Financiering Niet vermeld |
Aantal deelnemers n = 369, waarvan n = 171 diagnose polyneuropathie
Leeftijd Gemiddeld 64 jaar (26-92 jaar)
Geslacht 56% man |
Inclusie -diabetes mellitus -Symptomen zijn 3 of meer maanden aanwezig, stabiel of langzaam progressief. -sensibele klachten of milde zwakte van teen extensoren of -flexoren
Exclusie -
|
Polyneuropathie ≥2 symptomen passend bij polyneuropathie; afwijkend kwantitatief sensibel onderzoek, afwijkend kwantitatief autonoom onderzoek, ten minste 1 afwijking op EMG of bij kwantitatief onderzoek
EMG bevestigd: n = 103 |
Extra risicofactor naast diabetes mellitus: n = 8 (5%)
|
Diabetes mellitus en: -erfelijk n = 3 -alcohol n = 2 -Guillain-Barré syndroom n = 1 -amyloidose n = 1 -monoclonale gammopathie n = 1
|
Studiecohort bestaande uit diabetes mellitus patiënten |
Exclusietabel
|
Auteur en jaartal |
Reden van exclusie |
|
Bruce (2008) |
Gaat over risicofactoren voor diabetische polyneuropathie |
|
Farhad (2016)
|
Studie kijkt niet naar dubbel/meervoudig voorkomen van risicofactoren bij polyneuropathie |
|
Franklin (1994) |
Gaat over risicofactoren voor diabetische polyneuropathie |
|
Freeman (2009) |
Review, geen nieuwe data |
|
Hughes (2004) |
Zoekt naar nieuwe risicofactoren voor polyneuropathie |
|
McLeod (1984)
|
Studie kijkt niet naar dubbel/meervoudig voorkomen van risicofactoren bij polyneuropathie |
|
Micco (2003) |
Case report, slechts gebruikt om referentielijst na te gaan |
|
Visser (2017) |
Gaat over voeding als risicofactor voor polyneuropathie |
|
Sharma (2002) |
Beantwoordt de uitgangsvraag niet. Gaat over hoeveel mensen met diabetes mellitus ook CIDP hebben, en welk effect behandeling met immunglobuline daarop heeft. |
|
Straub (1993) |
Beantwoordt niet de uitgangsvraag. Vergelijkt vitamine levels in plasma van vrouwen met diabetes mellitus met en zonder polyneuropathie. |
|
Lubec (1999) |
Ontbrekende informatie (34 (27%) met meer dan 1 oorzaak, niet vermeld welke combinaties voorkwamen); Niet bij alle patiënten hetzelfde bloed onderzoek ingezet, maar veel op indicatie gedaan |
|
Lozeron (2002) |
Beantwoordt de uitgangsvraag niet. Gaat over welke andere neuropathieen bij diabetes mellitus patiënten voorkomen (CTS, CIDP, radiculopathie, etc), niet over welke andere risicofactoren/oorzaken voor polyneuropathie bij diabetes mellitus. |
Beoordelingsdatum en geldigheid
Publicatiedatum : 05-07-2019
Beoordeeld op geldigheid : 23-08-2019
Uiterlijk in 2024 bepaalt het bestuur van de Nederlandse Vereniging voor Neurologie of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Vereniging voor Neurologie is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Het doel van de richtlijn is het verbeteren van de zorg voor patiënten met polyneuropathie, met name betere diagnostiek naar de oorzaak van subacute en chronische polyneuropathie.
Doelgroep
De richtlijn is primair bedoeld voor neurologen en patiënten, maar kan ook gebruikt worden door huisartsen en andere beroepsgroepen die te maken hebben met patiënten met polyneuropathie, zoals internisten, anesthesiologen en revalidatieartsen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is een werkgroep ingesteld, bestaande uit neurologen, AIOS neurologie en een patiëntenvertegenwoordiger.
De werkgroepleden zijn door hun beroepsvereniging gemandateerd voor deelname.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Prof. dr. N.C. (Nicolette) Notermans, neuroloog, Universitair Medisch Centrum Utrecht, NVN (voorzitter)
- C. (Charlotte) van Esch, MSc, medewerker kwaliteit van zorg, Spierziekten Nederland
- Dr. C. (Camiel) Verhamme, neuroloog/klinisch neurofysioloog, Academisch Medisch Centrum Amsterdam, NVN
- Prof. dr. P.A. (Pieter) van Doorn, neuroloog, Erasmus MC Rotterdam, NVN
- Prof. dr. C.G. (Karin) Faber, neuroloog, Maastricht UMC+, NVN
- Drs. X.L. (Xenia) Stalpers, neuroloog, Máxima Medisch Centrum, Eindhoven/Veldhoven, NVN
- Dr. M. (Marijke) Eurelings, neuroloog, Spaarnegasthuis Haarlem/Hoofddorp, NVN
- Dr. F. (Filip) Eftimov, neuroloog, Academisch Medisch Centrum, Amsterdam, NVN
- Dr. A.F.J.E. (Alexander) Vrancken, neuroloog, Universitair Medisch Centrum Utrecht, persoonlijke titel
- Dr. I.W.M. (Inge) van Uden, AIOS neurologie, Radboud Universitair Medisch Centrum Nijmegen, NVN
- Dr. K. (Karlien) Mul, AIOS neurologie, Radboud Universitair Medisch Centrum Nijmegen, NVN
- I.J.T. (Ingrid) Herraets, MSc, AIOS neurologie, Elisabeth-Tweesteden ziekenhuis Tilburg , NVN
Met dank aan:
- Dr. H.S. (Stephan) Goedee, neuroloog en klinisch neurofysioloog, UMC Utrecht
- Dr. W.G.M. (Wim) Jansen, revalidatiearts, Erasmus MC Rotterdam
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten. Aangezien de richtlijn met name diagnostiek van polyneuropathie en de behandeling van onderliggende oorzaken van polyneuropathie omvat, werden genoemde nevenfuncties niet als conflicterende belangen beschouwd en is er geen actie ondernomen.
|
Werkgroeplid |
Gemelde nevenfuncties en mogelijke belangen |
|
van Doorn |
|
|
Eftimov |
|
|
van Esch |
|
|
Eurelings |
|
|
Faber |
|
|
Herraets |
|
|
Mul |
|
|
Notermans |
|
|
Stalpers |
Geen |
|
van Uden |
Geen |
|
Verhamme |
|
|
Vrancken |
|
Inbreng patiëntenperspectief
Patiënten met diverse typen polyneuropathieën waren aanwezig bij de invitational conference bij de initiatie van de huidige richtlijn. Een verslag hiervan (zie aanverwante producten) is besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de richtlijn. Tevens heeft een medewerker van Spierziekten Nederland actief geparticipeerd in de werkgroep en waar nodig ruggenspraak gehouden met de achterban. Dit lid van de werkgroep heeft tevens het module Organisatie van Zorg gecoördineerd.
Patiëntenvertegenwoordigers hebben tijdens de invitational conference aangegeven dat zij de volgende aspecten van belang vinden:
- Vaststellen van behandelbare oorzaken van polyneuropathie
- De behandeling van neuropathische pijn. Tijdens de invitational conference werd besproken dat neuropathische pijn niet binnen de herziening van de richtlijn valt. Wel zal in de module over behandeling een korte samenvatting van de behandeling van neuropathische pijn worden gegeven
- Beschrijven wanneer verwijzing naar de revalidatiearts zinvol is;
- Bijdragen aan kennis over dunnevezelneuropathie en de onderliggende oorzaken, zodat een behandelplan kan worden opgesteld.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. De implementatietabel is te vinden bij de afzonderlijke modules.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door verschillende partijen in de invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Niet alle uitgangsvragen leenden zich voor een systematische literatuuranalyse. Voor de vragen waarvoor wel een systematische literatuuranalyse is gedaan, zijn de individuele studies systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. Voor beoordeling van de RoB zijn de ACROBAT-NRS – voor observationeel onderzoek en QUADAS II – voor diagnostisch onderzoek gebruikt.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en de generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken wetenschappelijke vereniging en patiëntenorganisatie voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Zoekverantwoording
1 exp *Polyneuropathies/ or polyneuropath*.ab,ti. or exp Diabetic Neuropathies/ or 'peripheral neuropath*'.ab,ti. (67947)
2 exp Diabetes Mellitus/ or diabet*.ab,ti. or alcohol*.ab,ti. (948191)
3 1 and 2 (25725)
4 (medication* or (vitamin adj2 defic*) or 'renal disease' or inflamm* or heredit* or inherit* or vasculitis or 'risk factor*' or etiolog*).ab,ti. (2063054)
5 3 and 4 (4091)
6 limit 5 to (dutch or english) (3571)
7 (cause* or etiolog* or 'work-up' or riskfactor* or 'risk factor*' or suggestive).ti. (394207)
8 6 and 7 (417)
