Diagnostiek van overgewicht en obesitas bij volwassenen
Uitgangsvraag
Hoe herkennen we onderliggende oorzaken van overgewicht of obesitas?
Aanbeveling
- Vraag toestemming aan de cliënt/patiënt om het overgewicht te bespreken.
- Ga na welke onderliggende oorzaken en/of gewicht verhogende en/of in standhoudende factoren ten grondslag liggen aan het overgewicht (zie module ‘Gepersonaliseerde zorg’ hoe dit in kaart gebracht kan worden).
- Denk hierbij aan de volgende categorieën van oorzaken en factoren: leefstijl, sociaal-economisch, psychisch, medicamenteus, hormonaal, hypothalaam en/of (mono)genetisch. Optimaliseer of behandel deze oorzaken en factoren waar mogelijk, bij voorkeur voorafgaande aan de leefstijlbegeleiding of andere geïndiceerde obesitasbehandeling.
- Bepaal het gewichtsgerelateerde gezondheidsrisico (GGR) (zie ‘Tabel 2 in de startpagina’):
- Bepaal de body mass index (kg/m2) en meet de buikomvang. Houd hierbij rekening met lichaamssamenstelling en vetverdeling en verricht indien mogelijk metingen om deze te bepalen (zie module ‘Uitkomstmaten’). Houd hierbij rekening met obesitas- gerelateerde comorbiditeiten.
- Overweeg gericht onderzoek bij verdenking op comorbiditeiten die kunnen samenhangen met obesitas en aanvullend onderzoek behoeven (zie module ‘Obesitas-gerelateerde comorbiditeiten’). Dit is een taak van een arts.
- Na deze diagnostische fase:
- Bespreek intrinsieke motivatie en mogelijkheden (ook op het gebied van zelfmanagement).
- Stel gezamenlijk met de cliënt/patiënt een behandelplan op (zie module 'Gepersonaliseerde zorg’).
- Breng voor het individu relevante uitkomstmaten in kaart voor de start van de behandeling (zie module ‘Uitkomstmaten’).
- Zorg dat een behandeling gestart wordt die toegespitst is op het individu (zie module ’Gepersonaliseerde zorg’).
Overwegingen
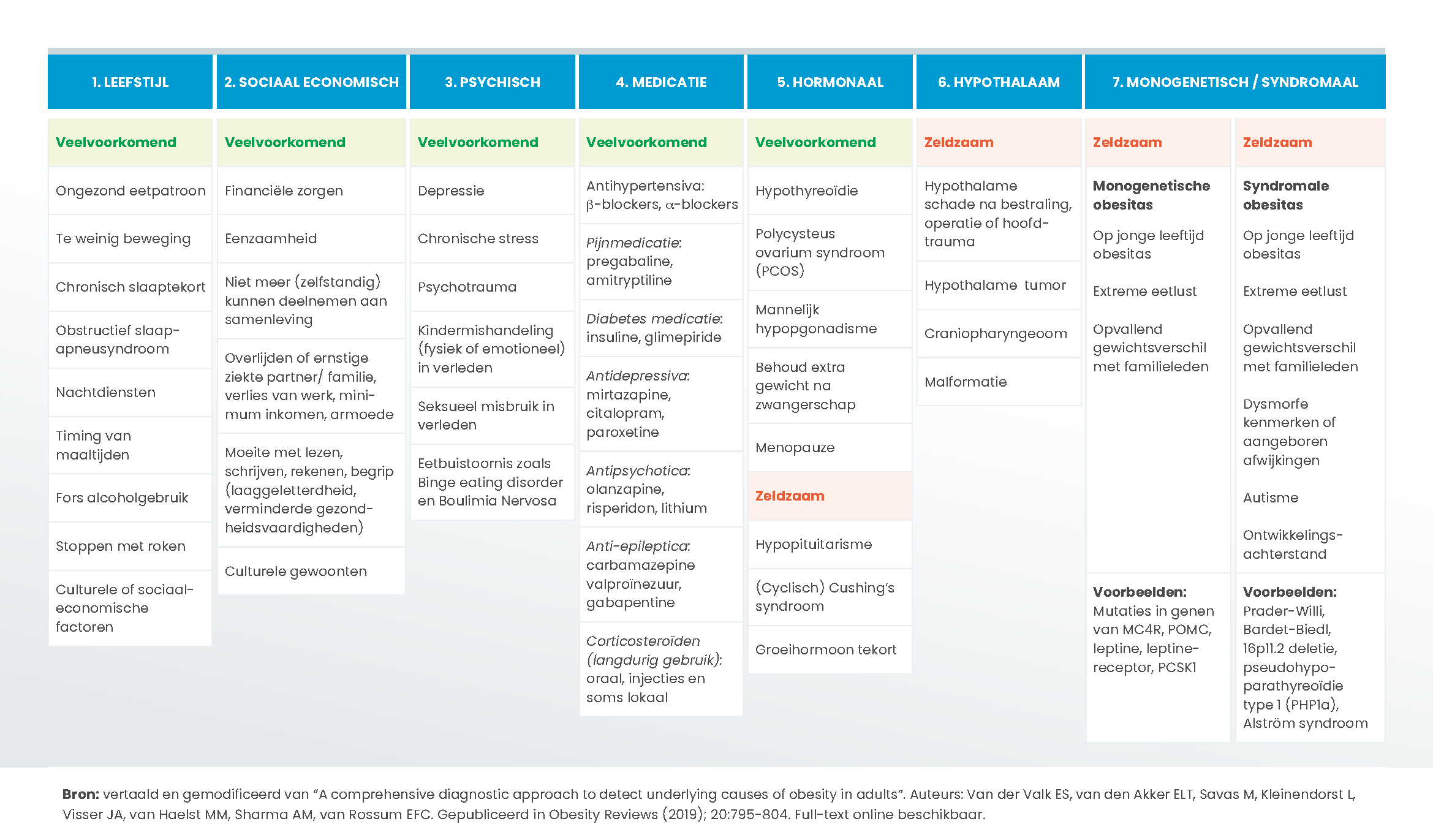
Obesitas is een chronische complexe ziekte met multiple symptomen en multifactoriële oorzaken. Niet alleen een ongezonde leefstijl kan overgewicht of obesitas veroorzaken, maar ook andere oorzaken en bijdragende factoren spelen vaak een rol. Daarnaast zijn er tal van factoren die afvallen juist tegenwerken en het overgewicht daarmee in stand houden. Al deze factoren zijn grofweg te verdelen in zeven categorieën: leefstijl, sociaal-economisch, psychisch, medicamenteus, hormonaal, hypothalaam, of genetisch (Tabel 1.2). Het is daarom belangrijk dat hulp-/zorgverleners ook aandacht geven aan onderliggende oorzaken en in stand houdende factoren voor men start met behandeling.
Klinische beoordeling
1. Toestemming
Zorgverleners spelen een belangrijke rol in de diagnostiek en behandeling van obesitas. De benadering, communicatie en houding van een zorgverlener speelt een significante rol in het succes van de behandeling van de patiënt. Veel patiënten met obesitas hebben een vorm van gewichtsdiscriminatie ervaren in een klinische setting (Puhl, 2014; Smigelski-Theiss, 2017; Rubino, 2020). Dit komt deels door het stimuleren van negatieve aannames met betrekking tot obesitas, misinformatie over de causaliteit en onderliggende factoren van obesitas. Als gevolg hiervan voelen veel patiënten met obesitas zich gediscrimineerd waardoor zij vaak vermijden hulp of een behandeling te zoeken wat tevens de mogelijkheden tot preventie beperkt (Hunte, 2009).
Het is van belang dat zorgverleners hun klinische beoordeling met betrekking tot obesitas uitvoeren op een empathische en niet-oordelende manier. Een eerste stap in de beoordeling en behandeling van patiënten is daarom het vragen van toestemming om het onderwerp met de patiënt te bespreken. Een ondersteunende omgeving met passende apparatuur en het vragen van toestemming om patiënten te wegen helpen het comfort en de waardigheid van de patiënt te bevorderen. Stigmatisering van patiënten leidt tot verslechterde resultaten met betrekking tot het opvolgen van leefstijladviezen door onder andere een risico op het bevorderen van verstoord eetgedrag, verhogen van het percentage patiënten dat depressieve symptomen ervaart en het verlagen van lichamelijke activiteit (Puhl, 2009). Het personaliseren van de diagnostiek en behandeling van patiënten met obesitas zijn belangrijke factoren die een positief effect hebben op de patiënten om langdurige veranderingen aan te brengen met betrekking tot de ontwikkeling van een gezonde leefstijl (WHO, 2000).
2. BMI en lichaamssamenstelling
Meet lengte, gewicht en buikomvang en bereken de body mass index (BMI)(kg/m2)(zie voor afkappunten tabel 12.1 in de module ‘Uitkomstmaten’). Houd hierbij rekening met de lichaamssamenstelling en vetverdeling (zie ook paragraaf lichaamssamenstelling in deze module). De volgende stappen bestaan uit het achterhalen van de onderliggende oorzaken en bijdragende factoren en het bepalen van de ernst van het overgewicht.
3. Onderliggende oorzaken en bijdragende factoren van obesitas
In de diagnostiek van overgewicht en obesitas zal in kaart gebracht moeten worden welke mogelijke factoren aanwezig zijn die invloed hebben op het ontstaan/bestaan van het overgewicht en obesitas (Tabel 1.2). De uitkomst van deze diagnostiek is de basis voor de invulling van de gepersonaliseerde zorg: het individuele behandelplan (zie module ‘Gepersonaliseerde zorg’). Ook dient er aandacht te zijn voor de soort obesitas zoals mogelijke sarcopenie bij de obesitas of een uitgesproken centrale vetverdeling, wat veelal duidt op overmatige hoeveelheid viscerale vetmassa.
Leefstijl factoren
Het is belangrijk om na te gaan of er bij een individu sprake is van leefstijl gerelateerde factoren als oorzaak van obesitas. Een ongezonde leefstijl, waarbij er teveel en/of te ongezond gegeten wordt en te weinig bewogen, is een veel voorkomende oorzaak. Een voedingspatroon dat onvoldoende verzadigt en voldoening geeft, leidt ook tot fysieke en bovendien psychische deprivatie en draagt daarmee bij aan de ontwikkeling van eetbuien (Herman,1999; Veenstra, 2010; Chandon, 2015; De Wit Huberts, 2013; Kristeller). Bij veel mensen is een ongezonde leefstijl niet de enige oorzaak, maar is ook sprake van een combinatie met bijkomende psychische, medicamenteuze en/of hormonale oorzaken of in stand houdende factoren. De leefstijl kan door vele zaken worden beïnvloed. Belangrijke elementen zijn onder meer schuldenproblematiek, nachtdiensten, crashdiëten, te weinig of slechte kwaliteit slaap en sedentaire leefstijl.
Sommige patiënten zijn misschien niet in staat om gewichtsmanagement te prioriteren door problemen met hun financiën, relatie of andere omstandigheden waar hun aandacht op is gevestigd. Ook hebben niet alle mensen voldoende gezondheidsvaardigheden of voedselkennis om de gezonde keuzes te maken (Ball, 2006). Het gebruik van een zeer lage calorische (crash) voeding leidt mogelijk tot een toename in hongergevoel of eetlust en een verlaging van het rustmetabolisme, hetgeen op termijn kan resulteren in gewichtstoename, ook wel bekend als het jojo-effect. Gewichtstoename die volgt na het stoppen met een dergelijk zeer lage calorische voeding is mogelijk geassocieerd met een disbalans in de honger-hormonen (zoals ghreline) en verzadigingshormonen (zoals leptine en petide YY). Uit onderzoek bleek dat deze disbalans in de eetlustregulatiehormonen langdurig kan aanhouden. Een jaar na het beëindigen van een zeer laag-calorische voeding bleek er nog steeds sprake was van een verstoorde balans (Heymsfield, 2007; Sumithran, 2011).
Ook een verminderde hoeveelheid of kwaliteit van slaap kan leiden tot gewichtstoename (Cappuccio, 2008), door een verlangen naar calorierijk voedsel en een disbalans van eetlust hormonen (zoals ghrelin en leptine) (Bayon, 2014), of hogere cortisol spiegels door verhoogde hypothalamus-hypofyse- activiteit van de bijnier-as (Minkel, 2014; Manenschijn, 2011; van der Valk, 2018). Circadiane ritmestoornis, zoals bijvoorbeeld door ploegenarbeid, wordt ook geassocieerd met een verminderd dagelijks energieverbruik en verhoogde calorie-inname (Broussard; 2016; Mc Hill, 2017). Obstructief-slaapapneusyndroom (OSAS) is eveneens van invloed op de slaap kwaliteit. Dit komt in hogere mate voor bij patiënten met obesitas en leidt ook tot verstoring van de slaap, die wederom mogelijk tot hierboven beschreven gedrag, metabole of hormonale veranderingen leidt (St-Onge, 2014). Het is nog onbekend of behandeling van OSAS een effect heeft op lichaamsgewicht. Tenslotte is sedentaire leefstijl nog een belangrijke bijdragende factor aan een verminderd metabolisme (Myers, 2017).
Sociaal-economische factoren
Sociaal-economische positie (SEP) is een belangrijke factor die verband houdt met obesitas. SEP kan worden bepaald aan de hand van variabelen zoals opleiding, inkomen en beroep (Anekwe, 2020). De sociale situatie is medebepalend voor het ontstaan van overgewicht. Zo kunnen armoede, slechte huisvesting, gebrekkige gezondheidsvaardigheden, slechte werkomstandigheden en ook werkloosheid en financiële onzekerheid leiden tot een ongezonde leefstijl (RVS, 2021; van Rossum, 2022). Ook kan een lage SEP via psychosociale stress een ongunstig effect hebben op het gewicht (Cuevas, 2020; Kwarteng, 2017). Er zijn grote verschillen in gezondheid tussen mensen met een laag en hoog inkomen. In de spreekkamer is aandacht voor deze kwetsbare groepen belangrijk. Ook wordt leefstijl mede bepaald door andere sociale en culturele invloeden. Soms worden ongezonde keuzes bijvoorbeeld gestimuleerd doordat bepaalde voedsel- en drinkgewoontes de sociale norm van een groep zijn en/of saamhorigheid bieden.
Psychische factoren
Het is ook belangrijk oog te hebben voor psychische factoren. Het verband tussen gewichtstoename en psychische aandoeningen is complex en wordt nog niet volledig begrepen (Taylor, 2012). Wel is bekend dat dit verband in twee richtingen werkt (Milaneschi, 2010, Avila, 2015), zoals duidelijk is aangetoond bij de combinatie obesitas en depressie (Milaneschi, 2019). Het is daarom belangrijk dat zorgverleners zich bewust zijn van het feit dat psychische en psychiatrische aandoeningen kunnen leiden tot gewichtstoename en andersom dat mensen als gevolg van gewichtsproblemen psychische en psychiatrische aandoeningen en problemen ontwikkelen.
Depressie
Verschillende studies laten zien dat depressie op bidirectionele wijze is gelinkt aan obesitas (Milaneschi, 2019; Faith, 2010; de Wit, 2010). Verschillende klinische en epidemiologische studies rapporteren een prevalentie van 20-50% van de volwassenen met overgewicht of obesitas die depressie ervaren (Goldstein, 2013; Avila, 2015; Taylor, 2020).
Eetbuistoornissen
Er zijn verschillende studies geweest die een associatie hebben gevonden tussen overgewicht en obesitas en eetbuistoornissen (Kivimakäki 2018; Taylor, 2012; Taylor, 2020). Een eetbuistoornis wordt onder andere gekenmerkt door terugkerende eetbuien. Dit zijn episodes waarin meer voedsel wordt geconsumeerd dan voor de meeste mensen normaal is en waar gevoelens van gebrek aan controle en angst een rol spelen.
Voor diagnostiek van eetstoornissen die gepaard kunnen gaan met een obesitas zoals een eetbuistoornis (binge eating disorder) of boulimia nervosa verwijzen we naar de betreffende richtlijnen (zie Zorgstandaard Eetstoornissen). Naast de DSM- criteria van BED ervaren veel mensen met overgewicht eet- en gewichtsproblemen die niet onder deze criteria vallen, maar relevant zijn bij de diagnostiek. Denk aan occupatie met gewicht en uiterlijk, te laag of onrealistisch streefgewicht, frequent lijnverleden, eetbuien en/of een verstoord eetpatroon, eten om emoties te reguleren, verstoring of inperking van het psychosociaal functioneren. Er zijn aanwijzingen dat een eetbuistoornis ook het vasthouden van verloren gewicht in de weg kan staan (Kantilafti, 2021). Soms kan er aan een eetbuistoornis een verstoring van het homeostatisch eetlustregulatiesysteem ten grondslag liggen, waarbij mensen een verminderd/geen gevoel van verzadiging ervaren. Een andere mogelijkheid is dat er onvoldoende bewustzijn is van hoe men zich verhoudt tot gedachten, gevoelens en verlangens rondom eten (zie Zorgstandaard Eetstoornissen).
Stress
Er is toenemend bewijs dat chronische stress via onder andere een verhoging van het cortisol zou kunnen leiden tot meer eetlust en bijdragen aan abdominale obesitas (van der Valk, 2018; Tamashiro, 2011; van der Valk, 2021).
Psychotraumata
Ernstige negatieve ervaringen in de kindertijd kunnen het risico op obesitas op volwassen leeftijd aanzienlijk verhogen. Dit kunnen bijvoorbeeld diverse vormen van mishandeling zijn. Seksueel misbruik is ook een risicofactor geassocieerd met obesitas (Fuemmeler, 2009). Een verleden van misbruik en huidig misbruik kan een barrière zijn tot obesitas beheersing en kan een impact hebben op voedsel gedrag en relatie met eten (Rueda-Clausen, 2020). Ook andere psychotraumata in de volwassenheid kunnen bijdragen aan gewichtstoename (Avila, 2015).
Medicamenteuze factoren
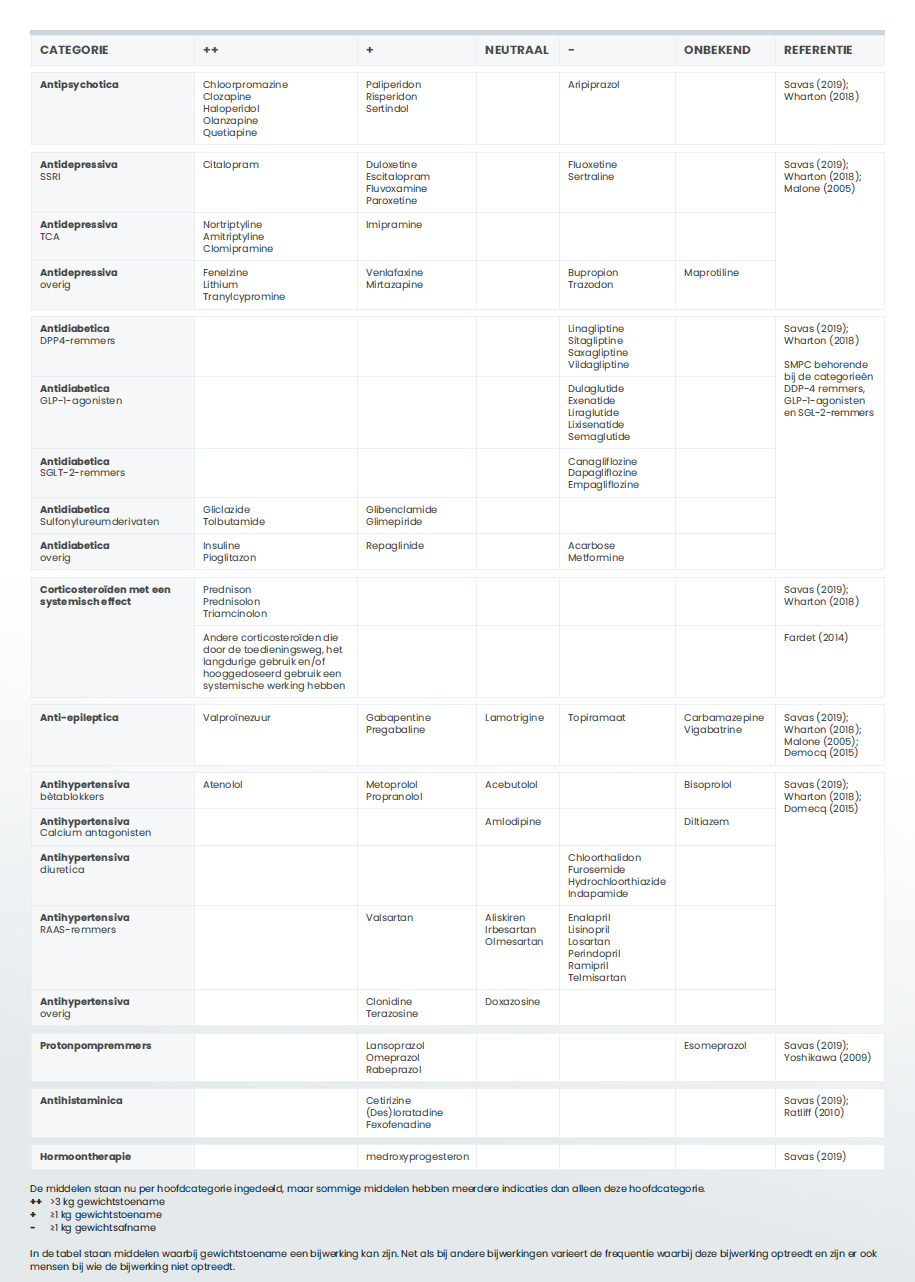
Het is ook van belang om na te gaan of er sprake is van het actueel of eerder gebruik van medicatie met een potentieel gewicht verhogende bijwerking. Hiervoor kan een medicatiebeoordeling of medicatie-evaluatie worden uitgevoerd. Medicatie kan de energiehomeostase beïnvloeden door bijvoorbeeld het bevorderen van honger, door het metabolisme in rust te verminderen of door lichaamsbeweging te belemmeren . Indien mogelijk kan het in sommige gevallen nuttig zijn om medicatie te wijzigen in een alternatief zonder gewichtsverhogende bijwerking. Het stoppen of afbouwen van deze medicatie zou kunnen resulteren in gewichtsvermindering of de gunstige effecten van een overgewicht of obesitasbehandeling minder belemmeren. Een grondige uitvraag van medicijngebruik moet daarom meer inzicht geven in het gebruik medicijnen met een potentieel gewicht verhogende werking en in welke mate de patiënt dit ervaart. Overweeg waar mogelijk alternatieve opties voor deze medicatie. De meest voorkomende potentieel gewicht verhogende medicijnen zijn weergegeven in tabel 1.1. De middelen staan nu per hoofdcategorie ingedeeld, maar sommige middelen hebben meerdere indicaties dan alleen deze hoofdcategorie.
De wijze waarop en de mate waarin deze medicamenten bijdragen aan gewichtstoename verschillen per middel. Zo kunnen sommige antidepressiva en antipsychotica de eetlust stimuleren en/of stofwisseling vertragen (Savas, 2019; Wharton, 2018; Malone, 2005). Gewichtstoename bij corticosteroïden ontstaat door onder andere een toename van de adipogenese van centraal vet, toename lipolyse en afname lipoproteine lipase activiteit in perifeer vet (Fardet 2014). Daarnaast kan er sprake zijn van een stimulatie van eetlust, vertraagde stofwisseling, en het vasthouden van vocht. Vooral langdurig gebruik van corticosteroïden is geassocieerd met significante gewichtstoename.
Hormonale factoren
Hypothyreoïdie
Een plotselinge gewichtstoename kan wijzen op een neuro-endocriene oorzaak. Vaak wordt er gescreend op hypothyreoïdie, omdat hiervan bekend is dat dit gepaard gaat met een bescheiden gewichtstoename. Dit wordt vooral aanbevolen als patiënten ook andere symptomen rapporteren zoals overmatige kouwelijkheid, obstipatie, trage hartslag of droge huid. De gewichtstoename als gevolg van hypothyreoïdie lijkt echter voornamelijk het gevolg te zijn van extra oedeem (Laurberg, 2012; van der Valk, 2019). Obesitas wordt zelf ook vaak geassocieerd met een licht verhoogde TSH spiegel in het bloed. Het verhoogde TSH kan onder andere worden verklaard door de aanwezigheid van perifere schildklierhormoon weerstand en verhoogde spiegels van leptine, stimulerend TRH en vervolgens TSH (Sanyal, 2016; van der Valk, 2019). Gewichtsverlies keert dit proces om en zal veelal leiden tot een verbetering van deze vorm van hyperthyrotropinemie (Reinehr, 2006), waarbij het gebruik van schidklierhormoonsuppletie in het algemeen niet nodig is.
Syndroom van Cushing
Het syndroom van Cushing omvat een grote groep symptomen die verband houden met een langdurige hoge blootstelling van weefsel aan glucocorticoïden. De meest voorkomende oorzaak van het syndroom van Cushing is iatrogeen als gevolg van medisch voorgeschreven corticosteroïden (Nieman, 2008; Savas, 2017; van der Valk, 2018). De zeldzame endogene vorm van het syndroom van Cushing, wordt meestal veroorzaakt door een hypofyse adenoom (Ziekte van Cushing), en in de minderheid van de gevallen door een bijnieradenoom of - nog zeldzamer - ectopische ACTH productie. Europese populatiestudies rapporteerden een incidentie van de Ziekte van Cushing van twee tot drie gevallen per 1 miljoen inwoners per jaar (Etxabe, 1994; Lindholm, 2001). Specifieke symptomen van het syndroom van Cushing zijn het gemakkelijk ontstaan van blauwe plekken, een rond en opgeblazen gezicht met rode blosjes, proximale myopathie en paarse striae (Nieman, 2008). Volwassenen met obesitas laten ook vaak minder specifieke symptomen zien die ook vaak voorkomen bij het syndroom van Cushing waaronder centrale obesitas, vermoeidheid, hyperglycemie, hoge bloeddruk en een verminderd libido (van der Valk, 2018).
Polycysteus Ovarium Syndroom
Polycysteus Ovarium Syndroom (PCOS) is een andere endocriene aandoening die een bidirectionele relatie heeft met obesitas. PCOS omvat meerdere factoren waaronder klinisch of biochemisch hyperandrogenisme, oligo-ovulatie of anovulatie en polycysteuze eierstokken (Al Wattar, 2021). Details omtrent de diagnostiek van PCOS en de internationale criteria hiervoor kunnen gevonden worden in de ''International evidence-based guideline for the assessment and management of polycystic ovary syndrome 2018’’.
Voor meer informatie omtrent PCOS verwijst de werkgroep naar de richtlijn Behandeling vruchtbaarheidsproblemen bij PCOS.
Mannelijk hypogonadisme
Mannelijk hypogonadisme heeft een complexe, bidirectionele relatie met obesitas. Het kan zowel oorzaak als gevolg zijn. Indien mannen met obesitas tekenen hebben passend bij hypogonadisme, verdient het aanbeveling om testosteron in bloed te bepalen (Pasquali, 2020). Bij patiënten met obesitas of diabetes met een duidelijk tekort aan testosteron (bij herhaling een te laag vrij testosteron en seksuele klachten) kan testosterontherapie in een verbetering van de lichaamssamenstelling en componenten van het metabool syndroom resulteren (Saad, 2015; Corona, 2016), maar het bewijs is momenteel nog te beperkt om testosteronsuppletie te duiden als een gewicht reducerend middel (Bhasin, 2018). In het algemeen is testosteronsuppletie bij mannen met name aangewezen als er sprake is een van primair (hypergonadotroop) hypogonadisme, waarbij het lage testosteron veroorzaakt wordt door een testiculaire aandoening en zo kan hebben bijgedragen aan gewichtstoename. Bij obesitas is de situatie meestal omgekeerd en wordt het (hypogonadotroop) hypogonadisme juist zeer frequent geïnduceerd door de te grote hoeveelheid vetmassa (Bhasin, 2018). Een gezond voedings- en bewegingspatroon en gewichtsreductie op andere manieren kunnen ervoor zorgen dat het hypogonadisme volledig normaliseert als gevolg van een toename in gebonden en ongebonden testosteronniveaus (Corona, 2013, Fernandez 2019).
Zwangerschap en menopauze
Vrouwen kunnen persisterende gewichtstoename ervaren na de zwangerschap of menopauze. Gewichtstoename tijdens de zwangerschap en het beperkte gewichtsverlies of een gebrek aan gewichtsverlies na de zwangerschap verhoogt het risico op lange termijn op obesitas, of het risico op toename van BMI (Piccinini-Vallis, 2020). De gemiddelde gewichtsverandering tussen het gewicht preconceptie en het eerste jaar postpartum wordt gedefinieerd als postpartum gewichtsbehoud. Dit gewichtsbehoud is over het algemeen heel gering (0,5 tot 1,5 kg), maar er is grote variabiliteit. Bij 13% tot 20% van de vrouwen is sprake van een postpartum gewichtsbehoud van 5 kg of meer (Gunderson, 2009).
Menopauze wordt ook vaak genoemd als bijdragende factor voor vrouwen. Hoewel experimentele data suggereren dat de sterk verlaagde oestrogeenproductie geassocieerd is met accumulatie van buikvet, suggereert epidemiologisch bewijs dat een gestage gewichtstoename van 0,5 kg per jaar met name te wijten is aan de biologische leeftijd in plaats van de menopauze zelf (Davis, 2012).
Overige endocriene oorzaken
Bij patiënten bij wie sprake is van een voorgeschiedenis met een hypofysetumor of andere hypofyse aandoening, operatie of bestraling in het hypofysaire gebied, ernstig hoofdtrauma of bewijs van andere hypofysehormoondeficiënties, is endocriene evaluatie geïndiceerd inclusief groeihormoon deficiëntie (Molitch, 2011). Groeihormoon deficiëntie kan, net als uitval van de hypofyse-schildklier as en hypofyse-gonaden as, bijdragen aan obesitas. Hiervoor zijn behandelopties beschikbaar (Maison, 2004; Cenci, 2008).
Hypothalame factoren
Hypothalame obesitas kan optreden na verschillende aandoeningen of behandelingen die leiden tot schade aan de hypothalame regio. Hypothalame obesitas wordt onder andere waargenomen bij patiënten met abnormaliteiten in de hypothalame regio zoals craniofaryngeoom (vooral na een operatie), inflammatoire processen zoals sarcoïdose en tuberculose, vasculaire schade, hoofdtrauma met bewustzijnverlies, of na craniale radiotherapie (Bereket, 2012). In ernstige gevallen kan deze schade aan de hypothalame regio leiden tot meerdere endocriene symptomen zoals verminderde voortplantingsfunctie met amenorroe of impotentie door uitval van de hypothalamus-hypofyse-gonaden as, diabetes insipidus en centrale hypothyreoïdie of bijnierinsufficiëntie. Ook neurologische symptomen kunnen worden gezien, waaronder convulsies, onderkoeling of hyperthermie, of slaperigheid (Lee, 2009).
Kenmerken van een hypothalame oorzaak van obesitas zijn, naast het rapporteren van een mogelijk beschadigend event in de voorgeschiedenis, onder andere het bestaan van hyperfagie, ofwel extreem hongergevoel en/of het ontbreken van een verzadigingsgevoel, insuline- en leptineresistentie en/of een verlaagd metabolisme (Roth, 2015).
Genetische factoren
Polygenetische factoren
De genetica van obesitas is erg complex. Of iemand obesitas ontwikkelt, is vaak een samenspel van enerzijds de genetische aanleg en anderzijds omgevings- en leefstijlfactoren. Grote genome-wide association studies (GWAS) hebben varianten in meerdere genen aangetoond (polygenetische factoren), die samenhangen met een hoger risico op het ontwikkelen van obesitas. Het bekendste en sterkst geassocieerde polygene obesitas gen is het FTO-gen (Ehrlich, 2016; Frayling, 2007; Dina, 2007). Deze polygene associaties zijn echter nog niet volledig opgehelderd en kunnen tot nu toe rond de 6% van de variatie in BMI verklaren (Yengo, 2018). Daarnaast zijn er steeds meer aanwijzingen dat epigenetische factoren bijdragen aan de toename van obesitas over de generaties (Bays, 2015). Mensen met een (poly)genetische aanleg kunnen door een gezonde leefstijl en gezonde leefomgeving ervoor zorgen dat ze op gezond gewicht blijven.
(Mono)genetische of syndromale factoren
Bij een klein percentage van de patiënten kan ernstige obesitas verklaard worden door een genetische variant in één specifiek gen, wat uiteindelijk leidt tot de diagnose monogenetische of syndromale obesitas (Bays, 2015). Een Nederlandse studie toonde aan dat bij volwassenen en kinderen die zich presenteerden met obesitas in een gespecialiseerd obesitascentrum, en aan specifieke criteria voldeden, het percentage mensen met een aangetoonde pathogene mutatie in een obesitas gen 3,9% was. Bij nog eens 5,4% werd een mogelijk pathogene genetische mutatie vastgesteld (Kleinendorst, 2018).
Vanwege deze lage incidentie, wordt er in de praktijk geen routinematige screening uitgevoerd op genetische oorzaken van obesitas. Er komen echter steeds meer en nieuwe behandelingen beschikbaar die zijn gericht op specifieke types van genetische obesitas, wat het belang van screening op genetische obesitas benadrukt indien hier een klinische indicatie voor is. Daarom pleit de werkgroep ervoor om te screenen op genetische obesitas in een subgroep van patiënten met een hoge klinische verdenking op deze genetische varianten.
Indicaties voor screening op genetische oorzaken van obesitas bij volwassenen zijn een combinatie van meerdere van onderstaande factoren (Kleinendorst, 2018; Farooqi, 2006; Styne, 2017) :
- Het ontwikkelen van obesitas op jonge (kinder)leeftijd.
- Hyperfagie. Naast een extreem grote eetlust, kan er ook sprake zijn van een afwezig, sterk verminderd of zeer kort aanhoudend verzadigingsgevoel.
- Opvallende gewichtsverschillen tussen gezinsleden, suggestief voor een dominante overerving (duidelijke lijn binnen de familie) of nieuw ontstane erfelijke afwijking (groot verschil met andere familieleden).
- Een intellectuele achterstand.
- Autisme spectrum stoornis
- Dysmorfe kenmerken en/of aangeboren afwijkingen.
Monogenetische obesitas
Monogene (niet-syndromale) oorzaken van obesitas worden gekarakteriseerd door een jonge leeftijd van het ontstaan van obesitas en hyperfagie (Alsters, 2016; Farooqi, 2006). In de praktijk wordt veelal een beginleeftijd van de obesitas ≤5 jaar gezien in de huidige generatie volwassenen met aangetoonde monogenetische obesitas. Tevens is er vaak een opvallend gewichtsverschil tussen patiënt en de andere gezinsleden. Andere klinische symptomen van monogenetische obesitas kunnen verschillen afhankelijk van het aangetaste gen. Bij defecten in pro-opiomelanocortine (POMC) gen zijn de symptomen rood of rossig haar, bleke huid en tekort aan adrenocorticotroop hormoon (ACTH) aanwezig. Ook sommige heterozygote variaties in het POMC gen kunnen een verhoogde gevoeligheid voor obesitas geven (Farooqi, 2006b). In het geval van melanocortine-4 receptor mutaties (MC4R) omvatten deze symptomen een versnelde lineaire groei gedurende de kinderjaren, verhoogde vetvrije massa, ernstige hyperinsulinemie en milde centrale hypothyreoïdie. In het geval van leptine deficiëntie of leptine receptor deficiëntie kan er een centrale hypothyreoïdie, hypogonadotroop hypogonadisme, frequente infecties en/of groeihormoondeficiëntie gezien worden. Bij (zeldzame homozygote) prohormoon convertase‐1 (PCSK1)-mutaties is er sprake van neonatale diarree, terugkerende hypoglykemie en globale endocriene dysfunctie (Farooqi, 2003; Farooqi, 2006).
Syndromale obesitas
Syndromale obesitas wordt ook vaak gekenmerkt door een relatief jonge beginleeftijd van obesitas, hoewel deze wel soms wat later (≤15 jaar) op kan treden dan bij een monogenetische vorm van obesitas. Andere typische kenmerken zijn: hyperfagie, intellectuele- of ontwikkelingsachterstand, autisme spectrum stoornis, gedragsproblemen, aangeboren afwijkingen en/of orgaandysfunctie. (van der Valk 2019). De meest voorkomende voorbeelden van syndromale obesitas zijn: Prader-Willi syndroom, Bardet Biedl syndroom, het 16p11.2 deletie syndroom en pseudohypoparathyreoïdie type 1 (PHP1a). Het Prader-Willi syndroom wordt gekenmerkt door hypotonie en voedingsproblemen in de neonatale periode, waarna later in het leven hyperfagie, obesitas, intellectuele achterstand, gedragsproblemen, korte lengte en hypogonadotroop hypogonadisme ontstaan (Holm, 1993). Bardet-Biedl-syndroom wordt, naast obesitas en hyperfagie, gekenmerkt door intellectuele achterstand, retinale dystrofie, polydactylie, hypogonadisme en (aangeboren) nierafwijkingen (Forsythe, 2013). Bij het 16p11.2-deletiesyndroom wordt vaak obesitas, hyperfagie, intellectuele beperkingen of ontwikkelingsachterstand (voornamelijk spraakontwikkelingsproblematiek), autisme, macrocefalie en/of epilepsie gezien (Miller, 2015). Milde verstandelijke beperking wordt ook gezien bij patiënten met PHP1a, wat veroorzaakt wordt door maternaal overgeërfde heterozygote mutaties in het GNAS gen. Inmiddels zijn er steeds meer vormen van genetische obesitas bekend, die vaak bestaan uit een combinatie van obesitas en verschillende typische kenmerken (Kaur, 2017).
Lichaamssamenstelling, vetverdeling en ondervoeding
Relatieve ondervoeding (chronisch of acuut) komt steeds vaker voor bij personen met overgewicht/obesitas en gaat gepaard met ziekte, letsel of een hoog energetisch voedingspatroon van slechte kwaliteit. Het onderliggende algemene mechanisme is een disbalans tussen de energie-inname, het energieverbruik en de kwaliteit van de voeding die niet de juiste voedingsstoffen biedt; dit heeft nadelige effecten op lichaamssamenstelling, functioneren en klinische resultaten (Cederholm, 2017). Er wordt onderscheid gemaakt in ondervoeding door een gebrek aan voedingsstoffen (door functionele, psychische en/of sociale factoren, een beperkte opname of een bewust laag calorische voeding) en verhoogd gebruik door inflammatie (gestrest metabolisme) of een combinatie daarvan.
Overmatige vetmassa, vooral in de vorm van centrale obesitas, wordt geassocieerd met een ontstekingsreactie die waarschijnlijk bijdraagt aan de toestand van ondervoeding.
Op deze wijze kunnen ondervoeding en overgewicht/obesitas gelijktijdig bestaan waardoor er sprake is van een zgn. ‘double burden’ (WHO, 2017). Door het uitvoeren van een nutritional assessment, kan vastgesteld worden of er sprake is van ondervoeding (zie sectie Nutritional Assessment). Meer over herkenning, diagnosestelling en behandeling van ondervoeding is weergegeven in de richtlijn Multidisciplinaire richtlijn Ondervoeding.
Sarcopene obesitas
Deze vorm bestaat uit obesitas in combinatie met sarcopenie, zoals bijvoorbeeld voorkomt bij oudere personen, bij Diabetes Mellitus type 2 (T2DM), COPD en bij patiënten met obesitas en kwaadaardige aandoeningen of langdurig corticosteroïdgebruik, en als gevolg van insulineresistentie. Insulineresistentie gecombineerd met bewegingsarmoede is een obesitas gerelateerde oorzaak van sarcopenie (Hong, 2020). Onderliggende mechanismen omvatten ontsteking en/of inactiviteit geïnduceerd spierkatabolisme bij patiënten met obesitas (Stenholm, 2008; Zamboni, 2008). De aandoening kan vrijwel op alle leeftijden voorkomen.
Centrale obesitas
Ophoping van intra-abdominaal vet is geassocieerd met een hoger risico op metabole en cardiovasculaire ziekten en vele andere aandoeningen (zie ook module ‘Obesitas-gerelateerde comorbiditeiten’)(WHO, 2000a; Yumuk, 2015) .
Naast een klinische inschatting bij lichamelijk onderzoek is het aan te bevelen om een ‘nutritional assessment’ uit te voeren voor de vaststelling van de betreffende lichaamssamenstelling en vetverdeling. Deze bepaling van de voedingstoestand geeft o.a. een goed inzicht in de verhouding vet- en spiermassa.
Nutritional assessment zou onderdeel moeten zijn van een volledige diagnostiek bij tal van aandoeningen en ziekten en kan ook van toegevoegde waarde zijn bij de patiënten doelgroep waarvoor deze richtlijn bedoeld is: personen met overgewicht en obesitas. Het is een onderdeel van de diëtistische diagnose zoals die door diëtisten wordt uitgevoerd bij overgewicht/obesitas.
Nutritional assessment:
Nutritional assessment is het systematisch beoordelen van de voedingstoestand en voedingsbehoefte, onderdeel van het diëtistisch onderzoek en helpt bij het vaststellen van de diagnose en het behandelplan. Op een gestructureerde wijze (subjectief en objectief) worden metingen gedaan die in te delen zijn in drie domeinen:
- voedselinname, verbruik en verliezen
- lichaamssamenstelling en nutriëntenreserves
- functionele parameters
Om uniformiteit te creëren in de uitvoering van de verschillende methodieken van nutritional assessment ontwikkelt Het Nutritional Assessment Platform (NAP) Standard Operating Procedures (SOP) (zie module ‘Uitkomstmaten’). Overige informatie over het nutritional assessment is te vinden op de website van het NAP.
Comorbiditeiten
Er zijn tal van comorbiditeiten die gepaard kunnen gaan met obesitas, zoals: cardiometabole complicaties, respiratoire aandoeningen, bepaalde vormen van kanker, gastro-intestinale ziekte, urogenitale aandoeningen, fertiliteitsproblemen, gewrichtsklachten, inflammatoire aandoeningen en psychosociale problemen. Zie hiervoor de module ‘Obesitas-gerelateerde comorbiditeiten’.
Onderbouwing
Obesitas is een chronische ziekte die een uitgebreide diagnose, klinische beoordeling en behandeling vereist (Bray, 2017). Nadat obesitas is geconstateerd bij een volwassene is het essentieel dat zorgverleners eerst inzicht krijgen in onderliggende aandoeningen en bijdragende factoren voor obesitas, voordat men start met een gepersonaliseerde behandeling van obesitas. Naast leefstijl gerelateerde factoren zijn er ook andere factoren waaronder hormonale en psychische factoren of ziekten, genetische afwijkingen, sociaalculturele en sociaal-economische factoren en bijwerkingen van medicijnen (van der Valk, 2018; Savas, 2019). Het identificeren van deze onderliggende factoren kan leiden tot meer gepersonaliseerde behandelstrategieën en kan daarnaast patiënten helpen om meer begrip te hebben voor hun obesitas en hun sociale stigma te verminderen. Naast de in deze module besproken oorzaken van obesitas, zijn er ook nog andere mogelijke oorzaken, die niet direct in de spreekkamer geadresseerd kunnen worden, zoals hormoon verstorende stoffen (“endocrine disrupting chemicals”), polygenetische oorzaken, intra-uteriene factoren en uiteraard de huidige obesogene omgeving. Deze factoren hebben we buiten beschouwing van deze module gelaten. In deze module bieden we evidence- en practice-based praktische aanbevelingen
om mogelijke onderliggende ziekten en bijdragende factoren te herkennen en op te sporen.
Introduction
Obesity is a chronic disease that requires a systematic and comprehensive diagnosis, assessment and treatment approach. After obesity is detected in adults, it is essential that clinicians first detect and address underlying diseases and contributing factors, before starting individualized obesity treatment. Besides lifestyle‐related factors, other factors include hormonal and genetic abnormalities, mental and socio‐cultural factors, and side effects of medications. Identifying these underlying factors may lead to more personalized treatment strategies, can also increase patients understanding of their obesity, and reduce their social stigma. In this module we provide evidence‐based and practice-based recommendations, to detect potential underlying diseases and contributing factors.
Not relevant
The Canadian Adult Obesity Clinical Practice Guideline (Rueda-Clausen, 2020; Taylor, 2020; Piccinini-Vallis, 2020) and relevant scientific articles were examined in order to answer the clinical question.
The Canadian Adult Obesity Clinical Practice Guideline has been developed in line with GRADE methodology. Search strategies and evidence tables are available on request. More information about the methodology is described in Wharton (2020).
- Al Wattar, B. H., Fisher, M., Bevington, L., Talaulikar, V., Davies, M., Conway, G., & Yasmin, E. (2021). Clinical Practice Guidelines on the Diagnosis and Management of Polycystic Ovary Syndrome: A Systematic Review and Quality Assessment Study. The Journal of clinical endocrinology and metabolism, 106(8), 24362446.
- Anekwe, C. V., Jarrell, A. R., Townsend, M. J., Gaudier, G. I., Hiserodt, J. M., & Stanford, F. C. (2020). Socioeconomics of Obesity. Current obesity reports, 9(3), 272279.
- Avila, C., Holloway, A. C., Hahn, M. K., Morrison, K. M., Restivo, M., Anglin, R., & Taylor, V. H. (2015). An overview of links between obesity and mental health. Current obesity reports, 4(3), 303-310.
- Bhasin, S., Brito, J. P., Cunningham, G. R., Hayes, F. J., Hodis, H. N., Matsumoto, A. M., ... & Yialamas, M. A. (2018). Testosterone therapy in men with hypogonadism: an Endocrine Society clinical practice guideline. The Journal of Clinical Endocrinology & Metabolism, 103(5), 1715-1744.
- Bayon V, Leger D, Gomez?Merino D, Vecchierini MF, Chennaoui M.Sleep debt and obesity. Ann Med. 2014;46(5):264?272.
- Bays, H., & Scinta, W. (2015). Adiposopathy and epigenetics: an introduction to obesity as a transgenerational disease. Current medical research and opinion, 31(11), 2059-2069.
- Bereket, A., Kiess, W., Lustig, R. H., Muller, H. L., Goldstone, A. P., Weiss, R., ... & Hochberg, Z. E. (2012). Hypothalamic obesity in children. Obesity Reviews, 13(9), 780-798.
- Bray, G. A., et al. "Obesity: a chronic relapsing progressive disease process. A position statement of the World Obesity Federation." Obesity reviews 18.7 (2017): 715-723.
- Broussard, J. L., & Van Cauter, E. (2016). Disturbances of sleep and circadian rhythms: novel risk factors for obesity. Current opinion in endocrinology, diabetes, and obesity, 23(5), 353.
- Cappuccio, F. P., Taggart, F. M., Kandala, N. B., Currie, A., Peile, E., Stranges, S., & Miller, M. A. (2008). Meta-analysis of short sleep duration and obesity in children and adults. Sleep, 31(5), 619-626.
- Cederholm, T., Barazzoni, R. O. C. C. O., Austin, P., Ballmer, P., Biolo, G. I. A. N. N. I., Bischoff, S. C., ... & Singer, P. (2017). ESPEN guidelines on definitions and terminology of clinical nutrition. Clinical nutrition, 36(1), 49-64.
- Cenci, M. C. P., Conceição, F. L., Soares, D. V., Spina, L. D. C., Brasil, R. R. D. L. O., Lobo, P. M., ... & Vaisman, M. (2008). Impact of 5 years of growth hormone replacement therapy on cardiovascular risk factors in growth hormonedeficient adults. Metabolism, 57(1), 121-129.
- Corona, G., Rastrelli, G., Monami, M., Saad, F., Luconi, M., Lucchese, M., ... & Maggi, M. (2013). Body weight loss reverts obesity-associated hypogonadotropic hypogonadism: a systematic review and meta-analysis. Eur J Endocrinol, 168(6), 829-843.
- Corona, G., Giagulli, V. A., Maseroli, E., Vignozzi, L., Aversa, A., Zitzmann, M., ... & Maggi, M. (2016). Testosterone supplementation and body composition: results from a meta-analysis study.
- Cuevas, A. G., Chen, R., Slopen, N., Thurber, K. A., Wilson, N., Economos, C., & Williams, D. R. (2020). Assessing the Role of Health Behaviors, Socioeconomic Status, and Cumulative Stress for Racial/Ethnic Disparities in Obesity. Obesity (Silver Spring, Md.), 28(1), 161170.
- Dallman, M. F. (2010). Stress-induced obesity and the emotional nervous system. Trends in Endocrinology & Metabolism, 21(3), 159-165.
- Davis, S. R., Castelo-Branco, C., Chedraui, P., Lumsden, M. A., Nappi, R. E., Shah, D., ... & Writing Group of the International Menopause Society for World Menopause Day 2012. (2012).
- De Wit, L., Luppino, F., van Straten, A., Penninx, B., Zitman, F., & Cuijpers, P. (2010). Depression and obesity: a meta-analysis of community-based studies. Psychiatry research, 178(2), 230-235.
- Dina, C., Meyre, D., Gallina, S., Durand, E., Körner, A., Jacobson, P., ... & Froguel, P. (2007). Variation in FTO contributes to childhood obesity and severe adult obesity. Nature genetics, 39(6), 724-726.
- Ehrlich, A. C., & Friedenberg, F. K. (2016). Genetic associations of obesity: The fat-mass and obesity-associated (FTO) gene. Clinical and translational gastroenterology, 7(1), e140.
- Etxabe, J. V. J. A., & Vazquez, J. A. (1994). Morbidity and mortality in Cushing's disease: an epidemiological approach. Clinical endocrinology, 40(4), 479-484.
- Faith, M. S., Butryn, M., Wadden, T. A., Fabricatore, A., Nguyen, A. M., & Heymsfield, S. B. (2011). Evidence for prospective associations among depression and obesity in population?based studies. Obesity Reviews, 12(5), e438-e453.
- Farooqi, I. S. (2006). The severely obese patienta genetic work-up. Nature clinical practice Endocrinology & metabolism, 2(3), 172-177.
- Farooqi, I. S., Drop, S., Clements, A., Keogh, J. M., Biernacka, J., Lowenbein, S., Challis, B. G., & O'Rahilly, S. (2006b). Heterozygosity for a POMC-null mutation and increased obesity risk in humans. Diabetes, 55(9), 25492553.
- Fardet, L., & Fève, B. (2014). Systemic glucocorticoid therapy: a review of its metabolic and cardiovascular adverse events. Drugs, 74(15), 17311745.
- Fernandez, C. J., Chacko, E. C., & Pappachan, J. M. (2019). Male obesity-related secondary hypogonadismpathophysiology, clinical implications and management. European endocrinology, 15(2), 83.
- Forsythe, E., & Beales, P. L. (2013). Bardet-Biedl syndrome. European journal of human genetics : EJHG, 21(1), 813. https://doi.org/10.1038/ejhg.2012.115
- Frayling TM, Timpson NJ, Weedon MN et al. A common variant in the FTO gene is associated with
- Goldstein, B. I., Liu, S. M., Schaffer, A., Sala, R., & Blanco, C. (2013). Obesity and the three?year longitudinal course of bipolar disorder. Bipolar disorders, 15(3), 284-293.
- Gunderson, E. P. (2009). Childbearing and obesity in women: weight before, during, and after pregnancy. Obstetrics and Gynecology Clinics, 36(2), 317-332.
- Lindholm, J., Juul, S., Jørgensen, J. O. L., Astrup, J., Bjerre, P., Feldt-Rasmussen, U., ... & Weeke, J. (2001). Incidence and late prognosis of Cushings syndrome: a population-based study. The Journal of Clinical Endocrinology & Metabolism, 86(1), 117-123.
- Heymsfield, S. B., Harp, J. B., Reitman, M. L., Beetsch, J. W., Schoeller, D. A., Erondu, N., & Pietrobelli, A. (2007). Why do obese patients not lose more weight when treated with low-calorie diets? A mechanistic perspective. The American journal of clinical nutrition, 85(2), 346-354.
- Hong IS-H, K M Choint. Sarcopenic Obesity, Insulin Resistance, and Their Implications in Cardiovascular and Metabolic Consequences Int. J. Mol. Sci. 2020, 21, 494; doi:10.3390/ijms21020494.
- Hunte, H. E., & Williams, D. R. (2009). The association between perceived discrimination and obesity in a population-based multiracial and multiethnic adult sample. American journal of public health, 99(7), 1285-1292.
- Kantilafti, M., Chrysostomou, S., Yannakoulia, M., & Giannakou, K. (2021). The association between binge eating disorder and weight management in overweight and obese adults: A systematic literature review. Nutrition and health, 2601060211032101. Advance online publication.
- Kaur, Y., de Souza, R. J., Gibson, W. T., & Meyre, D. (2017). A systematic review of genetic syndromes with obesity. Obesity reviews : an official journal of the International Association for the Study of Obesity, 18(6), 603634.
- Kiecolt-Glaser, J. K., Fagundes, C. P., Andridge, R., Peng, J., Malarkey, W. B., Habash, D., & Belury, M. A. (2017). Depression, daily stressors and inflammatory responses to high-fat meals: when stress overrides healthier food choices. Molecular psychiatry, 22(3), 476-482.
- Kleinendorst, L., Massink, M. P., Cooiman, M. I., Savas, M., van der Baan-Slootweg, O. H., Roelants, R. J., ... & van Haelst, M. M. (2018). Genetic obesity: next-generation sequencing results of 1230 patients with obesity. Journal of medical genetics, 55(9), 578-586.
- Kwarteng, J. L., Schulz, A. J., Mentz, G. B., Israel, B. A., & Perkins, D. W. (2017). Independent Effects of Neighborhood Poverty and Psychosocial Stress on Obesity Over Time. Journal of urban health: bulletin of the New York Academy of Medicine, 94(6), 791802.
- Laurberg, P., Knudsen, N., Andersen, S., Carlé, A., Pedersen, I. B., & Karmisholt, J. (2012). Thyroid function and obesity. European thyroid journal, 1(3), 159-167.
- Lee, M., & Korner, J. (2009). Review of physiology, clinical manifestations, and management of hypothalamic obesity in humans. Pituitary, 12(2), 87-95.
- Luig, T., Anderson, R., Sharma, A. M., & Campbell?Scherer, D. L. (2018). Personalizing obesity assessment and care planning in primary care: patient experience and outcomes in everyday life and health. Clinical obesity, 8(6), 411-423.
- Macht, M. (2008). How emotions affect eating: a five-way model. Appetite, 50(1), 1-11.
- Maison, P., Griffin, S., Nicoue-Beglah, M., Haddad, N., Balkau, B., & Chanson, P. (2004). Impact of growth hormone (GH) treatment on cardiovascular risk factors in GH-deficient adults: a metaanalysis of blinded, randomized, placebo-controlled trials. The Journal of Clinical Endocrinology & Metabolism, 89(5), 2192-2199.
- Manenschijn, L., van Kruysbergen, R. G., de Jong, F. H., Koper, J. W., & van Rossum, E. F. (2011). Shift work at young age is associated with elevated long-term cortisol levels and body mass index. The Journal of Clinical Endocrinology & Metabolism, 96(11), E1862-E1865.
- McHill, A. W., & Wright Jr, K. P. (2017). Role of sleep and circadian disruption on energy expenditure and in metabolic predisposition to human obesity and metabolic disease. Obesity reviews, 18, 15-24.
- Milaneschi, Y., Simmons, W. K., van Rossum, E. F., & Penninx, B. W. (2019). Depression and obesity: evidence of shared biological mechanisms. Molecular psychiatry, 24(1), 18-33.
- Miller, D. T., Chung, W., Nasir, R., Shen, Y., Steinman, K. J., Wu, B. L., & Hanson, E. (2015). 16p11. 2 Recurrent Microdeletion.
- Minkel, J., Moreta, M., Muto, J., Htaik, O., Jones, C., Basner, M., & Dinges, D. (2014). Sleep deprivation potentiates HPA axis stress reactivity in healthy adults. Health Psychology, 33(11), 1430.
- Molitch, M. E., Clemmons, D. R., Malozowski, S., Merriam, G. R., & Vance, M. L. (2011). Evaluation and treatment of adult growth hormone deficiency: an Endocrine Society clinical practice guideline. The Journal of Clinical Endocrinology & Metabolism, 96(6), 1587-1609.
- Myers, A., Gibbons, C., Finlayson, G., & Blundell, J. (2017). Associations among sedentary and active behaviours, body fat and appetite dysregulation: investigating the myth of physical inactivity and obesity. British Journal of Sports Medicine, 51(21), 1540-1544.
- Nieman, L. K., Biller, B. M., Findling, J. W., Newell-Price, J., Savage, M. O., Stewart, P. M., & Montori, V. M. (2008). The diagnosis of Cushing's syndrome: an endocrine society clinical practice guideline. The Journal of Clinical Endocrinology & Metabolism, 93(5), 1526-1540.
- Pasquali, R., Casanueva, F., Haluzik, M., van Hulsteijn, L., Ledoux, S., Monteiro, M. P., Salvador, J., Santini, F., Toplak, H., & Dekkers, O. M. (2020). European Society of Endocrinology Clinical Practice Guideline: Endocrine work-up in obesity. European journal of endocrinology, 182(1), G1G32. https://doi.org/10.1530/EJE-19-0893
- Puhl, R. M., Luedicke, J., & Grilo, C. M. (2014). Obesity bias in training: attitudes, beliefs, and observations among advanced trainees in professional health disciplines. Obesity, 22(4), 1008-1015.
- Raad voor de Volksgezondheid & Samenleving. (2021). Een eerlijke kans op gezond leven. Publicatie 2021-04. ISBN 9789057323072.
- Reinehr, T., de Sousa, G., & Andler, W. (2006). Hyperthyrotropinemia in obese children is reversible after weight loss and is not related to lipids. The Journal of Clinical Endocrinology & Metabolism, 91(8), 3088-3091.
- Roth C. L. (2015). Hypothalamic Obesity in Craniopharyngioma Patients: Disturbed Energy Homeostasis Related to Extent of Hypothalamic Damage and Its Implication for Obesity Intervention. Journal of clinical medicine, 4(9), 17741797.
- Rueda-Clausen CF, Poddar M, Lear SA, Poirier P, Sharma AM. Canadian Adult Obesity Clinical Practice Guidelines: Assessment of People Living with Obesity. Vazquez, G., Sue, D., David Jr, R. J., & Karri, S. (2007). Comparison of Body Mass Index, Waist Circumference, and Waist/Hip Ratio in Predicting Incident Diabetes. A Meta-Analysis, 29, 1-14.
- Saad, F., Yassin, A., Doros, G., & Haider, A. (2016). Effects of long-term treatment with testosterone on weight and waist size in 411 hypogonadal men with obesity classes I-III: observational data from two registry studies. International journal of obesity, 40(1), 162-170.
- Sanyal, D., & Raychaudhuri, M. (2016). Hypothyroidism and obesity: An intriguing link. Indian journal of endocrinology and metabolism, 20(4), 554.
- Savas, M., Wester, V. L., Visser, J. A., Kleinendorst, L., van der Zwaag, B., van Haelst, M. M., van den Akker, E., & van Rossum, E. (2019). Extensive Phenotyping for Potential Weight-Inducing Factors in an Outpatient Population with Obesity. Obesity facts, 12(4), 369384.
- Savas, M., Wester, V. L., Staufenbiel, S. M., Koper, J. W., Van Den Akker, E. L., Visser, J. A., ... & Van Rossum, E. F. (2017). Systematic evaluation of corticosteroid use in obese and non-obese individuals: a multi-cohort study. International journal of medical sciences, 14(7), 615.
- Smigelski-Theiss, R., Gampong, M., & Kurasaki, J. (2017). Weight bias and psychosocial implications for acute care of patients with obesity. AACN advanced critical care, 28(3), 254-262.
- Stenholm, S., Harris, T. B., Rantanen, T., Visser, M., Kritchevsky, S. B., & Ferrucci, L. (2008). Sarcopenic obesity-definition, etiology and consequences. Current opinion in clinical nutrition and metabolic care, 11(6), 693.
- St-Onge, M. P., & Shechter, A. (2014). Sleep disturbances, body fat distribution, food intake and/or energy expenditure: pathophysiological aspects. Hormone molecular biology and clinical investigation, 17(1), 29-37.
- Styne, D. M., Arslanian, S. A., Connor, E. L., Farooqi, I. S., Murad, M. H., Silverstein, J. H., & Yanovski, J. A. (2017). Pediatric obesityassessment, treatment, and prevention: an Endocrine Society clinical practice guideline. The Journal of Clinical Endocrinology & Metabolism, 102(3), 709-757.
- Sumithran, P., Prendergast, L. A., Delbridge, E., Purcell, K., Shulkes, A., Kriketos, A., & Proietto, J. (2011). Long-term persistence of hormonal adaptations to weight loss. The New England journal of medicine, 365(17), 15971604. https://doi.org/10.1056/NEJMoa1105816.
- Tamashiro, K. L., Sakai, R. R., Shively, C. A., Karatsoreos, I. N., & Reagan, L. P. (2011). Chronic stress, metabolism, and metabolic syndrome. Stress, 14(5), 468-474.
- Taylor, V. H., McIntyre, R. S., Remington, G., Levitan, R. D., Stonehocker, B., & Sharma, A. M. (2012). Beyond pharmacotherapy: understanding the links between obesity and chronic mental illness. The Canadian Journal of Psychiatry, 57(1), 5-12.
- van der Valk, E. S., Savas, M., & van Rossum, E. F. (2018). Stress and obesity: are there more susceptible individuals?. Current obesity reports, 7(2), 193-203.
- van der Valk, E. S., van der Voorn, B., Iyer, A. M., Mohseni, M., Leenen, P. J., Dik, W. A., ... & van Rossum, E. F. (2021). Hair Cortisol, Obesity and the Immune System: Results From a 3 Year Longitudinal Study. Journal of the Endocrine Society, 5(Suppl 1), A14.
- Van Rossum, E.F.C. (2022). Gezond leven: Een gedeelde publieke én individuele verantwoordelijkheid, Bundel Taboes en Belangen in de Zorg, Nederlands Tijdschrift voor Geneeskunde, December 2022.
- Wharton, S., Raiber, L., Serodio, K. J., Lee, J., & Christensen, R. A. (2018). Medications that cause weight gain and alternatives in Canada: a narrative review. Diabetes, metabolic syndrome and obesity: targets and therapy, 11, 427.
- World Health Organization. (2017). The Double Burden of Malnutrition Policy Brief. Geneva: World Health Organization.
- World Health Organization (2000). Obesity: preventing and managing the global epidemic Report of a WHO Consultation. WHO Technical Report Series, 894.
- World Health Organization (2000a). Obesity: preventing and managing the global epidemic. World Health Organization technical report series, 894, 1-253.
- Yengo, L., Sidorenko, J., Kemper, K. E., Zheng, Z., Wood, A. R., Weedon, M. N., Frayling, T. M., Hirschhorn, J., Yang, J., Visscher, P. M., & GIANT Consortium (2018). Meta-analysis of genome-wide association studies for height and body mass index in ?700000 individuals of European ancestry. Human molecular genetics, 27(20), 36413649.
- Zamboni, M., Mazzali, G., Fantin, F., Rossi, A., & Di Francesco, V. (2008). Sarcopenic obesity: a new category of obesity in the elderly. Nutrition, Metabolism and Cardiovascular Diseases, 18(5), 388-395.
Beoordelingsdatum en geldigheid
Publicatiedatum : 10-07-2023
Beoordeeld op geldigheid : 07-07-2023
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2027 bepalen Partnerschap Overgewicht Nederland (PON) en Care for Obesity/de Vrije Universiteit Amsterdam, of de modules van deze richtlijn nog actueel zijn. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden. De geldigheid van de richtlijnmodules komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn om een herzieningstraject te starten.
Het Partnerschap Overgewicht Nederland (PON) en Care for Obesity/de Vrije Universiteit Amsterdam (C4O/VU) zijn respectievelijk regiehouder van het volwassenendeel en het kinderdeel en van de richtlijn. Daarnaast zijn ze eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van hun deel van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd door de Vrije Universiteit Amsterdam en het Ministerie van Volksgezondheid, Welzijn en Sport. De financiers hebben geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Het doel van deze richtlijn is bij te dragen aan de verbetering van de ondersteuning en zorg voor volwassenen en kinderen met obesitas of overgewicht in combinatie met risicofactoren en/of comorbiditeit. Deze richtlijn is volgens Medische Specialistische Richtlijnen 2.0 tot stand gekomen, waarin de huidige stand van wetenschappelijke kennis en praktijkervaring aangaande het onderwerp is meegenomen.
De obesitasrichtlijn is ontwikkeld in samenwerking met veel partijen (zie samenstelling werkgroepen en klankbordgroepen) en is bedoeld voor de verschillende bij de ondersteuning en zorg voor obesitas of overgewicht in combinatie met risicofactoren en/of comorbiditeit betrokken beroepsgroepen.
Deze richtlijn gaat over de diagnostiek en behandeling van volwassenen en kinderen met obesitas of overgewicht in combinatie met risicofactoren en/of comorbiditeit. Het betreft hier zorggerelateerde preventie (VWS, 2021).
Deze richtlijn richt zich op de beste diagnostiek, ondersteuning en zorg voor volwassene en kinderen met obesitas, gebaseerd op de meest recente literatuur en expert-/practice-based adviezen. Daarnaast is deze richtlijn relevant voor de geïndiceerde preventie (VWS, 2021) van obesitas bij volwassenen en kinderen. Dit betreft volwassenen en kinderen met overgewicht zonder risicofactoren en/of comorbiditeit.
Hierbij moet worden opgemerkt dat het gezondheidsrisico van overgewicht en obesitas wordt bepaald aan de hand van de BMI in combinatie met wel of geen aanwezigheid van risicofactoren en/of comorbiditeit. De BMI is ingedeeld in categorieën. Echter, de afkappunten van die categorieën zijn niet voor alle groepen precies hetzelfde. De mate van vervetting van het lichaam bij een bepaalde BMI is afhankelijk van het geslacht (vrouwen hebben een hoger vetpercentage dan mannen), de leeftijd (oudere mensen hebben een hoger vetpercentage dan jongere) en de etniciteit (mensen uit Azië hebben een hoger vetpercentage dan Europeanen). Daarnaast kunnen mensen met een grote spiermassa zoals sporters en mensen die zwaar lichamelijk werk doen een lager gezondheidsrisico hebben dan van hun BMI afgeleid kan worden met de bestaande afkappunten. Dit is de reden dat naast de BMI ook de buikomvang van groot belang is bij de bepaling van het gezondheidsrisico bij volwassenen met overgewicht of obesitas (Wharton, 2020).
Doelgroep
Deze richtlijn is primair bedoeld voor de beroepsgroepen die betrokken zijn bij de diagnostiek, ondersteuning en zorg voor volwassenen en kinderen met obesitas of overgewicht in combinatie met risicofactoren en/of comorbiditeit.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2019 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van relevante specialismen die betrokken zijn bij de ondersteuning en zorg voor kinderen en volwassenen met obesitas of overgewicht in combinatie met risicofactoren en/of comorbiditeit.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Prof. dr. E.F.C. (Liesbeth) Van Rossum, PON, voorzitter
- W. (Wytse) Brongers, KNGF
- S.A. (Sione) Brugman, BLCN – tot februari 2023
- I. (Inge) Out, BLCN – vanaf februari 2023
- B. (Bernadette) Deenen, NVD
- K. (Karen) De Leest, KNMP
- Dr. K. (Karen) Freijer, PON
- E. (Ellen) Govers, NVD
- M. (Marc) Huls, NHG
- F. (Francoise) Langens, huisarts – tot februari 2021
- R.S.L. (Ronald) Liem, NVvH
- Dr. M. (Mattijs) Out, NIV
- E.M.J.N. (Evelyn) Sloots-Jongen, NIP
- N. (Nicolette) Slot, VvOCM
- I. (Inez) van den Anker, Stichting Over Gewicht (patiëntenorganisatie)
- J. (Jacqui) van Kemenade – van Vught, NHG
Klankbordgroep
- I.R.M. (Jurriaan) Blekemolen, NVAB
- Dr. G.J. (Gert-Jan) Braunstahl, NVALT
- D.O.A. (Darie) Daemers, KNOV
- D. (Dorenda) Dijken, NVOG
- S. (Sander) Galjaard, NVOG
- Prof. dr. A. (Annemieke) Hoek, NVOG
- M.M. (Maarten) Hoogbergen, NVPC
- Y.F.C. (Yvo) Kortmann, NVMDL
- P. (Patricia) Lottman, BLCN
- N. (Nienke) van der Putten, Hartstichting
- Dr. G.A.H. (Edgar) van Mil, NVK
- Dr. T.M. (Tessa) van Elten, Voedingscentrum
- Dr. M.E. (Janneke) Wittekoek, NVvC
Met ondersteuning van
- Dr. A.N. (Anh Nhi) Nguyen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. B. (Bart) Versteeg, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Overzicht van de belangen van werkgroepleden
|
Achternaam werkgroeplid |
Hoofdfunctie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Van Rossum (voorzitter) |
Internist-endocrinoloog/ hoogleraar Gezond Gewicht en biologisch stressonderzoek in het Erasmus MC |
-Voorzitter Partnerschap Overgewicht Nederland – onbetaald (met in dat kader extra werkzaamheden zoals: *vertegenwoordiger PON bij de tafel Overgewicht voor het Nationaal Preventie Akkoord (onbetaald ) *adviseur keten/netwerkaanpak overgewicht bij volwassenen (tijdelijk betaald) en *lid commissie onderwijs leefstijl en overgewicht in de basiscurricula van zorgprofessionals (onbetaald) -Voorzitter Nationaal Obesitas Symposium – betaald -Bestuurslid stichting STRESS-NL (platform Nederlandse stress onderzoekers)– onbetaald -Lid Koninklijke Hollandsche Maatschappij der Wetenschappen – onbetaald -Lid OPEN Policy working group European Association of the Study of Obesity (sinds Dec 2022) – onbetaald -Lid Voedingsbeleidadviesteam Erasmus MC – onbetaald -Lid Hogeschoolraad – onbetaald -Deelnemer netwerk NL2025 – onbetaald - Jurylid Heineken Award commissie - betaald - Lid voedingsbeleidcommissie Erasmus MC – onbetaald -Spreker /dagvoorzitter bij multipele (inter)nationale en regionale (wetenschappelijke) congressen, webinars, podcasts, media, en nascholingen voor zorgprofessionals. beleidsmakers of algemeen publiek : oa voor Langerhans symposia, Dutch Obesity Academy, Dutch Diabetes Academy, NVE Academy, E-wise, KOEL, SCEM, ASCEND, European Association of the Study of Obesity, International Medical Press, Food First Network, Obesitas Platform, overgewicht.tv, Breedenburg, Het Grote Obesitas Debat, POLITICO Health Care summit EU, European Commission, Diabetes Genootschap Zuid Nederland, Vereniging Arts en Leefstijl, Internistendagen – deels onbetaald en deels betaald (zonder belangenverstrengeling of bemoeienis over wetenschappelijke inhoud door commerciele partijen in geval van betaling).
Afgeronde nevenfuncties: Lid van diverse commissies en wetenschappelijke besturen (onbetaald) |
- In 2019 boek gepubliceerd met co-auteur Mariëtte Boon ""VET belangrijk: feiten en fabels over voeding, vetverbranding en verborgen dikmakers"". Inkomsten naar uitgever Ambo Anthos en boekwinkels en een klein deel naar de auteurs (Mariette Boon en Obesity Science). In 2020 is het boek internationaal gepubliceerd. - Elisabeth Fonds (ondergebracht bij Erasmus MC Trustfonds) financiert de ontwikkeling van de online diagnostische ObesEcare tool om oorzaken overgewicht op te sporen. Het Elisabeth Fonds is een maatschappelijk / charitatief fonds en heeft geen winstoogmerk. - Firma Rhythm financiert een internationale multicenter trial voor een nieuw geneesmiddel (setmelanotide) voor patiënten met een zeldzame vorm van genetische obesitas. - Bezoek aan internationale Masterclass: ''leading the change in the management of Obesity & T2D'', gesponsord door Johnson & Johnson, 2017 (geen honorarium ontvangen) - Actieve bijdrage aan de ontwikkeling van een gespecialiseerde leefstijlinterventie in het Erasmus MC en bij de ontwikkeling van een diagnostische (online) ondersteuningstool voor mensen met overgewicht of obesitas (ook in het Erasmus MC).
|
Geen |
|
Brongers |
Manager fysiotherapie, fysiotherapeut en leefstijlcoach (GLI aantekening). Werkgever: Leidsche Rijn Julius Gezondheidscentra |
Geen |
Geen |
Geen |
|
Brugman |
Zelfstandig Leefstijlcoach |
Bestuurslid BLCN, deel betaald |
Geen |
Geen |
|
De Leest |
Apotheker GHC de Roerdomp Nieuwegein 24 uur Apotheker Geneesmiddel Informatie Centrum KNMP 10 uur |
onbetaald redactie Vascazine/vrijwilliger Vasculitis Vereniging |
Geen |
Geen |
|
Freijer |
Algemeen manager Partnerschap Overgewicht Nederland (PON) ondergebracht bij Erasmus MC te Rotterdam |
- Voorzitter van ISPOR Special Interest Group (SIG) Nutrition Economics. Werkzaamheden: het nieuw opgezette gebied binnen het bestaande gebied van gezondheidseconomie en daarbuiten vergroten.
- Eigenaar van eenmanszaak met naam Freijer4Food & Health Care Activiteitenomschrijving: Geven van lezingen op gebied van voeding; ontwikkelen van kennis/kunde omtrent voedingseconomie (Nutrition Economics); Schrijver/publicist van (wetenschappelijke) artikelen; geven van workshops op bovengenoemd gebied; projectmatig begeleiden van (commerciële) onderzoeken; consultancy op gebied van voeding. |
Geen |
Geen |
|
Govers |
Voorzitter van het NVD netwerk Obesitas (Kenniscentrum Diëtisten Overgewicht en Obesitas; www.KDOO.nl) Dit is een niet betaalde functie |
Vice-voorzitter van de ESDN Obesity van the European Federation of Associations of Dietitians. Een niet betaalde functie |
Geen |
Geen |
|
Langens |
Huisarts |
Ontwikkelen e-learnings/ webinar ( CME-online/accredidact/medonline): betaald Preventieconsult: medische begeleiding bij overgewicht/leefstijl : betaald Huisartsen Eemland: bevorderen wijkgericht werken: betaald Fieldlab obesitas Amersfoort: onbetaald |
Geen |
Geen |
|
Liem |
Gastro-intestinaal en traumachirurg
Groene Hart Ziekenhuis (GHZ) in Gouda (60%) Alrijne Ziekenhuis in Leiderdorp/Alphen ad Rijn (10%) Nederlandse Obesitas Kliniek West in Den Haag (20%) Keizer Kliniek in Voorschoten (10%) |
- Hoofd afdeling chirurgie in GHZ - Voormalig voorzitter Dutch Society for Metabolic and Bariatric Surgery - Lid Auditcommissie (Ned Ver v Heelkunde) - Lid Landelijke Commissie Chirurgische Complicatie Registratie (Ned Ver v Heelkunde) - Clinical Audit Board Audit voor de Behandeling van Obesitas van DICA - Lid Registry Committee of the Internationale Federation for the Surgery of Obesity and Metabolic Disorders - Lid Multi-National Advisory Group of IFSO-European Chapter
Al deze nevenfuncties zijn onbetaald |
Nederlandse Obesitas Kliniek. De chirurgische behandeling van obesitas en obesitas gerelateerde metabole ziekten maakt onderdeel uit van het behandel spectrum. Als ervaren bariatrisch en metabool chirurg maak ik derhalve ondereel uit van deze commissie. De uiteindelijke richtlijn heeft invloed op de positionering van deze behandeling in het behandel spectrum. Voor de chirurgische behandeling zelf, is in 2020 een herziene richtlijn gepubliceerd door de NVVH en het Kennisinstituut. Hiernaar zal worden verwezen in deze Zorgstandaard. Ik heb een beperkt belang in NOK West in Den Haag.
Ik ben daarnaast regelmatig een gevraagde spreker op (internationale) bijeenkomsten en congressen, soms gefaciliteerd door Johnson & Johnson Institute, Medtronic, Gore en Olympus. Daar staat soms een tijdvergoeding tegenover, conform Europese regelgeving. |
Geen |
|
Out |
Internist-vasculair geneeskunde (MST Enschede, fulltime) |
Klinisch Netwerk Obesitas (commissie NVE, lid) |
Van januari t/m juni 2020 heb ik één dag per week onbetaald verlof om de mogelijkheden te exploreren van het opzetten van een leefstijicentrum (bijvoorbeeld als anderhalvelijns centrum, al dan niet in naam van/in samenwerking met het MST). - Deelname aan deze richtlijncommissie kan mijn naam/reputatie als leefstijlarts versterken |
Geen |
|
Out-Hoiting |
Eigenaar Mijn leefstijl op recept
Vice-voorzitter BLCN (deel betaald, deel vrijwillig) |
Geen |
In mijn bedrijf maak ik oa producten voor GLI coaches. Deze coaches hebben belang bij een goed obesitasbeleid waarbij de GLI blijft bestaan. ik ben zelf geen GLI coach meer. |
Geen |
|
Sloots-Jongen |
Klinisch psycholoog bij Maasstad Ziekenhuis |
Geen |
Geen |
Geen |
|
Slot |
VvOCM Nicolette Slot eigen praktijk voor oefentherapie, wandeltrainer en leefstijlcoach |
Oefentherapeut Mensendieck - betaald leefstijlcoach - betaald wandeltrainer - betaald voorzitter Drunens Wandelfestival - niet betaald voorzitter Avond4daagse Drunen - niet betaald |
Geen |
Geen |
|
Van den Anker |
Freelance opdracht HR bij WijzijnMeo (bedrijfsnaam Blue Wolf) Bestuurslid NSOG (Nederlandse stichtijng over gewicht) - Patiëntenorganisatie (onbezoldigd) |
Bestuurslid Pon (onbezoldigd) |
Als bestuurslid van de patiëntenorganisatie voor mensen die leven met obesitas kan de richtlijn ter uitleg en informatie gebruikt worden voor de patiënten |
Geen |
|
Van Kemenade |
Waarnemend huisarts (huisartspraktijk Biesbosch Made) |
Auteur Consult HZG (huisartszorggroep Breda) betaald per uur bij werkzaamheden Creeeren scholingen/presentaties op het gebied Diabetes/leefstijl. Betaald per scholing/presentatie |
Geen |
Geen |
|
Huls |
Huisarts, mede-eigenaar huisartsenpraktijk Arends, Huls & Tanck |
-Kaderhuisarts diabetes, consulterende functie en kaderfunctie bij Zorggroep ECT Tiel en Zorggroep Gelders Rivierenland, uitbetaling: vast bedrag per maand en op basis van declaratie -Docent Stichting Langerhans, geven van scholingen voor huisartsen (in opleiding) en POH-S, betaling per gegeven scholing -Gastdocent VOHA, huisartsenopleiding Nijmegen, betaling per gegeven scholing |
Geen |
Geen |
|
Deenen |
tot 1 januari 2022 werkzaam als diëtist bij de Nederlandse Obesitas Kliniek
vanaf 2022 werkzaam als diëtist bij Diëtistenpraktijk Bernadette Deenen |
bestuurslid KDOO, het betreft een onbetaalde functie als bestuurslid organiseer ik de webinars, journal club |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door afgevaardigden van de patiëntenverenigingen in de werkgroepen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Nederlandse Stichting Over Gewicht.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Module |
Uitkomst raming |
Toelichting |
|
Diagnostiek van overgewicht en obesitas bij volwassenen |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitters van de werkgroep en de adviseurs knelpunten in de zorg voor kinderen en volwassenen met obesitas of overgewicht in combinatie met risicofactoren en/of comorbiditeit. Tevens zijn er knelpunten aangedragen door AJN Jeugdartsen Nederland, Beroepsvereniging Gewichtsconsulenten Nederland, Beroepsvereniging Leefstijl Coaches Nederland, Care for Obesity (VU Amsterdam), Inspectie voor de Gezondheidszorg en Jeugd, Jongeren op Gezond Gewicht, GGD Har voor Brabant, Amsterdamse Aanpak Gezond Gewicht (GGD Amsterdam), Koninklijk Nederlands Genootschap voor Fysiotherapie, Koninklijke Nederlandse Maatschappij ter bevordering der Pharmacie, Koninklijke Nederlandse Maatschappij ter bevordering van de Tandheelkunde, Landelijke Verenging Medische Psychologie, Landelijke Huisartsen Vereniging, Nederlandse Associatie Physician Assistants, Nederlands Centrum Jeugdgezondheid, Nederlandse Diabetes Federatie, Nederlands Huisartsen Genootschap, Nederlandse Internisten Vereniging, Nederlands Jeugdinstituut, Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose, Nederlandse Vereniging van Diëtisten, Nederlandse Vereniging voor Kindergeneeskunde, Nederlandse Vereniging van Maag-Darm-Leverartsen, Nederlandse Vereniging voor Obstetrie & Gynaecologie, Nederlandse Vereniging voor Cardiologie, Nederlandse Vereniging voor Heelkunde, Nederlandse Vereniging voor Plastische Chirurgie, Partnerschap Overgewicht Nederland, Pharos, Stichting over gewicht, Vereniging Gehandicaptenzorg Nederland, Voedingscentrum, Vereniging Vertrouwensartsen Kindermishandeling, Vereniging van Oefentherapeuten Cesar en Mensendieck, Zorginstituut Nederland en Zelfstandige Klinieken Nederland via een Invitational conference. Een verslag van de Invitational conference is opgenomen in de bijlagen.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitters en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroepen besproken waarna de werkgroepen de definitieve uitgangsvragen hebben vastgesteld. Vervolgens inventariseerden de werkgroepen per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroepen waardeerden deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerden de werkgroepen ten minste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag.
Gezien de hoge mate van uitval en terugval en daarmee het teruglopen van het percentage succesvolle resultaten na verloop van tijd zijn korte-termijn leefstijlinterventies weinig informatief voor de klinische praktijk. Vanwege het belang van een duurzaam effect zijn bij de selectie van de literatuur daarom alleen studies met een minimale duur van 2 jaar geïncludeerd bij de kinderrichtlijn (Reinehr, 2009).
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur en de beoordeling van de risk-of-bias van de individuele studies is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk die meegewogen dienen te worden, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module ‘Organisatie van zorg’.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk onderzoek van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers, M. C., Kho, M. E., Browman, G. P., Burgers, J. S., Cluzeau, F., Feder, G., et al. (2010). AGREE II: advancing guideline development, reporting and evaluation in health care. Canadian Medical Association Journal, 182(18), E839-E842.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit.https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.htMl Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
Schünemann H., Brożek J., Guyatt G., et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013.
Schünemann, H. J., Oxman, A. D., Brozek, J., Glasziou, P., Jaeschke, R., Vist, G. E., et al. (2008). Rating Quality of Evidence and Strength of Recommendations: GRADE: Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ: British Medical Journal, 336(7653), 1106.
Reinehr, T., Widhalm, K., l'Allemand, D., Wiegand, S., Wabitsch, M., Holl, R. W., & APV‐Wiss Study Group and German Competence Net Obesity. (2009). Two‐year follow‐up in 21,784 overweight children and adolescents with lifestyle intervention. Obesity, 17(6), 1196-1199.
Wessels, M., Hielkema, L., & van der Weijden, T. (2016). How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. Journal of the Medical Library Association: JMLA, 104(4), 320.
Wharton, S., Lau, D. C., Vallis, M., Sharma, A. M., Biertho, L., Campbell-Scherer, D., ... & Boyling, E. (2020). Obesity in adults: a clinical practice guideline. CMAJ, 192(31), E875-E891.