Hysterosalpingografie olie versus water
Uitgangsvraag
Welke type contrastmiddel kan het beste worden gebruikt bij het verrichten van hysterosalpingografie?
Aanbeveling
Overweeg bij het aanwezig zijn van een indicatie voor HSG, deze uit te voeren met oliehoudend contrast vanwege een grotere kans op zwangerschap en levendgeborene in vergelijking met waterhoudend contrast.
Zie stroomschema Oriënterend fertiliteitsonderzoek.
Overwegingen
Balans tussen gewenste en ongewenste effecten
Bij een deel van de verminderd vruchtbare patiënten leeft de overtuiging dat een hysterosalpingografie met oliehoudend contrast de kans op spontane zwangerschap vergroot. In de spreekkamer wordt dan ook regelmatig gevraagd om ‘het doorspuiten van de eileiders’. In de loop van de jaren zijn er verschillende wetenschappelijke onderzoeken gedaan naar dit effect. De werkgroep heeft gekeken naar de verschillen tussen een HSG met een oliehoudend contrast en waterhoudend contrast. Het oudste onderzoek dat voldoet aan de PICO van onze uitgangsvraag, dateert van 1986. Het meest recente onderzoek dat uit onze literatuursearch naar voren kwam, is van 2022. Er zijn verschillende theorieën waarom oliehoudend contrast een vruchtbaarheidsverhogend effect kan hebben. De meest gangbare is dat het debris of slijmproppen uit de tubae wegspoelt. Verder zou het de ontvankelijkheid van het endometrium vergroten. Ook wordt gedacht dat het peritoneale macrofagen activiteit vermindert wat goed zou zijn voor de overleving van spermatozoa.
Verschillende studies laten zien dat er mogelijk een positief effect is bij het gebruiken van een oliehoudend contrastmiddel bij een hysterosalpingografie in vergelijking met contrastmiddelen op waterbasis. Er wordt een grotere kans op zwangerschap beschreven in de Cochrane systematic review van Wang (2020) en de studie van Zhang (2022) waarbij in totaal 3.550 patiënten zijn vergeleken. Er is een relatief risico van 1.30 (95% CI 1.15, 1.48) bij oliehoudend contrast ten opzichte van waterhoudend contrast.
Zhang (2022) beschrijft daarbij een kortere time to pregnancy in de oliehoudende groep van 41.7 weken versus 46.1 weken in de waterhoudende groep. Zhang (2022) vond ook een grotere kans op een doorgaande zwangerschap (positieve hartactie na 12 weken zwangerschap) binnen 6 maanden na HSG met een relatief risico van 1,44 (95% CI 1.14-1.80) ten voordele van oliehoudend contrast. Echter, in de secundaire analyses van de H2Oil studie werd bij een langere follow-up van 3 en 5 jaar geen verschil gevonden (Van Welie, 2020 respectievelijk Van Rijswijk, 2020). Het positieve effect lijkt na een jaar af te vlakken (Van Welie 2020). Bij het analyseren van het aantal levendgeborenen vonden we wel een grotere kans in de groep met oliehoudend contrast met een follow-up van maximaal 1 jaar. Daarbij zijn 3.002 patiënten vergeleken, met een relatief risico van 1,41 (95% CI 1.06-1.86).
Om een uitspraak te doen over het verschil in beeldkwaliteit, keek Zhang (2022) naar kwaliteitsscores bij uterus opacificatie of uterus omlijning, tuba omlijning, fimbriële rugae, tuba overloop, peritoneale verspreiding en diagnostische kwaliteit. Op alle onderdelen scoorden de beelden in de oliegroep statistisch significant beter. De werkgroep is van mening dat de verschillen in deze aspecten in de praktijk niet relevant zijn.
Wat betreft nadelige effecten hebben we naar verschillende onderstaande aspecten gekeken.
Er is nog weinig onderzoek gedaan naar het verschil tussen het effect van oliehoudend en waterhoudend contrast op de schildklierfunctie van de neonaat. Omdat in oliehoudend contrast meer jodium zit dan in waterhoudend contrast (Van Welie, 2020a), zou het een groter effect kunnen hebben op de schildklierfunctie van de neonaat. De enige studie die aan onze PICO voldeed, is de retrospectieve data-analyse van de H2Oil studie. De onderzoeksgroep heeft de schildklierfunctie van 140 neonaten kunnen vergelijken (76 in de olie groep en 64 in de watergroep). Bij geen van de neonaten werd congenitale hypothyreoïdie vastgesteld.
Van de geslecteerde studies keken Dreyer (2017), Spring (2000) en Zhang (2022) naar het verschil in de kans op miskraam. In totaal 1301 patiënten werden geanalyseerd, waarbij geen verschil werd gevonden (RR 1.06, 95% CI 0.61-1.86). In de studie van Van Rijswijk (2020) met een follow-up van 5 jaar werd eveneens geen verschil gevonden.
Voor het optreden van een extra-uteriene graviditeit werd een relatief risico van 0.66 (95% CI 0.18-2.36) gevonden ten voordele van oliehoudend contrast. Het betrouwbaarheidsinterval is echter zeer breed en het verschil was niet statistisch significant (Dreyer, 2017 en Spring, 2000). In de langere follow-up van 5 jaar werd tevens geen significant verschil gevonden (Van Rijswijk, 2020).
Alper (1986), Dreyer (2017) en Zhang (2022) hebben de piijnscores vergeleken. Hoewel Alper en Dreyer geen significant verschil vonden, vond Zhang dit wel. Het verschil in de pijnscore is echter zo klein (VAS score van 1.8 ± 1.5 in de oliegroep versus 2.3 ± 1.6 in de watergroep), dat wij dit als niet klinisch relevant beschouwen. Er is nog onvoldoende literatuur over pijnstilling bij HSG om hier een onderbouwde aanbeveling voor te schrijven. Pragmatisch kan overwogen worden te adviseren een uur van tevoren een NSAID te nemen.
Het risico op infectie is in beide groepen laag. Slechts 2 artikelen hebben het verschil bekeken. Er werd in de oliegroep een lagere kans op infectie gevonden (0.4%) in vergelijking met de watergroep (3.8%) (Lindequest, 1194 en Rasmussen, 1991). Het optreden van koorts is zeldzaam, Zhang (2022) vond geen statistisch significant verschil.
Een ander, zeldzaam, ongewenst effect is een allergische reactie. Dit werd in beide groepen (in totaal 982 patiënten) niet gevonden in de RCT van Zhang (2022).
Intravasatie trad vaker op in de groep met oliehoudend contrast, namelijk bij 2.6% versus 1.0% in de groep met waterhoudend contrast (Alper, 1986; Dreyer, 2017; Lindequest, 1994; Rasmussen, 1991; Zhang, 2022). Intravasatie op zich is niet schadelijk, maar geeft wel een risico op vetembolie met potentieel ernstige klachten. Daarom wordt in het geval van intravasatie het onderzoek direct gestaakt. Vetembolie wordt in de geïncludeerde studies niet gerapporteerd.
Kwaliteit van bewijs
De overall kwaliteit van bewijs is laag. Dit betekent dat we onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten.
Er is afgewaardeerd vanwege ernstige:
- Risk of Bias: methodologische beperkingen.
- Imprecisie: onnauwkeurigheid, omdat het betrouwbaarheidsinterval de grens van klinische relevantie overschrijdt.
Waarden en voorkeuren van patiënten (en eventueel hun partner)
Voor patiënten met een laag risico op tubapathologie, is het belangrijkste potentiële voordeel dat een HSG met oliehoudend contrast de kans op zwangerschap zou vergroten. Hoewel de overkoepelende kwaliteit van het bewijs laag is, laten de onderzoeken een redelijk gunstig effect van oliehoudend contrast zien. Veel vrouwen willen elke mogelijkheid aangrijpen om de kans te vergroten. Het is aan de zorgverlener om de beperkingen in het bewijs met de patiënt te bespreken en voor- en nadelen met elkaar af te wegen. Behalve pijn tijdens het onderzoek, is het risico op nadelige effecten klein. Wat betreft pijn zou het pijnstillingsgebeid nog geoptimaliseerd kunnen worden.
Kostenaspecten
Oliehoudend contrast is duurder dan waterhoudend contrast (prijsverschil €213 (Van Welie, 2021)).
In de studie van Van Welie (2021) die naar het langere termijneffect (5 jaar) keek, werd berekend dat er in de oliegroep per persoon gemiddeld €357 minder kosten gemaakt worden aan ART. De kosten die leiden tot doorgaande zwangerschap, waren lager in de oliegroep dan in de watergroep met een prijsverschil van €144 (95% CI - €579 tot €290). De totale kosten, inclusief de kosten voor zwangerschap en bevalling, zijn na 5 jaar in beide groepen vergelijkbaar (verschil van €50, 95% CI - €576 tot €475). De kwaliteit van het bewijs is ingeschat als laag omdat het een retrospectieve analysen is en er grote betrouwbaarheidsintervallen zijn.
Van Rijswijk (2018) vond met een follow-up van 6 maanden hogere kosten per live birth in de oliegroep in vergelijking met de watergroep (US$11532 versus US$8310). Deze hogere kosten zijn voor een groot deel een gevolg van het groter aantal doorgaande zwangerschappen en bevallingen. Hierbij dient te worden vermeld dat deze kosten zijn gebaseerd op de kosten in de Verenigde Staten, waar het verschil in prijs tussen oliehoudend en waterhoudend contrast wereldwijd het grootste is en ART meer kost dan in Europa.
Al met al lijkt er een beperkt verschil te zijn in de kosten die leiden tot zwangerschap na een HSG met oliehoudend of waterhoudend contrast in Europa.
Indirecte kosten, zoals werkverzuim bij zwangerschap en in de kraamtijd, maar ook werkverzuim door het ondergaan van een vruchtbaarheidsbehandeling en werkverzuim en psychische begeleiding bij en door ongewenste kinderloosheid, moeten nog onderzocht worden.
Gelijkheid ((health) equity/equitable)
De patiënt heeft over het algemeen geen keuze in het soort contrast dat wordt gebruikt. Zij is afhankelijk van de keuze die het ziekenhuis of de vruchtbaarheidskliniek heeft gemaakt, waarbij de prijs van het contrast vermoedelijk een grote rol speelt. In Nederland gebruiken niet alle ziekenhuizen een oliehoudend contrast. Dit kan potentieel ongelijkheid in spontane kans op zwangerschap geven. De zorgverlener kan overwegen de patiënt naar een kliniek te verwijzen waar oliehoudend contrast wel beschikbaar is.
Aanvaardbaarheid
Ethische aanvaardbaarheid
Het gebruik van oliehoudend contrast bij het verrichten van een HSG lijkt aanvaardbaar door de betrokkenen. Er zijn geen ethische bezwaren.
Duurzaamheid
Er is geen onderzoek gedaan naar het verschil in duurzaamheid tussen oliehoudend contrast en waterhoudende contrast.
Haalbaarheid
In het geval van het verrichten van een HSG is het gebruik van oliehoudend contrast over het algemeen al standaard zorg. Het overstappen van waterhoudend contrast naar oliehoudend contrast brengt extra kosten met zich mee. Dit kan een belemmering zijn in de eventuele overstap naar oliehoudend contrast.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
In de vergelijking tussen oliehoudend contrast en waterhoudend contrast bij HSG lijkt oliehoudend contrast voordelen te bieden op het gebied van diagnostische accuratesse, kans op zwangerschap en het aantal levendgeborenen. Het verschil in kans op zwangerschap is de eerste maanden het grootst en is afgevlakt na een jaar. Er werd geen verschil gevonden in kans op miskraam, EUG, infectie of allergische reactie en de pijnscore. Intravasatie treedt vaker op bij oliehoudend contrast, echter het optreden van een vetembolie is zeer zeldzaam. Het verschil in gevolgen voor de schildklierfunctie bij de neonaat is nog onvoldoende onderzocht. De kosten van oliehoudend contrast zijn hoger, echter het lijkt tot meer spontane zwangerschappen en minder noodzaak tot ART te leiden waardoor de uiteindelijke kosten vergelijkbaar lijken. De zekerheid van het bewijs is laag tot zeer laag gescoord volgens het GRADE systeem.
Eindoordeel:
Zwakke aanbeveling voor het gebruik van oliehouden contrast bij HSG.
Onderbouwing
In many clinics, hysterosalpingography (HSG) currently is the first choice for diagnosis of tubal pathology. An iodine-containing contrast is used, of which there are two types: oil-based and water-based contrast media. In Dutch clinics there is a variation in the type of contrast used. Considerations on the choice of contrast may include diagnostic properties, influence on the chance of pregnancy, risks (including risk of infection, (oil) embolism, miscarriage, ectopic pregnancy), patient preference, costs (effectiveness). Patients have picked up that there is research that shows oil-based contrast could increase the chance of pregnancy, hence this is often their preferred choice of contrast. With this initial question we focus on this primary outcome measure as well as other advantages and disadvantages.
Population: Women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography
Intervention: OSCM
Comparator: WSCM
|
Outcome
|
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence (Quality of evidence) |
Conclusions |
|
|
WSCM |
OSCM |
||||
|
Clinical pregnancy (critical)
|
Relative risk: 1.3 (CI 95% 1.15 - 1.48) Based on data from 3550 participants in 7 studies
|
266 per 1000 |
346 per 1000 |
Low Due to serious risk of bias, due to serious imprecision1 |
OSCM may increase clinical pregnancy when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Wang, 2020; Zhang, 2022) |
|
Difference: 80 more per 1000 (CI 95% 40 more - 128 more) |
|||||
|
Diagnostic value (important)
|
Measured by: Total image quality score Based on data from 982 participants in 1 study
|
(Mean) - |
(Mean) - |
Low Due to serious risk of bias, due to serious imprecision2 |
OSCM may increase the diagnostic value when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Zhang, 2022) |
|
Difference: MD 2.10 higher (CI 95% 1.69 higher – 2.51 higher) |
|||||
|
Time to pregnancy (important) |
Based on data from 952 participants in 1 study |
(Mean) - |
(Mean) - |
Low Due to serious risk of bias, due to serious imprecision3 |
The evidence suggests that OSCM results in little to no difference in time to pregnancy when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Zhang, 2022) |
|
Difference: MD 4.40 lower (CI 95% 6.65 lower – 2.15 lower)
|
|||||
|
Ongoing pregnancy |
|||||
|
Ongoing pregnancy - Within 6 months (important)
|
Relative risk: 1.43 (CI 95% 1.14 - 1.8) Based on data from 952 participants in 1 study
|
570 per 1000 |
815 per 1000 |
Low Due to serious risk of bias, due to serious imprecision4 |
OSCM may increase ongoing pregnancy within six months after HSG when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Zhang, 2022) |
|
Difference: 245 more per 1000 (CI 95% 80 more - 456 more)
|
|||||
|
Ongoing pregnancy - At 3 years follow-up (important)
|
Relative risk: 1.09 (CI 95% 1.02 - 1.17) Based on data from 1107 participants in 1 study
|
570 per 1000 |
621 per 1000 |
Low Due to serious risk of bias, due to serious imprecision5 |
The evidence suggests that OSCM results in little to no difference in ongoing pregnancy at 3 years after HSG when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Van Welie, 2020) |
|
Difference: 51 more per 1000 (CI 95% 11 more - 97 more)
|
|||||
|
Ongoing pregnancy - At 5 years follow-up (important)
|
Relative risk: 1.07 (CI 95% 1.0 - 1.14) Based on data from 1114 participants in 1 study
|
570 per 1000 |
610 per 1000 |
Low Due to serious risk of bias, due to serious imprecision6 |
The evidence suggests that OSCM results in little to no difference in ongoing pregnancy at 5 years after HSG when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Van Rijswijk, 2020) |
|
Difference: 40 more per 1000 (CI 95% 0 fewer - 80 more)
|
|||||
|
Live birth |
|||||
|
Live birth rate (important)
|
Relative risk: 1.41 (CI 95% 1.06 - 1.86) Based on data from 3002 participants in 4 studies
|
350 per 1000 |
493 per 1000 |
Low Due to serious inconsistency, due to serious imprecision7 |
OSCM may increase live birth rate after HSG when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Dreyer, 2017; Rasmussen, 1991; Spring, 2000; Zhang, 2022) |
|
Difference: 143 more per 1000 (CI 95% 21 more - 301 more) |
|||||
|
Live birth rate at 5 years follow-up (important)
|
Relative risk: 1.11 (CI 95% 1.03 - 1.2) Based on data from 1114 participants in 1 study
|
350 per 1000 |
389 per 1000 |
Low Due to serious risk of bias, due to serious imprecision8 |
The evidence suggests that OSCM results in little to no difference in live birth rate at 5 years after HSG when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Van Rijswijk, 2020) |
|
Difference: 39 more per 1000 (CI 95% 10 more - 70 more) |
|||||
|
Thyroid function (important)
|
Risk difference: 0.00 (95%-BI -0.03 — 0.03) Based on data from 140 participants in 1 study
|
None of the neonates conceived after OSCM or WSCM had a positive screening result for congenital hypothyroidism. T4 concentrations and T4 standard deviation scores were comparable between the two groups. None of the children were currently on thyroid hormone supplementation. |
Very low Due to serious risk of bias, due to very serious imprecision9 |
The evidence is very uncertain about the effect of OSCM on thyroid function when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Van Welie, 2020a) |
|
|
Miscarriage |
|||||
|
Miscarriage per woman (important)
|
Relative risk: 1.06 (CI 95% 0.61 - 1.86) Based on data from 2604 participants in 3 studies |
78 per 1000 |
83 per 1000 |
Low Due to very serious imprecision10 |
The evidence suggests that OSCM results in little to no difference in miscarriage when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Dreyer, 2017; Spring, 2000; Zhang, 2022) |
|
Difference: 5 more per 1000 (CI 95% 30 fewer - 67 more) |
|||||
|
Miscarriages at 5 years follow-up (important)
|
Relative risk: 0.84 (CI 95% 0.62 - 1.13) Based on data from 1114 participants in 1 study
|
78 per 1000 |
66 per 1000 |
Low Due to serious risk of bias, due to serious imprecision11 |
The evidence suggests that OSCM results in little to no difference in miscarriage at 5 years after HSG when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Van Rijswijk, 2020) |
|
Difference: 12 fewer per 1000 (CI 95% 30 fewer - 10 more) |
|||||
|
Ectopic pregnancy |
|||||
|
Ectopic pregnancy per woman (important) |
Relative risk: 0.66 (CI 95% 0.18 - 2.36) Based on data from 1652 participants in 2 studies
|
12 per 1000 |
8 per 1000 |
Low Due to very serious imprecision12
|
OSCM may reduce ectopic pregnancies when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Dreyer, 2017; Spring, 2000) |
|
Difference: 4 fewer per 1000 (CI 95% 10 fewer - 16 more) |
|||||
|
Ectopic pregnancy at 5 years follow-up (important)
|
Relative risk: 0.64 (CI 95% 0.25 - 1.64) Based on data from 1114 participants in 1 study
|
12 per 1000 |
8 per 1000 |
Very low Due to serious risk of bias, due to very serious imprecision13 |
The evidence is very uncertain about the effect of OSCM on ectopic pregnancy at 5 years after HSG when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Van Rijswijk, 2020) |
|
Difference: 4 fewer per 1000 (CI 95% 9 fewer - 8 more) |
|||||
|
Pain (important) |
Based on data from 3 studies |
Pain was measured using a scale from 0 to 5 (Alper, 1986) or the VAS-score (Dreyer, 2017; Zhang, 2022). Alper (1986) reported a mean difference of -0.30 (95% CI -0.78 to 0.18) in favor of OSCM. Dreyer (2017) reported a median VAS-score of 4.8 (IQR 3.0 to 6.4) for OSCM and 5.0 (IQR 3.0 to 6.7) for WSCM, favoring OSCM. Zhang (2022) reported a mean difference of -0.50 (95%CI |
Low Due to serious inconsistency, due to serious imprecision14 |
The evidence suggests that OSCM results in little to no difference in pain when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Alper, 1986; Dreyer, 2017; Zhang, 2022) |
|
|
Infection (important) |
Relative risk: 0.23 (CI 95% 0.04 - 1.28) Based on data from 662 participants in 2 studies
|
37 per 1000 |
9 per 1000 |
Low Due to very serious imprecision15
|
OSCM may reduce infection when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Lindequist, 1994; Rasmussen, 1991) |
|
Difference: 28 fewer per 1000 (CI 95% 36 fewer - 10 more) |
|||||
|
Allergic reaction (important) |
Risk difference: 0.00 (95%-BI -0.00 — 0.00) Based on data from 982 participants in 1 study |
No allergic reactions occurred for women who received either OSCM or WSCM. |
Very low Due to serious risk of bias, due to very serious imprecision16 |
The evidence is very uncertain about the effect of OSCM on allergic reactions when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Zhang, 2022) |
|
|
Oil embolism (important) |
- |
- |
No GRADE (no evidence was found)
|
No evidence was found regarding the effect of OSCM on oil embolism when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography. |
|
|
Intravasation (important) |
Relative risk: 3.19 (CI 95% 1.52 - 6.71) Based on data from 2894 participants in 5 studies
|
10 per 1000 |
32 per 1000 |
Low Due to serious risk of bias, due to serious imprecision17 |
OSCM may increase intravasation when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Alper, 1986; Dreyer, 2017; Lindequist, 1994; Rasmussen, 1991; Zhang, 2022) |
|
Difference: 22 more per 1000 (CI 95% 5 more - 57 more) |
|||||
|
Fever (important) |
Relative risk: 5.0 (CI 95% 0.24 - 103.88) Based on data from 982 participants in 1 study
|
0 per 1000 |
0 per 1000 |
Very low Due to serious risk of bias, due to very serious imprecision18 |
The evidence is very uncertain about the effect of OSCM on fever when compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Zhang, 2022) |
|
Difference: 0 fewer per 1000 (CI 95% 0 fewer - 0 more) |
|||||
|
Costs |
|||||
|
Costs - Ongoing pregnancy (important)
|
Based on data from 1108 participants in 1 study |
(Mean) - |
(Mean) - |
Low Due to serious risk of bias, due to serious imprecision19 |
The evidence suggests that OSCM results in little to no difference in costs for ongoing pregnancy compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Van Rijswijk, 2018) |
|
Difference: MD 870.0 higher (CI 95% 621.33 higher – 1118.67 higher) |
|||||
|
Costs - Ongoing pregnancy at 5 years follow-up (important)
|
Based on data from 1114 participants in 1 study |
(Mean) - |
(Mean) - |
Low Due to serious risk of bias, due to serious imprecision20 |
The evidence suggests that OSCM results in little to no difference in costs for ongoing pregnancy at 5 years after HSG compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Van Welie, 2021) |
|
Difference: MD 144.0 higher (CI 95% 578.10 lower – 290.10 higher) |
|||||
|
Costs - Live birth (important)
|
Based on data from 1108 participants in 1 study |
(Mean) - |
(Mean) - |
Low Due to serious risk of bias, due to serious imprecision21 |
The evidence suggests that OSCM results in little to no difference in costs for live birth compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Van Rijswijk, 2018)
|
|
Difference: MD 3222.0 higher (CI 95% 1647.20 higher – 4796.80 higher) |
|||||
|
Costs - Live birth at 5 years follow-up (important)
|
Based on data from 1114 participants in 1 study |
(Mean) - |
(Mean) - |
Low Due to serious risk of bias, due to serious imprecision22 |
The evidence suggests that OSCM results in little to no difference in costs for live birth at 5 years after HSG compared with WSCM in women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography.
(Van Welie, 2021) |
|
Difference: MD 50.0 lower (CI 95% 574.14 lower – 474.14 higher) |
|||||
1. Risk of Bias: serious. Due to many areas of the Risk of bias based on Cochrane 'Risk of bias' assessment tool being labeled as unclear; Imprecision: serious. Due to overlap of the upper limit of the 95% confidence interval with the minimal clinically important difference;
2. Risk of Bias: serious. Inadequate concealment of allocation during randomization process, resulting in bias, Inadequate blinding/lack of blinding of participants and personnel, potentially causing bias, Selective outcome reporting; Imprecision: serious. Due to the optimal information size which was not achieved;
3. Risk of Bias: serious. Inadequate concealment of allocation during randomization process, resulting in bias, Inadequate blinding/lack of blinding of participants and personnel, potentially causing bias, Selective outcome reporting; Imprecision: serious. Due to the optimal information size which was not achieved;
4. Risk of Bias: serious. Inadequate concealment of allocation during randomization process, resulting in bias, Inadequate blinding/lack of blinding of participants and personnel, potentially causing bias, Selective outcome reporting; Imprecision: serious. Due to overlap of the upper limit of the 95% confidence interval with the minimal clinically important difference;
5. Risk of bias: serious. Retrospective data analysis introducing possible ascertainment and selection bias. Imprecision: serious. Due to the optimal information size which was not achieved.
6. Risk of bias: serious. Retrospective data analysis introducing possible ascertainment and selection bias. Imprecision: serious. Due to the optimal information size which was not achieved.
7. Inconsistency: serious. The magnitude of statistical heterogeneity was high, with I^2: 80%.; Imprecision: serious. Due to overlap of the upper limit of the 95% confidence interval with the minimal clinically important difference;
8. Risk of bias: serious. Retrospective data analysis introducing possible ascertainment and selection bias. Imprecision: serious. Due to the optimal information size which was not achieved.
9. Risk of bias: serious. Frequent loss to follow-up. Imprecision: very serious. No events and low number of participants.
10. Imprecision: very serious. Due to overlap of both the lower and upper limit of the 95% confidence interval with the minimal clinically important difference.
11. Risk of bias: serious. Retrospective data analysis introducing possible ascertainment and selection bias. Imprecision: serious. Due to overlap of the lower limit of the 95% confidence interval with the minimal clinically important difference;
12. Imprecision: very serious. Due to overlap of both the lower and upper limit of the 95% confidence interval with the minimal clinically important difference.
13. Risk of bias: serious. Retrospective data analysis introducing possible ascertainment and selection bias. Imprecision: very serious. Due to overlap of both the lower and upper limit of the 95% confidence interval with the minimal clinically important difference;
14. Inconsistency: serious. Due to not being able to pool the studies because of differences in how the outcome was assessed. Imprecision: serious. Due to the optimal information size which was not achieved.
15. Imprecision: very serious. Due to overlap of both the lower and upper limit of the 95% confidence interval with the minimal clinically important difference.
16. Risk of bias: serious. Inadequate concealment of allocation during randomization process, resulting in bias, Inadequate blinding/lack of blinding of participants and personnel, potentially causing bias, Selective outcome reporting; Imprecision: very serious. No events and low number of participants.
17. Risk of Bias: serious. Due to many areas of the Risk of bias based on Cochrane 'Risk of bias' assessment tool being labeled as unclear; Imprecision: serious. Low number of events.
18. Risk of Bias: serious. Inadequate concealment of allocation during randomization process, resulting in bias, Inadequate blinding/lack of blinding of participants and personnel, potentially causing bias, Selective outcome reporting; Imprecision: very serious. Due to overlap of both the lower and upper limit of the 95% confidence interval with the minimal clinically important difference;
19. Risk of Bias: serious. Due to concerns about the calculation of the costs and generalizability to the Dutch situation. Imprecision: serious. Due to the optimal information size which was not achieved.
20. Risk of bias: serious. Retrospective data analysis introducing possible ascertainment and selection bias. Imprecision: serious. Due to the optimal information size which was not achieved.
21. Risk of Bias: serious. Due to concerns about the calculation of the costs and generalizability to the Dutch situation. Imprecision: serious. Due to the optimal information size which was not achieved.
22. Risk of bias: serious. Retrospective data analysis introducing possible ascertainment and selection bias. Imprecision: serious. Due to the optimal information size which was not achieved.
Description of studies
A total of seven studies were included in the analysis of the literature. Important study characteristics and results are summarized in table 1. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’). All studies included women with a low risk for tubal pathology.
The Cochrane review of Wang (2020) assessed the effectiveness and safety of tubal flushing with oil-soluble contrast media (OSCM) and water-soluble contrast media (WSCM) in women with infertility. In April 2020, Cochrane Gynaecology and Fertility Group Specialised Register of controlled trials, MEDLINE, Embase, CENTRAL, and PsycINFO were searched. Besides, reference lists of identified articles and trial registries were checked. Randomized controlled trials about women with infertility (defined as inability to achieve pregnancy after at least six months of regular unprotected intercourse) who compared OSCM with WSCM were included. Fifteen studies were included. However, only six studies that compared OSCM with WSCM were included (Alper, 1986; De Boer, 1988; Dreyer, 2017; Lindequist, 1994; Rasmussen, 1991; Spring, 2000). Except for De Boer, all studies defined infertility as a period of at least 12 months of trying to conceive. De Boer defined 6 months as infertility, however the mean duration was 37 months. The Cochrane review did not provide information about whether a chlamydia antibody titer (CAT) was performed among patients in the included studies. Only the study by Dreyer (2017) specifically reports known or high risk for tubal pathology as an exclusion criteria.
Zhang (2022) performed a randomized controlled trial in 15 medical centers to assess the efficacy and safety of HSG with ethiodized poppyseed oil-based contrast medium. Women between 21 and 39 years who have been trying to conceive for more than 12 months, with a spontaneous menstrual cycle and meeting the indications for HSG were included. Besides, they had to be able to understand the study contents and volunteer to sign the informed consent form. Exclusion criteria were known endocrine disorders (such as polycystic ovary syndrome, diabetes, hyperthyroidism and hyperprolactinemia), less than 8 menstrual cycles per year, high risk of fallopian tube disease (e.g., history of pelvic inflammatory disease, previous chlamydia infection or known endometritis), vaginitis, active acute or subacute pelvic inflammatory disease, uterine or fallopian tube tuberculosis, uterine or cervical bleeding, cessation of menstruation that could not rule out pregnancy, severe cardiopulmonary disease; body temperature higher than 37.5 ℃ within 3 days before HSG, total motile sperm counts of male partners at less than 1 million/mL; and comorbidity or social circumstances that may cause subjects to fail to follow the study plan or even endanger patient safety.
In the multicenter randomized H2Oil trial (performed in 27 hospitals in the Netherlands) oil-based contrast was compared with water-based contrast to evaluate the chance of ongoing pregnancy. In this trial, women aged 18 to 39, with a spontaneous menstrual cycle and an indication for tubal patency testing by HSG were eligible for study participation. Couples with male factor infertility, endocrine disorders, iodine allergy, or a high risk for tubal pathology (as indicated by a history of pelvic inflammatory disease, previous chlamydia infection, or known endometriosis) were excluded for study participation. The results of this trial have initially been described by Dreyer (2017) (included in the Cochrane review by Wang, 2020) and have also been described in other papers (as secondary analyses):
- Van Welie (2020) performed a 3-year follow-up study to evaluate whether the fertility-enhancing effects of the oil-based contrast changed over time. Ongoing pregnancy rates within 3 years of randomization were reported.
- Van Rijswijk (2020) performed a 5-year follow-up analysis of couples who participated in the H2Oil trial. Ongoing pregnancies, live births and time to pregnancy were reported.
- Van Rijswijk (2018) and Van Welie (2021) performed economic evaluations alongside the H2Oil trial. Van Rijswijk (2018) analyzed costs per additional ongoing pregnancy and per live birth within 6 months of randomization. Van Welie (2021) performed an economic evaluation of the costs within 5 years of randomization.
- Van Welie (2020a) evaluated the effect of HSG with oil-based contrast on neonatal thyroid function, as compared to HSG with water-based contrast. Of the 369 women who had a live born infant in the H2Oil trial, 208 women consented to be approached for future research and 138 provided informed consent to collect data on the thyroid function tests of their offspring (n = 140, with 76 conceived after HSG with oil-based contrast and 64 after HSG with water-based contrast). Thyroid function tests of these children were retrieved from the Dutch neonatal screening program, which includes the assessment of total thyroxine (T4) in all newborns, followed by thyroid-stimulating hormone only in those with a T4 level of ≤ −0.8 SD score.
Table 1. Characteristics of included studies
*For further details, see risk of bias table in the appendix
Results
1. Probability of spontaneous pregnancy (critical outcome)
1.1 Ongoing pregnancy (rate)
Ongoing pregnancy, defined as a positive fetal heartbeat on ultrasonographic examination after 12 weeks of gestation, from the first day of the last menstrual cycle of pregnancy within 6 months after HSG, was reported by Dryer (2017) and Zhang (2022).
Dreyer (2017) found an ongoing pregnancy rate of 220/554 (39.7%) in the oil-based group and 161/554 (29.1) in the water-based group with a Rate Ratio of 1.37 (P value <0.001).
Zhang (2022) found ongoing pregnancy was confirmed in the oil-based group in 136/473 (29.1%) women, while an ongoing pregnancy was confirmed in 96/479 (20.1%) women in the water-based group (RR 1.44, 95% CI 1.14 to 1.80). This difference was considered clinically relevant in favor of oil-based contrast.
Van Welie (2020) reported ongoing pregnancies at a follow-up of 3 years after HSG treatment. In the oil-based group, 426/550 (77%) women had a confirmed ongoing pregnancy, while an ongoing pregnancy was confirmed for 394/557 (71%) women in the water-based group (RR 1.09, 95% CI 1.02 to 1.17). This difference was considered not clinically relevant.
Van Rijswijk (2020) reported ongoing pregnancies at a follow-up of 5 years after HSG treatment. In the oil-based group, 444/555 (80.0%) women had a confirmed ongoing pregnancy, while an ongoing pregnancy was confirmed for 419/559 (75.0%) women in the water-based group (RR 1.07, 95% CI 1.00 to 1.14). This difference was considered not clinically relevant.
1.2. Clinical pregnancy (rate)
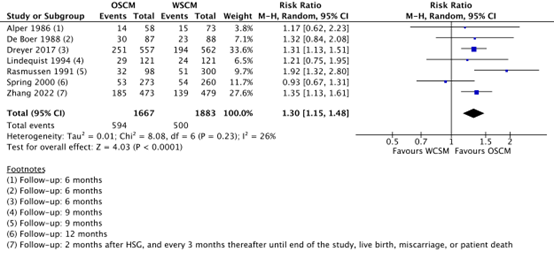
Clinical pregnancy was reported in Alper (1986), De Boer (1988), Dreyer (2017), Lindequist (1994), Rasmussen (1991), Spring (2000) and Zhang (2022). A clinical pregnancy was confirmed in 594/1667 (35.6%) of the women in the oil-based group, and in 500/1883 (26.6%) in the water-based group (RR 1.30, 95% CI 1.15 to 1.48). This difference was considered clinically relevant in favor of oil-based contrast (Figure 1).
Figure 1. The effect of oil-based contrast versus water-based contrast on clinical pregnancy
OSCM: oil-soluble contrast media, WSCM: water-soluble contrast media, CI: Confidence Interval
Source: Wang (2020), Zhang (2022)
2. Diagnostic value (important outcome)
The diagnostic value was reported by Zhang (2022) and was– in accordance with the European guidelines on quality criteria – based on the following five criteria:
- uterus opacification or uterine outline;
- fallopian tube outline;
- fimbrial rugae;
- fallopian tube spillage;
- peritoneal distribution.
A total image quality score was calculated from the five criteria, ranging from 0 to 15 (with higher scores indicating higher image quality).
The diagnostic quality was higher in the oil-based group (11.6 ± 3.4) in comparison with the water-based group (9.5 ± 3.1, p<0.001) (MD 2.10, 95% CI 1.69 to 2.51).
3. Long-term effects on fertility (important outcome)
3.1. Time to pregnancy
The time to pregnancy was reported by Zhang (2022). Time to pregnancy was shorter in the oil-based group (41.7 ± 18.5 weeks) than in the water-based group (46.1 ± 16.8 weeks) (MD -4.40, 95% CI -6.65 to -2.15). This difference was considered not clinically relevant.
3.2. Live birth rate
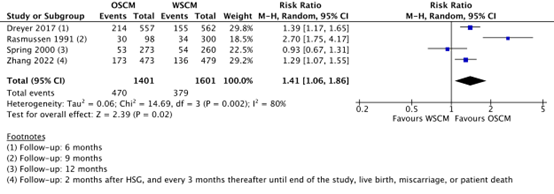
Live births are reported by Dreyer (2017), Rasmussen (1991), Spring (2000) and Zhang (2022). In the number of live births as reported by Zhang (2022), 4 twin-births are included in each group. A live birth occurred in 470/1401 (33.5%) of the women in the oil-based group, and in 379/1601 (23.7%) in the water-based group (RR 1.41, 95% CI 1.06 to 1.86). This difference was considered clinically relevant in favor of oil-based contrast (Figure 2).
Figure 2. The effect of oil-based contrast versus water-based contrast on live birth
OSCM: oil-soluble contrast media, WSCM: water-soluble contrast media, CI: Confidence Interval
Source: Wang (2020), Zhang (2022)
Van Rijswijk (2020) reported live births at a follow-up of 5 years after HSG treatment. In the oil-based group, 415/555 (74.8%) women had a live birth, while 376/559 (67.3%) women in the water-based group had a live birth (RR 1.11, 95% CI 1.03 to 1.20). This difference was considered not clinically relevant.
4. Effect on neonate (important outcome)
4.1. Thyroid function
Van Welie 2020a reported that none of the neonates conceived after HSG with oil- (n=76) or water-based (n=64) contrast had a positive screening result for congenital hypothyroidism. T4 concentrations and T4 standard deviation scores were comparable between the two groups. None of the children were currently on thyroid hormone supplementation.
5. Risk of miscarriage (important outcome)
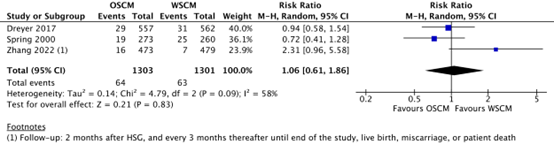
Miscarriage per woman was reported in Dreyer (2017), Spring (2000) and Zhang (2022). In the oil-based group, 64/1303 (4.9%) women reported a miscarriage, while 63/1301 (4.8%) women in the water-based group reported a miscarriage (RR 1.06, 95% CI 0.61 to 1.86). This difference was considered not clinically relevant (Figure 3).
Figure 3. The effect of oil-based contrast versus water-based contrast on miscarriage
OSCM: oil-soluble contrast media, WSCM: water-soluble contrast media, CI: Confidence Interval
Source: Wang (2020), Zhang (2022)
Van Rijswijk (2020) reported miscarriages (i.e., the amount of women with at least one miscarriage) at a follow-up of 5 years after HSG treatment. In the oil-based group, 68/555 (12.3%) women had at least one miscarriage, while 82/559 (14.7%) women in the water-based group had at least one miscarriage (RR 0.84, 95% CI 0.62 to 1.13). This difference was considered not clinically relevant.
6. Ectopic pregnancy (important outcome)
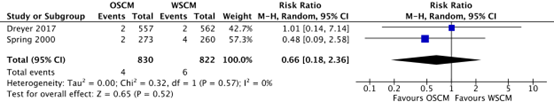
Ectopic pregnancy was reported in Dreyer (2017) and Spring (2000). In the oil-based group, 4/830 (0.5%) ectopic pregnancies were reported, while this was 6/822 (0.7%) in the water-based group (RR 0.66, 95% CI 0.18 to 2.36).
Figure 4. The effect of oil-based contrast versus water-based contrast on ectopic pregnancy
OSCM: oil-soluble contrast media, WSCM: water-soluble contrast media, CI: Confidence Interval
Source: Wang (2020)
Van Rijswijk (2020) reported ectopic pregnancies at a follow-up of 5 years after HSG treatment. In the oil-based group, 7/555 (1.3%) ectopic pregnancies were reported, while this was 11/559 (2.0%) in the water-based group (RR 0.64, 95% CI 0.25 to 1.64). This difference was considered clinically relevant in favor of oil-based contrast. However, there was no statistical difference (P value .35)
7. Side effects (important outcome)
7.1. Pain
Pain was reported by Alper (1986), Dreyer (2017) and Zhang (2022).
Alper (1986) reported pain on a scale from 0 to 5 (with 0 corresponding to no pain and 5 represents severe pain). The mean pain score for women in the oil-based group was 2.9 ± 0.9, while the mean pain score for women in the water-based group was 3.2 ± 1.6 (MD -0.30, 95% CI -0.78 to 0.18). This difference was considered not clinically relevant.
Dreyer (2017) reported median VAS-scores for pain (on a 0-10 cm scale). The median pain score was 4.8 (IQR: 3.0 to 6.4) in the oil-based group, and 5.0 (IQR 3.0 to 6.7] in the water-based group (p=0.28). The article does not mention whether analgesics were administered.
Zhang (2022) reported mean VAS-scores for pain (on a 0-10 cm scale, with higher scores meaning more pain). The mean pain score was 1.8 ±1.5 in the oil-based group, and 2.3 ± 1.6 in the water-based group (MD -0.50, 95% CI -0.70 to -0.30). The article does not mention whether analgesics were administered.
7.2. Infection
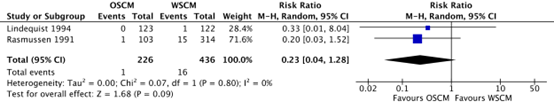
Infections were reported in Lindequist (1994) and Rasmussen (1991). In the oil-based group, 1/226 (0.4%) infections were reported, while 16/436 (3.8%) infections were reported in the water-based group (RR 0.23, 95% CI 0.04 to 1.28).
Figure 5. The effect of oil-based contrast versus water-based contrast on infection
OSCM: oil-soluble contrast media, WSCM: water-soluble contrast media, CI: Confidence Interval
Source: Wang (2020)
7.3. Allergic reaction
Zhang (2022) reported that no allergic reactions occurred during or after HSG for women who received either OSCM or WSCM.
7.4. Oil embolism
Not reported.
7.5. Intravasation
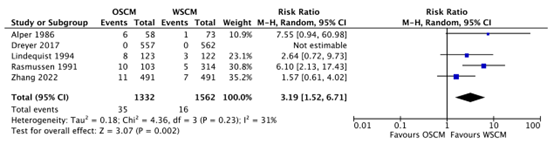
Intravasation was reported by Alper (1986), Dreyer (2017), Lindequist (1994), Rasmussen (1991) and Zhang (2022). Intravasation occurred in 35/1332 women (2.6%) in the oil-based group and in 16/1562 women (1.0%) in the water-based group (RR 3.19, 95% CI 1.52 to 6.71). This difference was considered clinically relevant in favor of water-based contrast (Figure 6).
Figure 6. The effect of oil-based contrast versus water-based contrast on intravasation
OSCM: oil-soluble contrast media, WSCM: water-soluble contrast media, CI: Confidence Interval
Source: Wang (2020), Zhang (2022)
7.6. Fever
Zhang (2022) reported that fever occurred 2/491 (0.4%) in the oil-based group, while this did not occur in the water-based group (RR 5.00, 95% CI 0.24 to 103.88).
8. Costs (important outcome)
Van Welie (2021) included 1.114 patients and calculated the mean costs per woman for ongoing pregnancy and per live birth at a follow-up of 5 years after HSG treatment. They considered direct medical costs (costs for the contrast medium intervention, infertility treatment and miscarriage) and performed an additional analysis on costs for pregnancy and delivery. The price difference between oil-based contrast and water-based contrast was €213 according to the price as provided by the manufacturer. The mean costs for infertility treatments were lower in the oil group (a difference of €357, (95% CI -€792-77, p=0.107)), as there were more women who had a spontaneous pregnancy in this group. The costs per woman for ongoing pregnancy were lower in the oil group (€2327 ± 3539) compared to the water group (€2471 ± 3848) with a mean difference of -€144 (95% CI -€579 to €290). For live birth, the mean costs were lower in the oil group (€5252 ± 4062) than in the water group (€5302 ± 4833) (MD -€50, 95% CI -€576 to €475). The similar costs, despite the higher costs of the oil based medium, are explained by less women needing fertility treatment compared to the water group.
Van Rijswijk (2018) compared the direct medical costs (contrast medium costs), costs of infertility treatments and costs related to pregnancy, delivery and miscarriage within the follow up of 6 months. They used US based prices to calculate the costs. The cost difference between oil-based and water-based contrast is globally the highest in the US.
They calculated the mean costs per woman for ongoing pregnancy and per live birth at a follow-up of 6 months after HSG treatment. The costs were higher in the oil-based group (US$2014 ± 2294) than in the water-based group (US$1144 ± 1912) for ongoing pregnancy (MD US$869, 95% CI US$620-1,118). For live birth, the mean costs were also higher in the oil group (US$11532 ± 13241) than in the water group (US$8310 ± 13503) (MD US$3,222, 95% CI US$1,645-4,798). The higher costs for the oil group arise mainly from pregnancy and delivery (as there were more live births in the oil group, the costs in this group are higher).
A systematic review of the literature was performed to answer the following question(s):
Is there a difference in the occurrence of spontaneous pregnancies after performing an HSG with a water-based and oil-based contrast media?
| Patients | Women of infertile couples (at low risk of tubal pathology) undergoing hysterosalpingography |
| Intervention | Oil-based contrast media |
| Control | Water-based contrast media |
| Outcomes |
Probability of spontaneous pregnancy, diagnostic value, long-term effects on fertility, effect on neonate, risk of miscarriage, ectopic pregnancy, side effects, costs |
| Other selection criteria |
Study design: systematic reviews and randomized controlled trials Minimal follow-up: 6 months Population: at least 100 women |
Relevant outcome measures
The guideline panel considered probability of spontaneous pregnancy as a critical outcome measure for decision making; and diagnostic value, long-term effect on fertility, effect on neonate, risk of miscarriage, ectopic pregnancy, side effects, costs as important outcome measures for decision making.
The guideline panel defined the outcome measures as follows:
- Probability of spontaneous pregnancy: ongoing pregnancy (rate) and clinical pregnancy (rate)
- Long-term effects on fertility: time to pregnancy, live birth rate
- Effect on neonate: thyroid function
- Side effects: pain, infection, allergic reaction, oil embolism, intravasation
For the other outcome measures, the guideline panel did not define the outcome measures a priori but used the definitions used in the studies.
The guideline panel defined 25% difference (RR <0.8 to >1.25) for dichotomous and 0.5 SD for continuous outcomes as a minimal clinically (patient) important difference.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 2010 until the 19th of April 2024. The detailed search strategy is listed under the tab ‘Literature search strategy’. The systematic literature search resulted in 48 hits. Studies were selected based on the following criteria:
- The study population had to meet the criteria as defined in the PICO
- The intervention had to meet the criteria as defined in the PICO
- Research type: systematic review or randomized-controlled trials
- Articles written in English or Dutch
Initially, seventeen studies were selected based on title and abstract screening. After reading the full text, ten studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and seven studies were included. The systematic review of Wang 2020 defined a broader PICO than the PICO defined for this module (it also included studies about oil-based contrast media or water-based contrast media versus no treatment or a combination of oil-based and water-based contrast media versus water-based contrast media). Therefore, six randomized controlled trials included in the review were selected for the literature analysis (Alper, 1986; De Boer, 1988; Dreyer, 2017; Lindequist, 1994; Rasmussen, 1991; Spring, 2000).
- Dreyer K, van Rijswijk J, Mijatovic V, Goddijn M, Verhoeve HR, van Rooij IAJ, Hoek A, Bourdrez P, Nap AW, Rijnsaardt-Lukassen HGM, Timmerman CCM, Kaplan M, Hooker AB, Gijsen AP, van Golde R, van Heteren CF, Sluijmer AV, de Bruin JP, Smeenk JMJ, de Boer JAM, Scheenjes E, Duijn AEJ, Mozes A, Pelinck MJ, Traas MAF, van Hooff MHA, van Unnik GA, de Koning CH, van Geloven N, Twisk JWR, Hompes PGA, Mol BWJ. Oil-Based or Water-Based Contrast for Hysterosalpingography in Infertile Women. N Engl J Med. 2017 May 25;376(21):2043-2052. doi: 10.1056/NEJMoa1612337. Epub 2017 May 18. PMID: 28520519.
- Kamphuis, D., Rosielle, K., Van Welie, N., Brinkhuis, E., Van Dongen, A., Bourdrez, P., ... & Mijatovic, V. (2024). O-022 Early tubal flushing with oil-based contrast during hysterosalpingography versus no tubal flushing in women with unexplained infertility–H2Oil-timing randomized controlled trial. Human Reproduction, 39(Supplement_1) abstract, deae108-022.
- van Rijswijk J, Pham CT, Dreyer K, Verhoeve HR, Hoek A, de Bruin JP, Nap AW, Wang R, Lambalk CB, Hompes PG, Mijatovic V. Oil-based or water-based contrast for hysterosalpingography in infertile women: a cost-effective analysis of a randomized controlled trial. Fertility and sterility. 2018 Sep 1;110(4):754-60.
- van Rijswijk J, van Welie N, Dreyer K, Pham CT, Verhoeve HR, Hoek A, de Bruin JP, Nap AW, van Hooff MHA, Goddijn M, Hooker AB, Bourdrez P, van Dongen AJCM, van Rooij IAJ, van Rijnsaardt-Lukassen HGM, van Golde RJT, van Heteren CF, Pelinck MJ, Duijn AEJ, Kaplan M, Lambalk CB, Mijatovic V, Mol BWJ. Tubal flushing with oil-based or water-based contrast at hysterosalpingography for infertility: long-term reproductive outcomes of a randomized trial. Fertil Steril. 2020 Jul;114(1):155-162. doi: 10.1016/j.fertnstert.2020.03.022. Epub 2020 Jun 16. PMID: 32553471.
- van Welie N, Pham CT, van Rijswijk J, Dreyer K, Verhoeve HR, Hoek A, de Bruin JP, Nap AW, van Hooff MHA, Goddijn M, Hooker AB, Gijsen AP, Traas MAF, Smeenk JMJ, Sluijmer AV, Lambers MJ, van Unnik GA, de Koning CH, Mozes A, Timmerman CCM, Lambalk CB, Karnon JD, Mijatovic V, Mol BWJ; H2Oil Study Group. The long-term costs and effects of tubal flushing with oil-based versus water-based contrast during hysterosalpingography. Reprod Biomed Online. 2021 Jan;42(1):150-157. doi: 10.1016/j.rbmo.2020.09.015. Epub 2020 Sep 17. PMID: 33077355.
- van Welie N, Roest I, Portela M, van Rijswijk J, Koks C, Lambalk CB, Dreyer K, Mol BWJ, Finken MJJ, Mijatovic V; H2Oil Study Group. Thyroid function in neonates conceived after hysterosalpingography with iodinated contrast. Hum Reprod. 2020 May 1;35(5):1159-1167. doi: 10.1093/humrep/deaa049. PMID: 32427280; PMCID: PMC7259368.
- van Welie N, Rosielle K, Dreyer K, van Rijswijk J, Lambalk CB, van Geloven N, Mijatovic V, Mol BWJ, van Eekelen R; H2Oil Study Group. How long does the fertility-enhancing effect of hysterosalpingography with oil-based contrast last? Reprod Biomed Online. 2020 Dec;41(6):1038-1044. doi: 10.1016/j.rbmo.2020.08.038. Epub 2020 Aug 30. PMID: 33012658.
- Wang R, Watson A, Johnson N, Cheung K, Fitzgerald C, Mol BWJ, Mohiyiddeen L. Tubal flushing for subfertility. Cochrane Database Syst Rev. 2020 Oct 15;10(10):CD003718. doi: 10.1002/14651858.CD003718.pub5. PMID: 33053612; PMCID: PMC9508794.
- Zhang J, Lan W, Wang Y, Chen K, Zhang G, Yang W, Chen H, Xu W, Ma J, Qin W, Zhang Y, Wang W, Wang H, Dong Z, Wang Y, Chen Y, Gang N, Tang Y. Ethiodized poppyseed oil-based contrast medium is superior to water-based contrast medium during hysterosalpingography regarding image quality improvement and fertility enhancement: A multicentric, randomized and controlled trial. EClinicalMedicine. 2022 Apr 5;46:101363. doi: 10.1016/j.eclinm.2022.101363. PMID: 35399811; PMCID: PMC8987810.
Risk of bias tables
Research question: Is there a difference in the occurrence of spontaneous pregnancies after performing an HSG with a water-based and oil-based contrast agent?
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated?
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented?
Were patients blinded?
Were healthcare providers blinded?
Were data collectors blinded?
Were outcome assessors blinded?
Were data analysts blinded?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measure
LOW Some concerns HIGH
|
|
Zhang, 2022 |
Definitely yes;
Reason: Block randomization was used to generate random assignment number.
|
Probably no;
Reason: Random assignment number and grouping information were made into scratch cards, but it did not achieve center randomization by using a computerized system.
|
Probably no;
Reason: Radiologist was blinded to study design, patient information, and contrast medium. Unclear if patient and healthcare providers were blinded.
|
Probably yes;
Reason: Loss to follow-up was infrequent in intervention and control group. |
Probably no;
Reason: In the protocol, only a selection of the outcome measures described in the article were presented. |
Definitely yes;
Reason: No other problems noted. |
Some concerns (clinical pregnancy, ongoing pregnancy, live birth, miscarriage, time to pregnancy)
|
|
Dreyer, 2017 |
Definitely yes;
Reason: Randomization was performed with the use of a secured online randomization program (ALEA, FormsVision) with random block sizes of 2, 4, or 6, stratified according to hospital. |
Definitely yes;
Reason: Randomization program was overseen by an independent data manager. |
Probably yes;
Reason: Owing to the difference in imaging between the use of oil-based contrast and water-based contrast and outcomes were objective, the trial was not blinded with respect to participants and caregivers. |
Probably yes;
Reason: Loss to follow-up was infrequent in intervention and control group. |
Probably yes;
Reason: Outcomes in protocol were also reported in the study. |
Definitely yes;
Reason: No other problems noted. |
Low |
|
Author, year |
Selection of participants
Was selection of exposed and non-exposed cohorts drawn from the same population?
|
Exposure
Can we be confident in the assessment of exposure? |
Outcome of interest
Can we be confident that the outcome of interest was not present at start of study? |
Confounding-assessment
Can we be confident in the assessment of confounding factors? |
Confounding-analysis
Did the study match exposed and unexposed for all variables that are associated with the outcome of interest or did the statistical analysis adjust for these confounding variables? |
Assessment of outcome
Can we be confident in the assessment of outcome? |
Follow up
Was the follow up of cohorts adequate? In particular, was outcome data complete or imputed?
|
Co-interventions
Were co-interventions similar between groups? |
Overall Risk of bias
|
|
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Low, Some concerns, High |
|
|
Van Welie, 2020a |
Probably yes
Reason: Participants were selected from previous study.
|
Probably yes
Reason: Derived from previous study.
|
Definitely yes
Reason: Outcome was assessed during heel prick at 4 to 7 days after birth and known endocrine disorders were excluded.
|
Probably yes
Reason: Demographic characteristic were assessed and additional information on the medical history of the child was provided by the parents.
|
Probably yes
Reason: Effect modification was used. Responders and non-responders have similar characteristics.
|
Probably yes
Reason: Derived from heel prick. The neonatal screening results were retrieved from database.
|
Probably yes
Reason: Follow-up was adequate. Missing data was similar between exposed and non-exposed.
|
Probably yes
Reason: No other co-interventions were used.
|
Low
|
Table of included studies
|
Reference |
Reason for exclusion |
|
Chen J, Liu S, Lu J. Comparison of fertility outcomes between oil‑based and water‑based contrast media during hysterosalpingography: A meta‑analysis. Exp Ther Med. 2023 Aug 3;26(3):449. doi: 10.3892/etm.2023.12148. PMID: 37614430; PMCID: PMC10443060. |
Better systematic review available. Also non-randomised controlled trials and no raw data available |
|
Dreyer K, van Rijswijk J, Mijatovic V, Goddijn M, Verhoeve HR, van Rooij IAJ, Hoek A, Bourdrez P, Nap AW, Rijnsaardt-Lukassen HGM, Timmerman CCM, Kaplan M, Hooker AB, Gijsen AP, van Golde R, van Heteren CF, Sluijmer AV, de Bruin JP, Smeenk JMJ, de Boer JAM, Scheenjes E, Duijn AEJ, Mozes A, Pelinck MJ, Traas MAF, van Hooff MHA, van Unnik GA, de Koning CH, van Geloven N, Twisk JWR, Hompes PGA, Mol BWJ. Oil-Based or Water-Based Contrast for Hysterosalpingography in Infertile Women. N Engl J Med. 2017 May 25;376(21):2043-2052. doi: 10.1056/NEJMoa1612337. Epub 2017 May 18. PMID: 28520519. |
Included in systematic review Wang 2020 |
|
Fang F, Bai Y, Zhang Y, Faramand A. Oil-based versus water-based contrast for hysterosalpingography in infertile women: a systematic review and meta-analysis of randomized controlled trials. Fertil Steril. 2018 Jul 1;110(1):153-160.e3. doi: 10.1016/j.fertnstert.2018.03.021. Epub 2018 Jun 13. Erratum in: Fertil Steril. 2019 Jun;111(6):1262. doi: 10.1016/j.fertnstert.2019.04.025. PMID: 29908778. |
More recent review available |
|
Geenen RWF, van der Molen AJ, Dekkers IA, Bellin MF, Bertolotto M, Correas JM, Heinz-Peer G, Mahnken AH, Quattrocchi CC, Radbruch A, Reimer P, Roditi G, Sebastià C, Stacul F, Romanini L, Clément O, Brismar TB. Contrast media for hysterosalpingography: systematic search and review providing new guidelines by the Contrast Media Safety Committee of the European Society of Urogenital Radiology. Eur Radiol. 2024 Apr 4. doi: 10.1007/s00330-024-10707-6. Epub ahead of print. PMID: 38573340. |
Better systematic review availabe. No clear search strategy and risk of bias assessment |
|
Johnson NP. Review of lipiodol treatment for infertility - an innovative treatment for endometriosis-related infertility? Aust N Z J Obstet Gynaecol. 2014 Feb;54(1):9-12. doi: 10.1111/ajo.12141. Epub 2013 Oct 19. PMID: 24138402. |
Wrong study design: narrative review |
|
Legro RS, Stetter CM, Kunselman AR, Geisler WM, Dodson WC, Estes SJ. Oil-based or saline contrast for sono-hysterosalpingography in infertile women: a pilot randomized controlled double blind trial. F S Rep. 2022 Nov 15;4(1):121-126. doi: 10.1016/j.xfre.2022.11.005. PMID: 36959970; PMCID: PMC10028425. |
Wrong intervention: differences between contrast in ultrasound HSG |
|
Liu L, Zhao J, Zhang G. Comparison of iodized oil with soluble iodized agents in hysterosalpingography and the evaluation of modified hysterosalpingography. Journal of Interventional Radiology. 2006. |
Article in Chinese |
|
Roest I, Rosielle K, van Welie N, Dreyer K, Bongers M, Mijatovic V, Mol BW, Koks C. Safety of oil-based contrast medium for hysterosalpingography: a systematic review. Reprod Biomed Online. 2021 Jun;42(6):1119-1129. doi: 10.1016/j.rbmo.2021.03.014. Epub 2021 Mar 23. PMID: 33931367. |
Better systematic review available. Supplementary data not available |
|
Tsui S, Sofy AA. A meta-analysis of fertility and adverse outcomes in oil- and water-based contrast for hysterosalpingography. Turk J Obstet Gynecol. 2023 Mar 10;20(1):64-73. doi: 10.4274/tjod.galenos.2023.67750. PMID: 36908096; PMCID: PMC10013086. |
Better systematic review available. Also studies not matching with PICO |
|
Wang R, van Welie N, van Rijswijk J, Johnson NP, Norman RJ, Dreyer K, Mijatovic V, Mol BW. Effectiveness on fertility outcome of tubal flushing with different contrast media: systematic review and network meta-analysis. Ultrasound Obstet Gynecol. 2019 Aug;54(2):172-181. doi: 10.1002/uog.20238. Epub 2019 Jun 26. Erratum in: Ultrasound Obstet Gynecol. 2019 Nov;54(5):708. doi: 10.1002/uog.21879. PMID: 30740799. |
More recent review available |
Beoordelingsdatum en geldigheid
Publicatiedatum : 30-10-2025
Beoordeeld op geldigheid : 07-10-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd door de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met subfertiliteit.
Werkgroep
- Verhoeve H.R. (Harold) voorzitter, gynaecoloog, OLVG te Amsterdam, NVOG
- Van Dongen A.J.C.M. (Angelique), gynaecoloog, Ziekenhuis Gelderse Vallei te Ede, NVOG
- Tanahatoe S.J. (Sandra), gynaecoloog, Universitair Medisch Centrum Utrecht te Utrecht, NVOG
- Lahley E.E.L.O. (Lisa), gynaecoloog, subspecialist voortplantingsgeneeskunde, Leids Universitair Medisch Centrum te Leiden, NVOG
- Twisk M. (Moniek), gynaecoloog, BovenIJ ziekenhuis te Amsterdam, NVOG
- Van den Boogaard N.M. (Noortje), gynaecoloog, Flevoziekenhuis te Almere, NVOG
- Bailleux B.B.E.P. (Bart), klinisch chemicus endocrinoloog, Leids Universitair Medisch Centrum te Leiden, NVKC
- Bijnevelt L. (Lianne), Fertiliteitsarts, Sint Antonius Ziekenhuis te Utrecht, VVF
- Silvius A.M. (Hèlen), huisarts, Huisartsenplartijk Laila te Den Haag, NHG
- Sinjorgo S.C.H. (Simone), medewerker medewerker patientenperspectief wetenschappelijk onderzoek en richtlijnen, Freya (vanaf december 2024)
- Vermeulen M. (Marloes), medewerker patientenperspectief wetenschappelijk onderzoek en richtlijnen, Freya (tot december 2024)
- Boomsma C. (Carolien), gynaecoloog, Bravis Ziekenhuis te Roosendaal, NVOG (tot december 2023)
Met ondersteuning van
- Mostovaya I.M. (Irina), senior-adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Pepping F. (Fieke), junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Middelhuis D. (Danique), adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Schultink J.M. (Janneke), adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Tabel Gemelde (neven)functies en belangen werkgroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke Financiële Belangen |
Persoonlijke Relaties |
Extern gefinancierd onderzoek |
Intell. belangen en reputatie |
Overige belangen |
Datum |
Acties |
|
Harold Verhoeve (voorzitter) |
Gynaecoloog OLVG |
Lid Adviesraad Ferring (1-2 keer per jaar), betaald |
geen |
nvt |
Ik ben betrokken bij de consortiumstudies van de voortplantingsgeneeskunde, als hoofdonderzoeker op lokatie OLVG. Hier vallen alle consortium-studies onder die over de eileider testen gaan. Het consortium concept houdt in dat zoveel mogelijk Nederlands klinieken aan de studies deelnemen. Deelname aan studies is ook een kwaliteitscriterium die wordt getoetst tijdens kwaliteitsvisitaties en gestimuleerd.
1. The effectiveness of immediate versus delayed tubal flushing with oil-based contrast in women with unexplained infertility (H2Oil-timing study) study protocol of a randomised controlled trial: D. Kamphuis et al. BMC womens Health. 2023 May 6 doi:10.1186 Projectleider (nee) Externe financiering : ZonMW Periode tot 2023 (studie inclusie compleet) 2. FOil study: Effectiveness of tubal flushing with oil-based contrast during hysterosalpingography and tubal flushing by hysterosalpingo-foam sonography in infertile women undergoing fertility work-up: study protocol of a randomised controlled trial (FOil study): D.Kamphuis et al. Accepted BMJ open 2024. Projectleider (nee) Externe financiering : ZonMW Periode 2023 tot inclusie is voltooid |
geen |
geen |
24/10/2022 |
Geen restricties. Deelname aan de adviesraad is met de heer Verhoeve besproken. Hieruit bleek dat er geen producten worden gemaakt die relevant zijn voor het orienterend fertiliteitsonderzoek. |
|
Sandra Tanahatoe |
Gynaecoloog, UMC Utrecht |
geen |
geen |
geen |
geen |
geen |
geen |
23/12/2022 |
Geen restricties. |
|
Lisa Lashley |
Gynaecoloog, specialist voortplantingsgeneeskunde LUMC |
Geen |
Geen |
nvt |
Geen onderzoek waarbij de financier belang kan hebben. Het betreft de DONOR studie (onderzoek naar prognose en ontwikkeling van pre eclampsie bij eiceldonatie) en de PREMI studie (onderzoek naar effect prednisolone bij herhaalde miskramen). Hoofdonderzoeker en projectleider bij beiden studies. |
Geen |
Geen |
1/11/2022 |
Geen restricties. |
|
Angelique van Dongen |
gynaecoloog - ZGV Ede - 0.75 fte (patiëntenzorg, betaald) gynaecoloog-docent - Radboudumc Nijmegen - 0.3 fte (onderwijs, betaald) |
geen |
geen |
geen |
De H2OlieTiming studie heeft in 15 Nederlandse klinieken gelopen, waaronder de kliniek waar ik werk. Omdat ik binnen ons fertiliteitsteam de enige gynaecoloog ben met een BROKregistratie, ben ik (automatisch) de lokale hoofdonderzoeker. 1 van onze fertiliteitsartsen is betrokken bij de selectie van kandidaten en invoeren van de lokale resultaten.
Ik ben niet betrokken geweest bij de opzet van deze studie, ook niet bij het studieprotocol, niet bij de resultaten en niet bij de interpretatie hiervan. Ik heb ook geen inzage in de resultaten van deze studie m.u.v. de inclusies vanuit mijn eigen kliniek. Ik ben minimaal betrokken geweest bij de publicatie: ik ben als lokale hoofdonderzoeker mede-auteur van het artikel en heb in die hoedanigheid de laatste versie vooraf aan het submitten wel gelezen. Ik heb geen invloed gehad op de publicatie en heb hier ook geen belang bij. Overigens is Harold Verhoeve ook betrokken bij deze studie (en ook mede-auteur van het artikel).
Tenslotte krijgt onze afdeling per geïncludeerde patiënt een (onkosten)vergoeding, ikzelf ontvang geen financiering hiervoor als lokale hoofdonderzoeker. Projectleider: NEE |
geen |
geen |
28/09/2022 |
Geen restricties. Mevrouw van Dongen is als meelezer betrokken bij de uitgangsvraag waarin de H2Olie studie mogelijk wordt gebruikt, op basis van de gegeven beschrijving van betrokkenheid aan deze studie worden geen restricties opgelegd. |
|
Moniek Twisk |
Gynaecoloog BovenIJ ziekenhuis |
Lesgeven O&G opleiding deel fertiliteit Amstelacademie |
Geen |
Geen |
Geen |
Geen |
Geen |
14/09/2022 |
Geen restricties. |
|
Noortje van den Boogaard |
Gynaecoloog Flevoziekenhuis Almere |
geen |
geen |
geen |
geen |
geen |
geen |
27/09/2022 |
Geen restricties. |
|
Carolien Boomsma |
gynaecoloog Bravis ziekenhuis. |
moet instructeur bestuur endometriose werkgroep opleidingsdagen opleiding gynaecologie |
geen. |
nee |
geen |
geen |
geen |
20/09/2022 |
Geen restricties. |
|
Bart Ballieux |
Laboratoriumspecialist Klinische Chemie en Endocrinologie Afdeling KCL, LUMC, Leiden |
nvt |
geen persoonlijke financiele belangen |
Geen relevante persoonlijke relaties die van invloed kunnen zijn op mijn adviezen |
geen |
Geen intellectuele belangen bij mijn adviezen |
Geen overige belangen |
10/01/2023 |
Geen restricties. |
|
Lianne Bijnevelt |
Fertiliteitsarts, St. Antonius ziekenhuis Utrecht |
Lid VVF |
Geen |
Geen |
Geen |
Geen |
Geen |
20/10/2022 |
Geen restricties. |
|
Hèlen Silvius |
Waarnemend huisarts bij huisartsenpraktijk Laila, Hadoks en De Limes Huisarts Docent bij PHEG LUMC (functie vervalt per 01-01-2023) Huisarts Docent bij Huisartsopleiding Amsterdam UMC per 01-11-2022) |
FMS, vertegenwoordiging NHG |
Geen |
Geen |
Geen |
Geen |
Ik heb kinderen. Ik hoop dat zij in de toekomst deze richtlijn niet nodig zullen hebben maar als dat wel zo is wil ik dat hij zo goed mogelijk is. |
18/10/2022 |
Geen restricties. |
|
Simone Sinjorgo |
Parttime medewerker patientenperspectief en -participatie bij Freya (vereniging voor mensen met vruchtbaarheidsproblemen) - betaald 14 uur https://www.freya.nl/over-freya/wie-we-zijn/de-werknemers. Ter info: door mijn functie bij Freya ben ik betrokken bij diverse richtlijnontwikkeling en/of onderzoeken op het gebied van fertiliteit. In de vorm van toelichten, belichten en/of vertegenwoordigen van alleen het patiëntenperspectief tav het bepaalde onderwerp, zoals bij deze 3 richtlijnen OFO, OHSS en mannelijke subfertiliteit. |
Lichaamsgericht psychosociaal therapeut - zzp eigen praktijk in Dongen-Vaart - geregistreerd therapeut RBCZ incl. AGB-codes. www.praktijkdediamant.nl
- Psychosociaal docent Bijscholing Instituut voor therapeuten - betaling via praktijk https://bivt.nl/?s=lichaamsgericht+coachen
- Psychosociaal docent vrouwencoach opleiding - betaling via praktijk https://www.devrouwencoach.nl/vrouwencoach-opleiding/ |
Geen |
Geen |
Geen |
Geen |
Geen |
03/12/2024 |
Geen restricties. |
|
Marloes Vermeulen |
Medewerker externe relaties, Freya |
N.v.t. |
Geen. |
Nee. |
Nee. |
N.v.t. |
Geen. |
27/09/2022 |
Geen restricties, mevrouw is niet langer werkzaam bij Freya en wordt vervangen door mevrouw Sinjorgo. |
Inbreng patiëntenperspectief
De werkgroep besteedde aandacht aan het patiëntenperspectief door het uitnodigen van Freya en de Patiëntenfederatie Nederland voor de invitational conference. Daarnaast zat namens Freya een afgevaardigde in de werkgroep. Het verslag van de invitational conference is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen (zie kop waarden en voorkeuren van patienten). De conceptrichtlijn is tevens voor commentaar voorgelegd aan Freya en de Patiëntenfederatie Nederland en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerde de werkgroep conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
Hysterosalpingografie olie versus water |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling breed toepasbaar is (5.000-40.000 patiënten), volgt ook dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.
Voor één module (Hysteroscopie) werd een adaptatie van de internationale ESHRE-richtlijn Unexplained infertility (Romualdi 2023) uitgevoerd. De werkwijze wordt in onderstaande alineas beschreven.
Werkwijze internationale richtlijn
De methode van de internationale richtlijn is beschreven in de ESHRE-guideline manual en de ESHRE-guideline Unexplained Infertility Annex 4: Methodology (p.107-111). Hier volgt een korte samenvatting.
Zoekstrategie
De zoekstrategie, uitgevoerd door een onafhankelijke zoekspecialist, is uitgevoerd in verschillende databases. Er is gezocht in MEDLINE/PubMed en de Cochrane bibliotheek tot 24 oktober 2022.
Literatuurselectie
De literatuur is voorgeselecteerd op titel (soms ook abstract) door de ESHRE-onderzoekspecialist en de uiteindelijke abstract-full tekst-selectie is gedaan door de werkgroep. Het selectieproces en de lijst van geëxcludeerde artikelen zijn terug te vinden in ‘Annex 6 Literature study’ van de ESHRE-guideline Unexplained infertility (los document). De zoekstrategie is bij de internationale werkgroep op te vragen.
Bewijskracht
De internationale werkgroep deed allereerst een kwaliteitscheck op elke individuele studie, om de studies eruit te halen die niet relevant waren of een zeer lage bewijskracht hadden (behalve als er geen betere studies beschikbaar waren). Hiervoor werden verschillende checklists gebruikt, zoals de AMSTAR-kwaliteitschecklist voor systematische reviews. Vervolgens werden evidence-tabellen opgesteld, door middel van het standaard template van Guidelines International Network (http://www.g-i-n.net/). The GRADE-methode werd gebruikt om een evidence-profiel op te stellen en ‘summary of findings’ tabellen. Deze zijn te vinden in ‘Annex 8 Summary of Evidence’ (los document). De kwaliteit van bewijs samen resulteerde in een ‘body of evidence’ van 4 niveaus:
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
De kwaliteit van bewijs werd beoordeeld door te beginnen met het studie design (trials of observationele studie) en vervolgens af te waarderen door factoren die de kwaliteit van bewijs verlagen en op te waarderen voor factoren die de kwaliteit van bewijs verhogen:
|
Bron van de ‘body of evidence’ |
Initiële kwaliteit van bewijs |
Factoren die de kwaliteit van bewijs verlagen |
Factoren die de kwaliteit van bewijs verhogen |
Kwaliteit van de ‘body of evidence’ |
|
RCT’s |
Hoog |
1. Risico op bias
|
1. Groot effect |
Hoog + + + + Gemiddeld + + + - Laag + + - - Zeer laag + - - -
|
|
Observationele studies |
Laag |
Aanbevelingen
Na de selectie en samenvatting van het bewijs werden door de internationale groep aanbevelingen opgesteld. Er werden ‘sterke’ en ‘conditionele’ aanbevelingen geformuleerd. Termen als ‘recommend’ en ‘concludes to’ werden gebruikt voor sterke aanbevelingen en ‘consider’ en ‘suggest’ werden gebruikt voor conditionele aanbevelingen. Interpretatie van sterke of conditionele aanbevelingen voor patiënten, behandelaars en beleidsmakers zijn als volgt:
|
|
Sterke aanbeveling |
Conditionele aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Conceptversie en publicatie
Nadat de conceptversie gereed was, werd het review proces gestart. De beoordelaars bestonden onder andere uit coördinators en afgevaardigden van de ESHRE SIG Reproductive Endocrinology, SIG Andrology, SIG Reproductive Surgery, SIG Safety and Quality in ART and SIG Nursing and Midwifery, contactpersonen en afgevaardigden van patiëntenverenigingen en organisaties door heel Europa. Tot slot zijn ook contactpersonen van internationale en nationale verenigingen met als aandachtsgebied IVF/ICSI in Europa benaderd. De lijst met peer-beoordelaars is te vinden in Annex 5 ‘Stakeholder consultation’ (p. 112-113) van de ESHRE-richtlijnUnexplained Infertility. De richtlijn is gepubliceerd op de ESHRE-website en in ‘Human Reproduction’.
Methode adaptatie
Toetsing internationale richtlijn op geschiktheid voor adaptatie
De internationale richtlijn is getoetst op basis van de adviezen uit het adviesrapport MSR 3.0. Dit bestond uit (1) onafhankelijkheid van de richtlijn, (2) methodologische kwaliteit, (3) inschatting of het adapteren leidt tot een kosten en/of tijdsbesparing ten opzichte van het ontwikkelen van een nieuwe richtlijn. Het stappenplan ‘adaptatietraject’ uit het adviesrapport MSR 3.0 is gevolgd om de tekst uit de internationale richtlijn naar een Nederlandse versie te adapteren.
Van bewijs naar aanbeveling
De literatuursamenvattingen zijn onvertaald overgenomen van de internationale richtlijn. De internationale aanbevelingen (‘recommendations’) en overwegingen (‘justifications’) zijn kritisch beoordeeld en aangepast naar de Nederlandse situatie. Hierbij is rekening gehouden met nieuwe literatuur, die verschenen is na het uitkomen van de ESHRE-richtlijn, en raakvlak met andere Nederlandse richtlijnen. Ook is rekening gehouden met de aspecten (1) balans tussen gewenste en ongewenste effecten, (2) waarden en voorkeuren van patiënten, (3) kostenaspecten (4) gelijkheid, (5) aanvaardbaarheid (ethisch en duurzaamheid) en haalbaarheid.
Zoekverantwoording
Zoekstrategie
Embase.com
|
No. |
Query |
Results |
|
#1 |
'hysterosalpingography'/exp OR 'tubal patency test'/exp OR hysterosalpingogr*:ti,ab,kw OR hysterosalpyngogr*:ti,ab,kw OR uterosalpingogr*:ti,ab,kw OR uterosalpyngogr*:ti,ab,kw OR salpingogr*:ti,ab,kw OR salpyngogr*:ti,ab,kw OR hsg:ti,ab,kw OR ('fallopian tube'/exp AND flush*:ti,ab,kw) OR (((tubal OR tuba OR tube*) NEAR/3 (flush* OR paten* OR test*)):ti,ab,kw) |
37445 |
|
#2 |
('contrast medium'/exp OR contrast*:ti,ab,kw OR radiocontrast*:ti,ab,kw OR media:ti,ab,kw OR medium:ti,ab,kw) AND ('oil'/exp OR 'water'/exp OR oil*:ti,ab,kw OR water*:ti,ab,kw OR aqu*:ti,ab,kw) OR oscm:ti,ab,kw OR obcm:ti,ab,kw OR wscm:ti,ab,kw OR wbcm:ti,ab,kw |
221227 |
|
#3 |
#1 AND #2 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
345 |
|
#4 |
#3 AND [2010-2024]/py |
119 |
|
#5 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
1020805 |
|
#6 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
4014801 |
|
#7 |
#4 AND #5 - SR |
9 |
|
#8 |
#4 AND #6 NOT #7 - RCT |
36 |
|
#9 |
#7 OR #8 |
45 |
Ovid/Medline
|
# |
Searches |
Results |
|
1 |
exp Hysterosalpingography/ or exp fallopian tube patency tests/ or hysterosalpingogr*.ti,ab,kf. or hysterosalpyngogr*.ti,ab,kf. or uterosalpingogr*.ti,ab,kf. or uterosalpyngogr*.ti,ab,kf. or salpingogr*.ti,ab,kf. or salpyngogr*.ti,ab,kf. or hsg.ti,ab,kf. or (exp Fallopian Tubes/ and flush*.ti,ab,kf.) or ((tubal or tuba or tube*) adj3 (flush* or paten* or test*)).ti,ab,kf. |
28242 |
|
2 |
((exp Contrast Media/ or contrast*.ti,ab,kf. or radiocontrast*.ti,ab,kf. or media.ti,ab,kf. or medium.ti,ab,kf.) and (exp Oils/ or exp Water/ or oil*.ti,ab,kf. or water*.ti,ab,kf. or aqu*.ti,ab,kf.)) or oscm.ti,ab,kf. or obcm.ti,ab,kf. or wscm.ti,ab,kf. or wbcm.ti,ab,kf. |
173960 |
|
3 |
(1 and 2) not (comment/ or editorial/ or letter/) not ((exp animals/ or exp models, animal/) not humans/) |
411 |
|
4 |
limit 3 to yr="2010 -Current" |
123 |
|
5 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
740450 |
|
6 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2714984 |
|
7 |
4 and 5 - SR |
9 |
|
8 |
(4 and 6) not 7 - RCT |
25 |
|
9 |
7 or 8 |
34 |