Tweedelijnsbehandeling BRAF-wild type gemuteerd irresectabel of gemetastaseerd stadium III/IV
Uitgangsvraag
Wat is de plaats van systemische therapie in de tweede lijns-behandeling van patiënten met een BRAF-wild type gemuteerd irresectabel of gemetastaseerd stadium III/IV melanoom?
Aanbeveling
Overweeg behandeling in studieverband.
Overweeg als tweedelijnsbehandeloptie voor patiënten met een BRAF wildtype irresectabel of gemetastaseerd melanoom volgende behandelopties: TIL- behandeling of anti-PD-1 blokkade met ipilimumab (indien niet gebruikt in de eerstelijns setting).
Individualiseer deze behandelbeslissing rekening houdend met het behandeldoel (kortetermijnvoordeel versus langetermijnvoordeel) en klinische kenmerken (lactaatdehydrogenase (LDH), betrokken organen, prestatiestatus (PS), tumorlast, snelheid van ziekteprogressie), comorbiditeiten, bijwerkingen van de verschillende therapieën en patiëntvoorkeuren.
Overwegingen
De cruciale uitkomstmaat overall survival in de context van patiënten met unresectable of gemetastaseerd stadium III/IV melanoom werd gerapporteerd door 5 RCTs die verschillende systemische behandelingen in de tweede lijn onderzochten.
OPTiM rapporteerde het effect van T-VEC in vergelijking met GM-CSF op overall survival bij patiënten met niet-receerbaar of gemetastaseerd stadium III/IV melanoom (Andtbacka, 2019; Andtbacka, 2015). Er werd daarbij geen klinisch relevant voordeel gevonden voor het gebruik van T-VEC. Het absolute verschil in mediane overall survival tussen behandeling met T-VEC versus behandeling met GM-CSF was 4.4 maanden met een hazard ratio 0.79 (95% CI 0.62–1.00). De bewijskracht van deze studie is zeer laag. Dit heeft te maken met het risico op bias (open-label studie design; meer patiënten stopten in de interventie groep; de rol van de sponsor) en door imprecisie, omdat het betrouwbaarheidsinterval de grens voor klinische besluitvorming omvat.
De studie rapporteerde ook het effect op adverse events. Er werd geen klinisch relevant verschil gevonden tussen de studiegroepen voor de uitkomst adverse events.
KEYNOTE-006 rapporteerde het effect van pembrolizumab (iedere 2 of 3 weken) in vergelijking met ipilimumab (iedere 3 weken) op overall survival bij patiënten met unresectable of gemetastaseerd stadium III/IV melanoom (Robert, 2019; Carlino, 2018; Schachter, 2017; Robert, 2015). Er werd daarbij geen klinisch relevant voordeel gevonden voor het gebruik van pembrolizumab. Het absolute verschil in mediane overall survival tussen behandeling met pembrolizumab versus behandeling met ipilimumab was 16.8 maanden met een hazard ratio van 0.73 (95% CI 0.61–0.88). De bewijskracht van deze studie is zeer laag. Dit heeft te maken met het risico op bias (open-label studie design; meer patiënten stopten in de controle groep; de rol van de sponsor) en door imprecisie, omdat de confidence interval de grens voor klinische besluitvorming omvat.
De studie rapporteerde ook het effect op progression free survival en adverse events. Voor de uitkomst progression free survival werd een klinisch relevant voordeel gevonden voor behandeling met pembrolizumab. Het absolute verschil in mediane progressievrije overleving was 5.0 maanden (HR 0.57; 95% CI 0.48–0.67). Er werd geen klinisch relevant verschil gevonden tussen de studiegroepen voor de uitkomst adverse events.
MDX010-20 rapporteerde het effect van ipilimumab met een gp100 peptide vaccine en ipilimumab zonder een gp100 peptide vaccine in vergelijking met alleen gp100 op overall survival bij patiënten met niet-receerbaar of gemetastaseerd stadium III/IV melanoom (Revicki, 2012; Hodi, 2010). Er werd daarbij een klinisch relevant voordeel gevonden voor het gebruik van ipilimumab met een gp100 peptide vaccine en voor ipilimumab zonder een gp100 peptide vaccine in vergelijking met gp100 alleen. Het absolute verschil in mediane overall survival tussen behandeling met ipilimumab met een gp100 peptide vaccine versus behandeling met alleen gp100 was 3.6 maanden met een hazard ratio van 0.68 (95% CI 0.55–0.85). Het absolute verschil in mediane overall survival tussen behandeling met ipilimumab zonder een gp100 peptide vaccine versus behandeling met alleen gp100 was 3.7 maanden met een hazard ratio van 0.66 (0.51–0.87). De bewijskracht van deze studie is laag. Dit heeft te maken met het risico op bias (de rol van de sponsor in deze studie) en door imprecisie omdat de confidence interval de grens voor klinische besluitvorming omvat.
De studie rapporteerde ook het effect op progression free survival, adverse events en kwaliteit van leven. Er werd geen klinisch relevant verschil gevonden tussen de studiegroepen voor de uitkomsten progression free survival, adverse events en kwaliteit van leven.
NCT02278887 rapporteerde het effect van tumor-infiltrating lymphocytes (TILs) versus ipilimumab op overall survival bij patiënten met unresectable of gemetastaseerd stadium III/IV melanoom (Rohaan, 2022). Er werd daarbij geen klinisch relevant voordeel gevonden voor het gebruik van TILs. Het absolute verschil in mediane overall survival was 6.9 maanden met een hazard ratio van 0.83 (95% CI, 0.54 to 1.27). De bewijskracht van deze studie is zeer laag. Dit heeft te maken met het risico op bias (onduidelijke randomisatie, open-label studie design, en doordat meer patiënten in de controle groep de behandeling stopten in vergelijking met de interventie groep) en imprecisie.
De studie rapporteerde ook het effect op progression free survival, adverse events en kwaliteit van leven. Een langere mediane progression free survival werd gevonden voor patiënten in de TILs groep, met een absoluut verschil van 4.1 maanden met patiënten in de ipilimumab groep (HR 0.50; 95% CI 0.35 to 0.72). Behandeling met TILs resulteerde in een hoger percentage patiënten met adverse events (risk difference: 0.43; 95% CI 0.32, 0.54; NNH=2). Er werd geen klinisch relevant verschil gevonden tussen de studiegroepen voor de uitkomst kwaliteit van leven.
Checkmate-037 rapporteerde het effect van nivolumab versus investigator’s choice chemotherapy (ICC; dacarbazine or carboplatin plus paclitaxel) op overall survival bij patiënten met unresectable of gemetastaseerd stadium III/IV melanoom (Weber, 2015; Larkin 2018). Er werd daarbij geen klinisch relevant voordeel gevonden voor het gebruik van nivolumab. Het absolute verschil in mediane overall survival was 1.3 maanden met een hazard ratio van 0.95 (95.54% CI 0.73 to 1.24). De bewijskracht van deze studie is zeer laag. Dit heeft te maken met het risico op bias (open-label studie design; doordat meer patiënten in de interventie groep de behandeling stopten in vergelijking met de controle groep; de rol van de sponsor in deze studie) en imprecisie.
De studie rapporteerde ook het effect op progression free survival, adverse events en kwaliteit van leven. Er werd geen klinisch relevant verschil gevonden tussen de studiegroepen voor de uitkomsten progression free survival, adverse events en kwaliteit van leven.
Kwaliteit van bewijs
T-VEC versus GM-CSF
De overall kwaliteit van bewijs is zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaat overall survival.
Pembrolizumab every 2 weeks or every 3 weeks vergeleken met ipilimumab
De overall kwaliteit van bewijs is zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaat overall survival.
Ipilimumab with or without a gp100 peptide vaccine vergeleken met gp100 alone
De overall kwaliteit van bewijs is laag. Dit betekent dat we onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaat overall survival.
Tumor-infiltrating lymphocytes (TILs) versus ipilimumab
De overall kwaliteit van bewijs is laag. Dit betekent dat we onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaat overall survival.
Nivolumab versus investigator’s choice chemotherapy
(ICC; dacarbazine of carboplatin plus paclitaxel)
De overall kwaliteit van bewijs is zeer laag. Dit betekent dat we zeer onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaat overall survival.
Ondanks de vooruitgang in de behandeling van irresectabel of gemetastaseerd melanoom, blijven veel vragen onbeantwoord en voor een belangrijke deel van de patiënten blijft de prognose slecht. Inclusie behandeling van irresectabel of gemetastaseerd melanoom patienten in klinische studies blijft daarom de hoogste prioriteit in alle settings.
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
Bij de behandeling van patiënten met een irresectabel of gemetastaseerd stadium III/IV melanoom dient zorgvuldig rekening te worden gehouden met de waarden en voorkeuren van de patiënt. De keuze voor deelname aan klinische studies of voor tweedelijnsbehandelopties – zoals TIL-therapie, anti-PD-1-blokkade met ipilimumab wordt bij voorkeur afgestemd op individuele patiëntkenmerken en specifieke behandeldoelen.
Professioneel perspectief
Factoren zoals het gewenste behandeldoel (kortetermijn- of langetermijnvoordeel), klinische kenmerken (bijvoorbeeld lactaatdehydrogenase-niveaus, betrokken organen, prestatiestatus, tumorlast en progressiesnelheid), evenals comorbiditeiten spelen een cruciale rol bij deze behandelbeslissing. Door deze aspecten zorgvuldig af te wegen in lijn met de voorkeuren van de patiënt kan een optimaal behandeltraject worden gekozen dat zowel klinische effectiviteit waarborgt als aansluit bij de persoonlijke waarden van de patiënt.
TIL-therapie is een intensieve behandeloptie voor geselecteerde patiënten (<76 jaar, PS 0-1, LDH <2 ULN en 1 eerdere anti-PD-1 bevattende behandeling) die de bijwerkingen ervan kunnen verdragen. Er is (nog) geen EMA goedkeuring voor deze behandeling.
Als de eerstelijnsbehandeling anti-PD-1-monotherapie was of als patiënten een primaire refractaire ziekte hadden na anti-PD-1-therapie, is ipilimumab en nivolumab een optie op basis van de resultaten van de fase II SWOG S1616-studie. In deze studie werd behandeling met ipilimumab en nivolumab geassocieerd met een statistisch significante verbetering van de PFS vergeleken met ipilimumab alleen (HR 0,63; 90% BI 0,41-0,97; p = 0,04).
Kostenaspecten
Vanwege geheime prijsafspraken, kan de exacte impact op het geneesmiddelenbudget niet worden vastgesteld, maar het staat vast dat deze impact hoog is. Het huidig prijsniveau wordt echter acceptabel geacht in verhouding tot de effectiviteit van de behandeling. Een lagere prijs van de behandelingen zou desondanks in alle opzichten zeer wenselijk en naar mening van de werkgroep zelfs noodzakelijk zijn, mede met het oog op de komende ontwikkelingen en het betaalbaar houden en borgen van een goede kwaliteit van de zorg in de nabije toekomst.
Haalbaarheid/aanvaardbaarheid
Bij de behandeling van patiënten met een irresectabel of gemetastaseerd stadium III/IV melanoom is het van belang niet alleen te kijken naar klinische effectiviteit en patiëntvoorkeuren, maar ook naar de haalbaarheid en aanvaardbaarheid van de aanbevolen behandelopties. Deelname aan klinische studies kan voor sommige patiënten een haalbare optie zijn, mits er toegang is tot geschikte onderzoeksfaciliteiten en de patiënt bereid is de mogelijk intensieve studieverplichtingen te dragen. Voor patiënten met een BRAF wildtype melanoom kunnen tweedelijnsopties zoals TIL-therapie of anti-PD-1-blokkade met ipilimumab passend zijn, maar de haalbaarheid van deze therapieën wordt mede bepaald door de beschikbaarheid en toegankelijkheid van specialistische zorg en middelen. De aanvaardbaarheid van deze behandelopties hangt bovendien sterk samen met het behandeldoel en de verwachte belasting voor de patiënt: sommige patiënten kunnen de voorkeur geven aan behandelingen met een potentieel kortetermijnvoordeel en lagere bijwerkingenlast, terwijl anderen bereid zijn intensievere therapieën te overwegen in ruil voor een mogelijke langere overlevingswinst. Zo kunnen haalbaarheid en aanvaardbaarheid per patiënt variëren, wat zorgvuldige overweging van hun persoonlijke en klinische omstandigheden vereist om een passend behandeltraject te waarborgen.
Rationale van de aanbevelingen
De werkgroep is van mening dat deelname aan klinische studies in de behandeling van irresectabel of gemetastaseerd stadium III/IV melanoom de hoogste prioriteit heeft, gezien de sombere prognose voor een groot deel van de patiënten en de noodzaak om effectiviteit en aanvaardbaarheid van behandelingen verder te optimaliseren. Hierbij is het essentieel om patiëntwaarden en individuele klinische kenmerken leidend te laten zijn, zodat behandelbeslissingen aansluiten bij zowel haalbaarheid als de persoonlijke voorkeuren van de patiënt.
Onderbouwing
Conclusies / Summary of Findings
T-VEC versus GM-CSF
Overall survival
|
Very low GRADE |
The evidence is very uncertain about the effect of T-VEC on overall survival compared to treatment with GM-CSF in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Sources: Andtbacka, 2019; Andtbacka, 2015 |
Adverse events
|
Very low GRADE |
The evidence is very uncertain about the effect of T-VEC on adverse events compared to treatment with GM-CSF in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Sources: Andtbacka, 2019; Andtbacka, 2015 |
Pembrolizumab every 2 weeks or every 3 weeks compared to ipilimumab
Overall survival
|
Very low GRADE |
The evidence is very uncertain about the effect of pembrolizumab every 2 weeks or every 3 weeks on overall survival compared to treatment with ipilimumab in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Sources: Robert, 2019; Carlino, 2018; Schachter, 2017; Robert, 2015 |
Progression free survival
|
Low GRADE |
Pembrolizumab every 2 weeks or every 3 weeks may increase progression free survival compared to treatment with ipilimumab in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Sources: Robert, 2019; Carlino, 2018; Schachter, 2017; Robert, 2015 |
Adverse events
|
Very low GRADE |
The evidence is very uncertain about the effect of pembrolizumab every 2 weeks or every 3 weeks on adverse events compared to treatment with ipilimumab in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Sources: Robert, 2019; Carlino, 2018; Schachter, 2017; Robert, 2015 |
Ipilimumab with or without a gp100 peptide vaccine compared to gp100 alone
Overall survival
|
Low GRADE |
Ipilimumab with or without a gp100 peptide vaccine may increase overall survival compared to treatment with gp100 alone in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma but the evidence is very uncertain receiving second line systemic therapy.
Source: Hodi, 2010 |
|
Low GRADE |
Ipilimumab with a gp100 peptide vaccine may have little to no effect on overall survival compared to treatment Ipilimumab alone in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma but the evidence is very uncertain receiving second line systemic therapy.
Source: Hodi, 2010 |
Progression free survival
|
Low GRADE |
Ipilimumab with or without a gp100 peptide vaccine may increase progression free survival compared to treatment with gp100 alone in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Source: Hodi, 2010 |
Adverse events
|
Low GRADE |
Ipilimumab with or without a gp100 peptide vaccine may increase adverse events slightly compared to treatment with gp100 alone in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Source: Hodi, 2010 |
Quality of Life
|
Low GRADE |
Ipilimumab with or without a gp100 peptide vaccine may may result in little to no difference compared to treatment with gp100 alone in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Source: Revicki, 2012 |
Tumor-infiltrating lymphocytes (TILs) versus ipilimumab
Overall survival
|
Low GRADE |
Treatment with tumor-infiltrating lymphocytes (TILs) may result in little to no difference in overall survival compared to ipilimumab in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Source: Rohaan, 2022 |
Progression free survival
|
Low GRADE |
Treatment with tumor-infiltrating lymphocytes (TILs) may increase progression free survival compared to ipilimumab in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Source: Rohaan, 2022 |
Adverse events
|
Moderate GRADE |
Treatment with tumor-infiltrating lymphocytes (TILs) likely increases adverse events compared to ipilimumab in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Source: Rohaan, 2022 |
Quality of life
|
Moderate GRADE |
Treatment with tumor-infiltrating lymphocytes (TILs) likely results in little to no difference in quality of life compared to ipilimumab in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Source: Rohaan, 2022 |
Nivolumab versus investigator’s choice chemotherapy
(ICC; dacarbazine or carboplatin plus paclitaxel)
Overall survival
|
Very low GRADE |
The evidence is very uncertain about the effect of treatment with nivolumab on overall survival compared to treatment with investigator’s choice chemotherapy in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Sources: Weber 2015; Larkin 2018 |
Progression free survival
|
Very low GRADE |
The evidence is very uncertain about the effect of treatment with nivolumab on progression free survival compared to treatment with investigator’s choice chemotherapy in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Sources: Weber 2015; Larkin 2018 |
Adverse events
|
Very low GRADE |
The evidence is very uncertain about the effect of treatment with nivolumab on adverse events compared to treatment with investigator’s choice chemotherapy in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Sources: Weber 2015; Larkin 2018 |
Quality of life
|
Low GRADE |
Treatment with nivolumab may have little to no effect on quality of life compared to investigator’s choice chemotherapy in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving second line systemic therapy.
Sources: Weber 2015; Larkin 2018 |
Samenvatting literatuur
Five randomized controlled trials that studied clinical outcomes of second line systemic therapy in patients with unresectable or metastatic stadium III/IV melanoma with a BRAF-wild type were included in the literature analysis.
Description of studies
The study characteristics of the included trials are summarized in Table 1 in the main module Systematische therapie.
Andtbacka, 2019 /Andtbacka, 2015 - OPTiM is a randomized open-label phase 3 trial at 64 sites in the United States, the United Kingdom, Canada, and South Africa. This trial evaluated outcomes after treatment with talimogene laherparepvec (T-VEC) compared with granulocyte macrophage colony-stimulating factor (GM-CSF) in patients with unresectable, stage IIIB/C/IV melanoma with ≥1 lesion that was suitable for direct or ultrasound-guided injection. Patients were randomized to T-VEC (at the approved dose) (n=295 (68%)) of subcutaneous recombinant GM-CSF (n=141 (32%)). The median age was 63 years in the T-VEC group and 64 years in the GM-CSF group. The percentage of males was 59% in the T-VEC group and 55% in the GM-CSF group. Of 204 of the 295 (69%) in the T-VEC group, and 95 of the 141 (67%) in the GM-CSF group, the BRAF mutation status was unknown. For 157 of the 295 (53%) patients in the T-VEC group, and 76 of the 141 (54%) in the GM-CSF group, this was a second line therapy or later. OS and AEs were reported after a median follow-up of 49 months in the final analysis of OS. In this literature analysis the median OS is analysed.
Robert, 2019 / Carlino, 2018 / Schachter, 2017 /Robert, 2015 - KEYNOTE-006 is an international, randomized, open-label phase 3 study performed in 16 countries. In this trial treatment with pembrolizumab versus ipilimumab was studied, to compare PD-1 inhibition with CTLA-4 blockade in patients with unresectable stage III/IV melanoma. Patients were randomized to pembrolizumab at a dose of 10 mg/kg of body weight every 2 weeks (n= 279); pembrolizumab at a dose of 10 mg/kg every 3 weeks (n=277); or ipilimumab at a dose of 3 mg/kg every 3 weeks (n=278). The mean age was 61 years in the pembrolizumab every 2 weeks group, 63 years in the pembrolizumab every 3 weeks group and 62 years in the ipilimumab group. The percentage of males was 57.7 %, 62.8%, and 58.3% for the three groups, respectively. Robert (2015) reported on OS, PFS, and AEs after a median follow-up of 7.9 months. Schachter (2017) reported updated results after a median follow-up of 22.9 months. Carlino (2018) reported updated outcomes by line of therapy and programmed death ligand 1 expression after a median follow-up of 33.9 months. Robert (2019) reported updated results of OS, PFS, and AES after a median follow-up of 57.7 months. In this literature analysis the median outcomes for OS and PFS are analysed and the last endpoints for OS and PFS (2-year OS rates and 2-year PFS rates) are described.
Revicki, 2012 / Hodi, 2010 - MDX010-20 is a randomized, double-blind phase 3 study that enrolled patients at 125 centres in 13 countries in North America, South America, Europe, and Africa. This trial evaluated the effect of ipilimumab with or without a gp100 peptide vaccine on overall survival compared to gp100 alone in patients with unresectable stage III or IV melanoma who received a previous therapeutic regimen containing one or more of the following: dacarbazine, temozolomide, fotemustine, carboplatin, or interleukin-2. Patients were randomized to ipilimumab, at a dose of 3 mg/kg of body weight, plus a gp100 peptide vaccine (n=403); ipilimumab plus gp100 placebo (n=137); or gp100 plus ipilimumab placebo (n=136). The mean age was 55.6 years in the ipilimumab plus gp100 peptide vaccine group, 56.8 years in the ipilimumab group and 57.4 years in the gp100 group. The percentage of males was 61.3 %, 59.1%, and 53.7% for the three groups, respectively. Hodi (2010) reported on OS, PFS, and AEs after a follow up time of 55 months. Revicki (2012) reported health related QoL outcomes during the 12 week treatment induction period. In this literature analysis the median outcomes for OS and PFS are analysed and the last endpoint for OS (2-year OS rates) are described.
Rohaan (2022) - NCT02278887 is a multicenter, open-label, phase 3, randomized trial with two participating clinical sites. In trial, tumor-infiltrating lymphocytes (TILs) were compared with ipilimumab in patients with unresectable or metastatic stage IIIC or IV cutaneous melanoma, with ≥1 lesions that could be surgically removed for generation of TILs. Patients were randomized to adoptive cell therapy with TILs (n=84) or ipilimumab at a dose of 3 mg/kg every 3 weeks (n=84). The median age was 59 years in both study groups. The percentage of males was 56% in the TILS group and 63% in the ipilimumab group. OS, PFS, AEs, and QoL were reported after a median follow-up of 33 months. In this literature analysis the median outcomes for OS and PFS are analysed and the last endpoints for OS and PFS (2-year OS rates and 6-month PFS rates) are described.
Weber (2015) / Larkin (2018) - CHECKMATE-037 described a randomized, controlled, open-label, phase III study, which was conducted in 90 sites in 14 countries with a median follow-up of approximately 2 years. They evaluated the efficacy and safety of second-line nivolumab versus investigator’s choice chemotherapy (ICC) in patients with metastatic melanoma who experienced progression after treatment with first-line ipilimumab (plus a BRAF inhibitor, if BRAF-mutation positive). A total of 405 patients were randomized 2:1 to receive nivolumab (n= 272, 3 mg/kg every two weeks) or ICC (n = 133, dacarbazine 1,000 mg/m2 every 3 weeks or carboplatin area under the curve 6 plus paclitaxel 175 mg/m2 every 3 weeks). The median age was 59 (23-88) years in the nivolumab group and 62 (29-85) years in the ICC group. In the nivolumab group 65% was male, compared to 64% in the ICC group. Of the 272 patients that received nivolumab, 212 (78%) had BRAF wild type. Of the 133 patients that received ICC, 104 (78%) had BRAF wild type. The following relevant outcomes were reported, OS, PFS, number of patients with serious AEs and QoL. For OS, the researchers performed a subgroup analysis on BRAF status.
Results
Overall survival (OS) – Critical outcome measure
Five of the five included studies reported on OS.
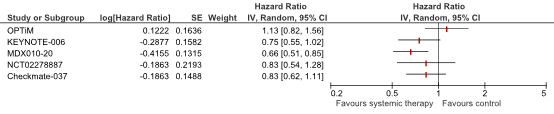
OPTiM reported the effect of T-VEC versus GM-CSF on OS in the second-line or greater treatment without analyzing subgroups based on BRAF mutation status. The absolute difference between the T-VEC group (17.1 months) and the GM-CSF group (23.2 months) was 6.1 months in favor of the GM-CSF group with a HR of 1.13 (95% CI 0.82–1.57). This difference was not considered clinically relevant according to the PASKWIL criteria.
KEYNOTE-006 reported the effect of pembrolizumab every 2 weeks or pembrolizumab every 3 weeks compared to ipilimumab every 3 weeks on OS. The 2-year OS rates were 55% in the pembrolizumab-every-2-weeks group, 55% in the pembrolizumab-every-3-weeks group, and 43% in the ipilimumab-every-3-weeks group. Treatment with pembrolizumab resulted in a longer median OS than treatment with ipilimumab. In patients receiving second-line therapy the absolute difference between the combined pembrolizumab groups (23.5 months) and the ipilimumab group (13.6 months) was 9.9 months with a HR of 0.75 (95% CI 0.55–1.03). This difference was not considered clinically relevant according to the PASKWIL criteria.
MDX010-20 reported the effect of ipilimumab with a gp100 peptide vaccine and ipilimumab without a gp100 peptide vaccine compared to gp100 alone on OS. The 2-year OS rates were 21.6% in the ipilimumab with a gp100 peptide vaccine group, 23.5% in the ipilimumab group, and 13.7% in the gp100 alone group. Treatment with ipilimumab with or without a gp100 peptide vaccine resulted in a longer median OS compared to treatment with gp100 alone. The absolute difference between treatment with ipilimumab with a gp100 peptide vaccine (10.0 months) and treatment with gp100 alone (6.2 months) was 3.8 months with a HR of 0.68 (95% CI 0.55–0.85). This difference was considered clinically relevant according to the PASKWIL criteria. The absolute difference between treatment with ipilimumab without gp100 (10.1 months) compared to treatment with gp100 peptide vaccine alone was 3.7 months with a HR of 0.66 (0.51–0.87). This difference was considered clinically relevant according to the PASKWIL criteria. Treatment with ipilimumab with a gp100 peptide vaccine resulted in a similar median OS compared to treatment with ipilimumab plus placebo, with an absolute difference of 0.1 months and HR of 1.04 (95% CI 0.83–1.30). This difference was not considered clinically relevant according to the PASKWIL criteria.
NCT02278887 reported the effect of tumor-infiltrating lymphocytes (TILs) versus ipilimumab on OS. The 2-year OS rates were 54.3% in the TILs group and 44.1% in the ipilimumab group. Treatment with TILs resulted in a longer median OS compared to treatment with ipilimumab. The absolute difference between the TILs group and the ipilimumab group was 6.9 months with a HR of 0.83 (95% CI, 0.54 to 1.27). This difference was not considered clinically relevant according to the PASKWIL criteria.
Checkmate-037 reported the effect of nivolumab versus investigator’s choice chemotherapy (ICC; dacarbazine or carboplatin plus paclitaxel) on OS in patients with BRAF wild type. The absolute difference in median OS between the nivolumab group (17.97 months) compared to the ICC group (14.32 months) was 3,65 with a HR of 0.83 (0.62 to 1.11). This difference was not considered clinically relevant according to the PASKWIL criteria.
Figure 1. Forest plot of median overall survival for second line systemic therapy versus placebo, other systemic therapy, or best supportive care in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving first line systemic therapy
a For KEYNOTE-006 the HR for combined pembrolizumab versus ipilimumab is shown.
b For MDX010-20 the HR for ipilimumab without gp100 versus gp100 vaccine alone is shown.
Progression free survival – important outcome measure
Four of the five included studies reported on PFS.
KEYNOTE-006 reported the effect of pembrolizumab every 2 weeks or pembrolizumab every 3 weeks compared to ipilimumab every 3 weeks on PFS. The 2-year PFS rates were 31% in the pembrolizumab-every-2-weeks group, 28% in the pembrolizumab-every-3-weeks group, and 14% in the ipilimumab-every-3-weeks group. Treatment with pembrolizumab resulted in a longer median PFS than treatment with ipilimumab. The absolute difference between the combined pembrolizumab groups and the ipilimumab group was 5.0 months with a HR of 0.57 (95% CI 0.48–0.67). This difference was considered clinically relevant according to the PASKWIL criteria.
MDX010-20 reported the effect of ipilimumab with a gp100 peptide vaccine plus ipilimumab without a gp100 peptide vaccine compared to gp100 alone on PFS. Median PFS was comparable between the three study groups. After the first assessment of progression at week 12 there was a separation between the curves. There was a 19% reduction in the risk of progression in the ipilimumab plus gp100 group, as compared with gp100 alone with a HR of 0.81. There was a 36% reduction in risk of progression in the ipilimumab alone group as compared with the gp100 alone group with a HR of 0.64. According to the PASKWIL criteria we could not assess clinical relevance (median OS in the control group was < 12 months).
NCT02278887 reported the effect of tumor-infiltrating lymphocytes (TILs) versus ipilimumab on PFS. The 6-month PFS rates were 52.7% in the TILs group and 21.4% in the ipilimumab group. Treatment with TILs resulted in a longer median PFS compared to treatment with ipilimumab. The absolute difference between the TILs group and the ipilimumab group was 4.1 months with a HR of 0.50 (95% CI, 0.35 to 0.72). This difference was considered clinically relevant according to the PASKWIL criteria.
Checkmate-037 reported the effect of nivolumab versus investigator’s choice chemotherapy (ICC; dacarbazine or carboplatin plus paclitaxel) on PFS. Treatment with nivolumab resulted in a shorter median PFS compared to treatment with ICC. The absolute difference was 0.6 months with a HR of 1.0 (95.1% CI, 0.78 to 1.44). This difference was not considered clinically relevant according to the PASKWIL criteria.
Figure 2. Forest plot of median progression free survival for second line systemic therapy versus placebo, other systemic therapy, or best supportive care in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving first line systemic therapy
a For KEYNOTE-006 the HR for combined pembrolizumab versus ipilimumab is shown.
b MDX010-20 did not report the 95% CI of the HR and therefore the HR is not shown.
Treatment related adverse events (AEs) grade ≥ 3 - Important outcome
Five of the five included studies reported on AEs. The percentages of treatment related AEs grade ≥3 ranged from 14% to 100%.
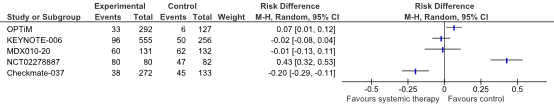
OPTiM reported the effect of T-VEC versus GM-CSF on AEs. Treatment with T-VEC resulted in a higher percentage of treatment related AEs grade ≥3 compared to treatment with GM-CSF. The risk difference between T-VEC and GM-CSF is 0.07 (95% CI 0.02, 0.12; NNH=14) favoring treatment with GM-CSF. This difference is not considered clinically relevant according to the PASKWIL criteria.
KEYNOTE-006 reported the effect of pembrolizumab every 2 weeks or pembrolizumab every 3 weeks compared to ipilimumab every 3 weeks on AEs. Treatment with pembrolizumab (pooled groups) resulted in a lower percentage of treatment related AEs grade ≥3 compared to treatment with ipilimumab. The risk difference between pembrolizumab (pooled groups) and ipilimumab is -0.01 (95% CI -0.06, 0.05; NNH=100) favoring treatment with pembrolizumab. This difference is not considered clinically relevant according to the PASKWIL criteria.
MDX010-20 reported the effect of ipilimumab with a gp100 peptide vaccine plus ipilimumab without a gp100 peptide vaccine compared to gp100 alone on AEs. Treatment with ipilimumab with a gp100 peptide vaccine resulted in a higher percentage of treatment related AEs grade ≥3 compared to treatment with gp100 alone. The risk difference between ipilimumab with a gp100 peptide vaccine and gp100 alone is 0.05 (95% CI -0.03, 0.13; NNH= 20) favoring treatment with gp100 alone. This difference is not considered clinically relevant according to the PASKWIL criteria. The risk difference between ipilimumab without a gp100 peptide vaccine and gp100 alone is 0.14 (95% CI 0.03, 0.25; NNH= 7) favoring treatment with gp100 alone. This difference is not considered clinically relevant according to the PASKWIL criteria.
NCT02278887 reported the effect of tumor-infiltrating lymphocytes (TILs) versus ipilimumab on AEs. Treatment with TILs resulted in a higher percentage of treatment related AEs grade ≥3 compared to treatment with ipilimumab. The risk difference between TILs and ipilimumab is 0.43 (95% CI 0.32, 0.54; NNH=2) favoring treatment with ipilimumab. This difference is considered clinically relevant according to the PASKWIL criteria.
Checkmate-037 reported the effect of nivolumab versus investigator’s choice chemotherapy (ICC; dacarbazine or carboplatin plus paclitaxel) on AES. Treatment with nivolumab resulted in a higher percentage of treatment related AEs grade ≥3 compared to treatment with ICC. The risk difference between nivolumab and ICC is 0.17 (95% CI 0.09, 0.25; NNH=6) favoring treatment with ICC. This difference is not considered clinically relevant according to the PASKWIL criteria.
Figure 3. Forest plot of adverse events for second line systemic therapy versus placebo, other systemic therapy, or best supportive care in patients with BRAF-wild type unresectable or metastatic stadium III/IV melanoma receiving first line systemic therapy
a For KEYNOTE-006 the risk difference for combined pembrolizumab versus ipilimumab is shown.
b For MDX010-20 the risk difference for ipilimumab without gp100 versus gp100 vaccine alone is shown.
Quality of life (QoL) - Important outcome
Three studies reported the effect of second line systemic therapy on QoL.
MDX010-20 analysed the effect of ipilimumab with or without a gp100 peptide vaccine compared to gp100 alone on health-related quality of life (HRQL) with the EORTC QLQ-C30. Mean changes of baseline to week 12 scores for function, global health status, and symptoms were analysed. These were categorized as “no change” (0–5), “a little” (5–10 points), “moderate” (10–20 points), and “very much” (>20). In general, the authors observed “no change” or “a little” impairment in the ipilimumab plus gp100 and ipilimumab alone groups. The study showed significant differences in constipation, favouring ipilimumab (p<0.05). This difference is not considered clinically relevant (difference less than 10 points). In the gp100 alone group, moderate to large changes for global health, role function, fatigue, and pain were observed. These differences between the treatment arms are not considered clinically relevant (difference less than 10 points). The authors conclude that ipilimumab with or without gp100 vaccine does not have a significant negative HRQL impact during the treatment induction phase relative to gp100 alone in stage III or IV melanoma patients.
NCT02278887 of tumor-infiltrating lymphocytes (TILs) versus ipilimumab on QoL. In this study, Health-related quality of life (HRQL) was measured with the EORTC Quality-of- Life Questionnaire Core 15 palliative care. In this questionnaire, higher scores on the global quality-of-life and functioning scales indicate better functioning and higher scores on the symptom scales indicate higher levels of symptom burden. Higher mean scores were observed after treatment among patients in the TIL group on the global health-related quality-of life (difference 7.7), physical functioning (difference 2.9), and emotional functioning (difference 9.7) domains compared to patients in the ipilimumab group. These differences are not considered clinically relevant (differences less than 10 points). Lower symptoms scores were observed after treatment among patients in the TIL group for fatigue, pain, and insomnia compared to patients in the ipilimumab group, with differences still observed at week 60. These differences are not considered clinically relevant (differences less than 10 points). Higher symptom scores of nausea and vomiting were observed among patients in the TIL group compared to patients in the ipilimumab group. This difference was not considered clinically relevant (difference less than 10 points).
Checkmate-037 analysed the effect of nivolumab versus investigator’s choice chemotherapy (ICC; dacarbazine or carboplatin plus paclitaxel) on QoL. HRQL was assessed using the EORTC QLQ-C30 version 3 and EuroQoL EQ-5D summary index and visual analog scale. The study showed that quality of life in patients on nivolumab remained stable for all EORTC QLQ-C30 individual scales during the treatment course. No scores reached the minimal important difference of ≥10 points. The authors stated that no clinically significant improvement was observed for either the EuroQoL EQ-5D utility index or the EuroQoL EQ-5D visual analog scale for nivolumab. In the article the authors mention that at 12 weeks, the ICC group demonstrated a clinically significant decrease in the EuroQoL EQ-5D utility index. These data are not shown in the article or supplementary material.
Level of evidence of the literature
There are four levels of evidence: high, moderate, low, and very low. RCTs start at a high level of evidence.
T-VEC versus GM-CSF
The level of evidence regarding the outcome measure overall survival was downgraded by three levels because of study limitations (risk of bias -2); the confidence interval encloses the threshold for a clinically relevant effect and no clinically relevant effect (imprecision). Therefore, the level of evidence was graded as very low.
The level of evidence regarding the outcome measure adverse events was downgraded by three levels because of study limitations (risk of bias -2) and was downgraded by one level because the optimal information size is not met (imprecision). Therefore, the level of evidence was graded as very low.
Pembrolizumab every 2 weeks or every 3 weeks compared to ipilimumab
The level of evidence regarding the outcome measure overall survival was downgraded by three levels because of study limitations (risk of bias -2); the confidence interval encloses the threshold for a clinically relevant effect and no clinically relevant effect (imprecision). Therefore, the level of evidence was graded as very low.
The level of evidence regarding the outcome measure progression free survival was downgraded by two levels because of study limitations (risk of bias -2). Therefore, the level of evidence was graded as low.
The level of evidence regarding the outcome measure adverse events was downgraded by three levels because of study limitations (risk of bias -2) and was downgraded by one level because the optimal information size is not met (imprecision). Therefore, the level of evidence was graded as very low.
Ipilimumab with or without a gp100 peptide vaccine compared to gp100 alone
The level of evidence regarding the outcome measure overall survival was downgraded by two levels because of study limitations (risk of bias) and the confidence interval encloses the threshold for a clinically relevant effect and no clinically relevant effect (imprecision). Therefore, the level of evidence was graded as low.
The level of evidence regarding the outcome measure progression free survival was downgraded by two levels because of study limitations (risk of bias) and because we could not asses clinical relevance according to the PASKWIL criteria (imprecision). Therefore, the level of evidence was graded as low.
The level of evidence regarding the outcome measure adverse events was downgraded by two levels because of study limitations (risk of bias) and was downgraded by one level because the optimal information size is not met (imprecision). Therefore, the level of evidence was graded as low.
The level of evidence regarding the outcome measure quality of life was downgraded by two levels because of study limitations (risk of bias) and was downgraded by one level because the optimal information size is not met (imprecision). Therefore, the level of evidence was graded as low.
Tumor-infiltrating lymphocytes (TILs) versus ipilimumab
The level of evidence regarding the outcome measure overall survival was downgraded by two levels because of study limitations (risk of bias) and because the confidence interval encloses the threshold for a clinically relevant effect and no clinically relevant effect (imprecision). Therefore, the level of evidence was graded as low.
The level of evidence regarding the outcome measure progression free survival was downgraded by two levels because of study limitations (risk of bias) and because the confidence interval encloses the threshold for a clinically relevant effect and no clinically relevant effect (imprecision). Therefore, the level of evidence was graded as low.
The level of evidence regarding the outcome measure adverse events was downgraded by one level because of study limitations (risk of bias). Therefore, the level of evidence was graded as moderate.
The level of evidence regarding the outcome measure quality of life was downgraded by one level because of study limitations (risk of bias). Therefore, the level of evidence was graded as moderate.
Nivolumab versus investigator’s choice chemotherapy
(ICC; dacarbazine or carboplatin plus paclitaxel)
The level of evidence regarding the outcome measure overall survival was downgraded by four levels because of study limitations (risk of bias -2), and because the optimal information size is not met and the confidence interval encloses the threshold for a clinically relevant effect and no clinically relevant effect (imprecision -2). Therefore, the level of evidence was graded as very low.
The level of evidence regarding the outcome measure progression free survival was downgraded by three levels because of study limitations (risk of bias -2); was downgraded by one level because the optimal information size is not met (imprecision). Therefore, the level of evidence was graded as very low.
The level of evidence regarding the outcome measure adverse events was downgraded by three levels because of study limitations (risk of bias -2) and the confidence interval encloses the threshold for a clinically relevant effect and no clinically relevant effect (imprecision). Therefore, the level of evidence was graded as very low.
The level of evidence regarding the outcome measure quality of life was downgraded by three levels because of study limitations (risk of bias -2). Therefore, the level of evidence was graded as low.
Zoeken en selecteren
The search and selection methods can be found in the main module Systematische therapie.
Referenties
- 1 - Andtbacka RH, Kaufman HL, Collichio F, Amatruda T, Senzer N, Chesney J, Delman KA, Spitler LE, Puzanov I, Agarwala SS, Milhem M, Cranmer L, Curti B, Lewis K, Ross M, Guthrie T, Linette GP, Daniels GA, Harrington K, Middleton MR, Miller WH Jr, Zager JS, Ye Y, Yao B, Li A, Doleman S, VanderWalde A, Gansert J, Coffin RS. Talimogene Laherparepvec Improves Durable Response Rate in Patients With Advanced Melanoma. J Clin Oncol. 2015 Sep 1;33(25):2780-8. doi: 10.1200/JCO.2014.58.3377. Epub 2015 May 26. PMID: 26014293.
- 2 - Andtbacka RHI, Collichio F, Harrington KJ, Middleton MR, Downey G, Ӧhrling K, Kaufman HL. Final analyses of OPTiM: a randomized phase III trial of talimogene laherparepvec versus granulocyte-macrophage colony-stimulating factor in unresectable stage III-IV melanoma. J Immunother Cancer. 2019 Jun 6;7(1):145. doi: 10.1186/s40425-019-0623-z. PMID: 31171039; PMCID: PMC6554874.
- 3 - Carlino MS, Long GV, Schadendorf D, Robert C, Ribas A, Richtig E, Nyakas M, Caglevic C, Tarhini A, Blank C, Hoeller C, Bar-Sela G, Barrow C, Wolter P, Zhou H, Emancipator K, Jensen EH, Ebbinghaus S, Ibrahim N, Daud A. Outcomes by line of therapy and programmed death ligand 1 expression in patients with advanced melanoma treated with pembrolizumab or ipilimumab in KEYNOTE-006: A randomised clinical trial. Eur J Cancer. 2018 Sep;101:236-243. doi: 10.1016/j.ejca.2018.06.034. Epub 2018 Aug 7. PMID: 30096704.
- 4 - Hodi FS, O'Day SJ, McDermott DF, Weber RW, Sosman JA, Haanen JB, Gonzalez R, Robert C, Schadendorf D, Hassel JC, Akerley W, van den Eertwegh AJ, Lutzky J, Lorigan P, Vaubel JM, Linette GP, Hogg D, Ottensmeier CH, Lebbé C, Peschel C, Quirt I, Clark JI, Wolchok JD, Weber JS, Tian J, Yellin MJ, Nichol GM, Hoos A, Urba WJ. Improved survival with ipilimumab in patients with metastatic melanoma. N Engl J Med. 2010 Aug 19;363(8):711-23. doi: 10.1056/NEJMoa1003466. Epub 2010 Jun 5. Erratum in: N Engl J Med. 2010 Sep 23;363(13):1290. PMID: 20525992; PMCID: PMC3549297.
- 5 - Larkin J, Minor D, D'Angelo S, Neyns B, Smylie M, Miller WH Jr, Gutzmer R, Linette G, Chmielowski B, Lao CD, Lorigan P, Grossmann K, Hassel JC, Sznol M, Daud A, Sosman J, Khushalani N, Schadendorf D, Hoeller C, Walker D, Kong G, Horak C, Weber J. Overall Survival in Patients With Advanced Melanoma Who Received Nivolumab Versus Investigator's Choice Chemotherapy in CheckMate 037: A Randomized, Controlled, Open-Label Phase III Trial. J Clin Oncol. 2018 Feb 1;36(4):383-390. doi: 10.1200/JCO.2016.71.8023. Epub 2017 Jul 3. PMID: 28671856; PMCID: PMC6804912.
- 6 - Revicki DA, van den Eertwegh AJ, Lorigan P, Lebbe C, Linette G, Ottensmeier CH, Safikhani S, Messina M, Hoos A, Wagner S, Kotapati S. Health related quality of life outcomes for unresectable stage III or IV melanoma patients receiving ipilimumab treatment. Health Qual Life Outcomes. 2012 Jun 13;10:66. doi: 10.1186/1477-7525-10-66. PMID: 22694829; PMCID: PMC3426458.
- 7 - Robert C, Grob JJ, Stroyakovskiy D, Karaszewska B, Hauschild A, Levchenko E, Chiarion Sileni V, Schachter J, Garbe C, Bondarenko I, Gogas H, Mandalá M, Haanen JBAG, Lebbé C, Mackiewicz A, Rutkowski P, Nathan PD, Ribas A, Davies MA, Flaherty KT, Burgess P, Tan M, Gasal E, Voi M, Schadendorf D, Long GV. Five-Year Outcomes with Dabrafenib plus Trametinib in Metastatic Melanoma. N Engl J Med. 2019 Aug 15;381(7):626-636. doi: 10.1056/NEJMoa1904059. Epub 2019 Jun 4. PMID: 31166680.
- 8 - Robert C, Schachter J, Long GV, Arance A, Grob JJ, Mortier L, Daud A, Carlino MS, McNeil C, Lotem M, Larkin J, Lorigan P, Neyns B, Blank CU, Hamid O, Mateus C, Shapira-Frommer R, Kosh M, Zhou H, Ibrahim N, Ebbinghaus S, Ribas A; KEYNOTE-006 investigators. Pembrolizumab versus Ipilimumab in Advanced Melanoma. N Engl J Med. 2015 Jun 25;372(26):2521-32. doi: 10.1056/NEJMoa1503093. Epub 2015 Apr 19. PMID: 25891173.
- 9 - Rohaan MW, Borch TH, van den Berg JH, Met Ö, Kessels R, Geukes Foppen MH, Stoltenborg Granhøj J, Nuijen B, Nijenhuis C, Jedema I, van Zon M, Scheij S, Beijnen JH, Hansen M, Voermans C, Noringriis IM, Monberg TJ, Holmstroem RB, Wever LDV, van Dijk M, Grijpink-Ongering LG, Valkenet LHM, Torres Acosta A, Karger M, Borgers JSW, Ten Ham RMT, Retèl VP, van Harten WH, Lalezari F, van Tinteren H, van der Veldt AAM, Hospers GAP, Stevense-den Boer MAM, Suijkerbuijk KPM, Aarts MJB, Piersma D, van den Eertwegh AJM, de Groot JB, Vreugdenhil G, Kapiteijn E, Boers-Sonderen MJ, Fiets WE, van den Berkmortel FWPJ, Ellebaek E, Hölmich LR, van Akkooi ACJ, van Houdt WJ, Wouters MWJM, van Thienen JV, Blank CU, Meerveld-Eggink A, Klobuch S, Wilgenhof S, Schumacher TN, Donia M, Svane IM, Haanen JBAG. Tumor-Infiltrating Lymphocyte Therapy or Ipilimumab in Advanced Melanoma. N Engl J Med. 2022 Dec 8;387(23):2113-2125. doi: 10.1056/NEJMoa2210233. PMID: 36477031.
- 10 - Schachter J, Ribas A, Long GV, Arance A, Grob JJ, Mortier L, Daud A, Carlino MS, McNeil C, Lotem M, Larkin J, Lorigan P, Neyns B, Blank C, Petrella TM, Hamid O, Zhou H, Ebbinghaus S, Ibrahim N, Robert C. Pembrolizumab versus ipilimumab for advanced melanoma: final overall survival results of a multicentre, randomised, open-label phase 3 study (KEYNOTE-006). Lancet. 2017 Oct 21;390(10105):1853-1862. doi: 10.1016/S0140-6736(17)31601-X. Epub 2017 Aug 16. PMID: 28822576.
- 11 - Weber JS, D'Angelo SP, Minor D, Hodi FS, Gutzmer R, Neyns B, Hoeller C, Khushalani NI, Miller WH Jr, Lao CD, Linette GP, Thomas L, Lorigan P, Grossmann KF, Hassel JC, Maio M, Sznol M, Ascierto PA, Mohr P, Chmielowski B, Bryce A, Svane IM, Grob JJ, Krackhardt AM, Horak C, Lambert A, Yang AS, Larkin J. Nivolumab versus chemotherapy in patients with advanced melanoma who progressed after anti-CTLA-4 treatment (CheckMate 037): a randomised, controlled, open-label, phase 3 trial. Lancet Oncol. 2015 Apr;16(4):375-84. doi: 10.1016/S1470-2045(15)70076-8. Epub 2015 Mar 18. PMID: 25795410.
Evidence tabellen
|
Revicki, 2012 Hodi, 2010 MDX010-20 NCT00094653 |
Randomized, double-blind, phase 3 study.
Patients at 125 centers in 13 countries in North America, South America, Europe, and Africa.
Patient enrolment between: September 2004 and August 2008.
Funding and conflicts of interest:
Bristol-Myers Squibb contributed to:
Disclosure forms provided by the authors are available with the full text of this article. |
Inclusion criteria:
Exclusion criteria:
Mean age, years I: 55.6 C1: 56.8 C2: 57.4
Male, n (%) I: 247 (61.3%) C1: 81 (59.1%) C2: 73 (53.7%)
ECOG PS: 0 – I: 232 (57.6%) 0 – C1: 72 (52.6%) 0 – C2: 70 (51.5%) 1 – I: 166 (41.2%) 1 – C1: 64 (46.7%) 1 – C2: 61 (44.9%) 2 – I: 4 (1%) 2 – C1: 1 (0.7%) 2 – C2: 4 (2.9%) 3 – I: 1 (0.2%) 3 – C1: 0 3 – C2: 0 Unknown: I: 0 C1: 0 C2: 1 (0.7%)
Groups were comparable at baseline. |
I: Ipilimumab, at a dose of 3 mg per kilogram of body weight, plus a gp100 peptide vaccine n= 403
|
C1: n=137
C2: n=136
|
Patients were followed for up to 55 months.
Median follow-up time for survival: I: 21.0 months C1: 27.8 months C2: 17.2 months |
Median OS, months (95% CI) I: 10.0 (8.5 to 11.5) C1: 10.1 (8.0 to 13.8) C2: 6.4 (5.5 to 8.7) I vs C2: HR for death: 0.68 (0.55–0.85); P<0.001 C1 vs C2: HR for death: 0.66 (0.51–0.87); P=0.003 I vs C1: HR for death: 1.04 (0.83–1.30). P=0.76
1-Year OS: I: 43.6% C1: 45.6% C2: 25.3%
18-month OS: I: 30.0%
2-Year OS: I: 21.6% C1: 23.5% C2: 13.7%
Median PFS, months (95% CI): I: 2.76 (2.73 to 2.79) C1: 2.86 (2.76 to 3.02) C2: 2.76 (2.73 to 2.83)
AEs grade 3 or 4: I: 173/374 C1: 60/127 C2: 62/128
Drug-related AEs, Grade 3 or 4/total: I: 66/338 C1: 30/105 C2: 15/104
Immune-related AEs, Grade 3 or 4/total: I: 39/221 C1: 19/80 C2: 4/42
Drug-related deaths, n: I: 8 C1: 4 C2: 2
For more information on AEs see results section of the article.
EORTC QLQ-C30 symptom scores (improvements are indicated by negative scores): Difference in constipation scores: I: 5.2 C1:1.9 C2:11.8 I vs C2: p<0.05 C1 vs C2: p<0.05 Favouring ipilimumab.
None of the other differences in HRQL scores between the three treatments were statistically significant. |
Authors conclusions: Hodi, 2010: Ipilimumab, with or without a gp100 peptide vaccine, as compared with gp100 alone, improved overall survival in patients with previously treated metastatic melanoma. Adverse events can be severe, long-lasting, or both, but most are reversible with appropriate treatment.
Revicki, 2012: Ipilimumab with/without gp100 vaccine does not have a significant negative HRQL impact during the treatment induction phase relative to gp100 alone in stage III or IV melanoma patients. |
|
Robert, 2019 KEYNOTE-006 NCT01866319 |
International, randomized, open-label phase 3 study.
In 16 countries.
Patient enrolment: From September 18, 2013, to March 3, 2014.
Funding and conflicts of interest:
contributed to:
Disclosure forms provided by the authors are available with the full text of this article. |
Inclusion criteria:
Exclusion criteria:
Mean age, years Ia: 61 (18–89) Ib: 63 (22–89) C: 62 (18–88)
Male, n (%) Ia: 161 (57.7) Ic: 174 (62.8) C: 162 (58.3)
ECOG PS: 0 – Ia: 196 (70.3) 0 – Ib: 189 (68.2) 0 – C: 188 (67.6) 1 – Ia: 83 (29.7) 1 – Ib: 88 (31.8) 1 – C: 90 (32.4)
PD-L1-positive tumours: 80.6%
Groups were comparable at baseline. |
Ia: pembrolizumab at a dose of 10 mg per kilogram of body weight every 2 weeks n= 279
Ib: n=277
|
C: dose of 3 mg per kilogram every 3 weeks n=278
|
Robert, 2019: Median follow-up for survival: 57.7 months (IQR 56.7–59.2).
Carlino, 2018: Median follow-up: 33.9 months.
Schachter, 2017: Median follow-up: 22.9 months
Discontinued treatment: Ia: 147 progressive disease 29 adverse events 2 deaths 2 complete responses 21 other
Ib: 139 progressive disease 45 adverse events 1 death 5 complete responses 23 other
C: 46 progressive disease 35 adverse events 5 deaths 24 other
Withdrew consent and did not receive treatment: Ia: n=1 C: n=22
Robert, 2015: Median follow-up at data cutoff (with 502 events reported), months: 7.9 (range: 6.1 to 11.5)
March 3, 2015: Follow-up for OS: Minimum follow-up: 12 months with 289 deaths occurred
Mean duration of exposure, days: Ia: 164 Ib: 151 C: 50
Rate discontinuation of a study drug because of treatment related AEs: Ia: 4.0%, Ib: 6.9%, C: 9.4%,
|
Robert, 2019: Median OS: C: 15.9 months (13.3–22.0) HR: 0.73 (95% CI 0.61–0.88, p=0·00049). Median PFS: C: 3.4 months (2.9–4.2) HR 0.57, 95% CI 0.48–0.67, p<0.0001.
Grade 3–4 treatment-related AEs: C: 50 (20%)
Treatment-related sepsis. C: n=1
Schachter, 2017: Death: n=383
Median OS: Ib: not reached (23.5 months–not reached) C: 16.0 months (range 13.5–22.0) HR pembro every 2 weeks vs ipi: 0.68, 95% CI 0·53–0·87; p=0·0009 HR pembro every 3 weeks vs ipi: 0.68, 0·53–0·86; p=0·0008.
2 year OS rate: Ia: 55% (95% CI 49–61) Ib: 55% (95% CI 49–61) C: 43% (95% CI 37–49)
PFS events: n= 566 I (pooled groups): 364 (65%) C: 202 (35%)
Median PFS, months: Ia: 5.6 months (range 3.4–8.2) Ib: 4.1 months (range 2.9–7.2) C: 2.8 months (range 2.8–2.9) HR for both Pembro schedules vs ipi: 0.61; 95% CI 0·50–0·75; p<0·0001 HR for Ia vs Ib: 0.95; 95% CI 0·77–1·17; p=0·62).
2-year PFS rate: Ia: 31% Ib: 28% C: 14%
Treatment related AEs grade 3 to 5: Ia: 47 (17%) of 278 Ib: 46 (17%) of 277 C: 50 (20%) of 256
Robert, 2015: Median overall survival was not reached in any study group.
1-Year OS: Ia: 74.1% Ib: 68.4% C: 58.2%
Median PFS, months (95% CI): Ia: 5.5 (95% CI, 3.4 to 6.9) Ib: 4.1 (95% CI, 2.9 to 6.9) C: 2.8 (95% CI, 2.8 to 2.9)
6-month PFS, months: Ia: 47.3% Ib: 46.4% C: 26.5%
Treatment related AEs grade 3 to 5: Ia: 13.3% Ib: 10.1% C: 19.9%
Drug-related deaths, n: Ia: 0 Ib: 0 C: 1
For more information on AEs see results section of the article. |
Co-primary endpoints were OS and PFS. Robert, 2019:
Carlino, 2018:
Schachter, 2017:
Robert, 2015:
Authors conclusions: Robert, 2019: Pembrolizumab continued to show superiority over ipilimumab after almost 5 years of follow-up. These results provide further support for use of pembrolizumab in patients with advanced melanoma.
Carlino, 2018: with advanced melanoma, regardless of first- or second-line therapy or PD-L1 status.
Schachter, 2017: Substantiating the results of the interim analyses of KEYNOTE-006, pembrolizumab continued to provide superior overall survival versus ipilimumab, with no difference between pembrolizumab dosing schedules. These conclusions further support the use of pembrolizumab as a standard of care for advanced melanoma.
Robert, 2015: The anti–PD-1 antibody pembrolizumab prolonged progression-free survival and overall survival and had less high-grade toxicity than did ipilimumab in patients with advanced melanoma.
|
|
Andtbacka, 2019 Andtbacka, 2015 OPTiM NCT00769704 |
A randomized open-label phase III trial at 64 sites in the United States, the United Kingdom, Canada, and South Africa.
Patient enrolment between: 2009 and 2011
Funding and conflicts of interest: - Funded by BioVex, who were subsequently acquired by Amgen Inc. during the OPTiM trial. The sponsor contributed to:
- A competing interests statement is provided at the end of the full text article. |
Main inclusion criteria:
Exclusion criteria:
For more information on in-/exclusion see the article.
Median age, years (range) I: 63 (22 to 94) C: 64 (26 to 91)
Male, n (%) I: 173 (59%) C: 77 (55%)
ECOG PS: 0 – I: 209 (71%) 0 – C: 97 (69%) 1 – I: 82 (28%) 1 – C: 32 (23%) Unknown: I: 4 (1%) C: 12 (9%)
Groups were comparable at baseline.
|
I: intratumoral Talimogene laherparepvec (T-VEC) (at the approved dose) n= 295 (68%)
|
C: subcutaneous recombinant granulocyte-macrophage colony-stimulating factor (GM-CSF) n= 141 (32%) |
Median follow-up in the final analysis of OS: 49 months.
Median duration of treatment in weeks (range): I: 23.1 (0.1–176.7) C: 10.0 (0.6–120.0)
Andtbacka, 2015: Discontinued T-VEC: n=291 Disease progression: n=191 PR or CR for ≥ 6 continuous months: n=42 Maximum allowed dose without PR/CR: n=26 Adverse event: n=11 Consent withdrawn: n=10 Physician decision: n=6 Death: n=5
Discontinued GM-CSF: n=127 Disease progression: n=95 PR or CR for ≥ 6 continuous months: n=0 Maximum allowed dose without PR/CR: n=9 Adverse event: n=3 Consent withdrawn: n=12 Physician decision: n=5 Death: n=3 |
Intent-to treat population (stage IIIB–IVM1c melanoma): Median OS, months (95% CI): I: 23.3 (19.5–29.6) C: 18.9 (16.0–23.7) unstratified HR for death, 0.79 (95% CI,0.62–1.00); P = 0.0494).
Estimated 5-year survival I: 33.4% C: Not estimable
Stage IIIB–IVM1a disease Effect of T-VEC on OS vs GM-CSF:
Effect of T-VEC on OS vs ITT population including stage IVM1b/c disease:
Estimated 5-year survival with T-VEC:
Treatment related AEs grade 3/4: I: 33 (11.3%) C: 6 (4.7%)
Immune-related AEs: I: 24/295 C: ?
Immune-related AEs grade 3: n=4
Immune-related AEs grade 4: None reported
Treatment-related deaths, n: I: 0 C: 0
For more information on AEs see results section of the article |
assessment. Key secondary end points: OS and overall response rate
Authors conclusions: Andtbacka, 2019: In conclusion, as well as demonstrating a longer-term effect on survival, this analysis confirms that T-VEC resulted in high CR rates, most notably in patients with early metastatic melanoma (stage IIIB–IVM1a). Once achieved, CRs were durable and associated with prolonged survival. The favorable clinical outcomes observed in some patients treated with T-VEC, along with its good safety profile, support continued efforts to further define its future role in melanoma as a combination partner with immunotherapy.
Andtbacka, 2015: T-VEC is the first oncolytic immunotherapy to demonstrate therapeutic benefit against melanoma in a phase III clinical trial. T-VEC was well tolerated and resulted in a higher DRR (P<0.001) and
|
|
Rohaan, 2022 NCT02278887 |
Multicenter, open-label, phase 3, randomized trial, two participating clinical sites (the Netherlands Cancer Institute, Amsterdam and National Center for Cancer Immune Therapy, Copenhagen University Hospital, Herlev, Denmark).
Patient enrolment between: September 2014 and March 2022.
Funding and conflicts of interest: - Supported by the Dutch Cancer Society, the Netherlands Organization for Health Research and Development, the Dutch Ministry of Health, Stichting Avento, the Antoni van Leeuwenhoek Foundation, Copenhagen University Hospital (Herlev), the Danish Cancer Society, and the Capital Region of Denmark Research Foundation. - Disclosure forms provided by the authors are available with the full text of this article at NEJM.org. |
Inclusion criteria:
Exclusion criteria:
to randomization.
For more information on in-/exclusion see the appendix of the article.
Median age, years (range) I: 59 (26–74) C: 59 (30–77)
Male, n (%) I: 47 (56) C: 53 (63)
WHO PS: 0 – I: 69 (82) 0 – C: 70 (83) 1 – I: 15 (18) 1 – C: 14 (17)
Groups were comparable at baseline.
|
Adoptive cell therapy with tumor-infiltrating lymphocytes (TILs).
Patients assigned to receive TILs underwent a metastasectomy for retrieval and expansion of TILs, followed by administration of nonmyeloablative, lymphodepleting chemotherapy, single intravenous adoptive transfer of 5×109 to 2×1011 TILs, and subsequent high-dose interleukin-2 every 8 hours, for a maximum of 15 doses per protocol.
n=84
|
Ipilimumab: 3 mg/kg intravenously every 3 weeks, for a maximum of 4 doses.
n=84 |
Median follow-up in months: 33
Median duration of hospital admission: 17 days (range, 12 to 38).
Median ipilimumab Infusions: 3 (range, 1 to 4)
Treatment discontinuation because of AEs: 26/42 (62%)
TIL arm: No patients were lost to follow-up No patients discontinued treatment
Ipilimumab arm: No patients were lost to follow-up 42 patients discontinued treatment:
1 death |
Median OS, months (95% CI): I: 25.8 (18.2 to not reached) C: 18.9 (13.8 to 32.6) HR for death 0.83 (95% CI, 0.54 to 1.27).
2-year OS (95% CI): I: 54.3% (43.9 to 67.2) C: 44.1% (33.6 to 57.8)
Median PFS, in months (95% CI): I: 7.2 (4.2 to 13.1) C: 3.1 (3.0 to 4.3) HR for progression or death, 0.50; 95% CI, 0.35 to 0.72
6-month PFS: I: 52.7% (95% CI, 42.9 to 64.7) C: 21.4% (95% CI, 14.2 to 32.2)
Treatment related AEs grade 3 or 4: I: 100% C: 57% In the TIL group, these events were mainly chemotherapy-related myelosuppression.
For more information on AEs see results section of the article.
EORTC QLQ-C15 PAL quality-of-life and functioning scales. Mean HRQOL score at 6 months:
I: 77.4 C:69.6 Difference: 7.7 (5.1 to 10.4)
I: 82.0 C: 79.1 Difference: 2.9 (1.4 to 4.5)
I: 85.4 C: 75.7 Difference: 9.7 (7.5 to 11.9)
Scores on the EORTC QLQ-C15 PAL symptom scales:
I: 25.9 C: 33.8 Difference: −7.9 (−11.2 to −4.6)
I: 7.5 C: 5.9 Difference: 1.6 (0.7 to 2.5)
I: 14.3 C: 20.7 Difference: −6.4 (−9.3 to −3.5)
I: 10.0 C: 12.4 Difference: −2.4 (−5.0 to 0.1)
I: 23.6 C: 28.1 Difference −4.5 (−7.2 to −1.9)
I: 12.4 C: 13.5 Difference: −1.1 (−2.9 to 0.7)
I: 6.7 C: 7.1 Difference: −0.4 (−1.3 to 0.5) |
Authors conclusions: In patients with advanced melanoma, progression-free survival was significantly longer
|
|
Weber 2015, Larkin 2018
|
Type of study: phase III, randomized, controlled, open-label study
Setting and country: Multicentre, 90 sites in 14 countries.
Funding and conflicts of interest: The study was designed jointly by the funder of the study and the senior investigators (JSW and JL). Data collected by the funder were analysed in collaboration with all authors. The funder of the study funded writing and editorial support.
Detailed declarations of interests are provided in the article. |
Inclusion criteria: -Patients with BRAF must have experienced progression after treatment with anti-CTLA-4 and BRAF inhibitor. -patients with BRAFV600 mutation must have experienced progression after treatment with anti–CTLA-4 and a BRAF inhibitor. Exclusion criteria: -active brain metastases More detailed inclusion and exclusion criteria are described in the appendix of Weber et al, 2015.
N total at baseline: 405 Intervention: 272 Control: 133
Important prognostic factors2:
Median age (IQR) I: 59 (23-88) C: 62 (29-85)
Sex: I: 65% M C: 64% M
ECOG performance status: I: 60% 0 C: 63% 0
BRAF mutant: I: 60 (22%) C: 29 (22%)
Treatment with PD-1/PD-L1: I: 11% C: 41%
Brain metastases: I: 20% C: 14%
Increased lactate dehydrogenase levels: I: 52% C: 38%
Groups comparable at baseline? Yes, except for brain metastases and lactate dehydrogenase levels.
|
Describe intervention (treatment/procedure/test):
Nivolumab 3 mg/kg intravenously every 2 weeks. |
Describe control (treatment/procedure/test):
Investigator’s choice chemotherapy (ICC), which consisted of dacarbazine 1,000 mg/m2 every 3 weeks or carboplatin area under the curve 6 plus paclitaxel 175 mg/m2 every 3 weeks intravenously. |
Larkin 2018 Clinical data cutoff March 29, 2016 Length of follow-up median (IQR): Approximately 2 years.
Length of duration therapy median: I: 4.7 months (95% CI 3.3-6.0) C: 2.0 months (95% CI 1.6-2.8)
Loss-to-follow-up: Intervention: 233 (86%) discontinued treatment. 182 disease progression 15 study drug toxicity 6 adverse event 19 patient request 3 withdrew consent 1 maximum clinical benefit 1 poor/noncompliance 4 no longer met study criteria 2 other
Control: 102 (77%) discontinued treatment. 74 disease progression 11 study drug toxicity 3 adverse event 7 patient request 2 withdrew consent 3 maximum clinical benefit 2 other Weber 2015 Clinical data cutoff not reported?
Range of follow-up: 5.2-16.7 months
Loss-to-follow-up: Intervention: 111 (53%) discontinued treatment. 96 disease progression 5 study drug toxicity 0 death 2 AE unrelated to study drug 5 request to discontinue 2 withdrew consent 1 max clinical benefit
Control: 129 (92%) discontinued treatment. 175 disease progression 7 study drug toxicity 0 death 3 AE unrelated to study drug 2 request to continue 3 withdrew consent 1 max clinical benefit 1 other |
Outcome measures and effect size (include 95%CI and p-value if available):
Larkin 2018 Median overall survival: C: 14.4 months (95% CI, 11.7 to 18.2) HR, 0.95; 95% CI, 0.73 to 1.24
Median progression-free survival: I: 3.1 months C: 3.7 months HR, 1.0; 95.1% CI, 0.78 to 1.436
Adverse events: I: 77% C: 82% Treatment related grade 3 and 4: I: 31% C: 14% Further specified in table 3.
Quality of life: I: C:
Weber 2015 Median overall survival:
Median progression-free survival: I: 4.7 months (95% CI 2.3–6.5) C: 4.2 months (2.1–6.3) HR, 0.82; 99% CI 0.32–2.05
Adverse events: I: 68% C: 79% Treatment related grade 3 and 4: I: 9% C: 31%
Quality of life: Not reported. |
Original trial Checkmate 037 and updated analysis. ITT and PP analyses performed.
Author’s conclusion in 2015: Findings from our study show that nivolumab leads to clinically meaningful improvements in the proportion of patients achieving an objective response and provide a manageable safety profile when compared with chemotherapy.
Authors ‘conclusion in 2018:
“Although there were no survival differences between nivolumab and ICC treatments, nivolumab treatment after progression on ipilimumab with or without a BRAF inhibitor does provide a higher rate of response and more durable responses. Some situations may still exist that necessitate the use of ipilimumab as first-line therapy and nivolumab provides a safer option with a better maintained quality of life for patients who have experienced failure with prior systemic therapies compared with cytotoxic chemotherapy. The OS outcome may have been impacted by the increased dropout rate before treatment and increased systemic therapy received after assigned therapy in the ICC group, as well as an increased proportion of patients with poor prognostic factors in the nivolumab group. Despite the lack of survival advantage, nivolumab remains an effective option for PD-1 inhibitor–naive patients who experienced failure with ipilimumab and a BRAF inhibitor if BRAF mutated.”
-Subgroup analysis was performed on the PD-1/PDL1 subgroup: Median overall survival sensitivity analysis PD-1/PD-L1 group Larkin 2018 I: 16.4 months (95% CI, 12.9 to 20.3) HR, 0.81; 99% CI, 0.59 to 1.1
|
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 09-10-2025
Beoordeeld op geldigheid : 01-08-2025
De richtlijnmodules zijn geautoriseerd door de: Nederlandse Vereniging voor Heelkunde, Nederlandse Vereniging voor Dermatologie en Venereologie, Nederlandse Internisten Vereniging, Nederlandse Vereniging voor Nucleaire Geneeskunde, Nederlandse Vereniging voor Radiologie, Nederlandse Vereniging voor Pathologie, Verpleegkundigen & Verzorgenden Nederland.
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2017 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met Melanoom.
Huidige samenstelling van de werkgroep:
- Dr. A.A.M. (Astrid) van der Veldt, voorzitter, internist-oncoloog, werkzaam in het Erasmus Medisch Centrum, NIV
- Dr. M.J.B. (Maureen) Aarts, internist-oncoloog, werkzaam in het Maastricht Universitair Medisch Centrum, NIV
- Prof. dr. A.J.M. (Fons) van den Eertwegh, internist-oncoloog, werkzaam in het Amsterdam Universitair Medisch Centrum, NIV
- Dr. M. (Hilde) Jalving, internist-oncoloog, werkzaam in het Universitair Medisch Centrum Groningen, NIV
- Dr. S. (Sofie) Wilgenhof, internist-oncoloog, werkzaam in het Antoni van Leeuwenhoek, NIV
- Dr. J.J. (Han) Bonenkamp, chirurgisch oncoloog, werkzaam in het Radboudumc, NVvH
- Dr. D.J. (Dirk) Grünhagen, chirurgisch oncoloog, werkzaam in het Erasmus Medisch Centrum, NVvH
- Dr. A.B. (Anne Brecht) Francken, chirurgisch oncoloog, werkzaam in het Isala, NVvH
- Dr. E.I. (Elsemieke) Plasmeijer, dermatoloog, werkzaam in het Antoni van Leeuwenhoek, NVDV
- Dr. R. (Remco) van Doorn, dermatoloog, werkzaam in het Leids Universitair Medisch Centrum, NVDV
- Dr. Q.G. (Quido) de Lussanet de la Sablonière, nucleair radioloog, werkzaam in het Erasmus Medisch Centrum, NVvR
- Dr. E.H.J.G. (Erik) Aarntzen, nucleair geneeskundige, werkzaam in het Universitair Medisch Centrum Groningen, NVNG
- Drs. B.A. (Beatrijs) Seinstra, radioloog, werkzaam in het Antoni van Leeuwenhoek, NVvR
- H.C. (Hanna) van der Pol, MSC, verpleegkundig specialist melanoom, werkzaam in het Antoni van Leeuwenhoek, V&VN
- Dr. T.P. (Thomas) Potjer, klinisch geneticus, werkzaam in het Leids Universitair Medisch Centrum, VKGN
- Dr. W.A.M. (Willeke) Blokx, patholoog, werkzaam in het Universitair Medisch Centrum Utrecht, NVVP
- Dr. A.M.L. (Anne) Jansen, klinisch moleculair bioloog in de pathologie, werkzaam in het Universitair Medisch Centrum Utrecht, NVVP
- K. (Koen) van Elst, Stichting Melanoom
Met speciale dank aan:
- Dr. B. Leeneman, Universitair docent, werkzaam in het Erasmus Medisch Centrum (bijdrage aan de doelmatigheidsmodule)
Met ondersteuning van:
- Dr. D. (Dagmar) Nieboer, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. R.J.S. (Rayna) Anijs, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. L. (Lisanne) Verbruggen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. F. (Fieke) Pepping, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Voormalig betrokken werkgroepleden:
- Drs. J.G.M. (Anne) van den Hoek, radiotherapeut, werkzaam in het Universitair Medisch Centrum Groningen, NVRO (tot en met juni 2024)
- Drs. B. (Bernies) van der Hiel, nucleair geneeskundige, werkzaam in het werkzaam in het Antoni van Leeuwenhoek, NVNG (tot en met mei 2024)
- Drs. A. (Annemarie) Bruining, radioloog, werkzaam in het Nederlands Kanker Instituut, NVVR (tot en met mei 2024)
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Veldt, van der (voorzitter) |
Internist-oncoloog, afdeling Interne Oncologie (0,8 fte) en afdeling Radiologie & Nucleaire Geneeskunde (0,2 fte) Erasmus MC, Rotterdam |
Adviesraden: BMS, MSD, Merck, Novartis, Pfizer, Eisai, Sanofi, Pierre-Fabre en Ipsen. Betaald aan het instituut (Erasmus MC) |
A.A.M. van der Veldt is principal investigator van meerdere studies van firma's (BMS, Exelexis, Novartis, Roche) en investigator-initiated studies (o.a. Safe Stop Trials) die financieel worden ondersteund door onder andere de zorgverzekeraars en non-profit organisaties Participatie aan NADINA-trial
|
Actie ondernomen bij modules over systemische behandelingen Zie hiervoor ‘Werkwijze en toelichting belangen richtlijn Melanoom’
|
|
Aarts |
Internist-oncoloog Maastricht Universitair Medisch Centrum |
* Bestuurslid WIN-O (Werkgroep Immunotherapie Nederland voor Oncologie) melanoom en nierkanker (onbetaald)
|
* Pfizer - Tyrosine Inhibitor effect op trombocyten - Co-promotor Participatie aan NADINA-trial
|
Actie ondernomen bij modules over systemische behandelingen Zie hiervoor ‘Werkwijze en toelichting belangen richtlijn Melanoom’
|
|
Eertwegh, van den |
Medisch-oncoloog, afdeling medische oncologie, Cancer Center Amsterdam, Amsterdam UMC, Vrije Universiteit Amsterdam Voorzitter DMTR (Dutch Melanoma Treatment registry)(vacatiegeld aan Amsterdam UMC)
|
Adviesraad (betaald aan Amsterdam UMC): Bristol-Myers Squibb, MSD Oncology, Ipsen, Pierre Fabre, Janssen Cilag BV |
* Sanofi - Prostaat studies (cabazipet en RECAB) - Projectleider * TEVA - prostaat studie (RECAB) - Projectleider * Bristol-Myers Squibb - Onco-kompas - Geen projectleider Huidig:" * Idera - INTRIM melanoom studie - Projectleider * Roche - REPOSIT melanoom studie - Projecteider * Novartis, Pierre Fabre, MSD, BMS en ziektekosten - DMTR - Geen projectleider
PI NADINA-trial |
Actie ondernomen bij modules over systemische behandelingen Zie hiervoor ‘Werkwijze en toelichting belangen richtlijn Melanoom’
|
|
Jalving |
Internist-oncoloog, UMCG Groningen |
Adviesraden: Bristol-Myers Squibb, AstraZenica,Pierre Fabre (betaald aan instituut (UMCG)
|
* KWF - TAMIC: Dichloroacetate in patients with metastatic melanoma prior to treatment with immune-checkpoint inhibition - Projectleider |
Actie ondernomen bij modules over systemische behandelingen Zie hiervoor ‘Werkwijze en toelichting belangen richtlijn Melanoom’
|
|
Wilgenhof |
Internist-oncoloog in het Antoni van Leeuwenziekenhuis |
Adviesraden: Eisai, Bristol-Myers Squibb, Pierre Fabre, Novartis, Pfizer en lpsen (betaald aan instituut (AVL)); educatief symposium: MSD en Bristol-Myers Squibb (betaald aan insituut (AVL)) |
* EU Horizon 2020 (no 875052) - CAPABLE: Pilot study of the eHealth application Cancer Patients Better Life Experience - Geen Projectleider * EU (101104801) - CARE-1: Optimizing Treatmensts for Metastatic Renal Carcinoma - Geen Projectleider
Studies: principal investigator: CA224020 studie (Clinicalîrials.gov number, NCT01968109) R3767-ONC-2011 studie (NCT05352672) E2139 (NCT05270044) vorinostat studie (NCT02836548)
subinvestigator: TIL studie (Clinicalîrials.gov number, NCT02278887) NADINA studie (Clinicalîrials.gov number, NCT04949113) safe stop studie safe stop ipi-nivo (NCT05652673) E1325 (NCT02362594) NIVEC studie (NCT04330430) NKTR-214 + nivolumab (NCT03635983) EBIN (NCT03235245) DONIMI (NCT04133948) MASTERKEY-115 (NCT04068181) IOB-013 (NCT05155254) |
Actie ondernomen bij modules over systemische behandelingen Zie hiervoor ‘Werkwijze en toelichting belangen richtlijn Melanoom’
|
|
Bonenkamp |
Chirurgisch oncoloog, RadboudUMC Nijmegen |
* Lid DB TFG Melanoom (onbetaald) |
Geen |
Geen actie |
|
Grünhagen |
Chirurg, Erasmus MC |
Lid bestuur WIN-O melanoom, onbetaald |
Deelname NADINA-trial |
Geen actie |
|
Francken |
Chirurgisch oncoloog, Isala |
* Voorzitter werkgroep audit NVvH |
Geen |
Geen actie |
|
Plasmeijer |
Dermatoloog, AVL |
* Bestuurslid Win-O: onbetaald |
Geen |
Geen actie |
|
Doorn, van |
Dermatoloog, Leids Universitair Medisch Centrum |
Onbetaald lid van enkele besturen (European Society for Dermatological Research, Nederlandse Vereniging voor Experimentele Dermatologie) |
Stichting KiKA - Therapeutic targeting of congenital melanocytic naevus and childhood melanoma using FOXO4 anti-senescence peptides - Projectleider |
Geen actie |
|
Lussanet de la Sablonière |
Nucleair- en Abdomen radioloog, Erasmus Medisch Centrum, Rotterdam |
Geen |
Geen |
Geen actie |
|
Aarntzen |
Nucleair geneeskundige, UMC Groningen (0,8 fte) * UMCGroningen, nucleair geneeskundige (0,8 fte) * Radboudumc, post-doc onderzoeker (0,1 fte) * Eberhard Karls University, Tuebingen, Duitsland (0,5 fte) |
* Post-doc onderzoeker Radboudumc, betaald (0,1 fte) * Post-doc onderzoeker Eberhard Karls University Tuebingen (Duitsland), betaald (0,05 fte)
|
* EU Innovatieve Health Initiative (IHI) - IMAGIO - IMAGING and advanced guidance for workflow optimalization in interventionaal oncology - Projectleider * Bergh in het Zadel/ Radboud oncologie Fonds - 'Breek de barrière: 'een nieuwe lokale en gerichte behandelmethode voor alvleesklierkanker' - Projectleider * ImaginAB Inc - iPREDICT, Trial: A phase IIB, Open Label, Study of 89Zr-crefmirlimab berdoxam PET/CT in Subjects with Selected Advanced or Metastetic Malignancies to ? - Geen projectleider site PI * Bergh in het Zadel/Radboud oncologie Fonds - Inzet AI voor betere overleving niet-kleincellig longkanker - Projectleider * ImaginAB Inc - (89Zr)Df-lAB22MC anti-CD8 minibody PET/CT-imaging to assess the in vivo distribution of CD8+ T-cells in COVID-19 patienst (NCT04874818) - Projectleider * KWF - Imaging tumor-infiltrating CD8+ T-cells in non-small cell lung cancer patienst upon neo-adjuvant treatment with Durvalumab - Projectleider |
Geen actie |
|
Seinstra |
Radioloog - Antoni van Leeuwenhoek Ziekenhuis |
Betrokken bij NADINA-trial als mede-auteur |
Geen |
Geen actie |
|
Van der Pol |
Verpleegkkundig specialist, Antoni van Leeuwenhoekziekenhuis, Amsterdam |
Geen |
Geen |
Geen actie |
|
Potjer |
Klinisch Geneticus, LUMC |
Cluster expertisegroep Maligniteiten van de huid |
Geen |
Geen actie |
|
Blokx |
Klinisch patholoog, UMC Utrecht |
Geen |
Geen |
Geen actie |
|
Jansen |
Klinisch Moleculair Bioloog in de Pathologie, UMC Utrecht |
Bestuurslid Stichting PALGA (vacatiegelden) |
Geen |
Geen actie |
|
Leeneman |
Universitair docent, Erasmus Universiteit Rotterdam |
Geen |
* ZIN - Ontwikkeling van ziektemodel voor melanoom - Geen projectleider * ZIN - Actualisatie van ziektemodel voor melanoom - Projectleider |
Geen actie |
|
Van der Elst |
Manager Quality and Improvement, Contour Advanced Systems B.V. |
Bestuurslid Stichting Melanoom |
Geen |
Geen actie |
Werkwijze en toelichting belangen richtlijn Melanoom
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
De NIV heeft vastgesteld dat het niet mogelijk was werkgroepleden af te vaardigen met voldoende expertise zonder potentiële belangenverstrengeling. Het gaat daarbij met name om werkgroepleden die deelnemen aan adviesraden/kennisuitwisselingsbijeenkomsten met de farmaceutische industrie of deel nemen of hebben genomen als onderzoeker van een klinische studie. Gedurende de ontwikkeling van de [richtlijn / modules] heeft daarom afstemming plaatsgevonden tussen de werkgroepvoorzitter, de belangencommissie van het Kennisinstituut van de Federatie Medisch Specialisten en de NIV over passende acties naar aanleiding van de gemelde belangen.
Restricties voor de modules over onderwerpen (medicamenteuze behandeling) waar de adviesraden betrekking op hebben:
- Werkgroeplid werkt niet als enige inhoudsdeskundige aan de module;
- Werkgroeplid werkt tenminste samen met een werkgroeplid met een vergelijkbare expertise in alle fasen (zoeken, studieselectie, data-extractie, evidence synthese, Evidence-to-decision, aanbevelingen formuleren) van het ontwikkelproces. Indien nodig worden werkgroepleden toegevoegd aan de werkgroep;
- In alle fasen van het ontwikkelproces is een onafhankelijk methodoloog betrokken;
- Overwegingen en aanbevelingen worden besproken en vastgesteld tijdens een werkgroepvergadering onder leiding van een onafhankelijk voorzitter (zonder gemelde belangen).
Aansluitend op de reguliere commentaarronde bij de achterban van de bij de richtlijn betrokken wetenschappelijke verenigingen, hebben (een aantal) leden van richtlijn- en kwaliteitscommissie van de NIV en een methodoloog van het Kennisinstituut die niet betrokken waren bij ontwikkeling van de modules, aanvullend beoordeeld of de aanbevelingen logischerwijs aansluiten bij het gevonden bewijs en de overwegingen, om de onafhankelijkheid van de richtlijn te waarborgen.
Wellicht ten overvloede willen wij erop wijzen dat medisch specialistische richtlijnen niet worden vastgesteld door de betreffende richtlijnwerkgroep maar door de besturen/ledenvergadering van de betrokken verenigingen.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Inbreng patiëntenperspectief
Bij elke module is het patiëntperspectief meegenomen door de werkgroep. Er werd aandacht besteed aan het patiënten perspectief door een afgevaardigde van een patiëntenvereniging, de Stichting Melanoom, in de werkgroep te laten participeren.
NHG-standaard Verdachte huidafwijkingen
Voor huisartsen is de NHG-Standaard Verdachte huidafwijkingen leidend. Deze sluit aan op de richtlijn Melanoom.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
|
Module |
Uitkomst raming |
Toelichting |
|
Systemische therapie - Tweedelijnsbehandeling BRAF-wild type gemuteerd irresectabel of gemetastaseerde stadium III/IV |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
De werkgroep beoordeelde de aanbeveling(en) uit de eerdere richtlijnmodules op noodzaak tot revisie.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.