Lentigo maligna
Uitgangsvraag
Wat is de beste methode van diagnostiek bij patiënten met een verdenking op lentigo maligna?
Wat is de optimale behandeling voor patiënten met een lentigo maligna en de in situ component van lentigo maligna melanoom?
Aanbeveling
Diagnostiek van lentigo maligna
- Voor de diagnostiek en follow-up dient gebruikt gemaakt te worden van dermatoscopie.
- De klinische uitbreiding van de laesie dient bepaald te worden op basis van dermatoscopie en niet met het blote oog.
- Reflectie confocale microscopie (RCM) kan (indien beschikbaar) overwogen worden om subklinische uitbreiding beter in kaart te brengen ten opzichte van gebruik van enkel dermatoscopie.
- Vanwege het risico op een ‘sampling error’ bij afname van een enkel stansbiopt is het wenselijk om meerdere stansbiopten af te nemen, dan wel een incisiebiopt, zeker als er gekozen wordt voor een niet-chirurgische behandelmethode. Bij beperkte grootte kan een diagnostische excisie worden overwogen.
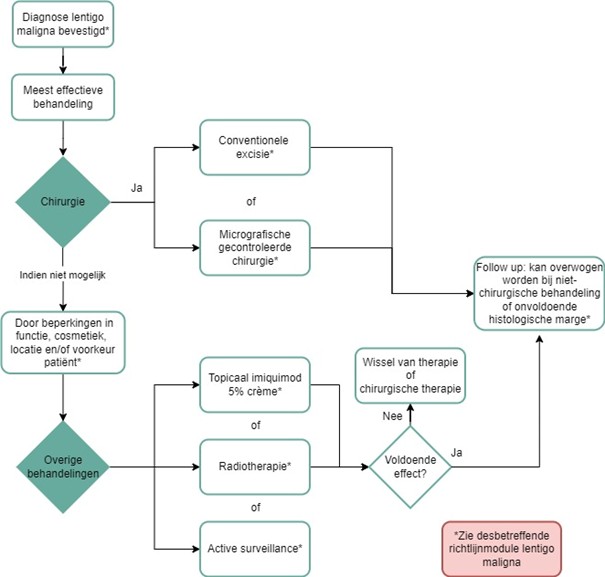
Behandeling van lentigo maligna (zie ook stroomschema)
- De eerste keuze therapie van lentigo maligna is chirurgische behandeling. Chirurgische behandeling (conventionele excisie en micrografisch gecontroleerde technieken) is het meest effectief gezien het weefsel gecontroleerd kan worden op de aanwezigheid van een invasieve component en de snijranden beoordeeld kunnen worden op radicaliteit.
- Vanwege de verhoogde kans op irradicaliteit wordt sluiting middels plastieken bij conventionele chirurgie afgeraden.
- Met micrografisch gecontroleerde technieken (zoals Breuninger) wordt vaker radicaliteit bereikt met een lagere kans op een lokaal recidief.
- Voor de in situ component van een lentigo maligna melanoom wordt in opzet altijd gestreefd naar radicaliteit.
- Overweeg alternatieve behandelmethoden zoals (off-label) topicaal imiquimod 5% crème of radiotherapie wanneer chirurgische behandeling niet wenselijk is of wanneer de chirurgische behandeling een significante impact heeft op de functie en/of cosmetiek van de specifieke locatie.
- Bij de keuze van niet-chirurgische behandelingen dient patiënt geïnformeerd te worden over eventuele onderbehandeling van een invasief melanoom.
- Behandel patiënten met imiquimod 5% crème als volgt: minimaal 60 behandeldagen met adequate inflammatierespons, bij voorkeur bereikt in 12 weken met toepassing van 7x/week.In geval van bijwerkingen of perioculaire laesies (Neumann et al., 2023) kan gekozen worden voor een milder behandelschema bestaande uit 5-6 dagen per week.
- Destructieve behandelingen zoals cryo- en lasertherapie worden niet aanbevolen omdat de bewijsvoering erg beperkt is.
- Op basis van leeftijd, comorbiditeit of beperkte levensverwachting is ‘active surveillance’ ook te overwegen.
Follow-up
- Bij een krappe histologische marge (<3 mm) na conventionele chirurgie is de kans op een lokaal recidief verhoogd (circa 25%). Overweeg in dat geval een re-excisie. Op basis van leeftijd of andere patiënt factoren kan hiervan worden afgezien.
- Bij een histologische marge van ≥3 mm na conventionele chirurgie, of bij radicaliteit na micrografisch gecontroleerde chirurgie, is de kans op een lokaal recidief laag (<2%) en kan worden afgezien van verdere follow-up.
- Overweeg in het geval van niet-chirurgische behandeling bij het afzien van een re-excisie ondanks te krappe histologische marges, jaarlijks follow-up gedurende 5 jaar. Op basis van leeftijd of andere patiëntfactoren kan in overleg afgezien worden van verdere follow-up met goede instructies m.b.t. alarmsymptomen.
Overwegingen
Diagnostiek
Kwaliteit van het bewijs
Er is geen systematische literatuuranalyse verricht voor diagnostiek bij lentigo maligna. Voor de optimale behandeling is wel een systematische literatuursearch verricht. De aanbevelingen en overwegingen zijn geschreven op basis van expert opinion met ondersteunende artikelen.
Professioneel perspectief
Histopathologisch onderzoek
Histopathologisch onderzoek is de gouden standaard voor zowel het bevestigen van de diagnose als het onderzoeken van de aanwezigheid van een invasieve component. Het afnemen van meerdere stansbiopten is wenselijk, want er is geen bewijs dat het afnemen van een biopt t.p.v. “het donkerste deel van de laesie” afdoende is om een invasieve component te bevestigen of uit te sluiten.
Dermatoscopie
Dermatoscopie is inmiddels onmisbaar bij de diagnostiek van gepigmenteerde laesies. Het is een niet-invasieve techniek waarbij een tien tot vijftienmaal vergroot beeld wordt verkregen van een gepigmenteerde laesie. Het benodigde apparaat is beschikbaar in zakformaat. De waarde van dermatoscopie ligt met name in het differentiëren van benigne afwijkingen en het beter dan met blote oog beoordelen van de uitgebreidheid van lentigo maligna. Toch is dermatoscopie van gepigmenteerde afwijkingen in het gelaat vaak complexer door het ontbreken van het klassieke pigmentnetwerk. Door afvlakken van de retelijsten kan het zogenaamd “pseudonetwerk” aanwezig zijn bij beide melanocytaire als niet-melanocytaire afwijkingen
Een dermatoscopisch progressiemodel is door Stolz in 2000 voorgesteld initieel bestaande uit een ‘annulair-granulair’ patroon (perifolliculaire dots) met asymmetrisch gepigmenteerde folliculaire openingen ([in]complete grijze cirkels), uitbreidend naar romboïdale structuren (polygonale lijnen) met uiteindelijk ‘blotches’ (structuurloze gepigmenteerde gebieden) met of zonder versluiering van de huidadnexen (Schiffner et al., 2000). Echter, met uitzondering van ‘blotches’, zijn alle andere dermatoscopische diagnostische criteria niet specifiek voor LM, en worden ze ook gezien bij o.a. gepigmenteerde actinische keratose en benigne lichenoïde keratose (Akay et al., 2010). De dermatoscopische sensitiviteit wordt verder beperkt door inter-observer variatie met name bij vroege LM (Lallas, Lallas, et al., 2021). Er wordt dan ook geadviseerd aanvullende diagnostiek te verrichten als er twijfel bestaat over een alternatieve diagnose zoals lentigo solaris, verruca seborrhoica of gepigmenteerde actinische keratose: de zogenaamde ‘inverse approach’. Ten slotte is de positief voorspellende waarde voor een invasieve component van klinische en dermatoscopische kenmerken, met uitzondering van exofytische groei, beperkt (Navarrete-Dechent et al., 2021; Peruilh-Bagolini et al., 2020; Zoutendijk et al., 2022). Ondanks dat de aanwezigheid van zwarte ‘blotches’, versluiering van de adnexale openingen en erytheem geassocieerd zijn met een hogere kans op de aanwezigheid van een invasieve component, leidt het afnemen van biopten op deze lokalisaties in de praktijk niet altijd tot een directe histologische correlatie met deze invasieve component (Peruilh-Bagolini et al., 2020; Pralong et al., 2012). In andere woorden: er is geen bewijs dat het afnemen van een biopt ter plaatse van “het donkerste deel van de laesie” afdoende is om een invasieve component te bevestigen of uit te sluiten. Het afnemen van meerdere stansbiopten is daarom wenselijk om eventuele ‘sampling errors’ te voorkomen, zeker als er gekozen wordt voor een niet-chirurgische behandelmethode.
Reflectie confocale microscopie
Reflectie confocale microscopie (RCM) kan (indien beschikbaar) overwogen worden om subklinische uitbreiding beter in kaart te brengen ten opzichte van gebruik van enkel dermatoscopie.
RCM is een relatief nieuwe beeldvormende techniek die evaluatie tot op het niveau van de papillaire dermis in cellulaire resolutie toelaat in horizontale oriëntatie. De diagnostische criteria voor LM zijn ondertussen al enkele jaren geleden beschreven en gevalideerd (Guitera et al., 2010; Melhoranse Gouveia et al., n.d.). De techniek kan gebruikt worden om het meest representatieve gebied te selecteren om biopten af te nemen met als gevolg een meer robuust histologisch substraat in vergelijking met selectie middels dermatoscopie (Mataca et al., 2018). Hierdoor neemt tegelijkertijd de kans op ‘sampling errors’ af. Dit blijkt uit twee recente studies waarin 75%-89% van de initieel gemiste invasieve LMM-componenten alsnog gediagnosticeerd konden worden door het gebruik van RCM. Van belang hierbij is de hoge negatief voorspellende waarde in beide studies (94%-99%), waardoor selectie van patiënten meer geschikt voor niet-chirurgische behandeling plaats kan vinden (Elshot et al., 2024; Gouveia et al., 2023).
Behandeling
Kwaliteit van het bewijs
Er is een systematische literatuuranalyse verricht. De eerder verrichte systematische zoekstrategie van 20 mei 2022 (Elshot et al, 2023) werd herhaald op 18 oktober 2024 en dit leverde geen nieuw vergelijkend onderzoek op. De aanbevelingen en overwegingen zijn daarom geschreven op basis van expert opinion en voor de chirurgische interventies werd de systematische review van Elshot et al. (2023) als basis gebruikt.
Tevens werden losse ondersteunende artikelen gebruikt. Hierbij is relevant om te melden dat bij de van tevoren gedefinieerde uitkomstmaten alleen gegevens over lokale recidieven zijn gevonden, beperkte gegevens over het effect van de behandelingen op de overleving en geen uitkomsten m.b.t. de kwaliteit van leven.
Professioneel perspectief
De recent verschenen resultaten van de RADICAL-trial waarin off-label topicaal imiquimod werd vergeleken met radiotherapie (ClinicalTrials.gov ID NCT02394132), is vooralsnog de enig beschikbare gerandomiseerde klinische trial die verschillende behandelmodaliteiten van LM met elkaar vergelijken (Hong, 2025). Bij de behandelkeuze voor de patiënt(e) moet er een duidelijk onderscheid gemaakt worden in het doel van de behandeling: voorkomen van progressie of radicaliteit.
(Micrografisch controleerde) chirurgie
In een systematische review en meta-analyse uit 2022 werd het effect van conventionele chirurgie en verschillende vormen van micrografisch gecontroleerde chirurgie op recidiefkans en overlevingsuitkomsten verricht (Elshot et al., 2023). De 5 mm chirurgische marge voor LM leidde tot radicaliteit in 83% tot 59% afhankelijk van de toegepaste insluiting van het weefsel (c.q. ‘bread-loaf’ of radiaire beoordeling t.o.v. complete beoordeling van het snijvlak). Deze uitkomsten waren vergelijkbaar voor de in situ component van LMM met chirurgische marges van 10 mm, namelijk 78% tot 55%. De recidief percentages waren het laagst voor de micrografisch gecontroleerde technieken met de beste uitkomsten bereikt met Mohs micrografische chirurgie in combinatie met immunohistochemie op vriescoupes (<1% 95% CI 0.3-10.9) of micrografisch gecontroleerde technieken met paraffine coupes (1.6%). De hoogste recidief percentages van 12% (95% CI 7.2-21.6) werden gezien bij conventionele chirurgie ondanks eventuele re-excisies. De recidiefkans bij conventionele chirurgie is ook afhankelijk van de histologische vrije marge, variërend van 2.6% bij een vrije marge van ≥3 mm en 27% als deze <3 mm is (Crouch et al., 2021; Hou et al., 2015). Middels het preoperatief toepassen van handheld-RCM al dan niet in combinatie met micrografisch gecontroleerde technieken werd een recidief percentage gezien van 1.1% (Elshot et al., 2023). Het gebruik van handheld-RCM leidde tot een significante afname in irradicaliteit (p<0.0001) en vermindering in het aantal rondes bij micrografisch gecontroleerde technieken (P<0.0001). Deze uitkomsten worden ondersteund door een recentere systematische review uit 2024 waarin een negatief voorspellende waarde voor subklinische uitbreiding gerapporteerd werd van 89% (95% CI 80.95-95.46; I2 = 80%) met een sensitiviteit en specificiteit t.o.v. histologie van respectievelijk 91.5% (95% CI 82.2-96.1; I2 = 0%) en 95.7% (95% CI 90.7-98; I2 = 68%) (Mesquita et al., 2024). Door selectie bias (m.n. hoog-risico tumoren in de conventionele chirurgie groep), heterogeniteit, lage prevalentie van progressie naar stadium III/IV ziekten en LMM-geassocieerde mortaliteit zijn er geen uitspraken te doen over enig overlevingsvoordeel tussen de verschillende chirurgische technieken (Elshot et al., 2023). Echter gezien minder dan 10% van de recidieven na chirurgische behandeling een invasief LMM betreft met in de meeste gevallen met een beperkte Breslowdikte (<1.0mm) (Elshot et al., 2023), zal het effect op progressievrije en melanoom-specifieke overleving beperkt zijn.
Bij de keuze voor een niet-chirurgische behandeling dient patiënt geïnformeerd te worden over eventuele onderbehandeling van een invasief melanoom, gezien in 10% van de initieel als LM afgegeven laesies alsnog een (micro)invasieve component wordt gevonden (Elshot et al., 2023; Zoutendijk et al., 2019).
Topicaal imiquimod vs. Radiotherapie
Voor patiënten met lentigo maligna (LM) die niet in aanmerking komen voor chirurgie, zijn zowel radiotherapie als topicale imiquimod effectieve behandelopties. Een multi-institutionele fase 3 gerandomiseerde studie (Hong et al., 2025) toonde een hoge en vergelijkbare effectiviteit aan, met histologisch bevestigde responspercentages van 95% in beide groepen na 6 maanden. Bij 24 maanden follow-up was er geen statistisch significant verschil in het percentage lokale recidieven (radiotherapie 20,7% vs. imiquimod 10%; OR 2.35, 95% CI 0.82-6.75, p=0.11). Opgemerkt dient te worden dat de studie 'underpowered' was door vroegtijdige beëindiging. Beide behandelingen werden goed verdragen, met voornamelijk graad 1-2 acute huidtoxiciteit. Er werden geen significante verschillen gevonden in de kwaliteit van leven op de lange termijn tussen de groepen; het emotionele welzijn van patiënten verbeterde in beide armen significant ten opzichte van de baseline
Gezien de vergelijkbare uitkomsten wordt de keuze tussen radiotherapie en imiquimod gebaseerd op praktische overwegingen, de locatie van de laesie en patiëntfactoren. Radiotherapie vereist frequente ziekenhuisbezoeken (bijvoorbeeld dagelijks gedurende een mediaan van 4,4 weken in de trial), wat zorgt voor nauwlettend toezicht en therapietrouw. Dit kan de voorkeur hebben bij patiënten die minder geschikt zijn voor zelfmanagement. Imiquimod wordt thuis toegepast gedurende een langere periode (doorgaans 12 weken) en vereist therapietrouw van de patiënt. Het hoge succespercentage van imiquimod in deze trial (superieur aan historische data) benadrukt het cruciale belang van actief management. Dit omvat nauwgezette monitoring en geïndividualiseerde dosisaanpassingen (escalatie of de-escalatie) om adequate inflammatie te bereiken en te onderhouden.
Radiotherapie
Bij behandeling met radiotherapie is de effectiviteit afhankelijk van de gebruikte techniek, dosis, fractionering en bestralingsmarge (Fogarty et al., 2018). In een systematische review door Fogarty, et al. werden behandelschema’s beschreven met oppervlakkige of orthovolt radiotherapie in 5-23 fracties met een totale dosis van 35-57 Gy. Doordat er een grote variatie is tussen de toegepaste vormen van radiotherapie, op basis van voornamelijk retrospectieve data, is het niet mogelijk uitspraken te doen over het meest effectieve behandelschema met gerapporteerde recidief percentages van 0%-31% (Canu et al., 2025; Drakensjö et al., 2020; Hendrickx et al., 2020).
Topicaal imiquimod
De effectiviteit van off-label topicale behandeling met imiquimod 5% crème is zeer afhankelijk van de behandelduur, frequentie en mate van inflammatie. In 2017 werd in de fase II LIMIT-1 studie geconcludeerd dat het bereikte deel patiënten met complete pathologische respons onvoldoende was om over te gaan naar een gerandomiseerde fase III studie (Marsden et al., 2017). In de LIMIT-1 trial werden de geïncludeerde LM na 12 weken imiquimod crème (in opzet 60 behandelingen in 12 weken) alsnog chirurgisch behandeld om de histologische complete respons te beoordelen. Een complete klinische respons werd gezien in 13 van de 28 patiënten (46%). Een punt van kritiek op de interpretatie van de resultaten is het feit dat er in 27% van de patiënten weinig tot geen (c.q. onvoldoende) inflammatie gezien en in deze groep maar bij 1 patiënt (13%) een complete pathologische respons van 13% optrad. Er werd verder geen onderscheid gemaakt in de uitkomsten tussen de patiënten met matige (28%) en hevige (38%) inflammatie waarbij de behandelintensiteit in sommige gevallen verlaagd werd naar 3 dagen per week. In een systematische review uit 2017 (Tio et al., 2017) werd een klinische respons van ongeveer 80% gerapporteerd. Hierbij is het van belang dat deze klinische respons niet altijd correleert met een histologische respons (Alarcon et al., 2014; Guitera et al., 2014). De meest effectieve resultaten lijken bereikt te worden met een intensiteit van 6-7 behandelingen per week gedurende een minimale periode van 12 weken waarin tenminste 60 behandelingen werden verricht (Tio et al., 2017). Het aangehouden schema in de LIMIT-1 studie van 5 dagen per week heeft t.o.v. 6-7 dagen een odds ratio van 8.85 (95% CI 5.33-11.15) voor het niet bereiken van een histologische respons. Het belang van bepaling van het meest optimale behandelschema werd wederom benadrukt in een recentere systematische review waarin patiënten werden geïncludeerd in verschillende klinische scenario’s waaronder mono-, adjuvant-, en neoadjuvante toepassingen met topicale imiquimod met tevens uitgebreide heterogeniteit in behandelschema’s resulterend in beperkte histologische respons van 57% (Vaienti et al., 2023). Ten slotte is het onbekend in welke mate behandeling met imiquimod de kans op het ontwikkelen van LMM verkleint, echter was het percentage van het ontwikkelen van een invasief recidief beperkt (2%) in de systematisch review door Tio, et al.
Het meest effectieve behandelschema van topicaal imiquimod bestaat uit: minimaal 60 behandeldagen met adequate inflammatierespons, bij voorkeur bereikt in 12 weken met toepassing van 7x/week. Adequate inflammatie wordt gedefinieerd als lokale huidinflammatierespons (erytheem met kleine crustae). Aangezien effectiviteit afhankelijk is van de aanwezigheid van inflammatie, kunnen perioden zonder zichtbare inflammatie resulteren in verlengde behandelduur. In geval van bijwerkingen of perioculaire laesies (Neumann et al., 2023) kan gekozen worden voor een milder behandelschema (5-6 dagen per week). Bij hevige inflammatie kan behandeling tijdelijk (circa 4 dagen) worden onderbroken om vervolgens met verminderde frequentie te hervatten. Adherente crustae dienen losgeweekt te worden met vaseline om voldoende penetratie van de imiquimod creme te waarborgen. De effectiviteit neemt significant af bij 4 dagen of minder per week.
De behandeling met imiquimod crème wordt in de thuissituatie toegepast, echter gezien de behandelduur en te verwachten inflammatie wordt geadviseerd patiënt hierin fysiek of op afstand te begeleiden. Bij oculaire inflammatie wordt overleg met of verwijzing naar een oogarts geadviseerd.
Destructieve therapie: cryotherapie/ lasertherapie
De bewijsvoering voor destructieve behandeling met cryotherapie en lasertherapie is erg beperkt omdat deze gebaseerd is op data uit case reports en kleine case series met wederom een grote variatie in behandelschema’s (McKenna et al., 2006; McLeod et al., 2011). Daarnaast worden er in deze studies nagenoeg geen histologische controle verricht met recidief percentages variërend van 0% tot 40% bij toepassing van cryotherapie en gemiddeld 34% voor laserbehandelingen (Greveling, De Vries, et al., 2016; Read et al., 2016). Gezien de beperkte bewijsvoering voor destructieve behandelingen zoals cryo- en lasertherapie worden deze niet aanbevolen.
Active surveillance
Op basis van leeftijd, comorbiditeit of beperkte levensverwachting is ‘active surveillance’ ook te overwegen gezien de beperkte kans op progressie naar invasief melanoom. Patiënten dienen in dit geval ten minste 1x per jaar gecontroleerd te worden en geïnstrueerd te zijn in eventuele alarmsymptomen zoals donkerder worden van de afwijking, het ontstaan van persisterend erytheem of palpabele afwijkingen.
Follow-up
Het is te overwegen patiënten 1x per jaar te vervolgen tot een periode van 5 jaar indien gekozen wordt voor een niet-chirurgische behandeling gezien het hoge risico op een lokaal recidief. Bij een histologische marge van ≥3mm na conventionele chirurgie of radicaliteit na micrografisch gecontroleerde is de kans op een lokaal recidief dermate beperkt (<2%) dat er kan worden afgezien van verdere follow-up.
Advies
De keuze van behandeling voor de individuele LM patiënt dient in samenspraak met de patiënt verricht te worden waarin de voor- en nadelen, maar ook eventuele risico’s aan bod horen te komen. In opzet is chirurgische behandeling de eerste keuze, echter kan hiervan afgeweken worden op basis van comorbiditeit, levensverwachting, cosmetische/functionele consequenties en eventuele weloverwogen voorkeur van de patiënt. Zie hiervoor ook het stroomschema Lentigo maligna behandelopties.
Lentigo maligna behandelopties
Waarden en voorkeuren van patiënten/ Samen beslissen
Bij de keuze van behandeling zijn een aantal aspecten van belang waaronder effectiviteit, cosmetische en functionele uitkomst en eventuele bijwerkingen van de interventie. Buiten eventueel leeftijd zijn er verder geen prognostische factoren bekend om het natuurlijke beloop van de LM laesie te kunnen voorspellen. Het blijft daarom een uitdaging om samen met de patiënt(e) tot de juiste behandelkeuze te komen (Vaidya et al., 2021). Bij de keuze van behandeling moet er een duidelijk onderscheid gemaakt worden in het doel van de behandeling: voorkomen van progressie of radicaliteit. Bij patiënten met een lange levensverwachting heeft chirurgische behandeling de voorkeur gezien de langere kans op progressie. Daarnaast verschillen de behandelingen significant in de uitkomst m.b.t. invasiviteit, littekenvorming, behandelduur/intensiteit, objectiveerbare effectiviteit, mogelijke onderhandeling van een invasieve component en eventuele bijwerkingen. Een zo goed mogelijke inschatting van de uitgebreidheid van de laesie draagt ook bij aan de keuze tussen chirurgische en niet chirurgische behandelopties.
Balans van gewenste en ongewenste effecten
De verschillende behandelingen van LM, waaronder (micrografisch gecontroleerde) chirurgie, topicaal imiquimod 5% crème, radiotherapie en “active surveillance’ verschillen in effectiviteit, intensiteit, hersteltijd, cosmetische uitkomsten en mogelijke bijwerkingen.
Chirurgische excisie is in zo verre het meest effectief gezien het weefsel gecontroleerd kan worden voor de aanwezigheid van een invasieve component en de snijranden beoordeeld kunnen worden voor radicaliteit. Hiernaast is de behandelduur relatief kort. Hier staat tegenover dat deze radicaliteit niet altijd haalbaar is, chirurgie tot littekens leidt en mogelijk gepaard gaat met grote defecten in het gelaat waarvoor uitgebreide reconstructies noodzakelijk kunnen zijn. De effectiviteit is ook afhankelijk van het type chirurgie waar gekozen voor wordt, met recidief percentages variërend van 12% voor conventionele excisie met 5 mm marge tot <2.5% voor micrografisch gecontroleerde technieken (Elshot et al., 2023). Bij micrografisch gecontroleerde technieken kunnen er uiteindelijk zeer grote defecten ontstaat die op voorhand niet te voorspellen zijn. De grootste kans op lokale recidieven wordt logischerwijs gezien bij irradicaliteit. Echter, in het geval van conventionele excisie is er bij een histologische marge van <3mm alsnog een 25% kans op een lokaal recidief (Crouch et al., 2021; Hou et al., 2015). Er zal afgewogen moeten worden of dit een acceptabel risico is (c.q. ‘active surveillance’) t.o.v. eventuele cosmetische of functionele consequenties van verdere chirurgische behandeling. Ook zou er gekozen kunnen worden voor adjuvante behandeling middels een niet-chirurgische modaliteit zoals topicale imiquimod 5% crème om de recidiefkans te verkleinen (Lallas, Moscarella, et al., 2021).
Bij het toepassen van niet-invasieve behandelmethoden is het bepalen van de effectiviteit minder duidelijk gezien de klinische follow-up met dermatoscopie leidt tot een reële kans op fout-negatieve beoordelingen (Alarcon et al., 2014; Guitera et al., 2014). Ook is er een kans op onderbehandeling van een eventuele gemiste invasieve component door de initiële diagnostiek gezien in ongeveer 10% van de als LM afgegeven laesies alsnog een invasieve component gevonden wordt na excisie. (Elshot et al., 2023; Zoutendijk et al., 2019)
Toch is radiotherapie een alternatieve behandelmethode met in het algemeen goede tot uitstekende cosmetische resultaten (Drakensjö et al., 2020). De behandeling kan echter, zeker bij oudere patiënten, zeer intensief zijn met behandelingen van meerdere dagen per week gedurende enkele weken. Mogelijke korte termijn complicaties bestaan uit acute radiatiedermatitis met jeuk of pijn variërend van roodheid en schilfering tot ulceraties. Op lange termijn is er kans op pigmentverschuivingen (hypo- of hyperpigmentaties) waardoor de follow-up bemoeilijkt wordt. Verder is er kans op het ontwikkelen van atrofie van de huid, teleangiëctastieën en fibrosering. De kans op secundaire maligniteiten is beperkt door de vaak oudere leeftijd van patiënten.
In vergelijking met radiotherapie is het voordeel van (off-label) topicale behandeling met imiquimod 5% crème dat deze thuis kan plaatvinden. Echter is goede begeleiding hiervan erg belangrijk om de therapietrouw te bevorderen gezien het effect van de behandeling op de huid en mogelijke bijwerkingen. De meest voorkomende verschijnselen bestaan uit roodheid, inflammatie en korstvorming waarbij griepachtige klachten en vermoeidheid ook kunnen voorkomen. Rondom de ogen is er kans op een toxische keratoconjunctivitis en preseptale cellulitis (Avallone, 2022). Het uiteindelijk cosmetische resultaat is meestal uitstekend echter komen littekenhypertrofie bij chirurgie in de voorgeschiedenis, persisterend oedeem of hypo- of depigmentatie ook voor.
Ten slotte kan er gekozen worden voor een ‘active surveillance’ beleid waarbij het natuurlijke beloop gemonitord wordt met kans op progressie.
|
Overzicht behandelopties lentigo maligna en in situ component lentigo maligna melanoom |
||||
|
|
Lokale recidiefkans |
Progressie naar LMM |
Voordelen |
Nadelen |
|
Chirurgie Conventioneel Micrografisch |
12%A <2,5% |
2%
|
Histologische beoordeling Behandelduur |
Cosmetische/functionele uitkomst Complicaties Mogelijke overbehandeling |
|
Imiquimod |
>23% |
<2% |
Cosmetische/ functionele uitkomst |
Kans op onderbehandeling Behandelduur Bijwerkingen behandeling |
|
Radiotherapie |
0-31% |
Onbekend |
Cosmetische/ functionele uitkomst |
Kans op onderbehandeling Behandelduur Bijwerkingen behandeling |
|
‘Active surveillance’ |
N.v.t. |
4% per jaar |
Niet-invasief |
Kans op progressie |
|
Reflectie confocale microscopieB |
<2% |
Onbekend |
Bepalen begrenzing Detectie subklinisch LMM Keuze behandeling |
Hoge kosten aanschaf Beperkt beschikbaar Geen vergoeding |
|
LMM = lentigo maligna melanoom A <3% bij een vrije histologische marge van ≥3 mm en 27% bij <3mm B Ondersteunende in vivo beeldvormende techniek voorafgaande (chirurgische) behandeling |
||||
Aanvaardbaarheid en haalbaarheid
Chirurgie vindt plaats in een klinische setting en radiotherapie in een poliklinische setting. Door de gefractioneerde behandeling van radiotherapie zal de patiënt(e) vaak meerdere keren per week naar het ziekenhuis moeten komen waar dus vervoer beschikbaar voor moet zijn. Deze invasieve therapieën zijn over het algemeen veel duurder, maar wel breed beschikbaar voor patiënten in verschillende centra in Nederland. De behandeling van imiquimod betreft een off-label behandeling en is relatief goedkoper t.o.v. meer invasieve behandelingen. Gezien de inflammatie en mogelijke bijwerkingen kan dit een erg intensieve behandeling voor patiënten zijn waar laagdrempelige begeleiding voor beschikbaar moet zijn om de therapietrouw te bevorderen.
Ondanks de veelbelovende resultaten van reflectie confocale microscopie, is breedschalige implementatie van deze techniek op het moment onwaarschijnlijk door de hoge kosten van de techniek zonder declareerbare zorgactiviteit.
Onderbouwing
Lentigo maligna (LM) presenteert zich meestal in het hoofd-hals gebied bij patiënten met een licht huidtype. Door de associatie met chronische UV-schade ligt de gemiddelde leeftijd rond de 70 jaar (Greveling, Wakkee, et al., 2016). LM wordt gekenmerkt door langzame groei en klinisch-dermatoscopische overlap met benigne afwijkingen; dit leidt regelmatig tot een patiënt- of diagnostische ‘delay’ (Lallas et al., 2014). Door het ontbreken van prospectieve data, is de exacte kans op progressie tot invasief lentigo maligna melanoom (LMM) onbekend. Het geschatte jaarlijks risico van onbehandelde LM op progressie is 3.5% (Menzies et al., 2020). De cumulatieve incidentie van LMM na conventionele chirurgische behandeling van LM is 2-3% na 25 jaar follow-up (Greveling, Wakkee, et al., 2016).
Dermatoscopisch onderzoek is waardevol in de diagnostiek en follow-up van LM. De histologische diagnostiek is erop gericht om i) de diagnose te bevestigen, ii) een eventuele invasieve component uit te sluiten en iii) de uitgebreidheid/begrenzing van de afwijking in te schatten om de behandelkeuze te ondersteunen. Dit kan verricht worden middels één of meerdere stansbiopten, een incisiebiopt of een diagnostische excisie bij laesies met een beperkte afmeting. Zowel dermatoscopie en Woods lamp onderzoek kunnen een meerwaarde hebben bij het aftekenen van LM, echter zal dit in de praktijk vooralsnog vaak leiden tot een onderschatting (Robinson, 2004). Tegenwoordig zijn er ook niet-invasieve beeldvormende technieken zoals reflectie confocale microscopie die, naast het stellen van de diagnose, met name een meerwaarde hebben bij het bepalen van de uitgebreidheid en diagnostiek naar een eventuele invasieve component (Elshot et al., 2024; Gouveia et al., 2023; Mesquita et al., 2024).
De meest gangbare behandelopties zijn chirurgische verwijdering, off-label imiquimod en radiotherapie. De chirurgische behandeling van LM wordt gecompliceerd door irradicaliteit en lokale recidieven t.g.v. de subklinische uitbreiding (Star et al., 2021). Verder kan de chirurgische behandeling van LM mogelijke cosmetische of functionele consequenties hebben bij een vaak oudere populatie. In deze gevallen zijn alternatieve behandelingen, waaronder radiotherapie en off-label topicaal imiquimod mogelijk. Tevens kan radiotherapie complicaties geven bij peri-oculaire laesies zoals ernstige droge ogen, retinopathie en cataract. Bij (kwetsbare) ouderen met veel co-morbiditeit en beperkte levensverwachting is ‘active surveillance’ ook te overwegen.
In deze module zal worden ingegaan op aanbevelingen m.b.t. de diagnostiek en (chirurgische) behandeling van LM.
Er werden in totaal 24 studies geïncludeerd (chirurgische interventies) op basis van beoordeling van titel en abstract. Uiteindelijk zijn er na het lezen van de volledige artikelen geen nieuwe studies geïncludeerd. Specifieke redenen voor exclusie zijn beschreven in bijlage 5.
Er werden in totaal 43 studies geïncludeerd (niet-chirurgische interventies) op basis van beoordeling van titel en abstract. Uiteindelijk zijn er na het lezen van de volledige artikelen geen studies geïncludeerd. Specifieke redenen voor exclusie zijn beschreven in bijlage 5.
Er is geen nieuw vergelijkend onderzoek gevonden.
Elshot et al. (2023) voerden een systematische review en meta-analyse uit. Het doel was om te onderzoeken wat de effecten van verschillende chirurgische technieken en reflectie confocale microscopie (RCM) zijn op lokale recidieven en overlevingsuitkomsten bij patiënten met lentigo maligna (LM) en lentigo maligna melanoom (LMM). Zie de overwegingen voor de beschrijving van de resultaten.
Om de uitgangsvraag te beantwoorden is een systematische literatuuranalyse uitgevoerd in de elektronische databases Embase en Medline. De zoekstrategie is toegevoegd in bijlage 4. Overwegingen en aanbevelingen zijn gebaseerd op basis van expert opinion aangezien er geen bruikbaar vergelijkend onderzoek gevonden werd. Voor de uitwerking is gebruik gemaakt van enkele losse ondersteunende artikelen.
Voor de chirurgische interventies werd de systematische review van Elshot et. al (2023) als basis gebruikt. De eerder verrichte systematische zoekstrategie van 20 mei 2022 werd herhaald op 18 oktober 2024 en dit leverde geen nieuw vergelijkend onderzoek op. Voor de niet-chirurgische behandelingen werd geen vergelijkend onderzoek gevonden.
Voor dit onderzoek is de volgende PICO opgesteld voor de niet chirurgische interventies:
P: Patiënten met lentigo maligna (melanoom) in het hoofd-hals gebied
I: Cryotherapie, imiquimod, radiotherapie, watch full waiting
C: Excisie met 5mm marge
O: Kwaliteit van leven, overleving, lokaal recidief
De werkgroep definieerde de uitkomstmaten als volgt en hanteerde de in de studies gebruikte definities.
Primair (cruciaal):
- Kwaliteit van leven
- Overleving
- Lokaal recidief
- 1 - Akay, B. N., Kocyigit, P., Heper, A. O., & Erdem, C. (2010). Dermatoscopy of flat pigmented facial lesions: Diagnostic challenge between pigmented actinic keratosis and lentigo maligna: Dermatoscopy of pigmented actinic keratosis. British Journal of Dermatology, 163(6), 1212–1217. https://doi.org/10.1111/j.1365-2133.2010.10025.x
- 2 - Alarcon, I., Carrera, C., Alos, L., Palou, J., Malvehy, J., & Puig, S. (2014). In vivo reflectance confocal microscopy to monitor the response of lentigo maligna to imiquimod. Journal of the American Academy of Dermatology, 71(1), 49–55. https://doi.org/10.1016/j.jaad.2014.02.043
- 3 - Avallone, G., Merli, M., Dell’Aquila, C., Quaglino, P., Ribero, S., Zalaudek, I., & Conforti, C. (2022). Imiquimod‐side effects in the treatment of periocular skin cancers: A review of the literature. Dermatologic Therapy, 35(4). https://doi.org/10.1111/dth.15326
- 4 - Canu, D., Kabore, R., Cogrel, O., Lamoureux, A., Gerard, E., Ouhabrache, N., & Beylot-Barry, M. (2025). Radiation therapy on lentigo maligna: A single-centre retrospective study on 91 patients. Annales de Dermatologie et de Vénéréologie, 152(1), 103342. https://doi.org/10.1016/j.annder.2025.103342
- 5 - Crouch, G., Sinha, S., Lo, S., Saw, R. P. M., Lee, K. K., Stretch, J., Shannon, K., Guitera, P., Scolyer, R. A., Thompson, J. F., & Ch’ng, S. (2021). Clinical outcomes following surgical treatment of lentigo maligna of the head and neck. European Journal of Surgical Oncology, 47(5), 1145–1151. https://doi.org/10.1016/j.ejso.2020.09.028
- 6 - Drakensjö, I., Rosen, E., Nilsson, M., & Girnita, A. (2020). Ten-year Follow-up Study of Grenz Ray Treatment for Lentigo Maligna and Early Lentigo Maligna Melanoma. Acta Dermato Venereologica, 0. https://doi.org/10.2340/00015555-3631
- 7 - Elshot, Y. S., Lasso Peña, D. J. P., Zupan‐Kajcovski, B., Bekkenk, M. W., Balm, A. J. M., Klop, W. M. C., & De Rie, M. A. (2024). Successful implementation of handheld reflectance confocal microscopy as the standard of care in the (surgical) management of lentigo maligna (melanoma). Journal of the European Academy of Dermatology and Venereology, jdv.20210. https://doi.org/10.1111/jdv.20210
- 8 - Elshot, Y. S., Tio, D. C. K. S., Van Haersma‐de With, A. S. E., Ouwerkerk, W., Zupan‐Kajcovski, B., Crijns, M. B., Limpens, C. E. J. M., Klop, W. M. C., Bekkenk, M. W., Balm, A. J. M., & De Rie, M. A. (2023). Lentigo maligna (melanoma): A systematic review and meta‐analysis on surgical techniques and presurgical mapping by reflectance confocal microscopy. Journal of the European Academy of Dermatology and Venereology, 37(5), 871–883. https://doi.org/10.1111/jdv.18880
- 9 - Fogarty, G. B., Hong, A., Economides, A., & Guitera, P. (2018). Experience with Treating Lentigo Maligna with Definitive Radiotherapy. Dermatology Research and Practice, 2018, 1–11. https://doi.org/10.1155/2018/7439807
- 10 - Gouveia, B. M., Carlos, G., Wadell, A., Sinz, C., Ahmed, T., Lo, S. N., Rawson, R. V., Ferguson, P. M., Scolyer, R. A., & Guitera, P. (2023). In vivo reflectance confocal microscopy can detect the invasive component of lentigo maligna melanoma: Prospective analysis and case–control study. Journal of the European Academy of Dermatology and Venereology, 37(7), 1293–1301. https://doi.org/10.1111/jdv.18998
- 11 - Greveling, K., De Vries, K., Van Doorn, M. B. A., & Prens, E. P. (2016). A two-stage treatment of lentigo maligna using ablative laser therapy followed by imiquimod: Excellent cosmesis, but frequent recurrences on the nose. British Journal of Dermatology, 174(5), 1134–1136. https://doi.org/10.1111/bjd.14330
- 12 - Greveling, K., Wakkee, M., Nijsten, T., Van Den Bos, R. R., & Hollestein, L. M. (2016). Epidemiology of Lentigo Maligna and Lentigo Maligna Melanoma in the Netherlands, 1989–2013. Journal of Investigative Dermatology, 136(10), 1955–1960. https://doi.org/10.1016/j.jid.2016.06.014
- 13 - Guitera, P., Haydu, L. E., Menzies, S. W., Scolyer, R. A., Hong, A., Fogarty, G. B., Gallardo, F., & Segura, S. (2014). Surveillance for treatment failure of lentigo maligna with dermoscopy and in vivo confocal microscopy: New descriptors. British Journal of Dermatology, 170(6), 1305–1312. https://doi.org/10.1111/bjd.12839
- 14 - Guitera, P., Pellacani, G., Crotty, K. A., Scolyer, R. A., Li, L.-X. L., Bassoli, S., Vinceti, M., Rabinovitz, H., Longo, C., & Menzies, S. W. (2010). The Impact of In Vivo Reflectance Confocal Microscopy on the Diagnostic Accuracy of Lentigo Maligna and Equivocal Pigmented and Nonpigmented Macules of the Face. Journal of Investigative Dermatology, 130(8), 2080–2091. https://doi.org/10.1038/jid.2010.84
- 15 - Hendrickx, A., Cozzio, A., Plasswilm, L., & Panje, C. M. (2020). Radiotherapy for lentigo maligna and lentigo maligna melanoma – a systematic review. Radiation Oncology, 15(1), 174. https://doi.org/10.1186/s13014-020-01615-2
- 16 - Hong AM, Lo SN, Fogarty GB, Stretch J, Wang W, Fernandez-Penas P, Martin RCW, Foote M, Soyer HP, Ruben J, Mar V, Rocha L, Festa-Neto C, Wratten C, Hogarth S, Collgros H, Glanz A, Gouveia BM, Scolyer RA, King MT, Guitera P. Radiotherapy versus imiquimod for complex lentigo maligna: A phase 3 randomized clinical trial. J Am Acad Dermatol. 2025 Jul 17:S0190-9622(25)02481-8. doi: 10.1016/j.jaad.2025.07.028. Epub ahead of print. PMID: 40683357.
- 17 - Hou, J. L., Reed, K. B., Knudson, R. M., Mirzoyev, S. A., Lohse, C. M., Frohm, M. L., Brewer, J. D., Otley, C. C., & Roenigk, R. K. (2015). Five-year outcomes of wide excision and Mohs micrographic surgery for primary lentigo maligna in an academic practice cohort. Dermatologic Surgery, 41(2), 211–218. https://doi.org/10.1097/DSS.0000000000000248
- 18 - Lallas, A., Argenziano, G., Moscarella, E., Longo, C., Simonetti, V., & Zalaudek, I. (2014). Diagnosis and management of facial pigmented macules. Clinics in Dermatology, 32(1), 94–100. https://doi.org/10.1016/j.clindermatol.2013.05.030
- 19 - Lallas, A., Lallas, K., Tschandl, P., Kittler, H., Apalla, Z., Longo, C., & Argenziano, G. (2021). The dermoscopic inverse approach significantly improves the accuracy of human readers for lentigo maligna diagnosis. Journal of the American Academy of Dermatology, 84(2), 381–389. https://doi.org/10.1016/j.jaad.2020.06.085
- 20 - Lallas, A., Moscarella, E., Kittler, H., Longo, C., Thomas, L., Zalaudek, I., Kyrgidis, A., Manoli, S. M., Meo, N., Papageorgiou, C., Apalla, Z., & Argenziano, G. (2021). Real‐world experience of off‐label use of imiquimod 5% as an adjuvant therapy after surgery or as a monotherapy for lentigo maligna. British Journal of Dermatology, 185(3), 675–677. https://doi.org/10.1111/bjd.20407
- 21 - Marsden, J. R., Fox, R., Boota, N. M., Cook, M., Wheatley, K., Billingham, L. J., Steven, N. M., & the NCRI Skin Cancer Clinical Studies Group, the U.K. Dermatology Clinical Trials Network and the LIMIT-1 Collaborative Group. (2017). Effect of topical imiquimod as primary treatment for lentigo maligna: The LIMIT-1 study. British Journal of Dermatology, 176(5), 1148–1154. https://doi.org/10.1111/bjd.15112
- 22 - Mataca, E., Migaldi, M., & Cesinaro, A. M. (2018). Impact of Dermoscopy and Reflectance Confocal Microscopy on the Histopathologic Diagnosis of Lentigo Maligna/Lentigo Maligna Melanoma. The American Journal of Dermatopathology, 40(12), 884–889. https://doi.org/10.1097/DAD.0000000000001212
- 23 - McKenna, J. K., Florell, S. R., Goldman, G. D., & Bowen, G. M. (2006). Lentigo maligna/lentigo maligna melanoma: Current state of diagnosis and treatment. Dermatologic Surgery, 32(4), 493–504. https://doi.org/10.1111/j.1524-4725.2006.32102.x
- 24 - McLeod, M., Choudhary, S., Giannakakis, G., & Nouri, K. (2011). Surgical treatments for lentigo maligna: A review. Dermatologic Surgery, 37(9), 1210–1228. https://doi.org/10.1111/j.1524-4725.2011.02042.x
- 25 - Melhoranse Gouveia, B., Ferguson, P. M., Lo, S. N., Collgros, H., Martin, L. K., Sinz, C., Smit, A. K., Gallo, B., Ho, G., Glanz, A., Scolyer, R. A., Cust, A. E., & Guitera, P. (n.d.). In vivo reflectance confocal microscopy role for early to advanced lentigo maligna melanoma spectrum: A systematic review and pooled analysis. Journal of the European Academy of Dermatology and Venereology, n/a(n/a). https://doi.org/10.1111/jdv.20389
- 26 - Menzies, S. W., Liyanarachchi, S., Coates, E., Smith, A., Cooke-Yarborough, C., Lo, S., Armstrong, B., Scolyer, R. A., & Guitera, P. (2020). Estimated risk of progression of lentigo maligna to lentigo maligna melanoma. Melanoma Research, 30(2), 193–197. https://doi.org/10.1097/CMR.0000000000000619
- 27 - Mesquita, Y., Marques, I. R., Pera Calvi, I., Cruz, S. A., Godoi, A., Lapenda, I. L., de Moraes-Souza, R., Relvas, J. H., Vilbert, M., Nehal, K. S., & Navarrete-Dechent, C. (2024). Reflectance confocal microscopy for margin mapping of melanoma of the lentigo maligna type: A systematic review and meta-analysis. Journal of the European Academy of Dermatology and Venereology: JEADV. https://doi.org/10.1111/jdv.20383
- 28 - Navarrete-Dechent, C., Aleissa, S., Connolly, K., Hibler, B. P., Dusza, S. W., Rossi, A. M., Lee, E., & Nehal, K. S. (2021). Clinical size is a poor predictor of invasion in melanoma of the lentigo maligna type. Journal of the American Academy of Dermatology, 84(5), 1295–1301. https://doi.org/10.1016/j.jaad.2020.10.023
- 29 - Neumann, I., Patalay, R., Kaushik, M., Timlin, H., & Daniel, C. (2023). Treatment of periocular lentigo maligna with topical 5% Imiquimod: A review. Eye, 37(3), 408–414. https://doi.org/10.1038/s41433-022-02165-5
- 30 - Peruilh-Bagolini, L., Apalla, Z., González-Cuevas, R., Lallas, K., Papageorgiou, C., Bobos, M., Manoli, S. M., Gkentsidi, T., Spyridis, I., Lazaridou, E., Sotiriou, E., Vakirlis, E., Ioannides, D., & Lallas, A. (2020). Dermoscopic predictors to discriminate between in situ and early invasive lentigo maligna melanoma: A retrospective observational study. Journal of the American Academy of Dermatology, 83(1), 269–271. https://doi.org/10.1016/j.jaad.2020.03.030
- 31 - Pralong, P., Bathelier, E., Dalle, S., Poulalhon, N., Debarbieux, S., & Thomas, L. (2012). Dermoscopy of lentigo maligna melanoma: Report of 125 cases: Dermoscopy of lentigo maligna melanoma. British Journal of Dermatology, 167(2), 280–287. https://doi.org/10.1111/j.1365-2133.2012.10932.x
- 32 - Read, T., Noonan, C., David, M., Wagels, M., Foote, M., Schaider, H., Soyer, H. P., & Smithers, B. M. (2016). A systematic review of non‐surgical treatments for lentigo maligna. Journal of the European Academy of Dermatology and Venereology, 30(5), 748–753. https://doi.org/10.1111/jdv.13252
- 33 - Robinson, J. K. (2004). Use of Digital Epiluminescence Microscopy to Help Define the Edge of Lentigo Maligna. Archives of Dermatology, 140(9). https://doi.org/10.1001/archderm.140.9.1095
- 34 - Schiffner, R., Schiffner-Rohe, J., Vogt, T., Landthaler, M., Wlotzke, U., Cognetta, A. B., & Stolz, W. (2000). Improvement of early recognition of lentigo maligna using dermatoscopy. Journal of the American Academy of Dermatology, 42(1), 25–32. https://doi.org/10.1016/S0190-9622(00)90005-7
- 35 - Star, P., Rawson, R. V., Drummond, M., Lo, S., Scolyer, R. A., & Guitera, P. (2021). Lentigo maligna: Defining margins and predictors of recurrence utilizing clinical, dermoscopic, confocal microscopy and histopathology features. Journal of the European Academy of Dermatology and Venereology, 35(9), 1811–1820. https://doi.org/10.1111/jdv.17349
- 36 - Tio, D., Van Der Woude, J., Prinsen, C. A. C., Jansma, E. P., Hoekzema, R., & Van Montfrans, C. (2017). A systematic review on the role of imiquimod in lentigo maligna and lentigo maligna melanoma: Need for standardization of treatment schedule and outcome measures. Journal of the European Academy of Dermatology and Venereology, 31(4), 616–624. https://doi.org/10.1111/jdv.14085
- 37 - Vaidya, T. S., Bander, T. S., Musthaq, S., Lampley, N., Lee, E. H., Nehal, K. S., & Rossi, A. M. (2021). Validation of a patient decision aid for the treatment of lentigo maligna. Journal of the American Academy of Dermatology, 84(6), 1751–1753. https://doi.org/10.1016/j.jaad.2020.10.043
- 38 - Vaienti, S., Calzari, P., & Nazzaro, G. (2023). Topical Treatment of Melanoma In Situ, Lentigo Maligna, and Lentigo Maligna Melanoma with Imiquimod Cream: A Systematic Review of the Literature. Dermatology and Therapy, 13(10), 2187–2215. https://doi.org/10.1007/s13555-023-00993-1
- 39 - Zoutendijk, J., Koljenovic, S., Wakkee, M., Mooyaart, A. L., Nijsten, T., & Van Den Bos, R. R. (2022). Clinical findings are not helpful in detecting lentigo maligna melanoma in patients with biopsy‐proven lentigo maligna. Journal of the European Academy of Dermatology and Venereology, 36(12), 2325–2330. https://doi.org/10.1111/jdv.18346
- 40 - Zoutendijk, J., Tio, D., Koljenovic, S., & Bos, R. R. (2019). Nine per cent of biopsy‐proven lentigo maligna lesions are reclassified as lentigo maligna melanoma after surgery. British Journal of Dermatology, 181(2), 383–384. https://doi.org/10.1111/bjd.17714
Overzicht van geëxcludeerde studies
|
Artikel |
Reden van exclusie |
|
Chirurgische interventies |
|
|
Ahn (2022) |
Voldoet niet aan PICO |
|
Carmona-Rocha (2024) |
Overzichtsartikel |
|
Charalambides (2022) |
Overzichtsartikel |
|
Curtis (2024) |
Voldoet niet aan inclusiecriteria (andere patiëntpopulatie) |
|
Himeles (2023) |
Voldoet niet aan inclusiecriteria (andere patiëntpopulatie) |
|
Martinez-Molina (2023) |
Voldoet niet aan PICO (interventie) |
|
Maurichi (2023) |
Voldoet niet volledig aan PICO (patiëntpopulatie), vergelijking 5 en 10 mm marge |
|
Maurichi, critical structures (2023) |
Voldoet niet volledig aan PICO (patiëntpopulatie) |
|
McInnis-Smith (2024) |
Voldoet niet aan inclusiecriteria (andere patiëntpopulatie) |
|
Navarrete-Dechent (2023) |
Voldoet niet aan PICO (controle) |
|
O'Hern (2023) |
Betreft een research letter (to the editor), voldoet niet aan inclusiecriteria |
|
Salih (2024) |
Voldoet niet aan PICO (outcome) |
|
Sun (2024) |
Voldoet niet aan PICO (interventie) en voldoet niet aan inclusiecriteria |
|
Tate (2024) |
Voldoet niet aan PICO (melanoma in situ; niet specifiek lentigo maligna) |
|
Taylor (2024) |
Betreft een letter to the editor, voldoet niet aan inclusiecriteria |
|
Taylor, retrospective cohort (2024) |
Betreft een letter to the editor, voldoet niet aan inclusiecriteria |
|
Theunissen (2021) |
Systematische review, alle artikelen van voor 2022 |
|
Tzellos (2016) |
Voldoet niet aan PICO (interventie) |
|
Vieira (2022) |
Geen vergelijkend onderzoek en voldoet niet aan inclusiecriteria |
|
Xia (2023) |
Voldoet niet aan PICO |
|
Zitelli (2024) |
Betreft een editorial |
|
Zoutendijk (2021) |
Overzichtsartikel |
|
Overige interventies |
|
|
Brand (2019) |
Voldoet niet aan PICO |
|
Campolmi (1994) |
Geen full tekst beschikbaar, enkel abstract |
|
Chambers (2021) |
Voldoet niet aan PICO (intervention) en geen vergelijkend onderzoek |
|
Coleman III (1980) |
Betreft een review, te kleine aantal cases per therapie |
|
Cordel (2004) |
Geen Engelstalig of Nederlands artikel, geen vertaling beschikbaar |
|
Craythorne (2008) |
Voldoet niet aan inclusiecriteria, < 10 cases |
|
Dancuart (1980) |
Geen vergelijkend onderzoek |
|
Daude (2023) |
Voldoet niet aan PICO (intervention) |
|
De Moraes (2007) |
Geen vergelijkend onderzoek |
|
Drakensjö (2020) |
Voldoet niet volledig aan PICO en inclusiecriteria (ook LM/LMM op het lichaam geïncludeerd in studie) |
|
Farshad (2002) |
Geen vergelijkend onderzoek |
|
Gautschi (2016) |
Voldoet niet volledig aan PICO en inclusiecriteria (ook LM/LMM op het lichaam geïncludeerd in studie) |
|
Harwood (1982) |
Niet vergelijkend onderzoek, zeer oude publicatie en voldoet niet volledig aan PICO |
|
Harwood (1983) |
Niet vergelijkend onderzoek, zeer oude publicatie en voldoet niet volledig aan PICO |
|
Harwood, Lawson (1983) |
Geen full tekst beschikbaar en kopie van bovenstaande artikel |
|
Hawkey (2017) |
Voldoet niet aan PICO (intervention/outcome) |
|
Hedblad (2012) |
Geen vergelijkend onderzoek |
|
Hendrickx (2020) |
Systematische review, maar voldoet niet aan PICO |
|
Kai (2016) |
Geen vergelijkend onderzoek |
|
Kirtschig (2015) |
Geen vergelijkend onderzoek |
|
Kuflik (1994) |
Voldoet niet aan PICO (patiëntpopulatie) |
|
Lazarevic (2019) |
Voldoet niet aan PICO (patiëntpopulatie) |
|
Ly (2011) |
Voldoet niet aan PICO (intervention) |
|
Marsden (2017) |
Voldoet niet aan PICO (outcomes) |
|
Mora (2015) |
Voldoet niet aan PICO (patiëntpopulatie) |
|
Naylor (2003) |
Voldoet niet aan PICO (patiëntpopulatie) |
|
Panizzon (1999) |
Geen full tekst beschikbaar |
|
Papanikolaou (2019) |
Geen vergelijkend onderzoek |
|
Pastore (2024) |
Betreft een letter to the editor en voldoet niet aan PICO (intervention) |
|
Powell (2004) |
Geen vergelijkend onderzoek |
|
Powell (2009) |
Geen vergelijkend onderzoek |
|
Ramsdell (2009) |
Betreft een case report |
|
Read (2016) |
Voldoet niet aan PICO (patiëntpopulatie, locaties van LM laesies niet gespecificeerd) |
|
Seyed Jafari (2023) |
Voldoet niet aan PICO (patiëntpopulatie) |
|
Spenny (2007) |
Voldoet niet aan PICO (outcomes) |
|
Swetter (2015) |
Voldoet niet aan PICO (patiëntpopulatie en intervention) |
|
Swetter (2019) |
Betreft een richtlijn, Voldoet niet aan PICO (patiëntpopulatie, locaties van LM laesies niet gespecificeerd) |
|
Tio (2017) |
Voldoet niet aan PICO (patiëntpopulatie) |
|
Tio (2019) |
Geen vergelijkend onderzoek |
|
Tsang (1994) |
Geen full tekst beschikbaar |
|
Vaienti (2023) |
Voldoet niet aan PICO (patiëntpopulatie) en geen vergelijkend onderzoek |
|
Van Meurs (2010) |
Geen vergelijkend onderzoek |
|
Wong (2012) |
Geen vergelijkend onderzoek |
Beoordelingsdatum en geldigheid
Publicatiedatum : 27-01-2026
Beoordeeld op geldigheid : 27-01-2026
Algemene gegevens
De ontwikkeling van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Samenstelling van het cluster
Voor het ontwikkelen van de richtlijnmodule is in 2024 een multidisciplinaire cluster ingesteld. Dit cluster bestaat uit vertegenwoordigers van alle relevante organisaties die betrekking hebben op de zorg voor patiënten met cutane maligniteiten.
Het cluster Cutane Maligniteiten bestaat uit meerdere richtlijnen, zie hier voor de actuele clusterindeling. De stuurgroep bewaakt het proces van modulair onderhoud binnen het cluster. De expertisegroepsleden worden indien nodig gevraagd om hun expertise in te zetten voor een specifieke richtlijnmodule. Het cluster Cutane Maligniteiten bestaat uit de volgende personen:
Clusterstuurgroep
|
Clusterstuurgroepleden – 2024-2025 |
Vereniging |
|
Wetenschappelijke verenigingen; |
|
|
E. I. Plasmeijer |
NVDV |
|
K. Mosterd |
NVDV |
|
N. C. Naus |
NOG |
|
D. J. Grünhagen |
NVvH |
|
J. J. Bonenkamp |
NVvH |
|
A. B. Francken |
NVvH |
|
A. J. M. van den Eertwegh |
NIV |
|
K. Hendriks / J. Collette (huidig) |
HUKAS |
Clusterexpertisegroep
|
Expertisegroepleden – 2024-2025 |
Vereniging |
|
Wetenschappelijke verenigingen; |
|
|
E. I. Plasmeijer |
NVDV |
|
K. Mosterd |
NVDV |
|
E. Rácz |
NVDV |
|
Y. S. Elshot |
NVDV |
|
R. van Doorn |
NVDV |
|
N. C. Naus |
NOG |
|
D. J. Grünhagen |
NVvH |
|
J. J. Bonenkamp |
NVvH |
|
A. B. Francken |
NVvH |
|
S. Wilgenhof |
NIV |
|
A. Joosse |
NIV |
|
K. F. Bol |
NIV |
|
E. J. Blok |
NIV |
|
A. J. M. van den Eertwegh |
NIV |
|
M. Jalving |
NIV |
|
W. A. M. Blokx |
NVVP |
|
R. O. B. de Keizer |
NOG |
|
A. Bruining |
NVvR |
|
P. de Graaf |
NVvR |
|
Patiëntenverenigingen; |
|
|
K. Hendriks / J. Collette (huidig) |
HUKAS |
Met ondersteuning van
- Nederlandse Vereniging voor Dermatologie en Venereologie, NVDV
- Drs. T. A. Teunissen, arts-onderzoeker richtlijnontwikkeling (vanaf oktober 2024)
- Dr. W. A. van Enst, directeur NVDV en epidemioloog
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle clusterstuurgroepleden en actief betrokken expertisegroepsleden (fungerend als schrijver en/of meelezer bij tenminste één van de geprioriteerde richtlijnmodules) hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een richtlijnmodule worden wijzigingen in belangen aan de projectleider doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase. Een overzicht van de belangen van de clusterleden en betrokken expertisegroepsleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Tabel 1. Gemelde (neven)functies en belangen stuurgroep
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
E.I. Plasmeijer (NVDV) |
Dermatoloog, Antoni van Leeuwenhoek |
Detachering als dermatoloog LUMC vanuit AVL 1 dag per week, onbetaald Lid richtlijn melanoom, SCC en PeIN, onbetaald Lid bestuur Win-O, onbetaald Lid bestuur SCOPE Europe, onbetaald |
Geen. |
Geen. |
|
K. Mosterd (NVDV) |
Dermatoloog, hoofd afdeling dermatologie MUMC+, hoogleraar onco-dermatologie |
Consultancy Allmiral en Pierre Fabre (betaald] Lid commissie nascholing (onbetaald) Lid stuurgroep huidkanker (onbetaald) Voorzitter en docent landelijke AIOS nascholing COCOM (betaald) Verschillende presentaties voor congressen (dermatologendagen, MKA nascholing, EADO): deels betaald |
Geen. Wel extern gefinancierd onderzoek (Diverse ZonMW gesubsidieerde studies verricht op het gebied van huidkanker. Registry hedgehog inhibitors registratie, gefinancieerd doeo Sun Pharma). |
Geen. |
|
N.C. Naus (NOG) |
Oogarts, afdelingshoofd Erasmus MC |
Voorzitter richtlijnencomissie NOG (vacatiegelden) |
Geen. |
Geen. |
|
D.J. Grünhagen (NVvH) |
Chirurg, Erasmus MC |
Bestuurslid NVCO Bestuurslid DMSCG Bestuurslid DSG (sarcomen) VZ richtlijn weke delen tumoren (opgeleverd) Lid richtlijncie melanomen |
Geen. Wel extern gefinancierd onderzoek (Projectleider OMIT-trial, gefinancierd door SGS). Niet relevant voor deze richtlijn. PI van 2 recent gepubliceerde studies naar de meerwaarde van resp re-excisie en SN bij dunne melanomen (EJC 2025). |
Geen |
|
J. J. Bonenkamp (NVvH) |
Chirurg, Radboud UMC |
Bestuurslid bij DMTR Bestuurslid bij TFG Raad van Advies van Stichting Melanoom |
Geen. |
Geen. |
|
A.B. Francken (NVvH) |
Chirurg, Isala Zwolle |
Lid richtlijncomissie, FMS Bestuur Nederlandse Werkgroep voor Endocriene Chirurgie Voorzitter werkgroep Audit NVvH Voorzitter weke delen werkgroep Isala Docent module anatomie mamma/axilla (voor)opleiding Heelkunde Lid tumorfocusgroep melanoom, IKNL Lid werkgroep mammacarcinoom, NVCO, sectie kwaliteit Redactieraad Nederlands Tijdschrift voor Heelkunde Reviewer van verschillende wetenschappelijke tijdschriften |
Geen. |
Geen. |
|
A. J. M. van den Eertwegh (NIV) |
Medisch oncoloog, Amsterdam UMC |
Voorzitter DMTR (Dutch Melanoma Treatment registry)(vacatiegeld aan Amsterdam UMC) Deelname aan adviesraad (betaald aan Amsterdam UMC): Bristol-Myers Squibb, MSD Oncology, Ipsen, Pierre Fabre, Janssen Cilag BV |
Geen. Wel extern gefinancierd onderzoek (Projectleider INTRIM melanoom studie van IDERA. Projectleider REPOSIT melanoom studie van ROCHE en deelnemer aan DMTR van Novartis, Pierre Fabre, MSD, BMS en ziektekosten) |
Geen. |
|
J. Collette (HUKAS) |
Patiëntvertegenwoordiger De Huidkanker Stichting. |
|
|
|
Clusterexpertisegroep
Tabel 2. Gemelde (neven)functies en belangen expertisegroep
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Y.S. Elshot (NVDV) |
Dermatoloog 1) Amsterdam UMC (0,4 FTE), betaald 2) Antoni van Leeuwenhoek ziekenhuis (0,4 FTE), betaald |
Geen |
Geen |
Geen |
|
K.F. Bol (NVDV) |
participeren in de herziening/ontwikkeling van de Cluster Maligniteiten van de huid - vergoeding van vacatiegelden |
Geen |
Geen |
Geen |
|
R. Van Doorn (NVDV) |
Dermatoloog, Leids Universitair Medisch Centrum en Antoni van Leeuwenhoek ziekenhuis |
Onbetaald lid van het bestuur van de European Society for Dermatological Research en de Nederlandse Vereniging voor Experimentele Dermatologie en de Stichting Opsporing Erfelijke Tumoren. |
Geen. Wel extern gefinancierd onderzoek verricht (therapie voor naevus en melanoom precursurs, gefinancierd door Stichting Dioraphte. Screens voor nieuwe melanoom precursor therapieën, gefinancierd door Stichting Josephine Nefkens. DNA methylatie biomarkers voor melanoom, gefinancierd door PPS/Health Holland. Preventie en therapie van melanoom bij FAMM syndroom, gefinancierd door Zeldzame Zieken Fonds). |
Geen |
|
W.A.M. Blokx (NVVP) |
Patholoog, UMC Utrecht |
Geen |
Geen. Wel extern gefinancierd onderzoek, niet van invloed op richtlijn (projectleider; onderzoek naar toepassing van kunstmatige intelligentie bij diagnosticeren van melanocytaire tumoren. Gefinancierd door Hanarth fonds). |
Geen |
|
E.I. Plasmeijer (NVDV) |
Dermatoloog, Antoni van Leeuwenhoek |
Detachering als dermatoloog LUMC vanuit AVL 1 dag per week, onbetaald Lid richtlijn melanoom, SCC en PeIN, onbetaald Lid bestuur Win-O, onbetaald Lid bestuur SCOPE Europe, onbetaald |
Geen. |
Geen. |
|
K. Mosterd (NVDV) |
Dermatoloog, hoofd afdeling dermatologie MUMC+, hoogleraar onco-dermatologie |
Consultancy Allmiral en Pierre Fabre (betaald] Lid commissie nascholing (onbetaald) Lid stuurgroep huidkanker (onbetaald) Voorzitter en docent landelijke AIOS nascholing COCOM (betaald) Verschillende presentaties voor congressen (dermatologendagen, MKA nascholing, EADO): deels betaald |
Geen. Wel extern gefinancierd onderzoek (Diverse ZonMW gesubsidieerde studies verricht op het gebied van huidkanker. Registry hedgehog inhibitors registratie, gefinancieerd doeo Sun Pharma). |
Geen |
|
E. Rácz (NVDV) |
Dermatoloog, Universitair Medisch Centrum Groningen |
Geen |
Geen. Wel extern gefinancierd odnerzoek (Deelname aan studie naar de behandeling van cutaan plaveiselcelcarcinoom met intralesionale immunotherapie; sponsor Regeneron, 1 pt geincludeerd; looptijd maart-december 2025). |
Geen |
|
S. Wilgenhof (NIV) |
Internist-oncoloog in het Antoni van Leeuwenhoek ziekenhuis. Principal investigator: CA224020 studie (ClinicalTrials.gov number, NCT01968109) R3767-ONC-2011 studie (NCT05352672) E2139 (NCT05270044) vorinostat studie (NCT02836548) Subinvestigator: TIL studie (ClinicalTrials.gov number, NCT02278887) NADINA studie (ClinicalTrials.gov number, NCT04949113) safe stop studie safe stop ipi-nivo (NCT05652673) E1325 (NCT02362594) NIVEC studie (NCT04330430) NKTR-214 + nivolumab (NCT03635983) EBIN (NCT03235245) DONIMI (NCT04133948) MASTERKEY-115 (NCT04068181) IOB-013 (NCT05155254) |
Adviesraden: Eisai, Bristol-Myers Squibb, Pierre Fabre, Novartis, Pfizer en Ipsen (betaald aan instituut (AVL)); educatief symposium: MSD en Bristol-Myers Squibb (betaald aan insituut (AVL)) |
Geen. Wel extern gefinancierd onderzoek, niet van invloed op richtlijn (EU Horizon 2020 (No 875052): CAPABLE: Pilot study of the eHealth application Cancer Patients Better Life Experience EU (101104801): CARE-1: Optimizing Treatments for Metastatic Renal Carcinoma) |
Geen |
|
K. F. Bol (NIV) |
Participeren in de herziening/ontwikkeling van de Cluster Maligniteiten van de huid - vergoeding van vacatiegelden |
Geen |
Geen. Wel extern gefinancierd onderzoek, niet van invloed op richtlijn |
Geen |
|
M. Jalving (NIV) |
Internist-oncoloog, UMCG |
ESMO climate change task force, onbetaald Richtlijn Melanoom, alleen SKMS vergoeding Richtlijn Endometriumcarcinoom, allen SKMS vergoeding Voorzitter Adviesraad Junior Scientific Masterclass UMCG, onbetaald Deelname adviesraden Pierre Fabre en Regeneron (geld naar UMCG) |
Geen |
Geen |
|
E. J. Blok (NIV) |
Internist-oncoloog, LUMC |
Geen |
Geen |
Geen |
|
R. O. B. de Keizer (NOG) |
Oogarts, oogziekenhuis Rotterdam |
Oogarts, Erasmus MC. |
Geen |
Geen |
|
A. Bruining (NVvR) |
NKI AVL |
Richtlijn revisie commissie |
Geen |
Geen |
|
J. Collette (HUKAS) |
Patiëntvertegenwoordiger De Huidkanker Stichting. |
|
|
|
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door deelname van relevante patiëntenorganisaties aan de need-for-update en/of prioritering. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijnmodule is tevens ter commentaar voorgelegd aan alle relevante patiëntenorganisaties in de stuur- en expertisegroep (zie ‘Samenstelling cluster’ onder ‘Verantwoording’) en aan alle patiëntenorganisaties die niet deelnemen aan de stuur- en expertisegroep, maar wel hebben deelgenomen aan de need-for-update (zie ‘Need-for-update’ onder ‘Verantwoording’). De eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Module |
Uitkomst raming |
Toelichting |
|
Module lentigo maligna |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 3.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Need-for-update, prioritering en uitgangsvragen
Tijdens de need-for-update fase (december, 2023) inventariseerde het cluster de geldigheid van de richtlijnmodules binnen het cluster. Naast de partijen die deelnemen aan de stuur- en expertisegroep zijn hier ook andere stakeholders voor benaderd. Per richtlijnmodule is aangegeven of deze geldig is, herzien moet worden, kan vervallen of moet worden samengevoegd. Ook was er de mogelijkheid om nieuwe onderwerpen aan te dragen die aansluiten bij één (of meerdere) richtlijn(en) behorend tot het cluster. De richtlijnmodules waarbij door één of meerdere partijen werd aangegeven herzien te worden, werden doorgezet naar de prioriteringsronde. Ook suggesties voor nieuwe richtlijnmodules werden doorgezet naar de prioriteringsronde. Afgevaardigden vanuit de partijen in de stuur- en expertisegroep werden gevraagd om te prioriteren (zie ‘Samenstelling cluster’ onder ‘Verantwoording’). Hiervoor werd de RE-weighted Priority-Setting (REPS) – tool gebruikt. De uitkomsten (ranklijst) werd gebruikt als uitgangspunt voor de discussie. Voor de geprioriteerde richtlijnmodules zijn door de het cluster concept-uitgangsvragen herzien of opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde het cluster welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. Het cluster waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde het cluster tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. [Review Manager 5.4] werd indien mogelijk gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding). GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
Tabel 3. Gradaties voor de kwaliteit van wetenschappelijk bewijs
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in een richtlijnmodule volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door het cluster wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. Het cluster heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Tabel 4. Sterkte van de aanbevelingen
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
Bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de richtlijnmodule Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd voorgelegd aan alle partijen die benaderd zijn voor de need-for-update fase. De commentaren werden verzameld en besproken met het cluster. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door het cluster. De definitieve richtlijnmodule werd ter autorisatie of goedkeuring voorgelegd aan de partijen die beschreven staan bij ‘Initiatief en autorisatie’ onder ‘Verantwoording’.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
- Chirurgische interventies
De search is geüpdatet tot 18-10-2024 (periode 2022-2025). Voor deze vraag is een update uitgevoerd van de zoekstrategie van de systematische review van Elshot uit 2023. Lentigo maligna (melanoma): ‘A systematic review and meta-analysis on surgical techniques and presurgical mapping by reflectance confocal microscopy’.
De zoekactie is met behulp van de PICO-systematiek opgebouwd. De zoekvragen hebben de P als gemeenschappelijke onderdeel. De overige onderdelen van de PICO werden geformuleerd op basis van de uitgangsvraag.
De volgende afbakening is gebruikt:
Voor de P: Patiënten met lentigo maligna (melanoom) in het hoofd-hals gebied
Voor de I: Micrografische chirurgie, conservatieve chirurgie, in vivo presurgical mapping by reflectance confocal microscopy)
Voor de C: Excisie met 5mm marge
Voor de O: Kwaliteit van leven, overleving, lokaal recidief
Inclusie- en exclusiecriteria
|
Inclusiecriteria |
Exclusiecriteria |
|
lentigo maligna (melanoom) in het hoofd-hals gebied |
Lentigo maligna op andere locatie op het lichaam |
|
Nederlandstalige en Engelstalige publicaties |
niet-chirurgische of destructieve therapieën, zoals (neo)adjuvant topicaal imiquimod gecombineerd met chirurgische behandeling |
|
Toepassing van een referentiestandaard |
Andere typen melanoom (zoals superficieel spreidend melanoom) |
|
Systematische reviews, randomized controlled trials (RCT’s) of observationele studies; |
Case reports, letters to the editor, conference abstract, algemene reviews |
Uitgangsvragen
- Wat is de optimale behandeling voor patiënten met een lentigo maligna en de in situ component van lentigo maligna melanoom?
EMBASE (18-10-2024)
Zoektermen
- 'malignant lentigo'/exp OR 'melanoma in situ'/exp OR ('cutaneous melanoma'/exp AND 'precancer and cancer-in-situ'/exp) OR (((lentig* OR freckle*) NEAR/3 (melanom* OR malign* OR hutchinson*)):ti,ab,kw) OR 'hutchinson* melano*':ti,ab,kw OR dubreuilh*:ti,ab,kw OR (((melanom* OR melanos*) NEAR/6 ('in situ' OR precancer* OR 'pre-cancer*' OR 'pre-invasive')):ti,ab,kw) [zoekterm].mp
- 'surgical margin'/exp OR 'second look surgery'/exp OR 'microsurgery'/exp OR 'mohs micrographic surgery'/exp OR margin:ti,ab,kw OR margins:ti,ab,kw OR perimeter*:ti,ab,kw OR 'peri meter*':ti,ab,kw OR contoured:ti,ab,kw OR (cme:ti,ab,kw AND (excis*:ti,ab,kw OR resect*:ti,ab,kw OR procedur*:ti,ab,kw OR staged:ti,ab,kw)) OR coll?ret*:ti,ab,kw OR spaghett*:ti,ab,kw OR 'bread loaf*':ti,ab,kw OR breadloaf*:ti,ab,kw
- ((excis* OR reexcis* OR resect* OR 're-sect*' OR surg* OR resurg* OR presurg* OR operat* OR reoperat* OR preoperat* OR cut OR cutting OR remov* OR wide OR wider OR width* OR larger OR deep OR depth* OR size OR sizes OR narrow* OR extensiv* OR nonextensiv* OR nonradical* OR 'non-radical*' OR limited OR control OR controlled OR safety OR safe OR secure OR security OR clinical* OR subclinic* OR delimitat* OR delineat* OR determin* OR evaluat* OR assess* OR map* OR confocal* OR rcm OR dermascop* OR vivascop* OR microscop* OR positive OR free OR negative OR clear OR clearance OR mm OR 3mm* OR 5mm* OR 10mm* OR 3d OR '1-cm' OR 1cm OR '1?0-cm' OR '1?0cm' OR '3-d' OR '3-dimension*') NEAR/5 (border OR borders OR boundar* OR bounds OR rim OR rims OR margin* OR periphery OR peripheries OR stripe OR stripes OR circumferential)):ti,ab,kw
- (((rcm* OR microscop* OR vivascop* OR confoc* OR dermascop* OR immun* OR histo* OR lentigo OR l?esion* OR lm OR lmm) NEAR/3 (delineation* OR demarcation* OR contour* OR outline OR outlines)):ti,ab,kw) OR (((rcm* OR vivascop* OR confoc* OR microscop* OR dermascop*) NEAR/4 (map* OR clearance)):ti,ab,kw)
- (((wide OR wider OR width* OR narrow* OR squar* OR staged OR stages OR multistag* OR phases OR '2-phas*' OR 'two-phas*' OR multiphas* OR multistep OR 'multi-step' OR mapped) NEAR/6 (excis* OR reexci* OR surg* OR resurg* OR section* OR resect* OR 're-sect*')):ti,ab,kw) OR wle*:ti,ab,kw
- ((excision OR reexcision OR resection OR 're-section' OR removal OR cutting OR delineat*) NEAR/2 (techni* OR method* OR approach* OR procedur*)):ti,ab,kw
- ((excis* OR reexcis* OR resect* OR 're-sect*' OR remov* OR surg* OR cutting OR cut OR delineat*) NEAR/3 (geometric* OR fusiform*)):ti,ab,kw
- ((squar* OR staged) NEAR/3 (procedur* OR technique* OR method* OR approach OR johnson*)):ti,ab,kw
- (staged NEAR/3 (squar* OR serial OR geometric*)):ti,ab,kw
- ((serial OR 'en-face') NEAR/2 (excis* OR reexci* OR surg* OR resurg* OR map*)):ti,ab,kw
- moh:ti,ab,kw OR mohs*:ti,ab,kw OR 'micro-surg*':ti,ab,kw OR microsurg*:ti,ab,kw OR 'micro-exc*':ti,ab,kw OR microexc*:ti,ab,kw OR 'micro-graph*':ti,ab,kw OR micrograph*:ti,ab,kw
- ((conservativ* OR conventional OR standard OR traditional*) NEAR/2 (excis* OR reexcis* OR resect* OR 're-sect*' OR surg* OR cut OR cutting OR remov*) NEAR/9 (lentig* OR lm OR lmm OR mis)):ti,ab,kw
- #2 OR #3 OR #4 OR #5 OR #6 OR #7 OR #8 OR #9 OR #10 OR #11 OR #12
- #1 AND #13
- #14 AND [01-01-2022]/sd NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)
Resultaten = 218
OVID/MEDLINE (18-10-2024)
Zoektermen
- Hutchinson's melanotic freckle/
- (melanoma/ or lentigo/) and carcinoma in situ/
- (lentig* adj3 (melanom* or malign* or Hutchinson*)).tw,kf.
- Hutchinson* melano*.tw,kf.
- ((Hutchinson* or melanotic or melanocyt*) adj3 freckl*).tw,kf.
- Dubreuilh.tw,kf.
- ((melanom* or melanos*) adj6 (in situ or precancer* or pre-cancer*)).tw,kf.
- or/1-7
- "margins of excision"/
- second look surgery/
- microsurgery/
- Mohs surgery/
- (margin or margins or perimeter* or peri-meter*).tw,kf.
- (contoured or (CME and (excis* or resect* or procedur* or staged)) or coll#ret* or spaghett* or bread-loaf* or breadloaf*).tw,kf.
- ((excis* or reexcis* or resect* or re-sect* or surg* or resurg* or presurg* or operat* or reoperat* or preoperat* or cut or cutting or remov* or wide or wider or width* or larger or deep or depth* or size or sizes or narrow* or extensiv* on nonextensiv* or nonradical* or non-radical* or limited or control or controlled or safety or safe or secure or security or clinical* or subclinic* or delimitat* or delineat* or determin* or evaluat* or assess* or map* or confocal* or RCM or dermascop* or vivascop* or microscop* or positive or free or negative or clear or clearance or mm or 3mm* or 5mm* or 10mm* or 1-cm or 1cm or 1?0-cm or 1?0cm or 3D or 3-D or 3-dimension*) adj5 (border or borders or boundar* or bounds or rim or rims or margin* or periphery or peripheries or stripe or stripes or circumferential)).tw,kf.
- ((RCM* or microscop* or vivascop* or confoc* or dermascop* or immun* or histo* or lentigo or l?esion* or LM or LMM) adj3 (delineation* or demarcation* or contour* or outline or outlines)).tw,kf.
- ((RCM* or vivascop* or confoc* or microscop* or dermascop*) adj4 (map* or clearance)).tw,kf.
- (((wide or wider or width* or narrow* or squar* or staged or stages or multistag* or phases or 2-phas* or two-phas* or multiphas* or multistep or multi-step or mapped) adj6 (excis* or reexci* or surg* or resurg* or section* or resect* or re-sect*)) or WLE*).tw,kf.
- ((excision or reexcision or resection or re-section or removal or cutting or delineat*) adj2 (techni* or method* or approach* or procedur*)).tw,kf.
- ((excis* or reexcis* or resect* or re-sect* or remov* or surg* or cutting or cut or delineat*) adj3 (geometric* or fusiform*)).tw,kf.
- ((squar* or staged) adj3 (procedur* or technique* or method* or approach or Johnson*)).tw,kf.
- (staged adj3 (squar* or serial or geometric*)).tw,kf.
- ((serial or en-face) adj2 (excis* or reexci* or surg* or resurg* or map*)).tw,kf.
- (Moh or Mohs*).tw,kf.
- (micro-surg* or microsurg* or micro-exc* or microexc* or micro-graph* or micrograph*).tw,kf.
- ((conservativ* or conventional or standard or traditional*) adj2 (excis* or reexcis* or resect* or re-sect* or surg* or cut or cutting or remov*) adj9 (lentig* or LM or LMM or (melanom* adj1 "in situ") or MIS)).tw,kf.
- or/9-26
- 8 and 27
- 28 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/)
- limit 29 to yr="2022 - 2025"
Resultaten = 132
Alle resultaten
|
Database |
Datum |
# hits |
|
EMBASE |
18-10-2024 |
218 |
|
OVID/MEDLINE |
18-10-2024 |
132 |
|
Totaal |
350 |
|
|
Duplicates |
112 |
|
|
Netto aantal |
238 |
|
- Niet-chirurgische interventies (cryotherapie, radiotherapie, imiquimod, watchfull waiting)
In de databases Embase.com en Ovid/Medline is op 24-10-2024 met relevante zoektermen systematisch gezocht naar systematische reviews, clinical trials, observationele studies en richtlijnen over de behandeling van lentigo maligna met crytoherapie, radiotherapie, imiquimod of watchfull waiting. De literatuurzoekactie leverde 492 unieke treffers op.
De zoekactie is met behulp van de PICO-systematiek opgebouwd. De zoekvragen hebben de P als gemeenschappelijke onderdeel. De overige onderdelen van de PICO werden geformuleerd op basis van de uitgangsvraag.
De volgende afbakening is gebruikt:
Voor de P: Patiënten met lentigo maligna (melanoom) in het hoofd-hals gebied
Voor de I: Cryotherapie, imiquimod, radiotherapie, watch full waiting
Voor de C: Excisie met 5mm marge
Voor de O: Kwaliteit van leven, overleving, lokaal recidief
Inclusie- en exclusiecriteria
|
Inclusiecriteria |
Exclusiecriteria |
|
Lentigo maligna (melanoom) in het hoofd-hals gebied |
Lentigo maligna op andere locatie op het lichaam |
|
Nederlandstalige en Engelstalige publicaties |
Chirurgische therapieën |
|
Toepassing van een referentiestandaard |
Andere typen melanoom (zoals superficieel spreidend melanoom) |
|
Systematische reviews, randomized controlled trials (RCT’s) of observationele studies; |
Case reports, letters to the editor, conference abstract, algemene reviews |
Uitgangsvragen
- Wat is de optimale behandeling voor patiënten met een lentigo maligna en de in situ component van lentigo maligna melanoom?
EMBASE (24-10-2024)
Zoektermen
- 'malignant lentigo'/exp OR 'melanoma in situ'/exp OR ('cutaneous melanoma'/exp AND 'precancer and cancer-in-situ'/exp) OR (((lentig* OR freckle*) NEAR/3 (melanom* OR malign* OR hutchinson*)):ti,ab,kw) OR 'hutchinson* melano*':ti,ab,kw OR dubreuilh*:ti,ab,kw OR (((melanom* OR melanos*) NEAR/6 ('in situ' OR precancer* OR 'pre-cancer*' OR 'pre-invasive')):ti,ab,kw)
- 'cryotherapy'/exp OR (((cold OR cryo*) NEAR/3 (therap* OR treatment* OR immuno*)):ti,ab,kw) OR cryoablation:ti,ab,kw OR cryoblation:ti,ab,kw OR cryoimmuno*:ti,ab,kw OR cryosurg*:ti,ab,kw OR 'cryo surg*':ti,ab,kw OR cryocoagulat*:ti,ab,kw OR (((induced OR gastric OR mild OR moderate) NEAR/3 hypotherm*):ti,ab,kw) OR 'hypothermic neuroprotect*':ti,ab,kw
- 'imiquimod'/exp OR 'aldara':ti,ab,kw OR 'beselna':ti,ab,kw OR 'imiquimod':ti,ab,kw OR 'limtop':ti,ab,kw OR 'mob 012':ti,ab,kw OR 'mob012':ti,ab,kw OR 'mtd 39':ti,ab,kw OR 'mtd39':ti,ab,kw OR 'tmx 101':ti,ab,kw OR 'tmx101':ti,ab,kw OR 'ugn 201':ti,ab,kw OR 'ugn201':ti,ab,kw OR 'vesimune':ti,ab,kw OR 'vyloma':ti,ab,kw OR 'zartra':ti,ab,kw OR 'zyclara':ti,ab,kw
- 'radiotherapy'/exp OR 'bioradiant therapy':ti,ab,kw OR 'bucky ray':ti,ab,kw OR 'bucky therapy':ti,ab,kw OR 'radio therapy':ti,ab,kw OR 'radio treatment':ti,ab,kw OR 'radiohypophysectomy':ti,ab,kw OR 'radiotherapy':ti,ab,kw OR 'roentgen therapy':ti,ab,kw OR 'roentgen treatment':ti,ab,kw OR 'rontgen therapy':ti,ab,kw OR 'therapeutic radiology':ti,ab,kw OR 'x radiotherapy':ti,ab,kw OR 'x ray therapy':ti,ab,kw OR 'x ray treatment':ti,ab,kw OR 'x-ray therapy':ti,ab,kw OR irradiati*:ti,ab,kw OR radiati*:ti,ab,kw
- 'watchful waiting'/exp OR 'active surveillance'/exp OR ((observative NEAR/2 (management* OR treatment*)):ti,ab,kw) OR expectative*:ti,ab,kw OR expectantly:ti,ab,kw OR 'watchful* waiting*':ti,ab,kw OR 'wait* and see*':ti,ab,kw OR 'wait* & see*':ti,ab,kw OR 'no treatment*':ti,ab,kw OR 'natural course*':ti,ab,kw OR 'no intervention*':ti,ab,kw OR 'active surveillance*':ti,ab,kw
- #2 OR #3 OR #4 OR #5
- #1 AND #6
- #7 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)
- 'meta-analysis'/exp OR 'meta-analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab
- 'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti
- 'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)
- 'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab)))
- #8 AND #9 SR
- #8 AND #10 NOT #13 Clinical trials
- #8 AND (#11 OR #12) NOT #13 NOT #14 OBS
- #13 OR #14 OR #15
Resultaten = 440
OVID/MEDLINE (24-10-2024)
Zoektermen
- Hutchinson's melanotic freckle/
- (melanoma/ or lentigo/) and carcinoma in situ/
- (lentig* adj3 (melanom* or malign* or Hutchinson*)).tw,kf.
- Hutchinson* melano*.tw,kf.
- ((Hutchinson* or melanotic or melanocyt*) adj3 freckl*).tw,kf.
- Dubreuilh.tw,kf.
- ((melanom* or melanos*) adj6 (in situ or precancer* or pre-cancer*)).tw,kf.
- or/1-7
- exp Cryotherapy/ or ((cold or cryo*) adj3 (therap* or treatment* or immuno*)).ti,ab,kf. or cryoablation.ti,ab,kf. or cryoblation.ti,ab,kf. or cryoimmuno*.ti,ab,kf. or cryosurg*.ti,ab,kf. or cryo surg*.ti,ab,kf. or cryocoagulat*.ti,ab,kf. or ((induced or gastric or mild or moderate) adj3 hypotherm*).ti,ab,kf. or hypothermic neuroprotect*.ti,ab,kf.
- Imiquimod/ or aldara.ti,ab,kf. or beselna.ti,ab,kf. or imiquimod.ti,ab,kf. or limtop.ti,ab,kf. or "mob 012".ti,ab,kf. or mob012.ti,ab,kf. or mtd 39.ti,ab,kf. or mtd39.ti,ab,kf. or tmx 101.ti,ab,kf. or tmx101.ti,ab,kf. or ugn 201.ti,ab,kf. or ugn201.ti,ab,kf. or vesimune.ti,ab,kf. or vyloma.ti,ab,kf. or zartra.ti,ab,kf. or zyclara.ti,ab,kf.
- exp Radiotherapy/ or (bioradiant therapy or bucky ray or bucky therap* or radio therap* or radio treatment or radiohypophysectomy or radiotherap* or roentgen therap* or roentgen treatment or rontgen therap* or therapeutic radiology or x radiotherapy or x ray therap* or x ray treatment or x-ray therapy or irradiati* or radiati*).ti,ab,kf.
- exp Watchful Waiting/ or ((conservative or observative) adj2 (management* or treatment*)).ti,ab,kf. or expectative*.ti,ab,kf. or expectantly.ti,ab,kf. or watchful* waiting*.ti,ab,kf. or "wait* and see*".ti,ab,kf. or wait* & see*.ti,ab,kf. or "no treatment*".ti,ab,kf. or natural course*.ti,ab,kf. or "no intervention*".ti,ab,kf. or active surveillance*.ti,ab,kf.
- 9 or 10 or 11 or 12
- 8 and 13
- 14 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/)
- meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.
- exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.
- Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies]
- Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.))
- 15 and 16 SR
- (15 and 17) not 20 Clinical trials
- (15 and (18 or 19)) not 20 not 21 OBS
- 20 or 21 or 22
Resultaten = 209
Alle resultaten
|
Database |
Datum |
# hits |
|
EMBASE |
24-10-2024 |
440 |
|
OVID/MEDLINE |
24-10-2024 |
209 |
|
Totaal |
649 |
|
|
Duplicates |
157 |
|
|
Netto aantal |
492 |
|