Anamnese en lichamelijk onderzoek bij LRS
Uitgangsvraag
Waaruit dienen anamnese en lichamelijk onderzoek bij de diagnostiek voor lumbosacraal radiculair syndroom (LRS) te bestaan?
Aanbeveling
Vraag bij de anamnese in ieder geval naar:
- klachtenduur;
- soort pijn;
- ernst pijn in been;
- dermatomale verdeling van de pijn;
- toename pijn bij drukverhogende momenten;
- spierzwakte;
- subjectief gevoelsverlies (dermatomale verdeling);
- symptomen passend bij caudalaesie
- comorbiditeit;
- risicofactoren ernstige pathologie (maligniteit voorgeschiedenis, recente ingreep aan de wervelkolom, malaise, onverklaard gewichtsverlies, koorts, eerdere tekenbeet en klachten systemische Borrelia burgdorferi infectie).
Het lichamelijk onderzoek dient in ieder geval te bestaan uit:
Onderzoek bovenste extremiteiten:
- reflexen.
Onderzoek van de onderste extremiteiten:
- tonus;
- kracht;
- tastzin;
- reflexen (kniepees, achilles, voetzool);
- Lasegue & gekruiste Lasegue;
- Looppatroon;
- hakken en tenen loop.
Heup onderzoek:
- flexie;
- endo- en exorotatie.
Onderzoek van de wervelkolom:
- stand van de wervelkolom en krommingen: recht, normale lordose, kyfose;
- vinger-top-vloer afstand > 25cm.
Vaatonderzoek:
- inspectie voeten;
- voelen van perifere pulsaties.
Bij vermoeden op caudalaesie:
- voelen anale sfincterspanning;
- sensibiliteit rijbroekgebied.
Overwegingen
Anamnese
Het typische beeld van een LRS is een heftige schietende, scherpe pijn, waarbij de distributie van pijn en of paresthesieën langs een specifiek dermatoom verlopen. De pijn is vaak erger in het been dan in de rug en kan toenemen bij drukverhogende momenten. Bij een lumbale kanaalstenose kan de pijn toenemen bij wandelen en vermindert/verdwijnt deze bij vooroverbuigen of zitten. Er dient altijd gevraagd te worden naar symptomen passend bij caudalaesie (rijbroekanesthesie, urine-incontinentie of retentie, verminderd passage gevoel, tekenen van verminderde anale sfincterfunctie)
Meer zeldzame oorzaken van wortelcompressie zijn onder andere een foraminale stenose, spondylolisthesis, wervelfractuur, wervelmetastase, epiduraal abces of hematoom. Ook een ontsteking van een zenuwwortel (radiculitis), door bijvoorbeeld Borrelia burgdorferi of Herpes zoster, kan tot een LRS leiden (Schaafstra, 2015).
Belangrijke risicofactoren voor ernstige onderliggende aandoeningen zijn:
- een maligniteit in de voorgeschiedenis;
- een recente ingreep aan de wervelkolom;
- bijkomende klachten (malaise, onverklaard gewichtsverlies, koorts) en
- een voorafgaande tekenbeet (erythema migrans, hersenzenuwuitval, artritis).
De aanwezigheid van een enkel kenmerk hoeft niet direct op ernstige pathologie te wijzen; een combinatie van verschillende kenmerken, zeker bij een onverklaarbaar langdurig of progressief beloop, vergroot de waarschijnlijkheid dat de pijnklachten door een andere aandoening dan een discushernia worden veroorzaakt.
De diagnose LRS berust grotendeels op de anamnese met als activerend gegeven uitstralende pijn volgens een dermatoom. De werkgroep neemt een standpunt ten aanzien van de te gebruiken dermatoom kaart. Recente reviews maken duidelijk dat de kaart van Keegan op veel punten onjuist is: deze moet niet meer gebruikt worden (Downs, 2011; Lee, 2008). Alhoewel niet volmaakt, geven de kaarten van Foerster, Heerinham en Head de beste informatie passend bij de moderne klinische waarnemingen. Deze kaarten zijn herzien en samengevoegd door Lee (Lee, 2008) (Figuur 1).
Figuur 1
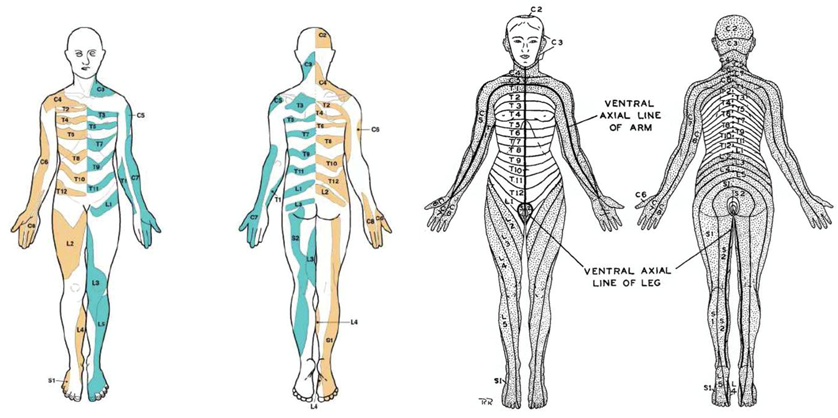
Links: De dermatoom kaart van Lee (2008) op basis van eerdere kaarten van Foerster, Head, Cambell, Inouye en Buchtaal, Nittaa.
Rechts: kaart van Keegan
De werkgroep is van mening dat er bij de anamnese in ieder geval de volgende onderwerpen nagegaan dienen te worden:
- klachtenduur;
- soort pijn;
- ernst pijn in been;
- dermatomale verdeling van de pijn;
- toename pijn bij drukverhogende momenten;
- spierzwakte;
- subjectief gevoelsverlies (dermatomale verdeling);
- symptomen passend bij caudalaesie;
- comorbiditeit;
- risicofactoren ernstige pathologie (maligniteit voorgeschiedenis, recente ingreep aan de wervelkolom, malaise, onverklaard gewichtsverlies, koorts, eerdere tekenbeet en klachten systemische Borrelia burgdorferi infectie).
Lichamelijk onderzoek
Het lichamelijk onderzoek kan gebruikt worden om enerzijds het vermoeden van een LRS te versterken en anderzijds andere (grove) pathologie uit te sluiten. Bij het lichamelijk onderzoek zijn vooral spierzwakte, de (gekruiste) proef van Lasègue en de vinger-vloerafstand (>25 cm) van belang. De (gekruiste) proef van Lasègue om een LRS aan te tonen. De aanwezigheid van een parese, verlaagde reflex en/of gestoorde sensibiliteit maken de aanwezigheid van discushernia met wortelcompressie meer waarschijnlijk, vooral als dit, in combinatie met de lokalisatie van de pijn, te herleiden is tot één zenuwwortel.
Bij de diagnostiek wordt ook aandacht besteedt aan symptomen die wijzen op een andere oorzaak van het LRS dan wortelcompressie door een discushernia en aan symptomen passend bij een caudalaesie.
Onderzoeken die kunnen helpen zijn (zie ook figuur 2)
Onderzoek bovenste extremiteiten:
- reflexen.
Onderzoek van de onderste extremiteiten:
- tonus;
- kracht;
- tastzin;
- reflexen (kniepees, achilles, voetzool);
- Lasegue & gekruiste Lasegue;
- Looppatroon;
- hakken en tenen loop.
Heup onderzoek:
- flexie;
- endo- en exorotatie.
Onderzoek van de wervelkolom:
- stand van de wervelkolom en krommingen: recht, normale lordose, kyfose;
- vinger-top-vloer afstand > 25cm.
Vaatonderzoek:
- inspectie voeten;
- voelen van perifere pulsaties.
Bij vermoeden op caudalaesie:
- voelen anale sfincterspanning;
- sensibiliteit rijbroekgebied.
Figuur 2 Lichamelijk onderzoek (Deyo, 2016)
Rode vlaggen: De differentiaaldiagnose voor LRS omvat neoplastische, infectieuze en ontstekings-problematiek. Belangrijke risicofactoren voor ernstige onderliggende aandoeningen zijn leeftijd hoger dan 50 jaar, geschiedenis van kanker, onverklaard gewichtsverlies en gebrek aan verbetering na 1 maand conservatieve therapie (Tarulli, 2007). De waarde van rode vlaggen is echter uiterst beperkt: 80% van de patiënten met acute lage rugpijn heeft tenminste 1 rode vlag maar slechts < 1% heeft een ernstige onderliggende ziekte (Hartvigsen, 2018 (Lancet serie)). De meeste rode vlaggen zijn niet informatief en maken de kans op een ernstige ziekte zichtbaar met beeldvorming nauwelijks groter. Integendeel, de lage specificiteit van rode vlaggen zorgen voor vele onnodige verwijzingen en beeldvorming (Hartvigsen, 2018; Downie, 2013; Henschke, 2009).
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Patiënten met een LRS ervaren heftige neuropathische pijn en zijn vaak ongerust. Het verrichten van een goede anamnese en een goed uitgevoerd lichamelijk onderzoek is van belang om de patiënt gerust te kunnen stellen. Tevens is het van belang dat ernstige pathologie wordt uitgesloten. Uitleg over de verschillende testen is dus van groot belang (zie ook de module 'Informeren van de patiënt').
Kosten (middelenbeslag)
Zowel anamnese en lichamelijk onderzoek brengen weinig meerkosten met zich mee en ook de tijdsinvestering is gering.
Aanvaardbaarheid voor de overige relevante stakeholders
Het stellen van het LRS blijft een klinische diagnose waarbij met name het uitsluiten van ernstige pathologie van belang is. Er zullen altijd patiënten zijn die zekerheid willen met betrekking tot de definitieve diagnose LRS als gevolg van wortelcompressie. Voor deze groep mensen is de klinische diagnose op basis van anamnese en lichamelijk onderzoek niet voldoende en zal een MRI-LWK gerechtvaardigd zijn.
Haalbaarheid en implementatie
Het afnemen of verrichten van een gestructureerde anamnese en een uniform lichamelijk onderzoek is haalbaar. Patiënten met een LRS worden vaak heen en weer verwezen tussen verschillende medisch specialisten (neurologie-pijnbestrijding-neurochirurgie-revalidatie en natuurlijk de huisarts). Er zou per regio gekozen kunnen worden om in een interdisciplinaire setting te gaan werken waarbij alle LRS patiënten verdeeld worden over de disciplines aan de poort waarbij men werkt volgens de vaste afspraken. Nu kan het zijn dat een patiënt bij alle disciplines op het spreekuur gezien wordt.
Rationale/ balans tussen de argumenten voor en tegen de interventie
Bij patiënten met een verdenking op een LRS is de anamnese het meest van belang. Hierbij dienen in ieder geval de lokalisatie van de pijn en de provocerende (onder andere drukverhogende) momenten van de pijn in het been aan bod te komen. Bij het lichamelijk onderzoek zijn vooral de vinger-vloerafstand, spierzwakte en (gekruiste) proef van Lasègue van belang. Bij de diagnostiek wordt ook aandacht besteedt aan symptomen die wijzen op een andere oorzaak van het LRS dan wortelcompressie door een discushernia en aan symptomen passend bij een caudalaesie.
Onderbouwing
Bij LRS dienen twee entiteiten te worden onderscheiden:
- De syndroomdiagnose LRS, met andere woorden een set van tests (uit anamnese en lichamelijk onderzoek) die samen een zenuwwortelaandoening suggereren. Aangezien hiervoor een gouden standaard ontbreekt zijn de anamnese en het lichamelijk onderzoek gebaseerd op de consensus tussen experts. Deze is weergegeven in de definitie.
- Het LRS door een discushernia: de meest voorkomende oorzaak van een LRS is een lumbosacrale discushernia. Het belang van het aantonen van een discushernia als oorzaak van het LRS is vooral het bewijs van het anatomisch pathologisch substraat, wanneer een operatieve ingreep wordt overwogen.
Klinische diagnose
Patiënten presenteren zich meestal niet met een volledig klinisch beeld van radiculaire pijn en uitval. In de kliniek wordt gebruikt gemaakt van de volgende indeling:
- Radiculaire pijn: dit is lumbosacrale uitstralende pijn verlopend via een of meerdere dermatomen. Op dit moment is er geen consensus over de juiste dermatoomkaart (zie paragraaf resultaten). Dit kan ook sensitisatie met uitbreiding van pijn in meerdere dermatomen betreffen.
- Radiculopathie: dit is een enkelvoudig klinisch teken: krachtsverlies, motore uitval, sensibiliteitsuitval of reflexuitval, of een combinatie van meerdere tekenen, passend bij de aangedane wortel.
- Het wortelsyndroom: de combinatie van radiculaire pijn en radiculopathie.
Radiculaire pijn zonder uitval sluit de diagnose niet uit, maar de aanwezigheid van passende tekenen maakt de diagnose veel zekerder.
De klinische diagnose LRS wordt gesteld op basis van de anamnese en het lichamelijk onderzoek en is matig betrouwbaar voor de diagnose wortelcompressie.
Diagnostische tests richten zich op het voorspellen van de aanwezigheid van een discushernia en/of wortelcompressie op beeldvormend onderzoek
Differentiaal diagnostisch moet er gedacht worden aan gerefereerde pijn vanuit de rug- en heupstructuren en vasculaire claudicatio. Meer zeldzame oorzaken van wortelcompressie zijn onder andere een foraminale stenose, spondylolisthesis, wervelfractuur, wervelmetastase, epiduraal abces of hematoom. Ook een ontsteking van een zenuwwortel (radiculitis), door bijvoorbeeld Borrelia burgdorferi of Herpes zoster, kan tot een LRS leiden (Schaafstra, 2015). Bovenstaande lijst is niet uitputtend.
Belangrijke risicofactoren voor ernstige onderliggende aandoeningen zijn een maligniteit in de voorgeschiedenis, een recente ingreep aan de wervelkolom, bijkomende klachten (malaise, onverklaard gewichtsverlies, koorts), en een voorafgaande tekenbeet (erythema migrans, hersenzenuwuitval, artritis). De aanwezigheid van een enkel kenmerk hoeft niet direct op ernstige pathologie te wijzen; een combinatie van verschillende kenmerken, zeker bij een onverklaarbaar langdurig of progressief beloop, vergroot de waarschijnlijkheid dat de pijnklachten door een andere aandoening dan een discushernia worden veroorzaakt.
|
- GRADE |
Geen enkel onderdeel van de anamnese of lichamelijk onderzoek heeft voldoende diagnostische waarde om een discushernia met wortelcompressie met voldoende zekerheid aan te tonen dan wel uit te sluiten.
Bronnen: (Tawa, 2017; Van der Windt, 2010; Vroomen, 1999) |
|
- GRADE |
Bij lichamelijk onderzoek heeft de straight leg raise test de hoogste sensitiviteit, waarbij de diagnostische waarde verbeterd kan worden wanneer dermatomale pijn, sensorische uitval, reflexuitval en spierzwakte betrokken worden. Een aanvullende gekruiste straight leg raise kan de specificiteit verder verhogen.
Bronnen: (Deyo, 2016; Genevay, 2017; Hancock, 2011; Majlesi, 2008; Petersen, 2017; Rubinstein, 2008; Scaia, 2012; Tawa, 2017; Visser, 2013; Van der Windt, 2010; Vroomen, 1999; Deville, 2000) |
|
- GRADE |
Voor het bepalen van het niveau van een discushernia is dermatomale locatie van pijn het meest informatief; een combinatie van motorische, sensorische en reflextesten verbetert de nauwkeurigheid.
Bronnen: (Hancock, 2011; Vroomen, 1999) |
|
- GRADE |
Onafhankelijke voorspellers in de anamnese voor een LRS zijn dermatomale pijn, en toename bij drukverhogende momenten.
Bronnen: (Aizawa, 2016; Genevay, 2017; Konno, 2007; Schultz, 2015) |
Beschrijving studies
In de literatuur is de referentie “discushernia met wortelcompressie” zelden gebruikt, er is daarom breder gekeken naar lage rugpijn, sciatica, discushernia, lumbale/lumbosacrale stenose, radiculopathie en zenuwwortelcompressie. Er is voor beantwoording van de uitgangsvraag gebruik gemaakt van zowel systematische reviews als observationeel onderzoek.
Petersen (2017) heeft op basis van 21 systematische reviews diagnostische regels opgesteld voor lage rugpijn.
Van der Windt (2010) maakte een zeer uitgebreid overzicht van de diagnostische waarde van lichamelijk onderzoek bij LRS in een Cochrane Diagnostic Test Accuracy Review.
Tawa (2017) beschreef op basis van 12 diagnostische studies de diagnostische waarde van sensorische onderzoeken, motorische onderzoeken, reflextesten en neuro-dynamische testen voor het vaststellen van lumbosacrale radiculopathie.
Vroomen (1999) beschreef in een systematische review de diagnostische waarde van geschiedenis en lichamelijk onderzoek bij vermoeden op sciatica door discushernia in 37 studies.
Deville (2000) analyseerde de diagnostische waarde van de Lasègue test voor vaststelling van discushernia op basis van 17 studies.
Scaia (2012) analyseerde uit 7 studies de waarde van de straight leg raise test (SLR) voor discushernia, lumbale radiculopathie en/of sciatica.
Rubinstein (2008) beschreef in een systematische review diagnostiek van zowel nek- als lage rugpijn.
In de review van Hooten (2015) werd diagnose en behandeling van lage rugpijn voor de eerstelijnszorg beschreven.
Tarulli (2007) beschreef in een narratieve review de diverse aspecten van epidemiologie, klinische presentatie en (differentiaal)diagnose van LRS.
Deyo (2016) beschreef in een narrative review klinische aspecten van diagnose en behandeling van discushernia behandeld.
Majlesi (2008) bestudeerde in een prospectieve case-controlstudie met 75 discushernia-patiënten de SLR en slump test.
Verwoerd (2016) voerde een posthoc analyse van een eerdere cross-sectionele studie uit waarin een groep van 395 patiënten was beschreven met de waarde van pijnverergering bij hoesten, niezen en drukverhogende momenten bij zenuwwortelcompressie.
Hancock (2011) onderzocht in een cross-sectionele studie bij 283 patiënten met sciatica uit een eerdere RCT de diagnostische waarde van lichamelijk onderzoek voor het bepalen van het niveau van een discushernia.
Genevay (2017) stelde op basis van een groep van 209 patiënten criteria op voor geschiedenis en lichamelijk onderzoek bij de bepaling van zenuwwortelcompressie, de “Radicular pain caused by disc herniation” (RAPIDH) criteria.
Visser (2013) onderzocht criteria om pijnklachten veroorzaakt door het SI-gewricht te onderscheiden van radiculopathie in een observationele studie bij 186 patiënten.
Suri (2010) onderzocht in een cross-sectionele studie bij 154 patiënten het effect van blindering voor MRI resultaten op resultaten van het lichamelijk onderzoek. Twee studies evalueerden vragenlijsten voor de diagnose van rugklachten.
Konno (2007) ontwikkelde en valideerde bij 250 patiënten een vragenlijst om de diagnose van lumbale spinale stenose te stellen/ondersteunen.
Aizawa (2016) nam bij 342 patiënten een vragenlijst af voor de diagnose van lumbale spinale stenose en lumbale discushernia.
Resultaten
Het onderzoek naar de diagnostische karakteristieken van symptomen en verschijnselen bij het LRS is bemoeilijkt door het ontbreken van een “gouden” referentiestandaard. Het uitvoeren van de (invasieve) referentietests bij controlegroepen ontbreekt veelal, waardoor selectiebias bestaat en de testkarakteristieken worden beïnvloed.
Anamnese
Konno (2007) ontwikkelde en valideerde bij 250 patiënten een vragenlijst om in het geval van lumbale spinale stenose onderscheid te maken tussen het radiculaire type stenose en het cauda equina type stenose. Op basis van tien vragen konden de aandoeningen worden onderscheiden met een AUC van 0,78, een sensitiviteit van 0,84 en een specificiteit van 0,78. Verder ontwikkelde Aizawa (2016) een vragenlijst om lumbale spinale stenose te onderscheiden van lumbale discushernia met 15 vragen. Voor lumbale stenose waren de sensitiviteit en specificiteit respectievelijk 0,93 en 0,85, voor discushernia 0,91 en 0,85, gevalideerd bij 342 patiënten.
Ten aanzien van de gele vlaggen (yellow flags - psychosociale factoren) kan gebruik worden gemaakt van de informatie van de huisarts en een korte gestandaardiseerde vragenlijst (bijvoorbeeld de HADS score: hospital anxiety an depression score). De patient kan deze voorafgaande aan het poli bezoek opgestuurd krijgen en deze thuis invullen.
Ten aanzien van de blauwe vlaggen (blue flags - werk) wordt aangeraden te vragen naar de beperkingen die worden ervaren bij het werk. Op dit punt is het noodzakelijk te vragen naar de cognities over rugpijn en werken. Er wordt aanbevolen om uitleg te geven over werk en pijn conform het advies van de bedrijfs- en verzekeringsartsen (NVAB, 2020): een actieve benadering vermindert het beste de pijn en beperkingen en men hoeft niet volledig pijnvrij te zijn om te blijven werken of het werk te hervatten. Aan het werk blijven is een goede interventie om van de klachten te herstellen.
Lichamelijk onderzoek
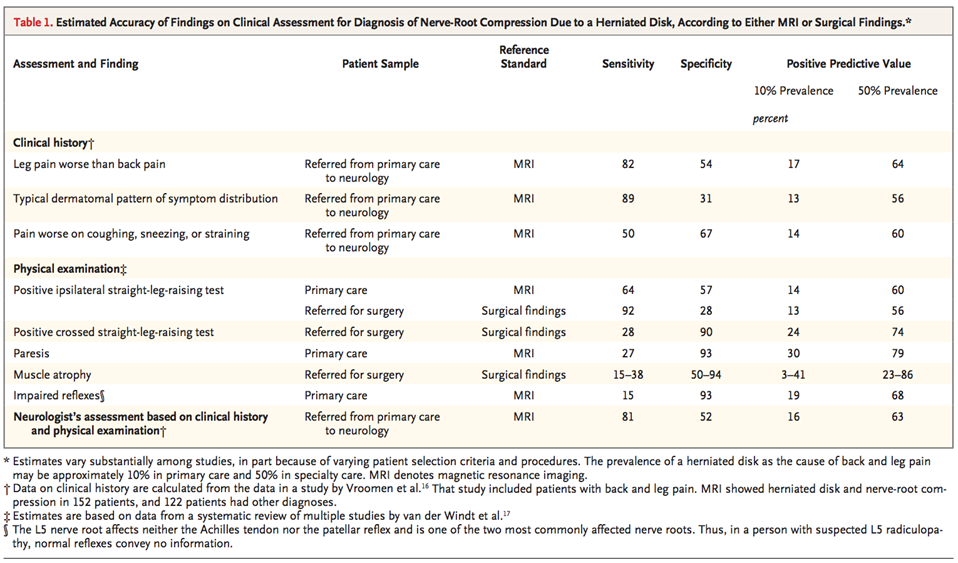
In de studies is lichamelijke onderzoek soms in categorieën en soms op individueel niveau beschreven. Tawa (2017) beschreef de diagnostische waarde van sensorische onderzoeken, motorische onderzoeken, reflextesten en neuro-dynamische testen voor het vaststellen van lumbosacrale radiculopathie. Onder sensorisch onderzoek vielen bepaling van paresthesie, vermindering of uitval van de sensibiliteit, motorisch onderzoek bepaalde parese, de geteste reflexen waren van de patella- en de achillespees, en onder neuro-dynamisch onderzoek vielen de SLR en slump test. De review beschreef sensitiviteit, specificiteit en positieve en negatieve likelihood ratios. De data van deze review zijn weergegeven in tabel 1, gecombineerd met de data uit de Cochrane review van Van der Windt (2010), waarin vormen van lichamelijk onderzoek (of een combinatie van meerdere) vergeleken werden met MRI/CT of chirurgische bevindingen in cohort- en case-controlstudies. Hierin werden geen likelihood ratios beschreven. Gepoolde waarden konden niet worden berekend door enerzijds een grote statistische heterogeniteit en anderzijds de verschillende manieren waarop de data gepresenteerd waren. Daarnaast bestond er veel variatie in de uitvoering van de SLR, die in de literatuur bovendien door elkaar is gebruikt met Lasègue test en Lasègue’s sign. Vergelijking van de indextesten met beeldvormende technieken en chirurgie als referentie zijn uitgesplitst, omdat door verificatiebias in chirurgische populaties de diagnostische waarden doorgaans overschat worden (Van der Windt, 2010). Het is belangrijk om op te merken dat in Nederland soms een definitie gehanteerd wordt waarbij een blokkade bij het heffen van het been dient op te treden om van een positieve Lasègue te spreken. Te verwachten valt dat door deze aangescherpte definitie de specificiteit toeneemt ten koste van de sensitiviteit. De waarde van deze variant is echter niet goed onderzocht.
Vergelijkbare waarden werden gevonden in een oudere systematische review van Vroomen (1999), die de diagnostische waarde evalueerde specifiek voor discushernia. Hier werd een vergelijkbare gepoolde sensitiviteit van 0,91 beschreven (95% betrouwbaarheidsinterval (BI) van 0,78 tot 0,97) en een specificiteit van 0,32 (95% BI van 0,17 tot 0,52) voor de SLR vergeleken met chirurgische bevindingen. Deville (2000) rapporteerde op basis van 15 studies een diagnostische odds ratio van 3,97 (95% BI 3,22 tot 4,90) van de SLR voor een discushernia. De systematische review van Scaia (2012) waarschuwde op basis van variabele sensitiviteit en specificiteit in 7 studies dat een positieve SLR alleen zinvol is als diagnostisch instrument in de context van andere bevindingen. In de narratieve review van Deyo (2016) werd geconcludeerd dat in het geval van een lumbale discushernia de SLR positief was wanneer het been 30 tot 70 graden werd geheven. Een positieve ipsilaterale SLR was sensitief maar niet specifiek. Een positieve gekruiste SLR daarentegen was specifiek maar niet sensitief voor een lumbale discushernia. Wanneer de gekruiste SLR werd vergeleken met imaging of chirurgische bevindingen, werd in 5 studies een sensitiviteit gevonden van 0,23 tot 0,43 bij een specificiteit van 0,83 tot 1,00 (Van der Windt, 2010). In een niet-chirurgische populatie met discushernia vond Vroomen (1999) voor de gekruiste SLR een gepoolde sensitiviteit van 0,32 (95% BI 0,16 tot 0,54) en een specificiteit van 0,98 (95% BI 0,94 tot 0,99). Walter (2000) vond vergelijkbare waarden in 8 studies, een sensitiviteit van 0,29 en een specificiteit van 0,88, en berekende een diagnostische odds ratio voor de gekruiste SLR van 4,39 (95% BI 0,71 tot 25,9). De slump test, die kan worden beschouwd als een SLR in zittende positie, werd in een prospectieve case-controlstudie onderzocht bij 75 patiënten met verdenking op discushernia (Majlesi, 2008). Vergeleken met MRI had de slump test met 0,84 (95% BI 0,74 tot 0,90) een hogere sensitiviteit dan de SLR (0,52 met 95% BI van 0,42 en 0,58); en een ietwat lagere specificiteit (slump 0,83 met 95% BI van 0,73 tot 0,90, SLR 0,89 met 95% BI van 0,79 tot 0,95). Er werd ook naar de diagnostische waarde van de slump test gekeken in subgroepen. Bij een discushernia op L5-S1 waren sensitiviteit (0,90) en specificiteit (0,91) hoger, op het niveau van een L4-L5 lager (sensitiviteit 0,78, specificiteit 0,88). Bij patiënten met zenuwwortelcompressie was de sensitiviteit 0,84 met een specificiteit van 0,90 (Majlesi, 2008).
Tabel 1 Diagnostische waarden van lichamelijk onderzoek voor LRS
|
Lichamelijk onderzoek |
referentie |
studies |
Sensitiviteit |
specificiteit |
+LR |
-LR |
|
Sensibel onderzoek |
MRI/CT |
4 |
0,13-0,33 |
0,74-0,93 |
1,5-2,8 |
0,9-1,3 |
|
|
chirurgie |
6 * |
0,28-0,67 * |
0,42-0,69 * |
1,6 |
1,6 |
|
Motorisch onderzoek |
MRI/CT |
5 |
0,19-0,49 |
0,68-0,93 |
0,9-3,9 |
1,0-1,7 |
|
|
chirurgie |
1 |
0,34 |
0,47 |
0,6 |
0,7 |
|
Patellapees-reflex |
MRI/CT |
2 |
0,32-0,67 |
0,83-0,90 |
3,2-4,0 |
1,3-2,5 |
|
|
EMG |
1 |
0,18 |
0,66 |
0,5 |
0,8 |
|
Achillespees-reflex |
MRI/CT |
3 |
0,14-0,67 |
0,60-0,93 |
1,7-3,7 |
1,1-1,8 |
|
|
chirurgie |
6 * |
0,31-0,61 * |
0,60-0,89 * |
1,8 |
1,6 |
|
SLR/Lasègue |
MRI/CT |
9 * |
0,29-0,81* |
0,37-1,00* |
0,7-4,7 |
0,8-1,9 |
|
|
chirurgie |
10 * |
0,79-0,98 * |
0,11-0,82* |
1,1 |
1,3 |
|
Gekruiste SLR |
MRI/ chirurgie |
5 # |
0,23-0,43 # |
0,83-1,00 # |
|
|
|
Slump test |
MRI/CT |
2 |
0,84-1,00 |
0,83 |
5,0-5,9 |
0,8-5,2 |
|
Waarden zijn laagste en hoogste waarde van gerapporteerde studies uit de review van Tawa (2017) tenzij anders aangegeven. Wanneer diagnostische waarden waren uitgedrukt per ruggenmergwervel in de studies, zijn de gemiddelde waarden per studie berekend. +LR postieve likelihood ratio, -LR negatieve likelihood ratio. * gecombineerde data van Van der Windt (2010) en Tawa (2017). # Van der Windt (2010) |
||||||
Bij gebruik van slechts één test hadden scoliose, parese, spieratrofie, verlaagde reflexen, en sensibele uitval een beperkte diagnostische waarde volgens Van der Windt (2010). Ook Vroomen (1999) vond sensibele uitval en verminderde reflexen specifiek noch sensitief. De review van Rubinstein (2008) daarentegen beschreef afnames in spierkracht en sensibiliteit als goed correlerend, veranderingen in reflexen enigszins correlerend en onderzoek van de onderrug nauwelijks correlerend met lumbale radiculopathie. Forward flexion test, hyper-extension test, en slump test hadden een betere diagnostische waarde, maar werden in maximaal drie studies beschreven met een beperkt aantal patiënten (Van der Windt, 2010). Parese was niet specifiek of sensitief in een chirurgische populatie, maar wanneer aanwezig nam de kans op zenuwwortelbetrokkenheid met 90% toe (Vroomen, 1999). Het combineren van onderdelen van lichamelijk onderzoek verhoogde de specificiteit (Van der Windt, 2010). Hierop aansluitend raadde Peterson (2017), die op basis van 21 systematische reviews diagnostische regels heeft opgesteld, aan om de SLR uit te voeren in combinatie met de Hancock rule, bestaande uit ten minste drie positieve uitslagen bij vier onderdelen van het lichamelijk onderzoek (dermatomale pijnlocatie corresponderend met een zenuwwortel, corresponderende sensibele uitval, verlaagde reflex en parese). Aanvullend werd de gekruiste SLR aangeraden, op basis van positieve likelihood ratios in het merendeel van de studies (Peterson, 2017). Pijnklachten veroorzaakt door het SI-gewricht kunnen aangezien worden voor radiculopathie. Spierzwakte, corkscrew phenomenon (kurketrekker fenomeen: niet vloeiend overeind komen na lumbale anteflexie), vinger-vloerafstand > 25 cm, lumbale scoliose, positieve Bragard of Kemp score en positieve SLR test zijn een indicatie voor betrokkenheid van de zenuwwortel, maar aanvullende MRI is nodig om de diagnose te bevestigen (Visser, 2013). Overigens bleek uit de studie van Suri (2010) dat kennis van de MRI-uitslag door de arts de interpretatie van sensorische tests mogelijk kan beïnvloeden.
Verschillende studies hebben de diagnostische waarde bepaald van lichamelijk onderzoek bij het bepalen van het niveau van een discushernia. Verlaagde reflexen hadden een sensitiviteit van 0,82 voor een discushernia van L1-L2, L2-L3, L3-L4. Voor de kniepeesreflex was deze sensitiviteit 0,40. De SLR test was positief in 38% en de omgekeerde SLR in 9% van de hoge discushernia’s. Typische L5 en S1 pijnverdeling hebben een hoge specificiteit van respectievelijk 0,90 voor L4-L5 en 0,88 voor L5-S1 discushernia. Een afgenomen achillespeesreflex was 1,5 tot 2,6 maal zo waarschijnlijk bij een L5-S1 als bij een L4-L5 hernia. Parese van de extensor hallucis longus kwam voor bij 69% van de discushernia’s op L4-L5 niveau (Vroomen, 1999). In de cross-sectionele studie van Hancock (2011) bij 283 patiënten met sciatica (uit een eerdere RCT) werd geconcludeerd dat bij lichamelijk onderzoek een enkele test niet voldoende diagnostische nauwkeurigheid bood (area under the curve (AUC) < 0,75) om de locatie van discushernia in de lagere lumbale wervels te bepalen. Dermatomale locatie van pijn was de meest informatieve test, maar een combinatie van (motorische, sensorische en reflex-) testen verbeterde de nauwkeurigheid.
Combinaties van anamnese en lichamelijk onderzoek
Multivariate modellen zijn gebruikt om te bepalen welke combinaties van diagnostische tests de beste voorspellende waarde hebben voor aanwezigheid van lumbale discushernia (Van der Windt, 2010). Een studie vond de sterkste associatie met zenuwwortelcompressie op MRI wanneer leeftijd, klachtenduur tussen 15 en 30 dagen, paroxysmale pijn, meer pijn in been dan rug, dermatomale verdeling van pijn, verergering van pijn bij hoesten/niezen/drukverhogende momenten, vinger-vloerafstand en parese werden gecombineerd. De maximale diagnostische waarde van het model was bij een voorspelde probabiliteit van 62,5%, met een sensitiviteit van 0,72 en een specificiteit van 0,80. Een ander model combineerde de volgende factoren: hoog opleidingsniveau, afwezigheid van comorbiditeit, geen eerdere chirurgie, ernstige pijn, beperkte range of motion, positieve gekruiste SLR en dislocated dura or root on myelography. Hierbij werd alleen de verklaarde variantie van 0,495 gerapporteerd. Bij beide modellen werd geen indicatie gegeven van het aantal positieve tests nodig om patiënten te identificeren met een grote kans op radiculopathie door lumbale discushernia (Van der Windt, 2010). Genevay (2017) ontwikkelde de “Radicular pain caused by disc herniation” (RAPIDH) criteria. Uit een door experts opgestelde lijst van 74 potentiële voorspellende factoren werden de items geselecteerd die het best radiculaire pijn veroorzaakt door discushernia konden identificeren, in een cohort van 209 patiënten met discushernia, neurogene claudicatie of aspecifieke lage rugklachten (laatste twee als controlegroep; duur van de klachten werd niet vermeld). Met de vijf criteria monoradiculaire beenpijnverdeling, een positieve SLR bij minder dan 60˚ (of femorale stretch test), afname in unilaterale enkelreflex, unilaterale spierzwakte en door de patiënt gerapporteerde unilaterale beenpijn werd een sensitiviteit gehaald van 0,71, een specificiteit van 0,90 en een AUC van 0,91 (Genevay, 2017).
Bewijskracht van de literatuur
Gezien de aard van de vraag is er geen GRADE-beoordeling toegepast op de literatuur. De meeste studies die gebruikt konden worden voor de analyse waren cross-sectionele studies en ook de meeste systematische reviews waren (grotendeels) gebaseerd op observationele studies. Ook in de Cochrane review van Van der Windt (2010) werd al vastgesteld dat er zowel in de uitvoering en interpretatie van de diagnostische tests als in de methodologische uitvoering van de studies te veel variatie voorkwam om resultaten te kunnen poolen.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Wat is de waarde van de gegevens uit de anamnese en het lichamelijk onderzoek bij het vaststellen van wortelcompressie?
PICO
P: patiënten met (lage rugpijn en) uitstraling naar 1 of beide benen ten gevolge van een HNP of van een (lumbosacrale/lumbale) stenose;
I: Gegevens uit anamnese, lichamelijk onderzoek;
C: MRI of Operatie;
O: Bewezen wortelcompressie.
Relevante uitkomstmaten
De werkgroep achtte bewezen dat wortelcompressie een voor de besluitvorming cruciale uitkomstmaat is; andere uitkomstmaten werden niet gedefinieerd. De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
Zoeken en selecteren (Methode)
In de databases Medline (via OVID) & Embase (via Embase.com) is op 12 april 2019 met relevante zoektermen gezocht naar studies die de anamnese en het lichamelijk onderzoek beschreven bij patiënten met patiënten met (lage rugpijn en) uitstraling naar 1 of beide benen. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 455 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria:
- gepubliceerd tussen 1999 en april 2019;
- systematische reviews of RCT’s;
- volwassen patiënten met acute of subacute LRS.
Op basis van titel en abstract werden in eerste instantie 32 studies voorgeselecteerd. Na raadpleging van de volledige tekst, werden vervolgens 14 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording), en 18 studies definitief geselecteerd.
Resultaten
Negentien artikelen zijn opgenomen in de literatuuranalyse. Door de exploratieve aard van de uitgangsvraag en de bestudeerde artikelen zijn er geen evidencetabel en risk-of-bias tabel gemaakt. Waar mogelijk is informatie samengevat in tabellen in de tekst.
- Aizawa T, Tanaka Y, Yokoyama T, Shimada Y, Yamazaki K, Takei H, Konno S, Kawahara C, Itoi E, Kokubun S. New diagnostic support tool for patients with leg symptoms caused by lumbar spinal stenosis and lumbar intervertebral disc herniation: A self-administered, self-reported history questionnaire. J Orthop Sci. 2016 Sep;21(5):579-85. doi: 10.1016/j.jos.2016.07.012. Epub 2016 Aug 12. PubMed PMID: 27527658.
- Devillé WL, van der Windt DA, Dzaferagić A, Bezemer PD, Bouter LM. The test of Lasègue: systematic review of the accuracy in diagnosing herniated discs. Spine (Phila Pa 1976). 2000 May 1;25(9):1140-7. Review. PubMed PMID: 10788860.
- Deyo RA, Mirza SK. CLINICAL PRACTICE. Herniated Lumbar Intervertebral Disk. N Engl J Med. 2016 May 5;374(18):1763-72. doi: 10.1056/NEJMcp1512658. Review. PubMed PMID: 27144851.
- Downie A, Williams CM, Henschke N, Hancock MJ, Ostelo RW, de Vet HC, Macaskill P, Irwig L, van Tulder MW, Koes BW, Maher CG. Red flags to screen for malignancy and fracture in patients with low back pain: systematic review. BMJ. 2013 Dec 11;347:f7095. doi: 10.1136/bmj.f7095. Review. Erratum in: BMJ. 2014;348:g7. PubMed PMID: 24335669; PubMed Central PMCID: PMC3898572.
- Downs MB, Laporte C. Conflicting dermatome maps: educational and clinical implications. J Orthop Sports Phys Ther. 2011 Jun;41(6):427-34. doi: 10.2519/jospt.2011.3506. Epub 2011 May 31. PubMed PMID: 21628826.
- Genevay S, Courvoisier DS, Konstantinou K, Kovacs FM, Marty M, Rainville J, Norberg M, Kaux JF, Cha TD, Katz JN, Atlas SJ. Clinical classification criteria for radicular pain caused by lumbar disc herniation: the radicular pain caused by disc herniation (RAPIDH) criteria. Spine J. 2017 Oct;17(10):1464-1471. doi: 10.1016/j.spinee.2017.05.005. Epub 2017 May 5. PubMed PMID: 28483706.
- Hancock MJ, Koes B, Ostelo R, Peul W. Diagnostic accuracy of the clinical examination in identifying the level of herniation in patients with sciatica. Spine (Phila Pa 1976). 2011 May 15;36(11):E712-9. doi: 10.1097/BRS.0b013e3181ee7f78. PubMed PMID: 21224761.
- Hartvigsen J, Hancock MJ, Kongsted A, Louw Q, Ferreira ML, Genevay S, Hoy D, Karppinen J, Pransky G, Sieper J, Smeets RJ, Underwood M; Lancet Low Back Pain Series Working Group. What low back pain is and why we need to pay attention. Lancet. 2018 Jun 9;391(10137):2356-2367. doi: 10.1016/S0140-6736(18)30480-X. Epub 2018 Mar 21. Review. PubMed PMID: 29573870.
- Henschke N, Maher CG, Refshauge KM, Herbert RD, Cumming RG, Bleasel J, York J, Das A, McAuley JH. Prevalence of and screening for serious spinal pathology in patients presenting to primary care settings with acute low back pain. Arthritis Rheum. 2009 Oct;60(10):3072-80. doi: 10.1002/art.24853. PubMed PMID: 19790051.
- Hooten WM, Cohen SP. Evaluation and Treatment of Low Back Pain: A Clinically Focused Review for Primary Care Specialists. Mayo Clin Proc. 2015 Dec;90(12):1699-718. doi: 10.1016/j.mayocp.2015.10.009. Review. PubMed PMID: 26653300.
- Konno S, Kikuchi S, Tanaka Y, Yamazaki K, Shimada Y, Takei H, Yokoyama T, Okada M, Kokubun S. A diagnostic support tool for lumbar spinal stenosis: a self-administered, self-reported history questionnaire. BMC Musculoskelet Disord. 2007 Oct 30;8:102. PubMed PMID: 17967201; PubMed Central PMCID: PMC2176057.
- Majlesi J, Togay H, Unalan H, Toprak S. The sensitivity and specificity of the Slump and the Straight Leg Raising tests in patients with lumbar disc herniation. J Clin Rheumatol. 2008 Apr;14(2):87-91. doi: 10.1097/RHU.0b013e31816b2f99. PubMed PMID: 18391677.
- NVAB. Richtlijn Lage Rugpijn en Lumbosacraal Radiculair Syndroom. 2020
- Lee MW, McPhee RW, Stringer MD. An evidence based approach to human dermatomes. Clin Anat. 2008;21:363-373. http://dx.doi. org/10.1002/ca.20636 23. Lundy-Ekman L. Neuroscience.
- Petersen T, Laslett M, Juhl C. Clinical classification in low back pain: best-evidence diagnostic rules based on systematic reviews. BMC Musculoskelet Disord. 2017 May 12;18(1):188. doi: 10.1186/s12891-017-1549-6. Review. PubMed PMID: 28499364; PubMed Central PMCID: PMC5429540.
- Rubinstein SM, van Tulder M. A best-evidence review of diagnostic procedures for neck and low-back pain. Best Pract Res Clin Rheumatol. 2008 Jun;22(3):471-82. doi: 10.1016/j.berh.2007.12.003. Review. PubMed PMID: 18519100.
- Scaia V, Baxter D, Cook C. The pain provocation-based straight leg raise test for diagnosis of lumbar disc herniation, lumbar radiculopathy, and/or sciatica: a systematic review of clinical utility. J Back Musculoskelet Rehabil. 2012;25(4):215-23. doi: 10.3233/BMR-2012-0339. Review. PubMed PMID: 23220802.
- Schaafstra, A., Spinnewijn, W., Bons, S., Borg, M., Koes, B., Ostelo, R., Spijker‐Huiges, A., Burgers, J., Bouma, M., & Verburg, A. (2015). NHG‐Standaard Lumbosacraal radiculair syndroom. (Tweede herziening). Huisarts Wet, 58(6), 308‐20.
- Shultz S, Averell K, Eickelman A, Sanker H, Donaldson MB. Diagnostic accuracy of self-report and subjective history in the diagnosis of low back pain with non-specific lower extremity symptoms: A systematic review. Man Ther. 2015 Feb;20(1):18-27. doi: 10.1016/j.math.2014.08.002. Epub 2014 Aug 29. Review. PubMed PMID: 25231775.
- Suri P, Hunter DJ, Katz JN, Li L, Rainville J. Bias in the physical examination of patients with lumbar radiculopathy. BMC Musculoskelet Disord. 2010 Nov 30;11:275. doi: 10.1186/1471-2474-11-275. PubMed PMID: 21118558; PubMed Central PMCID: PMC3009628.
- Tarulli AW, Raynor EM. Lumbosacral radiculopathy. Neurol Clin. 2007 May;25(2):387-405. Review. PubMed PMID: 17445735.
- Tawa N, Rhoda A, Diener I. Accuracy of clinical neurological examination in diagnosing lumbo-sacral radiculopathy: a systematic literature review. BMC Musculoskelet Disord. 2017 Feb 23;18(1):93. doi: 10.1186/s12891-016-1383-2. Review. PubMed PMID: 28231784; PubMed Central PMCID: PMC5324296.
- Verwoerd AJH, Mens J, El Barzouhi A, Peul WC, Koes BW, Verhagen AP. A diagnostic study in patients with sciatica establishing the importance of localization of worsening of pain during coughing, sneezing and straining to assess nerve root compression on MRI. Eur Spine J. 2016 May;25(5):1389-1392. doi: 10.1007/s00586-016-4393-8. Epub 2016 Feb 2. PubMed PMID: 26842881.
- Visser LH, Nijssen PG, Tijssen CC, van Middendorp JJ, Schieving J. Sciatica-like symptoms and the sacroiliac joint: clinical features and differential diagnosis. Eur Spine J. 2013 Jul;22(7):1657-64. doi: 10.1007/s00586-013-2660-5. Epub 2013 Mar 2. PubMed PMID: 23455949; PubMed Central PMCID: PMC3698344.
- Vroomen PC, de Krom MC, Knottnerus JA. Diagnostic value of history and physical examination in patients suspected of sciatica due to disc herniation: a systematic review. J Neurol. 1999 Oct;246(10):899-906. PubMed PMID: 10552236.
- van der Windt DA, Simons E, Riphagen II, Ammendolia C, Verhagen AP, Laslett M, Devillé W, Deyo RA, Bouter LM, de Vet HC, Aertgeerts B. Physical examination for lumbar radiculopathy due to disc herniation in patients with low-back pain. Cochrane Database Syst Rev. 2010 Feb 17;(2):CD007431. doi: 10.1002/14651858.CD007431.pub2. Review. PubMed PMID: 20166095.
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Al Nezari, 2013 |
Chronische LRS |
|
Fairbank 2011 |
Cauda equina syndroom |
|
Graves, 2012 |
Predictieve waarde van MRI |
|
Kohns, 2018 |
Klinische voorspellers van MRI en opiatengebruik |
|
Konstantinou, 2012a |
Protocol, geen resultaten |
|
Konstantinou, 2012b |
Self reported items vergeleken met lichamelijk onderzoek, geen juiste controlegroep |
|
Kovacs, 2012 |
Prognostische waarde van “catastrophizing” |
|
Lao, 2014 |
Waarde van kinetische MRI |
|
Nunn, 2017 |
Beschrijving van patiëntkarakteristieken |
|
Press, 2013 |
Evaluatie van physician performance |
|
Rade, 2017 |
Mechanisme, geen antwoord op PICO |
|
Schultz, 2015 |
Niet de juiste patiëntenpopulatie |
|
Stynes, 2016 |
Classificatie van LBP, geen diagnose |
|
Yu, 2012 |
Chronische pijn |
Beoordelingsdatum en geldigheid
Publicatiedatum : 03-08-2020
Beoordeeld op geldigheid : 21-09-2020
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2025 bepaalt het bestuur van de Nederlandse Vereniging voor Neurologie (NVN) of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NVN is regiehouder van deze richtlijnmodules en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module1 |
Regiehouder(s)2 |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn3 |
Frequentie van beoordeling op actualiteit4 |
Wie houdt er toezicht op actualiteit5 |
Relevante factoren voor wijzigingen in aanbeveling6 |
|
Anamnese en Lichamelijk onderzoek |
NVN |
2020 |
2025 |
1x per 5 jaar |
NVN |
- |
|
1 Naam van de module 2 Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders) 3 Maximaal na vijf jaar 4 (half)Jaarlijks, eens in twee jaar, eens in vijf jaar 5 regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft 6 Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen |
||||||
Algemene gegevens
Deze richtlijn is ontwikkeld in samenwerking met:
-
Nederlands Huisartsen Genootschap
- Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde
-
Koninklijk Nederlands Genootschap voor Fysiotherapie
- Samenwerkingsverband Pijnpatiënten naar één stem
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
Doel en doelgroep
Doel
Het doel van de richtlijn is tweeledig. Enerzijds is de richtlijn een voortzetting van de richtlijn LRS uit 2008 met herziening op basis van de nieuwe literatuur. Anderzijds dient de richtlijn als handleiding voor de praktijk met betrekking tot de patiënt met rugpijn met uitstraling in een been. Er is namelijk, voorafgaande aan beeldvorming, geen klinische test of vragenlijst waarmee de klinische diagnose LRS met volledige zekerheid kan worden gesteld (zie module diagnostiek). Het kunstmatige onderscheid tussen radiculaire en niet-radiculaire pijn komt hiermee te vervallen.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met LRS. De richtlijn is bedoeld voor neurologen, anesthesiologen, radiologen, neurochirurgen, orthopeden, huisartsen, fysiotherapeuten, bedrijfs- en verzekeringsartsen revalidatieartsen, en eventuele andere behandelaars van patiënten zoals Caesar- en Mensendieck therapeuten en ergotherapeuten.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met een verdenking lumbosacraal radiculair syndroom (LRS) te maken hebben.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname. De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Dr. R.H. Boerman, neuroloog, werkzaam in Rijnstate, Arnhem, NVN (voorzitter)
- Dr. W.J.P. Henneman, radioloog, werkzaam in het Maastricht UMC+, Maastricht, NVvR (vanaf oktober 2019)
- Drs. B.A. Brouwer, neuroloog, werkzaam in het Maastricht UMC+, Maastricht, NVN
- Drs. J. de Haan, orthopedisch chirurg, werkzaam in het Amphia Ziekenhuis, Breda, NOV
- Dr. J.L. Hoving, senior onderzoeker, werkzaam in het Amsterdam UMC, locatie AMC, Amsterdam, NVAB
- Dr. E.M. Kingma, AIOS neurologie, werkzaam in het Universitair Medisch Centrum Groningen, Groningen, NVN
- Dr. B.C. ter Meulen, neuroloog, werkzaam in het Zaans Medisch Centrum, Zaandam, NVN
- Dr. E. de Schepper, huisarts, werkzaam in het Erasmus MC, Rotterdam. NHG
- Prof. dr. R.J.E.M. Smeets, hoogleraar Revalidatiegeneeskunde & revalidatiearts, werkzaam in bij de Universiteit Maastricht & CIR Revalidatie, VRA
- Dr. J. B. Staal, fysiotherapeut n.p. & senior onderzoeker/epidemioloog, werkzaam in het Radboudumc en de Hogeschool van Arnhem en Nijmegen, Nijmegen, KNGF
- Drs. M.A.M.B. Terheggen, anesthesioloog, werkzaam in Rijnstate, Arnhem, NVA
- Drs. I.L. Thomassen, patiëntvertegenwoordiger & voorzitter van Samenwerkingsverband Pijnpatiënten naar één stem.
- Dr. C.L.A.M. Vleggeert – Lankamp, Neurochirurg, Leids Universitair Medisch Centrum, Leiden, NVvN
Met ondersteuning van
- Dr. J. Buddeke, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. A.A. Lamberts, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Drs. L.H.M. Niesink-Boerboom, literatuurspecialist, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u hieronder. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Achternaam werkgroeplid |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Getekend op |
Ondernomen actie? |
|
Boerman |
neuroloog staflid Rijnstate ziekenhuis |
lid tuchtcolleges Groningen, Eindhoven, Amsterdam en Zwolle |
geen |
geen |
geen |
geen |
geen |
20-6-2018 |
Geen actie |
|
Brouwer |
Neuroloog afdeling anesthesiologie MUMC+ |
Lid algemeen bestuur P.A.I.N. (onbetaald) |
geen |
geen |
geen |
geen |
Afdeling waar WG-lid werkzaam is heeft van Medtronic een Grant ontvangen. |
12-6-2018 |
Geen actie |
|
Buddeke |
Adviseur, Kennisinstituut van de Federatie Medisch Specialisten |
geen |
geen |
geen |
geen |
geen |
geen |
2018 |
Geen actie |
|
de Haan |
Orthopaedisch chirurg, Amphia breda |
geen |
geen |
geen |
geen |
geen |
geen |
5-6-2018 |
Geen actie |
|
de Schepper |
Onderzoeker (UD), huisarts (np), afdeling Huisartsgeneeskunde, Erasmus MC Rotterdam |
geen |
geen |
geen |
geen |
Promotieonderzoek Beeldvormende diagnostiek |
geen |
1-5-2018 |
Geen actie |
|
Henneman |
Radiolooog MUMC+, Maastricht |
geen |
geen |
geen |
geen |
geen |
geen |
16-12-2019 |
Geen actie |
|
Hoving |
Wetenschappelijk onderzoeker, Coronel Instituut voor Arbeid en Gezondheid, Academisch Medisch Centrum in Amsterdam |
geen |
geen |
geen |
geen |
Betrokken bij richtlijn Arbeid en rugklachten LRS van de NVAB. |
geen |
2-7-2018 |
Geen actie |
|
Kingma |
Arts-assistent in opleiding tot neuroloog, Universitair Medisch Centrum Groningen |
geen |
geen |
geen |
geen |
geen |
geen |
11-6-2018 |
Geen actie |
|
Lamberts |
Senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten |
Beleidsmedewerker Kwaliteit Nederlandse Vereniging voor Klinische Geriatrie |
geen |
geen |
geen |
geen |
geen |
2014 |
Geen actie |
|
Smeets |
Hoogleraar Revalidatiegeneeskunde, Universiteit Maastricht (0.4 fte) |
Eigen bedrijf genaamd RevaXpert; inhuur van mijn expertise voor scholing derden op het gebied van chronische pijn in houding en bewegingsapparaat in de vorm van presentaties, gemiddeld twee keer per jaar. (Betaald) |
geen |
geen |
Niet betrokken bij wetenschappelijk onderzoek dat betrekking heeft op de inhoud van deze richtlijn. |
Geen risico op aantasting van intellectuele belangen of reputatie |
geen |
8-6-2018 |
Geen actie |
|
Staal |
Lector musculoskeletale revalidatie hogeschool, van Arnhem en Nijmegen (0,8 fte), |
-Section editor BMC Musculosceletal disorders (betaald) |
geen |
geen |
geen |
geen |
geen |
14-5-2018 |
Geen actie |
|
ter Meulen |
Neuroloog zaans MC |
Lid Raad van Advies NVvR de Wervelkolom (onbetaald) |
geen |
geen |
geen |
Promotieonderzoek naar Wortelblokkades, Amsterdam UMC, locatie Vumc |
geen |
27-6-2018 |
Geen actie |
|
Terheggen |
Anesthesioloog/pijnspecialist Rijnstate Arnhem/Velp/Zevenaar (1,0 fte) |
Specialist-manager Pijncentrum en Acute PijnService Rijnstate (betaald) |
geen |
Echtgenote is werkzaam bij Pfizer inc. .Geen mogelijke belangen-verstrengeling aangezien Pfizer geen gepatenteerde producten (meer) levert geïndiceerd bij LRS |
geen |
geen |
geen |
3-7-2018 |
Geen actie |
|
Thomassen |
Voorzitter Samenwerkingsverband Pijnpatiënten naar één stem (vacatiegelden) Voorzitter Patiëntenvereniging CRPS (vrijwilliger) |
geen |
geen |
geen |
geen |
geen |
geen |
19-7-2018 |
Geen actie |
|
Vleggeert |
Neurochirurg LUMC, (1,0 fte) |
- Secretaris van de Board van de Cervical Spine Research Society Europe (onbetaald) |
geen |
geen |
Onderzoek naar epiduraalinjecties bij sciatica (Ynske Meyesfonds). |
geen |
geen |
25-4-2018 |
Geen actie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een afgevaardigde van een patiëntenvereniging plaats te laten nemen in de werkgroep. Tijdens de oriënterende zoekactie werd gezocht op literatuur naar patiëntenperspectief (zie Strategie voor zoeken en selecteren van literatuur). De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland, het Samenwerkingsverband Pijnpatiënten naar één stem, de Nederlandse Vereniging van Rugpatiënten 'De Wervelkolom' en de Dwarslaesie Organisatie Nederland.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijnmodules en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naarhet stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van de Federatie Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door verschillende stakeholders tijdens de invitational conference. Een verslag van deze bijeenkomst is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur conceptuitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er is op 23 januari 2019 oriënterend gezocht naar bestaande buitenlandse richtlijnen en literatuur over patiëntvoorkeuren en patiëntrelevante uitkomstmaten. Voor de afzonderlijke uitgangsvragen is aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR - voor systematische reviews; Cochrane - voor gerandomiseerd gecontroleerd onderzoek; Newcastle-Ottowa - voor observationeel onderzoek; QUADAS II - voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk* |
|
|
Laag |
|
|
Zeer laag |
|
*in 2017 heeft het Dutch GRADE Network bepaalt dat de voorkeursformulering voor de op een na hoogste gradering ‘redelijk’ is in plaats van ‘matig’
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Randvoorwaarden conservatief en in de module Randvoorwaarden chirurgische ingreep.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers, M. C., Kho, M. E., Browman, G. P., Burgers, J. S., Cluzeau, F., Feder, G., ... & Littlejohns, P. (2010). AGREE II: advancing guideline development, reporting and evaluation in health care. Canadian Medical Association Journal, 182(18), E839-E842.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann, H. J., Oxman, A. D., Brozek, J., Glasziou, P., Jaeschke, R., Vist, G. E., ... & Bossuyt, P. (2008). Rating Quality of Evidence and Strength of Recommendations: GRADE: Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ: British Medical Journal, 336(7653), 1106.
Wessels, M., Hielkema, L., & van der Weijden, T. (2016). How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. Journal of the Medical Library Association: JMLA, 104(4), 320.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
1999 – april 2019
|
1 (((lumbosacral or lumbar) adj2 radicular adj2 (pain or syndrom*)) or lumboradicular compression syndrome or lumbosacral radiculopathy).ti,ab,kw. or radiculopathy.ti. or exp Sciatica/ or sciatic*.ti,ab,kw. or exp Intervertebral Disc Displacement/ or (lumbar disc hernia* or herniated disc or disc protusion or nerve root pain or disc degeneration or discitis or disc extrusion or disc disease).ti,ab,kw. or lumbar stenos*.ti,ab,kw. (54291) 2 exp Low Back Pain/ or (acute adj2 low back adj2 pain*).ti,ab,kw. or (chronic adj2 low back adj2 pain*).ti,ab,kw. (22535) 3 1 or 2 (73595) 4 exp Physical Examination/ or (physical examination or physical test* or lasegue or anamnesis).ti,ab,kw. or history.ti. (1426039) 5 diagnos*.ti,ab,kw. (2265873) 6 3 and 4 and 5 (1745) 7 limit 6 to (english language and yr="1999 -Current") (1247) 8 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (388616) 9 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1845211) 10 7 and 8 (78) 11 7 and 9 (267) 12 11 not 10 (247) 13 10 or 12 (325)
= 325 |
455 |
|
Embase (Elsevier) |
((('lumbosacral radicular pain'/exp OR (((lumbosacral OR lumbar) NEAR/2 radicular NEAR/2 (pain OR syndrom*)):ab,ti)) OR ('lumbosacral radiculopathy'/exp OR 'lumbosacral radiculopathy':ab,ti OR radiculopath*:ti OR 'lumboradicular compression syndrome':ab,ti)) OR ('sciatica'/exp OR sciatic*:ab,ti OR 'lumbar disk hernia'/exp OR 'lumbar disc hernia*':ab,ti OR 'herniated disc':ab,ti OR 'disc protusion':ab,ti OR 'nerve root pain':ab,ti OR 'disc degeneration':ab,ti OR discitis:ab,ti OR 'disc extrusion':ab,ti OR 'disc disease':ab,ti OR 'lumbar stenos*':ab,ti) OR ('low back pain'/exp OR (((acute OR chronic) NEAR/2 'low back' NEAR/2 pain*):ab,ti))) AND ('physical examination'/exp OR 'physical examinations and diagnoses'/exp OR 'physical examination':ab,ti OR 'physical test*':ab,ti OR 'lasegue sign'/exp OR lasegue:ab,ti OR 'anamnesis'/exp OR anamnesis:ab,ti OR history:ti) AND ('diagnostic value'/exp OR diagnos*:ab,ti) AND (1999-2019)/py AND (english)/lim NOT 'conference abstract':it
Gebruikte filters: Systematische reviews: ('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) = 44
RCT’s: ('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it = 139 = 183 |
