Checklist en luchtwegalgoritme
Uitgangsvraag
Wat is de waarde van een checklist en algoritme voor luchtwegmanagement bij de vitaal bedreigde patiënt buiten de operatiekamer?
Aanbeveling
Overweeg het gebruik van een checklist tijdens de voorbereidende fase van een intubatie van een vitaal bedreigde patiënt. Indien in een ziekenhuis een checklist wordt gebruikt, dient deze hetzelfde te zijn voor alle afdelingen waar spoedintubaties worden verricht.
Stel een lokaal toepasbaar luchtwegalgoritme op. Overweeg hiervoor incorporatie van de vortexapproach (of vergelijkbaar) in het lokale algoritme. Stel dit lokale algoritme op met alle afdelingen die potentieel betrokken zijn bij luchtwegmanagement buiten de OK, maar tenminste de anesthesiologie, intensive care en spoedeisende hulp.
Overwegingen
Checklist
Het voorbereiden van een intubatie met behulp van een checklist heeft als doel het minimaliseren van omgevingsfactoren. Er wordt met een checklist gecontroleerd of alle benodigde materialen en apparatuur aanwezig zijn, of de benodigde monitoring aangesloten is, de juiste medicatie beschikbaar is en de patiënt optimaal gepositioneerd is en gepreoxygeneerd wordt. Door de voorbereiding volgens een vaste checklist te doen wordt getracht verschillen tussen afdelingen te minimaliseren. Een voorbeeld checklist staat hieronder weergegeven. Deze checklist is vergelijkbaar met de checklist uit de richtlijn voor intubatie van ICU-patiënten van de difficult airway society (Higgs, 2018). Deze checklist bevat vier onderdelen. Naast het voorbereiden van de patiënt en het voorbereiden van de materialen en apparatuur wordt in deze checklist ook aandacht besteed aan voorbereiding van het team en voorbereiden van moeilijkheid van intubatie door het bespreken van een plan A, B/C en D bij een gefaalde intubatiepoging. Het intubatieteam wordt besproken in submodule 2 en hier alleen genoemd omdat het onderdeel is van de checklist van de difficult airway society. Door het kort benoemen van de taken van de teamleden, af te spreken wat moet gebeuren bij welke gebeurtenis, en te benoemen wat het nieuwe plan wordt bij een gefaalde intubatiepoging wordt gepoogd de kans te vergroten dat alle teamleden als team adequaat handelen indien acute problemen ontstaan tijdens een intubatieprocedure.
Er is onderzoek gedaan naar het effect van een checklist voor acuut luchtwegmanagement bij vitaal bedreigde patiënten (Janz, 2018). In deze gerandomiseerde studie werd een checklist gebruikt met tien items aangaande voorbereiding van de patiënt en materialen en het benoemen van het luchtwegplan en back-up plan. Er werden in totaal 262 patiënten geanalyseerd. Er werd geen verschil gevonden op de primaire en secundaire eindpunten. Deze studie laat zien dat werken zonder checklist mogelijk is. Het feit dat de intubatoren in deze studie gewend waren om met checklists te werken kan echter hebben gezorgd voor confounding, omdat de kans dat iets vergeten wordt indien de patiënt gerandomiseerd was naar standaard zorg kleiner is. Derhalve lijken checklists met name zinvol indien relatief onervaren intubatoren en onervaren overige teamleden aanwezig zijn bij een intubatie. Omdat de afdelingen spoedeisende hulp en intensive care met veel personeelsleden werken en er frequent nieuwe professionals bijkomen is de werkgroep van mening dat een checklist die is afgestemd op zowel de spoedeisende hulp als intensive care altijd zinvol is.
Luchtwegalgoritme
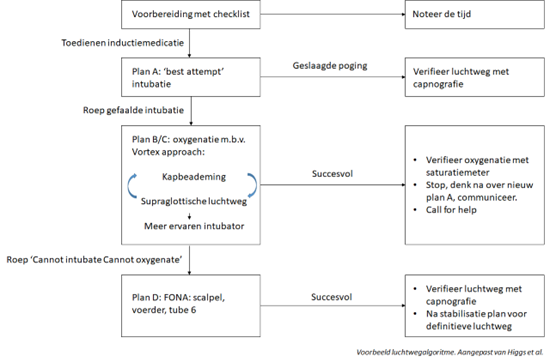
Tijdens een intubatie dient voor ogen gehouden te worden de patiënt gedurende de gehele procedure voldoende te oxygeneren en dienen complicaties zo goed mogelijk te worden voorkomen. Omdat desaturatie makkelijk kan ontstaan en er tegelijkertijd veel kan gebeuren verdient het de voorkeur een algoritme te hebben dat voor alle teamleden duidelijk is. De difficult airway society heeft een voorbeeld algoritme gepubliceerd (Higgs, 2018). In dit algoritme ligt de focus op oxygenatie. Hieronder staat een voorbeeld algoritme dat gebaseerd is op het algoritme van Higgs et al.
Oxygenatie kan worden bewerkstelligd door middel van drie hulpmiddelen waarvan de eerste een intubatiepoging is (plan A). Dit is een intubatiepoging met optimaal gebruik van alle hulpmiddelen die de intubator tot zijn beschikking heeft. Dit houdt in dat indien vooraf besloten wordt dat een bougie gebruikt moet worden dat de bougie dan bij de eerste poging gebruikt wordt. Afhankelijk van de toestand van de patiënt kan plan A tijdens uitvoering worden uitgebreid met 1-2 aanpassingen in positie, hulpmiddelen of laryngoscoop. Indien plan A is gefaald wordt dit bekend gemaakt aan het team en direct overgegaan op plan B/C. Bij plan B/C wordt gepoogd te oxygeneren door middel van kapbeademing of via een supraglottische luchtweg. Plan B/C houdt derhalve geen nieuwe intubatiepoging in en de overstap naar plan B/C dient bij voorkeur te gebeuren voordat er een saturatiedaling optreedt. Indien het met plan B/C lukt om te oxygeneren kan vervolgens worden nagedacht over waarom de intubatie niet gelukt is en een nieuw plan worden bedacht voor een succesvolle intubatie. Indien oxygenatie via kapbeademing of supraglottische luchtweg niet lukt wordt direct overgenomen door een meer ervaren intubator. Indien de intubator reeds de meest ervaren intubator is wordt een ‘cannot intubate cannot oxygenate’ (CICO) situatie uitgeroepen en wordt doorgepakt naar plan D (front of neck access). Afhankelijk van hoe snel de saturatie daalt dient sneller te worden doorgepakt naar het volgende plan. Na overname door de meest ervaren intubator met voldoende training in een CICIO situatie, heeft deze intubator drie opties om de patiënt te oxygeneren. De intubator beslist aan de hand van de situatie welke van de drie mogelijkheden (intubatie, kapbeademing, supraglottische luchtweg) als eerst wordt gepoogd. Oxygenatie heeft prioriteit, dan pas intubatie.
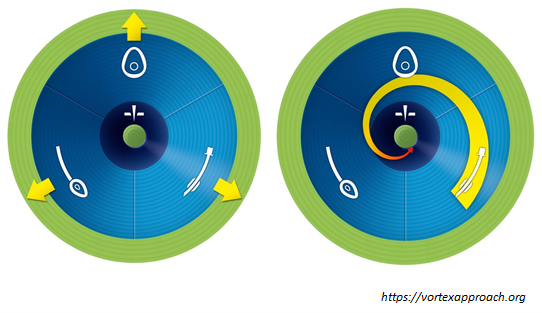
Dit concept, focus op oxygenatie via drie beschikbare tools (kapbeademing, supraglottische luchtweg of intubatie), kan worden gevisualiseerd als de vortexapproach (Chrimes, 2016). Na toedienen van inductiemedicatie bevindt de patiënt zich in de onveilige blauwe zone. Indien het lukt om te oxygeneren verplaatst de patiënt zich naar de veilige groene zone en is er tijd om na te denken over de beste strategie voor een succesvolle intubatie. Naarmate de saturatie daalt ‘daalt’ de patiënt dieper in de onveilige blauwe zone en nadert het moment dat een FONA noodzakelijk is.
Toelichting figuur: Bij adequaat behoud van oxygenatie tijdens de luchtwegprocedure blijft men in de groene zone en is er tijd. Zodra oxygenatie niet voldoende behouden kan worden komt men terecht bij het donkerblauw en moet zodra de gebruikelijke interventies onvoldoende zijn, gekozen worden voor een FONA (Front of neck approach/airway).
Er is volgens deze benadering geen voorkeur voor de volgorde van tools om oxygenatie te bewerkstelligen. Zo kan plan A (een intubatiepoging) worden overgeslagen indien er vlak na toedienen van inductiemedicatie een saturatiedaling optreedt (zie ook module peroxygenatie). Bijvoorbeeld bij een patiënt met ernstige bilaterale pneumonie of een patiënt met morbide obesitas. Anderzijds zal een intubatiepoging de voorkeur hebben als eerste oxygenatiepoging bij patiënten met hoog risico op aspiratie zoals bij patiënten met een ileus. De vortexapproach geeft speelruimte in het algoritme en voorziet in oxygenatiepogingen via kapbeademing of supraglottische luchtweg tussen meerdere intubatiepogingen in. De focus ligt op oxygeneren en dit voorkomt dat via dezelfde techniek meerdere intubatiepogingen worden gedaan met onnodig risico op schade en daardoor risico op bemoeilijkte oxygenatie (Higgs, 2018).
Onderbouwing
Achtergrond
Een spoedintubatie bij een vitaal bedreigde patiënt is een hoog-risico procedure die op verschillende afdelingen uitgevoerd moet kunnen worden. Om invloeden van de omgeving te reduceren wordt uitgezocht wat de meerwaarde is van een checklist en wordt ingegaan op het reduceren van menselijke en mentale invloeden tijdens de procedure door het toepassen van een luchtwegalgoritme.
Samenvatting literatuur
Voor deze module is gebruik gemaakt van de bestaande richtlijn van de difficult airway society en van de literatuur en overwegingen uit andere modules. Voor onderbouwing van de voor- en nadelen van de beschreven behandelstappen wordt verwezen naar de betreffende modules.
Referenties
- Chrimes N (2016). The vortex: a universal 'high-acuity implementation tool' for emergency airway management. Br J Anaesth, 117(S1):i20-i27.
- Higgs A, McGrath BA, Goddard C, Rangasami J, Suntharalingam G, Gale R, et al (2018). Guidelines for the management of tracheal intubation in critically ill adults. Br J Anaesth, 120(2):323-352.
- Janz DR, Semler MW, Joffe AM, Casey JD, Lentz RJ, de Boisblanc BP, et al (2018). A multicenter randomized trial of a checklist for endotracheal intubation of critically ill patients. Chest, 153(4):816-824.
Verantwoording
Beoordelingsdatum en geldigheid
Laatst beoordeeld : 23-02-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS).
De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor vitaal bedreigde patiënten die geïntubeerd worden buiten de OK.
Werkgroep
Dr. J.A.M. (Joost) Labout (voorzitter tot september 2023), intensivist, NVIC
Drs. J.H.J.M. (John) Meertens (interim-voorzitter), intensivist, NVIC
Drs. P. (Peter) Dieperink (interim-voorzitter), intensivist, NVIC
Drs. M.E. (Mengalvio) Sleeswijk (interim-voorzitter), intensivist, NVIC
Dr. F.O. (Fabian) Kooij, anesthesioloog/MMT-arts, NVA
Drs. Y.A.M. (Yvette) Kuijpers, anesthesioloog-intensivist, NVA
Drs. C. (Caspar) Müller, anesthesioloog/MMT-arts, NVA
Drs. M.E. (Mark) Seubert, internist-intensivist, NIV
Drs. S.J. (Sjieuwke) Derksen, internist-intensivist, NIV
Dr. R.M. (Rogier) Determann, internist-intensivist, NIV
Drs. H.J. (Harry) Achterberg, anesthesioloog-SEH-arts, NVSHA
Drs. M.A.E.A. (Marianne) Brackel, patiëntvertegenwoordiger, FCIC/IC Connect
Klankbordgroep
Dr. C.L. (Christiaan) Meuwese, cardioloog-intensivist, NVVC
Drs. J.T. (Jeroen) Kraak, KNO-arts, NVKNO
Drs. H.R. (Harry) Naber, anesthesioloog, NVA
Drs. H. (Huub) Grispen, anesthesiemedewerker, NVAM
Met ondersteuning van
dr. M.S. Ruiter, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
drs. I. van Dijk, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Caspar Müller |
Anesthesioloog/MMT-arts ErasmusMC |
Geen |
Geen |
Geen restricties. |
|
Fabian Kooij |
Anesthesioloog/MMT-arts, Amsterdam UMC |
Chair of the Board, European Trauma Course Organisation |
Geen |
Geen restricties. |
|
Harry Achterberg |
SEH-arts, Isala Klinieken, fulltime - 40u/w (~111%) |
Geen |
Geen |
Geen restricties. |
|
John Meertens |
Intensivist-anesthesioloog, Intensive Care Volwassenen, UMC Groningen |
Secretaris Commissie Luchtwegmanagement, Nederlandse Vereniging voor Intensive Care |
Geen |
Geen restricties. |
|
Joost Labout |
Intensivist |
Redacteur A & I |
Geen |
Geen restricties. |
|
Marianne Brackel |
Patiëntvertegenwoordiger Stichting FCIC en patiëntenorganisatie IC Connect |
Geen |
Voormalig voorzitter IC Connect |
Geen restricties. |
|
Mark Seubert |
Internist-intensivist, |
Waarnemend internist en intensivist |
Lid Sectie IC van de NIV |
Geen restricties. |
|
Mengalvio Sleeswijk |
Internist-intensivist, Flevoziekenhuis |
Medisch Manager ambulancedienst regio Flevoland Gooi en Vecht / TMI Voorzitter Commissie Luchtwegmanagement, Nederlandse Vereniging voor Intensive Care |
Geen |
Geen restricties. |
|
Peter Dieperink |
Intensivist-anesthesioloog, Intensive Care Volwassenen, UMC Groningen |
Lid Commissie Luchtwegmanagement, Nederlandse Vereniging voor Intensive Care |
Geen |
Geen restricties. |
|
Rogier Determann |
Intensivist, OLVG, Amsterdam |
Docent Amstelacademie en Expertcollege |
Geen |
Geen restricties. |
|
Sjieuwke Derksen |
Intensivist - MCL |
Geen |
Geen |
Geen restricties. |
|
Yvette Kuijpers |
Anesthesioloog-intensivist, CZE en MUMC + |
Geen |
Geen |
Geen restricties. |
|
Klankbordgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Christiaan Meuwese |
Cardioloog intensivist, Erasmus MC, Rotterdam |
Section editor Netherlands Journal of Critical Care (onbetaald) |
Extern gefinancierd onderzoek: - REMAP ECMO (Hartstichting) - PRECISE ECLS (Fonds SGS) |
Geen restricties. |
|
Jeroen Kraak |
KNO-arts & Hoofd-halschirurgie |
Geen |
Geen |
Geen restricties. |
|
Huub Grispen |
Anesthesiemedewerker Zuyderland MC |
Geen |
Geen |
Geen restricties. |
|
Harry Naber |
Anesthesioloog MSB Isala |
Geen |
Geen |
Geen restricties. |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het uitnodigen van FCIC/IC Connect voor de schriftelijke knelpunteninventarisatie en deelname aan de werkgroep. Het verslag hiervan [zie aanverwante producten] is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. Ter onderbouwing van de module Aanwezigheid van naaste heeft IC Connect een achterbanraadpleging uitgevoerd. De conceptrichtlijn is tevens voor commentaar voorgelegd aan FCIC/IC Connect en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor vitaal bedreigde patiënten die geïntubeerd worden buiten de OK. Tevens zijn er knelpunten aangedragen door verschillende stakeholders via een schriftelijke knelpunteninventarisatie. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.