Criteria voor luchtkwaliteit in de operatiekamer
Uitgangsvraag
Aan welke minimale criteria moet luchtkwaliteit voldoen op operatiekamers, behandelkamers en opdekruimtes?
Aanbeveling
Onderstaande aanbevelingen betreffen minimale criteria. Het verdient aanbeveling om een goede registratie van postoperatieve wondinfecties bij te houden, waardoor (onverwachte) effecten van eventuele wijzigingen in beleid of techniek kunnen worden gevolgd.
|
Operatiekamer klasse 1+ |
Operatiekamer klasse 1 | Operatiekamer klasse 2 | Zelfstandige behandelkamer | |
| Luchtwisselingen/uur | Ten minste 20x | Ten minste 20x | Ten minste 6x | Ten minste 4x |
| Luchtkwaliteit (isoklasses)$ |
ISO 5 (NEN EN ISO 14644-1) |
ISO 7 (NEN EN ISO 14644-1) |
ISO 7 (NEN EN ISO 14644-1) |
Geen bijzondere vereisten |
| Hersteltijd (1:100) | ≤3 min | ≤20 min (NEN EN ISO 14644-3) | Niet van toepassing | Niet van toepassing |
| Filtering lucht | Ten minste HEPA-filter H13 (EN 1822) | Ten minste HEPA-filter H13 (EN 1822) | Ten minste HEPA-filter H13 (EN 1822) | Geen specifieke eisen |
| Temperatuur* | 18o – 23o | 18o – 23o | 18o – 23o |
Geen specifieke eisen |
| Relatieve vochtigheid* | < 65% | < 65% | < 65% | < 65% |
| Drukhiërarchie/stroomrichting | 3 in zuiverheid aflopende zones (op bouwtekening inzichtelijk gemaakt) ten opzichte van het overige gebouw | 3 in zuiverheid aflopende zones (op bouwtekening inzichtelijk gemaakt) ten opzichte van het overige gebouw | 2 in zuiverheid aflopende zones (op bouwtekening inzichtelijk gemaakt) ten opzichte van het overige gebouw | Niet van toepassing |
$ ISO 7 geldt voor de hele operatiekamer.
* De temperaturen en relatieve vochtigheid die worden aanbevolen zijn richtinggevend, zie toelichting.
Overwegingen
De werkgroep kiest voor minimumcriteria omdat er geen bewijs is dat strengere criteria leiden tot minder postoperatieve wondinfecties. Indien het operatiecomplex voorzien is van een separate opdekruimte, dan worden voor een dergelijke opdekruimte dezelfde eisen gehanteerd als voor de operatiekamer.
Luchtwisselingen/uur
Het ventilatievoud van een ruimte is het getal dat aangeeft hoeveel keer per uur de ruimte van verse buitenlucht wordt voorzien. Een ruimte met ventilatievoud 20 is een ruimte waarin ieder uur 20 maal het volume van de ruimte aan verse buitenlucht wordt toegevoerd. Een deel van de lucht die wordt afgezogen uit de ruimte kan na behandeling (o.a. filteren, koelen, verwarmen) weer ingeblazen worden. Dit deel wordt recirculatievoud genoemd. Het totaal van het ventilatievoud en het recirculatievoud wordt aangeduid als het aantal luchtwisselingen per uur (ook wel aangeduid als circulatievoud (CV)). Dit is een maat voor de ventilatie van die ruimte wat resulteert in het “verdunnen” van de verontreinigingen in de lucht. Waar veel bronnen van verontreiniging aanwezig zijn en/of waar een lage verontreiniging van de lucht gewenst is, is een hoog aantal luchtwisselingen per uur noodzakelijk. Het is niet aannemelijk dat de kans op het ontstaan van een POWI wordt beïnvloed door de oorsprong van de lucht, mits voldoende filtering plaatsvindt.
De ervaring en de literatuurgegevens hebben internationaal geleid tot het voorstellen van minimale aanbevelingen inzake luchtbehandeling voor een operatiekamer in termen van aantal luchtwisselingen (15-20/uur). Bij een mengend systeem resulteert dit iedere 10 tot 13 minuten in een tienvoudige verdunning van een verontreiniging. Dergelijke systemen zijn steeds gebruikt in de vergelijkende studies tussen UDF en mengende systemen. In Nederland wordt sinds geruime tijd minimaal 20 luchtwisselingen per uur aangehouden, maar is het aantal luchtwisselingen vaak veel hoger. Het aantal luchtwisselingen is in belangrijke mate bepalend voor het maximaal aantal personen die in een operatiekamer of opdekruimte aanwezig mogen zijn om een bepaalde maximale concentratie aan deeltjes of kolonievormende eenheden te kunnen realiseren.
Voor lagere klassen operatieruimtes worden zes luchtwisselingen per uur aangehouden. De relatie met de kans op het optreden van POWI is onbekend. Voor het afvoeren van dampvormige anesthetica kan een hogere ventilatievoud (dus hoger aandeel verse buitenlucht) noodzakelijk zijn.
Luchtkwaliteit (isoklasses)
ISO-klasse 7, ‘in rust’, voor ≥ 0,5 μm (NEN-EN-ISO 14644-1) betekent dat er maximaal 352.000 deeltjes met een omvang gelijk aan of groter dan 0,5 μm per m3 ‘in rust’ mogen worden aangetroffen. Deze eis geldt voor de hele operatiekamer.
Het is onduidelijk wat de relatie is tussen het aantal (kleine) stofdeeltjes in de lucht en het optreden van POWI. Toch wordt hier een minimumeis opgenomen op basis van het eerder genoemde uitgangspunt dat besmetting van de wond tijdens de operatie zoveel als mogelijk moet worden beperkt. Een goed reinigbare/gereinigde operatiekamer klasse 1 of 2 met de juiste filters moet in rust tenminste aan ISO 7 kunnen voldoen.
Voorzie de operatieafdeling van een eigen luchtbehandelingsysteem dat qua lucht onafhankelijk functioneert van het ventilatiesysteem van de rest van het gebouw. Dit geldt niet voor een zelfstandige behandelkamer.
Hersteltijd (1:100)
Hersteltijd (NEN-EN-ISO 14644-3) is de tijd die nodig is om, na een verhoging van de concentratie van deeltjes (met een omvang gelijk aan of groter dan 0,5 μm), de concentratie met een factor 100 te verlagen ten opzichte van de situatie direct na het verhogen van de concentratie. Het is van belang te beseffen dat ‘in rust’ een bepaalde basisconcentratie niet met een factor 100 kan worden verlaagd. De hersteltijd geeft aan hoe snel een verstoring (verhoging) ten opzichte van de concentratie ‘in rust’ wordt weggewerkt door het systeem. Hoe meer schone lucht er aan een ruimte wordt toegevoerd hoe korter de hersteltijd zal zijn.
De 100-voudige hersteltijd (t0,01) is in sterke mate gerelateerd aan het aantal luchtwisselingen per uur (CV). Bij optimale menging geldt t0.01[min] = ![]() .
.
De grens is opgenomen om vast te stellen dat de lucht ook effectief wordt gemengd en zodoende de verontreiniging wordt verdund en afgevoerd. De hersteltijd is geen verplichte wachttijd tussen twee ingrepen. De hersteltijd geeft slechts aan hoe lang het duurt om tot een 100-voudige verdunning van de contaminatie van de lucht te komen. Waar veel bronnen van verontreiniging aanwezig zijn en/of waar een lage verontreiniging van de lucht gewenst is, is een hoog aantal luchtwisselingen per uur noodzakelijk, wat resulteert in een korte hersteltijd (1:100).
Filtering lucht
Filters worden onderverdeeld in grofstoffilters, fijnstoffilters (NEN-EN-ISO 16890-1) en eindfilters/absoluutfilters (NEN-EN 1822).
HEPA-filter: High-Efficiency Particulate Air filter conform NEN-EN 1822.
ePM1 90% filter: fijnstoffilter conform NEN-EN-ISO 16890-1:2016 en “Technische specificaties, eisen en classificatiesysteem gebaseerd op vaste deeltjes rendement (ePM)”. In de voorgaande WIP-richtlijn was F9-gefilterde (conform de inmiddels vervallen norm EN779:2012) lucht opgenomen als minimumeis voor de toegevoerde lucht voor zone A, B en C (voor zone A aangevuld met een HEPA eindfilter). Alhoewel dit een proceseis is en geen uitkomstmaat, is de werkgroep van mening dat hiermee de reinheid van de lucht in voldoende mate wordt gewaarborgd. Voor een operatiekamer van Klasse 1 wordt in Nederland al geruime tijd minimaal HEPA H13 gehanteerd.
Aanbevolen wordt om de eisen m.b.t. hersteltijd en ISO klassificatie conform NEN EN ISO 14644-3 vast te stellen op de volgende momenten:
- na aanpassingen in het luchtbehandelingsysteem;
- bij vervanging van de eindfilters indien niet alle bij het systeem behorende eindfilters gelijktijdig worden vervangen;
- als daar op andere gronden aanleiding toe is.
Het functioneren van de HEPA eindfilters moet na installatie, demontage en montage of vervaning worden aangetoond conform NEN EN ISO 14644-3 (installed filter test) of als daar om een andere reden noodzaak toe is.
Drukhiërarchie/stroomrichting
Om de lucht in de operatiekamer/opdekruimte schoon te houden wordt, naast de aanvoer van schone lucht in de operatiekamer, ook een overdruk aangehouden in de operatiekamer ten opzichte van de aangrenzende ruimtes. In de aangrenzende ruimtes wordt een overdruk aangehouden ten opzichte van de ruimtes die verbonden zijn met de rest van het ziekenhuis (drie of twee zones; zie figuur 1). Tussen de operatieafdeling en de rest van het gebouw (zone D) zijn aerogene sluizen aangebracht om personen en goederen vanuit zone D naar het operatiecomplex te transporteren en vice versa. Ruimten zoals de holding, verkoever en kleedruimten (zone C) mogen naast hun primaire functie ook dienstdoen als sluis tussen de operatieafdeling en het overige deel van het gebouw. Hierbij geldt wel dat er een voorziening moet worden getroffen dat de drukhiërarchie over de zones bewaakt wordt. Het doel is dat de lucht op de operatieafdeling van de schoonste naar minder schone ruimten stroomt. Een drukverschil is in de regel makkelijker te bepalen dan een stromingsrichting. Bij een drukverschil van 5 Pa of meer mag worden aangenomen dat er een luchtstroom is. Andere methoden om aan te tonen dat de juiste stromingsrichting is gerealiseerd zijn ook acceptabel, als het ziekenhuis dit inzichtelijk kan maken, bijvoorbeeld door middel van rook.
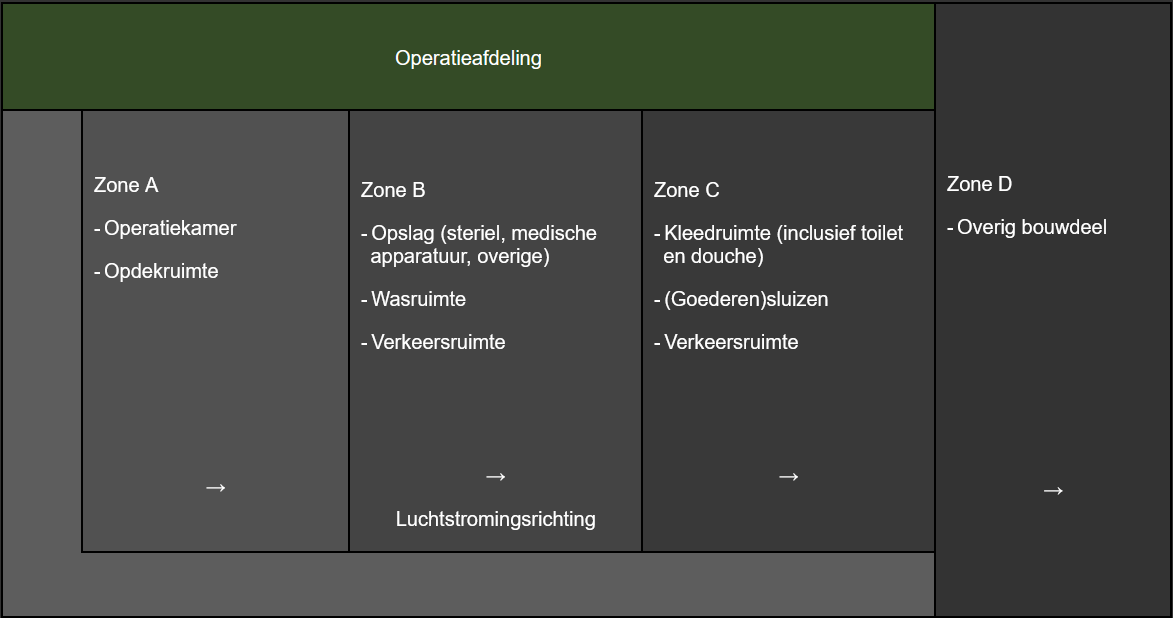
Figuur 1 Voorbeeld van schematisch overzicht van de zone-indeling van de operatieafdeling klasse 1. Holding, verkoever, kantoren en koffiekamer kunnen in zone C worden ondergebracht, maar dat hoeft niet.

Figuur 2 Voorbeeld van schematisch overzicht van de zone-indeling van de operatieafdeling klasse 2
Temperatuur
Een lage lichaamstemperatuur van de patiënt is geassocieerd met een hogere kans op postoperatieve wondinfecties. De meest recente richtlijn van het CDC (Berríos-Torres et al., 2017) beveelt dan ook aan om tijdens de operatie normothermie na te streven. Ook de huidige richtlijn Preventie van postoperatieve wondinfecties (2011) beveelt aan om de lichaamstemperatuur van de patiënt tussen de 36 en 38 graden celsius te houden. Hoewel de temperatuur van de lucht op de operatiekamer zonder twijfel een effect heeft op de lichaamstemperatuur, is er geen wetenschappelijk bewijs dat de temperatuur van de lucht geassocieerd is met meer postoperatieve wondinfecties. De temperaturen die hieronder worden aanbevolen zijn richtinggevend. In voorkomende gevallen kan er afgeweken worden van de aanbevolen temperaturen, bijvoorbeeld bij ingrepen bij neonaten zou een hogere ruimtetemperatuur wenselijk kunnen zijn.
Relatieve vochtigheid
Er is geen relatie tussen relatieve vochtigheid van de lucht en POWI aangetoond. Redenen waarom de werkgroep voor de relatieve vochtigheid van de lucht toch minimum criteria stelt is dat een te hoge vochtigheid tot schimmelgroei kan leiden. Voor de relatieve luchtvochtigheid beveelt de werkgroep aan niet meer dan 1 week achtereen een waarde ≥65%. Een lagere relatieve luchtvochtigheid dan 40% verhoogt de kans op het opbouwen van elektrostatische lading.
Classificatie ingrepen op basis van minimale criteria
De werkgroep heeft aan alle snijdende specialismen gevraagd om per ingreep aan te geven in welke operatiekamer of behandelkamer deze bij voorkeur dient te worden verricht (zie bijlagen). Deze classificatie is gedaan aan de hand van de minimale criteria (zie aanbevelingen). Het betreft hier een dynamisch document waarvan de regie over de inhoud ligt bij de betreffende wetenschappelijke verenigingen.
Onderbouwing
Postoperatieve wondinfecties zijn belangrijke complicaties van operatieve ingrepen. Om deze te voorkomen is het algemene uitgangspunt dat contaminatie van de wond tijdens de ingreep zoveel als mogelijk moet worden beperkt. Een van de potentiële besmettingsbronnen is de omgevingslucht. Het uitgangspunt is dan ook om schone lucht in te blazen en de gecontamineerde lucht af te voeren. Daartoe worden verschillende luchtbehandelingsystemen toegepast. Er is geen wetenschappelijk bewijs gevonden dat een bepaald luchtbehandelingsysteem resulteert in minder wondinfecties dan een ander (zie systematic review van de module ‘Voorkomen van postoperatieve wondinfecties (POWI’s) in de operatiekamer’). Derhalve worden in deze richtlijn de minimale criteria gedefinieerd waaraan een luchtbehandelingsysteem moet voldoen.
Om de uitgangsvraag te beantwoorden is geen systematische literatuuranalyse verricht, omdat het effect van de verschillende criteria op de uitkomstmaat ‘postoperatieve wondinfectie’ niet is onderzocht. Relevante literatuur, richtlijnen en normen werden geraadpleegd (zie literatuurlijst). De werkgroep is op basis van expert opinion tot aanbevelingen gekomen.
- Berríos-Torres SI, Umscheid CA, Bratzler DW et al., for the Healthcare Infection Control Practices Advisory Committee. Centers for Disease Control and Prevention Guideline for the Prevention of Surgical Site Infection, 2017. JAMA Surg. 2017;152(8):784-791.
- NEN-EN 1822-1:2009 en Luchtfilters met een hoog rendement (EPA, HEPA en ULPA) - Deel 1: Classificatie, beproevingsmethoden, merken
- NEN-EN-ISO 14644-1 Stof- en kiemarme ruimten en omgevingen - Deel 1: Classificatie van luchtreinheid op basis van deeltjesconcentraties
- NEN-EN-ISO 14644-3 Stof- en kiemarme ruimten en omgevingen - Deel 3: Beproevingsmethoden
- NEN-EN-ISO 16890-1:2016 en - Luchtfilters voor algemene ventilatie - Deel 1: Technische specificaties, eisen en classificatiesysteem gebaseerd op vaste deeltjes rendement (ePM)
- NEN-EN-ISO 16890-1:2016 en “Technische specificaties, eisen en classificatiesysteem gebaseerd op vaste deeltjes rendement (ePM)”
- Werkgroep Infectie Preventie. Luchtbehandeling in operatiekamer en opdekruimte in operatieafdeling klasse 1. 2014
- Werkgroep Infectie Preventie. Preventie van postoperatieve wondinfecties. 2011
Beoordelingsdatum en geldigheid
Publicatiedatum : 08-04-2022
Beoordeeld op geldigheid : 07-04-2022
Algemene gegevens
Regiehouder: Samenwerkingsverband Richtlijnen Infectiepreventie (SRI)
De richtlijnontwikkeling werd ondersteund door drs. B.S. Niël-Weise, zelfstandig richtlijnmethodoloog, en dr. M.A. Pols, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten, en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Deze richtlijn heeft tot doel om aanbevelingen te doen over de luchtkwaliteit in operatiekamers, opdekruimten en zelfstandige behandelkamers in ziekenhuizen en particuliere klinieken. De richtlijn beschrijft de minimale criteria van de luchtkwaliteit op basis van wetenschappelijk bewijs en de kennis van experts.
Doelgroep
Deze richtlijn is primair geschreven voor medewerkers die beleid maken op het gebied van infectiepreventie, waaronder raden van bestuur van zorginstellingen, deskundigen infectiepreventie, artsen-microbiologen en internist-infectiologen, en alle medisch specialisten die interventies doen op operatiekamers en zelfstandige behandelkamers.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van specialismen die betrokken zijn bij de zorg voor patiënten die een ingreep ondergaan, medisch specialisten die interventies doen op operatiekamers en zelfstandige behandelkamers en (arts-)specialisten op het gebied van infectiepreventie.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Dr. J.J. Duvekot (voorzitter), gynaecoloog-perinatoloog, Erasmus MC, Rotterdam
- Prof. Dr. J. Kluytmans, arts-microbioloog, Amphia Ziekenhuis/Molengracht, Breda; Julius Center for Health Sciences and Primary Care, Universitair Medisch Centrum Utrecht, Utrecht
- Prof. Dr. A. Voss, arts-microbioloog, Radboud Universitair Medisch Centrum en Canisius Wilhelmina Ziekenhuis, Nijmegen
- Dr. I.J.B. Spijkerman, arts-microbioloog, Amsterdam Universitair Medische Centra, locatie AMC, Amsterdam
- Dr. M.V. Joosse, oogarts, Haaglanden MC, Den Haag
- Prof. Dr. P.C. Jutte, orthopedisch chirurg, Universitair Medisch Centrum Groningen, Groningen
- Dr. F.O. Kooij, anesthesioloog, Amsterdam Universitair Medische Centra, locatie AMC, Amsterdam
- Dr. P.M.N.Y.H. Go, chirurg, St Antonius Ziekenhuis, Nieuwegein
- Dr. A.B. Steensma, gynaecoloog, Erasmus MC, Rotterdam
- Dr. M. Cromheecke, plastisch chirurg, Zipper Clinics, Enschede
- Dr. P. Segers, cardiothoracaal chirurg, Maastricht Universitair Medisch Centrum, Maastricht
- Dr. F. d’Ancona, uroloog, Radboud Universitair Medisch Centrum, Nijmegen
- Dr. Ir. L. Poot, klinisch fysicus, Isala, Zwolle
- Ir. R. Wientjes, klinisch fysicus, Universitair Medisch Centrum Utrecht, Utrecht
- Dhr. K. Ballemans, deskundige infectiepreventie, Unic Medical Services BV, Nieuwegein
- Dhr. P. Bergervoet, deskundige infectiepreventie, Tensen & Nolte Infectiepreventie, Nieuwe Niedorp
- Prof. dr. M.W. de Haan, interventieradioloog, Maastricht Universitair Medisch Centrum, Maastricht
- Prof. dr. M.J. Schalij, interventiecardioloog, Leids Universitair Medisch Centrum, Leiden
- Dr. G.A.M. Krekels, dermatoloog, MohsA, Venray
Met ondersteuning van
- Drs. B.S. Niël-Weise, zelfstandig richtlijnmethodoloog, Deventer
- Dr. M.A. Pols, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
|
Werkgroeplid |
Functie |
Nevenfuncties |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatie-management |
Extern gefinancierd onderzoek |
Kennis Valorisatie |
Overige belangen |
|
J.J. Duvekot |
Gynaecoloog-perinatoloog |
Directeur Medisch Advies en Expertise Bureau Duvekot |
geen |
geen |
Voorzitter Adviescommissie Richtlijnen FMS |
geen |
geen |
geen |
|
J. Kluytmans |
Arts-microbioloog Amphia Ziekenhuis Breda (0,6); onderzoeker UMC Utrecht (0,4) |
|
Geen directe belangen (beleg in aandelen zonder te beleggen in specifieke bedrijven, maar mogelijk wel als onderdeel van pakketten en sectoren). Oefen daar geen directe invloed op uit.
Lid advisory board 3M; Lid advisory board Destiny Farma. |
geen |
Voorzitter NVMM |
geen |
geen |
geen |
|
A. Voss |
Arts-microbioloog. CWZ; Hoogleraar infectiepreventieRadboud UMC |
|
geen |
geen |
geen |
geen |
geen |
geen |
|
I.J.B. Spijkerman |
Arts-microbioloog, AMC, Amsterdam |
geen |
geen |
geen |
geen |
geen |
geen |
geen |
|
M.V. Joosse |
Oogarts, opleider |
|
Adviseur Micreos Human Health BV en opties. Micreos ontwikkelt geneesmiddelen en preparaten die bacteriofaagafgeleiden bevatten waarmee bacteriële infecties kunnen worden bestreden op de huid en in voedingsmiddelen. |
CEO van Micreos is broer van echtgenote. |
|
geen |
geen |
geen |
|
F.O. Kooij |
Anesthesioloog/ MMT arts |
|
geen |
geen |
Deelname aan de vorige expertgroep, nog onder WIP regie |
geen |
geen |
geen |
|
P.M.N.Y.H. Go |
Chirurg |
|
geen |
geen |
VMS St. Antonius ziekenhuis, Nieuwegein. |
geen |
geen |
geen |
| P.C. Jutte |
Orthopedisch chirurg |
|
geen |
geen |
Lid wetenschappelijke commissie Sarcoom patiënten vereniging |
ZonMW LEAK study. De beste behandeling van wondlekkage na heup of knieprothese |
geen |
geen |
|
A.B. Steensma |
Gynaecoloog |
|
geen |
Geen |
geen |
geen |
geen |
Eerder echo apparatuur (GE Kretz) geleend; dit heeft niet geleid tot inmenging in onderzoek dan wel aankoop echo apparatuur. |
|
M. Cromheecke |
Plastisch chirurg; DGA privekliniek Zipper Clinics |
|
geen |
Geen |
geen |
geen |
geen |
geen |
|
P. Segers |
Cardiothoracaal chirurg |
geen |
geen |
Geen |
geen |
geen |
geen |
geen |
|
F. d’Ancona |
Uroloog, Radboudumc |
|
geen |
Geen |
geen |
PI van tweetal door industrie gefinancierde klinische onderzoeken die in Radboudumc worden uitgevoerd: Storz; Neotract. |
geen |
geen |
|
L. Poot |
Klinisch Fysicus te Isala Zwolle |
|
geen |
Geen |
Voorzitter NVKF |
geen |
geen |
geen |
|
R. Wientjes |
Klinisch Fysicus, UMC Utrecht |
geen |
geen |
Geen |
geen |
geen |
geen |
geen |
|
K. Ballemans |
Deskundige infectiepreventie Unic Medical Services BV |
geen |
geen |
Geen |
geen |
geen |
geen |
geen |
|
P. Bergervoet |
Deskundige infectiepreventie bij Tensen en Nolte infectiepreventie |
geen |
geen |
Geen |
geen |
geen |
geen |
geen |
|
M.W. de Haan |
Interventieradioloog |
Voorzitter Centrale Opleiding Commissie Maastricht UMC+ (niet persoonsgebonden vergoeding aan afdeling radiologie) |
geen |
Geen |
Voorzitter Centrale Opleiding Commissie Maastricht UMC+ |
Principal investigator:
Deelname aan:
|
geen |
geen |
|
M.J. Schalij |
Hoofd Cardiologie UMC |
geen |
geen |
Geen |
geen |
geen |
geen |
geen |
|
G.A.M. Krekels |
Dermatoloog (80%)/ Bestuurder Stichting Mohsa/Mohs Expert (20%) |
geen |
Vertegenwoordig de NVDV als dermatoloog / lid, tevens bestuurder van een huidcentrum |
Geen |
geen |
geen |
geen |
geen |
Inbreng patiëntenperspectief
In het kader van de knelpuntanalyse was de Patiëntenfederatie Nederland uitgenodigd voor een invitational conference. Zij hebben laten weten hieraan niet deel te nemen vanwege het technische karakter van de richtlijn. Ook tijdens de commentaarfase is de Patiëntenfederatie Nederland gevraagd om input.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren (zie het implementatieplan). Hiertoe is het concept van de richtlijn met de belangrijkste stakeholders besproken in het kader van haalbaarheid alvorens de richtlijn ter becommentariëring naar de wetenschappelijke verenigingen te sturen.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwalitieit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers et al., 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep, de werkgroepleden en de adviseurs de knelpunten: er is veel discussie over de WIP-richtlijn ‘Luchtbehandeling in operatiekamer en opdekruimte in operatieafdeling klasse 1 (2014)’. De discussie over deze richtlijn betrof met name het feit dat bepaalde operatiekamers, na metingen conform VCCN-RL 7 niet bleken te voldoen aan de gestelde prestatie-eisen voor het beschermde gebied.
Tevens zijn er via een invitational conference knelpunten aangedragen door vertegenwoordigers van de Inspectie voor de Gezondheidszorg, Nederlands Oogheelkundig Gezelschap, Nederlandse Orthopedische Vereniging, Nederlandse Vereniging voor Anesthesiologie, Nederlandse Vereniging voor Klinische Fysica, Nederlandse Vereniging voor Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied, Nederlandse Vereniging voor Plastische Chirurgie, Vereniging voor Hygiëne en Infectiepreventie in de Gezondheidszorg, Nederlandse Vereniging van Ziekenhuizen, Radboud UMC, UMC Groningen, UMC Utrecht, LUMC, VUMC, Ziekenhuis Tergooi, TNO, Kalibra, Surgicube en Vereniging Contamination Control Nederland. Een verslag van de invitational conference kunt u vinden in de bijlagen.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep uitgangsvragen opgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar bestaande buitenlandse richtlijnen en naar systematische reviews in de databases Medline en Embase (vanaf het jaar 2000). Zie hiervoor de zoekverantwoording. Vervolgens werd voor de uitgangsvraag over welk type luchtbehandelingsysteem aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases (vanaf het jaar 1990). Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in de module van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de risk-of-bias tabel.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij voldoende overeenkomsten tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kwaliteit van bewijs (‘quality of evidence’) werd beoordeeld met behulp van GRADE (Guyatt et al., 2008). GRADE is een methode die per uitkomstmaat van een interventie, of voor een risico- of prognostische factor, een gradering aan de kwaliteit van bewijs toekent op basis van de mate van vertrouwen in de schatting van de effectgrootte (tabel 1 en 2).
Tabel 1 Indeling van de kwaliteit van bewijs volgens GRADE
|
Hoog |
Er is veel vertrouwen dat het werkelijke effect dicht in de buurt ligt van het geschatte effect. |
|
|
|
|
Matig |
Er is matig vertrouwen in het geschatte effect: het werkelijk effect ligt waarschijnlijk dicht bij het geschatte effect, maar er is een mogelijkheid dat het hiervan substantieel afwijkt. |
|
|
|
|
Laag |
Er is beperkt vertrouwen in het geschatte effect: het werkelijke effect kan substantieel verschillen van het geschatte effect. |
|
|
|
|
Zeer laag |
Er is weinig vertrouwen in het geschatte effect: het werkelijke effect wijkt waarschijnlijk substantieel af van het geschatte effect. |
Tabel 2 De kwaliteit van bewijs wordt bepaald op basis van de volgende criteria
|
Type bewijs |
Voor studies over interventies: RCT start in de categorie ‘hoog’. Observationele studie start in de categorie ‘laag’. Alle overige studietypen starten in de categorie ‘zeer laag’.
Voor studies over een risico- of prognostische factor: Prospectieve of retrospectieve cohortstudie start in de categorie ‘hoog’. Voor andere studieontwerpen wordt afgewaardeerd via ‘risk of bias’. |
|
|
Afwaarderen |
‘Risk of bias’ |
- 1 Ernstig - 2 Zeer ernstig |
|
|
Inconsistentie |
- 1 Ernstig - 2 Zeer ernstig |
|
|
Indirect bewijs |
- 1 Ernstig - 2 Zeer ernstig |
|
|
Onnauwkeurigheid |
- 1 Ernstig - 2 Zeer ernstig |
|
|
Publicatiebias |
- 1 Waarschijnlijk - 2 Zeer waarschijnlijk |
|
Opwaarderen |
Groot effect |
+ 1 Groot + 2 Zeer groot |
|
|
Dosis-respons relatie |
+ 1 Bewijs voor gradiënt |
|
|
Alle plausibele ‘confounding’ |
+ 1 zou een effect kunnen reduceren + 1 zou een tegengesteld effect kunnen suggereren terwijl de resultaten geen effect laten zien. |
Formuleren van de conclusies
Een conclusie verwijst niet naar één of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence).
Overwegingen
Voor het formuleren van een aanbeveling zijn naast de kwaliteit van het wetenschappelijk bewijs over de gewenste en ongewenste effecten van een interventie, of over de effectgrootte van een risico- of prognostische factor, vaak ook nog andere factoren van belang (Alonso-Coello et al., 2016).
Genoemd kunnen worden:
- kosten,
- waarden, voorkeuren en ervaringen van patiënten en behandelaars met betrekking tot interventies en uitkomsten van zorg,
- balans van gewenste en ongewenste effecten van interventies ten opzichte van geen of andere interventies,
- aanvaardbaarheid van interventies,
- haalbaarheid van een aanbeveling.
Deze aspecten worden besproken na de ‘conclusie’ onder het kopje ‘overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven een antwoord op de uitgangsvraag en zijn gebaseerd op het beste beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. Dit is afhankelijk van het gewicht dat wordt toegekend aan kosten, gewenste of ongewenste effecten en andere onder de overwegingen genoemde factoren.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in module 5.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is. Een overzicht van aanbevelingen voor nader/vervolg onderzoek staat in de Kennislacunes.
Commentaar- en autorisatiefase
De conceptrichtlijn is aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. Tevens is de richtlijn voorgelegd aan de volgende organisaties ter becommentariëring: Inspectie voor de Gezondheidszorg, Zorgverzekeraars Nederland, Zorginstituut Nederland, Samenwerkende Topklinische Ziekenhuizen, Nederlandse Vereniging van Ziekenhuizen, Nederlandse Federatie van Universitair Medische Centra, Patiëntenfederatie Nederland, Nederlandse Vereniging voor Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied, Nederlandse Internisten Vereniging, Nederlandse Vereniging voor Neurochirurgie, Nederlands Huisartsen Genootschap, Nederlands Genootschap van Abortusartsen, Koninklijke Nederlandse Maatschappij tot bevordering der Tandheelkunde, NVMKA, TNO, VCCN. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn is aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
Literatuur
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ 2016;353:i2089.
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ 2010;182:E839-42.
Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P, Schünemann HJ; GRADE Working Group. GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ 2008;336: 924-6.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site/richtlijnontwikkeling.html
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
Zoekverantwoording
Algemene zoekstrategie
Medline
Database: MEDLINE <1946 to 2018 February 14>
Search Strategy:
--------------------------------------------------------------------------------
1 "update WIP richtlijn luchtbehandeling operatiekamers".ti. (0)
2 Operating Rooms/ (12397)
3 (operating adj3 (room? or theatre? or department?)).tw. (27220)
4 (operating adj3 (room? or theatre? or department?)).kf. (1057)
5 (surgical adj3 suite?).tw. (492)
6 (surgical adj3 suite?).kf. (1)
7 or/2-6 (34096) setting
8 ((clean or ultraclean or indoor) adj3 air).tw. (7309)
9 ((clean or ultraclean or indoor) adj3 air).kf. (640)
10 (air adj3 (particle? or flow or ventilation or handling or counts)).tw. (8072)
11 (air adj3 (particle? or flow or ventilation or handling or counts)).kf. (78)
12 ((turbulen* or displacement) adj3 ventilation).tw. (73)
13 ((turbulen* or displacement) adj3 ventilation).kf. (1)
14 ((((ventilation or air) adj handling) or air-handling) adj3 system).tw. (34)
15 ((((ventilation or air) adj handling) or air-handling) adj3 system).kf. (0)
16 Ventilation/ (5273)
17 ((laminar adj3 flow) or (laminar adj3 airflow) or (conventional adj3 flow) or (conventional adj3 airflow)).tw. (4903)
18 ((laminar adj3 flow) or (laminar adj3 airflow) or (conventional adj3 flow) or (conventional adj3 airflow)).kf. (88)
19 ((conventional or ultraclean or plenum or hori?ontal or vertical) adj3 ventilat*).tw. (2408)
20 ((conventional or ultraclean or plenum or hori?ontal or vertical) adj3 ventilat*).kf. (16)
21 or/8-20 (26185) lucht kenmerken
22 7 and 21 (933) kenmerken in operatieruimte
23 ((air or airborne) adj3 bacteri*).tw. (1331)
24 ((air or airborne) adj3 bacteri*).kf. (154)
25 Air Microbiology/ (7065)
26 Air Pollution, Indoor/ (11714)
27 ((air or airborne) adj3 (microbiol* or pollution or pollutant? or contamination?)).tw. (25380)
28 ((air or airborne) adj3 (microbiol* or pollution or pollutant? or contamination?)).kf. (6143)
29 or/23-28 (44198) luchtkwaliteit
30 Surgical Wound Infection/ (32966)
31 ((surgical or postoperative or site) adj3 infection?).tw. (30567)
32 ((surgical or postoperative or site) adj3 infection?).kf. (1737)
33 ((exogenous or wound? or injur*) adj3 infect*).tw. (33267)
34 ((exogenous or wound? or injur*) adj3 infect*).kf. (1393)
35 or/30-34 (78438) infectie risico onderdeel
36 22 and 29 (428) kenmerken operatieruimte en luchtkwaliteit
37 35 and 36 (227) kenmerken operatieruimte en luchtkwaliteit en infectie risico
38 37 (227)
39 limit 38 to yr="2000 -Current" (75)
40 (dutch or german or english).la. (24416262)
41 39 and 40 (72) spec search
42 "bischoff$".fc_auts. and "effect of laminar airflow".fc_titl. (1)
43 41 and 42 (0)
44 Infection Control/ (21623)
45 Infection/pc [Prevention & Control] (145)
46 Bacterial Infections/pc [Prevention & Control] (8707)
47 35 or 44 or 45 or 46 (105550) infectie risico
48 36 and 47 (254) kenmerken operatieruimte en luchtkwaliteit
49 7 and 21 and 47 (402)
50 49 (402)
51 limit 50 to yr="2000 -Current" (163)
52 40 and 51 (153) specifieke search
53 "Hospital Design and Construction"/ (9592)
54 47 and (21 or 29) and 40 (1112)= infectie risico en lucht kenmerken of luchtkwaliteit
55 54 (1112)
56 limit 55 to yr="2000 -Current" (487)
57 guideline/ or practice guideline/ (30259)
58 (guideline? or protocol? or standard?).ti. (165993)
59 (guideline? or protocol? or standard?).kf. (17410)
60 57 or 58 or 59 (192870) richtlijnen
61 "filter systematic reviews".ti. (0)
62 meta analysis.pt. (84720)
63 (meta-anal$ or metaanal$).af. (150663)
64 (quantitativ$ adj10 (review$ or overview$)).tw. (7235)
65 (systematic$ adj10 (review$ or overview$)).tw. (130114)
66 (methodologic$ adj10 (review$ or overview$)).tw. (9507)
67 (quantitativ$ adj10 (review$ or overview$)).kf. (35)
68 (systematic$ adj10 (review$ or overview$)).kf. (10127)
69 (methodologic$ adj10 (review$ or overview$)).kf. (46)
70 medline.tw. and review.pt. (67440)
71 (pooled adj3 analy*).tw. (14519)
72 (pooled adj3 analy*).kf. (152)
73 "cochrane$".fc_jour. (13431)
74 or/62-73 (270752) SR
75 56 and 60 (20)= guidelines
76 (56 and 74) not 60 (20)= SR
77 42 and 47 (1)
78 (7 or 21 or 29) and 47 and 40 and 60 (106)= (operatie ruimte of lucht kenmerken of lucht kwaliteit ) en infectie risico en talen en richtlijnen
79 (7 or 21 or 29) and 47 and 40 and 74 (57) )= (operatie ruimte of lucht kenmerken of lucht kwaliteit ) en infectie risico en talen en SR
80 79 (57)
81 limit 80 to yr="2000 -Current" (55)
82 78 (106)
83 limit 82 to yr="2000 -Current" (64) guidelines vanaf 2000
84 78 (106)
85 79 not 78 (54)
86 85 (54)
87 limit 86 to yr="2000 -Current" (52) SR vanaf 2000
Embase
Database: Embase <1974 to 2018 February 14>
Search Strategy:
--------------------------------------------------------------------------------
1 bacteriological standards for air in ultraclean operating rooms.ti. (1)
2 *"air sampling"/ (4247)
3 operating room/ (30635)
4 (operating adj3 (room? or theatre? or department?)).tw. (36747)
5 (operating adj3 (room? or theatre? or department?)).kw. (1307)
6 (surgical adj3 suite?).tw. (640)
7 (surgical adj3 suite?).kw. (9)
8 ((clean or ultraclean or indoor) adj3 air).tw. (10717)
9 ((clean or ultraclean or indoor) adj3 air).kw. (2476)
10 (air adj3 (particle? or flow or ventilation or handling or counts)).tw. (11485)
11 (air adj3 (particle? or flow or ventilation or handling or counts)).kw. (327)
12 ((turbulen* or displacement) adj3 ventilation).tw. (131)
13 ((turbulen* or displacement) adj3 ventilation).kw. (17)
14 ((((ventilation or air) adj handling) or air-handling) adj3 system).tw. (49)
15 ((((ventilation or air) adj handling) or air-handling) adj3 system).kw. (0)
16 air conditioning/ (22739)
17 exp microclimate/ (49264)
18 ((laminar adj3 flow) or (laminar adj3 airflow) or (air adj3 condition*) or microclimate or (conventional adj3 flow) or (conventional adj3 airflow)).tw. (14935)
19 ((laminar adj3 flow) or (laminar adj3 airflow) or (air adj3 condition*) or microclimate or (conventional adj3 flow) or (conventional adj3 airflow)).kw. (900)
20 ((conventional or ultraclean or plenum or hori?ontal or vertical) adj3 ventilat*).tw. (3222)
21 ((conventional or ultraclean or plenum or hori?ontal or vertical) adj3 ventilat*).kw. (82)
22 or/3-7 (49072) operatie ruimte
23 or/8-21 (79517) lucht kenmerken
24 ((air or airborne) adj3 bacteri*).tw. (1590)
25 ((air or airborne) adj3 bacteri*).kw. (185)
26 microbiology/ or environmental microbiology/ (278101)
27 air sampling/ (13186)
28 indoor air pollution/ (12266)
29 ((air or airborne) adj3 (microbiol* or pollution or pollutant? or contamination?)).tw. (36821)
30 ((air or airborne) adj3 (microbiol* or pollution or pollutant? or contamination?)).kw. (10262)
31 or/24-30 (339143) lucht kwaliteit
32 surgical infection/ (37425)
33 ((surgical or postoperative or site) adj3 infection?).tw. (41170)
34 ((surgical or postoperative or site) adj3 infection?).kw. (3459)
35 ((exogenous or wound? or injur*) adj3 infect*).tw. (44606)
36 ((exogenous or wound? or injur*) adj3 infect*).kw. (2291)
37 wound infection/ (40718)
38 exp infectious complication/ (148840)
39 infection control/ (78408)
40 or/32-39 (260511)
41 40 and 22 (3801) )=infectie risico en operatie ruimte
42 40 and 22 and (23 or 31) (669)=infectie risico en operatie ruimte en lucht kenmerken of lucht kwaliteit )
43 "construction work and architectural phenomena"/ (7883)
44 hospital building/ (1533)
45 hospital design/ (9404)
46 (dutch or german or english).la. (27927468)
47 42 and 46 (584) infectie risico en operatie ruimte en lucht kenmerken of lucht kwaliteit ) en talen
48 limit 47 to yr="2010 -Current" (184)
49 "filter systematic reviews & meta-analyses Embase".ti. (0)
50 meta analysis/ (138059)
51 "systematic review"/ (156492)
52 (meta-analy$ or metaanaly$).tw. (159554)
53 (systematic$ adj4 (review$ or overview$)).tw. (155503)
54 (quantitativ$ adj5 (review? or overview?)).tw. (4078)
55 (methodologic adj5 (overview? or review?)).tw. (337)
56 (review$ adj3 (database? or medline or embase or cinahl)).tw. (21150)
57 (pooled adj3 analy$).tw. (22074)
58 (extensive adj3 review$ adj3 literature).tw. (3078)
59 (meta or synthesis or (literature adj8 database?) or extraction).tw. (1243154)
60 review.pt. (2328762)
61 59 and 60 (119814)
62 (systematic$ adj4 (review$ or overview$)).kw. (18697)
63 (quantitativ$ adj5 (review? or overview?)).kw. (52)
64 (pooled adj3 analy$).kw. (387)
65 or/50-58,61-64 (413604)sr
66 48 and 65 (16)
67 from 66 keep 1-16 (16)
68 practice guideline/ or health care quality/ or good clinical practice/ (533007)
69 (guideline? or protocol? or standard?).ti. (212896)
70 (guideline? or protocol? or standard?).kw. (51376)
71 or/68-70 (695692) richtlijnen
72 48 and 71 (22)
73 66 not 72 (12)
74 exp health care facility/ (1387651)
75 from 72 keep 1-22 (22)
76 from 73 keep 1-12 (12)
77 40 and 71 and 74 (3799)
78 77 (3799)
79 limit 78 to yr="2010 -Current" (2086)
80 79 and (31 or air.tw.) (111)
81 air monitoring/ or environmental monitoring/ (61869)
82 31 or 81 (391819)
83 40 and (22 or 74) and (23 or 82) and 46 and 71 (255)
84 83 (255)
85 limit 84 to yr="2010 -Current" (127)
86 85 not 72 (105)
87 (40 and (22 or 74) and (23 or 82) and 46 and 65) not (66 or 85) (40)
88 47 (584)
89 47 and 71 (51)
90 limit 89 to yr="2000 -Current" (45)
91 47 and 65 (17)
92 91 not 90 (13)
93 92 (13)
94 limit 93 to yr="2000 -Current" (12)
95 40 and (23 or 31) and (22 or 43 or 44 or 45) (755)
96 95 (755)
97 limit 96 to yr="2000 -Current" (383)
98 97 and 46 and 71 (63)
99 (97 and 46 and 65) not 71 (12)
100 46 and 47 and 71 (51)
101 100 (51)
102 limit 101 to yr="2000 -Current" (45)=guidelines
103 (46 and 47 and 65) not 71 (13)
104 103 (13)
105 limit 104 to yr="2000 -Current" (12)=SR
