Optimale bedbezetting
Uitgangsvraag
Wat is het minimale bedbezettingspercentage op de IC?
Aanbeveling
Neem maatregelen om een hoge bedbezetting en/of een laag aantal beschikbare IC-bedden te voorkomen.
Houd bij eventueel te nemen maatregelen rekening met het aantal operationele bedden en de dynamiek en het karakter van de eigen afdeling en organisatie. Een bedbezetting van 80% tot 90% kan gezien worden als optimaal. Naarmate het aantal operationele bedden kleiner is lijkt het raadzaam om te streven naar een lager maximaal bedbezettingspercentage binnen de genoemde bandbreedte.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is literatuuronderzoek verricht naar het effect van bedbezettingspercentage op mortaliteit, heropname, complicaties, patiënt- en zorgverlenerstevredenheid en werkverzuim in volwassen patiënten die zijn opgenomen op de IC-afdeling. In de literatuursamenvatting zijn twee observationele studies geïncludeerd die aan de PICO voldeden. Daarnaast zijn er nog vier niet-vergelijkende observationele studies geïncludeerd waarvan de resultaten apart zijn uitgewerkt in een tabel zonder GRADE beoordeling.
De cruciale uitkomstmaten waren mortaliteit, heropname en complicaties. Mortaliteit en heropname werden gerapporteerd. De bewijskracht voor beide uitkomstmaten was echter zeer laag. Dit komt door een risico op bias en de brede betrouwbaarheidsintervallen rondom de puntschatters, welke de grenzen voor klinische besluitvorming overschrijden. Complicaties werden niet gerapporteerd.
Vijf van de zes geselecteerde artikelen tonen een associatie tussen een hogere bedbezetting en/of minder beschikbare bedden en een verhoogde IC- of ziekenhuismortaliteit, voortijdige overplaatsing naar de verpleegafdeling, vaker overplaatsing naar een ander ziekenhuis, meer heropnames en meer reanimaties op de verpleegafdeling (Bagshaw, 2018; Blayney, 2020; Gabler, 2013; Town, 2014; Wilcox, 2020).
Blayney (2020) beschrijft de relatie tussen het bedbezettingspercentage van alle Schotse IC’s en voortijdige overplaatsing naar de verpleegafdeling of overplaatsing naar een ander ziekenhuis. Hierbij ligt het inflectiepunt van de associatie tussen het bezettingspercentage en voortijdig ontslag of overplaatsing naar een ander ziekenhuis rond de 80-90%. Zowel voortijdig ontslag als overplaatsing naar een ander ziekenhuis waren in deze studie geassocieerd met een verhoogde ziekenhuismortaliteit (Blayney, 2020).
Town (2014) beschrijft een associatie tussen een hogere kans op heropnames naarmate het aantal beschikbare IC-bedden verder afneemt in de context van een Amerikaans academisch ziekenhuis.
Bagshaw (2018) beschrijft een associatie tussen het aantal beschikbare bedden en het bedbezettingspercentage en IC-mortaliteit op negen Canadese IC’s. Deze associatie wordt sterker en tevens significant (en relevant) als er ≤ 1 bed beschikbaar is of bij een bezettingspercentage van ≥ 95%.
Bovenstaande zou kunnen suggereren dat er niet alleen een associatie is tussen parameters van ‘beddendruk’ en belangrijke uitkomstmaten zoals mortaliteit, heropnames en reanimaties op verpleegafdelingen, maar dat deze associatie mogelijk ook sterker is naarmate de beddendruk toeneemt. Dit sluit aan bij ander onderzoek waar de impact van een hoog bedbezettingspercentage op belangrijke uitkomstmaten lijkt af te nemen naarmate het aantal operationele bedden toeneemt (Blayney, 2020).
De geselecteerde artikelen geven geen informatie over een minimaal bedbezettingspercentage in relatie tot de uitkomstmaten. De belangrijke uitkomstmaten, patiënt- en zorgverlenerstevredenheid en werkverzuim, werden niet gerapporteerd in de geïncludeerde studies. Deze uitkomstmaten kunnen dan ook geen verdere richting geven voor de besluitvorming. De aanbevelingen zijn daarom voornamelijk gebaseerd op expert opinie en waar mogelijk onderbouwd met (indirecte) literatuur.
Berekening bedbezetting
Er zijn verschillende manieren om bedbezetting uit te drukken en er is geen gevalideerde methode beschikbaar. Een van de methoden die als nauwkeuriger wordt beschreven, is het totaal van de dagelijkse werkelijke patiënturen op de IC, waarbij de operationele (en bij voorkeur volledig bemande) bedden als noemer gebruikt wordt (Tierney, 2014). Dit betekent dat het bedbezettingspercentage wordt gedefinieerd als het aantal uren per 24 uur waarop de operationele bedden in gebruik zijn voor een patiënt. Ter illustratie: op een IC met vier operationele bedden verblijven er drie patiënten de hele dag en een vierde patiënt wordt om 12:00 uur opgenomen. De bedbezetting is dan 3,5/4 = 0,875 (87,5%). Dit wordt ook wel de warme bedbezetting genoemd. Voor de huidige financiering wordt gebruik gemaakt van de koude bedbezetting: een IC declareert een IC-ligdag als een patiënt (een deel van) een kalenderdag op de IC behandeld is. In het bovenstaande voorbeeld is de bedbezetting dan 100%, op elk van die 4 bedden heeft op die kalenderdag minstens 1 patiënt gelegen. De warme bedbezetting zegt iets over kwaliteit van zorg en over beschikbaarheid van een ‘leeg’ operationeel bed. De koude bedbeztting is bedoeld voor bekostiging.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Er is niet gesproken met patiëntvertegenwoordigers rondom de uitwerking van deze module. De werkgroep neemt aan dat burgers waarde hechten aan 24/7 toegang tot acute zorg inclusief IC geneeskunde. Een te hoge bedbezetting kan deze toegang beperken of verplaatsingen met zich meebrengen buiten het adherentiegebied van het ziekenhuis.
Kosten (middelenbeslag)
Gezien de huidige uitdagingen van ons zorgstelsel rondom bijvoorbeeld de financiering en personele krapte in relatie tot een toename van de zorgvraag is het belangrijk om het stelsel zo efficiënt mogelijk in te richten. Hierin is het de uitdaging om een optimum te vinden in het benutten van de beschikbare middelen (financiële middelen, personeel, IC-afdelingen) en tegelijk de toegang tot IC-zorg 24/7 te borgen. Dit optimum zal voor elke IC-afdeling en desbetreffende ziekenhuis anders zijn.
Binnen een IC-netwerk zal gekeken kunnen worden om dit optimum op netwerkniveau te optimaliseren door intensievere samenwerking. Onder- en overbenutting van middelen zal hierdoor mogelijk kunnen worden voorkomen of worden verminderd.
Aanvaardbaarheid, haalbaarheid en implementatie
Het is voor de werkgroep niet duidelijk op hoeveel IC-afdelingen er sprake is van een hoog bezettingspercentage. Daarnaast spelen er op elke IC specifieke factoren die niet of minder van toepassing zijn op andere IC-afdelingen. Derhalve is er geen goede inschatting te maken in hoeverre de uitvoering van de aanbevelingen haalbaar is. Dit neemt niet weg dat IC-afdelingen binnen de eigen context en organisatie en in samenwerking met het desbetreffende IC-netwerk maatregelen kunnen nemen om te komen tot een optimale afweging tussen de beschikbare opties en deze als zodanig te implementeren. Daar waar mogelijkheden beperkt zijn vanwege personeelsproblemen en/of bouwkundige beperkingen en die niet oplosbaar zijn, kan worden gekeken of verschuiving van IC-zorg binnen het IC-netwerk kan bijdragen aan een duurzame oplossing.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Op basis van de beschikbare literatuur is het niet mogelijk om een aanbeveling te geven over een minimaal bedbezettingspercentage welke nodig is om de kwaliteit van zorg te borgen.
Op basis van de beschikbare literatuur is de bewijskracht voor de gegeven aanbevelingen laag. Vijf van de zes geselecteerde artikelen tonen echter een associatie tussen een hogere bedbezetting en/of minder beschikbare bedden en een verhoogde IC- of ziekenhuismortaliteit, voortijdige overplaatsing naar de verpleegafdeling, vaker overplaatsing naar een ander ziekenhuis, meer heropnames, en meer reanimaties op de verpleegafdeling. Dit is gezien de ervaring in de praktijk een associatie waarbij de relatie met de negatieve uitkomstmaten invoelbaar is en ook te verklaren is. Het bedbezettingspercentage waarbij er een omslagpunt is aan te wijzen waarbij de kwaliteit van zorg duidelijk in het gedrang komt, is lastig aan te geven. Dit zal een range betreffen welk tevens afhankelijk is van het aantal operationele bedden, de weigeringskans, en overige karakteristieken van de specifieke IC-afdeling. De literatuur suggereert een percentage van 80% tot 90% als bovengrens. De werkgroep heeft deze, mede gezien de eigen ervaring, overgenomen.
Onderbouwing
Binnen de Kwaliteitsstandaard Organisatie van Intensive Care 2016 werd gerefereerd aan een minimaal bedbezettingspercentage van 70% in relatie tot afdelingen met 12 of meer IC-bedden. Intensivisten die werken op een afdeling die hier niet aan voldoen dienen in bepaalde situaties te overleggen met een collega intensivist van een afdeling die hier wel aan voldoet. In de standaard inclusief de bijlagen wordt gesuggereerd dat dit overleg ten goede komt aan de kwaliteit van zorg. Binnen de Checklist Zorgbeleidsplan IC-afdelingen in Nederland komt een minimaal bedbezettingspercentage van 70% ook terug in relatie tot de formatie-eisen voor intensivisten en IC-voorwachten.
Uit de Evaluatie Kwaliteitsstandaard Organisatie van de Intensive Care bleek dat er geen consensus was over het nut van de momenten waarop er onderling overleg plaats diende te vinden met de aanbeveling deze kaders te herzien. Dit betreft onder andere onduidelijkheid over het nut van het gebruik van het bedbezettingspercentage, evenals de gehanteerde definitie. Daarnaast is het onduidelijk wat hiervan de functie is; gebruik je het bezettingspercentage als veronderstelde ondergrens van een bepaald kwaliteitsniveau en indien dit het geval is, is er dan ook niet een bepaalde bovengrens waarboven dit eveneens raakt aan de kwaliteit van zorg?
Mortality
|
Very low GRADE |
The evidence is very uncertain about the effect of different bed occupancy rates on mortality when comparing adult patients admitted to the ICU.
Sources: Wilcox, 2020; Iwashyna, 2009 |
Readmissions
|
Very low GRADE |
The evidence is very uncertain about the effect of different bed occupancy rates on readmissions in adult patients admitted to the ICU.
Source: Iwashyna, 2009 |
Complications, patient satisfaction, absenteeism from work, and employee satisfaction
|
No GRADE |
No evidence was found regarding the effect of different bed occupancy rates on complications, patient satisfaction, absenteeism from work, and employee satisfaction in adult patients admitted to the ICU. |
Description of studies
Two studies are included in the analysis of the literature. Additionally, four studies are described in a table without GRADE assessment, as these are non-comparative studies which cannot be graded.
Wilcox (2020) performed a multicentre observational cohort study to determine whether patients admitted to an intensive care unit (ICU) during times of strain, when compared with its own norm (i.e. accommodating a greater number of patients, higher acuity of illness, or frequent turnover), is associated with a higher risk of death in ICUs with closed models of intensivist staffing. ICU capacity strain is defined as a time varying shortfall of resources (e.g. availability of beds, staff, and equipment) when compared with patient demand (e.g. number and complexity of patients). The patient cohort included 142,310 adult patients admitted between January 1, 2015, and December 31, 2016, to 214 adult general ICUs in 213 hospitals. Primary analysis included admissions during the weekday (Monday to Friday) on daytime (08:00 to 19:59). Secondary analysis included ICU admissions during the (1) weekday (all admissions for 24-hr period) and (2) daytime on the weekend. ICU capacity strain was defined in three ways: 1) bed census (i.e. the number of patients), 2) severity-weighted bed census (i.e. the sum of the ICNARCH-2015 risk prediction model estimate of risk of acute hospital mortality for such patients), and (3) activity-weighted bed census (the sum of assigned weights for such patients (determined, a priori, new admissions = 2.0, patients present throughout period of interest = 1.0, patients discharged or identified as ready for discharge = 0.5). For each strain metric, patients were then categorized as having been admitted to ICU during periods of low, typical, and high ICU capacity strain for that ICU, defined by being admitted on that calendar day during daytime hours at least 10% below or above the median value for bed census and activity-weighted bed census (3) or 20% below or above the median value for severity-weighted bed census. The primary outcome was acute hospital mortality, and the secondary outcome was ICU mortality. All patients were followed up until ultimate discharge from acute hospital, whether discharged from acute hospital from the original hospital or from a subsequent acute hospital to which the patient was transferred. The median ICU size was 12 beds (interquartile range 8–16; range 3–65). A previous survey of ICUs participating in the audit identified a median of one fulltime equivalent intensivist for every nine patients (interquartile range, 7–11). The mean patient age was 62 years and 55% were men.
Iwashyna (2009) conducted a multicentre observational cohort study to examine the association of daily ICU occupancy with outcomes of patients admitted to the ICU on that day. Data from patients admitted to ICUs participating in the APACHE clinical information system was obtained for the period between January 2002 through June 2005. Included ICUs were diverse in size, geographic region and teaching status. A total of 200,499 patients from 108 ICUs in 46 hospitals were included in the study. The exposure of interest is the census of each ICU on the day of ICU admission. Census is defined as the total number of patients who spent at least 2 hours in each ICU on the calendar day on which a given patient was admitted. Primary outcomes were in-hospital mortality and discharge to another hospital. Secondary outcome was ICU length of stay. The mean age of the patient group was 61.5 years (SD 17.60). The mean daily census for the included intensive care units (n=108) was 12.8 (median 11, interquartile range 9-15).
Four additional studies (Bagshaw, 2018; Blayney, 2020; Gabler, 2013; Town, 2014) are included and described in a table without GRADE assessment, as these are non-comparative studies which cannot be graded. The results can be found in Table 4.
Results
Mortality
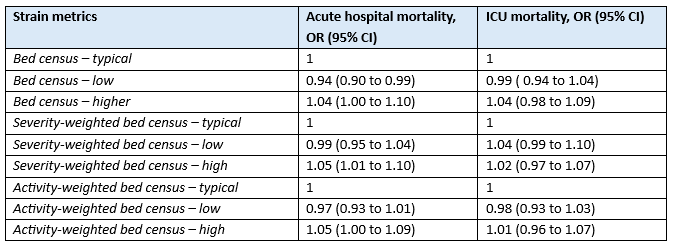
Wilcox (2020) reported acute hospital death and ICU mortality in relation to bed census, severity-weighted bed census, and activity-weighted bed census. Results for daytime hours on weekdays are reported in this section. Results are reported in Table 1 and written out below.
Acute hospital mortality
When calculated by bed census, the adjusted Odds Ratio (OR) for acute hospital mortality was 0.94 (95%CI 0.90 to 0.99) for admission during a period of low ICU capacity strain compared with typical ICU capacity strain. The OR was 1.04 (95%CI 1.00 to 1.10) for admission during a period of high ICU capacity strain compared with typical ICU capacity strain.
When calculated by severity-weighted bed census, the adjusted OR for acute hospital mortality was 0.99 (95%CI 0.95 to 1.04) for admission during a period of low ICU capacity strain compared with typical ICU capacity strain. The OR was 1.05 (95%CI 1.01 to 1.10) for admission during a period of high ICU capacity strain compared with typical ICU capacity strain.
When calculated by activity-weighted bed census, the adjusted OR for acute hospital mortality was 0.97 (95%CI 0.93 to 1.01) for admission during a period of low ICU capacity strain compared with typical ICU capacity strain. The OR was 1.05 (95%CI 1.00 to 1.09) for admission during a period of high ICU capacity strain compared with typical ICU capacity strain.
ICU mortality
When calculated by bed census, the adjusted OR for ICU mortality was 0.99 (95%CI 0.94 to 1.04) for admission during a period of low ICU capacity strain compared with typical ICU capacity strain. The OR was 1.04 (95%CI 0.98 to 1.09) for admission during a period of high ICU capacity strain compared with typical ICU capacity strain.
When calculated by severity-weighted bed census, the adjusted OR for ICU mortality was 1.04 (95%CI 0.99 to 1.10) for admission during a period of low ICU capacity strain compared with typical ICU capacity strain. The OR was 1.02 (95%CI 0.97 to 1.07) for admission during a period of high ICU capacity strain compared with typical ICU capacity strain.
When calculated by activity-weighted bed census, the adjusted OR for ICU mortality was 0.98 (95%CI 0.93 to 1.03) for admission during a period of low ICU capacity strain compared with typical ICU capacity strain. The OR was 1.01 (95%CI 0.96 to 1.07) for admission during a period of high ICU capacity strain compared with typical ICU capacity strain.
Table 1. Logistic regression analyses for the relationship between ICU capacity strain on day of admission and risk-adjusted acute hospital and ICU mortality for weekdays during daytime hours
OR, Odds Ratio; CI, confidence interval
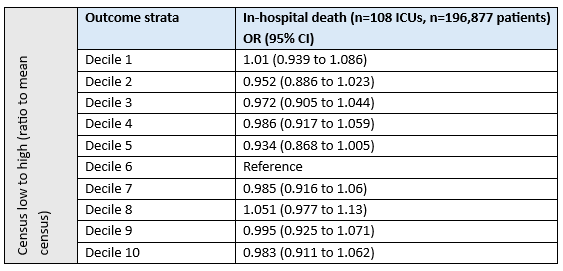
Iwashyna (2009) reported in-hospital mortality after adjustment for differences in predicted inpatient mortality using APACHE IV. The results are reported in Table 2.
Table 2. Effect on in-hospital death of daily census for all patients
OR, Odds Ratio; CI, confidence interval
Readmission
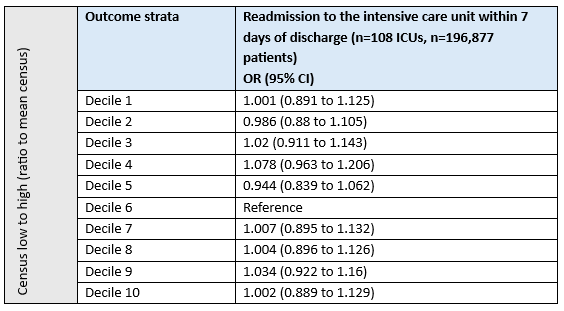
Iwashyna (2009) reported readmission to the intensive care unit within 7 days of discharge. Results are depicted in Table 3.
Table 3. Effect on readmission to the intensive care unit within 7 days of daily census for all patients
Wilcox (2020) did not report readmission.
Complications
Wilcox (2020) and Iwashyna (2009) did not report complications.
Patient satisfaction
Wilcox (2020) and Iwashyna (2009) did not report patient satisfaction.
Absenteeism from work
Wilcox (2020) and Iwashyna (2009) did not report absenteeism from work.
Employee satisfaction
Wilcox (2020) and Iwashyna (2009) did not report employee satisfaction.
Table 4. Non-comparative studies
Level of evidence of the literature
Mortality
The level of evidence regarding the outcome measure mortality was downgraded by two levels to very low because of study limitations in the study of Wilcox et al. (risk of bias, -1); and the confidence intervals around the point estimates crossing either the upper or lower boundary for clinical relevance (imprecision, -1).
Readmission
The level of evidence regarding the outcome measure readmissions was downgraded by two levels to very low because of study limitations (risk of bias, -1); and the confidence intervals around the point estimates crossing either the upper or lower boundary for clinical relevance (imprecision, -1).
Complications, patient satisfaction, absenteeism from work, and employee satisfaction
No study reported these outcome measures, and these could therefore not be graded.
A systematic review of the literature was performed to answer the following question:
What is the influence of bed occupancy percentage X on mortality, readmission, complications, patient satisfaction, absenteeism from work and employee satisfaction when compared with bed occupancy percentage Y in adult patients admitted to the ICU?
| P: | Adult patients admitted to the ICU |
| I: | Bed occupancy percentage X |
| C: | Bed occupancy percentage Y |
| O: | Mortality, readmission, complications, patient satisfaction, absenteeism from work, employee satisfaction |
Relevant outcome measures
The guideline development group considered mortality, readmission and complications as critical outcome measures for decision making; and patient satisfaction, absenteeism from work and employee satisfaction as an important outcome measure for decision making.
A priori, the working group did not define the outcome measures listed above but used the definitions used in the studies.
The working group defined the following minimal clinically (patient) important difference:
- mortality: 0.95 < OR < 1.05;
- readmission: 0.8 < OR < 1.25;
- complications: 0.8 < OR < 1.25;
- patient satisfaction: 10% (e.g. 1 point on a 10-point scale);
- absenteeism from work: 0.8 < OR < 1.25;
- employee satisfaction: 10% (e.g. 1 point on a 10-point scale).
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched for systematic reviews and randomized controlled trials (RCTs) with relevant search terms from 2000 until October 26th, 2023. On January 12th, 2024, the search was updated with observational studies. The detailed search strategy is depicted under the tab Methods. The systematic literature search was combined with the search for the module minimum number of ICU beds and resulted in 1,585 hits. Studies were selected based on the following criteria:
- Systematic review, RCT or observational study;
- comparing bed occupancy percentage X with bed occupancy percentage Y in adult patients admitted to the ICU;
- reporting at least one of the outcomes specified in the PICO;
- published after 2000.
Initially, 18 studies were selected for both modules based on title and abstract screening.
After reading the full text, 12 studies were excluded (see the table with reasons for exclusion under the tab Methods), and 6 studies were included.
Results
Two studies were included in the analysis of the literature and four studies were described in a table without GRADE assessment. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Bagshaw SM, Wang X, Zygun DA, Zuege D, Dodek P, Garland A, Scales DC, Berthiaume L, Faris P, Chen G, Opgenorth D, Stelfox HT. Association between strained capacity and mortality among patients admitted to intensive care: A path-analysis modeling strategy. J Crit Care. 2018 Feb;43:81-87. doi: 10.1016/j.jcrc.2017.08.032. Epub 2017 Aug 24. PMID: 28854400.
- Blayney MC, Donaldson L, Smith P, Wallis C, Cole S, Lone NI; Scottish Intensive Care Society Audit Group. Intensive care unit occupancy and premature discharge rates: A cohort study assessing the reporting of quality indicators. J Crit Care. 2020 Feb;55:100-107. doi: 10.1016/j.jcrc.2019.09.018. Epub 2019 Oct 9. PMID: 31715526.
- Gabler NB, Ratcliffe SJ, Wagner J, Asch DA, Rubenfeld GD, Angus DC, Halpern SD. Mortality among patients admitted to strained intensive care units. Am J Respir Crit Care Med. 2013 Oct 1;188(7):800-6. doi: 10.1164/rccm.201304-0622OC. PMID: 23992449; PMCID: PMC3826272.
- Iwashyna TJ, Kramer AA, Kahn JM. Intensive care unit occupancy and patient outcomes. Crit Care Med. 2009 May;37(5):1545-57. doi: 10.1097/CCM.0b013e31819fe8f8. PMID: 19325466; PMCID: PMC2782597.
- Tierney LT, Conray MC. Optimal occupancy in the ICU: a literature review. Aust Crit Care. 2014 May;27(2):77-84. doi: 10.1016/j.aucc.2013.11.003. PMID: 24373914.
- Town JA, Churpek MM, Yuen TC, Huber MT, Kress JP, Edelson DP. Relationship between ICU bed availability, ICU readmission, and cardiac arrest in the general wards. Crit Care Med. 2014 Sep;42(9):2037-41. doi: 10.1097/CCM.0000000000000401. PMID: 24776607; PMCID: PMC4134732.
- Wilcox ME, Harrison DA, Patel A, Rowan KM. Higher ICU Capacity Strain Is Associated With Increased Acute Mortality in Closed ICUs. Crit Care Med. 2020 May;48(5):709-716. doi: 10.1097/CCM.0000000000004283. PMID: 32141924.
Evidence table for intervention studies
|
Study reference |
Study characteristics |
Patient characteristics 2 |
Intervention (I) |
Comparison / control (C) 3
|
Follow-up |
Outcome measures and effect size 4 |
Comments |
||||||||||||||||||||||||||||||||||||||||||||||
|
Wilcox, 2020 |
Type of study: large, multicenter, observational cohort study
Setting and country: 215 adult general ICUs in 213 hospitals in United Kingdom, Wales, and Northern Ireland
Funding and conflicts of interest: Nothing to declare. |
Inclusion criteria: All participating ICUs are closed, patients are primarily cared for by Anesthetists with specific Critical Care training, and nurses provide one-to-one care to patients. Analyses were restricted to participating ICUs that had submitted a minimum of 1 year’s data within the 2-year study period. Only the first ICU admission in each patient’s hospital stay was included so as to not double count hospital deaths.
Exclusion criteria: missing data (e.g. date and timing of discharge, primary outcome, or all physiologic variables) or death at admission or admitted for organ the sole purpose of organ procurement
N total at baseline: Intervention 1: 38,125 Intervention 2: 68,403 Control: 35,782
Important prognostic factors2: For example age ± SD: I1: 62.9±17.2 I2: 61.9±17.2 C: 62.6±17.2
Sex: I1: 54.9% M I2: 55.3% M C: 54.9% M
Presence of any severe comorbidity, n (%) I1: 7,231 (19.0) I2: 13,426 (19.6) C: 6.385 (17.8)
Groups are comparable at baseline |
Describe intervention (treatment/procedure/test):
Three groups compared: low (intervention 1), typical (intervention 2) or high (control) ICU capacity strain.
The strain metrics used were defined in three ways (1): bed census, (2) severity-weighted bed census, and (3) activity-weighted bed census.
For each strain metric, patients were then categorized as having been admitted to ICU during periods of low, typical, and high ICU capacity strain for that ICU, defined by being admitted on that calendar day during daytime hours at least 10% below or above the median value for bed census (1) and activity-weighted bed census (3) or 20% below or above the median value for severity-weighted bed census (2), where these percentage thresholds were chosen to ensure that approximately 50% of patients fell into each metric’s typical strain category. In this way, low or high ICU capacity strain was estimated relative to the typical ICU capacity strain for each ICU. |
Describe control (treatment/procedure/test):
See intervention description. |
Length of follow-up: Hospital discharge
Loss-to-follow-up: Excluded from the analysis (total): N=19,715 out of 335,703 (5.9%) Reasons: 0.7% admitted before Jan 2015 4.7% readmission within the same acute hospital stay 0.1% dead on admission or organ donation 0.2% missing acute hospital outcome 0.2% missing all physiology
Incomplete outcome data: See above, patients with missing data were excluded
|
Mortality Logistic regression analyses for the relationship between ICU capacity strain on day of admission and risk-adjusted acute hospital and ICU mortality for weekdays during daytime hours:
Readmission Not reported.
Complications Not reported
Patient satisfaction Not reported
Absenteeism from work Not reported
Employee satisfaction Not reported |
Author’s conclusion: In closed staffing models of care, variations in bed census within individual ICUs was associated with patient’s predicted risk of acute hospital mortality, particularly when its standardized bed census consisted of sicker patients.
Limitations: we are unable to provide unit-level data on key organizational covariates such as educational qualifications of nursing staff or experienced strain in the emergency department or ward on the index day of ICU admission or on important outcomes that have been suggested to contribute to mortality during periods of high strain (e.g. provision of deep vein thrombosis prophylaxis or availability of a pharmacist for best possible medication review). Although analyses of the interaction between the effect of strain and acute severity of illness showed no statistically significant heterogeneity, the study was likely to be underpowered to detect such a relationship, and we cannot rule out the potential for endogeneity between severity, capacity strain and mortality |
||||||||||||||||||||||||||||||||||||||||||||||
|
Iwashyna, 2009 |
Type of study: large, multicenter, observational study
Setting and country: 108 ICUs in 46 hospitals in the USA
Funding and conflicts of interest: supported by NIH/NHLBI 5T32HL007891 and K08- HL091249 (to TJI). Dr. Kramer is employed by Cerner Corporation and has stock ownership and stock options in Cerner Corporation, which provides the APACHE data systems used as a basis of the analysis. The remaining authors have not disclosed any potential conflicts of interest |
Inclusion criteria: All patients admitted to APACHE ICUs were eligible for the study
Exclusion criteria: Patients with CABG, and ICUs caring for fewer than 100 patients in the data and the first 100 patients at a site to ensure that our census measures were stable
N total at baseline: Not reported per group. Total: 200,499
Important prognostic factors2: Not reported per group age ± SD (total), y: 61.54±17.60
Sex: Not reported
Acute Physiology Score, median: 34
Groups comparable at baseline? Not compared, only baseline data from total population available |
Describe intervention (treatment/procedure/test):
High census days
Census is defined as the total number of patients who spent at least 2 hours in each ICU on the calendar day on which a given patient was admitted. The mean census of each ICU across the study period was computed. ICU census is analyzed as the ratio of the day-of-admission census to the mean census, divided into deciles.
Mean daily census was12.8 across ICUs, with a median of 11 and an interquartile range of 9–15. There was wide variability in the day-of-admission census. The lowest decile of patients were admitted to ICUs with a census at 65% of their mean daily census; the highest decile of patients were admitted to ICUs operating at 147% of their mean daily census. |
Describe control (treatment/procedure/test):
Low census days
See intervention description |
Length of follow-up: Hospital discharge
Loss-to-follow-up: For length of stay in the ICU, 16,400 patients (total) in eight ICUs were excluded from analysis. Reason: the precise entrance and exit times within a given day are not in the dataset.
Incomplete outcome data: See above
|
Mortality
Readmission
Complications Not reported
Patient satisfaction Not reported
Absenteeism from work Not reported
Employee satisfaction Not reported |
Author’s conclusion: Our results demonstrate that unusually high census on day of admission is not associated with clinically meaningful negative outcomes among critically ill patients across a range of conditions. this implies, but does not yet prove, that patients may be concentrated in high-volume ICUs without overwhelming those ICUs, and without thereby losing the potential benefits of concentration. |
Risk of bias table for interventions studies
|
Author, year |
Selection of participants
Was selection of exposed and non-exposed cohorts drawn from the same population?
|
Exposure
Can we be confident in the assessment of exposure?
|
Outcome of interest
Can we be confident that the outcome of interest was not present at start of study?
|
Confounding-assessment
Can we be confident in the assessment of confounding factors? |
Confounding-analysis
Did the study match exposed and unexposed for all variables that are associated with the outcome of interest or did the statistical analysis adjust for these confounding variables? |
Assessment of outcome
Can we be confident in the assessment of outcome?
|
Follow up
Was the follow up of cohorts adequate? In particular, was outcome data complete or imputed?
|
Co-interventions
Were co-interventions similar between groups?
|
Overall Risk of bias
|
|
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Low, Some concerns, High |
|
|
Wilcox, 2020 |
Probably yes
Reason: All ICU admissions within a 24 hour time frame were identified
|
Probably no
Reason: low or high ICU capacity strain was estimated relative to the typical ICU capacity strain for each ICU |
Definitely yes
Reason: Outcome of interest is hospital mortality, participants were excluded if dead on admission |
Probably yes
Reason: Primary and secondary outcomes were analyzed by multilevel mixed effects logistic regression, with separate models for each strain metric, including random effects for each ICU, and with the following covariates: ICU capacity strain (high and low vs typical), age (linear), sex, severe comorbidities, dependency prior to ICU admission, location prior to ICU admission, urgency (elective/ emergency) of surgery, ICNARC Physiology Score (linear) (10), primary reason for ICU admission (categorized according to the ICNARCH-2015 risk prediction model) (11), and time trend (linear). |
Probably no
Reason: Outcomes were risk adjusted. However, key organizational covariates such as educational qualifications of nursing staff or experienced strain in the emergency department or ward could contribute to mortality, and were not taken into account. |
Probably yes
Reason: Reasons for missing outcome data unlikely to be related to true outcome
|
Definitely yes
Reason: follow up was adequate for all outcomes. Missing data cases were excluded. |
Unclear
|
Some concerns (mortality)
Due to no correction for key organizational confounders |
|
Iwashyna, 2009 |
Probably yes
Reason: All participants were admitted to APACHE ICUs, no further selection made |
Probably no
Reason: Daily census on the day of admission was estimated for each patient and defined in relation to the mean census. |
Definitely yes
Reason: outcome of interest is mortality, and therefore quite certainly not present at start of the study |
Probably yes;
Reason: adjustment for all plausible confounding variables |
Probably yes;
Reason: Quote from method section: “risk adjustment was performed using the APACHE IV risk-adjustment formulae. The risk equations include the day one acute physiology score, age, select chronic health items, primary diagnosis, hospital admission source, pre-ICU length of stay, whether a sedated patient could have his/her Glasgow Coma Score assessed, a patient was receiving invasive mechanical ventilation, and the patient had received emergency surgery.”
However, a lot of data was presented as unadjusted. For readmissions, no information was given as to whether this data was adjusted or not. |
Probably no
Reason: 16,400 patients excluded for length of ICU stay. Not reported in which decile they belong. |
Definitely yes
Reason: follow up was adequate for all outcomes. |
Unclear |
Low (mortality)
Some concerns (readmissions) |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Botros AR, El Razik GM, Alanwer KM, Abd El Salam MM. The association between ICU occupancy rate and each of premature discharge, early readmission, and mortality rate. J Cardiovasc Dis Res. 2021;12(4):476. doi: 10.31838/jcdr.2021.12.04.53 |
Setting not relevant |
|
Esparza. Analysis of the intensive care unit bed occupancy and its relationship with the length of stay of admitted patients. Intensive Care Medicine Experimental. 2019 |
Wrong publication type (meeting abstract) |
|
Holmberg, M. and Steins, K. and Walther, S. M. Does high ICU occupancy have adverse effects on patient outcomes? an observational multicentre study of the relationship between occupancy, length-of-stay and mortality. Intensive Care Medicine. 2013; 39 :S464 |
Wrong publication type (conference paper) |
|
Kim SH, Chan CW, Olivares M, Escobar GJ. Association Among ICU Congestion, ICU Admission Decision, and Patient Outcomes. Crit Care Med. 2016 Oct;44(10):1814-21. doi: 10.1097/CCM.0000000000001850. PMID: 27332046. |
Different study aim/wrong outcome (effect of ICU occupancy on ICU admission) |
|
Mathews KS, Durst MS, Vargas-Torres C, Olson AD, Mazumdar M, Richardson LD. Effect of Emergency Department and ICU Occupancy on Admission Decisions and Outcomes for Critically Ill Patients. Crit Care Med. 2018 May;46(5):720-727. doi: 10.1097/CCM.0000000000002993. PMID: 29384780; PMCID: PMC5899025. |
Different study aim/wrong outcome (effect of ICU occupancy on ICU admission) |
|
Nguyen YL, Wallace DJ, Yordanov Y, Trinquart L, Blomkvist J, Angus DC, Kahn JM, Ravaud P, Guidet B. The Volume-Outcome Relationship in Critical Care: A Systematic Review and Meta-analysis. Chest. 2015 Jul;148(1):79-92. doi: 10.1378/chest.14-2195. PMID: 25927593; PMCID: PMC4493880. |
Wrong topic/comparison (not about occupancy rate) |
|
Robert R, Coudroy R, Ragot S, Lesieur O, Runge I, Souday V, Desachy A, Gouello JP, Hira M, Hamrouni M, Reignier J. Influence of ICU-bed availability on ICU admission decisions. Ann Intensive Care. 2015 Dec;5(1):55. doi: 10.1186/s13613-015-0099-z. Epub 2015 Dec 30. PMID: 26714805; PMCID: PMC4695477. |
Wrong outcome (triage decisions) |
|
Sasabuchi Y, Yasunaga H, Matsui H, Lefor AK, Horiguchi H, Fushimi K, Sanui M. The Volume-Outcome Relationship in Critically Ill Patients in Relation to the ICU-to-Hospital Bed Ratio. Crit Care Med. 2015 Jun;43(6):1239-45. doi: 10.1097/CCM.0000000000000943. PMID: 25756414. |
Wrong topic/comparison (not about occupancy rate) |
|
Stelfox HT, Hemmelgarn BR, Bagshaw SM, Gao S, Doig CJ, Nijssen-Jordan C, Manns B. Intensive care unit bed availability and outcomes for hospitalized patients with sudden clinical deterioration. Arch Intern Med. 2012 Mar 26;172(6):467-74. doi: 10.1001/archinternmed.2011.2315. Epub 2012 Mar 12. PMID: 22412076. |
Wrong population (patients not yet admitted to ICU) |
|
Varney J, Bean N, Mackay M. The self-regulating nature of occupancy in ICUs: stochastic homoeostasis. Health Care Manag Sci. 2019 Dec;22(4):615-634. doi: 10.1007/s10729-018-9448-4. Epub 2018 May 3. PMID: 29725895. |
Wrong study design (simulation study) |
|
Wortel SA, de Keizer NF, Abu-Hanna A, Dongelmans DA, Bakhshi-Raiez F. Number of intensivists per bed is associated with efficiency of Dutch intensive care units. J Crit Care. 2021 Apr;62:223-229. doi: 10.1016/j.jcrc.2020.12.008. Epub 2020 Dec 19. PMID: 33434863. |
Wrong topic/comparison (number of intensivists per bed) |
|
Yergens DW, Ghali WA, Faris PD, Quan H, Jolley RJ, Doig CJ. Assessing the association between occupancy and outcome in critically Ill hospitalized patients with sepsis. BMC Emerg Med. 2015 Oct 19;15:31. doi: 10.1186/s12873-015-0049-y. PMID: 26481448; PMCID: PMC4610044. |
Wrong population (patients not yet admitted to ICU) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 16-10-2025
Beoordeeld op geldigheid : 16-10-2025
Algemene gegevens
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze leidraad is hieronder weergegeven.
De ontwikkeling/herziening van deze module werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de module.
Samenstelling werkgroep
Voor het ontwikkelen van de module is in 2023 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten die zijn opgenomen op de Intensive Care.
Werkgroep
Dr. I.A. (Iwan) Meynaar (voorzitter), internist-intensivist, HagaZiekenhuis, NVIC
Drs. B. (Ben) de Jong, internist-intensivist, Saxenburgh Medisch Centrum, NVIC
Dr. M. (Marieke) Zegers, Associate Professor, Radboudumc, NVIC
Drs. T.C. (Corien) Veenstra, longarts-intensivist, UMCG, NVIC
Dr. J. (Jasper) van Bommel, anesthesioloog-intensivist, Erasmus MC, NVIC
Dr. P. (Peter) van Vliet, neuroloog-intensivist, Haaglanden Medisch Centrum, NVN/NVIC
Dr. G.J. (Jan) Zijlstra, longarts-intensivist, Amsterdam UMC, NVALT
Dr. M.A.M. (Miriam) Moviat, internist-intensivist, Jeroen Bosch Ziekenhuis, NIV
Dr. M.V. (Mark) Koning, anesthesioloog-intensivist, Rijnstate Ziekenhuis, NVA
Drs. R.W.L. (Rens) van de Weyer, cardioloog-intensivist, Elkerliek Ziekenhuis, NVVC
Drs. J.M.R. (Joost) Meijer, chirurg-intensivist, Noordwest Ziekenhuisgroep, NVvH
Drs. L. (Lea) van Duijvenbode-den Dekker, IC verpleegkundige, Amphia Ziekenhuis, V&VN-IC
Dr. W. (Willemke) Stilma (vanaf maart 2024), Hoofddocent en postdoc onderzoeker, Hogeschool van Amsterdam, V&VN-IC
Dr. P.J.T. (Paul) Rood (tot maart 2024), bestuurder V&VN-IC, senior onderzoeker HAN University of applied sciences & Ziekenhuis Rijnstate
Dr. M.M.C. (Margo) van Mol, Assistant Professor, Erasmus MC, FCIC/IC-Connect
Klankbordgroep
Mevr. J.E. (Janine) de Kleijn, MSc, Physician Assistant, Catharina Ziekenhuis, NAPA
Dr. J.M. (Joep) Droogh, intensivist, UMCG, NVIC (namens de transportcommissie)
Dr. D.J. (David) van Westerloo, intensivist, LUMC, NVIC (namens de LHIC)
Drs. C.J.G.M. (Crétien) Jacobs, anesthesioloog-intensivist, Elkerliek Ziekenhuis, NVIC (namens de werkgroep beroepsprofiel intensivisten)
Drs. C. (Coby) Heij, anesthesioloog-intensivist, Spaarne Gasthuis, NVIC (namens de commissie beroepsbelangen intensivisten)
Drs. J. (Jacco) Rozendaal, Verpleegkundig Specialist IC/MC, St. Antonius Ziekenhuis, V&VN-VS
Met dank aan
Dr J. J. Spijkstra, intensivist, AmsterdamUMC (namens de taakgroep formatie)
Drs. A. (Arianne) Doorduin-Schmeets, Unithoofd Intensive Care, Jeroen Bosch Ziekenhuis, ’s-Hertogenbosch (namens het LHIC)
Dhr. F. (Frank) van der Zee, IC verpleegkundige/Avond-nacht-weekend Hoofd, Frisius MC locatie Leeuwarden, Leeuwarden (namens LNICV)
Mw. I. (Iepie) Plagge van der Vliet, manager intensive care en medium care, Martini ziekenhuis, Groningen (namens LHIC)
Dhr. D.R. (Dick) Streefkerk, hoofd IC, Alrijne ziekenhuis, Leiderdorp, namens LHIC
Drs. T. (Toine) Klarenbeek, Intensive Care Verpleegkundige/Klinisch epidemioloog, Maxima medisch centrum, Veldhoven (namens LNICV)
Mevr, L. (Lisette) Epping - Tijdhof, Adviseur Kwaliteit en Veiligheid / niet-praktiserende IC verpleegkundige, Medisch Spectrum Twente, Enschede (namens V&VN IC expertise kwaliteit en veiligheid)
Dhr. R. (Renze) Jongstra, IC-verpleegkundige volwassenen en kinderen, Circulation Practitioner (namens bestuur V&VN-IC)
Met ondersteuning van
Drs. F.M. (Femke) Janssen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Dr. S.N. (Stefanie) Hofstede, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Meynaar, voorzitter |
Intensivist, HagaZiekenhuis |
Bestuurslid Nederlandse Vereniging voor Intensive Care, onbetaald behoudens een onkostenvergoeding, onderzoeker |
Leren van Juiste Diagnoses, door ZonMw gesubsidieerd onderzoek 160.000 euro (inmiddels afgerond 2021-2023)
|
Geen restricties |
|
De Jong |
Internist-intensivist |
- Cliëntenraad Prinses Maxima Centrum (onkostenvergoeding) |
Eenmalige deelname binnen adviesraad voor Paion t.a.v. positionering van giapreza binnen intensive care geneeskunde
|
Geen restricties |
|
Veenstra |
Intensivist
|
Instructeur NVIC bronchoscopie cursus (onbetaald) Lid NVIC commissie pulmonale diagnostiek en interventies (onbetaald) Lid NVIC commissie simulatie (onbetaald) FCCS instructeur (vergoeding wordt overgemaakt naar het UMCG) Medisch visiteur externe kwaliteitsvisitaties NVIC (vergoeding wordt overgemaakt naar het UMCG) Lid Zinnige Zorg traject Zorginstituut VTE (NVIC afgevaardigde, onbetaald) Secretaris sectie IC, NVALT (onbetaald) Lid sectie pulmonale interventies, NVALT (onbetaald) |
Geen |
Geen restricties |
|
Zijlstra |
Longarts-Intensivist, Dijklander Ziekenhuis, betaald |
Geen |
Geen |
Geen restricties |
|
Van Bommel |
Intensivist, Erasmus Medisch Centrum Rotterdam. Werkzaam als staflid op de Intensive Care Volwassenen (betaald). |
Geen |
Geen |
Geen restricties |
|
Meijer |
Chirurg-intensivist bij de Noordwest Ziekenhuisgroep (1,0 FTE) |
Lid toelatingscommissie binnen Noordwestziekenhuisgroep (onbetaald) |
Geen |
Geen restricties |
|
Van Duijvenbode – den Dekker |
IC verpleegkundige, Amphia Ziekenhuis |
Docent Erasmus MC Academie |
Geen |
Geen restricties |
|
Van Mol |
Assistant Professor |
Bestuurslid Stichting FCIC (onbezoldigd) |
1. ZonMw - hoofdonderzoeker van de ICNaVen-studie, ontwikkelen digitale ondersteuning in IC-nazorg voor naasten van een IC-patiënt. Dit is een multicenter studie (nationale en internationale samenwerking) waarbij eerst de behoeften en prioritering wordt verkend en vervolgens een daarop aangepaste interventie wordt ontwikkeld. (Projectleider) 2. ZonMw - hoofdonderzoeker van de DIPIC-studie, een implementatiestudie voor een digitaal dagboek op de IC, als opmaat naar persoonsgerichte zorg. Dit is een multicenter studie in een multi-methods benadering, om het gebruik van een digitaal dagboek op de IC te stimuleren. (Projectleider) 3. ZonMw - Ik ben mede-onderzoeker bij het ontwikkelen van een PGO-IC(na)zorg. Hierbij wordt in co-creatie met verschillende stakholders en Quli een digitale omgeving specifiek ingericht op de voormalig IC-patiënt. Stichting FCIC is penvoerder. (Projectleider) |
Geen restricties |
|
Zegers |
Associate Professor Radboudumc |
Geen |
1. Zorginstituut - Evaluatie van IC Nazorg (Projectleider) 2. ZonMw/NWO- Evaluatie van de kosten-effectivieti van IC-zorg (Projectleider) 3. NFU-Zire (Projectleider) 4. ZonMw - Safety 2 (Projectleider) |
Geen restricties |
|
Koning |
Anesthesioloog-intensivist, Rijnstate Ziekenhuis, Arnhem |
Geen
|
Geen |
Geen restricties |
|
Moviat |
Intensivist Jeroen Bosch ziekenhuis
|
FCCS instructeur
|
Geen |
Geen restricties |
|
Rood (tot 11-03-2024) |
Senior onderzoeker - Projectleider, HAN University of applied sciences |
Vicevoorzitter, V&VN-IC, beroepsvereniging van IC verpleegkundigen |
Ja, NWO Raak SIA |
Geen restricties |
|
Stilma (vanaf 11-03-2024) |
Hogeschool hoofddocent bij cluster verpleegkunde, Hogeschool van Amsterdam, Amsterdam (0,8 FTE) |
Bestuurslid V&VN-IC |
1. NWO - NWO docentenbeurs - promotietraject (Projectleider) 2. KIEM-MV - Circulaire kansen beademingszorg (Projectleider) |
Geen restricties |
|
Van Vliet |
Intensivist / Haaglanden Medisch Centrum |
Bestuursvoorzitter MuzIC (onbetaald) ATLS instructeur (onbetaald) Docent bij de Hogeschool Utrecht bij de PA-opleiding (betaald) |
Geen |
Geen restricties |
|
Weyer |
Cardioloog-intensivist Elkerliek ziekenhuis Helmond |
FCCS instructeur |
Geen |
Geen restricties |
|
De Kleijn |
Physician assistant Intensive care Catharina ziekenhuis Eindhoven |
Commissielid NVIC richtlijnontwikkeling lid NAPA vakgroep intensive care |
Geen |
Geen restricties |
|
Droogh |
Intensivist, UMCG |
Voorzitter commissie transport NVIC, onbetaald Hoofd MICU UMCG |
Geen |
Geen restricties |
|
Van Westeloo |
Intensivist LUMC |
MICU Zuidwest Nederland Eurocross |
Circadiaan onderzoek Philips |
Geen restricties |
|
Jacobs |
Intensivist |
Geen |
Geen |
Geen restricties |
|
Heij |
Intensivist, Spaarne Gasthuis |
Bestuurslid NVIC, onkostenvergoeding Voorzitter cie Beroepsbelangen NVIC Lid ledenraad LAD, onkostenvergoeding |
Geen |
Geen restricties |
|
Rozendaal |
Verpleegkundig Specialist IC/MC |
Docent respiratie en beademing, St. Antoniusacademie (parttime) |
Geen |
Geen restricties |
|
Janssen |
Adviseur Kennisinstituut FMS |
Promovendus UMCU |
Geen |
Geen restricties |
|
Hofstede |
Senior adviseur Kennisinstituut FMS |
Geen |
Geen |
Geen restricties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een afgevaardigde patiëntenvereniging in de werkgroep (FCIC/IC-Connect). De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptleidraad is tevens voor commentaar voorgelegd aan de FCIC/IC-Connect en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de leidraad voerde de werkgroep conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
| Module |
Uitkomst raming |
Toelichting |
|
Optimale bedbezetting |
geen financiële gevolgen |
Aanbeveling is weinig veranderd t.o.v. vorige versie. Het overgrote deel van de IC’s voldoet al aan de norm. |
Werkwijze
Achtergrond voor de herziening
In 2006 is de eerste kwaliteitsstandaard over de organisatie van de intensive care gepubliceerd en in werking getreden (NVA, 2006). In 2016 werd een herziene kwaliteitsstandaard gepubliceerd door het Zorginstituut Nederland (2016). Deze kwaliteitsstandaard werd vanuit de NVIC aangevuld met de zogenaamde blauwdruk (NVIC, 2021). Daaruit werd een visitatie normenkader ontwikkeld, wat deel uit maakt van de feitelijke handhaving en controle op de kwaliteit door de NVIC (NVIC, 2022).
De kwaliteitsstandaard uit 2016 had een looptijd van vijf jaar en moest na vijf jaar worden geëvalueerd en herzien. Door de COVID-19 pandemie kon de evaluatie pas in 2022 plaatsvinden. De NVIC benoemde een werkgroep die de evaluatie uitvoerde door middel van een enquête die werd gevolgd door interviews (NVIC, 2023). Het Kennisinstituut van de Federatie Medisch Specialisten ondersteunde deze evaluatie. In 2023 is gestart met de herziening van de kwaliteitsstandaard. Gezien de organisatorische aard van de uitgangsvragen, wordt de herziene versie een leidraad genoemd. Dit sluit aan bij de beschreven definities in het rapport Medisch Specialistische Richtlijnen 3.0.
Tijdens de voorbereidende fase voor deze herziening inventariseerde de werkgroep middels de evaluatie van kwaliteitsstandaard en een invitational conference de knelpunten met betrekking tot de organisatie van intensive care afdelingen. Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Aan de start van het proces is met de werkgroep besproken hoe de uitgangsvragen onderbouwd kunnen worden. De werkgroep heeft gekozen voor een combinatie van uitgangsvragen met en zonder literatuursearch. Dit vanwege het organisatorische karakter van de leidraad en specifieke situaties die alleen in Nederland van toepassing zijn. Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht. Daar waar de literatuur geen antwoord leverde, werd gebruik gemaakt van expert opinie.
Relevante conceptmodules zijn vóór de commentaar- en autorisatiefase eerst nog langs partijen uit de klankbordgroep gestuurd voor input. Binnen de NVIC en de V&VN betrof het de beroepsbelangen commissie, de visitatiecommissie NKIC, de richtlijncommissie, de werkgroep beroepsprofiel, het landelijk netwerk van ICs, de transportcommissie van de NVIC, de V&VN-IC, de V&VN-VS en de besturen van NVIC en V&VN. Buiten de NVIC betrof het, VPned (de vereniging voor practitioners) en NAPA (Nederlandse Associatie Physician Assistants), de NICE (Nationale Intensive Care Evaluatie), en de LHIC (landelijke IC hoofden overleg).
De conceptleidraadmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Tijdens de commentaarfase heeft tevens een Webinar plaatsgevonden (d.d. 07-01-2025). Naar aanleiding van de commentaren werd de conceptleidraadmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve leidraadmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze.
Zoekverantwoording
Algemene informatie
|
Cluster/richtlijn: NVIC – organisatie van zorg op de IC |
|
|
Uitgangsvraag/modules: 7 Wat is het minimale bedbezettingspercentage en de beddencapaciteit op de IC? |
|
|
Database(s): Embase.com, Ovid/Medline |
Datum: 26-10-2023 |
|
Periode: vanaf 2000 |
Talen: geen restrictie |
|
Literatuurspecialist:Ingeborg van Dusseldorp |
Rayyan review: https://rayyan.ai/reviews/818713 |
|
BMI-zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting: Voor deze vraag is gezocht met de concepten:
IC EN bedbezetting en beddencapaciteit EN volwassenen
Vanwege de hoge aantallen worden in eerste instantie de SRs en RCTs aangeboden. Als daarin niet voldoende bewijs wordt gevonden kunnen de 1031 observationele studies worden toegevoegd.
12-01-2024: De 1031 observationele studies zijn in Rayyan toegevoegd.
De 6 sleutelartikelen worden gevonden met deze search |
|
|
Te gebruiken voor richtlijntekst: In de databases Embase.com en Ovid/Medline is op 26-10-2023 systematisch gezocht vanaf 2000 naar systematische reviews, RCTs en observationele studies over bedbezetting en beddencapaciteit op de IC. De literatuurzoekactie leverde 1585 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SR |
48 |
24 |
58 |
|
RCT |
429 |
128 |
496 |
|
Observationele studies |
847 |
467 |
1031 |
|
Totaal |
1324 |
619 |
1585* |
*in Rayyan
Zoekstrategie
Embase.com
|
No. |
Query |
Results |
|
#1 |
'intensive care'/de OR 'intensive care unit'/exp OR 'artificial feeding'/exp OR 'artificial ventilation'/exp OR 'early goal-directed therapy'/exp OR 'sepsis'/exp OR 'acute respiratory failure'/exp OR 'respiratory tract intubation'/exp OR 'critically ill patient'/exp OR (((intensive OR critical OR medium) NEAR/2 care):ti,ab,kw) OR 'critically ill':ti,ab,kw OR 'acutely ill':ti,ab,kw OR weaning:ti,kw OR (((mechanical* OR artificial) NEAR/2 ventilat*):ti,ab,kw) |
1170582 |
|
#2 |
'hospital bed utilization'/exp OR 'hospital bed capacity'/exp OR (((ratio* OR reduc* OR capacit*) NEAR/3 (bed OR beds)):ti,ab,kw) OR 'occupanc* rate':ti,ab,kw OR 'bed use':ti,ab,kw OR 'bed utiliz*':ti,ab,kw OR 'bed occupanc*':ti,ab,kw |
29752 |
|
#3 |
#1 AND #2 |
3386 |
|
#4 |
#3 AND [2000-2024]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) NOT (('child'/exp OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw)) |
1677 |
|
#5 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
971882 |
|
#6 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
3899806 |
|
#7 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
7896434 |
|
#8 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
14520192 |
|
#9 |
#4 AND #5 SR |
48 |
|
#10 |
#3 AND #6 NOT #9 Clinical trials |
429 |
|
#11 |
(#7 OR #8) AND #4 NOT #9 NOT #10 OBS |
847 |
|
#12 |
#9 OR #10 OR #11 |
1324 |
|
#13 |
'a mathematical model for simulating daily bed occupancy in an intensive care unit' |
1 |
|
#14 |
'the relationship between labour cost per patient and the size of intensive care units: a multicentre prospective study' |
1 |
|
#15 |
volume AND of AND activity AND occupancy AND rate AND in AND intensive AND care AND units. AND association AND with AND mortality |
1 |
|
#16 |
'rationing critical care beds: a systematic review' |
1 |
|
#17 |
'evaluation of icus and weight of quality control indicators: an exploratory study based on chinese icu quality data from 2015 to 2020' |
1 |
|
#18 |
#13 OR #14 OR #15 OR #16 OR #17 sleutelartikelen |
5 |
|
#19 |
#12 AND #18 sleutelartikelen gevonden |
5 |
Ovid/Medline
|
# |
Searches |
Results |
|
1 |
Critical Care/ or Critical Illness/ or Early Goal-Directed Therapy/ or exp Intensive Care Units/ or exp Sepsis/ or exp Respiratory Distress Syndrome/ or exp Respiration, Artificial/ or exp Intubation, Intratracheal/ or Ventilator Weaning/ or weaning.ti,ab,kf. or ((intensive or critical) adj2 care).ti,ab,kf. or critically ill.ti,ab,kf. or acutely ill.ti,ab,kf. or (mechanical*or artificial adj2 ventilat*).ti,ab,kf. or intubat*.ti,ab,kf. |
628749 |
|
2 |
exp bed occupancy/ or exp Hospital Bed Capacity/ or "bed occupanc*".ti,ab,kf. or "occupanc* rate".ti,ab,kf. or "bed use".ti,ab,kf. or "bed utiliz*".ti,ab,kf. or ((ratio* or reduc*) adj3 (bed or beds)).ti,ab,kf. |
29658 |
|
3 |
1 and 2 |
2345 |
|
4 |
limit 3 to yr="2000 -Current" |
1294 |
|
5 |
4 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) not ((Adolescent/ or Child/ or Infant/ or adolescen*.ti,ab,kf. or child*.ti,ab,kf. or schoolchild*.ti,ab,kf. or infant*.ti,ab,kf. or girl*.ti,ab,kf. or boy*.ti,ab,kf. or teen.ti,ab,kf. or teens.ti,ab,kf. or teenager*.ti,ab,kf. or youth*.ti,ab,kf. or pediatr*.ti,ab,kf. or paediatr*.ti,ab,kf. or puber*.ti,ab,kf.) not (Adult/ or adult*.ti,ab,kf. or man.ti,ab,kf. or men.ti,ab,kf. or woman.ti,ab,kf. or women.ti,ab,kf.)) |
1072 |
|
6 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
701591 |
|
7 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2646651 |
|
8 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] |
4560645 |
|
9 |
Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) |
5537929 |
|
10 |
5 and 6 SR |
24 |
|
11 |
(5 and 7) not 10 Clinical trials |
128 |
|
12 |
(5 and (8 or 9)) not 10 not 11 OBS |
467 |
|
13 |
10 or 11 or 12 |
619 |