Baked Milk (hoogverhitte melk)
Uitgangsvraag
Bij welke kinderen kan bij voorbaat baked milk (= hoogverhitte melk) worden ontraden (i.e. bij welke kinderen bied je geen baked milk provocatie aan)?
Aanbeveling
De consumptie van baked milk (hoogverhitte melk) kan niet worden aanbevolen of ontraden zonder het verrichten van een provocatie.
Bied een provocatie met hoogverhitte melk aan bij kinderen met een bewezen IgE-gemedieerde koemelkallergie, om mogelijke uitbreiding van het dieet te kunnen realiseren. Neem wat betreft de timing hiervan de dosis waarop is gereageerd (‘drempelwaarde’), de leeftijd van het kind, en de hoogte van sensibilisatie mee in de afweging, alsmede de wensen van (de ouders van) het kind.
Bied kinderen met een IgE-gemedieerde koemelkallergie met een recente reactie op onverhitte koemelk, een provocatie aan met hoogverhitte melk.
Betrek een diëtist bij het vermijden of introduceren van koemelk.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
In de richtlijn worden de definities voor verschillende vormen van melk, waaronder baked milk/hoogverhitte melk, gehanteerd volgens tabel 1 in de module Blootstelling kleine hoeveelheden.
Op basis van de systematische literatuursearch is er geen gevalideerd predictiemodel gevonden dat specifiek een reactie op hoogverhitte melk kan voorspellen bij kinderen met een IgE-gemedieerde koemelk allergie (KMA). Hoewel zes cohortstudies verschillende risicofactoren hebben onderzocht die mogelijk geassocieerd zijn met reacties op hoogverhitte melk, vertoonden deze studies diverse methodologische beperkingen, waaronder een hoog risico op bias. Een overzicht van deze studies is te vinden in Tabel 1 (in de bijlage). De belangrijkste gerapporteerde risicofactoren waren: (1) verhoogde serum IgE-niveaus (specifiek voor caseïne en koemelk) en (2) hoeveelheid koemelk die werd geconsumeerd tijdens een orale voedselprovocatie met gepasteuriseerde koemelk.
Vanwege deze beperkingen kunnen er geen definitieve conclusies worden getrokken uit de beschikbare studies. Dit benadrukt de behoefte aan verder onderzoek met robuustere methodologieën om voorspellende modellen te ontwikkelen die klinisch bruikbaar zijn.
Er bestaat een correlatie tussen een hogere IgE-waarde en een verhoogd risico op een allergische reactie, zowel bij koemelk als bij caseïne, zoals vaak het geval is bij voedselallergieën. Daarnaast blijkt uit de studies dat een hoge drempelwaarde bij een provocatietest met gepasteuriseerde koemelk de kans vergroot dat een kind ook hoogverhitte melk goed verdraagt. Deze bevindingen bieden echter weinig praktische houvast, aangezien er geen eenduidige afkapwaarde bestaat die voorspelt bij welke sIgE-waarde (koemelk of componenten) of hoeveelheid gepasteuriseerde koemelk een kind met zekerheid zal reageren op hoogverhitte melk, of wanneer het zonder klachten kan worden verdagen.
We kunnen niet met zekerheid aangeven bij welke kinderen hoogverhitte melk vooraf ontraden moet worden, omdat de bestaande studies onvoldoende informatie bieden om dit op basis van IgE-waarden of andere factoren te voorspellen. Een provocatietest met hoogverhitte melk blijft daarom noodzakelijk om te bepalen of het veilig is voor een kind om deze te consumeren.
Een recente studie (d’Art, 2022) toont aan dat begeleide en geleidelijke introductie van hoogverhitte melk direct na de diagnose van koemelkallergie bij kinderen <12 maanden effectief kan zijn voor het opbouwen van tolerantie. Deze kinderen kregen echter ook gepasteuriseerde melkproducten via de melkladder. Een gecontroleerde introductie van hoogverhitte melk in een klinische setting kan thuisintroductie versnellen, het vertrouwen van ouders vergroten en het veiliger maken voor bepaalde kinderen. Dit ondersteunt de wenselijkheid van begeleiding van thuisintroductie door arts en diëtist.
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
Het is wenselijk dat de beslissing om blootstelling aan hoogverhitte melk koemelk te proberen, wordt genomen in overleg met het kind en diens ouders of verzorgers. De voordelen en risico’s van blootstelling kunnen variëren per individu en vereisen persoonlijke afwegingen. De behandelaar moet duidelijke informatie verstrekken over de mogelijke uitkomsten en risico’s, zodat het kind en de ouders/verzorgers een goed geïnformeerde beslissing kunnen nemen. De mening van het kind en ouders/verzorgers is hierbij van groot belang. Bovendien blijft er altijd een risico op allergische reacties bij het introduceren van hoogverhitte melk als het kind allergisch is voor koemelk in een andere vorm. Het niet naleven van afspraken of therapie-ontrouw kan gevaarlijk zijn en moet daarom ook worden meegenomen in de overweging om hoogverhitte melk al dan niet te introduceren.
De voordelen van de introductie van hoogverhitte melk voor kind en ouders zijn:
- Uitbreiding van het dieet; mogelijkheid om hoogverhitte melk in de voeding op te nemen, wat voedingskeuzes verruimt en gemak biedt
- Potentiële tolerantieontwikkeling; bij sommige kinderen kan blootstelling aan hoogverhitte melk bijdragen aan het ontwikkelen van tolerantie voor koemelk
De nadelen van de diagnostische procedure voor het kind zijn:
- Risico op allergische reacties: mogelijk acute allergische reacties, variërend van mild tot ernstig. Zowel bij de provocaties, als bij thuisintroductie van de hoogverhitte melk.
- Stress en angst; mogelijk emotionele belasting voor zowel het kind als ouders/verzorgers tijdens de provocatietesten. Hiervoor is een gedegen kennis bij ouders/verzorgers nodig over welke producten wel en niet toegestaan zijn.
De waarde die aan deze voor- en nadelen wordt gehecht, kan sterk variëren tussen patiënten en ouders/verzorgers. Ouders van kinderen die in het verleden ernstige allergische reacties hebben gehad, kunnen meer terughoudend zijn en veiligheid hoger waarderen. Ouders van jonge kinderen kunnen voorzichtiger zijn vanwege de kwetsbaarheid van hun kind, terwijl ouders van oudere kinderen misschien meer bereid zijn om risico’s te nemen en de voordelen van een uitgebreid dieet en mogelijke tolerantieontwikkeling hoger waarderen. Kinderen en ouders/verzorgers die eerder positieve of negatieve ervaringen hebben gehad met koemelk kunnen hun voorkeuren daarop baseren.
Het is van belang om alle hierboven genoemde voor- en nadelen, waarden en voorkeuren grondig te overwegen voordat een beslissing wordt genomen in samenspraak met het kind en ouders/verzorgers. Dit draagt bij aan het verminderen van het risico op allergische reacties en het bevorderen van therapietrouw en mogelijke tolerantieontwikkeling.
Kosten (middelenbeslag)
Het ontraden van koemelk en hoogverhitte melk kost in principe geen geld: de dieetkosten zijn beperkt omdat er voldoende koemelkvrije of veganistische alternatieven zijn. Het kunnen consumeren van hoogverhitte melk (bijvoorbeeld in gebakken producten) draagt wel sterk bij aan de kwaliteit van leven. Om dat te kunnen adviseren, moet echter een provocatie plaatsvinden – er komt namelijk niet goed uit de literatuur naar voren wanneer je, op basis van andere factoren, het consumeren van hoogverhitte melk moet ontraden. Een provocatie is duur omdat een dagopname vereist is, voorbereiding nodig is en de inzet van gespecialiseerd personeel nodig is. Daarom is het essentieel om provocaties op het juiste moment in te zetten om onnodige zorgkosten te voorkomen.
Aanvaardbaarheid, haalbaarheid en implementatie
Provocaties met hoogverhitte melk (baked milk) als onderdeel van de diagnostiek en behandeling van koemelk allergie zijn niet in alle medische centra standaard beschikbaar. Dit komt omdat:
- Er strenge criteria zijn rondom de uitvoering van provocaties (zie richtlijn Voedselprovocatie): de patiënt moet continu gemonitord worden tijdens en na de test, en eventuele allergische reacties moeten opgevangen kunnen worden. Hiermee wordt de betrouwbaarheid van de test en de veiligheid van de patiënt gewaarborgd
- Expertise nodig is voor het stellen van de juiste indicaties en het geven van adviezen voor het dagelijks dieet. Hiervoor is de betrokkenheid van allergie-kinderdiëtist noodzakelijk
Verder bestaan er uitdagingen rondom de praktische uitvoerbaarheid: Als er eerst een provocatie met gepasteuriseerde koemelk wordt uitgevoerd, gevolgd door een provocatie met hoogverhitte melk, kan dit leiden tot een dubbele belasting voor zowel het kind als de zorgverleners, aangezien er twee keer een provocatie moet worden uitgevoerd. Hoewel dit vaak niet te vermijden is, moet de juiste indicatie dus aanwezig zijn, en deze afweging vooraf zorgvuldig worden gemaakt op basis van de juiste kennis en wetenschappelijke inzichten.
Daarnaast is er op dit moment weinig standaardisatie van praktijken en is er geen onderlinge uniformiteit in de uitvoering van hoogverhitte melk provocaties. Om nauwkeurige hoeveelheden hoogverhitte melk aan te kunnen bieden zijn verschillende recepten beschikbaar (zie de bijlage bij Module Blootstelling aan kleine hoeveelheden). Het ontwikkelen van verdere gestandaardiseerde protocollen en richtlijnen, gebaseerd op de beste beschikbare gegevens, zal helpen om praktijkvariatie te minimaliseren en de veiligheid en effectiviteit van deze provocaties te vergroten. In de huidige praktijk verdient het de voorkeur om het provocatieproduct af te stemmen met ouders, zodat het past bij de voorkeuren voor het dieet thuis.
Het betrekken van een diëtist, bij voorkeur een diëtist die aangesloten is bij DAVO (Diëtisten Alliantie Voedselovergevoeligheid), is essentieel bij het vermijden of introduceren van koemelk, in alle vormen, voor kinderen met een IgE-gemedieerde koemelkallergie. De expertise van de diëtist is cruciaal om het risico op allergische reacties te minimaliseren en om een veilige en verantwoorde zorgomgeving te creëren in de thuissituatie. Door gepersonaliseerde begeleiding te bieden bij de introductie van koemelkproducten, kan de diëtist niet alleen helpen bij het bepalen van een veilige aanpak, maar ook ouders ondersteunen in het verkrijgen van vertrouwen en het juist toepassen van de voorgestelde voedingsinterventies. Dit zorgt ervoor dat de zorg zowel effectief als veilig is voor het kind.
Rationale van de aanbeveling: weging van argumenten voor en tegen de diagnostische procedure
Gezien het ontbreken van gevalideerde predictiemodellen, wordt aanbevolen om klinische beslissingen te baseren op een combinatie van individuele risicofactoren, zoals de leeftijd van het kind, verhoogd serum IgE-niveaus voor caseïne en koemelk en de hoeveelheid koemelk geconsumeerd tijdens eerdere reacties of provocaties. Elk kind met een koemelkallergie zal individueel beoordeeld moeten worden, waarbij rekening wordt gehouden met de beschikbare klinische gegevens en risicofactoren. Dit kan helpen om te bepalen of een hoogverhitte melk provocatie passend is, vooral in gevallen waarin fors verhoogde sIgE-niveaus zijn gedetecteerd. Uiteraard moet hierbij aansluiting worden gezocht met de wensen van (ouders van) het kind. De werkgroep redeneert dat er vooralsnog weinig evidentie is gevonden om een hoogverhitte melk provocatie af te raden voor kinderen met een koemelk allergie en een positieve provocatie of allergische reactie op laag verhitte koemelk.
Onderbouwing
The severity of allergic reactions to cow’s milk allergy depends on different factors, for example the amount of cow’s milk ingested but also on the degree of food processing. See table 1 in the module Blootstelling aan kleine hoeveelheden. Heating can denature or change the protein structures, which makes these proteins less allergenic. Some children with a cow’s milk allergy tolerate cow’s milk when extensively heated in the oven in a matrix of grain for a certain time (so called ‘baked milk’), but still experience allergic complaints after consuming unheated cow’s milk. But not all cow’s milk allergic children can tolerate baked milk. Therefore, it is important to identify risk factors and signals which may advise against the consumption of baked milk. In other words, is it possible to predict which children will have an allergic reaction after ingestion of baked milk?
|
No GRADE |
No validated prediction models were found to determine in which children baked milk provocation can be discouraged. Source: - |
Description of studies
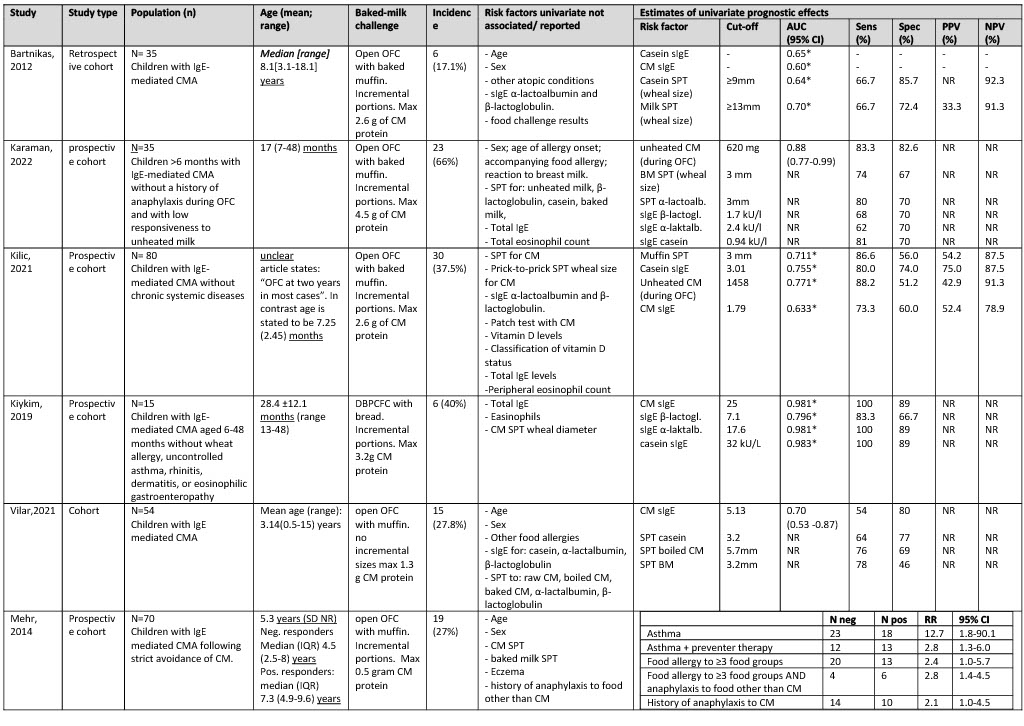
Of the six included studies, five studies retrospectively reviewed the results of open baked milk challenges in a pediatric clinic using muffins and one study (Kiykim, 2019) reported results of a double blind, placebo-controlled food challenge with baked milk using bread. Studies included 35 to 80 children, median ages ranging from 1.4 years (17 months) to 5.3 years. Positive response to the food challenges was defined as clinical (objective) symptoms during the food challenge. However, follow-up time for symptoms differed between studies. The study by Mehr (2014) assigned children with symptoms >2 hours after the challenge to the non-responder groups, whereas the study by Bartnikas (2012) assigned children who passed a challenge but had an allergic reaction to baked milk at home afterwards, to the responder group. Study characteristics are presented in Table 1.
Incidence of reaction to baked milk differed from 17.1% (Bartnikas, 2012) to 66% (Karaman, 2022).
All studies reported on the predictor skin prick testing. Five out of six studies reported on sIgE levels to cow’s milk, casein, α-lactoalbumin and β-lactoglobulin. The study by Mehr (2014) did not report on these values but reported on several specific atopic conditions and their risk ratio. Three studies reported on food allergy and general other atopic conditions (Bartnikas, 2021; Karaman, 2022; Mehr, 2014). Total IgE-levels and eosinophil count were also reported in three studies (Karaman, 2022; Kilic, 2021; Kiykim, 2019). Results of the univariate analyses of the predictive factors are reported in Table 1.
OFC – Oral Food Challenge, SPT – Skin Prick Test, AUC – Area Under the Curve, CMA - cow’s milk allergy, CM - cow’s milk, nr – not reported, DBPCFC – double blind placebo-controlled food challenge, PPV-positive predictive values, NPV-negative predictive value, RR – risk ratio, * no CI reported , BM -baked milk
Level of evidence of the literature
No level of evidence could be determined as no studies were included in this literature analysis that reported multivariate models predicting outcome of a baked-milk food challenge in children with IgE-mediated cow’s milk allergy.
No GRADE assessment was performed for the studies from the pragmatic selection, as none met all the elements of the PICO.
A systematic review of the literature was performed to answer the following question:
In which children can baked milk provocation be discouraged (i.e. which factors predict a reaction to baked milk in children?)?
| Patients: | Children with IgE-mediated cow’s milk allergy |
| Intervention: | (Model with) risk factors for a reaction to baked milk (e.g. age, sensibilisation profile/components (blood or skin prick test (SPT)), eczema, other food allergies, atopy, duration of allergy, difference in reaction (mild/serious/anaphylaxis and symptoms: skin reaction, dyspnoea, angio-oedema), Sampson criteria) |
| Comparison: | None, or a model without predetermined risk factors |
| Outcomes: |
Performance of the model (in case of prediction model studies: Area under the ROC-curve, calibration), or a reaction to baked milk (in case of risk factor studies) Timing and setting: use of prediction model before or during contact with medical specialist for follow-up in disease course |
Relevant outcome measures
The guideline development group considered area under the curve or assessed predictive value as a critical outcome measure for decision making.
The working group defined the performance of the included models as follows:
- 0.7≤AUC<0.8: acceptable,
- 0.8≤AUC<0.9: excellent,
- AUC≥0.9: outstanding.
The working group defined a 25% difference for dichotomous outcomes (0.8 ≥ RR ≥ 1.25), as a minimal clinically (patient) important difference.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until November 6th, 2023. The detailed search strategy is available upon request. The systematic literature search resulted in 24 hits. Studies were selected based on the following criteria:
- Including only children with IgE-mediated cow’s milk allergy;
- Reporting clinical prediction rules, prospective multivariable models or prediction models with allergic reaction to baked milk as dependent variable and risk factors (as defined in PICO) as independent variables;
- Studies were in English.
No studies were initially selected based on title and abstract screening, because of the lack of prediction rules and models. Therefore, a pragmatic selection of observational studies focusing on univariate association between risk factors and a reaction to baked milk was performed based on the following criteria:
- Reporting of logistic regression parameters or Risk or Odd ratios
Ten studies were then selected based on title and abstract screening. After reading the full text, 4 studies were excluded (see the table with reasons for exclusion under the heading Evidence tables), and 6 studies were included.
Results
Six studies were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the table of quality assessment.
- Bartnikas, L. M., Sheehan, W. J., Hoffman, E. B., Permaul, P., Dioun, A. F., Friedlander, J., Baxi, S. N., Schneider, L. C., & Phipatanakul, W. (2012). Predicting food challenge outcomes for baked milk: role of specific IgE and skin prick testing. Annals of allergy, asthma & immunology : official publication of the American College of Allergy, Asthma, & Immunology, 109(5), 309–313.e1. https://doi.org/10.1016/j.anai.2012.07.026
- d'Art YM, Forristal L, Byrne AM, Fitzsimons J, van Ree R, DunnGalvin A, Hourihane JO. Single low-dose exposure to cow's milk at diagnosis accelerates cow's milk allergic infants' progress on a milk ladder programme. Allergy. 2022 Sep;77(9):2760-2769. doi: 10.1111/all.15312. Epub 2022 Apr 22. PMID: 35403213; PMCID: PMC9543429.
- Karaman, S., Erdem, S. B., Nacaroğlu, H. T., Karkiner, C. Ş., & Can, D. (2022). The quantity of unheated milk tolerated as a predictor of tolerance to baked milk. Asian Pacific journal of allergy and immunology, 40(4), 353–358. https://doi.org/10.12932/AP-280419-0549
- Kilic, M., Çilkol, L., & Taşkın, E. (2021). Evaluation of some predictive parameters for baked-milk tolerance in children with cow's milk allergy. Allergologia et immunopathologia, 49(2), 53–59. https://doi.org/10.15586/aei.v49i2.64
- Mehr, S., Turner, P. J., Joshi, P., Wong, M., & Campbell, D. E. (2014). Safety and clinical predictors of reacting to extensively heated cow's milk challenge in cow's milk-allergic children. Annals of allergy, asthma & immunology : official publication of the American College of Allergy, Asthma, & Immunology, 113(4), 425–429. https://doi.org/10.1016/j.anai.2014.06.023
- Kiykim, A., Karakoc-Aydiner, E., Gunes, E., Nain, E., Ogulur, I., Yazici, D., Aktac, S., Bicer, A. H., Sackesen, C., Baris, S., & Ozen, A. (2019). Evaluation of a Standardized Bakery Product (SUTMEK) as a Potential Tool for Baked-Milk Tolerance and Immunotherapy Research Studies. International archives of allergy and immunology, 178(1), 1–9. https://doi.org/10.1159/000492824
- Vilar, L. K., Araújo, F. A., Santos, T. P., Menezes, T. T., Cheik, M. F., & Segundo, G. R. S. (2021). Baked Tolerance in Cow's Milk Allergy: Quite Frequent, Hard to Predict!. International archives of allergy and immunology, 182(4), 319–323. https://doi.org/10.1159/000511148
|
Study reference |
Study characteristics |
Patient characteristics |
Prognostic factor(s) |
Type of OFC and outcome |
Outcome measure and effect size |
Comments |
||
|
Bartnikas, 2012 |
Type of study retrospective review
Setting one centre in the United States.
Funding and conflicts of interest: First author is supported by the American Academy of Allergy, Asthma and Immunolgy. Research supported by a grant of the NIH. |
Inclusion criteria: *History of prior allergic reactions to milk (baked / unheated) AND *a positive SPT result (>3mm larger than negative control) OR elevated serum sIgE level.
Exclusion criteria: None stated
Participants: N= 35
Median age [range]: 8.1 [3.1-18.1] I: 3.7 [31.-11.0] C: 8.9 [3.9-18.1]
% male: 71% I: 69% | C: 83% |
Prognostic factor(s) and method of measurement: - Age - Sex - other atopic conditions (asthma, atopic dermatitis, ARC, Other food allergies)
- SPT to milk, wheal size - SPT to casein, wheal size SPT measured 3 [0.82-32.0] months before OFC - sIgE levels to milk, casein α-lactoalbumin and/or β-lactoglobulin. sIgE Measured 3.1[1.15-34.6] months before OFC manufacturer: Phadia
- food challenge results |
Intervention Baked Milk Challenge Open challenge. Muffins with graded increments in ingestion. Totaling max 2.6 g of milk protein. Monitoring until 30-60min after challenge. Failed when any reaction to baked milk during or after (up to 10 months) after OFC.
Missing data: SPT to casein wheal size n =1 (2.9% missing) sigE to casein, α-lactoalbumin and/or β-lactoglobulin n=2(5.7%) missing.
Reasons for incomplete outcome data described? Not described. |
Outcome OFC 6/35 (17.1%) positive OFC= (reactivity to baked milk OFC) *
sIgE - Casein AUC: 0.56 - CM AUC: 0.60
SPT wheal diameter - Casein ≥9mm AUC: 0.64, sensitivity: 66.7%, specificity 85.7% - CM ≥13mm AUC: 0.70, sensitivity: 66.7%, specificity: 72.4%
|
*3 of the pt classified as failed, did not fail during the clinical challenge but later, up to 10 months.
|
||
|
Karaman, 2022
|
Type of study: January 2015 to January 2016 – prospective?
Setting Department of Pediatric Allergy – Childresne Hospital - Turkey
Funding and conflicts of interest: None declared. |
Inclusion criteria: - History of suspicion for IgE mediated CMA - open OFC testing - SPT and ssIgE below cut-off point (≤ 5kU/L and ≤ 6mm) - CMA confirmed by positive oral challenge after 4 weeks of abstinence. - age >6 months
Exclusion criteria: History of anaphylaxis during OFC
N=35
Mean age ± SD: 17 (7-48) months
Sex: n= 23 (65.7%) M
|
Prognostic factor(s) and method of measurement: - age - gender (sex) - accompanying food allergies - patients reactivity following mothers consumption of milk or dairy products - Total eosinophil count, total igE, ssigE (for cow’s milk, β-lactoglobulin, casein, α-lactoalbumin) manufacturer: Phadia -Prick-to-prick diameter (unheated milk, baked milk) - SPT wheal diameter (for unheated milk, baked milk, β-lactoglobulin, casein, α-lactoalbumin) - The amount of milk ingested before the development of reaction during OFC with unheated milk
Data derived from patient history All measured prior to OFC. |
open OFC for baked milk Min 3 mg, to 3 g of protein. Max 4,5 gr of milk protein.
Observation for at least 4 hours after OFC. Positive test: Any symptom (skin, gastrointestinal, respiratory, cardiovascular).
For how many participants were no complete outcome data available? N (%):0 Reasons for incomplete outcome data described? One case excluded before trial due to anaphylaxis during OFC. |
Outcome OFC 23/35 (66%) positive OFC (= reactivity to baked milk)
OFC unheated milk - amount of ingested unheated milk during OFC ≥ 620mg; AUC (95%CI): 0.88 (0.77-0.99), sensitivity: 83.3%, specificity: 82.6%
|
Patients with high reactivity to SPT and high sIgE are excluded from this trial, decreasing generalizability of the results.
Authors conclusion: “During OFC testing for suspicion of milk allergy, the amount of unheated milk protein that is tolerated by the patient until the development of reaction may be used as a marker to predict tolerance to baked milk. In addition, baked milk products can be given more safely in case milk protein-specific IgE levels are low.” |
||
|
Kilic, 2021 |
Type of study: Prospective follow-up
Setting and country: Hospital based outpatients center in Turkey
Funding and conflicts of interest: None disclosed |
Inclusion criteria: - diagnosed with IgE-mediated CMA:
- positive OFC test with unheated milk OR - a history of an allergic reaction to CM <six months AND - sIgE levels ≤2 years, ≥5 kUA/L | >2 years, ≥15 kUA/L OR SPT wheal diam ≤2 years, ≥6 mm | >2 years, ≥8 mm)
Exclusion criteria - chronic systemic diseases
N= 80
Age = unclear article states: OFC at “at least one year old, (two year in most cases)”. But age of group is stated to be 7.25 ± 2.45 range (3–13) months
% male: I: 53% | C: 64% |
Prognostic factor(s) and method of measurement: Derived from patient history - SPT wheel diameter, - prick-to-prick SPT wheal size for CM test, sIgE (for CM, β-lactoglobulin, casein, α-lactoalbumin) manufacturer n.r. - allergen patch test, and OFC test prior to OFC for baked milk. - Atopy patch tests with native food allergens
Unclear how much time between measurement of predictor and OFC. |
open OFC for baked milk Baked muffin, following EAACI guidelines. 15 min interval, incremental portions. Maximum 2.6 g of milk protein.
For how many participants were no complete outcome data available? Not reported
Reasons for incomplete outcome data described? Not reported |
Outcome OFC 30/80 (37.5%) positive OFC (=reactivity to baked milk)
OFC unheated milk - amount of ingested unheated milk during OFC ≥ 458mg;
SPT wheel diameter - muffin 3mm AUC (95%CI): 0.88 (0.77-0.99), sensitivity: 86.6%, specificity:56.0%
sIgE - casein ≥ 3.01 AUC: 0.711, sensitivity: 86.6%, specificity 84.0%, PPV 75%, NPV 87.5%. - CM ≥ 5.77 AUC: 0.633, sensitivity: 73.3%, specificity: 60.0%, PPV 52.4%, NPV 78.9%
|
|
||
Kiykim, 2019 |
Type of study: Prospective cohort
Setting and country: Peadiatric allergy clinic of a university in Turkey.
Funding and conflicts of interest: Funding by: Marmara University Scientific Research Committee. The study names a brand of “bakery tools” with baked milk that could be used for immunotherapy. |
Inclusion criteria: - age 6-48 months - IgE-mediated CMA according to EAACI guidelines. - positive skin prick test and/or sIgE
Exclusion criteria: - wheat protein allergy - uncontrolled asthma, rhinitis, dermatitis, eosinophilic gastroenteropathy - history of reaction to baked-milk < 6 months
N= 15
Mean age ± SD*: 28.4±12.1 months (range 13-48 months)
% Male*: 46.7% |
Prognostic factor(s) and method of measurement:
- Total IgE - Easinophils - CM SPT wheal diameter - sIgE (for CM, β-lactoglobulin, casein, α-lactoalbumin) manufacturer: IMMULITE system.
Unclear when the SPT and (s)IgE measures were carried out.
|
OFC Before baked-milk: DBPCFC with unheated CM. DBPCFC by bread (with and without baked milk) produced in a factory. 4 incremental portions, max total 3.2 g of milk protein. Monitoring for at least 2 hours after final dose. No symptoms : tolerant to heated milk.
For how many participants were no complete outcome data available? N (%): Not reported
Reasons for incomplete outcome data described? Not reported |
Outcome OFC 6/15 (40%) positive DBPCFC (=reactive to baked milk)
sIgE - CM ≥ 25 kU/L AUC: 0.981, sensitivity: 100%, specificity 89% - casein ≥ 32 kU/L AUC: 0.983, sensitivity: 100%, specificity: 89% - α-lactalbumin ≥17.6 kU/L AUC: 0.981, sensitivity: 100%, specificity: 89% - β-lactoglobulin ≥7.1 kU/L AUC: 7.96, sensitivity: 83.3%, specificity: 66.7% |
Study also contains detailed description of production of heated milk bread and placebo. 9 tolerant patients used the bread or placebo for 6 months
*Not reported for incidence groups seperately |
||
|
Mehr, 2014 |
Type of study: Prospective cohort
Setting and country: Tertiary clinic in Australia Funding and conflicts of interest: Funding from Medical research council and NIHR. |
Inclusion criteria - Children presenting at clinic jan 2019-dec 2013 - completely avoiding all forms of CM. - CMA diagnosed by: *CMA clinical reaction <12 months AND positive SPT or SSiGE * Clinical reaction to CM >12 months AND SPT wheal >7mm (>2 years) and SPT wheal >5mm (<2 years). Exclusion criteria: - allergic reaction to baked CM < 6 months - refusal/no consent
N = 70 Age = 5.3 years (range or SD not reported for total group) I: median (IQR): 7.3(4.9-9.6) C: median (IQR): 4.5(2.5-8)
% male I: 58% | C: 59% |
Prognostic factor(s) and method of measurement: - Age - Sex - Coexisting atopy (asthma, allergic rhinitis and/or eczema). - Allergy to other foods than CM : clinical reaction with confirmatory testing (SPT or sIgE) - SPT to baked milk and CM SPT was performed at the day of the OFC. positive SPT was: wheal >3mm than control at 15 min. |
OFC open OFC to baked CM: incremental doses of baked muffin at 20 min intervals. Clinical symptoms: failed challenge. Observation for 2 hours after last dose. Follow up after 1 week to confirm tolerance.
For how many participants were no complete outcome data available? N (%): Not reported
Reasons for incomplete outcome data described? Not reported |
OFC outcome 19/70 (27%) positive OFC (=reactive to baked milk)* 4/17(21%) presented with anaphalaxis
Atopic conditions
- Asthma C: 23(45%) | I: 18(95%) RR: 12.7(95%CI 1.8-90.1) - Asthma & on preventer therapy C: 12(24%) | I: 13(68%) RR: 2.8(95%CI 1.3-6.0) - Food allergy to >3 allergy groups C: 20 (39%) | I: 13 (68%) RR: 2.4 (95%CI 1.0-5.7) - Food allergy to >3 allergy groups & Prior anaphylaxis to food other than CM C: 4(85%) | 6(32%) RR 2.8(95%CI 1.4-4.5) - Previous anaphylaxis to CM C: 14(27%) | I: 10(52%) RR 2.1 (95%CI 1.0-4.5)
|
* Three children passed the OFC but developed symptoms at home with ongoing exposure 1 week later. They are included in the negative group. (contrary to Bartnikas)
|
||
|
Vilar,2021 |
Type of study: Cross-sectional
Setting and country: Paediatric outpatient clinic of a hospital. Brazil.
Funding and conflicts of interest: None reported |
Inclusion criteria: - <18 years - presenting in clinic with history of allergic reaction after contact with milk protein < 6 months - allergenic sensitization to milk protein and - exclusion of CM diet.
Exclusion criteria: - CM sIgE < 0.35 kU/L - CM SPT < 3 mm
N= 54
Median age (range): 3.14(0.5-15) years I: 2.81(0.53-10.1) | C:3.91(1.1-15.5)
% Male: 48% I: 60% | C: 44% |
Describe prognostic factor(s) and method of measurement: - Age - Sex - Other food allergies - SPT to casein, α-lactalbumin, β-lactoglobulin, raw CM, boiled CM, and baked CM following EAACI. Positive test was >3mm compared to control. -sIgE to CM, casein, α-lactalbumin, β-lactoglobulin manufacturer: Immunocap,
|
OFC open OFC to baked milk following PRACTALL recommendations via muffin. ¼ of 1.3 g protein every 20 min. no graded increments positive at signs of allergic reaction Monitoring for 2 hours.
For how many participants were no complete outcome data available? N (%): Not reported
Reasons for incomplete outcome data described? Not reported |
OFC outcome 15/53 (27.8%) positive OFC to baked milk
sIgE - sIgE CM <5.13kU/L AUC(95%CI): 0.70 (0.53-0.87), sensitivity:54%, specificity 80%.
SPT - SPT casein <3.2 mm AUC: not reported, sensitivity: 64%, specificity: 77%
|
|
||
OFC: Oral Food Challenge, SPT: Skin Prick Test, AUC: Area Under the Curve, CMA: cow’s milk allergy, CM: cow’s milk, DBPCFC: double blind placebo-controlled food challenge
Risk of bias table
Table of quality assessment – prognostic factor (PF) studies
Based on: QUIPSA (Haydn, 2006; Haydn 2013)
|
Study reference
(first author, year of publication) |
Study participation1
Study sample represents the population of interest on key characteristics?
(high/moderate/low risk of selection bias) |
Study Attrition2
Loss to follow-up not associated with key characteristics (i.e., the study data adequately represent the sample)?
(high/moderate/low risk of attrition bias) |
Prognostic factor measurement3
Was the PF of interest defined and adequately measured?
(high/moderate/low risk of measurement bias related to PF) |
Outcome measurement3
Was the outcome of interest defined and adequately measured?
(high/moderate/low risk of measurement bias related to outcome) |
Study confounding4
Important potential confounders are appropriately accounted for?
(high/moderate/low risk of bias due to confounding) |
Statistical Analysis and Reporting5
Statistical analysis appropriate for the design of the study?
(high/moderate/low risk of bias due to statistical analysis) |
|
Bartnikas, 2012 |
Moderate risk of selection bias
Reason: All patients who underwent an oral challenge to baked milk. Not clear what the target population was and which selection criteria were used to include patients for this challenge. |
Low risk of bias
Reason: Only a small number of data is missing, and characteristics with missing values were not significant. Note: Challenges were not blinded. |
Moderate risk of bias
Reason: Skin prick test was max 32 months before baked milk challenge, on average 3 months. Serum testing was a maximum of 34 months before challenge. |
Low risk of bias
Reason: Passed or failed was very clearly defined and failed challenges were extensively described. Challenge was not blinded but symptoms were very clearly and objectively defined. |
Moderate risk of bias
Reason: Small incidence group, age ranges do not seem very different. |
High risk of bias
Reason: No CI for ROC measurement reported. Only selective (not predefined) outcome measures are repored in ROC terms. Only values for sensitivity and specificity. (Figure 1C). Very large CI presented in eFigure 1 B,D and F. No multivariate model was defined. |
|
Karaman, 2022 |
Moderate risk of selection bias
Reason: All patients with suspicion for IgE-mediated allergy were screened. Not clear what the target population was and which selection criteria were used to include patients for this challenge. No exclusion mentioned (e.g. based on IC)
|
Low risk of bias
Reason: no missing data reported. |
Moderate risk of bias
Reason: Timing of measurement of predictors is not reported. |
Low risk of bias
Reason: symptoms that confirmed a fail were very clearly stated as was monitoring time of the challenge Challenge was not blinded but symptoms were very clearly and objectively defined. |
Moderate risk of bias
Reason: Children that were high predictive for clinical reactivity were excluded from the challenge. |
High risk of bias
Reason: Overfitting – 8 parameters, ntotal = 35 (12 in smallest group) No confidence intervals for testing group differences provided . Not clear how cut-off values were specified No multivariate model was defined. |
|
Kilic, 2021 |
High risk of bias
Reason: Unclear definition of participant selection. No timeframe mentioned. Unclear how many potential participants were not enrolled. (see Figure 1). |
Low risk of bias
Reason: no missing data reported. |
Moderate risk of bias
Reason: Timing of measurement of PF to OFC is not reported. |
Moderate risk of bias
Reason: no clear definition of the outcome tolerant vs reactive is given. Challenge was not blinded |
Moderate risk of bias
Reason: Children that were high predictive for clinical reactivity were excluded from OFC test with unheated milk. |
High risk of bias
Reason: Overfitting of the model. No CI intervals for group differences provided. No CI interval for AUC provided. Unclear how cut-off values for ROC were defined. No multivariate model was defined. |
|
Kiykim 2018 |
High risk of bias
Reason: Unclear definition of participant selection. No timeframe mentioned. Unclear how many potential participants were not enrolled |
Low risk of bias
Reason: no missing data reported. |
Moderate risk of bias
Reason: Timing of measurement of predictors is not reported. |
Low risk of bias
Reason: Outcome very clearly defined and described. Blinded challenge |
|
High risk of bias
Reason: No CI intervals for group differences, no CI for AUC. Overfitting. No multivariate model defined.
Note: Name a brand of “bakery tools” with baked milk that could be used for immunotherapy. Potential publication bias. |
|
Mehr,2014 |
Low risk of bias
reason: clear description of in- and exclusion and method and time period of recruitment |
Low risk of bias
reason: no missing data reported. |
Low risk of bias
SPT was performed at day of testing. |
Low risk of bias
Reason: symptoms that confirmed a positive test were very clearly stated as was monitoring time of the challenge and reasons for positive outcome. Challenge was not blinded but symptoms were very clearly and objectively defined. |
Moderate risk of bias
Children that were high predictive for clinical reactivity were excluded from OFC test with unheated milk. |
High risk of bias
70 cases, 14 comparisons: overfitting of the data. Chance of false positive result. No multivariate model defined. |
|
Vilar, 2022 |
Low risk of bias
Reason: clear description of in- and exclusion and method and time period of recruitment |
Low risk of bias
Reason: no missing data reported. |
Low risk of bias
Reason: SPT an ssIGE were collected/performed at day of testing. |
Low risk of bias
Reason: symptoms that confirmed a positive test were very clearly stated as was monitoring time of the challenge and reasons for positive outcome. Challenge was not blinded but symptoms were very clearly and objectively defined. |
|
High risk of bias
Reason: No CI intervals for group differences, no CI for AUC. Overfitting
No multivariate model defined. |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Sirin Kose, S., Asilsoy, S., Uzuner, N., Karaman, O., & Anal, O. (2019). Outcomes of Baked Milk and Egg Challenge in Cow's Milk and Hen's Egg Allergy: Can Tolerance Be Predicted with Allergen-Specific IgE and Prick-to-Prick Test?. International archives of allergy and immunology, 180(4), 264–273. https://doi.org/10.1159/000502957 |
Does not comply to predefined definition of IgE mediation |
|
Kwan, A., Asper, M., Lavi, S., Lavine, E., Hummel, D., & Upton, J. E. (2016). Prospective evaluation of testing with baked milk to predict safe ingestion of baked milk in unheated milk-allergic children. Allergy, asthma, and clinical immunology : official journal of the Canadian Society of Allergy and Clinical Immunology, 12, 54. https://doi.org/10.1186/s13223-016-0162-9 |
Wrong population, does not include specifically IgE mediated allergy |
|
Cuomo, B., Indirli, G. C., Bianchi, A., Arasi, S., Caimmi, D., Dondi, A., La Grutta, S., Panetta, V., Verga, M. C., & Calvani, M. (2017). Specific IgE and skin prick tests to diagnose allergy to fresh and baked cow's milk according to age: a systematic review. Italian journal of pediatrics, 43(1), 93. https://doi.org/10.1186/s13052-017-0410-8 |
Wrong population, does not include specifically IgE mediated allergy |
|
Faraj, Z., & Kim, H. L. (2012). Skin prick testing with extensively heated milk or egg products helps predict the outcome of an oral food challenge: a retrospective analysis. Allergy, asthma, and clinical immunology : official journal of the Canadian Society of Allergy and Clinical Immunology, 8(1), 5. https://doi.org/10.1186/1710-1492-8-5 |
Wrong population, does not include specifically IgE mediated allergy |
Beoordelingsdatum en geldigheid
Publicatiedatum : 14-07-2025
Beoordeeld op geldigheid : 14-07-2025
Algemene gegevens
De herziening van deze richtlijn werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor kinderen met een IgE-gemedieerde koemelkallergie.
Werkgroep
- Mevr. dr. E.C. (Eva) Koffeman, kinderarts-allergoloog, namens de Nederlandse Vereniging voor Kindergeneeskunde (NVK) (voorzitter)
- Mevr. dr. L.J. (Lonneke) Landzaat, kinderarts-allergoloog, namens de NVK
- Mevr. dr. M.M.J. (Marjoke) Verweij, kinderarts, namens de NVK
- Mevr. drs. K. (Kelly) van de Vorst-van der Velde, kinderarts-allergoloog, namens de NVK
- Mevr. dr. L. (Lonneke) van Onzenoort-Bokken, kinderarts, namens de NVK
- Mevr. drs. M.F. (Maartje) van Velzen, kinderarts, namens de NVK
- Mevr. dr. B. (Berber) Vlieg-Boerstra, diëtist, namens de Nederlandse Vereniging van Diëtisten (NVD/DAVO)
- Mevr. O. (Olga) Benjamin-Aalst, diëtist, namens de NVD/DAVO
- Mevr. E. (Erna) Botjes, voedselallergie en niet-allergische voedselovergevoeligheid belangenbehartiger, namens Stichting Voedselallergie
- Mevr. C. (Chantal) Janssen, verpleegkundig specialist, namens het Netwerk van Allergie Professionals (NAPRO)
Klankbordgroep
- Mevr. drs. D.A. (Dana-Anne) de Gast-Bakker, kinderarts, namens de NVK
- Mevr. drs. E.A. (Ellen) Croonen, kinderlongarts, namens de NVK
- Mevr. drs. E. (Ester) Rijks, jeugdarts, namens AJN Jeugdartsen Nederland
- Mevr. D.G. (Daphne) Philips, verpleegkundig specialist, namens NAPRO
- Mevr. (M.) Mathilde Serné, lactatiekundige, namens de Nederlandse Vereniging van Lactatiekundigen (NVL)
- Mevr. M. (Maria) Oligschläger-Lindelauf, lactatiekundige, namens de NVL
Met ondersteuning van
- Mevr. dr. M.M.J. (Machteld) van Rooijen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. drs. L.C. (Laura) van Wijngaarden, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Koffeman (voorzitter) |
kinderarts-allergoloog, Rijnstate Arnhem |
Geen. |
Extern gefinancierd onderzoek: 1. Onderzoeksproject SinFoNIA: Specialist Infant Formulas in non-IgE mediated cow's milk allergy. In 2018 financiering toegezegd gekregen (Health Holland met behulp van Nutricia Research) maar geannuleerd door stopzetting project (maart 2020). Het project heeft niet geleid tot publicaties. 2. Lokale hoofdonderzoeker voor BAT koemelk bij koemelkallergie, gefinancierd met de beurs van ZonMW Veelbelovende Zorg.
Presentaties koemelkallergie, voedselallergie en FPIES (in brede zin: het gehele ziektebeeld in het kader van congres of nascholing) wanneer deze onderwijskundig belang dienen. - 2020 Mead Johnson, webinar voor kinderartsen en jeugdartsen - 2021 NVK congres (sessie gesponsord door Nestle) De eventuele honoraria die voortvloeien uit deze presentaties werden tot start van de richtlijn gestort aan het Vriendenfonds Rijnstate t.b.v. opleiding en onderzoek binnen de kinderallergologie. Gedurende voorzitterschap richtlijn is voor deze presentaties geen honorarium meer aangenomen. . |
Geen restricties |
|
Landzaat |
Kinderarts-allergoloog, Elisabeth-Tweesteden ziekenhuis Tilburg |
Geen. |
Geen. |
Geen restricties. |
|
Verweij |
Kinderarts, VieCurie Medisch centrum |
Geen. |
In het VieCurie wordt gewerkt aan uitbreiding van het kinderallergiecentrum. |
Geen restricties. |
|
Van der Vorst- van der Velde |
Kinderarts-allergoloog, Maasstad ziekenhuis Rotterdam |
Geen. |
Geen. |
Geen restricties. |
|
Onzenoort |
Kinderarts, Máxima Medisch centrum Eindhoven |
Financiële vergoeding voor deze werkzaamheden. |
Extern gefinancierd onderzoek: Lokale hoofdonderzoeker voor 3 projecten: 1. D-CAAP studie: onderzoek naar 0- toepassing corticosteroïden naast IVIG en acetylsalicylzuur (gefinancierd door UCL) 2. COPP studie: onderzoek naar covid infecties in kinderen (gefinancierd door LUMC/ ZonMW) 3. SVSpread: observationeel onderzoek naar RSV infecties (gefinancierd door UMCU/ ZonMW)
Presentaties koemelkeiwitallergie (gehele ziektebeeld en behandeling daarvan, geen invloed van sponsor op inhoud) in het kader van scholingen of congressen (Nutricia). |
Geen restricties. |
|
Van Velzen |
Kinderarts, Meander MC Amerstfoort |
Geen. |
Presentaties voedselallergie (gehele ziektebeeld en behandeling daarvan, geen invloed van sponsor op inhoud) in het kader van scholing, waarvoor honorarium beschikbaar werd gesteld. Bewuste samenwerking met alle spelers op de Nederlandse markt om binding met enkel bedrijf te voorkomen (o.a. Nutricia, Mead Johnson, Friso/Hero). |
Geen restricties. |
|
Vlieg-Boerstra |
Diëtist, Rijnstate Arnhem |
Lid Advisory board: Nestle, Nutricia, Vini Mini (producent pindapoeder), tot 1-1-2023: Marfo Food Groups (waarvoor vergoeding) |
Extern gefinancierd onderzoek: 1. Principal investigator van Groei studie: studie over de groei bij kinderen met allergie (sponsoring Nutricia) 2. Principal investigator van studie voeding bij borstvoeding, waarin voedingspatroon van moeder en HMO's in moedermelk worden onderzocht. Studie is volledig onafhankelijk opgezet en de resultaten worden niet beïnvloedt door de sponsor (Nutricia betaalt enkel de HMO bepalingen)
Expertise voedselprovocaties en dieetbehandeling van koemelkallergie via eigen praktijk (maatschap Vlieg Diëtisten)
Presentaties voedselallergie (inclusief koemelkallergie, en indicatie over typen voedingen in het algemeen; vrije invulling van inhoud) in het kader van scholing, waarvoor honorarium beschikbaar werd gesteld (Nestle, Nutricia). |
Geen restricties. Studies (externe onderzoeken) hebben geen invloed op de modules in de richtlijn, De studies gaan over de bestanddelen van moedermelk. |
|
Benjamin- van Aalst |
Diëtist-onderzoeker, OLVG Amsterdam Diëtist, Noordwest ziekenhuisgroep |
Lid dagelijks bestuur Netwerk Kinderdiëtisten. |
Presentaties voedselallergie (gehele ziektebeeld en behandeling daarvan) in het kader van scholing, waarvoor honorarium beschikbaar werd gesteld. Bewuste samenwerking met alle spelers op de Nederlandse markt om binding met enkel bedrijf te voorkomen (Nutricia, Reckitt, Abbott). |
Geen restricties. |
|
Janssen |
Verpleegkundig specialist kinderallergologie, Zuyderland Medisch centrum, Heerlen |
Geen. |
Geen. |
Geen restricties. |
|
Botjes |
Voedselallergie belangenbehartiger, Stichting Voedselallergie |
Geen. |
Geen. |
Geen restricties. |
Overkoepelend: Sommige Nederlandse ziekenhuizen (onder andere een aantal waarin de werkgroepleden werkzaam zijn) hebben een samenwerkingsovereenkomst met Nutricia. Het onderzoek dat door deze werkgroepleden wordt verricht, wordt niet beïnvloed door deze samenwerkingsbijdrage.
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door een afgevaardigde van de patiëntenvereniging Stichting Voedselallergie in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen (zie kop ‘Waarden en voorkeuren van patiënten’). De conceptrichtlijn is tevens voor commentaar voorgelegd aan Stichting Voedselallergie en Patiëntenfederatie Nederland, en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
|
Module |
Uitkomst raming |
Toelichting |
|
Module Baked milk (hoogverhitte melk) |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (>40.000 patiënten), volgt uit de toetsing dat het overgrote deel (±90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet. Er worden daarom geen financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Binnen het SKMS project “Inventarisatie en optimalisatie modulair onderhoud richtlijn kindergeneeskunde” is breed geïnventariseerd welke kindergeneeskundige modules toe waren aan herziening, en er is een onderhoudsplan opgeleverd. De modules van deze richtlijn, herzien in 2022-2024, kwamen uit dit project naar voren. De modules zijn kritisch beoordeeld en de uitgangsvraag en zoekvraag werden aangepast of aangescherpt.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Referenties
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Zoekverantwoording
Algemene informatie
|
Cluster/richtlijn: UV7 Baked milk |
|
|
Uitgangsvraag/modules: Bij welke kinderen kan bij voorbaat baked milk worden ontraden (= bij welke kinderen bied je baked milk provocatie aan)? |
|
|
Database(s): Embase.com, Ovid/Medline |
Datum: 6 november 2023 |
|
Periode: vanaf: geen restrictie |
Talen: geen restrictie |
|
Literatuurspecialist: Alies van der Wal en Esther van der Bijl |
Rayyan review: https://rayyan.ai/reviews/834888 |
|
BMI-zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting: Voor deze vraag is gezocht op de elementen: koemelkallergie kinderen baked milk prognostisch filter (gericht op predictiemodellen) à de vraag is opgevat als een prognostische vraag. Hiervoor is het prognostisch filter, gericht op predictiemodellen, gebruikt. De sleutelartikelen PMID33641294 en PMID36162375 worden gevonden met deze search. |
|
|
Te gebruiken voor richtlijntekst: In de databases Embase.com en Ovid/Medline is op 6 november 2023 systematisch gezocht naar systematische reviews, RCTs en observationele studies over het bij voorbaat ontraden van baked milk bij kinderen. De literatuurzoekactie leverde 24 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SR |
1 |
1 |
1 |
|
RCT |
5 |
2 |
7 |
|
Observationeel |
16 |
8 |
16 |
|
Totaal |
22 |
11 |
24* |
*in Rayyan
Zoekstrategie Embase.com
|
No. |
Query |
Results |
|
#1 |
'milk allergy'/exp OR 'milk intolerance'/exp OR (('cow milk'/exp OR 'whey'/exp OR 'whey protein'/exp OR 'casein'/exp) AND ('allergy'/exp OR 'hypersensitivity'/exp OR 'food allergen'/exp OR 'immunoglobulin e'/exp OR 'ige mediated food allergy'/exp OR 'nutritional intolerance'/de OR 'adverse food reaction'/de OR 'food allergy'/de)) OR ((('cow s milk' OR 'cow* milk' OR casein* OR whey) NEAR/3 (allerg* OR intoleran* OR sensitization OR sensitisation OR hypersensitization OR hypersensitisation OR sensitivity OR hypersensitivity OR anaphyla* OR ige OR 'ig e' OR 'gammaglubulin e' OR 'gamma e' OR 'immunoglobulin gamma e' OR 'immunoglobulin e')):ti,ab,kw) |
10537 |
|
#2 |
'adolescent'/exp OR 'baby'/exp OR 'boy'/exp OR 'child'/exp OR 'minors'/exp/mj OR 'pediatric patient'/exp OR 'pediatrics'/exp OR 'schoolchild'/exp OR infan*:ti,ab OR newborn*:ti,ab OR 'new born*':ti,ab OR perinat*:ti,ab OR neonat*:ti,ab OR baby*:ti,ab OR babies:ti,ab OR toddler*:ti,ab OR minors*:ti,ab OR boy:ti,ab OR boys:ti,ab OR boyfriend:ti,ab OR boyhood:ti,ab OR girl*:ti,ab OR kid:ti,ab OR kids:ti,ab OR child*:ti,ab OR children*:ti,ab OR schoolchild*:ti,ab OR adolescen*:ti,ab OR juvenil*:ti,ab OR youth*:ti,ab OR teen*:ti,ab OR pubescen*:ti,ab OR pediatric*:ti,ab,kw OR paediatric*:ti,ab,kw OR peadiatric*:ti,ab,kw OR school:ti,ab OR school*:ti,ab OR prematur*:ti,ab OR preterm*:ti,ab |
5810330 |
|
#3 |
'baked milk'/exp OR 'boiled milk'/exp OR 'pasteurized milk'/exp OR (((baked OR heat* OR boiled OR steril* OR pasteuri*) NEAR/3 (milk* OR cow* OR cm OR dairy)):ti,ab,kw) |
6360 |
|
#4 |
'area under the curve'/exp OR 'brier score'/exp OR 'computer prediction'/exp OR 'c statistic'/exp OR 'c statistics'/exp OR 'integrated discrimination improvement'/exp OR 'net reclassification improvement'/exp OR 'net reclassification index'/exp OR 'prediction'/exp OR 'predictive model'/exp OR 'predictive modeling'/exp OR 'predictive validity'/exp OR 'predictive value'/exp OR 'regression analysis'/exp OR 'statistical model'/exp OR 'area under the curve':ti,ab,kw OR 'brier score*':ti,ab,kw OR 'c statistic*' OR 'computer prediction':ti,ab,kw OR 'decision curve anal*':ti,ab,kw OR (('net reclassification' NEAR/2 (improvement OR index)):ti,ab,kw) OR (((predict* OR statistical*) NEAR/3 (model* OR validity OR value)):ti,ab,kw) OR 'proportional hazards model*':ti,ab,kw OR 'r square*':ti,ab,kw OR regression:ti,ab,kw OR predict*:ti OR multivariate:ti,ab,kw OR multivariab*:ti,ab,kw |
3329425 |
|
#5 |
#1 AND #2 AND #3 AND #4 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
29 |
|
#6 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
974287 |
|
#7 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
3905896 |
|
#8 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
7910149 |
|
#9 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
14542914 |
|
#10 |
#5 AND #6 – SR’s |
1 |
|
#11 |
#5 AND #7 NOT #10 – RCT’s |
5 |
|
#12 |
#5 AND (#8 OR #9) NOT (#10 OR #11) – Observationeel |
16 |
|
#13 |
#10 OR #11 OR #12 |
22 |
Ovid/Medline
|
# |
Searches |
Results |
|
1 |
exp Milk Hypersensitivity/ or ((Milk/ or exp Milk Proteins/ or exp Whey/) and (exp Hypersensitivity/ or exp Allergens/ or exp Immunoglobulin E/)) or (('cow s milk' or 'cow* milk' or casein* or whey) adj3 (allerg* or intoleran* or sensitization or sensitisation or hypersensitization or hypersensitisation or sensitivity or hypersensitivity or anaphyla* or ige or 'ig e' or 'gammaglubulin e' or 'gamma e' or 'immunoglobulin gamma e' or ' immunoglobulin e')).ti,ab,kf. |
6656 |
|
2 |
(child* or schoolchild* or infan* or adolescen* or pediatri* or paediatr* or neonat* or boy or boys or boyhood or girl or girls or girlhood or youth or youths or baby or babies or toddler* or childhood or teen or teens or teenager* or newborn* or postneonat* or postnat* or puberty or preschool* or suckling* or picu or nicu or juvenile?).ti,ab,kf. |
3015879 |
|
3 |
(exp Pasteurization/ and exp Milk/) or ((baked or heat* or boiled or steril* or pasteuri*) adj3 (milk* or cow* or cm or dairy)).ti,ab,kf. |
6091 |
|
4 |
Area Under Curve/ or exp Forecasting/ or "Predictive Value of Tests"/ or exp Multivariate Analysis/ or exp Regression Analysis/ or exp Models, Statistical/ or area under the curve.ti,ab,kf. or brier score*.ti,ab,kf. or c statistic*.ti,ab,kf. or computer prediction.ti,ab,kf. or decision curve anal*.ti,ab,kf. or (net reclassification adj2 (improvement or index)).ti,ab,kf. or ((predict* or statistical*) adj3 (model* or validity or value)).ti,ab,kf. or proportional hazards model*.ti,ab,kf. or r square*.ti,ab,kf. or regression.ti,ab,kf. or predict*.ti. or multivaria*.ti,ab,kf. |
2481991 |
|
5 |
1 and 2 and 3 and 4 |
17 |
|
6 |
5 not (comment/ or editorial/ or letter/) not ((exp animals/ or exp models, animal/) not humans/) |
14 |
|
7 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
704666 |
|
8 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2651935 |
|
9 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] |
4571910 |
|
10 |
Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) |
5548024 |
|
11 |
6 and 7 – SR’s |
1 |
|
12 |
(6 and 8) not 11 – RCT’s |
2 |
|
13 |
(6 and (9 or 10)) not (11 or 12) – Observationeel |
8 |
|
14 |
11 or 12 or 13 |
11 |