Prothetisch herstel
Uitgangsvraag
Wat is het beste moment voor het plaatsen van implantaten in het hoofd-halsgebied ter ondersteuning van de prothetische rehabilitatie bij patiënten met hoofd-halskanker?
De uitgangsvraag bestaat uit de volgende deelvragen:
- Wat is het beste moment voor het plaatsen van intra-orale implantaten ter ondersteuning van de prothetische rehabilitatie bij patiënten met hoofd-halskanker?
- Wat is het beste moment voor het plaatsen van extra-orale implantaten in het hoofd-halsgebied ter ondersteuning van de prothetische rehabilitatie (anaplastologie) bij patiënten met hoofd-halskanker?
Anaplastologie is een paramedische specialisatie die zich richt op het vervaardigen van epithesen ter vervanging van externe lichaamsdelen, met name in het gelaat, bij congenitale afwijkingen, na trauma of chirurgische ingrepen.
Aanbeveling
Beoordeel bij iedere patiënt met hoofd-halskanker tijdens het pre-therapeutische diagnostische proces in nauwe samenwerking met een gespecialiseerd MKA-chirurg, tandarts- maxillofaciale prothetiek (MFP), tandtechnicus-MFP of anaplastoloog en mondhygiënist binnen het interdisciplinaire hoofd-hals team, de mogelijkheid tot plaatsing van intra-orale en/of extra-orale implantaten bij voorkeur tijdens de chirurgie of panendoscopie onder narcose ter ondersteuning van de toekomstige prothetische rehabilitatie.
De prothetisch-herstel coördinerend tandarts-MFP bespreekt met de patiënt – in het kader van gedeelde besluitvorming – de mogelijke gevolgen van de behandeling op de slik-, spraak- en kauwfunctie (bij intra-orale implantaten) dan wel op de esthetiek, retentie van prothese, gehoor en neusademhaling (bij extra-orale implantaten), evenals de impact hiervan op de kwaliteit van leven.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Er is systematisch literatuuronderzoek verricht naar het plaatsen van implantaten tijdens de primaire oncologische chirurgie (tumor ablation surgery) in vergelijking met plaatsing na chirurgie en eventuele aanvullende behandeling zoals postoperatieve (chemo)radiotherapie, bij volwassen patiënten met hoofd-halskanker.
Daarbij zijn twee deelvragen geformuleerd: één met betrekking tot het plaatsten van intra-orale implantaten en één betreffende extra-orale implantaten in het hoofd-halsgebied. Voor de eerste deelvraag (intra-orale implantaten) werden zes studies geïdentificeerd. Twee studies van Wetzels (2016 en 2017) betroffen hetzelfde patiëntencohort. De studie van Mizbah (2013) kende drie overlappende auteurs met bovengenoemde studies van Wetzels. Voor de tweede deelvraag (extra-orale implantaten) werden geen studies gevonden die voldeden aan de opgestelde PICO-criteria.
De geïncludeerde studies beschrijven uitsluitend het plaatsen van implantaten tijdens een chirurgische ingreep vergeleken met plaatsing na een chirurgische ingreep al dan niet na adjuvante (chemo)radiotherapie. In alle geïncludeerde studies (Tabel 2) bestond subgroep C1 (implantaatplaatsing na tumorablatiechirurgie) uit een heterogene groep patiënten die al dan niet adjuvante (postoperatieve) (chemo)radiotherapie hadden ondergaan. Deze patiënten werden als één groep geanalyseerd, ondanks dat een subgroepanalyse op basis van de (chemo)radiotherapie—specifiek implantaatplaatsing voor of na de adjuvante (chemo)radiotherapie—gerechtvaardigd zou zijn geweest. Het onderscheiden van deze subgroepen is van essentieel belang, aangezien implantaatplaatsing ná adjuvante (chemo)radiotherapie waarschijnlijk gepaard gaat met een verhoogd risico op nadelige uitkomsten over alle geëvalueerde parameters heen.
Er is geen literatuur gevonden die het plaatsen van implantaten voorafgaand aan primaire (chemo)radiotherapie (subgroep I2 in de PICO) bespreekt bij patiënten die geen chirurgische behandeling (zullen) ondergaan. Evenmin is in de beschikbare studies aandacht besteed aan de mogelijkheid om implantaten te plaatsen tijdens de panendoscopie onder narcose.
Onder een panendoscopie onder narcose verstaan we een procedure waarbij een starre endoscoop met een optiek wordt gebruikt om de mond- en keelholte (cavum oris, oro- en hypofarynx), larynx, trachea en soms slokdarm en nasofarynx te onderzoeken eventueel gevolgd door bioptname.
Voor de cruciale uitkomstmaat osteoradionecrose was de bewijskracht van de literatuur zeer laag. Voor de uitkomstmaat kauwfunctie (masticatory performance) werd onvoldoende wetenschappelijk bewijs aangetroffen. Voor de uitkomstmaten overdenture placement (zowel ten aanzien van tijd tot plaatsing als succespercentage) en bite force was de kwaliteit van het bewijs eveneens zeer laag. Voor de overige belangrijke uitkomstmaten zoals kwaliteit van leven, slik- en spraakfunctie werden geen (vergelijkende) studies met voldoende wetenschappelijke onderbouwing gevonden waarin deze uitkomstmaten expliciet werden beschreven. Bij het ontbreken van voldoende wetenschappelijk bewijs om eenduidig voorkeur te geven aan implantaatplaatsing tijdens de oncologische chirurgie dan wel na chirurgie en eventuele aanvullende behandeling zoals postoperatieve (chemo)radiotherapie, baseert de richtlijnwerkgroep haar aanbeveling voornamelijk op klinische ervaring en expertise.
De richtlijnwerkgroep adviseert om bij iedere patiënt met hoofd-halskanker tijdens het pre-therapeutische diagnostische proces de mogelijkheid tot plaatsing van intra-orale en/of extra-orale implantaten, bij voorkeur tijdens de primaire oncologische chirurgie of panendoscopie onder narcose, ter ondersteuning van de toekomstige prothetische rehabilitatie te beoordelen. Deze beoordeling vindt bij voorkeur plaats in nauwe samenwerking met een gespecialiseerd MKA-chirurg, tandarts- maxillofaciale prothetiek (MFP), tandtechnicus-MFP of anaplastoloog en een mondhygiënist binnen het interdisciplinaire hoofd-hals team. Tevens adviseert de richtlijnwerkgroep de coördinerend tandarts-MFP met de patiënt – in het kader van gedeelde besluitvorming – de mogelijke gevolgen van de behandeling op de slik-, spraak- en kauwfunctie (bij intra-orale implantaten) dan wel op de esthetiek, retentie van prothese, gehoor en neusademhaling (bij extra-orale implantaten), evenals de impact hiervan op de kwaliteit van leven te laten bespreken. Voor het plaatsen van implantaten in een autologe mandibulaire reconstructie tijdens de oncologische chirurgie, zijn in meerdere studies functionele voordelen beschreven, die volgens de richtlijnwerkgroep opwegen tegen het potentiële risico dat geplaatste implantaten uiteindelijk niet worden benut (Kwakman, 1997; Mizbah, 2013; Wetzels, 2017; Schoen, 2008; McMillan, 2022; Tumuluri, 2023; Woods, 2019). De meest overtuigende voordelen betreffen een versneld en verbeterd functioneel herstel, met name door behoud of herstel van de bijtkracht en de kauwfunctie, die cruciaal zijn voor de kwaliteit van leven van de patiënt (Wetzels, 2016). Het vroegtijdig betrekken van een tandarts maxillofaciale prothetiek is essentieel om vóór de oncologische chirurgie, panendoscopie onder narcose of primaire (upfront) (chemo)radiotherapie te beoordelen of de uitgangssituatie voldoende prothetische ruimte biedt om een optimaal functioneel resultaat te behalen (Dugast, 2025).
Deze overweging is met name van belang bij patiënten die als gevolg van de oncologische chirurgie of ter voorbereiding op (chemo)radiotherapie edentaat zullen worden, bij patiënten met een minimaal geresorbeerde mandibula, of bij wie postoperatief trismus of een beperkte tongmobiliteit wordt verwacht. In het laatste geval is het relevant te vermelden dat het verlagen van de kaakwal (processus alveolaris) voorafgaand aan implantaatplaatsing bijdraagt aan een verlaging van de beethoogte in de uiteindelijke prothese. Door het dieper/verder occluderen (dichtbijten) wordt de onderkaak, samen mét de minder beweeglijke tong, verder naar craniaal en dichter bij de maxillaire tandboog en het palatum gebracht. Dit bevordert een betere mondsluiting, wat de verminderde mobiliteit van de tong gedeeltelijk kan compenseren. Dit is van wezenlijk belang voor een optimale functionele rehabilitatie in deze patiëntengroep.
Bij complexe reconstructieve casuïstiek is een gepersonaliseerde, interdisciplinaire behandelaanpak noodzakelijk, bij voorkeur ondersteund door 3D-virtuele planningsmethoden. Binnen deze aanpak verdient een occlusie-gestuurde planning de voorkeur, aangezien dit kan bijdragen aan een voorspelbaar functioneel en esthetisch eindresultaat (Seikaly, 2019; Vosselman, 2021; Rohner, 2013).
In dit kader dient te worden gewezen op de verhoogde risico’s die zijn gerapporteerd bij implantaatplaatsing in vrij gevasculariseerde ossale transplantaten tijdens reconstructieve chirurgie (Tumuluri, 2023; Fenlon, 2012). Desondanks onderstreept een recente systematische review (gepubliceerd na de zoekdatum) de voorkeur voor primaire implantaatplaatsing tijdens de oncologische chirurgie met reconstructie, in vergelijking met uitgestelde implantaatplaatsing (Dugast, 2025). Deze review beschrijft een gemiddeld kortere tijd tot functionele revalidatie in de primaire implantatiegroep (gemiddeld 5,3 maanden, variërend van 1,7 tot 12 maanden) ten opzichte van de secundaire implantatiegroep (gemiddeld 20,7 maanden, variërend van 9 tot 40,8 maanden). Daarnaast werden een hogere implantaatoverleving (92,5% versus 88,5%) en minimaal transplantaatverlies (één geval van botflapverlies en één geval van gedeeltelijke flapnecrose) gerapporteerd in de groep met primaire plaatsing versus zes gevallen van gedeeltelijke of totale flapnecrose in de groep met secundaire plaatsing.
Voor defecten van de maxilla, met name de lagere defecten, worden in de literatuur diverse reconstructieve methoden beschreven. Ook hier lijkt implantaatplaatsing tijdens de primaire oncologische chirurgie functionele voordelen te bieden. Bij edentate patiënten die met een klosprothese worden gerehabiliteerd, is aangetoond dat implantaten zowel de objectieve als de subjectieve kauwfunctie verbeteren (Buurman, 2020b). Eveneens zijn positieve resultaten beschreven met het gebruik van zygoma-implantaten, waarbij een sneller functioneel herstel als een van de belangrijkste voordelen wordt benoemd (Butterworth, 2022; Butterworth, 2017; Hackett, 2021). Tot slot zijn er ook voor de maxilla vergelijkbare resultaten gerapporteerd als voor de mandibula bij het combineren van een vrij gevasculariseerde ossale lap met gelijktijdige implantaatplaatsing (Seikaly, 2019; Johal, 2021). Echter, deze reconstructies leiden niet vanzelfsprekend tot een verbeterde kauwfunctie, mogelijk vanwege een vertraagd of complexer prothetisch revalidatietraject (Buurman, 2020a).
Extra-orale implantaten worden reeds meer dan twee decennia beschouwd als een waardevolle aanvulling binnen de anaplastologie (Dings, 2011; Chang, 2005). Deze implantaten kennen hoge succespercentages, ook op de langere termijn. Voor de mastoïdregio wordt een 10 jaars overleving van 93,7-95,9% gerapporteerd, voor de neusregio 86,9-92,5%, en voor de orbita 53,7-84,2% (Subramaniam, 2018; Alberga, 2022). Tevens suggereren meerdere studies dat implantaten die tijdens de primaire oncologische chirurgie worden geplaatst een betere prognose kennen dan implantaten die pas na afloop van de oncologische behandeling worden geplaatst (Dings, 2011; Subramaniam, 2018). Voor het behalen van een optimaal behandelresultaat, zowel chirurgisch als prothetisch, is een interdisciplinaire, preoperatieve planning van de implantaatplaatsing essentieel (Alberga, 2022).
Waarden en voorkeuren van patiënten (en evt. hun naasten en/of verzorgers)
Patiënten die een behandeling voor hoofd-halskanker hebben ondergaan, rapporteren frequent problemen op het gebied van mondgezondheid, kauwfunctie, voedingsinname, vermoeidheid, slikfunctie en pijn, ongeacht hun leeftijd (Kanatas, 2022).
Bij edentate patiënten is aangetoond dat implantaat-gedragen protheses de patiënttevredenheid, orale functionaliteit en de kwaliteit van leven aanzienlijk verbeteren ten opzichte van conventionele protheses (Schoen, 2008; Harris, 2013; Rogers, 1999; Schiegnitz, 2021; Garner, 2023). Bovendien ervaren edentate patiënten die geen prothese dragen een significant slechtere kwaliteit van leven, met onder andere beperkingen op het gebied van pijn, dagelijkse activiteiten, sociale participatie, spraakverstaanbaarheid en eten in het openbaar (Rogers, 1999; Duke, 2005).
Het plaatsen van implantaten bij voorkeur tijdens de oncologische chirurgie of panendoscopie onder narcose draagt bij aan een vermindering van de totale behandellast (bijvoorbeeld door reductie van het aantal operaties en ziekenhuisopnames), en verkort de tijd tot plaatsing van de definitieve prothese aanzienlijk in vergelijking met uitgestelde implantaatplaatsing. Dit resulteert in een snellere verbetering van de kwaliteit van leven (Woods, 2019). Bij implantaatplaatsing tijdens mandibulaire reconstructies is daarnaast een hogere gezondheid-gerelateerde kwaliteit van leven gerapporteerd, met positieve effecten op domeinen zoals voedingsinname, ervaren eetproblemen, en tevredenheid over de verstrekte informatie (Tumuluri, 2025).
Een goede voorlichting over de beschikbare revalidatiemogelijkheden inclusief eventuele effecten op gehoor en nasale functies (mogelijk beter richtinghoren en behoud van nasale ademhaling)(American College of Prosthodontists 2020) en de verwachte functionele uitkomsten, herstelduur, complicatie risico’s, financiële implicaties en eventuele aanvullende procedures, is van groot belang voor gedeelde besluitvorming. Dit geldt in het bijzonder voor oudere patiënten, bij wie een hogere informatiebehoefte en een lagere tevredenheid met verstrekte informatie is gerapporteerd (Tumuluri, 2025).
Kosten (middelenbeslag)
Implantaatplaatsing bij edentate patiënten tijdens de primaire oncologische chirurgie is aanzienlijk kostenefficiënter in Nederland dan secundaire implantaatplaatsing, met geschatte kostenbesparingen tot circa 86% (Wetzels, 2017). Deze kostenreductie is grotendeels toe te schrijven aan het lagere gebruik van aanvullende interventies zoals hyperbare zuurstoftherapie, de verminderde noodzaak tot algehele anesthesie met dagopname, en een lager tarief voor de ingreep zelf bij primaire plaatsing. Indien de volledige ziekenhuiskosten worden meegenomen – zoals het gebruik van de operatiekamer, inzet van medisch personeel en anesthesie – kan de werkelijke kostenbesparing nog groter zijn, aangezien primaire implantatie enkel leidt tot verlenging van de operatieduur binnen een reeds geplande ingreep (Wetzels, 2017). In een studie verricht aan de Mayo Clinic (VS) werd bij patiënten met een fibulareconstructie geen verschil gevonden in het complicatierisico tussen primaire en secundaire implantatie. Wel werd bij primaire implantaatplaatsing een kostenbesparing van 24% gerapporteerd, mede doordat patiënten eerder konden starten met orale voedingsinname en prothetisch gebruik (80 vs. 126 weken)(Menapace, 2018). Tevens werd geen negatieve invloed van de implantaatplaatsing op lapoverleving vastgesteld (Menapace, 2018). Gegeven het sneller functioneel herstel en de lagere kosten die gepaard gaan met primaire implantaatplaatsing, adviseert de richtlijnwerkgroep om bij iedere patiënt de mogelijkheid van implantaatplaatsing tijdens de primaire oncologische chirurgie of panendoscopie onder narcose voorafgaand aan (chemo)radiotherapie expliciet te overwegen. Aangezien implantaatplaatsing en prothetische revalidatie binnen Nederland tot het verzekerde zorgpakket behoren, is het van belang deze optie ook in de gedeelde besluitvorming met de patiënt te bespreken.
Aanvaardbaarheid, haalbaarheid en implementatie
Voor implantaatplaatsing tijdens primaire oncologische chirurgie of panendoscopie onder narcose voorafgaand aan (chemo)radiotherapie mogelijk te maken, is het essentieel dat de patiënt voorafgaand aan deze ingrepen wordt geëvalueerd door een interdisciplinair team. Dit team dient in elk geval te bestaan uit een mondziekten, kaak- en aangezichts (MKA)-chirurg of hoofd-halschirurg met ervaring in implantologie, of een tandarts-implantoloog èn een tandarts maxillofaciale prothetiek.
Bij complexere reconstructieve trajecten, zoals maxillaire defecten, is een gepersonaliseerde, interdisciplinaire benadering vereist. Hierbij geniet een occlusie-gestuurde planning, ondersteund door 3D-technologieën, de voorkeur. Voor een optimale planning is aanvulling van het hoofd-hals oncologisch team met een technisch geneeskundige met expertise in virtuele chirurgische planning wenselijk. In het geval van extra-orale implantaten is de betrokkenheid van een anaplastoloog of tandtechnicus-MFP onmisbaar voor het behalen van een optimaal prothetisch en esthetisch resultaat.
Voor zover bij de richtlijnwerkgroep bekend, beschikken alle hoofd-halscentra in Nederland over de benodigde expertise om interdisciplinair behandelplannen op te stellen. De richtlijnwerkgroep benadrukt het belang van vroegtijdige consultatie van betrokken disciplines, bij voorkeur in de diagnostische fase van het oncologisch behandeltraject, om tijdig implantologische mogelijkheden in kaart te brengen en met de patiënt te bespreken (Vosselman, 2021).
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Er is systematisch literatuuronderzoek verricht naar de optimale timing van implantaatplaatsing bij volwassen patiënten met hoofd-halskanker. Voor intra-orale implantaten werden 6 studies geïdentificeerd, voor extra-orale implantaten werd geen relevante literatuur gevonden die voldeed aan de opgestelde PICO-criteria. De wetenschappelijke bewijskracht voor cruciale en belangrijke uitkomstmaten – zoals ORN, kauwfunctie, overdenture placement (zowel ten aanzien van tijd tot plaatsing als succespercentage), bite force, kwaliteit van leven, slik- en spraakfunctie – werd als zeer laag tot onvoldoende beoordeeld.
Bij afwezigheid van robuust bewijs baseert de richtlijnwerkgroep haar aanbeveling op klinische expertise. Zij adviseert om tijdens het pre-therapeutische diagnostische proces de mogelijkheid tot plaatsing van intra-orale en/of extra-orale implantaten, bij voorkeur tijdens de primaire oncologische chirurgie of panendoscopie onder narcose, ter ondersteuning van de toekomstige prothetische rehabilitatie te beoordelen. Meerdere studies rapporteren functionele voordelen van primaire plaatsing, waaronder een snellere en effectievere functionele rehabilitatie, behoud van kauwfunctie en ‘bite force’, en hogere patiënttevredenheid. Tevens wordt een kostenbesparing gerapporteerd bij primaire ten opzichte van secundaire implantatie, zonder verhoogd complicatierisico.
Een interdisciplinaire preoperatieve beoordeling en planning – bij voorkeur ondersteund door 3D-technologie en occlusie-gestuurde benadering – is essentieel, met betrokkenheid van MKA-chirurgen, tandartsen-MFP, anaplastologen en andere relevante disciplines. Tot slot onderstrepen de gerapporteerde voordelen het belang van tijdige besluitvorming en uitgebreide patiëntvoorlichting.
Onderbouwing
Head and neck cancer, along with its treatment, can result in oromaxillofacial deformities, with significant functional impairments, psychosocial and esthetic deficits, and a consequent decline in quality of life (QoL). For many of these defects prosthetic rehabilitation is the most commonly employed approach to restore form and function. The use of osseointegrated implants in this patient population has significantly improved prosthesis retention and functionality, thereby enhancing patient's QoL (Roumanas, 2006). Implants can be placed either primarily, during tumor ablation surgery, or secondarily, following completion of oncological treatment. A key advantage of delayed (secondary) placement is that it allows for a more thorough assessment of the patient’s disease-free status and overall survival. Allowing time for surgical site healing and reassessing the patient's prosthetic needs can further support precise and well-informed planning of implant placement. However, advancements in three-dimensional (3D) virtual surgical planning permit implant planning to occur prior to the initiation of oncological treatment (Witjes, 2018). Despite the potential benefits of secondary placement, this approach is associated with notable drawbacks. These include delayed rehabilitation, the need for additional interventions such as prophylactic antibiotics or hyperbaric oxygen therapy, and the requirement for a second surgical procedure. Furthermore, placing implants in previously irradiated tissue introduces a higher risk of complications, with osteoradionecrosis (ORN) representing the most feared one (Rogers, 2005; Ihde, 2008). As early as 1997, authors have advocated for evaluating the feasibility of osseointegrated oral implants during the pre-treatment diagnostic phase, enabling implant placement to be carried out concurrently with tumor ablation surgery. This integrated approach facilitates earlier prosthetic rehabilitation – such as the placement of overdentures or extra-oral prostheses – and expands access to functional reconstruction for a greater number of patients (Kwakman, 1997; Mizbah, 2013; Wetzels, 2021; Dings, 2011; Schoen, 2001; Elledge 2017; Subramaniam, 2018). The use of implant-retained prostheses has been shown to improve functional outcomes, including prosthesis stability, masticatory efficiency, and overall patient satisfaction, when compared to conventional dentures (Wetzels, 2017; Korfage, 2014; Schoen, 2008; Sumida, 2016). For extra-oral prostheses (epitheses), implant retention is also preferred over adhesive-based or mechanical retention alternatives due to its superior stability, ease of placement, and removability (Dings, 2018; Ariani, 2013).
Nevertheless, it remains unclear whether a systematic assessment of the potential for implant-supported rehabilitation is routinely incorporated into the diagnostic process across all head and neck cancer centers. This module provides evidence-based recommendations regarding the optimal timing of implant placement to support prosthetic orofacial or maxillofacial rehabilitation in patients with head and neck cancer.
Subquestion 1 (intra-oral implants):
I1 versus C1 of the PICO question (implant placement during versus after tumor ablation surgery)
1. ORN – critical outcome
|
Very low GRADE |
The evidence is very uncertain about the effect of immediate implant placement (during tumor ablation surgery) on the risk of osteoradionecrosis compared to delayed implant placement (after tumor ablation surgery) in patients with head and neck cancer.
Sources: Wetzels, 2017; McMillan, 2023; Tumuluri, 2023 |
2. Masticatory performance/masticatory ability/chewing – critical outcome
|
No GRADE |
No comparative evidence was found regarding the outcome masticatory performance/masticatory ability/chewing in patients with head and neck cancer receiving immediate implant placement (during tumor ablation surgery) compared to delayed implant placement (after tumor ablation surgery).
Source: Wetzels 2016 |
3. Moment of completing rehabilitation – critical outcome
|
Very low GRADE |
The evidence is very uncertain about the effect of immediate implant placement (during tumor ablation surgery) on time to overdenture placement compared to delayed implant placement in patients with heck and neck cancer.
Sources: Mizbah, 2013; Wetzels, 2017; Woods, 2019, Tumuluri, 2023; McMillan, 2023 |
|
Very low GRADE |
The evidence is very uncertain about the effect of immediate implant placement (during tumor ablation surgery) on successful overdenture placement compared to delayed implant placement in patients with heck and neck cancer.
Sources: Mizbah, 2013; Wetzels, 2017; Woods, 2019, Tumuluri, 2023 |
4. Quality of life – critical outcome
|
No GRADE |
No evidence was found regarding the outcome quality of life in patients with head and neck cancer receiving implants during tumor ablation surgery compared to placing implants after surgery. |
5. Bite force – important outcome
|
Very low GRADE |
The evidence is very uncertain about the effect of immediate implant placement (during tumor ablation surgery) on the outcome bite force compared to delayed implant placement (after tumor ablation surgery) in patients with head and neck cancer.
Source: Wetzels, 2016 |
6. Swallowing – important outcome
|
No GRADE |
No evidence was found regarding the outcome swallowing in patients with head and neck cancer receiving implants during tumor ablation surgery compared to implant placement after surgery. |
7. Speech – important outcome
|
No GRADE |
No evidence was found regarding the outcome speech in patients with head and neck cancer receiving implants during surgery compared to implant placement after surgery. |
I2 versus C2 of the PICO question question (implant placement before versus after (chemo)radiotherapy in patients who do not undergo surgery)
|
No GRADE |
No evidence was found regarding all the outcomes in patients with head and neck cancer receiving implants before (chemo)radiotherapy (in patients who do not undergo surgery) compared to implant placement after (chemo)radiotherapy (in patients who do not undergo surgery). |
Subquestion 2 (extra-oral implants):
No studies were included in the analysis of the literature.
Description of studies
Subquestion 1 (intra-oral implants):
A systematic review by In ‘t Veld (2021) identified and critically appraised the treatment outcomes of immediate placement and loading of dental implants in the edentulous mandible, as well as the performance of overdentures in patients with head and neck cancer (In ‘t Veld, 2021). For the purpose of this guideline, only the four studies comparing immediate (i.e., during tumor ablation surgery) versus delayed (i.e., postoperative) dental implant placement were included (Mizbah, 2013; Wetzels, 2016; Wetzels, 2017; Woods, 2019). Study characteristics are summarized in Table 2. In addition to the four studies included in the systematic review of In ‘t Veld (2021), two more studies - McMillan (2022) and Tumuluri (2023) were included into the current analysis for the guideline.
Table 2. Study characteristics
|
First author (year) |
Cancer diagnosis and treatment |
Number of subjects - (DAS/P) |
No. implants placed: DAS/P |
Population characteristics |
Timing implant placement & Radiotherapy (DAS) |
Timing implant placement & Radiotherapy (P) |
Outcome measures |
Comments |
|
Mizbah, 2013 |
Oral cavity – surgery with or without postoperative RT |
99/29 |
249/65 |
Male/Female 294/216 (this is the ratio for the total group of patients included in this study, information for subgroup that complies with our PICO was not available) Mean age (SD) Not reported |
N= 47/99 RT after surgery (within 6 weeks) N= 52/99 no RT after surgery |
N= 17/29 RT before implant placement; N= 12/29 no RT after surgery/before implant placement |
-Time to overdenture placement (reported as time of becoming functional (i.e. the time of abutment placement)) -Successful overdenture placement |
|
|
Wetzels, 2016 |
Oral cavity – surgery with or without postoperative RT |
18/9 |
40/19 |
Male/Female DAS:15/8 P: 18/15
Mean age (SD) DAS: 67.95 (11.4) P: 70.95 (9.8)
Primary tumor location (%) Maxilla DAS : 2 (12) P : 8 (22) Mandible DAS : 11 (46) P : 16 (50) FOM or tongue DAS : 10 (42) P : 9 (28)
(these are the ratios for the total group of patients included in this study, information for subgroup that complies with our PICO was not available) |
N= 16/23 RT after surgery (within 6 weeks) N= 7/23 no RT after surgery (this is the ratio for the total group of patients included in this study, information for subgroup that complies with our PICO was not available) |
N= 18/33 RT before implant placement; N= 15/33 no RT after surgery/before implant placement (this is the ratio for the total group of patients included in this study, information for subgroup that complies with our PICO was not available) |
-Masticatory performance (mixing ability test) -Bite force |
Same cohort as Wetzels (2017) |
|
Wetzels, 2017 |
Oral cavity – surgery with or without postoperative RT |
79/18 |
225/43 |
Male/Female DAS: 55/43 P: 49/46
Mean age (SD) DAS: 66.25 (11.5) P: 66.25 (11.5)
Primary tumor location (%) Maxilla DAS: 6 (6) P: 11(12)
Lower alveolar process DAS: 24 (25) P: 26 (27)
Cheek DAS: 8 (8) P: 9 (10)
Tongue DAS: 17 (28) P: 24 (25)
FOM DAS: 29 (30) P: 24 (25)
Lip DAS: 4 (4) P: 1 (1) (these are the ratios for the total group of patients included in this study, information for subgroup that complies with our PICO was not available) |
N= 54/98 RT after surgery (within 6 weeks) N= 44/98 no RT after surgery |
N= 50/95 RT before implant placement; N= 45/95 no RT after surgery/before implant placement |
-ORN -Time to overdenture placement -Successful overdenture placement |
Same cohort as Wetzels (2016) |
|
Woods, 2019 |
Tumors of the jaws – surgery with or without postoperative RT |
20 (NR/NR) |
39/63 |
Male/Female 13/7
Mean age (range) 56 (17-91) |
Postoperative radiotherapy (PORT) was administered to 10 patients No additional information was provided in the paper. |
-Time to overdenture placement -Successful overdenture placement |
|
|
|
McMillan, 2023 |
Oral cavity – surgery with or without adjuvant therapy (RT, CRT or chemo) |
33 (15/18) |
unknown |
Male/Female DAS: 7/8 P: 11/7
Mean age (SD) DAS: 55.6 (13.81) P: 55.6 (13.81) |
6/15 patients received no adjuvant therapy 9/15 patients received adjuvant radiotherapy 2/15 received adjuvant chemotherapy |
Postponed-placement protocol 6/18 patients received no adjuvant therapy 8/18 patients received adjuvant radiotherapy 6/18 received adjuvant chemotherapy |
-ORN -Time to overdenture placement |
|
|
Tumuluri, 2023 |
Unknown- Surgery (mandible resection and vascularised free bone flaps with or without pre or postoperative RT |
34/18 |
123/64 |
Male/Female DAS: 20/14 P: 6/12
Mean age DAS: 58.4 P: 57.6
Reason for surgery (%) Malignancy DAS: 28 (82.4) P: 11 (61.1)
Osteoradionecrosis DAS: 3 (8.8) P: 4 (22.2)
Defect following previous surgery DAS: 3 (8.8) P: 3 (17) |
21/34 patients received no adjuvant therapy (of which 3 had ORN due to previous RT) 13/34 patients received surgery and radiotherapy |
14/18 patients received no adjuvant therapy (of which 4 had ORN due to previous RT) 4/18 patients received surgery and radiotherapy |
-ORN -Time to overdenture placement -Successful overdenture placement |
|
FOM: floor of mouth; DAS: placement during tumor ablation surgery (Intervention); P: placement postponed(Control)
Subquestion 2 (extra-oral implants):
No studies were included in the analysis of the literature.
Results
Subquestion 1 (intra-oral implants):
I1 versus C1 of the PICO question (implant placement during versus after tumor ablation surgery)
1. ORN – critical outcome
Wetzels (2017) reported that ORN occurred in both the immediate placement group (i.e., implants placed during tumor ablation surgery; five patients affected with ORN of which four with implants) and the delayed placement group (five patients affected with ORN of which none with implants).
McMillan (2023) reported that ORN occurred in both the immediate placement group (i.e., implants placed during tumor ablation surgery (four of the nine patients (37.5%) that received adjuvant RT affected with ORN of which four with implants) and the delayed placement group (three patients of the eight (44.4%) that received adjuvant RT affected with ORN of which three with implants) (p=1.000).
Tumuluri (2023) reported a single case of ORN in the delayed group and no cases in the immediate placement group.
The findings of these studies illustrate that while ORN can occur in both timing strategies, no consistent advantage of one approach over the other has been demonstrated in terms of ORN risk reduction. However, the sample size is too small for any definitive conclusions. It should also be noted that the results of these studies do not provide sufficient clarity regarding the timing of onset of ORN and the role that implant placement played in the development of ORN. This lack of information applies to both the immediate and delayed implant placement groups.
2. Masticatory performance/masticatory ability/chewing – critical outcome
Wetzels (2016) evaluated masticatory performance using a validated mixing ability test. This test utilizes a bilayered red and blue wax tablet; upon mastication, the degree of color mixing is quantified on a linear scale from 0 (optimal mixing) to 30 (no mixing).
Using a linear mixed-effects model, the authors included the following variables: denture type (conventional denture, implant-retained overdenture (IOD), or no functional prosthesis), time since surgery (0.5, 1, and 5 years), and radiotherapy. The study reports that patients in the delayed placement group with an IOD demonstrated significantly poorer masticatory performance compared to those who received IODs on implants placed during tumor ablation surgery (p = .001). This suggests that implant placement during surgery may yield superior long-term functional outcomes in terms of masticatory performance. However, data was provided in a figure, and absolute numbers were not available. For this reason, we cannot determine if these results are clinically relevant.
3. Moment of completing rehabilitation – critical outcome
Time to overdenture placement
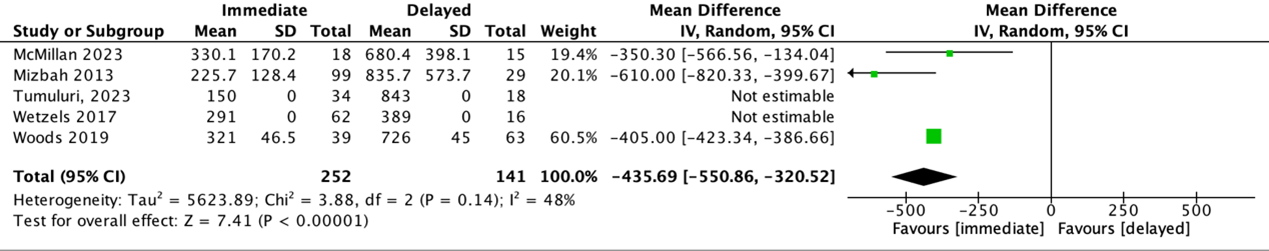
Five studies reported the interval between tumor ablation surgery and final overdenture placement (McMillan, 2023; Mizbah, 2013; Wetzels, 2017; Woods, 2019; Tumuluri, 2023) (Figure 1).
The pooled mean difference in time to overdenture placement was −435.69 days (95% CI: −550.86 to −320.52), favoring the immediate implant placement approach. This difference is considered clinically relevant, highlighting the substantial delay in rehabilitation associated with secondary implant placement.
Figure 1. Forest plot of risk ratio of immediate (during tumor ablation surgery) versus delayed (postponed) implant placement regarding the outcome measure Time to overdenture placement in patients with head or neck cancer
Successful overdenture placement
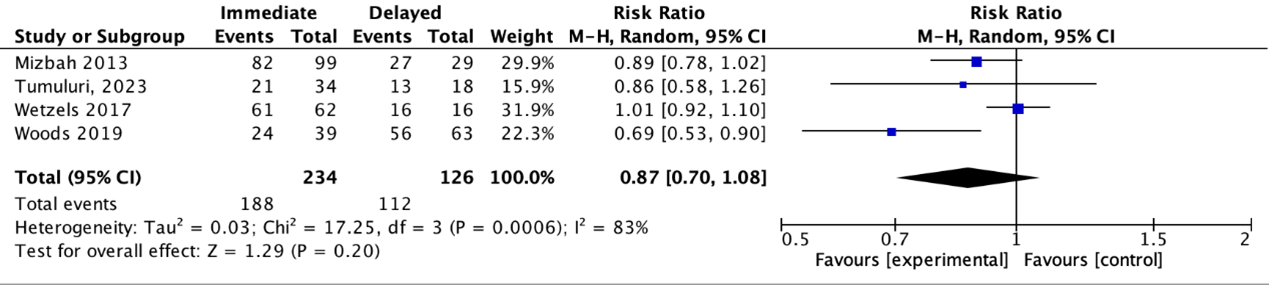
Four studies reported on the rate of successful overdenture placement in patients receiving either immediate (during tumor ablation surgery) or delayed implant placement (Mizbah, 2013; Wetzels, 2017; Woods, 2019; Tumuluri, 2023) (Figure 2). The pooled risk ratio for successful overdenture placement was 0.87 (95% CI: 0.70 to 1.08), with a high degree of heterogeneity (I2) 83%). This result indicates a 13% lower probability of successful overdenture placement in the delayed-placement group compared to the immediate-placement group (during tumor ablation surgery). This difference is considered clinically relevant, highlighting the substantial lower probability of successful rehabilitation associated with secondary implant placement.
Figure 2. Forest plot of risk ratio of immediate (during tumor ablation surgery) versus delayed (postponed) implant placement regarding the outcome measure Successful overdenture placement in patients with head or neck cancer
4. Quality of life – critical outcome
Quality of life was not reported in the included studies.
5. Bite force – important outcome
Wetzels (2016) reported that at the 5-year follow-up, bite force was significantly greater in patients who received implant-supported overdentures placed during tumor ablation surgery, compared to those in the delayed implantation group (p < .001). This suggests a potential long-term functional advantage associated with immediate implant placement.
6. Swallowing – important outcome
Swallowing was not reported in the included studies.
7. Speech – important outcome
Speech was not reported in the included studies.
In all included studies (Table 2), subgroup C1 (implant placement after tumor ablation surgery) comprised a heterogeneous mix of patients who had or had not received postoperative (chemo)radiotherapy. These patients were analyzed as a single group, despite the fact that a subgroup analysis based on the timing of (chemo)radiotherapy—specifically, implant placement before or after adjuvant (postoperative) (chemo)radiotherapy—would have been warranted. Distinguishing between these subgroups is essential, as implant placement following adjuvant (chemo)radiotherapy is likely associated with an increased risk of adverse outcomes across all measured endpoints.
I2 versus C2 of the PICO question (implant placement before versus after (chemo)radiotherapy in patients who do not undergo surgery).
No studies were found regarding the comparison between implant placement before versus after primary (chemo)radiotherapy.
Subquestion 2 (extra-oral implants):
No studies were included in the analysis of the literature.
Level of evidence of the literature
Subquestion 1 (intra-oral implants):
I1 versus C1 of the PICO question (implant placement during versus after tumor ablation surgery).
1. ORN – critical outcome
The level of evidence regarding the outcome ORN was downgraded by one level to VERY LOW because of low number of events (imprecision).
2. Masticatory performance/masticatory ability/chewing – critical outcome
Due to the lack of multiple comparative studies and data, the level of evidence could not be assessed using the GRADE methodology.
3. Moment of completing rehabilitation – critical outcome
Timing of overdenture placement
The level of evidence regarding the outcome measure timing of overdenture placement was downgraded by one level to VERY LOW because of risk of bias (heterogeneity in study population).
Successful overdenture placement
The level of evidence regarding the outcome measure successful overdenture placement was downgraded by one level to VERY LOW because of imprecision (95% CI crossing the boundaries of clinical relevance).
4. Quality of life – critical outcome
Due to the lack of comparative studies, the level of evidence could not be assessed using the GRADE methodology.
5. Bite force – important outcome
The level of evidence regarding the outcome measure bite force was downgraded by one level to VERY LOW because of risk of bias (heterogeneity in study population).
6. Swallowing – important outcome
Due to the lack of comparative studies, the level of evidence could not be assessed using the GRADE methodology.
7. Speech – important outcome
Due to the lack of comparative studies, the level of evidence could not be assessed using the GRADE methodology.
I2 versus C2 of the PICO question (implant placement before versus after (chemo)radiotherapy in patients who do not undergo surgery).
No studies were included the analysis of the literature.
Subquestion 2 (extra-oral implants):
No studies were included in the analysis of the literature.
A systematic review of the literature was performed to answer the following question:
What are the risks and benefits of placing implants during tumor ablation surgery compared to placing implants after surgery (before and after radiotherapy) in patients with head and neck cancer?
| P (Patients): |
Patients with head and neck cancer/patients with oropharyngeal cancer/patients with oral cancer having a need for prosthetic orofacial or maxillofacial rehabilitation |
| I1 (Intervention): |
Implant placement during tumor ablation surgery (non-irradiated bone) |
| I2: |
Implant placement before (chemo)radiotherapy (in patients who do not undergo surgery) |
| C1 (Comparison): |
Implant placement after tumor ablation surgery with or without adjuvant therapy |
| C2 |
Implant placement after (chemo)radiotherapy (in patients who do not undergo surgery) |
| O (Outcomes): |
ORN, masticatory performance/masticatory ability/chewing, moment of completing rehabilitation, QoL, bite force, swallowing and speech |
Relevant outcome measures
The guideline development group considered ORN, masticatory performance/masticatory ability/chewing, moment of completing rehabilitation, and QoL as critical outcome measures for decision making; and bite force, swallowing, and speech as important outcome measures for decision making.
A priori, the guideline development group did not define the outcome measures listed above but used the definitions used in the studies (Table 1).
The guideline development group defined minimal clinically important differences for patients with head and neck cancer for each outcome measure as follows:
Table 1. Outcome measures and minimal clinically important differences
|
Outcome |
Measurement method/ operationalization |
Minimal clinically important difference |
|
Clinical prevalence rate |
Unclear - a 10% relative difference for dichotomous outcomes (ORN present/absent)(RR < 0.9 or > 1.1) |
|
Mixing ability test (MAT) (Vermaire, 2020) |
A change of 2,12 points in the score |
|
Overdenture placement: -Time to overdenture placement in months
-Successful overdenture placement |
-Unclear - a mean difference of 1 month
-Unclear - a 10% relative difference for dichotomous outcomes (successful/unsuccessful overdenture placement)(RR < 0.9 or > 1.1) |
|
Not reported |
- |
|
The maximum vertical interocclusal bite forces (N) during unilateral intermittent clenching (Ganesan, 2024) |
Unclear for patients with head and neck cancer - a change of 25% in the score A gain in maximum vertical interocclusal bite force of 147.9–159.1 N is clinically relevant for patients treated for maxillofacial trauma (Ganesan, 2024) |
|
Not reported |
See Module Slikfunctiebehoud via prehabilitatie en revalidatie |
|
Not reported |
See Module Stem- en spraakfunctiebehoud via prehabilitatie en revalidatie |
Search and select (Methods)
Subquestion 1 (intra-oral implants):
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until 14 July 2024. The detailed search strategy is available on request (info@richtlijnendatabase.nl). The systematic literature search resulted in 619 hits. Studies were selected based on the following criteria:
- Systematic reviews searched in at least two databases (only reviews with a detailed search strategy, risk of bias assessment, and results of individual studies available).
- Randomized controlled trials (RCTs) and observational studies answering the search question.
- Published in English.
- Published between January 1st 2000 and July 14th 2024.
Exclusion criteria included animal or cadaveric studies and articles that did not constitute original research (e.g., case reports, editorials, letters to the editor, oral presentations, posters, and conference abstracts).
Twenty-one systematics reviews, seven RCTs, and twenty-two non-randomized studies were initially selected based on title and abstract screening. After reading the full text, twenty systematic reviews, seven RCTs, and twenty non-randomized studies were excluded (see the Table with reasons for exclusion), leaving one systematic review (including four studies) and two non-randomized studies to be included.
Subquestion 2 (extra-oral implants):
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until 14 July 2024. The detailed search strategy is available on request (info@richtlijnendatabase.nl). The systematic literature search resulted in 878 hits. Studies were selected based on the following criteria:
- Systematic reviews searched in at least two databases (only reviews with a detailed search strategy, risk of bias assessment, and results of individual studies available).
- RCTs and observational studies answering the search question.
- Published in English.
- Published between January 1st 2000 and July 14th 2024.
Exclusion criteria included animal or cadaveric studies and articles that did not constitute original research (e.g., case reports, editorials, letters to the editor, oral presentations, posters, and conference abstracts).
Eighteen studies were initially selected based on title and abstract screening. After reading the full text, all studies were excluded (see the Table with reasons for exclusion).
Results
Subquestion 1 (intra-oral implants):
Six studies were included in the analysis of the literature. Important study characteristics and results are summarized (Table 2). The assessment of the risk of bias is summarized in the risk of bias Tables.
Subquestion 2 (extra-oral implants):
No studies were included in the analysis of the literature.
- Alberga J, Eggels I, Visser A, van Minnen B, Korfage A, Vissink A, Raghoebar G. Outcome of implants placed to retain craniofacial prostheses - A retrospective cohort study with a follow-up of up to 30 years. Clin Implant Dent Relat Res. 2022 Oct;24(5):643-654. doi: 10.1111/cid.13106. Epub 2022 Jun 14. PMID: 35699941; PMCID: PMC9796566.
- Ariani N, Visser A, van Oort RP, Kusdhany L, Rahardjo TB, Krom BP, van der Mei HC, Vissink A. Current state of craniofacial prosthetic rehabilitation. Int J Prosthodont. 2013 Jan-Feb;26(1):57-67. doi: 10.11607/ijp.3220. PMID: 23342336.
- Butterworth CJ, Lowe D, Rogers SN. The Zygomatic Implant Perforated (ZIP) flap reconstructive technique for the management of low-level maxillary malignancy - clinical & patient related outcomes on 35 consecutively treated patients. Head Neck. 2022;44(2):345-58. Epub 20211126. doi: 10.1002/hed.26933. PubMed PMID: 34825746.
- Butterworth CJ, Rogers SN. The zygomatic implant perforated (ZIP) flap: a new technique for combined surgical reconstruction and rapid fixed dental rehabilitation following low-level maxillectomy. Int J Implant Dent. 2017;3(1):37. Epub 20170729. doi: 10.1186/s40729-017-0100-8. PubMed PMID: 28756563; PubMed Central PMCID: PMC5534193.
- Buurman DJM, Speksnijder CM, de Groot RJ, Kessler P, Rieger JM. Mastication in maxillectomy patients: A comparison between reconstructed maxillae and implant supported obturators: A cross-sectional study. J Oral Rehabil. 2020a;47(9):1171-7. Epub 20200713. doi: 10.1111/joor.13043. PubMed PMID: 32613633; PubMed Central PMCID: PMC7497273.
- Buurman DJM, Speksnijder CM, Engelen B, Kessler P. Masticatory performance and oral health-related quality of life in edentulous maxillectomy patients: A cross-sectional study to compare implant-supported obturators and conventional obturators. Clin Oral Implants Res. 2020b;31(5):405-16. Epub 20200127. doi: 10.1111/clr.13577. PubMed PMID: 31944417; PubMed Central PMCID: PMC7319476.
- Chang TL, Garrett N, Roumanas E, Beumer J, 3rd. Treatment satisfaction with facial prostheses. J Prosthet Dent. 2005;94(3):275-80. doi: 10.1016/j.prosdent.2005.06.002. PubMed PMID: 16126080.
- Dings JP, Maal TJ, Muradin MS, Ingels KJ, Klevering BJ, Koole R, Merkx MA, Meijer GJ. Extra-oral implants: insertion per- or post-ablation? Oral Oncol. 2011 Nov;47(11):1074-8. doi: 10.1016/j.oraloncology.2011.07.015. Epub 2011 Aug 10. PMID: 21835682.
- Dings JPJ, Merkx MAW, de Clonie Maclennan-Naphausen MTP, van de Pol P, Maal TJJ, Meijer GJ. Maxillofacial prosthetic rehabilitation: A survey on the quality of life. J Prosthet Dent. 2018;120(5):780-6. doi: 10.1016/j.prosdent.2018.03.032. PubMed PMID: 30414646.
- Dugast S, Longis J, Anquetil M, Corre P, Komarova S, Bertin H. Assessing Dental Implant Success: A Systematic Review and Meta-Analysis of Primary Versus Secondary Implantation in Free Bone Flap Reconstruction for Malignant Tumors. Head Neck. 2025;47(4):1277-90. Epub 20241231. doi: 10.1002/hed.28059. PubMed PMID: 39737519.
- Duke RL, Campbell BH, Indresano AT, Eaton DJ, Marbella AM, Myers KB, Layde PM. Dental status and quality of life in long-term head and neck cancer survivors. Laryngoscope. 2005 Apr;115(4):678-83. doi: 10.1097/01.mlg.0000161354.28073.bc. PMID: 15805880.
- Elledge R, Chaggar J, Knapp N, Martin T, White N, Evriviades D, Edmondson S, Parmar S. Craniofacial implants at a single centre 2005-2015: retrospective review of 451 implants. Br J Oral Maxillofac Surg. 2017 Apr;55(3):242-245. doi: 10.1016/j.bjoms.2016.11.324. Epub 2017 Feb 16. Erratum in: Br J Oral Maxillofac Surg. 2018 Jan;56(1):83. doi: 10.1016/j.bjoms.2017.09.014. PMID: 28216308.
- Fenlon MR, Lyons A, Farrell S, Bavisha K, Banerjee A, Palmer RM. Factors affecting survival and usefulness of implants placed in vascularized free composite grafts used in post-head and neck cancer reconstruction. Clin Implant Dent Relat Res. 2012;14(2):266-72. Epub 20091016. doi: 10.1111/j.1708-8208.2009.00250.x. PubMed PMID: 19843102.
- Ganesan A, Rustagi N, Kaur A, Chaudhry K, Kumar P, Chopane S, Chugh A. Minimal clinically important difference in maxillofacial trauma patients: a prospective cohort study. Br J Oral Maxillofac Surg. 2024 Feb;62(2):177-183. doi: 10.1016/j.bjoms.2023.11.016. Epub 2023 Dec 5. PMID: 38336576.
- Garner SJ, Patel S, Pollard AJ, Jerreat MP. Post-treatment evaluation of oral health-related quality of life in head and neck cancer patients after dental implant rehabilitation. Br Dent J. 2023. Epub 20230124. doi: 10.1038/s41415-023-5460-2. PubMed PMID: 36693964.
- Hackett S, El-Wazani B, Butterworth C. Zygomatic implant-based rehabilitation for patients with maxillary and mid-facial oncology defects: A review. Oral Dis. 2021;27(1):27-41. Epub 20200305. doi: 10.1111/odi.13305. PubMed PMID: 32048429.
- Harris D, Höfer S, O'Boyle CA, Sheridan S, Marley J, Benington IC, Clifford T, Houston F, O'Connell B. A comparison of implant-retained mandibular overdentures and conventional dentures on quality of life in edentulous patients: a randomized, prospective, within-subject controlled clinical trial. Clin Oral Implants Res. 2013 Jan;24(1):96-103. doi: 10.1111/j.1600-0501.2011.02368.x. Epub 2011 Nov 24. PMID: 22111872.
- Ihde S, Kopp S, Gundlach K, Konstantinovic VS. Effects of radiation therapy on craniofacial and dental implants: a review of the literature. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2009;107(1):56-65. Epub 20080828. doi: 10.1016/j.tripleo.2008.06.014. PubMed PMID: 18755611.
- In 't Veld M, Schulten E, Leusink FKJ. Immediate dental implant placement and restoration in the edentulous mandible in head and neck cancer patients: a systematic review and meta-analysis. Curr Opin Otolaryngol Head Neck Surg. 2021;29(2):126-37. doi: 10.1097/MOO.0000000000000685. PubMed PMID: 33278135; PubMed Central PMCID: PMC7969163.
- Johal M, Leinkram D, Wallace C, Clark JR. The Sydney Modified Alberta Reconstruction Technique (SM-ART) for dental rehabilitation following mandibulectomy or maxillectomy. Int J Oral Maxillofac Surg. 2021;50(5):615-8. Epub 20201014. doi: 10.1016/j.ijom.2020.09.013. PubMed PMID: 33069518.
- Kanatas A, Lowe D, Rogers SN. The Patient Concerns Inventory in head and neck oncology: a structured review of its development, validation and clinical implications. Eur Arch Otorhinolaryngol. 2022;279(11):5097-111. Epub 20220717. doi: 10.1007/s00405-022-07499-0. PubMed PMID: 35842858; PubMed Central PMCID: PMC9519723.
- Korfage A, Raghoebar GM, Slater JJ, Roodenburg JL, Witjes MJ, Vissink A, Reintsema H. Overdentures on primary mandibular implants in patients with oral cancer: a follow-up study over 14 years. Br J Oral Maxillofac Surg. 2014 Nov;52(9):798-805. doi: 10.1016/j.bjoms.2014.05.013. Epub 2014 Jun 17. Erratum in: Br J Oral Maxillofac Surg. 2015 Apr;53(4):e23-5. PMID: 24951245.
- Kwakman JM, Freihofer HP, van Waas MA. Osseointegrated oral implants in head and neck cancer patients. Laryngoscope. 1997;107(4):519-22. doi: 10.1097/00005537-199704000-00016. PubMed PMID: 9111383.
- McMillan DC, McMillan KB, Lee SKY, Vierkant RA, Salinas TJ, Ettinger K, Arce K. What is the Incidence of Oral Cancer Recurrence in Patients Reconstructed With a Microvascular Free Flap, Endosseous Implants, and an Oral Prosthesis and How Does the Timing of Implant Placement Influence Recurrence? J Oral Maxillofac Surg. 2023 Jan;81(1):120-128. doi: 10.1016/j.joms.2022.09.005. Epub 2022 Sep 10. PMID: 36209893.
- Menapace DC, Van Abel KM, Jackson RS, Moore EJ. Primary vs Secondary Endosseous Implantation After Fibular Free Tissue Reconstruction of the Mandible for Osteoradionecrosis. JAMA Facial Plast Surg. 2018;20(5):401-8. doi: 10.1001/jamafacial.2018.0263. PubMed PMID: 29801119; PubMed Central PMCID: PMC6233614.
- Mizbah K, Dings JP, Kaanders JH, van den Hoogen FJ, Koole R, Meijer GJ, Merkx MA. Interforaminal implant placement in oral cancer patients: during ablative surgery or delayed? A 5-year retrospective study. Int J Oral Maxillofac Surg. 2013 May;42(5):651-5. doi: 10.1016/j.ijom.2012.09.013. Epub 2012 Oct 24. PMID: 23102901.
- Rogers SN, McNally D, Mahmoud M, Chan MF, Humphris GM. Psychologic response of the edentulous patient after primary surgery for oral cancer: A cross-sectional study. J Prosthet Dent. 1999;82(3):317-21. doi: 10.1016/s0022-3913(99)70087-9. PubMed PMID: 10479259.
- Rogers SN, Panasar J, Pritchard K, Lowe D, Howell R, Cawood JI. Survey of oral rehabilitation in a consecutive series of 130 patients treated by primary resection for oral and oropharyngeal squamous cell carcinoma. Br J Oral Maxillofac Surg. 2005;43(1):23-30. doi: 10.1016/j.bjoms.2004.08.020. PubMed PMID: 15620770.
- Rohner D, Bucher P, Hammer B. Prefabricated fibular flaps for reconstruction of defects of the maxillofacial skeleton: planning, technique, and long-term experience. Int J Oral Maxillofac Implants. 2013;28(5):e221-9. doi: 10.11607/jomi.te01. PubMed PMID: 24066339.
- Roumanas ED, Chang TL, Beumer J. Use of osseointegrated implants in the restoration of head and neck defects. J Calif Dent Assoc. 2006;34(9):711-8. PubMed PMID: 17022295.
- Schiegnitz E, Müller LK, Sagheb K, Theis L, Cagiran V, Kämmerer PW, Wegener J, Wagner W, Al-Nawas B. Clinical long-term and patient-reported outcomes of dental implants in oral cancer patients. Int J Implant Dent. 2021 Jul 13;7(1):93. doi: 10.1186/s40729-021-00373-4. PMID: 34255187; PMCID: PMC8276905.
- Schoen PJ, Raghoebar GM, Bouma J, Reintsema H, Burlage FR, Roodenburg JL, Vissink A. Prosthodontic rehabilitation of oral function in head-neck cancer patients with dental implants placed simultaneously during ablative tumour surgery: an assessment of treatment outcomes and quality of life. Int J Oral Maxillofac Surg. 2008 Jan;37(1):8-16. doi: 10.1016/j.ijom.2007.07.015. Epub 2007 Sep 4. PMID: 17766084.
- Schoen PJ, Raghoebar GM, van Oort RP, Reintsema H, van der Laan BF, Burlage FR, Roodenburg JL, Vissink A. Treatment outcome of bone-anchored craniofacial prostheses after tumor surgery. Cancer. 2001 Dec 15;92(12):3045-50. doi: 10.1002/1097-0142(20011215)92:12<3045::aid-cncr10147>3.0.co;2-k. PMID: 11753982.
- Seikaly H, Idris S, Chuka R, Jeffery C, Dzioba A, Makki F, Logan H, O'Connell DA, Harris J, Ansari K, Biron V, Cote D, Osswald M, Nayar S, Wolfaardt J. The Alberta Reconstructive Technique: An Occlusion-Driven and Digitally Based Jaw Reconstruction. Laryngoscope. 2019 Dec;129 Suppl 4:S1-S14. doi: 10.1002/lary.28064. Epub 2019 Jun 26. PMID: 31241771.
- Subramaniam SS, Breik O, Cadd B, Peart G, Wiesenfeld D, Heggie A, Gibbons SD, Nastri A. Long-term outcomes of craniofacial implants for the restoration of facial defects. Int J Oral Maxillofac Surg. 2018 Jun;47(6):773-782. doi: 10.1016/j.ijom.2018.01.013. Epub 2018 Feb 7. PMID: 29428340.
- Sumida T, Kobayashi Y, Ishikawa A, Shinohara K, Matsumoto E, Kamakura S, Mori Y. Bite Force and Masticatory Performance Using Implant-supported Overdentures After Treatment of Mandibular Cancer. Anticancer Res. 2016 Aug;36(8):4077-80. PMID: 27466516.
- Tumuluri V, Charters E, Venchiarutti RL, Leinkram D, Froggatt C, Dunn M, Wykes J, Singh J, Hubert Low TH, Palme CE, Howes D, Ch'ng S, Clark JR. Quality of life outcomes in patients receiving dental implants in vascularised bone flaps for mandibular reconstruction. Br J Oral Maxillofac Surg. 2025 Jan;63(1):32-38. doi: 10.1016/j.bjoms.2024.04.017. Epub 2024 May 23. PMID: 39550329.
- Tumuluri V, Leinkram D, Froggatt C, Dunn M, Wykes J, Singh J, Low TH, Palme CE, Howes D, Clark JR. Outcomes of immediate dental implants in vascularised bone flaps for mandibular reconstruction. ANZ J Surg. 2023 Jun;93(6):1682-1687. doi: 10.1111/ans.18427. Epub 2023 Apr 7. PMID: 37026415; PMCID: PMC10953371.
- Vermaire JA, Weinberg FM, Raaijmakers CPJ, Verdonck-de Leeuw IM, Terhaard CHJ, Speksnijder CM. Reliability of the mixing ability test testing masticatory performance in patients with head and neck cancer and healthy controls. J Oral Rehabil. 2020;47(8):961-6. Epub 20200620. doi: 10.1111/joor.13029. PubMed PMID: 32495364; PubMed Central PMCID: PMC7497093.
- Vosselman N, Alberga J, Witjes MHJ, Raghoebar GM, Reintsema H, Vissink A, Korfage A. Prosthodontic rehabilitation of head and neck cancer patients-Challenges and new developments. Oral Dis. 2021 Jan;27(1):64-72. doi: 10.1111/odi.13374. Epub 2020 May 26. PMID: 32343862; PMCID: PMC7818410.
- Wetzels JGH, Meijer GJ, de Haan AFJ, Merkx MAW, Speksnijder CM. Immediate implant placement in edentulous oral cancer patients: a long-term retrospective analysis of 207 patients. Int J Oral Maxillofac Surg. 2021;50(11):1521-8. Epub 20210226. doi: 10.1016/j.ijom.2021.01.015. PubMed PMID: 33642151.
- Wetzels JGH, Meijer GJ, Koole R, Adang EM, Merkx MAW, Speksnijder CM. Costs and clinical outcomes of implant placement during ablative surgery and postponed implant placement in curative oral oncology: a five-year retrospective cohort study. Clin Oral Implants Res. 2017;28(11):1433-42. Epub 20170302. doi: 10.1111/clr.13008. PubMed PMID: 28251678.
- Wetzels JW, Koole R, Meijer GJ, de Haan AF, Merkx MA, Speksnijder CM. Functional benefits of implants placed during ablative surgery: A 5-year prospective study on the prosthodontic rehabilitation of 56 edentulous oral cancer patients. Head Neck. 2016;38 Suppl 1:E2103-11. Epub 20160213. doi: 10.1002/hed.24389. PubMed PMID: 26873437.
- Witjes MJH, Schepers RH, Kraeima J. Impact of 3D virtual planning on reconstruction of mandibular and maxillary surgical defects in head and neck oncology. Curr Opin Otolaryngol Head Neck Surg. 2018;26(2):108-14. doi: 10.1097/MOO.0000000000000437. PubMed PMID: 29470184.
- Woods B, Schenberg M, Chandu A. A Comparison of Immediate and Delayed Dental Implant Placement in Head and Neck Surgery Patients. J Oral Maxillofac Surg. 2019;77(6):1156-64. Epub 20190213. doi: 10.1016/j.joms.2019.02.007. PubMed PMID: 30851250.
Risk of bias Table
|
Author, year |
Selection of participants
Was selection of exposed and non-exposed cohorts drawn from the same population?
|
Exposure
Can we be confident in the assessment of exposure?
|
Outcome of interest
Can we be confident that the outcome of interest was not present at start of study?
|
Confounding-assessment
Can we be confident in the assessment of confounding factors? |
Confounding-analysis
Did the study match exposed and unexposed for all variables that are associated with the outcome of interest or did the statistical analysis adjust for these confounding variables? |
Assessment of outcome
Can we be confident in the assessment of outcome?
|
Follow up
Was the follow up of cohorts adequate? In particular, was outcome data complete or imputed?
|
Co-interventions
Were co-interventions similar between groups?
|
Overall Risk of bias
|
|
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Definitely yes, probably yes, probably no, definitely no |
Low, Some concerns, High |
|
|
Mizbah, 2013 |
Definitely yes
Reason: From same hospital, same study cohort |
Definitely yes
Reason: Impossible otherwise. |
Definitely yes
Reason: Only possible after intervention. |
Probably yes
Reason: Not mentioned in article |
Definitely yes
Reason: Not applicable for this analysis |
Definitely yes
Reason: Not possible. |
Probably yes
Reason: No information in the article. |
Definitely yes
Reason: Radiotherapy was similar in both groups. |
Low |
|
Wetzels, 2016 |
Definitely yes
Reason: From same hospital, same study cohort |
Definitely yes
Reason: Impossible otherwise. |
Definitely yes
Reason: Only possible after intervention. |
Probably yes
Reason: Not mentioned in article |
Definitely yes
Reason: Not applicable for this analysis |
Definitely yes
Reason: Not possible. |
Definitely yes
Reason: Analysis was adjusted for loss of participants |
Definitely yes
Reason: Radiotherapy was similar in both groups. |
Low |
|
Wetzels, 2017 |
Definitely yes
Reason: From same hospital, same study cohort |
Definitely yes
Reason: Impossible otherwise. |
Definitely yes
Reason: Only possible after intervention. |
Probably yes
Reason: Not mentioned in article |
Definitely yes
Reason: Not applicable for this analysis |
Definitely yes
Reason: Not possible. |
Probably yes
Reason: No information in the article. |
Definitely yes
Reason: Radiotherapy was similar in both groups.
|
Low |
|
Woods, 2019 |
Definitely yes
Reason: From same hospital, same study cohort |
Definitely yes
Reason: Impossible otherwise. |
Definitely yes
Reason: Only possible after intervention. |
Probably yes
Reason: Not mentioned in article |
Definitely yes
Reason: Not applicable for this analysis |
Definitely yes
Reason: Not possible. |
Probably yes
Reason: No information in the article. |
Probably yes
Reason: No information in the article. |
Low |
|
Tumuluri, 2023 |
Definitely yes
Reason: From same hospital, same study cohort |
Definitely yes
Reason: Impossible otherwise. |
Definitely yes
Reason: Only possible after intervention. |
Probably yes
Reason: Not mentioned in article |
Definitely yes
Reason: Not applicable for this analysis |
Definitely yes
Reason: Not possible. |
Probably yes
Reason: No information in the article. |
Definitely yes
Reason: Radiotherapy was similar in both groups |
Low |
|
McMillan, 2023 |
Definitely yes
Reason: From same hospital, same study cohort |
Definitely yes
Reason: Impossible otherwise. |
Definitely yes
Reason: Only possible after intervention. |
Probably yes
Reason: Not mentioned in article |
Definitely yes
Reason: Not applicable for this analysis |
Definitely yes
Reason: Not possible. |
Probably yes
Reason: No information in the article. |
Definitely yes
Reason: Radiotherapy was similar in both groups |
Low |
Table of excluded studies
Subquestion 1
Systematic reviews
|
Reference |
Reason for exclusion |
|
Alberga, Jamie M. and Vosselman, Nathalie and Korfage, Anke and Delli, Konstantina and Witjes, Max J. H. and Raghoebar, Gerry M. and Vissink, Arjan What is the optimal timing for implant placement in oral cancer patients? A scoping literature review. Oral diseases. 2021; 27 (1) :94-110 |
Not a systematic review (only 1 database was searched) |
|
Atanasio Pitorro, Tassio Edno and de Araujo Reis, Nayara Teixeira and Paranhos, Luiz Renato and Ferreira Soares, Priscilla Barbosa Survival of Dental Implants Placed Pre-Radiotherapy Versus Post-Radiotherapy in Native Bone: A Systematic Review. The International journal of oral & maxillofacial implants. 2022; 37 (6) :1100-1109 |
Wrong I/C/O (Compares survival rates of implants placed pre- and post RDT compared to those without RDT) |
|
Kende, Prajwalit Prakash and Ranganath, Suleka and Landge, Jayant Shivaji and Sarda, Ashish and Wadewale, Maroti and Patil, Akshay and Singhavi, Hitesh R. Survival of Dental Implants on Irradiated Jaws: A Systematic Review and Meta-analysis. Journal of maxillofacial and oral surgery. 2022; 21 (3) :787-795 |
Wrong O (implant survival) |
|
Koudougou, Carine and Bertin, Helios and Lecaplain, Bastien and Badran, Zahi and Longis, Julie and Corre, Pierre and Hoornaert, Alain Postimplantation radiation therapy in head and neck cancer patients: Literature review. Head & neck. 2020; 42 (4) :794-802 |
Not a systematic review (only 1 database was searched) |
|
Shugaa-Addin, Bassam and Al-Shamiri, Hashem-Motahir and Al-Maweri, Sadeq and Tarakji, Bassel The effect of radiotherapy on survival of dental implants in head and neck cancer patients. Journal of clinical and experimental dentistry. 2016; 8 (2) :e194-200 |
Low quality review (only 1 database was searched and low quality search strategy) |
|
Abed, H. National and international guidelines on the replacement of missing teeth with dentures for head and neck cancer patients post-radiotherapy: A rapid review. Saudi Dental Journal. 2023; 35 (2) :125-132 |
Not a systematic review, but a collection of international guidelines on dental care |
|
Barber, A. J. and Butterworth, C. J. and Rogers, S. N. Systematic review of primary osseointegrated dental implants in head and neck oncology. The British journal of oral & maxillofacial surgery. 2011; 49 (1) :29-36 |
The review does not report information on outcome measures |
|
Bhandari, S. and Soni, B. W. and Jamwal, A. and Ghoshal, S. Oral and dental care before radiotherapy: Guidelines and development of a time-bound protocol. Indian Journal of Cancer. 2022; 59 (2) :159-169 |
Wrong article type: not a systematic review or RCT. Paper desribes a local protocol. |
|
Corrao G, Mazzola GC, Lombardi N, Marvaso G, Pispero A, Baruzzi E, Decani S, Tarozzi M, Bergamaschi L, Lorubbio C, Repetti I, Starzyńska A, Alterio D, Ansarin M, Orecchia R, D'Amore F, Franchini R, Nicali A, Castellarin P, Sardella A, Lodi G, Varoni EM, Jereczek-Fossa BA. Oral Surgery and Osteoradionecrosis in Patients Undergoing Head and Neck Radiation Therapy: An Update of the Current Literature. Biomedicines. 2023 Dec 18;11(12):3339. doi: 10.3390/biomedicines11123339. PMID: 38137559; PMCID: PMC10742198. |
Wrong study type: narrative review |
|
Gupta, S. and Mortellaro, C. and Panda, S. and Rovati, M. and Giacomello, M. S. and Colletti, L. and Greco Lucchina, A. and Del Fabbro, M. Dental implant survival rate in irradiated and non-radiated patients: a systematic review and meta-analysis. Journal of biological regulators and homeostatic agents. 2021; 35 (2) :53-65 |
Only one study was included that described one of the outcome measures of interest. This study will be assessed/included separately. |
|
Marques, Nelson Pereira and Perez-de-Oliveira, Maria Eduarda and Normando, Ana Gabriela Costa and Marques, Nadia Carolina Teixeira and Epstein, Joel B. and Migliorati, Cesar A. and Martelli-Junior, Hercilio and Ribeiro, Ana Carolina Prado and Rocha, Andre Caroli and Brandao, Thais Bianca and Sanchez, Francisco German Villanueva and Gueiros, Luiz Alcino Monteiro and Lopes, Marcio Ajudarte and Santos-Silva, Alan Roger Clinical outcomes of dental implants in head and neck cancer patients: An overview. Oral surgery, oral medicine, oral pathology and oral radiology. 2023; 136 (1) :42-53 |
Low quality review (no systematic report of results that meet our PICO) |
|
Nooh, Nasser Dental implant survival in irradiated oral cancer patients: a systematic review of the literature. The International journal of oral & maxillofacial implants. 2013; 28 (5) :1233-42 |
Wrong O (implant survival) |
|
Systematic review of literature: functional outcomes of implant-prosthetic treatment in patients with surgical resection for oral cavity tumors. Br Dent J. 2017 Aug 25;223(4):254. doi: 10.1038/sj.bdj.2017.709. PMID: 28840883. |
Provides no data on the outcome measures, only a general description. |
|
Shokouhi, Bizhan and Cerajewska, Tanya Radiotherapy and the survival of dental implants: a systematic review. The British journal of oral & maxillofacial surgery. 2022; 60 (4) :422-429 |
Wrong O (implant survival) |
|
Zarzar, Adriana Machado and Sales, Pedro Henrique da Hora and Barros, Ana Waleska Pessoa and Arreguy, Ingrid Melo Schuler and Carvalho, Alessandra Albuquerque Tavares and Leao, Jair Carneiro Effectiveness of dental implants in patients undergoing radiotherapy for head and neck cancer: An umbrella review. Special care in dentistry : official publication of the American Association of Hospital Dentists, the Academy of Dentistry for the Handicapped, and the American Society for Geriatric Dentistry. 2024; 44 (1) :40-56 |
Wrong I/C/O (does not compare the timing of implant placement) |
|
Colella, Giuseppe and Cannavale, Rosangela and Pentenero, Monica and Gandolfo, Sergio Oral implants in radiated patients: a systematic review. The International journal of oral & maxillofacial implants. 2007; 22 (4) :616-22 |
Conference abstract |
|
Hackett, Stephanie and El-Wazani, Basma and Butterworth, Chris Zygomatic implant-based rehabilitation for patients with maxillary and mid-facial oncology defects: A review. Oral diseases. 2021; 27 (1) :27-41 |
Low quality review (no search date provided, no systematic analysis of outcome measures) |
|
Jokstad, Asbjorn Patients undergoing craniofacial tumour ablation surgery may benefit from having the implants placed simultaneously instead of waiting. Evidence-based dentistry. 2010; 11 (2) :52-3 |
Not a systematic review (summary review) |
|
Schiegnitz, E. and Al-Nawas, B. and Kammerer, P. W. and Grotz, K. A. Oral rehabilitation with dental implants in irradiated patients: a meta-analysis on implant survival. Clinical oral investigations. 2014; 18 (3) :687-98 |
Not a aystematic review (comprehensive review, only 1 database was searched) |
|
Sriram, Shreya and Njoroge, Moreen W. and Lopez, Christopher D. and Zhu, Lily and Heron, Matthew J. and Zhu, Katherine J. and Yusuf, Cynthia T. and Yang, Robin Optimal Treatment Order With Fibula-Free Flap Reconstruction, Oncologic Treatment, and Dental Implants: A Systematic Review and Meta-Analysis. The Journal of craniofacial surgery. 2024; 35 (4) :1065-1073 |
Wrong O (implant survival) |
RCTs
|
Reference |
Reason for exclusion |
|
Korfage, Anke and Schoen, Pieter J. and Raghoebar, Gerry M. and Roodenburg, Jan L. N. and Vissink, Arjan and Reintsema, Harry Benefits of dental implants installed during ablative tumour surgery in oral cancer patients: a prospective 5-year clinical trial. Clinical oral implants research. 2010; 21 (9) :971-9 |
Wrong I/C (bij alle patienten zijn implantaten geplaatst, daarna vgl wel/niet radiotherapie gemaakt) |
|
Wetzels, Jan Willem and Koole, Ron and Meijer, Gert J. and de Haan, Anton F. J. and Merkx, Matthias A. W. and Speksnijder, Caroline M. Functional benefits of implants placed during ablative surgery: A 5-year prospective study on the prosthodontic rehabilitation of 56 edentulous oral cancer patients. Head & neck. 2016; 38 :E2103-11 |
Included in SR |
|
Doll, C. and Nack, C. and Raguse, J. D. and Stricker, A. and Duttenhoefer, F. and Nelson, K. and Nahles, S. Survival analysis of dental implants and implant-retained prostheses in oral cancer patients up to 20 years. Clinical oral investigations. 2015; 19 (6) :1347-1352 |
Wrong I/C/O (implant survival) |
|
Garrett, Neal and Roumanas, Eleni D. and Blackwell, Keith E. and Freymiller, Earl and Abemayor, Elliot and Wong, Weng Kee and Gerratt, Bruce and Berke, Gerald and Beumer, John, 3rd and Kapur, Krishan K. Efficacy of conventional and implant-supported mandibular resection prostheses: study overview and treatment outcomes. The Journal of prosthetic dentistry. 2006; 96 (1) :13-24 |
Describes study methods but no information on outcome measures |
|
Givens, Daniel J. and Karnell, Lucy Hynds and Gupta, Anjali K. and Clamon, Gerald H. and Pagedar, Nitin A. and Chang, Kristi E. and Van Daele, Douglas J. and Funk, Gerry F. Adverse events associated with concurrent chemoradiation therapy in patients with head and neck cancer. Archives of otolaryngology--head & neck surgery. 2009; 135 (12) :1209-17 |
Wrong I/C (no comparison) |
|
Talaat, M. A. The Influence of Radiation Therapy on Dental Implantation in Head and Neck Cancer Patients. Journal of Analytical Oncology. 2023; 12 :1-6 |
Wrong article type (not a RCT or systematic review, but low quality descriptive review) |
|
Visch, L. L. and van Waas, M. A. J. and Schmitz, P. I. M. and Levendag, P. C. A clinical evaluation of implants in irradiated oral cancer patients. Journal of dental research. 2002; 81 (12) :856-9 |
Wrong I/C/O (does not compare timing of implant placement, outcome measure is implant survival) |
Non-randomized studies
|
Reference |
Reason for exclusion |
|
Vosselman, N. and Kraeima, J. and Ng Wei Siang, K. and Raghoebar, G. M. and Witjes, M. J. H. and de Visscher, S. A. H. J. Guided placement of zygomatic implants in head and neck cancer patients: implant survival and patient outcomes at 1-3 years of follow-up. International journal of oral and maxillofacial surgery. 2024; 53 (7) :600-606 |
Wrong study type (no a comparative study) |
|
Alberga JM, Vissink A, Korfage A, de Visscher SAHJ, Witjes MJH, Langendijk JA, Raghoebar GM. Site-specific radiation dosage and implant survival in oral cancer patients: A cohort study. Oral Dis. 2024 Sep;30(6):3866-3872. doi: 10.1111/odi.14813. Epub 2023 Nov 20. PMID: 37983849. |
no comparison betweeon immediatie vs. delayed. |
|
Chang, Y. M. and Tsai, C. Y. and Wei, F. C. Fibula Jaw-during-Admission. Journal of Plastic, Reconstructive and Aesthetic Surgery. 2023; 82 :247-254 |
Wrong study type (no a comparative study) |
|
McCaul, L. K. and Barclay, S. and Nixon, P. and Yule, P. L. and Trainor, J. and Stevenson, B. and Paterson, A. and Nicol, A. and Keys, W. and Donachie, M. and Barker, D. and Rollings, S. and Killough, S. and Ban, J. and Chatzipantelis, A. and Gaitonde, P. and Ranka, M. and Ali, Z. and MacInnes, A. and Taylor, C. and Gopakumar, A. and Sharma, P. and Harper, V. and Rasaratnam, L. and Toor, I. and Rodriguez, J. M. Oral prehabilitation for patients with head and neck cancer: getting it right - the Restorative Dentistry-UK consensus on a multidisciplinary approach to oral and dental assessment and planning prior to cancer treatment. British dental journal. 2022; 233 (9) :794-800 |
Wrong study type (guideline) |
|
Rogers, Simon N. and Adatia, Ashni and Hackett, Stephanie and Boscarino, Angela and Patel, Anika and Lowe, Derek and Butterworth, Christopher J. Changing trends in the microvascular reconstruction and oral rehabilitation following maxillary cancer. European archives of oto-rhino-laryngology : official journal of the European Federation of Oto-Rhino-Laryngological Societies (EUFOS) : affiliated with the German Society for Oto-Rhino-Laryngology - Head and Neck Surgery. 2022; 279 (8) :4113-4126 |
Wrong study type (no a comparative study) |
|
Goker, F. and Beretta, P. and Baj, A. and Bolzoni, A. R. and Maiorana, C. and Beltramini, G. and Russillo, A. and Greco Lucchina, A. and Rossi, D. S. and Polo, M. R. D. and Del Fabbro, M. and Mortellaro, C. and Gianni, A. B. Oral rehabilitation of oncology patients with dental implants after reconstruction surgery with autogenous flaps. European review for medical and pharmacological sciences. 2022; 26 (3) :51-61 |
Wrong study type (no a comparative study) |
|
Kang, Yi-Fan and Ding, Meng-Kun and Qiu, Shi-Yu and Cai, Zhi-Gang and Zhang, Lei and Shan, Xiao-Feng Mandibular Reconstruction Using Iliac Flap Based on Occlusion-Driven Workflow Transferred by Digital Surgical Guides. Journal of oral and maxillofacial surgery : official journal of the American Association of Oral and Maxillofacial Surgeons. 2022; 80 (11) :1858-1865 |
Wrong I/C |
|
Lodders, Johannes N. and van Baar, Gustaaf J. C. and Vergeer, Marije R. and Jansen, Femke and Schulten, Engelbert A. J. M. and Lissenberg-Witte, Birgit I. and Verdonck-de Leeuw, Irma M. and Forouzanfar, Tymour and Leusink, Frank K. J. Implant-based dental rehabilitation in head and neck cancer patients after maxillofacial reconstruction with a free vascularized fibula flap: the effect on health-related quality of life. Supportive care in cancer : official journal of the Multinational Association of Supportive Care in Cancer. 2022; 30 (6) :5411-5420 |
Wrong I/C |
|
Petrides, George A. and Hicks, Gabrielle and Dunn, Masako and Froggatt, Catriona and Wallace, Christine and Howes, Dale and Leinkram, David and Low, Tsu-Hui Hubert and Ch'ng, Sydney and Wykes, James and Palme, Carsten E. and Clark, Jonathan R. Dentoalveolar outcomes in maxillary reconstruction: A retrospective review of 85 maxillectomy reconstructions. ANZ journal of surgery. 2021; 91 (7) :1472-1479 |
Wrong study type (no a comparative study) |
|
Schiegnitz, Eik and Muller, Lena Katharina and Sagheb, Keyvan and Theis, Lisa and Cagiran, Vahide and Kammerer, Peer W. and Wegener, Joachim and Wagner, Wilfried and Al-Nawas, Bilal Clinical long-term and patient-reported outcomes of dental implants in oral cancer patients. International journal of implant dentistry. 2021; 7 (1) :93 |
Wrong O (implant survival) |
|
Wetzels, J. G. H. and Meijer, G. J. and de Haan, A. F. J. and Merkx, M. A. W. and Speksnijder, C. M. Immediate implant placement in edentulous oral cancer patients: a long-term retrospective analysis of 207 patients. International journal of oral and maxillofacial surgery. 2021; 50 (11) :1521-1528 |
Wrong study type (no a comparative study) |
|
Alberga, Jamie M. and Korfage, Anke and Bonnema, Ilse and Witjes, Max J. H. and Vissink, Arjan and Raghoebar, Gerry M. Mandibular dental implant placement immediately after teeth removal in head and neck cancer patients. Supportive care in cancer : official journal of the Multinational Association of Supportive Care in Cancer. 2020; 28 (12) :5911-5918 |
wrong comparison (radiated vs. nonradiated) |
|
Allen, Robert J., Jr. and Nelson, Jonas A. and Polanco, Thais O. and Shamsunder, Meghana G. and Ganly, Ian and Boyle, Jay and Rosen, Evan and Matros, Evan Short-Term Outcomes following Virtual Surgery-Assisted Immediate Dental Implant Placement in Free Fibula Flaps for Oncologic Mandibular Reconstruction. Plastic and reconstructive surgery. 2020; 146 (6) :768e-776e |
Wrong O |
|
Patel, J. and Antov, H. and Nixon, P. Implant-supported oral rehabilitation in oncology patients: a retrospective cohort study. The British journal of oral & maxillofacial surgery. 2020; 58 (8) :1003-1007 |
Wrong O |
|
Sandoval, Maria L. and Rosen, Evan B. and Robert, Allen J. and Nelson, Jonas A. and Matros, Evan and Gelblum, Daphna Y. Immediate dental implants in fibula free flaps to reconstruct the mandible: A pilot study of the short-term effects on radiotherapy for patients with head and neck cancer. Clinical implant dentistry and related research. 2020; 22 (1) :91-95 |
Wrong I/C |
|
Xia Y, Feng ZC, Li C, Wu H, Tang C, Wang L, Li H. Application of additive manufacturing in customized titanium mandibular implants for patients with oral tumors. Oncol Lett. 2020 Oct;20(4):51. doi: 10.3892/ol.2020.11912. Epub 2020 Jul 27. PMID: 32788938; PMCID: PMC7416405. |
Wrong I |
|
Butterworth, Chris J. Primary vs secondary zygomatic implant placement in patients with head and neck cancer-A 10-year prospective study. Head & neck. 2019; 41 (6) :1687-1695 |
Wrong study type (no a comparative study) |
|
Strohl, Madeleine P. and Chen, Jennifer Perkins and Ha, Patrick K. and Seth, Rahul and Yom, Sue S. and Heaton, Chase M. Can Early Dental Extractions Reduce Delays in Postoperative Radiation for Patients With Advanced Oral Cavity Carcinoma?. Journal of oral and maxillofacial surgery : official journal of the American Association of Oral and Maxillofacial Surgeons. 2019; 77 (11) :2215-2220 |
Wrong O |
|
Woods, B. and Schenberg, M. and Chandu, A. A Comparison of Immediate and Delayed Dental Implant Placement in Head and Neck Surgery Patients. Journal of Oral and Maxillofacial Surgery. 2019; 77 (6) :1156-1164 |
Included in SR |
|
de Groot, R. J. and Wetzels, J. W. and Merkx, M. A. W. and Rosenberg, A. J. W. P. and de Haan, A. F. J. and van der Bilt, A. and Abbink, J. H. and Speksnijder, C. M. Masticatory function and related factors after oral oncological treatment: A 5-year prospective study. Head and Neck. 2019; 41 (1) :216-224 |
Wrong study type (not a comparative study), prognostic factor |
Subquestion 2
|
Reference |
Reason for exclusion |
|
Talaat, M. A. The Influence of Radiation Therapy on Dental Implantation in Head and Neck Cancer Patients. Journal of Analytical Oncology. 2023; 12 :1-6 |
Focussess on dental implants
|
|
Hackett, Stephanie and El-Wazani, Basma and Butterworth, Chris Zygomatic implant-based rehabilitation for patients with maxillary and mid-facial oncology defects: A review. Oral diseases. 2021; 27 (1) :27-41 |
Low quality review (no search date provided, no systematic analysis of outcome measures) |
|
Atanasio Pitorro, Tassio Edno and de Araujo Reis, Nayara Teixeira and Paranhos, Luiz Renato and Ferreira Soares, Priscilla Barbosa Survival of Dental Implants Placed Pre-Radiotherapy Versus Post-Radiotherapy in Native Bone: A Systematic Review. The International journal of oral & maxillofacial implants. 2022; 37 (6) :1100-1109 |
Wrong I/C/O (Compares survival rates of implants placed pre- and post RDT compared to those without RDT) |
|
Gupta, S. and Mortellaro, C. and Panda, S. and Rovati, M. and Giacomello, M. S. and Colletti, L. and Greco Lucchina, A. and Del Fabbro, M. Dental implant survival rate in irradiated and non-radiated patients: a systematic review and meta-analysis. Journal of biological regulators and homeostatic agents. 2021; 35 (2) :53-65 |
Wrong implant type (dental implants) |
|
Koudougou, Carine and Bertin, Helios and Lecaplain, Bastien and Badran, Zahi and Longis, Julie and Corre, Pierre and Hoornaert, Alain Postimplantation radiation therapy in head and neck cancer patients: Literature review. Head & neck. 2020; 42 (4) :794-802 |
Not a systematic review (only 1 database was searched) |
|
Sriram, Shreya and Njoroge, Moreen W. and Lopez, Christopher D. and Zhu, Lily and Heron, Matthew J. and Zhu, Katherine J. and Yusuf, Cynthia T. and Yang, Robin Optimal Treatment Order With Fibula-Free Flap Reconstruction, Oncologic Treatment, and Dental Implants: A Systematic Review and Meta-Analysis. The Journal of craniofacial surgery. 2024; 35 (4) :1065-1073 |
Wrong O (implant survival) |
|
Zarzar, Adriana Machado and Sales, Pedro Henrique da Hora and Barros, Ana Waleska Pessoa and Arreguy, Ingrid Melo Schuler and Carvalho, Alessandra Albuquerque Tavares and Leao, Jair Carneiro Effectiveness of dental implants in patients undergoing radiotherapy for head and neck cancer: An umbrella review. Special care in dentistry : official publication of the American Association of Hospital Dentists, the Academy of Dentistry for the Handicapped, and the American Society for Geriatric Dentistry. 2024; 44 (1) :40-56 |
Wrong I/C/O (does not compare the timing of implant placement) |
|
Barber, A. J. and Butterworth, C. J. and Rogers, S. N. Systematic review of primary osseointegrated dental implants in head and neck oncology. The British journal of oral & maxillofacial surgery. 2011; 49 (1) :29-36 |
The review does not report information on outcome measures |
|
Jokstad, Asbjorn Patients undergoing craniofacial tumour ablation surgery may benefit from having the implants placed simultaneously instead of waiting. Evidence-based dentistry. 2010; 11 (2) :52-3 |
Not a systematic review (summary review) |
|
Jokstad, Asbjorn Patients undergoing craniofacial tumour ablation surgery may benefit from having the implants placed simultaneously instead of waiting. Evidence-based dentistry. 2010; 11 (1) :22-3 |
double |
|
Patel J, Antov H, Nixon P. Implant-supported oral rehabilitation in oncology patients: a retrospective cohort study. Br J Oral Maxillofac Surg. 2020 Oct;58(8):1003-1007. doi: 10.1016/j.bjoms.2020.05.016. Epub 2020 May 27. PMID: 32474015. |
Wrong O |
|
Di Carlo S, De Angelis F, Ciolfi A, Quarato A, Piccoli L, Pompa G, Brauner E. Timing for implant placement in patients treated with radiotherapy of head and neck. Clin Ter. 2019 Sep-Oct;170(5):e345-e351. doi: 10.7417/CT.2019.2153. PMID: 31612191. |
Wrong I/C (implants were placed after abblative surgery for all patients) |
|
Dings JP, Maal TJ, Muradin MS, Ingels KJ, Klevering BJ, Koole R, Merkx MA, Meijer GJ. Extra-oral implants: insertion per- or post-ablation? Oral Oncol. 2011 Nov;47(11):1074-8. doi: 10.1016/j.oraloncology.2011.07.015. Epub 2011 Aug 10. PMID: 21835682. |
Wrong O (implant survival) |
|
Elledge R, Chaggar J, Knapp N, Martin T, White N, Evriviades D, Edmondson S, Parmar S. Craniofacial implants at a single centre 2005-2015: retrospective review of 451 implants. Br J Oral Maxillofac Surg. 2017 Apr;55(3):242-245. doi: 10.1016/j.bjoms.2016.11.324. Epub 2017 Feb 16. Erratum in: Br J Oral Maxillofac Surg. 2018 Jan;56(1):83. doi: 10.1016/j.bjoms.2017.09.014. PMID: 28216308. |
Wrong I/C/O |
|
Ettl T, Weindler J, Gosau M, Müller S, Hautmann M, Zeman F, Koller M, Papavasileiou D, Bürgers R, Driemel O, Schneider I, Klingelhöffer C, Meier J, Wahlmann U, Reichert TE. Impact of radiotherapy on implant-based prosthetic rehabilitation in patients with head and neck cancer: A prospective observational study on implant survival and quality of life-Preliminary results. J Craniomaxillofac Surg. 2016 Sep;44(9):1453-62. doi: 10.1016/j.jcms.2016.07.016. Epub 2016 Jul 21. PMID: 27519660. |
Focussess on dental implants and does not compare implants placed during and after surgery |
|
Irish J, Sandhu N, Simpson C, Wood R, Gilbert R, Gullane P, Brown D, Goldstein D, Devins G, Barker E. Quality of life in patients with maxillectomy prostheses. Head Neck. 2009 Jun;31(6):813-21. doi: 10.1002/hed.21042. PMID: 19280665. |
Wrong I/C (not a comparison between patients receiving implants during and after surgery) |
|
Lodders JN, van Baar GJC, Vergeer MR, Jansen F, Schulten EAJM, Lissenberg-Witte BI, Verdonck-de Leeuw IM, Forouzanfar T, Leusink FKJ. Implant-based dental rehabilitation in head and neck cancer patients after maxillofacial reconstruction with a free vascularized fibula flap: the effect on health-related quality of life. Support Care Cancer. 2022 Jun;30(6):5411-5420. doi: 10.1007/s00520-022-06944-4. Epub 2022 Mar 17. PMID: 35298715; PMCID: PMC9046363. |
Wrong I/C (not a comparison between patients receiving implants during and after surgery) |
|
Mizbah K, Dings JP, Kaanders JH, van den Hoogen FJ, Koole R, Meijer GJ, Merkx MA. Interforaminal implant placement in oral cancer patients: during ablative surgery or delayed? A 5-year retrospective study. Int J Oral Maxillofac Surg. 2013 May;42(5):651-5. doi: 10.1016/j.ijom.2012.09.013. Epub 2012 Oct 24. PMID: 23102901. |
Included in 10A (focuses on dental implants) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 28-01-2026
Beoordeeld op geldigheid : 28-01-2026
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd door de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2023 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met hoofd-halskanker.
Werkgroep
- Prof. dr. L.W.J. (Laura) Baijens, voorzitter, Nederlandse Vereniging van Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied (NVKNO)
- A.C.P. (Anne) Kauerz-de Rooij, Ergotherapie Nederland (EN)
- Dr. C.M. (Caroline) Speksnijder, Koninklijk Nederlands Genootschap Fysiotherapie (KNGF)
- Dr. D.J.M. (Doke) Buurman - Koninklijke Nederlandse Maatschappij tot bevordering der Tandheelkunde (KNMT)
- Dr. K.S. (Kathelijn) Versteeg, Nederlandse Internisten Vereniging (NIV)
- Drs. D. (Desiree) Dona, Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde (NVAB)
- Dr. A. (Annemieke) Kok, Nederlandse Vereniging van Diëtisten (NVD)
- Drs. M. (Marieke) Jacobs, Nederlandse Vereniging voor Klinische Arbeidsgeneeskunde (NVKA)
- Dr L. (Lisette) van der Molen, Nederlandse Vereniging voor Logopedie en Foniatrie (NVLF)
- Dr. L.H.E. (Luc) Karssemakers, Nederlandse Vereniging voor Mondziekten, Kaak- en Aangezichtschirurgie (NVMKA)
- Dr. J. (Jos) Elbers, Nederlandse Vereniging voor Radiotherapie en Oncologie (NVRO)
- R.A. (Rob) Burdorf, Patiëntenvereniging HOOFD-HALS (PvHH)
- P.S. (Petra) Verdouw, Patiëntenvereniging HOOFD-HALS (PvHH)
- Drs. M. (Michael) Brouwers, Nederlandse Vereniging van Revalidatieartsen (VRA)
- Drs. E. (Ellen) Passchier, Verpleegkundigen en Verzorgenden Nederland (V&VN)
- Drs. N. (Narda) Hendriks, Nederlandse Vereniging voor Plastische Chirurgie (NVPC)
Klankbordgroep
- Prof. dr. R. (Remco) de Bree, Nederlandse Vereniging van Keel-Neus-Oorheelkunde en Heelkunde van het Hoofd-Halsgebied (NVKNO)
- Dr. P. (Pim) de Graaf, Nederlandse Vereniging voor Radiologie (NVvR)
- Dr. D.S.V.M. (Dominique) Clément, Nederlandse Vereniging van Maag-Darm-Leverartsen (NVMDL)
- J. (Jesmin) Poelstra, Beroepsvereniging van Professionals in Sociaal Werk (BPSW)
- Dr. G. (Gerben) van Hinte, Koninklijk Nederlands Genootschap Fysiotherapie (KNGF)
- Drs. A. (Anne) Arens, Nederlandse Vereniging voor Nucleaire Geneeskunde (NVNG)
- Dr. F. (Femke) Jansen, Nederlandse Vereniging voor Psychosociale Oncologie (NVPO)
Met ondersteuning van
- Dr. L.M. (Lisette) van Leeuwen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. E. (Evelien) Belfroid, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
Gemelde (neven)functies en belangen richtlijnwerkgroep
|
Naam |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Datum |
Restrictie |
|
Laura Baijens |
KNO-arts/Laryngoloog/Hoofd-hals chirurg Maastricht Universitair Medisch Centrum (MUMC+) |
Consultant for Phagenesis Limited, The Elms Courtyard, Bromesberrow, Ledbury, HR8 1RZ UK. The PhINEST Study – Pharyngeal ICU - Novel Electrical Stimulation Therapy: a prospective, European multi-site, randomised, sham-controlled, single-blind (outcome assessor-blinded) study. August 2018 – 2030 (Consultancy Agreement via the Clinical Trial Center Maastricht) |
Consultant for Phagenesis Limited in the PhINEST Study heeft geen betrekking of relaties met de huidige richtlijn. Het is een Europese multicenter studie over dysfagie bij CVA patiënten waarin ik advies geef. De opbrengsten gaan naar het Clinical Trial Center Maastricht. |
Neen |
Phagenesis Limited Advies geven in een studie over faryngeale elektrostimulatie bij CVA patiënten, MUMC+ is geen site en betreft geen patiënten met hoofd-halskanker.
Michel Keijzer Fonds PVHH Multi-domein screening van hoofd-halskankerpatiënten |
Intellectueel eigendom: Ik ben PI in meerdere lopende niet-WMO studies over dysfagie bij hoofd-halskanker. Ik heb vele internationale W1-publicaties over dysfagie bij hoofd-halskanker. De kans is reëel dat deze publicaties terecht zullen komen in de output van systematic literatuur searches voor deze richtlijn. Er is geen sprake van 'vermarkting' of verwerven van een boegbeeldfunctie bij organisaties. |
Nee |
juli 2025 |
Geen restricties (extern gefinancierd onderzoek heeft geen relatie met het onderwerp van de richtlijn) |
|
Anne Kauerz |
Ergotherapeut UMC Utrecht |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
juli 2025 |
Geen restricties |
|
Desiree Dona |
bedrijfsarts / klinisch arbeidsgeneeskundige oncologie 1.0 fte Radboudumc werkzaamheden: arbeidsgeneeskundige begeleiding in behandelteam van oncologiepatienten, projectmanagement, onderzoek en onderwijs. Alle werkzaamheden zijn betaald. |
vennoot van DELEN ABC (arbeidsdeskundige advisering en coaching) generieke module Arbeidsparticipatie voor medisch specialistische richtlijnen (vacatiegelden) |
Geen |
neen |
Prehabilitatie en werkbegeleiding voor borstkankerpatienten (gefinancierd door MOVIR en Stichting Enjoy the ride, unrestricted grant, geen PI) |
Ik heb een boegbeeldfunctie bij het Radboudumc (Principal Clinician) op de zorginnovatie arbeidsgerichte zorg. Vanuit die functie heb ik een groot netwerk (zorgprofessionals, politiek, ministeries, beroepsverenigingen, patientorganisaties, richtlijn cie's, NZa, ZiNl). Ik ben actief betrokken bij het NKC en in de TF cancersurvivorship care werkgroep werk. We proberen tzt onze innovatie te vermarkten om zodoende de voorinvestering die het Radboudumc doet terug te kunnen verdienen. Dit betreft mn onderwijsmodules. Ik heb meegeschreven aan de generieke module Arbeidsparticipatie voor in medisch specialistische RL. Ik zal een voortrekkersrol hebben in het vervolgtraject: het maken van ene ziektespecifieke module Arbeidsparticipatie voor oncologische RL. En ik ben kerngroeplid van de update van de RL kanker en werk voor bedrijfsartsen |
Ontwikkelen zorgmodel arbeidsgerichte zorg (Janssen Pharma en Radboudumc, in-kind projectondersteuning van Janssen Pharma) |
juli 2025 |
Geen restricties |
|
Ellen Passchier |
Verpleegkundig specialist revalidatie hoofd-hals oncologie tot november 2024 in Antoni van Leeuwenhoek
Heden: - verpleegkundig specialist in de wijk (Buurtzorg Amsterdam) - docent aan de Master ANP (Hogeschool inHolland) - buitenpromovendus afdeling hoofd-hals oncologie (Antoni van Leeuwenhoek) |
Geen |
Geen |
Geen |
Met ingang van november 2016 promotieonderzoek (evaluatie van revalidatieprogramma bij patiënten met een HHT - haalbaarheidsonderzoek naar beweeginterventie, analyses op kwaliteit van leven uitkomsten) |
Door deze richtlijn zal mijn promotie onderzoek (publicaties) meer belangstelling krijgen. |
Geen |
juli 2025 |
Geen restiricties |
|
Jos Elbers |
Radiotherapeut-oncoloog Erasmus MC |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
juli 2025 |
Geen restricties |
|
Kathelijn Versteeg |
internist-oncoloog AmsterdamUMC internist-ouderengeneeskunde AmsterdamUMC |
geen |
geen |
geen |
geen |
geen |
geen |
juli 2025 |
Geen restricties |
|
Lisette van der Molen |
logopedist/senior onderzoek aan het NKI-AVL. |
Het geven van bij/nascholing met betrekking tot de (logopedische) functionele uitkomsten na een behandeling in het HH gebied. Deze scholing kan zowel onbetaald als betaald zijn. |
Geen |
nvt |
ja Atos Medical AB Zweden Unrestricted research grant waardoor er PhD studenten kunnen worden aangenomen
De afdeling hoofd-halsoncologie van het AvL krijgt deze unrestricted research grant van Atos Medical (dus niet op persoonlijke titel van dit werkgroeplid). Ik ben in vaste dienst bij het AvL en ook niet afhankelijk van deze grant.
|
In 2010 heb ik samen met Prof. Hilgers het hoofd-halsrevalidatieprogramma ontwikkeld, welke als (standaard) nazorg binnen het NKI-AVL wordt aangeboden. Mocht dit ook het advies worden van deze richtlijn, dan zal het NKI-AVL een voorsprong hebben op de andere HH centra mbt implementatie.
Als kartrekker van de onderzoekslijn: survivorship rehabilitation and QoL na Hoofd-Halskanker begeleiden van meerdere PhD studenten met o.a. het onderwerp dysfagie. De kans is aanwezig dat er publicaties uit onze onderzoeksgroep terecht zullen komen in de output van de systematische literatuur searches voor deze richtlijn. Er is geen sprake van vermarkting of verwerven van een boegbeeldfunctie bij organisaties. |
nvt |
juli 2025 |
Geen restricties |
|
Luc Karssemakers |
Antoni v Leeuwenhoek Ziekenhuis, afdeling hoofd-hals chirurgie |
Afdeling Kaakchirurgie Slotervaart |
Geen |
Geen |
zie onderstaand STW Craniosafe, ideale implantaat schedelplastieken TKI Sternofix, implantaten sternaal voor laryngectomiepatienten |
Geen |
Geen |
juli 2025 |
Geen restricties (extern gefinancierd onderzoek heeft geen relatie met het onderwerp van de richtlijn) |
|
Marieke Jacobs |
Bedrijfsarts / klinisch arbeidsgeneeskundige, Radboudumc |
Werkzaam als instituutsopleider bedrijfsartsenopleiding bij de SGBO, Radboudumc |
Geen |
Niet van toepassing |
Niet van toepassing |
Niet bewust van |
Nee |
juli 2025 |
Geen restricties |
|
Narda Hendriks-Brouwer |
Medisch Spectrum Twente- plastisch chirurg Ziekenhuisgroep Twente-plastisch chirurg |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
juli 2025 |
Geen restricties |
|
Rob Burdorf |
Patiëntenvertegenwoordiger. Lid van de Wetenschappelijke Advies Commissie van de PVHH. Onbetaald |
geen |
geen |
nvt |
nvt |
nvt |
geen |
juli 2025 |
Geen restricties |
|
Caroline Speksnijder |
Associate professor UMC Utrecht |
Docent: *MSc Oncologie Fysiotherapie; Avans+ *MSc Orofaciale Fysiotherapie SOMT Physiotherapy University Werkgroep Kennisagendaherziening KNO Bestuurstaken: *Koninklijk Genootschap voor Fysiotherapie (KNGF): Bestuurslid Wetenschappelijk College Fysiotherapie (WCF) *Paramedische Werkgroep Hoofdhalstumoren (PWHHT): voorzitter *Dutch Association of Supportive Care in Cancer (DASCC): voorzitter *International Physiotherapy in HIV/Aids, Oncology, and Hospice and Palliative Care (IPT-HOPE part of World Physiotherapy): Vice-president |
Geen |
Nee |
Perioperative nutritional intervention with Fortifit Energy® in combination with exercise versus standard of care in head and neck cancer patients undergoing combined approach resection: a pilot study(gefinancierd door Danone, unrestricted grant, geen PI)
Integrating the Knowledge Agenda Physiotherapy into the science policy of the Royal Dutch Association for Physiotherapy (KNGF) (gefinancierd door ZonMw)
Prehabilitatie fysieke fitheid vooraf aan totale laryngectomie (gefinancierd door Nederlands Fonds tegen Kanker, unrestricted grant) |
nee |
nvt |
juli 2025 |
Restricties ten aanzien van het formuleren van aanbevelingen over het onderwerp op UV6 (nutritionele en excerise interventies ter preventie en behandeling) |
|
Petra Verdouw |
Patiëntenvereniging HOOFD-HALS Directeur |
geen |
geen |
geen |
geen |
geen |
geen |
juli 2025 |
Geen restricties |
|
Annemieke Kok |
Diëtist, onderzoeker |
secretaris PWHHT lid Landelijke Werkgroep Diëtisten Oncologie (tot jan 2024)
Vice-voorzitter van de Landelijke Werkgroep Diëtisten Oncologie (LWDO) (sinds april 2025). |
geen |
nee |
zie onder Ontwikkeling PEG keuzehulp voor hoofd-halskankerpatienten (Michel Keijzer Fonds) Perioperative nutritional intervention with Fortifit Energy® in combination with exercise versus standard of care in head and neck cancer patients undergoing combined approach resection: a pilot study(gefinancierd door Danone, unrestricted grant, geen PI) |
nee |
nee |
juli 2025 |
Restricties ten aanzien van het formuleren van aanbevelingen over het onderwerp op UV5 (nutritionele en excerise interventies ter preventie en behandeling) |
|
Doke Buurman |
Tandarts-MFP bij Maastricht UMC+ (betaald) |
Lid Consilium MFP bij de NVGPT (onbetaald) Lid ROC Mondzorg voor mensen met kanker (in de voorgeschiedenis) van KIMO (vacatieregeling) |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
juli 2025 |
Geen restricties |
|
Michael Brouwers |
Revalidatiearts Anthony van Leeuwenhoek Ziekenhuis Amsterdam |
geen |
geen |
geen |
geen |
geen belangen |
geen belangen |
juli 2025 |
|
Inbreng patiëntenperspectief
De richtlijnwerkgroep besteedde aandacht aan het patiëntenperspectief door het uitnodigen van Patiëntenvereniging Hoofd-Hals voor de schriftelijke invitational conference, en twee afgevaardigde namens deze patiëntenorganisatie in de werkgroep. Het verslag van de invitational conference (zie aanverwante producten) is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de patiëntenvereniging en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule voerde de werkgroep conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uit om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema bij Werkwijze).
|
Module |
Uitkomst raming |
Toelichting |
|
Prothetisch herstel |
geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en daarom naar verwachting geen substantiële financiële gevolgen zal hebben voor de collectieve uitgaven.
|