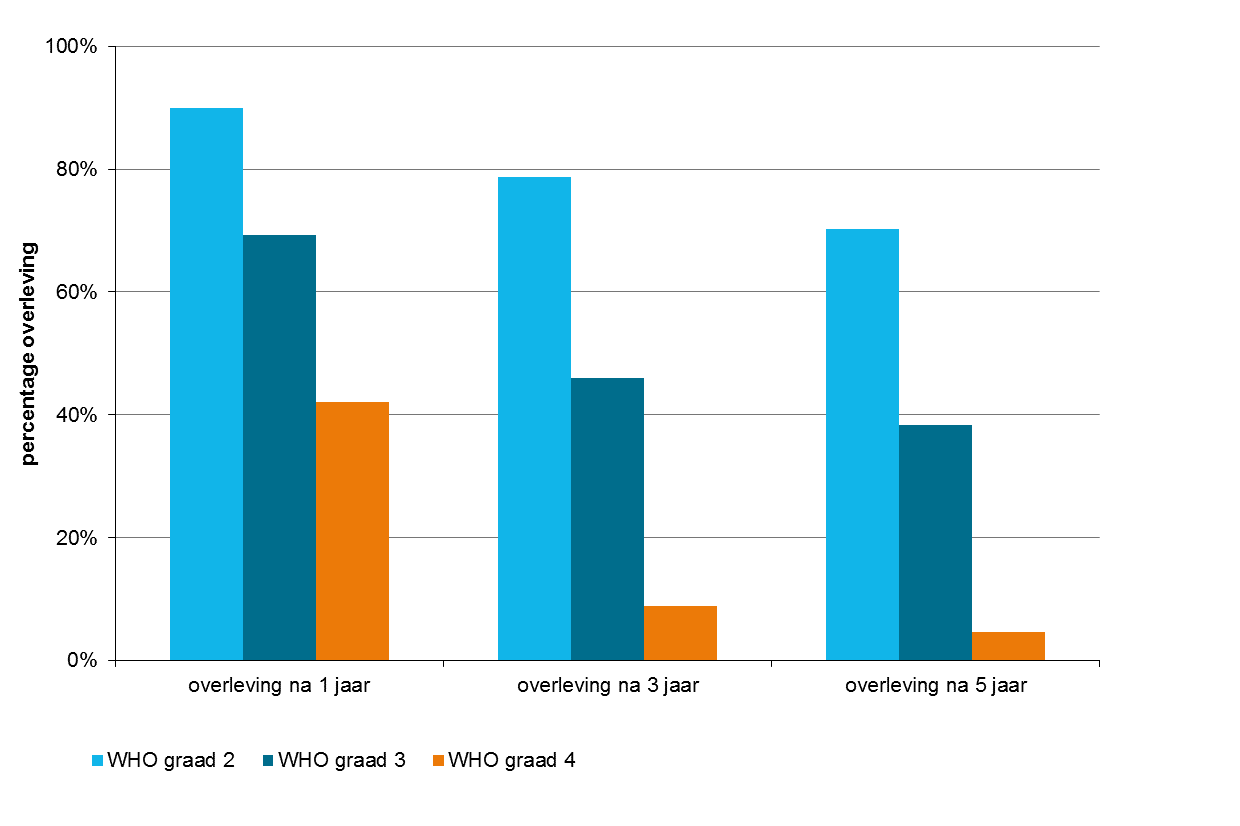Epidemiologie
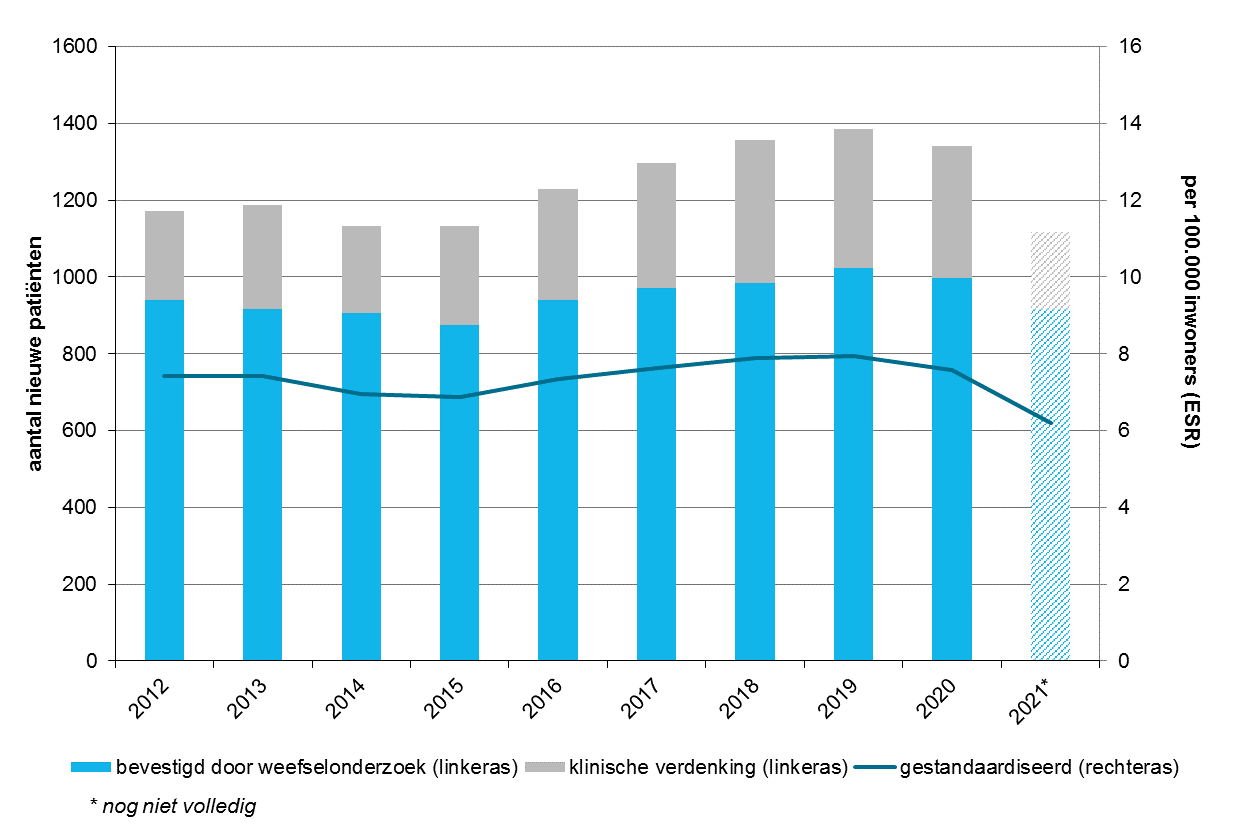
Gliomen zijn een relatief zeldzame vorm van kanker. Jaarlijks krijgen ongeveer 1300 volwassen patiënten in Nederland de diagnose diffuus glioom (grafiek 1), waarvan 1000 bevestigd door weefselonderzoek. De incidentie is al jaren stabiel en ligt gestandaardiseerd voor de Europese bevolking rond 6 per 100.000 inwoners voor tumoren bevestigd door weefselonderzoek, en rond 8 per 100.000 als klinisch verdachte gevallen worden meegerekend. Deze laatste groep betreft patiënten die niet zijn geopereerd, bijvoorbeeld vanwege hun slechte conditie.
Diffuse gliomen komen vaker voor bij mannen (Ostrom, 2022). Hoewel verschillende risicofactoren zijn onderzocht, heeft alleen therapeutische, ioniserende straling een duidelijke etiologische invloed. Vooral degenen die als kind radiotherapie ondergingen, bijvoorbeeld vanwege leukemie, hebben een hogere kans op het ontwikkelen van een glioom (Ohgaki, 2005).
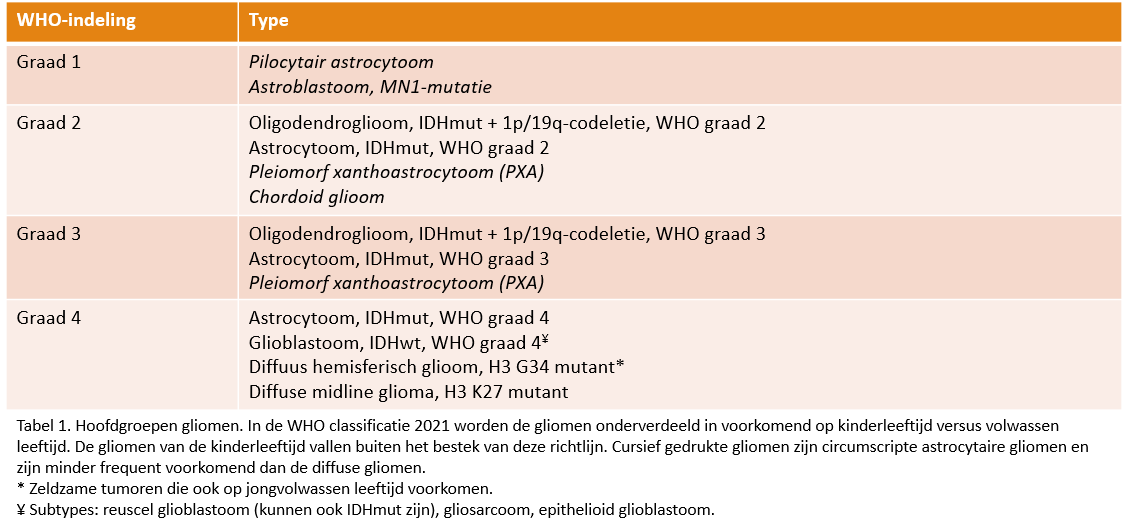
Gliomen worden geclassificeerd volgens de Wereldgezondheidsorganisatie (WHO, 2021), zie tabel 1.
Tabel 1. WHO-classificatie (2021) van diffuse gliomen
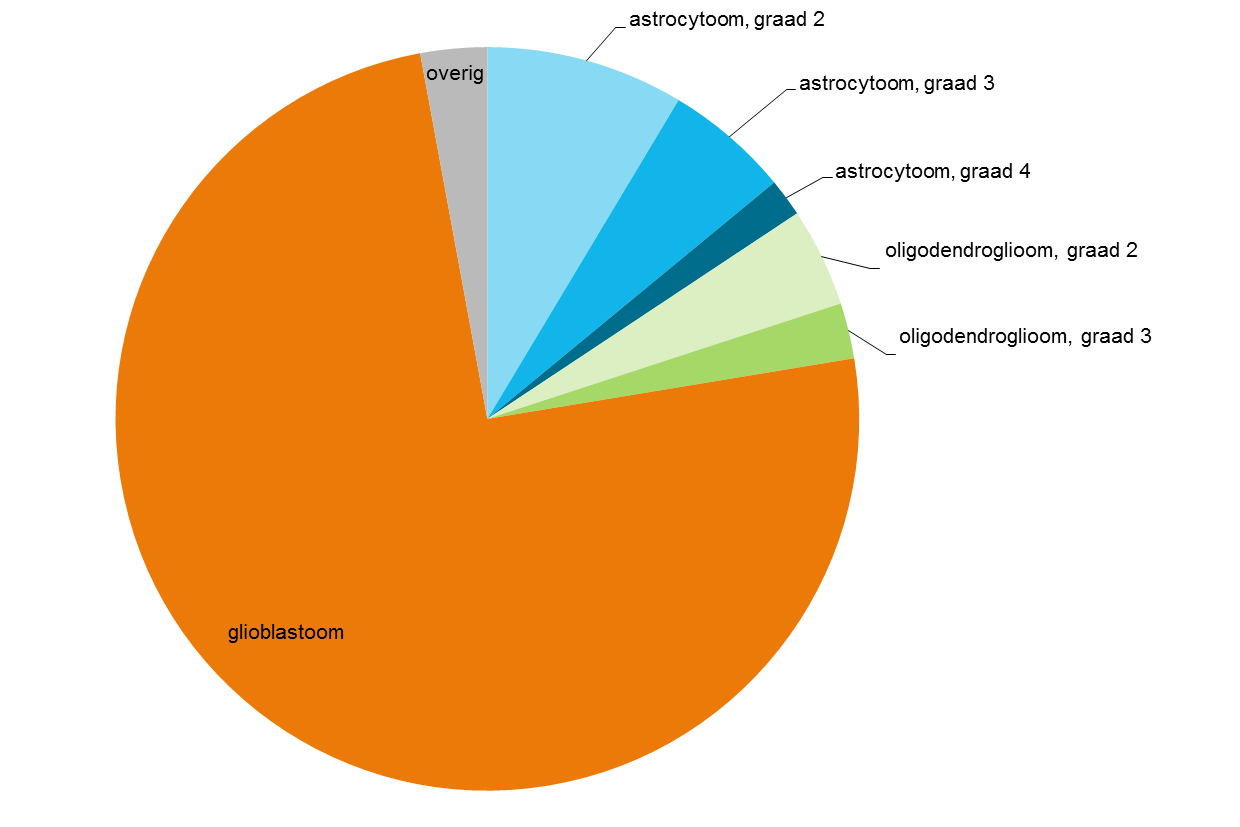
Van de door weefselonderzoek bevestigde diffuse gliomen betreft het merendeel (75%) een glioblastoom (grafiek 2).
Gliomen groeien vaak uitgebreid in het omliggende hersenweefsel, wat adequate behandeling bemoeilijkt. Metastasering naar andere delen van het lichaam komt vrijwel niet voor. Afhankelijk van het tumortype en de tumorgraad krijgen vrijwel alle patiënten te maken met recidiefgroei na een eerste behandeling.
De overleving van patiënten met een glioom is sterk afhankelijk van de WHO-graad: in de periode 2012–2021 in Nederland was de 1-jaarsoverleving van patiënten met een door weefselonderzoek bevestigd WHO graad 2 glioom 90%, van degenen met een WHO graad 3 glioom 69%, en van degenen met een WHO graad 4 glioom 42% (grafiek 3). De 5-jaarsoverleving van deze patiënten bedroeg respectievelijk 70%, 38% en 5%.
Grafiek 1. Aantal nieuwe gevallen van diffuse gliomen per incidentiejaar (Nederland) in de periode 2012–2021, absoluut (staaf) alsmede gestandaardiseerd voor de leeftijdsopbouw van de Europese bevolking (ESR; lijn)
Grafiek 2. Subtypes diffuse gliomen door weefseldiagnostiek bevestigd in de periode 2012–2021, in Nederland.
Grafiek 3. De 1-, 3-, 5-jaarsoverleving voor de diagnose diffuus glioom per WHO gradering ( (WHO graad 2, 3 en 4) in Nederland.
Beoordelingsdatum en geldigheid
Publicatiedatum : 22-09-2023
Beoordeeld op geldigheid : 01-06-2025
Algemene gegevens
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
Module |
Uitkomst raming |
Toelichting |
|
Module 1 |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
|
Module 2 |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
|
Module 3 Beeldvorming ter nadere differentiatie |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
|
Module 4 Beeldvorming ten behoeve van behandeling |
Geen financiële gevolgen |
Uit de toetsing volgt dat de aanbeveling(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven. |
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2021 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met gliomen.
Werkgroep
- Mevr. dr. Monique Anten, neuroloog, Maastricht Universitair Medisch Centrum, Maastricht; NVN
- Mevr. dr. Jacoline Bromberg, neuroloog/ neuro-oncoloog, Erasmus MC, Rotterdam; NVN
- Mevr. drs. Sammy Olijslagers, neuroloog-in-opleiding, Canisius Wilhelmina Ziekenhuis, Nijmegen; NVN
- Mevr. drs. Sandra Huijs, neuroloog-in-opleiding, Zuyderland ziekenhuis, Heerlen; NVN
- Dhr. dr. Filip de Vos, internist-neuroloog, Universitair Medisch Centrum Utrecht, Utrecht; NIV
- Mevr. prof. dr. Marion Smits, radioloog, Erasmus MC, Rotterdam; NVvR
- Dhr. drs. Wouter Teunissen, radioloog-in-opleiding, Erasmus MC, Rotterdam; NVvR
- Dhr. Jelle de Vries, ervaringsdeskundige; Hersenletsel.nl
- Dhr. Hugo van Bers, ervaringsdeskundige; Hersenletsel.nl
- Dhr. dr. Joost Verhoeff, radiotherapeut-oncoloog, Universitair Medisch Centrum Utrecht, Utrecht; NVRO
- Dhr. prof. dr. Philip de Witt Hamer, neurochirurg, Amsterdam Universitair Medisch Centrum, Amsterdam; NVvN
- Mevr. Ilse Vosman, Verpleegkundig Specialist neuro-oncologie, Universitair Medisch Centrum Utrecht, Utrecht; V&VN (tot juni 2022)
Klankbordgroep
- Dhr. prof. dr. Johan Kros, ordinarius neuropathologie, Erasmus Medisch Centrum, Rotterdam; NVvP
Met ondersteuning van:
- Mevr. drs. Beatrix Vogelaar, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. dr. Josefien Buddeke, senior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. dr. Marja Molag, adviseur, Kennisinstituut van de Federatie Medisch Specialisten (dec 2021 tot april 2022)
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Anten (voorzitter) |
Neuroloog, Maastricht UMC+ |
Geen |
Geen |
Geen |
|
Bromberg |
Neuroloog / neuro-oncoloog Erasmus MC, Rotterdam |
Bestuur stichting hersentumor.nl, onbetaald |
Geen |
Geen |
|
Olijslagers |
AIOS neurologie, |
Geen |
Geen |
Geen |
|
Huijs |
AIOS neurologie, Zuyderland Medisch Centrum |
Onderzoeker sarcopenie en invloed hiervan op prognose bij patiënten met glioblastoma multiforme (geen PI), onbetaald. |
Geen |
Geen |
|
Vos, de |
Internist-oncoloog, UMC Utrecht |
Lid palliatie consultatieteam UMC Utrecht, onbetaald |
Geen |
Geen |
|
Vosman |
Verpleegkundig Specialist AGZ (neuro-oncologie), UMC Utrecht |
Geen |
Geen |
Geen |
|
Smits |
Radioloog, Erasmus MC afdeling radiologie & nucleaire geneeskunde |
Voorzitter sectie neuroradiologie van de NVvR, onbetaald (tot 2021). Lid bestuur NVvR, portefeuille Wetenschap en internationale betrekkingen, onbetaald. Voorzitter van de Research Committee van de European Society of Radiology, onbetaald. |
Extern gefinancierde onderzoeksprojecten: - Deep Medical Imaging, gefinancierd door Convergence. - The Sound of Flow, gefinancierd door NWO Hestia. Consultancy Sprekershonorarium |
Geen |
|
Witt Hamer, de |
Neurochirurg, Amsterdam UMC, locatie VUmc |
Bestuurder stichting Hersentumor.nl, onbetaald |
Geen |
Geen |
|
Vries, de |
Projectmanager VanMeijel Automatisering |
Lid van het dagelijks bestuur van de Hersentumoren Contactgroep van hersenletsel.nl |
|
|
|
Bers, van |
ex-Patient |
Geen |
Geen |
Geen |
|
Verhoeff |
Associate professor radiotherapy UMC Utrecht |
Geen |
Geen |
Geen |
|
Teunissen |
Arts-onderzoeker afdeling radiologie en nucleaire geneeskunde, Erasmus MC Rotterdam
|
Geen |
Leading the change - Waarde van perfusie MRI bij hersentumoren - Geen projectleider |
Geen |
|
Kros (klankbordgroep) |
Hoogleraar / medisch specialist neuropathologie, Erasmus MC, Rotterdam |
Onbetaalde lidmaatschappen: |
Geen |
Geen |
|
Molag |
Adviseur, Kennisinstituut, Utrecht |
Geen |
Geen |
Geen |
|
Buddeke |
Senior adviseur, Kennisinstituut, Utrecht |
Geen |
Geen |
Geen |
|
Vogelaar |
Junior adviseur, Kennisinstituut, Utrecht |
Geen |
Geen |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door afgevaardigden van de patiëntenvereniging Hersenletsel.nl te betrekken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen (zie kop “Waarden en voorkeuren van patiënten”). De conceptrichtlijn is tevens voor commentaar voorgelegd aan Hersenletsel.nl en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten met een glioom. Het verzoek om knelpunten aan te leveren is voorgelegd aanVerenso, Nederlands Huisartsen Genootschap, Nederlandse Vereniging van Ziekenhuizen, Patiëntenfederatie Nederland, Verpleegkundingen & Verzorgenden Nederland, Zelfstandige Klinieken Nederland, Zorgverzekeraars Nederland, Vereniging voor Neurologie, de Landelijke Werkgroep Neuro-Oncologie (via Vereniging voor Neurologie), Nederlandse vereniging voor Radiologie en de Nederlandse Vereniging van Klinische geriatrie via enquête. Een verslag hiervan is opgenomen onder aanverwante producten. Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.