Differentiaaldiagnose bij hypertriglyceridemie
Uitgangsvraag
Hoe kan bepaald worden welke lipoproteïnepartikels aanwezig zijn voor het stellen van een differentiaaldiagnose bij patiënten met hypertriglyceridemie?
Deelvragen
- Hoe kan bepaald worden welke lipoproteïnepartikels aanwezig zijn voor het stellen van een differentiaaldiagnose bij patiënten met hypertriglyceridemie op basis van chylomicronen?
- Hoe kan bepaald worden welke lipoproteïnepartikels aanwezig zijn voor het stellen van een differentiaaldiagnose bij patiënten met hypertriglyceridemie op basis van chylomicronen en VLDL?
- Hoe kan bepaald worden welke lipoproteïnepartikels aanwezig zijn voor het stellen van een differentiaaldiagnose bij patiënten met hypertriglyceridemie op basis van VLDL?
Aanbeveling
Bepaal bij patiënten met hypertriglyceridemie welke triglyceriderijke lipoproteïnepartikels verhoogd zijn: chylomicronen en/of VLDL.
Overweeg apoB, totaalcholesterol en triglyceriden te meten en overweeg om het apoB-algoritme toe te passen bij patiënten met hypertriglyceridemie voor het vaststellen welke triglyceriderijke lipoproteïnepartikels verhoogd zijn.
Overweeg bij patiënten met hypertriglyceridemie de volgende primaire oorzaken afhankelijk van welke triglyceridenrijke partikels aanwezig zijn:
- verhoogde chylomicronen:
- familiaire hyperchylomicronemie (FHC) op basis van complete LPL-deficiëntie;
- apoCII-deficiëntie.
- verhoogde chylomicronen en VLDL:
- partiële LPL-deficiëntie vaak gecombineerd met secundaire oorzaak;
- apoAV-deficiëntie, vaak gecombineerd met secundaire oorzaak.
- verhoogde VLDL:
- familiaire hypertriglyceridemie;
- partiële LPL-deficiëntie;
- partiële apoAV-deficiëntie.
Bepaal bij iedere patiënt met nieuwe hypertriglyceridemie de glucoseconcentratie en registreer bij anamnese en lichamelijk onderzoek de volgende parameters:
- overgewicht (met name hoge middelomtrek);
- diabetes mellitus type 2;
- end-stage renal disease;
- hemodialyse;
- metabool syndroom;
- polycysteus ovariumsyndroom;
- alcoholgebruik.
Vraag tevens naar gebruik van medicatie, zoals antipsychotica, glucocorticoïden, estrogenen en/of HAART-therapie. Het gebruik van deze medicatie kan hypertriglyceridemie veroorzaken, dan wel verergeren.
Hoe kan bepaald worden welke lipoproteïnepartikels aanwezig zijn voor het stellen van een differentiaaldiagnose bij patiënten met hypertriglyceridemie op basis van chylomicronen?
Bepaal bij patiënten met hypertriglyceridemie welke triglyceriderijke lipoproteïnepartikels verhoogd zijn: chylomicronen en/of VLDL.
Overweeg apoB, totaalcholesterol en triglyceriden te meten en overweeg om het apoB-algoritme toe te passen bij patiënten met hypertriglyceridemie voor het vaststellen welke triglyceriderijke lipoproteïnepartikels verhoogd zijn.
Overweeg bij patiënten met hypertriglyceridemie op basis van chylomicronen de volgende primaire oorzaken:
- familiaire hyperchylomicronemie (FHC) ten gevolge van LPL-deficiëntie en/of apoCII-deficiëntie;
- defect in GPI-anchored HDL;
- apoAV-deficiëntie.
Overweeg bij patiënten met hypertriglyceridemie op basis van chylomicronen een secundaire oorzaak te weten verworven apoCII-deficiëntie bij systemische lupus erythematosus.
Hoe kan bepaald worden welke lipoproteïnepartikels aanwezig zijn voor het stellen van een differentiaaldiagnose bij patiënten met hypertriglyceridemie op basis van chylomicronen en VLDL?
Bepaal bij patiënten met hypertriglyceridemie welke triglyceriderijke lipoproteïnepartikels verhoogd zijn: chylomicronen en/of VLDL.
Overweeg apoB, totaalcholesterol en triglyceriden te meten en overweeg om het apoB-algoritme toe te passen bij patiënten met hypertriglyceridemie voor het vaststellen welke triglyceriderijke lipoproteïnepartikels verhoogd zijn.
Overweeg bij patiënten met hypertriglyceridemie op basis van chylomicronen en VLDL de volgende primaire oorzaken:
- partiële LPL-deficiëntie; vaak in combinatie met een secundaire oorzaak;
- apoAV-deficiëntie; vaak in combinatie met een secundaire oorzaak.
Bepaal bij iedere patiënt met nieuwe hypertriglyceridemie op basis van chylomicronen en VLDL de glucoseconcentratie en registreer bij anamnese en lichamelijk onderzoek de volgende parameters:
- overgewicht (met name hoge middelomtrek);
- diabetes mellitus type 2;
- end-stage renal disease;
- hemodialyse;
- metabool syndroom;
- polycysteus ovariumsyndroom;
- alcoholgebruik.
Vraag tevens naar gebruik van medicatie, daar antipsychotica, steroïden (waaronder oestrogenen en glucocorticoïden) en HAART-therapie hypertriglyceridemie kunnen veroorzaken, dan wel verergeren, indien er sprake is van partiële LPL-deficiëntie of apoAV-deficiëntie.
Hoe kan bepaald worden welke lipoproteïnepartikels aanwezig zijn voor het stellen van een differentiaaldiagnose bij patiënten met hypertriglyceridemie op basis van VLDL?
Bepaal bij patiënten met hypertriglyceridemie welke triglyceriderijke lipoproteïnepartikels verhoogd zijn: chylomicronen en/of VLDL.
Overweeg apoB, totaalcholesterol en triglyceriden te meten en overweeg om het apoB-algoritme toe te passen bij patiënten met hypertriglyceridemie voor het vaststellen welke triglyceriderijke lipoproteïnepartikels verhoogd zijn.
Overweeg bij patiënten met hypertriglyceridemie op basis van VLDL de volgende primaire oorzaken:
- familiaire hypertriglyceridemie;
- partiële LPL-deficiëntie;
- partiële apoAV-deficiëntie.
Bepaal bij iedere patiënt met nieuwe hypertriglyceridemie op basis van VLDL de glucoseconcentratie en registreer bij anamnese en lichamelijk onderzoek de volgende parameters:
- overgewicht (met name hoge middelomtrek);
- diabetes mellitus type 2;
- end-stage renal disease;
- hiv;
- hemodialyse;
- metabool syndroom;
- polycysteus ovariumsyndroom;
- alcoholgebruik.
Vraag tevens naar gebruik van medicatie, daar antipsychotica, glucocorticoïden, estrogenen en HAART-therapie hypertriglyceridemie kunnen veroorzaken, dan wel verergeren, indien er sprake is van partiële LPL-deficiëntie of apoAV-deficiëntie.
Overwegingen
Bij patiënten met hypertriglyceridemie (TG hoger dan 1,5 mmol/l) is het belangrijk onderscheid te maken welke triglyceriderijke lipoproteïnepartikels verhoogd zijn: chylomicronen of chylomicronen en VLDL of alleen VLDL (zie figuur 1 in de module ‘(Patho)fysiologie van dyslipidemieën’). Dit onderscheid is belangrijk om een aantal redenen:
- verhoogd risico op pancreatitis bij hypertriglyceridemie op basis van chylomicronen al dan niet in combinatie met VLDL;
- differentiaaldiagnose afhankelijk van de (verhoogde) aanwezige triglyceridenrijke lipoproteïnenpartikels.
In tabel 1 worden de verschillende primaire en secundaire oorzaken van hypertriglyceridemie op basis van aanwezige lipoproteïnen weergegeven.
Tabel 1 Primaire en secundaire oorzaken van hypertriglyceridemie op basis van verschillende lipoproteïnen
|
Hypertriglyceridemie Op basis van: |
Chylomicronen |
Chylomicronen en VLDL |
VLDL |
|
Primaire oorzaken |
Familiaire hyperchylomicronemie |
Partiele LPL-deficiëntie* |
Familiaire hypertriglyceridemie |
|
|
Complete LPL-deficiëntie |
apoAV-deficiëntie* |
Partiele LPL-deficiëntie |
|
|
ApoCII-deficiëntie |
|
Partiele apoAV-deficiëntie |
|
Secundaire oorzaken |
Systemische lupus erythematosus |
Abdominale obesitas |
Abdominale obesitas |
|
|
|
Diabetes mellitus type 2 |
Diabetes mellitus type 2 |
|
|
|
Metabool syndroom |
Metabool syndroom |
|
|
|
Glucocorticoïden en steroïden gebruik |
Glucocorticoïden en steroïden gebruik |
|
|
|
Alcoholgebruik |
Alcoholgebruik |
|
|
|
Antipsychotica |
Antipsychotica |
|
|
|
End-stage renal disease |
End-stage renal disease |
|
|
|
|
Polycysteus-ovariumsyndroom |
|
|
|
|
Hemodialyse |
|
|
|
|
Hiv |
|
|
|
|
HAART |
* Vaak gecombineerd met een secundaire oorzaak
De differentiaaldiagnose kan worden gemaakt door adequaat lichamelijk onderzoek, uitgebreide familieanamnese met betrekking tot dyslipidemie, hart- en vaatziekten en pancreatitis en desgewenst genetisch onderzoek. Wanneer men alleen de lipiden TC en TG en het LDL-C en HDL-C meet, dan kan niet worden gedifferentieerd tussen de 3 verschillende vormen van hypertriglyceridemie op basis van 1) VLDL-partikels; 2) VLDL en chylomicronen; 3) chylomicronen. Traditioneel kunnen de triglyceridenrijke partikels gemeten worden middels dure, tijdrovende geavanceerde technieken, die vaak alleen beschikbaar zijn in gespecialiseerde laboratoria. Het betreffen geen routine bepalingen.
Het meten van apoB in combinatie met TC en TG en het toepassen van het apoB- algoritme maken het eenvoudig mogelijk vast te stellen welke triglyceriderijke deeltjes verhoogd aanwezig zijn en dus welke differentiaaldiagnoses overwogen kunnen worden (zie figuur 2 in de module ‘Diagnose bij hypercholesterolemie met LDL’). Voor een precieze diagnose is een volledige (familie) anamnese, met lichamelijk onderzoek en eventueel nader laboratoriumonderzoek nodig (zie figuur 2 in de module ‘Diagnose bij hypercholesterolemie met LDL’ en overige submodules).
Hoe kan bepaald worden welke lipoproteïnepartikels aanwezig zijn voor het stellen van een differentiaaldiagnose bij patiënten met hypertriglyceridemie op basis van chylomicronen?
Chylomicronen zijn zeer grote, triglyceride-rijke partikels. De triglyceriden worden normaal gesproken zeer snel gehydrolyseerd door lipoproteïne lipase (LPL) in vetweefsel en in de spieren. Een belangrijke cofactor voor LPL-activiteit is het apoCII. Het apoCIII remt de LPL-activiteit. Het remnantpartikel dat vervolgens ontstaat - kleiner en relatief cholesterolrijk partikel – wordt vervolgens snel door de lever opgenomen en afgebroken (figuur 1).
Figuur 1 Exogene lipoproteïnenmetabolisme
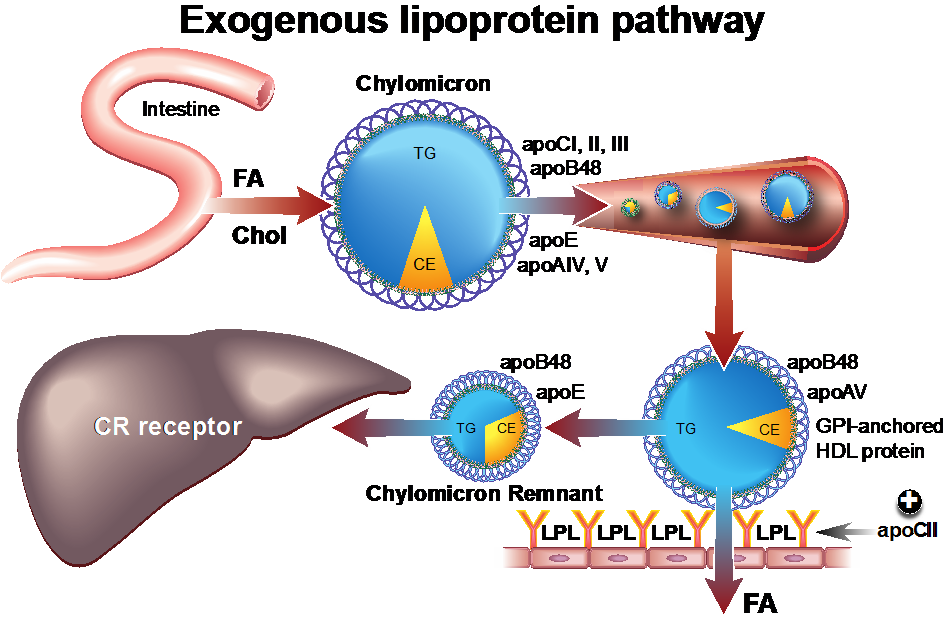
Een van de primaire oorzaken van hypertriglyceridemie op basis van chylomicronen is familiaire hyperchylomicronemie (tabel 1).
Familiaire hyperchylomicronemie (FHC)
Diagnostiek: Bij patiënten met hypertriglyceridemie TG >10 mmol/l moet men overwegen of er sprake kan zijn van hyperchylomicronemie. Met de traditionele lipiden en lipoproteïne metingen is dit niet mogelijk. Bij zeer hoge TG-concentraties >20 mmol/l is het steeds waarschijnlijker dat er sprake is van hyperchylomicronemie. Een hulpmiddel om een indicatie te krijgen of er sprake is van hyperchylomicronemie is het toepassen van het apoB diagnostisch algoritme (zie de module ‘(Patho)fysiologie van dyslipidemieën’). Tevens kan gebruik worden van het algoritme ontwikkeld door Stroes (2017). LPL-activiteit kan worden gemeten in het plasma na toediening van heparine, waardoor LPL loskomt van het endotheel. Tevens kan in gespecialiseerde laboratoria de apoCII/CIII-ratio gemeten worden (zoals bij het AMC, ErasmusMC of UMCU). In de praktijk heeft dit geen invloed op de keuze voor therapie. Tevens kan genetisch onderzoek overwogen worden (mutaties in LPL, ApoA5, ApoCII of GPIHBP1).
Klinische diagnostische kenmerken: FHC is een zeldzame aandoening (1:1.000.000). Vaak presenteert het zich al op kinderleeftijd met buikpijn en pancreatitis. Daar apoB normaal is – vaak juist laag – is het risico op hart- en vaatziekten niet verhoogd. Wanneer TG >10 mmol/l is er grotere kans op pancreatitis. Bij lichamelijk onderzoek let men op de aanwezigheid van eruptieve xanthomen. Dit zijn kleine, gele papula vaak in clusters op de rug, op de billen en dorsale zijde van handen, armen en benen. Bij fundoscopie is sprake van lipaemia retinalis en bij buikonderzoek hepatosplenomegalie door opname van chylomicronen door reticuloendotheliale cellen in de lever en de milt. Na centrifugatie van het bloed is het plasma/serum melkachtig in plaats van lichtgeel. Hypertriglyceridemie kan leiden tot pseudohyponatriemie, afhankelijk van de gebruikte natriummethode in het laboratorium.
Pathofysiologie: Bij FHC is er sprake van genetisch defect waardoor LPL niet wordt aangemaakt en er dus sprake is van complete LPL-deficiëntie. Er kan ook sprake zijn van genetisch defect waardoor er geen apoCII wordt gemaakt (apoCII-deficiëntie), een belangrijke cofactor voor LPL-activiteit. Tot slot kan er sprake zijn van een defect in GPI-anchored HDL – een eiwit dat betrokken is bij de binding van LPL aan het endotheel, of een apoAV-deficiëntie, een apoproteïne dat nodig is voor binding van LPL aan triglyceriden (figuur 2). In zeer zeldzame gevallen kan er sprake zijn van een defect in het Lipase Maturation Factor 1 (LMF1), een eiwit dat essentieel is voor de vouwing en uitrijping van het LPL-eiwit in het endoplamatisch reticulum.
Figuur 2 Pathofysiologie van hyperchylomicronemie
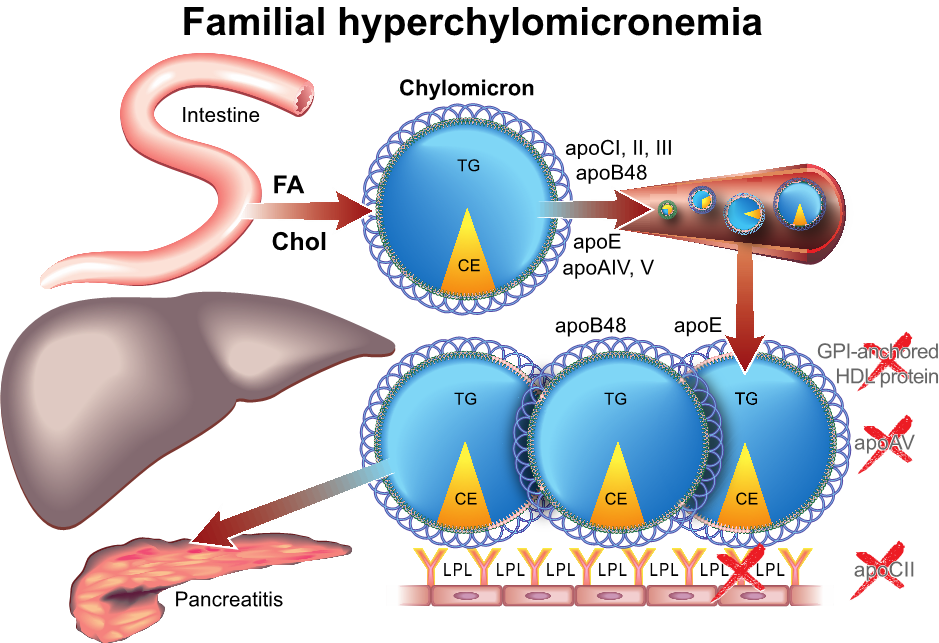
De secundaire oorzaak van hypertriglyceridemie op basis van chylomicronen is systemische lupus erythematosus (SLE). Bij patiënten met SLE kan er sprake zijn van hypertriglyceridemie, hypercholesterolemie en laag HDL-C.
Pathofysiologie: Bij patiënten met SLE kunnen antistoffen tegen apoCII en/of LPL gevormd worden waardoor patiënten zich presenteren met hyperchylomicronemie.
Klinische diagnose: zie FHC.
De differentiaaldiagnose kan worden gemaakt door adequaat lichamelijk onderzoek, uitgebreide familieanamnese met betrekking tot dyslipidemie en pancreatitis en desgewenst nader laboratorium bestaande uit chylomicronen, LPL-activiteit, ApoCII/III ratio, apoA-V-meting. Tevens kan genetisch onderzoek overwogen worden (mutaties in LPL, apoA5, apoCII of GPIHBP1).
Hoe kan bepaald worden welke lipoproteïnepartikels aanwezig zijn voor het stellen van een differentiaaldiagnose bij patiënten met hypertriglyceridemie op basis van chylomicronen en VLDL?
Bij patiënten met hypertriglyceridemie TG >10 mmol/l moet men overwegen of er sprake is van aanwezigheid van zowel chylomicronen als VLDL-partikels (figuur 3). Met de traditionele lipiden en lipoproteïnen metingen is dit niet mogelijk. Bij zeer hoge TG-concentraties >20 mmol/l is het steeds waarschijnlijker dat er sprake is van hyperchylomicronemie.
Een hulpmiddel om een indicatie te krijgen of er sprake is van aanwezigheid van chylomicronen en VLDL-partikels is het toepassen van het apoB diagnostisch algoritme (zie de module ‘(Patho)fysiologie van dyslipidemieën’).
Normaal worden de triglyceriden in chylomicronen en VLDL-partikels gehydrolyseerd door LPL. ApoAV is een apolipoproteïne dat betrokken is bij de interactie van LPL met triglyceriden. Voor de VLDL-partikels is dit de eerste stap naar conversie in LDL-partikels (figuur 3).
LPL-activiteit kan worden gemeten in het plasma na toediening van heparine, waardoor LPL loskomt van het endotheel. Tevens kan in gespecialiseerde laboratoria de apoAV gemeten worden. In de praktijk biedt dit geen meerwaarde daar het therapeutisch beleid niet verandert.
De primaire oorzaken van hypertriglyceridemie op basis van chylomicronen en VLDL zijn partiële LPL-deficiëntie en apoAV-deficiëntie (beide vaak gecombineerd met secundaire oorzaak) (tabel 1).
Partiële LPL-deficiëntie en/of apoAV-deficiëntie
Diagnostiek: Bij zeer sterk verhoogde TG (>10 mmol/l) kan er sprake zijn van verhogingen van chylomicronen en VLDL-partikels. Meet bij patiënten met hypertriglyceridemie het apoB en TC en pas het apoB diagnostisch algoritme toe. Patiënten met partiële LPL-deficiëntie en/of apoAV-deficiëntie hebben vaak een verhoogd aantal VLDL-partikels, die triglyceridenrijk zijn met een normaal aantal LDL-partikels. Daarom is het apoB vaak normaal (<1,2 g/l) en dus is het cardiovasculaire risico niet echt verhoogd. Vaak zien we dat juist patiënten met partiële LPL-deficiëntie en of apoAV-deficiëntie hypertriglyceridemie kunnen ontwikkelen wanneer er tevens sprake is van DM2, abdominale obesitas, alcohol gebruik en medicatie gebruik als steroïden of estrogenen.
Klinische diagnostische kenmerken: Wanneer TG >10 mmol/l is er grotere kans op pancreatitis. Bij lichamelijk onderzoek let men op de aanwezigheid van eruptieve xanthomen. Dit zijn kleine, gele papula vaak in clusters op de rug, op de billen en dorsale zijde van handen, armen en benen. Bij fundoscopie is sprake van lipaemia retinalis en bij buikonderzoek hepatosplenomegalie door opname van chylomicronen door reticuloendotheliale cellen in de lever en de milt. Na centrifugatie van het bloed is het plasma/serum melkachtig in plaats van lichtgeel. Hypertriglyceridemie kan leiden tot pseudohyponatriemie, afhankelijk van de gebruikte natriummethode in het laboratorium.
Figuur 3 Endogene lipoproteïnemetabolisme
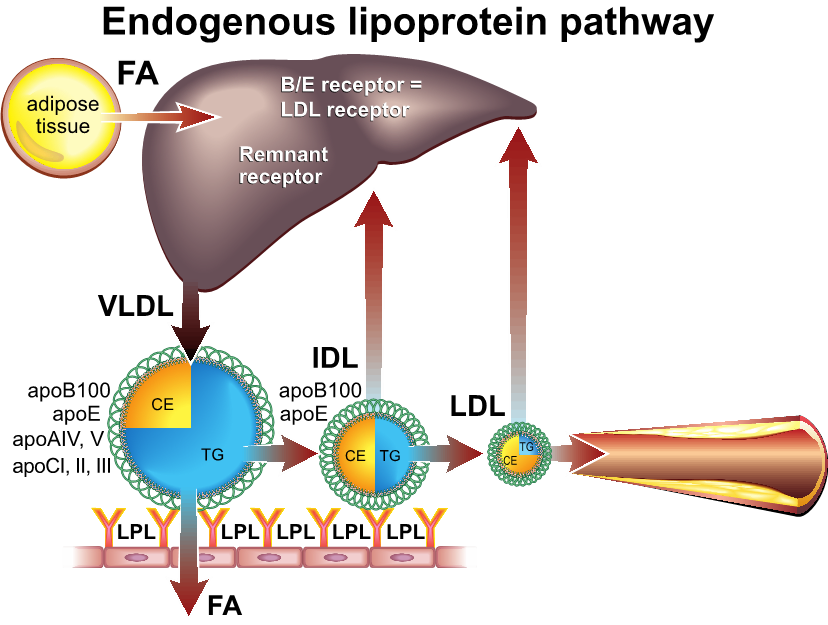
De differentiaaldiagnose kan worden gemaakt door volledige (familie) anamnese, met lichamelijk onderzoek en eventueel nader laboratorium en/of genetisch onderzoek bestaande uit Chylomicronen, LPL-activiteit, apoAV-meting. Tevens kan genetisch onderzoek overwogen worden (mutaties in LPL, apoA5) (zie www.dnadiagnostiek.nl en www.jojogenetics.nl/wp voor een aanvraagformulier).
Hoe kan bepaald worden welke lipoproteïnepartikels aanwezig zijn voor het stellen van een differentiaaldiagnose bij patiënten met hypertriglyceridemie op basis van VLDL?
De triglyceriden in VLDL-partikels worden normaal gehydrolyseerd door LPL, waarna verder conversie plaatsvindt naar LDL-partikels. ApoAV is betrokken bij de associatie van VLDL met LPL en mogelijk ook bij activatie van LPL (figuur 3). Hypertriglyceridemie kan het gevolg zijn van een toename in het aantal VLDL-partikels en/of triglyceride verrijking van de VLDL-partikels (figuur 4).
Bij patiënten met hypertriglyceridemie TG <10 mmol/l moet men overwegen of er sprake is van een toename in het aantal van alléén VLDL-partikels. Met de traditionele lipiden en lipoproteïnenmetingen is dit niet mogelijk. Wel is het mogelijk om met tijdrovende, kostbare ultracentrifugatie methode VLDL-cholesterol en VLDL-triglyceriden direct te meten.
Een hulpmiddel om een indicatie te krijgen of er sprake is van toename in het aantal VLDL-partikels is het toepassen van het apoB diagnostisch algoritme (zie de module ‘(Patho)fysiologie van dyslipidemieën’).
Figuur 4 Verhoogde triglyceriden op basis van een toename in het aantal VLDL-partikels en/of triglyceride verrijking van de VLDL-partikels
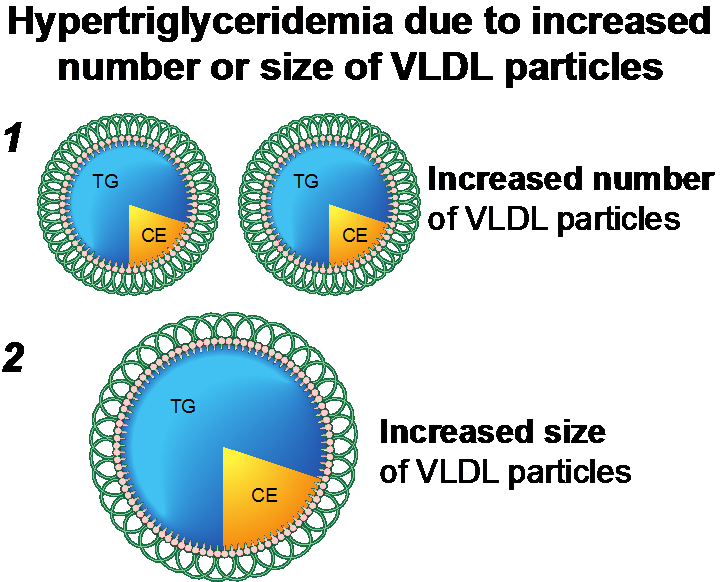
Een van de primaire oorzaken van hypertriglyceridemie op basis van VLDL is familiaire hypertriglyceridemie (tabel 1).
Familiaire hypertriglyceridemie (FHTG)
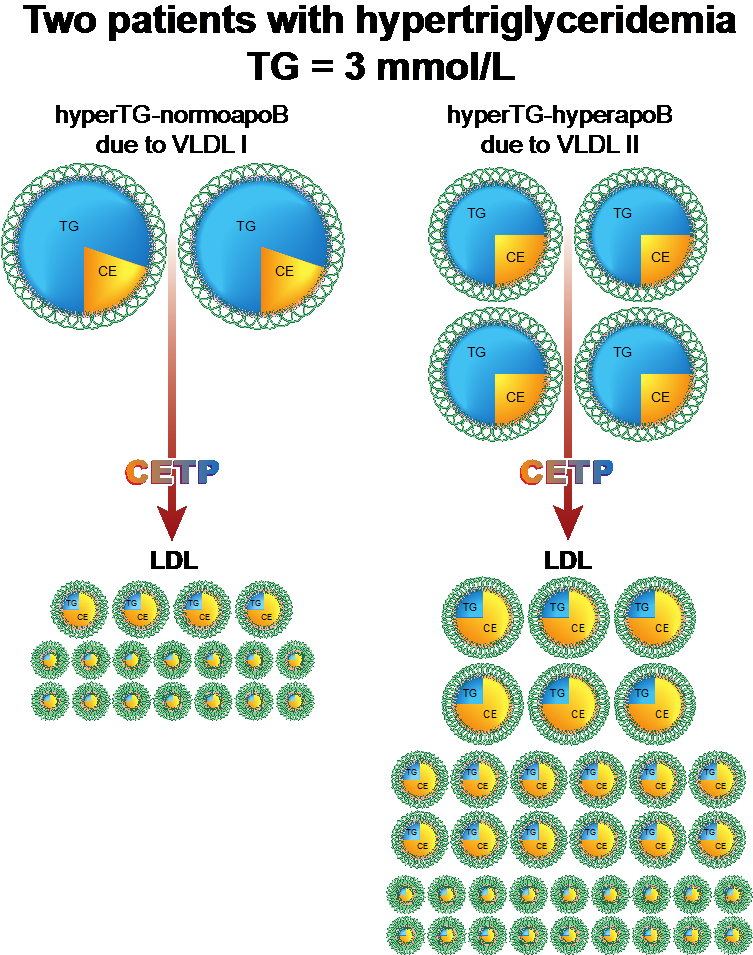
FHTG is een relatief frequent voorkomende autosomaal dominante aandoening (1:500) van onbekende origine waarbij diverse factoren betrokken bij toegenomen productie en/of gestoorde klaring van VLDL-partikels een rol spelen. Er is meestal sprake van milde hypertriglcyeridemie (TG <5 mmol/l). Hypertriglyceridemie is het gevolg van een toename in het aantal VLDL-partikels en/of triglyceride verrijking van de VLDL-partikel. Echter, het aantal LDL-partikels is normaal en dus is apoB normaal (hyperTG-normoapoB). Wanneer patiënten DM2 of overgewicht of metabool syndroom ontwikkelen dan verergert het metabole defect (door toegenomen vrije vetzuur flux naar de lever en dus stimulering van TG-productie) waardoor het fenotype kan veranderen in hyperTG-hyperapoB. Het hyperTG-hyperapoB fenotype is zeer atherogeen en indicatie voor behandeling (figuur 5). Het fenotype hyperTG-normoapoB kan ook het gevolg zijn van partiële LPL-deficiëntie of apoAV-deficiëntie.
Figuur 5 Fysiologie van hypertriglyceridemie met laag apoB (hyperTG-normoapoB) en hypertriglyceridemie met hoog apoB (hyperTG-hyperapoB) met de aanwezigheid van kleine, dense LDL-partikels
Diagnostiek: Meestal is er sprake van milde hypertriglyceridemie (<5 mmol/l). Bepaal in patiënten met hypertriglyceridemie altijd het TC en apoB om vervolgens via het apoB-algoritme vast te stellen welke lipoproteïnenpartikels in verhoogd aantal aanwezig zijn. Wanneer er sprake is van verhoogd aantal van alléén VLDL-partikels dan moet men de diagnose FHTG overwegen. Er zijn geen specifieke diagnostische testen. Belangrijk is het om de familieanamnese uit te diepen op 1e graads familieleden met hypertriglyceridemie.
Klinische diagnostiek: Er zijn geen specifieke kenmerken bij lichamelijk onderzoek. Wanneer apoB normaal is, is het risico op hart- en vaatziekten niet verhoogd (hyperTG-normoapoB). Men kan dan terughoudend zijn, zeker in primaire preventie setting, om de FHTG te behandelen, tenzij de triglyceriden dusdanig verhoogd zijn dat risico op pancreatitis is toegenomen. Juist die patiënten met FHTG die DM2, overgewicht of metabool syndroom ontwikkelen, zullen het hyperTG-hyperapoB fenotype gaan ontwikkelen hetgeen een indicatie voor behandeling is.
Secundaire oorzaken van hypertriglyceridemie op basis van VLDL
In een groot aantal gevallen is milde hypertriglyceridemie (<5 mmol/l) secundair aan adipositas, overmatig alcoholgebruik, het metabool syndroom en diabetes mellitus type 2 of bepaalde medicatie; veelal is er dan tevens sprake van een verlaagd HDL-cholesterol. De LDL-cholesterolconcentratie is vaak volledig normaal. Daarnaast is het van groot belang dat men bij patiënten met FHTG en normaal LDL-C vaststelt of er sprake is van de aanwezigheid van small, dense LDL, daar dit juist zeer atherogene partikels zijn. Wanneer er sprake is van normaal LDL-C met een verhoogd apoB (>1,2 g/l) is er sprake van zeer vele – relatief cholesterol-arme- LDL-partikels. Dus FHTG–hyperapoB wijst op een zeer atherogeen lipidenprofiel. Meet dus bij iedere patiënt met FHTG het apoB en TC opdat u 1) via het apoB diagnostische algoritme een indicatie krijgt welke triglyceride-rijke en cholesterolrijke lipoproteïnenpartikels verhoogd in aantal aanwezig zijn EN 2) u weet of er sprake is van small, dense LDL (zie figuur 2 in de module ‘(Patho)fysiologie van dyslipidemieën’ en figuur 5).
Onderbouwing
Beoordelingsdatum en geldigheid
Publicatiedatum : 03-04-2018
Beoordeeld op geldigheid : 03-04-2018
Deze richtlijn is geautoriseerd is door de in de werkgroep participerende partijen; daarnaast ligt deze richtlijn nog ter autorisatie voor bij de VKGN.
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep wel in stand gehouden. Het bestuur van de Nederlandse Internisten Vereniging bepaalt uiterlijk na de autorisatie van de multidisciplinaire richtlijn CardioVasculair RisicoManagement (CVRM) of de modules van deze richtlijn nog actueel zijn. Aangezien de richtlijn naar de huidige CVRM-richtlijn uit 2011 refereert, zal bij een herziene CVRM-richtlijn gecontroleerd moeten worden of de verwijzingen nog kloppen. De geldigheid van deze richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De Nederlandse Internisten Vereniging is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten (www.kennisinstituut.nl) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Het doel van deze richtlijn is het bevorderen van een optimale diagnostiek en behandeling van patiënten met een (erfelijke) dyslipidemie. Door het optimaliseren van de diagnostiek en behandeling bij een (erfelijke) dyslipidemie wordt het risico op het krijgen van hart- en vaatziekten en de andere genoemde aandoeningen verkleind.
Doelgroep
Deze richtlijn is geschreven voor alle leden van de beroepsgroepen van internisten, cardiologen en kinderartsen. Daarnaast is deze richtlijn bedoeld om zorgverleners die anderzijds betrokken zijn bij patiënten met (erfelijke) dyslipidemie te informeren, waaronder (kader)huisartsen, neurologen, vaatchirurgen, laboratoriumspecialisten klinische chemie, klinisch genetici/genetisch consulenten (klinische genetica), verpleegkundig specialisten hart- en vaatziekten en praktijkondersteuners.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2015 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met (erfelijke) dyslipidemie te maken hebben.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Professor dr. J. (Jacqueline) de Graaf, internist-vasculaire geneeskunde, werkzaam in het Radboudumc te Nijmegen, voorzitter, NIV
- Dr. J.E. (Jeanine) Roeters van Lennep, internist-vasculaire geneeskunde, werkzaam in het Erasmus MC te Rotterdam, voorzitter, NIV
- Professor dr. F.L.J. (Frank) Visseren, internist-vasculaire geneeskunde, werkzaam in het UMCU te Utrecht, NIV
- Dr. B.P.M. (Ben) Imholz, internist-vasculaire geneeskunde, werkzaam in het Elisabeth-TweeSteden Ziekenhuis te Tilburg, NIV
- Dr. J.J.J. (Jeroen) de Sonnaville, internist-endocrinoloog, werkzaam in het Tergooi Ziekenhuis te Hilversum, NIV
- Dr. P.E. (Petr) Jira, kinderarts, werkzaam in het Jeroen Bosch Ziekenhuis te ’s-Hertogenbosch, NVK
- Dr. A. (Anho) Liem, cardioloog, werkzaam in het Sint Franciscus Gasthuis te Rotterdam, NVVC
- Dr. T. (Talip) Tumkaya, huisarts, werkzaam in de Huisartsenpraktijk Parkhof te Maassluis, NHG
- H. (Hans) van Laarhoven, manager team collectieve belangenbehartiging, werkzaam bij de Hart&Vaatgroep te Den Haag, De Hart&Vaatgroep
Meelezers:
- J.M.H. (Annette) Galema-Boers, verpleegkundig specialist, werkzaam bij Erasmus MC te Rotterdam, NVHVV
- Dr. R.P. (Raoul) Kloppenborg, neuroloog, werkzaam bij het UMCU te Utrecht, NVN
- Dr. J.C. (Joep) Defesche, staflid Laboratorium voor Genoom diagnostiek, werkzaam bij het AMC te Amsterdam
- Dr. J. (Peter) van Tintelen, klinisch geneticus, werkzaam bij het AMC te Amsterdam, VKGN
- Dr. S. (Sjana) Kos, klinisch chemicus, werkzaam bij het Maasstadziekenhuis te Rotterdam, NVKC
- Dr. B.H.P. (Bernard) Elsman, chirurg, werkzaam bij het Deventer Ziekenhuis te Deventer, NVVH
- Dr. M.E. (Janneke) Wittekoek, cardioloog en medisch directeur Stichting LEEFH, werkzaam bij Heartlife Klinieken & Stichting LEEFH, StLEEFH
Met ondersteuning van:
- Dr. B.H. (Bernardine) Stegeman, adviseur, Kennisinstituut van Medisch Specialisten
- A. (Anouk) Rozeboom, MSc, junior adviseur, Kennisinstituut van Medisch Specialisten
- Ing. L.H.M. (Linda) Niesink-Boerboom, MSc, literatuurspecialist, Kennisinstituut van Medisch Specialisten
- S. (Samara) de Jong-Jaber, MSc, beleidsadviseur, Nederlandse Internisten Vereniging
- G.M. (Maike) van Leeuwen, beleid- en projectondersteuner, Nederlandse Internisten Vereniging
- N.F. (Natalia) Bullock, projectsecretaresse, Kennisinstituut van Medisch Specialisten
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling” is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventueel belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
De Graaf |
|
Geen |
Ontwikkelaar van de ApoB-app (diagnostisch tool op basis van apoB) |
Geen opsteller aanbevelingen over het gebruik van de ApoB-app |
|
Roeters van Lennep |
Internist-vasculair geneeskundige |
|
|
Geen actie; Lomitapide wordt niet in de richtlijn besproken en lezingen zijn overschrijdend over de hele richtlijn. |
|
Visseren |
|
|
Deelname aan verschillende fase II en III multicenter klinische trials met PCSK9 monoklonale antilichamen of PCSK9 siRNA (Amgen, Sanofi, Pfizer), antisense apoB (GenZyme), antisense Lp(a) (ISIS) antisense apoCIII (ISIS).
|
Geen actie (PCSK9 monoklonale antilichamen: alleen betrokken bij patiënteninclusie; PCSK9 siRNA: nog niet beschikbaar en naar verwachting ook niet binnen twee jaar)
|
|
Imholz |
Internist-vasculair geneeskundige |
|
|
Geen actie; gemelde belangen zijn overschrijdend aan de gehele richtlijn |
|
De Sonnaville |
Internist-endocrinoloog |
Geen |
Geen |
Geen actie |
|
Jira |
Kinderarts |
Geen |
Geen |
Geen actie |
|
Liem |
|
|
|
Geen actie; gemelde belangen zijn overschrijdend aan de gehele richtlijn |
|
Tumkaya |
|
Geen |
Geen |
Geen actie |
|
Van Laarhoven |
|
Lid Raad van Toezicht LAREB (bestuurskostenvergoeding conform NVTZ)
|
Geen |
Geen actie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door afgevaardigde patiëntenvereniging in de werkgroep. De conceptrichtlijn is tevens voor commentaar voorgelegd aan De Hart&Vaatgroep.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door De Hart&Vaatgroep, NHG en VIG (voorheen Nefarma) via invitational conference. Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitters en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR – voor systematische reviews; Cochrane – voor gerandomiseerd gecontroleerd onderzoek; ROBINS-I – voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008), en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module 'Randvoorwaarden bij dyslipidemie'.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review.
Medisch Specialistische Richtlijnen 2.0. Adviescommissie Richtlijnen van de Raad Kwalitieit. https://richtlijnendatabase.nl/over_deze_site.html. 2012.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten, 2015.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html. 2013.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID) 2005 – augustus 2017
|
1 exp Dyslipidemias/ or dyslipidemia*.ab,ti. (66941) 2 exp Algorithms/ or algorithm*.ab,ti. (263050) 3 1 and 2 (307) 4 limit 3 to yr="2005 -Current" (216) 5 limit 4 to (dutch or english) (187) 6 not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (178) 7 exp "Sensitivity and Specificity"/ or (Sensitiv* or Specific*).ti,ab. or (predict* or ROC-curve or receiver-operator*).ti,ab. or (likelihood or LR*).ti,ab. or exp Diagnostic Errors/ or (inter-observer or intra-observer or interobserver or intraobserver or validity or kappa or reliability).ti,ab. or reproducibility.ti,ab. or (test adj2 (re-test or retest)).ti,ab. or "Reproducibility of Results"/ or accuracy.ti,ab. or Diagnosis, Differential/ or Validation Studies.pt. (5678848 8 6 and 7 (85) 9 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (337183) 10 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] (2919218) 11 8 and 9 (2) 12 8 and 10 (34) 13 11 or 12 (36)
= 36 (33 uniek) |
33 |

