Chirurgische behandeling van Lynch syndroom
Uitgangsvraag
Wat is de optimale chirurgische behandeling bij patiënten met Lynch syndroom en primair resectabel CRC?
De uitgangsvraag omvat de volgende deelvragen:
- Wat is de optimale chirurgische behandeling van patiënten met Lynch syndroom en coloncarcinoom?
- Wat is de optimale chirurgische behandeling van patiënten met Lynch syndroom en rectumcarcinoom?
- Wat is de optimale behandeling van vrouwelijke patiënten met Lynch syndroom en endometriumcarcinoom of ovariumcarcinoom?
- Wat is de optimale behandeling van vrouwelijke patiënten met Lynch syndroom en coloncarcinoom met betrekking tot (preventieve) hysterectomie en adnexextirpatie?
- Is er invloed van het type pathogene variant van het mismatch repair gen op de chirurgische behandeling van CRC bij patiënten met Lynch syndroom?
Aanbeveling
Bespreek de voor- en nadelen van de behandeling(en) met de patiënt middels shared decision making.
Colon en rectum carcinoom:
- Overweeg bij patiënten met Lynch syndroom (LS) met een MSH2 of MLH1 pathogene variant en coloncarcinoom een subtotale colectomie met ileorectale of ileosigmoidale anastomose. Overweeg bij oudere patiënten een segmentele resectie.
- Verricht bij patiënten met Lynch syndroom met een MSH6 of PMS2 pathogene variant en coloncarcinoom bij voorkeur een segmentele resectie.
- Bespreek bij vrouwen met MLH1-LS, MSH2-LS en MSH6-LS en een coloncarcinoom de optie om tegelijk met colonchirurgie een preventieve hysterectomie met dubbelzijdige adnexextirpatie verrichten vanaf 40-45 jaar na goede counseling van de voor- en nadelen.
Verricht geen aanvullende preventieve hysterectomie en dubbelzijdige adnexextirpatie bij PMS2 gen draagsters voor het 50e jaar. Bespreek en overweeg bij deze vrouwen een preventieve hysterectomie en dubbelzijdige adnexextirpatie of dubbelzijdige tubectomie postmenopauzaal.
- Behandel patiënten met Lynch syndroom en rectumcarcinoom volgens de richtlijn colorectaal carcinoom: behandeling rectumcarcinoom met betrekking tot indicatie voor neoadjuvante behandeling en chirurgische resectie. Verricht een rectumresectie in plaats van primair een proctocolectomie.
Endometrium en ovariumcarcinoom
- Behandel patiënten met Lynch en een endometriumcarcinoom volgens de richtlijn behandeling endometriumcarcinoom
- Behandel patiënten met Lynch en een ovariumcarcinoom volgens de richtlijn ovariumcarcinoom.
Preventieve gynaecologische chirurgie:
- Overweeg preventieve gynaecologische chirurgie, (laparoscopische uterusextirpatie met dubbelzijdige adnexextirpatie bij patiënten met MLH1-LS, MSH2-LS en MSH6-LS vanaf 40-45 jaar, na goede counseling van de voor- en nadelen.
- Er is geen indicatie voor preventieve gynaecologische chirurgie bij PMS2-LS bij premenopauzale vrouwen. Overweeg preventieve chirurgie bij patiënten met PMS2-LS bij postmenopauzale vrouwen, waarbij de afweging kan worden gemaakt om een uterusextirpatie met dubbelzijdige tubectomie i.p.v. een dubbelzijdige adnexextirpatie te verrichten, omdat het risico op een ovariumcarcinoom bij PMS2-LS niet verhoogd is.
Overwegingen
Balans tussen gewenste en ongewenste effecten
De nieuwe richtlijn erfelijke darmkanker uit Groot-Brittannië en Ierland benoemt op basis van de huidige literatuur dat er in de laag-risico PV-groepen onvoldoende oncologisch bewijs is voor subtotale colectomie (Monahan, 2020).
De kans op metachroon CRC correleert met de mismatch repair gen status. In een retrospectieve cohortstudie in Lynch patiënten die onder controle waren na segmentele colectomie voor CRC was het percentage metachrone CRC 20%; geen van de patiënten met een PMS2 of MSH6 pathogene variant ontwikkelden een metachrone tumor (Quezada-Diaz, 2020).
Een grote studie (n=522) naar de kwaliteit van leven na CRC-resectie bij Lynch patiënten, patiënten met FAP en patiënten met multipele poliepen zag 25% kans op perioperatieve complicaties na segmentele colectomie versus 40–57% kans op complicaties na subtotale colectomie met ileosigmoidale of ileorectale anastomose. Op langere termijn was sprake van sociaal invaliderende slechtere darmfunctie bij 32% van de patiënten na subtotale colectomie. Dit was hoger dan in de groep na segmentele resectie, maar had geen invloed op de kwaliteit van leven tussen beide groepen; derhalve adviseren de auteurs individuele besluitvorming (You, 2008). Deze resultaten over lange termijneffecten van een segmentele of subtotale resectie aangaande darmfunctie; frequentie van defecatie en consistentie van defecatie relevant in de spreekkamer bij het gezamenlijk komen tot een beslissing tot het ene of het andere type operatie.
Markov-modellering voor de potentiële overlevingswinst van subtotale colectomie versus segmentele colectomie toont een geschatte overlevingswinst van 2,7 jaar bij 27-jarigen, 1 jaar bij 47-jarigen en 4 maanden bij 67-jarigen met primair CRC, dus leeftijd ten tijde van het eerste CRC kan worden meegenomen in de beslissing voor een segmentele of subtotale resectie (De Vos tot Nederveen, 2003).
Nieuwe ontwikkelingen behandeling CRC
Neoadjuvante chemotherapie
Bij Lynch patiënten met primair irresectabel, niet op afstand gemetastaseerd CRC kunnen worden voorbehandeld volgens de huidige richtlijn colorectaal carcinoom_primaire_behandeling_coloncarcinoom. In de FOxTROT-studie (Foxtrot collaborative group, 2012) zijn patiënten met primair resectabel cT3 of cT4 coloncarcinoom gerandomiseerd tussen 24 weken adjuvante chemotherapie (controle) en 6 weken chemotherapie neoadjuvant, waarna adjuvant continueren tot een totaal van 24 weken (experimenteel).
De fase 3 studie (n=699) laat zien dat neoadjuvante chemotherapie veilig is in termen van niet-verschillende perioperatieve complicaties en effectief in termen van het verkrijgen van meer tumorregressie, met een betere ziekte specifieke controle na 2 jaar. Een relevante subgroep analyse uit de FoxTROT data toont echter dat MMRp tumoren een significant betere tumorregressie na NAC tonen dan MMRd tumoren (23% vs. 7%, P < .001). Dit moet worden meegenomen in besluitvorming rondom inductietherapie met chemotherapie bij Lynch patiënten met een irresectabel CRC (Morton, 2023).
Neoadjuvante immunotherapie
Er is goede evidence dat neoadjuvante immunotherapie leidt tot pathologische tumorrespons in MMRd tumoren. De NICHE studie (Chalabi, 2020) onderzocht het effect en de veiligheid van een enkele dosis ipilimumab en twee doses nivolumab voorafgaand aan curatieve resectie van CRC in MMRp en MMRd patiënten. In 20/20 (100%) van de MMRd tumoren werd een pathologische respons gezien, met 19 ‘majeure’ pathologische reponses (< 10% tumorresidu) en 12 complete pathologische respons; de auteurs pleiten dat deze strategie de potentiële nieuw behandeling wordt voor MMRd coloncarcinomen. De vervolgstudie (NICHE-2; Chalabi, 2024) met 107 MMRd tumoren toont ook een vergelijkbare zeer hoge pathologische respons na neoadjuvante immunotherapie, met 68% complete pathologische respons. Momenteel loopt er een Nederlandse studie naar de waarde van inductietherapie met pembrolizumab voor patiënten met een irresectabel dMMR CRC; de PUMA trial (Clinical trials register.eu EudraCT Number: 2021-005731-23). De chirurgische behandeling van CRC bij patiënten met Lynch zal hierdoor mogelijk in de toekomst veranderen.
Behandeling rectumcarcinoom
Bij patiënten met rectumcarcinoom en Lynch syndroom wordt geadviseerd het rectumcarcinoom te behandelen conform de richtlijn colorectaal carcinoom_ primaire behandeling rectumcarcinoom. Totale proctocolectomie beschermt tegen metachrone colontumoren, maar gaat gepaard met aanzienlijke morbiditeit. Het risico op het ontwikkelen van een metachrone colontumor na proctocolectomie werd onderzocht in 2 retrospectieve onderzoeken. Kalady vindt een percentage mCRC van 15% na gemiddelde follow-up van 6 jaar in een kleine cohortstudie (n=30) (Kalady, 2012). Een tweede cohortstudie vindt een mCRC percentage van 23% na proctocolectomie en adviseert om deze reden wel een proctocolectomie in jongere patiënten (Win, 2013).
Patiënten met Lynch en rectumcarcinoom hebben mogelijk een slechtere respons op neoadjuvante chemoradiotherapie (NAC) dan patiënten zonder Lynch. Een recente analyse toont tumorprogressie onder het standaard neoadjuvante regime van 29% (Cercek, 2020) en adviseert stringente monitoring gedurende neoadjuvante CRT bij deze groep. Daarbij is de pathologische respons na NAC beperkt bij patiënten met MMR deficiënte (MMRd) ten opzichte van patiënten met MMR proficiënte (MMRp) rectumtumoren (Farchoukh, 2022). Er zijn sterke aanwijzingen uit case series dat neoadjuvante immuun checkpoint inhibitors (ICI) bij patiënten met Lynch en rectumcarcinoom juist resulteren in uitstekende pathologische respons (Demisse, 2020), met zelfs 100% pathologische complete respons in een kleine cohortstudie.
Gynaecologische maligniteiten bij Lynch syndroom
Het life-time risico op het ontwikkelen van een endometriumcarcinoom bij een vrouw met het Lynch syndroom is afhankelijk van het type pathogene variant (PV). Voor MLH1- en MSH2-Lynch syndroom geldt een risico van 30-50%, voor MSH6-Lynch syndroom 20-50% en voor PMS2-Lynch syndroom PV-draagsters is het risico 10-15%. Zie ook submodule Extracolonische kankerrisico en surveillance bij het Lynch syndroom voor kankerrisico’s per type gen mutatie.
De gemiddelde leeftijd waarop dit endometriumcarcinoom zich ontwikkelt ligt tussen de 50-55 jaar (Bonadona, 2011; Baglietto ,2010; Dominquez-Valentin, 2023; Moller, 2017). Het life time risico op het ontwikkelen van een ovariumcarcinoom bij vrouwen met het Lynch syndroom is bij MLH1-Lynch syndroom PV-draagsters 5-15%, voor MSH2-Lynch syndroom is het 10-20%, voor MSH6-Lynch syndroom is het 5-10%. Voor PMS2-Lynch syndroom PV-draagsters is het risico niet verhoogd t.o.v. de algemene populatie. De gemiddelde leeftijd waarop het ovariumcarcinoom ontstaat vrouwen met het Lynch syndroom is tussen de 40-45 jaar met een grote mate van spreiding (20-80 jaar). (Helder-Woolderink, 2016; Ryan, 2017; Woolderink, 2018; Ran, 2022, Dominguez Valentin 2023).
Chirurgische behandeling van gynaecologische maligniteiten bij patiënten met Lynch syndroom.
Endometriumcarcinoom bij het Lynch syndroom
De gemiddelde leeftijd waarop endometriumcarcinomen bij Lynch syndroom ontstaat is tussen 50-55e jaar Om (voorstadia van) endometriumcarcinomen bij vrouwen met Lynch syndroom vroegtijdig op te sporen adviseert de Nederlandse richtlijn jaarlijkse screening tussen 40-60 jaar. Hierbij wordt geadviseerd om een transvaginale echo te verrichten met beoordeling van de endometriumdikte en het aspect van de ovaria te beoordelen. Tevens wordt de afname van een endometriumbiopsie geadviseerd. (Renkonen, 2007; Gerritzen, 2009) Indien bij een patiënte met het Lynch syndroom een endometriumcarcinoom wordt gediagnosticeerd is dit vaak een vroeg stadium carcinoom (FIGO-stadium 1-2). De aanbevolen behandeling is een totale laparoscopische uterusextirpatie met medenemen van de adnexen en op indicatie adjuvante radiotherapie. Dit is conform de landelijke richtlijn endometriumcarcinoom bij patiënten zonder het Lynch syndroom.
Ovariumcarcinoom bij het Lynch syndroom
Ovariumcarcinomen bij Lynch syndroom ontstaan gemiddeld rond het 45e jaar met een brede spreiding beschreven in de literatuur (20-80 jaar). Zie ook submodule Extracolonische kankerrisico en surveillance bij het Lynch syndroom . Ovariumcarcinomen bij het Lynch syndroom zijn vaker non-sereus en worden gediagnosticeerd in een vroeg stadium (FIGO-stadium I-II) in tegenstelling tot sporadische en BRCA gerelateerde ovariumcarcinomen die in een ver gevorderd stadium worden gevonden. Lynch geassocieerde ovariumcarcinomen hebben derhalve een betere prognose dan de sporadische en BRCA-gen gerelateerde ovariumcarcinomen met een 5-jaars overleving van rond de 80-85%. (Helder-Woolderink, 2016; Ryan, 2017; Woolderink, 2018; Ran 2022, Dominquez-Valentin 2023) Er zijn weinig data over de effectiviteit van screening en het vroegtijdig opsporen van ovariumcarcinomen bij Lynch syndroom. De aanbevolen behandeling van een ovariumcarcinoom bij Lynch is een proeflaparotomie met vriescoupe of een primaire debulkingsoperatie bij primair operabel ovariumcarcinoom. Bij vergevorderde stadia wordt eerst gestart met neoadjuvante chemotherapie en bij goede respons wordt een intervaldebulking verricht gevolgd door chemotherapie. De behandeling van ovariumcarcinomen bij het Lynch syndroom is conform de landelijke richtlijn ovariumcarcinomen.
Profylactische chirurgie ter preventie van endometrium- en een ovariumcarcinoom bij vrouwen met het Lynch syndroom wordt uitgevoerd middels een laparoscopische procedure. Hierbij wordt de uterus met ovaria en tubae verwijderd, dit is een effectieve procedure om endometrium en ovariumcarcinoom te voorkomen. (Schmeler, 2006; Mourits, 2010; Chen, 2007; Dominguez-Valentin, 2020) Bovendien is het een veilige minimaal invasieve procedure met een lage kans op complicaties. De mogelijke complicaties die kunnen optreden zijn een blaas/darm/uretherletsel tijdens de ingreep of adhesies en een verhoogde kans op een vaginatopprolaps na enkele jaren. (Mourits, 2010; Bijen, 2011; Obermaier, 2005; Sheyn, 2018; Lykke, 2017) De intra-operatieve risico’s zijn hoger bij oudere vrouwen en bij degenen met uitgebreide buikchirurgie in de voorgeschiedenis. (Bijen, 2011; Keurentjes, 2018; Tozzi, 2011).
Als profylactische chirurgie ter preventie van een ovariumcarcinoom bij vrouwen met Lynch syndroom premenopauzaal wordt uitgevoerd komt een vrouw vervroegd in de menopauze met vaak hinderlijke symptomen (o.a. opvliegers, humeurschommelingen, vaginale droogheid). (Etchegary, 2018; Tucker, 2017) Deze ingreep geeft ook op lange termijn een grotere kans op hart- en vaatziekten en osteoporose. (Gaba, 2020; Sideris, 2024)
De nadelen van een preventieve laparoscopische adnexextirpatie samen met het risico op een ovariumcarcinoom (<5% onder de 50 jaar) en de grote spreiding waarop ovariumcarcinoom ontstaat maakt het lastig om een uniform advies te geven over de optimale leeftijd waarop preventieve chirurgie kan worden uitgevoerd en zal per patiënt moeten worden overwogen.
In het algemeen geldt dat een preventieve laparoscopische uterusextirpatie met medenemen van het adnex overwogen kan worden bij vrouwen met een PV in het MLH1, MSH2 of MSH6 gen vanaf 40-45 jaar, met goede counseling van de voor- en nadelen. (Helder-Woolderink, 2016; Woolderink, 2018; Schmeler, 2006; Dominguez Valentin 2021) Indien er geen contra-indicatie bestaat voor hormoon substitutie na preventieve adnexextirpatie, wordt dit geadviseerd tot de leeftijd van 50 jaar.
Voor vrouwen met een PMS2-gen PV is geen reden voor een preventieve laparoscopische uterusextirpatie onder de 50 jaar aangezien een endometriumcarcinoom bij deze leeftijdsgroep nagenoeg niet voorkomt. (Dominguez Valentin, 2020; ten Broeke, 2018) Gezien het risico op ovariumcarcinoom bij PMS2-LS niet verhoogd is, kan bij preventieve uterusextirpatie overwogen worden alleen een tubectomie te doen.
Bij vrouwen met CRC en MLH1-PV, MSH2-PV, MSH6-PV of PMS2-PV kan overwogen worden tegelijk met de darmresectie ook een preventieve laparoscopische hysterectomie met bilaterale adnexextirpatie of in geval van PMS2-LS alleen tubectomie uit te voeren vanaf de leeftijd 40-45 jaar. (Dominguez Valentin, 2021; Sideris, 2024; Lu, 2008) Deze patiënt en moet preoperatief verwezen worden naar de gynaecoloog voor een gesprek over de voor- en nadelen van deze ingreep en samen met de colorectaal chirurg kan dan een perioperatief multidisciplinair plan worden opgesteld.
Kwaliteit van bewijs
Er wordt een relatief groot effect gevonden van het type colectomie op het risico op mCRC; waarbij een subtotale colectomie minder vaak leidt tot mCRC dan een segmentele colectomie. De overall kwaliteit van bewijs is laag tot zeer laag. Dit betekent dat we zeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaat mCRC en onzeker over de belangrijke uitkomstmaten mortaliteit en kwaliteit van leven.
Er is afgewaardeerd vanwege:
- Imprecisie: onnauwkeurigheid, vanwege een zeer klein aantal events bij een kleine steekproefgrootte voor de uitkomstmaat CRC gerelateerde mortaliteit
Er is opgewaardeerd vanwege:
- Relatief groot effect en consistent effect OR>3, voor de uitkomstmaat mCRC.
Waarden en voorkeuren van patiënten (en eventueel hun naasten/verzorgers)
Bij de keuze voor welk type operatie CRC bij patiënten met Lynch is shared decision making van het grootste belang. Hierbij wordt samen met de patiënt afgewogen wat de voordelen zijn van subtotale colectomie (kleinere kans op recidief CRC en minder uitgebreide controle endoscopie) en wat de nadelen zijn (veranderde stoelgang, hogere morbiditeit van de operatie). Bij vrouwelijke patiënten wordt met de gynaecoloog de voor- en nadelen van preventieve adnexextirpatie en hysterectomie afgewogen.
Kostenaspecten
In een Amerikaanse studie naar de kosteneffectiviteit van de segmentele versus de subtotale resecties wordt in een Markov beslissingsanalyse geconcludeerd, dat subtotale colectomie kosten effectiever is dan een segmentele resectie maar adviseert eerst nader onderzoek hiernaar; bij deze analyse zijn ook de kosten van (behandeling van) mCRC meegenomen. Er is niet onderzocht hoe deze analyse zich verhoudt naar de Nederlandse situatie (Jiang, 2019).
Gelijkheid ((health) equity/equitable)
Er is geen reden om aan te nemen dat de keuze voor segmentele colectomie dan wel subtotale colectomie is gerelateerd is aan gezondheidsongelijkheid.
Aanvaardbaarheid:
De aanbevelingen uit de richtlijn zijn aanvaardbaar voor betrokkenen. Er zijn geen ethische bezwaren die de uitvoer van subtotale colectomie of segmentele colectomie zoals beschreven in de aanbevelingen belemmeren.
Haalbaarheid
De aanbevelingen lijken haalbaar, dit vereist in sommige gevallen een nieuwe manier van zorgverlening (in de zin van keuze voor een operatie). De subtotale colectomie bij Lynch patiënten met CRC is over het algemeen al standaardzorg in de praktijk; de aanbeveling voor een minder invasieve behandeling met segmentele resectie voor patiënten met een MSH6 of PMS2 mutatie is haalbaar.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventies
Voor het formuleren van de aanbevelingen is afgewogen de huidige kennis uit literatuur over de kans ontwikkelen van metachrone CRC en de morbiditeit na chirurgische behandeling van primair CRC. Hierbij is de nieuwe kennis over de specifieke gen mutatie per patiënt meegenomen.
Eindoordeel:
Sterke aanbeveling voor (Doen)
Onderbouwing
Achtergrond
In patients with Lynch syndrome and CRC, subtotal (extended) colectomy may be performed due to the risk of metachronous tumors in the future. Though, after segmental colectomy of the affected part of the colon/rectum, also stringent endoscopic monitoring can be offered and discussed with the patient. However, the effectiveness of subtotal colectomy with ileosigmoidal or ileorectal anastomosis compared to segmental colectomy on the incidence of metachronous colorectal cancers, disease-specific mortality, and quality of life in patients with Lynch syndrome and primary resectable colorectal carcinoma is still unclear. This knowledge could aid in making better informed treatment choices. As in practice, the decision on the best treatment option is often based on a shared decision-making process between practitioner and patient in which age, comorbidity and patient preferences are important factors that should be taken into account.
For oncological treatment, we refer to the Dutch Colorectal Carcinoma Guideline (richtlijn behandeling colorectaal carcinoom), which also distinguishes between mismatch repair (MMR) proficient and deficient tumors (MMRp and MMRd). The vast majority of CRCs in patients with Lynch syndrome are MMRd.
Conclusies / Summary of Findings
Table 2 Summary of findings table including GRADE
|
Outcome |
Study results and measurements |
Absolute effect estimates (95% CI) |
Certainty of evidence (GRADE) |
Conclusions |
|
|
Risk with subtotal colectomy |
Risk with segmental colectomy |
|
|||
|
Metachronous CRC (crucial)
|
OR 3.43 (95% CI: 2.16 to 5.46)
Based on data from 1425 participants from 7 observational studies
|
72 per 1000 210 per 1000
Difference 138 less per 1000 (95% CI: 72 less to 226 less)
|
Moderate
Due to large and consistent effect1 |
Subtotal colectomy likely reduces the risk of mCRC compared with segmental colectomy in patients with Lynch.
De Vos tot Nederveen, 2002; Natarajan, 2010; Parry, 2011; Stupart, 2011; Aronson, 2015; Kim, 2017 and Eikenboom, 2023 |
|
|
CRC related mortality (important)
|
OR 1.66 (95% CI: 0.48 to 5.72)
Based on data from 527 participants from 1 observational study |
28 per 1000 45 per 1000b Difference 18 less per 1000 (95% CI: 113 less - 14 more) |
Very low
Due to serious imprecision2 |
The evidence is very uncertain about the effect of subtotal colectomy on mortality when compared with segmental colectomy in patients with Lynch.
Eikenboom, 2023 |
|
|
quality of life (important) measured by the SF-36 EOORTC QLQ CR-38 and COREFO questionnaire |
Based on data from 104 participants from 1 observational study |
- |
NO GRADE3
|
No evidence was found regarding the effect of subtotal colectomy on quality of life when compared with segmental colectomy in patients with Lynch. |
|
|
complications (important) |
No studies |
- |
No GRADE
|
No evidence was found regarding the effect of subtotal colectomy on complications when compared with segmental colectomy in patients with Lynch. |
|
Reasons for downgrading certainty of evidence (RCTs start at high GRADE and observational studies start at low GRADE)
- Upgraded for showing a large and consistent effect among studies
- Observational study downgraded for serious imprecision due to small number of events in only 1 study (-1 levels
- No grade was performed as study only presented a significance level and no data to reconstruct effect measures with 95% CI on overall QoL scores.
Samenvatting literatuur
Description of studies
A total of 4 studies were included in the analysis of the literature (Anele, 2017; Malik, 2018; Eikenboom, 2023; Haanstra, 2012) Important study characteristics and results are summarized. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
A meta-analysis of metachronous CRC risk after segmental colectomy and extended (subtotal) colectomy in Lynch syndrome-CRC included six studies with a total of 871 patients (mean age 36.4 years, 35% male and a median follow-up of 91.2 months). 705 patients underwent segmental colectomy, and 166 patients underwent subtotal colectomy. The authors found an increased mCRC risk in the segmental colectomy group of 22.8% (161/705) compared to 6% (10/156) in the subtotal colectomy group. (Anele, 2017)
Another meta-analysis performed by Malik, 2018 to evaluate the risk of mCRC and mortality in Lynch syndrome following segmental and subtotal colectomy. This meta-analysis largely included the same studies as the meta-analysis performed by Anele, 2017. Thus, only additional studies were added. Thereby, studies in which Lynch syndrome was based on the Amsterdam criteria, i.e. with an unknown germline status, were excluded. As a result, only one study (Kim, 2017) was added. This retrospective study investigated the risk of metachronous CRC and survival outcome after surgery in Lynch syndrome. 106 patients were included of which 30 underwent subtotal colectomy (mean follow- up of 68 months for mCRC) and 76 segmental colectomy (with a mean follow-up of 77 months). For the total cohort, the mean age was 43 years, 56% was male, and no significant difference was observed between both groups in the proportion of MMR genes mutated (p = 0.0670). No mCRC was found in the subtotal colectomy group (0/30) and in 17% (13/76) of patients who underwent segmental colectomy. No difference was found in both overall as well as CRC specific survival between the subtotal and segmental colectomy group (p = 0.65). The study did not present data to calculate effect measures on mortality. (Kim, 2017)
A recent retrospective cohort study assessed the risk of metachronous CRC between high (MLH1 and MSH2) and low risk (MSH6 and PMS2) pathogenic variants (PV) in patients with Lynch syndrome with CRC. This cohort included 527 patients of which 364 carriers with a high-risk PV and 163 with a low-risk PV. For the total cohort, the mean age at time of primary CRC was 48.7 years, 52% was male, median follow-up from the time of primary CRC diagnosis was 17.3 years. mCRC occurred in 121 (23%) and of these 97 occurred in high-risk PV (12 (10%) who underwent subtotal colectomy and 85 (70%) after segmental colectomy). mCRC occurred in 24 (20%) in low-risk PV (all segmental colectomy). Within the group with high-risk PV, segmental colectomy was associated with a significantly higher risk of mCRC compared with subtotal colectomy (HR 1·97, 95% CI 1·04–3·73; p=0·039). The risk of mCRC was similar between carriers of low-risk PV who had segmental colectomy and carriers of high-risk PV who had subtotal colectomy (HR 1·14, 0·55–2·36; p=0·72). 91 (17%) of all carriers died during follow-up in total 22 (24%) of all deaths was considered a CRC-related death. (Eikenboom, 2023).
A cross-sectional study was performed among 104 patients with Lynch syndrome who underwent a segmental or subtotal colectomy to assess quality of life (QoL). This was assessed using several questionnaires: the SF-36, the EORTC QLQ CR-38 (both QoL) and the COREFO questionnaire to assess functional outcome. 51 participants underwent segmental colectomy, and 53 patients subtotal colectomy. They found no significant differences in QoL as measured by the SF36 questionnaire in any of the domains on QoL between both groups (subtotal vs segmental). And a significant difference with more defecation problems in patients in the subtotal colectomy group (p < 0.01) and with more male sexual problems in the segmental colectomy group (p =0.02) as assessed by the EORTC QLQ CR-38 scale. In addition, patients in the subtotal colectomy group reported a higher stool frequency (p<0.01) and a higher score on social impact (p = 0.03) and stool related aspects (p = 0.06). They concluded that functional outcome is worse after subtotal colectomy than after segmental colectomy, but quality of life does not differ between both types of surgery in Lynch syndrome (Haanstra, 2012).
Results
Results are described per outcome measure. All results are summarized and presented in the Summary of Findings table, including the level of evidence, using GRADE (table 2 Summary of findings table including GRADE).
Metachronous CRC (crucial)
From seven studies data could be extracted to assess the difference between segmental and subtotal colectomy on the occurrence of mCRC. ((De Vos tot Nederveen, 2002; Natarajan, 2010; Parry, 2011; Stupart, 2011; Aronson, 2015; all from Anele, 2017), Kim 2017 and Eikenboom, 2023).
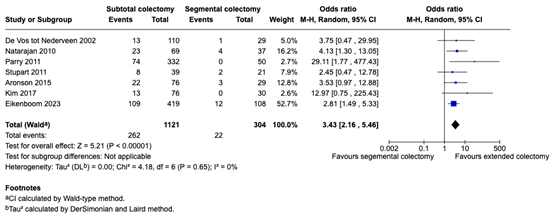
Pooled analysis included 304 patients in whom subtotal colectomy was performed and 1121 in whom segmental colectomy was performed.
Metachronous CRC was found in 22 of the 304 patients with subtotal colectomy (7,2%) and in 262 of the 1121 with segmental colectomy (23,4%). All studies demonstrated an effect in favor of the subtotal colectomy group; with a pooled OR of 3,43 (95% CI: 2,16 to 5,46) in favor of the subtotal colectomy group. Results are summarized in a forest plot (Figure 1 (submodule Chirurgische behandeling van Lynch syndroom)).
Figure 1 (submodule Chirurgische behandeling van Lynch syndroom): forest plot on mCRC occurrence
Mortality (important)
Two studies assessed mortality (Eikenboom, 2023; Kim, 2017). However, only one study reported outcome data to assess the difference in disease-specific mortality between segmental and subtotal colectomy (Eikenboom, 2023). This study found a difference in CRC- related mortality (assessed during study period 17.3 years (IQR 11.0 to25.7 years) between those with subtotal colectomy 2,8% (3/108 patients all carriers with high risk variants) or those with a segmental colectomy 4,5% (19/419 patients; of which 16 carriers with high risk variants and 3 with low risk variants); OR 1,66, 95% CI: 0,48 to 5.72).
Quality of life (important)
Only one study reported the differences in QoL between segmental and subtotal colectomy. (Haanstra, 2012). This study presented data on QoL and mentioned statistically different effects between groups on individual aspects measured by the QoL scale but did not present data to calculate effect measures on overall QoL scores between the segmental and subtotal colectomy group.
Complications (important)
This outcome was not assessed in these studies.
Zoeken en selecteren
A systematic review of the literature was performed to answer the following question(s):
What is the effect of subtotal colectomy with ileorectal or ileosigmoidal anastomosis compared with segmental colectomy on the incidence of metachronous colorectal tumors, disease specific mortality, quality of life and complications in patients with Lynch syndrome and primary resectable CRC? Recent observational studies on the comparison between subtotal and segmented colectomy on any of these outcomes that were known to the guideline panel were added to answer the specified (sub-) questions.
Table 1. PICO
|
Patients |
Patients with Lynch syndrome and primary colorectal cancer |
|
Intervention |
Subtotal colectomy with ileorectal/ ileosigmoidal anastomosis |
|
Control |
Segmental colectomy |
|
Outcomes |
Incidence of metachronous colorectal cancer, disease-specific mortality, quality of life and complications |
|
Other selection criteria |
Study design: systematic reviews, randomized controlled trials and observational studies |
Relevant outcome measures
The guideline panel considered incidences of metachronous colorectal cancer as a critical outcome measure for decision making; and (disease-specific) mortality, quality of life and complications as important outcome measures for decision making.
A priori, the guideline panel did not define the outcome measures listed above but used the definitions used in the studies.
The guideline panel defined 10% difference for dichotomous outcome measures informing on relative risk or odds ratio (0.91 ≤ OR ≥ 1.10), as minimal clinically (patient) important differences.
Search and select (Methods)
A systematic literature search was performed by a medical information specialist using the following bibliographic databases: Embase.com and Ovid/Medline. Both databases were searched to March 12th, 2024, for systematic reviews, RCTs and observational studies. Systematic searches were completed using a combination of controlled vocabulary/subject headings (e.g., Emtree-terms, MeSH) wherever they were available and natural language keywords.
The overall search strategy was derived from the primary search concepts described in the PICO: 1) patients with Lynch syndrome and CRC and (2) colectomy. Duplicates were removed using EndNote software.
After deduplication a total of 243 records were imported for title/abstract screening. Initially, 17 studies were selected based on title and abstract screening. After reading the full text, 14 studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), one observational study was added and thus 4 studies were included.
Referenties
- Anele CC, Adegbola SO, Askari A, Rajendran A, Clark SK, Latchford A, Faiz OD. Risk of metachronous colorectal cancer following colectomy in Lynch syndrome: a systematic review and meta-analysis. Colorectal Dis. 2017 Jun;19(6):528-536. doi: 10.1111/codi.13679. PMID: 28407411.
- Aronson M, Holter S, Semotiuk K, Winter L, Pollett A, Gallinger S, Cohen Z, Gryfe R. DNA Mismatch Repair Status Predicts Need for Future Colorectal Surgery for Metachronous Neoplasms in Young Individuals Undergoing Colorectal Cancer Resection. Dis Colon Rectum. 2015 Jul;58(7):645-52. doi: 10.1097/DCR.0000000000000391. PMID: 26200678.
- Baglietto L, Lindor NM, Dowty JG, White DM, Wagner A, Gomez Garcia EB, Vriends AH; Dutch Lynch Syndrome Study Group; Cartwright NR, Barnetson RA, Farrington SM, Tenesa A, Hampel H, Buchanan D, Arnold S, Young J, Walsh MD, Jass J, Macrae F, Antill Y, Winship IM, Giles GG, Goldblatt J, Parry S, Suthers G, Leggett B, Butz M, Aronson M, Poynter JN, Baron JA, Le Marchand L, Haile R, Gallinger S, Hopper JL, Potter J, de la Chapelle A, Vasen HF, Dunlop MG, Thibodeau SN, Jenkins MA. Risks of Lynch syndrome cancers for MSH6 mutation carriers. J Natl Cancer Inst. 2010 Feb 3;102(3):193-201. doi: 10.1093/jnci/djp473. Epub 2009 Dec 22. PMID: 20028993; PMCID: PMC2815724.
- Bijen CB, de Bock GH, Vermeulen KM, Arts HJ, ter Brugge HG, van der Sijde R, Kraayenbrink AA, Bongers MY, van der Zee AG, Mourits MJ. Laparoscopic hysterectomy is preferred over laparotomy in early endometrial cancer patients, however not cost effective in the very obese. Eur J Cancer. 2011 Sep;47(14):2158-65. doi: 10.1016/j.ejca.2011.04.035. Epub 2011 Jun 1. PMID: 21636268.
- Bonadona V, Bonaïti B, Olschwang S, Grandjouan S, Huiart L, Longy M, Guimbaud R, Buecher B, Bignon YJ, Caron O, Colas C, Noguès C, Lejeune-Dumoulin S, Olivier-Faivre L, Polycarpe-Osaer F, Nguyen TD, Desseigne F, Saurin JC, Berthet P, Leroux D, Duffour J, Manouvrier S, Frébourg T, Sobol H, Lasset C, Bonaïti-Pellié C; French Cancer Genetics Network. Cancer risks associated with germline mutations in MLH1, MSH2, and MSH6 genes in Lynch syndrome. JAMA. 2011 Jun 8;305(22):2304-10. doi: 10.1001/jama.2011.743. PMID: 21642682.
- Chalabi M, Fanchi LF, Dijkstra KK, Van den Berg JG, Aalbers AG, Sikorska K, Lopez-Yurda M, Grootscholten C, Beets GL, Snaebjornsson P, Maas M, Mertz M, Veninga V, Bounova G, Broeks A, Beets-Tan RG, de Wijkerslooth TR, van Lent AU, Marsman HA, Nuijten E, Kok NF, Kuiper M, Verbeek WH, Kok M, Van Leerdam ME, Schumacher TN, Voest EE, Haanen JB. Neoadjuvant immunotherapy leads to pathological responses in MMR-proficient and MMR-deficient early-stage colon cancers. Nat Med. 2020 Apr;26(4):566-576. doi: 10.1038/s41591-020-0805-8. Epub 2020 Apr 6. PMID: 32251400.
- Chalabi M, Verschoor YL, Tan PB, Balduzzi S, Van Lent AU, Grootscholten C, Dokter S, Büller NV, Grotenhuis BA, Kuhlmann K, Burger JW, Huibregtse IL, Aukema TS, Hendriks ER, Oosterling SJ, Snaebjornsson P, Voest EE, Wessels LF, Beets-Tan RG, Van Leerdam ME, Schumacher TN, van den Berg JG, Beets GL, Haanen JB. Neoadjuvant Immunotherapy in Locally Advanced Mismatch Repair-Deficient Colon Cancer. N Engl J Med. 2024 Jun 6;390(21):1949-1958. doi: 10.1056/NEJMoa2400634. PMID: 38838311.
- Cercek A, Dos Santos Fernandes G, Roxburgh CS, Ganesh K, Ng S, Sanchez-Vega F, Yaeger R, Segal NH, Reidy-Lagunes DL, Varghese AM, Markowitz A, Wu C, Szeglin B, Sauvé CG, Salo-Mullen E, Tran C, Patel Z, Krishnan A, Tkachuk K, Nash GM, Guillem J, Paty PB, Shia J, Schultz N, Garcia-Aguilar J, Diaz LA, Goodman K, Saltz LB, Weiser MR, Smith JJ, Stadler ZK. Mismatch Repair-Deficient Rectal Cancer and Resistance to Neoadjuvant Chemotherapy. Clin Cancer Res. 2020 Jul 1;26(13):3271-3279. doi: 10.1158/1078-0432.CCR-19-3728. Epub 2020 Mar 6. PMID: 32144135; PMCID: PMC7348681.
- Chen LM, Yang KY, Little SE, Cheung MK, Caughey AB. Gynecologic cancer prevention in Lynch syndrome/hereditaire nonpolyposis colorectal cancer families. Obstet Gynecol. 2007 Jul;110(1):18-25. doi: 10.1097/01.AOG.0000267500.27329.85. PMID: 17601891.
- Chikatani K, Ishida H, Mori Y, Nakajima T, Ueki A, Akagi K, Takao A, Yamada M, Taniguchi F, Komori K, Sasaki K, Sudo T, Miyakura Y, Chino A, Yamaguchi T, Tanakaya K, Tomita N, Ajioka Y. Risk of metachronous colorectal cancer after colectomy for first colon cancer in Lynch syndrome: multicenter retrospective study in Japan. Int J Clin Oncol. 2023 Dec;28(12):1633-1640. doi: 10.1007/s10147-023-02412-z. Epub 2023 Sep 26. PMID: 37752370.
- De Vos tot Nederveen Cappel WH, Nagengast FM, Griffioen G, Menko FH, Taal BG, Kleibeuker JH, Vasen HF. Surveillance for hereditary nonpolyposis colorectal cancer: a long-term study on 114 families. Dis Colon Rectum. 2002 Dec;45(12):1588-94. doi: 10.1007/s10350-004-7244-3. PMID: 12473880.
- de Vos tot Nederveen Cappel WH, Buskens E, van Duijvendijk P, Cats A, Menko FH, Griffioen G, Slors JF, Nagengast FM, Kleibeuker JH, Vasen HF. Decision analysis in the surgical treatment of colorectal cancer due to a mismatch repair gene defect. Gut. 2003 Dec;52(12):1752-5. doi: 10.1136/gut.52.12.1752. PMID: 14633956; PMCID: PMC1773904.
- Demisse R, Damle N, Kim E, Gong J, Fakih M, Eng C, Oesterich L, McKenny M, Ji J, Liu J, Louie R, Tam K, Gholami S, Halabi W, Monjazeb A, Dayyani F, Cho M. Neoadjuvant Immunotherapy-Based Systemic Treatment in MMR-Deficient or MSI-High Rectal Cancer: Case Series. J Natl Compr Canc Netw. 2020 Jul;18(7):798-804. doi: 10.6004/jnccn.2020.7558. PMID: 32634770.
- Dominguez-Valentin M, Sampson JR, Seppälä TT, Ten Broeke SW, Plazzer JP, Nakken S, Engel C, Aretz S, Jenkins MA, Sunde L, Bernstein I, Capella G, Balaguer F, Thomas H, Evans DG, Burn J, Greenblatt M, Hovig E, de Vos Tot Nederveen Cappel WH, Sijmons RH, Bertario L, Tibiletti MG, Cavestro GM, Lindblom A, Della Valle A, Lopez-Köstner F, Gluck N, Katz LH, Heinimann K, Vaccaro CA, Büttner R, Görgens H, Holinski-Feder E, Morak M, Holzapfel S, Hüneburg R, Knebel Doeberitz MV, Loeffler M, Rahner N, Schackert HK, Steinke-Lange V, Schmiegel W, Vangala D, Pylvänäinen K, Renkonen-Sinisalo L, Hopper JL, Win AK, Haile RW, Lindor NM, Gallinger S, Le Marchand L, Newcomb PA, Figueiredo JC, Thibodeau SN, Wadt K, Therkildsen C, Okkels H, Ketabi Z, Moreira L, Sánchez A, Serra-Burriel M, Pineda M, Navarro M, Blanco I, Green K, Lalloo F, Crosbie EJ, Hill J, Denton OG, Frayling IM, Rødland EA, Vasen H, Mints M, Neffa F, Esperon P, Alvarez K, Kariv R, Rosner G, Pinero TA, Gonzalez ML, Kalfayan P, Tjandra D, Winship IM, Macrae F, Möslein G, Mecklin JP, Nielsen M, Møller P. Cancer risks by gene, age, and gender in 6350 carriers of pathogenic mismatch repair variants: findings from the Prospective Lynch Syndrome Database. Genet Med. 2020 Jan;22(1):15-25. doi: 10.1038/s41436-019-0596-9. Epub 2019 Jul 24. Erratum in: Genet Med. 2020 Sep;22(9):1569. doi: 10.1038/s41436-020-0892-4. PMID: 31337882; PMCID: PMC7371626.
- Dominguez-Valentin M, Crosbie EJ, Engel C, Aretz S, Macrae F, Winship I, Capella G, Thomas H, Nakken S, Hovig E, Nielsen M, Sijmons RH, Bertario L, Bonanni B, Tibiletti MG, Cavestro GM, Mints M, Gluck N, Katz L, Heinimann K, Vaccaro CA, Green K, Lalloo F, Hill J, Schmiegel W, Vangala D, Perne C, Strauß HG, Tecklenburg J, Holinski-Feder E, Steinke-Lange V, Mecklin JP, Plazzer JP, Pineda M, Navarro M, Vidal JB, Kariv R, Rosner G, Piñero TA, Gonzalez ML, Kalfayan P, Ryan N, Ten Broeke SW, Jenkins MA, Sunde L, Bernstein I, Burn J, Greenblatt M, de Vos Tot Nederveen Cappel WH, Della Valle A, Lopez-Koestner F, Alvarez K, Büttner R, Görgens H, Morak M, Holzapfel S, Hüneburg R, von Knebel Doeberitz M, Loeffler M, Rahner N, Weitz J, Pylvänäinen K, Renkonen-Sinisalo L, Lepistö A, Auranen A, Hopper JL, Win AK, Haile RW, Lindor NM, Gallinger S, Le Marchand L, Newcomb PA, Figueiredo JC, Thibodeau SN, Therkildsen C, Okkels H, Ketabi Z, Denton OG, Rødland EA, Vasen H, Neffa F, Esperon P, Tjandra D, Möslein G, Sampson JR, Evans DG, Seppälä TT, Møller P. Risk-reducing hysterectomy and bilateral salpingo-oophorectomy in female heterozygotes of pathogenic mismatch repair variants: a Prospective Lynch Syndrome Database report. Genet Med. 2021 Apr;23(4):705-712. doi: 10.1038/s41436-020-01029-1. Epub 2020 Dec 1. PMID: 33257847; PMCID: PMC8026395.
- Eikenboom EL, Moen S, van Leerdam ME, Papageorgiou G, Doukas M, Tanis PJ, Dekker E, Wagner A, Spaander MCW; collaborative investigators from the Dutch Foundation for Detection of Hereditary Tumors. Metachronous colorectal cancer risk according to Lynch syndrome pathogenic variant after extensive versus partial colectomy in the Netherlands: a retrospective cohort study. Lancet Gastroenterol Hepatol. 2023 Dec;8(12):1106-1117. doi: 10.1016/S2468-1253(23)00228-5. Epub 2023 Oct 18. PMID: 37865103.
- Etchegary H, Dicks E, Tamutis L, Dawson L. Quality of life following prophylactic gynecological surgery: experiences of female Lynch mutation carriers. Fam Cancer. 2018 Jan;17(1):53-61. doi: 10.1007/s10689-017-9997-6. PMID: 28551770.
- Farchoukh LF, Celebrezze J, Medich D, Cunningham K, Holder-Murray J, Holtzman M, Lee K, Choudry H, Pai RK. DNA Mismatch Repair-deficient Rectal Cancer Is Frequently Associated With Lynch Syndrome and With Poor Response to Neoadjuvant Therapy. Am J Surg Pathol. 2022 Sep 1;46(9):1260-1268. doi: 10.1097/PAS.0000000000001918. Epub 2022 May 13. PMID: 35551135.
- Foxtrot Collaborative Group. Feasibility of preoperative chemotherapy for locally advanced, operable colon cancer: the pilot phase of a randomised controlled trial. Lancet Oncol. 2012 Nov;13(11):1152-60. doi: 10.1016/S1470-2045(12)70348-0. Epub 2012 Sep 25. PMID: 23017669; PMCID: PMC3488188.
- Gaba F, Manchanda R. Systematic review of acceptability, cardiovascular, neurological, bone health and HRT outcomes following risk reducing surgery in BRCA carriers. Best Pract Res Clin Obstet Gynaecol. 2020 May;65:46-65. doi: 10.1016/j.bpobgyn.2020.01.006. Epub 2020 Feb 4. PMID: 32192936.
- Gerritzen LH, Hoogerbrugge N, Oei AL, Nagengast FM, van Ham MA, Massuger LF, de Hullu JA. Improvement of endometrial biopsy over transvaginal ultrasound alone for endometrial surveillance in women with Lynch syndrome. Fam Cancer. 2009;8(4):391-7. doi: 10.1007/s10689-009-9252-x. Epub 2009 Jun 6. PMID: 19504173; PMCID: PMC2771130
- Haanstra JF, de Vos Tot Nederveen Cappel WH, Gopie JP, Vecht J, Vanhoutvin SA, Cats A, van der Zaag-Loonen HJ, Langers AM, Bergmann JH, van de Meeberg PC, Dekker E, Kleibeuker JH, Vasen HF, Nagengast FM, van Duijvendijk P. Quality of life after surgery for colon cancer in patients with Lynch syndrome: partial versus subtotal colectomy. Dis Colon Rectum. 2012 Jun;55(6):653-9. doi: 10.1097/DCR.0b013e31824f5392. PMID: 22595844.
- Helder-Woolderink JM, Blok EA, Vasen HF, Hollema H, Mourits MJ, De Bock GH. Ovarian cancer in Lynch syndrome; a systematic review. Eur J Cancer. 2016 Mar;55:65-73. doi: 10.1016/j.ejca.2015.12.005. Epub 2016 Jan 13. PMID: 26773421.
- Heneghan HM, Martin ST, Winter DC. Segmental vs extended colectomy in the management of hereditary nonpolyposis colorectal cancer: a systematic review and meta-analysis. Colorectal Dis. 2015 May;17(5):382-9. doi: 10.1111/codi.12868. PMID: 25510173.
- Jiang B, Ofshteyn A, Idrees JJ, Giglia M, Gallego C, Stein SL, Steinhagen E; University Hospitals Research in Surgical Outcome & Effectiveness (UH-RISES). Total abdominal colectomy is cost-effective in treating colorectal cancer in patients with genetically diagnosed Lynch Syndrome. Am J Surg. 2019 Nov;218(5):928-933. doi: 10.1016/j.amjsurg.2019.03.011. Epub 2019 Mar 16. PMID: 30904142.
- Kalady MF, Lipman J, McGannon E, Church JM. Risk of colonic neoplasia after proctectomy for rectal cancer in hereditary nonpolyposis colorectal cancer. Ann Surg. 2012 Jun;255(6):1121-5. doi: 10.1097/SLA.0b013e3182565c0b. PMID: 22549751.
- Keurentjes JHM, Briët JM, de Bock GH, Mourits MJE. Surgical volume and conversion rate in laparoscopic hysterectomy: does volume matter? A multicenter retrospective cohort study. Surg Endosc. 2018 Feb;32(2):1021-1026. doi: 10.1007/s00464-017-5780-x. Epub 2017 Aug 25. PMID: 28842767; PMCID: PMC5772131.
- Kim TJ, Kim ER, Hong SN, Kim YH, Huh JW, Park YA, Cho YB, Yun SH, Kim HC, Lee WY, Kim K, Kim K, Chang DK. Survival Outcome and Risk of Metachronous Colorectal Cancer After Surgery in Lynch Syndrome. Ann Surg Oncol. 2017 Apr;24(4):1085-1092. doi: 10.1245/s10434-016-5633-1. Epub 2016 Oct 20. PMID: 27766559.
- Lu KH. Hereditary gynecologic cancers: differential diagnosis, surveillance, management and surgical prophylaxis. Fam Cancer. 2008;7(1):53-8. doi: 10.1007/s10689-007-9144-x. Epub 2007 Jul 17. PMID: 17636427.
- Lykke R, Blaakær J, Ottesen B, Gimbel H. Incidence of pelvic organ prolapse repair subsequent to hysterectomy: a comparison between radical hysterectomy and total abdominal hysterectomy. Int Urogynecol J. 2017 May;28(5):745-749. doi: 10.1007/s00192-016-3173-7. Epub 2016 Oct 17. PMID: 27752747.
- Malik SS, Lythgoe MP, McPhail M, Monahan KJ. Metachronous colorectal cancer following segmental or extended colectomy in Lynch syndrome: a systematic review and meta-analysis. Fam Cancer. 2018 Oct;17(4):557-564. doi: 10.1007/s10689-017-0062-2. PMID: 29189962; PMCID: PMC6182577.
- Møller P, Seppälä T, Bernstein I, Holinski-Feder E, Sala P, Evans DG, Lindblom A, Macrae F, Blanco I, Sijmons R, Jeffries J, Vasen H, Burn J, Nakken S, Hovig E, Rødland EA, Tharmaratnam K, de Vos Tot Nederveen Cappel WH, Hill J, Wijnen J, Green K, Lalloo F, Sunde L, Mints M, Bertario L, Pineda M, Navarro M, Morak M, Renkonen-Sinisalo L, Frayling IM, Plazzer JP, Pylvanainen K, Sampson JR, Capella G, Mecklin JP, Möslein G; Mallorca Group (http://mallorca-group.eu). Cancer incidence and survival in Lynch syndrome patients receiving coloscopic and gynaecological surveillance: first report from the prospective Lynch syndrome database. Gut. 2017 Mar;66(3):464-472. doi: 10.1136/gutjnl-2015-309675. Epub 2015 Dec 9. PMID: 26657901; PMCID: PMC5534760.
- Monahan KJ, Bradshaw N, Dolwani S, Desouza B, Dunlop MG, East JE, Ilyas M, Kaur A, Lalloo F, Latchford A, Rutter MD, Tomlinson I, Thomas HJW, Hill J; Hereditary CRC guidelines eDelphi consensus group. Guidelines for the management of hereditary colorectal cancer from the British Society of Gastroenterology (BSG)/Association of Coloproctology of Great Britain and Ireland (ACPGBI)/United Kingdom Cancer Genetics Group (UKCGG). Gut. 2020 Mar;69(3):411-444. doi: 10.1136/gutjnl-2019-319915. Epub 2019 Nov 28. PMID: 31780574; PMCID: PMC7034349.
- Morton D, Seymour M, Magill L, Handley K, Glasbey J, Glimelius B, Palmer A, Seligmann J, Laurberg S, Murakami K, West N, Quirke P, Gray R; FOxTROT Collaborative Group. Preoperative Chemotherapy for Operable Colon Cancer: Mature Results of an International Randomized Controlled Trial. J Clin Oncol. 2023 Mar 10;41(8):1541-1552. doi: 10.1200/JCO.22.00046. Epub 2023 Jan 19. PMID: 36657089; PMCID: PMC10022855.
- Mourits MJ, Bijen CB, Arts HJ, ter Brugge HG, van der Sijde R, Paulsen L, Wijma J, Bongers MY, Post WJ, van der Zee AG, de Bock GH. Safety of laparoscopy versus laparotomy in early-stage endometrial cancer: a randomised trial. Lancet Oncol. 2010 Aug;11(8):763-71. doi: 10.1016/S1470-2045(10)70143-1. Epub 2010 Jul 16. PMID: 20638901.
- Natarajan N, Watson P, Silva-Lopez E, Lynch HT. Comparison of extended colectomy and limited resection in patients with Lynch syndrome. Dis Colon Rectum. 2010 Jan;53(1):77-82. doi: 10.1007/DCR.0b013e3181c702de. PMID: 20010355.
- Obermair A, Manolitsas TP, Leung Y, Hammond IG, McCartney AJ. Total laparoscopic hysterectomy versus total abdominal hysterectomy for obese women with endometrial cancer. Int J Gynecol Cancer. 2005 Mar-Apr;15(2):319-24. doi: 10.1111/j.1525-1438.2005.15223.x. PMID: 15823119.
- Parry S, Win AK, Parry B, Macrae FA, Gurrin LC, Church JM, Baron JA, Giles GG, Leggett BA, Winship I, Lipton L, Young GP, Young JP, Lodge CJ, Southey MC, Newcomb PA, Le Marchand L, Haile RW, Lindor NM, Gallinger S, Hopper JL, Jenkins MA. Metachronous colorectal cancer risk for mismatch repair gene mutation carriers: the advantage of more extensive colon surgery. Gut. 2011 Jul;60(7):950-7. doi: 10.1136/gut.2010.228056. Epub 2010 Dec 30. PMID: 21193451; PMCID: PMC3848416.
- Quezada-Diaz FF, Hameed I, von Mueffling A, Salo-Mullen EE, Catalano A, Smith JJ, Weiser MR, Garcia-Aguilar J, Stadler ZK, Guillem JG. Risk of Metachronous Colorectal Neoplasm after a Segmental Colectomy in Lynch Syndrome Patients According to Mismatch Repair Gene Status. J Am Coll Surg. 2020 Apr;230(4):669-675. doi: 10.1016/j.jamcollsurg.2020.01.005. Epub 2020 Jan 30. PMID: 32007537; PMCID: PMC7104918.
- Ran X, Jing H, Li Z. The clinical features and management of Lynch syndrome-associated ovarian cancer. J Obstet Gynaecol Res. 2022 Jul;48(7):1538-1545. doi: 10.1111/jog.15273. Epub 2022 Apr 27. PMID: 35478369.
- Ryan NAJ, Evans DG, Green K, Crosbie EJ. Pathological features and clinical behavior of Lynch syndrome-associated ovarian cancer. Gynecol Oncol. 2017 Mar;144(3):491-495. doi: 10.1016/j.ygyno.2017.01.005. Epub 2017 Jan 6. PMID: 28065618; PMCID: PMC5345899.
- Renkonen-Sinisalo L, Bützow R, Leminen A, Lehtovirta P, Mecklin JP, Järvinen HJ. Surveillance for endometrial cancer in hereditary nonpolyposis colorectal cancer syndrome. Int J Cancer. 2007 Feb 15;120(4):821-4. doi: 10.1002/ijc.22446. PMID: 17096354.
- Schmeler KM, Lynch HT, Chen LM, Munsell MF, Soliman PT, Clark MB, Daniels MS, White KG, Boyd-Rogers SG, Conrad PG, Yang KY, Rubin MM, Sun CC, Slomovitz BM, Gershenson DM, Lu KH. Prophylactic surgery to reduce the risk of gynecologic cancers in the Lynch syndrome. N Engl J Med. 2006 Jan 19;354(3):261-9. doi: 10.1056/NEJMoa052627. PMID: 16421367.
- Sheyn D, Bretschneider CE, Mahajan ST, Ridgeway B, Davenport A, Pollard R. Incidence and risk factors of early postoperative small bowel obstruction in patients undergoing hysterectomy for benign indications. Am J Obstet Gynecol. 2019 Mar;220(3):251.e1-251.e9. doi: 10.1016/j.ajog.2018.11.1095. Epub 2018 Nov 22. PMID: 30471258.
- Sideris M, Menon U, Manchanda R. Screening and prevention of ovarian cancer. Med J Aust. 2024 Mar 18;220(5):264-274. doi: 10.5694/mja2.52227. Epub 2024 Feb 14. PMID: 38353066.
- Stupart DA, Goldberg PA, Baigrie RJ, Algar U, Ramesar R. Surgery for colonic cancer in HNPCC: total vs segmental colectomy. Colorectal Dis. 2011 Dec;13(12):1395-9. doi: 10.1111/j.1463-1318.2010.02467.x. PMID: 20969713.
- Ten Broeke SW, van der Klift HM, Tops CMJ, Aretz S, Bernstein I, Buchanan DD, de la Chapelle A, Capella G, Clendenning M, Engel C, Gallinger S, Gomez Garcia E, Figueiredo JC, Haile R, Hampel HL, Hopper JL, Hoogerbrugge N, von Knebel Doeberitz M, Le Marchand L, Letteboer TGW, Jenkins MA, Lindblom A, Lindor NM, Mensenkamp AR, Møller P, Newcomb PA, van Os TAM, Pearlman R, Pineda M, Rahner N, Redeker EJW, Olderode-Berends MJW, Rosty C, Schackert HK, Scott R, Senter L, Spruijt L, Steinke-Lange V, Suerink M, Thibodeau S, Vos YJ, Wagner A, Winship I, Hes FJ, Vasen HFA, Wijnen JT, Nielsen M, Win AK. Cancer Risks for PMS2-Associated Lynch Syndrome. J Clin Oncol. 2018 Oct 10;36(29):2961-2968. doi: 10.1200/JCO.2018.78.4777. Epub 2018 Aug 30. Erratum in: J Clin Oncol. 2019 Mar 20;37(9):761. doi: 10.1200/JCO.19.00316. PMID: 30161022; PMCID: PMC6349460.
- Tozzi R, Malur S, Koehler C, Schneider A. Analysis of morbidity in patients with endometrial cancer: is there a commitment to offer laparoscopy? Gynecol Oncol. 2005 Apr;97(1):4-9. doi: 10.1016/j.ygyno.2004.12.048. PMID: 15790430.
- Tucker PE, Cohen PA. Review Article: Sexuality and Risk-Reducing Salpingo-oophorectomy. Int J Gynecol Cancer. 2017 May;27(4):847-852. doi: 10.1097/IGC.0000000000000943. PMID: 28333842.
- You YN, Chua HK, Nelson H, Hassan I, Barnes SA, Harrington J. Segmental vs. extended colectomy: measurable differences in morbidity, function, and quality of life. Dis Colon Rectum. 2008 Jul;51(7):1036-43. doi: 10.1007/s10350-008-9325-1. Epub 2008 May 10. PMID: 18470560.
- Win AK, Parry S, Parry B, Kalady MF, Macrae FA, Ahnen DJ, Young GP, Lipton L, Winship I, Boussioutas A, Young JP, Buchanan DD, Arnold J, Le Marchand L, Newcomb PA, Haile RW, Lindor NM, Gallinger S, Hopper JL, Jenkins MA. Risk of metachronous colon cancer following surgery for rectal cancer in mismatch repair gene mutation carriers. Ann Surg Oncol. 2013 Jun;20(6):1829-36. doi: 10.1245/s10434-012-2858-5. Epub 2013 Jan 29. PMID: 23358792; PMCID: PMC4041733.
- Woolderink JM, De Bock GH, de Hullu JA, Hollema H, Zweemer RP, Slangen BFM, Gaarenstroom KN, van Beurden M, van Doorn HC, Sijmons RH, Vasen HFA, Mourits MJE. Characteristics of Lynch syndrome associated ovarian cancer. Gynecol Oncol. 2018 Aug;150(2):324-330. doi: 10.1016/j.ygyno.2018.03.060. Epub 2018 Jun 5. PMID: 29880284.
Evidence tabellen
Risk of Bias tables
Assessment of study quality was performed using the Newcastle Ottawa Scale (conform the systematic Review of Anele, 2017)
|
Study |
Selection |
Comparability |
Outcome |
Total Score |
|||||
|
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
De Vos tot Nederveen, 2002* |
* |
* |
* |
* |
* |
* |
|
* |
7 |
|
Natarajan, 2010* |
* |
* |
* |
* |
* |
* |
* |
* |
8 |
|
Parry, 2011* |
* |
* |
* |
* |
** |
* |
* |
* |
9 |
|
Stupart, 2011* |
* |
* |
|
* |
** |
* |
* |
* |
8 |
|
Aronson, 2015 * |
|
* |
* |
* |
* |
* |
* |
* |
7 |
|
|
|
|
|
|
|
|
|
|
|
|
Kim, 2017 |
* |
* |
* |
* |
* |
* |
* |
* |
8 |
|
Eikenboom, 2023 |
* |
* |
* |
* |
** |
* |
* |
* |
9 |
*Results extracted from the Systematic Review from Anele, 2017
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Chikatani K, Ishida H, Mori Y, Nakajima T, Ueki A, Akagi K, Takao A, Yamada M, Taniguchi F, Komori K, Sasaki K, Sudo T, Miyakura Y, Chino A, Yamaguchi T, Tanakaya K, Tomita N, Ajioka Y. Risk of metachronous colorectal cancer after colectomy for first colon cancer in Lynch syndrome: multicenter retrospective study in Japan. Int J Clin Oncol. 2023 Dec;28(12):1633-1640. doi: 10.1007/s10147-023-02412-z. Epub 2023 Sep 26. PMID: 37752370. |
No comparison of I and C |
|
Demisse R, Damle N, Kim E, Gong J, Fakih M, Eng C, Oesterich L, McKenny M, Ji J, Liu J, Louie R, Tam K, Gholami S, Halabi W, Monjazeb A, Dayyani F, Cho M. Neoadjuvant Immunotherapy-Based Systemic Treatment in MMR-Deficient or MSI-High Rectal Cancer: Case Series. J Natl Compr Canc Netw. 2020 Jul;18(7):798-804. doi: 10.6004/jnccn.2020.7558. PMID: 32634770. |
Wrong study design (case reports) |
|
Half EE, Bresalier RS. Treatment of Hereditary Colorectal Cancer Syndromes. Curr Treat Options Gastroenterol. 2004 Jun;7(3):213-224. doi: 10.1007/s11938-004-0042-0. PMID: 15149583 |
Wrong study design, no comparison |
|
Heneghan HM, Martin ST, Winter DC. Segmental vs extended colectomy in the management of hereditary nonpolyposis colorectal cancer: a systematic review and meta-analysis. Colorectal Dis. 2015 May;17(5):382-9. doi: 10.1111/codi.12868. PMID: 25510173. |
Wrong population: no distinction between Lynch or HNPCC; relevant studies already included in SR of Anele (2017) |
|
Heijink DM, de Vries EG, Koornstra JJ, Hospers GA, Hofstra RM, van Vugt MA, de Jong S, Kleibeuker JH. Perspectives for tailored chemoprevention and treatment of colorectal cancer in Lynch syndrome. Crit Rev Oncol Hematol. 2011 Nov;80(2):264-77. doi: 10.1016/j.critrevonc.2010.11.009. Epub 2010 Dec 14. PMID: 21159521. |
No comparative study |
|
Hewish M, Lord CJ, Martin SA, Cunningham D, Ashworth A. Mismatch repair deficient colorectal cancer in the era of personalized treatment. Nat Rev Clin Oncol. 2010 Apr;7(4):197-208. doi: 10.1038/nrclinonc.2010.18. Epub 2010 Feb 23. PMID: 20177404. |
Wrong study design |
|
Jiang B, Ofshteyn A, Idrees JJ, Giglia M, Gallego C, Stein SL, Steinhagen E; University Hospitals Research in Surgical Outcome & Effectiveness (UH-RISES). Total abdominal colectomy is cost-effective in treating colorectal cancer in patients with genetically diagnosed Lynch Syndrome. Am J Surg. 2019 Nov;218(5):928-933. doi: 10.1016/j.amjsurg.2019.03.011. Epub 2019 Mar 16. PMID: 30904142. |
Wrong outcome |
|
McNamara KL, Aronson MD, Cohen Z. Is there a role for prophylactic colectomy in Lynch syndrome patients with inflammatory bowel disease? Int J Colorectal Dis. 2016 Jan;31(1):9-13. doi: 10.1007/s00384-015-2398-0. Epub 2015 Sep 28. PMID: 26412249. |
No comparative study |
|
Monahan KJ, Bradshaw N, Dolwani S, Desouza B, Dunlop MG, East JE, Ilyas M, Kaur A, Lalloo F, Latchford A, Rutter MD, Tomlinson I, Thomas HJW, Hill J; Hereditary CRC guidelines eDelphi consensus group. Guidelines for the management of hereditary colorectal cancer from the British Society of Gastroenterology (BSG)/Association of Coloproctology of Great Britain and Ireland (ACPGBI)/United Kingdom Cancer Genetics Group (UKCGG). Gut. 2020 Mar;69(3):411-444. doi: 10.1136/gutjnl-2019-319915. Epub 2019 Nov 28. PMID: 31780574; PMCID: PMC7034349. |
Wrong study design |
|
Rodriguez-Bigas MA, Möeslein G. Surgical treatment of hereditary nonpolyposis colorectal cancer (HNPCC, Lynch syndrome). Fam Cancer. 2013 Jun;12(2):295-300. doi: 10.1007/s10689-013-9626-y. PMID: 23508345. |
No comparative study |
|
Seppälä TT, Latchford A, Negoi I, Sampaio Soares A, Jimenez-Rodriguez R, Sánchez-Guillén L, Evans DG, Ryan N, Crosbie EJ, Dominguez-Valentin M, Burn J, Kloor M, Knebel Doeberitz MV, Duijnhoven FJBV, Quirke P, Sampson JR, Møller P, Möslein G; European Hereditary Tumour Group (EHTG) and European Society of Coloproctology (ESCP). European guidelines from the EHTG and ESCP for Lynch syndrome: an updated third edition of the Mallorca guidelines based on gene and gender. Br J Surg. 2021 May 27;108(5):484-498. doi: 10.1002/bjs.11902. PMID: 34043773; PMCID: PMC10364896. |
Wrong study design |
|
Smith KD, Rodriguez-Bigas MA. Role of surgery in familial adenomatous polyposis and hereditary nonpolyposis colorectal cancer (Lynch syndrome). Surg Oncol Clin N Am. 2009 Oct;18(4):705-15. doi: 10.1016/j.soc.2009.07.006. PMID: 19793576. |
Wrong study design: Case report |
|
Stupart DA, Goldberg PA, Baigrie RJ, Algar U, Ramesar R. Surgery for colonic cancer in HNPCC: total vs segmental colectomy. Colorectal Dis. 2011 Dec;13(12):1395-9. doi: 10.1111/j.1463-1318.2010.02467.x. PMID: 20969713. |
Already included in SR of Anele (2017) |
|
Tomita N, Ishida H, Tanakaya K, Yamaguchi T, Kumamoto K, Tanaka T, Hinoi T, Miyakura Y, Hasegawa H, Takayama T, Ishikawa H, Nakajima T, Chino A, Shimodaira H, Hirasawa A, Nakayama Y, Sekine S, Tamura K, Akagi K, Kawasaki Y, Kobayashi H, Arai M, Itabashi M, Hashiguchi Y, Sugihara K; Japanese Society for Cancer of the Colon, Rectum. Japanese Society for Cancer of the Colon and Rectum (JSCCR) guidelines 2020 for the Clinical Practice of Hereditary Colorectal Cancer. Int J Clin Oncol. 2021 Aug;26(8):1353-1419. doi: 10.1007/s10147-021-01881-4. Epub 2021 Jun 29. PMID: 34185173; PMCID: PMC8286959. |
Wrong study design |
Verantwoording
Beoordelingsdatum en geldigheid
Publicatiedatum : 29-09-2025
Beoordeeld op geldigheid : 15-09-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Belangrijkste wijzigingen t.o.v. vorige versie:
|
Onderwerp |
Wijzigingen meest recente versie |
|
Module 1: Diagnostiek en verwijzing |
|
|
Module 2: Familiair colorectaal carcinoom |
|
|
Module 3: Lynch syndroom |
|
|
Module 4: Adenomateuze polyposis |
|
|
Module 5: Serrated polyposis en overige vormen van polyposis |
|
|
Andere aanpassingen |
|
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2022 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met Erfelijke darmkanker.
Werkgroep
- dr. M. (Maartje) Nielsen (voorzitter), Klinisch geneticus, Leids Universitair Medisch Centrum, Leiden, VKGN
- prof. dr. N. (Nicoline) Hoogerbrugge, internist, Radboud UMC, Nijmegen, VKGN
- dr. A. (Anja) Wagner, Klinisch geneticus, Erasmus MC Kanker Instituut, Universitair Medisch Centrum Rotterdam, Rotterdam, VKGN
- dr. S.W. (Sanne) Bajwa – ten Broeke, Klinisch geneticus, Universitair Medisch Centrum Groningen, Groningen, VKGN
- prof. Dr. M.E. (Monique) van Leerdam, MDL-arts, Nederlands Kanker Instituut, Amsterdam, Leiden University Medical Center, NVMDL
- dr. T.M. (Tanya) Bisseling, MDL-arts, Radboud UMC, Nijmegen, NVMDL
- dr. M.C.A. (Mariëtte) van Kouwen, MDL-arts, Radboud UMC, Nijmegen, NVMDL
- prof. Dr. E. (Evelien) Dekker, MDL-arts, Amsterdam UMC, Amsterdam, NVMDL
- drs. H. (Hicham) Bouchiba, Arts-onderzoeker MDL, Amsterdam UMC, Amsterdam, persoonlijke titel
- dr. C.J. (Charlotte) Verberne, Chirurg, Ziekenhuis Amstelland, Amstelveen
- dr. J.M. (Jorien) Woolderink, Gynaecoloog, Martini Ziekenhuis, Groningen, NVOG
- dr. R.S. (Chella) van der Post, Patholoog, Radboud UMC, Nijmegen, NVVP
- dr. J.E. (Jurgen) Seppen, Patiëntvertegenwoordiger, Stichting Lynch Polyposis
- dr. A.R. (Arjen) Mensenkamp, laboratoriumspecialist Klinische genetica, Radboud UMC, Nijmegen, VKGL
- dr. C.M.J. (Carli) Tops, laboratoriumspecialist Klinische genetica, Leids Universitair Medisch Centrum, Leiden, VKGL
- I.J.H. (Ivonne) Schoenaker, Verpleegkundig specialist MDL, Isala Ziekenhuis, Zwolle, V&VN oncologie
- L.J.(Lisette) Saveur, Verpleegkundig specialist MDL, Nederlands Kanker Instituut, Amsterdam, V&VN oncologie
Klankbordgroep:
- Dr. F.J.B. (Fränzel) van Duijnhoven, Universitair hoofddocent voeding, genen en kanker WUR, Wageningen, persoonlijke titel
- Dr. J.A.J. (Job) Verdonschot, AIOS klinische Genetica, Maastricht Universitair Medisch Centrum, Maastricht, persoonlijke titel
- Dr. A.G. (Toine) van der Heijden, Oncologisch uroloog, Radboud UMC, Nijmegen, persoonlijke titel
Met ondersteuning van
- dr. J. (Joppe) Tra, Senior-Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. D. (Dagmar) Nieboer, Senior-Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. J. (Josefien) Buddeke, Senior-Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. M. (Mirre) den Ouden-Vierwind, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. M. (Merel) Wassenaar, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. A.C. (Anniek) van Westing, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. L. (Leanne) Küpers, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. J. (Jing) de Haan- Du, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. S.N. (Sarah) van Duijn, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- dr. M. (Majke) van Bommel, Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- drs. E. (Evie) Verweg, Junior Adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- D.P. (Diana) Gutierrez, projectsecretaresse, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een (sub-) module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Werkgroepleden |
||||
|
Nielsen |
Klinisch geneticus, volledig betaald door de afdeling. |
2012 - present: the International Society for Gastrointestinal Hereditary Tumors (InSiGHT)
Betaling per bijeenkomst (vacation money for expenses made)
Lid adviesraad Stichting Lynch- Polyposis (onbetaald) |
Lopende subsidiegelden – waar ik bij betrokken bij ben:
|
Geen |
|
Hoogerbrugge – van der Linden |
Medisch specialist en hoogleraar erfelijke kanker
|
Geen |
Geen extern gefinancierd onderzoek in relatie tot deze functie |
Geen |
|
Wagner |
Klinisch geneticus |
Bestuurslid Stichting Opsporing Erfelijke tumoren (onbetaald); |
Extern gefinancierd onderzoek. WP3 leider KWF-project nr: 14976 (Smart measurement of circulating tumour DNA: a tumour-agnostic computational tool to improve CRC-care) |
Geen |
|
Bajwa – ten Broeke |
Klinische geneticus UMCG PI, betaald (vanuit KWF-subsidie) |
Lid European Hereditary Tumor Group (onbetaald), Bestuurslid DCCG |
Ja, subsidie voor onderzoek door KWF (young investigator grant), 2021-2025 |
Geen |
|
Van Leerdam |
MDL-arts Antoni van Leeuwenhoek, Amsterdam (0,6 FTE) betaald
|
Medisch directeur stichting opsporing erfelijke tumoren, Leiden, onbetaald |
Extern gefinancierd onderzoek |
Geen |
|
Bisseling |
MDL-arts Radboud UMC 0.9 fte |
Geen |
Geen |
Geen |
|
Van Kouwen |
Maag-Darm-Leverarts Radboud UMC Nijmegen |
Geen |
Geen |
Geen |
|
Dekker |
Maag-Darm-Leverarts, FT, Amsterdam UMC (betaald)
|
Lid raad van Commissarissen The eNose Company (betaald)
|
I have received honorarium for consultancy* from FujiFilm, Olympus, GI Supply, PAION and Ambu, and speakers' fees from Olympus, GI Supply, Norgine, IPSEN, PAION and FujiFilm. -Studies gefinancierd door KWF, MLDS, TKI, ZonMW, Celtic, FujiFilm. * Single meeting about development, innovation and research |
Geen
Geen deelname aan adviesraden gedurende de richtlijnontwikkeling |
|
Bouchiba |
PhD kandidaat/Arts-onderzoeker maag-darm-leverziekten Amsterdam UMC. |
Geen |
Geen |
Geen |
|
Verberne |
Chirurg in het ziekenhuis Amstelland, Amstelveen |
Geen |
Geen |
Geen |
|
Woolderink |
Gynaecoloog, Martini Ziekenhuis Groningen |
Lid adviesraad Stichting Lynch- Polyposis (onbetaald) |
Geen |
Geen |
|
Van der Post |
Patholoog, Radboud UMC
|
Bestuurslid Stichting Opsporing Erfelijke tumoren (onbetaald) |
Geen extern gefinancierd onderzoek in relatie tot deze functie |
Geen |
|
Seppen |
Universitair hoofddocent, Amsterdam UMC |
Bestuurslid Stichting Lynch Polyposis |
Geen |
Geen |
|
Mensenkamp |
Laboratoriumspecialist klinische genetica, Radboud UMC Nijmegen |
Voorzitter landelijk overleg erfelijke borstkankerdiagnostiek (LOB)
|
-Medewerking verleend aan workshops variantclassificatie en betrokken als assessor bij kwaliteitsrondzendingen BRCA-diagnostiek op tumorweefsel (EMQN/GenQA, gesponsord door AstraZeneca, betaald aan de afdeling Genetica) -VCo-applicant CRAFT project bij KWF. |
Geen |
|
Tops |
Laboratorium specialist klinische genetica, KG, LUMC
|
Geen |
KWF 14469 - Functionele test Lynch genen - Geen projectleider |
Geen |
|
Schoenaker |
Verpleegkundige specialist AGZ (MDL Oncologie) Isala, betaald
|
Geen |
EASIER study; Electronic nose for breath Analysis after curative Surgery to detect dIstant mEtastases or locoregional Recurrence of colon cancer |
Geen |
|
Saveur |
Verpleegkundig specialist Antoni van Leeuwenhoek |
Geen |
Geen |
Geen |
|
|
||||
|
Klankbordgroepleden |
||||
|
Van Duijnhoven |
Associate Professor
|
Geen |
Onderzoeksproject gefinancierd door World Cancer Research Fund/ Wereld Kanker Onderzoek Fonds |
Geen |
|
Verdonschot |
AIOS Klinische Genetica, MUMC+ |
Geen |
Geen |
Geen |
|
Van der Heijden |
Oncologisch uroloog
|
Geen |
ZonMW; BladParadigm; RCT mpMRI versus TURT.Projectleider ja |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door afvaardiging vanuit de patiëntenvereniging Stichting Lynch Polyposis in de werkgroep. De afgevaardigde heeft meebeslist bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen.
De conceptrichtlijn is tevens voor commentaar voorgelegd aan Stichting Lynch Polyposis de Nederlandse Federatie van Kankerpatiëntenorganisaties (NFK). De eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
|
Module |
Uitkomst raming |
Toelichting |
|
Submodule Chirurgische behandeling van Lynch syndroom |
Geen mogelijk financiële gevolgen |
Uit de toetsing volgt dat de aanbevelingen niet breed toepasbaar zijn (<5.000 patiënten) en daarom naar verwachting geen substantiële financiële gevolgen zullen hebben voor de collectieve uitgaven. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep schriftelijk de knelpunten in de zorg voor patiënten met Erfelijke darmkanker. Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
er is hoge zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; het is zeer onwaarschijnlijk dat de literatuurconclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Redelijk |
er is redelijke zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; het is mogelijk dat de conclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Laag |
er is lage zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; er is een reële kans dat de conclusie klinisch relevant verandert wanneer er resultaten van nieuw grootschalig onderzoek aan de literatuuranalyse worden toegevoegd. |
|
Zeer laag |
er is zeer lage zekerheid dat het ware effect van behandeling dichtbij het geschatte effect van behandeling ligt; de literatuurconclusie is zeer onzeker. |
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello, 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Voor- en nadelen van interventies dienen goed met de patiënt te worden doorgenomen.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Literature search strategy
|
Cluster/richtlijn: VKGN Erfelijke darmkanker |
|
|
Uitgangsvraag/submodules: UV3 Wat is de optimale chirurgische behandeling bij Lynch en primair resectabel colorectaal carcinoom? |
|
|
Database(s): Embase.com, Ovid/Medline |
Datum: 12 maart 2024 |
|
Periode: geen restrictie |
Talen: geen restrictie |
|
Literatuurspecialist: Alies Oost |
Rayyan review: https://rayyan.ai/reviews/961540 |
|
BMI-zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Deduplication: voor het ontdubbelen is gebruik gemaakt van http://dedupendnote.nl/ |
|
|
Toelichting: Voor deze vraag is gezocht op de elementen:
De sleutelartikelen worden gevonden met deze search |
|
|
Te gebruiken voor richtlijntekst: In de databases Embase.com en Ovid/Medline is op 12 maart 2024 systematisch gezocht naar systematische reviews en RCTs over chirurgische behandeling bij Lynch. De literatuurzoekactie leverde 243 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SR |
76 |
20 |
76 |
|
RCT |
153 |
37 |
167 |
|
Totaal |
229 |
57 |
243* |
*in Rayyan
Zoekstrategie
Embase.com
|
No. |
Query |
Results |
|
#1 |
'Lynch syndrome'/exp OR 'Lynch syndrome ii'/exp OR 'Lynch like syndrome'/exp OR ((Lynch NEAR/3 (syndrome* OR like)):ti,ab,kw) OR 'ls related':ti,ab,kw OR lls:ti,ab,kw OR 'muir torre syndrome*':ti,ab,kw OR 'hereditary colorectal cancer'/exp OR (((hereditary OR inherited OR familial OR 'type x') NEAR/3 ('colorectal cancer*' OR 'colorectal neoplasm*' OR 'colorectal carcinoma*' OR 'colon cancer*' OR 'colon neoplasm*' OR 'colon carcinoma*' OR crc* OR nonpolyposis OR 'non polyposis')):ti,ab,kw) OR hnpcc:ti,ab,kw OR fcctx:ti,ab,kw |
18869 |
|
#2 |
'colectomy'/exp OR 'ileorectal anastomosis'/exp OR 'proctocolectomy'/exp OR 'segmental colectomy'/exp OR 'colorectal surgery'/de OR 'cancer surgery'/de OR colectom*:ti,ab,kw OR hemicolectom*:ti,ab,kw OR proctocolectom*:ti,ab,kw OR coloproctectom*:ti,ab,kw OR rectocolectom*:ti,ab,kw OR coloproctotom*:ti,ab,kw OR (((ileorect* OR 'ileo rect*' OR rectoileal OR 'recto ileal' OR 'ileal pouch' OR 'ileo anal') NEAR/3 (anastomos* OR excis*)):ti,ab,kw) OR ipaa:ti,ab,kw OR ira:ti,ab,kw OR (((colon* OR proctocolon* OR rect* OR colorect* OR segment*) NEAR/3 (surg* OR resect* OR excis* OR extirpat*)):ti,ab,kw) |
543478 |
|
#3 |
#1 AND #2 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
1498 |
|
#4 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
1008862 |
|
#5 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
3988229 |
|
#6 |
#3 AND #4 - SR |
76 |
|
#7 |
#3 AND #5 NOT #6 - RCT |
153 |
|
#8 |
#6 OR #7 |
229 |
Ovid/Medline
|
# |
Searches |
Results |
|
1 |
exp Lynch Syndrome II/ or (Lynch adj2 (syndrome* or like)).ti,ab,kf. or 'ls related'.ti,ab,kf. or lls.ti,ab,kf. or 'Muir Torre syndrome*'.ti,ab,kf. or exp Colorectal Neoplasms, Hereditary Nonpolyposis/ or ((hereditary or inherited or familial or 'type x') adj3 ('colorectal cancer*' or 'colorectal neoplasm*' or 'colorectal carcinoma*' or 'colon cancer*' or 'colon neoplasm*' or 'colon carcinoma*' or crc* or nonpolyposis or 'non polyposis')).ti,ab,kf. or hnpcc.ti,ab,kf. or fcctx.ti,ab,kf. |
11131 |
|
2 |
exp Colectomy/ or Anastomosis, Surgical/ or exp Proctocolectomy, Restorative/ or exp Colorectal Surgery/ or exp Surgical Oncology/ or colectom*.ti,ab,kf. or hemicolectom*.ti,ab,kf. or proctocolectom*.ti,ab,kf. or coloproctectom*.ti,ab,kf. or rectocolectom*.ti,ab,kf. or coloproctotom*.ti,ab,kf. or ((ileorect* or 'ileo rect*' or rectoileal or 'recto ileal' or 'ileal pouch' or 'ileo anal') adj3 (anastomos* or excis*)).ti,ab,kf. or ipaa.ti,ab,kf. or ira.ti,ab,kf. or ((colon* or proctocolon* or rect* or colorect* or segment*) adj3 (surger* or resect* or excis* or extirpat*)).ti,ab,kf. |
119317 |
|
3 |
(1 and 2) not (comment/ or editorial/ or letter/) not ((exp animals/ or exp models, animal/) not humans/) |
543 |
|
4 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
731800 |
|
5 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2700517 |
|
6 |
3 and 4 - SR |
20 |
|
7 |
(3 and 5) not 6 - RCT |
37 |
|
8 |
6 or 7 |
57 |