Classificatie
Uitgangsvraag
Welke indeling wordt gebruikt voor epileptische aanvallen en epilepsie?
Aanbeveling
Gebruik de classificatie van aanvallen en epilepsiesyndromen uit 2017 en 2022 (zie Bijlages). Stel zodoende aanvalstype, epilepsieclassificatie, indien mogelijk epilepsiesyndroom, etiologie en comorbiditeit vast
Overwegingen
De classificatie van epilepsie en epileptische aanvallen wordt vastgesteld door de classificatiecommissie van de International League Against Epilepsy (ILAE). De ILAE heeft in 2017 twee classificaties gepubliceerd; een classificatie van epileptische aanvallen (Fisher, 2017) en een classificatie van epilepsieën en epilepsiesyndromen (Scheffer, 2017). De classificatie van epilepsiesyndromen is in 2022 verder uitgewerkt in een serie van publicaties (zie referentielijst). Het landelijk multidisciplinair cluster ‘Epilepsie’ heeft besloten deze classificaties voor Nederland over te nemen. Met deze update komen bepaalde termen uit de voorgaande classificaties te vervallen. Het doel van de geüpdatete classificaties is om een meer uniforme en transparante terminologie te presenteren voor klinische toepassing. Hiermee vervallen de (ILAE) aanvalsclassificaties (met hun modificaties) uit 1981 en de epilepsie classificatie van 1989.
Voor definities wordt verwezen naar ‘Definities en epidemiologie bij epilepsie’.
Classificatie van epileptische aanvallen
De vorige classificatie uit 1981 (met enkele modificaties) had een aantal tekortkomingen: verschillende termen om aanvallen te classificeren zijn nooit goed ingeburgerd geraakt en een aantal aanvalstypes ontbreken. In de meest recente classificatie zijn termen zoals, 'partieel’, 'simpel (eenvoudig) partieel’, 'complex partieel’ en 'dyscognitief’ komen te vervallen. De update van de classificatie heeft tot doel beter aan te sluiten bij de huidige inzichten in epilepsie.
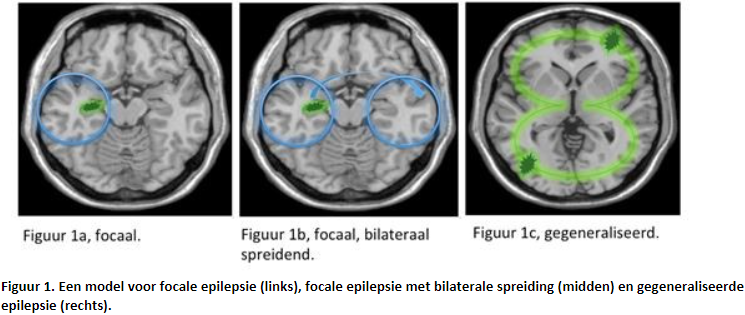
In de meest recente classificatie worden epileptische aanvallen eerst ingedeeld op basis van kenmerken bij de aanvang van de aanval. Er wordt nog steeds onderscheid gemaakt tussen focale en gegeneraliseerde aanvallen. Een focale aanval ontstaat binnen een netwerk van één hemisfeer (zie figuur 1a). Dit kan in een klein gebied gelokaliseerd zijn of meer verspreid in één hemisfeer voorkomen. Focale aanvallen kunnen ontstaan in subcorticale structuren. Focale aanvallen kunnen ook naar beide hersenhelften spreiden (zie figuur 1b). Bij gegeneraliseerde aanvallen zijn vanaf het begin bilateraal verdeelde netwerken actief (zie figuur 1c). Sommige aanvalstypes, bijvoorbeeld tonische aanvallen of epileptische spasmen, kunnen een focaal of generaliseerd begin hebben.
Systematiek van aanvalsclassificatie
Een schematische weergave van de basisclassificatie van epileptische aanvallen (vertaald van Fischer 2017) wordt weergegeven in Figuur 2. De uitgebreide ILAE 2017 operationele classificaties van aanvalstypes is te zien in Bijlage 1. De aangepaste terminologie die gebruikt dient te worden om aanvallen te classificeren is te zien in Bijlage 2. In deze tabel staan de ouderwetse en meest recente terminologie voor het classificeren van epileptische aanvallen (zowel Engelse als Nederlandse terminologie) naast elkaar.
Hieronder volgt een korte toelichting en beschrijving.
De classificatie van een epileptische aanval begint met het afnemen van een gedetailleerde anamnese en/of het observeren van de uitingsvorm van de aanval, de zogenaamde semiologie. Na het beschrijven van de semiologie is het van belang om de aanval te classificeren. Bij aanvalsclassificatie is de eerste stap het vaststellen of de epileptische aanval focaal of gegeneraliseerd begint. Dit wordt gedaan aan de hand van de eerste verschijnselen van de aanval. Naast klinische informatie kan ook aanvullende informatie van elektro-encefalografie (EEG), beeldvorming of laboratoriumonderzoek gebruikt worden om een aanval te classificeren. Indien het begin van de aanval gemist of onduidelijk is, kan aangegeven worden dat het begin onbekend is. De basisclassificatie van epileptische aanvallen is schematisch weergegeven in Figuur 2. Het is bovendien waardevol om beschrijvingen toe te voegen na het classificeren van de initiële verschijnselen. Maak hierbij gebruik van de schematische weergave van de aanvalsclassificatie (Bijlage 1) en de terminologie die in de tabel ‘Oude en meest recente terminologie voor het classificeren van epileptische aanvallen’ (Bijlage 2).
Focale aanvallen worden onderverdeeld in focale aanvallen met intacte of verminderde gewaarwording. Hiermee wordt het waarnemen en het besef hebben van de omgeving bedoeld. Een intacte gewaarwording betreft de perceptie of kennis van gebeurtenissen die zich voordoen tijdens een aanval, ook indien er geen motorische activiteit of reactie op de omgeving is. Er hoeft achteraf geen kennis te zijn van het feit dat een aanval plaatsvond. De werkgroep heeft bewust gekozen voor de term ‘gewaarwording’ en niet voor de term ‘bewustzijn’ als vertaling van de Engelse term 'awareness'. Deze keuze is in lijn met het besluit van de ILAE Task Force om 'awareness' te gebruiken als een relatief simpele surrogaatmarker voor bewustzijn. Voor focale aanvallen is de specificatie van het niveau van gewaarwording optioneel.
Een focale aanval met intacte gewaarwording komt overeen met de oude classificatie van een eenvoudige partiële aanval. Een focale aanval met verminderde gewaarwording komt overeen met de oude classificatie van een complex partiële aanval. Verminderde gewaarwording tijdens een deel van de aanval maakt het een focale aanval met verminderde gewaarwording. De term ‘focaal naar bilateraal tonisch-clonisch’ is de nieuwe term voor ‘secundair gegeneraliseerd tonisch-clonisch’.
Indeling van focale epilepsie op basis van anatomische lokalisatie kan nog steeds nuttig zijn, bijvoorbeeld bij de evaluatie voor epilepsiechirurgie. Zie ‘Oude en meest recente terminologie voor het classificeren van epileptische aanvallen’ (Bijlage 2); bijvoorbeeld focale aanval met intacte gewaarwording vanuit de temporaalkwab. Hiervoor is aanvullende informatie van elektro-encefalografie (EEG) ook erg belangrijk. Daarnaast kunnen nog andere motorische of niet-motorische kenmerken beschreven worden. Zie schematische weergave van de aanvalsclassificatie (Bijlage 1). Bijvoorbeeld: Cognitieve aanvallen impliceren problemen in taalfunctie of andere cognitieve domeinen of positieve kenmerken zoals ‘déja vu’, hallucinaties, illusies of perceptuele vervormingen. Emotionele aanvallen omvatten epileptische uitingen van angst, vreugde, agitatie of andere emoties zonder bijpassende beleving, zoals bij een gelastische aanval. Bij een ‘focale gedragsonderbreking’ is het stoppen van de activiteit het dominante kenmerk tijdens de hele aanval.
Gegeneraliseerde aanvallen kunnen ook onderverdeeld worden in motorisch (bijvoorbeeld tonisch-clonisch of myoclonisch) of niet-motorisch (absence). Absences kunnen weer onderverdeeld worden in bijvoorbeeld typisch of atypisch. Een absence is atypisch bij een langzame start of einde van de aanval, of bij significante veranderingen in de tonus. Dit wordt vaak ondersteund door atypische, langzame, gegeneraliseerde piekgolfcomplexen op het EEG. Een aanval is niet te classificeren als er onvoldoende informatie is of als het niet mogelijk is om het type aanval in andere categorieën te plaatsen.
Samenvatting van regels om epileptische aanvallen te classificeren:
-
Begin van de aanval: besluit of de epileptische aanval focaal of gegeneraliseerd is. Indien er onvoldoende zekerheid is op basis van kliniek (in combinatie met eventueel aanvullend onderzoek) dan is het begin niet vast te stellen en de aanval niet te classificeren als focaal of gegeneraliseerd.
-
Classificeer aan de hand van de eerste verschijnselen of een aanval focaal of gegeneraliseerd is. Bevindingen van een EEG kunnen worden meegenomen in de classificatie.
-
Gewaarwording: Beslis voor focale epileptische aanvallen of geclassificeerd wordt aan de hand van het niveau van gewaarwording, of om geen uitspraak te doen over het wel of niet intact zijn van de gewaarwording. De oude term 'eenvoudige partiële aanval' is nu een 'focale aanval met intacte gewaarwording'. De oude term 'complex partiële aanval' is nu een 'focale aanval met verminderde gewaarwording'.
-
Als er bij een focale epileptische aanval op enig moment een verminderde gewaarwording is, wordt het geclassificeerd als een ‘focale aanval met verminderde gewaarwording ‘
-
Gedragsonderbreking (behavior arrest): bij deze aanvalsvorm is een onderbreking van gedragingen het voornaamste kenmerk van de gehele aanval.
-
Motorisch/niet-motorisch: een focale aanval met intacte of verminderde gewaarwording kan verder worden onderverdeeld door vast te stellen of er motorische verschijnselen zijn. Indien het niveau van gewaarwording niet bekend is, kan een focale aanval ook primair gekarakteriseerd worden door motorische of niet-motorische aspecten. Bijvoorbeeld: een focale tonische aanval.
-
Optionele termen: termen zoals motorisch of niet-motorisch kunnen worden weggelaten wanneer het aanvalstype zonder deze toevoeging al duidelijk is. Bijvoorbeeld een focale clonische aanval.
-
Aanvullende beschrijvingen: Na het classificeren van het aanvalstype op basis van initiële verschijnselen, wordt aanbevolen om beschrijvingen van andere tekenen en symptomen toe te voegen. Maak hierbij gebruik van de omschrijvingen die in de tabel ‘Algemene beschrijvingen van gedragsfenomenen tijdens en na een aanval’ (zie bijlage 4 tabel 2) zijn aangegeven. Dit verandert het aanvalstype niet. Bijvoorbeeld: (initieel) focale emotionele aanval (aanvullend) met tonische activiteit in de rechterarm en hyperventilatie.
-
Bilateraal versus gegeneraliseerd: gebruik de term 'bilateraal' voor tonisch-clonische aanvallen die zich uitbreiden naar beide hemisferen en 'generaliseerd' voor aanvallen die gelijktijdig in beide hemisferen ontstaan.
-
Atypische absence: een absence is atypisch als het een langzaam begin of einde heeft, er duidelijke verandering in de tonus te zien is, of in het EEG gepaard gaat met piekgolf- complexen van <3 per seconde.
-
Clonisch versus myoclonisch: clonisch verwijst naar aanhoudend ritmische trekkingen en myoclonisch naar korte schokken met onderbrekingen (vaak aritmisch).
-
Ooglidmyoclonieën: absence met ooglidmyoclonieën verwijst naar geforceerde opwaartse trekkingen van de oogleden tijdens een absence (aanval).
De ILAE-classificatiecommissie heeft de geüpdatete classificatie voor epilepsie gepubliceerd (Scheffer, 2017). Schematisch is dit weergegeven in het raamwerk voor de classificatie van de epilepsie (Bijlage 3). Na de classificatie van het aanvalstype is de volgende stap om (indien mogelijk) de epilepsie te classificeren. Er moet dan sprake zijn van één van de volgende voorwaarden (Fisher, 2014):
(1) Minstens twee ongeprovoceerde (of reflexmatige) aanvallen met een interval tussen de aanvallen van meer dan 24 uur.
(2) Eén ongeprovoceerde (of reflexmatige) aanval met een herhalingskans van minstens 60% in tien jaar (gelijk aan de herhalingskans bij twee ongeprovoceerde aanvallen).
(3) er is sprake van een epilepsiesyndroom.
Het is onvoldoende om te volstaan met de diagnose ‘epilepsie’. Epilepsie is een symptoom van een onderliggende neurologische aandoening of stoornis. Het is belangrijk dat artsen die mensen met epilepsie behandelen niet alleen het aanvalstype maar ook de epilepsie classificeren, en indien mogelijk, een epilepsiesyndroom en een etiologische diagnose stellen. Zie ook het raamwerk voor de classificatie van de epilepsie (Bijlage 3). Adequaat aanvullend onderzoek, keuze van behandeling en informatie over de prognose is gebaseerd op correcte classificatie van de aanvallen en het epilepsiesyndroom. Goede classificatie geeft ook zicht op het mortaliteitsrisico en mogelijke comorbiditeit. Foute classificatie kan leiden tot overbodige diagnostiek, onjuiste behandeling en onnodig persisteren van aanvallen. Betrek ook alle bekende comorbide aandoeningen bij het classificatieproces aangezien dit soms ook een aanwijzing kan geven voor de diagnose.
Het epilepsietype kan focaal of gegeneraliseerd, of gecombineerd focaal en gegeneraliseerd zijn. Het epilepsietype wordt vastgesteld op klinische gronden, zo mogelijk ondersteund door EEG-bevindingen en resultaten van beeldvormend onderzoek. Focale epilepsie kan het gevolg zijn van een uni- en multifocale aandoening, en bestaat uit aanvallen waarbij één hemisfeer betrokken is. Het interictale EEG (gemaakt tussen aanvallen door) kan typische focale epileptiforme activiteit tonen. De diagnose gegeneraliseerde epilepsie wordt meestal ondersteund door een EEG met gegeneraliseerde piek-golfactiviteit.
Een nieuw epilepsietype is de ‘gecombineerde gegeneraliseerde en focale epilepsie’, bestaande uit zowel focale als gegeneraliseerde aanvalstypen. De diagnose wordt op klinische gronden gemaakt, ondersteund door EEG-bevindingen en met de huidige kennis, ook vaak genetische veranderingen die verklarend zijn voor de epilepsie. Ictaal EEG (tijdens een aanval) kan nuttig zijn maar is niet essentieel. Het interictale EEG kan zowel gegeneraliseerde piek-golven als focale epileptiforme ontladingen laten zien, maar epileptische activiteit is niet nodig voor de diagnose. Een voorbeeld van dit epilepsietype waarbij zich beide soorten aanvallen voordoen is het Dravet-syndroom.
Men kan er (voorlopig) ook op uitkomen dat het onbekend is of het gaat om focale of gegeneraliseerde epilepsie. Een etiologische diagnose dient echter altijd overwogen te worden.
Epilepsiesyndroom
Het derde niveau van classificeren is die van een epilepsiesyndroom. Hierbij is weer belangrijk dat men de aanvallen goed geclassificeerd heeft. Een belangrijke factor bij het vaststellen van het epilepsiesyndroom is leeftijd van eerste aanvallen. Daarnaast geven EEG-patronen onmisbare informatie voor het vaststellen van het epilepsiesyndroom. Vaak wordt dit nog ondersteund door specifieke etiologische bevindingen (structureel, genetisch, metabolisch, immuun en infectieus). De diagnose van een syndroom bij een persoon met epilepsie heeft vaak prognostische en behandelingsimplicaties. Veel syndromen zijn sterk gecorreleerd met specifieke comorbiditeiten.
Bij de classificatie van het epilepsiesyndroom zijn enkele termen aangepast; zo is bijvoorbeeld de term ‘benigne’ vervangen door de term ‘vanzelf overgaand’ of de term ‘farmacoresponsief’ (afhankelijk van de situatie). De commissie adviseert verder om de term ‘genetische gegeneraliseerde epilepsie’ te gebruiken. De idiopathische gegeneraliseerde epilepsie zoals de absence epilepsie van de kinderleeftijd (childhood absence epilepsy) en de juveniele myoclonus epilepsie (JME) maken deel uit van de genetische gegeneraliseerde epilepsie. In de praktijk wordt doorgaans de term ‘gegeneraliseerde epilepsie’ gebruikt.
De term ‘epileptische encephalopathie’ (epileptic encephalopathy, EE) is gedefinieerd als een aandoening waar de epileptische activiteit zelf bijdraagt tot ernstige cognitieve en gedragsstoornissen boven van wat van de onderliggende pathologie alleen verwacht kan worden. Een voorbeeld hiervan is het Lennox Gastaut syndroom. Het concept van de epileptische encefalopathie kan van toepassing zijn op epilepsie van alle leeftijden en moet ruimer gebruikt worden dan alleen voor de ernstige epilepsie met aanvang in kinderjaren. Een belangrijk onderdeel van het concept is dat verminderen van de epileptische activiteit het potentieel heeft om consequenties op de ontwikkeling te verbeteren.
Bij de term ‘ontwikkelings- en epileptische encefalopathie (developmental and epileptic encephalopathy, DEE)’ gaat de encefalopathie en de ontwikkelingsstoornis door, ook bij vermindering van de epileptische activiteit. Een voorbeeld hiervan is het Angelman syndroom.
De termen 'maligne' en 'catastrofale' zullen niet langer gebruikt worden in het kader van epilepsie, wegens hun ernstige of desastreuze connotaties.
Een overzicht van leeftijdsgebonden syndromen is te zien in bijlage 5). De syndromen zijn hier onderverdeeld naar aanvallentype(n) (focaal, gegeneraliseerd), met een aparte categorie voor syndromen met ontwikkelings- en epileptische encefalopathie (DEE) of progressieve neurologische achteruitgang.
Daarnaast is er een categorie etiologie specifieke syndromen, om concreet gedefinieerde entiteiten aan te duiden met een duidelijk fenotype geassocieerd met een specifieke etiologie. Voorbeelden hiervan zijn bepaalde monogene epilepsiesyndromen, zoals CDKL5-DEE en PCDH19 en structurele etiologieën zoals mesiale temporaalkwabepilepsie met hippocampussclerose en gelastische aanvallen op basis van een hypothalamushamartoom.
Voor ondersteuning bij de classificatie van epilepsie kan ook gebruik worden gemaakt van de website www.epilepsydiagnosis.org
Etiologie
Een etiologische diagnose dient in elke stap van het proces overwogen te worden. De etiologie is verdeeld in zes subgroepen (structureel, genetisch, infectieus, metabool, immunologisch, onbekend). Het kan zijn dat een epilepsie zowel een genetische als een structurele oorzaak heeft. Een voorbeeld hiervan is tubereuze sclerose. Deze aandoening is het gevolg van een genetische verandering die leidt tot de tubers in de hersenen, de pathognomonische structurele afwijkingen. In dit soort gevallen sluit een genetische verklaring voor de epilepsie epilepsiechirurgie zeker niet uit, sterker, epilepsiechirurgie kan dan vaak een uitkomst bieden.
Comorbiditeit
De comorbiditeit en beperkingen die een patiënt vanwege de epilepsie ondervindt, kunnen naast de classificatie nog toegevoegd worden. Het is optioneel om de beperkingen te classificeren volgens de International Classification of Impairment, Disability and Handicap (ICIDH-2) van de WHO (Engel, 2001). De ICIDH-2 wordt nu ICF genoemd.
Onderbouwing
Het is onvoldoende om bij een patiënt te volstaan met de diagnose “epilepsie". Epilepsie is een symptoom van een onderliggende neurologische aandoening. Het is belangrijk dat artsen die patiënten met epilepsie behandelen, weten dat epilepsie moet worden geclassificeerd op basis van aanvalstype en (indien mogelijk) epilepsiesyndroom. Dit is met name van belang bij leeftijdsgebonden epilepsiesyndromen op de kinderleeftijd. Adequaat aanvullend onderzoek, de juiste behandeling en informatie over de prognose met betrekking tot de aanvallen en het syndroom is gebaseerd op de correcte classificatie van de aanvallen en het epilepsiesyndroom. Als aanvallen en of het syndroom niet correct worden geclassificeerd kan dit leiden tot onjuiste behandeling en persisteren van aanvallen.
No systematic literature review was conducted for this question. Known literature on the classification of epilepsy and epileptic seizures, including the literature from the Classification Commission of the International League Against Epilepsy (ILAE), was used by the working group.
- Engel J Jr; International League Against Epilepsy (ILAE). A proposed diagnostic scheme for people with epileptic seizures and with epilepsy: report of the ILAE Task Force on Classification and Terminology. Epilepsia. 2001 Jun;42(6):796-803. doi: 10.1046/j.1528-1157.2001.10401.x. PMID: 11422340.
- Fisher RS, Acevedo C, Arzimanoglou A, Bogacz A, Cross JH, Elger CE, Engel J Jr, Forsgren L, French JA, Glynn M, Hesdorffer DC, Lee BI, Mathern GW, Moshé SL, Perucca E, Scheffer IE, Tomson T, Watanabe M, Wiebe S. ILAE official report: a practical clinical definition of epilepsy. Epilepsia. 2014 Apr;55(4):475-82. doi: 10.1111/epi.12550. Epub 2014 Apr 14. PMID: 24730690.
- Fisher RS, Cross JH, D'Souza C, French JA, Haut SR, Higurashi N, Hirsch E, Jansen FE, Lagae L, Moshé SL, Peltola J, Roulet Perez E, Scheffer IE, Schulze-Bonhage A, Somerville E, Sperling M, Yacubian EM, Zuberi SM. Instruction manual for the ILAE 2017 operational classification of seizure types. Epilepsia. 2017 Apr;58(4):531-542. doi: 10.1111/epi.13671. Epub 2017 Mar 8. PMID: 28276064.
- Hirsch E, French J, Scheffer IE, Bogacz A, Alsaadi T, Sperling MR, Abdulla F, Zuberi SM, Trinka E, Specchio N, Somerville E, Samia P, Riney K, Nabbout R, Jain S, Wilmshurst JM, Auvin S, Wiebe S, Perucca E, Moshé SL, Tinuper P, Wirrell EC. ILAE definition of the Idiopathic Generalized Epilepsy Syndromes: Position statement by the ILAE Task Force on Nosology and Definitions. Epilepsia. 2022 Jun;63(6):1475-1499. doi: 10.1111/epi.17236. Epub 2022 May 3. PMID: 35503716.
- Riney K, Bogacz A, Somerville E, Hirsch E, Nabbout R, Scheffer IE, Zuberi SM, Alsaadi T, Jain S, French J, Specchio N, Trinka E, Wiebe S, Auvin S, Cabral-Lim L, Naidoo A, Perucca E, Moshé SL, Wirrell EC, Tinuper P. International League Against Epilepsy classification and definition of epilepsy syndromes with onset at a variable age: position statement by the ILAE Task Force on Nosology and Definitions. Epilepsia. 2022 Jun;63(6):1443-1474. doi: 10.1111/epi.17240. Epub 2022 May 3. PMID: 35503725.
- Scheffer IE, Berkovic S, Capovilla G, Connolly MB, French J, Guilhoto L, Hirsch E, Jain S, Mathern GW, Moshé SL, Nordli DR, Perucca E, Tomson T, Wiebe S, Zhang YH, Zuberi SM. ILAE classification of the epilepsies: Position paper of the ILAE Commission for Classification and Terminology. Epilepsia. 2017 Apr;58(4):512-521. doi: 10.1111/epi.13709. Epub 2017 Mar 8. PMID: 28276062; PMCID: PMC5386840.
- Specchio N, Wirrell EC, Scheffer IE, Nabbout R, Riney K, Samia P, Guerreiro M, Gwer S, Zuberi SM, Wilmshurst JM, Yozawitz E, Pressler R, Hirsch E, Wiebe S, Cross HJ, Perucca E, Moshé SL, Tinuper P, Auvin S. International League Against Epilepsy classification and definition of epilepsy syndromes with onset in childhood: Position paper by the ILAE Task Force on Nosology and Definitions. Epilepsia. 2022 Jun;63(6):1398-1442. doi: 10.1111/epi.17241. Epub 2022 May 3. PMID: 35503717.
- Wirrell EC, Nabbout R, Scheffer IE, Alsaadi T, Bogacz A, French JA, Hirsch E, Jain S, Kaneko S, Riney K, Samia P, Snead OC, Somerville E, Specchio N, Trinka E, Zuberi SM, Balestrini S, Wiebe S, Cross JH, Perucca E, Moshé SL, Tinuper P. Methodology for classification and definition of epilepsy syndromes with list of syndromes: Report of the ILAE Task Force on Nosology and Definitions. Epilepsia. 2022 Jun;63(6):1333-1348. doi: 10.1111/epi.17237. Epub 2022 May 3. PMID: 35503715.
- Wirrell E, Tinuper P, Perucca E, Moshé SL. Introduction to the epilepsy syndrome papers. Epilepsia. 2022 Jun;63(6):1330-1332. doi: 10.1111/epi.17262. Epub 2022 May 3. PMID: 35503711.
- Zuberi SM, Wirrell E, Yozawitz E, Wilmshurst JM, Specchio N, Riney K, Pressler R, Auvin S, Samia P, Hirsch E, Galicchio S, Triki C, Snead OC, Wiebe S, Cross JH, Tinuper P, Scheffer IE, Perucca E, Moshé SL, Nabbout R. ILAE classification and definition of epilepsy syndromes with onset in neonates and infants: Position statement by the ILAE Task Force on Nosology and Definitions. Epilepsia. 2022 Jun;63(6):1349-1397. doi: 10.1111/epi.17239. Epub 2022 May 3. PMID: 35503712.
Beoordelingsdatum en geldigheid
Publicatiedatum : 30-10-2024
Beoordeeld op geldigheid : 18-09-2024
Het cluster Epilepsie is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. Jaarlijks wordt de geldigheid van elke module herbeoordeeld.
De onderstaande modules zijn herzien in cyclus ’23-’24:
- Richtlijn Epilepsie: ‘Classificatie’
- Richtlijn Epilepsie: ‘Genetisch onderzoek’
- Richtlijn Epilepsie: ‘Welk anti-aanvalsmedicatie: Aanvallen met een focaal begin’
- Richtlijn Dravetsyndroom: ‘Anti-aanvalsmedicatie’
- Richtlijn Dravetsyndroom: ‘Klinische criteria’
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodules is in 2020 een multidisciplinair cluster ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met epilepsie.
Clusterstuurgroep
- Prof. dr. H.J.M. Majoie (voorzitter), neuroloog, Academisch Centrum voor Epileptologie Kempenhaeghe/ Maastricht UMC+, Heeze en Maastricht
- Dr. C.M. Delsman-van Gelder, kinderneuroloog, Maxima Medisch Centrum, Eindhoven
- Drs. M.H.G. Dremmen, radioloog, Erasmus MC Rotterdam
- Dr. P. Klarenbeek, neuroloog, Zuyderland Medisch Centrum, Heerlen
- Dr. L. M’Rabet, patiëntvertegenwoordiger, EpilepsieNL, Houten
- Dr. P. van Vliet, neuroloog/intensivist, Haaglanden Medisch Centrum, Den Haag
- Drs. R. van Vugt, anesthesioloog, Sint Maartens Kliniek, Nijmegen
Clusterleden betrokken bij module ‘Classificatie’
- Prof. dr. H.J.M. Majoie (voorzitter), neuroloog, Academisch Centrum voor Epileptologie Kempenhaeghe/ Maastricht UMC+, Heeze en Maastricht
- Met dank aan dr. F.E. Jansen, kinderneuroloog, UMC Utrecht
Met ondersteuning van
- Dr. M.M.J. van Rooijen, adviseur Kennisinstituut van de Federatie Medisch Specialisten Utrecht
- Dr. J. Buddeke, senior adviseur Kennisinstituut van de Federatie Medisch Specialisten Utrecht
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle clusterleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van de clusterleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
Stuurgroep
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Majoie* |
Functie: Neurologie Werkgever: Academisch Centrum voor Epileptologie Kempenhaeghe, Maastricht UMC+ |
Relevante commissies
NB geen betaalde functies |
Lopende onderzoek- en zorginnovatieprojecten (anders dan contract research) worden gefinancierd uit ZonMW, Nationaal epilepsiefonds, stichting vrienden van Kempenhaeghe, en SKMS.
Incidenteel financiële ondersteuning aan stichting Kempenhaeghe voor organisatie refereeravonden en workshops/symposia (telkens volgens geldende wet en regelgeving). |
Geen actie |
|
Delsman |
Kinderneuroloog/kinderarts Werkgever: Maxima Medisch Centrum Veldhoven |
Geen |
Geen |
Geen actie |
|
Dremmen |
Functie: Kinderradioloog met subspecialisatie kinderneuroradiologie Werkgever: ErasmusMC te Rotterdam |
Een van de voorzitters van de richtlijn Radiologische diagnostiek acute trauma-opvang bij kinderen Expertisegroep richtlijn Traumatologie Uitgenodigd spreker op meerdere nationale en internationale cursussen en congressen |
Geen |
Geen actie |
|
Klarenbeek |
Functie: Neuroloog Werkgever: Zuyderland te Heerlen/Sittard (vrijgevestigd) |
Geen |
Geen |
Geen actie |
|
Van Vliet |
Functie: Intensivist Werkgever: Haaglanden Medisch Centrum te Den Haag |
|
Geen |
Geen actie |
|
Van Vugt |
Functie: Anesthesioloog Werkgever: Sint Maartenskliniek te Nijmegen |
Lid commissie kwaliteitsdocumenten NVA (onbetaald) |
Geen |
Geen actie |
Expertisegroep
|
Clusterlid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Altinbas |
Functie: Neuroloog-kinderneuroloog Werkgever: SEIN locatie Meer en Bosch werkzaam op de polikliniek en kliniek |
|
Per 2023 zal het landelijk CBD consortium een onderzoek starten naar de behandeling van kinderen met therapieresistente epilepsie met CBD (gesubsidieerd door ZonMW). |
Geen actie |
|
Balvers |
Functie: Neuroloog (Behandeling van patiënten met epilepsie; klinisch, poliklinisch en in woonzorg) Werkgever: Stichting Epilepsie Instellingen Nederland (SEIN) (0.6fte)
Functie: Neuroloog (Behandeling van patiënten met hoofdpijn; poliklinisch) Werkgever: The Migraine Clinic, Amsterdam (0.2 fte) |
|
|
Geen restrictie voor Epilepsie. |
|
Comans |
Hoogleraar nucleaire geneeskunde Amsterdam UMC (0.4 FTE) en nuclair geneeskundige HMC Den Haag (0.6 FTE) |
Lid cluster Longoncologie (onbetaald) |
Geen |
Geen actie. |
|
De Bruijn |
Functie: neuroloog in opleiding Werkgever: ETZ Tilburg |
Geen |
Geen |
Geen actie |
|
Draak |
Functie: Kinderneuroloog, neuroloog. Werkgever: Zuyderland Medisch Centrum |
Geen |
Geen |
Geen actie |
|
Eshuis |
Functie: AIOS Spoedeisende geneeskunde Werkgever: Catharina Ziekenhuis te Eindhoven |
|
Geen |
Geen actie |
|
Hofman |
Functie: Radioloog Werkgever: Maastricht UMC+ (1.0fte) |
|
Geen |
Geen actie |
|
Koekkoek |
Functie: Neuroloog Werkgever: Leids Universitair Medisch Centrum (0.8fte), Haaglanden Medisch Centrum (0.2fte) |
|
Geen |
Geen actie |
|
Lazeron |
Functie: Neuroloog Werkgever: Academisch centrum Epileptologie Kempenhaeghe Maastricht UMC+ (voltijds).
Functie: Wetenschappelijk onderzoeker Werkgever: Technische universiteit te Eindhoven (nul uren aanstelling) |
|
Lid van het TeleEpilepsie consortium. Met dit consortium hebben een aanvalsdetector ontwikkeld, de Nightwatch(R) die door LivAssured geproduceerd wordt. Geen direct financieel belang in dit bedrijf, maar van eventuele toekomstige winsten van LivAssured vloeit een klein percentage terug naar het consortium voor epilepsie-onderzoek |
Restricties ten aanzien van besluitvorming met betrekking tot apparaten die aanvallen detecteren (e.g. Nightwatch) |
|
Mantione |
Klinisch neuropsycholoog UMC Utrecht |
|
Geen |
Geen actie |
|
Masselink |
Functie: Ziekenhuisapotheker Werkgever: Medisch Spectrum Twente |
|
Geen |
Geen actie |
|
M’Rabet |
Functie: MT-lid Kennis en Innovatie Werkgever: EpilepsieNL, Houten |
Geen |
|
Geen actie |
|
Reijneveld |
Functie: Neuroloog, Werkgever: Stichting Epilepsie Instellingen Nederland (SEIN) te Heemstede (0.8 fte)
Functie: Universitair Hoofddocent, afdeling Neurologie Werkgever: Amsterdam UMC (0.2 fte) |
|
Geen |
Geen actie |
|
Ronner |
Functie: Neuroloog Werkgever: Amsterdam UMC (0.8 fte) |
|
Geen |
Geen actie |
|
Schijns |
Functie: Neurochirurg met specialisatie Epilepsiechirurgie en Neuro-oncologische Chirurgie |
|
|
Geen actie |
|
Snoeijen-Schouwenaars |
Functie: Arts Verstandelijk Gehandicapten Werkgever: Kempenhaeghe, fulltime |
Geen |
Geen |
Geen actie |
|
Thijs |
Functie: neuroloog Werkgever: Stichting Epilepsie Instellingen Nederland (1.0 fte) Leids Universitair Medisch Centrum (detachering vanuit SEIN voor 0.2 fte) |
|
|
Restrictie ten aanzien van besluitvorming met betrekking tot apparaten die aanvallen detecteren (e.g. Nightwatch®). |
|
Tousseyn |
Functie: neuroloog Werkgever: Academisch Centrum voor Epileptologie (ACE) Kempenhaeghe/Maastricht UMC+, locatie Heeze |
|
|
Geen actie |
|
Uiterwijk |
Functie: Epileptoloog Werkgever: Academisch Centrum voor Epileptologie Kempenhaeghe |
Geen |
Geen |
Geen actie |
|
Van 't Hof |
Functie: neuroloog Werkgever: SEIN (Stichting Epilepsie Instellingen Nederland) |
|
Geen |
Geen actie |
|
Van Schie |
AIOS neurologie LUMC (tot 05-2023) |
Geen |
Geen |
Geen actie |
|
Van Tuijl |
Functie: Neuroloog Werkgever: ETZ Tilburg |
|
|
Geen actie |
|
Tolboom |
Functie: Nucleair geneeskundige Werkgever: UMC Utrecht |
Geen |
Geen |
Geen actie |
|
Verbeek |
Functie: Klinisch geneticus Werkgever: UMC Utrecht
|
Geen |
Geen |
Geen actie |
|
Verhoeven |
Functie: Kinderarts-kinderneuroloog |
Geen |
|
Geen actie |
|
Vlooswijk |
Functie: Neuroloog Werkgever: Maastricht UMC+ |
|
|
Geen actie |
|
Wegner |
Functie: Neuroloog Werkgever: Stichting Epilepsie instellingen Nederland (SEIN) |
|
Geen |
Geen actie |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door de afvaardiging van EpilepsieNL in het cluster. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptmodule is tevens voor commentaar voorgelegd aan Epilepsie NL en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming per module blijkt dat er geen substantiële financiële gevolgen zijn.
Module |
Uitkomst raming |
Toelichting |
|
Classificatie |
Geen financiële gevolgen |
|
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Cyclus werkwijze
Bij de start van de cyclus is de geldigheid van alle modules geïnventariseerd, waarna er een prioriteringsronde heeft plaatsgevonden. De geprioriteerde modules zijn herzien en geüpdatet door het cluster.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde het cluster welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. Het cluster waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde het cluster tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder ‘Onderbouwing’. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
Definitie |
|
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Netwerk meta-analyse
Voor de beoordeling van de bewijskracht uit een netwerk meta-analyse (NMA) wordt gebruik gemaakt van de CINeMA-tool (Nikolakopoulou, 2020; Papakonstantinou, 2020). Met deze tool wordt op basis van een analyse in R de effectschattingen berekend. Voor het beoordelen van de bewijskracht, op basis van de berekende effectschattingen, worden zes domeinen geëvalueerd, namelijk Risk-of-Bias, publicatiebias, indirectheid, imprecisie, heterogeniteit en incoherentie. Voor het opstellen van de conclusies zijn principes van de GRADE working group gebruikt op basis van grenzen van klinische besluitvorming (Brignardello-Petersen, 2020).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door het cluster wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. Het cluster heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
Bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module ‘Organisatie van zorg’.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met het cluster. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door het cluster. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt)organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brignardello-Petersen R, Florez ID, Izcovich A, Santesso N, Hazlewood G, Alhazanni W, Yepes-Nuñez JJ, Tomlinson G, Schünemann HJ, Guyatt GH; GRADE working group. GRADE approach to drawing conclusions from a network meta-analysis using a minimally contextualised framework. BMJ. 2020 Nov 11;371:m3900. doi: 10.1136/bmj.m3900. PMID: 33177059.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Nikolakopoulou A, Higgins JPT, Papakonstantinou T, Chaimani A, Del Giovane C, Egger M, Salanti G. CINeMA: An approach for assessing confidence in the results of a network meta-analysis. PLoS Med. 2020 Apr 3;17(4):e1003082. doi: 10.1371/journal.pmed.1003082. PMID: 32243458; PMCID: PMC7122720.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Papakonstantinou T, Nikolakopoulou A, Higgins JPT, Egger M & Salanti G. CINeMA: Software for semiautomated assessment of the confidence in the results of network meta-analysis. Campbell Systematic Reviews 2020;16:e1080.