Behandeling instabiele enkelfractuur
Uitgangsvraag
Is de beste behandeling voor volwassenen met een instabiele enkelfractuur operatief of conservatief?
Aanbeveling
Behandel een instabiele enkelfractuur bij voorkeur operatief.
Overwegingen
Het besluit tot operatieve of conservatieve behandeling is afhankelijk van de stabiliteit van de fractuur en patiëntspecifieke kenmerken. Ook uit de patiëntenvragenlijst behorende bij deze richtlijn is naar voren gekomen dat patiënten het belangrijk vinden dat er gekeken wordt naar de persoonlijke situatie van de patiënt en er aandacht is voor co-morbiditeit (zie ook de module ‘Enkelfracturen met ernstige comorbiditeit’) (Patiëntenfederatie Nederland, 2016). Stabiele fracturen kunnen conservatief worden behandeld, terwijl een operatieve behandeling bij instabiele fracturen beter lijkt. Voor de definitie van stabiele en instabiele fracturen wordt verwezen naar het stroomdiagram.
Bij conservatieve behandeling van instabiele enkelfracturen wordt middels immobilisatie fractuurgenezing nagestreefd. Langdurige immobilisatie kan leiden tot spieratrofie en een pijnlijk gezwollen gewricht. Ook kan secundaire dislocatie van de fractuur optreden waarvoor alsnog operatieve interventie nodig is. Daarnaast kan delayed of nonunion optreden. Bij operatieve behandeling van instabiele enkelfracturen worden fractuurfragmenten idealiter in anatomische positie gefixeerd met als doel voorkomen van complicaties op de lange termijn (artrose, pijn, verminderde functie). De oefenstabiele situatie die hiermee wordt nagestreefd kan in potentie leiden tot sneller herstel en daarmee kostenbesparing voor de samenleving. Dit potentiële voordeel moet worden opgewogen tegen de kans op het optreden van complicaties (infectie, trombose, longembolie, nonunion, falen van implantaat of fixatie, zenuwletsel, mortaliteit, amputatie en re-operatie). De kans hierop varieert tussen de 0,30 en 10,8% (SooHoo, 2009; Ovaska, 2015; Lindsjo, 1985; Peters, 2013; Pelet, 2012; Belmont, 2015, Zaghloul 2014). Uit de patiëntenvragenlijst bleek dat in de acute fase heeft een zo goed mogelijk herstel van de enkel prioriteit heeft. In een latere fase is het voor mensen ook belangrijk dat er voldoende aandacht is voor vermindering van pijn en volledige beweeglijkheid van de enkel (Patiëntenfederatie Nederland, 2016).
De definitie van ‘instabiele’ en ‘stabiele’ fracturen is in de geïncludeerde studies niet eenduidig. Dit en de grote variëteit aan verschillende uitkomstmaten bemoeilijkt meta-analyse. Daarnaast was in de geïncludeerde RCTs niet altijd sprake van intention-to-treat-analysis (Makwena 2001 en Rowley 1986). Sanders (2012) is de enige RCT waarin intention-to-treat-analysis goed werd gedocumenteerd. Daarnaast was in geïncludeerde studies soms sprake lost-to-follow-up van een substantieel deel van de geïncludeerde patiënten (bijvoorbeeld 49% in Phillips 1985). De duur van follow up om end-stage artrose te detecteren is 20 jaar (Horrisberger 2009). Geen van de geïncludeerde studies kwam tot deze duur van follow up. Vanwege methodologische tekortkomingen van de studies is bij alle uitkomstmaten de bewijslast met minimaal één (maar vaak ook twee of drie) niveau(`s) verlaagd. Tot slot is er een zeer grote studie gaande welke mogelijk in 2017 wordt gepubliceerd (Willett). Deze studie van Willett betreft een multicenter-trial met 620 geïncludeerde patiënten met een instabiele type B-fractuur die gerandomiseerd werden tussen close-contact-casting na onbloedige repositie versus operatieve behandeling. Het aantal geïncludeerde patiënten in de studies van Bauer, Phillips, Rowley, Makwena en Sanders bedraagt tezamen slechts 373 patiënten. De primaire uitkomstmaat van de studie van Willett is de Olerud score, welke in de toekomst eventueel zou kunnen worden gepooled met de studies van Sanders en Makwena.
De directe kosten van een operatie zijn hoger onder andere vanwege opnameduur, personele kosten en implantaten. Echter, op lange termijn kan een operatieve behandeling wel kosten besparend zijn, als hiermee posttraumatische artrose wordt voorkomen (Høiness, 2002; Bhandari, 2004; Slobogean, 2012).
De beschikbare literatuur levert bewijskracht op van lage of zeer lage kwaliteit. De combinatie van röntgenologische en andere patiënt specifieke factoren moet steeds individueel gewogen worden om tot een goed besluit te komen voor de operatieve dan wel conservatieve behandeling van instabiele enkelfracturen. De module ‘Enkelfracturen met ernstige comorbiditeit’ behandelt de rol van comorbiditeit. De werkgroep is van mening dat de nadelen van onderbehandeling van instabiele fracturen (conservatief) over het algemeen groter worden geacht dan de nadelen van overbehandeling (operatief). Belangrijk zijn hierbij het risico op secundaire dislocatie, posttraumatische arthrose, nonunion en delayed union. In meer algemene zin is de werkgroep tot onderstaande aanbeveling gekomen.
Onderbouwing
Voor de indeling van instabiele en stabiele enkelfracturen verwijzen we naar de flowchart. Een enkelfractuur heeft grote impact op het functioneren van de patiënt en zijn participatie in de maatschappij. Er bestaat controverse of enkelfracturen het beste operatief of niet-operatief geïmmobiliseerd dienen te worden (Donken, 2012; Strauss, 2007). Dit leidt tot ongewenste praktijkvariatie. In een Amerikaanse studie varieerde de operatieve behandeling van enkelfracturen bij oudere patiënten per plaats van 14 tot 72% (Koval, 2005).
Functioneren
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat operatie van instabiele fracturen mogelijk leidt tot beter functioneren van de enkel dan een conservatieve behandeling.
Bronnen (Sanders, 2012; Makwana, 2001; Phillips, 1985) |
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat de hersteltijd / tijd tot functioneren naar het niveau van voor het letsel, korter is na operatieve behandeling dan na conservatieve behandeling van instabiele enkelfracturen. Na operatieve behandeling kan de aangedane enkel weer sneller functioneren zoals de contralaterale enkel.
Bronnen (Rowley, 1986) |
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat operatieve behandeling van instabiele enkelfracturen de kans op klachten van zwelling van de enkel op lange termijn verhoogt ten opzichte van conservatieve behandeling.
Bronnen (Bauer, 1985) |
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat er een verlaagd risico is op klachten van instabiliteit na operatieve behandeling van instabiele enkelfracturen ten opzichte van conservatieve behandeling.
Bronnen (Bauer, 1985) |
Complicaties
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat een conservatieve behandeling een grotere kans heeft op secundaire dislocatie ten opzichte van operatieve behandeling waardoor patiënten alsnog geopereerd moeten worden.
Bronnen (Bauer, 1985; Makwana, 2001; Phillips, 1985; Rowley, 1986; Sanders, 2012) |
Pijn
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat op middellange termijn (twee tot zeven jaar) er geen verschil in pijn tussen operatief en conservatief behandelde enkelfracturen is.
Bronnen (Makwana, 2001; Bauer, 1985) |
Heling van de enkelfractuur
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat een operatieve behandeling van instabiele enkelfracturen het risico op malunion of nonunion reduceert ten opzichte van conservatieve behandeling.
Bronnen (Bauer, 1985; Makwana, 2001; Phillips, 1985; Rowley, 1986; Sanders, 2012) |
Artrose in het enkelgewricht
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat het risico op radiologische tekenen van artrose na operatieve of conservatieve behandeling van instabiele enkelfracturen niet verschilt op korte en middellange termijn (3,5 tot zeven jaar).
Bronnen (Bauer, 1985; Phillips, 1985) |
Beweeglijkheid van het enkelgewricht
|
Zeer laag GRADE |
Er zijn voorzichtige aanwijzingen dat de beweeglijkheid van het enkelgewricht niet verschilt na operatieve en conservatieve behandeling van instabiele enkelfracturen.
Bronnen (Bauer, 1985; Makwana, 2001) |
Duur van ziekenhuisopname
|
Laag GRADE |
Operatieve behandeling van instabiele enkelfracturen leidt zeer waarschijnlijk tot langere ziekenhuisopname dan conservatieve behandeling.
Bronnen (Bauer, 1985; Makwana, 2001) |
Beschrijving studies
In de originele review van Donken (2012) zijn drie gerandomiseerde studies (Bauer 1985, n=111; Makwana 2001, n=43; Phillips 1985, n=96) en een quasi-gerandomiseerde studie (Rowley 1986, n=42) opgenomen. In de update van de review is daar één studie aan toegevoegd (Sanders 2012). De studies zijn uitgevoerd in Europa (Zweden [Bauer], Groot-Brittannië [Makwana; Rowley]) of Noord-Amerika (VS [Phillips] en Canada [Sanders, 2012]). Ongeveer 42% van de 373 patiënten is man en de leeftijd van de patiënten varieert tussen 15 en 91 jaar. Hoewel in de studie van Makwana (2001) alleen oudere patiënten (55 jaar en ouder) zijn opgenomen, sluit de studie van Sanders 2012 ouderen juist uit (tot 65 jaar). Het betreft patiënten met verplaatste enkelfracturen (Makwana 2001; Rowley, 1986) van het Weber type B (Sanders, 2012), Weber type A of B (Bauer, 1985) of Lauge Hansen supinatie exorotatie (SER) type 4 of pronatie exorotatie (PER) type 4 breuken (Phillips, 1985). In alle studies worden behandeluitkomsten van opereren (open reductie en interne fixatie, ORIF) vergeleken met conservatieve behandeling door middel van immobilisatie met gips. In de conservatieve behandelingen varieerde de lengte van het gips van onderbeengips (Makwana, 2001) tot bovenbeengips (Phillips, 1985). Het materiaal gebruikt voor immobilisatie was meestal gips, hoewel Sanders (2012) ook braces gebruikt. Follow-up varieerde tussen 20 weken (Rowley, 1986) tot zeven jaar (Bauer, 1985).
Resultaten: functioneren
Rowley (1986; n=42) rapporteerde de tijd tot functioneel herstel. Zij hebben de tijd tot belasting, dorsaalflexie (ten opzichte van de contralaterale enkel) en de hoek van de voetafdruk op de grond in relatie tot de looprichting gemeten (ten opzichte van de contralaterale voet) op 8, 10, 12, 16 en 20 weken na de behandeling. Conservatief behandelde patiënten konden de enkel sneller weer zelfstandig belasten en ook waren de belaste dorsaalflexie en de hoek van de voetafdruk sneller weer normaal.
Na twintig weken was bij 35% (7/20) van de operatief behandelde enkels en 10% (2/20) van de conservatief behandelde enkels nog steeds sprake van een abnormale hoek van de voetafdruk (RR= 3,50 [95% BI 0,8 tot 14,8]).
Functioneren is gemeten met de enkel-specifieke Olerud Molander score (Sanders, 2012 en Makwana, 2001), de algemene SF-36 fysieke componentscore (Sanders, 2012) en middels een gecombineerde score samen met andere klinische uitkomsten, anatomische uitkomsten en artrose-uitkomsten (Phillips, 1985). Met alle meetinstrumenten in alle drie studies was een trend waarneembaar van betere uitkomsten na operatieve behandeling. De Olerud Molander score loopt van nul tot 100 waarbij hogere scores duiden op gunstigere uitkomsten. Sanders (2012; n=81) heeft de Olerud Molander scores gemeten op baseline, na zes weken, twaalf weken, een half jaar en een jaar follow-up. Op geen van de momenten is een significant verschil gevonden tussen de behandelgroepen, wel is er een kleine trend ten gunste van operatie (gemiddelde verschillen variëren tussen -0,90 en 6,20 punten). Makwana heeft de Olerud Molander score gemiddeld 27 maanden na de behandeling afgenomen. Hierbij scoren operatief behandelde patiënten gemiddeld zeventien punten hoger dan conservatief behandelde patiënten ([95% BI 0,6 tot 33,4], P<0,05). In het gepoolde resultaat van deze twee studies met respectievelijk een à twee jaar follow-up was er een trend ten gunste van de operatief behandelde patiënten (MD= 6,8 [95% BI -1,6 tot 15,2]; I2=50,0%; n=112), maar dit verschil is niet significant. Vanwege de matige heterogeniciteit van de studies (I2=50%), staat het poolen van de resultaten ter discussie.
Het algemeen fysiek functioneren is in de studie van Sanders (2012) gemeten op dezelfde vijf momenten tussen baseline en één jaar follow-up. Gebruik is gemaakt van de fysieke componentscore van de SF-36 bestaande uit de vier subschalen: fysiek functioneren, rolbeperkingen door fysieke problemen, lichamelijke pijn en algemene gezondheid. Er is een trend richting beter functioneren in de operatieve groep, maar op geen enkel moment in de follow-up is er een significant verschil tussen beide behandelgroepen (gemiddeld verschil varieert tussen -0,50 en 6,60 punten). In de studie van Phillips (1985) zijn klinische uitkomsten (onder andere pijn, functioneren en bewegingsvrijheid), anatomische uitkomsten en artrose-uitkomsten gecombineerd tot één uitkomstmaat. In deze studie doen patiënten in de operatieve groep het na drieënhalf jaar significant beter (MD= 10,30 [95% BI 0,9 tot 19,7]; p<0,05) dan patiënten in de conservatieve behandelgroep.
Zeven jaar na de behandeling blijkt er geen significant verschil tussen beide behandelgroepen in problemen met lopen op even of oneffen ondergrond. Veertien procent van de conservatief behandelde patiënten ervaart problemen bij lopen op een even ondergrond in vergelijking met 9% van de operatief behandelde patiënten (operatie 4/43, conservatief 7/49; RR= 0,65 [95% BI 0,20 tot 2,07]; Bauer, 1985). In beide behandelgroepen ervaren elf patiënten problemen bij lopen op een oneffen ondergrond (RR=1,14 [95% BI 0,6 tot 2,4]; Bauer, 1985).
Aanzienlijke klachten van zwelling, pijn, instabiliteit, bewegingsvrijheid en/of passagère stijfheid zeven jaar na de behandeling worden ervaren door 26% van de operatief en 29% van de conservatief behandelde patiënten (RR= 0,90 [95% BI 0,5 tot 1,8]; NS). Klachten van zwelling kwamen significant vaker voor onder operatief behandelde patiënten (RR= 2,14 [95% BI 1,0 tot 4,5]; p<0,05). Klachten van instabiliteit kwamen waren daarentegen minder frequent (RR= 0,38 [95% BI 0,1 tot 1,1]; NS). Het risico op klachten van passagère stijfheid (RR= 0,81 [95% BI 0,3 tot 2,4]; NS) was in beide behandelgroepen nagenoeg gelijk (Bauer, 1985). De gerapporteerde klachten van beperkte bewegingsvrijheid en pijn worden in de betreffende paragraaf beschreven.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat functioneren is met drie niveaus verlaagd. Er zijn beperkingen in de onderzoeksopzet; metingen kunnen beïnvloed zijn omdat de RCTs niet zijn geblindeerd tevens is niet in alle RCTs de analyse uitgevoerd volgens het intention-to-treat principe. Daarnaast is de bewijskracht verlaagd vanwege het geringe aantal patiënten (imprecisie).
De totale bewijskracht komt hiermee uit op zeer laag.
Resultaten
Complicaties
Complicaties die zijn gerapporteerd zijn: falen van de behandeling, diepe infecties, oppervlakkige infecties, blaarvorming, trombose, complex regionaal pijnsyndroom, wondhelingsstoornissen, gevoeligheid van het litteken en de noodzaak tot het verwijderen van de interne fixatie.
Falen van de behandeling (secundaire dislocatie) is gerapporteerd in vijf studies (Bauer, 1985; Makwana, 2001; Phillips, 1985; Rowley, 1986; Sanders, 2012) met gezamenlijk 323 patiënten. Uit het gepoolde resultaat van deze vier studies blijkt dat een operatieve behandeling significant minder vaak faalt (RR= 0,18 [95%CI 0,1 tot 0,5]; I2=0,0%; p<0,05).
Het risico op diepe en oppervlakkige infecties, onderzocht door (Bauer, 1985; Makwana, 2001; Phillips, 1985; Sanders, 2012) bij in totaal 253 patiënten en bedraagt voor de operatief behandelde groep 6.6% (12/182 operatief behandelde patiënten).
Het risico op trombose (RR=0,76 [95% BI 0,1 tot 4,3]; Bauer, 1985), complex regionaal pijn syndroom (RR=3,25 [95% BI 0,2 tot 62,4]; Makwana, 2001), wondhelingsstoornissen (RR= 1,95 [0,1 tot 44,3]; Makwana, 2001) en gevoeligheid van het litteken (RR= 3,25 [95% BI 0,2 tot 62,4]; Makwana, 2001) is gelijk in beide groepen.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat complicaties is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (analyse niet volgens intention-to-treat principe); tegenstrijdige resultaten (inconsistentie van de uitkomstmaat infecties; oppervlakkig/diep niet goed gespecificeerd) en het geringe aantal patiënten (imprecisie).
Resultaten
Pijn
Pijnscore gemeten met een visual analogue scale (VAS) twee jaar na de behandeling is in beide behandelgroepen gelijk, het gemiddeld verschil in pijnscore bedroeg slechts 0,30 punten [95% BI -16,9 tot 17,5]; NS; Makwana, 2001). Ook na zeven jaar follow-up is het aantal patiënten met klachten dichotoom gemeten pijn in beide behandelgroepen gelijk (operatief 30% (13/43), conservatief 29% (14/49); RR= 1,06 [95% BI 0,6 tot 2,0]; NS; Bauer, 1985).
Bewijskracht van de literatuur
Gezien beperkingen in de onderzoeksopzet is de bewijskracht voor de uitkomstmaat pijn met twee niveaus verlaagd. In de studie van Makwana zijn acht conservatief behandelde patiënten met secundaire dislocatie onterecht niet zijn meegenomen in de analyse. Ook zijn patiënten en onderzoekers in beide studies niet geblindeerd. Daarnaast is sprake van imprecisie waarvoor de bewijskracht met nog eens twee niveaus is verlaagd. In beide studies is het aantal patiënten en daarmee de power onvoldoende en zijn er brede betrouwbaarheidsintervallen met daarin zowel een heel gunstig als heel ongunstig effect mogelijk geven. De totale bewijskracht voor de uitkomstmaat pijn is met drie niveaus verlaagd en komt daarmee uit op zeer laag.
Resultaten
Radiologische heling van de fractuur
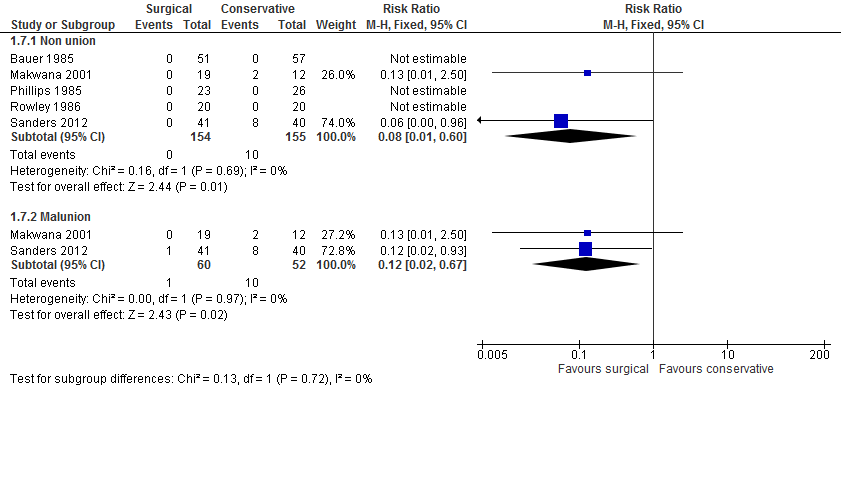
Eén van de doelen van een operatie is verlaging van het risico op delayed union of nonunion door perfecte anatomische reconstructie en rigide fixatie. Cases van delayed of nonunion zijn gerapporteerd in alle vijf studies met in totaal 373 patiënten (Bauer, 1985; Makwana, 2001; Phillips, 1985; Rowley, 1986; Sanders, 2012). Bij operatief behandelde enkelfracturen trad significant minder vaak delayed of nonunion op ten opzichte van conservatief behandelde fracturen. Het gepoold relatief risico op delayed union of nonunion is 0,08 [95% BI 0,0 tot 0,6]; fixed effects model; I2=0,0%; n=209). Daarnaast blijkt uit de studies van Makwana (2001) en Sanders (2012) het risico op malunion significant lager voor operatief behandelde patiënten. Het gepoolde relatief risico op malunion was 0,12 [95% BI 0,0 tot 0,7] (fixed effects model; I2= 0,0%; n=112). In de studie van Rowley (1986) zijn patiënten met onacceptabele positie na gesloten repositie en patiënten waarbij verlies van repositie tijdens de gipsbehandeling optrad na een of twee weken niet meegenomen in analyse. Dit geeft te positieve resultaten voor gipsbehandeling. Conservatief behandelde patiënten zonder goede uitlijning zijn niet meegenomen in de analyse (geen intention-to-treat analyse), hierdoor lijken de uitkomsten van de conservatieve behandeling gunstiger.
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat heling van de breuk is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (één niveau; beoordelaars van de röntgenfoto’s zijn niet geblindeerd) en vanwege imprecisie (twee niveaus; het aantal patiënten is onvoldoende, zeker gezien het lage aantal events).
Resultaten
Artrose van het enkelgewricht
Radiologische tekenen van artrose drieënhalf (Bauer, 1985) en zeven (Philips, 1985) jaar na de behandeling zijn gerapporteerd. In de studie van Bauer was er sprake van artrose bij 72% (31/43) operatief behandelde patiënten en bij 65% (32/49) conservatief behandelde patiënten. Phillips rapporteerde artrose bij respectievelijk 65% (15/23) en 69% (18/26) patiënten. Uit deze studies blijkt geen verschil in risico op artrose (gepoold RR=1,05 [95% BI 0,8 tot 1,3]; fixed effects model; I2=0,0%; n=141).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat artrose is met drie niveaus verlaagd gezien beperkingen in de onderzoeksopzet (één niveau vanwege het niet blinderen van beoordelaars). Bovendien zijn de uitkomsten gebaseerd op een kleine onderzoekspopulatie en vallen zowel grote positieve als negatieve effecten in het brede betrouwbaarheidsinterval (imprecisie; twee niveaus).
Resultaten
Beweeglijkheid van het enkelgewricht
Beweeglijkheid (ook wel range of motion genoemd) gemeten met goniometrie en patiënt-gerapporteerd is beschreven door Makwana (2001) bij ca. twee jaar follow-up en door Bauer (1985) bij zeven jaar follow-up. Makwana rapporteerde in de operatieve groep 9° minder plantair-dorsaalflexie ten opzichte van de contralaterale enkel. In de conservatieve groep was dit verschil significant groter, nl. 16° verschil, p=0,044. In de studie van Bauer (1985) bleek dorsaal-plantairflexie, dorsaalflexie met belasting en pronatie-supinatie van de aangedane enkels niet beperkt ten opzichte van de contralaterale enkel en was er geen verschil tussen beide groepen. Het gemiddeld verschil tussen beide groepen was respectievelijk -0,90 graden [95% BI -4,3 tot 2,5], -0,70 graden [95% BI -3,5 tot 2,1] en 0,40 graden [95% BI -1,2 tot 2,0]. Het aantal patiënten met klachten over beperkte beweeglijkheid was na zeven jaar ook statistisch gelijk (operatief 21% (9/43), conservatief 12% (6/49); RR= 1,71 [95% BI 0,7 tot 4,4]).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat beweeglijkheid is met drie niveaus verlaagd. Er zijn beperkingen in de onderzoeksopzet (twee niveaus; de studies zijn niet geblindeerd en ook is er niet altijd een intention-to-treat analyse uitgevoerd). Daarnaast is de bewijskracht verlaagd vanwege het geringe aantal patiënten (imprecisie).
Resultaten
Duur van ziekenhuisopname
Uit de twee studies (n=154) die de duur van de ziekenhuisopname rapporteren blijkt dat de opnameduur na operatieve behandeling significant langer is dan bij conservatieve behandeling. In de studie van Bauer (1985) verbleven conservatief behandelde patiënten gemiddeld vijf dagen in het ziekenhuis en operatief behandelde patiënten gemiddeld 9,5 dagen (p<0,05). In de studie van Makwana (2001) verbleven conservatief behandelde patiënten gemiddeld 2,6 dagen en operatief behandelde patiënten 6,7 dagen in het ziekenhuis (MD= 4,10 dagen [95% BI 2,6 tot 5,6]; p=0,01).
Bewijskracht van de literatuur
De bewijskracht voor de uitkomstmaat opnameduur is met twee niveaus verlaagd gezien de extrapoleerbaarheid en het geringe aantal patiënten (imprecisie);
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende wetenschappelijke vraagstelling(en):
Wat zijn de (on)gunstige effecten van chirurgische therapie versus conservatieve therapie ter behandeling van patiënten met een instabiele enkelfractuur?
P patiënten met een instabiele enkelfractuur (verschillende diagnoses);
I chirurgische therapie;
C conservatieve therapie;
O loopafstand, pijn, terugkeer naar werk of sport, complicaties (infecties, heroperaties).
Relevante uitkomstmaten
De werkgroep achtte functionele resultaten, pijn en complicaties voor de besluitvorming kritieke uitkomstmaten. Tijd tot terugkeer naar werk, range of motion van het gewricht, radiologisch anatomisch resultaat en radiologische artrose voor de besluitvorming belangrijke uitkomstmaten.
Zoeken en selecteren (Methode)
De Cochrane review van Donken (2012) sluit aan bij de uitgangsvraag en is van goede kwaliteit. Daarom is besloten deze review te updaten met recente literatuur. De zoekactie is herhaald voor de periode februari 2012 tot 5 oktober 2015. In de databases Medline (OVID), Embase (Elsevier), Cochrane (Wiley) en Pubmed is met relevante zoektermen gezocht naar gerandomiseerde en quasi-gerandomiseerde gecontroleerde trials. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 611 treffers op. Studies werden geselecteerd op grond van de selectiecriteria beschreven in de review. Op basis van titel en abstract werden in eerste instantie twee studies voorgeselecteerd. Na raadpleging van de volledige tekst, werd vervolgens één studie geëxcludeerd (zie exclusie-tabel) en één studie definitief geselecteerd en toegevoegd aan de review.
(Resultaten)
De originele review bevat vier (quasi) gerandomiseerde gecontroleerde studies (Donken, 2012). Naar aanleiding van de update is hier één studie aan toegevoegd (Sanders, 2012). De evidence-tabellen en beoordeling van individuele studiekwaliteit kunt u vinden onder het tabblad Onderbouwing.
- Bauer M, Jonsson K, Nilsson B. Thirty-year follow-up of ankle fractures. Acta Orthop Scand. 1985;56:103-106. PMID: 3925709.
- Belmont PJ Jr, Davey S, Rensing N, et al. Patient-Based and Surgical Risk Factors for Thirty-Day Post-operative Complications and Mortality Following Ankle Fracture Fixation in Hospitalized Patients. J Orthop Trauma. 2015;14. PubMed PMID: 25785357.
- Bhandari M, Sprague S, Ayeni OR, et al. A prospective cost analysis following operative treatment of unstable ankle fractures: 30 patients followed for 1 year. Acta Orthop Scand. 2004;75(1):100-105. PubMed PMID: 15022817.
- Court-Brown CM, McBirnie J, Wilson G. Adult ankle fractures an increasing problem? Acta Orthopedica Scandinaar aanleiding vanica. 1998;69(1):43-47. PMID: 9524517.
- DeAngelis NA, Eskander MS, French BG. Does medial tenderness predict deep deltoid ligament incompetence in supination-external rotation type ankle fractures? J Orthop Trauma. 2007;21:244-247. PMID: 17414551.
- Donken CC, Al-Khateeb H, Verhofstad MH, et al. Surgical versus conservative interventions for treating ankle fractures in adults. Cochrane Database Syst Rev. 2012;15;8:CD008470.
- Gardner MJ, Demetrakopoulos D, Briggs SM, et al. The Ability of the Lauge-Hansen Classification to Predict Ligament Injury and Mechanism in Ankle Fractures: An MRI study. J Orthop Trauma. 2006;20:267-272. PMID: 16721242.
- Høiness P, Engebretsen L, Strømsøe K. Cost of surgical treatment of closed ankle fractures. Eur J Trauma. 2002;28:258-262. (niet op Pubmed, dus geen PMID).
- Horisberger M, Valderrabano V, Hintermann B. Posttraumatic ankle osteoarthritis after ankle-related fractures. J Orthop Trauma. 2009;23:60-67. PMID: 19104305.
- Koval KJ, Lurie J, Zhou W, et al. Ankle fractures in the elderly: what you get depends on where you live and who you see. J Orthop Trauma. 2005;19(9):635-639. PubMed PMID: 16247309.
- Kristensen KD, Hansen T. Closed treatment of ankle fractures. Stage II supination-eversion fractures followed for 20 years. Acta Orthop Scand. 1985;56:107-109. PMID: 3925710.
- Kwon JY, Chacko AT, Kadzielski JJ, et al. A novel methodology for the study of injury mechanism: ankle fracture analysis using injury videos posted on youtube.com. J Orthop Trauma. 2010;24:477-482. PMID: 20657256.
- Lauge-Hansen N. Fractures of the ankle IV. Clinical use of genetic roentgen diagnosis and genetic reduction. Arch Surg. 1952;64:488-500. PMID: 14902249.
- Lindsjö U. Operative treatment of ankle fracture-dislocations. A follow-up study of 306/321 consecutive cases. Clin Orthop Relat Res. 1985;(199):28-38. PubMed PMID: 3930122.
- Ovaska M. Complications in ankle fracture surgery. Acta Orthop Suppl. 2015;86(358):1-32. PubMed PMID: 25586467.
- Patiëntenfederatie Nederland. Rapport gebroken enkel. 2016.
- Pelet S, Roger ME, Belzile EL, et al. The incidence of thromboembolic events in surgically treated ankle fracture. J Bone Joint Surg Am. 2012;21;94(6):502-506. PubMed PMID: 22437998.
- Ramsey PL, Hamilton W. Changes in the tibiotalar area of contact caused by lateral shift. J Bone Joint Surg (Am). 1979;58:356-357. PMID: 1262367.
- Sanders DW, Tieszer C, Corbett B, et al. Operative versus nonoperative treatment of unstable lateral malleolar fractures: a randomized multicenter trial. J Orthop Trauma. 2012;26(3):129-134. PMID: 22330975.
- Schepers T, De Vries MR, Van Lieshout EMM, et al. The timing of ankle fracture surgery and the effect on infectious complications; A case series and systematic review of the literature. International Orthopaedics. 2013;37:489-494. PMID: 23288046.
- Slobogean GP, Marra CA, Sadatsafavi M, et al. Is surgical fixation for stress-positive unstable ankle fractures cost effective? Results of a multicenter randomized control trial. J Orthop Trauma. 2012;26(11):652-658. PubMed PMID: 22473067.
- SooHoo NF, Krenek L, Eagan MJ, et al. Complication rates following open reduction and internal fixation of ankle fractures. J Bone Joint Surg Am. 2009;91(5):1042-1049. PubMed PMID:19411451.
- Strauss EJ, Egol KA. The management of ankle fractures in the elderly. Injury. 2007;38(Supplement3):S2-S9.
- Stufkens SAS, van den Bekerom MPJ, Kerkhoffs GMMJ, et al. Long-term outcome after 1822 operatievely treated ankle fractures: A systematic review of the literature. Injury 2011;42(2):119-127. PMID: 20444447.
- Zaghloul A, Haddad B, Barkfield R, et al. Early complications of surgery in operative treatment of ankle fractures in those over 60: a review of 186 cases. Injury, Int J Care Injured. 2014;45:780-3. PubMed PMID: 24388418.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison / control (C)
|
Follow-up |
Outcome measures and effect size
Effect measure: RR or MD [95% CI] |
Comments |
|
Donken, 2012
|
SR and meta-analysis of randomised and quasi-randomised controlled clinical studies
Original literature search up to Feb 2012 and updated until Oct 2015
A: Bauer, 1985 B: Makwana, 2001 C: Phillips, 1985 D: Rowley, 1986 E: Sanders, 2012*
Study design: Randomised and quasi randomised Controlled Trials, parallel group
Setting and Country: A: Dep. of Orthopaedic surgery, Malmö general Hospital and Österund Hospital, Sweden B: Level 1 trauma centre, Leicester Royal Infirmary, UK C: level 1 trauma centre, University of Chicago Hospitals, USA D: The Royal Hallamshire Hospital, University of Sheffield, UK E: Six level 1 trauma centers, Canada
Source of funding: [commercial / non-commercial / industrial co-authorship] A: B: non-commercial (No benefits in any form have been received or will be received from a commercial party related directly or indirectly to the subject of this article) C: D: not reported E: non-commercial (Canadian Orthopedic Trauma Society AO Foundation and OTC/AIOD Foundation)
|
Inclusion criteria SR: Randomised and quasi-randomised controlled clinical studies comparing surgical and conservative treatments for ankle fractures in adults
Exclusion criteria SR: Studies including adult participants with ankle fractures who underwent a surgical or conservative intervention were included. Trials containing adults and children were included if the proportion of children was clearly small (< 5%), or if separate data for adults could be obtained. Similarly, we excluded studies in which participants with more extensive fractures of the distal third of the tibia (pilon or tibial plafond fractures) or studies that included more than 5% fractures with delayed presentation, unless separate data for acute ankle fractures could be obtained. Studies evaluating surgical revision of displaced fractures were excluded.
5 studies included in total; original review 4 studies, update 1 study
Important patient characteristics at baseline:
N, mean age A: 111 patients, 44 yrs. B: 43 patients, 66 yrs. C: 96 patients, 42 yrs. D: 42 patients, mean age not reported, range [16-70] yrs. E: 81 patients, 41 yrs.
Sex, n (%) male: A: 44 (40%) B: 12 (28%) C: 42 (44%) D: not reported E: 41 (51%)
Ankle fracture: A: displaced type A or B malleolar fractures B: displaced ankle fractures C: closed Lauge Hansen SER type 4 or PER type 4 ankle fractures for which a satisfactory closed reduction had been achieved D: displaced ankle fractures E: Weber B fibular fractures with MCS>5mm on stress radiograph
Comorbidity (diabetes)?
Lifestyle (smoking, alcohol)?
Groups comparable at baseline? Yes |
All: open reduction and internal fixation (ORIF)
A: according to the AO principles (Müller 1979). Ligamentous injuries were sutured. Suction drainage as applied for 24 hours. Active movements started on the first postoperative day. The patients were kept in bed with the operated leg elevated in a splint until the fifth postoperative day. After 6 weeks, 20% weight bearing was allowed. Full weight bearing was allowed after 9 weeks B: standard AO implants and techniques according to the AO/ASIF manual (Müller 1979). Additional information from correspondence (Ramasamy 2001): Nearly all the fractures of the ankle (96%) were fixed using a 1/3 semitubular plate on the lateral side, with or without lag screws. In one patient the lateral malleolus was treated by a Rush pin. AO cancellous screws were used in 82% of cases on the medial side, and this was supplemented in one by a Kirschner wire. No fixation was necessary in three medial malleoli. Postoperative regimen: a below-knee cast was retained for six weeks. The leg was elevated for 48 hours after which protected weight-bearing was allowed C: satisfactory closed reduction and then open reduction and internal fixation by the Association for the Study of Internal Fixation (ASIF) technique. The leg was immobilised in a below-the-knee plaster cast. Walking on crutches without weight bearing started a few days after surgery until the tenth week. The cast was removed after 1 week to allow early active motion exercises. The trans-syndesmotic screw (if present) was removed after 10 weeks D: Open reduction and internal fixation, using the standard AO technique (Müller 1979), fixing the fibula with compression screws and a buttress plate, and the medial malleolus with screws or tension bands according to the fragment size. No attempt was made to institute any ligamentous repair. After fixation, the limb was placed in a below-knee backslab; early active movement was started on the first day after operation and continued for five days until a reasonable range of movement was established. The ankle was then placed in a below-knee plaster for 6 weeks and early weight-bearing was encouraged. At 6 weeks, patients were mobilised out of plaster and weight bearing was encouraged as soon as possible. No formal physiotherapy was offered E: open reduction and internal fixation of the lateral malleolus within 2 weeks of the injury. Specific elements of operative care were standardized. All patients received preoperative antibiotics before skin incision. Standard fixation techniques were used, including direct reduction, lag screw fixation where possible, and fibular stabilization using neutralization or antiglide plates. Tourniquet use and the choice of hardware material and manufacturer were allowed at the discretion of the operating surgeon. After surgery, the ankle was splinted in neutral dorsiflexion for 2 weeks. This was followed by early mobilization and protected weight bearing in a removable cast brace until the 6-week visit. Weight bearing was permitted within the limits of patient discomfort.
|
All: plaster cast immobilisation (conservative treatment)
A: closed reduction was performed and a plaster cast was applied. The patients were discharged as soon as they were able to walk on crutches. Weight bearing was not allowed during the first 6 weeks in either group to prevent load-induced displacement. After 6 weeks, the cast was removed and 20% weight bearing was allowed. Full weight bearing was allowed after 12 weeks B: a moulded below-knee plaster cast, with 48 hours limb elevation, after which protected weight-bearing was allowed for 6 weeks C: satisfactory closed reduction followed by continued closed treatment. A toe-to-thigh cast with the knee flexed in 30 degrees was applied for 6 weeks, without weight-bearing. At the end of 6 weeks a below-the-knee walking cast was applied for an additional 4 weeks D: After manipulation, the position of the fracture was subsequently maintained in a long-leg plaster for 6 weeks and early weight-bearing was encouraged. The criteria of a good reduction were defined as correction of talar shift on the anterolateral radiograph and of posterior talar subluxation on the lateral film. On both views, the fibula had to be corrected in terms of rotation and length. The medial malleolus had to have a smooth articular profile, although a small step on its medial aspect was acceptable. Further radiographs were taken at one and two weeks from injury; if there was significant loss of position the patient was re-admitted and open reduction and internal fixation was carried out. At 6 weeks, patients were mobilised out of plaster and weight bearing was encouraged as soon as possible. No formal physiotherapy was offered E: Nonoperative intervention included treatment with a plaster or fiberglass cast or brace and protected weight bearing (avoidance of full unrestricted weight bearing without the use of crutches) for 6 weeks. Patients in the nonoperative group were reviewed 1 or 2 weeks post randomization, to ensure appropriate cast or brace fit and for repeat radiographic assessment of alignment.
|
End-point of follow-up: A: mean 7 years B: mean 27 months C: 3.5 years D: 20 weeks E: 52 weeks after treatment
For how many participants were no complete outcome data available? (intervention/control) A: 19 (17%) B: 12 (28%) C: 47 (49%) D: 2 (5%) E: 13 (16%)
|
Functioning Symptoms at 7 years Complaints of significant symptoms A: I: 11/43 (25.6%) C: 14/49 (28.6%) RR= 0.90 [0.46, 1.76], NS Swelling A: RR= 2.14 [1.01, 4.54], p<0,05 Unsteadiness A: RR= 0.38 [0.13, 1.09], NS Passing stiffness A: RR= 0.81 [0.28, 2.38], NS E: Not reported
Functional impairment at 20 weeks Restricted dorsiflexion D: RR= 1.33 [ 0.34, 5.21 ] Abnormal foot angle D: RR= 3.50 [ 0.83, 14.83 ] Time to independent weight bearing D: I: 16 weeks C: 12 weeks Time to normal range of motion A: I: 9 weeks [6-12] C: 12 weeks [9-15] P<0.01
OMA scores Baseline E: MD=6.20 [-3.03, 15.43], NS 6 weeks E: MD=-0.40 [-8.96, 8.16], NS 12 weeks E: MD=4.60 [-5.68, 14.88], NS 24 weeks E: MD=-0.90 [-9.90, 8.10], NS 52 weeks E: MD= 3.20 [-6.56, 12.96], NS 27 mo. (mean) B: MD=17.00 [0.64, 33.36], P<0,05 Pooled effect (Sanders 52 weken; Makwana 27 maanden; n=112): MD= 6.82 [-1.56, 15.20] favoring surgery, NS Heterogeneity (I2): 50.0%
SF-36 PCS score Baseline (0 weeks) E: MD= 5.80 [-2.63, 14.23], NS 6 weeks E: MD= 3.00 [-2.73, 8.73], NS 12 weeks E: MD= 6.60 [-1.55, 14.75], NS 24 weeks E: MD= -0.50 [-8.99, 7.99], NS 52 weeks E: MD= 2.00 [-6.61, 10.61], NS
Combined scores (clinical, anatomical + arthritis) at mean 3.5 yrs. C: MD= 10.30 [0.93, 19.67], p<0.05
Complaints of walking difficulties on rough ground at 7 yrs. A: I 11/43 (25.6%), C 11/49 (22.4%); RR= 1.14 [0.55, 2.36], NS
Complaints of walking difficulties on even ground at 7 yrs. A: I 4/43 (9.3%), C 7/49 (14.3%); RR= 0.65 [0.20, 2.07], NS
Pain: VAS scores at 27 mo. B: MD= 0.30 [-16.90, 17.50], NS E: Not reported
Complaints of pain at 7 yrs. A: RR= 1.06 [0.56, 2.00], NS
Adverse events: Early treatment failure (usually secondary operation) A: RR= 0.28 [ 0.06, 1.26 ], NS B: RR= 0.06 [ 0.00, 0.92 ], <0.05 C: RR= 0.38 [ 0.02, 8.78 ] NS D: RR= 0.22 [ 0.01, 4.30 ], NS E: RR=0.2 [0.01, 0.51], NS Pooled effect (fixed effects model; n=): RR= 0.18 [95%CI 0.07 to 0.51] favoring surgery, p<0.05 Heterogeneity (I2): 0.0%
Deep / more serious infection A: I: 0/43 C: 2/49 RR= 0.23 [ 0.01, 4.61 ], NS B: I: 0/19 C: 0/12 RR=Not estimable C: I: 0/23 C: 0/26 RR=Not estimable E: I: 1/41; C: 0/40; RR= 2.93 [0.12, 69.83], NS
Pooled effect (fixed effects model n=253): RR= 0.71 [0.12, 4.33] favoring surgery, NS Heterogeneity (I2): 24%
Superficial infection A:RR= 0.23 [ 0.01, 4.61], NS B: RR= 1.95 [ 0.09, 44.32 ], NS C: RR= 3.38 [ 0.14, 79.00 ], NS E: I: 5/41; C: 0/40; RR= 10.74 [0.61, 188.05] Pooled effect (fixed effects model; n=253): RR= 2.23 [0.68, 7.29], NS favoring conservative treatment Heterogeneity (I2): 13.0%
Skin ulcers B: RR= 0.22 [ 0.01, 4.92 ], NS C: RR= 0.23 [ 0.01, 4.46 ], NS Pooled effect (fixed effects model; n=80): RR=0.22 [95% CI 0.22 to 1.93], NS favoring surgery Heterogeneity (I2): 0.0%
Deep vein thrombosis A: RR= 0.76 [0.13, 4.34]
Complex regional pain syndrome B: RR= 3.25 [0.17, 62.40] E: Not reported
Wound closure problem B: RR= 1.95 [0.09, 44.32]
Removal of internal fixation B: I: 3/19 (15.8%) C: 0/12 (0%) RR= 4.55 [0.26, 81.03] E: I: 5/41 (12.2%) C: 0/40 (0%) RR= 10.74 [0.61, 188.05] Pooled effect (fixed effects model; n=112): RR= 7.37 [1.00, 54.36] favoring conservative Heterogeneity (I2): 0.0%
Surgical scar tenderness B: RR= 3.25 [0.17, 62.40]
Range of motion: E: Not reported
Difference in range of motion (injured ankle – other ankle) at 7 yrs. FU Dorso-plantar in degrees, mean (SD) A: I: -4.3 (7.2) C: -3.4 (9.3) MD= -0.90 [ -4.28, 2.48 ] Dorsiflexion in degrees, mean (SD) A: I: -4.0 (4.9) C: -3.3 (8.5) MD= -0.70 [ -3.49, 2.09 ] Pro-supination in degrees, mean (SD) A: I: -1.4 (3.5) C: -1.8 (4.4) MD= 0.40 [ -1.22, 2.02 ]
B: defined as difference in range of plantar and dorsiflexion between injured and uninjured ankle at 27 mo. FU) I: 9 degrees C: 16 degrees, p=0.044
Complaints of restricted range of motion at 7 yrs. FU A: RR= 1.71 [0.66, 4.41]
Radiological results: Delayed union or non-union A: I: 0/51 C: 0/57 RR= Not estimable B: I: 0/19 (0%) C: 2/12 (16.7%) RR= 0.13 [0.01, 2.50] C: I: 0/23 C: 0/26 RR= Not estimable D: I:0/20 C: 0/20 RR= Not estimable Delayed union† or nonunion‡ E: I: 0/41 C: 8/40 RR= 0.06 [0.00, 0.96] Pooled effect (fixed effects model; n=209): RR= 0.08 [0.01, 0.60] favoring surgery Heterogeneity (I2): 0.0%
Malunion/Misalignment B (defined as malunion): I: 0/19 C: 2/12 RR= 0.13 [0.01, 2.50] E (defined asmisalignment (MCS≥5mm or TFCS≥2mm): I: 1/41; C: 8/40; RR= 0.12 [0.02, 0.93], p<0.05 Pooled effect (fixed effects model; n=112): RR= 0.12 [0.02, 0.67] favoring surgery Heterogeneity (I2): 0.0%
Loss of reduction E: Not reported
Osteoarthritis: Radiological signs of osteoarthritis Findings at 7 yrs. A: I: 31/43 (72.1%) C: 32/49 (65.3%) RR= 1.10 [ 0.84, 1.45 ] Findings at mean 3.5 yrs. C: I: 15/23 (65.2%) C: 18/26 (69.2%) RR= 0.94 [ 0.64, 1.40 ] Pooled effect (fixed effects model; n=141): RR=1.05 [95% CI 0.83 to 1.31] favoring conservative Heterogeneity (I2): 0.0%
Ankle arthritis or stiffness E: Not reported
Length of hospital stay (days) B: RR= 4.10 [ 2.62, 5.58 ] |
Abbreviations: SR= systematic review RR= risk ratio MD= mean difference n.a.= Not applicable SER= supination- external rotation PER= pronation-external rotation NS= not significant FU= follow-up
Measurement instruments: Olerud-Molander Ankle (OMA) score Range [0 to 100], high scores indicate better outcomes Combined score Range [0 to 150], high scores indicate better outcomes SF-36 PCS Physical Component Score (PCS) of the Short Form 36 (SF-36)
* studies added to the review after update
† Delayed union defined as: a lack of bridging callus on 3 of 4 cortices at 12 weeks ‡ Nonunion defined as: lack of cortical bridging or a clearly visible fracture line at 24 weeks post injury |
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea et al.; 2007, BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher et al 2009, PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
- Research question (PICO) and inclusion criteria should be appropriate and predefined
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs)
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table etc.)
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (e.g. Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (e.g., funnel plot, other available tests) and/or statistical tests (e.g., Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Donken, 2012 |
Yes |
Yes |
Yes |
Yes |
n.a. |
Yes |
Yes |
No |
Yes |
Exclusietabel
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Patel, 2015 |
Artikel is teruggetrokken |
Beoordelingsdatum en geldigheid
Publicatiedatum : 01-09-2017
Beoordeeld op geldigheid : 25-07-2017
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2021 bepaalt het bestuur van de Nederlandse Vereniging voor Heelkunde (NVvH) of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is moet in 2019 gekeken worden of de module 'Behandeling instabiele enkelfractuur' (Willett, 2016 en Crossbat trial NCT01134094 in trialregister) en de module 'Nabehandeling gestabiliseerde enkelfractuur' (WOW-studie; Briet, 2015) herziening nodig in verband met het uitkomen van een nieuwe studies (zie kennislacunes). Bij de update van de module 'Enkelfracturen met ernstige comorbiditeit' zal de studie van White (2016) worden toegevoegd.
Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NVvH is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module |
Eerstvolgende beoordeling actualiteit richtlijn |
|
Diagnostiek bij patienten met radiologisch bewezen enkelfractuur |
2021 |
|
Diagnostiek differentieatie SE2 en SE4 |
2021 |
|
Conservatieve behandeling |
2021 |
|
Operatieve vs. conservatieve behandeling |
2019 |
|
5Behandeling begeleidende letsels |
2021 |
|
Optimale behandeling syndesmoseletsels |
2021 |
|
Beste behandeling acuut geinfecteerd osteosynthesemateriaal |
2021 |
|
Operatietechniek bij patiënten met ernstige comorbiditeit |
2021 |
|
Optimale nabehandeling operatief gestabiliseerde enkelfractuur |
2019 |
|
Fysiotherapie indicatie |
2021 |
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten (www.kennisinstituut.nl) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Patiëntenparticipatie bij deze richtlijn werd mede gefinancierd uit de Kwaliteitsgelden Patiënten Consumenten (SKPC) binnen het programma KIDZ.
Doel en doelgroep
Doel
Deze richtlijn beoogt een leidraad te geven voor de dagelijkse praktijk van diagnostiek en behandeling van enkelfracturen. Het doel van deze richtlijn is het vaststellen van de zorg betreffende de diagnostiek en behandeling van enkelfracturen. Standaardisatie van therapeutische opties door middel van een diagnose- en behandelalgoritme is noodzakelijk om praktijkvariatie te reduceren en de kwaliteit van de zorg te verhogen zonder de kosten te doen stijgen.
Doelgroep
De richtlijn beperkt zicht tot de diagnostiek en (na)behandeling van enkelfracturen bij volwassenen. De diagnostiek van enkelfracturen is gericht op het beoordelen van het soort fractuur, niet het vaststellen van de fractuur zelf. De Ottowa Ankle Rules zijn inmiddels de gouden standaard om de fractuur vast te stellen en behoeft geen verdere evaluatie. Ook wordt in deze richtlijn niet ingegaan op behandeling van osteoporose, open fracturen of pilon tibiale fracturen.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in 2015 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met enkelfracturen (zie hiervoor de samenstelling van de werkgroep).
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
- Dr. M. (Martijn) Poeze, traumachirurg, Maastricht University Medical Centre, Maastricht, NVvH (voorzitter).
- Dr. T. (Tim) Schepers, traumachirurg, Academisch Medisch Centrum, Amsterdam, NVvH
- Dr. J.M. (Jochem) Hoogendoorn, traumachirurg, Haaglanden MC, Den Haag, NVvH
- Drs. L. W. (Laurens) van der Plaat, orthopedisch chirurg-traumatoloog, AVE Orthopedische Klinieken, Huizen, NOV
- Dr. C.C.M.A. (Christian) Donken, orthopedisch chirurg in opleiding, Isala, Zwolle, NOV
- Dr. G (Göran) Zemack, revalidatiearts, Libra Revalidatie & Audiologie, Eindhoven, VRA
- Drs. A.C.L.F. (Arjan) Steenbakkers, musculoskeletaal-radioloog, Maartenskliniek, Nijmegen, NVvR
- Dr. A.F. (Ton) Lenssen, fysiotherapie, Maastricht University Medical Centre, Maastricht, KNGF
- B. A. (Annet) Warners, gipsverbandmeester, Medisch Centrum, Leeuwarden, VGN
Klankbordgroep:
- R. (Rinie) Lammers, MSc, beleidsadviseur, Patiëntenfederatie Nederland, Utrecht
- E. (Esther) Mik, MSc, commissie kwaliteit en richtlijnen, Orthobanda, Soest
Met ondersteuning van:
- Dr. W.A. (Annefloor) van Enst, senior adviseur, Kennisinstituut van Medisch Specialisten
- H.L. (Hilde) Vreeken, MSc., adviseur, Kennisinstituut van Medisch Specialisten (tot december 2015)
- E.A. (Ester) Rake, MSc., junioradviseur, Kennisinstituut van Medisch Specialisten (vanaf januari 2016)
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventueel belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Achternaam |
Functie |
Nevenfuncties |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatiemanagement |
Extern gefinancierd onderzoek |
Kennisvalorisatie |
Overige belangen |
Getekend |
|
Donken |
AIOS orthopedie Medisch Spectrum Twente |
nvt |
nvt |
nvt |
nvt |
AO research Grant (project number: AO Start-up Grant S-10-60D) voor een biomiechanisch studie naar enkelfracturen. |
nvt |
nvt |
ja, 05-04-2015 |
|
Harsevoort |
Verpleegkundig Specialist (VS) orthopedie/traumatologie 50% Coordinator expertise centrum Osteogenesis Imperfecta (OI) Isala Zwolle 50% |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
ja, 28-9-2015 |
|
Hoogendoorn |
Traumachirurg |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
ja, 10-07-2015 |
|
Lenssen |
Onderzoeker afdeling fysiotherapie MUMC (0,8FTe) senior docent fysiotherapie Hogeschool Zuyd (0,3FTe) |
Tutor Stichting Opleidingen Muskuloskeletale Therapie (freelance, docent Manuele therapie, Kerpen, Duitsland) |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
Ja, 03-10-2016 |
|
Poeze |
Traumachirurg |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
ja, 25-06-2015 |
|
Schepers |
Traumachirurg |
nvt |
nvt |
nvt |
nvt |
Nvt |
Nvt |
nvt |
Ja, 14-04-2015 |
|
Steenbakkers |
Radioloog |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
ja, 09-04-2015 |
|
Van der Plaat |
Orthopedisch Chirurg |
Medisch directeur AVE Orthopedische Klinieken |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
ja, 31-03-2015 |
|
Van Warners |
Gipsverbandmeester |
Bestuurslid Verenigde Gipsverbandmeesters Nederland met protefeuille Registratie en Accreditatie, onbetaald |
nvt |
nvt |
als (bestuurs)lid VGN belang bij goede beschrijving van de richtlijn enkelfracturen en tevens boegbeeld voor de VGN |
nvt |
nvt |
nvt |
ja, 20-04-2015 |
|
Zemack |
Revalidatiearts |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
nvt |
ja, 30-03-2015 |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door het afnemen van een enquête onder het patiëntenpanel van Patiëntenfederatie Nederland. Verder las de Patiëntenfederatie Nederland mee met de conceptteksten. Een verslag van de patiëntenenquête (zie de ‘Enquête enkelfracturen Patiëntenfederatie Nederland’) is besproken in de werkgroep en de belangrijkste knelpunten zijn verwerkt in de richtlijn. De conceptrichtlijn is tevens voor commentaar voorgelegd aan de Patiëntenfederatie Nederland. Gedurende de commentaarfase is samen met Patiëntenfederatie Nederland gewerkt aan uniforme patiënteninformatie via de patienteninformatietool.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten. De werkgroep heeft besloten geen indicatoren te ontwikkelen bij de huidige richtlijn, omdat er of geen substantiële barrières konden worden geïdentificeerd die implementatie van de aanbeveling zouden kunnen bemoeilijken.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens werden de volgende partijen uitgenodigd op de invitational conference om knelpunten aan te dragen: NOV, NVvR, VRA, KNGF, Verenigde Gipsverbandmeesters Nederland en de NVOS-Orthobanda, NPCF, Inspectie voor de Gezondheidszorg, Nefarma, Nederlandse Zorgautoriteit, Zorginstituut Nederland (ZiNL), Koepels van zorginstellingen (Nederlandse Vereniging van Ziekenhuizen (NVZ), Nederlandse Federatie van Universitair Medische Centra (NFU), Samenwerkende Topklinische Ziekenhuizen (STZ), Zelfstandige Particuliere Klinieken Nederland (ZKN), het Nederlands Huisartsen Genootschap (NHG), Vereniging voor Sportgeneeskunde (VSG), Nederlandse Vereniging voor Anesthesiologie (NVA), Verpleegkundigen & Verzorgenden Nederland (V&VN), DBC onderhoud, Federatie Medisch Coördinerende Centra (FMCC),VEKTIS en Zorgverzekeraars Nederland (ZN). Een verslag hiervan is opgenomen onder aanverwante producten.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk (maar niet kritiek) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de kritieke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Voor iedere uitgangsvraag werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen onder aanverwante producten.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR – voor systematische reviews; Cochrane – voor gerandomiseerd gecontroleerd onderzoek; ACROBAT-NRS – voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence-tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, matig, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008). In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (eindconclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De totale bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin, naast de conclusies uit de systematische literatuuranalyse, aanvullende argumenten (overwegingen) een rol spelen werd afgezien van een eindconclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje Overwegingen.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt, kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje Overwegingen.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs, de belangrijkste overwegingen en een weging van de (on)gunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in een aparte module.
Indicatorontwikkeling
Er werden geen indicatoren opgesteld, in de module Organisatie van Zorg is een suggestie opgenomen voor een toekomstige registratie van enkelfracturen.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de Kennislacunes beschreven (onder aanverwante producten).
Commentaar- en autorisatiefase
De conceptrichtlijn wordt aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren worden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren wordt de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn wordt aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Briet JP, Houwert RM, Smeeing DP, Pawiroredjo JS, Kelder JC, Lansink KW, Leenen LP, van der Zwaal P, van Zutphen SW, Hoogendoorn JM, van Heijl M, Verleisdonk EJ, van Lammeren GW, Segers MJ, Hietbrink F. Weight bearing or non-weight bearing after surgically fixed ankle fractures, the WOW! Study: study
protocol for a randomized controlled trial. Trials. 2015 Apr 18;16:175. doi: 10.1186/s13063-015-0714-1. PubMed PMID: 25927626.
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Dehghan N, McKee MD, Jenkinson RJ, Schemitsch EH, Stas V, Nauth A, Hall JA, Stephen DJ, Kreder HJ. Early Weightbearing and Range of Motion Versus Non-Weightbearing and Immobilization After Open Reduction and Internal Fixation of Unstable Ankle Fractures: A Randomized Controlled Trial. J Orthop Trauma. 2016 Jul;30(7):345-52. doi: 10.1097/BOT.0000000000000572. PubMed PMID: 27045369.
Keene DJ, Mistry D, Nam J, Tutton E, Handley R, Morgan L, Roberts E, Gray B, Briggs A, Lall R, Chesser TJ, Pallister I, Lamb SE, Willett K. The Ankle Injury Management (AIM) trial: a pragmatic, multicentre, equivalence randomised controlled trial and economic evaluation comparing close contact casting with open surgical reduction and internal fixation in the treatment of unstable ankle fractures in patients aged over 60 years. Health Technol Assess. 2016 Oct;20(75):1-158. Review. PubMed PMID: 27735787.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit. http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann HJ, Oxman AD, Brozek J, et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336(7653):1106-10. doi: 10.1136/bmj.39500.677199.AE. Erratum in: BMJ. 2008;336(7654). doi: 10.1136/bmj.a139. PubMed PMID: 18483053.
Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Kennisinstituut van Medisch Specialisten.
White TO, Bugler KE, Appleton P, Will E, McQueen MM, Court-Brown CM. A prospective randomised controlled trial of the fibular nail versus standard open reduction and internal fixation for fixation of ankle fractures in elderly
patients. Bone Joint J. 2016 Sep;98-B(9):1248-52. doi: 10.1302/0301-620X.98B9.35837. PubMed PMID: 27587528.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
2012-2015
|
1 exp Ankle Dislocation/ or exp Ankle Injury/ or exp Ankle/ or exp Ankle Fracture/ (14892) 2 Fracture Healing/ or exp Fractures, Bone/ or exp Fracture Fixation/ (155844) 3 1 and 2 (4096) 4 (ankle* or malleol* or unimalleo* or bimalleo* or potts or weber or (distal and (tibia* or fibula*))).tw. (58149) 5 fracture*.tw. (187317) 6 4 and 5 (7732) 7 3 or 6 (9233) 8 limit 7 to yr="2012 -Current" (1897) 9 limit 8 to (dutch or english) (1648) 10 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (251720) 11 9 and 10 (83) – 81 uniek 12 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1520499) 13 9 and 12 (220) 14 13 not 11 (199) – 185 uniek 15 [zoekstrategie uit SR Donken 2012 - CD008470] |
611 |
|
Embase (Elsevier) |
'ankle'/exp OR 'ankle fracture'/exp/mj OR 'ankle injury'/exp/mj OR 'ankle dislocation'/exp/mj AND ('fracture'/exp/mj OR 'fracture healing'/exp/mj OR 'fracture fixation'/exp/mj OR 'joint injury'/exp/mj OR 'bone injury'/exp/mj) OR (fracture* AND (ankle* OR malleol* OR unimalleo* OR bimalleo* OR trimalleo* OR potts OR weber)) OR (fracture* AND distal AND (tibia* OR fibula*)) AND ([dutch]/lim OR [english]/lim) AND [embase]/lim AND [2012-2015]/py
AND ('meta analysis'/de OR cochrane:ab OR embase:ab OR psychlit:ab OR cinahl:ab OR medline:ab OR (systematic NEAR/1 (review OR overview)):ab,ti OR (meta NEAR/1 analy*):ab,ti OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT ('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp NOT 'human'/exp) NOT 'conference abstract':it (114) – 79 uniek
AND 'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti NOT 'conference abstract':it (363) – 248 uniek |
|
|
Cochrane (Wiley) |
1 MeSH descriptor: [Ankle] explode all trees #2 MeSH descriptor: [Ankle Injuries] explode all trees #3 MeSH descriptor: [Ankle Joint] explode all trees #4 (#1 or #2 or #3) #5 MeSH descriptor: [Fractures, Bone] explode all trees #6 MeSH descriptor: [Fracture Healing] explode all trees #7 MeSH descriptor: [Fracture Fixation] explode all trees #8 (#5 or #6 or #7) #9 (#4 and #8) #10 (fracture* near/5 (ankle or malleol* or unimalleo* or bimalleo* or trimalleo* or potts or weber or (distal and (tibia* or fibula*)))):ti,ab #11 #9 or #10 #12 #11 Publication Year from 2012 to 2015 82: 16 SR, 66 trials 0,10 uniek |
|
|
Pubmed |
(((Fracture*[TW] AND (ankle[TW] OR malleol*[TW] OR unimalleo*[TW] OR bimalleo*[TW] OR trimalleo*[TW] OR potts[TW] OR weber[TW] OR (distal[TW] AND (tibia*[TW] OR fibula*[TW])))) AND (publisher[sb])))) A
AND (systematic[sb] – (8) – 5 uniek
AND ((Therapy/Broad[filter]) – (9) – 3 uniek |
|
