Transcraniële stimulatie
Uitgangsvraag
Wat is de aanbevolen strategie voor het toepassen van transcraniële stimulatie bij de behandeling van neuropathische pijn bij volwassenen met een dwarslaesie?
Aanbeveling
Er is bewijs van lage kwaliteit dat aanwijzingen geeft voor de mogelijke effectiviteit van transcraniële stimulatie voor de behandeling van neuropathische pijn bij volwassenen met een dwarslaesie. Echter, door het ontbreken van ervaring en beschikbaarheid in Nederland, kan deze behandeling momenteel niet worden aanbevolen dan wel ontraden voor deze indicatie.
De werkgroep is van mening dat transcraniële stimulatie voor deze indicatie daarom enkel kan worden overwogen in studieverband.
Overwegingen
Balans tussen gewenste en ongewenste effecten
Er is een literatuuronderzoek verricht naar de effectiviteit van transcraniële stimulatie voor de behandeling van neuropathische pijn bij volwassenen met een dwarslaesie. In totaal zijn er één systematische review en één RCT gevonden die transcraniële stimulatie hebben onderzocht bij volwassenen met een dwarslaesie en neuropathische pijn. De cruciale uitkomstmaat pijn (direct gemeten nadat de interventie was afgerond) werd gerapporteerd door alle geïncludeerde studies. Daarnaast rapporteerden zes studies – geïncludeerd in de systematische review – de uitkomstmaat pijn, gemeten na follow-up (variërend van 16 dagen tot 3 maanden). Beide resultaten werden beoordeeld als klinisch relevant in het voordeel van transcraniële stimulatie ten opzichte van schijnbehandeling. Dit betekent dat transcraniële stimulatie neuropathische pijn zou kunnen verminderen bij volwassenen met een dwarslaesie, wanneer dit wordt vergeleken met schijnbehandeling. De cruciale uitkomstmaat complicaties en belangrijke uitkomstmaten kwaliteit van leven en participatie werden niet gerapporteerd.
Transcraniële stimulatie is op dit moment geen standaard aangeboden of beschikbare zorg in Nederland voor volwassenen met een dwarslaesie en neuropathische pijn. In Nederland valt repetitieve transcraniële magnetische stimulatie (rTMS) momenteel enkel onder vergoede zorg voor personen met een depressie in specialistische centra. Daarnaast wordt het in onderzoeksverband toegepast bij mensen met obsessief-compulsieve stoornis en bipolaire stoornis, en bij mensen met functieverlies van hun arm/hand ten gevolge van CVA. In de richtlijn 'Depressie' wordt beschreven dat de behandeling met rTMS tijdsintensief is, maar daarentegen weinig bijwerkingen heeft. In de richtlijn ‘Complex regionaal pijn syndroom type 1 (CRPS-1)’ staat dat rTMS kan worden overwogen in studieverband.
The safety of TMS-consensusgroup (Rossi, 2021) formuleerde veiligheidsrichtlijnen voor transcraniële magnetische stimulatie (TMS). De richtlijnen schrijven voor dat TMS niet dient te worden uitgevoerd bij mensen met epilepsie in de voorgeschiedenis, metalen voorwerpen in het hoofd of een cochleair implantaat (relatieve contra-indicaties). Dit rapport rapporteert ook complicaties: bij een gering aantal participanten (2-4 op de 100) kan een lichte hoofdpijn optreden, meestal van korte duur en voorbijgaande aard, en goed te behandelen met bijvoorbeeld paracetamol. In uitzonderlijke gevallen (3-5 op de 1000) kan er zware hoofdpijn optreden. Een zeer zeldzame bijwerking van TMS is een epileptische aanval (0.003%).
Kwaliteit van bewijs
De overall kwaliteit van bewijs is laag. Dit betekent dat we onzeker zijn over het gevonden geschatte effect van de cruciale uitkomstmaten. Er is afgewaardeerd vanwege:
- Risk of Bias: methodologische beperkingen (ontbrekende informatie over het proces van toewijzing en blindering)
- Imprecisie: onnauwkeurigheid, omdat het betrouwbaarheidsinterval de grens van klinische relevantie overschrijdt, en de brede betrouwbaarheidsintervallen van de individuele studies.
Waarden en voorkeuren van volwassenen met een dwarslaesie en neuropathische pijn
rTMS kan belastend zijn vanwege frequente bezoeken (dagelijks, 5-10 dagen op een rij) aan het centrum waar de behandeling wordt uitgevoerd. De gerapporteerde bijwerkingen zijn minimaal (Rossi, 2021).
Kostenaspecten
De werkgroep is niet bekend met resultaten over kosteneffectiviteit van transcraniële stimulatie in de Nederlandse situatie.
Gelijkheid ((health) equity/equitable)
Transcraniële stimulatie is momenteel geen aangeboden behandeling in Nederland voor volwassenen met een dwarslaesie en neuropathische pijn, en wordt dus ook niet vergoed. Aangezien de behandeling momenteel niet wordt toegepast, kan de werkgroep geen uitspraak doen over mogelijke gevolgen betreffende gezondheids(on)gelijkheid.
Aanvaardbaarheid
Ethische aanvaardbaarheid
Aangezien de behandeling momenteel niet wordt toegepast in Nederland voor deze indicatie, kan de werkgroep hier geen uitspraak over doen.
Duurzaamheid
Bij de interventie spelen duurzaamheidsaspecten een rol, omdat volwassenen met een dwarslaesie mogelijk gemotoriseerd vervoer nodig hebben naar de plek van de behandeling.
Haalbaarheid
Transcraniële stimulatie wordt momenteel niet toegepast in Nederland voor de behandeling van neuropathische pijn bij volwassenen met een dwarslaesie. Er is geen ervaring onder zorgverleners met de behandeling voor deze indicatie, en er is geen apparatuur goedgekeurd voor gebruik hiervoor. Bovendien ontbreken onderzoeksresultaten in een Nederlandse setting. Dit maakt de haalbaarheid van implementatie onzeker. Verdere studies zijn nodig om de effectiviteit en veiligheid in Nederland te evalueren.
Rationale van de aanbeveling: weging van argumenten voor en tegen de interventie
In Nederland is ten tijde van het opstellen van deze richtlijn, geen ervaring met de toepassing van transcraniële stimulatie voor volwassenen met een dwarslaesie. Daarnaast lijkt de behandeling zeer intensief qua tijdsinvestering en personele inzet. Er is wel evidentie van lage kwaliteit voor mogelijke effectiviteit van repetitieve transcraniële magnetische stimulatie (rTMS) voor neuropathische pijn bij een dwarslaesie. De gerapporteerde bijwerkingen zijn over het algemeen mild. Daarom ziet de werkgroep reden voor toekomstig wetenschappelijk onderzoek naar de meerwaarde van transcraniële stimulatie voor de behandeling van neuropathische pijn bij volwassenen met een dwarslaesie.
Eindoordeel: Neutrale aanbeveling.
Onderbouwing
Neuropathic pain in individuals with spinal cord injury (SCI) leads to disrupted pain modulation in both the central and peripheral nervous systems. Research shows that neuropathic pain following SCI is associated with functional reorganization of central nervous system activity and hyperexcitability of the somatosensory and motor cortex. Non-invasive transcranial stimulation, such as repetitive transcranial magnetic stimulation (rTMS) and transcranial direct current stimulation (TDCS) are forms of neuromodulation that target the central component of neuropathic pain. These methods have shown potential for reducing neuropathic pain, but their application in practice remains limited.
Summary of Findings table: Transcranial stimulation compared to any other intervention for neuropathic pain in people with spinal cord injury
Population: Adults with SCI and neuropathic pain at or below lesion level
Intervention: Transcranial stimulation
Comparator: No transcranial stimulation, any other type of transcranial stimulation, or any other intervention
|
Outcome |
Study results and measurements |
Absolute effect estimates |
Certainty of the Evidence (Quality of evidence) |
Summary |
||
|
Any other intervention |
Transcranial stimulation |
|||||
|
Pain Post-intervention (critical) |
Measured by NRS and VAS. Based on data from 207 participants in 9 studies. |
(Mean) - |
(Mean) - |
Low Due to serious risk of bias*, Due to serious imprecision1 |
Transcranial stimulation may reduce pain post-intervention when compared with sham treatment in adults with SCI and neuropathic pain.
(Li, 2022; Kim, 2023) |
|
|
Difference: MD 1.35 lower (CI 95% 2.06 fewer – 0.64 fewer) |
||||||
|
Pain At follow-up (critical) |
Measured by NRS and VAS. Based on data from 110 participants in 6 studies. |
(Mean) - |
(Mean) - |
Low Due to serious risk of bias*, Due to serious imprecision2 |
Transcranial stimulation may reduce pain at follow-up when compared with sham treatment in adults with SCI and neuropathic pain.
(Li, 2022) |
|
|
Difference: MD 1.34 lower (CI 95% 2.46 fewer – 0.21 fewer) |
||||||
|
Complications (critical)
|
- |
- |
No GRADE (no evidence was found) |
No evidence was found regarding the effect of transcranial stimulation on complications when compared with no transcranial stimulation, any other type of transcranial stimulation or any other intervention in adults with SCI and neuropathic pain. |
||
|
Quality of life (important)
|
- |
- |
No GRADE (no evidence was found) |
No evidence was found regarding the effect of transcranial stimulation on quality of life when compared with no transcranial stimulation, any other type of transcranial stimulation or any other intervention in adults with SCI and neuropathic pain. |
||
|
Participation (important) |
- |
- |
No GRADE (no evidence was found) |
No evidence was found regarding the effect of transcranial stimulation on participation when compared with no transcranial stimulation, any other type of transcranial stimulation or any other intervention in adults with SCI and neuropathic pain. |
||
1. Risk of Bias: serious. Due to missing information about the allocation and blinding procedure. Imprecision: serious. Due to overlap of confidence interval with border of clinical relevance.
2. Risk of Bias: serious. Due to missing information about the allocation and blinding procedure. Imprecision: serious. Due to overlap of confidence interval with border of clinical relevance.
*For further details, see risk of bias table in the appendix
Description of studies
A total of two studies (one systematic review and one RCT) were included in the analysis of the literature. Important study characteristics and results are summarized in table 1. The assessment of the risk of bias is summarized in the risk of bias tables (under the tab ‘Evidence tabellen’).
Kim (2023) performed an RCT to compare the effects of intermittent theta burst stimulation (iTBS) and high-frequency repetitive transcranial magnetic stimulation (rTMS) on SCI-related neuropathic pain. Adults with neuropathic pain who had been undergoing treatment for SCI were included if: 1) they got diagnosed with SCI according to Korean Standard Classification of Diseases (KCD-8, 2021), 2) diagnosis of central neuropathic pain was made using the Neuropathic Pain Special Interest Group guidelines, and 3) self-completed Leeds Assessment of Neuropathic Symptoms and Signs (S-LANSS) score was ≥12. People were excluded if they had any cognitive deficits that might inhibit comprehension of the evaluation scales, headache, metallic body implant, musculoskeletal pain or lesions in the area of neuropathic pain, pregnancy, or a history of epileptic seizures. Participants were randomly assigned to one of the three groups: real iTBS (n=11), real rTMS (n=11), or sham rTMS (n=11). The iTBS protocol comprised bursts incorporating three pulses (60 ms) at 50 Hz and a 5 Hz TBS train lasting 2s repeated every 10s for a total of 200s (total 600 stimuli) at an intensity of 80% active motor threshold (aMT). The rTMS protocol comprised a total of 2000 pulses of 10 Hz at an intensity of 80% resting motor threshold (rMT). Each train was composed of 8s stimulations (80 stimuli), and a total of 25 trains with 10s intertrain intervals were provided. The sham-rTMS was applied by tilting the coil 90 degrees to the scalp. Participants underwent one assigned stimulation session daily for five days. The outcome measure pain (NRS) was evaluated post-treatment. Additional study characteristics can be found in Table 2.
Li (2022) aimed to evaluate the effect of non-invasive brain stimulation (NIBS) on neuropathic pain after SCI. Four international databases (PubMed, Embase, Cochrane Library, Web of Science) and four Chinese databases (Chinese National Knowledge Infrastructure, VIP database, Wanfang database, Chinese Biomedical Database) were searched from inception to September 2021. Studies that meet the following criteria included: 1) study participants included individuals with neuropathic pain after SCI, 2) intervention included NIBS, including tDCS and rTMS, 3) the control group received sham-NIBS, 4) primary outcome include VAS or NRS, and 5) study design was RCT. The Cochrane risk of bias tool for assessing risk of bias in randomized trials and Physiotherapy Evidence Database were used for quality assessment. The study included 17 RCTs with a total of 466 subjects with SCI and neuropathic pain. Eventually, 8 out of 17 studies were included in the current literature analysis, and 9 studies were excluded because they used a crossover design (n=3) or had no available English full text (n=6). Characteristics of the included studies are displayed in Table 1.
Table 1. Characteristics of included studies in systematic review Li (2022)
Table 2. Characteristics of individual included studies
|
Study |
Participants (number, age, other important characteristics) |
Interventions |
Intervention length |
Outcome measures |
Comments |
Risk of bias (per outcome measure)* |
|
Kim, 2023 RCT, Korea |
N at baseline iTBS: 11 rTMS: 10 Sham: 11
Age (mean, SD) iTBS: 61.3 (13.6) years rTMS: 60.1 (9.4) years Sham: 58.3 (20.1) years
Sex (% female) iTBS: 18.2% rTMS: 10.0% Sham: 18.2%
Duration of pain (mean, SD) iTBS: 50.6 (26.5) days rTMS: 53.3 (27.8) days Sham: 51.6 (24.4) days
Mean S-LANSS (SD) iTBS: 16.8 (1.7) rTMS: 16.6 (2.5) Sham: 16.5 (1.5) |
iTBS: three pulses (60 ms) at 50 Hz and a 5 Hz TBS train lasting 2s repeated every 10s for a total of 200s (total 600 stimuli) at an intensity of 80% aMT.
rTMS: 2000 pulses of 10 Hz at an intensity of 80% rMT. Each train was composed of 8s stimulations (80 stimuli), and a total of 25 trains with 10s intertrain intervals were provided.
Sham: sham-rTMS was applied by tilting the coil 90 degrees to the scalp. |
1/day for 5 days |
Pain (NRS) |
The authors reported there is no funding. The authors declare no conflict of interest. |
Low |
|
Abbreviations: aMT = active motor threshold; iTBS = intermittent theta burst stimulation; LANSS = leeds assessment of neuropathic symptoms and signs; NRS = numeric rating scale; RCT = randomized controlled trial; rMT = resting motor threshold; rTMS = repetitive transcranial magnetic stimulation; SD = standard deviation. *For further details, see risk of bias table in the appendix |
||||||
Results
1. Pain
Post-intervention
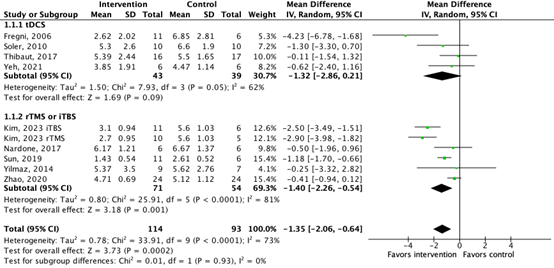
Eight studies included in Li (2022) and Kim (2023) reported on the outcome measure pain assessed by using NRS or VAS (range: 0-10) immediately post-intervention (treatment duration range: 5 days - 6 weeks). Higher scores on both scales indicate higher pain severity.
The pooled data show a mean difference of -1.35 (95%CI -2.06 to -0.64) in favor of transcranial stimulation (Figure 1). This difference is considered clinically relevant.
Figure 1. The effect of transcranial stimulation on pain (VAS, NRS) immediately post-intervention
Z: p-value of the pooled effect; df: degrees of freedom; I2: statistic heterogeneity; CI: confidence interval
At follow-up
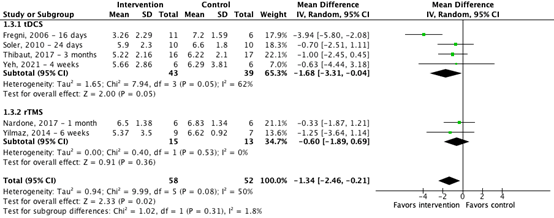
Additionally, six studies included in Li (2022) reported on pain assessed by using NRS or VAS (range: 0-10) at follow-up (range: 16 days – 3 months). The pooled data show a mean difference of -1.34 (95%CI -2.46 to -0.21) in favor of transcranial stimulation (Figure 2). This difference is considered clinically relevant.
Figure 2. The effect of transcranial stimulation on pain (VAS, NRS) at follow-up (16 days-3 months)
Z: p-value of the pooled effect; df: degrees of freedom; I2: statistic heterogeneity; CI: confidence interval
2. Complications, 3. Quality of life, 4. Participation
None of the studies reported on the outcome measures complications, quality of life, and participation.
A systematic review of the literature was performed to answer the following question:
What are the benefits and risks of transcranial stimulation in adults with spinal cord injury and neuropathic pain?
| Patients | Adults with spinal cord injury and neuropathic pain at or below lesion level |
| Intervention | Transcranial stimulation |
| Control | No transcranial stimulation, any other type of transcranial stimulation, or any other intervention |
| Outcomes | Pain, complications, participation, quality of life |
| Other selection criteria | Study design: Study design: systematic reviews, randomized controlled trials or other comparative studies |
Relevant outcome measures
The guideline panel considered pain and complications as critical outcome measures for decision making, and participation and quality of life as important outcome measures for decision making.
The guideline panel defined that the outcome measure pain preferably had to be assessed with the visual analogue scale (VAS), numeric rating scale (NRS) or neuropathic pain scale (NPS). The guideline panel did not define the other outcome measures listed above but used the definitions used in the studies.
The guideline panel defined 25% (0.8 ≥ RR ≥ 1.25) for dichotomous outcomes, 0.5 SD for continuous outcomes and standardized mean difference (0.5 ≥ SMD ≥ 0.5) as minimal clinically (patient) important differences.
Search and select (Methods)
The databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms until 8 November 2024. The detailed search strategy is listed under the tab ‘Literature search strategy’. The systematic literature search resulted in 135 hits. Studies were selected based on the following criteria:
- Systematic reviews (searched in two databases, detailed search strategy with search date, clear description of in- and exclusion criteria, table with excluded studies, evidence table for included studies, risk of bias assessment performed), randomized controlled trials (RCT) or other comparative studies;
- Studies had to assess the outcome measure pain to be eligible;
- Full-text English language publication;
- Studies according to the PICO.
Thirty studies were initially selected based on title and abstract screening. After reading the full text, 28 studies were excluded (see the exclusion table under the tab ‘Evidence tabellen’), and two studies were included.
- Kim JK, You J, Son S, Suh I, Lim JY. Comparison of intermittent theta burst stimulation and high-frequency repetitive transcranial magnetic stimulation on spinal cord injury-related neuropathic pain: A sham-controlled study. J Spinal Cord Med. 2023 Nov 20:1-7. doi: 10.1080/10790268.2023.2277964. Epub ahead of print. PMID: 37982995.
- Li L, Huang H, Yu Y, Jia Y, Liu Z, Shi X, Wang F, Zhang T. Non-invasive Brain Stimulation for Neuropathic Pain After Spinal Cord Injury: A Systematic Review and Network Meta-Analysis. Front Neurosci. 2022 Feb 11;15:800560. doi: 10.3389/fnins.2021.800560. PMID: 35221889; PMCID: PMC8873374.
- Rossi S, Antal A, Bestmann S, Bikson M, Brewer C, Brockmöller J, Carpenter LL, Cincotta M, Chen R, Daskalakis JD, Di Lazzaro V, Fox MD, George MS, Gilbert D, Kimiskidis VK, Koch G, Ilmoniemi RJ, Lefaucheur JP, Leocani L, Lisanby SH, Miniussi C, Padberg F, Pascual-Leone A, Paulus W, Peterchev AV, Quartarone A, Rotenberg A, Rothwell J, Rossini PM, Santarnecchi E, Shafi MM, Siebner HR, Ugawa Y, Wassermann EM, Zangen A, Ziemann U, Hallett M; basis of this article began with a Consensus Statement from the IFCN Workshop on "Present, Future of TMS: Safety, Ethical Guidelines", Siena, October 17-20, 2018, updating through April 2020. Safety and recommendations for TMS use in healthy subjects and patient populations, with updates on training, ethical and regulatory issues: Expert Guidelines. Clin Neurophysiol. 2021 Jan;132(1):269-306. doi: 10.1016/j.clinph.2020.10.003. Epub 2020 Oct 24. PMID: 33243615; PMCID: PMC9094636.
- Stichting hersenstimulatie (z.d.). Onderzoek voor patiënten. Geraadpleegd op 20 februari 2025, van https://www.hersenstimulatie.com/kopie-van-klinische-toepassing.
- Xi M, Shen X, Guliyeva K, Hancock-Howard R, Coyte PC, Chan BCF. Cost-utility analysis of transcranial direct current stimulation therapy with and without virtual illusion for neuropathic pain for adults with spinal cord injury in Canada. J Spinal Cord Med. 2021;44(sup1):S159-S172. doi: 10.1080/10790268.2021.1961051. PMID: 34779737; PMCID: PMC8604475.
Risk of Bias
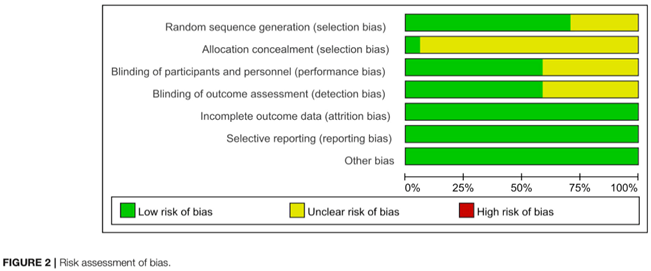
For further details about the risk of bias assessment of the studies included in Li (2022), see https://www.frontiersin.org/journals/neuroscience/articles/10.3389/fnins.2021.800560/full#h12. For this module, we focus on the quality assessment performed by using the Cochrane risk of bias tool (see figure below).
|
Study reference
(first author, publication year) |
Was the allocation sequence adequately generated?
Definitely yes Probably yes Probably no Definitely no |
Was the allocation adequately concealed?
Definitely yes Probably yes Probably no Definitely no |
Blinding: Was knowledge of the allocated interventions adequately prevented? Were patients, healthcare providers, data collectors, outcome assessors, data analysts blinded?
Definitely yes Probably yes Probably no Definitely no |
Was loss to follow-up (missing outcome data) infrequent?
Definitely yes Probably yes Probably no Definitely no |
Are reports of the study free of selective outcome reporting?
Definitely yes Probably yes Probably no Definitely no |
Was the study apparently free of other problems that could put it at a risk of bias?
Definitely yes Probably yes Probably no Definitely no |
Overall risk of bias If applicable/necessary, per outcome measure
LOW Some concerns HIGH
|
|
Kim, 2023 |
Definitely yes
Reason: Computer-generated randomization was used. |
Definitely yes
Reason: Opaque envelopes were used. |
Definitely yes
Reason: Double-blinded trial, only one of the investigators had knowledge of patient allocation and conducted the assigned stimulation. |
Definitely yes
Reason: Only one participant in the rTMS group discontinued the intervention |
Definitely yes
Reason: Trial is registered (KCT0004976). Primary outcomes are reported as specified beforehand. |
Definitely yes
Reason: Nothing reported. |
Low |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Allison DJ, Ahrens J, Mirkowski M, Mehta S, Loh E. The effect of neuropathic pain treatments on pain interference following spinal cord injury: A systematic review. J Spinal Cord Med. 2024 Jul;47(4):465-476. doi: 10.1080/10790268.2023.2218186. Epub 2023 Jul 10. PMID: 37428448; PMCID: PMC11218591. |
Includes only 3-4 studies on transcranial stimulation, also includes non-randomized studies. |
|
Defrin R, Grunhaus L, Zamir D, Zeilig G. The effect of a series of repetitive transcranial magnetic stimulations of the motor cortex on central pain after spinal cord injury. Arch Phys Med Rehabil. 2007 Dec;88(12):1574-80. doi: 10.1016/j.apmr.2007.07.025. PMID: 18047871. |
No absolute VAS data is presented, small study population (n=5 per arm), unclear whether participants have neuropathic pain. |
|
Fregni F, Boggio PS, Lima MC, Ferreira MJ, Wagner T, Rigonatti SP, Castro AW, Souza DR, Riberto M, Freedman SD, Nitsche MA, Pascual-Leone A. A sham-controlled, phase II trial of transcranial direct current stimulation for the treatment of central pain in traumatic spinal cord injury. Pain. 2006 May;122(1-2):197-209. doi: 10.1016/j.pain.2006.02.023. Epub 2006 Mar 27. PMID: 16564618. |
Included in Li (2022) |
|
Galhardoni R, Aparecida da Silva V, García-Larrea L, Dale C, Baptista AF, Barbosa LM, Menezes LMB, de Siqueira SRDT, Valério F, Rosi J Jr, de Lima Rodrigues AL, Reis Mendes Fernandes DT, Lorencini Selingardi PM, Marcolin MA, Duran FLS, Ono CR, Lucato LT, Fernandes AMBL, da Silva FEF, Yeng LT, Brunoni AR, Buchpiguel CA, Teixeira MJ, Ciampi de Andrade D. Insular and anterior cingulate cortex deep stimulation for central neuropathic pain: Disassembling the percept of pain. Neurology. 2019 Apr 30;92(18):e2165-e2175. doi: 10.1212/WNL.0000000000007396. Epub 2019 Apr 5. PMID: 30952795. |
Wrong population (patients with central neuropathic pain after stroke or SCI), no subgroup analysis available. |
|
Gao F, Chu H, Li J, Yang M, DU L, Li J, Chen L, Yang D, Zhang H, Chan C. Repetitive transcranial magnetic stimulation for pain after spinal cord injury: a systematic review and meta-analysis. J Neurosurg Sci. 2017 Oct;61(5):514-522. doi: 10.23736/S0390-5616.16.03809-1. Epub 2016 Sep 7. PMID: 27603408. |
Full-text not available |
|
Gatzinsky K, Bergh C, Liljegren A, Silander H, Samuelsson J, Svanberg T, Samuelsson O. Repetitive transcranial magnetic stimulation of the primary motor cortex in management of chronic neuropathic pain: a systematic review. Scand J Pain. 2020 Sep 7;21(1):8-21. doi: 10.1515/sjpain-2020-0054. PMID: 32892189. |
Less recent and complete compared to Li (2022). |
|
Jiang X, Yan W, Wan R, Lin Y, Zhu X, Song G, Zheng K, Wang Y, Wang X. Effects of repetitive transcranial magnetic stimulation on neuropathic pain: A systematic review and meta-analysis. Neurosci Biobehav Rev. 2022 Jan;132:130-141. doi: 10.1016/j.neubiorev.2021.11.037. Epub 2021 Nov 24. PMID: 34826512. |
Unclear which studies are in participants with SCI. Less recent compared to Li (2022). |
|
Jin L, Wang H, Dong Y, Chen Q, Li L, Li Y. Choosing the optimal target area for repeated transcranial magnetic stimulation in treating neuropathic pain in spinal cord injury patients: a comparative analysis. Front Neurol. 2024 Mar 27;15:1370420. doi: 10.3389/fneur.2024.1370420. PMID: 38601340; PMCID: PMC11004227. |
No raw data is presented; results are not useful. |
|
Koukoulithras I, Alkhazi A, Gkampenis A, Stamouli A, Plexousakis M, Drousia G, Xanthi E, Roussos C, Kolokotsios S. A Systematic Review of the Interventions for Management of Pain in Patients After Spinal Cord Injury. Cureus. 2023 Jul 29;15(7):e42657. doi: 10.7759/cureus.42657. PMID: 37644939; PMCID: PMC10461890. |
No meta-analysis, no subgroup analysis for TCS. |
|
Mehta S, McIntyre A, Guy S, Teasell RW, Loh E. Effectiveness of transcranial direct current stimulation for the management of neuropathic pain after spinal cord injury: a meta-analysis. Spinal Cord. 2015 Nov;53(11):780-5. doi: 10.1038/sc.2015.118. Epub 2015 Jul 21. PMID: 26193817. |
Less recent and complete compared to Li (2022); studied the effectiveness of tDCS alone (instead of tDCS and rTMS in Li). |
|
Nardone R, Höller Y, Langthaler PB, Lochner P, Golaszewski S, Schwenker K, Brigo F, Trinka E. rTMS of the prefrontal cortex has analgesic effects on neuropathic pain in subjects with spinal cord injury. Spinal Cord. 2017 Jan;55(1):20-25. doi: 10.1038/sc.2016.87. Epub 2016 May 31. PMID: 27241450. |
Included in Li (2022) |
|
Ngernyam N, Jensen MP, Arayawichanon P, Auvichayapat N, Tiamkao S, Janjarasjitt S, Punjaruk W, Amatachaya A, Aree-uea B, Auvichayapat P. The effects of transcranial direct current stimulation in patients with neuropathic pain from spinal cord injury. Clin Neurophysiol. 2015 Feb;126(2):382-90. doi: 10.1016/j.clinph.2014.05.034. Epub 2014 Jun 21. PMID: 25027640. |
Included in Li (2022) |
|
Prévinaire JG, Nguyen JP, Perrouin-Verbe B, Fattal C. Chronic neuropathic pain in spinal cord injury: efficiency of deep brain and motor cortex stimulation therapies for neuropathic pain in spinal cord injury patients. Ann Phys Rehabil Med. 2009 Mar;52(2):188-93. doi: 10.1016/j.rehab.2008.12.002. Epub 2009 Jan 22. PMID: 19909709. |
Descriptive review of insufficient quality |
|
Quesada C, Pommier B, Fauchon C, Bradley C, Créac'h C, Vassal F, Peyron R. Robot-Guided Neuronavigated Repetitive Transcranial Magnetic Stimulation (rTMS) in Central Neuropathic Pain. Arch Phys Med Rehabil. 2018 Nov;99(11):2203-2215.e1. doi: 10.1016/j.apmr.2018.04.013. Epub 2018 May 9. PMID: 29750900. |
Non-randomized design |
|
Saleh C, Ilia TS, Jaszczuk P, Hund-Georgiadis M, Walter A. Is transcranial magnetic stimulation as treatment for neuropathic pain in patients with spinal cord injury efficient? A systematic review. Neurol Sci. 2022 May;43(5):3007-3018. doi: 10.1007/s10072-022-05978-0. Epub 2022 Mar 3. PMID: 35239053. |
Less recent and complete compared to Li (2022); studied the effectiveness of TMS alone (instead of TMS and tDCS in Li). |
|
Shen Z, Li Z, Ke J, He C, Liu Z, Zhang D, Zhang Z, Li A, Yang S, Li X, Li R, Zhao K, Ruan Q, Du H, Guo L, Yin F. Effect of non-invasive brain stimulation on neuropathic pain following spinal cord injury: A systematic review and meta-analysis. Medicine (Baltimore). 2020 Aug 21;99(34):e21507. doi: 10.1097/MD.0000000000021507. PMID: 32846761; PMCID: PMC7447445. |
Less recent and complete compared to Li (2022), includes non-randomized, comparative studies. |
|
Soler MD, Kumru H, Pelayo R, Vidal J, Tormos JM, Fregni F, Navarro X, Pascual-Leone A. Effectiveness of transcranial direct current stimulation and visual illusion on neuropathic pain in spinal cord injury. Brain. 2010 Sep;133(9):2565-77. doi: 10.1093/brain/awq184. Epub 2010 Aug 4. PMID: 20685806; PMCID: PMC2929331. |
Included in Li (2022) |
|
Soler D, Moriña D, Kumru H, Vidal J, Navarro X. Transcranial Direct Current Stimulation and Visual Illusion Effect According to Sensory Phenotypes in Patients With Spinal Cord Injury and Neuropathic Pain. J Pain. 2021 Jan;22(1):86-96. doi: 10.1016/j.jpain.2020.06.004. Epub 2020 Jul 3. PMID: 32629032. |
Non-randomized design, unclear what type of intervention the control group received. |
|
Sun X, Long H, Zhao C, Duan Q, Zhu H, Chen C, Sun W, Ju F, Sun X, Zhao Y, Xue B, Tian F, Mou X, Yuan H. Analgesia-enhancing effects of repetitive transcranial magnetic stimulation on neuropathic pain after spinal cord injury:An fNIRS study. Restor Neurol Neurosci. 2019;37(5):497-507. doi: 10.3233/RNN-190934. PMID: 31381538. |
Included in Li (2022) |
|
Thibaut A, Carvalho S, Morse LR, Zafonte R, Fregni F. Delayed pain decrease following M1 tDCS in spinal cord injury: A randomized controlled clinical trial. Neurosci Lett. 2017 Sep 29;658:19-26. doi: 10.1016/j.neulet.2017.08.024. Epub 2017 Aug 16. PMID: 28822837. |
Included in Li (2022) |
|
Wrigley PJ, Gustin SM, McIndoe LN, Chakiath RJ, Henderson LA, Siddall PJ. Longstanding neuropathic pain after spinal cord injury is refractory to transcranial direct current stimulation: a randomized controlled trial. Pain. 2013 Oct;154(10):2178-2184. doi: 10.1016/j.pain.2013.06.045. Epub 2013 Jul 4. PMID: 23831866. |
Included in Li (2022) |
|
Yang C, Bi Y, Hu L, Gong L, Li Z, Zhang N, Wang Q, Li J. Effects of different transcranial magnetic stimulations on neuropathic pain after spinal cord injury. Front Neurol. 2023 Jul 13;14:1141973. doi: 10.3389/fneur.2023.1141973. PMID: 37521294; PMCID: PMC10374342. |
Comparison between transcranial stimulation and a combination. All other included studies compare transcranial stimulation with sham treatment. There is no added value of adding the results of this study for answering the research question. |
|
Yeh NC, Yang YR, Huang SF, Ku PH, Wang RY. Effects of transcranial direct current stimulation followed by exercise on neuropathic pain in chronic spinal cord injury: a double-blinded randomized controlled pilot trial. Spinal Cord. 2021 Jun;59(6):684-692. doi: 10.1038/s41393-020-00560-x. Epub 2020 Oct 6. PMID: 33024299. |
Included in Li (2022) |
|
Yılmaz B, Kesikburun S, Yaşar E, Tan AK. The effect of repetitive transcranial magnetic stimulation on refractory neuropathic pain in spinal cord injury. J Spinal Cord Med. 2014 Jul;37(4):397-400. doi: 10.1179/2045772313Y.0000000172. Epub 2013 Nov 11. PMID: 24621025; PMCID: PMC4116723. |
Included in Li (2022) |
|
Yoon EJ, Kim YK, Kim HR, Kim SE, Lee Y, Shin HI. Transcranial direct current stimulation to lessen neuropathic pain after spinal cord injury: a mechanistic PET study. Neurorehabil Neural Repair. 2014 Mar-Apr;28(3):250-9. doi: 10.1177/1545968313507632. Epub 2013 Nov 8. PMID: 24213958. |
Non-randomized design |
|
Yu B, Qiu H, Li J, Zhong C, Li J. Noninvasive Brain Stimulation Does Not Improve Neuropathic Pain in Individuals With Spinal Cord Injury: Evidence From a Meta-Analysis of 11 Randomized Controlled Trials. Am J Phys Med Rehabil. 2020 Sep;99(9):811-820. doi: 10.1097/PHM.0000000000001421. PMID: 32175926. |
Less recent and complete compared to Li (2022). |
|
Zhang KL, Yuan H, Wu FF, Pu XY, Liu BZ, Li Z, Li KF, Liu H, Yang Y, Wang YY. Analgesic Effect of Noninvasive Brain Stimulation for Neuropathic Pain Patients: A Systematic Review. Pain Ther. 2021 Jun;10(1):315-332. doi: 10.1007/s40122-021-00252-1. Epub 2021 Mar 22. PMID: 33751453; PMCID: PMC8119533. |
Review of insufficient quality, less recent compared to Li (2022). |
|
Zhao CG, Sun W, Ju F, Wang H, Sun XL, Mou X, Yuan H. Analgesic Effects of Directed Repetitive Transcranial Magnetic Stimulation in Acute Neuropathic Pain After Spinal Cord Injury. Pain Med. 2020 Jun 1;21(6):1216-1223. doi: 10.1093/pm/pnz290. PMID: 31722404. |
Included in Li (2022) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 07-10-2025
Beoordeeld op geldigheid : 07-10-2025
Algemene gegevens
De ontwikkeling/herziening van deze richtlijnmodule werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten (www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in oktober 2023 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor volwassenen met een dwarslaesie.
Werkgroep
- Mevr. A. (Anke) Tigchelaar, vertegenwoordiger Dwarslaesie Organisatie Nederland (DON)
- Dhr. A.W.H. (Bram) van Bekkem, vertegenwoordiger DON
- Mevr. C.C.M. (Charlotte) van Laake-Geelen, revalidatiearts, namens de Nederlandse Vereniging van Revalidatieartsen (VRA)
- Mevr. E.H. (Ellen) Roels, revalidatiearts, namens de VRA
- Mevr. I.J.W. (Ilse) van Nes, revalidatiearts, namens de VRA
- Mevr. J. (Janneke) Stolwijk-Swüste (voorzitter), revalidatiearts, namens de VRA
- Mevr. J. (Jolien) Schuttevaar, revalidatiearts, namens de VRA
- Mevr. L. (Lianne) Stevens, fysiotherapeut, namens het Koninklijk Nederlands Genootschap voor Fysiotherapie (KNGF)
- Mevr. L.A. (Poldi) Wilbrink, neuroloog, namens de Nederlandse Vereniging voor Neurologie (NVN)
- Mevr. L.M.M. (Laura) Rustemeijer, GZ-psycholoog, namens het Nederlands Instituut van Psychologen (NIP)
- Dhr. M.W.M. (Marcel) Post, senior-onderzoeker, persoonlijke titel
Met ondersteuning van
- Mevr. I.J. (Ilse) Blokland, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Mevr. L.C. (Laura) van Wijngaarden, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement) hebben gehad. Gedurende de ontwikkeling of herziening van een module worden wijzigingen in belangen aan de voorzitter doorgegeven. De belangenverklaring wordt opnieuw bevestigd tijdens de commentaarfase.
Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Mevr. A. (Anke) Tigchelaar |
Vertegenwoordiger DON |
Geen |
Geen |
Geen restricties |
|
Dhr. A.W.H. (Bram) van Bekkem |
Vertegenwoordiger DON |
Geen |
Geen |
Geen restricties |
|
Mevr. C.C.M. (Charlotte) van Laake-Geelen |
Revalidatiearts, Adelante, Maastricht UMC |
* Medisch afdelingshoofd, Adelante, Maastricht UMC. * Onderzoeker CAPHRI, afdeling revalidatiegeneeskunde, Universiteit Maastricht. |
* ZonMw subsidie Klinische Fellow. Onderwerp: Pijn bij dwarslaesie * ZonMw. Onderzoek naar de impact van chronische pijn bij mensen dwarslaesie en naar nieuwe niet-medicamenteuze behandelmethoden die betrekking hebben op hoe patiënten beter kunnen leren omgaan met chronische pijn. |
Geen restricties |
|
Mevr. E.H. (Ellen) Roels |
Revalidatiearts, UMC Groningen |
* Werkgroep lid ter ontwikkeling dataset Vocational Rehabilitation voor de ISCoS (International Spinal Cord Society). * Betrokkenheid bij (opzetten van) ITB zorg UMCG. * Management activiteiten voor dwarslaesieteam UMCG. |
ZonMw Prevolt studie: Elektrostimulatie ter preventie van decubitus bij dwarslaesie Swasci studie (interne UMCG gelden): lokale onderzoeker Insci studie (gaat uit van Swiss Paraplegic Research) dat in Nederland gecoördineerd wordt door het Erasmus MC; in het protocol voor Nederland van Erasmus MC staat bij Sponsor NA en bij Subsiding party NA. Lokale onderzoeker. |
Geen restricties |
|
Mevr. I.J.W. (Ilse) van Nes |
Revalidatiearts, Sint Maartenskliniek |
* Eindredacteur handboek dwarslaesierevalidatie (betaald). * Lid Scientific Committee ISCoS (onbetaald). * Lid commissie Klinisch Fellows ZonMW (onbetaald). |
* HEMON-NL: onderzoek naar het gebruik van ARC-IM Therapie om hemodynamische instabiliteit na dwarslaesie aan te pakken. Onward Medical, projectleider voor Nijmegen. * Uplift, Onward: Beïnvloeding bloeddrukregulatie en rompcontrole bij volwassenen met een dwarslaesie * Onward: Verbetering van armhandfunctie bij volwassenen met een dwarslaesie |
Geen restricties |
|
Mevr. J. (Janneke) Stolwijk-Swüste (voorzitster) |
Revalidatiearts, De Hoogstraat Revalidatie |
* Onderzoeker, KennisCentrum Revalidatiegeneeskunde Utrecht, De Hoogstraat Revalidatie. * Gastaanstelling, UMC Utrecht, afdeling revalidatie-, fysiotherapiewetenschappen en sport. * Lid scientific and research committee ISCoS (mondiale dwarslaesie vereniging) (2023-heden) (onbetaald). * General member Affiliated Societies and Networks Subcommittee ISCoS (2021-heden) (onbetaald). * Lid redactieraad Nederlands Tijdschrift voor Revalidatiegeneeskunde (2021-heden) (onbetaald). * Medisch adviseur Spina Bifida en Hydrocephalus Nederland (2020-heden) (onbetaald). * Vice voorzitter Nederlands Vlaams Dwarslaesie Genootschap (2018-heden) (onbetaald). * Board member EndParalysis Foundation (2018-heden) (onbetaald). * Lid ISCoS International Spinal Cord Rehabilitation study group (2018-heden) (onbetaald). |
* SKMS/VRA: herziening Nederlandse dwarslaesie database * NIDILRR: duur van uitkomsten van dwarslaesierevalidatie (A Heinemann, SRA Lab, Michigan, US) * ZonMW: coping met chronische pijn na een dwarslaesie (A. van Laake, MUMC+) * De Hoogstraat: pilotstudie naar effect van topicale amitriptyline creme op neuropathische pijn bij dwarslaesie * De Hoogstraat: Reducept (geen subsidiegever): Pijneducatie en –training door middel van Virtual Reality voor volwassenen met een dwarslaesie. Rol als co-promotor. |
Geen restricties |
|
Mevr. J. (Jolien) Schuttevaar |
Revalidatiearts, Revalidatiecentrum Roessingh |
Geen |
* Prevolt studie: elektrostimulatie bij decubitus (geen persoonlijke betrokkenheid, maar Roessingh doet mee als centrum). * Cervit B (promotieonderzoek cervicale ITB van collega E. Maas). |
Geen restricties |
|
Mevr. L. (Lianne) Stevens |
Fysiotherapeut, UMC Groningen |
Geen |
Geen |
Geen restricties |
|
Mevr. L.A. (Poldi) Wilbrink |
Neuroloog, Zuyderland MC |
* Adviesraad Abbvie (betaald). * Adviesraad Teva (betaald). * Richtlijncommissie trigeminus neuralgie (betaald). * Richtlijn hoofdpijn (betaald). *Spreker Biemond Cursus (NVN) (onbetaald). |
Geen |
Geen restricties |
|
Mevr. L.M.M. (Laura) Rustemeijer |
GZ-psycholoog, Rijndam Revalidatie |
Geen |
Geen |
|
|
Dhr. M.W.M. (Marcel) Post |
Senior-onderzoeker, KennisCentrum Revalidatiegeneeskunde Utrecht, De Hoogstraat Revalidatie. |
* Bijzonder hoogleraar dwarslaesierevalidatie, afdeling revalidatiegeneeskunde UMC Groningen. |
* ZonMW: Meting van uitkomsten van revalidatiebehandeling (MUREVAN). Rol als projectleider. * ZonMW: Begeleiding van naasten van volwassenen met een dwarslaesie. Rol als projectleider. * Handicap.NL: Zelfmanagement en eigen regie in de dwarslaesierevalidatie. Rol als projectleider. * SKMS/VRA: Herziening Nederlandse Dwarslaesie Dataset. Nee, Projectleidersrol. * AOSpine: Validering van de AOSpine PROSî vragenlijst bij mensen met een motorisch complete dwarslaesie. Geen projectleidersrol. * N!D!LRR: Duur van uitkomsten van dwars!aesiereva!idatie. Nee, Projectleidersrol. * Swiss Paraplegie Research: Internationale enquête functioneren en kwaliteit van leven van volwassenen met een dwarslaesie. Geen projectleidersrol. * ZonMW: Coping met chronische pijn na een dwarslaesie. Nee, Projectleidersrol. * De Hoogstraat: Pilotstudie naar effect van topicale amitriptyline creme op neuropathische pijn bij dwarslaesie. Geen projectleidersrol. * De Hoogstraat: Reducept (geen subsidiegever): Pijneducatie en –training door middel van Virtual Reality voor volwassenen met een dwarslaesie. Geen projectleidersrol. * Factoren en motieven die voor volwassenen met een dwarslaesie de keuze voor een niet farmacologische behandeling van neuropathische pijn bepalen. Geen projectleidersrol. * In hoeverre de richtlijn Dwarslaesierevalidatie met betrekking tot neuropathische pijn en de WHO standaard voor nociceptieve pijn wordt gevolgd op de klinische dwarslaesie afdeling van De Hoogstraat Revalidatie. Geen projectleidersrol. |
Geen restricties |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door twee afgevaardigden van Dwarslaesie Organisatie Nederland (DON) in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen [(zie kop ‘Waarden en voorkeuren van volwassenen met een dwarslaesie en neuropathische pijn’). De conceptrichtlijn is tevens voor commentaar voorgelegd aan DON en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
| Module |
Uitkomst raming |
Toelichting |
|
Module Transcraniële Stimulatie |
Geen substantiële financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor volwassenen met een dwarslaesie en neuropathische pijn. Tevens zijn er knelpunten aangedragen door Dwarslaesie Organisatie Nederland, Koninklijk Nederlands Genootschap voor Fysiotherapie, Nederlands Instituut van Psychologen, Nederlandse Vereniging Ziekenhuizen, V&VN Pijnverpleegkundigen en de Nederlandse Vereniging Revalidatieartsen via een enquête.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder ‘Zoeken en selecteren’ onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet één op één vergelijkbaar met het minimaal klinisch relevant verschil (Minimal Clinically Important Difference, MCID). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming met betrekking tot de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van volwassenen met een dwarslaesie en neuropathische pijn, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’ en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision framework is een integraal onderdeel van de GRADE methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
|
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers |
||
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, mankracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit.
http://richtlijnendatabase.nl/over_deze_site/over_richtlijnontwikkeling.html
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Algemene informatie
|
Cluster/richtlijn: Neuropathische pijnmodules bij de richtlijn dwarslaesie |
|
|
Uitgangsvraag/modules: UV8 Wat is de aanbevolen strategie voor het toepassen van (non-invasieve) transcraniële stimulatie bij de behandeling van neuropathische pijn voor volwassenen met een dwarslaesie? |
|
|
Database(s): Embase.com, Ovid/Medline |
Datum: 2-11-2024, 3-11-2024 en 8-11-2024 |
|
Periode: n.v.t. |
Talen: geen restrictie |
|
Literatuurspecialist: Eugenie Delvaux |
Rayyan review: |
|
BMI-zoekblokken: voor verschillende opdrachten wordt (deels) gebruik gemaakt van de zoekblokken van BMI-Online https://blocks.bmi-online.nl/ Bij gebruikmaking van een volledig zoekblok zal naar de betreffende link op de website worden verwezen. |
|
|
Toelichting: Voor deze vraag is gezocht met de concepten:
‘Neuropatische pijn’ EN ‘dwarslaesie’ EN ‘transcraniële stimulatie’
Alle referentieartikelen komen uit de search.
Er is géén filter gebruikt voor volwassenen aangezien de aantallen klein zijn.
|
|
|
Te gebruiken voor richtlijntekst: In de databases Embase.com en Ovid/Medline is op systematisch gezocht naar systematische reviews, RCTs en observationele studies over. De literatuurzoekactie leverde 135 unieke treffers op. |
|
Zoekopbrengst
|
|
EMBASE |
OVID/MEDLINE |
Ontdubbeld |
|
SR |
48 |
26 |
50 |
|
RCT |
28 |
60 |
36 |
|
Observationele studies |
94 |
28 |
48 |
|
Totaal |
|
|
135 |
*in Rayyan
Zoekstrategie
Embase.com
|
No. |
Query |
Results |
|
#14 |
#6 AND #11 |
94 |
|
#13 |
#6 AND #9 |
28 |
|
#12 |
#6 AND #7 |
48 |
|
#11 |
#9 OR #10 |
17475948 |
|
#10 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
15515871 |
|
#9 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
8480397 |
|
#8 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
4137761 |
|
#7 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
1075620 |
|
#6 |
#5 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) |
187 |
|
#5 |
#3 AND #4 |
259 |
|
#4 |
'transcranial electrical stimulation'/exp OR 'transcranial magnetic stimulation'/exp OR ((transcran* NEAR/4 stimulation*):ti,ab,kw) OR tdcs:ti,ab,kw OR 'cerebral cortical stimulation':ti,ab,kw OR 'non invasive brain stimulation':ti,ab,kw OR 'intermittent theta burst stimulation':ti,ab,kw OR 'motor cortex stimulation':ti,ab,kw |
53245 |
|
#3 |
#1 AND #2 |
9702 |
|
#2 |
'neuropathic pain'/exp OR 'neuralgia'/exp OR 'allodynia'/exp OR ((pain* NEAR/3 ('neuro pathic' OR neurogenic OR neuropathic OR management OR treatment*)):ti,ab,kw) OR allodynia*:ti,ab,kw OR neuralgia:ti,ab,kw OR (((nerve* OR induced) NEAR/5 pain*):ti,ab,kw) OR neurodynia:ti,ab,kw OR 'chronic pain*':ti,ab,kw |
346468 |
|
#1 |
'spinal cord injury'/exp OR 'spinal cord injury' OR 'paraplegia'/exp OR 'paraplegia' OR 'quadriplegia'/exp OR 'quadriplegia' OR ((('spinal cord' OR spine) NEAR/3 (injur* OR trauma* OR compression OR transection OR transverse OR contusion OR laceration OR hemisection OR lesion* OR damag*)):ti,ab,kw) OR paraparesis:ti,ab,kw OR parapleg*:ti,ab,kw OR quadriparesi*:ti,ab,kw OR 'quadriplegia':ti,ab,kw OR tetraplegia:ti,ab,kw OR 'tetraparesis':ti,ab,kw OR 'tetraplagia':ti,ab,kw OR 'tetraplegia':ti,ab,kw OR (('cental cord' NEAR/3 syndrome*):ti,ab,kw) OR sci:ti,ab,kw |
219205 |
Ovid/Medline
|
# |
Searches |
Results |
|
12 |
6 and 9 |
28 |
|
11 |
6 and 8 |
60 |
|
10 |
6 and 7 |
26 |
|
9 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort*.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ |
4924224 |
|
8 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2801629 |
|
7 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
787786 |
|
6 |
5 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/) |
105 |
|
5 |
3 and 4 |
116 |
|
4 |
exp Transcranial Direct Current Stimulation/ or exp Transcranial Magnetic Stimulation/ or (transcran* adj4 stimulation*).ti,ab,kf. or tdcs.ti,ab,kf. or (('motor cort*' or 'cerebral cort*' or 'non-invasive brain*' or 'intermittent theta burst') adj3 stimulation*).ti,ab,kf. |
34699 |
|
3 |
1 and 2 |
3819 |
|
2 |
exp Neuralgia/ or exp Hyperalgesia/ or exp Pain Management/ or (pain* adj3 (neurogenic or neuropathic or management or treatment*)).ti,ab,kf. or allodynia*.ti,ab,kf. or neuralgia.ti,ab,kf. or ((nerve or induced) adj5 pain*).ti,ab,kf. or neurodynia.ti,ab,kf. |
185982 |
|
1 |
exp Spinal Cord Injuries/ or exp Paraplegia/ or exp Quadriplegia/ or ((('spinal cord' or spine) adj3 (injur* or trauma* or compression or transection or transverse or contusion or laceration or hemisection or lesion* or damag*)) or paraparesis or parapleg* or quadriparesi* or quadriplegia or tetraplegia or tetraparesis or tetraplagia or tetraplegia).ti,ab,kf. or ('central cord' adj3 syndrome*).ti,ab,kf. or sci.ti,ab,kf. |
145477 |