Achtergrond CMN
Uitgangsvraag
Achtergrondinformatie bij Congenitale Melanocytaire Naevi (CMN).
Aanbeveling
Klinisch beeld
CMN zijn vaak groter dan verworven naevi en hebben een meer heterogene morfologie, met vaak donkerdere en wisselende pigmentatie, hypertrichose en soms een verdikt en/of gerimpeld oppervlak. Met name in grotere CMN kunnen tevens noduli (dermaal of subcutaan) in de CMN voorkomen.
CMN veranderen met de leeftijd, met name in de eerste levensjaren. CMN groeien mee met de huid, in elke lichaamsregio (hoofd, romp+armen, benen) volgens een andere groeifactor (1,7~3,4).
Benigne cutane complicaties
In grotere CMN kunnen o.a. proliferatieve noduli (PN’s) aanwezig zijn of ontstaan. Bij PN’s is het onderscheid met melanoom lastig.
Pathogenese
Een enkele postzygotische somatische mutatie in NRAS of BRAF kan aanleiding geven tot CMN. De timing van deze mutatie speelt een rol bij de uitgebreidheid van CMN, zowel cutaan als extracutaan (centraal zenuwstelsel). Hoe vroeger de mutatie in de embryogenese, hoe uitgebreider het beeld.
Onderbouwing
Definities
Congenitale melanocytaire naevi (CMN) zijn benigne melanocytaire proliferaties die aanwezig zijn bij de geboorte of verschijnen in de eerste levensweken tot en met de leeftijd van 3 maanden. Ze kunnen al dan niet samengaan met satellietnaevi (kleinere naevi verspreid over het lichaam) die nog in de loop van de eerste levensjaren kunnen verschijnen. De meeste satellietnaevi zullen op de leeftijd van één jaar zichtbaar zijn, de werkgroep hanteert daarom verschijnen tot één jaar als afkappunt.
Bij de beschrijvingen in deze richtlijn zijn CMN ingedeeld in grootte volgens de classificatie van Krengel et al [Krengel 2013], naar verwachte grootte op volwassen leeftijd (‘projected adult size’, ‘PAS’) [zie ook de module ‘Classificatie van CMN’]:
- kleine CMN <1,5 cm PAS
- middelgrote CMN 1,5-20 cm PAS
- grote CMN >20-40 cm PAS
- reuze CMN >40 cm PAS
Indien in de richtlijn wordt gesproken over kleinere CMN wordt CMN <20cm PAS bedoeld, bij grotere CMN van >20cm PAS. Een exactere indeling is dan vaak niet te geven, omdat in de literatuur verschillende classificaties en afkappunten voor grootte zijn gehanteerd.
CMN kunnen volgens de volgende verdeling voorkomen:
- Solitair (één enkele laesie)
- Een (grotere) ‘moedernaevus’, gepaard gaand met satellietnaevi
- Multipele (≥3) middelgrote CMN (1,5~20cm PAS) verspreid over het lichaam, zónder duidelijke moedernaevus. Deze kunnen al dan niet samengaan met kleine CMN (<1,5 cm PAS). In de richtlijn wordt dit fenotype veelal aangeduid als ‘multipele kleinere CMN’

Fig. 1: CMN fenotypen bij uitgebreidere CMN: links. satellietnaevi bij ‘moedernaevus’, rechts. multipele CMN zónder moedernaevus [bron: oral presentation dr. V. Kinsler]
Bij CMN kan de overmatige aanwezigheid van naevuscellen in de huid ook in het centraal zenuwstelsel voorkomen, omdat in het embryo beide zich uit het ectoderm ontwikkelen. Bij symptomatische betrokkenheid van zowel huid als zenuwstelsel spreekt men van neurocutane melanocytose of soms van neurocutane melanose (NCM).
Klinisch beeld
Presentatie CMN
Congenitale melanocytaire naevi zijn vaak groter dan verworven naevi en hebben een meer heterogene morfologie, met vaak ook sterkere beharing en donkerdere pigmentatie [Lyon 2010]. De meest voorkomende CMN zijn solitair, van kleine of middelgrote grootte. Het typische uiterlijk is een (wisselend) gepigmenteerde bruine plaque, rond tot ovaal van vorm, met goed gedefinieerde randen [Alikhan 2012].
Het uiterlijk van CMN kan sterk variëren, zowel intra- als interindividueel. Er is een spreiding in grootte, aantal en lokalisatie (primaire kenmerken), daarnaast kan de morfologie van CMN sterk variëren qua vorm, begrenzing, kleur, aspect/textuur en beharing (secundaire kenmerken). [Lyon 2010].
Primaire kenmerken
- Grootte: De grootte van een CMN kan enorm variëren, van enkele millimeters tot een reuze CMN die grote delen van het lichaam bedekt. Ook satellietnaevi kunnen van kleine en middelgrote grootte zijn. Hoe groter de naevus hoe zeldzamer. Grootte is een belangrijk kenmerk bij de classificatie van CMN.
- Aantal: CMN kunnen solitair voorkomen als enkele laesie, maar ook multipel. Multipele laesies kunnen elkaar ook soms overlappen (conflueren).Ongeveer 3% van de patiënten heeft meerdere CMN [Alikhan 2012]. Het aantal satellietnaevi kan enorm variëren, van enkele tot incidenteel wel >200. Vaak geldt hoe groter de CMN, hoe meer satellietnaevi, maar dit is geen 1 op 1 verband [Ruiz-Maldonado 1992]. Ongeveer 75% van de patiënten met een grotere CMN heeft satellietnaevi.
- Lokalisatie/verdeling over het lichaam: CMN kunnen op elke locatie op de huid voorkomen, inclusief de behaarde hoofdhuid, voetzolen, handpalmen en nagelapparaat. Ook de mucosa (o.a. mondholte) kan aangedaan zijn. Een speciale en zeldzame vorm en lokalisatie van CMN is de zogenaamde ‘divided naevus’ (‘panda naevus’, ‘kissing naevus’). Deze bevindt zich meestal op de oogleden (boven- en onderooglid), en heel incidenteel op de geslachtsdelen of tussen de vingers.
Secundaire kenmerken
Tot de secundaire kenmerken behoort het morfologisch spectrum van CMN:
- Vorm: CMN zijn meestal rond tot ovaal, met de lange as georiënteerd aan de huidlijnen. Alle vormen zijn echter mogelijk;
- Begrenzing: Randen van een CMN kunnen alle verschijningsvormen hebben, van vaag tot scherp, maar wel voornamelijk scherp begrensd;
- Kleur: Meestal hebben CMN een bruine tot zwarte kleur, alle bruinschakeringen zijn mogelijk. Soms kan een CMN ook iets roze- of roodkleurig zijn, en tinten grijs en blauw komen ook voor. Kleuren kunnen ook binnen en tussen CMN verschillen. In de eerste levensjaren zijn CMN vaak minder sterk gepigmenteerd (soms lijkend op cafe-au-lait maculae). CMN kunnen ook ‘naevus spilus-like’ van karakter zijn (‘NSL-variant’). Men spreekt van deze variant bij een café-au-lait macula met daarin een gespikkeld patroon;
- Aspect/Textuur: Bij de geboorte zijn CMN vaak maculeus, maar later zijn ze vaker verheven en/of hebben een geplooid (rimpelig) oppervlak;
- Noduli en papels: Het oppervlak van een CMN kan bobbelig zijn (‘lumpy and bumpy’) door dermale noduli of papels, en/of noduli die zich subcutaan bevinden. Uitgebreide en of grotere noduli komen niet vaak voor en worden met name gezien bij reuze CMN, daar komen ze ongeveer bij 19% van de patiënten voor [Ruiz-Maldonado 1992]. Deze noduli zijn dan vaak gelokaliseerd op de rug, billen, genitalia of meer zelden op het hoofd [Krengel 2012b];
- Beharing/hypertrichose: CMN <5 cm PAS zijn meestal niet behaard, maar ongeveer 75% van grotere CMN wel. De haarkleur kan alle varianten aannemen, meestal gehyperpigmenteerd, soms hetzelfde als het hoofdhaar van het kind, soms lichter of zelden zelfs zonder pigment (wit/grijs). Ook lagunobeharing kan voorkomen. De haargroei kan zeer dicht zijn, of meer diffuus verspreid over een CMN. Vaak groeien haren in een CMN sneller dan de haren op de rest van het lichaam. CMN op het behaarde hoofd hebben vrijwel altijd hypertrichose [Lyon 2010].
Evolutie
CMN veranderen qua uiterlijk spontaan met toenemen van de leeftijd, met name tijdens de eerste levensjaren.
Bij de geboorte zijn CMN vaak maculeus en bruin, de kleur wordt later vaak donkerder bruin. Verder is er regelmatig vorming van terminale haren (bij grotere CMN), op de hoofdhuid is beharing vaak direct bij de geboorte al aanwezig. Ook verschijnen vaak platte of licht verheven, kleine donkerbruine maculae of papels binnen de moederlaesie. De meeste CMN worden verheven en vormen plaques. In oudere CMN worden dan regelmatig verruceuze veranderingen gezien, en een geplooid uiterlijk. Met name in grotere CMN kunnen zich subcutaan ook grote noduli en papels ontwikkelen. Satellietnaevi kunnen aanwezig zijn of in het eerste levensjaar verschijnen of in aantal toenemen. Verder kunnen als secundaire verschijnselen hyperkeratose, erosies en ulceraties ontwikkelen.
Daarentegen kunnen CMN ook juist spontaan lichter worden (resolutie, regressie). Resolutie van CMN is vaker partieel dan compleet. Enkele studies suggereren dat resolutie bij 17~35% van de CMN optreedt [Dawson 1996, Kinsler 2009II]. Dit fenomeen van resolutie kan optreden bij CMN van alle typen en groottes, complete regressie wordt vaker gezien bij CMN op het hoofd [Ruiz-Maldonado 1992, Strauss 2008]. Resolutie kan zich presenteren als een geleidelijk lichter worden van de naevus. Soms presenteert resolutie zich met het ‘halo fenomeen’, het optreden van een gedepigmenteerde halo rond de naevus [Strauss 2008]. Depigmentatie kan gepaard gaan met dermatitis en/of fibrose in of rondom de naevus [Mundinger 2014, Ruiz-Maldonado 2003].
Groei
Een CMN groeit over het algemeen mee met de huid in proportie met het kind, dus bedekt meestal naar verhouding hetzelfde lichaamsoppervlak als bij de geboorte het geval was. De groeifactor waarmee CMN van geboorte tot volwassen leeftijd groeien is afhankelijk van de lichaamsregio [Krengel 2013, Marghoob 1996]., zie onderstaande tabel.
Tabel 1: groeifactor CMN per lichaamsregio [Krengel 2013]
|
Lichaamsregio |
Groeifactor vanaf geboorte |
Grootte bij geboorte in cm als grote CMN (≥20 cm PAS) |
|
Hoofd |
1,7x |
≥ 12 cm |
|
Romp + armen |
2,8x |
≥ 7 cm |
|
Benen |
3,4x |
≥ 6 cm |
Symptomen
Er is maar weinig bekend over klachten bij CMN, hier is geen goed onderzoek naar gedaan. Empirisch gaat het hebben van (kleinere) CMN in principe niet gepaard met symptomen, als ook niet bij verworven melanocytaire naevi.
Het hebben van een CMN kan wel gepaard gaan met symptomen, zeker bij grotere CMN:
- Kwetsbare huid: de CMN huid is vaak kwetsbaarder dan normale huid, met name bij pasgeborenen. Door wrijving/trauma kan een CMN dus gemakkelijk beschadigen.
- Droge huid: een CMN is vaak droger dan normale huid door een verminderde aanleg van talgklieren en/of zweetklieren (laatste is zelden). Soms kan secundair aan de droge huid hyperkeratose/eczeem ontstaan [Rolland 2009].
- Jeuk: jeuk kan voorkomen bij (grotere) CMN [Price, personal communication]. Dit treedt mogelijk secundair op aan de droge huid, maar er zijn ook aanwijzingen dat zich in de CMN-huid meer mestcellen bevinden die de jeuk zouden kunnen veroorzaken [Salgado 2014].
- Ulceratie/bloeding: in CMN (m.n. in grotere) kunnen erosies of ulceraties optreden, deze kunnen gaan bloeden.
- Verstoorde zweetregulatie: In grotere CMN zijn soms de zweetklieren ter plaatse van de naevus minder goed aangelegd/ontwikkeld dan in normale huid, met name wanneer er subcutane noduli aanwezig zijn. Om toch de lichaamswarmte kwijt te kunnen zullen patiënten via de normale huid soms meer transpireren en zal de huid daar vochtig zijn, terwijl de naevushuid eerder droog blijft. Indien patiënten door het verminderde aantal zweetklieren hun warmte niet kwijt kunnen bestaat er (met name op warme dagen) een kans op oververhitting.
Benigne cutane complicaties
Er kunnen soms benigne cutane complicaties optreden binnen de CMN, met name in grotere. Dit zijn o.a.:
- Hypotrofie/atrofie: In de naevushuid kan het voorkomen dat er minder subcutaan vet aanwezig is ter plaatse van de naevus, hierdoor kan de CMN lager komen te liggen dan de omringende huid, of een extremiteit dunner van omvang zijn.
- Proliferatieve noduli (PN’s): Meestal zijn subcutane noduli in CMN aanwezig vanaf de geboorte dan blijven ze relatief stabiel, maar soms kunnen ze tijdens de kinderjaren ontwikkelen en groeien dan vaak snel (proliferatieve noduli, PN’s). Ze kunnen zacht of hard zijn, variërend van enkele millimeters tot een paar centimeter. Klinisch is het onderscheid met melanoom zeer lastig, het is meestal nodig deze PN’s te verwijderen om maligniteit uit te sluiten.
- Plexiforme overgroeiingen: er kunnen overgroeiingen van naevusweefsel ontstaan, lijkend op plexiforme neurofibromin
Proliferatieve noduli en overgroeiingen lijken voor te komen bij respectievelijk ±20% en 5% van de patiënten met reuze CMN [Ruiz-Maldonado 1992]. Naast bovenstaande zijn andere goedaardige complicaties die kunnen voorkomen o.a. lipoom, hamartoom of cutis verticis gyrata (de laatste bij CMN op het hoofd) [Alikhan 2012].
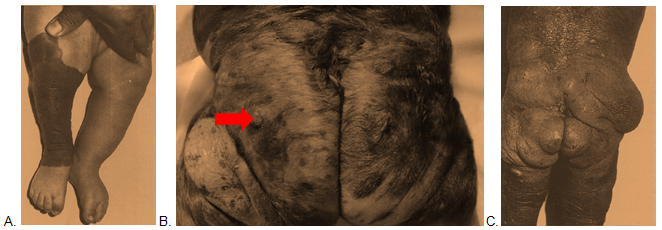
Fig. 2: Benigne complicaties in grotere CMN: A. hypotrofie van een extremiteit B. prolferatieve nodus C. plexiforme neurofibroom-achtige overgroeiing; [bron: Ruiz-Maldonado 1992 J of Pediatrics, Viana 2014 Ann Bras Dermatol]
Differentiaal diagnose
Een congenitale melanocytaire naevus is vrijwel altijd goed te diagnosticeren door de clinicus (zie ook de module ‘Classificatie van CMN’), de differentiaal diagnose is daarmee beperkt.
Op jonge leeftijd kan het soms lastig zijn een CMN van een café-au-lait macula te onderscheiden. De mongolenvlek, naevus van Ota en naevus van Ito kunnen soms iets weg hebben van een CMN, maar bij deze naevi staat de blauwverkleuring duidelijk op de voorgrond. De naevus van Becker kan op een CMN lijken door de hypertrichose, maar is slechts zelden al bij de geboorte aanwezig deze ontstaat meestal pas bij jongvolwassenen. Ook kan het onderscheid met een naevus spilus lastig zijn, daarbij kan een CMN ook ‘naevus spilus-like’ van karakter zijn (‘NSL’-variant, zie ook de paragraaf ‘Klinisch beeld’ ). Verder kunnen complexe/plexiforme neurofibromen op jonge leeftijd klinisch vergelijkbaar zijn.
Epidemiologie
In pasgeborenen varieert de incidentie van CMN van internationale studies van 0,4~2,7%, vrijwel allen van kleine en hoogstens middelgrote grootte [Kanada 2012]. De meeste studies rapporteren een incidentie van kleine CMN rond 1% [Krengel 2008]. Er is één grotere studie (500.000 pasgeborenen) die ook een uitspraak kon doen over de prevalentie van grotere laesies [Castilla 1981]: een ratio van 15:100.000 voor CMN van ≥ 4cm in diameter en 5:100.000 voor CMN van ≥10 cm. Reuze CMN hebben een geschatte incidentie van 1:500.000.
Hamm en Höger publiceerden de volgende getallen als leidraad voor incidentie van [Hamm 2011]:
Tabel 2.: Geschatte incidentie verschillende groottes CMN
|
Classificatie grootte |
Grootte in ‘projected adult size’ |
Geschatte incidentie |
|
Kleine CMN |
<1,5cm |
1:100 |
|
Middelgrote CMN |
1,5-20cm |
1:1000 |
|
Grote CMN |
20-40cm |
1:20.000 |
|
Reuze CMN |
>40cm |
1:500.000 |
CMN komen voor bij alle ethniciteiten en elk huidtype. Er zijn aanwijzingen dat (kleine) CMN vaker voorkomen in kinderen met een donkere huid [Kanada 2012, Laude 1996] en in Aziatische kinderen [Shpall 1994]. Andere studies beweren dat de incidentie onafhankelijk is van huidskleur/huidtype of andere factoren gerelateerd aan ethniciteit [Castilla 1981, Krengel 2008].
In klinische studies wordt vaak gerapporteerd dat CMN vaker voorkomen bij vrouwen dan bij mannen. In de grootste populatiestudie is echter geen verschil gevonden [Castilla 1981].
Pathogenese
Naevi zijn benigne clonale proliferaties van melanocyten. Naevuscellen zijn afkomstig van melanocyten in de neurale lijst, van waaruit ze migreren naar het overliggende ectoderm. Proliferatie, differentiatie en migratie van melanocyten wordt gereguleerd door een complex netwerk van signaalmoleculen. Bij CMN kan alleen de huid zijn aangedaan (zowel epidermis, dermis als het subcutane weefsel kunnen geïnfiltreerd zijn met naevuscellen), of ook het centraal zenuwstelsel.
De pathogenese van CMN is nog niet geheel opgehelderd, maar recent zijn wel belangrijke nieuwe inzichten verschenen.
Kinsler et al. onderzochten en vergeleken in patiënten met multipele CMN meerdere weefsels van zowel huid als centraal zenuwstelsel met elkaar [Kinsler 2013]. Bij 80% werd een NRAS-mutatie gevonden, en bleek in dezelfde patiënten dezélfde mutatie aanwezig in meerdere aangedane gebieden van de huid ÉN het centraal zenuwstelsel (zowel melanocytair als niet-melanocytair), terwijl deze áfwezig was in de niet-aangedane gebieden en in het bloed. Bovenstaande bevindingen wijzen op:
- somatisch mosaïcisme; er is sprake van een lethale mutatie die overleefd door mosaïcisme (theorie van Happle 1987);
- indien er sprake is van zowel betrokkenheid van huid als hersenen, deze mutaties optreden in het zich ontwikkelend neuro-ectoderm vroeg in de embryogenese;
Charbel et al. vonden met ‘whole-exome sequencing’ in grote CMN dat somatische NRAS mutaties voldoende zijn om te zorgen voor melanocytaire proliferatie in utero, er werden geen andere mutaties gevonden naast NRAS [Charbel 2014].
De heersende gedachte is nu dat postzygotisch, vroeg in de embryogenese voorlopercellen van melanocyten een enkele somatische mutatie krijgen, resulterend in een mozaiek patroon van melanocyten die de huid en leptomeningen kunnen coloniseren [van Engen-van Grunsven 2014]. Deze ontstaanswijze is voor NRAS aangetoond in een muismodel [Pedersen 2013].
Waarschijnlijk bepaalt ‘timing’ van de mutatie voor een belangrijk deel hoe uitgebreid een CMN zich presenteert. Een mutatie vroeg in de embryonale ontwikkeling leidt tot wijde verspreiding van naevuscellen naar de huid (reuze CMN en satellieten of enkel multipele CMN) en ook het centraal zenuwstelsel, structuren die beide uit het ectoderm ontstaan. Een mutatie pas laat in de embryogenese geeft kleinere, alleen cutane CMN, in een omschreven gebied, zonder satellieten [Fernandez 2016, oral communication Kinsler]. Zie ook fig. 3.
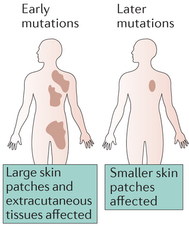
Fig. 3: ‘Timing’ van de postzygotische somatische mutatie bepaalt het fenotype van CMN [Bron: Fernandez 2016 Nature Reviews]
In de meeste studies zijn NRAS (codon 61) of BRAF (V600E) mutaties beschreven in CMN. NRAS en BRAF zijn beide onderdeel van de RAS/RAF/MEK/ERK ‘pathway’, betrokken bij o.a. celgroei, -differentiatie en -overleving. Beide mutaties zijn bekend van melanomen, mogelijk daarom zijn deze ook het meest onderzocht in naevi. Er lijkt een genotype-fenotype correlatie te zijn tussen grootte van CMN en het type mutatie [van Engen-van Grunsven 2014]. Grotere CMN hebben vaker NRAS-mutaties, kleinere naevi zijn minder vaak NRAS gemuteerd en hebben (net als verworden naevi) vaker een BRAF mutatie [Roh 2015]. Van NRAS-mutaties was reeds bekend dat dezelfde mutatie zich in zowel aangedane huid als zenuwweeefsel bevindt [Kinsler 2013], dit blijkt ook te gelden voor incidentele BRAF-mutaties in grotere CMN hoewel dit slechts zelden voorkomt [Salgado 2015].
Niet in alle patiënten kan een NRAS of BRAF mutatie worden gevonden. Eerdere studies beschrijven andere mutaties: in MC1R, TP53, GNAQ [Kinsler 2014]. Mogelijk dat deze de expressie van NRAS/BRAF moduleren, of nog een andere rol spelen in de pathogenese. Er zullen meerdere ‘pathways’ betrokken zijn in de pathogenese van CMN dan nu beschreven of bekend.
Hoe vanuit naevuscellen in de huid en het centraal zenuwstelsel melanoom ontstaat is nog niet opgehelderd. Theoretisch is in CMN een eerste ‘hit’ reeds aanwezig (BRAF/NRAS mutatie), er is nog een tweede ‘hit’ nodig voor het ontstaan van melanoom. Daarvoor zijn additionele ‘driver’ mutaties nodig. Deze theorie is aangetoond voor verworven naevi [Shain 2015]. Welke mutaties dit zijn bij CMN is nog onduidelijk, er wordt o.a. een mogelijke rol toebedacht aan ‘Wnt signaling’ [Pawlikowski 2015, Shakhova 2012].
In recente studies blijkt in in vitro en in muismodellen verder dat de naevuscellen in CMN zowel cutaan als in het centraal zenuwstelsel na de geboorte en tot op latere leeftijd nog verscheidene proliferatieve, klonogene en tumerogene eigenschappen bevatten [Charbel 2015, Basu 2015]. Guégan vergeleken dit tussen middelgrote CMN (1,5~10cm PAS) en grote CMN (20~40cm PAS). De hoeveelheid stamcelachtige cellen lijken per zelfde oppervlakte significant meer aanwezig in grote CMN dan in kleinere CMN [Guégan 2016]. De hypothese hierbij is dat om deze reden in grotere CMN eerder een tweede somatische activatie (‘second hit’) kan optreden die leidt tot melanoom (of mogelijk proliferatieve leptomeningeale melanocytose). Ook is denkbaar dat repigmentatie en de vorming van proliferatieve noduli hier mogelijk verband mee houden.
Verder onderzoek naar zowel de pathogenese van CMN, als van het ontstaan van melanoom uit CMN is nodig.
Histologie
Histologisch gezien is het onderscheid tussen congenitale en verworven naevi lastig, met name met betrekking tot kleine congenitale naevi. Naevi bestaan uit een neoplastische populatie melanocyten, aanwezig in de epidermis en/of dermis. In de epidermis worden veelal nesten en/of lentigineuze verdeelde proliferaties langs het dermo-epidermale grensvlak aangetroffen, terwijl de dermale component vaak bestaat uit nesten en meer verspreid verdeelde cellen, in oppervlakkige delen vaak wat groter en vaker pigment houdend dan in diepere delen [Viana 2013].
In het algemeen kunnen CMN van verworven naevi worden onderscheiden door een grotere omvang en de verspreiding van naevuscellen in diepere lagen van de huid en zelfs de subcutis. Het voorkomen van naevuscellen in talgklieren, zenuwen en bloedvaten diep in de reticulaire dermis is vrijwel bewijzend vor congenitale (i.p.v. verworven) naevus [Mark 1973, Rhodes 1985]. Hoewel deze kenmerken aanwezig kunnen zijn in CMN van alle groottes zijn ze aanzienlijk frequenter in reuze CMN. In grotere CMN reiken naevuscellen bij vrijwel 100% tot in de reticulaire dermis, en bij 75% tot in de subcutis [Barnhill 1995]. In kleine naevi zijn deze karakteristieke kenmerken vaak niet aanwezig, deze bevinden zich ook vaak oppervlakkiger [Magana 2015].
Er doet zich een moeilijkheid voor bij het beoordelen van noduli in CMN. Bij geboorte of in het spontane beloop kunnen in CMN proliferatieve noduli (PN’s) ontstaan. Het is lastig deze (klinisch en) histopathologisch te onderscheiden van melanomen, hetgeen grote consequenties kan hebben. Beide kunnen zich histologisch presenteren met verhoogde mitotische activiteit, nucleaire atypie en zelfs de aanwezigheid van atypische mitosefiguren en van necrose. Er zijn wel enkele kenmerken die bij benigne PN’s vaker lijken voor te komen dan bij melanomen (zoals multifoculiteit) en andersom, maar er zijn geen eenduidige criteria om deze entiteitten van elkaar te onderscheiden [Leech 2004, Yelamos 2015]. De laatste jaren worden moleculaire technieken vaker ingezet om benigne melanocytaire laesies van melanomen te onderscheiden, zoals CGH-array (‘comparative genomic hybridization’) en FISH (‘fluorescence in situ hybridization’). Hierbij geldt in het algemeen dat in PN’s vaker complete ‘copy number gains en ‘losses’ van chromosomen worden gezien, terwijl dit in melanomen (soms naast numerieke afwijkingen) vaak meer complexe structurele en partiële afwijkingen zijn [Yelamos 2015, Bastian 2002].
Familiair voorkomen
CMN ontstaan over het algemeen sporadisch, en komen dan bij slechts één lid in de familie voor. Bij grotere CMN is slechts zeer incidenteel familiaire clustering beschreven. In de Nederlandse studie van de Wijn et al. vonden zij bij 1,7% van patiënten met grote of reuze CMN (2/120) familiair voorkomen [de Wijn 2010]. Zij consulteerden tevens diverse internationale ‘registries’, hier waren destijds geen familiaire gevallen bekend.
Kinsler et al. beschrijven in 301 families met CMN van alle groottes bij 25% van de ouders een positieve familie-anamnese voor CMN van eenzelfde grootte bij tweedegraads familieleden [Kinsler 2009 partI]. Het ging hier over het algemeen om kleinere CMN, zonder satellietnaevi.
Op basis van de de pathogenese van CMN, een postzygotische somatische mutatie in utero, is CMN in principe niet erfelijk. Dit wordt onderstreept doordat er casus bekend zijn van eeneiige tweelingen waarvan slechts één kind is aangedaan [Amir 1982, Cantu 1973, Morganroth 1991].
- Alikhan A, Ibrahimi OA, Eisen DB. Congenital melanocytic nevi: where are we now? Part I. Clinical presentation, epidemiology, pathogenesis, histology, malignant transformation, and neurocutaneous melanosis. J Am Acad Dermatol. 2012;67(4):495 e1-17; quiz 512-4.
- Amir J, Metzker A, Nitzan M. Giant pigmented nevus occurring in one identical twin. Arch Dermatol. 1982;118(3):188-9.
- Bastian BC, Xiong J, Frieden IJ, Williams ML, Chou P, Busam K, et al. Genetic changes in neoplasms arising in congenital melanocytic nevi: differences between nodular proliferations and melanomas. Am J Pathol. 2002;161(4):1163-9.
- Basu D, Salgado CM, Bauer BS, Johnson D, Rundell V, Nikiforova M, et al. Nevospheres from neurocutaneous melanocytosis cells show reduced viability when treated with specific inhibitors of NRAS signaling pathway. Neuro Oncol. 2016;18(4):528-37.
- Cantu JM, Urrusti J, Hernandez A, Del Castillo V, Macotela-Rutz E. Discordance for giant pigmented nevi in monozygotic twins. Ann Genet. 1973;16(4):289-92.
- Castilla EE, da Graca Dutra M, Orioli-Parreiras IM. Epidemiology of congenital pigmented naevi: I. Incidence rates and relative frequencies. Br J Dermatol. 1981;104(3):307-15.
- Castilla EE, da Graca Dutra M, Orioli-Parreiras IM. Epidemiology of congenital pigmented naevi: II. Risk factors. Br J Dermatol. 1981;104(4):421-7.
- Charbel C, Fontaine RH, Kadlub N, Coulomb-L'Hermine A, Rouille T, How-Kit A, et al. Clonogenic cell subpopulations maintain congenital melanocytic nevi. J Invest Dermatol. 2015;135(3):824-33.
- Charbel C, Fontaine RH, Malouf GG, Picard A, Kadlub N, El-Murr N, et al. NRAS mutation is the sole recurrent somatic mutation in large congenital melanocytic nevi. J Invest Dermatol. 2014;134(4):1067-74.
- Dawson HA, Atherton DJ, Mayou B. A prospective study of congenital melanocytic naevi: progress report and evaluation after 6 years. Br J Dermatol. 1996;134(4):617-23.
- de Wijn RS, Zaal LH, Hennekam RC, van der Horst CM. Familial clustering of giant congenital melanocytic nevi. J Plast Reconstr Aesthet Surg. 2010;63(6):906-13.
- Fernandez LC, Torres M, Real FX. Somatic mosaicism: on the road to cancer. Nat Rev Cancer. 2016;16(1):43-55.
- Guegan S, Kadlub N, Picard A, Rouille T, Charbel C, Coulomb-L'Hermine A, et al. Varying proliferative and clonogenic potential in NRAS-mutated congenital melanocytic nevi according to size. Exp Dermatol. 2016.
- Hamm H, Hoger PH. Skin tumors in childhood. Dtsch Arztebl Int. 2011;108(20):347-53.
- Kanada KN, Merin MR, Munden A, Friedlander SF. A prospective study of cutaneous findings in newborns in the United States: correlation with race, ethnicity, and gestational status using updated classification and nomenclature. J Pediatr. 2012;161(2):240-5.
- Kinsler VA, Birley J, Atherton DJ. Great Ormond Street Hospital for Children Registry for Congenital Melanocytic Naevi: prospective study 1988-2007. Part 2--Evaluation of treatments. Br J Dermatol. 2009;160(2):387-92.
- Kinsler VA, Birley J, Atherton DJ. Great Ormond Street Hospital for Children Registry for congenital melanocytic naevi: prospective study 1988-2007. Part 1-epidemiology, phenotype and outcomes. Br J Dermatol. 2009;160(1):143-50.
- Kinsler VA, Thomas AC, Ishida M, Bulstrode NW, Loughlin S, Hing S, et al. Multiple congenital melanocytic nevi and neurocutaneous melanosis are caused by postzygotic mutations in codon 61 of NRAS. J Invest Dermatol. 2013;133(9):2229-36.
- Kinsler VA. An update on congenital melanocytic naevi in children. Nederlands Tijdschrijft Dermatologie en Venereologie. 2014(8).
- Kinsler VA. Spinoza lecture: Congenital melanocytic nevi. In: Academic Medical Center Amsterdam, 2015 Okt. (oral communication)
- Krengel S, Breuninger H, Hauschild A, Hoger P, Merl V, Hamm H. Installation of a network for patients with congenital melanocytic nevi in German-speaking countries. J Dtsch Dermatol Ges. 2008;6(3):204-8.
- Krengel S, Marghoob AA. Current management approaches for congenital melanocytic nevi. Dermatol Clin. 2012;30(3):377-87.
- Krengel S, Scope A, Dusza SW, Vonthein R, Marghoob AA. New recommendations for the categorization of cutaneous features of congenital melanocytic nevi. J Am Acad Dermatol. 2013;68(3):441-51.
- Laude TA. Skin disorders in black children. Curr Opin Pediatr. 1996;8(4):381-5.
- Leech SN, Bell H, Leonard N, Jones SL, Geurin D, McKee PH, et al. Neonatal giant congenital nevi with proliferative nodules: a clinicopathologic study and literature review of neonatal melanoma. Arch Dermatol. 2004;140(1):83-8.
- Lyon VB. Congenital melanocytic nevi. Pediatr Clin North Am. 2010;57(5):1155-76.
- Magana M, Sanchez-Romero E, Magana P, Beck-Magana A, Magana-Lozano M. Congenital melanocytic nevus: two clinicopathological forms. Am J Dermatopathol. 2015;37(1):31-7.
- Marghoob AA, Schoenbach SP, Kopf AW, Orlow SJ, Nossa R, Bart RS. Large congenital melanocytic nevi and the risk for the development of malignant melanoma. A prospective study. Arch Dermatol. 1996;132(2):170-5.
- Mark GJ, Mihm MC, Liteplo MG, Reed RJ, Clark WH. Congenital melanocytic nevi of the small and garment type. Clinical, histologic, and ultrastructural studies. Hum Pathol. 1973;4(3):395-418.
- Morganroth GS, Taylor RS, Izenberg PH. Congenital giant pigmented nevus presenting in one identical twin. Cutis. 1991;48(1):53-5.
- Mundinger GS. Images in clinical medicine. Halo phenomenon. N Engl J Med. 2014;370(3):262.
- Pawlikowski JS, Brock C, Chen SC, Al-Olabi L, Nixon C, McGregor F, et al. Acute Inhibition of MEK Suppresses Congenital Melanocytic Nevus Syndrome in a Murine Model Driven by Activated NRAS and Wnt Signaling. J Invest Dermatol. 2015;135(11):2902.
- Pedersen M, Kusters-Vandevelde HV, Viros A, Groenen PJ, Sanchez-Laorden B, Gilhuis JH, et al. Primary melanoma of the CNS in children is driven by congenital expression of oncogenic NRAS in melanocytes. Cancer Discov. 2013;3(4):458-69.
- Price H. Oral presentation about results of a survey about itch in CMN. In: 2013 Large Nevus Expert Meeting Marseille. (oral communication)
- Rhodes AR, Silverman RA, Harrist TJ, Melski JW. A histologic comparison of congenital and acquired nevomelanocytic nevi. Arch Dermatol. 1985;121(10):1266-73.
- Roh MR, Eliades P, Gupta S, Tsao H. Genetics of melanocytic nevi. Pigment Cell Melanoma Res. 2015;28(6):661-72.
- Rolland S, Kokta V, Marcoux D. Meyerson phenomenon in children: observation in five cases of congenital melanocytic nevi. Pediatr Dermatol. 2009;26(3):292-7.
- Ruiz-Maldonado R, Orozco-Covarrubias L, Ridaura-Sanz C, DurAn-McKinster C, Del Mar Saez De Ocariz Gutierrez M, Tamayo-Sanchez L. Desmoplastic hairless hypopigmented naevus: a variant of giant congenital melanocytic naevus. Br J Dermatol. 2003;148(6):1253-7.
- Ruiz-Maldonado R, Tamayo L, Laterza AM, Duran C. Giant pigmented nevi: clinical, histopathologic, and therapeutic considerations. J Pediatr. 1992;120(6):906-11.
- Salgado CM, Basu D, Nikiforova M, Bauer BS, Johnson D, Rundell V, et al. BRAF mutations are also associated with neurocutaneous melanocytosis and large/giant congenital melanocytic nevi. Pediatr Dev Pathol. 2015;18(1):1-9.
- Salgado CM, Silver RB, Bauer BS, Basu D, Schmitt L, Khakoo Y, et al. Skin of patients with large/giant congenital melanocytic nevi shows increased mast cells. Pediatr Dev Pathol. 2014;17(3):198-203.
- Shain AH, Yeh I, Kovalyshyn I, Sriharan A, Talevich E, Gagnon A, et al. The Genetic Evolution of Melanoma from Precursor Lesions. N Engl J Med. 2015;373(20):1926-36.
- Shakhova O, Zingg D, Schaefer SM, Hari L, Civenni G, Blunschi J, et al. Sox10 promotes the formation and maintenance of giant congenital naevi and melanoma. Nat Cell Biol. 2012;14(8):882-90.
- Shpall S, Frieden I, Chesney M, Newman T. Risk of malignant transformation of congenital melanocytic nevi in blacks. Pediatr Dermatol. 1994;11(3):204-8.
- Strauss RM, Newton Bishop JA. Spontaneous involution of congenital melanocytic nevi of the scalp. J Am Acad Dermatol. 2008;58(3):508-11.
- van Engen-van Grunsven A, Kusters-Vandevelde H, Groenen P, Blokx W. Update on Molecular Pathology of Cutaneous Melanocytic Lesions: What is New in Diagnosis and Molecular Testing for Treatment? Front Med (Lausanne). 2014;31(1):39.
- Viana AC, Gontijo B, Bittencourt FV. Giant congenital melanocytic nevus. An Bras Dermatol. 2013;88(6):863-78.
- Yelamos O, Arva NC, Obregon R, Yazdan P, Wagner A, Guitart J, et al. A comparative study of proliferative nodules and lethal melanomas in congenital nevi from children. Am J Surg Pathol. 2015;39(3):405-15.
Beoordelingsdatum en geldigheid
Publicatiedatum : 19-05-2026
Beoordeeld op geldigheid : 17-11-2017
Een richtlijn heeft alleen zeggingskracht als op continue basis onderhoud plaatsvindt, op grond van systematische monitoring van zowel de medisch wetenschappelijke literatuur als praktijkgegevens en door gebruikers van de richtlijn aangeleverde commentaren. Voor deze richtlijn is afgesproken één keer per jaar de literatuur te evalueren om nieuwe ontwikkelingen te volgen. Bij essentiële ontwikkelingen kan besloten worden om een gehele richtlijnwerkgroep bij elkaar te roepen en tussentijdse elektronische amendementen te maken en deze onder de verschillende beroepsgroepen te verspreiden. Om de richtlijn ‘levend’ te houden is modulaire herziening mogelijk, waarbij slechts een deel of delen van de richtlijn kunnen worden gereviseerd.
Algemene gegevens
De richtlijnontwikkeling werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Doel
Deze richtlijn is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering in de begeleiding van patiënten met congenitale melanocytaire naevi (CMN) en hun directe omgeving. De richtlijn berust op de resultaten van wetenschappelijk onderzoek en aansluitende meningsvorming, door experts, gericht op het vaststellen van goed medisch handelen. De financiering van deze richtlijn is tot stand gekomen met gelden die de NVDV uit zijn SKMS-programma heeft vrijgemaakt.
Doelgroep
De richtlijn is bestemd voor leden van de medische en paramedische beroepsgroepen, waartoe tenminste behoren: dermatologen, plastisch chirurgen, pathologen, kinderartsen, neurologen, huisartsen, verpleegkundigen en huidtherapeuten. Tevens is in een samenwerking tussen patiëntenvereniging NNN en de VSOP een huisartsbrochure ontwikkeld.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn werd een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordiging van de bij CMN betrokken disciplines. Bij het samenstellen van de werkgroep is getracht rekening te houden met de geografische spreiding van de werkgroepleden en met een evenredige vertegenwoordiging van academische en niet-academische werkgroepleden. De werkgroepleden hebben onafhankelijk gehandeld en geen enkel werkgroeplid ontving gunsten met het doel de richtlijn te beïnvloeden.
|
Werkgroepleden |
Vereniging |
|
Prof.dr. Suzanne Pasmans (voorzitter) |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Drs. Céline Eggen (secretaris) |
Promovendus kinderdermatologie Erasmus MC (NVDV)
|
|
Prof.dr. Wilma Bergman |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Nicole Kukutsch |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Albert Wolkerstorfer |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Simone Stadhouders-Keet |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Dr. Marianne Crijns |
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Drs. Annelies Lommerts
|
Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) |
|
Prof.dr. Chantal van der Horst |
Nederlandse Vereniging voor Plastische Chirurgie (NVPC) |
|
Dr. Corstiaan Breugem |
Nederlandse Vereniging voor Plastische Chirurgie (NVPC) |
|
Prof.dr. Wolter Mooi |
Nederlandse Vereniging voor Pathologie (NVVP) |
|
Dr. Hanneke Rijk-van Gent |
Nederlandse Vereniging voor Kindergeneeskunde (NVK) |
|
Prof.dr. Michèl Willemsen |
Nederlandse Vereniging voor Neurologie (NVN) en Nederlandse Vereniging voor Kinderneurologie (NVKN) |
|
Mw. Anja Ebus |
Verpleegkundigen en Verzorgenden Nederland Verpleegkundig Specialist (V&VN VS) en V&VN Dermatologie. |
|
Mw. Marjolein van Kessel |
Nevus Netwerk Nederland (NNN)
|
Verder hebben aan deze richlijn meegewerkt drs. Joep Wijnand en drs. Michéle Hennekam.
Inbreng patiëntenperspectief
Reeds sinds de start van het richtlijntraject is de patiëntenvereniging Nevus Netwerk Nederland (NNN) zeer betrokken geweest bij de totstandkoming van deze richtlijn, door afvaarding van een bestuurslid in de werkgroep. Zij zijn in deze hoedanigheid tijdens het gehele richtlijntraject betrokken geweest, door actieve participatie tijdens werkgroepvergaderingen, en het aandragen van knelpunten die vanuit patiëntenperspectief van groot belang zijn, evenals het deelgenoot maken van lopende initiatieven in het veld. Nevus Netwerk Nederland heeft ook zijn fiat verleend aan de inhoud van de richtlijn.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de ontwikkeling van de conceptrichtlijn is zoveel mogelijk rekening gehouden met de implementatie van de richtlijn en de daadwerkelijke uitvoerbaarheid van de aanbevelingen. De richtlijn wordt gepubliceerd op de website van de NVDV, de website van de richtlijnen database en wordt tevens verspreid onder alle bij CMN betrokken beroepsgroepen. Ook wordt een samenvatting van de richtlijn gepubliceerd en er zal in verschillende specifieke vaktijdschriften aandacht aan worden besteed. Daarnaast wordt de richtlijn onder de aandacht gebracht via de betrokken patiëntenvereniging. De richtlijn is ondergebracht in huidhuis.nl (vanuit de NVDV) en gekoppeld aan het persoonlijk gezondheidsdossier van Patient1 in huidhuis.nl voor mensen met een huidafwijking en de betrokken professionals.
Werkwijze
De richtlijn congenitale melanocytaire naevi is een geheel nieuwe richtlijn. In de richtlijn melanoom (goedgekeurd op 13.08.2012) wordt reeds verwezen naar de in wording zijnde richtlijn CMN. De richtlijnwerkgroep is opgestart in het najaar van 2011, maar heeft tussendoor enkele malen stil gelegen onder andere vanwege een andere prioritering op de richtlijnagenda van de NVDV.
In de eerste vergadering(en) werden de knelpunten en wensen ten aanzien van het onderwerp CMN geïnventariseerd binnen de werkgroep. De werkgroep formuleerde aan de hand hiervan in de richtlijn vermelde uitgangsvragen. Ook werd aan de start van het traject een enquête uitgezet onder dermatologen en plastisch chirurgen in Nederland om het huidige beleid omtrent CMN te inventariseren. De doelen van deze enquête waren het vastleggen van de uitgangssituatie om tot een richtlijn te komen die aansluit op de werkvloer, en het identificeren van aanvullende knelpunten.
De uitgangsvragen werden op het bureau van de Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) uitgewerkt tot PICO-zoekvragen. Via systematische zoekopdrachten en reference checking is bruikbare literatuur verzameld. De secretaris van de richtlijn en studenten hebben samen met de werkgroepleden de literatuur beoordeeld op inhoud en kwaliteit. Vervolgens zijn er teksten geschreven waarin de beoordeelde literatuur werd verwerkt. Deze teksten, op basis van de evidencetabellen met de verwerkte literatuur, zijn tijdens een tweedaagse vergadering besproken en van nuances en aanbevelingen voorzien. Na verdere discussie binnen de gehele richtlijnwerkgroep is de tekst verder afgestemd.
De uiteindelijke tekst werd in september 2016 aan alle betrokken wetenschappelijke verenigingen aangeboden. Men is in staat gesteld om via websites van de betrokken verenigingen commentaar op de richtlijn te geven. De commentaren zijn in de definitieve versie van de richtlijn verwerkt.
Wetenschappelijke bewijsvoering
De aanbevelingen uit deze richtlijn zijn, voor zover mogelijk, gebaseerd op bewijs uit gepubliceerd wetenschappelijk onderzoek.
Relevante artikelen zijn gezocht via een systematische, oriënterende zoekopdracht in Pubmed, overkoepelend voor het onderwerp congenitale melanocytaire naevi (van 1987 tot november 2014, talen Nederlands, Engels, Frans, Duits). Voor specifieke uitgangsvragen werd nog een aanvullende systematische search verricht met meer specifieke zoektermen voor de desbetreffende vraag, en in aanvullende databases (zoals Embase, CENTRAL, Cochrane library etc). Tevens is voor enkele uitgangsvragen en passages de search meer recent herhaald (2014~2016). Zie ook de zoekstrategie.
De zoekacties zijn met behulp van de PICO-systematiek opgebouwd. Dit houdt in dat voor elke uitgangsvraag een zoekvraag is geformuleerd waarbij zoveel mogelijk de volgende structuur is gehanteerd: Patiënt-Interventie-Controle-Outcome. De zoekvragen hebben de P als gemeenschappelijk onderdeel, de overige onderdelen van de PICO zijn geformuleerd op basis van de uitgangsvraag. Het merendeel van de zoekcriteria is afhankelijk van de uitgangsvraag.
Algemeen werden de volgende zoek- en selectiecriteria opgesteld:
|
Taal |
Engels, Nederlands, Duits, Frans |
|
Populatie |
Congenitale melanocytaire naevi (in alle synoniemen), alle groottes, alle leeftijden (exclusie van verworven melanocytaire naevi, of als niet gespecifieerd was of de naevi congenitaal waren) |
|
level of evidence |
Literatuurselectie volgens piramide van bewijs (EBRO-methode). Vanwege het veelal ontbreken van studies van goede kwaliteit (gerandomiseerd of prospectief) is er niet beperkt op de fundamentele opzet van de studie |
|
grootte van de studies |
Hier is in het algemeen geen limiet aangesteld, omdat voor de meeste uitgangsvragen slechts caseseries met enkele patiënten beschikbaar zijn. Wel zijn bij meerdere uitgangsvragen casereports en caseseries met <5 patiënten geëxcludeerd, omdat deze een nog grotere selectiebias geven en daarmee een mogelijk te vertekend beeld van de werkelijkheid. |
Van de geselecteerde referenties op basis van titel en/of abstract werd de full-text aangevraagd. Op basis van full-text artikelen is vervolgens verder geselecteerd en zijn artikelen zonder informatie over de betreffende uitgangsvraag geëxcludeerd. De overgebleven artikelen zijn full-text beoordeeld op kwaliteit en inhoud.
Tijdens de search werden geen (buitenlandse) richtlijnen over dit onderwerp geïdentificeerd, maar wel enkele relevante en betrouwbare ‘learning articles’, waarin op gedegen wijze relevante literatuur over het onderwerp CMN in zijn totaliteit is samengebracht. Deze artikelen vormen deels de basis voor de enkele richtlijnteksten [Alikhan 2012, Ibrahimi 2012, Viana 2013], aangevuld met andere relevante literatuur.
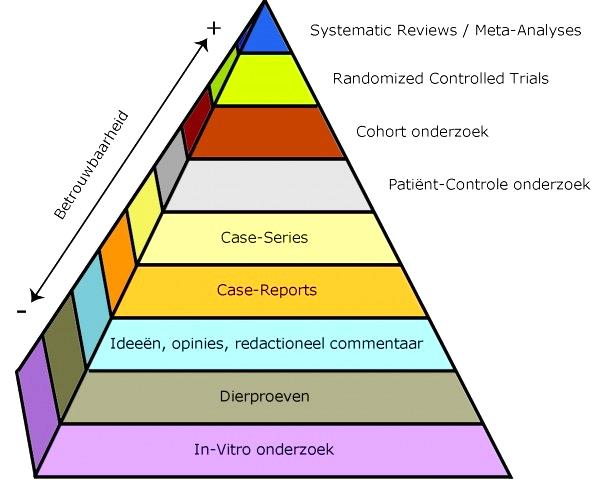
Fig. 1: Piramide van wetenschappelijk bewijs
Methode van literatuurbeoordeling
De richtlijn is ontwikkeld volgens de EBRO-methode (Evidence-based Richtlijn Ontwikkeling). Per deelonderwerp is van de relevante artikelen een ‘evidencetabel’ opgesteld, waarin de literatuur is samengevat en beoordeeld op kwaliteit. De beschrijving en beoordeling van de artikelen staan in de verschillende module onder het kopje ‘wetenschappelijke onderbouwing’, en de literatuur is vervolgens samengevat in ‘conclusies’. De kwaliteit van de artikelen en het niveau van het relevante bewijs is volgens de EBRO-methode gegradeerd, aan de hand van de indeling in tabel 1.
Daarnaast is voor de beoordeling van uitgangsvraag 12 gekozen voor de GRADE methodiek (Grading of Recommendations Assessment, Development and Evaluation), waarbij per uitkomstmaat het beschikbare bewijs is ‘gepooled’ en beoordeeld op de kwaliteit van het bewijs, zie tabel 2. De toepassing van GRADE voor deze richtlijn was lastig omdat er alleen observationele studies zijn, geen vergelijkende studies, en de studies erg heterogeen zijn qua patiënt- en naevuskenmerken. Deze methodiek is daarom alleen toegepast bij behandelmodaliteiten waarbij ‘pooling’ van resultaten volgens de werkgroep mogelijk was.
Tabel 1: EBRO methode; A. niveau van conclusies volgens EBRO; B. Indeling van methodologische kwaliteit van individuele studies
A.
|
niveau |
Conclusie gebaseerd op |
|
1 |
Onderzoek van niveau A1 of tenminste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau A2 |
|
2 |
1 onderzoek van niveau A2 of tenminste 2 onafhankelijk van elkaar uitgevoerde onderzoeken van niveau B |
|
3 |
1 onderzoek van niveau B of C |
|
4 |
Mening van deskundigen |
B.
|
Kwaliteit |
Interventie |
Diagnostisch accuratesse onderzoek |
Schade / bijwerkingen*, etiologie, prognose |
|
A1 |
Systematische review van tenminste twee onafhankelijk van elkaar uitgevoerde onderzoeken van A2-niveau |
||
|
A2 |
Gerandomiseerd dubbelblind vergelijkend klinisch onderzoek van goede kwaliteit van voldoende omvang |
Onderzoek ten opzichte van een referentietest (een ‘gouden standaard’) met tevoren gedefinieerde afkapwaarden en onafhankelijke beoordeling van de resultaten van test en gouden standaard, betreffende een voldoende grote serie van opeenvolgende patiënten die allen de index- en referentietest hebben gehad |
Prospectief cohortonderzoek van voldoende omvang en follow-up, waarbij adequaat gecontroleerd is voor ‘confounding’ en selectieve follow-up voldoende is uitgesloten. |
|
B |
Vergelijkend onderzoek, maar niet met alle kenmerken als genoemd onder A2 (hieronder valt ook patiënt-controle onderzoek, cohortonderzoek) |
Onderzoek ten opzichte van een referentietest, maar niet met alle kenmerken die onder A2 zijn genoemd |
Prospectief cohortonderzoek, maar niet met alle kenmerken als genoemd onder A2 of retrospectief cohortonderzoek of patiënt-controle onderzoek |
|
C |
Niet-vergelijkend onderzoek |
||
|
D |
Mening van deskundigen |
||
* Deze classificatie is alleen van toepassing in situaties waarin om ethische of andere redenen gecontroleerde trials niet mogelijk zijn. Zijn die wel mogelijk dan geldt de classificatie voor interventies.
Tabel 2: GRADE methode; A. niveau van bewijs volgens GRADE; C. wijze van beoordelen niveau van bewijs per uitkomstmaat
A.
|
GRADE Working Group grades of quality of evidence |
|
|
High |
We are very confident that the true effect lies close to that of the estimate of the effect |
|
Moderate |
We are moderately confident in the effect estimate: The true effect is likely to be close to the estimate of the effect, but there is a possibility that it is substantially different |
|
Low |
Our confidence in the effect estimate is limited: The true effect may be substantially different from the estimate of the effect |
|
Very low |
We have very little confidence in the effect estimate: The true effect is likely to be substantially different from the estimate of effect |
B.
|
Startpunt van beoordelen kwaliteit van bewijs |
|
|
RCT’s |
Beginnen als ‘high quality’ |
|
Observationele studies |
Beginnen als ‘low quality’ |
|
Per uitkomstmaat over de studies heen evt quality of evidence één of twee niveaus downgraden (1-5) of upgraden (6-8) |
|
|
1. |
risk of bias |
|
2. |
inconsistency |
|
3. |
indirectness |
|
4. |
imprecision |
|
5. |
publication bias |
|
6. |
large effect |
|
7. |
plausible confounding |
|
8. |
dose response gradient |
Totstandkoming van de aanbevelingen
Voor het komen tot een aanbeveling zijn er naast het wetenschappelijke bewijs vaak andere aspecten van belang, bijvoorbeeld: patiëntvoorkeuren, beschikbaarheid van speciale technieken of expertise, organisatorische aspecten, maatschappelijke consequenties of kosten. Deze aspecten worden besproken na de conclusie(s) onder ‘overige overwegingen’. Hierin wordt de conclusie op basis van de literatuur geplaatst in de context van de dagelijkse praktijk en vindt een afweging plaats van de voor- en nadelen van de verschillende beleidsopties. De uiteindelijk geformuleerde aanbeveling is het resultaat van het beschikbare bewijs in combinatie met deze overwegingen vanuit expert opinion. Het volgen van deze procedure en het opstellen van de richtlijn in dit format heeft als doel de transparantie van de richtlijn te verhogen.
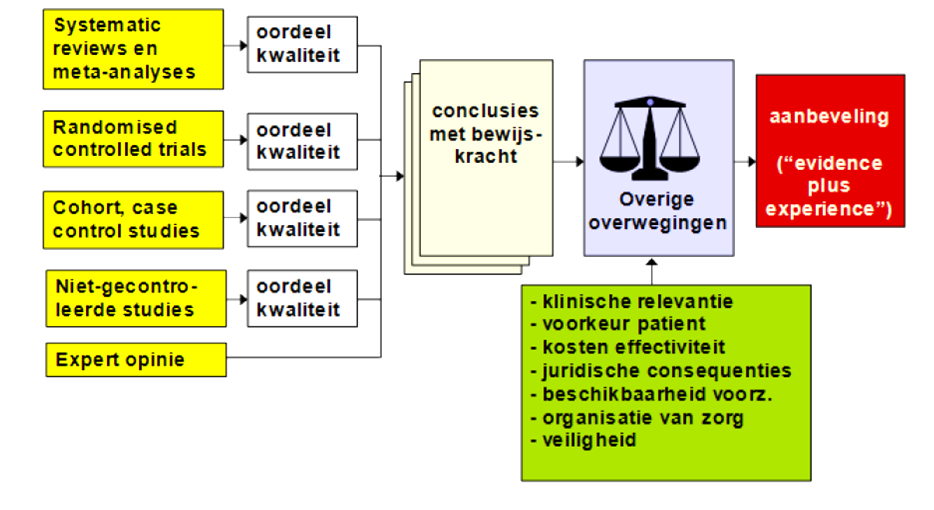
Fig. 2: Schematisch weergave methodiek van evidence-based richtlijnontwikkeling
Innovatie
Het veld van de congenitale melanocytaire naevi is in beweging. Enerzijds wordt langzamerhand de moleculaire signatuur van CMN ontrafeld, hetgeen belangrijke nieuwe aanknopingspunten geeft voor nieuwe (genetische) diagnostiek en (niet-chirurgische) therapieën. Daarnaast is er in de loop der jaren een verschuiving opgetreden van invasief en agressief behandelen om zoveel mogelijk naevusweefsel te verwijderen in het kader van een vermeend hoog melanoomrisico, naar minder agressief en meer oppervlakkig of partieel ingrijpen met meer oog voor het cosmetisch resultaat. Verder is er in het verleden veelal slechts retrospectief onderzoek verricht met een hoog risico op bias. Er zijn inmiddels enkele prospectieve studies verschenen over melanoomrisico, maar nog niet over therapie in CMN.
Advies voor onderzoek
Over de gehele linie ontbreekt het aan goed uitgevoerde studies op het gebied van CMN. Veelal zijn er alleen caseseries en casereports verschenen, met een hoog risico op bias. Dit is ergens inherent aan het onderwerp, waarbij met name grotere CMN zeldzaam zijn, en CMN daarnaast nog in grote mate interindividueel verschillen. Met name op het gebied van therapieën ontbreekt het aan betrouwbaar onderzoek. Bijna alle auteurs meten verschillende of niet-gevalideerde uitkomstmaten, en ‘patient-important outcomes’, zoals kwaliteit van leven, patiënttevredenheid maar ook veiligheid, worden vrijwel niet onderzocht. In de studies over melanoomrisico ontbreekt het aan studies in volwassen patiënten en kleinere CMN, en studies met langere follow-up duur (>10 jaar). Dit geldt ook voor studies naar het risico op NCM, hierbij zijn tevens veel verschillende definities voor NCM gehanteerd.
Onderzoek naar CMN zou moeten bestaan uit prospectief onderzoek, met nauwkeurige en gestandaardiseerde registratie van patiëntkenmerken, en gevalideerde en gestandaardiseerde registratie van uitkomsten, over een lange tijd. Hierbij moet er ten aanzien van behandeling ook meer aandacht komen voor voor de patiënt belangrijke uitkomsten en veiligheid. Op het gebied van melanoomrisico is dit internationaal reeds opgepakt, door het in diverse landen opzetten van (nationale) prospectieve registries. De werkgroep is van plan op korte termijn een dergelijke registry op te zetten in Nederland (via huidhuis.nl vanuit de NVDV), waarbij ook de uitkomsten van therapieën zullen worden meegenomen. Later zal deze gekoppeld worden aan internationale registries.
Daarnaast is meer en beter onderzoek nodig naar diagnostische modaliteiten bij CMN, zoals dermatoscopie en MRI, en diagnostische technieken om melanoom in CMN te ontdekken en te kunnen onderscheiden van benigne naevusweefsel of proliferaties.
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften, maar wetenschappelijk onderbouwde en breed gedragen inzichten en aanbevelingen waaraan zorgverleners zouden moeten voldoen om kwalitatief goede zorg te verlenen. Aangezien richtlijnen uitgaan van ‘gemiddelde patiënten’, kunnen zorgverleners in individuele gevallen zo nodig afwijken van de aanbevelingen in de richtlijn. Afwijken van richtlijnen is, als de situatie van de patiënt dat vereist, soms zelfs noodzakelijk. Wanneer bewust van de richtlijn wordt afgeweken, moet dit echter beargumenteerd, gedocumenteerd en waar nodig in overleg met de patiënt worden gedaan.
Zoekverantwoording
Search richtlijn overkoepelend
Zoekstrategie voluit:
(nevi OR naevi OR nevus OR naevus OR mole OR moles OR birthmark* OR “Nevus”[MESH] OR “Nevus, pigmented”[MESH])
AND
((congenita* OR inborn OR hereditary OR newborn OR “congenital”[Subheading]) OR
(giant OR garment OR Tierfell OR gigantic OR ‘bathing trunk’))
NOT
connective tissue OR anaemicus OR elasticus OR inelasticus OR depigmentosus OR mucinosis OR lipomatosus OR sebaceus OR blue OR comedonicus OR spindle OR sponge OR woolly OR spilus OR spider OR flammeus OR Jadassohn OR Ota OR Becker OR Sutton OR Unna OR neurofibromatosis OR pancreas* OR placenta
Filters: taal: NL, EN, DU; jaar: vanaf 1987
Gezocht op 22.11.2014: 1934 hits (PubMed)
Tussentijds (2014~2016) op specifieke uitgangsvragen geupdate.
Search fotografie
Zoekstrategie voluit:
("congenital naevus".ti,ab OR "congenital naevi".ti,ab OR "congenital nevus".ti,ab OR "congenital nevi".ti,ab OR "congenital melanocytic naevus".ti,ab OR "congenital melanocytic naevi".ti,ab OR "congenital melanocytic nevus".ti,ab OR "congenital melanocytic nevi".ti,ab OR (("naevus".ti,ab OR "naevi".ti,ab OR "nevus".ti,ab OR "nevi".ti,ab OR "melanocytic naevus".ti,ab OR "melanocytic naevi".ti,ab OR "melanocytic nevus".ti,ab OR "melanocytic nevi".ti,ab) AND congenital*.ti,ab)) AND (Photography/ OR medical photography/ OR Photograph*.ti,ab) AND (english.la OR dutch.la)
Gezocht op 07.05.2014: 44 hits (34 Pubmed, 37 Embase waarvan 10 uniek)
Search dermatoscopie
Zoekstrategie voluit:
("congenital naevus".ti,ab OR "congenital naevi".ti,ab OR "congenital nevus".ti,ab OR "congenital nevi".ti,ab OR "congenital melanocytic naevus".ti,ab OR "congenital melanocytic naevi".ti,ab OR "congenital melanocytic nevus".ti,ab OR "congenital melanocytic nevi".ti,ab OR (("naevus".ti,ab OR "naevi".ti,ab OR "nevus".ti,ab OR "nevi".ti,ab OR "melanocytic naevus".ti,ab OR "melanocytic naevi".ti,ab OR "melanocytic nevus".ti,ab OR "melanocytic nevi".ti,ab) AND congenital*.ti,ab)) AND (Dermoscopy/ OR Dermascopy/ OR dermatosc*.ti,ab) AND (english.la OR dutch.la OR german.la)
Filters: taal: NL, EN, DU (zie searchtermen) en jaar vanaf 1990
Gezocht in mei/juni 2014: 243 hits (Pubmed, Embase) >> na ontdubbeling 171; met reference checking 2 extra artikelen
Search chirurgie
Chirurgische ingrepen (excision, tissue expansion, skin grafting)
((nevus/de AND ('congenital disorder'/de OR congenital:lnk OR (congent* OR unacquir* OR 'not acquired' OR 'non acquired'):ab,ti)) OR 'congenital nevus'/de OR 'pigmented nevus'/de OR 'melanocytic nevus'/de OR (((congenit* OR unacquir* OR 'not acquired' OR 'non acquired' OR pigment* OR melanocyt* OR nevocell* OR naevocell* OR 'nevo cellular' OR 'naevo cellular' OR giant OR gigantic OR medium OR large* OR multiple OR small* OR pilos* OR hair* OR divided) NEAR/3 (nevus OR naevus OR nevi OR naevi OR mole OR moles OR birthmark* OR nævi OR nævus)) OR nevocyt* OR nevomelanocyt* OR naevocyt* OR naevomelanocyt* OR ((nevocell* OR naevocell* OR 'nevo cellular' OR 'naevo cellular') NEAR/3 (lesion* OR laesion*)) OR tierfell* OR (bathing NEXT/1 trunk*) OR (((pigment* NEAR/3 (lesion* OR laesion*))) AND (nevus OR naevus OR nevi OR naevi OR mole OR moles OR birthmark*) AND (melanom* OR pseudomelanom*))):ab,ti) AND (surgery/de OR 'surgical technique'/de OR excision/de OR 'local excision'/de OR surgery:lnk OR 'minor surgery'/de OR 'major surgery'/de OR 'pediatric surgery'/exp OR 'plastic surgery'/exp OR dermatome/de OR 'skin surgery'/exp OR autograft/de OR allograft/de OR transplantation/de OR (surg* OR dermatosurg* OR excis* OR resect* OR remov* OR dermatome* OR shaving OR shave OR shaved OR ((skin OR tissue) NEAR/3 (flap* OR expan* OR stretch* OR transplant* OR replace*)) OR graft* OR autograft* OR allograft* OR reconstruct* OR resurfac*):ab,ti)
Gezocht in juli 2014: 4609 hits na ontdubbelen
|
Embase.com |
3134 |
|
Medline (OvidSP) |
393 |
|
Web-of-science |
304 |
|
Scopus |
618 |
|
PubMed publisher |
35 |
|
Cochrane |
0 |
|
Google scholar |
125 |
|
Total |
4609 |
Curettage, dermabrasie
Uit bovenstaande search kwamen ook artikelen over curettage en dermabrasie naar boven. Met reference checking en een korte search op synoniemen voor ‘congenital n(a)evi, dermbrasion, curettage) is gekeken of de gevonden artikelen voor dit onderwerp compleet waren.
Search lasertherapie
(((nevus[tiab] OR nevi[tiab] OR naevus[tiab] OR naevi[tiab] OR CMNs[tiab] OR SCMN[tiab] OR MCMN[tiab] OR LCMN[tiab] OR LCMNs[tiab] OR GCMN[tiab] OR GCMNs[tiab] OR CNNs[tiab] OR SCNN[tiab] OR MCNN[tiab] OR MCNNs[tiab] OR GCNN[tiab] OR Tierfell*[tiab] OR bathing-trunk*[tiab] OR garment-like[tiab] OR ((CNN[tiab] OR CMN[tiab] OR mole[tiab] OR moles[tiab] OR birthmark*[tiab]) AND (giant[tiab] OR gigantic[tiab] OR medium[tiab] OR large[tiab] OR multiple[tiab] OR pilos*[tiab] OR hairy[tiab] OR melanocytic[tiab] OR naevocytic[tiab] OR nevocytic[tiab] OR naevocell*[tiab] OR nevocell*[tiab] OR naevomelanocytic[tiab] OR nevomelanocytic[tiab] OR congenital*[tiab] OR unacquired[tiab] OR non-acquired[tiab]))) AND (laser[tiab] OR lasers[tiab] OR yttrium[tiab] OR erbium[tiab] OR neodymium[tiab] OR aluminum oxide[tiab] OR QSRL*[tiab] OR QSNYL*[tiab] OR QSND[tiab] OR FDQS*[tiab] OR NMRL*[tiab] OR NM-QS*[tiab] OR ND-QS*[tiab] OR Q-switch*[tiab] OR Qswitch*[tiab] OR YAG*[tiab] OR NDYAG*[tiab] OR ND-YAG*[tiab] OR ERYAG*[tiab] OR ER-YAG*[tiab] OR Neodymi*[tiab] OR Erbium*[tiab] OR Yttrium*[tiab] OR Alexandrit*[tiab] OR UCO2*[tiab] OR UltraPulse[tiab])) NOT ota[ti])
Gezocht in November 2015: 683 hits
|
Medline (OvidSP) |
330 |
|
Embase.com |
554 |
|
Central |
33 |
|
PubMed publisher |
7 |
|
Total (na ondubb.) |
683 |
