Overige behandeling van volwassenen met CU
Uitgangsvraag
Welke overige behandelmogelijkheden worden aanbevolen als het stepped care model onvoldoende effect geeft bij volwassenen met CU?
Aanbeveling
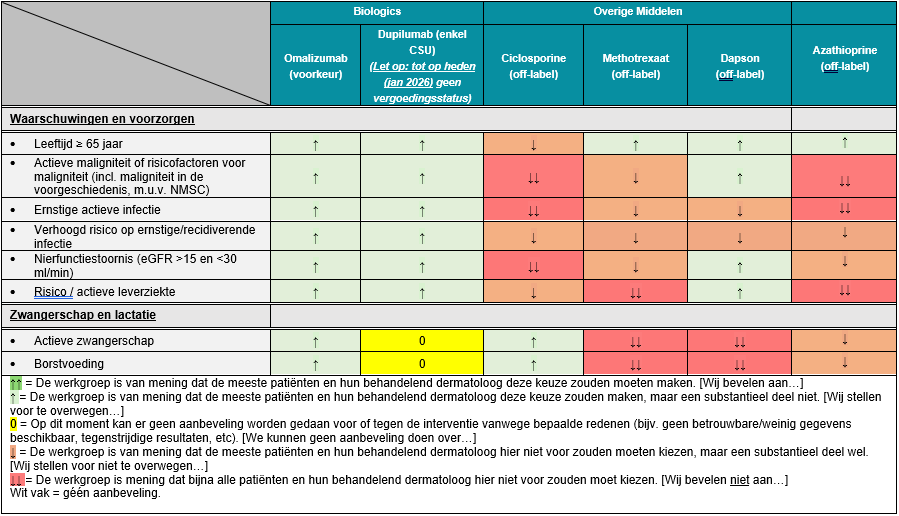
Overweeg behandeling met azathioprine, methotrexaat (MTX), dapson, UVB-therapie, mycofenolaat mofetil (MMF) bij patiënten met CU die onvoldoende effect, bijwerkingen of contra-indicaties hebben bij de behandeling met omalizumab, dupilumab (CSU) en ciclosporine. Neem in de keuze van het middel mee: comorbiditeit, voorkeur van de patiënt, veiligheidsprofiel en snelheid van werking (zie Tabel 1. Overzicht geneesmiddelen voor volwassenen met CU).
Disclaimer: er is tot op heden (januari 2026) in Nederland nog geen vergoedingsstatus beschikbaar voor dupilumab bij chronische spontane urticaria
Let op: Wanneer een off-label medicament wordt voorgeschreven, dient gehandeld te worden volgens de bijbehorende voorwaarden (zie voorwaarden van de IGJ).
Overwegingen
Kwaliteit van het bewijs
Voor deze module werd voor enkele middelen de internationale richtlijn van Zuberbier et al. (2022) als basis genomen. De kwaliteit van het bewijs is over het algemeen zeer laag tot laag. Voor enkele middelen zijn geen vergelijkende onderzoeken gevonden in het systematisch literatuuronderzoek, de aanbevelingen hiervan zijn geheel gebaseerd op expert opinion.
Balans van gewenste en ongewenste effecten
Gezien het beperkte bewijs voor de effectiviteit van de in de aanbevelingen genoemde middelen voor de behandeling van CSU, moeten de gewenste en ongewenste effecten zorgvuldig worden afgewogen. Deze middelen hebben namelijk relatief veel kans op bijwerkingen. Bij dapson kunnen bijvoorbeeld hemolyse en methemoglobinemie optreden. Methotrexaat (MTX) kan leiden tot levertoxiciteit, beenmergsuppressie en gastro-intestinale klachten. Azathioprine kan infecties, beenmergsuppressie en leverenzymstoornissen veroorzaken. Bij UVB-therapie moet bovendien voorzichtigheid worden geboden vanwege verhoogde risicio op huidkanker van cumulatieve UV-licht behandelingen.
Professioneel perspectief
Overweeg de behandeling van dapson, MTX, of azathioprine indien andere behandelingen genoemd in de module “Behandeling van volwassenen met CU” falen. Er is weinig bewijs beschikbaar die de effectiviteit van deze middelen steunen. Echter kunnen deze middelen toch relevant zijn bij individuele patiënten en ook vanwege de relatief lage geneesmiddelkosten (Zuberbier, 2022). De eerste keuze voor een van deze drie middelen hangt af van de individuele patiënt, waarbij rekening wordt gehouden met patiëntvoorkeuren, het veiligheidsprofiel en de snelheid van de werking.
Voor de behandeling van CSU kan overwogen worden een ultraviolet B (UVB) behandeling gedurende 1-3 maanden worden toegevoegd aan de behandeling met, antihistaminica (Zuberbier, 2022). Een behandeling met MMF kan ook worden overwogen, maar het is belangrijk te benadrukken dat MMF zeer teratogeen is, wat betekent dat het ernstige schade kan toebrengen aan het ongeboren kind als het tijdens de zwangerschap wordt gebruikt. Bespreek met de patiënte de risico's en wijs haar op het zwangerschapspreventieprogramma. Voor vrouwen in de vruchtbare levensfase moet voorafgaand aan de behandeling, idealiter maandelijks tijdens de behandeling, en nog één maand na de behandeling een zwangerschapstest worden uitgevoerd.
Bij patiënten met specifieke comorbiditeiten, zoals eosinofiele oesofagitis, prurigo nodularis, comorbide astma of chronische rhinosinusitis met neuspoliepen, heeft dupilumab de voorkeur (echter nog geen vergoedingsstatus, januari 2026).
Tabel 1. Overzicht geneesmiddelen voor volwassenen met CU en de evidence en (indien geen evidence beschikbaar) de expert opinion beoordeling van hun geschiktheid in specifieke behandelomstandigheden. Deze tabel kan gebruikt worden als hulpmiddel in shared-decision making
Let op: voor dupilumab is nog geen vergoedingsstatus (januari 2026). Zie ook Dupixent | European Medicines Agency (EMA).
Waarden en voorkeuren van patiënten
Bij de behandeling van CSU is het belangrijk om rekening te houden met de voorkeuren van patiënten. De ernst van de symptomen en de impact op het dagelijks leven van de diverse middelen en daarbij te maken keuzen, moeten worden afgewogen tegen de bijwerkingen en lasten van de behandeling. Deze lasten kunnen bijvoorbeeld bestaan uit regelmatige bloedonderzoeken bij middelen zoals MTX, of de tijdsinvestering die nodig is voor UVB-therapie. Gezien het beperkte bewijs voor de effectiviteit van deze behandelingen, is het van belang dat de patiënt samen met de zorgverlener een afweging maakt tussen de benodigde investering, potentiele bijwerkingen en de te verwachten effectiviteit ervan. Het is verder belangrijk om het effect van de behandeling en bijwerkingen goed te monitoren en zonodig de behandeling aan te passen. Verder is het van belang om aandacht te hebben voor de psychosociale aspecten van de aandoening en eventueel benodigde psychologische ondersteuning.
Aanvaardbaarheid en haalbaarheid
Gezien de ruime ervaring met de genoemde behandelingen voor andere dermatologische indicaties en de betaalbaarheid ervan, verwacht de werkgroep dat het opvolgen van de aanbevelingen geen aanzienlijke problemen zal veroorzaken met betrekking tot toepasbaarheid of kosten.
Onderbouwing
Wanneer het stepped-care model voor de behandeling van CSU bij volwassenen niet het gewenste effect heeft, zijn er enkele alternatieve behandelingen beschikbaar. Er is weinig literatuur en de bewijskracht is laag voor de effectiviteit van deze middelen. Ondanks het gebrek aan bewijs kunnen enkele van deze geneesmiddelen in de passende klinische situaties waardevol zijn voor individuele patiënten.
Kwaliteit van bewijs
Hydroxychloroquine versus placebo
Click here to see these tables in a document
|
Certainty assessment |
|
|
|
|
|
|
Impact |
Certainty |
Importantie |
|
Aantal studies |
Studieopzet |
Risk of bias |
Inconsistentie |
Indirect bewijs |
Onnauwkeurigheid |
Andere factoren |
|
|
|
|
SF-12 (mentaal) [Reeves, 2004] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
1 (n=18) |
gerandomiseerde trials |
ernstiga |
niet ernstig |
niet ernstig |
zeer ernstigb |
niet gevonden |
Het is onzeker wat het effect is van hydroxychloroquine op de kwaliteit van leven gemeten met SF-12. |
⨁◯◯◯ Zeer laag |
BELANGRIJK |
|
GSSS [Reeves, 2004] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
1 (n=18) |
gerandomiseerde trials |
ernstiga |
niet ernstig |
niet ernstig |
zeer ernstigb |
niet gevonden |
Het is onzeker wat het effect is van hydroxychloroquine op de kwaliteit van leven gemeten met GSSS. |
⨁◯◯◯ Zeer laag |
BELANGRIJK |
CI: Confidence interval; MD: Mean difference
Explanations
a. Risk of bias is verhoogd door onduidelijk beschrijving van randomisatie en blindering.
b. Erg breed betrouwbaarheidsinterval door kleine populatie
Dapson als add-on therapie
|
Certainty assessment |
|
|
|
|
|
|
Aantal patiënten |
|
Effect |
|
Certainty |
Importantie |
|
Aantal studies |
Studieopzet |
Risk of bias |
Inconsistentie |
Indirect bewijs |
Onnauwkeurigheid |
Andere factoren |
Dapson |
antihistaminica |
Relatief (95% CI) |
Absoluut (95% CI) |
|
|
|
UAS7 [Engin, 2007] (follow up: 3 maanden) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=65) |
gerandomiseerde trials |
ernstiga |
niet ernstig |
niet ernstig |
niet ernstig |
niet gevonden |
Dapson heeft waarschijnlijk geen of nauwelijks effect op de UAS7 |
|
|
|
⨁⨁⨁◯ Redelijkd |
CRUCIAAL |
|
Goede respons ( UAS score < 2 en DLQI score < 2) [Soni,2023] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=100) |
gerandomiseerde trials |
ernstigb |
niet ernstig |
niet ernstig |
niet ernstig |
niet gevonden |
28/50 (56.0%) |
13/50 (26.0%) |
RR 2.15 (1.27 tot 3.65) |
299 meer per 1.000 (from 70 meer tot 689 meer) |
⨁⨁⨁◯ Redelijk |
CRUCIAAL |
|
Redelijke respons (UAS score 2 - 4 en DLQI score 2 – 9) [Soni,2023] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=100) |
gerandomiseerde trials |
ernstigb |
niet ernstigc |
niet ernstig |
ernstigc |
niet gevonden |
21/50 (42.0%) |
11/50 (22.0%) |
RR 1.91 (1.03 tot 3.53) |
200 meer per 1.000 (from 7 meer tot 557 meer) |
⨁⨁◯◯ Laag |
CRUCIAAL |
|
Veiligheid (bijwerkingen) [Engin, 2007; Soni, 2023] (follow up: range 12 weken tot 13 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
2 (n=165) |
gerandomiseerde trials |
ernstiga,b |
niet ernstig |
niet ernstig |
ernstigc |
niet gevonden |
8/88 (9.1%) |
0/77 (0.0%) |
RR 8.26 (1.02 tot 67.22) |
0 minder per 1.000 (from 0 minder tot 0 minder) |
⨁⨁◯◯ Laag |
CRUCIAAL |
Explanations
a. Hoge risico op selection, performance en detection bias gezien geen blindering. Tevens is lost to follow up niet beschreven in de studie dus onduidelijk of er sprake is van attrition bias.
b. Onduidelijke beschrijving van randomisatie en blindering evenals lost to follow up. Hierdoor risico op selection, performance, detection en attrition bias.
c. Breed betrouwbaarheidsinterval waarbij het effect klinisch relevant of niet klinisch relevant kan zijn
d. In Zuberbier et al. (2021) 1 RCT met dezelfde uitkomst na 4 weken (gemiddelde verandering van UAS7) MD 1,23 lager (1,54 lager tot 0,92 lager), bewijskracht is redelijk.
MTX als add-on therapie
|
Certainty assessment |
|
|
|
|
|
|
Aantal patiënten |
|
Effect |
|
Certainty |
Importantie |
|
Aantal studies |
Studieopzet |
Risk of bias |
Inconsistentie |
Indirect bewijs |
Onnauwkeurigheid |
Andere factoren |
MTX |
antihistaminica |
Relatief (95% CI) |
Absoluut (95% CI) |
|
|
|
Goede respons ( UAS score < 2 en DLQI score < 2) [Soni,2023] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=100) |
gerandomiseerde trials |
ernstiga |
niet ernstig |
niet ernstig |
zeer ernstigb |
niet gevonden |
15/50 (30.0%) |
13/50 (26.0%) |
RR 1.15 (0.61 tot 2.17) |
39 meer per 1.000 (from 101 minder tot 304 meer) |
⨁◯◯◯ Zeer laag |
CRUCIAAL |
|
Redelijke respons (UAS score 2 - 4 en DLQI score 2 – 9) [Soni,2023] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=100) |
gerandomiseerde trials |
ernstiga |
niet ernstig |
niet ernstig |
niet ernstig |
niet gevonden |
25/50 (50.0%) |
11/50 (22.0%) |
RR 2.27 (1.26 tot 4.10) |
279 meer per 1.000 (from 57 meer tot 682 meer) |
⨁⨁⨁◯ Redelijk |
CRUCIAAL |
|
Veiligheid (bijwerkingen) [Soni,2023] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=100) |
gerandomiseerde trials |
ernstiga |
niet ernstig |
niet ernstig |
zeer ernstigb |
niet gevonden |
5/50 (10.0%) |
0/50 (0.0%) |
RR 12.21 (0.66 tot 226.97) |
0 minder per 1.000 (from 0 minder tot 0 minder) |
⨁◯◯◯ Zeer laag |
CRUCIAAL |
CI: Confidence interval; RR: Risk ratio
Explanations
a. Onduidelijke beschrijving van randomisatie en blindering evenals lost to follow up. Hierdoor risico op selection, performance, detection en attrition bias.
b. Zeer breed betrouwbaarheidsinterval waarbij het effect zowel klinisch relevant positief als klinisch relevant negatief kan zijn
Benralizumab 30 mg versus placebo
|
Certainty assessment |
|
|
|
|
|
|
Aantal patiënten |
|
Effect |
|
Certainty |
Importantie |
|
Aantal studies |
Studieopzet |
Risk of bias |
Inconsistentie |
Indirect bewijs |
Onnauwkeurigheid |
Andere factoren |
Benralizumab |
placebo |
Relatief (95% CI) |
Absoluut (95% CI) |
|
|
|
Complete respons (UAS7 = 0) [Altrichter, 2024] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=99) |
gerandomiseerde trials |
niet ernstig |
niet ernstig |
ernstiga |
zeer ernstigb |
niet gevonden |
7/59 (11.9%) |
4/40 (10.0%) |
RR 1.19 (0.37 tot 3.79) |
19 meer per 1.000 (from 63 minder tot 279 meer) |
⨁◯◯◯ Zeer laag |
CRUCIAAL |
|
Gedeeltelijke respons (UAS7 ≤ 6) [Altrichter, 2024] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=99) |
gerandomiseerde trials |
niet ernstig |
niet ernstig |
ernstiga |
zeer ernstigb |
niet gevonden |
13/59 (22.0%) |
4/40 (10.0%) |
RR 2.20 (0.77 tot 6.27) |
120 meer per 1.000 (from 23 minder tot 527 meer) |
⨁◯◯◯ Zeer laag |
CRUCIAAL |
|
CU-Q2oL [Altrichter, 2024] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=99) |
gerandomiseerde trials |
niet ernstig |
niet ernstig |
ernstiga,c |
ernstigd |
niet gevonden |
Er was geen klinisch relevant verschil in least square mean tussen benralizumab en placebo. Benralizumab lijkt de kwaliteit van leven niet te verbeteren. |
|
|
|
⨁⨁◯◯ Laag |
BELANGRIJK |
|
DLQI [Altrichter, 2024] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=99) |
gerandomiseerde trials |
niet ernstig |
niet ernstig |
ernstiga,c |
ernstigd |
niet gevonden |
Er was geen klinisch relevant verschil in least square mean tussen benralizumab en placebo. Benralizumab lijkt de kwaliteit van leven niet te verbeteren. |
|
|
|
⨁⨁◯◯ Laag |
BELANGRIJK |
|
UAS7 [Altrichter, 2024] (follow up: 12 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=99) |
gerandomiseerde trials |
niet ernstig |
niet ernstig |
ernstiga,c |
ernstigd |
niet gevonden |
Er was geen klinisch relevant verschil in least square mean tussen benralizumab en placebo. Benralizumab lijkt de UAS7 niet te verbeteren. |
|
|
|
⨁⨁◯◯ Laag |
CRUCIAAL |
|
Veiligheid (bijwerkingen) [Altrichter, 2024] (follow up: 24 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=99) |
gerandomiseerde trials |
niet ernstig |
niet ernstig |
ernstiga |
zeer ernstigb |
niet gevonden |
34/59 (57.6%) |
23/40 (57.5%) |
RR 1.00 (0.66 tot 1.31) |
0 minder per 1.000 (from 195 minder tot 178 meer) |
⨁◯◯◯ Zeer laag |
CRUCIAAL |
|
Veiligheid (ernstige bijwerkingen) [Altrichter, 2024] (follow up: 24 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=99) |
gerandomiseerde trials |
niet ernstig |
niet ernstig |
ernstiga |
zeer ernstigb |
niet gevonden |
3/59 (5.1%) |
0/40 (0.0%) |
RR 5.02 (0.25 tot 99.83) |
0 minder per 1.000 (from 0 minder tot 0 minder) |
⨁◯◯◯ Zeer laag |
CRUCIAAL |
CI: Confidence interval; MD: Mean difference; RR: Risk ratio
Explanations
a. Dosering is benralizumab 30 mg elke 4 weken voor 12 weken
b. Zeer breed betrouwbaarheidsinterval waarbij het effect zowel klinisch relevant positief als klinisch relevant negatief kan zijn
c. LS mean en SE gebruikt
d. Betrouwbaarheidsinterval niet betrouwbaar gezien kleine steekproefomvang
Azathioprine versus placebo
|
Certainty assessment |
|
|
|
|
|
|
Aantal patiënten |
|
Effect |
|
Certainty |
Importantie |
|
Aantal studies |
Studieopzet |
Risk of bias |
Inconsistentie |
Indirect bewijs |
Onnauwkeurigheid |
Andere factoren |
Azathioprine |
placebo |
Relatief (95% CI) |
Absoluut (95% CI) |
|
|
|
TSS [Bhanja, 2015] (follow up: range 8 weken tot 36 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=52) |
gerandomiseerde trials |
ernstiga |
niet ernstig |
ernstigb |
ernstigc |
niet gevonden |
Het is onzeker wat het effect is van azathiprine op de TSS. |
|
|
|
⨁◯◯◯ Zeer laag |
CRUCIAAL |
|
Veiligheid (bijwerkingen) [Bhanja,2015] (follow up: 36 weken) |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 (n=52) |
gerandomiseerde trials |
ernstiga |
niet ernstig |
niet ernstig |
ernstigd |
niet gevonden |
Er waren twee patiënten in de interventie-groep met bijwerkingen. Het is onduidelijk of patiënten in de placebogroep bijwerkingen hadden. |
|
|
|
⨁⨁◯◯ Laag |
CRUCIAAL |
CI: Confidence interval
Explanations
a. Onduidelijk wat het risico is op selection en attrition bias. Er is een hoog risico op detection en reporting bias.
b. TSS is niet geïncludeerd als uitkomst in de PICO
c. Kleine steekproefomvang en betrouwbaarheidsintervallen niet genoemd
d. Kleine steekproefomvang, bijwerkingen in placebogroep niet genoemd
Er werden in totaal 27 studies geïncludeerd op basis van beoordeling van titel en abstract. Uiteindelijk zijn er na full tekst screening 22 studies geëxcludeerd. Er werd één publicatie aangeleverd door de werkgroep. Specifieke redenen voor exclusie zijn beschreven in de evidence tabellen.
Beschrijving van de resultaten
Azathioprine
De studie van Bhanja et al. (2015) betreft een RCT waarbij patiënten werden gerandomiseerd in een groep behandeld met azathioprine (n= 26) en een placebogroep (n=26). Patiënten met CU en een positieve autoloog serum huidtest werden geïncludeerd. Als uitkomst werd de ziekte ernst gemeten met total severity score (TSS). De TSS score in de interventie-groep gedurende alle meet momenten (8, 12, 4 en 36 weken) was significant beter dan in de placebogroep, er werden geen exacte aantallen en percentages beschreven. Er waren twee patiënten in de interventie-groep met bijwerkingen van braken en dunne ontlasting. De bewijskracht voor de effectiviteit van azathioprine is zeer laag, het is dus onduidelijk wat het effect is van azathioprine op de TSS.
Pathania et al. (2019) vergeleken in een prospectieve, gerandomiseerde studie de effectiviteit van azathioprine en ciclosporine in de behandeling van CSU. In totaal werden 40 patiënten gedurende 90 dagen behandeld met ciclosporine en 40 patiënten met azathioprine. Na 90 dagen behaalde 31 (79,5%) van de patiënten in de ciclosporinegroep en 32 (80%) in de azathioprinegroep een vermindering van 75% in de UAS7-score. Na 180 dagen behield 19 (47,95%) van de patiënten in de ciclosporinegroep en 24 (60%) in de azathioprinegroep deze 75% reductie. Deze verschillen waren niet significant. De gemiddelde UAS7-score nam in beide groepen aanzienlijk af, van respectievelijk 28,7 en 28,88 bij aanvang tot 5,56 in de ciclosporinegroep en 7,0 in de azathioprinegroep op de 90e dag.
Dapson/MTX
In de studie van Engin et al. [2007] werden 68 patiënten gerandomiseerd in twee groepen. De interventiegroep werd behandeld met dapson (n=38) en antihistaminica, terwijl de controlegroep alleen antihistaminica 28 (n=27) ontving. Na drie maanden werd een gemiddelde reductie in UAS7 van 7 waargenomen in de interventiegroep en 5,77 in de controlegroep (p < 0,001). Bijwerkingen kwamen voor bij vijf personen in de dapson-groep versus nul in de placebogroep.
Soni et al. (2023) onderzochten de effectiviteit van MTX en dapson bij patiënten met CSU. Er werden 200 participanten onderverdeeld in vier groepen; groep A (n=50) werd behandeld met dapson en antihistaminica voor 12 weken, groep B (n=50) met MTX en antihistaminica, groep C (n=50) met autologe serum huid therapie en groep D (n=50) werd behandeld met antihistaminica. In de dapson-groep hadden 28(56%) een goede respons (UAS7 score < 2 en DLQI score < 2) ten opzichte van 13(26%) in de antihistaminica-groep. In totaal hadden in de dapson-groep 21(42%) patiënten een redelijke respons (UAS7 score 2 - 4 en DLQI score 2 – 9) versus 11(22%) in de placebogroep.
De gevonden bewijskracht voor de effectiviteit is laag tot redelijk, vergelijkbaar met de bevindingen in de richtlijn van Zuberbier et al. (2022). Het effect dat hier werd gevonden, leek in het voordeel van dapson te zijn. Concluderend zou dapson de klachten van CSU enigszins kunnen verminderen.
In de MTX-groep hadden 15 (30%) een goede respons tegen over 13 (26%) in de antihistaminica-groep. In totaal hadden in de MTX-groep 25 (50%) patiënten een redelijke respons versus 11 (22%) in de placebogroep.
De gevonden bewijskracht is zeer laag tot redelijk. In de internationale richtlijn werd een zeer laag bewijs gevonden waarbij er geen verschil was in DLQI tussen MTX en placebo. Het is onzeker of MTX effectief is bij de behandeling van CSU.
Hydroxychloroquine
In een studie van Reeves et al. (2004) werden 18 patiënten gerandomiseerd voor hydroxychloroquine (n=9) of placebo (n=9). Naast de interventie mochten zij hun eigen medicatie (zoals corticosteroïden, H2-antihistaminica, H1-antihistaminica en doxepine) blijven doorgebruiken. Het gemiddelde verschil over 12 weken in de interventiegroep versus de placebogroep was als volgt: 2,01 versus 3,73 voor SF-12 (fysiek), 9,7 versus 4,58 voor SF12 (mentaal), 0,4 versus 5,2 voor de global symptom severity score (GSSS). Alleen voor de Global Symptom Severity Score (GSSS) bleek dit verschil significant. De bewijskracht voor het gevonden effect is zeer laag. Dit is een bevestiging van wat gevonden werd in de internationale richtlijn. Er werd hier geen verschil gevonden in effectiviteit en veiligheid tussen hydroxychloroquine en placebo. Het is onzeker wat het effect is van hydroxychloroquine op de kwaliteit van leven en de effectiviteit.
Benralizumab
De studie van Altrichter et al. (2024) is een dubbelblinde RCT naar de effectiviteit van benralizumab. In totaal werden 155 patiënten willekeurig verdeeld over drie groepen: benralizumab 30 mg elke 4 weken (n=59), benralizumab 60 mg elke 4 weken voor 12 weken gevolgd door 30 mg (n=56) en een placebogroep (n=40). Na 12 weken hadden 13 (22%) deelnemers in groep A een goede respons (UAS7 ≤ 6), terwijl dit in groep B 12 (21,2%) was en in de placebogroep 4(10%). Complete respons (UAS7 = 0) werd bereikt door 7 (11,9%) deelnemers in groep A, 4 (7,1%) in groep B en 4 (10,0%) in de placebogroep.
Na 12 weken was het least-squares gemiddelde UAS7 verlaagd met 14,48 in groep A 16,77 in groep B en 12,41 in de placebogroep. De CU-Q2oL was met 16,7 verlaagd in groep A, 20,34 in groep B en 18,10 in de placebogroep. Als laatste was de DLQI in groep A verlaagd met 7,58, in groep B verlaagd met 9,31 en in de placebogroep met 8,06.
Het effect op de effectiviteit was niet groot en de bewijskracht was zeer laag tot laag. Het is onzeker wat het effect is van benralizumab op de kwaliteit van leven en de klachten.
Risk of bias
De vijf geïncludeerde studies hebben redelijk hoge risk of bias. Met name Engin et al. (2007) heeft een verhoogd risco op bias namelijk op selectie, performance en detectie bias. Reeves et al. (2004) en Bhanja et al. (2015) beschreven hun randomisatiemethode niet, of deden dit onduidelijk, waardoor niet duidelijk is of er sprake kan zijn van selectiebias in deze studies.
De Risk of bias analyse is te vinden in de evidence tabellen.
Om de uitgangsvraag te beantwoorden zijn de uitkomsten te vinden in het evidence report van de internationale richtlijn van Zuberbier et al. (2022) als basis genomen. De zoekstrategie van Zuberbier et al. (2022) liep tot 2020. Om de recentere gepubliceerde artikelen te includeren in de richtlijn is een systematische literatuuranalyse vanaf 2020 uitgevoerd. Sommige middelen werden door Zuberbier et al. (2022) niet opgenomen in de richtlijn, hiervoor is de systematische literatuuranalyse verder uitgebreid.
Voor dit onderzoek is de volgende PICO opgesteld:
| P: | Patiënten met CU |
| I: |
Dapson Methotrexaat/MTX Azathioprine Mycofenolaatmofetil UV-B Hydroxychloroquine/Plaquenil Rituximab Anti-IL-5 Anti-IL-17 Anti-IL-23 Anti-TNF |
| C: | Placebo of add-on vergelijkingen |
| O: |
Gemiddelde afname in wekelijkse Urticaria activiteitenscore (UAS7) Bijwerkingen Percentage deelnemers dat binnen een maand na het stoppen met de interventie terugvalt Percentage deelnemers met volledige onderdrukking van urticaria Percentage deelnemers met 'goede' of 'uitstekende' respons Verbetering in kwaliteit van leven |
De werkgroep definieerde de uitkomstmaten als volgt en hanteerde de in de studies gebruikte definities.
Primair (cruciaal):
- Gemiddelde afname in wekelijkse Urticaria activiteitenscore (UAS7)
- Bijwerkingen
- Percentage deelnemers dat binnen een maand na het stoppen met de interventie terugvalt
- Percentage deelnemers met volledige onderdrukking van urticaria
- Percentage deelnemers met 'goede' of 'uitstekende' respons
Secundair (belangrijk):
- Verbetering in kwaliteit van leven
Er werd een systematische zoekstrategie uitgevoerd in de elektronische databases Embase en Medline. De zoekstrategie is toegevoegd in bijlage 2. Studies werden geïncludeerd wanneer deze overeenkwamen met de elementen van de PICO en aan de volgende in- en exclusiecriteria voldeden:
Inclusie:
- Patiënten met CSU
- SR, RCT’s en CCT’s, observationeel vergelijkende studies
- Volledig tekst beschikbaar in Nederlands of Engels
Exclusie:
- Dierenstudies
- Follow-up van korter dan 4 weken
- Observationeel niet vergelijkende studies
- Altrichter, S., Giménez-Arnau, A. M., Bernstein, J. A., Metz, M., Bahadori, L., Bergquist, M., Brooks, L., Ho, C. N., Jain, P., Lukka, P. B., Rodriguez-Suárez, E., Walton, C., & Datto, C. J. (2024). Benralizumab does not elicit therapeutic effect in patients with chronic spontaneous urticaria: Results from the phase IIb multinational randomized double-blind placebo-controlled ARROYO trial. British Journal of Dermatology, 190(1), 1-13. https://doi.org/10.1111/bjd.12345.
- Bhanja, D. C., Ghoshal, L., Das, S., Das, S., & Roy, A. K. (2015). Azathioprine in autologous serum skin test positive chronic urticaria: A case-control study in a tertiary care hospital of eastern India. Indian dermatology online journal, 6(3), 185–188. https://doi.org/10.4103/2229-5178.156391.
- Engin, B., & Ozdemir, M. (2008). Prospective randomized non-blinded clinical trial on the use of dapsone plus antihistamine vs. antihistamine in patients with chronic idiopathic urticaria. Journal of the European Academy of Dermatology and Venereology : JEADV, 22(4), 481–486. https://doi.org/10.1111/j.1468-3083.2007.02510.x.
- Pathania, Y. S., Bishnoi, A., Parsad, D., Kumar, A., & Kumaran, M. S. (2019). Comparing azathioprine with cyclosporine in the treatment of antihistamine refractory chronic spontaneous urticaria: A randomized prospective active-controlled non-inferiority study. The World Allergy Organization journal, 12(5), 100033. https://doi.org/10.1016/j.waojou.2019.100033.
- Reeves, G. E., Boyle, M. J., Bonfield, J., Dobson, P., & Loewenthal, M. (2004). Impact of hydroxychloroquine therapy on chronic urticaria: chronic autoimmune urticaria study and evaluation. Internal medicine journal, 34(4), 182–186. https://doi.org/10.1111/j.1444-0903.2004.00532.x.
- Soni, P., Yadav, M., & Arora, A. (2023). To evaluate the efficacy of Methotrexate versus Dapsone/ASST in the treatment of chronic urticaria. International Journal of Life Sciences Biotechnology and Pharma Research, 12(3), 1-13.
- Zuberbier, T., Abdul Latiff, A. H., Abuzakouk, M., Aquilina, S., Asero, R., Baker, D., Ballmer-Weber, B., Bangert, C., Ben-Shoshan, M., Bernstein, J. A., Bindslev-Jensen, C., Brockow, K., Brzoza, Z., Chong Neto, H. J., Church, M. K., Criado, P. R., Danilycheva, I. V., Dressler, C., Ensina, L. F., Fonacier, L., … Maurer, M. (2022). The international EAACI/GA²LEN/EuroGuiDerm/APAAACI guideline for the definition, classification, diagnosis, and management of urticaria. Allergy, 77(3), 734–766. https://doi.org/10.1111/all.15090.
Risico op bias tabellen
Randomized controlled trial (RCT)
Beoordeling risk of bias door middel van Cochrane collaboration tool.
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Random sequence generation (selection bias)2
(high/unclear/low risk) |
Allocation concealment (selection bias)3
(high/unclear/low risk) |
Blinding of participants and personnel (performance bias)4,6 All outcomes
(high/unclear/low risk) |
Blinding of outcome assessor (detection bias)5,6 All outcomes
(high/unclear/low risk) |
Incomplete outcome data (attrition bias)7 All outcomes
(high/unclear/low risk) |
Selective reporting (reporting bias)8
(high/unclear/low risk) |
Other bias9
(high/unclear/low risk) |
|
Reeves, 2004 |
Niet beschreven |
Unclear risk |
Unclear risk |
Unclear risk |
High risk |
Low risk 14% lost to follow up redenen genoemd |
Unclear risk |
Low risk |
|
Engin, 2007 |
De participanten warden gelabeld, vervolgens werd een tabel met willeukerige getallen gebruikt. |
Low risk |
High risk |
High risk |
High risk |
Unclear risk |
Unclear risk |
Low risk |
|
Soni, 2023 |
De participanten werden willekeurig gerandomiseerd op basis van UAS en DLQI score |
Unclear risk |
Unclear risk |
Unclear risk |
Unclear risk |
Unclear risk |
Unclear risk |
Low risk |
|
Altrichter, 2024 |
Patiënten werden willekeurig toegewezen en gestratificeerd op geografische regio met behulp van een interactief spraak-/webresponssysteem. |
Low risk |
Low risk |
Low risk |
Low risk |
Low risk 7,7% lost to follow up |
Unclear risk |
Low risk |
|
Bhanja, 2015 |
Ondoorzichtige enveloppen met een volgnummer |
Unclear risk |
Low risk |
Low risk |
High risk |
Unclear risk 13,3% lost to follow up geen redenen genoemd |
High risk |
Unclear risk |
Overzicht van geëxcludeerde studies
|
Artikel |
Reden van exclusie |
|
Bernstein, 2020 |
Geen controlegroep |
|
Boonpiyathad, 2017 |
Al opgenomen in internationale richtlijnen |
|
Chen, 2024 |
Interventie komt niet overeen met PICO |
|
Di gioacchino, 2003 |
Artikel niet gevonden |
|
Gabizon, 2020 |
Geen controlegroep |
|
Giménez, 2022 |
Interventie komt niet overeen met PICO |
|
Goswamy, 2022 |
Geen CU, alleen patiënten met angio oedeem |
|
Grattan, 2000 |
Al opgenomen in internationale richtlijnen |
|
Honeywell, 2007 |
Artikel niet gevonden |
|
Jain, 2024 |
Geen controlegroep |
|
Kim, 2023 |
Interventie komt niet overeen met PICO |
|
Leducq, 2020 |
Al opgenomen in internationale richtlijnen |
|
Maurer, 2022 |
Interventie komt niet overeen met PICO |
|
Maurer, 2024 |
Interventie komt niet overeen met PICO |
|
Morgan, 2014 |
Al opgenomen in internationale richtlijnen |
|
Pathania, 2019 |
Geen controlegroep |
|
Sanchez, 2020 |
Geen controlegroep |
|
Serhat inaloz, 2008 |
Komt niet overeen met PICO |
|
Shah, 2022 |
Geen controlegroep |
|
Sussman, 2020 |
Komt niet overeen met PICO |
|
Vena, 2006 |
Reeds opgenomen in internationale richtlijn |
|
Yuan, 2022 |
Interventie komt niet overeen met PICO |
Beoordelingsdatum en geldigheid
Publicatiedatum : 28-01-2026
Beoordeeld op geldigheid : 28-01-2026
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep grotendeels in stand gehouden. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update).
De Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV) is regiehouder van deze richtlijn Chronische Urticaria (CU) en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
Algemene gegevens
Aanleiding en afbakening onderwerp
Op initiatief van de Nederlandse Vereniging voor Dermatologie en Venereologie is de richtlijn chronische urticaria in 2023-2024 modulair herzien. De herziening betreft overwegend de toevoeging van nieuwe modules met klinische relevante onderwerpen welke ontbraken of toe waren aan herziening: classificatie, monitoring van ziekteactiviteit, ziektecontrole en ziektelast, behandeling van CSU en CIndU bij volwassenen, behandeling bij kinderen, behandeling tijdens zwangerschap, borstvoeding en kinderwens, organisatie van zorg en gepersonaliseerd behandelplan.
Financiering
De ontwikkeling van deze richtlijn is gefinancierd door de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De SKMS ondersteunt medisch-specialistische beroepsverenigingen bij het bevorderen van de kwaliteit van zorg. De financiering heeft geen invloed gehad op de inhoudelijke totstandkoming van de richtlijn. De werkgroep heeft onafhankelijk gewerkt conform de geldende methodologische standaarden.
Doel en doelgroep
Doel
Deze richtlijn is een document met aanbevelingen ter ondersteuning van de dagelijkse praktijkvoering. De richtlijn berust op de resultaten van wetenschappelijk onderzoek en aansluitende meningsvorming gericht op het vaststellen van goed medisch handelen. De richtlijn geeft aanbevelingen over begeleiding en behandeling van patiënten met chronische urticaria.
Doelgroep
De richtlijn is bestemd voor leden van de medische en paramedische beroepsgroep. Daartoe behoren onder andere: Dermatologen, verpleegkundig specialisten, physician assistants, Secundair kan de richtlijn nuttig zijn voor internisten, allergologen, kinderartsen, huisartsen en apothekers. Voor patiënten werd informatie op thuisarts.nl en een patiënten folder ontwikkeld.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn werd een multidisciplinaire werkgroep ingesteld. Bij het samenstellen van de werkgroep werd rekening gehouden met de geografische spreiding van de werkgroepleden en met een evenredige vertegenwoordiging van academische en niet-academische achtergrond. De werkgroepleden hebben onafhankelijk gehandeld en geen enkel lid ontving gunsten met het doel de richtlijnen te beïnvloeden. Naast de afgevaardigden van de verschillende beroepsgroepen is er ook een patiëntvertegenwoordiger betrokken geweest bij de ontwikkeling van de richtlijn.
|
Werkgroepleden |
Vereniging |
|
Dr. H. Röckman, dermatoloog (voorzitter) |
NVDV |
|
Dr. M.B.A. van Doorn, dermatoloog |
NVDV |
|
Drs. B. Peters, dermatoloog |
NVDV |
|
Drs. M. Stadermann, kinderarts-allergoloog |
NVK |
|
Dr. J.N.G. Oude Elberink, internist-allergoloog |
NVvAKI |
|
P.A. Kentie, verpleegkundig specialist |
V&VN |
|
Prof. Dr. E.P. van Puijenbroek, arts, klinisch farmacoloog |
Lareb |
|
P. van den Broek, patiëntvertegenwoordiger |
HN |
|
C. Berkhof, patiëntvertegenwoordiger |
PU |
|
Ondersteuning werkgroep |
Vereniging |
|
Drs. T. M. Nlgisang, arts-onderzoeker (vanaf juni 2023) |
NVDV |
|
Drs. L.J. van den Oord, arts-onderzoeker (vanaf april 2024) |
NVDV |
|
Dr. W.A. van Enst, klinisch epidemioloog & directeur NVDV |
NVDV |
|
Drs. M.R. Masselink, arts-onderzoeker (vanaf april 2025) |
NVDV |
|
Drs. T. A. Teunissen, arts-onderzoeker (vanaf april 2025) |
NVDV |
Belangenverklaringen
De KNMG-Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of ze in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciëring) of indirecte belangen (persoonlijke relaties, reputatie management, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van de Nederlandse Vereniging voor Dermatologie en Venereologie.
|
Werkgroeplid |
Hoofdfunctie(s) |
Nevenfunctie(s) |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Getekend op |
Acties (voorstel) |
|
Mw. Dr. H. Röckman, (voorzitter) |
Dermatoloog (UMC Utrecht) |
Geen |
(nationale) global adviesraad Novartis Sanofi
Research Roundup ThirdHarmonic
Spreker vergoeding Novartis |
Geen |
Geen |
Geen |
Geen |
16-4-2023 |
Geen |
|
Dhr. Dr. M.B.A. van Doorn |
Dermatoloog-klinisch farmacoloog (Erasmus MC) 0,8 fte
Dermatoloog-klinisch farmacoloog (Centre for Human Drug Research) 0,2 fte |
Spreker, deelname aan adviesraden en organisatie van nascholingen i.s.m. de farmaceutische industrie waarvoor financiële vergoeding (Novartis, AbbVie, Pfizer, LEO pharma, Sanofi, Lilly, Janssen, UCB, BMS, Celgene, Third Harmonic) |
Adviseur voor Novartis (deelname adviesraden) |
Geen |
Uitvoering/deelname aan verschillende extern gefinancierde clinical trials op gebied van chronische urticaria (Novartis, Sanofi, ThirdHarmonic) |
Geen |
Geen |
25-09-2023 |
Geen |
|
Dhr. Drs. B. Peters |
Dermatoloog (Rijnstate) |
|
|
|
|
|
|
|
|
|
Mw. Drs. M. Stademann |
Kinderarts-allergoloog (UMC Utrecht en Diakonessenhuis Utrecht)
Adviseur Allergie team (Kinderkliniek Almere) |
Bestuursectie KinderAllergologie (NVK)
Organisator basiscurcus kinderallergologie |
Geen |
Geen |
Geen |
Geen |
Geen |
16-11-2023 |
Geen |
|
Mw. Dr. J.N.G. Oude Elberink |
Internist-allergoloog (UMCG) |
|
|
|
|
|
|
|
|
|
Mw. P.A. Kentie |
Verpleegkundig specialist allergologie (UMC Utrecht) |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
23-09-2023 |
Geen |
|
Dhr. Prof. Dr. E.P. van Puijenbroek |
Senior adviseur Bijwerkingen centrum Lareb |
Verbonden aan Rijksuniversiteit Groningen waarvan tot 1 maart 2024 als bijzonder hoogleraar |
Geen |
Geen |
Geen |
Geen |
Geen |
29-72024 |
Geen |
|
Dhr. P. van den Broek |
Eigenaar Van den Broek Advies & Interim
Adviseur/projectleider voor Huid Nederland
Een deel van die activiteiten wordt mede mogelijk gemaakt door externe financiëring van Novartis (publicatie naar patiënten in kader van Wereldnetelroosdag, informatie over urticaria op de websittes Patiëntenplatform Urticaria en Huid Nederland). Die activiteiten staan los van de inzet in het kader van de richtlijnen
|
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
22-09-2023 |
Geen |
|
Dhr. C. Berkhof |
Patiëntenvertegenwoordiger
Key Accountmanager Benelux Sunrise Medical BV |
Beheerder van de Facebook Pagina Urticaria NL/BE; met 800+ leden.
Eigenaar van de website www.urticaria.nl
Alle werkzaamheden zijn onbetaald vanuit een derde partij; dit wordt betaald uit eigen (privé) middelen.
EMA; soms meedenken of deelname over het uitvoeren van nieuwe studies |
Geen |
Geen |
Geen |
Geen |
Geen |
22-09-2023 |
Geen |
Inbreng patiëntenperspectief
Er is aandacht besteed aan het patiënten perspectief in alle modules van de herziende richtlijn Chronische Urticaria door de zitting neming van afgevaardigden van Huid Nederland (HN) en Patiëntenplatform Urticariapatiënt (PU) in de werkgroep en de opname van een module over patiëntenvoorlichting. conceptrichtlijn is tevens voor commentaar voorgelegd aan HN en PU.
Wkkgz & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Bij de richtlijn is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (gebaseerd op het stroomschema ontwikkeld door FMS).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst Raming |
Toelichting |
|
Overige behandeling van volwassenen met CU |
Geen substantiële financiële gevolgen |
Uit de toetsing volgt dat de aanbevelingen(en) niet breed toepasbaar zijn (<5.000 patiënten) en zal daarom naar verwachting geen substantiële financiële gevolgen hebben voor de collectieve uitgaven |
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn(module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. De richtlijn wordt via het internet verspreid onder alle relevante beroepsgroepen en ziekenhuizen en er zal in verschillende specifieke vaktijdschriften aandacht worden besteed aan de richtlijn. Tevens zal een samenvatting worden gemaakt. De voorlichtingsfolder van de NVDV zal worden afgestemd op de richtlijn. Het volledige implementatieplan is opgenomen in het bijlagedocument.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Onderstaand is de methode stapsgewijs beschreven.
Knelpuntenanalyse
In de voorbereidingsfase heeft een bijeenkomst plaatsgevonden waarvoor alle belanghebbenden zijn uitgenodigd. In deze bijeenkomst zijn knelpunten aangedragen door de werkgroepleden en gemandateerde van verschillende (wetenschappelijke) verenigingen en stakeholders.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse heeft de werkgroep uitgangsvragen opgesteld. Daarbij inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Voor de afzonderlijke uitgangsvragen werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen en consultatie van experts. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. Literatuur is geselecteerd op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden bij de Zoekverantwoording.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR - voor systematische reviews; Cochrane - voor gerandomiseerd gecontroleerd onderzoek; Newcastle-Ottowa - voor observationeel onderzoek; QUADAS II – voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen zijn overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs (2021)
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/). GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog
|
|
|
Redelijk
|
|
|
Laag
|
|
|
Zeer laag
|
|
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
C) Voor vragen over de waarde van meet- of classificatie-instrumenten (klinimetrie)
Deze instrumenten werden beoordeeld op validiteit, intra- (test-hertest) en inter-beoordelaarsbetrouwbaarheid, responsiviteit (alleen bij meetinstrumenten) en bruikbaarheid in de praktijk. (naar keuze: optie-1 ‘Bij ontbreken van een gouden standaard, werd een beoordeling van de bewijskracht van literatuurconclusies achterwege gelaten.’ Of optie-2 ‘De kracht van het wetenschappelijk bewijs werd bepaald met de generieke GRADE-methode’).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in één of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overkoepelende bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overkoepelende conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk. Door gebruik te maken van de Guideline Development Tool werd het Evidence to decision framework conform GRADE methodiek toegepast. Alle werkgroepleden hebben systematisch antwoord gegeven op vragen over de grootte van het effect en grootte van negatieve consequenties, waarden en voorkeuren van de patiënt, kosten en kosteneffectiviteit, beschikbaarheid van voorzieningen, aanvaardbaarheid, en overwegingen voor subgroepen in de patiëntenpopulatie. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van zorg.
Indicatorontwikkeling
Er werden geen indicatoren ontwikkeld voor deze richtlijn.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling beschreven (zie bijlagen bij de modules).
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften maar wetenschappelijk onderbouwde en breed gedragen inzichten en aanbevelingen waaraan zorgverleners zouden moeten voldoen om kwalitatief goede zorg te verlenen. Aangezien richtlijnen uitgaan van ‘gemiddelde patiënten’, kunnen zorgverleners in individuele gevallen zo nodig afwijken van de aanbevelingen in de richtlijn. Afwijken van richtlijnen is, als de situatie van de patiënt dat vereist, soms zelfs noodzakelijk. Een richtlijn beschrijft wat goede zorg is, ongeacht de financieringsbron Zorgverzekeringswet (Zvw), Wet langdurige zorg (Wlz), Wet maatschappelijke ondersteuning (Wmo), aanvullende verzekering of eigen betaling door de cliënt/patiënt. Opname van een richtlijn in een register betekent dus niet noodzakelijkerwijs dat de in de richtlijn beschreven zorg verzekerde zorg is. Informatie over kosten zoals beschreven in de richtlijn is gebaseerd op beschikbare gegevens ten tijde van schrijven.
Commentaar- en autorisatiefase
De conceptrichtlijn is aan de betrokken (wetenschappelijke) verenigingen, (patiënt) organisaties en stakeholders voorgelegd ter commentaar (zie ook tabel 1). De commentaren zijn verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren is de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn is aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter autorisatie.
Literatuur
Brouwers MC, Kho ME, Browman GP, et al. AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in health care. CMAJ. 2010;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348.
Higgins JPT, Green S (editors). Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0 [updated March 2011]. The Cochrane Collaboration, 2011. Available from www.handbook.cochrane.org.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwalitieit.. Online beschikbaar op http://richtlijnendatabase.nl/ Laatst geraadpleegd op [DATUM geraadpleegd voor concepttekst].
Van Everdingen JJE, Burgers JS, Assendelft WJJ, et al. Evidence-based richtlijnontwikkeling. Bohn Stafleu Van Loghum 2004.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Zoekverantwoording
Behandeling van chronische urticaria [TT1] (CSU en CIndU) overkoepelende zoekopdracht
De volgende afbakening is gebruikt:
Voor de P: Patiënten met CSU en CIndU
Voor de I: Tweede generatie antihistaminica (cetirizine, desloradatine, ebastine, fexofenadine, levocetirizine, rupatadine)
Leukotriene receptor antagonisten
Omalizumab
Ciclosporine
Orale corticosteroïden (prednison, prednisolon, methylprednisolon, triamcinolon, betamethason, dexamethason)
Remibrutinib
Dupilumab
Dapson
Methotrexaat/MTX
Azathioprine
Mycofenolaatmofetil
UVB
Hydroxychloroquine/Plaquenil
Rituximab
Anti-IL-5
Anti-IL-17
Anti-IL-23
Anti-TNF
Voor de C: Placebo of add-on vergelijkingen
Voor de O: Gemiddelde afname in wekelijkse Urticaria activiteitenscore (UAS7)
Bijwerkingen
Percentage deelnemers dat binnen een maand na het stoppen met de interventie terugvalt
Percentage deelnemers met volledige onderdrukking van urticaria
Percentage deelnemers met 'goede' of 'uitstekende' respons
Verbetering in kwaliteit van leven
Inclusie- en exclusiecriteria
|
Inclusiecriteria |
Exclusiecriteria |
|
Patiënten met CSU en CIndU |
Dierenstudies |
|
SR, RCT’s en CCT’s, observationeel vergelijkende studies vanaf 2020 |
Follow-up van korter dan 4 weken |
|
Volledig tekst beschikbaar in Nederlands of Engels |
Observationeel niet vergelijkende studies |
Uitgangsvragen
- Wat is de aanbevolen behandeling voor volwassenen met CSU en kan het huidige stepped care model worden aangepast?
- Welke overige behandelmogelijkheden worden aanbevolen als het stepped care model onvoldoende effect geeft bij volwassenen met CSU?
- Welke behandeling wordt aanbevolen voor volwassenen met CIndU en kan hier een stepped care model voor worden gemaakt?
EMBASE (3-4-2024)
Zoektermen
- 'urticaria'/exp OR urticaria*:ti,ab,kw OR weal:ti,ab,kw OR wheal:ti,ab,kw OR wealing:ti,ab,kw OR weals:ti,ab,kw OR whealing:ti,ab,kw OR wheals:ti,ab,kw OR dermatographi*:ti,ab,kw OR 'muckle wells syndrome*':ti,ab,kw OR 'schnitzler syndrome*':ti,ab,kw OR hives:ti,ab,kw OR ((vibrator* NEAR/3 (angioedema OR angiooedema OR 'angio edema' OR 'angio oedema')):ti,ab,kw)
- #1 AND [2020-2024]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)
- 'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti
- #2 AND #3 Clinical trials
Resultaten = 1779
MEDLINE (3-4-2024)
Zoektermen
- exp Urticaria/ or urticaria*.ti,ab,kf. or weal.ti,ab,kf. or wheal.ti,ab,kf. or wealing.ti,ab,kf. or weals.ti,ab,kf. or whealing.ti,ab,kf. or wheals.ti,ab,kf. or dermatographi*.ti,ab,kf. or muckle wells syndrome*.ti,ab,kf. or schnitzler syndrome*.ti,ab,kf. or hives.ti,ab,kf. or (vibrator* adj3 (angioedema or angiooedema or angio edema or angio oedema)).ti,ab,kf.
- 2 limit 1 to yr="2020 - 2024"
- exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.
- 2 and 3 Clinical trials
Resultaten = 568
Alle resultaten
|
Database |
Datum |
# hits |
|
EMBASE |
3-4-2024 |
1779 |
|
MEDLINE |
3-4-2024 |
568 |
|
Totaal |
2347 |
|
|
Duplicates |
317 |
|
|
Netto aantal |
2030 |
|
Behandeling van chronische urticaria [TT1] (CSU en CIndU) bij volwassenen
De volgende afbakening is gebruikt:
Voor de P: Volwassen (>17 jaar) patiënten met CSU en CIndU
Voor de I:
Remibrutinib
Dupilumab
Azathioprine
Mycofenolaatmofetil
Anti-IL-5
Anti-IL-17
Anti-IL-23
Anti-TNF
Voor de C: Placebo of add-on vergelijkingen
Voor de O: Gemiddelde afname in wekelijkse Urticaria activiteitenscore (UAS7)
Bijwerkingen
Percentage deelnemers dat binnen een maand na het stoppen met de interventie terugvalt
Percentage deelnemers met volledige onderdrukking van urticaria
Percentage deelnemers met 'goede' of 'uitstekende' respons
Verbetering in kwaliteit van leven
Inclusie- en exclusiecriteria
|
Inclusiecriteria |
Exclusiecriteria |
|
Volwassen patiënten met CSU en CIndU |
Dierenstudies |
|
SR, RCT’s en CCT’s, observationeel vergelijkende studies van 1990-2020 |
Follow-up van korter dan 4 weken |
|
Volledig tekst beschikbaar in Nederlands of Engels |
Observationeel niet vergelijkende studies |
Uitgangsvragen
- Wat is de aanbevolen behandeling voor volwassenen met CSU en kan het huidige stepped care model worden aangepast?
- Welke overige behandelmogelijkheden worden aanbevolen als het stepped care model onvoldoende effect geeft bij volwassenen met CSU?
- Welke behandeling wordt aanbevolen voor volwassenen met CIndU en kan hier een stepped care model voor worden gemaakt?
EMBASE (25-4-2024)
Zoektermen
- 'urticaria'/exp OR urticaria*:ti,ab,kw OR weal:ti,ab,kw OR wheal:ti,ab,kw OR wealing:ti,ab,kw OR weals:ti,ab,kw OR whealing:ti,ab,kw OR wheals:ti,ab,kw OR dermatographi*:ti,ab,kw OR 'muckle wells syndrome*':ti,ab,kw OR 'schnitzler syndrome*':ti,ab,kw OR hives:ti,ab,kw OR ((vibrator* NEAR/3 (angioedema OR angiooedema OR 'angio edema' OR 'angio oedema')):ti,ab,kw)
- 'remibrutinib'/exp OR 'remibrutinib':ti,ab,kw
- 'dupilumab'/exp OR 'dupilumab':ti,ab,kw OR 'dupixent':ti,ab,kw
- 'azathioprine'/exp OR 'arathioprin':ti,ab,kw OR 'arathioprine':ti,ab,kw OR 'azafalk':ti,ab,kw OR 'azafor':ti,ab,kw OR 'azahexal':ti,ab,kw OR 'azamedac':ti,ab,kw OR 'azamun':ti,ab,kw OR 'azanin':ti,ab,kw OR 'azapin':ti,ab,kw OR 'azapress':ti,ab,kw OR 'azaprine':ti,ab,kw OR 'azarex':ti,ab,kw OR 'azasan':ti,ab,kw OR 'azathiodura':ti,ab,kw OR 'azathiopine':ti,ab,kw OR 'azathioprim':ti,ab,kw OR 'azathioprin':ti,ab,kw OR 'azathioprine':ti,ab,kw OR 'azathiopurine':ti,ab,kw OR 'azathropsin':ti,ab,kw OR 'azatioprina':ti,ab,kw OR 'azatox':ti,ab,kw OR 'azatrilem':ti,ab,kw OR 'azopi':ti,ab,kw OR 'azoran':ti,ab,kw OR 'azothioprin':ti,ab,kw OR 'azothioprine':ti,ab,kw OR 'colinsan':ti,ab,kw OR 'immuran':ti,ab,kw OR 'immurel':ti,ab,kw OR 'immuthera':ti,ab,kw OR 'imunen':ti,ab,kw OR 'imuprin':ti,ab,kw OR 'imuran':ti,ab,kw OR 'imurane':ti,ab,kw OR 'imurek':ti,ab,kw OR 'imurel':ti,ab,kw OR 'imuren':ti,ab,kw OR 'jayempi':ti,ab,kw OR 'oraprine':ti,ab,kw OR 'ozathuia':ti,ab,kw OR 'thioazeprine':ti,ab,kw OR 'thioprine':ti,ab,kw OR 'transimune':ti,ab,kw OR 'zytrim':ti,ab,kw
- 'mycophenolate mofetil'/exp OR 'cell cept':ti,ab,kw OR 'cellcept':ti,ab,kw OR 'cellsept':ti,ab,kw OR 'mowel':ti,ab,kw OR 'munoloc':ti,ab,kw OR 'myclausen':ti,ab,kw OR 'mycofit':ti,ab,kw OR 'mycolat':ti,ab,kw OR 'myfenax':ti,ab,kw OR 'trixin':ti,ab,kw
- 'interleukin 5 antibody'/exp OR 'interleukin 17 antibody'/exp OR 'interleukin 23 antibody'/exp OR 'interleukin 5 antibod*':ti,ab,kw OR 'il5 antibod*':ti,ab,kw OR 'il 17 antibod*':ti,ab,kw OR 'interleukin 17 antibody*':ti,ab,kw OR 'il 23 antibod*':ti,ab,kw OR 'interleukin 23 antibod*':ti,ab,kw OR ((('anti interleukin' OR 'anti il') NEAR/2 (5 OR 17 OR 23)):ti,ab,kw)
- 'tumor necrosis factor inhibitor'/exp OR 'tnf alpha inhibitor*':ti,ab,kw OR 'tnf inhibitor*':ti,ab,kw OR 'anti tnf agent*':ti,ab,kw OR 'anti tnf alpha agent*':ti,ab,kw OR 'anti tumor necrosis factor agent*':ti,ab,kw OR 'anti tumour necrosis factor agent*':ti,ab,kw OR 'tumor necrosis factor alpha inhibitor*':ti,ab,kw OR 'tumor necrosis factor inhibitor*':ti,ab,kw OR 'tumour necrosis factor alpha inhibitor*':ti,ab,kw OR 'tumour necrosis factor inhibitor*':ti,ab,kw
- #2 OR #3 OR #4 OR #5 OR #6 OR #7
- #1 AND #8
- #9 NOT (('adolescent'/exp OR 'child'/exp OR adolescent*:ti,ab,kw OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw))
- #10 AND [1990-2020]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)
- 'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab
- 'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti
- 'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)
- 'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab)))
- #11 AND #12 SR
- #11 AND #13 NOT #16 Clinical trials, RCTs
- #11 AND (#14 OR #15) NOT #16 NOT #17 OBS
- #16 OR #17 OR #18
Resultaten = 1059
MEDLINE (25-4-2024)
Zoektermen
- exp Urticaria/ or urticaria*.ti,ab,kf. or weal.ti,ab,kf. or wheal.ti,ab,kf. or wealing.ti,ab,kf. or weals.ti,ab,kf. or whealing.ti,ab,kf. or wheals.ti,ab,kf. or dermatographi*.ti,ab,kf. or muckle wells syndrome*.ti,ab,kf. or schnitzler syndrome*.ti,ab,kf. or hives.ti,ab,kf. or (vibrator* adj3 (angioedema or angiooedema or angio edema or angio oedema)).ti,ab,kf.
- 1 not ((Adolescent/ or Child/ or Infant/ or adolescen*.ti,ab,kf. or child*.ti,ab,kf. or schoolchild*.ti,ab,kf. or infant*.ti,ab,kf. or girl*.ti,ab,kf. or boy*.ti,ab,kf. or teen.ti,ab,kf. or teens.ti,ab,kf. or teenager*.ti,ab,kf. or youth*.ti,ab,kf. or pediatr*.ti,ab,kf. or paediatr*.ti,ab,kf. or puber*.ti,ab,kf.) not (Adult/ or adult*.ti,ab,kf. or man.ti,ab,kf. or men.ti,ab,kf. or woman.ti,ab,kf. or women.ti,ab,kf.))
- 1 and 2
- remibrutinib.ti,ab,kf.
- (dupilumab or dupixent).ti,ab,kf.
- exp Azathioprine/ or arathioprin.ti,ab,kf. or arathioprine.ti,ab,kf. or azafalk.ti,ab,kf. or azafor.ti,ab,kf. or azahexal.ti,ab,kf. or azamedac.ti,ab,kf. or azamun.ti,ab,kf. or azanin.ti,ab,kf. or azapin.ti,ab,kf. or azapress.ti,ab,kf. or azaprine.ti,ab,kf. or azarex.ti,ab,kf. or azasan.ti,ab,kf. or azathiodura.ti,ab,kf. or azathiopine.ti,ab,kf. or azathioprim.ti,ab,kf. or azathioprin.ti,ab,kf. or azathioprine.ti,ab,kf. or azathiopurine.ti,ab,kf. or azathropsin.ti,ab,kf. or azatioprina.ti,ab,kf. or azatox.ti,ab,kf. or azatrilem.ti,ab,kf. or azopi.ti,ab,kf. or azoran.ti,ab,kf. or azothioprin.ti,ab,kf. or azothioprine.ti,ab,kf. or colinsan.ti,ab,kf. or immuran.ti,ab,kf. or immurel.ti,ab,kf. or immuthera.ti,ab,kf. or imunen.ti,ab,kf. or imuprin.ti,ab,kf. or imuran.ti,ab,kf. or imurane.ti,ab,kf. or imurek.ti,ab,kf. or imurel.ti,ab,kf. or imuren.ti,ab,kf. or jayempi.ti,ab,kf. or oraprine.ti,ab,kf. or ozathuia.ti,ab,kf. or thioazeprine.ti,ab,kf. or thioprine.ti,ab,kf. or transimune.ti,ab,kf. or zytrim.ti,ab,kf.
- exp Mycophenolic Acid/ or cell cept.ti,ab,kf. or cellcept.ti,ab,kf. or cellsept.ti,ab,kf. or mowel.ti,ab,kf. or munoloc.ti,ab,kf. or myclausen.ti,ab,kf. or mycofit.ti,ab,kf. or mycolat.ti,ab,kf. or myfenax.ti,ab,kf. or trixin.ti,ab,kf.
- exp Interleukin-5/ or exp Interleukin-17/ or exp Interleukin-23/ or interleukin 5 antibod*.ti,ab,kf. or il5 antibod*.ti,ab,kf. or il 17 antibod*.ti,ab,kf. or interleukin 17 antibody*.ti,ab,kf. or il 23 antibod*.ti,ab,kf. or interleukin 23 antibod*.ti,ab,kf. or ((anti interleukin or anti il) adj2 (dupilumab or dupixent or "17" or "23")).ti,ab,kf.
- exp Tumor Necrosis Factor Inhibitors/ or alpha inhibitor*.ti,ab,kf. or tnf inhibitor*.ti,ab,kf. or anti tnf agent*.ti,ab,kf. or anti tnf alpha agent*.ti,ab,kf. or anti tumor necrosis factor agent*.ti,ab,kf. or anti tumour necrosis factor agent*.ti,ab,kf. or tumor necrosis factor alpha inhibitor*.ti,ab,kf. or tumor necrosis factor inhibitor*.ti,ab,kf. or tumour necrosis factor alpha inhibitor*.ti,ab,kf. or tumour necrosis factor inhibitor*.ti,ab,kf.
- or/4-9
- 3 and 10
- limit 11 to yr="1990 - 2020"
- 12 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/)
- meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf
- exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.
- Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies]
- Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.))
- 13 and 14 SR
- (13 and 15) not 18 Clinical trials, RCTs
- (13 and (16 or 17)) not 18 not 19 OBS
- 18 or 19 or 20
Resultaten = 60
Alle resultaten
|
Database |
Datum |
# hits |
|
EMBASE |
25-4-2024 |
1059 |
|
MEDLINE |
25-4-2024 |
60 |
|
Totaal |
1119 |
|
|
Duplicates |
29 |
|
|
Netto aantal |
1090 |
|
De volgende afbakening is gebruikt:
Voor de P: Volwassen (17> jaar) patiënten met CSU en CIndU
Voor de I: Ciclosporine
Dapson
Rituximab
Plaquenil
Voor de C: Placebo of add-on vergelijkingen
Voor de O: Gemiddelde afname in wekelijkse Urticaria activiteitenscore (UAS7)
Bijwerkingen
Percentage deelnemers dat binnen een maand na het stoppen met de interventie terugvalt
Percentage deelnemers met volledige onderdrukking van urticaria
Percentage deelnemers met 'goede' of 'uitstekende' respons
Verbetering in kwaliteit van leven
Inclusie- en exclusiecriteria
|
Inclusiecriteria |
Exclusiecriteria |
|
Volwassen patiënten met CSU en CIndU |
Dierenstudies |
|
SR, RCT’s en CCT’s, observationeel vergelijkende studies van 1990-2020 |
Follow-up van korter dan 4 weken |
|
Volledig tekst beschikbaar in Nederlands of Engels |
Observationeel niet vergelijkende studies |
Uitgangsvragen
- Wat is de aanbevolen behandeling voor volwassenen met CSU en kan het huidige stepped care model worden aangepast?
- Welke overige behandelmogelijkheden worden aanbevolen als het stepped care model onvoldoende effect geeft bij volwassenen met CSU?
- Welke behandeling wordt aanbevolen voor volwassenen met CIndU en kan hier een stepped care model voor worden gemaakt?
EMBASE (15-5-2024)
Zoektermen
- 'urticaria'/exp OR urticaria*:ti,ab,kw OR weal:ti,ab,kw OR wheal:ti,ab,kw OR wealing:ti,ab,kw OR weals:ti,ab,kw OR whealing:ti,ab,kw OR wheals:ti,ab,kw OR dermatographi*:ti,ab,kw OR 'muckle wells syndrome*':ti,ab,kw OR 'schnitzler syndrome*':ti,ab,kw OR hives:ti,ab,kw OR ((vibrator* NEAR/3 (angioedema OR angiooedema OR 'angio edema' OR 'angio oedema')):ti,ab,kw)
- 'cyclosporine'/exp OR 'atopica':ti,ab,kw OR 'capimune':ti,ab,kw OR 'capsorin*':ti,ab,kw OR 'cequa':ti,ab,kw OR 'ciclograft':ti,ab,kw OR 'ciclomulsion':ti,ab,kw OR 'cicloral':ti,ab,kw OR 'ciclosporin*':ti,ab,kw OR 'cipol':ti,ab,kw OR 'ciqorin':ti,ab,kw OR 'consupren':ti,ab,kw OR 'cyclaid':ti,ab,kw OR 'cyclasol':ti,ab,kw OR 'cyclokat':ti,ab,kw OR 'cyclosporin*':ti,ab,kw OR 'deximune':ti,ab,kw OR 'equoral':ti,ab,kw OR 'gengraf':ti,ab,kw OR 'ikervis':ti,ab,kw OR 'iminoral':ti,ab,kw OR 'immunosporin*':ti,ab,kw OR 'implanta':ti,ab,kw OR 'imunofar':ti,ab,kw OR 'imusporin':ti,ab,kw OR 'menelri':ti,ab,kw OR 'mitogard':ti,ab,kw OR 'neciclopin':ti,ab,kw OR 'neoimmun':ti,ab,kw OR 'opsisporin':ti,ab,kw OR 'optimmune':ti,ab,kw OR 'padciclo':ti,ab,kw OR 'papilock':ti,ab,kw OR 'pulminiq':ti,ab,kw OR 'ramihyphin a':ti,ab,kw OR 'restasis':ti,ab,kw OR 'restaysis':ti,ab,kw OR 'sanciclo':ti,ab,kw OR 'sandimmun':ti,ab,kw OR 'sandimmune':ti,ab,kw OR 'sandimun':ti,ab,kw OR 'sporilen':ti,ab,kw OR 'vanquoral':ti,ab,kw OR 'vekacia':ti,ab,kw OR 'verkazia':ti,ab,kw OR 'vevye':ti,ab,kw OR 'zinograf me':ti,ab,kw
- 'dapsone'/exp OR 'aczone':ti,ab,kw OR 'atrisone':ti,ab,kw OR 'avlosulfan':ti,ab,kw OR 'avlosulfon':ti,ab,kw OR 'avlosulfone':ti,ab,kw OR 'croysulfone':ti,ab,kw OR 'dapsoderm-x':ti,ab,kw OR 'dapson':ti,ab,kw OR 'dapsona':ti,ab,kw OR 'dapsone':ti,ab,kw OR 'diamino diphenyl sulfone':ti,ab,kw OR 'diaminodiphenyl sulfone':ti,ab,kw OR 'diaminodiphenylosulfone':ti,ab,kw OR 'diaminodiphenylsulfon':ti,ab,kw OR 'diaminodiphenylsulfone':ti,ab,kw OR 'diammodiphenylsulfone':ti,ab,kw OR 'diaphenyl sulfone':ti,ab,kw OR 'diaphenylsulfon':ti,ab,kw OR 'diaphenylsulfone':ti,ab,kw OR 'diaphenylsulphone':ti,ab,kw OR 'diphenason':ti,ab,kw OR 'diphenasone':ti,ab,kw OR 'diphone':ti,ab,kw OR 'disulone':ti,ab,kw OR 'dopsan':ti,ab,kw OR 'dumitone':ti,ab,kw OR 'eporal':ti,ab,kw OR 'lepravir':ti,ab,kw OR 'novasulfon':ti,ab,kw OR 'novophone':ti,ab,kw OR 'servidapson':ti,ab,kw OR 'servidapsone':ti,ab,kw OR 'sulfadione':ti,ab,kw OR 'sulfadoine':ti,ab,kw OR 'sulfona':ti,ab,kw OR 'sulfone mere':ti,ab,kw OR 'udolac':ti,ab,kw
- 'rituximab'/exp OR 'acellbia':ti,ab,kw OR 'blitzima':ti,ab,kw OR 'cimabior':ti,ab,kw OR 'kikuzubam':ti,ab,kw OR 'mabthera':ti,ab,kw OR 'monoclonal antibody idec c2b8':ti,ab,kw OR 'redditux':ti,ab,kw OR 'reditux':ti,ab,kw OR 'retuxira':ti,ab,kw OR 'riabni':ti,ab,kw OR 'ristova':ti,ab,kw OR 'ritemvia':ti,ab,kw OR 'ritucad':ti,ab,kw OR 'ritumax':ti,ab,kw OR 'rituxan':ti,ab,kw OR 'rituximab':ti,ab,kw OR 'rituxin':ti,ab,kw OR 'rituzena':ti,ab,kw OR 'rixathon':ti,ab,kw OR 'riximyo':ti,ab,kw OR 'ruxience':ti,ab,kw OR 'tidecron':ti,ab,kw OR 'truxima':ti,ab,kw OR 'tuxella':ti,ab,kw OR 'zytux':ti,ab,kw
- 'hydroxychloroquine sulfate'/exp OR 'dimard':ti,ab,kw OR 'dolquine':ti,ab,kw OR 'duplaxil':ti,ab,kw OR 'erquin':ti,ab,kw OR 'evoquin':ti,ab,kw OR 'geniquin':ti,ab,kw OR 'oxiklorin':ti,ab,kw OR 'plaquenil':ti,ab,kw OR 'plaquinol':ti,ab,kw OR 'quensil':ti,ab,kw OR 'quineprox':ti,ab,kw OR 'reuquinol':ti,ab,kw OR 'sovuna':ti,ab,kw OR 'toremonil':ti,ab,kw OR 'yuma':ti,ab,kw OR hydroxychloroquin*:ti,ab,kw
- #2 OR #3 OR #4 OR #5
- #1 AND #6
- #7 NOT (('adolescent'/exp OR 'child'/exp OR adolescent*:ti,ab,kw OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw))
- #8 AND [1990-2020]/py NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp)
- 'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab
- 'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti
- 'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti)
- 'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab)))
- #9 AND #10 SR
- #9 AND #11 NOT #14 Clinical trials, RCTs
- #9 AND (#12 OR #13) NOT #14 NOT #15 OBS
- #14 OR #15 OR #16
Resultaten = 1286
MEDLINE (15-5-2024)
Zoektermen
- exp Urticaria/ or urticaria*.ti,ab,kf. or weal.ti,ab,kf. or wheal.ti,ab,kf. or wealing.ti,ab,kf. or weals.ti,ab,kf. or whealing.ti,ab,kf. or wheals.ti,ab,kf. or dermatographi*.ti,ab,kf. or muckle wells syndrome*.ti,ab,kf. or schnitzler syndrome*.ti,ab,kf. or hives.ti,ab,kf. or (vibrator* adj3 (angioedema or angiooedema or angio edema or angio oedema)).ti,ab,kf.
- 1 not ((Adolescent/ or Child/ or Infant/ or adolescen*.ti,ab,kf. or child*.ti,ab,kf. or schoolchild*.ti,ab,kf. or infant*.ti,ab,kf. or girl*.ti,ab,kf. or boy*.ti,ab,kf. or teen.ti,ab,kf. or teens.ti,ab,kf. or teenager*.ti,ab,kf. or youth*.ti,ab,kf. or pediatr*.ti,ab,kf. or paediatr*.ti,ab,kf. or puber*.ti,ab,kf.) not (Adult/ or adult*.ti,ab,kf. or man.ti,ab,kf. or men.ti,ab,kf. or woman.ti,ab,kf. or women.ti,ab,kf.))
- 1 and 2
- Cyclosporine/ or atopica.ti,ab,kf. or capimune.ti,ab,kf. or capsorin*.ti,ab,kf. or cequa.ti,ab,kf. or ciclograft.ti,ab,kf. or ciclomulsion.ti,ab,kf. or cicloral.ti,ab,kf. or ciclosporin*.ti,ab,kf. or cipol.ti,ab,kf. or ciqorin.ti,ab,kf. or consupren.ti,ab,kf. or cyclaid.ti,ab,kf. or cyclasol.ti,ab,kf. or cyclokat.ti,ab,kf. or cyclosporin*.ti,ab,kf. or deximune.ti,ab,kf. or equoral.ti,ab,kf. or gengraf.ti,ab,kf. or ikervis.ti,ab,kf. or iminoral.ti,ab,kf. or immunosporin*.ti,ab,kf. or implanta.ti,ab,kf. or imunofar.ti,ab,kf. or imusporin.ti,ab,kf. or menelri.ti,ab,kf. or mitogard.ti,ab,kf. or neciclopin.ti,ab,kf. or neoimmun.ti,ab,kf. or opsisporin.ti,ab,kf. or optimmune.ti,ab,kf. or padciclo.ti,ab,kf. or papilock.ti,ab,kf. or pulminiq.ti,ab,kf. or ramihyphin a.ti,ab,kf. or restasis.ti,ab,kf. or restaysis.ti,ab,kf. or sanciclo.ti,ab,kf. or sandimmun.ti,ab,kf. or sandimmune.ti,ab,kf. or sandimun.ti,ab,kf. or sporilen.ti,ab,kf. or vanquoral.ti,ab,kf. or vekacia.ti,ab,kf. or verkazia.ti,ab,kf. or vevye.ti,ab,kf. or zinograf me.ti,ab,kf.
- Dapzone/ or aczone.ti,ab,kf. or atrisone.ti,ab,kf. or avlosulfan.ti,ab,kf. or avlosulfon.ti,ab,kf. or avlosulfone.ti,ab,kf. or croysulfone.ti,ab,kf. or dapsoderm-x.ti,ab,kf. or dapson.ti,ab,kf. or dapsona.ti,ab,kf. or dapsone.ti,ab,kf. or diamino diphenyl sulfone.ti,ab,kf. or diaminodiphenyl sulfone.ti,ab,kf. or diaminodiphenylosulfone.ti,ab,kf. or diaminodiphenylsulfon.ti,ab,kf. or diaminodiphenylsulfone.ti,ab,kf. or diammodiphenylsulfone.ti,ab,kf. or diaphenyl sulfone.ti,ab,kf. or diaphenylsulfon.ti,ab,kf. or diaphenylsulfone.ti,ab,kf. or diaphenylsulphone.ti,ab,kf. or diphenason.ti,ab,kf. or diphenasone.ti,ab,kf. or diphone.ti,ab,kf. or disulone.ti,ab,kf. or dopsan.ti,ab,kf. or dumitone.ti,ab,kf. or eporal.ti,ab,kf. or lepravir.ti,ab,kf. or novasulfon.ti,ab,kf. or novophone.ti,ab,kf. or servidapson.ti,ab,kf. or servidapsone.ti,ab,kf. or sulfadione.ti,ab,kf. or sulfadoine.ti,ab,kf. or sulfona.ti,ab,kf. or sulfone mere.ti,ab,kf. or udolac.ti,ab,kf.
- rituximab/ or acellbia.ti,ab,kf. or blitzima.ti,ab,kf. or cimabior.ti,ab,kf. or kikuzubam.ti,ab,kf. or mabthera.ti,ab,kf. or monoclonal antibody idec c2b8.ti,ab,kf. or redditux.ti,ab,kf. or reditux.ti,ab,kf. or retuxira.ti,ab,kf. or riabni.ti,ab,kf. or ristova.ti,ab,kf. or ritemvia.ti,ab,kf. or ritucad.ti,ab,kf. or ritumax.ti,ab,kf. or rituxan.ti,ab,kf. or rituximab.ti,ab,kf. or rituxin.ti,ab,kf. or rituzena.ti,ab,kf. or rixathon.ti,ab,kf. or riximyo.ti,ab,kf. or ruxience.ti,ab,kf. or tidecron.ti,ab,kf. or truxima.ti,ab,kf. or tuxella.ti,ab,kf. or zytux.ti,ab,kf
- exp Hydroxychloroquine/ or dimard.ti,ab,kf. or dolquine.ti,ab,kf. or duplaxil.ti,ab,kf. or erquin.ti,ab,kf. or evoquin.ti,ab,kf. or geniquin.ti,ab,kf. or oxiklorin.ti,ab,kf. or plaquenil.ti,ab,kf. or plaquinol.ti,ab,kf. or quensil.ti,ab,kf. or quineprox.ti,ab,kf. or reuquinol.ti,ab,kf. or sovuna.ti,ab,kf. or toremonil.ti,ab,kf. or yuma.ti,ab,kf. or hydroxychloroquin*.ti,ab,kf.
- or/4-7
- 3 and 8
- limit 9 to yr="1990 - 2020"
- 10 not ((exp animals/ or exp models, animal/) not humans/) not (letter/ or comment/ or editorial/)
- meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf.
- exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.
- Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies]
- Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.))
- 11 and 12 SR
- (11 and 13) not 16 RCT, clinical trials’
- (11 and (14 or 15)) not 16 not 17 obs
- 16 or 17 or 18
Resultaten = 154
Alle resultaten
|
Database |
Datum |
# hits |
|
EMBASE |
15-5-2024 |
1286 |
|
MEDLINE |
15-5-2024 |
154 |
|
Totaal |
1440 |
|
|
Duplicates |
8 |
|
|
Netto aantal |
1332 |
|