1e en 2e lijn en verwijsindicaties bij CNS
Uitgangsvraag
Samenwerking in de 1e en 2e lijn en verwijsindicaties bij chronische nierschade (CNS)
Aanbeveling
In deze module worden de termen internist en internist-nefroloog gebruikt.
Met internist-nefroloog wordt in dit geval bedoeld: internist-nefroloog of internist met een samengesteld profiel waaronder nefrologie.
Indicaties voor verwijzing bij chronische nierschade met mild tot matig verhoogd risico (geel en oranje in de stadiëringstabel)
Voor patiënten met chronische nierschade wordt verwijzing naar een internist-nefroloog geadviseerd in de volgende gevallen:
- vermoeden van acute nierschade;
- een persisterende ernstig verhoogde albuminurie (ACR > 30 mg/mmol, of AER > 300 mg/24 uur; A3);
- de aanwezigheid van ≥40% dysmorfe erytrocyten (bij ten minste 20 erytrocyten/µl) en/of de aanwezigheid van erytrocyten celcilinders in het urinesediment.
- vermoeden op of een bekende onderliggende nierziekte (een bekende auto-immuunziekte, recidiverende pyelonefritis, anti-refluxoperaties, nefrectomie);
- vermoeden van een erfelijke nierziekte, of een erfelijke nierziekte in de familie (bijvoorbeeld cystenieren).
- snelle progressie van chronische nierschade:
- daling van de eGFR van 25% ten opzichte van de eerste meting in de afgelopen vijf jaar, in combinatie met een verslechtering in stadium van nierschade (zie stadiëringstabel), of
- daling van de eGFR van ten minste 5 ml/min/1,73 m2/jaar, vastgesteld met ten minste 3 metingen.
Voor patiënten met chronische nierschade wordt consultatie van een internist-nefroloog geadviseerd bij twijfel of verwijzing zinvol is en adviezen over de behandeling bij patiënten die in de eerste lijn behandeld willen worden ondanks een verwijsindicatie. Dit kan onder andere vragen betreffen over de progressie van de nierschade, therapieresistente hypertensie en afwijkende laboratoriumuitslagen wijzend op metabole complicaties.
Indicaties voor verwijzing bij chronische nierschade met sterk verhoogd risico (rood in de stadiëringstabel)
Het wordt aanbevolen patiënten met een sterk verhoogd risico te verwijzen naar de internist-nefroloog, tenzij er redenen zijn om dit niet te doen (bijvoorbeeld als de patiënt na adequate voorlichting kiest voor behandeling in de eerste lijn).
Tijdige verwijzing van patiënten met progressieve nierschade, waarbij noodzaak tot start nierfunctievervangende behandeling binnen één tot twee jaar te verwachten is, wordt aanbevolen om deze patiënten multidisciplinair voor te bereiden op nierfunctievervangende behandeling middels een gestructureerd programma.
Conservatieve behandeling is aangewezen voor patiënten die ervoor kiezen af te zien van nierfunctievervangende behandeling (zie ook de richtlijnen ‘Nierfunctievervangende behandeling: wel of niet?’ en ‘Palliatieve zorg bij eindstadium nierfalen’).
Indien een patiënt en/of het medisch team niet kiest voor nierfunctievervangende behandeling moet deze patiënt, indien door hem/haar gewenst, multidisciplinair ondersteund worden in eerste en/of tweede lijn, met aandacht voor medische, psychologische en sociaal-culturele aspecten.
Terugverwijzen
De internist-nefroloog kan de patiënt, bijvoorbeeld na afronding van specialistische diagnostiek of optimalisatie van medicatie bij een stabiele patiënt, terugverwijzen naar de eerste lijn. Hij geeft daarbij aan de huisarts aan welke controles zijn geïndiceerd en bij welke ontwikkelingen hij de patiënt terug wil zien.
Niet verwijzen ondanks indicatie
Er kan in overleg met de patiënt van verwijzing/consultatie worden afgezien indien er sprake is van een beperkte levensverwachting, bijvoorbeeld vanwege hoge leeftijd en/of ernstige comorbiditeit, of indien een patiënt dit niet wil.
Indien de huisarts de patiënt met een verwijsindicatie niet verwijst, dient de huisarts bedacht te zijn op eventuele metabole complicaties, anemie en/of ondervoeding bij sterk verminderde nierfunctie. Diagnostiek en behandeling daarvan kan eventueel plaatsvinden met behulp van consultatie van een internist-nefroloog.
Een verslechtering van de situatie van de patiënt kan in een latere fase aanleiding zijn de patiënt alsnog te verwijzen of de internist-nefroloog te consulteren.
Controlefrequentie
Aanbevolen controlefrequentie (per jaar) op basis van eGFR en albumine/creatinine ratio
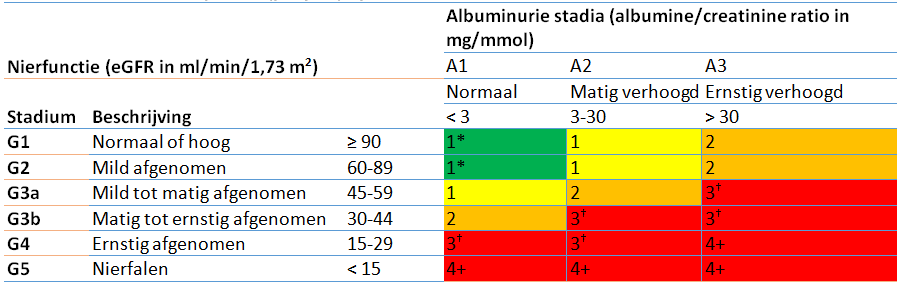
* indien er sprake is van CNS
† het is aan te bevelen in de eerste lijn controlemomenten met de reguliere controles voor DM of CVRM samen te laten vallen
Overwegingen
CNS met mild tot matig verhoogd risico (geel en oranje in de stadiëringstabel (G1A2, G1A3, G2A2, G2A3, G3aA1, G3aA2, G3bA1))
Bij de meeste gevallen van CNS met mild tot matig verhoogd risico is het beleid relatief eenvoudig. Alle diagnostische en beleidsmaatregelen zijn routine in de huisartspraktijk. Er is echter een aantal situaties waarin nader overleg met of verwijzing naar de internist-nefroloog aangewezen is.
Snellere nierfunctie achteruitgang dan normaal is een consultatie- dan wel verwijsindicatie, ook als de nierfunctie misschien nog relatief goed is, omdat er bij dergelijke patiënten vaak een onderliggend probleem is dat behandeling vereist om verder nierfunctieverlies te voorkomen.
Verwijzing is bovendien zinvol wanneer er ernstig verhoogde albuminurie (> 30 mg/mmol) blijkt te zijn omdat in die gevallen sprake kan zijn van een specifieke nierziekte, die mogelijk specifieke therapie vereist, en waarvoor een nierbiopt noodzakelijk kan zijn ter diagnosestelling. Hetzelfde geldt in geval van dysmorfe erytrocyturie, zeker als dit gepaard gaat met matig of ernstig verhoogde albuminurie en/of een verminderde nierfunctie. Macroscopische hematurie heeft meestal een urologische oorzaak, waarvoor verwijzing naar een uroloog geïndiceerd is. In geval van microscopische hematurie dienen echter ook nefrologische oorzaken overwogen te worden omdat de work-up verschillend is. Er is helaas geen simpele test om onderscheid te maken tussen nefrologische en urologische oorzaken van hematurie. Het onderscheid zal meestal gemaakt moeten worden op basis van patroonherkenning. Behulpzaam daarbij zijn het bepalen van nierfunctie, albuminurie en het microscopisch beoordelen van het urine sediment. Macroscopische hematurie gaat altijd gepaard met enig urine eiwitverlies, ook als deze van urologische oorsprong is. In geval van microscopische hematurie wijst een ernstig verhoogde albuminurie (ofwel > 200 mg/l ofwel > 30 mg/mmol creatinine) vaak op een nefrologische aandoening, zeker als daar ook een gestoorde nierfunctie bij aanwezig is (eGFR < 60 ml/min/1,73m2). De aanwezigheid van ≥40% dysmorfe erytrocyten (bij ten minste 20 erytrocyten/µl) in het urinesediment is een sterke aanwijzing voor een glomerulaire oorzaak van een hematurie [Van der Snoek, 1994; Crop, 2010]. Ook de aanwezigheid van celcilinders is van belang. Met name het vinden van erytrocytencilinders is een zeer sterke aanwijzing voor een renale oorzaak van hematurie. Patiënten met deze afwijkingen dienen geanalyseerd te worden door een internist-nefroloog, naast eventueel urologische analyse.
Omgekeerd geldt dat nefrologische beoordeling van asymptomatische microscopische hematurie geen toegevoegde waarde heeft indien albuminurie niet verhoogd is en de nierfunctie normaal. Een dergelijke bevinding heeft namelijk geen diagnostische of therapeutische consequenties op nefrologisch terrein. Wel wordt aanbevolen dat huisartsen deze patiënten volgen op het eventueel optreden van afwijkingen wat betreft albuminurie en nierfunctie, omdat deze nefrologische ziekten progressief kunnen zijn. De frequentie van follow-up is arbitrair en kan de eerste drie jaar jaarlijks zijn en daarna gedurende enige tijd eens per 3 jaren.
Bij nierschade en een moeilijk behandelbare hypertensie is nader overleg dan wel verwijzing gewenst.
De huisarts kan daarnaast de internist-nefroloog consulteren bij patiënten met stabiele nierfunctie indien er specifieke expertise vereist is omtrent bijvoorbeeld medicatie, prognose of metabole stoornissen (voor criteria voor consultatie zie de aanbevelingen).
Wanneer de huisarts de internist-nefroloog consulteert doet hij dit aan de hand van de volgende gegevens:
- anamnestische gegevens en gegevens uit lichamelijk onderzoek (bloeddruk/beloop);
- eGFR, mate van albuminurie, uitslag van sedimentsonderzoek op specifieke afwijkingen (indien verricht)/beloop;
- indien verricht: uitslag van echografie van de nieren;
- medische voorgeschiedenis;
- actueel medicatieoverzicht (waaronder ook allergieën);
- bijzondere psychosociale omstandigheden
CNS met sterk verhoogd risico (rood in de stadiëringstabel (G3aA3, G3bA2, G3bA3, G4, G5))
Patiënten met een sterk verhoogd risico (rood in de stadiëringstabel) hebben een hoog risico op cardiovasculaire eindpunten, het ontstaan van eindstadium nierfalen en noodzaak tot voorlichting over de keuze t.a.v. behandelopties (nierfunctievervangende behandeling (dialyse of transplantatie) of afzien daarvan (en conservatieve behandeling)). Uit een aantal onderzoeken is gebleken dat van patiënten bij wie kort (<90 dagen) na verwijzing naar een dialysecentrum gestart moet worden met nierfunctievervangende therapie, de morbiditeit en sterfte hoger zijn dan van patiënten die in een vroeger stadium worden verwezen [Levin, 2000; Cass, 2002; Roderick, 2002; Stoves, 2001; Kessler, 2003; Frimat,2004]. Late verwijzing is geassocieerd met meerdere problemen zoals meer uremische klachten [Innes, 1992; Jungers, 1993; Eadington, 1996], ernstigere anemie, slechter gereguleerde bloeddruk [Eadington, 1996], meer gestoord calciumfosfaat metabolisme en daardoor een hoger PTH (parathyreoïd hormoon), en een ernstigere metabole acidose [Eadington, 1996]. Patiënten die in een laat stadium worden verwezen, worden vaker en langer in het ziekenhuis opgenomen [Arora, 1999; Cass, 2002] en vaker via een tijdelijke toegang tot de bloedbaan gedialyseerd [Avorn, Arch Int Med 2002; Avorn, J Clin Epid 2002; Chesser, 1999], wat tot meer infectieuze complicaties leidt en tot hogere kosten van behandeling van laat verwezen patiënten. Ook blijken laat verwezen patiënten vaker werkloos te worden. Er zijn dus vele factoren die er toe bijdragen dat de morbiditeit en mortaliteit van laat verwezen patiënten hoger is dan van tijdig verwezen patiënten [Innes, 1992; Jungers, 1993; Sesso, 1996; Ifudu, 1996; Ellis, 1998; Arora, 1999; Churchill, 1997; Levin, 2000; Cass, 2002; Roderick, 2002; Stoves, 2001; Kessler, 2003; Frimat, 2004; Kazmi, 2004; Goncalves, 2004; Khan, 2005; Ravani, 2004], hetgeen ook geldt voor ouderen [Schwenger, 2006]. In Denemarken werd in een cohortstudie van >1700 patiënten aangetoond dat bij degenen die laat (<16 weken voor start dialyse) waren verwezen naar een internist-nefroloog, veel minder patiënten de volgens richtlijnen geadviseerde behandeling kregen en dat zij een hogere mortaliteit hadden [Hommel, 2012]. Vergelijkbare data werden uit Korea gemeld [Kim, 2013]. Verder werd in een recente meta-analyse, waarin data van meer dan 63.000 patiënten werden geanalyseerd, aangetoond dat patiënten die korter dan 6 maanden voor start van dialyse waren verwezen naar een specialist op het gebied van nierziekten, een hogere mortaliteit hadden en meer ziekenhuisopnames behoefden [Smart, 2014]. Dit verschil werd niet verklaard door comorbiditeit of verschillen in serum fosfaat tussen de groepen, maar wel door betere voorbereiding bij degenen die vroeg waren verwezen en tijdige realisatie van toegang tot de bloedbaan (hemodialyse) of buikholte (peritoneale dialyse). Op al deze waarnemingen stoelt het advies om patiënten met een sterk verhoogd risico (rood in de stadiëringstabel) voor verdere behandeling te verwijzen naar een nefroloog, tenzij zij niet in aanmerking (willen) komen vanwege een beperkte levensverwachting of bepaalde vormen van comorbiditeit (bijvoorbeeld dementie of permanent verblijf in een verpleeghuis).
Indien er geen klachten bestaan, kunnen patiënten met CNS met sterk verhoogd risico (rood in de stadiëringstabel) eens per drie maanden gecontroleerd worden, waarbij naast de eerder genoemde zaken tevens gelet dient te worden op de voedingstoestand van de patiënt. Wanneer ingeschat wordt dat nierfalen binnen één tot twee jaar bereikt zal worden, dient tijdige voorlichting over de juiste vorm van nierfunctievervangende behandeling te starten. Daarbij dient waar mogelijk bij patiënten die voor niertransplantatie in aanmerking komen, gestreefd te worden naar een pre-emptieve transplantatie met een nier van een levende donor. Het begeleiden van patiënten met nierfalen dient plaats te vinden op een gespecialiseerd spreekuur, waar alle betrokkenen (internist-nefroloog, verpleegkundig specialist, verpleegkundige, maatschappelijk werker, diëtist) vertegenwoordigd zijn. Ook dient, zo nodig in samenspraak met bedrijfsarts en/of Arboarts, er naar gestreefd te worden patiënten zo verantwoord mogelijk aan het werk te houden.
Overigens is aangetoond dat vroeg starten met hemodialysebehandeling niet tot betere overleving leidt en zelfs gepaard gaat met verhoogde mortaliteit [Pan, 2012]. Derhalve wordt tegenwoordig, zeker bij patiënten die weinig klachten hebben, niet gestart met dialysebehandeling bij een eGFR >15 ml/min/1,73 m2. Steeds vaker wordt, in overleg tussen patiënt, familie en medisch team, er in geval van hoge leeftijd en/of ernstige comorbiditeit voor gekozen om niet over te gaan tot dialyse of niertransplantatie, omdat die behandeling als te intensief wordt ervaren. In een dergelijk geval zal de begeleiding met dieet en medicatie doorgaan, zoals in de eerdere periode. Het accent zal nu logischerwijs ook meer op conservatieve behandeling liggen. In de oncologie is aangetoond dat tijdige palliatieve zorg gepaard gaat met een betere kwaliteit van leven, met minder bezoeken aan en opnames in het ziekenhuis, met minder invasieve zorg in een laatste levensfase en, verrassenderwijs, met soms een langere overleving [Temel, 2010]. Het is waarschijnlijk dat dit ook zal gelden voor vergelijkbare initiatieven in de nefrologie, waarbij passende palliatieve maatregelen zijn ingebouwd [Chandna, 2011; Davison, 2010; Davison, 2008; De Biase, 2008; Ellam, 2009; Germain, 2011] (zie ook de richtlijnen ‘Nierfunctievervangende behandeling: wel of niet?’ en ‘Palliatieve zorg bij eindstadium nierfalen’).
Taak van de huisarts
De huisarts ziet patiënten bij wie in het kader van het cardiovasculair risicomanagement, diabetes mellitus, de medicatiebewaking of bij oriënterend onderzoek een verminderde nierfunctie en/of verhoogde albuminurie gevonden wordt. Bij deze patiënten voert hij een diagnostisch traject uit om na te gaan wat de meest waarschijnlijke oorzaak van de verminderde nierfunctie en/of de verhoogde albuminurie is, en of sprake is van acute dan wel CNS. Patiënten die verdacht worden van acute nierschade worden onmiddellijk verwezen. Ook bij twijfel aan de oorzaak van de nierschade (onder andere vermoeden van een specifieke nieraandoening) is verwijzing aangewezen. De meeste patiënten met CNS begeleidt de huisarts echter zelf. Dit zijn vooral patiënten met CNS op basis van een vasculaire oorzaak (diabetes mellitus en hypertensie). De huisarts informeert de patiënt over de mate van nierschade en de praktische (onder andere leefstijl, handverkoop NSAID’s, zoutgebruik) en medische (onder andere aandacht bij intercurrente ziektes, medicatiebewaking) consequenties. In overleg wordt de apotheek in kennis gesteld van de verminderde nierfunctie. Zo nodig wordt de bestaande medicatie aangepast al dan niet na overleg met de apotheker. De bewaking van het beloop van de CNS zal meestal onderdeel zijn van het totale cardiovasculair risicomanagement. Hierbij kan de praktijkondersteuner een belangrijke rol vervullen. Strikte behandeling van de bloeddruk heeft een centrale rol. Zoutbeperking heeft daarbij een belangrijke aanvullende waarde en advies van een diëtist kan nodig zijn. Voor patiënten met CNS betekent dit dat de behandeling veelal binnen de geprotocolleerde zorg voor patiënten met diabetes mellitus en/of een verhoogd cardiovasculair risico valt en dat de huisarts in samenspraak met de patiënt de afweging zal maken voor de intensiteit van de behandeling en het al dan niet verwijzen naar de internist-nefroloog. Specifieke aandacht dient geschonken te worden aan de systematische behandeling van patiënten die niet onder geprotocolleerde ketenzorg vallen. Zo nodig kan de huisarts de internist-nefroloog consulteren (bijvoorbeeld via teleconsultatie) bijvoorbeeld bij vragen omtrent progressie van de nierschade, medicatie, streefwaarden van de bloeddruk, metabole afwijkingen of indien een verwijzing door de patiënt als te belastend wordt ervaren.
Typerend voor de huisarts is dat hij generalistische, persoonsgerichte en continue zorg levert. De huisarts combineert zijn medische kennis en vaardigheden met kennis van de levensloop en medische voorgeschiedenis van de patiënt in diens leef- en werkomgeving en sociale context. Bovendien is de huisarts gedurende langere tijd de constante factor in de medische zorg voor de patiënt. De huisarts kan vanuit deze positie een specifieke aanvullende rol hebben in geval van het al dan niet kiezen voor nierfunctievervangende behandeling dan wel conservatieve behandeling en in geval van de terminale zorg bij nierfalen.
Taken van de internist-nefroloog
Werkzaamheden in de poliklinische setting bij patiënten met CNS bestaan allereerst uit diagnostiek als de oorzaak van nierfalen niet meteen duidelijk is. Als er specifieke richtinggevende gegevens zijn, die bijvoorbeeld wijzen op een glomerulaire aandoening of een systeemziekte, wordt de indicatie voor een nierbiopt afgewogen op basis van therapeutische of prognostische consequenties. Bovendien wordt informatie gegeven over nierfunctie, nierschade, de effecten van leefstijl en behandeling op progressie van nierschade en de consequenties van verminderde nierfunctie.
In de therapeutische setting is de bijdrage van de internist-nefroloog sterk afhankelijk van het stadium van CNS, maar bestaat in het algemeen uit 4 pijlers:
- Voorkomen van progressie van nierfalen;
- Voorkomen van cardiovasculaire ziekte door aangepaste behandeling van (cardiovasculaire) risicofactoren;
- Behandeling van eventuele metabole en overige complicaties van nierfalen;
- Eventueel voorbereiden op nierfunctievervangende behandeling.
Taken van de internist-nefroloog bij het voorkomen van progressie van nierfalen
- voorkomen van acute verslechtering van chronisch nierschade:
- door medicatiecontrole en advies, bijvoorbeeld m.b.t. het staken van potentieel nefrotoxische medicatie (ook zgn. “over-the-counter” NSAID’s).
- het aanpassen van medicatiedosering aan nierfunctie (ter voorkoming van risico’s op zowel over- als onderdosering).
- adviezen over hoe bepaalde middelen in specifieke situatie gebruikt moeten worden (bijvoorbeeld eventueel tijdelijk staken van ACE-remmers en/of diuretica bij dreigende dehydratie). Patiënten worden geïnformeerd bij welke verschijnselen zij zich tot een arts moeten wenden.
- adviezen over nierfunctie bescherming bij toedienen van jodiumhoudend röntgencontrast (met name vanaf stadium G3b).
- Op basis van een individueel behandelplan, bijvoorbeeld bij ouderen of bij patiënten met ernstig (perifeer) vaatlijden, kunnen t.a.v. bloeddrukregulatie andere streefwaarden en middelen van voorkeur voor cardiovasculair risico management worden toegepast dan gebruikelijk.
- T.a.v. albuminurie in de sterk verhoogde range (A3) kunnen aanvullende behandelingen gekozen worden, waaronder:
- in specifieke gevallen het “optitreren” van dosering ACE-remmer of ARB tot boven hetgeen gebruikelijk is, dan wel dit in combinatie voorschrijven.
- het toevoegen van diuretica (ook spironolacton) en/of een eiwit- en zoutbeperkt dieet (met verwijzing naar een diëtist met aandachtsgebied nierziekten) ter versterking van het renoprotectieve effect van RAAS-blokkade.
- Daarnaast zal bij specifieke nierziekten een indicatie gesteld worden voor een nierbiopsie of de start van immuunmodulerende therapie dan wel innovatieve ziekte specifieke behandeling (bijvoorbeeld V2 receptor antagonist voor cystenieren).
Taken van de internist-nefroloog bij het voorkomen van cardiovasculaire ziekte door aangepaste behandeling van (cardiovasculaire) risicofactoren:
- bloeddrukcontrole, zoals bij punt 1 zijn genoemd.
- indicatie stelling voor statines.
- er is een categorie patiënten met gecombineerd hart- en nierfalen die intensief gezien worden in verband met een wankele vullingsbalans, waarbij ook periodieke controle door een internist-nefroloog gewenst is.
Taken van de internist-nefroloog bij behandeling van eventuele metabole en overige complicaties van nierfalen:
- aanpassen van medicamenteuze behandeling van diabetes mellitus afhankelijk van de nierfunctie.
- behandeling van veranderingen in het calcium-fosfaatmetabolisme en de ontwikkeling van secundaire hyperparathyreoïdie, welke soms al vanaf stadium G3a kunnen optreden.
- diagnostiek en behandeling van renale anemie; behandeling met ijzersuppletie en erythropoiesis stimulating agents (ESA’s).
- behandeling van metabole acidose en hyperkaliëmie.
- Signalering van ziektegerelateerde ondervoeding
Taken van de internist-nefroloog bij het eventueel voorbereiden op nierfunctievervangende behandeling:
- patiënten met CNS en een matig tot sterk verhoogd risico (oranje en rood in de stadiëringstabel) dienen aanvullende informatie van de internist-nefroloog te krijgen over de risicofactoren voor progressie van nierschade en de wijze waarop dit beïnvloed kan worden.
- patiënten kunnen soms gerust gesteld worden als de noodzaak tot starten met nierfunctievervangende therapie onwaarschijnlijk geacht wordt, en dat behandeling zich met name zal richten op het voorkomen van progressieve hart- vaat- en nierschade en correctie van metabole afwijkingen.
- de verschillende vormen van nierfunctievervangende therapie worden besproken.
- bij patiënten die er voor in aanmerking kunnen komen kan het streven naar een pre-emptieve levende donorniertransplantatie soms in vroeg stadium aan de orde komen.
- bij kwetsbare patiënten kunnen ook de verwachtingen en (palliatieve) opties in de behandeling zónder nierfunctievervangende therapie besproken worden.
Onderbouwing
Verwijzing van een patiënt met CNS kan twee verschillende doelen dienen: bij de patiënt met CNS met een mild (geel in de stadiëringstabel) tot matig (oranje in de stadiëringstabel) verhoogd risico betreft dat meestal een diagnostisch dilemma, terwijl het bij de patiënt met CNS met sterk verhoogd risico (rood in de stadiëringstabel) meestal gaat om specifieke nefrologische therapeutische begeleiding en/of het op termijn voorbereiden op nierfunctievervangende behandeling: dialyse of niertransplantatie. Deze twee doelgroepen worden daarom apart besproken.
In deze module worden de termen internist en internist-nefroloog gebruikt.
Met internist-nefroloog wordt in dit geval bedoeld: internist-nefroloog of internist met een samengesteld profiel waaronder nefrologie.
Stadiëring van chronische nierschade op basis van eGFR en albumine/creatinine ratio en daaraan gekoppelde risicoschatting
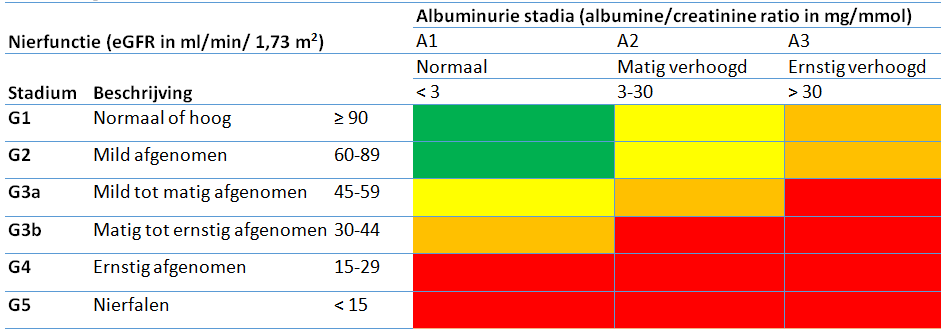
Voor afspraken over behandelaarschap en regie wordt verwezen naar de KNMG-Handreiking verantwoordelijkheidsverdeling bij samenwerking in de zorg [KNMG, 2010].
De werkgroep is uitgegaan van de uitgangspunten in de overige modules en heeft op basis daarvan samenwerkingsafspraken geformuleerd.
- Arora P, Obrador GT, Ruthazer R et al. Prevalence, predictors, and consequences of late nephrology referral at a tertiary care center. J Am Soc Nephrol 1999;10:1281-6
- Avorn J, Bohn RL, Levy E et al. Nephrologist care and mortality in patients with chronic renal insufficiency. Arch Intern Med 2002;162:2002-6
- Avorn J, Winkelmayer WC, Bohn RL et al. Delayed nephrologist referral and inadequate vascular access in patients with advanced chronic kidney failure. J Clin Epidemiol 2002;55:711-6
- Cass A, Cunningham J, Arnold PC et al. Delayed referral to a nephrologist: outcomes among patients who survive at least one year on dialysis. Med J Aust 2002;177:135-8
- Chandna SM, Da Silva-Gane M, Marshall C et al. Survival of elderly patients with stage 5 CKD: comparison of conservative management and renal replacement therapy. Nephrol Dial Transplant 2011;26:1608-14
- Chesser AM, Baker LR. Temporary vascular access for first dialysis is common, undesirable and usually avoidable. Clin Nephrol 1999;51:228-32
- Churchill DN. An evidence-based approach to earlier initiation of dialysis. Am J Kidney Dis 1997;30:899-906
- Davison SN, Murtagh FE, Higginson IJ. Methodological considerations for end-of-life research in patients with chronic kidney disease. J Nephrol 2008;21:268-82
- Davison SN. End-of-life care preferences and needs: perceptions of patients with chronic kidney disease. Clin J Am Soc Nephrol 2010;5:195-204
- De Biase V, Tobaldini O, Boaretti C et al. Prolonged conservative treatment for frail elderly patients with end-stage renal disease: the Verona experience. Nephrol Dial Transplant 2008;23:1313-7
- Eadington DW. Delayed referral for dialysis. Nephrol Dial Transplant 1996;11:2124-6
- Ellam T, El-Kossi M, Prasanth KC et al. Conservatively managed patients with stage 5 chronic kidney diseaseoutcomes from a single center experience. QJM 2009;102:547-54
- Ellis PA, Reddy V, Bari N, Cairns HS. Late referral of end-stage renal failure. QJM 1998;91:727-32
- Frimat L, Loos-Ayav C, Panescu V et al. Early referral to a nephrologist is associated with better outcomes in type 2 diabetes patients with end-stage renal disease. Diabetes Metab 2004;30:67-74
- Germain MJ, Kurella Tamura M, Davison SN. Palliative care in CKD: the earlier the better. Am J Kidney Dis 2011;57:378-80
- Goncalves EA, Andreoli MC, Watanabe R et al. Effect of temporary catheter and late referral on hospitalization and mortality during the first year of hemodialysis treatment. Artif Organs 2004;28:1043-9
- Hommel K, Madsen M, Kamper AL. The importance of early referral for the treatmen of chronic kidney disease: a Danish nationwide cohort study. BMC Nephrol 2012:13:108
- Ifudu O, Dawood M, Homel P, Friedman EA. Excess morbidity in patients starting uremia therapy without prior care by a nephrologist. Am J Kidney Dis 1996;28:841-5
- Innes A, Rowe PA, Burden RP, Morgan AG. Early deaths on renal replacement therapy: the need for early nephrological referral. Nephrol Dial Transplant 1992;7:467-71
- Jungers P, Zingraff J, Albouze G et al. Late referral to maintenance dialysis: detrimental consequences. Nephrol Dial Transplant 1993;8:1089-93
- Kazmi WH, Obrador GT, Khan SS, Pereira BJ, Kausz AT. Late nephrology referral and mortality among patients with end-stage renal disease: a propensity score analysis. Nephrol Dial Transplant 2004;19:1808-14
- Kessler M, Frimat L, Panescu V, Briancon S. Impact of nephrology referral on early and midterm outcomes in ESRD: EPidemiologie de l'Insuffisance REnale chronique terminale en Lorraine (EPIREL): results of a 2-year, prospective, community-based study. Am J Kidney Dis 2003;42:474-85
- Khan SS, Xue JL, Kazmi WH et al. Does predialysis nephrology care influence patient survival after initiation of dialysis? Kidney Int 2005;67:1038-46
- Kim DH, Kim M, Kim H et al. Early referral to a nephrologist improved patient survival: prospective cohort study for end-stage renal disease in Korea. PLoS One 2013:8:1-10
- Levin A. Consequences of late referral on patient outcomes. Nephrol Dial Transplant 2000;15 Suppl 3:8-13
- Pan Y, Xu XD, Guo LL, Cai LL, Jin HM. Association of early versus late initiation of dialysis with mortality: systematic review and meta-analysis. Nephron Clin Pract 2012:120;c121-31
- Ravani P, Brunori G, Mandolfo S et al. Cardiovascular comorbidity and late referral impact arteriovenous fistula survival: a prospective multicenter study. J Am Soc Nephrol 2004;15:204-9
- Roderick P, Jones C, Drey N et al. Late referral for end-stage renal disease: a region-wide survey in the south west of England. Nephrol Dial Transplant 2002;17:1252-9
- Schwenger V, Morath C, Hofmann A et al. Late referral--a major cause of poor outcome in the very elderly dialysis patient. Nephrol Dial Transplant 2006;21:962-7
- Sesso R, Belasco AG. Late diagnosis of chronic renal failure and mortality on maintenance dialysis. Nephrol Dial Transplant 1996;11:2417-20
- Smart NA, Dieberg G, Ladhani M, Titus T. Early referral to specialist nephrology services for preventing the progression to end-stage kidney disease. Cochrane Darabase Syst Rev 2014: Jun 18;6:CD007333
- Stoves J, Bartlett CN, Newstead CG. Specialist follow up of patients before end stage renal failure and its relationship to survival on dialysis. Postgrad Med J 2001;77:586-8
- Temel JS, Greer JA, Muzikansky A et al. Early palliative care for patients with metastatic non-smallcell lung cancer. N Engl J Med 2010;363:733-42
Beoordelingsdatum en geldigheid
Publicatiedatum : 06-04-2018
Beoordeeld op geldigheid : 18-01-2018
Jaarlijks wordt door de initiatiefnemers van de ontwikkeling van deze richtlijn bepaald of actualisatie van de richtlijn nodig is. Indien actualisatie gewenst is, spannen de initiatiefnemers zich in om de hiervoor noodzakelijke voorwaarden (bijvoorbeeld financiering, samenstelling werkgroep) te realiseren. Nieuwe of nog niet behandelde knelpunten kunnen aanleiding zijn tot actualisatie van de richtlijn.
Algemene gegevens
Deze richtlijn is ontwikkeld in samenwerking met:
- Koninklijke Nederlandse Maatschappij ter Bevordering der Pharmacie
- Nederlandse Federatie voor Nefrologie
- Nederlandse Vereniging van Diëtisten / Diëtisten Nierziekten Nederland
- Nederlandse Vereniging van Ziekenhuisapothekers
- Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde
- Nierpatiënten Vereniging Nederland
Met ondersteuning van:
- Nederlands Huisartsen Genootschap
- Nederlandse Internisten Vereniging
- PROVA
De ontwikkeling van deze richtlijn is gefinancierd vanuit een projectbudget door de Stichting Kwaliteitsgelden Medisch Specialisten en het Nederlands Huisartsen Genootschap.
Doel en doelgroep
Doel
Het doel van deze richtlijn is de kwaliteit van zorg en patiëntveiligheid van patiënten met CNS te waarborgen en waar mogelijk te verbeteren. In deze richtlijn zijn aanbevelingen geformuleerd die professionals in de zorg hiertoe handvaten geven. Daarbij is het doel bovendien de zorg in de eerste en tweede lijn zoveel mogelijk op elkaar af te stemmen en daarbij uitdrukkelijk het patiëntenperspectief een plaats te geven.
Doelgroep
De doelgroep van deze richtlijn zijn professionals die zich bezig houden met de zorg voor patiënten met CNS. Hieronder worden in ieder geval verstaan: huisartsen, internisten, internist-nefrologen, apothekers, laboratoriumspecialisten klinische chemie en diëtisten. Ook andere professionals, zoals andere medisch specialisten, verpleegkundigen en maatschappelijk werkenden, kunnen hun voordeel doen met deze richtlijn.
Samenstelling werkgroep
Voor de ontwikkeling van deze richtlijn is een multidisciplinaire werkgroep ingesteld, onder voorzitterschap van dhr. dr. Marc Hemmelder, internist-nefroloog, en mw. drs. Jacintha van Balen, huisarts. In de werkgroep hebben gemandateerde vertegenwoordigers van de volgende beroepsverenigingen zitting:
- Koninklijke Nederlandse Maatschappij ter Bevordering der Pharmacie
- Nederlands Huisartsen Genootschap
- Nederlandse Internisten Vereniging / Nederlandse Federatie voor Nefrologie
- Nederlandse Vereniging van Diëtisten / Diëtisten Nierziekten Nederland
- Nederlandse Vereniging van Ziekenhuisapothekers
- Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde
Om het patiëntenperspectief in de werkgroep te waarborgen, hadden twee vertegenwoordigers van de Nierpatiënten Vereniging Nederland zitting in de werkgroep. De werkgroep werd procedureel en methodologisch ondersteund door PROVA. Logistieke ondersteuning is gegeven door de Nederlandse Internisten Vereniging en het Nederlands Huisartsen Genootschap. Het secretariaat is gevoerd door het Nederlands Huisartsen Genootschap.
Synchroon aan de ontwikkeling van deze multidisciplinaire richtlijn zijn de NHG-Standaard Chronische Nierschade en aanvullende NIV-modules Chronische Nierschade ontwikkeld. De werkgroepleden van de Standaardwerkgroep en van de NIV-werkgroep maakten deel uit van de werkgroep van de multidisciplinaire richtlijn, om zo alle trajecten zo veel mogelijk op elkaar af te stemmen.
- Mw. drs. Jacintha van Balen, huisarts, Nederlands Huisartsen Genootschap, Utrecht, namens het Nederlands Huisartsen Genootschap – voorzitter
- Dhr. dr. Marc Hemmelder, internist-nefroloog, Nefrovisie, Utrecht, namens de Nederlandse Internisten Vereniging en de Nederlandse Federatie voor Nefrologie – voorzitter
- Mw. drs. Mariska Tuut, epidemioloog, PROVA, Varsseveld – secretaris
- Dhr. Peter van Cuijk, Apeldoorn, ervaringsdeskundige, namens de Nierpatiënten Vereniging Nederland
- Dhr. prof. dr. Ron Gansevoort, internist-nefroloog, UMC Groningen, namens de Nederlandse Internisten Vereniging en de Nederlandse Federatie voor Nefrologie
- Dhr. dr. Wim de Grauw, huisarts te Berghem, Radboudumc, Nijmegen, namens het Nederlands Huisartsen Genootschap
- Mw. Inez Jans, diëtist, Ziekenhuis Gelderse Vallei, Ede, namens Nederlandse Vereniging van Diëtisten en Diëtisten Nierziekten Nederland
- Mw. dr. Birgit Koch, ziekenhuisapotheker-klinisch farmacoloog, Erasmus MC, Rotterdam, namens de Nederlandse Vereniging van Ziekenhuisapothekers
- Mw. drs. Karen de Leest, apotheker, Apotheek de Roerdomp, Nieuwegein, namens de Koninklijke Nederlandse Maatschappij ter Bevordering der Pharmacie
- Mw. drs. Karen Prantl, Bussum, coördinator kwaliteit & onderzoek, Nierpatiënten Vereniging Nederland, namens de Nierpatiënten Vereniging Nederland
- Dhr. dr. Paul Schenk, laboratoriumspecialist klinische chemie / klinisch chemicus, LUMC, Leiden, namens de Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde
- Mw. dr. Nynke Scherpbier, huisarts, Radboudumc, Nijmegen, namens het Nederlands Huisartsen Genootschap
- Mw. drs. Judith Tjin-A-Ton, huisarts, Amstelveen, namens het Nederlands Huisartsen Genootschap
- Mw. dr. Neelke van der Weerd, internist-nefroloog, AMC, Amsterdam, namens de Nederlandse Internisten Vereniging en de Nederlandse Federatie voor Nefrologie
Belangenverklaringen
|
Naam |
Namens |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Reputatie-management |
Extern gefinancierd onderzoek |
Kennis-valorisatie |
Overige belangen |
|
Jacintha van Balen |
NHG |
Huisarts 0,6 FTE; Teamleider afdeling Richtlijnen en Wetenschap |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Marc Hemmelder |
NIV / NFN |
Internist-nefroloog Medisch Centrum Leeuwarden (0,6 FTE) Uitvoerend bestuurder Nefrovisie (0,4 FTE) |
Geen |
Geen |
Geen |
Geen |
Dolomites studie van Astellas |
Renine, registratie van patiënten met nierfunctievervaning in Nederland. Onderdeel van Nefrovisie |
Geen |
|
Mariska Tuut |
onafhankelijk |
Eigenaar PROVA, adviesbureau voor procesmatige en methodologische ondersteuning bij de ontwikkeling van evidence-based richtlijnen en andere kwaliteitsinstrumenten |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Peter van Cuijk |
NVN |
Ruim 35 jaar gewerkt in de Jeugdhulpverlening als orthopedagoog en manager. Ervaring in diverse settingen en diverse functie's, zowel inhoudelijk, uitvoerend en in de aansturing/management. |
bestuursfunctie (penningmeester) amateur-theatervereniging De Apeldoornse Komedie |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
|
Ron Gansevoort |
NIV / NFN |
Internist-nefroloog, UMCG |
Lid bestuur Nederlandse Federatie voor Nefrologie (sectie Wetenschap); Lid Wetenschappelijke Adviesraad Nierstichting; Lid redactie wetenschappelijke tijdschriften: American Journal of Kidney Diseases, Clinical Journal of the American Society of Neprology, European Medical Journal Nephrology, Journal of Nephrology, Nephrology Dialysis and Transplantation, Nephron Clinical Practice (alle functies onbetaald) |
Geen |
Geen |
Lid wetenschappelijke adviesraad Nierstichting |
Geen |
Geen |
Geen |
|
Wim de Grauw |
NHG |
Huisarts te Berghem (0,7 fte); Senior staflid huisarts-onderzoeker afdeling Eerstelijns Geneeskunde Radboudumc Nijmegen (0,3 fte) |
Herder bij diverse professionele begrazingsbedrijven |
Geen |
Geen |
Onderzoek op het gebied van Chronische Nierschade is een belangrijk onderdeel van de onderzoekslijn vaatschade van de afdeling Eerstelijnsgeneeskunde Radboudumc in samenwerking met de afdeling Nefrologie Radboudumc |
De afdeling Eerstelijns Geneeskunde ontvangt subsidie van de Nierstichting Nederland voor onderzoek op het gebied van Chronische Nierschade |
Afdeling Eerstelijnsgeneeskunde Radboudumc heeft samen met de afdeling Nefrologie Radboudumc en Zorgdomein Telenefrologie ontwikkeld, een e-health applicatie voor consultatie tussen huisarts en nefroloog |
Geen |
|
Inez Jans |
NVD / DNN |
Diëtist, aandachtsgebied nierziekten en voedingsteam, Ziekenhuis Gelderse Vallei (fulltime dienstverband) |
Extern assessor Hogeschool van Arnhem en Nijmegen, opleiding Voeding en Diëtetiek (flex contract); Actief lid Diëtisten Nierziekten Nederland (voorzitter DNN werkgroep kwaliteit; lid DNN werkgroep richtlijnen); vanuit die rol lid van de werkgroep multidisciplinaire richtlijn chronisch nierfalen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Birgit Koch |
NVZA |
Ziekenhuisapotheker-klinisch farmacoloog 0,85 FTE |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
ZonMw: PK/PD antipsychotica; Stichting Coolsingel: middelenmisbruik zwangerschap |
n.v.t. |
n.v.t. |
|
Karen de Leest |
KNMP |
Apotheker, Apotheek de Roerdomp, Nieuwegein, 24 uur/week |
Wetenschappelijk medewerker KNMP, 10 uur/week |
Geen |
Geen |
Redactielid Vascuzine, tijdschrift v.d. Vasculitis patiënten vereniging, vrijwilligerswerk, geen boegbeeldfunctie |
Geen |
Geen |
Nee |
|
Karen Prantl |
NVN |
Beleidsmedewerker kwaliteit |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Paul Schenk |
NVKC |
Klinisch chemicus/ laboratoriumspecialist Klinische chemie, LUMC Leiden (voltijds, loondienst) |
Geen nevenwerkzaamheden buiten LUMC |
Geen persoonlijke financiële belangen |
Geen relevante persoonlijke relaties als hier bedoeld |
Geen relevante posities als hier bedoeld |
Geen relevant extern gefinancierd onderzoek |
Geen relevante valorisatie |
Nee, geen relevante overige belangen |
|
Nynke Scherpbier |
NHG |
Opleidingsdirecteur extramurale vervolgopleidingen RadboudUMC 0,8 FTE; huisarts 0,2 FTE |
Council member EURACT, Europese organisatie voor opleiden in de huisartsgeneeskunde (onbetaald) |
Geen |
Geen |
Geen |
Ik ben co-promotor van een promotietraject dat wordt gefinancierd door de Nierstichting met als doel te onderzoeken: 1. wat belemmerende en bevorderende factoren zijn in het naleven van de LTA; 2. hoe patiënten de voorlichting over CNS ervaren; 3. of het mogelijk is om veilige wijze bepaalde patiënten terug te verwijzen vanuit de tweede naar de eerste lijn |
Afdeling Eerstelijnsge-neeskunde Radbou-dumc heeft samen met de afdeling Nefro-logie Radboudumc en Zorgdomein Telenefrologie ontwikkeld, een e-health applicatie voor consultatie tus-sen huisarts en nefroloog |
Geen |
|
Judith Tjin-A-Ton |
NHG |
Huisarts |
Kaderhuisarts hart- en vaatziekten: kwaliteitscommissie en werkgroep HVZ bij Amstellandzorg BV (betaald) |
Geen |
Geen |
Geen |
Geen |
Geen |
Geen |
|
Neelke van der Weerd |
NIV / NFN |
Internist-nefroloog AMC Amsterdam |
- |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
n.v.t. |
Methode ontwikkeling
Evidence based
Implementatie
Gedurende het hele proces van richtlijnontwikkeling is rekening gehouden met implementatie van de richtlijn in de praktijk, bijvoorbeeld bij de samenstelling van de werkgroep, de brede knelpunteninventarisatie en de uitgebreide commentaarronde. De werkgroep heeft adviezen voor implementatie (implementatieplan) en indicatoren geformuleerd. Deze zijn opgenomen onder de aanverwante producten.
Na autorisatie van de richtlijn wordt deze ten minste op de website van de Nederlandse Internisten Vereniging en het Nederlands Huisartsen Genootschap gepubliceerd. Ook andere deelnemende partijen zijn vrij de richtlijn op hun website te publiceren. De richtlijn wordt ter publicatie aangeboden aan www.richtlijnendatabase.nl. Daarnaast wordt getracht samenvattingen van de richtlijn in Nederlandse tijdschriften te publiceren, aandacht aan de richtlijn te besteden op congressen, en nascholingsmateriaal en voorlichtingsmateriaal te ontwikkelen, om zo de implementatie van de richtlijn te bevorderen.
Een voor patiënten begrijpelijke samenvatting van de aanbevelingen uit deze richtlijn komt beschikbaar via www.thuisarts.nl. Een verdieping daarvan komt beschikbaar via de website van de Nierstichting/Nederlandse Vereniging van Nierpatiënten.
Werkwijze
Knelpunteninventarisatie
De richtlijnwerkgroep heeft in de eerste werkgroepvergadering knelpunten benoemd in de zorg voor patiënten met CNS. Deze knelpunten zijn in een invitational conference voorgelegd aan belanghebbenden, waarbij ook is gediscussieerd over aanvullende knelpunten. Voor deze invitational conference zijn, naast vertegenwoordigers van verenigingen die in de werkgroep afgevaardigd zijn, de volgende partijen uitgenodigd:
- Federatie Medisch Coördinerende Centra
- Inspectie voor de Gezondheidszorg
- Nederlandse Federatie van Universitair Medische Centra
- Nederlandse Vereniging van Ziekenhuizen
- Nederlandse Zorgautoriteit
- Nierstichting Nederland
- Patiëntenfederatie Nederland
- Vereniging Innovatieve Geneesmiddelen
- Vereniging Maatschappelijk Werk Nefrologie
- Verpleegkundigen & Verzorgenden Nederland
- ZorgInstituut Nederland
- Zorgverzekeraars Nederland
De richtlijnwerkgroep heeft de input vanuit de knelpunteninventarisatie geanalyseerd en in de tweede werkgroepvergadering de knelpunten en uitgangsvragen vastgesteld.
Uitwerking knelpunten en uitgangsvragen in conceptrichtlijn
Per knelpunt werd door de werkgroep vooraf bepaald op welke wijze dit knelpunt zou worden behandeld: met behulp van systematisch literatuuronderzoek (evidence-based) of meer op basis van bestaande richtlijnen en professionele expertise in de werkgroep. Er was financiering voor de uitwerking van een beperkt aantal vragen met behulp van systematisch literatuuronderzoek. Om toch ook de andere belangrijke knelpunten een plaats te geven in deze richtlijn, is voor uitwerking van de resterende knelpunten voor een minder arbeidsintensieve wijze gekozen. De wijze van uitwerking van de knelpunten/uitgangsvragen staat per uitgangsvraag vermeld in de verschillende modules van deze richtlijn. De keuze van de knelpunten die met systematisch literatuuronderzoek zijn beantwoord is gemaakt door de gezamenlijke werkgroep, op basis van verwachting dat het literatuuronderzoek mogelijk tot nieuwe inzichten zou leiden en de afwezigheid van recente internationale richtlijnen over de specifieke uitgangsvraag.
De uitwerking van de knelpunten in conceptteksten werd voorbereid door de epidemioloog die bij de ontwikkeling van de richtlijn betrokken was. Per knelpunt werd deze inhoudelijk bijgestaan door een aantal werkgroepleden, afhankelijk van het onderwerp. De conceptteksten werden plenair tijdens de werkgroepvergaderingen besproken, en na discussie bijgesteld. De richtlijnwerkgroep is 9 maal bijeen geweest, alvorens de conceptrichtlijn is vastgesteld.
Bij veel uitgangsvragen is voor de onderbouwing gebruik gemaakt van internationale richtlijnen op het gebied van CNS. De KDIGO richtlijn en de NICE richtlijn over chronische nierschade zijn op kwaliteit beoordeeld bij aanvang van de ontwikkeling van deze multidisciplinaire richtlijn. De wijze van onderbouwing van deze internationale richtlijnen werd door de richtlijnwerkgroep als adequaat beoordeeld. Beide richtlijnen maakten gebruik van de GRADE methodiek.
Voor de uitgangsvragen die met behulp van systematisch literatuuronderzoek zijn uitgewerkt, is gebruik gemaakt van de principes van de GRADE Working Group. Voor achtergrondinformatie over deze methodiek wordt verwezen naar het Dutch GRADE Network (www.dutchgradenetwork.org). Vanwege de verschillende totstandkoming van de diverse aanbevelingen heeft de werkgroep ervoor gekozen om het graderen van aanbevelingen, zoals dit wordt gepropageerd in de GRADE-methodiek, niet door te voeren in deze richtlijn. Hiermee is eenheid in de formulering van aanbevelingen gecreëerd.
De module ‘Samenwerking bij CNS’ bevat samenwerkingsafspraken: aanbevelingen voor consultatie en verwijzing tussen eerste en tweede lijn, en aanbevelingen voor samenwerking met laboratoriumspecialisten klinische chemie, diëtisten en apothekers. Hierbij zijn geen specifieke uitgangsvragen genoemd, maar is uitgegaan van eerdere samenwerkingsafspraken en uitgangspunten en aanbevelingen uit de modules ‘Diagnostiek en stadiëring bij CNS’ en ‘Beleid en behandeling bij CNS’.
Daar waar in deze richtlijn ‘hij’ genoemd staat, kan ook ‘zij’ gelezen worden.
Commentaar en autorisatie
De conceptrichtlijn is ter commentaar aangeboden aan alle partijen die bij de knelpunteninventarisatie om input gevraagd zijn. Het binnengekomen commentaar is door de werkgroep beoordeeld en verwerkt in de richtlijn. Daarbij is beargumenteerd welke commentaren wel en welke niet zijn overgenomen.
Daarna is de richtlijn ter autorisatie voorgelegd aan de partijen die in de werkgroep vertegenwoordigd zijn. De richtlijn is geautoriseerd door de Nederlandse Internisten Vereniging, het Nederlands Huisartsen Genootschap, de Nederlandse Vereniging voor Diëtisten, de Nederlandse Vereniging voor Ziekenhuisapothekers en de Nederlandse Vereniging voor Klinische Chemie en Laboratoriumgeneeskunde. Ook is de richtlijn goedgekeurd door de Nierpatiënten Vereniging Nederland.
Juridische betekenis van richtlijnen
Richtlijnen zijn geen wettelijke voorschriften, maar op ‘evidence' gebaseerde inzichten en aanbevelingen waaraan zorgverleners moeten voldoen om kwalitatief goede zorg te verlenen. Na autorisatie van de richtlijn door een beroepsvereniging, wordt de richtlijn gezien als deel van de ‘professionele standaard'. Aangezien de aanbevelingen hoofdzakelijk gebaseerd zijn op de ‘gemiddelde patiënt', kunnen zorgverleners op basis van hun professionele autonomie waar nodig afwijken van de richtlijn. Afwijken van richtlijnen kan in bepaalde situaties zelfs noodzakelijk zijn. Wanneer van de richtlijn wordt afgeweken, dient dit beargumenteerd en gedocumenteerd te worden.
