Pijnblokkades bij chronische bekkenpijn
Uitgangsvraag
Wat is de plaats van invasieve behandeling door middel van blokkades door de anesthesioloog-pijnspecialist voor patiënten met chronische bekkenpijn?
Aanbeveling
Aanbeveling-1
Overweeg een behandeling met impar blokkade bij patiënten met chronische bekkenpijn en/of perineale pijn (inclusief coccygodynie).
Laat de keuze voor behandeling met impar blokkade door middel van pulsed of thermaal radiofrequency ablatie afhangen van de ervaring en voorkeur van de pijnspecialist en houd rekening met de voorkeur van de patiënt.
Aanbeveling-2
Overweeg een behandeling met wortelblokkade bij patiënten met chronische bekkenpijn alleen indien er sprake is van onbegrepen chronische bekkenpijn en andere behandelopties ineffectief zijn gebleken.
Aanbeveling-3
Overweeg een perifere zenuwblokkade als diagnostische blokkade bij patiënten met chronische bekkenpijn.
Overweeg een n. pudendus blokkade (met of zonder pulsed radiofrequency) bij patiënten met pudendale neuralgie.
Overweeg een n. ilioinguinalis en n. genitofemoralis blokkade met pulsed radiofrequency bij mannen met chronische testiculaire pijn.
Overwegingen
De onderstaande overwegingen en aanbevelingen gelden voor het overgrote deel van de populatie waarop de uitgangsvraag betrekking heeft.
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Plexusblokkade
Op basis van de literatuur lijkt het erop dat impar blokkades (plexusblokkades) de pijnintensiteit verminderen bij patiënten met chronische bekkenpijn en/of chronische perineale pijn, tenminste op 1 en 6 maanden post-interventie. De bewijskracht werd gegradeerd als ‘laag’, doordat dit berust op observationeel onderzoek. De bewijskracht voor het effect op de pijnintensiteit 12 maanden na behandeling is onduidelijk doordat het gepoolde effect de grens van klinische relevantie overlapt. Daarnaast lijkt plexusblokkade met conventionele radiofrequente thermocoagulatie effectiever in het verminderen van de pijnintensiteit en is dit geassocieerd met een hogere patiënttevredenheid dan pulsed radiofrequency ablatie. Het effect op complicaties of kwaliteit van leven is niet duidelijk. Er was onvoldoende informatie beschikbaar om een GRADE-beoordeling voor de uitkomstmaat complicaties uit te kunnen voeren.
De bewijskracht voor de effectiviteit van plexusblokkades bij patiënten met chronische bekkenpijn is als laag gegradeerd, maar op basis van expert opinion, de lage invasiviteit en beperkte complicatie risico’s van deze behandeling kan een impar blokkade (pulsed radiofrequency of radiofrequency) een goede behandeloptie zijn, welke laagdrempelig toe te passen is bij patiënten met chronische bekkenpijn en coccygodynie voor een bepaalde periode. Voor de effectiviteit van plexus hypogastricus blokkade bij patiënten met chronische bekkenpijn zijn er geen goede studies gevonden, derhalve kan hierover geen aanbeveling worden gedaan.
Wortelblokkade
Op basis van de literatuur is het onduidelijk wat het effect van wortelblokkades bij patiënten met chronische bekkenpijn is. Er zijn geen studies gevonden die het effect van een selectieve wortelblokkade behandeling bij patiënten met chronische bekkenpijn hebben onderzocht. Een proefblokkade wordt in de praktijk echter wel veelvuldig gebruikt bij chronisch pijn, zowel diagnostisch om de bron van de pijn te kunnen identificeren als therapeutisch. Het langdurige effect van een wortelblokkade is eveneens niet onderzocht. Op basis van deze overwegingen is besloten om een wortelblokkade in de praktijk wel te overwegen bij patiënten met onbegrepen chronische bekkenpijn bij wie andere behandelopties ineffectief zijn gebleken.
Perifere zenuwblokkade
In totaal werden 2 studies geïncludeerd over de effectiviteit van perifere zenuwblokkade met/zonder pulsed radiofrequency ablatie bij patiënten met chronische bekkenpijn. Op basis van de literatuur lijkt het erop dat de pijnintensiteit na perifere zenuwblokkades met pulsed radiofrequency ablatie bij patiënten met pudendale neuralgie (n. pudendus) sterker verminderd, vergeleken met periferere zenuwblokkade zonder pulsed radiofrequency ablatie. Daarnaast lijkt het er ook op dat de pijnintensiteit sterker verminderd bij patiënten met chronische testiculaire pijn na perifere zenuwblokkade met pulsed radiofrequency (n. ilioinguinalis en n. genitofemoralis) vergeleken met een shambehandeling. De bewijskracht werd in beide gevallen gegradeerd als ‘laag’, vanwege risk of bias en doordat het effect de grens van een klinisch relevant effect overlapt. Bij patiënten met pudendale neuralgie lijkt na interventie met of zonder pulsed radiofrequency ablatie (n. pudendus) geen verschil in het voorkomen van de complicaties hypertensie en duizeligheid te zijn. Deze uitkomst had een GRADE ‘laag’, vanwege risk of bias.
Er werden geen studies geïncludeerd waarin het effect van perifere zenuwblokkade zonder pulsed radiofrequency ablatie werd vergeleken met geen behandeling of baseline score bij patiënten met chronische bekkenpijn. Op basis van de literatuuranalyse werd daarom geconcludeerd dat het onduidelijk is wat de effectiviteit van perifere zenuwblokkade zonder pulsed radiofrequency ablatie is wanneer dit wordt vergeleken met geen behandeling of baseline score (GRADE ‘zeer laag’).
Op basis van expert opinion en de literatuur kan een zenuwblokkade (een pulsed radiofrequency van de n. pudendus, ilio-inguinalis, genitofemoralis) een goede pijnbehandeling zijn voor een bepaalde periode. Verder kan een perifere zenuwblokkade als een goed diagnosticum dienen bij het opsporen van de oorzaak van de pijn.
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
De patiënt dient goed geïnformeerd te worden over de effectiviteit en de kans op complicaties van deze blokkades zodat een de patiënt de juiste behandeling op maat krijgt. Een blokkade is geen permanente of een curatieve optie, dus kans op de herhaling van de blokkade is groot.
Kosten (middelenbeslag)
Er zijn geen studies over de kosteneffectiviteit van deze blokkades.
Aanvaardbaarheid voor de overige relevante stakeholders
Het is onbekend of er bezwaren zijn van relevante stakeholders.
Haalbaarheid en implementatie
Er worden geen beperkingen zien ten aanzien van de haalbaarheid en implementatie van de aanbevelingen.
Rationale/ balans tussen de argumenten voor en tegen de interventie
Aanbeveling-1
De bewijskracht van impar blokkade (Plexus blokkade) is gegradeerd met GRADE laag, echter gezien de lage invasiviteit en beperkte complicatie risico’s van deze behandeling kan een impar blokkade een goede behandeloptie zijn, welke laagdrempelig toe te passen is bij chronische bekkenpijn. De pijnintensiteit bij patiënten met chronische perineale pijn lijkt 6 weken na ganglion impar blokkade met conventionele radiofrequente thermocoagulatie sterker te verminderen, vergeleken met pulsed radiofrequency ablatie.
Aanbeveling-2
Op basis van literatuur is er geen indicatie voor een wortelblokkade bij een chronische bekkenpijn. Ervaring uit de praktijk bij chronische pijnpatiënten ondersteunt alleen een behandeling door middel van wortelblokkade bij chronische bekkenpijn indien het om onbegrepen pijn gaat en andere behandelopties ineffectief zijn gebleken.
Aanbeveling-3
Op basis van de literatuur is het effect van een perifere zenuwblokkade zonder pulsed radiofrequency ablatie vergeleken met geen behandeling of baseline bij patiënten met chronische bekkenpijn beoordeeld met een GRADE zeer laag. Er werd geen literatuur hierover geïncludeerd.
Literatuur over de effectiviteit van n. pudendus blokkade met of zonder pulsed radiofrequency op de pijnintensiteit bij patiënten met pudendale neuralgie werd gegradeerd met een GRADE laag, vanwege risk of bias en doordat het effect de grens van een klinisch relevant effect overlapt.
Literatuur over de effectiviteit van perifere zenuwblokkade (n. ilioinguinalis en n. genitofemoralis) met pulsed radiofrequency op de pijnintensiteit bij patiënten met chronische testiculaire pijn werd gegradeerd met een GRADE laag, vanwege risk of bias en doordat het effect de grens van een klinisch relevant effect overlapt.
Op basis van expert opinion en de literatuur kan een zenuwblokkade (een pulsed radiofrequency van de n. pudendus, ilio-inguinalis, genitofemoralis) een goede pijnbehandeling zijn voor een bepaalde periode. Verder kan een perifere zenuwblokkade als een goed diagnosticum dienen bij het opsporen van de oorzaak van de pijn.
Onderbouwing
Er worden steeds meer patiënten met chronische bekkenpijn doorverwezen voor een zenuwblokkade. De blokkades kunnen bestaan uit selectieve sacrale wortelblokkades (bijvoorbeeld S1,S2), perifere zenuwblokkades (n. ilio-inguinalis, n. pudendus) en plexus blokkades (plexus hypogastricus, ganglion impar). Helaas zijn er nog geen duidelijke richtlijnen binnen de pijnbestrijding voor chronische bekkenpijn. Door middel van deze richtlijnen wordt er gekeken naar de effectiviteit van deze invasieve pijnbehandelingen.
1.1. Plexusblokkade (effectiviteit pre- versus post-baseline)
|
Laag Grade |
Patiënten met chronische bekkenpijn en/of chronische perineale pijn lijken een grotere kans te hebben op > 50% afname van de pijn na behandeling met ganglion impar blokkade (gemiddelde tijdsinterval onbekend), vergeleken met baseline.
Bronnen: (Li, 2016) |
|
Laag Grade |
De pijnintensiteit bij patiënten met chronische bekkenpijn en/of chronische perineale pijn lijkt 1 maand na behandeling met ganglion impar blokkade te kunnen verminderen.
Bronnen: (Li, 2016; Kircelli, 2019) |
|
Laag Grade |
De pijnintensiteit bij patiënten met chronische bekkenpijn en/of chronische perineale pijn lijkt 6 maanden na behandeling met ganglion impar blokkade te kunnen verminderen.
Bronnen: (Li, 2016; Kircelli, 2019) |
|
Zeer laag Grade |
Het is onduidelijk wat de effectiviteit van ganglion impar blokkade bij patiënten met chronische bekkenpijn en/of chronische perineale pijn is 12 maanden na behandeling.
Bronnen: (Li, 2016; Kircelli, 2019) |
|
- Grade |
Het is onbekend wat de effectiviteit van plexusblokkades op de patiënttevredenheid, complicaties en kwaliteit van leven bij patiënten met chronische bekkenpijn en/of chronische perineale pijn is 12 maanden na behandeling. |
1.2. Plexusblokkades (effectiviteit conventionele thermocoagulatie versus pulsed radiofrequency ablatie)
|
Laag Grade |
De pijnintensiteit bij patiënten met chronische perineale pijn lijkt 6 weken na ganglion impar blokkade met conventionele radiofrequente thermocoagualtie sterker te verminderen, vergeleken met pulsed radiofrequency ablatie.
Bronnen: (Usmani, 2018) |
|
Laag Grade |
De patiënttevredenheid bij patiënten met chronische perineale pijn lijkt 6 weken na ganglion impar blokkade met conventionele radiofrequente thermocoagulatie hoger te zijn, vergeleken met pulsed radiofrequency ablatie.
Bronnen: (Usmani, 2018) |
|
- Grade |
Het is onbekend wat de effectiviteit van conventionele thermocoagulatie versus pulsed radiofrequency ablatie na ganglion impar blokkade is op de uitkomsten complicaties en kwaliteit van leven bij patiënten met chronische bekkenpijn is. |
2. Wortelblokkade
|
- Grade |
Het is onbekend wat de effectiviteit van wortelblokkades op de pijnintensiteit, patiënttevredenheid, complicaties en kwaliteit van leven bij patiënten met chronische bekkenpijn is. |
3.1. Perifere zenuwblokkade (zonder pulsed radiofrequency ablatie)
|
- Grade |
Het is onbekend wat de effectiviteit van perifere zenuwblokkade zonder pulsed radiofrequency ablatie is op de pijnintensiteit, patiënttevredenheid, complicaties en kwaliteit van leven bij patiënten met chronische bekkenpijn, wanneer dit werd vergeleken met geen behandeling of baseline. |
3.2. Perifere Zenuwblokkade (met pulsed radiofrequency ablatie)
|
Laag Grade |
De pijnintensiteit bij patiënten met pudendale neuralgie lijkt 1 en 3 maanden na perifere zenuwblokkade met pulsed radiofrequency ablatie (n. pudendus) sterker te verminderen, vergeleken met zenuwblokkade (n. pudendus) zonder pulsed radiofrequency ablatie.
Bronnen: (Fang, 2018) |
|
Laag Grade |
De pijnintensiteit bij mannen met chronische testiculaire pijn lijkt 3 maanden na perifere zenuwblokkade met pulsed radiofrequency ablatie (n. ilioinguinalis en n. genitofemoralis) sterker te verminderen, vergeleken met shambehandeling.
Bronnen: (Hetta, 2018) |
|
Laag Grade |
De complicaties hypertensie en duizeligheid lijken even vaak voor te komen na zenuwblokkade (n. pudendus) met of zonder pulsed radiofrequency ablatie bij patiënten met pudendale neuralgie.
Bronnen: (Fang, 2018) |
|
- Grade |
Het is onbekend welke complicatiescomplicatie voorkomen na zenuwblokkade (n. ilioinguinalis en n. genitofemoralis) met pulsed radiofrequency ablatie vergeleken met een shambehandeling.
|
|
- Grade |
Het is onbekend wat de effectiviteit van perifere zenuwblokkades met pulsed radiofrequency ablatie is op de patiënttevredenheid en kwaliteit van leven bij patiënten met pudendale neuralgie. |
Beschrijving studies
De beschrijving van de geïncludeerde studies is gestratificeerd voor het type pijnblokkade.
1. Plexusblokkades
Li (2016) voerde een systematische review en meta-analyse uit naar de effectiviteit en veiligheid van ganglion impar blokkade bij patiënten met hardnekkige chronische bekkenpijn en/of perineale pijn. De search werd verricht in mei 2015 in de databases MEDLINE, Embase en het Cochrane Central Register of Controlled Trials (CENTRAL). In totaal werden 16 trials met 245 patiënten geïncludeerd: tien studies met patiënten met chronische perineale pijn (Abejon, 2007; Agarwal-Kozlowski, 2009; Hamaguchi, 2003; Johnston, 2012; Mastroluca, 2011; Ozyalcin, 1996; Plancarte-Sanchez, 2005; Park, 2015; Reig, 2005; Swofford, 1998), één studie met patiënten met chronische bekkenpijn (Malec-Milewska, 2014), twee studies met patiënten met chronische bekkenpijn en/of chronische perineale pijn (Ahmed, 2015; Anwer, 2011) en drie studies met chronische coccygodynie (Demircay, 2010; Gunduz, 2015; Sagir, 2011). Er werd niet gerapporteerd hoeveel mannen/vrouwen waren geïncludeerd of wat de duur van de pijn was. Follow-up varieerde van enkele dagen tot 2 jaar (gemiddelde niet gerapporteerd). Voor een uitgebreid overzicht van de studiedetails wordt verwezen naar de bijgevoegde evidencetabellen.
Kircelli (2019) beschreef een retrospectieve observationele studie waarin patiënten met coccygodynie werden behandeld met ganglion impar blokkade met radiofrequente thermocoagulatie (RFT). Inclusiecriteria betroffen patiënten met traumatische of niet-traumatische coccygodynie waarbij eerdere conservatieve behandeling niet werkte. Patiënten hadden > 6 maanden coccygodynie. In totaal werden 20 patiënten geïncludeerd bij wie ganglion impar block ten behoeve van de diagnose tenminste 80% tijdelijke pijnverlichting gaf. RFT (80°C, 120 seconden, 50-Hz cyclus/cylci) werd daarna uitgevoerd, vooraf verdoofd met 1 ml 2% lidocaïne. Gemiddelde leeftijd was 48,7 jaar (SD 14,3), n=11 (55%) waren mannen. Etiologie van coccygodynie was bij n=8 (40%) traumatisch en n=12 (60%) idiopathisch. Gemiddelde duur van de pijn was niet gerapporteerd. Effect van interventie werd gemeten op 1, 6 en 12 maanden post-baseline. Gemiddelde duur van follow-up was 17,3 maanden (SD 2,9).
Usmani (2018) beschreef en prospectieve, dubbelblind, gerandomiseerde studie waarin patiënten met chronische (niet-oncologische) perineale pijn werden behandeld met ganglion impar blokkade door middel van conventionele dan wel gepulseerde radiofrequente ablatie (CRF; PRF). Inclusiecriteria betroffen volwassen patiënten (15 tot 75 jaar) met minimaal 6 weken chronische perineale pijn, waarbij eerder conservatieve behandeling niet werkzaam was. Ten behoeve van de diagnose werd een ganglion impar blokkade met 1,5 ml 0,25% bupivacaine uitgevoerd. Patiënten die 50% afname van pijn rapporteerden na 2 tot 6 uur werden geïncludeerd in de studie. In totaal werden 70 patiënten geïncludeerd, 35 deelnemers werden gerandomiseerd in de conventionele radiofrequente thermocoagulatie groep (80°C, 90 seconden, 1 cyclus), 35 deelnemers werden gerandomiseerd in de PRF-groep (42°C, 4 minuten, 2 cylci (1 cyclus was 120 seconden)). Beide groepen kregen vooraf een injectie met 1 mL 2% lidocaïne, dit omdat CRF een pijnlijke procedure is en om confounding te voorkomen kreeg de PRF-groep dit ook. Er was 1 (3%) patiënt in de CRF-groep lost to follow-up en 4 patiënten in de PRF-groep (11%), redenen hiervoor werd niet gerapporteerd. Gemiddelde leeftijd in CRF-groep was 39,3 (SD 14,3) jaar en 42,3 (SD 15,6) jaar in de PRF-groep. Gemiddelde duur van de klachten was 13,7 (SD 9,3) maanden in de CRF en 15,2 (SD 8,3) maanden in de PRF-groep. Patiënten verschilden op baseline niet. Het was onduidelijk hoeveel mannen en vrouwen er waren geïncludeerd. Follow-up eindigde na 6 weken.
2. Wortelblokkades
Er werden geen studies geïncludeerd waarin de effectiviteit wortelblokkades werden bestudeerd bij patiënten met chronische bekkenpijn.
3. Perifere Zenuwblokkades
3.1. Perifere zenuwblokkades (zonder pulsed radiofrequency ablatie).
Er werden geen studies geïncludeerd waarin werd gekeken naar de effectiviteit van perifere zenuwblokkades zonder pulsed radiofrequency ablatie, vergeleken met geen behandeling of baseline.
3.2. Perifere zenuwblokkades (met pulsed radiofrequency ablatie).
Er werden 2 studies over perifere zenuwblokkades geïncludeerd waarin werd gekeken naar de effectiviteit van perifere zenuwblokkade met pulsed radiofrequency vergeleken met een behandeling zonder pulsed radiofrequency ablatie of een shambehandeling.
Fang (2018) beschreef een prospectieve, placebogecontroleerde RCT waarin patiënten met pudendale neuralgie werden behandeld met zenuwblokkade (n. pudendus) vergeleken met een zenuwblokkade (n. pudendus) met pulsed radio frequency (PRF). Inclusiecriteria betrof volwassen patiënten met gediagnosticeerde pudendale neuralgie. In totaal werden 80 patiënten geïncludeerd, 40 deelnemers werden gerandomiseerd in de groep die zenuwblokkade van de pudendale zenuw kreeg met 5 ml anestheticum (compound liquid 20 ml bestaande uit: Neurotropin® 6 ml, 2% lidocaïne 5 ml, 0,75% ropivacaïne 2 ml en 0.9% NaCl 7 ml) (groep 1); 40 deelnemers werden gerandomiseerd in de groep die PRF kreeg (42°C, 120 seconde puls modus, 2 cycli) gevolgd door dezelfde zenuwblokkade van de pudendale zenuw (groep 2). In groep 1 was 1 patiënt lost to follow-up (2,5%), in groep 2 waren 2 patiënten lost to follow-up (5%). Redenen hiervoor waren onduidelijk. Gemiddelde leeftijd was 45 jaar (SD 15,1) in groep 1 en gemiddeld 45,1 jaar (SD 12,6) in groep 2. Gemiddelde duur van de klachten was 7,4 (SD 3,9) maanden in groep 1, 6,4 (SD 3,8) maanden in groep 2. Patiënten verschilden niet op baseline, behalve in BMI: groep 1 had een hoger BMI dan groep 2 (25,4 (SD 3,9) versus 23,3 (SD 3)). Het was onduidelijk hoeveel mannen en vrouwen er waren geïncludeerd. Follow-up eindigde na 3 maanden post-interventie.
Hetta (2018) beschreef een dubbelblinde, sham gecontroleerde RCT waarin patiënten met chronische scrotale pijn (orchialgie) werden behandeld met zenuwblokkade van de n. ilioinguinalis en n. genitofemoralis met pulsed radiofrequency ablatie (PRF) of een sham behandeling. Inclusiecriteria betrof volwassen mannen chronische post-chirurgische testiculaire pijn met minimaal 3 maanden pijnklachten. Om geïncludeerd te worden moesten mannen > 50% pijnreductie op een VAS-schaal (0-10, geen - maximale pijn) gedurende 6 uur na behandeling van de spermatic cord met 2% lidocaïne 6 ml. In totaal werden 70 patiënten geïncludeerd, 35 deelnemers werden gerandomiseerd in de groep die zenuwblokkade van de n.ilioinguinalis en n.genitofemoralis door middel van PRF (40 tot 60 Volt; 2 Hertz frequentie; 20 milliseconde in 1-seconde-cyclus; cyclus duur 120 seconden, 4 cycli in totaal; 42°C). De controlegroep (n=35) kreeg een shambehandeling, dit betrof dezelfde behandelingsprocedure maar dan zonder daadwerkelijke PRF. In beide groepen werden 5 deelnemers uitgesloten van analyse: in de interventiegroep waren 3 patiënten lost to follow-up (reden onbekend) en werden 2 geëxcludeerd wegens het overtreden van studieprotocol (niet nader toegelicht); in de controlegroep waren 2 patiënten lost to follow-up (reden onbekend) en werden 3 geëxcludeerd wegens het overtreden van studieprotocol (niet nader toegelicht). Gemiddelde leeftijd was 35,8 (SD 9,7) jaar in de interventiegroep, 37,7 (SD 10,4) jaar. Gemiddelde duur van de klachten werd niet gerapporteerd. Patiënten verschilden niet op baseline. Follow-up eindigde na 3 maanden post-interventie.
Resultaten
De resultaten uit de studies worden hieronder beschreven per uitkomstmaat, gestratificeerd voor het type pijnblokkade en vergelijking. Resultaten worden zo veel mogelijk gepoold in een meta-analyse.
1. Pijnintensiteit
1.1. 1. Plexusblokkade (effectiviteit pre- versus post-baseline)
De uitkomstmaat pijnintensiteit na behandeling met plexusblokkade (ganglion impar blokkade) werd in 17 studies gerapporteerd (alle studies uit Li, 2016; Kircelli, 2018). De meta-analyse van Li (2016) rapporteerde deze uitkomstmaat op twee manieren: de odds op minder dan 50% verbetering in pijnscore post-baseline (exacte moment niet gerapporteerd) (Abejon, 2007; Agarwal-Koziowski, 2009; Ahmed, 2015; Anwar, 2011; Demircay, 2010; Gunduz, 2010; Hamaguchi, 2003; Johnston, 2012; Malec-Milewska, 2014; Mastroluca, 2011; Ozyalcin, 1996; Plancarte-Sanchez, 2005; Park, 2015; Reig, 2005; Swofford, 1998; Sagir, 2011). Daarnaast beschreven zeven studies het gemiddelde verschil in de pijnintensiteit tussen pre- en post-baseline: zes studies beschreven de uitkomstmaat 1 maand na post-baseline (Abejon, 2007; Ahmed, 2015; Demircay, 2010; Kircelli, 2019; Malex-Milewska, 2014), vier studies (ongeveer) 6 maanden post-baseline (4 maanden: Agarwal-Koziowski, 2009; 6 maanden: Gunduz, 2010; Kircelli, 2019; en gemiddeld 9 maanden: Demircay (2010)) en twee studies 12 maanden post-baseline (Abejon, 2007; Kircelli, 2019). Daarnaast rapporteerde Usmani (2018) het effect van conventionele versus. gepulseerde radiofrequente na ganglion impar blokkade. In alle studies werd de gemiddelde pijnscore gerapporteerd op basis van een VAS-schaal van 0 tot 10, geen tot maximale pijn.
Figuur 1 presenteert de gepoolde odds ratio (OR) voor de odds op < 50% verbetering in pijnintensiteit post-baseline. Patiënten die behandeld werden met een ganglion impar blokkade hadden een lagere odds (OR 0,01 (95%BI 0,00 tot 0,02)) op < 50% pijnvermindering post-baseline.
Figuur 2, 3 en 4 presenteren het gepoolde, gewogen gemiddelde verschil in de pijnintensiteit tussen de pre- en post-baseline score respectievelijk 1, 6 en 12 maanden na plexusblokkade. De overall verbetering in pijnscore na plexusblokkade was −5,90 (95% BI -6,98 tot -4,81) na 1 maand, -6,58 (95%BI -7,09 tot -6,07) na 6 maanden en -5,47 (95%BI -8,51 tot -2,43) na 12 maanden, vergeleken met baseline.
Figuur 1 Forest plot uitkomstmaat ‘< 50% verbetering in pijnintensiteit post-baseline’ op basis van het verschil tussen de pre- en post-baseline aantal events na plexusblokkade
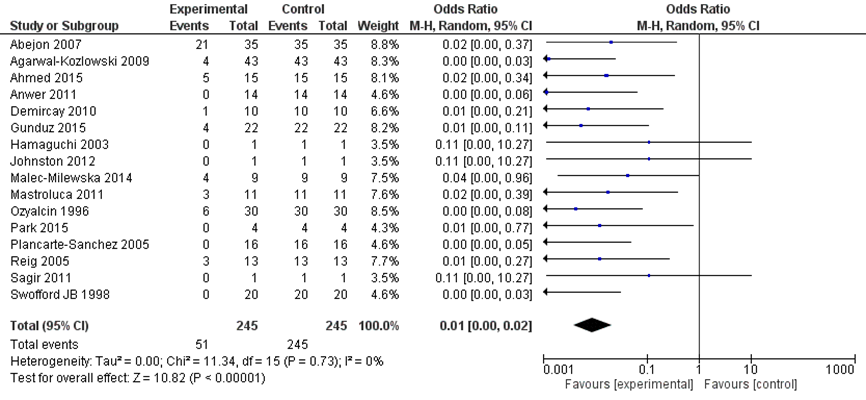
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Figuur 2 Forest plot uitkomstmaat ‘pijnintensiteit na 1 maand’ op basis van het gewogen gemiddelde verschil tussen de pre- en post-baseline score na plexusblokkade
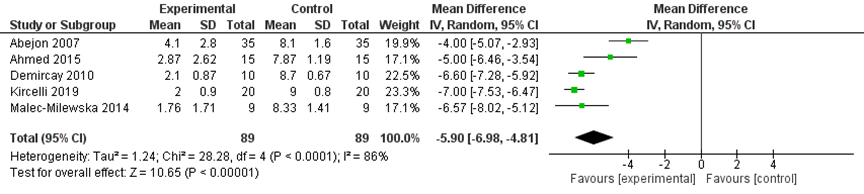
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Figuur 3 Forest plot uitkomstmaat ‘pijnintensiteit na (ongeveer) 6 maanden’ op basis van het gewogen gemiddelde verschil tussen de pre- en post-baseline score na plexusblokkade
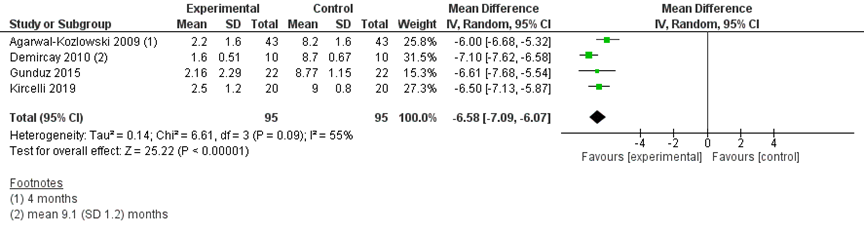
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
Figuur 4 Forest plot uitkomstmaat ‘pijnintensiteit na 1 jaar’ op basis van het gewogen gemiddelde verschil tussen de pre- en post-baseline score na plexusblokkade
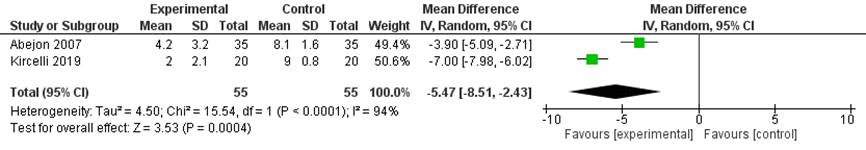
Z: p-waarde van het gepoolde effect; df: degrees of freedom (vrijheidsgraden); I2: statistische heterogeniteit; CI: betrouwbaarheidsinterval
1.1.2. Plexusblokkades (effectiviteit conventionele thermocoagulatie versus pulsed radiofrequency ablatie)
De uitkomstmaat pijnintensiteit na conventionele thermocoagulatie versus gepulseerde radiofrequente na ganglion impar blokkade werd door 1 studie gerapporteerd (Usmani, 2018). De gemiddelde pijnscore gerapporteerd op basis van een VAS-schaal van 0 tot 10, geen tot maximale pijn.
Usmani (2018) rapporteerde dat bij patiënten met chronische perineale pijn de pijnintensiteit 6 weken post-baseline lager was bij patiënten die met conventionele radiofrequente thermocoagulatie groep (80°C, 90 seconden, 1 cyclus) waren behandeld, vergeleken met de groep die met pulsed radiofrequente therapie (PRF) (42°C, 4 minuten, 2 cylci (1 cyclus was 120 seconden)) waren behandeld: gemiddelde pijnscore 6 weken post-baseline 1,96 (SD 1,4) versus 6,12 (SD 2,02) (P=0,0001).
1.2. Wortelblokkade
Er werden geen studies geïncludeerd waarin de uitkomstmaat pijnintensiteit na wortelblokkade werd bestudeerd bij patiënten met chronische bekkenpijn.
1.3.1. Perifere zenuwblokkade (zonder pulsed radiofrequency ablatie)
Er werden geen studies geïncludeerd waarin de uitkomstmaat pijnintensiteit na perifere zenuwblokkade zonder pulsed radiofrequency ablatie werd bestudeerd bij patiënten met chronische bekkenpijn.
1.3.2. Perifere zenuwblokkade (met pulsed radiofrequency ablatie)
Twee studies rapporteerden de uitkomstmaat pijnintensiteit na behandeling met zenuwblokkade met versus zonder pulsed radiofrequency ablatie (Fang, 2018; Hetta, 2018). Fang (2018) beschreef zenuwblokkade van de n. pudendus bij patiënten met pudendale neuralgie, Hetta (2018) beschreef zenuwblokkade van de n. ilioinguinalis en n. genitofemoralis bij mannen met chronische testiculaire pijn. De gemiddelde pijnscore werd in beide studies gerapporteerd op basis van een VAS-schaal van 0 tot 10, geen tot maximale pijn.
Fang (2018) rapporteerde een verschil in post-baseline score tussen de groep die zenuwblokkade van de pudendale zenuw kreeg en de groep die deze zenuwblokkade met PRF kreeg. Op 1 maand post-baseline was de gemiddelde pijnscore 5,1 (SD 1,8) versus 3,3 (SD 1,9); P=0,001 (gemiddeld verschil tussen de groepen 1,8 (95%BI 0,99 tot 2,61)). Drie maanden post-baseline was de gemiddelde pijnscore 5,2 (SD 1,9) versus 3,9 (SD 2,1), het gemiddelde verschil tussen de groepen was 1,30 (95%BI 0,40 tot 2,20)). De resultaten werden niet voor baseline score gecorrigeerd (er werd geen verschil in baseline score geobserveerd tussen de groepen).
Hetta (2018) rapporteerde een verschil in post-baseline score tussen de groep die zenuwblokkade van de n. ilioinguinalis en n. genitofemoralis kreeg met PRF vergeleken met een shambehandeling. Op 3 maanden post-baseline was de gemiddelde pijnscore 2,40 (95%CI 1,92 tot 2,89) in de PRF-groep, vergeleken met 3,17 (95%BI 2,79 tot 3,56) in de sham groep (P=0.001). Gemiddeld verschil tussen de groepen is -0,77 (95BI -1,37 tot -0,17). De resultaten werden niet voor baseline score gecorrigeerd (er werd geen verschil in baseline score geobserveerd tussen de groepen).
2. Patiënttevredenheid
2.1.1. Plexusblokkade
Er werden geen studies geïncludeerd waarin de uitkomstmaat patiënttevredenheid na plexusblokkade werd bestudeerd bij patiënten met chronische bekkenpijn.
2.2. Wortelblokkade
Er werden geen studies geïncludeerd waarin de uitkomstmaat patiënttevredenheid na wortelblokkade werd bestudeerd bij patiënten met chronische bekkenpijn.
2.3. Perifere Zenuwblokkade
2.3.1. Perifere zenuwblokkade (zonder pulsed radiofrequency ablatie)
Er werden geen studies geïncludeerd waarin de uitkomstmaat patiënttevredenheid na perifere zenuwblokkade zonder pulsed radiofrequency ablatie werd bestudeerd bij patiënten met chronische bekkenpijn.
2.3.2. Perifere zenuwblokkade (met pulsed radiofrequency ablatie)
Er werden geen studies geïncludeerd waarin de uitkomstmaat patiënttevredenheid na perifere zenuwblokkade met pulsed radiofrequency ablatie werd bestudeerd bij patiënten met chronische bekkenpijn.
3. Complicaties
3.1. 1. Plexusblokkade (effectiviteit pre- versus. post-baseline)
De uitkomstmaat complicaties na plexusblokkades werd gerapporteerd door twee studies (Li, 2016; Kircelli, 2018). Alle complicaties werden beschrijvend gepresenteerd.
Li (2016) rapporteerde dat van alle 16 geïncludeerde studies, alleen de studie van Ahmed (2015) beschreef tijdelijke paresthesie (n=5 (33%)) en injectiepijn (n=3 (20%)) na ganglion impar blokkade bij patiënten met chronische bekkenpijn en/of chronische perineale pijn.
Kircelli (2018) rapporteerde dat er geen enkele complicatie werd gerapporteerd bij ganglion impar blokkade met radiofrequente thermocoagulatie (RFT) bij patiënten met coccygodynie.
3.1.2. Plexusblokkades (effectiviteit conventionele thermocoagulatie versus pulsed radiofrequency ablatie)
De uitkomstmaat complicaties na conventionele versus gepulseerde radiofrequente ablatie na ganglion impar blokkade werd gerapporteerd door één studie (Usmani, 2018). Alle complicaties werden beschrijvend gepresenteerd.
Usmani (2018) rapporteerde een infectie bij de plek van injectie bij 3 van de 34 patiënten (9%) die behandeld werden met conventionele radiofrequente thermocoagulatie en bij 2 van de 31 patiënten (7%) die behandeld werden met pulsed radiofrequency ablatie na ganglion impar blokkade. Alle infecties werden succesvol behandelde met orale antibiotica.
3.2. Wortelblokkade
Er werden geen studies geïncludeerd waarin de uitkomstmaat complicaties na wortelblokkade werden bestudeerd bij patiënten met chronische bekkenpijn.
3.2.1. Perifere zenuwblokkade (zonder pulsed radiofrequency ablatie).
Er werden geen studies geïncludeerd waarin de uitkomstmaat complicaties na perifere zenuwblokkade zonder pulsed radiofrequency ablatie werden bestudeerd bij patiënten met chronische bekkenpijn.
3.3. 2.Perifere zenuwblokkade (met pulsed radiofrequency ablatie)
De uitkomstmaat complicaties na zenuwblokkade (n. pudendus) met versus zonder pulsed radiofrequency ablatie werd door Fang (2018) gerapporteerd.
Fang (2018) rapporteerde hypertensie bij 1 van de 39 patiënten (3%) in de groep die behandeld werd met zenuwblokkade van de pudendale zenuw vergeleken met 1 van de 38 patiënten (3%) die dezelfde zenuwblokkade met pulsed radiofrequency ablatie (P=0,985). Duizeligheid kwam bij 2 van de 39 (6%) patiënten voor na zenuwblokkade, vergeleken bij 1 van de 38 (3%) na zenuwblokkade van pudendale zenuw me pulsed radiofrequency ablatie (P=0,547). Er werden geen andere complicaties door patiënten gerapporteerd.
Het is onbekend welke complicatie voorkomen na zenuwblokkade (n. ilioinguinalis en n. genitofemoralis) met pulsed radiofrequency ablatie vergeleken met een shambehandeling, dit werd niet door Hetta (2018) gerapporteerd.
4. Kwaliteit van leven
4.1. Plexusblokkade
Er werden geen studies geïncludeerd waarin de uitkomstmaat kwaliteit van leven na plexusblokkade werden bestudeerd bij patiënten met chronische bekkenpijn.
4.2. Wortelblokkade
Er werden geen studies geïncludeerd waarin de uitkomstmaat kwaliteit van leven na wortelblokkade werden bestudeerd bij patiënten met chronische bekkenpijn.
4.3. Perifere zenuwblokkade
4.3.1. Perifere zenuwblokkade (zonder pulsed radiofrequency ablatie)
Er werden geen studies geïncludeerd waarin de uitkomstmaat kwaliteit van leven na perifere zenuwblokkade zonder pulsed radiofrequency ablatie werd bestudeerd bij patiënten met chronische bekkenpijn.
4.3.2. Perifere zenuwblokkade (met pulsed radiofrequency ablatie)
Er werden geen studies geïncludeerd waarin de uitkomstmaat kwaliteit van leven na perifere zenuwblokkade met pulsed radiofrequency ablatie werd bestudeerd bij patiënten met chronische bekkenpijn.
Bewijskracht van de literatuur
1.1. Plexusblokkade (effectiviteit pre- versus post-baseline)
Observationeel vergelijkend onderzoek begint op een laag niveau van bewijskracht. De bewijskracht voor de uitkomstmaat pijnintensiteit gedefinieerd als < 50% vermindering post-interventie (tijdsinterval onbekend) is niet verder verlaagd. Hierdoor kwam de bewijskracht uit op een GRADE laag.
Observationeel vergelijkend onderzoek begint op een laag niveau van bewijskracht. De bewijskracht voor de uitkomstmaat pijnintensiteit 1 maand na plexusblokkade vergeleken met baseline is niet verder verlaagd. Hierdoor kwam de bewijskracht uit op een GRADE laag.
Observationeel vergelijkend onderzoek begint op een laag niveau van bewijskracht. De bewijskracht voor de uitkomstmaat pijnintensiteit 6 maanden na plexusblokkade vergeleken met baseline is niet verder verlaagd. Hierdoor kwam de bewijskracht uit op een GRADE laag.
Observationeel vergelijkend onderzoek begint op een laag niveau van bewijskracht. De bewijskracht voor de uitkomstmaat pijnintensiteit 12 maanden na plexusblokkade vergeleken met baseline is met één niveau verlaagd wegens imprecisie (het gepoolde effect overlapt met de grens van klinische relevantie). Hierdoor kwam de bewijskracht uit op een GRADE zeer laag.
De bewijskracht voor de uitkomstmaat complicaties kon niet worden gegradeerd door middel van GRADE doordat de geïncludeerde studies onvoldoende informatie rapporteerden.
De bewijskracht voor de uitkomstmaat patiënttevredenheid en kwaliteit van leven kon niet worden gegradeerd doordat er geen studies zijn geïncludeerd waarin deze uitkomst werd bestudeerd bij patiënten met chronische bekkenpijn die behandeld werden met plexusblokkades.
1.2. Plexusblokkades (effectiviteit conventionele thermocoagulatie versus pulsed radiofrequency ablatie)
RCT’s beginnen op een hoog niveau van bewijskracht. De bewijskracht voor de uitkomstmaat pijnintensiteit 6 weken na plexusblokkade met conventionele versus pulsed radiofrequency ablatie is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias vanwege onduidelijke loss to follow-up en onduidelijke blindering (Usmani, 2018)). Hierdoor kwam de bewijskracht uit op een GRADE laag.
RCT’s beginnen op een hoog niveau van bewijskracht. De bewijskracht voor de uitkomstmaat patiënttevredenheid 6 weken na plexusblokkade met conventionele thermocoagulatie versus pulsed radiofrequency ablatie is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias vanwege onduidelijke loss to follow-up en onduidelijke blindering (Usmani, 2018)). Hierdoor kwam de bewijskracht uit op een GRADE laag.
De bewijskracht voor de uitkomstmaat complicaties en kwaliteit van leven kon niet worden gegradeerd doordat er geen studies zijn geïncludeerd waarin deze uitkomst werd bestudeerd bij patiënten met chronische bekkenpijn die behandeld werden met plexusblokkades met conventionele thermocoagulatie versus. pulsed radiofrequency ablatie.
2. Wortelblokkade
De bewijskracht voor de uitkomstmaten pijnintensiteit, patiënttevredenheid, complicaties en kwaliteit van leven konden niet worden gegradeerd doordat er geen studies zijn geïncludeerd waarin deze uitkomsten werd bestudeerd bij patiënten met chronische bekkenpijn die behandeld werden met wortelblokkades.
3. Perifere zenuwblokkade
3.1. Perifere zenuwblokkade (zonder pulsed radiofrequency ablatie)
De bewijskracht voor de uitkomstmaten pijnintensiteit, patiënttevredenheid, complicaties en kwaliteit van leven na perifere zenuwblokkade zonder pulsed radiofrequency ablatie kon niet worden gegradeerd. Er konden geen studies worden geïncludeerd waarin deze uitkomsten werden bestudeerd bij patiënten met chronische bekkenpijn die behandeld werden met perifere zenuwblokkades zonder pulsed radiofrequency ablatie vergeleken met geen behandeling of baseline score.
3.2. Perifere zenuwblokkade (met pulsed radiofrequency ablatie)
RCT’s beginnen op een hoog niveau van bewijskracht. De bewijskracht voor de uitkomstmaat pijnintensiteit 1 en 3 maanden na perifere zenuwblokkade (n. pudendus) met versus zonder pulsed radiofrequency ablatie is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias vanwege onduidelijke loss to follow-up en onduidelijke blindering (Fang, 2018)) en imprecisie (het effect overlapt met de grens van klinische relevantie). Hierdoor kwam de bewijskracht uit op een GRADE laag.
RCT’s beginnen op een hoog niveau van bewijskracht. De bewijskracht voor de uitkomstmaat pijnintensiteit 3 maanden na perifere zenuwblokkade (n. ilioinguinalis en n. genitofemoralis) met pulsed radiofrequency ablatie versus shambehandeling is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias vanwege onduidelijke loss to follow-up en exclusie wegens protocol schending (Hetta, 2018)) en imprecisie (het effect overlapt met de grens van klinische relevantie). Hierdoor kwam de bewijskracht uit op een GRADE laag.
RCT’s beginnen op een hoog niveau van bewijskracht. De bewijskracht voor de uitkomstmaat complicaties 1 en 3 maanden na perifere zenuwblokkade met versus zonder pulsed radiofrequency ablatie is met twee niveaus verlaagd gezien beperkingen in de onderzoeksopzet (risk of bias vanwege onduidelijke loss to follow-up en onduidelijke blindering (Fang, 2018)). Hierdoor kwam de bewijskracht uit op een GRADE laag.
De bewijskracht voor de uitkomstmaat complicaties 3 maanden na perifere zenuwblokkade (n. ilioinguinalis en n. genitofemoralis) met pulsed radiofrequency ablatie versus shambehandeling kon niet worden gegradeerd doordat er geen studies zijn geïncludeerd waarin deze uitkomsten werden bestudeerd bij patiënten met chronische bekkenpijn die behandeld werden met perifere zenuwblokkades met pulsed radiofrequency ablatie versus shambehandeling.
De bewijskracht voor de uitkomstmaten patiënttevredenheid en kwaliteit van leven kon niet worden gegradeerd doordat er geen studies zijn geïncludeerd waarin deze uitkomsten werden bestudeerd bij patiënten met chronische bekkenpijn die behandeld werden met perifere zenuwblokkades met pulsed radiofrequency ablatie vergeleken met behandeling zonder pulsed radiofrequency ablatie of vergeleken met een shambehandeling.
Om de uitgangsvraag te kunnen beantwoorden is er een systematische literatuuranalyse verricht naar de volgende zoekvraag:
Wat is de effectiviteit (en veiligheid) van plexusblokkades, wortelblokkades of zenuwblokkades vergeleken met medicamenteuze behandeling, conservatieve behandeling, sham of placebo bij patiënten met chronische bekkenpijn?
P: patiënten met chronische bekkenpijn (duur van de pijn > 6 maanden);
I: plexusblokkades, wortelblokkades of perifere zenuwblokkades*;
C: pijnblokkades, medicamenteuze behandeling, conservatieve behandeling, sham of placebo;
O: pijnintensiteit, patiënttevredenheid, complicaties, kwaliteit van leven.
*Blokkades (thermisch radio frequency (RF), pulsed RF of chemisch) waren gedefinieerd als:
- Plexus blokkades: ganglion impar blokkade (ganglion of Walther of sacroccygeale ganglion), superior/inferior hypogastric plexus blockade.
- Wortelblokkades: caudaal of selectieve sacrale wortels S1 tot en met S5.
- Perifere zenuwblokkades: n. ilioinguinalis, n. iliohypogastricus, n. genitofemoralis, n. pudendus.
Relevante uitkomstmaten
De werkgroep achtte pijnintensiteit een voor de besluitvorming cruciale uitkomstmaat; en patiënttevredenheid, complicaties, kwaliteit van leven voor de besluitvorming belangrijke uitkomstmaten.
De werkgroep definieerde niet a priori de genoemde uitkomstmaten, maar hanteerde de in de studies gebruikte definities.
De werkgroep hield de GRADE-default grenzen (25% voor dichotome uitkomstmaten en 0,5 SD voor continue uitkomstmaten) aan als een klinisch (patiënt) relevant verschil (Schüneman, 2013).
Zoeken en selecteren (Methode)
In de databases Medline (via OVID) en Embase (Elsevier) is op 5 juli 2019 met relevante zoektermen gezocht naar systematische reviews, randomized controlled trials (RCT’s) en observationele cohortstudies waarin was gekeken naar de effectiviteit en veiligheid van behandeling van chronische bekkenpijn door middel van plexus-, wortel- of zenuwblokkades. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. De literatuurzoekactie leverde 206 treffers op. Studies werden geselecteerd op grond van de volgende selectiecriteria: 1) studie betrof patiënten met chronische bekkenpijn (duur pijn > 6 maanden); 2) studie betrof een RCT waarin plexus-, wortel- of zenuwblokkades werden vergeleken met een andere behandeling of placebo/sham-behandeling; 3) minimaal één van de volgende uitkomstmaten werd gerapporteerd: pijnintensiteit, patiënttevredenheid, complicaties, kwaliteit van leven. Op basis van titel en abstract werden in eerste instantie 97 studies voorgeselecteerd. Na raadpleging van de volledige tekst en referentielijsten werden nog 20 aanvullende studies gevonden. In totaal werden 117 studies fulltekst gecontroleerd. In totaal werden 111 studies geëxcludeerd (zie exclusietabel onder het tabblad Verantwoording) en 6 studies geïncludeerd in de literatuuranalyse.
Resultaten
Er werd één systematisch review en meta-analyse van observationeel onderzoek over de effectiviteit van plexusblokkades geïncludeerd (Li, 2016). Dit review werd aangevuld met één recent gepubliceerde observationele studie over plexusblokkades uit de search (Kircelli, 2019). Daarnaast werd 1 RCT geïncludeerd waarin verschillenden verschillende manieren van behandeling met ganglion impar blokkade (Usmani, 2018) werd vergeleken. Verder werden 2 RCT’s geïncludeerd over perifere zenuwblokkades (Fang, 2018; Hetta, 2018). Er werden geen studies geïncludeerd over wortelblokkades. Er werden geen studies geïncludeerd waarin pijnblokkades werden vergeleken met een medicamenteuze behandeling of conservatieve behandeling bij patiënten met chronische bekkenpijn. Er werden geen studies geïncludeerd waarin de effectiviteit van wortelblokkades werd bestudeerd.
- Fang H, Zhang J, Yang Y, Ye L, Wang X. Clinical effect and safety of pulsed radiofrequency treatment for pudendal neuralgia: a prospective, randomized controlled clinical trial. J Pain Res. 2018 Oct 16;11:2367-2374.
- Hetta DF, Mahran AM, Kamal EE. Pulsed Radiofrequency Treatment for Chronic Post-Surgical Orchialgia: A Double-Blind, Sham-Controlled, Randomized Trial: Three-Month Results. Pain Physician. 2018 Mar;21(2):199-205.
- Kırcelli A, Demirçay E, Özel Ö, Çöven I, Işık S, Civelek E, Kabataş S. Radiofrequency Thermocoagulation of the Ganglion Impar for Coccydynia Management: Long-Term Effects. Pain Pract. 2019 Jan;19(1):9-15.
- Li, C. B., Fang, S. P., Chen, Y. L., Huang, Y., Yao, X. Y., Ge, X. Y.,... & Tian, F. B. (2016). The efficacy and safety of the ganglion impar block in chronic intractable pelvic and/or perineal pain: a systematic review and meta-analysis. Int J Clin Exp Med, 9(8), 15746-15754.
- Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
- Usmani H, Dureja GP, Andleeb R, Tauheed N, Asif N. Conventional Radiofrequency Thermocoagulation versus Pulsed Radiofrequency Neuromodulation of Ganglion Impar in Chronic Perineal Pain of Nononcological Origin. Pain Med. 2018 Dec 1;19(12):2348-2356.
Evidence table for systematic review of RCTs and observational studies (intervention studies)
Research question:
|
Study reference |
Study characteristics |
Patient characteristics |
Intervention (I) |
Comparison/ control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Li, 2016
PS., study characteristics and results are extracted from the SR (unless stated otherwise) |
SR and meta-analysis of (cohort studies)
Literature search up to May, 2015
A: Ahmed, 2015 B: Maleo-Milewska, 2014 C: Johnston, 2012 D: Sagir, 2011 E: Demircay, 2010 F: Agarwal-Kozlowski, 2009 G: Reig, 2005 H: Park, 2015 I: Gunduz, 2015 J: Mastroluca, 2011 K: Abejon, 2007 L: Plancarte-Sanchez, 2005 M: Hamaguchi, 2003 N: Swofford, 1998 O: Anwer, 2011 P: Ozyalcin, 1996
Study design: All were cohort studies, type of cohort study not reported (prospective / retrospective).
Setting and Country: not reported per study.
Source of funding and conflicts of interest: Not reported per study.
Li (2016) declares the authors have no conflict of interest. Funding not reported.
|
Inclusion criteria SR: (1) GIB as an intervention for chronic intractable pelvic and/or perineal pain; (2) Including the effective rate or the VAS score comparison between baseline and post-treatment.
Exclusion criteria SR: (1) Patients with severe cardiovascular and cerebrovascular diseases or other contradictions of the block; (2) Duplications; (3) Missing data; (4) The simple qualitative description; (5) Incorrect statistical analysis performed in the report.
16 studies included
Important patient characteristics at baseline: Number of patients; characteristics important to the research question and/or for statistical adjustment (confounding in cohort studies); for example, age, sex, bmi,...
N, mean age A: 15 patients, 54.3 (SD 13.3) yrs B: 9 patients, 43-73 years C: 1 patients, 67 years D: 1 patient, age unknown E: 10 patients, 42.9 (SD 14.4) years F: 43 patients, 64.4 (SD 12.4) years G: 13 patients, 35-76 years H: 4 patients, age not reported I: 22 patients, 41 (SD 9) years J: 11 patients, age not reported K: 35 patients, 53 (SD 17) years L: 16 patients, 24-87 years M: 1 patient, 62 years N: 20 patients, 35-70 years O: 14 patients, age not reported P: 30 patients, 36-68 years.
Sex: not reported per study.
Pain: A: chronic pelvic pain and chronic perineal pain B: chronic pelvic pain C: chronic perineal pain D: Chronic coccydynia E: Chronic coccydynia F: chronic perineal pain G: chronic perineal pain H: chronic perineal pain I: Chronic coccydynia J: chronic perineal pain K: chronic perineal pain L: chronic perineal pain M: chronic perineal pain N: chronic perineal pain O: chronic pelvic pain and chronic perineal pain P: chronic perineal pain
Groups comparable at baseline? |
Describe intervention: Post-intervention outcome
Block: A: GIB + SHGPB B: GIB C: GIB D: GIB E: GIB +RFT F: GIB + N G: GIB + RFT H: GIB I: GIB J: GIB +PR K: GIB + RFT L: GIB M: GIB + CB N: GIB O: GIB+N P: GIB
Block drugs A: 4-6 mL 8% phenol + 1 mL saline + 10 mL 10% phenol + 1 mL saline B: 4-6 mL (65% alcohol + lidocaine) C: 10 mL 0.25% chirocaine + 75 ug clonidine D: 9 mL 0.25% chirocaine + 1 mL-40 mg methylprednisolone E: 10 mL 0.25% chirocaine F: 10 mL 1.0% ropivacaine + 2 mL 95% alcohol G: 5 mL 0.2% ropivacaine + 40 mg triamcinolone H: 4 mL 0.5% lidocaine + 5 mL 0.2% ropivacaine + 20 mg triamcinolone I: 2 mL 0.5% bupivacaine + 2 mL saline + 40 mg methylprednisolone J: not reported K: not reported L: 4 mL (1% lidocaine or 0.25% bupivacaine) + 4-6 mL 10% phenol M: 5 mL 0.25% bupivacaine + 4 mL 7% phenol N: 5 mL 0.25% bupivacaine + 20 mg triamcinolone O: Bupivacaine + absolute alcohol P: 6 mL 0.25% bupivacaine + 6 mL 6% phenol |
Describe control: Baseline score
|
End-point of follow-up:
A: 2 months B: 3 years C: 5 days D: not reported E: 9.1 (SD 1.2) months F: 4 months G: 6 months H: 3 months – 2 years I: 6 months J: 6 months K: 1 year L: 14-120 days M: 6 months N: not reported O: 1 month P: 6 months
For how many participants were no complete outcome data available? Not reported per study.
|
Outcome measure-1: pain Defined by VAS score 0-10, no to maximum pain.
Pain score was calculated in 2 manners: 1. OR (95% CI) of the VAS score lowering <50%
Pooled effect (fixed effects model): 0.01 (95%CI 0.00, 0.02) favoring post-treatment score (people treated with GIB have an extremely low odds to experience less than 50% improvement in pain.
Heterogeneity (I2): 0%
2. mean difference between pre- and post-procedure VAS score: Pooled mean difference -5.98 (95%CI -7.14 to -4.81) favoring post-procedure. N=110 patients, n=4 studies included (K, F, E. I)
3. mean difference between pre- and 1 month post-procedure: Pooled mean difference -5.56 (95%CI -6.93 tot -4.18) favoring 1 month post-procedure. N=69, n=4 studies included (K,A,E,B)
Outcome measure-2: patient satisfaction Not reported
Outcome measure-3: complications Number of complications as reported per study.
All the included studies described the complications of GIB. Of all the 245 participants, however, there were only five patients with transient paresthesia and three patients with injection pain (study A).
Outcome measure-4: quality of life Not reported.
|
Facultative:
Brief description of author’s conclusion
“In conclusion, this meta-analysis demonstrated that GIB can effectively alleviate the chronic intractable pain with few complications. And our results provided the true and reliable evidence for the clinical application of GIB in chronic intractable pelvic and/or perineal pain. Accordingly, the clinicians should further understand this method and keep improving it. Nevertheless, we don’t primarily recommend GIB for the general pain because of the probable damage of nerve. Further investigations should be operated to explore and improve the application of GIB.”
Personal remarks on study quality, conclusions, and other issues (potentially) relevant to the research question
Level of evidence: GRADE (per comparison and outcome measure) including reasons for down/upgrading
Sensitivity analyses (excluding small studies; excluding studies with short follow-up; excluding low quality studies; relevant subgroup-analyses); mention only analyses which are of potential importance to the research question
Heterogeneity: clinical and statistical heterogeneity; explained versus unexplained (subgroupanalysis) |
Abbreviations: GIB = The ganglion impar block; SHGPB = The superior hypogastric plexus block; RFT = Radiofrequency thermocoagulation; PR = Pulsed radiofrequency; CB = Caudal block; N = Neuroablation.
Table of quality assessment for systematic reviews of RCTs and observational studies
Based on AMSTAR checklist (Shea, 2007; BMC Methodol 7: 10; doi:10.1186/1471-2288-7-10) and PRISMA checklist (Moher, 2009; PLoS Med 6: e1000097; doi:10.1371/journal.pmed1000097)
|
Study
First author, year |
Appropriate and clearly focused question?1
Yes/no/unclear |
Comprehensive and systematic literature search?2
Yes/no/unclear |
Description of included and excluded studies?3
Yes/no/unclear |
Description of relevant characteristics of included studies?4
Yes/no/unclear |
Appropriate adjustment for potential confounders in observational studies?5
Yes/no/unclear/notapplicable |
Assessment of scientific quality of included studies?6
Yes/no/unclear |
Enough similarities between studies to make combining them reasonable?7
Yes/no/unclear |
Potential risk of publication bias taken into account?8
Yes/no/unclear |
Potential conflicts of interest reported?9
Yes/no/unclear |
|
Li, 2016 |
Yes |
Yes |
Yes |
Yes, except it was not reported whether outcome data were all complete and how many men and women were included. |
Unclear, not performed (comparison of pre- and post-baseline scores) |
Yes |
Yes |
Yes |
No |
- Research question (PICO) and inclusion criteria should be appropriate and predefined.
- Search period and strategy should be described; at least Medline searched; for pharmacological questions at least Medline + EMBASE searched.
- Potentially relevant studies that are excluded at final selection (after reading the full text) should be referenced with reasons.
- Characteristics of individual studies relevant to research question (PICO), including potential confounders, should be reported.
- Results should be adequately controlled for potential confounders by multivariate analysis (not applicable for RCTs).
- Quality of individual studies should be assessed using a quality scoring tool or checklist (Jadad score, Newcastle-Ottawa scale, risk of bias table et cetera).
- Clinical and statistical heterogeneity should be assessed; clinical: enough similarities in patient characteristics, intervention and definition of outcome measure to allow pooling? For pooled data: assessment of statistical heterogeneity using appropriate statistical tests (for example Chi-square, I2)?
- An assessment of publication bias should include a combination of graphical aids (for example funnel plot, other available tests) and/or statistical tests (for example Egger regression test, Hedges-Olken). Note: If no test values or funnel plot included, score “no”. Score “yes” if mentions that publication bias could not be assessed because there were fewer than 10 included studies.
- Sources of support (including commercial co-authorship) should be reported in both the systematic review and the included studies. Note: To get a “yes,” source of funding or support must be indicated for the systematic review AND for each of the included studies.
Evidence table for intervention studies (randomized controlled trials and non-randomized observational studies (cohort studies, case-control studies, case series))1
This table is also suitable for diagnostic studies (screening studies) that compare the effectiveness of two or more tests. This only applies if the test is included as part of a test-and-treat strategy - otherwise the evidence table for studies of diagnostic test accuracy should be used.
Research question:
Notes:
- Prognostic balance between treatment groups is usually guaranteed in randomized studies, but non-randomized (observational) studies require matching of patients between treatment groups (case-control studies) or multivariate adjustment for prognostic factors (confounders) (cohort studies); the evidence table should contain sufficient details on these procedures.
- Provide data per treatment group on the most important prognostic factors ((potential) confounders).
- For case-control studies, provide sufficient detail on the procedure used to match cases and controls.
- For cohort studies, provide sufficient detail on the (multivariate) analyses used to adjust for (potential) confounders.
Risk of bias table for intervention studies (randomized controlled trials)
Research question:
|
Study reference
(first author, publication year) |
Describe method of randomisation1 |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?3
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?4
(unlikely/likely/unclear) |
Bias due to loss to follow-up?5
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?6
(unlikely/likely/unclear) |
|
Fang, 2018 |
A random assignment sequence was generated by the computer |
Unlikely |
Unlikely |
Unclear, it was not possible to blind care providers to the treatment allocation. All treatments were performed by the same surgeon, follow-up and evaluation were done by others. |
Unclear, not reported |
Unlikely |
Unclear, follow-up was almost equal (1 versus. 2) in both groups; reasons not reported. |
Unlikely |
|
Hetta, 2018 |
The patients were randomly allocated to 2 groups by using a computer-created number list, which was concealed in sealed envelopes without blocking, and they were open by the researcher before application of the procedure. |
Unlikely |
Unlikely |
Unlikely |
Unclear, it was reported that allocation was revealed to the researcher before application of the procedure. Unclear whether this researcher was the analyst also. |
Unlikely |
Unclear, follow-up was almost equal (2 versus. 3) in both groups; reasons not reported. |
Likely, in the intervention group 2 patients (5.7%) were excluded due to protocol violation, in the control group 3 patients (8.7%) were excluded due to protocol violation. Not explained what the violations were or why they decided not to execute an intention to treat analysis and/or per protocol analysis. |
|
Usmani, 2018 |
Patients were randomly divided into two groups using a computer-generated randomization schedule |
Unlikely |
Unclear, it was a double-blind design so bias seems unlikely. However it is not clarified in text how this was established. |
Unclear, it was a double-blind design so bias seems unlikely. However it is not clarified in text how this was established. |
Unclear, not reported |
Unlikely |
Likely, follow-up was 4 times higher in the PRF (n=4) versus. CRF group (n=1). Reasons not reported. |
Unlikely. |
- Randomisation: generation of allocation sequences have to be unpredictable, for example computer generated random-numbers or drawing lots or envelopes. Examples of inadequate procedures are generation of allocation sequences by alternation, according to case record number, date of birth or date of admission.
- Allocation concealment: refers to the protection (blinding) of the randomisation process. Concealment of allocation sequences is adequate if patients and enrolling investigators cannot foresee assignment, for example central randomisation (performed at a site remote from trial location) or sequentially numbered, sealed, opaque envelopes. Inadequate procedures are all procedures based on inadequate randomisation procedures or open allocation schedules.
- Blinding: neither the patient nor the care provider (attending physician) knows which patient is getting the special treatment. Blinding is sometimes impossible, for example when comparing surgical with non-surgical treatments. The outcome assessor records the study results. Blinding of those assessing outcomes prevents that the knowledge of patient assignment influences the process of outcome assessment (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Results of all predefined outcome measures should be reported; if the protocol is available, then outcomes in the protocol and published report can be compared; if not, then outcomes listed in the methods section of an article can be compared with those whose results are reported.
- If the percentage of patients lost to follow-up is large, or differs between treatment groups, or the reasons for loss to follow-up differ between treatment groups, bias is likely. If the number of patients lost to follow-up, or the reasons why, are not reported, the risk of bias is unclear
- Participants included in the analysis are exactly those who were randomized into the trial. If the numbers randomized into each intervention group are not clearly reported, the risk of bias is unclear; an ITT analysis implies that (a) participants are kept in the intervention groups to which they were randomized, regardless of the intervention they actually received, (b) outcome data are measured on all participants, and (c) all randomized participants are included in the analysis.
Risk of bias table for intervention studies (observational: non-randomized clinical trials, cohort and case-control studies)
Research question:
|
Study reference
(first author, year of publication) |
Bias due to a non-representative or ill-defined sample of patients?1
(unlikely/likely/unclear) |
Bias due to insufficiently long, or incomplete follow-up, or differences in follow-up between treatment groups?2
(unlikely/likely/unclear) |
Bias due to ill-defined or inadequately measured outcome ?3
(unlikely/likely/unclear) |
Bias due to inadequate adjustment for all important prognostic factors?4
(unlikely/likely/unclear) |
|
Kircelli 2019 |
Unclear, patients with both trauma (n=8) and idiopathic (n=12) chronic coccydynia included. |
Unclear, follow-up duration was 17.3 +/- 2.9 months on average, which implies almost every patient will have had follow-up data until 12 months. Lost to follow-up was not reported. |
Unlikely |
Unlikely, within-person comparisons were made with no drop-out. |
- Failure to develop and apply appropriate eligibility criteria: a) case-control study: under- or over-matching in case-control studies; b) cohort study: selection of exposed and unexposed from different populations.
- 2 Bias is likely if: the percentage of patients lost to follow-up is large; or differs between treatment groups; or the reasons for loss to follow-up differ between treatment groups; or length of follow-up differs between treatment groups or is too short. The risk of bias is unclear if: the number of patients lost to follow-up; or the reasons why, are not reported.
- Flawed measurement, or differences in measurement of outcome in treatment and control group; bias may also result from a lack of blinding of those assessing outcomes (detection or information bias). If a study has hard (objective) outcome measures, like death, blinding of outcome assessment is not necessary. If a study has “soft” (subjective) outcome measures, like the assessment of an X-ray, blinding of outcome assessment is necessary.
- Failure to adequately measure all known prognostic factors and/or failure to adequately adjust for these factors in multivariate statistical analysis.
Tabel Exclusie na het lezen van het volledige artikel
|
Auteur en jaartal |
Redenen van exclusie |
|
Adas, 2016 |
voldoet niet aan PICO (onder andere oncologische pijn) |
|
Ahmed, 2015 |
voldoet niet aan PICO (maligniteit) |
|
Amin, 2015 |
voldoet niet aan PICO (vergelijkt met acupunctuur) |
|
Antolak, 2009 |
case report |
|
Antolak, 2016 |
voldoet niet aan PICO (geen vergelijkend onderzoek naar blokkades bij CPP) |
|
Atkin, 2011 |
patiëntkenmerken anorectale pijn |
|
Basal, 2012 |
case report |
|
Binkert, 2015 |
voldoet niet aan PICO (geen CPP) |
|
Birthi, 2013 |
narrative review |
|
Cervigni, 2014 |
narrative review |
|
Choi, 2012 |
case report |
|
Choi, 2017 |
voldoet niet aan PICO |
|
Comin, 2013 |
voldoet niet aan PICO (vergelijkt geen behandeling middel blokkades met elkaar; betreft patiënten met liespijn). |
|
Cox, 2018 |
narrative review |
|
da Rosa, 2015 |
voldoet niet aan PICO |
|
Daniels, 2013 |
narrative review |
|
De Andres, 2016 |
narrative review |
|
Demircay, 2010 |
narrative review |
|
Dickson, 2019 |
voldoet niet aan PICO (patiënten met transient pijn ook geïncludeerd) |
|
Diniz, 2013 |
narrative review |
|
Ducic, 2004 |
kadaverstudie |
|
El-Hakim, 2004 |
narrative review |
|
El-Hefnawy, 2015 |
voldoet niet aan PICO (methodologisch slecht onderzoek: plexus alleen maar verdoofd met lokale anesthesticum, dus niet met pulsed RF of RF) |
|
Elkhashab, 2018 |
narrative review |
|
Elkins 2017, 2017 |
narrative review |
|
Ellinas, 2009 |
narrative review |
|
Fall, 2010 |
guideline |
|
Frank, 2019 |
geen vergelijkend onderzoek |
|
Gaines, 2018 |
voldoet niet aan PICO (genital arousal disorder) |
|
Gao, 2012 |
voldoet niet aan PICO (geen vergelijking van blokkades) |
|
geen auteur, 2019 |
congres abstracts |
|
Ghai, 2019 |
geen vergelijkend onderzoek |
|
Ghoneim, 2014 |
vergelijkt benaderingswijze (klassiek versus. CT geleide blokkade) |
|
Gonnade, 2017 |
onduidelijke meting van pijn (schaal onbekend); klinische relevantie niet te bepalen |
|
Gopal, 2014 |
valt binnen search Li 2016 |
|
Green, 2010 |
narrative review |
|
Gunduz, 2015 |
reeds geïncludeerd in Li 2016 |
|
Gunduz, 2017 |
narrative review |
|
Hamaguchi, 2003 |
case report |
|
Han, 2018 |
narrative review |
|
Howard, 2003 |
narrative review |
|
Hunter, 2018 |
narrative review |
|
Ilfeld, 2017 |
narrative review |
|
Jain, 1999 |
tutorial |
|
Jarvi, 2018 |
guideline |
|
Johnson, 2004 |
voldoet niet aan PICO (chirurgische interventie) |
|
Kalliomäki, 2009 |
voldoet niet aan PICO (geen vergelijkend onderzoek naar blokkades bij CPP) |
|
Kapural, 2006 |
geen vergelijkend onderzoek |
|
Kapural, 2015 |
narrative review |
|
Karp, 2019 |
voldoet niet aan PICO (gaat over methodologische aspecten botox behandeling CPP) |
|
Karp, 2019 |
methologische review |
|
Khambati, 2014 |
valt binnen search Li 2016 |
|
Khan, 2016 |
narrative review |
|
Khosla, 2013 |
voldoet niet aan PICO (maligniteit) |
|
Kim, 2016 |
case report |
|
Kim, 2016 |
case report |
|
King, 2018 |
voldoet niet aan PICO (gaat over verwijderen vestibulum) |
|
Koo, 2011 |
geen vergelijkend onderzoek |
|
Kumar, 2010 |
narartive review |
|
Labat, 2017 |
voldoet niet aan PICO (kijkt naar corticosteroïden) |
|
Landau, 2013 |
narrative review |
|
Le Clerc, 2017 |
voldoet niet aan PICO (herhaalde injecties) |
|
Le Clerc, 2017 |
voldoet niet aan PICO (herhaalde injecties) |
|
Learman, 2011 |
voldoet niet aan PICO (betreft effect depressie op behandeling) |
|
Liliang, 2018 |
technische les |
|
Lim, 2012 |
valt binnen search Li 2016 |
|
Makharita, 2015 |
voldoet niet aan PICO (liespijn) |
|
Malde, 2018 |
guideline |
|
Malec-Milewska, 2015 |
geen vergelijkend onderzoek |
|
Masala, 2014 |
valt binnen search Li 2016 |
|
Masala, 2017 |
voldoet niet aan PICO (atleten met chronische pubalgia bij wie diagnostisch onderzoek naar oorzaak nog moet plaatsvinden). |
|
Mishra, 2013 |
voldoet niet aan PICO (maligniteit) |
|
Misra, 2009 |
geen vergelijkend onderzoek |
|
Mohamed, 2013 |
voldoet niet aan PICO (maligniteit) |
|
Montenegro, 2008 |
narrative review |
|
Montero-Cruz, 2018 |
voldoet niet aan PICO (plasma injecties) |
|
Moreno-Egea, 2016 |
chirurgische behandeling inguinodynia |
|
Nagpal, 2017 |
narrative review |
|
Nalini, 2018 |
voldoet niet aan PICO (maligniteiten geïncludeerd) |
|
Nasir, 2004 |
narrative review |
|
Nelson, 2011 |
narrative review |
|
Niraj, 2018 |
narrative review |
|
Niraj, 2018 |
audit van een kliniek |
|
no author, |
narrative review |
|
no author, 2018 |
congres abstracts |
|
Oikawa, 2012 |
voldoet niet aan PICO (liespijn) |
|
Oomen, 2014 |
voldoet niet aan PICO (vergelijkt met chirurgische behandeling van spermatic cord) |
|
Ozkan, 2016 |
narrative review |
|
Ozkan, 2016 |
narrative review |
|
Poh, 2019 |
cross-sectionele studie lies- en genitale pijnpatiënten |
|
Reig, 2005 |
valt binnen search Li 2016 |
|
Reyad, 2018 |
voldoet niet aan PICO (pelvic malignancy) |
|
Robert, 2005 |
voldoet niet aan PICO (chirurgische interventie) |
|
Rofaeel, 2008 |
feasbility trial of duur ingreep |
|
Rojas-Gómez, 2017 |
narrative review |
|
Rosen, 2006 |
voldoet niet aan PICO (gaat over open versus. laparoscopische behandeling hernia). |
|
Roy, 2018 |
narrative review |
|
Schmidt, 2005 |
narrative review |
|
Scott, 2017 |
voldoet niet aan PICO (geen blokkades) |
|
Sencan, 2018 |
voldoet niet aan PICO (gaat over effect coccygeal dynamic patterns) |
|
Stav, 2009 |
narrative review |
|
Stogicza, 2012 |
kadaverstudie |
|
Strom, 2008 |
valt binnen search Li 2016 |
|
Tang, 2013 |
voldoet niet aan PICO (hernia) |
|
Toshniwal, 2007 |
valt binnen search Li 2016 |
|
Toshniwal, 2007 |
valt binnen search Li 2016 |
|
Trainor, 2015 |
voldoet niet aan PICO (gaat over benaderingswijze blokkade; patiënten met liespijn). |
|
Vancaillie, 2012 |
valt binnen search Li 2016 |
|
Vicariotto, 2017 |
voldoet niet aan PICO (geen CPP-patiënten). |
|
Voorbrood, 2015 |
voldoet niet aan PICO (liespijn) |
|
Wan, 2017 |
voldoet niet aan PICO (geen blokkades) |
|
Zacest, 2010 |
voldoet niet aan PICO (liespijn) |
Beoordelingsdatum en geldigheid
Publicatiedatum : 04-08-2021
Beoordeeld op geldigheid : 31-08-2021
Voor het beoordelen van de actualiteit van deze richtlijn is de werkgroep niet in stand gehouden. Uiterlijk in 2025 bepaalt het bestuur van de Nederlandse Vereniging voor Urologie (NVU) of de modules van deze richtlijn nog actueel zijn. Op modulair niveau is een onderhoudsplan beschreven. Bij het opstellen van de richtlijn heeft de werkgroep per module een inschatting gemaakt over de maximale termijn waarop herbeoordeling moet plaatsvinden en eventuele aandachtspunten geformuleerd die van belang zijn bij een toekomstige herziening (update). De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen aanleiding zijn een herzieningstraject te starten.
De NVU is regiehouder van deze richtlijn en eerstverantwoordelijke op het gebied van de actualiteitsbeoordeling van de richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijke verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de regiehouder over relevante ontwikkelingen binnen hun vakgebied.
|
Module[1] |
Regiehouder(s)[2] |
Jaar van autorisatie |
Eerstvolgende beoordeling actualiteit richtlijn[3] |
Frequentie van beoordeling op actualiteit[4] |
Wie houdt er toezicht op actualiteit[5] |
Relevante factoren voor wijzigingen in aanbeveling[6] |
|
Pijnblokkades |
NVU |
2020 |
2025 |
Elke 5 jaar |
NVU |
Nieuwe literatuur |
[1] Naam van de module
[2] Regiehouder van de module (deze kan verschillen per module en kan ook verdeeld zijn over meerdere regiehouders)
[3] Maximaal na vijf jaar
[4] (half)Jaarlijks, eens in twee jaar, eens in vijf jaar
[5] regievoerende vereniging, gedeelde regievoerende verenigingen, of (multidisciplinaire) werkgroep die in stand blijft
[6] Lopend onderzoek, wijzigingen in vergoeding/organisatie, beschikbaarheid nieuwe middelen
Algemene gegevens
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en werd gefinancierd uit de Stichting Kwaliteitsgelden Medisch Specialisten (SKMS). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijn.
De richtlijn is ontwikkeld in samenwerking met:
- Nederlandse Vereniging van Maag-Darm-Leverartsen
- Nederlandse Vereniging voor Anesthesiologie
- Nederlandse Vereniging voor Obstetrie en Gynaecologie
- Nederlandse Vereniging voor Bekkenfysiotherapie
- Nederlandse Vereniging voor Heelkunde
- Nederlandse Wetenschappelijke Vereniging voor Seksuologie
- Nederlands Instituut van Psychologen
- Landelijke Vereniging Medische Psychologie
- Koninklijke Nederlandse Organisatie van Verloskundigen
- Nederlands Huisartsen Genootschap
- Verpleegkundigen & Verzorgenden Nederland
- Stichting Bekkenbodem4All
- Interstitiële Cystitis Patiëntenvereniging
Doel en doelgroep
Doel
Het ontwikkelen van een evidence based richtlijn over chronische bekkenpijn volgens richtlijnen 2.0.
Doelgroep
Patiënten met chronische bekkenpijn. Alle zorgverleners die betrokken zijn bij de zorg voor patiënten met chronische bekkenpijn.
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijn is in december 2018 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen die betrokken zijn bij de zorg voor patiënten met chronische bekkenpijn.
De werkgroepleden zijn door hun beroepsverenigingen gemandateerd voor deelname.
De werkgroep is verantwoordelijk voor de integrale tekst van deze richtlijn.
Werkgroep
- Dr. E.J. (Bert) Messelink, uroloog-seksuoloog NVVS, NVU (voorzitter).
- Dr. A. (Afina) Glas, uroloog, NVU
- Dr. J. (Jacqueline) Groeneweg, gynaecoloog, NVOG
- Dr. D. (Dick) Janssen, arts-onderzoeker urologie, NVU
- Drs. K. (Karlijn) Schweitzer, gynaecoloog, NVOG
- Drs. V. (Wafa) Rezvani, anesthesioloog-pijnbestrijder, NVA
- Dr. R.J.F. (Richelle) Felt-Bersma, maag-darm-leverarts, NVMDL
- Dr. R.J. (Remmie) Hammers, huisarts, kaderarts urogynaecologie, NHG
- Drs. G. (Gidia) Jacobs, gezondheidszorgpsycholoog, pedagoog, seksuoloog NVVS, NVVS, NIP, LVMP.
- Drs. C. (Corine) Adamse, geregistreerd bekkenfysiotherapeut, NVFB
- (Ana) dos Santos, MSc, geregistreerd bekkenfysiotherapeut, NVFB
- H.J. (Henk-Jan) Mulder, verpleegkundig specialist urologie, V&VN
- C.W.L. (Tine) van den Bos, MSPT, belangenbehartiger patiënten namens Stichting Bekkenbodem4All, voorzitter Stichting Bekkenbodem4All, geregistreerd bekkenfysiotherapeut, Stichting Bekkenbodem4All
Klankbordgroep
- Prof. dr. E.J.C. (Esther) Consten, chirurg, NVvH
- B.B.M. (Brigitte) Tebbe, verloskundige, KNOV
- H.M.T. Andriesse-Walhain, patiëntvertegenwoordiger, ICP
Met ondersteuning van
- Dr. I. (Irina) Mostovaya, senior-adviseur en teamleider, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. A (Anne) Bijlsma-Rutte, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J. (Janneke) Hoogervorst-Schilp, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. J. (José) Maas, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Y.J. (Yvonne) Labeur, MSc, junior adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- M. (Monique) Wessels, MSc, literatuurspecialist, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van Medisch Specialisten.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
* Messelink |
Uroloog - Seksuoloog NVVS Medisch Centrum Leeuwarden |
Verzorgen onderwijs: SOMT Amersfoort. Opleiding Bekkenfysiotherapeuten, 1,5 dag/jaar. Betaald RINO Utrecht. Opleiding seksuologie, 0,5 dag/jaar. Betaald Opleiding Stomaverpleegkundige Groningen. 2 uur/jaar. Betaald
Europese cursus: Chronic Pelvic Pain, European Association of Urology. Halve dag 1x/jaar. Betaald |
* Voorzitter Pelvic Floor Network, een non-profit organisatie die zich inzet voor het structureren van landelijk onderwijs en het opzetten van een zorg-netwerk betreffende chronische bekkenpijn. * Lid medische adviesraad van de patiëntenverenigingen: BB4All, PVVN. * Vice-chairman EAU Guideline panel Chronic Pelvic Pain. |
Geen |
|
Groeneweg |
gynaecoloog IJsselland ziekenhuis 0,625 fte expert gynaecologie Zorginstituut Nederland 0,2 fte |
bestuurslid werkgroep Bekkenbodem NVOG onbetaald
|
vanuit werkgroep Bekkenbodem ben ik de contactpersoon voor de patiëntenorganisatie BB4all |
Geen |
|
Schaapveld |
Voorzitter Bekkenbodem4all |
Lid cliëntenraad Residentie Molenwijck |
Niet van toepassing |
Geen |
|
Glas |
Uroloog, vrij gevestigd. ZaansMC |
Geen |
Ben betrokken bij opzet onderzoek naar blaasspoelingen bij preventie van urineweginfecties. Dit onderzoek wordt mogelijk gefinancierd (aanvraag unrestricted grant) door bedrijf dat ook blaasspoelingen verkoopt voor indicatie chronische bekkenpijn
Ik hoop dat eerder ontwikkelde standpunt BPS/ic waar ik actief betrokken bij ben geweest een plaats krijgt, qua inhoud, inde de nieuw te ontwikkelen richtlijn bekkenpijn.
Het meehelpen bij ontwikkelen van een dergelijke richtlijn, zal voor mij persoonlijke een intellectueel gewin opleveren. In die zin dat ik er ook iets hoop van te leren.
Het mee ontwikkelen van de richtlijn zal denk ik een gunstige invloed hebben op mijn rol als specialist met affiniteit voor de patiëntengroep en het ziektebeeld. |
Geen actie; NB-blaasspoelingen worden niet besproken in de richtlijn |
|
Adamse |
Bekkenfysiotherapeut en klinisch Epidemiologie Docent EBP en begeleider onderzoekstagiaires Antonius ziekenhuis Sneek |
Bekkenfysiotherapeut: Alle klinische en poliklinische zorg rondom bekken patiënten deelname aan multidisciplinair overleg met gynaecologie, urologie en chirurgie. Deelname aan seksuologisch spreekuur en MDO. samenwerking met MDL-artsen en gespecialiseerde verpleegkundigen. klinisch epidemioloog/ docent EBP/ begeleider onderzoekstherapie lesgeven en ondersteunen van onderzoeksvragen op het gebied van EBP voor zowel fysiotherapeuten als verpleegkundigen. Evidence based practise docent (gastdocent) NHL/stenden hogeschool Leeuwarden |
nee, behalve dat richtlijn mogelijk meer werk/aandacht oplevert voor bekkenfysiotherapie in het ziekenhuis
mogelijk meer aandacht voor bekkenfysiotherapie en de NVFB. Review gedaan naar chronische pijn en effectiviteit van e-health toepassingen en gepubliceerd (2017) |
Geen |
|
Santos |
Geregistreerd bekkenfysiotherapeut MSc bij PelviCentrum- Centrum voor Bekkenfysiotherapie Leiden Eigenaresse van PelviCentrum - Centrum l voor Bekkenfysiotherapie Leiden |
Lid van NVFB Wetenschappelijke Commissie. Vergoeding van de reiskosten en bijwonen van vergaderingen.
In samenwerking met verloskundigenpraktijk en Mamacafe Leiden geef ik workshops aan zwangeren en vrouwen postpartum. Deze werkzaamheden zijn onbetaald. |
Deelname aan het ontwikkelen van de richtlijn kan ervoor zorgen dat collega vaker gaan verwijzen naar mijn praktijk vanwege meer bekendheid. |
Geen |
|
Hammers |
Waarnemend huisarts Kaderhuisarts Urogyneacologie |
Lid medische adviesraad stichting Bekkenbodem4All. Onkostenvergoeding |
Ik ben de afgevaardigde vanuit de UgynHag (kaderhuisartsenartsen urogynaecologie) |
Geen |
|
Jacobs |
Gezondheidszorgpsycholoog, seksuoloog NVVS in vrijgevestigde praktijk: centrum voor psychische, relationele en seksuele gezondheid te Voorschoten. Gezondheidspsycholoog seksuoloog NVVS in deeltijd bij proctosklinkiek te Bilthoven Hoofdopleider post-big-opleiding seksuologie rino te Utrecht |
Lid van Tuchtrechtcommissietucht van de NVVS onbezoldigd. Adviseur van het bestuur van PFN onbezoldigd. Lesgeven bij diverse organisaties bv. SOMT, ZEL. (bezoldigd) |
Adviseur van het bestuur van PFN ik neem deel uit interesse voor het complexe vakgebied met als doelgroep patiëntenzorg te verbeteren. |
Geen |
|
Mulder |
Verpleegkundig specialist urologie Martini Ziekenhuis Groningen |
Lid van Adviesraad Hollister BV. |
|
Geen actie; NB (thuiszorg) hulpmiddelen worden niet besproken in de richtlijn |
|
Rezvani |
Anesthesioloog/pijnbestrijder, werkzaam in het St. Antonius ziekenhuis Nieuwegein/Utrecht in een maatschap |
Lid ledenraad NVA-sectie pijnbestrijding, onbetaald. |
|
Geen |
|
Janssen |
Arts bij Gynos vrouwenkliniek Den Haag, blaaspijn/bps-spreekuur (onderdeel van Andros klinieken)
Arts-onderzoeker, afdeling urologie, Radboudumc
|
Coördinator en docent Technische Geneeskunde Faculteit, Universiteit Twente.
- Medische adviesraad (MAR) patiëntenvereniging ICP |
Te vermelden voor openheid van zaken:
- Werkzaam in 2 medische centra (Radboudumc & Gynos vrouwenkliniek) die patiëntenzorg op dit deelgebied verlenen.
Meegeschreven aan NVU-standpunt BPS 2017 (onbetaald).
- In verleden tegen betaling eenmalig advies gegeven voor Bene Arzneimittel GMBH farmaceuticals, producent van Elmiron, medicijn voor blaaspijn syndroom.
- In 2017 tegen eenmalige vergoeding gesproken op European Association of Urology congres op gesponsorde sessie door IBSA farmaceuticals (producent GAG-therapie voor blaaspijnsyndroom)
- Eigenaar eenmanszaak dr. Dr. D.A.W. Janssen, Urology Science & Healthcare (KvK nr. 77488881). Geen bezit van patenten, geen (incl. toekomstige beloften voor) financieel gewin door participatie aan deze richtlijn commissie.
Deelname aan deze commissie zou impact kunnen hebben op mijn aanzien als klinisch professional binnen mijn vakgebied. De mate van impact kan ik niet overzien |
Geen actie; NB-blaasspoelingen worden niet besproken in de richtlijn |
|
Schweitzer |
Gynaecoloog UMC Utrecht, Bergman Clinics Hilversum vrouwenzorg |
Trainer KNOV-hechtcursus. Trainer hechtcursus Leiderdorp NVOG voor beiden ontvang ik een vergoeding |
Bij Bergman Clinics zien we patiënten met chronische pijn in buik en bekken mogelijk dat er een toename van pte gaat komen
Deelname aan deze het ontwikkelen van de richtlijn kan ervoor zorgen dat collega vaker gaan verwijzen vanwege meer bekendheid |
Geen |
|
Felt - Bersma |
MDL-arts Amsterdam UMC, locatie VUMC |
MDL-arts Proctoskliniek te Bilthoven MDL-arts MCV de Veluwe, Apeldoorn |
ROAD-studie, een studie met een medicament versus placebo ter preventie van recidief diverticulitis |
Geen |
|
Van den Bos |
1. Bekkenfysiotherapeut MSPT (Master of Specialised Physical Therapy) bij AdFysio te De Lier 0.6 fte 2. Bekkenfysiotherapeut MSPT LUMC, afd. urologie 0.2 fte onbezoldigd 3. Voorzitter BB4All (Bekkenbodem4All), vrijwilliger |
Lid MAR (Medische Advies Raad) Lichen Sclerosis Nederland: reiskostenvergoeding Lid MAR Lichen Planus Vereniging Nederland: reiskostenvergoeding Penningmeester zorggroep FEL (Fysiotherapie 1e Lijn) Zuid-Holland West: onkostenvergoeding |
Geen |
Geen |
|
Klankbordgroep |
|
|
|
|
|
Tebbe (klankbordgroep) |
Wetenschappelijk adviseur KNOV (ZZP) verloskundige |
Communicatie + tekstschrijver (ZZP) |
Geen |
Geen |
|
Andriesse (klankbordgroep) |
Voorzitter van de Interstitiële cystitis vereniging, ICP |
Ik ben vrijwilliger niet betaald |
Geen |
Geen |
|
Consten (klankbordgroep) |
chirurg, meander medisch centrum MMC en hoogleraar universitair medisch centrum Groningen UMCG in de chirurgie aandachtsgebied robotica en computer geassisteerde chirurgie |
voorzitter werkgroep coloproctologie opleideer heelkunde mmc |
arts in tertiair bekkenbodem centrum van het meander medisch centrum te Amersfoort |
Geen |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door middel van een afgevaardigde patiëntenvereniging in de werkgroep en in de klankbordgroep.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden in de bijlagen. Er zijn geen indicatoren ontwikkeld bij deze richtlijn.
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is. Voor een stap-voor-stap beschrijving hoe een evidence-based richtlijn tot stand komt wordt verwezen naar het stappenplan Ontwikkeling van Medisch Specialistische Richtlijnen van het Kennisinstituut van Medisch Specialisten.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de voorzitter van de werkgroep en de adviseur de knelpunten. Tevens zijn er knelpunten aangedragen door verschillende partijen/vertegenwoordigers van relevante stakeholders via een Invitational conference. Een verslag hiervan is opgenomen in de bijlagen.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur concept-uitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Tevens definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Per uitgangsvraag werd aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekstrategie en de gehanteerde selectiecriteria zijn te vinden in de module met desbetreffende uitgangsvraag. De zoekstrategie voor de oriënterende zoekactie en patiëntenperspectief zijn opgenomen in de bijlagen.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen inschatten. Deze beoordelingen kunt u vinden in de Risk of Bias (RoB) tabellen. De gebruikte RoB instrumenten zijn gevalideerde instrumenten die worden aanbevolen door de Cochrane Collaboration: AMSTAR - voor systematische reviews; Cochrane - voor gerandomiseerd gecontroleerd onderzoek; Newcastle-Ottowa - voor observationeel onderzoek; QUADAS II - voor diagnostisch onderzoek.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidencetabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen (vragen over therapie of screening)
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org/).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie (Schünemann, 2013).
|
GRADE |
Definitie |
|
Hoog |
|
|
Redelijk* |
|
|
Laag |
|
|
Zeer laag |
|
*in 2017 heeft het Dutch GRADE Network bepaald dat de voorkeursformulering voor de op een na hoogste gradering ‘redelijk’ is in plaats van ‘matig’
B) Voor vragen over diagnostische tests, schade of bijwerkingen, etiologie en prognose
De kracht van het wetenschappelijke bewijs werd eveneens bepaald volgens de GRADE-methode: GRADE-diagnostiek voor diagnostische vragen (Schünemann, 2008) en een generieke GRADE-methode voor vragen over schade of bijwerkingen, etiologie en prognose. In de gehanteerde generieke GRADE-methode werden de basisprincipes van de GRADE-methodiek toegepast: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van bewijskracht op basis van de vijf GRADE-criteria (startpunt hoog; downgraden voor risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias).
Formuleren van de conclusies
Voor elke relevante uitkomstmaat werd het wetenschappelijk bewijs samengevat in een of meerdere literatuurconclusies waarbij het niveau van bewijs werd bepaald volgens de GRADE-methodiek. De werkgroepleden maakten de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de cruciale uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen en organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. Meer algemene, overkoepelende, of bijkomende aspecten van de organisatie van zorg worden behandeld in de module Organisatie van Zorg.
Indicatorontwikkeling
Er werden geen indicatoren ontwikkeld bij deze richtlijn.
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is om de uitgangsvraag te kunnen beantwoorden. Een overzicht van de onderwerpen waarvoor (aanvullend) wetenschappelijk van belang wordt geacht, is als aanbeveling in de bijlage Kennislacunes beschreven.
Commentaar- en autorisatiefase
De conceptrichtlijn werd aan de betrokken (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Literatuur
Brouwers, M. C., Kho, M. E., Browman, G. P., Burgers, J. S., Cluzeau, F., Feder, G.,... & Littlejohns, P. (2010). AGREE II: advancing guideline development, reporting and evaluation in health care. Canadian Medical Association Journal, 182(18), E839-E842.
Kennisinstituut van de Federatie Medisch Specialisten. Ontwikkeling van Medisch Specialistische Richtlijnen: stappenplan. Utrecht, 2015.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwaliteit. https://richtlijnendatabase.nl/werkwijze/richtlijnen_3_0.html.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013. Available from http://gdt.guidelinedevelopment.org/central_prod/_design/client/handbook/handbook.html.
Schünemann, H. J., Oxman, A. D., Brozek, J., Glasziou, P., Jaeschke, R., Vist, G. E.,... & Bossuyt, P. (2008). Rating Quality of Evidence and Strength of Recommendations: GRADE: Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ: British Medical Journal, 336(7653), 1106.
Wessels, M., Hielkema, L., & van der Weijden, T. (2016). How to identify existing literature on patients' knowledge, views, and values: the development of a validated search filter. Journal of the Medical Library Association: JMLA, 104(4), 320.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID) |
1 exp pelvic pain/ or dysmenorrhea/ or pelvic girdle pain/ or piriformis muscle syndrome/ or Pelvic Floor Disorders/ or pudendal Neuralgia/ (9507) 2 ((pelvic or pelvis or pudendal) adj3 (pain* or syndrome or neuralgia or myalgia)).ti,ab,kf. (10481) 3 ((prostatitis or prostate or "levator ani" or constipation or puborectalis) adj3 (neuralgia* or pain* or sydrome* or spasm*)).ti,ab,kf. (2731) 4 (prostatalgia or prostatodynia or orchialgia or dyssynergia or Coccydynia or coccygodynia or proctalgia or vestibulodynia or dysmenorrhea* or dysmenorrhoea or vulvodynia or Dyspareunia or "Pyriformis syndrome").ti,ab,kf. (11482) 5 ((bladder or testicular or urethral or scrotal or groin or epididymal or "post vasectom*" or genital or coccyx or sacrococcygeal or anal or anorectal or vestibular or vulvar or "Fissure in Ano" or perineal) adj3 pain*).ti,ab,kf. (8623) 6 (((interstitial or recurrent) adj2 (cystitides or cystitis)) or ((suprapubic or abdominal or endometriosis) adj3 (neuralgia* or pain*))).ti,ab,kf. (61213) 7 ((proctitis or defecation or hemorrhoid* or haemorrhoid* or diverticulitis or PID or "pelvic inflammatory disease*") adj3 (neuralgia* or pain*)).ti,ab,kf. (994) 8 ((voiding or prostat* or menstrual or menstruation or childbirth or vaginal or vulvar or urethral or "cauda equina") adj3 (neuralgia* or pain*)).ti,ab,kf. (5104) 9 ("pelvic floor" adj3 (overactivity or dysfunction or "resting tone" or hypertonicity)).ti,ab,kf. (1025) 10 or/1-9 (91451) 11 exp Chronic Disease/ or (chronic or chronically or persistent or constant* or continuing or sustained or lasting or refractor*).ti,ab,kf. or Chronic Pain/ (2183355) 12 10 and 11 (20177) 13 (Groin/ or exp Testicular Diseases/ or Scrotum/ or Pelvic Floor/) and Chronic Pain/ (140) 14 12 or 13 (20201) 15 limit 14 to english language (17541) 16 limit 15 to yr="1999 -Current" (14429) 17 nerve block/ or autonomic nerve block/ (20623) 18 Pulsed Radiofrequency Treatment/ (396) 19 Radiofrequency.ti,ab,kf. (31801) 20 ((nerve* or pain or plexus or root*) adj3 block*).ti,ab,kf. (18209) 21 ((ilioinguin* or Iliohypogastri* or genitofemoral* or pudend* or Ganglion*) adj3 block*).ti,ab,kf. (5563) 22 ((caudal or Sacral or S1 or S2 or S3 or S4 or S5) adj3 block*).ti,ab,kf. (1191) 23 17 or 18 or 19 or 20 or 21 or 22 (65820) 24 16 and 23 (334) 25 ((meta-analysis/ or meta-analysis as topic/ or (metaanaly* or metanaly* or meta-analy* or meta synthes* or metasynthes* or (pooled adj3 analysis)).ti,ab,kf. or ((systematic* or scoping or evidence based) adj3 (review* or overview*)).ti,ab,kf. or ((evidence or research) adj3 synthesis).ti,kf. or systematic review.pt. or (prisma or (("structured literature" or comprehensive or "quantitative literature" or evidence-based) adj2 (search or review)) or "systematic search" or ((systemic or systematized) adj3 review) or "systematic research synthesis" or (review* adj3 independent*))).ti,ab,kf. or (((quantitative or rapid or short or critical* or structured or comparative or comparitive or evidence or comprehensive) adj3 (review* or overview*)).ti. and search.ab.) or "Review Literature as Topic"/ or cochrane.jw. or (cochrane or embase or medline or cinahl or cinhal or cancerlit).ab. or (("selection criteria" or "data extraction").ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (335799) 26 24 and 25 (14) 27 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1873255) 28 24 and 27 (64) 29 Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or (cohort adj (study or studies)).tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ (Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies) (3214241) 30 24 and 29 (108) 31 26 or 28 or 30 (143) 32 26 or 28 (70) 33 30 not 32 (73) |
206 |
|
|
((((((('pelvic pain'/exp/mj OR 'dysmenorrhea'/exp/mj OR 'pelvic girdle pain'/exp/mj OR 'piriformis syndrome'/exp/mj OR 'pelvic floor disorder'/exp/mj OR 'pudendal neuralgia'/exp/mj) OR ((pelvic OR pelvis OR pudendal) NEAR/3 (pain* OR syndrome OR neuralgia OR myalgia)):ti,ab OR ((prostatitis OR prostate OR 'levator ani' OR constipation OR puborectalis) NEAR/3 (neuralgia* OR pain* OR sydrome* OR spasm*)):ti,ab OR (prostatalgia:ti,ab OR prostatodynia:ti,ab OR orchialgia:ti,ab OR dyssynergia:ti,ab OR coccydynia:ti,ab OR coccygodynia:ti,ab OR proctalgia:ti,ab OR vestibulodynia:ti,ab OR dysmenorrhea*:ti,ab OR dysmenorrhoea:ti,ab OR vulvodynia:ti,ab OR dyspareunia:ti,ab OR 'pyriformis syndrome*':ti,ab) OR ((bladder OR testicular OR urethral OR scrotal OR groin OR epididymal OR 'post vasectom*' OR genital OR coccyx OR sacrococcygeal OR anal OR anorectal OR vestibular OR vulvar OR 'fissure in ano' OR perineal) NEAR/3 pain*):ti,ab OR ((((interstitial OR recurrent) NEAR/2 (cystitides OR cystitis)):ti,ab) OR (((suprapubic OR abdominal OR endometriosis) NEAR/3 (neuralgia* OR pain*)):ti,ab)) OR ((voiding OR prostat* OR menstrual OR menstruation OR childbirth OR vaginal OR vulvar OR urethral OR 'cauda equina') NEAR/3 (neuralgia* OR pain*)):ti,ab OR ('pelvic floor' NEAR/3 (overactivity OR dysfunction OR 'resting tone' OR hypertonicity)):ti,ab OR ((proctitis OR defecation OR hemorrhoid* OR haemorrhoid* OR diverticulitis OR pid OR 'pelvic inflammatory disease*') NEAR/3 (neuralgia* OR pain*)):ti,ab)
AND ('chronic disease'/exp OR 'chronic pain'/exp OR 'chronic inflammatory pain'/exp OR chronic:ti,ab OR chronically:ti,ab OR persistent:ti,ab OR constant*:ti,ab OR continuing:ti,ab OR sustained:ti,ab OR lasting:ti,ab OR refractor*:ti,ab))
OR (('inguinal region'/exp/mj OR 'testis disease'/exp/mj OR 'pelvis floor'/exp/mj) AND 'chronic pain'/exp) OR 'chronic scrotal pain'/exp)
AND (english)/lim AND ((embase)/lim OR (pubmed-not-medline)/lim) NOT 'conference abstract':it)
AND ('nerve block'/exp OR 'radiofrequency therapy'/exp OR radiofrequency:ti,ab OR ((nerve* OR pain OR plexus OR root*) NEAR/3 block*):ti,ab OR ((ilioinguin* OR iliohypogastri* OR genitofemoral* OR pudend* OR ganglion*) NEAR/3 block*):ti,ab OR ((caudal OR sacral OR s1 OR s2 OR s3 OR s4 OR s5) NEAR/3 block*):ti,ab)
AND (1999-2019)/py) AND (('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp))) OR (('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it)) (97) > 44 uniek
AND 'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) (47) > 19 uniek |
|
