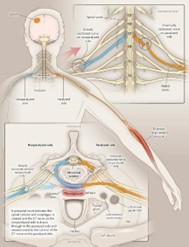
Chirurgische behandelingen aan de bovenste en onderste extremiteit
Uitgangsvraag
Wat is de rol van (functionele) chirurgie aan de bovenste en onderste extremiteit bij volwassenen met cerebrale spasticiteit?
Aanbeveling
Stel de indicatie voor een chirurgische ingreep bij patiënten met cerebrale spasticiteit, bij wie het neurologische beeld stabiel is. Het doel van de chirurgische ingreep is in ieder geval één van de volgende:
- De verbetering van een actieve of passieve vaardigheid.
- Reductie van symptomen (bijv. pijn).
- Het voorkomen van progressie van de deformiteit.
- Het verminderen van afhankelijkheid van tijdelijke behandelingen of orthesen/aangepast schoeisel.
Bespreek de mogelijke chirurgische opties altijd in een multidisciplinair overleg (MDO). Verwijs voor definitieve indicatiestelling en behandeling naar een specialistisch centrum. Relateer de behandelopties altijd aan de behandeldoelen van de patiënt. Indiceer chirurgische interventies aan de onderste extremiteit bij lopende patiënten bovendien altijd op basis van 3D-gangbeeldanalyse. In het specialistische, chirurgische behandelteam zijn tenminste de revalidatiearts, neurochirurg/plastisch chirurg en/of orthopeed en minimaal een paramedicus (fysiotherapeut en/of ergotherapeut) met specifieke expertise op spasticiteitsbehandeling betrokken.
Bespreek de mogelijke (chirurgische) opties met de patiënt aan de hand van zijn/haar/hun behandeldoelen.
- Voer voorafgaand aan een neurectomie een check uit middels botulinetoxine of selectieve zenuwblokkades om het effect na te bootsen; doe dit ook bij orthopedische interventies indien mogelijk, of test het verwachte resultaat van orthopedische chirurgie met spalken of schoenaanpassingen.
- Evalueer de behandeling van een chirurgische interventie in ieder geval op basis van de vooraf gestelde doelen en na een voldoende lang interval postoperatief. In het geval van de onderste extremiteit is dit interval 6-12 maanden en wordt postoperatieve 3D-gangbeeldanalyse aangeraden.
- Bespreek de uitkomsten van chirurgische interventies regelmatig in het interdisciplinaire behandelteam ter verbetering van de kwaliteit van zorg.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
De wetenschappelijke basis voor uitkomsten van chirurgische behandelingen op groepsniveau blijven beperkt tot enkele studies van beperkte omvang; er werden in de literatuursearch twee kleine RCT’s gevonden over chirurgie. Beide studies lieten een verbetering van spasticiteit zien (voor een aantal spiergroepen), maar de bewijskracht is zeer laag. Op basis van klinische ervaring (inter)nationaal, wordt wel een duidelijke meerwaarde gezien van individueel – op de specifieke patiënt – afgestemde chirurgische behandeling. Dit geldt vooral bij hinderlijke spasticiteit en daarmee samenhangende standsafwijkingen van arm of been. Hieronder volgen:
- Algemene overwegingen over alle vormen van chirurgie gericht op bovenste én onderste extremiteit.
- Specifieke overwegingen voor de bovenste extremiteit, waarbij onderscheid wordt gemaakt tussen de functioneel niet-inzetbare en de functioneel inzetbare arm/hand:
- Ingedeeld naar ingrepen
- en integraal gericht op zenuwen, spieren/pezen en botten/gewrichten
- Specifieke overwegingen voor de onderste extremiteit, waarbij er vrijwel altijd sprake is van een functioneel inzetbaar been t.b.v. lopen, staan en/of het maken van transfers:
- Ingedeeld naar ingrepen
- en integraal gericht op zenuwen, spieren/pezen en botten/gewrichten
- Overige overwegingen: voorkeuren van patiënten, kosten, gelijkheid en haalbaarheid/aanvaardbaarheid.
1. Algemene overwegingen
Ervaring (wie): De indicatie voor chirurgische ingrepen bij spasticiteit moet altijd worden gesteld op basis van interdisciplinaire diagnostiek in een ervaren team, dat bestaat uit (minimaal) een revalidatiearts, plastisch/ neuro-/ of orthopedisch chirurg, en paramedicus (fysiotherapeut en/of ergotherapeut). De operatie dient ook door een ervaren behandelteam te worden uitgevoerd, inclusief de begeleiding tijdens de eerste post-operatieve fase in nauwe samenwerking met de eerste lijn en/of verwijzer uit de tweede lijn.
Timing van chirurgie (wanneer): Uitgangspunt is dat zoveel mogelijk alle geïndiceerde ingrepen in één sessie dienen plaats te vinden en op het juiste moment in de levensfase van de patiënt (zie ook Richtlijn CP bij kinderen voor de zogenaamde single-event multi-level surgery;). Dit voorkomt onnodig opereren in meerdere sessies, met de daarbij behorende extra belasting voor de patiënt, familie en de gezondheidszorg. Het behandelteam moet hiervoor goed inzicht hebben in de (oorzaak, stabiliteit en prognose van de) aandoening en in de fysiologische en biomechanische mechanismen die leiden tot standsveranderingen in de te behandelen spastische extremiteit. Gelijktijdig opereren van een bovenste en onderste extremiteit wordt afgeraden, gezien de noodzakelijke nabehandeling en de daarmee samenhangende belasting voor de patiënt.
Alternatieve behandeling: Functionele chirurgie van een spastische extremiteit dient als behandeloptie altijd te worden afgewogen tegen alternatieve behandelopties, waaronder spalkbehandelingen, fysiotherapeutische interventies, botulinetoxine behandelingen en, niet te vergeten, geen behandeling. In veel gevallen zullen alternatieve behandelingen al hebben plaats gevonden als patiënten multidisciplinair, samen met een van de chirurgische disciplines, worden gezien. Toch is chirurgie niet per definitie een ‘last resort’ behandeling.
Correctie van de standsafwijking in de drie vlakken (hoe): Functionele chirurgie van een spastische extremiteit dient zoveel mogelijk gericht te zijn op het weer in balans brengen van de krachten rondom de gewrichten waarop de operatie is gericht. De krachten in het sagittale, frontale, en transversale vlak moeten goed uitgelijnd worden en leiden tot een goede axiale belastbaarheid (dit laatste vooral van belang voor de onderste extremiteit). Dit kan door ingrepen op het niveau van de zenuwen, pezen, gewrichten of botten. Vaak gaat het om een combinatie van (complexe) ingrepen, waarbij soms ook een combinatie van chirurgische disciplines nodig is om een optimaal resultaat te bereiken.
1.1 Randvoorwaarden
De volgende randvoorwaarden zijn belangrijk bij chirurgische interventie voor spasticiteit:
- Stabiel beeld: Het neurologische beeld van de patiënt dient stabiel te zijn. Symptomen van spasticiteit sinds het hersenletsel kunnen zich namelijk voortzetten na de interventie (bijv. langzame verandering van spiertonus) en het resultaat ervan beïnvloeden. Om vergelijkbare redenen is ook terughoudendheid met chirurgisch ingrijpen geboden bij overheersende (extrapyramidale) dystone of dyskinetische problematiek.
- Hulpvraag: De hulpvraag van de patiënt of mantelzorger(s) moet goed omschreven zijn. Hulpvragen die vaak goed te behandelen zijn met een chirurgische interventie betreffen: (a) lokale pijn samenhangend met de deformiteit, (b) hygiëneproblemen, (c) praktische (zoals functieverlies) en cosmetische bezwaren van een veranderde stand, en (d) de wens om het gebruik van spasmolytica of orthesen te kunnen afbouwen. Als het doel van de patiënt duidelijk wordt, kan een keuze gemaakt worden welke specifieke ingrepen dit doel dienen. Het interdisciplinaire behandelteam moet een dan een realistisch verwachtingspatroon van de interventie scheppen.
- Pre- en post-operatieve zorg: Het interdisciplinaire behandelteam moet ook anticiperen op de vorm en duur van de vereiste nabehandeling: immobilisatie, training en andere aspecten van revalidatie. Deze dienen in detail met patiënt en mantelzorgers te worden besproken, voordat een definitieve indicatie wordt gesteld en een operatie wordt ingepland. In sommige gevallen (bijv. bij ernstige adipositas) kan het ook zinvol zijn om te denken aan een pre-operatief trainings- en begeleidingstraject (‘prevalidatie’), om het postoperatieve traject beter te kunnen volbrengen; vooral bij ingrepen aan de onderste extremiteit voor het bereiken van een goede functie en vaardigheid.
2. Bovenste extremiteit
Voor de indicatiestelling van chirurgie aan de arm/hand wordt vaak onderscheid gemaakt tussen een functioneel inzetbare en niet-functioneel inzetbare arm/hand. De beoordeling van de functionele inzetbaarheid vormt een valkuil: een spastische arm/hand kan gemakkelijk als “niet-functioneel” worden geduid, met als conclusie dat er “niets te verliezen is”, maar er is vaak nog wel een belangrijke steun-, klem- en/of fixatiefunctie. Chirurgie kan dan risico’s opleveren voor de resterende functie(s). Een voorbeeld hiervan is de clenched fist: een gespannen spastische vuist, waardoor de hand slecht te verzorgen is en pijnlijk kan zijn, maar die nog een klemfunctie kan hebben om objecten mee te fixeren. Deze resterende inzetbaarheid zou verloren kunnen gaan na chirurgie. Hier moet ook in het bijzonder aandacht voor zijn bij volwassenen met CP met een bilaterale parese. Een hulpvraag naar functionele verbetering betreft hier meestal de ‘betere’ arm/hand, waarbij verlies van resterende functie nog fnuikender is.
Bij elke functionele inzetbaarheid van het ledemaat is de keuze voor een chirurgische interventie aan een aantal overwegingen onderhevig. Een grondig lichamelijk en ergotherapeutisch onderzoek is daarom essentieel om het niveau van functionele inzetbaarheid goed in te schatten. Belangrijke restfuncties zijn de steunfunctie van de hand bij bimanuele taken, klemfuncties van de vuist, haakfuncties van de pols en elleboog, fixatiefunctie van de bovenarm tegen het lichaam, en steunfunctie van de arm/hand bij transfers. Meestal wordt een combinatie van verschillende procedures ingezet. Zeker bij de overweging om de pols te opereren: de stand van de pols beïnvloedt ook de stand en functie van de vingers en duim, daarom moeten deze vaak samen worden geopereerd.
Zie tabel 5 voor een overzicht van de meest voorkomende ingrepen per gewrichtsniveau.
Tabel 5. Meest voorkomende ingrepen aan de bovenste extremiteit (niet uitputtend, opties moeten altijd op individueel niveau in multidisciplinair overleg worden afgestemd)
|
Ingreep |
Uitleg |
Meest voorkomende voorbeelden |
|
Myotomie/ Tenotomie |
Doornemen van een spier of pees ten behoeve van standsverbetering van gewrichten (met name bij spierverkorting). De functie van de betrokken spier(en) gaat hierbij verloren. |
|
|
Verlengingsplastiek pezen |
Verlenging van pezen op spier-pees overgang of op pees alleen. Hierdoor kan een standsverbetering verkregen worden. Deze verlenging gaat vaak gepaard met krachts-vermindering van de betrokken spiergroepen |
|
|
Peestranspositie |
Verplaatsen van individueel aan te sturen spieren die misbaar zijn, om een afwezige functie over te nemen. |
|
|
Selectieve neurectomie |
Doornemen van alle motorische zenuwen naar een specifieke spier om spasticiteit te verminderen. Dit neemt ook de actieve aansturing van deze spier weg. |
|
|
Hyperselectieve neurectomie |
Doornemen van percentage van motorische zenuwen naar een specifieke spier (ca. 70%). Het actief aansturen blijft daarmee intact. |
|
|
Arthrodese/ Capsulodese/ Tenodese |
Plaatsen van een gewricht in een betere stand door vastzetten van gewricht(skapsel) of pees. Dit kan t.b.v. de functie of de verzorging. |
|
3. Onderste extremiteit
Voor de indicatiestelling van functionele chirurgie aan de onderste extremiteit moet ervan uit worden gegaan dat er vrijwel altijd sprake is van (resterende) relevante functie zoals steunen, staan en transfereren. Los daarvan is het relevant om vast te stellen of mensen nog beschikken over loopvaardigheid, waarbij meestal de ondergrens wordt aangehouden van 0,1 m/s loopsnelheid. De volgende 3 aspecten van het lopen spelen een belangrijke rol bij het maken van een (operatief) behandelplan:
- stabiliteit van het been in de standfase;
- klaring van het been in de zwaaifase; en
- prepositionering van de voetlanding op de overgang van zwaai- naar standfase.
Om te beslissen of een operatie kan helpen, wordt in beginsel altijd een 3D-gangbeeldanalyse uitgevoerd. Dit is een uitgebreide bewegingsanalyse waarbij naast bovenstaande aspecten ook spatio-temporele (o.a. snelheid, staplengte, staptijd), kinematische (bewegingen in gewrichten) en kinetische variabelen (krachtsmomenten en powers rond gewrichten) worden beoordeeld. Tevens wordt daarbij oppervlakte-elektromyografie uitgevoerd (spieractiveringen tijdens lopen). Als dit preoperatief niet goed in kaart wordt gebracht, kan een operatie mogelijk ongewenste gevolgen hebben. Er kan bijvoorbeeld verlies van functie optreden. Een bekend voorbeeld is het verlies van kniestabiliteit na een achillespeesverlening bij mensen met een zwakke kuitspier, vooral als zij pre-operatief voor hun kniestabiliteit gebruik maakten van de passieve veereigenschappen van de verkorte kuit. Ook kan een afwijkende stand in het ene gewricht leiden tot een probleem in een hoger gelegen gewricht: bijvoorbeeld kan een verkorte kuitspier niet alleen leiden tot een spitsstand van de enkel, maar ook tot overstrekking van de knie in de standfase, waardoor instabiliteit ontstaat. Daarom is het cruciaal om voor een operatie precies te analyseren hoe de hele bewegingsketen (van voet tot bekken en romp) functioneert en wordt belast. Op basis van de verschillende factoren in de analyse kan (interdisciplinair) een patiënt-specifiek behandelplan worden opgesteld met procedures die nodig zijn om het evenwicht in de hele belastings- en bewegingsketen te optimaliseren. Soms kunnen botulinetoxine injecties of selectieve zenuwblokkades pre-operatief worden gegeven om beter te differentiëren welke spieren bijdragen aan een myogene disbalans, en te helpen inschatten wat de effecten van een operatie gaan zijn.
Chirurgische ingrepen voor functionele verbetering van de onderste extremiteit bij mensen met cerebrale spasticiteit kunnen gericht zijn op verschillende gewrichtsniveaus. We maken daarbij onderscheid tussen operaties aan pezen, botten, gewrichten en zenuwen.
- Voor omzetting van pezen is het van belang dat er sprake is van een goede kracht van de betreffende spier en er mag geen sprake zijn van een contractuur in het gewricht dat door de spier wordt bestuurd/bewogen. Weke-delen interventies hebben als voordeel dat de gewrichtsbeweeglijkheid behouden blijft.
- Bij parese en gefixeerde standsafwijkingen verdient het de voorkeur om een benige oplossing te treffen voor de standsafwijking.
- Specifiek voor de behandeling van pes equinovarus is een eerder beschreven behandelalgoritme beschikbaar, waarin de plaats van zowel benige als weke-delen interventies wordt benoemd (Nonnekes, 2018).
Zie voor een overzicht van de meest voorkomende ingrepen aan de onderste extremiteit per gewrichtsniveau tabel 6 (niet uitputtend).
Tabel 6. Meest voorkomende ingrepen per gewrichtsniveau aan de onderste extremiteit (niet uitputtend, opties moeten altijd op individueel niveau in multidisciplinair overleg worden afgestemd)
|
Ingreep |
Uitleg |
Meest voorkomende voorbeelden |
|
Myotenotomie/ Tenotomie |
Doornemen op niveau spier-peesovergang of pees ten behoeve van standsverbetering van gewrichten (met name bij verkorting). |
Enkel-achtervoet: achillespeesverlenging bij verkorting van de kuitspier door zowel de m. soleus als de m. gastrocnemius Enkel-achtervoet: geïsoleerde gastrocnemiusverlenging (gastroc slide) bij verkorting van de kuitspier door alleen de m. gastrocnemius (te objectiveren door bij lichamelijk onderzoek enkeldorsaalflexie te testen met gebogen en gestrekte knie)
|
|
Peestranspositie |
Verplaatsen van individueel aan te sturen spieren die misbaar zijn, om een afwezige functie over te nemen. |
|
|
(selectieve) neurectomie |
Doornemen van (een deel van) de motorische zenuwen naar een specifieke spier om spasticiteit te verminderen. De mate van doornemen beïnvloedt de mate waarin de spier actief kan blijven aansturen. |
|
|
Arthrodese |
Plaatsen van een gewricht in een betere stand door vastzetten van gewricht |
|
|
Osteotomie |
Het wegnemen van stukjes/wiggen bot voor standsverbetering van een gewricht, waardoor belasting goed uitgelijnd is. |
|
4. Overige overwegingen
Waarden en voorkeuren van patiënten (en evt. hun verzorgers)
De afwijkingen en klachten van spasticiteit moeten beschouwd worden in een groter geheel: spasticiteit betreft een groot deel van het lichaam, en heeft effect op meerdere lichamelijke, mentale, en sociale aspecten. Een interdisciplinair behandelteam (in een gespecialiseerd centrum) heeft aandacht voor de verschillende behandelmogelijkheden, en kan goede ondersteuning bieden bij het samen beslissen met de patiënt voor de beste behandeling. Dit kan ertoe leiden dat patiënten in een vroeger stadium verbetering van kwaliteit van leven ondervinden, en dat een mogelijk zwaardere zorgvraag op termijn kan worden voorkómen.
Kosten
Een operatieve behandeling is vaak een duurdere behandeling, maar heeft vaak ook een definitiever effect. Bijvoorbeeld, als van herhaalde botulinetoxine injecties een verminderd effect wordt ervaren, kan chirurgie als behandeling worden ingezet voor een definitief effect. Dit bespaart herhaalde injecties of andere terugkerende behandelingen, of extra hulpmiddelen zoals orthopedisch schoeisel. Een voordeel van een operatie is dat kwaliteit van leven en zelfredzaamheid mogelijk worden vergroot, waardoor een kostenbesparing voor de maatschappij m.b.t. chronische zorgondersteuning wordt gerealiseerd. Dit draagt ook bij aan een ontlasting van de (toenemende) zorgvraag bij thuiszorginstellingen.
Gelijkheid
Een operatie biedt mogelijkheden tot toename van kwaliteit van leven en zelfredzaamheid. Door betere participatie aan de maatschappij kan gezondheidsgelijkheid mogelijk toenemen.
Aanvaardbaarheid
Ethische aanvaardbaarheid
Chirurgische interventies lijken aanvaardbaar voor de betrokkenen. Chirurgie werpt geen ethische bezwaren op; wel moet altijd de afweging tussen gezondheidswinst en niet schaden worden afgewogen (zie ook kopje “Alternatieve behandeling”).
Duurzaamheid
Chirurgische interventies in het algemeen zorgen voor milieubelasting. De indicatiestelling voor chirurgie bij spasticiteit wordt nauw afgewogen binnen een interdisciplinair behandelteam, waarbij gekeken wordt naar verwachte effectiviteit/meerwaarde en de belasting voor de patiënt. De duurzaamheidsaspecten worden daarbij afgewogen tegen die van conservatieve behandeling (bijv. spalken of orthopedisch schoeisel).
Haalbaarheid
Operatieve behandeling van patiënten met spasticiteit en afwijkingen van het steun- en bewegingsstelsel gebeurt al in de praktijk. Het is echter wenselijk dat deze zorg (verder) gecentreerd wordt in 4-6 landelijk verdeelde centra met interdisciplinaire behandelteams, die beschikking hebben over de benodigde diagnostiek (onder andere 3D-gangbeeldanalyse lab). In de toekomst zouden de interdisciplinaire teams van de verschillende centra binnen Nederland een kennisnetwerk kunnen opbouwen, hetgeen tot betere toegankelijkheid van de centra voor de patiënt kan leiden en kan leiden tot nog betere kwaliteit van zorg.
Onderbouwing
A wide range of surgical interventions is available for managing spasticity of the upper and lower extremities in patients with cerebral spasticity. Depending on the stage or progression of the spasticity, the goals of surgery may differ:
- In a functionally usable extremity: restoration or improvement of function, pain reduction, and/or optimization of the weight-bearing axis in the lower extremity.
- In a non-functional extremity: correction of position or alignment to improve overall posture, enhance cosmetic appearance, facilitate hygiene, support basic activities of daily living (e.g., dressing, washing), and relieve pain.
In clinical practice, multiple factors and uncertainties must be considered when evaluating surgical options. Key considerations and challenges include:
- Underlying etiology: Cerebral spasticity may result from various acquired conditions, such as stroke or traumatic brain injury, as well as congenital conditions like cerebral palsy (CP). The prognosis and potential benefits of surgery vary depending on the underlying disorder and are influenced by the expected course—either progression or regression—of both the neurological condition and the musculoskeletal deformity. The heterogeneity of these factors complicates the evidence base for surgical interventions. This module focuses on operative options for adults with spasticity due to stroke or CP, conditions in which the neurological deficits and associated spasticity are generally considered to be stable over time.
- Type of intervention: Which surgical procedures are effective for the upper and lower limbs? Should these be performed in isolation or in combination?
- Timing of intervention: When is surgery indicated? Early surgical intervention may offer benefits such as improved functionality or prevention of progression in joint deformities and contractures. However, there is often reluctance to indicate surgery in the early phase (e.g., shortly after a stroke), with procedures typically postponed to a later stage. It remains unclear which patients will benefit most and which clinical factors (e.g., functional assessment of the upper limb, gait analysis) can best predict favorable postoperative outcomes.
Due to the aforementioned complexities and uncertainties, surgical treatment options are currently often considered a “last resort” in clinical practice. This is likely no longer justified. Accordingly, this module focuses on the potential added value of surgical procedures for the upper and lower extremities following stroke or in cerebral palsy—with special attention to early-phase interventions after stroke where appropriate.
Note: Functional surgery for spinal spasticity is excluded from this module due to its highly specialized nature. In cases such as cervical spinal cord injury, surgical interventions are primarily aimed at compensating for loss of strength and require a separate, specific approach.
Effects on spasticity symptoms
|
Very low GRADE |
The evidence is very uncertain about the added effect of neurosurgery on spasticity symptoms in upper and lower extremities as compared to a non-surgical intervention or conventional rehabilitation in adults with cerebral spasticity.
Source: (Bollens, 2013; Zheng, 2018) |
|
NO GRADE |
No evidence was found regarding the effect of surgery as compared to a non-surgical intervention, conventional rehabilitation or no treatment in adults with cerebral spasticity on pain. |
Effects on skills and abilities
|
Very low GRADE |
The evidence is very uncertain about the effect of neurosurgery on ambulation as compared to a non-surgical intervention in adults with chronic stroke.
Source: (Bollens, 2013) |
|
Very low GRADE |
The evidence is very uncertain about the effect of neurosurgery on upper limb function as compared to conventional rehabilitation in adults with cerebral spasticity.
Source: (Zheng, 2018) |
|
NO GRADE |
No evidence was found regarding the effect of surgery as compared to a non-surgical intervention, conventional rehabilitation or no treatment in adults with cerebral spasticity on stability. |
Quality of life – lower extremity
|
Very low GRADE |
The evidence is very uncertain about the added effect of neurosurgery on quality of life as compared to a non-surgical intervention for spastic pes equinovarus in adults with chronic stroke.
Source: (Bollens, 2013) |
|
NO GRADE |
No evidence was found regarding the effect of surgery as compared to a non-surgical intervention, conventional rehabilitation or no treatment in adults with cerebral spasticity on sleep quality. |
Description of studies
Two RCTs were found describing the effect of surgery on the extremities for adults with cerebral spasticity, one RCT studied the lower extremity (Bollens, 2013) and one the upper extremity (Zheng 2018). Study characteristics are reported in Table 2.
Lower extremity
The RCT by Bollens (2013) studied the effects of selective tibial neurotomy compared to botulinum toxin A injections as a treatment for post-CVA spastic pes equinovarus. The study had an open label design, so patients and healthcare providers were not blinded. However, the assessor of outcome measures was blinded. The study included 16 patients in the chronic phase after CVA (>6 months) that showed an improvement of foot positioning after a selective tibial nerve block. Exclusion criteria were a contracture in the ankle-foot, previous history of local surgery, or pathology interfering with gait. Patients were enrolled from two Belgian university hospitals from July 2008 to January 2011. Eight patients underwent a selective tibial neurotomy, and 8 received injection of botulinum toxin type A (BoNT-A) under electrical stimulation guidance. The neurotomy involved the soleus in all cases and the nerves to the tibialis posterior and flexor hallucis longus in 5 (out of 8) cases. Patients were evaluated before treatment and two and six months after treatment. Outcomes assessed were spasticity, quality of life, walking and functioning.
Upper extremity
The RCT by Zheng (2013) studied the effects of contralateral C7 nerve-transfer surgery followed by rehabilitation compared to rehabilitation alone as a treatment for hemiparesis following CVA, traumatic brain injury, CP or encephalitis. The study had an open label design, patients and physiotherapist were not blinded. However, the assessor of outcome measures was blinded. The study included 36 male patients who were median 15 years after the incident causing hemiparesis. Patients were enrolled in a hospital in Shanghai, China. Eighteen were enrolled in the intervention group and 18 in the control group. Both groups received intensive rehabilitation for 12 months with treatments 4 times a week. Follow up was reported for 12 months after baseline and thus 12 months after intervention for the intervention group. Adherence to rehabilitation was not reported. Outcomes assessed were spasticity and functioning.
Table 2. Study characteristics of included studies
|
Study |
Patients |
Intervention |
Comparison |
Outcomes of interest reported |
Follow-up |
||
|
Characteristics |
Type |
Characteristics |
Type |
||||
|
Bollens, 2013
Open-label RCT |
Adult CVA patients (>6 months after CVA) presenting with spastic pes equinovarus |
N= 8 Mean age (range): 49.9 (32.1-70.2) % Male: 38 |
Selective tibial neurotomy performed by one neurosurgeon |
N= 8 Mean age (range): 52.3 (35.7-65.2) % Male: 50 |
Injection of BoNT-A under electrical stimulation guidance |
- Spasticity (MAS) - QOL (SF-36 physical and mental health) - Walking (gait speed) - Function(ing) (SIAS, FAC, FWC) |
2 and 6 months |
|
Zheng, 2018
Open-label RCT |
Patients (12-45 years of age) with hemiplegia in the upper extremity due to CVA, TBI, CP, or encephalitis |
N= 18 Mean age±SD: 27±9 % Male: 100
Cause of injury (n (%)): - Stroke 5 (28) - TBI 6 (33) - CP 5 (28) - Encephalitis 2 (11) |
C7 nerve-transfer surgery followed by 12 months of rehabilitation (4x week) |
N= 18 Mean age (SD): 26±8 % Male: 100
Cause of injury (n (%)): - Stroke 4 (22) - TBI 6 (33) - CP 8 (44) - Encephalitis 0 (0) |
Rehabilitation only (4x week) |
- Spasticity (MAS) - Function(ing) (Fugl-Meyer Assessment - upper extremity, ADL performance)
|
2,4, 6,8,10 and 12 months |
|
Abbreviations: ADL – activities of daily living; BoNT-A – botulinum toxin type A; CVA – cerebrovascular accident; CP – Cerebral Palsy; FAC – Functional Ambulation Categories; FWC – Functional walking categories; MAS – Modified Ashworth Scale; RCT – Randomized Controlled Trial; SD - standard deviation; SIAS -Stroke Impairment Assessment Set; TBI – Traumatic Brain Injury; QOL – quality of life |
|||||||
Results
1. Effects on body functions and structures
1.1. Spasticity/ Muscle tone
Lower extremity
Both Bollens (2013) and Zheng (2018) reported on spasticity measured with the Modified Ashworth Scale (MAS). Bollens (2013) used a scale of 0-4 and Zheng a scale of 0-5. Higher scores indicate more severe spasticity.
Bollens (2013) reported median (IQR) MAS of the triceps surae and the soleus muscle separately after 6 months (Table 3). The difference in MAS for the triceps surae was not clinically relevant, whereas the difference in the MAS for the soleus was clinically relevant.
Table 3. Spasticity as change in MAS (within-group difference from baseline to 6 months) and between-group difference at 6 months reported by Bollens (2013)
|
|
Modified Ashworth Scale (0-4) |
||
|
|
Median change within group from baseline to 6 months (IQR) |
Between-group difference at 6-month score (p-value) |
|
|
|
TTN |
BoNT-A |
|
|
Triceps surae |
-1 (-1.5 to -0.5) |
0 (-1 to 0.5) |
p = 0.161 |
|
Soleus |
-2.5 (-3 to -1.5) |
-1 (-1.5 to -0.5) |
p = 0.021 |
Abbreviations: TNN- tibial nerve neurotomy; BoNT-A – botulinum toxin type A
Upper extremity
Zheng (2018) reported the change in MAS (0-5) for extension in five joints: elbow, forearm, wrist, thumb and index fingers 2-5. Table 4 shows the results for these joints per group.
Table 4. Spasticity as change in MAS (within-group difference from baseline to 12 months) and between-group difference at 12 months reported by Zheng (2018)
|
|
Modified Ashworth Scale (0-5) |
||
|
|
Median change within group from baseline to 12 months (min-max) |
Between-group difference in change score (p-value) |
|
|
|
Intervention |
Control |
|
|
Elbow |
-1 (-2 to 0) |
0 (-1 to 1) |
P = 0.002 |
|
Forearm |
-1 (-2 to 0) |
0 (-1 to 1) |
P = 0.008 |
|
Wrist |
-1 (-2 to 0) |
0 (-2 to 1) |
P = 0.001 |
|
Thumb |
-1 (-2 to 0) |
0 (-2 to 1) |
P = 0.005 |
|
Digits 2-5 |
-1 (-2 to 0) |
0 (-1 to 1) |
P = 0.001 |
2.2. Pain
No studies reported on pain outcomes.
2. Effects on skills and abilities
2.1. Ambulation – lower extremity
Gait speed was reported by Bollens (2013) measured with the 10-meter walking test. They reported a gait speed of 0.59±0.35 m/s for the TNN group at 6 months after intervention and 0.64±0.39 m/s for the BoNT-A group. The BoNT-A group walked on average 0.05 (95% CI -0.41 to 0.31) m/s faster than the intervention group. This difference was not clinically significant.
With regard to gait, Bollens (2013) reported no differences in Functional Ambulation Categories nor in Functional Walking Categories between baseline and 6 months for either intervention or control group. However, they did not report exact values.
No studies reported on stability.
2.2. Limb function – Upper extremity
Zheng (2018) reports on the Fugl-Meyer upper extremity scale. This scale ranges from 0 to 66 with a higher score indicating better function. After 12 months, Fugl-Meyer for the intervention group was 17.7±5.6 points higher than at baseline. The Fugl-Meyer of the control group had increased by 2.6±2.0 points. Thus, the increase in the Fugl-Meyer was mean 15.1 points (95%CI 12.2 to 17.9) higher in the group receiving contralateral nerve transfer.
In addition, Zheng (2018) reported the performance of four functional hand tasks 12 months after treatment. After contralateral nerve transfer, 16/18 (88.9%) of patients could accomplish 3 or 4 of the functional tasks. None of the patients in the control group could perform 3 or 4 tasks.
3. Quality of life – lower extremity
3.1. Overall quality of life – lower extremity
Only Bollens (2013) reported on quality of life. They reported physical and mental health from the SF-36 scale (0 to 100, a higher score defining a more favorable health state). Six months after treatment, physical health changed with +4.1 for the group after tibial nerve neurotomy (TNN) and with -0.6 for the BoNT-A group. This resulted in a mean difference of +4.7 in favor of the TNN group. Mental health changed with +1.5 for the group after tibial nerve neurotomy and +3.2 for the BoNT-A group. Mean difference after treatment was +1.7 in favor of the control group (yet the TNN group had higher baseline values, and after six months a higher absolute score than the control group). Both differences were not statistically significant, nor clinically relevant.
3.2. Sleep quality
No studies reported on sleep quality after surgical interventions.
Level of evidence of the literature
1. Effects on spasticity symptoms
The level of evidence regarding the outcome measure spasticity started at High since it was based on RCT data. It was downgraded by 4 levels to Very Low, due to study limitations: overfitting of the data, insufficient blinding and inadequate reporting of rehabilitation adherence (risk of bias -2); low number of included patients and studies and inclusion of non-adult patients (imprecision -2).
No studies were found reporting on pain; therefore this outcome measure was not graded.
2. Effects on skills and abilities
2.1. Ambulation
The level of evidence regarding the outcome measure gait speed started as High since it was based on RCT data and was downgraded by 3 levels to Very Low because of study limitations (risk of bias, -1); low number of included patients and inclusion of non-adult patients (imprecision, -2).
No studies were found reporting on stability, therefore this outcome measure was not graded.
2.2. Limb function
The level of evidence regarding limb function started as High since it was based on RCT data and was downgraded by 3 levels to Very Low because of study limitations (risk of bias due, -1); low number of included patients and studies and inclusion of non-adult patients (imprecision, -2).
3. Quality of life
The level of evidence regarding the outcome measure quality of life started as High since it was based on RCT data and was downgraded by 4 levels to Very Low because of study limitations (risk of bias due to lack of blinding, baseline differences between groups and large percentage of missing data) (-2); imprecision due to the confidence interval crossing the borders of clinical relevance and only one available study with a small number of participants (-2).
No studies were found reporting on sleep quality; therefore this outcome measure was not graded.
A systematic review of the literature was performed to answer the following question:
What is the effectiveness of surgery compared to a non-surgical intervention or no treatment in adults with cerebral spasticity?
| P: | Adults with cerebral spasticity as a consequence of cerebrovascular accident (CVA) or cerebral palsy (CP) |
| I: | Surgery on the extremities |
| C: | No intervention or a non-surgical intervention |
| O: |
Quality of life, spasticity / muscle tone; For functional extremities: measures of arm or leg function, gait pattern, gait speed, functioning / basic ADL; For non-functional extremities: functioning / basic ADL, pain, sleep quality, posture, stability |
Relevant outcome measures
The guideline development group considered quality of life and spasticity as critical outcome measures for decision making; and gait pattern, gait speed, functioning (skills/abilities), pain, sleep quality and stability as important outcome measures for decision making.
The working group defined the outcome measures as shown in Table 1.
Table 1. Definitions and minimally clinical important differences for assessed outcome measures
|
Outcome units |
Outcome measures |
Definition |
Minimal clinically important difference |
|
Effects on body functions and structures (ICF-impairments) |
Muscle tone/ spasticity |
measured with the (modified) Ashworth scale (AS) or (modified) Tardieu scale (TS) |
1 point on the (m)AS, PSFS or (m)TS |
|
Cramps and pain |
measured with Visual Analog Scale, or Numeric (Pain) Rating Scale |
1.65 point difference (scale 0 to 10) or 16.55 (scale 0 to 100) (Bahreini, 2020) |
|
|
Effects on skills and abilities (ICF-activities) |
Arm function |
Measured with Action Research Arm Test (ARAT) or 9HPT (9-hole peg test) |
5.7 points on the ARAT (Lang, 2008) and 20% in test score for the 9HPT (Feys, 2017) |
|
Gait pattern and gait speed (walking) |
measured with 10-meter walking test (10MWT), 6-min WT, |
0.1 m/s gait speed difference for 10-meter WT; 54 meter difference for 6MWT (Wise, 2005) |
|
|
Standing, posture and balance |
Berg Balance Scale (or other) |
6 points on Berg Balance Scale |
|
|
Activities of Daily Living (ADL) |
for example using Barthel Index, including social functioning |
Barthel Index: 1.85 points (scale 0-20) (Hsieh, 2007) |
|
|
Quality of life |
Overall quality of life |
For example SF-36, EQ-5D
|
25% difference for dichotomous outcomes (0.8 ≥ RR ≥ 1.25), and 0.5 SD or -0.5 > SMD > 0.5 for continuous outcomes |
|
Sleep quality |
|
Search and select (Methods)
An earlier search was performed to answer a similar question in the previous guideline. The search strategy from that guideline did not result in relevant literature (search strategy available upon request).
To update the guideline, the databases Medline (via OVID) and Embase (via Embase.com) were searched with relevant search terms from 1995 until July 7, 2023. The detailed search strategy is available upon request. The systematic literature search resulted in 597 hits. Studies were selected based on the following criteria:
- Observational studies, randomized controlled trials, systematic review and/or meta-analysis.
- Studies on adults with cerebral spasticity as a consequence of CVA or CP.
- Studies describing (a type of) surgery on the extremities as intervention.
- Studies describing no intervention or a non-surgical intervention as control.
- Studies described at least one of the outcome measures as described in the PICO.
Twenty-six studies were initially selected based on title and abstract screening. After reading the full text, 24 studies were excluded (see the table with reasons for exclusion under the tab Methods), and two studies were included.
Results
Two studies were included in the analysis of the literature. Important study characteristics and results are summarized in the evidence tables. The assessment of the risk of bias is summarized in the risk of bias tables.
- Berger A, Salhi S, Payares-Lizano M. Surgical Management of Spasticity of the Elbow. Hand Clin. 2018 Nov;34(4):503-510. doi: 10.1016/j.hcl.2018.06.007. Epub 2018 Aug 20. PMID: 30286964.
- Bollens B, Gustin T, Stoquart G, Detrembleur C, Lejeune T, Deltombe T. A randomized controlled trial of selective neurotomy versus botulinum toxin for spastic equinovarus foot after stroke. Neurorehabil Neural Repair. 2013 Oct;27(8):695-703. doi: 10.1177/1545968313491002. Epub 2013 Jun 10. PMID: 23757297.
- Duquette SP, Adkinson JM. Surgical Management of Spasticity of the Forearm and Wrist. Hand Clin. 2018 Nov;34(4):487-502. doi: 10.1016/j.hcl.2018.06.006. PMID: 30286963.
- Fahrenkopf MP, Rhee PC. Surgical Management of Spastic Shoulder Deformities in Adult Patients. J Hand Surg Am. 2022 Sep;47(9):906.e1-906.e9. doi: 10.1016/j.jhsa.2022.03.023. Epub 2022 Jun 3. PMID: 35660337.
- Leclercq C, Perruisseau-Carrier A, Gras M, Panciera P, Fulchignoni C, Fulchignoni M. Hyperselective neurectomy for the treatment of upper limb spasticity in adults and children: a prospective study. J Hand Surg Eur Vol. 2021 Sep;46(7):708-716. doi: 10.1177/17531934211027499. Epub 2021 Jul 13. PMID: 34256619.Waljee JF, Chung KC. Surgical Management of Spasticity of the Thumb and Fingers. Hand Clin. 2018 Nov;34(4):473-485. doi: 10.1016/j.hcl.2018.06.005. PMID: 30286962.
- Nonnekes J, Benda N, van Duijnhoven H, Lem F, Keijsers N, Louwerens JWK, Pieterse A, Renzenbrink B, Weerdesteyn V, Buurke J, Geurts ACH. Management of Gait Impairments in Chronic Unilateral Upper Motor Neuron Lesions: A Review. JAMA Neurol. 2018 Jun 1;75(6):751-758. doi: 10.1001/jamaneurol.2017.5041. PMID: 29482203.
- Tenniglo MJB, Buurke JH, Zeegers AVCM, Fleuren JFM, Rietman JS, Prinsen EC. The effect of rectus femoris transfer om kinematics and functional outcomes in adult stroke patients walking with stiff knee gait. Gait & pasture 114 (2024) 101-107.
- Zheng MX, Hua XY, Feng JT, Li T, Lu YC, Shen YD, Cao XH, Zhao NQ, Lyu JY, Xu JG, Gu YD, Xu WD. Trial of Contralateral Seventh Cervical Nerve Transfer for Spastic Arm Paralysis. N Engl J Med. 2018 Jan 4;378(1):22-34. doi: 10.1056/NEJMoa1615208. Epub 2017 Dec 20. PMID: 29262271.
Evidence table for intervention studies
|
Study reference |
Study characteristic |
Patient characteristics 2 |
Intervention (I) |
Control (C) |
Follow-up |
Outcome measures and effect size |
Comments |
|
Bollens, 2013 |
Type of study: RCT
Setting and country: Two Belgian university hospitals July 2008- Jan 2011
Funding and conflicts of interest: Grants from the Belgian National Fund for Scientific Research (FNRS) and Horlait-Dapsen Fund |
Inclusion criteria: (1) Stroke patients presenting with SEF due to overactivity of calf muscles, (2) spastic hemiparesis >6 months after stroke, (3) improvement of foot positioning after selective nerve block, (4) lack of associated contracture (dorsal flexion >0, (5) ability to walk on a treadmill ~2 min Exclusion criteria: (1) previous history of local surgery, (2) phenol denervation or BTX injection <6 months, (3) pathology interfering with gait
N total at baseline: Intervention: 8 | Control: 8
Important prognostic factors2: mean age (range): I: 49.9 (32.1-70.2) C: 52.3 (35.7-65.2)
N Male/Female: C: 3/5 | C: 4/4
Stroke type Ischemic/Hemorragic I: 6/2 | C: 7/1 Left/Right Stroke I:6/2 | C: 4/4
SIAS I: 42.5 (23-64) | C: 50 (35-64)
Walking speed (m/s) I: 0.55±0.39 | C: 0.62± 0.41 |
selective diagnostic nerve block determined muscles to treat before randomization
- Selective tibial neurotomy performed by one neurosurgeon - soleus nerve in all cases (mean section ~ 2/3), tibialis posterior (mean section ~ 1/2) and flexor hallucis longus (100% section) nerves in 5 cases
|
selective diagnostic nerve block determined muscles to treat before randomization
- Injection of BTX under electrical stimulation guidance by one physician - Soleus muscle was injected in all patients, tibialis posterior and hallucis longus in 4 patients. |
Length of follow-up: 2 months and 6 months
Loss-to-follow-up: None reported
Incomplete outcome data: Questionnaires (ABILOCO, SATISPART & SF-36) not administered in pt with MMSE<24. missing I: n = 1 | C: n=3 |
Outcome measures and effect size – median(interquartile range):
Muscle tone/spasticity MAS (0-4) after 6 months Triceps surae I: 2(1.5/2) | C: 2.5(1/3.5) Soleus I: 0(0/1) I C: 2(0.5/2)
Impairment SIAS improvement 0-2 months I: 3(2/4.5) | C: 1.5 (−0.5/2.5), p=0 .028 SIAS improvement 0-6 months I: 3 (2/4) | C: 0 (0/1.5), p=0.003
QOL - SF-36, Physical health at 6 months I: 38.1±5.12 | C: 33.7±11.6
- SF-36 Mental health at 6 months* I: 43.8±9.6 C:37.2±12.5
Walking Gait speed at 6 months: I: 0.59±0.35 | C: 0.64±0.39*
FAC at 6 months: I: 4±n.r. | C: 4±n.r.
FWC at 6 months I: 5±n.r. | C: 5±n.r. |
Very small n, two measures of spasticity: overfitting.
* Difference in baseline |
|
Type of study RCT
Setting and country: Hospital, Shanghai China,
Funding and conflicts of interest: Grants from the national natural science foundation of China, science and technology commission of shanghai, health and family planning commission of Shanghai, Shanghai Shen-Kang hospital development centre
No other author reported conflicts
|
Inclusion criteria: (1) hemiplegia after stroke or traumatic brain injury or cerebral palsy manifesting mainly as spasticity and weakness in the upper extremity contralateral to the cerebral lesion, (2) age 12 to 45, (3) no improvement in paresis in last 5 years, (4) muscle power & tactile sensitivity in affected hand decreased but not absent, (4) TMS results in activation from contralesional hemisphere and exclusive activation of the paralyzed hand by ipsilesional hemisphere
Exclusion criteria (1) systemic diseases, (2) poor cognitive ability, (3) fixed contracture or joint deformity of the paralyzed arm
N total at baseline: Intervention: 18 | Control: 18
Important prognostic factors: %male: I: 100% | C: 100%
Age (years) I: 27±9 | C: 26±8
Side of paralysis: (n left (%)) I: 10(56), C: 10(56)
Cause of injury (n (%)): - Stroke I: 5 (28) | C: 4 (22) - TBI I: 6 (33) | C 6 (33) - CP I: 5 (28) | C: 8 (44) - Encephalitis I: 2 (11) | C: 0 (0)
TSI (years) I: 15 ± 9 | C: 15 ± 8
Fugl-Meyer I: 29.0 ± 3.0 | C: 29.1 ± 3.5 |
Contralateral C7 nerve-transfer surgery followed by rehabilitation
1. Zheng 2008
Rehabilitation similar to control group aside from an immobilizing cast during posoperatieve period. |
Rehabilitation only
Rehabilitation: 4 times a week, 12 months, physiotherapy. Active exercise, passive range of motion, occupational therapy, functional training, physical therapy, acupuncture, massage and orthoses. |
Follow up baseline, 2, 4, 6,8,10 and 12 months after recruitment
Loss-to-follow-up:
Incomplete outcome data:
|
Fugl-Meyer upper extremity (0-66, higher score is better function) Change from baseline to month 12 I: 17.7±5.6 | C: 2.6±2.0 MD(range) 15.1 (12.2 -17.9)
MAS (0-5, higher is more spasticity) Mean±SD at month 12 Elbow I: 0.8±0.5 | C: 1.5±0.6 Forearm I: 1.8±0.6 |C: 2.4±0.6 Wrist I: 1.4±0.6 | C: 2.4 ±0.6 Thumb I: 1.2±0.6 | C: 1.9±0.8 Digits 2-5 I: 0.8±0.5 | C: 1.6±0.7
ADL Ability to accomplish ≥3 out of 4 functional tasks I: 16 (88.9%) | C: 0
|
|
SEF - spastic equinovarus of the foot; I – Intervention; C – Control; QOL – quality of life; MAS – Modified Ashworth Scale; SIAS -Stroke Impairment Assessment Set; ADL-Activities of Daily Living
Risk of bias table for intervention studies
|
Study reference |
Was the allocation sequence adequately generated? |
Was the allocation adequately concealed? |
Blinding:
|
Was loss to follow-up (missing outcome data) infrequent? |
Are reports of the study free of selective outcome reporting? |
Was the study apparently free of other problems that could put it at a risk of bias? |
Overall risk of bias If applicable/necessary, per outcome measure
|
|
Bollens, 2013 |
Definitely yes
Reason: Authors used constrained balance randomization. |
Probably no
Reason: No information is provided. |
probably no
Reason: Open-label trial (patients and health care providers not blinded). However, data collectors were blinded (blinding of outcome assessors and data analysts not reported. |
Probably yes
Reason: No missing follow-up data is reported
QOL and locomotion measures not available for all participants. “Questionnaires were not presented to patients showing a major cognitive dysfunction as observed with the Mini-Mental State Examination (MMSE ≤ 24),30 which concerned 1 patient in the TNN group and 3 patients in the BTX group.” |
Probably yes
Reason: All outcome measures mentioned in the methods section are reported. Spasticity is measured using two outcome measures for one muscle group.
|
Probably no
Reason: Overfitting of the data (many outcome measures, many comparisons for only 8 pt per group)
Mental health: large difference between groups at the start. Locomotion: large difference between groups for ABILOCO and SATISPART (both higher in TNN group). |
Quality of life HIGH Reason: Baseline difference between groups, large% of missing data. Patient reported and patients were not blinded.
Walking speed Some concerns
Reason: Patients were not blinded and could determine speed
Spasticity (MAS) Some concerns
Reason: Data collectors were blinded. All assessments performed by the same person. However patients were not blinded and very small n per arm |
|
Zheng, 2018 |
Definitely yes
Reason: 1:1 ratio simple, nonstratified randomization. Computer generated |
Probably yes
Reason: Assignment by an independent statistician. Not known to trial personnel until assignment |
Probably no
Reason: Physiotherapist in rehabilitation were aware of treatments. Patients were aware. Data outcome assessors were blinded
Unclear if data-collectors/outcome assessors/ data analysts were blinded. |
Definitely yes
Reason: No loss to follow-up |
Definitely yes
Reason: All outcome parameters are reported (or included in supplementary material) |
Probably no
Reason: Overfitting in secondary analysis and adherence to rehabilitation treatment not reported. |
Spasticity Some concerns
Function Some concerns
Overall reason: Adherence to rehabilitation treatment not reported. Unclear blinding |
Table of excluded studies
|
Reference |
Reason for exclusion |
|
Allart E, Rogeau C, Grauwin MY, Nachef N, Lannes X, Rousseaux M, Thevenon A, Fontaine C. Treatment of dystonia in extensor hallucis longus and digitorum muscles with neurotomy of the branches of the deep fibular nerve: Preliminary results. Orthop Traumatol Surg Res. 2015 May;101(3):341-4. doi: 10.1016/j.otsr.2015.01.006. Epub 2015 Mar 25. PMID: 25819290. |
Dystonia was not part of PICO |
|
Bamal R, Sultan R, Cappuyns L, Hassan Z, McArthur P. Use of volar distal radius plate dorsally for wrist arthrodesis in patients with upper limb spasticity: A retrospective review. J Plast Reconstr Aesthet Surg. 2023 Aug;83:318-325. doi: 10.1016/j.bjps.2023.05.005. Epub 2023 May 7. PMID: 37295156. |
Mixed etiology of spasticity |
|
de Morais Filho MC, Blumetti FC, Kawamura CM, Ferreira CL Júnior, Lopes JAF, Fujino MH, Neves DL. The effect of the Majestro-Frost procedure on internal hip rotation during gait in patients with cerebral palsy. Gait Posture. 2018 Oct;66:32-37. doi: 10.1016/j.gaitpost.2018.08.014. Epub 2018 Aug 18. PMID: 30142452. |
Not adults at time of surgery |
|
Deltombe T, Gilliaux M, Peret F, Leeuwerck M, Wautier D, Hanson P, Gustin T. Effect of the neuro-orthopedic surgery for spastic equinovarus foot after stroke: a prospective longitudinal study based on a goal-centered approach. Eur J Phys Rehabil Med. 2018 Dec;54(6):853-859. doi: 10.23736/S1973-9087.18.04993-6. Epub 2018 Jun 14. PMID: 29904043. |
pre-post design |
|
Hashemi M, Sturbois-Nachef N, Keenan MA, Winston P. Surgical Approaches to Upper Limb Spasticity in Adult Patients: A Literature Review. Front Rehabil Sci. 2021 Aug 31;2:709969. doi: 10.3389/fresc.2021.709969. PMID: 36188802; PMCID: PMC9397894. |
Review whithout meta-analysis |
|
Hosalkar H, Babatunde O, Goebel J, Rendon N, Bashyal R, Keenan M. Outcomes of musculoskeletal surgeries in adult patients with cerebral palsy. Cur Orth Pract. 2010 Jan; doi: 10.1097/BCO.0b013e3181b8b8a7. |
Spasticity is not an inclusion criteria. |
|
Kakodkar P, Girgis H, Nabhan P, Chee SS, Tu A. Efficacy of Selective Dorsal Rhizotomy and Intrathecal Baclofen Pump in the Management of Spasticity. Adv Tech Stand Neurosurg. 2022;45:379-403. doi: 10.1007/978-3-030-99166-1_13. PMID: 35976458. |
Review of insufficient quality |
|
LaMarca AL, Krenn MJ, Kelso-Trass MA, MacDonald KC, Demeo CC, Bazarek SF, Brown JM. Selective Tibial Neurotomy Outcomes for Spastic Equinovarus Foot: Patient Expectations and Functional Assessment. Neurosurgery. 2023 Nov 1;93(5):1026-1035. doi: 10.1227/neu.0000000000002530. Epub 2023 May 18. PMID: 37199494. |
Population not following PICO, primary aim to describe patient motivation to undergo procedure
|
|
Le Bocq C, Rousseaux M, Buisset N, Daveluy W, Blond S, Allart E. Effects of tibial nerve neurotomy on posture and gait in stroke patients: A focus on patient-perceived benefits in daily life. J Neurol Sci. 2016 Jul 15;366:158-163. doi: 10.1016/j.jns.2016.04.055. Epub 2016 May 7. PMID: 27288797. |
pre-post design |
|
Namdari S, Park MJ, Baldwin K, Hosalkar HS, Keenan MA. Effect of age, sex, and timing on correction of spastic equinovarus following cerebrovascular accident. Foot Ankle Int. 2009 Oct;30(10):923-7. doi: 10.3113/FAI.2009.0923. PMID: 19796584. |
Wrong study desing: predicitve model |
|
Ng BKW, Chau WW, Hung ALH, Lam TP, Cheng JCY. Soft tissue release and osteotomies in the treatment of patients with spastic diplegic cerebral palsy. Journal of Orthopaedics, Trauma. 2018. Doi: 10.1016/j.jotr.2017.12.004 |
Not adults at time of surgery |
|
Ozkan T, Bicer A, Aydin HU, Tuncer S, Aydin A, Hosbay ZY. Brachialis muscle transfer to the forearm for the treatment of deformities in spastic cerebral palsy. J Hand Surg Eur Vol. 2013 Jan;38(1):14-21. doi: 10.1177/1753193412444400. Epub 2012 Apr 23. PMID: 22526513. |
Not adults at time of surgery |
|
Paul SM, Siegel KL, Malley J, Jaeger RJ. Evaluating interventions to improve gait in cerebral palsy: a meta-analysis of spatiotemporal measures. Dev Med Child Neurol. 2007 Jul;49(7):542-9. doi: 10.1111/j.1469-8749.2007.00542.x. PMID: 17593129. |
No description of population of included studies. No subanalysis for surgical procedures |
|
Putz C, Mertens EM, Wolf SI, Geisbüsch A, Niklasch M, Gantz S, Döderlein L, Dreher T, Klotz MC. Equinus Correction During Multilevel Surgery in Adults With Cerebral Palsy. Foot Ankle Int. 2018 Jul;39(7):812-820. doi: 10.1177/1071100718765161. Epub 2018 Apr 2. PMID: 29606023. |
pre-post design |
|
Putz C, Wolf SI, Mertens EM, Geisbüsch A, Gantz S, Braatz F, Döderlein L, Dreher T. Effects of multilevel surgery on a flexed knee gait in adults with cerebral palsy. Bone Joint J. 2017 Sep;99-B(9):1256-1264. doi: 10.1302/0301-620X.99B9.BJJ-2016-1155.R1. PMID: 28860409. |
Spasticity is not an inclusion criterium nor is it an outcome measure
|
|
Reynolds MR, Ray WZ, Strom RG, Blackburn SL, Lee A, Park TS. Clinical outcomes after selective dorsal rhizotomy in an adult population. World Neurosurg. 2011 Jan;75(1):138-44. doi: 10.1016/j.wneu.2010.09.010. PMID: 21492678. |
pre-post design |
|
Rousseaux M, Buisset N, Daveluy W, Kozlowski O, Blond S. Comparison of botulinum toxin injection and neurotomy in patients with distal lower limb spasticity. Eur J Neurol. 2008 May;15(5):506-11. doi: 10.1111/j.1468-1331.2008.02112.x. Epub 2008 Mar 5. PMID: 18325022. |
Cohort similar to Rousseaux (2009). Selection bias – only responders included.
|
|
Rousseaux M, Buisset N, Daveluy W, Kozlowski O, Blond S. Long-term effect of tibial nerve neurotomy in stroke patients with lower limb spasticity. J Neurol Sci. 2009 Mar 15;278(1-2):71-6. doi: 10.1016/j.jns.2008.11.024. Epub 2008 Dec 23. PMID: 19106001. |
pre-post design |
|
Salame K, Ouaknine GE, Rochkind S, Constantini S, Razon N. Surgical treatment of spasticity by selective posterior rhizotomy: 30 years experience. Isr Med Assoc J. 2003 Aug;5(8):543-6. PMID: 12929289. |
Different aetiology of spasticity (and when CP, not adults)
|
|
Sitthinamsuwan B, Phonwijit L, Khampalikit I, Nitising A, Nunta-Aree S, Suksompong S. Comparison of efficacy between dorsal root entry zone lesioning and selective dorsal rhizotomy for spasticity of cerebral origin. Acta Neurochir (Wien). 2017 Dec;159(12):2421-2430. doi: 10.1007/s00701-017-3322-x. Epub 2017 Sep 17. PMID: 28920167. |
adults and children, mixed eatiology. No subanalyses possible in small group
|
|
Sung KH, Lee J, Chung CY, Lee KM, Cho BC, Moon SJ, Kim J, Park MS. Factors influencing outcomes after medial hamstring lengthening with semitendinosus transfer in patients with cerebral palsy. J Neuroeng Rehabil. 2017 Aug 14;14(1):83. doi: 10.1186/s12984-017-0296-0. PMID: 28806980; PMCID: PMC5556982. |
Not adults at time of surgery
|
|
Van Heest AE, House JH, Cariello C. Upper extremity surgical treatment of cerebral palsy. J Hand Surg Am. 1999 Mar;24(2):323-30. doi: 10.1053/jhsu.1999.0323. PMID: 10194018. |
Not all adults at time of surgery - no subanalysis for age
|
|
Wangdell J, Fridén J. Rehabilitation After Spasticity-Correcting Upper Limb Surgery in Tetraplegia. Arch Phys Med Rehabil. 2016 Jun;97(6 Suppl):S136-43. doi: 10.1016/j.apmr.2016.01.033. PMID: 27233588. |
wrong population: SCI, pre-post design
|
|
Yu UB, Progress in surgical treatment for cerebral palsy. Chinese Journal of Clinical Rehabilitation. 2005 |
Article in Chinese |
Beoordelingsdatum en geldigheid
Publicatiedatum : 06-01-2026
Beoordeeld op geldigheid : 06-01-2026
Samenstelling werkgroep
Voor het ontwikkelen van de richtlijnmodule is in 2023 een multidisciplinaire werkgroep ingesteld, bestaande uit vertegenwoordigers van alle relevante specialismen (zie hiervoor de Samenstelling van de werkgroep) die betrokken zijn bij de zorg voor patiënten met Cerebrale en/of spinale spasticiteit.
Werkgroep
- prof. dr. A.C.H. Geurts (voorzitter), hoogleraar neurorevalidatie, Radboud UMC en Sint Maartenskliniek, namens de Nederlandse Vereniging voor Revalidatieartsen
- drs. A.M.V. Dommisse, revalidatiearts, Isala Klinieken Zwolle, namens de Nederlandse Vereniging voor Revalidatieartsen
- drs. P.J. van Dongen, patiëntvertegenwoordiger bij Hersenletsel.nl
- Dr. M. van Eijk, specialist ouderengeneeskunde, Marnix Medisch B.V., namens Verenso
- dr. J.F.M. Fleuren, revalidatiearts, Jeroen Bosch Ziekenhuis / Tolbrug, ‘s Hertogenbosch, namens de Nederlandse Vereniging voor Revalidatieartsen
- F. van Gorp-Swart, MSc, ziekenhuisapotheker, Diakonessenhuis, Utrecht/Zeist/Doorn, namens de Nederlandse Vereniging voor Ziekenhuisapothekers
- prof. dr. G. Kwakkel, hoogleraar neurorevalidatie, Amsterdam UMC, Amsterdam, namens het Koninklijk Nederlands Genootschap voor Fysiotherapie
- drs. E. Kurt, neurochirurg, Radboud UMC en Canisius Wilhelmina Ziekenhuis, Nijmegen, namens de Nederlandse Vereniging voor Neurochirurgie
- Prof. dr. C.G.M. Meskers, hoogleraar revalidatiegeneeskunde, Amsterdam UMC, Amsterdam, namens de Nederlandse Vereniging voor Revalidatieartsen
- dr. H.A. Moser, anesthesioloog, Radboud UMC, Nijmegen en Care4homecare, Bladel, namens de Nederlandse Vereniging voor Anesthesiologie
- drs. W.P. Polomski, revalidatiearts (gepensioneerd), voorheen in Spaarne Gasthuis, Hoofddorp, namens de Nederlandse Vereniging voor Revalidatieartsen
- drs. M.N. Ruissen-Eversdijk, ergotherapeut en bewegingswetenschapper, Reade, Amsterdam, namens Ergotherapie Nederland
- dr. A.V.C.M. Zeegers, orthopedisch chirurg, Medisch Spectrum Twente, Enschede, namens de Nederlandse Orthopaedische Vereniging
- dr. J.M. Zuidam, plastisch chirurg, Erasmus MC, namens de Nederlandse Vereniging voor Plastische Chirurgie
Klankbordgroep
- P.M. van Lamoen, gepensioneerd, namens Dwarslaesieorganisatie Nederland
- M. Pol, Dwarslaesie Organisatie Nederland, tot september 2024*
- Dr. A.E. Tigchelaar, Dwarslaesie Organisatie Nederland, vanaf september 2024
- Dr. W.J. Kruithof, revalidatiearts, Universitair Medisch Centrum Utrecht
- Dr. I.H. Zaal-Schuller, arts verstandelijk gehandicapten/kaderarts palliatieve zorg
*Overleden
Met ondersteuning van
- Dr. M.L. Molag, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
- Dr. M.M.J. van Rooijen, adviseur, Kennisinstituut van de Federatie Medisch Specialisten
Belangenverklaringen
De Code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten via secretariaat@kennisinstituut.nl.
|
Werkgroeplid |
Functie |
Nevenfuncties |
Gemelde belangen |
Ondernomen actie |
|
Geurts (voorzitter) |
Hoogleraar neurorevalidatie, Radboud UMC, Nijmegen en Sint Maartenskliniek |
|
Geen. |
Geen restricties. |
|
Dommisse |
Revalidatiearts, Vogellanden |
Geen |
Speakerfee bij Ipsen farmaceutica voor:
|
Geen restricties; e-learning en presentaties betreffen de volle breedte van de behandel opties |
|
van Dongen |
Patiëntvertegenwoordiger Hersenletsel.nl |
Deelname andere werkgroepen |
Geen |
Geen restricties. |
|
van Eijk |
Specialist Ouderengeneeskunde, Marnix Medisch B.V |
|
Extern gefinancierd onderzoek over heupfracturen: 1. FITHIP; onderzoek naar valangst bij patienten met heupfractuur 2. GR HIP; onderzoek naar herstel na heupfractuur 3. HIPCARE; onderzoek naar herstel en biomarkers bij heupfractuur |
Geen restricties; De webinars waren gericht op samenwerking specialisten ouderengeneeskunde en revalidatieartsen |
|
Fleuren |
Revalidatiearts, Tolbrug |
Bestuurslid VRA (onbetaald) |
Geen. |
Geen restricties. |
|
van Gorp |
Ziekenhuisapotheker |
Lid werkgroep interacties KNMP |
Geen. |
Geen restricties. |
|
Kwakkel |
Hoogleraar neurorevalidatie, Amsterdam UMC, locatie VUMC |
|
Geen |
Geen restricties. |
|
Kurt |
Neurochirurg, Radboud UMC, Nijmegen |
Geen |
Geen |
Geen restricties. |
|
Meskers |
Revalidatiearts, Amsterdam UMC locatie VUMC |
Geen |
Geen. |
Geen restricties. |
|
Moser |
Anesthesioloog, Radboud UMC, Nijmegen en Care4homecare, Bladel |
Geen |
Geen |
Geen restricties. |
|
Polomski |
Revalidatiearts Spaarne Gasthuis (gepensioneerd vanaf 1 mei 2023). |
Geen |
Lid Adviesraad Merz Benelux, raakt niet aan de modules |
Restrictie ten aanzien van besluitvorming met betrekking tot botulinetoxine |
|
Ruissen-Eversdijk |
Ergotherapeut bij Reade Revalidatie. |
Geen. |
Geen. |
Geen restricties. |
|
Zeegers |
Orthopedisch chirurg, Medisch Spectrum Twente, Enschede (tot 1-6-2025), en UMCG (vanaf 1-6-2025) |
|
Geen. |
Geen restricties. |
|
Zuidam |
Plastisch chirurg, Erasmus MC Rotterdam |
Geen. |
Geen. |
Geen restricties. |
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door uitnodigen van Hersenletsel.nl en Dwarslaesie Organisatie Nederland (DON) bij de schriftelijke knelpuntenanalyse. DON heeft een enquête bij hun achterban uitgezet, en knelpunten werden meegenomen in het proces. Het verslag van deze enquête is besproken in de werkgroep. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. In de werkgroep heeft een vertegenwoordiger van Hersenletsel.nl deelgenomen. De conceptrichtlijn is tevens voor commentaar voorgelegd aan Hersenletsel.nl, DON, MS Nederland en Spierziekten Nederland.
Kwalitatieve raming van mogelijke financiële gevolgen in het kader van de Wkkgz
Bij de richtlijnmodule is conform de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd om te beoordelen of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling is de richtlijnmodule op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase). Uit deze kwalitatieve raming bleek dat er geen grote financiële gevolgen te verwachten zijn.
|
Module |
Uitkomst raming |
Toelichting |
|
Chirurgische behandelingen aan de bovenste en onderste extremiteit |
geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbevelingen breed toepasbaar zijn (5.000-40.000 patiënten), volgt ook uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft. Er worden daarom geen substantiële financiële gevolgen verwacht. |
Werkwijze
Voor meer details over de gebruikte richtlijnmethodologie verwijzen wij u naar de Werkwijze. Relevante informatie voor de ontwikkeling/herziening van deze richtlijnmodule is hieronder weergegeven.
Zoekverantwoording
|
On the 7th of July 2023, a systematic search was performed in the databases Embase.com and Ovid/Medline for systematic reviews, RCTs and observational studies on surgical procedures for adults with spasticity due to cerebral palsy or post-stroke from 1995 until search date. The search resulted in 597 unique hits. |
Zoekstrategie
Embase.com
|
No. |
Query |
Results |
|
#14 |
#6 NOT (#11 OR #12 OR #13) = overig |
524 |
|
#13 |
#6 AND (#9 OR #10) NOT (#11 OR #12) = observationeel |
321 |
|
#12 |
#6 AND #8 NOT #11 = RCT |
120 |
|
#11 |
#6 AND #7 = SR |
53 |
|
#10 |
'case control study'/de OR 'comparative study'/exp OR 'control group'/de OR 'controlled study'/de OR 'controlled clinical trial'/de OR 'crossover procedure'/de OR 'double blind procedure'/de OR 'phase 2 clinical trial'/de OR 'phase 3 clinical trial'/de OR 'phase 4 clinical trial'/de OR 'pretest posttest design'/de OR 'pretest posttest control group design'/de OR 'quasi experimental study'/de OR 'single blind procedure'/de OR 'triple blind procedure'/de OR (((control OR controlled) NEAR/6 trial):ti,ab,kw) OR (((control OR controlled) NEAR/6 (study OR studies)):ti,ab,kw) OR (((control OR controlled) NEAR/1 active):ti,ab,kw) OR 'open label*':ti,ab,kw OR (((double OR two OR three OR multi OR trial) NEAR/1 (arm OR arms)):ti,ab,kw) OR ((allocat* NEAR/10 (arm OR arms)):ti,ab,kw) OR placebo*:ti,ab,kw OR 'sham-control*':ti,ab,kw OR (((single OR double OR triple OR assessor) NEAR/1 (blind* OR masked)):ti,ab,kw) OR nonrandom*:ti,ab,kw OR 'non-random*':ti,ab,kw OR 'quasi-experiment*':ti,ab,kw OR crossover:ti,ab,kw OR 'cross over':ti,ab,kw OR 'parallel group*':ti,ab,kw OR 'factorial trial':ti,ab,kw OR ((phase NEAR/5 (study OR trial)):ti,ab,kw) OR ((case* NEAR/6 (matched OR control*)):ti,ab,kw) OR ((match* NEAR/6 (pair OR pairs OR cohort* OR control* OR group* OR healthy OR age OR sex OR gender OR patient* OR subject* OR participant*)):ti,ab,kw) OR ((propensity NEAR/6 (scor* OR match*)):ti,ab,kw) OR versus:ti OR vs:ti OR compar*:ti OR ((compar* NEAR/1 study):ti,ab,kw) OR (('major clinical study'/de OR 'clinical study'/de OR 'cohort analysis'/de OR 'observational study'/de OR 'cross-sectional study'/de OR 'multicenter study'/de OR 'correlational study'/de OR 'follow up'/de OR cohort*:ti,ab,kw OR 'follow up':ti,ab,kw OR followup:ti,ab,kw OR longitudinal*:ti,ab,kw OR prospective*:ti,ab,kw OR retrospective*:ti,ab,kw OR observational*:ti,ab,kw OR 'cross sectional*':ti,ab,kw OR cross?ectional*:ti,ab,kw OR multicent*:ti,ab,kw OR 'multi-cent*':ti,ab,kw OR consecutive*:ti,ab,kw) AND (group:ti,ab,kw OR groups:ti,ab,kw OR subgroup*:ti,ab,kw OR versus:ti,ab,kw OR vs:ti,ab,kw OR compar*:ti,ab,kw OR 'odds ratio*':ab OR 'relative odds':ab OR 'risk ratio*':ab OR 'relative risk*':ab OR 'rate ratio':ab OR aor:ab OR arr:ab OR rrr:ab OR ((('or' OR 'rr') NEAR/6 ci):ab))) |
14230870 |
|
#9 |
'major clinical study'/de OR 'clinical study'/de OR 'case control study'/de OR 'family study'/de OR 'longitudinal study'/de OR 'retrospective study'/de OR 'prospective study'/de OR 'comparative study'/de OR 'cohort analysis'/de OR ((cohort NEAR/1 (study OR studies)):ab,ti) OR (('case control' NEAR/1 (study OR studies)):ab,ti) OR (('follow up' NEAR/1 (study OR studies)):ab,ti) OR (observational NEAR/1 (study OR studies)) OR ((epidemiologic NEAR/1 (study OR studies)):ab,ti) OR (('cross sectional' NEAR/1 (study OR studies)):ab,ti) |
7725904 |
|
#8 |
'clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti |
3826186 |
|
#7 |
'meta analysis'/exp OR 'meta analysis (topic)'/exp OR metaanaly*:ti,ab OR 'meta analy*':ti,ab OR metanaly*:ti,ab OR 'systematic review'/de OR 'cochrane database of systematic reviews'/jt OR prisma:ti,ab OR prospero:ti,ab OR (((systemati* OR scoping OR umbrella OR 'structured literature') NEAR/3 (review* OR overview*)):ti,ab) OR ((systemic* NEAR/1 review*):ti,ab) OR (((systemati* OR literature OR database* OR 'data base*') NEAR/10 search*):ti,ab) OR (((structured OR comprehensive* OR systemic*) NEAR/3 search*):ti,ab) OR (((literature NEAR/3 review*):ti,ab) AND (search*:ti,ab OR database*:ti,ab OR 'data base*':ti,ab)) OR (('data extraction':ti,ab OR 'data source*':ti,ab) AND 'study selection':ti,ab) OR ('search strategy':ti,ab AND 'selection criteria':ti,ab) OR ('data source*':ti,ab AND 'data synthesis':ti,ab) OR medline:ab OR pubmed:ab OR embase:ab OR cochrane:ab OR (((critical OR rapid) NEAR/2 (review* OR overview* OR synthes*)):ti) OR ((((critical* OR rapid*) NEAR/3 (review* OR overview* OR synthes*)):ab) AND (search*:ab OR database*:ab OR 'data base*':ab)) OR metasynthes*:ti,ab OR 'meta synthes*':ti,ab |
942266 |
|
#6 |
#5 AND [1995-2023]/py |
1018 |
|
#5 |
#4 NOT ('conference abstract'/it OR 'editorial'/it OR 'letter'/it OR 'note'/it) NOT (('animal'/exp OR 'animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp) NOT (('adolescent'/exp OR 'child'/exp OR adolescent*:ti,ab,kw OR child*:ti,ab,kw OR schoolchild*:ti,ab,kw OR infant*:ti,ab,kw OR girl*:ti,ab,kw OR boy*:ti,ab,kw OR teen:ti,ab,kw OR teens:ti,ab,kw OR teenager*:ti,ab,kw OR youth*:ti,ab,kw OR pediatr*:ti,ab,kw OR paediatr*:ti,ab,kw OR puber*:ti,ab,kw) NOT ('adult'/exp OR 'aged'/exp OR 'middle aged'/exp OR adult*:ti,ab,kw OR man:ti,ab,kw OR men:ti,ab,kw OR woman:ti,ab,kw OR women:ti,ab,kw)) |
1183 |
|
#4 |
#1 AND #2 AND #3 |
3054 |
|
#3 |
'rhizotomy'/exp OR 'radicotom*':ti,ab,kw OR 'radiculotom*':ti,ab,kw OR 'rhizotom*':ti,ab,kw OR 'thermorhizotom*':ti,ab,kw OR 'neurotomy'/exp OR 'neurotom*':ti,ab,kw OR denervation*:ti,ab,kw OR 'neurectomy'/exp OR (((nerve* OR neuron*) NEAR/3 (transection OR transsection OR excision* OR exeresis OR removal OR resection OR dissection)):ti,ab,kw) OR 'neurectom*':ti,ab,kw OR 'neuronectom*':ti,ab,kw OR aponeurectom*:ti,ab,kw OR 'tenotomy'/exp OR 'tendotom*':ti,ab,kw OR 'tenontom*':ti,ab,kw OR 'tenotom*':ti,ab,kw OR (((musc* OR tendon OR hamstring* OR quadricep* OR 'heel cord') NEAR/3 (lengthen* OR elongation OR surg* OR microsurg* OR releas*)):ti,ab,kw) OR ('muscle length'/exp AND 'surgery'/exp) OR 'orthopedic surgery'/de OR 'orthopedic surg*':ti,ab,kw OR 'fasciotomy'/exp OR 'fasciotom*':ti,ab,kw OR 'arthrodesis'/exp OR 'arthrodes*':ti,ab,kw OR 'artificial ankylosis':ti,ab,kw OR 'joint fusion*':ti,ab,kw OR 'fusion'/exp OR fusion*:ti,ab,kw OR 'nerve transplantation'/exp OR 'tendon transfer'/exp OR neurotization*:ti,ab,kw OR (((tendon OR nerve* OR 'motor branch*') NEAR/3 (transfer* OR graft* OR transplant* OR allotransplant* OR crossover*)):ti,ab,kw) |
493310 |
|
#2 |
'cerebral palsy'/exp OR (((cerebral* OR brain OR central) NEAR/3 (pares* OR pals* OR paralys*)):ti,ab,kw) OR 'little disease*':ti,ab,kw OR 'diplegia spastic*':ti,ab,kw OR 'spastic diplegi*':ti,ab,kw OR 'intractable spastic*':ti,ab,kw OR 'spinal cord injury'/exp OR 'spine injury'/exp OR (((spinal OR spine) NEAR/2 (injur* OR trauma*)):ti,ab,kw) OR 'cerebrovascular accident'/exp OR 'brain hemorrhage'/exp OR 'brain infarction'/exp OR 'intracranial aneurysm'/exp OR 'stroke patient'/exp OR 'stroke unit'/exp OR cva:ti,ab,kw OR cvas:ti,ab,kw OR stroke:ti,ab,kw OR poststroke:ti,ab,kw OR (((cerebrovascular OR 'cerebro vascular' OR cerebral OR intracerebral OR cerebellum OR brain OR 'corpus callosum' OR intracranial OR intraventricular OR periventricular OR subarachnoid) NEAR/3 (accident* OR attack* OR infarct* OR insult* OR event* OR bleed* OR microbleed* OR aneurysm* OR hemorrhage* OR haemorrhage* OR microhemorrhage* OR microhaemorrhage* OR ischemi* OR ischaemi* OR haematoma* OR hematoma* OR thrombo* OR emboli* OR occlus*)):ti,ab,kw) OR apoplex*:ti,ab,kw OR encephalorrhagia:ti,ab,kw |
1110321 |
|
#1 |
'spasticity'/exp OR 'muscle hypertonia'/de OR 'muscle rigidity'/de OR 'spastic paraplegia'/exp OR 'spastic paresis'/exp OR 'muscle spasm'/de OR 'muscle tone'/de OR 'dystonia'/exp OR spastic*:ti,ab,kw OR spasm*:ti,ab,kw OR 'high tone':ti,ab,kw OR hypertonia:ti,ab,kw OR hypertonus:ti,ab,kw OR hypertonicity:ti,ab,kw OR hypermyoton*:ti,ab,kw OR dyston*:ti,ab,kw OR myodyston*:ti,ab,kw OR (((muscle* OR muscular) NEAR/3 (rigid* OR tone OR tonus OR overactiv* OR 'over activ*' OR paretic)):ti,ab,kw) OR (((motor OR movement OR gait OR walk*) NEAR/3 (disabilit* OR disfunction* OR dysfunction* OR disorder* OR impair* OR compromises OR compromised)):ti,ab,kw) |
271014 |
Ovid/Medline
|
# |
Searches |
Results |
|
14 |
6 not (11 or 12 or 13) = overig |
323 |
|
13 |
(6 and (9 or 10)) not (11 or 12) = observationeel |
215 |
|
12 |
(6 and 8) not 11 = RCT |
59 |
|
11 |
6 and 7 = SR |
26 |
|
10 |
Case-control Studies/ or clinical trial, phase ii/ or clinical trial, phase iii/ or clinical trial, phase iv/ or comparative study/ or control groups/ or controlled before-after studies/ or controlled clinical trial/ or double-blind method/ or historically controlled study/ or matched-pair analysis/ or single-blind method/ or (((control or controlled) adj6 (study or studies or trial)) or (compar* adj (study or studies)) or ((control or controlled) adj1 active) or "open label*" or ((double or two or three or multi or trial) adj (arm or arms)) or (allocat* adj10 (arm or arms)) or placebo* or "sham-control*" or ((single or double or triple or assessor) adj1 (blind* or masked)) or nonrandom* or "non-random*" or "quasi-experiment*" or "parallel group*" or "factorial trial" or "pretest posttest" or (phase adj5 (study or trial)) or (case* adj6 (matched or control*)) or (match* adj6 (pair or pairs or cohort* or control* or group* or healthy or age or sex or gender or patient* or subject* or participant*)) or (propensity adj6 (scor* or match*))).ti,ab,kf. or (confounding adj6 adjust*).ti,ab. or (versus or vs or compar*).ti. or ((exp cohort studies/ or epidemiologic studies/ or multicenter study/ or observational study/ or seroepidemiologic studies/ or (cohort* or 'follow up' or followup or longitudinal* or prospective* or retrospective* or observational* or multicent* or 'multi-cent*' or consecutive*).ti,ab,kf.) and ((group or groups or subgroup* or versus or vs or compar*).ti,ab,kf. or ('odds ratio*' or 'relative odds' or 'risk ratio*' or 'relative risk*' or aor or arr or rrr).ab. or (("OR" or "RR") adj6 CI).ab.)) |
5461853 |
|
9 |
Epidemiologic studies/ or case control studies/ or exp cohort studies/ or Controlled Before-After Studies/ or Case control.tw. or cohort.tw. or Cohort analy$.tw. or (Follow up adj (study or studies)).tw. or (observational adj (study or studies)).tw. or Longitudinal.tw. or Retrospective*.tw. or prospective*.tw. or consecutive*.tw. or Cross sectional.tw. or Cross-sectional studies/ or historically controlled study/ or interrupted time series analysis/ [Onder exp cohort studies vallen ook longitudinale, prospectieve en retrospectieve studies] |
4479207 |
|
8 |
exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw. |
2607704 |
|
7 |
meta-analysis/ or meta-analysis as topic/ or (metaanaly* or meta-analy* or metanaly*).ti,ab,kf. or systematic review/ or cochrane.jw. or (prisma or prospero).ti,ab,kf. or ((systemati* or scoping or umbrella or "structured literature") adj3 (review* or overview*)).ti,ab,kf. or (systemic* adj1 review*).ti,ab,kf. or ((systemati* or literature or database* or data-base*) adj10 search*).ti,ab,kf. or ((structured or comprehensive* or systemic*) adj3 search*).ti,ab,kf. or ((literature adj3 review*) and (search* or database* or data-base*)).ti,ab,kf. or (("data extraction" or "data source*") and "study selection").ti,ab,kf. or ("search strategy" and "selection criteria").ti,ab,kf. or ("data source*" and "data synthesis").ti,ab,kf. or (medline or pubmed or embase or cochrane).ab. or ((critical or rapid) adj2 (review* or overview* or synthes*)).ti. or (((critical* or rapid*) adj3 (review* or overview* or synthes*)) and (search* or database* or data-base*)).ab. or (metasynthes* or meta-synthes*).ti,ab,kf. |
679070 |
|
6 |
limit 5 to yr="1995 -Current" |
623 |
|
5 |
4 not (comment/ or editorial/ or letter/) not ((exp animals/ or exp models, animal/) not humans/) not ((Adolescent/ or Child/ or Infant/ or adolescen*.ti,ab,kf. or child*.ti,ab,kf. or schoolchild*.ti,ab,kf. or infant*.ti,ab,kf. or girl*.ti,ab,kf. or boy*.ti,ab,kf. or teen.ti,ab,kf. or teens.ti,ab,kf. or teenager*.ti,ab,kf. or youth*.ti,ab,kf. or pediatr*.ti,ab,kf. or paediatr*.ti,ab,kf. or puber*.ti,ab,kf.) not (Adult/ or adult*.ti,ab,kf. or man.ti,ab,kf. or men.ti,ab,kf. or woman.ti,ab,kf. or women.ti,ab,kf.)) |
846 |
|
4 |
1 and 2 and 3 |
1770 |
|
3 |
exp Rhizotomy/ or 'radicotom*'.ti,ab,kf. or 'radiculotom*'.ti,ab,kf. or 'rhizotom*'.ti,ab,kf. or 'thermorhizotom*'.ti,ab,kf. or 'neurotom*'.ti,ab,kf. or Denervation/ or denervation*.ti,ab,kf. or ((nerve* or neuron*) adj3 (transection or transsection or excision* or exeresis or removal or resection or dissection)).ti,ab,kf. or 'neurectom*'.ti,ab,kf. or 'neuronectom*'.ti,ab,kf. or aponeurectom*.ti,ab,kf. or exp Tenotomy/ or 'tendotom*'.ti,ab,kf. or 'tenontom*'.ti,ab,kf. or 'tenotom*'.ti,ab,kf. or ((musc* or tendon or hamstring* or quadricep* or 'heel cord') adj3 (lengthen* or elongation or surg* or microsurg* or releas*)).ti,ab,kf. or Orthopedic Procedures/ or 'orthopedic surg*'.ti,ab,kf. or exp Fasciotomy/ or 'fasciotom*'.ti,ab,kf. or exp Arthrodesis/ or 'arthrodes*'.ti,ab,kf. or 'artificial ankylosis'.ti,ab,kf. or 'joint fusion*'.ti,ab,kf. or fusion*.ti,ab,kf. or exp Nerve Transfer/ or exp Tendon Transfer/ or neurotization*.ti,ab,kf. or ((tendon or nerve* or 'motor branch*') adj3 (transfer* or graft* or transplant* or allotransplant* or crossover*)).ti,ab,kf. |
394798 |
|
2 |
exp Cerebral Palsy/ or ((cerebral* or brain or central) adj3 (pares* or pals* or paralys*)).ti,ab,kf. or 'little disease*'.ti,ab,kf. or 'diplegia spastic*'.ti,ab,kf. or 'spastic diplegi*'.ti,ab,kf. or 'intractable spastic*'.ti,ab,kf. or exp Spinal Injuries/ or ((spinal or spine) adj2 (injur* or trauma*)).ti,ab,kf. or Cerebrovascular Disorders/ or exp Stroke/ or exp Intracranial Aneurysm/ or exp Intracranial Hemorrhages/ or exp Brain Infarction/ or exp Stroke Rehabilitation/ or cva.ti,ab,kf. or cvas.ti,ab,kf. or stroke.ti,ab,kf. or poststroke.ti,ab,kf. or ((cerebrovascular or 'cerebro vascular' or cerebral or intracerebral or cerebellum or brain or 'corpus callosum' or intracranial or intraventricular or periventricular or subarachnoid) adj3 (accident* or attack* or infarct* or insult* or event* or bleed* or microbleed* or aneurysm* or hemorrhage* or haemorrhage* or microhemorrhage* or microhaemorrhage* or ischemi* or ischaemi* or haematoma* or hematoma* or thrombo* or emboli* or occlus*)).ti,ab,kf. or apoplex*.ti,ab,kf. or encephalorrhagia.ti,ab,kf. |
663283 |
|
1 |
exp Muscle Hypertonia/ or Paraplegia/ or exp Paraparesis, Spastic/ or Spasm/ or exp Muscle Tonus/ or exp Dystonia/ or spastic*.ti,ab,kf. or spasm*.ti,ab,kf. or 'high tone'.ti,ab,kf. or hypertonia.ti,ab,kf. or hypertonus.ti,ab,kf. or hypertonicity.ti,ab,kf. or hypermyoton*.ti,ab,kf. or dyston*.ti,ab,kf. or myodyston*.ti,ab,kf. or ((muscle* or muscular) adj3 (rigid* or tone or tonus or overactiv* or 'over activ*' or paretic)).ti,ab,kf. or ((motor or movement or gait or walk* or ambulat*) adj3 (disabilit* or disfunction* or dysfunction* or disorder* or impair* or compromises or compromised)).ti,ab,kf. |
175993 |