Katheter-geleide-trombolyse DVT van het been of arm
Uitgangsvraag
Deelvraag 1: Is katheter-geleide-trombolyse, al dan niet gecombineerd met trombectomie, geïndiceerd bij de behandeling van diepe veneuze trombose (DVT) van het been?
Deelvraag 2: Is katheter-geleide-trombolyse, al dan niet gecombineerd met trombectomie, geïndiceerd bij de behandeling van DVT van de arm?
Aanbeveling
Katheter-geleide-trombolyse van DVT van het been
Geef geen katheter geleide trombolyse aan patiënten met een acute DVT van het iliofemorale traject van het been.
Katheter-geleide-trombolyse van DVT van de arm
Geef geen katheter geleide trombolyse bij patiënten met een DVT van de arm.
Overwegingen
Katheter-geleide-trombolyse van DVT van het been
Allereerst dient opgemerkt te worden dat in de studies naar trombolyse bij DVT geselecteerde patiënten zijn geïncludeerd en de uitkomsten alleen van toepassing zijn op patiënten die voldoen aan de studie-voorwaarden.
Er bestaat nog geen gestandaardiseerde vorm van katheter-geleide-trombolyse met of zonder trombectomie bij acute trombose van het iliofemorale traject. Katheter-geleide-trombolyse wordt uitgevoerd met verschillende technieken, afhankelijk van lokale beschikbaarheid, middelen en expertise. Na geslaagde katheter-geleide-trombolyse met residuale afwijkingen in de vena femoralis communis of meer proximaal gelegen venen, worden soms ballon angioplastiek en stent plaatsing gebruikt om de obstructie op te heffen. Percutane mechanische veneuze trombectomie zonder trombolyse is nog niet geëvalueerd in een gerandomiseerde studie en het gebruik van deze techniek wordt ontraden omdat kleine retrospectieve studies aanwijzingen laten zien dat vaak weinig trombus wordt verwijderd (Kasirajan, 2001; Vedantham, 2002) en dat deze techniek geassocieerd lijkt met een hoog risico op het optreden van longembolie (Delomez, 2001; Kinney, 2000). Er is onvoldoende bewijs dat katheter-geleide-trombolyse bij een trombose in het iliofemorale traject het ontstaan van post-trombotisch syndroom vermindert, zonder het aantal bloedingscomplicaties belangrijk te verhogen. Additioneel aan de twee gerandomiseerde studies (Elsharawy, 2002; Enden, 2012) suggereren de resultaten van observationele studies dat katheter-geleide-trombolyse de veneuze doorgankelijkheid verbetert na een week en 6 maanden, maar niet na 2 jaar, wanneer het vergeleken wordt met standaard antistolling. Het gebruik van katheter-geleide-trombolyse vereist substantiële voorzieningen en expertise. Verdere resultaten van lopende RCT’s moeten worden afgewacht om de toepassing van katheter-geleide-trombolyse als standaard therapie bij iliofemorale DVT te rechtvaardigen ten opzichte van standaard antistollingsbehandeling.
De werkgroep is van mening dat trombolyse bij DVT van het iliofemorale segment alleen overwegen zou kunnen worden als de patiënt voldoet aan alle van de volgende voorwaarden: uitgebreide iliofemorale diepe veneuze trombose met een bedreigde arteriële circulatie door veneuze stuwing; veel pijn en/of een aanzienlijk omtrekverschil, symptoomduur korter dan 14 dagen, goede functionele status van de patiënt, levensverwachting van 1 jaar of meer en (relatief) laag risico op bloedingscomplicaties. Contra indicaties voor trombolyse staan samengevat in de richtlijn Herseninfarct en hersenbloeding.
Gegeven het feit dat de balans tussen de risico’s en de baten van alle vormen van trombolytische therapie nog steeds onduidelijk is, geniet therapie met alleen antistolling als initiële therapie de voorkeur in patiënten met een DVT. Er zijn geen aanwijzingen in de literatuur gevonden dat katheter geleide trombolyse de kans op recidief trombose vermindert.
Er zijn geen studies verricht die duidelijkheid geven over de gewenste duur van antistolling na katheter geleide trombolyse en/of veneuze stentplaatsing. Het is daarom niet mogelijk hierover een advies over te geven. Het lijkt de werkgroep redelijk om hiervoor de richtlijn van duur van antistolling bij DVT of longembolie aan te houden (REF antitrombotisch beleid 2016).
Katheter-geleide-trombolyse van DVT van de arm
De werkgroep is van mening dat trombolyse bij DVT van de arm alleen overwegen zou kunnen worden als de patiënt voldoet aan alle van de volgende voorwaarden: ernstige symptomen, met bedreigde arteriële circulatie door veneuze stuwing; trombus aanwezig in het grootste deel van de vena subclavia en axillaris, symptoomduur korter dan 14 dagen, goede functionele status van de patiënt, levensverwachting van 1 jaar of meer en (relatief) laag risico op bloedingscomplicaties. Contra indicaties voor trombolyse staan samengevat in de richtlijn Herseninfarct en hersenbloeding.
Gegeven het feit dat de balans tussen de risico’s en de baten van alle vormen van trombolytische therapie nog steeds onduidelijk is, is therapie met alleen anticoagulantia naast compressietherapie een goede initiële therapie in alle patiënten met een arm vene trombose. Er zijn geen aanwijzingen in de literatuur gevonden dat CDT de kans op recidief trombose van de arm vermindert. Indien wordt gekozen voor trombolyse verdient CDT de voorkeur boven systemische trombolyse. CDT lijkt minder risico op bloedingscomplicaties te geven, mede doordat de te gebruiken dosis van trombolytica lager is bij CDT dan bij systemische trombolyse (Kearon, 2012). Er zijn geen studies verricht die duidelijkheid geven over de gewenste duur van antistolling na trombolyse en/of veneuze stentplaatsing. Het is daarom niet mogelijk hierover een advies over te geven
Een eerste rib resectie kan overwogen worden, indien het duidelijk is dat de vena subclavia gecomprimeerd wordt tussen de clavicula en de eerste rib. Het therapeutisch voordeel van deze procedure is echter onduidelijk. Daarom dient deze ingreep slechts bij uitzondering overwogen te worden, bijvoorbeeld bij zeer ernstige klachten van zogenaamd ‘thoracic outlet’ syndroom of bij jonge patiënten met massieve arm vene trombose met een bedreiging van de arm, secundair aan de veneuze obstructie en bij patiënten met werkzaamheden met de armen of topsporters (Kearon, 2008; Flinterman, 2008; Machleder, 1993; Schneider, 2004; Spence, 1999; Feugier, 2001; Lee, 1998; Malcynski, 1993; Meier, 1996; Sanders, 1995; Sheeran, 1997; Urschel, 2003; Yilmaz, 2000).
Onderbouwing
Direct na het vaststellen van een diep veneuze trombose (DVT) van het been of de arm wordt gestart met antistollingsbehandeling. Deze therapie vermindert aantoonbaar progressie van de trombose en vermindert de kans op het optreden van een longembolie. Ondanks deze therapie ontwikkelt tot 50% van de patiënten met een DVT proximaal in het been tot jaren na de primaire DVT, een post-trombotisch syndroom (PTS). Ook bij een trombose proximaal in de arm kan tot 20% van de patiënten een PTS ontwikkelen. De klachten bij een PTS kunnen variëren van licht oedeem, kramp en tintelingen tot veneuze claudicatio bij grote inspanning en ulcus cruris. Het is onduidelijk of katheter-geleide-trombolyse (Catheter Directed Thrombolysis) bij een DVT van het been of de arm, al dan niet gecombineerd met trombectomie, resulteert in een lagere incidentie van het PTS ten opzichte van de standaard behandeling met antistollingstherapie. Deze katheter-geleide-trombolyse mag niet leiden tot een onacceptabel hoog percentage bloedingscomplicaties.
Katheter-geleide-trombolyse van DVT van het been
Post-trombotisch syndroom
|
Laag GRADE |
Het is onzeker of twee jaar na katheter-geleide-trombolyse (al dan niet gecombineerd met trombectomie of een andere aanvullende techniek) gevolgd door standaard antistollingsbehandeling, het risico op het ontwikkelen van een post-trombotisch syndroom lager is vergeleken met alleen standaard antistollingsbehandeling bij patiënten met een DVT in het iliofemorale traject in het been.
Bronnen: (Enden, 2012; Haig, 2016; Vedantham, 2017) |
Recidief VTE
|
Laag GRADE |
Het is onzeker of katheter geleide trombolyse (al dan niet gecombineerd met trombectomie of andere aanvullende techniek) gevolgd door standaard antistollingsbehandeling, het risico op ontwikkelen van een recidief VTE verlaagt vergeleken met alleen standaard antistollingstherapie bij patiënten met een DVT in het iliofemorale traject in het been.
Bronnen: (Enden, 2012; Vedantham, 2017) |
Ernstige bloedingen
|
Zeer laag GRADE |
Het is mogelijk dat katheter-geleide-trombolyse (al dan niet gecombineerd met trombectomie of een andere aanvullende techniek) gevolgd door standaard antistollingsbehandeling, in vergelijking met alleen standaard antistollingsbehandeling, rond de trombolyse leidt tot een verhoogd risico op ernstige bloedingen bij patiënten met een DVT in het iliofemorale traject in het been.
Bronnen: (Enden, 2012; Elsharawy, 2002; Vedantham, 2017) |
Mortaliteit
|
Zeer laag GRADE |
Het is onzeker of katheter-geleide-trombolyse (al dan niet gecombineerd met trombectomie of een andere aanvullende techniek) gevolgd door standaard antistollingsbehandeling, in vergelijking met standaard antistollingsbehandeling alleen, leidt tot een verlaagd of verhoogd risico op overlijden bij patiënten met een DVT in het iliofemorale traject in het been.
Bronnen: (Enden, 2012; Vedantham, 2017) |
Katheter-geleide-trombolyse van DVT van de arm
De literatuur search heeft geen gerandomiseerde trials gevonden die katheter-geleide-trombolyse vergelijken met standaard antistollingsbehandeling in patiënten met een DVT van de arm.
De belangrijkste studiekarakteristieken en resultaten zijn samengevat in de bewijstabellen.
De beoordeling van de individuele studieopzet (risk of bias) is opgenomen in de risk-of-biastabellen.
Katheter-geleide-trombolyse van DVT van het been
Beschrijving studies
Eén systematische literatuurstudie (Robertson, 2016) onderzocht het effect van katheter-geleide-trombolyse in combinatie met trombectomie bij patiënten met een DVT in het been. Deze literatuurstudie (Robertson, 2016) doorzocht de literatuur tot december 2015, maar vond geen gerandomiseerde studies die het effect van katheter-geleide-trombolyse in combinatie met trombectomie onderzochten. Daarom is deze systematische literatuurstudie (Robertson, 2016) buiten beschouwing gelaten in de literatuuranalyse.
In een studie uit 2012 (Enden, 2012; Haig, 2016) werden patiënten tussen 18 en 75 jaar oud, met beginnende verschijnselen in de laatste 21 dagen en DVT van het femorale- en/of iliofemorale segment geïncludeerd. Patiënten werden gerandomiseerd naar een behandelarm met katheter-geleide-trombolyse in combinatie met een standaard antistollingsbehandeling met LMWH en warfarine, of naar een controle arm met de standaard antistollingsbehandeling. De follow-up bedroeg twee (Enden, 2012) tot vijf jaar (Haig, 2016).
Een studie uit 2002 (Elsharawy, 2002) includeerde patiënten jonger dan 70 jaar met een iliofemorale DVT en een levensverwachting van meer dan zes maanden. Patiënten werden gerandomiseerd naar een groep met katheter-geleide-trombolyse gevolgd door standaard antistolling, of naar een groep met standaard antistolling (heparine met warfarine). De follow-up bedroeg zes maanden. Een studie uit 2017 (Vedantham, 2017) includeerde patiënten met een DVT van het femorale- en/of iliofemorale segment. Patiënten werden gerandomiseerd naar een groep met katheter-geleide-trombolyse gecombineerd met trombectomie, of naar een groep met standaard antistollingsbehandeling. De follow-up bedroeg twee jaar.
Post-trombotisch syndroom (Villalta score ≥ 5 of veneus ulcus)
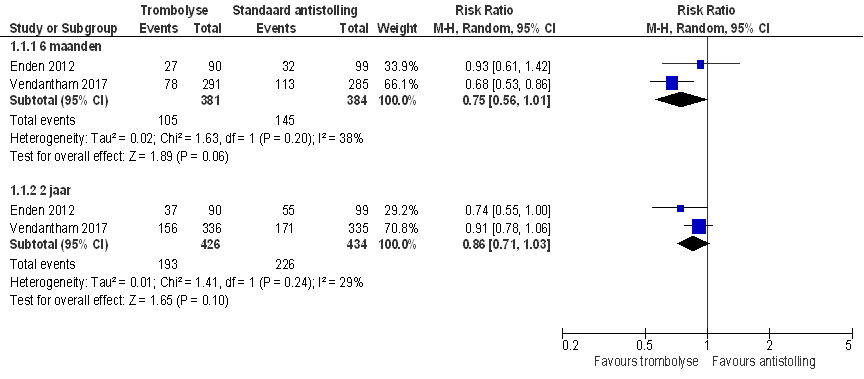
Meerdere studies (Enden, 2012; Haig, 2016; Vendantham, 2017) onderzochten de kans op het optreden van een PTS na katheter-geleide-trombolyse in vergelijking met standaard antistolling. Figuur 1. vat de gepoolde resultaten samen voor de meetmomenten zes maanden- en twee jaar na katheter-geleide-trombolyse.
Na zes maanden follow-up (N = 765, gepoolde relatief risico (RR) (95% betrouwbaarheidsinterval (BI)) = 0,75 (0,56 tot 1,01), I2 = 38%, en twee jaar follow-up (N = 860, gepoolde RR (95% BI) = 0,86 (0,71 tot 1,03), I2 = 29%, is het risico op een post-trombotisch syndroom (Villalta score ≥ 5) statistisch niet significant lager in de katheter-geleide-trombolyse groep dan in de groep die standaard antistolling kreeg.
Figuur 1 Risico op post-trombotisch syndroom (Villalta score ≥ 5) 6 maanden tot 2 jaar na katheter-geleide-trombolyse gevolgd door antistollingsbehandeling versus standaard antistollingsbehandeling alleen
Slechts één studie rapporteerde het risico op het optreden van een PTS (Villalta score ≥ 5 of veneus ulcus) vijf jaar na katheter geleide trombolyse, welke lager was in de katheter-geleide-trombolyse groep dan in de groep die standaard antistolling kreeg (RR (95% BI) = 0,60 (0,45 tot 0,79)) (Enden, 2012; Haig, 2016). Door het lage aantal patiënten dat een ernstig PTS (Villalta score > 14) kreeg in de katheter-geleide-trombolyse groep (N = 4; 4,6%), en het lage aantal patiënten dat een ernstig post-trombotisch syndroom kreeg in de standaard antistolling groep (N = 1; 1,12%) is het niet mogelijk om een uitspraak te doen over het optreden van een ernstig post-trombotisch syndroom (Enden, 2012; Haig, 2016).
Recidief VTE
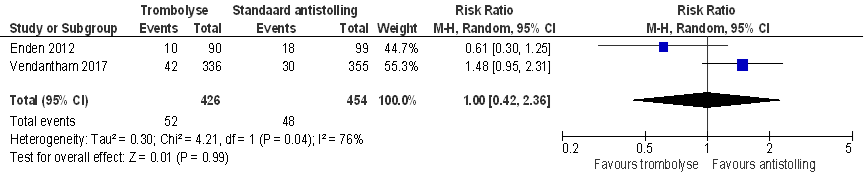
Figuur 2. laat het gepoolde risico op een recidief VTE twee jaar na katheter-geleide-trombolyse zien (RR (95% BI) = 1,00 (0,42 tot 2,36), I2 = 76%). De resultaten van de geïncludeerde studies (Enden, 2012; Vendantham, 2017) zijn inconsistent. In één studie (Enden, 2012) kregen 10 deelnemers (11%) in de kathetergeleide-trombolyse groep een recidief VTE ten opzichte van 18 deelnemers (18%) in de groep die standaard antistolling kreeg (RR = 0,61 95% BI (0,30 tot 1,25). In een andere studie, waarin katheter-geleide-trombolyse gecombineerd werd met trombectomie, hadden (na twee jaar) 42 deelnemers (12%) in de katheter-geleide-trombolyse groep een recidief VTE ten opzichte van 30 deelnemers (8%) in de groep die standaard antistolling kreeg (RR (95% BI) = 1,47 (0,94 tot 2,29) (Vedantham, 2017).
Figuur 2 Risico op recidief VTE 2 jaar na katheter-geleide-trombolyse gevolgd door antistollingsbehandeling versus standaard antistollingsbehandeling alleen
Ernstige bloedingen
Eén studie (Vendantham, 2017) onderzocht het risico op ernstige bloedingen binnen 10 dagen na inclusie in de studie. Zes mensen in de katheter-geleide-trombolyse groep (1,7%) en 1 persoon in de groep met alleen standaard antistolling (0,3%) kregen een ernstige bloeding (RR (95% BI) = 6,54 (0,78 tot 49,2)). Enden en collega’s (Enden, 2012) rapporteerden alleen het aantal ernstige bloeding gerelateerd aan katheter-geleide-trombolyse zonder het aantal bloedingen in de groep met standaard antistolling te vermelden; 3 deelnemers (3,3%) kregen een ernstige bloeding gerelateerd aan de katheter-geleide-trombolyse (Enden, 2012).
In één studie (Elsharawy, 2002) traden binnen zes maanden na de interventie, in zowel de katheter-geleide-trombolyse groep als de groep met standaard antistolling, geen ernstige bloedingen op.
Mortaliteit
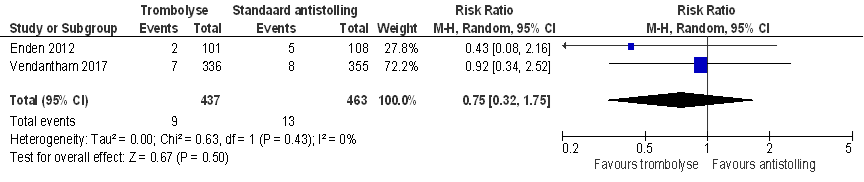
In één studie, met een follow-up van zes maanden (Elsharawy, 2002) overleden geen deelnemers. Deze resultaten van twee andere studies (Enden, 2012; Vendantham, 2017), beide met een follow-up van twee jaar, werden gecombineerd in een meta-analyse (Figuur 3). Na twee jaar follow-up (N = 900, gepoolde RR (95% BI) = 0,75 (0,32 tot 1,75), I2 = 0%), is het risico op overlijden lager in de katheter geleide trombolyse groep dan in de groep die standaard antistolling kreeg. Dit verschil is statistisch niet significant.
Figuur 3 Risico op overlijden 2 jaar katheter-geleide-trombolyse gevolgd door antistollingsbehandeling versus standaard antistollingsbehandeling alleen
Bewijskracht van de literatuur
De bewijskracht voor de uitkomst PTS komt uit op laag (verlaagd met één niveau voor studiedesign (‘on treatment’ analyse in plaats van ‘intention-to-treat’) en één voor imprecisie (brede betrouwbaarheidsintervallen).
De bewijskracht voor de uitkomst recidief veneuze trombose wordt met twee niveaus verlaagd naar laag (één voor studiedesign (‘on treatment’ analyse in plaats van ‘intention-to-treat’), één voor imprecisie vanwege brede betrouwbaarheidsintervallen en inconsistentie).
De bewijskracht voor ernstige bloedingen is zeer laag; deze werd verlaagd met drie niveaus vanwege inconsistentie (verschil in resultaat tussen trials), indirectheid (vanwege een verschil in follow-up duur) en imprecisie (vanwege brede betrouwbaarheidsintervallen). Vanwege dezelfde redenen is ook de bewijskracht voor mortaliteit verlaagd naar zeer laag.
Katheter-geleide-trombolyse van DVT van de arm
Beschrijving studies
We vonden één systematische literatuurstudie (Feinberg, 2017). De auteurs doorzochten de literatuur tot maart 2017 maar vonden geen gerandomiseerde studies die het effect van katheter-geleide-trombolyse onderzocht bij patiënten met DVT van de arm. De auteurs concluderen dat er onvoldoende bewijs is om conclusies te trekken over de voor en nadelen van trombolyse in aanvulling op standaard antistollingsbehandeling naast compressietherapie bij mensen met DVT in de arm. We hebben deze systematische literatuurstudie (Feinberg, 2017) buiten beschouwing gelaten in de literatuuranalyse.
In de Richtlijn Antitrombotisch Beleid (2016) worden wel enkele niet gerandomiseerde studies samengevat. Een aantal kleine observationele studies zijn gepubliceerd, waarin streptokinase, urokinase of rt-PA is toegepast met variërende doses, methoden van toediening (IV, katheter geleid) en duur van toediening (AbuRahma, 1996; Horne, 2000; Lee, 2000; Lokanathan, 2001; Pegis, 1997; Petrakis, 2000; Sabeti, 2002; Schindler, 1999). Drie van deze studies hanteerden niet-gerandomiseerde controle groepen die alleen antistollingsbehandeling kregen (AbuRahma, 1996; Petrakis, 2000; Sabeti, 2002). In sommige studies werd ook een veneuze angioplastiek verricht (Lokanathan, 2001) of chirurgische decompressie (AbuRahma, 1996; Lokanathan, 2001; Sabeti, 2002).
Deze studies suggereren dat trombolyse de vroege en late doorgankelijkheid zou kunnen verbeteren maar dat het gepaard gaat met verhoogde bloedingscomplicaties. Echter het is niet bekend of in de arm katheter-geleide-trombolyse (CDT) vermindering geeft van PTS of recidief VTE. Het lijkt dat PTS een minder voorkomende complicatie is van trombose in de arm dan in het been (Flinterman, 2008; Lechner, 2008; Spencer, 2007; Prandoni, 1997; Prandoni, 2004; Kahn, 2005).
Om de uitgangsvraag te kunnen beantwoorden is een systematische literatuuranalyse verricht naar de volgende zoekvragen:
Deelvraag 1
Wat zijn de effecten van een in de acute fase van DVT van het been uitgevoerde katheter-geleide-trombolyse, al dan niet gecombineerd met trombectomie, gevolgd door antistollingsbehandeling, in vergelijking met alleen antistollingsbehandeling met LMWH, VKA of DOACs?
P: patiënten in de acute fase van DVT (iliofemoraal) van het been;
I: katheter-geleide-trombolyse, of katheter-geleide-trombolyse gecombineerd met trombectomie gevolgd door antistollingsbehandeling;
C: antistollingstherapie alleen met laagmoleculair heparine (LMWH), vitamine K antagonisten (VKA), of directe orale anticoagulantia (DOAC).
Deelvraag 2
Wat zijn de effecten van een in de acute fase van DVT van de arm uitgevoerde katheter-geleide-trombolyse, al dan niet gecombineerd met trombectomie, gevolgd door antistollingsbehandeling, in vergelijking met alleen antistollingsbehandeling met LMWH, VKA of DOACs?
P: patiënten in de acute fase van DVT van de arm;
I: katheter-geleide-trombolyse, of katheter-geleide-trombolyse gecombineerd met trombectomie gevolgd door antistollingsbehandeling;
C: antistollingstherapie met laagmoleculair heparine (LMWH), vitamine K antagonisten (VKA), of directe orale anticoagulantia (DOAC).
Relevante uitkomstmaten
De werkgroep achtte het optreden van het PTS, het optreden van een recidief DVT, het optreden van een longembolie, het optreden van ernstige bloedingen en het optreden van complicaties en mortaliteit tijdens, of gelieerd aan, katheter-geleide-trombolyse cruciaal voor de besluitvorming. Belangrijke uitkomstmaten waren: kwaliteit van leven, opname duur in het ziekenhuis en totale kosten van katheter-geleide-trombolyse ten opzichte van systemische therapieën.
De werkgroep hanteerde voor de uitkomsten de in de studies gebruikte definities.
Zoeken en selecteren
In de Richtlijn Antitrombotisch Beleid (2016) zijn twee gerandomiseerde studies samengevat die het effect van katheter-geleide-trombolyse gevolgd door antistollingsbehandeling met LMWH en warfarine vergeleken met conventionele antistollingstherapie met alléén LMWH en warfarine (Enden, 2012; Elsharawy, 2002). Bij de huidige herziening zijn ook studies meegenomen, die het effect van katheter-geleide-trombolyse in combinatie met trombectomie hebben onderzocht. In aanvulling op de literatuur die samengevat is in de Richtlijn Antitrombotisch Beleid (2016) is op 8 juni 2018 in de databases Medline (via OVID) en Embase (via Embase.com) gezocht naar studies die het effect van katheter-geleide-trombolyse met daarna antistolling, vergeleken met het gebruik van alleen antistolling: LMWH, VKA of DOAC’s bij patiënten met acute DVT van het been of van de arm. De zoekverantwoording is weergegeven onder het tabblad Verantwoording. Zowel systematische literatuurstudies als gerandomiseerde studies zijn geselecteerd.
De literatuurzoekactie leverde 789 treffers op. Op basis van titel en abstract werden 37 studies geselecteerd. Vier systematische literatuurstudies (Elbasty, 2017; Lu, 2017; Wang, 2017; Watson, 2016) zijn uitgesloten. Deze systematische literatuurstudies onderzochten het effect van katheter-geleide-trombolyse bij patiënten met DVT van het been maar presenteren, naast de al beschreven studies in de Richtlijn Antitrombotisch Beleid 2016 (Enden, 2012; Elsharawy, 2002) geen nieuwe studies. Er werd één publicatie (Haig, 2016) gevonden, die de vijf jaar follow-up resultaten beschrijft van de studie van Enden (Enden, 2012). Verder werd er één systematische literatuurstudie (Robertson, 2016) en één gerandomiseerde studie (Vedantham, 2017) gevonden, die het effect onderzocht van katheter-geleide-trombolyse in combinatie met trombectomie bij patiënten met een DVT van het been. Tenslotte werd er één systematische literatuurstudie (Feinberg, 2017) gevonden, die het effect van katheter-geleide-trombolyse onderzocht bij patiënten met DVT van de arm.
De exclusietabel (zie tabblad Verantwoording) bevat zowel de studies, die werden uitgesloten van de literatuuranalyse voor de Richtlijn Antitrombotisch Beleid (2016) als de studies die bij deze herziening zijn uitgesloten.
- AbuRahma AF, Short YS, White JF 3rd, Boland JP. Treatment alternatives for axillary-subclavian vein thrombosis: long-term follow-up. Cardiovasc Surg. 1996 Dec;4(6):783-7.
- Delomez M , Beregi JP , Willoteaux S , et al . Mechanical thrombectomy in patients with deep venous thrombosis. Cardiovasc Intervent Radiol . 2001 ; 24 ( 1 ): 42 - 48 .
- Dopheide JF, Sebastian T, Engelberger RP, Haine A, Kucher N. Early clinical outcomes of a novel rheolytic directional thrombectomy technique for patients with iliofemoral deep vein thrombosis. 2018; Vasa - European Journal of Vascular Medicine. 47(1):56-62.
- Elsharawy M, Elzayat E. Early results of thrombolysis versus anticoagulation in iliofemoral venous thrombosis. A randomized clinical trial. Eur J Vasc Endovasc Surg. 2002;24(3): 209-214.
- Enden T, Haig Y, Kløw NE, et al. Long-term outcome after additional catheter-directed thrombolysis versus standard treatment for acute iliofemoral deep vein thrombosis (the CaVenT study): a randomized controlled trial. Lancet. 2012;379(9810):31-8.
- Feinberg J, Nielsen EE, Jakobsen JC.Thrombolysis for acute upper extremity deep vein thrombosis. 2017; Cochrane Database of Systematic Reviews. 2017(12).
- Feugier P , Aleksic I , Salari R , Durand X , Chevalier JM . Long-term results of venous revascularization for Paget-Schroetter syndrome in athletes . Ann Vasc Surg . 2001; 15 ( 2 ): 212 - 218 .
- Flinterman LE , Van Der Meer FJ , Rosendaal FR , Doggen CJ .Current perspective of venous thrombosis in the upper extremity . J Thromb Haemost . 2008 ; 6 ( 8 ): 1262 - 1266 .
- Haig Y, Enden T, Grøtta O, Kløw NE, Slagsvold CE, Ghanima W, Sandvik L, Hafsahl G, Holme PA, Holmen LO, Njaaastad AM, Sandbæk G, Sandset PM; CaVenT Study Group. Post-thrombotic syndrome after catheter-directed thrombolysis for deep vein thrombosis (CaVenT): 5-year follow-up results of an open-label, randomised controlled trial. Lancet Haematol. 2016 Feb;3(2):e64-71. doi:10.1016/S2352-3026(15)00248-3. Epub 2016 Jan 6. PubMed PMID: 26853645.
- Horne MK III , Mayo DJ , Cannon RO III , Chen CC, Shawker TH , Chang R . Intraclot recombinant tissue plasminogen activator in the treatment of deep venous thrombosis of the lower and upper extremities . Am J Med . 2000; 108( 3): 251- 255.
- Kahn SR , Elman EA , Bornais C , Blostein M , Wells PS . Postthrombotic syndrome, functional disability and quality of life after upper extremity deep venous thrombosis in adults . Thromb Haemost . 2005 ; 93 ( 3 ): 499 - 502 .
- Kasirajan K , Gray B , Ouriel K . Percutaneous AngioJet thrombectomy in the management of extensive deep venous thrombosis . J Vasc Interv Radiol . 2001 ; 12 ( 2 ): 179 - 185 .
- Kearon C, Kahn SR, Agnelli G, Goldhaber S, Raskob GE , Comerota AJ ; American College of Chest Physicians . Antithrombotic therapy for venous thromboembolic disease: American College of Chest Physicians evidence-based clinical practice guidelines (8th Edition) . Chest . 2008 ; 133 ( 6 suppl ): 454S - 545S.
- Kinney TB , Valji K , Rose SC , et al . Pulmonary embolism from pulse-spray pharmacomechanical thrombolysis of clotted hemodialysis grafts: urokinase versus heparinized saline . J Vasc Interv Radiol . 2000 ; 11 ( 9 ): 1143 - 1152 .
- Klitfod L, Broholm R, Baekgaard N. Deep venous thrombosis of the upper extremity. A review. (Review). Int Angiol 2013 Oct;32(5):447-52.
- Lechner D , Wiener C , Weltermann A , Eischer L , Eichinger S , Kyrle PA . Comparison between idiopathic deep vein thrombosis of the upper and lower extremity regarding risk factors and recurrence . J Thromb Haemost . 2008 ; 6 ( 8 ): 1269 - 1274 .
- Lee JJ, Al-Jubouri M, Acino R, Comerota AJ, Lurie F. Role of coexisting contralateral primary venous disease in development of post-thrombotic syndrome following catheter-based treatment of iliofemoral deep venous thrombosis Presented at the Twenty-sixth Annual Meeting of the American Venous Forum, New Orleans, La, February 19-21, 2014. 2015; Journal of Vascular Surgery: Venous and Lymphatic Disorders. 3(4):354-7.
- Lee JT , Karwowski JK , Harris EJ , Haukoos JS , Olcott C IV . Long-term thrombotic recurrence after nonoperative management of Paget-Schroetter syndrome . J Vasc Surg . 2006 ; 43 ( 6 ): 1236 - 1243.
- Lee MC , Grassi CJ , Belkin M , Mannick JA , Whittemore AD, Donaldson MC . Early operative intervention after thrombolytic therapy for primary subclavian vein thrombosis: an effective treatment approach . J Vasc Surg . 1998 ; 27 ( 6 ): 1101 - 1107.
- Lee KA, Ramaswamy RS. Interventional approaches to deep venous thrombosis. 2017; Current Opinion in Cardiology. 32(6):679-86.
- Lokanathan R , Salvian AJ , Chen JC , Morris C , Taylor DC , Hsiang YN . Outcome after thrombolysis and selective thoracic outlet decompression for primary axillary vein thrombosis . J Vasc Surg . 2001 ; 33 ( 4 ): 783 - 788 .
- Machleder HI . Evaluation of a new treatment strategy for Paget-Schroetter syndrome: spontaneous thrombosis of the axillary-subclavian vein . J Vasc Surg . 1993 ; 17 ( 2 ): 305 - 315 . , discussion 316-317.
- Malcynski J , O’Donnell TF Jr , Mackey WC , Millan VA . Long-term results of treatment for axillary subclavian vein thrombosis . Can J Surg . 1993 ; 36 ( 4 ): 365 - 371 .
- Meier GH , Pollak JS , Rosenblatt M , Dickey KW , Gusberg RJ . Initial experience with venous stents in exertional axillary-subclavian vein thrombosis . J Vasc Surg . 1996 ; 24 ( 6 ): 974 – 981.
- Ng TT, Sigman M, Weaver FA. Basic data related to thrombolytic therapy for acute venous thrombosis. Ann Vasc Surg 2014 May;28(4):1039-44.
- Pegis JD , Papon X , Pasco A , Regnard O , Abraham P , Enon B. (In situ thrombolysis in the treatment of venous thrombosis of effort in the arm (in French) . J Mal Vasc . 1997 ; 22 ( 3 ): 187 - 192 .
- Petrakis IE , Katsamouris A , Kafassis E , D’Anna M, Sciacca V V . Two Different Therapeutic Modalities in the Treatment of the Upper Extremity Deep Vein Thrombosis: Preliminary Investigation With 20 Case Reports . Int J Angiol . 2000 ; 9 ( 1 ): 46 - 50 .
- Prandoni P, Bernardi E , Marchiori A , et al . The long term clinical course of acute deep vein thrombosis of the arm: prospective cohort study . BMJ . 2004 ; 329 ( 7464 ): 484 - 485.
- Prandoni P, Polistena P , Bernardi E , et al . Upper-extremity deep vein thrombosis. Risk factors, diagnosis, and complications . Arch Intern Med . 1997 ; 157 ( 1 ): 57 - 62.
- Robertson L, McBride O, Burdess A. Pharmacomechanical thrombectomy for iliofemoral deep vein thrombosis. 2016; Cochrane Database of Systematic Reviews. 2016(11).
- Sabeti S , Schillinger M , Mlekusch W , Haumer M , Ahmadi R , Minar E . Treatment of subclavian-axillary vein thrombosis: long-term outcome of anticoagulation versus systemic thrombolysis . Thromb Res . 2002 ; 108 ( 5-6 ): 279 - 285 .
- Sanders RJ , Cooper MA . Surgical management of subclavian vein obstruction, including six cases of subclavian vein bypass . Surgery . 1995 ; 118 ( 5 ): 856 - 863 .
- Schindler J , Bona RD , Chen HH , et al . Regional thrombolysis with urokinase for central venous catheter-related thrombosis in patients undergoing high-dose chemotherapy with autologous blood stem cell rescue . Clin Appl Thromb Hemost . 1999 ; 5 ( 1 ): 25 - 29 .
- Schneider DB , Dimuzio PJ , Martin ND , et al . Combination treatment of venous thoracic outlet syndrome: open surgical decompression and intraoperative angioplasty . J Vasc Surg . 2004 ; 40 ( 4 ): 599 - 603 .
- Sheeran SR , Hallisey MJ , Murphy TP , Faberman RS, Sherman S . Local thrombolytic therapy as part of a multidisciplinary approach to acute axillosubclavian vein thrombosis (Paget-Schroetter syndrome) . J Vasc Interv Radiol . 1997 ; 8 ( 2 ): 253 - 260 .
- Spence LD , Gironta MG , Malde HM , Mickolick CT , Geisinger MA , Dolmatch BL . Acute upper extremity deep venous thrombosis: safety and effectiveness of superior vena caval filters . Radiology . 1999 ; 210 ( 1 ): 53 - 58.
- Spencer FA , Emery C , Lessard D , Goldberg RJ ; Worcester Venous Thromboembolism Study. Upper extremity deep vein thrombosis: a community-based perspective . Am J Med . 2007 ; 120 ( 8 ): 678 - 684 .
- Urschel HC Jr , Patel AN . Paget-Schroetter syndrome therapy: failure of intravenous stents . Ann Thorac Surg. 2003 ; 75 ( 6 ): 1693 - 1696 .
- Vedantham S, Goldhaber SZ, Julian JA, Kahn SR, Jaff MR, Cohen DJ, et al. Pharmacomechanical catheter-directed thrombolysis for deep-vein thrombosis. 2017; New England Journal of Medicine. 377(23):2240-52.
- Vedantham S, Goldhaber SZ, Kahn SR, Julian J, Magnuson E, Jaff MR, et al. Rationale and design of the ATTRACT Study: a multicenter randomized trial to evaluate pharmacomechanical catheter-directed thrombolysis for the prevention of postthrombotic syndrome in patients with proximal deep vein thrombosis. Am Heart J 2013 Apr;165(4):523-30.
- Vedantham S, Vesely TM, Parti N, Darcy M, Hovsepian DM, Picus D . Lower extremity venous thrombolysis with adjunctive mechanical thrombectomy . J Vasc Interv Radiol . 2002; 13( 10): 1001 - 1008 .
- Yilmaz EN , Vahl AC , van Heek NT, Vermeulen, EGJ, Rauwerda JA. Long-term results of local thrombolysis followed by first rib resection: an encouraging clinical experience in treatment subclavian vein thrombosis. Vasc Surg. 2000;34(1):17–23.
Evidence table for intervention studies
Research question: Wat zijn de effecten van katheter-geleide-trombolyse (CDT) gevolgd door antistollingsbehandeling in vergelijking met alleen antistollingsbehandeling met laagmoleculair heparine (LMWH), vitamine K antagonisten (VKA) of directe orale anticoagulantia (DOAC) in de acute fase van diep veneuze trombose (DVT) in het been?
Risk of bias table for intervention studies (randomized controlled trials)
Research question: Wat zijn de effecten van katheter-geleide-trombolyse (CDT) gevolgd door antistollingsbehandeling in vergelijking met alleen antistollingsbehandeling met laagmoleculair heparine (LMWH), vitamine K antagonisten (VKA) of directe orale anticoagulantia (DOAC) in de acute fase van diep veneuze trombose (DVT) in het been?
|
Study reference
(first author, publication year) |
Describe method of randomisation |
Bias due to inadequate concealment of allocation?2
(unlikely/likely/unclear) |
Bias due to inadequate blinding of participants to treatment allocation?
(unlikely/likely/unclear) |
Bias due to inadequate blinding of care providers to treatment allocation?
(unlikely/likely/unclear) |
Bias due to inadequate blinding of outcome assessors to treatment allocation?
(unlikely/likely/unclear) |
Bias due to selective outcome reporting on basis of the results?
(unlikely/likely/unclear) |
Bias due to loss to follow-up?
(unlikely/likely/unclear) |
Bias due to violation of intention to treat analysis?
(unlikely/likely/unclear) |
|
Enden, 2012 |
Random block (size of six) allocation sequence for each trial site with stratification for involvement of the pelvic veins; treatment assignment was done by picking the lowest number of sealed, opaque, numbered envelopes |
Unlikely |
Unlikely (not possible, but not possible to switch or not adhere) |
Unlikely (not possible, but judged low risk as interventions were well defined) |
Unlikely |
Unlikely |
Unlikely (none were loss to follow-up) |
Likely (although described as ITT, but analysed as treated) |
|
Elsharawy, 2002 |
Randomisation was achieved by computer designated cards assigning patients to either groups |
Unlikely |
Unlikely (not possible, but not possible to switch or not adhere) |
Unlikely (not possible, but judged low risk as interventions were well defined) |
Unlikely |
Unlikely |
Unlikely (none were loss to follow-up) |
Unlikely |
|
Vendantham 2017 |
Randomly assigned in a 1:1 ratio with the use of a Web-based central randomization system |
Unlikely |
Unlikely (not possible, but not possible to switch or not adhere) |
Unlikely (not possible, but judged low risk as interventions were well defined) |
Unlikely |
Unlikely |
Unlikely |
Unlikely |
Exclusietabel
|
Auteur en jaartal |
Redenen van exclusie |
|
Alkhouli 2015 |
Niet gerandomiseerde studie |
|
Avgerinos 2016 |
Niet gerandomiseerde studie |
|
Baekgaard 2014 |
Editorial |
|
Bashir 2014 |
Niet gerandomiseerde studie |
|
Behravesh 2017 |
Beschrijvende literatuurstudie |
|
Berczi 2013 |
Conference abstract |
|
Cakir 2014 |
Thromboectomie |
|
Calik 2015 |
Niet vergelijkende studie |
|
Chan 2014 |
Richtlijntekst VTE bij zwangerschap |
|
Chaudery 2011 |
Geen toevoeging ten opzichte van ACCP |
|
Chen 2016 |
Beschrijvende literatuurstudie |
|
Comerota 2013 |
Presentatie, geen artikel |
|
Comerota 2015 |
Editorial |
|
Dopheide 2018 |
Niet gerandomiseerde studie |
|
Dandoy 2014 |
Geen vergelijkende studie |
|
Duan 2016 |
Vergelijking van drie verschillende CDT-procedures (CDT via small saphenous vein, or great saphenous vein, or popliteal vein) |
|
Dumantepe 2013 |
Niet vergelijkende studie |
|
Elbasty 2017 |
Systematische literatuurstudie, search geen nieuwe data ten opzichte van literatuur in Richtlijn Antitrombotisch Beleid 2016 |
|
Engelberger 2014 |
Niet vergelijkende studie |
|
Engelberger 2015 |
Vergelijking van verschillende CDT-procedures (‘ultrasound-assisted’ met conventionele CDT) |
|
Engelberger 2017 |
Vergelijking van verschillende CDT-procedures (‘ultrasound-assisted’ met conventionele CDT) |
|
Fiengo 2015 |
Niet gerandomiseerde studie |
|
Fleck 2017 |
Beschrijvende literatuurstudie |
|
Foegh 2017 |
Niet gerandomiseerde studie |
|
Gaballah 2016 |
Niet gerandomiseerde studie |
|
Gagne 2015 |
Niet gerandomiseerde studie |
|
Gebauer 2013 |
Exclusie: is een presentatie, geen studie of systematische review |
|
Gombert 2018 |
Niet gerandomiseerde studie |
|
Gotlieb 2017 |
Samenvatting Cochrane Review (Watson 2016) |
|
Haig 2014 |
Publicatie van ingesloten studie (Enden 2012) |
|
Klitford 2013 |
Beschrijvende literatuurstudie |
|
Köksoy 2014 |
Niet gerandomiseerde studie |
|
Konstantinides 2014 |
Beschrijvende literatuurstudie, geen specifieke resultaten voor CDT |
|
Konstantinides 2015 |
Beschrijvende literatuurstudie |
|
Kuo 2013 |
Commentary |
|
Kuo 2017 |
Niet gerandomiseerde studie |
|
Lee 2015 |
Niet gerandomiseerde studie |
|
Lee 2017 |
Beschrijvende literatuurstudie |
|
Lichtenberg 2013 |
Beschrijvende literatuurstudie |
|
Liew 2013 |
Beschrijvende literatuurstudie, andere patiëntengroep en interventies |
|
Lu 2017 |
Systematische literatuurstudie, search geen nieuwe data ten opzichte van literatuur in Richtlijn Antitrombotisch Beleid 2016 |
|
Mahmoud 2018 |
Niet gerandomiseerde studie |
|
Nakamura 2014 |
Niet gerandomiseerde studie |
|
Ng 2014 |
Beschrijvende literatuurstudie |
|
Ozcinar 2017 |
Niet gerandomiseerde studie |
|
Rodiere 2013 |
Beschrijvende literatuurstudie |
|
Saha 2016 |
Beschrijvende literatuurstudie |
|
Saseedharan 2012 |
Beschrijvende literatuurstudie |
|
Sharifi 2014 |
Beschrijvende literatuurstudie |
|
Srinivas 2015 |
Niet gerandomiseerde studie |
|
Strijkers 2014 |
Beschrijvende literatuurstudie |
|
Sui 2013 |
Publicatie in Chinees |
|
Taha 2018 |
Systematische literatuurstudie, alleen observationeel onderzoek geïncludeerd |
|
Vedantham 2013 |
Studieprotocol |
|
Vedantham 2015a |
Beschrijvende literatuurstudie |
|
Vedantham 2015b |
Beschrijvende literatuurstudie |
|
Virk 2013 |
Exclusie, geen systematische review en ook geen origineel onderzoek |
|
Wang 2017 |
Systematische literatuurstudie, search geen nieuwe data ten opzichte van literatuur in Richtlijn Antitrombotisch Beleid 2016 |
|
Watson 2014 |
Oudere versie van Cochrane Review (Watson 2016) |
|
Watson 2016 |
Systematische literatuurstudie, search geen nieuwe data ten opzichte van literatuur in Richtlijn Antitrombotisch Beleid 2016 |
|
Wells 2014 |
Beschrijvende literatuurstudie |
|
Zhang 2014 |
Vergelijking van verschillende CDT-procedures (CDT gevolgd door stentplaatsing met alléén CDT) |
|
Zheng 2014 |
Systematische literatuurstudie, search geen nieuwe data ten opzichte van literatuur in Richtlijn Antitrombotisch Beleid 2016 |
|
Zhu 2014 |
Niet gerandomiseerde studie |
Beoordelingsdatum en geldigheid
Publicatiedatum : 29-03-2016
Beoordeeld op geldigheid : 01-09-2020
Deze richtlijn is modulair herzien. Een aantal modules dienen binnen de tijdstermijn van 5 jaar herzien te worden. De NIV is daarom voornemens een deel van de werkgroep in stand te houden. Een nader uitgewerkt onderhoudsplan wordt tijdens de commentaarronde ter consultatie voorgelegd aan de NIV commissie richtlijnen en kwaliteitsmeting.
De NIV is als houder van deze richtlijn de eerstverantwoordelijke voor de actualiteit van deze richtlijn. De andere aan deze richtlijn deelnemende wetenschappelijk verenigingen of gebruikers van de richtlijn delen de verantwoordelijkheid en informeren de eerstverantwoordelijke over relevante ontwikkelingen binnen hun vakgebied.
Omdat deze richtlijn in modulair onderhoud is zullen er de komende tijd regelmatig modules van deze richtlijn worden geüpdatet of waar nodig nieuwe modules worden ontwikkeld en toegevoegd. Er volgen hiervoor nog aparte commentaar- en autorisatiefases. Zie het ‘Overzicht modulair onderhoud’ bij de aanverwante producten van deze module voor een overzicht van de vragen die momenteel uitgewerkt worden.
Algemene gegevens
Deze richtlijnmodule is goedgekeurd door:
- Patiëntenfederatie Nederland
- Harteraad
De richtlijnontwikkeling werd ondersteund door het Kennisinstituut van Medisch Specialisten (https://www.demedischspecialist.nl/kennisinstituut) en werd gefinancierd uit de Kwaliteitsgelden Medisch Specialisten (SKMS).
Doel en doelgroep
Het doel is de multidisciplinaire nationale richtlijn Antitrombotisch beleid te herzien, waarbij er een duidelijke invulling komt van de gesignaleerde klinische knelpunten. Als voorbeeld wordt de hiaat met betrekking tot het beleid van perioperatief gebruik van antistolling herzien en wordt aandacht gegeven aan de introductie van DOACs.
Deze richtlijn is geschreven voor patiënten, trombosediensten, en alle leden van de beroepsgroepen die betrokken zijn bij de zorg voor patiënten met antitrombotische therapie.
Samenstelling werkgroep
Kerngroep
- prof. dr. M.V. (Menno) Huisman, internist-vasculaire geneeskunde, LUMC, NIV (voorzitter)
- dr. M.J.H.A. (Marieke) Kruip, internist-hematoloog, ErasmusMC, NIV, NVVH (Nederlandse Vereniging voor Hematologie)
- dr. F.A. (Erik) Klok, internist-vasculaire geneeskunde, LUMC, NIV
- dr. M.A. (Marc) Brouwer, cardioloog, RadboudUMC, NVVC
- dr. H.B. (Harmen) Ettema, orthopedisch chirurg, Isala, NOV
- drs. B. (Banne) Nemeth, aios orthopedie, LUMC, NOV
- dr. A.M. (Arno) Wiersema, vaatchirurg, NVVH
- dr. M.E. (Maarten) Tushuizen, maag-darm-leverarts, LUMC, NVMDL
- dr. J.M. (Jonathan) Coutinho, neuroloog, AMC-UVA, NVN
- drs. A. (Andrew) Oostindjer, huisarts/ Kaderhuisarts HVZ, NHG
Klankbordgroep
- dr. J.J.C.M. (Sjef) van de Leur, arts klinische chemie, Isala, NVKC
- dr. A.W.M.M. (Ankie) Koopman - van Gemert, anesthesioloog, ASZ, NVA
- dr. M.G. (Mariëlle) van Pampus, gynaecoloog, OLVG, NVOG
- drs. R.J. (Repke) Snijder, longarts, Antoniusziekenhuis, NVALT
- drs. R.J. Lely, radioloog, VUMC, NVVR
- dr. C. van Montfrans, dermatoloog, ErasmusMC, NVDV
- dr. R.A. (Richard) Faaij, klinisch geriater, Diakonessenhuis, NVKG
- dr. B. van Minnen, kaakchirurg, UMCG, NVMKA
- mw. A (Annemarie) Auwerda, beleidsadviseur, Harteraad (vanaf maart 2019)
- A.M. (Anne) Kors-Walraven MSc BA, beleidsadviseur, Harteraad (van November 2018 tot maart 2019).
- prof. dr. S (Saskia) Middeldorp, internist vasculaire-geneeskunde, AMC-UVA, NIV
- M.J. (Jacqueline) Krol- van Straaten, internist – nefroloog, Hagaziekenhuis, NIV
- dr. M. (Marcel) Schouten, internist – nefroloog, Tergooi, NIV
- dr. N. (Nakisa) Khorsand, ziekenhuisapotheker, OLVG, NVZA
- dr. M.F. (Margreet) Warlé- van Herwaarden, openbaar apotheker, KNMP
Belangenverklaringen
De KNMG-code ter voorkoming van oneigenlijke beïnvloeding door belangenverstrengeling is gevolgd. Alle werkgroepleden hebben schriftelijk verklaard of zij in de laatste drie jaar directe financiële belangen (betrekking bij een commercieel bedrijf, persoonlijke financiële belangen, onderzoeksfinanciering) of indirecte belangen (persoonlijke relaties, reputatiemanagement, kennisvalorisatie) hebben gehad. Een overzicht van de belangen van werkgroepleden en het oordeel over het omgaan met eventuele belangen vindt u in onderstaande tabel. De ondertekende belangenverklaringen zijn op te vragen bij het secretariaat van het Kennisinstituut van de Federatie Medisch Specialisten.
|
Achternaam werkgroeplid |
Hoofdfunctie |
Nevenwerkzaamheden |
Persoonlijke financiële belangen |
Persoonlijke relaties |
Extern gefinancierd onderzoek |
Intellectuele belangen en reputatie |
Overige belangen |
Getekend op |
Acties |
|
Huisman |
Internist vasculaire geneeskunde Leids Universitair Medisch Centrum |
- Voorzitter commissie herziening Antitrombotisch Beleid, onbetaald |
Adviseur farmaceutische bedrijven die (nieuwe) antistollingsmiddelen maken - betaald; gelden gaan naar afdeling Interne Geneeskunde LUMC |
Niet van toepassing |
ZONMW grant Dutch-AF - registry met onderzoek op het gebied van antistolling bij patiënten met atriumfibrilleren; betaald, gelden gaan naar afdeling Interne Geneeskunde LUMC |
Niet van toepassing |
Niet van toepassing |
14-6-2018 |
Deelname in werkgroep als voorzitter in verband met expertise op dit gebied. In verband met adviseur farmaceutische bedrijven: participeert niet bij besluitvorming middelen |
|
Kruip |
Internist-hematoloog Erasmus MC |
Medisch leider trombosedienst Star-SHL, gedetacheerd vanuit het Erasmus MC |
Geen |
Geen |
- Anti-thrombotic standardship S-team introduction (2015-2016) Boehringer-Ingelheim |
Niet van toepassing |
- 2015: bezoek Sheffield trombosekliniek / Bayer / € 500,- (reiskosten) |
26-6-2018 |
In verband met belangen geen participatie besluitvorming keuze middelen |
|
Wiersema |
Vaatchirurg in het Westfriesgasthuis te Hoorn en AUMC, locatie Vumc |
Grant onderzoek ACT en heparine arteriële vaatingrepen Medtronic, geen onderwerp van deze richtlijn |
Geen |
Geen |
Grant onderzoek ACT en heparine arteriële vaatingrepen Medtronic, geen onderwerp van deze richtlijn |
Geen |
Geen |
24-7-2018 |
Geen acties |
|
Ettema |
Orthopedisch chirurg Isala Klinieken, Zwolle |
geen |
geen van bovenstaande |
geen van bovenstaande |
In verleden deelname verschillende RCT waarvan de laatste > 2 jaar gelden |
geen van bovenstaande |
geen |
31-7-2018 |
RCT's >3 jaar geleden, geen actie |
|
Coutinho |
Neuroloog Amsterdam UMC |
geen |
geen |
geen |
RESPECT-CVT studie. Gefinancierd door Boehringer. Ondergetekende zit in het steering Committee van deze studie |
geen |
geen |
31-8-2018 |
geen actie, studie gaat over andere patiëntpopulatie |
|
Warlé-van Herwaarden |
Apotherker, Apotheek Groesbeek |
participeert af en toe in onderzoek (onbetaald) |
geen |
geen |
geen |
geen |
Geen |
3-9-2018 |
Geen acties |
|
Brouwer |
Cardioloog, Radboudumc |
Afgevaardigde van de NVVO bij LSKA (Landelijke Standaard Keten Antistolling), onbetaald |
De research-afdeling cardiologie heeft voor verschillende projecten financiële ondersteuning ontvangen van : Astra Zeneca, BMS-Pfizer, Boehringer Ingelheim, Beyer, Daiichi Sankyo |
nee |
Dutch AF registry |
Niet van toepassing |
Niet van toepassing |
8-11-2017 |
Geen, ander onderwerp |
|
Klok |
Internist Vasculair geneeskundige, LUMC, Leiden |
Adjunct Professor Universiteit van Mainz, Duitsland (onbetaald) |
Geen |
Geen |
Dr. F.A. Klok heeft financiële steun ontvangen voor studies (unrestricted research grants) van Bayer, BMS/Pfizer, Boehringer Ingelheim, Daiichi Sankyo, MSD, Actelion, Trombose Stichting Nederland en de Hartstichting. Dit betroffen allen studies naar diagnostiek van longembolie/DVT of voorkomen van langetermijn effecten (pulmonale hypertensie, lagere kwaliteit van leven et cetera). |
Geen |
Geen |
21-9-2018 |
Geen, gesponsorde studies gaan over diagnostiek. Diagnostiek komt vooralsnog niet aan bod in deze richtlijn. Mocht dit het geval zijn belangen opnieuw bespreken. Geen actie nodig |
|
Alikhil |
* Huisarts, werkzaam in huisartspraktijk Alikhil |
* Huisartsenzorg in volle breedte |
Neen |
Neen |
Neen |
Neen |
Neen |
1-11-2018 |
Geen acties |
|
Tushuizen |
MDL-arts, staflid Leids Universitair Medisch Centrum, Leiden |
MDL-arts; DC-kliniek Almere, Almere, verrichten van endoscopie (betaald) |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
Niet van toepassing |
14-12-2018 |
Geen acties |
|
Oostindjer |
Huisarts - eigen praktijk in Oldenzaal. |
Als Kaderhuisarts HVZ: |
Ik heb momenteel geen (financiële) belangen bij welke organisatie dan ook die producten produceert die van belang zijn voor deze richtlijn (antistolling). |
nvt |
nvt |
Ik heb geen belangen die geschaad of bevoordeeld kunnen worden. Enige wat zou kunnen is dat er meer vraag komt naar onderwijs op dit onderwerp welke ik dan zou kunnen verzorgen mogelijk een vorm van “vermarkting”. |
nvt |
19-8-2019 |
|
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiënten perspectief door een search naar het patiënten perspectief. Daarnaast zal bij de richtlijn een zogenaamde ‘option grid’ worden ontwikkeld (keuzehulp voor patiënten en zorgverleners samen) voor het onderwerp continueren antistolling.
Methode ontwikkeling
Evidence based
Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn (module) en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is uitdrukkelijk gelet op factoren die de invoering van de richtlijn in de praktijk kunnen bevorderen of belemmeren. Het implementatieplan is te vinden bij de aanverwante producten. De werkgroep heeft tevens interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken (zie indicatorenontwikkeling).
Werkwijze
AGREE
Deze richtlijn is opgesteld conform de eisen volgens het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II) (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010), dat een internationaal breed geaccepteerd instrument is en op ‘richtlijnen voor richtlijn’ voor de beoordeling van de kwaliteit van richtlijnen (www.zorginstituutnederland.nl).
Doordat delen van de richtlijn niet herzien zijn, zijn door de evolutie van richtlijn ontwikkelmethodologie de gebruikte methodes verschillend voor verschillende delen.
De delen over diagnostiek bij diepe veneuze trombose, diagnostiek longembolie, aparte categorieën in kader van diagnostiek, arteriële preventie en bijzondere situaties veneuze preventie veneuze trombo-embolie uit de CBO richtlijn van 2008 zijn zo veel mogelijk in originele structuur en stijl behouden (hoewel er aan de structuur wijzigingen zijn gemaakt zodat deze teksten conform het richtlijnendatabase format zijn). De additionele secties over medicamenteuze behandeling van veneuze trombo-embolie, niet-medicamenteuze behandeling van veneuze trombo-embolie, bijzondere situaties veneuze trombo-embolie en preventie veneuze trombo-embolie bevatten nieuwe literatuur en aanbevelingen die werden ontwikkeld volgens nieuwe methodologie. Dit heeft onvermijdelijk geleid tot inconsistenties in de stijl. Bijvoorbeeld is de GRADE methodologie gebruikt in de nieuwe teksten om de kwaliteit en sterkte van de bewijskracht en aanbevelingen te graderen in de nieuwe stukken, waar in de oude stukken gebruik is gemaakt van de oudere EBRO methodologie, of gradering van de oude ACCP richtlijn (2004) is overgenomen. Daarnaast wordt in de oude delen van de richtlijn asymptomatische DVT als uitkomstmaat gehanteerd, maar meer recentelijk wordt zowel nationaal als internationaal deze uitkomstmaat niet meer gebruikt. In de nieuwe delen worden daarom alleen de resultaten met betrekking tot symptomatische DVT gerapporteerd.
De beschrijving van de methodologie bij de verschillende teksten bevatten een beschrijving van de details met betrekking tot de methodologie voor de betreffende module.
Het is van belang om te benadrukken dat hoewel de richtlijn methodologie is veranderd, ook de oudere aanbevelingen uit de CBO richtlijn 2008 onverminderd van kracht zijn.
Knelpuntenanalyse
Tijdens de voorbereidende fase inventariseerden de werkgroep de knelpunten middels een enquête. Naast de in de kern- en klankbordgroep vertegenwoordigde partijen werden de FNT, IGJ, KiMO, NHG, NFU, NVZ, STZ, V&VN, Verenso, VIG, VWS, ZiNL en ZN uitgenodigd deze enquête in te vullen.
Uitgangsvragen en uitkomstmaten
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de voorzitter en de adviseur conceptuitgangsvragen opgesteld. Deze zijn met de werkgroep besproken waarna de werkgroep de definitieve uitgangsvragen heeft vastgesteld. Vervolgens inventariseerde de werkgroep per uitgangsvraag welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als kritiek, belangrijk en onbelangrijk. Tevens definieerde de werkgroep voor de kritieke en belangrijke uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Strategie voor zoeken en selecteren van literatuur
Er werd eerst oriënterend gezocht naar systematische reviews [EMBASE, MEDLINE, Cochrane library]. Vervolgens werd voor de afzonderlijke uitgangsvragen aan de hand van specifieke zoektermen gezocht naar gepubliceerde wetenschappelijke studies in (verschillende) elektronische databases. Tevens werd aanvullend gezocht naar studies aan de hand van de literatuurlijsten van de geselecteerde artikelen. In eerste instantie werd gezocht naar studies met de hoogste mate van bewijs. De werkgroepleden selecteerden de via de zoekactie gevonden artikelen op basis van vooraf opgestelde selectiecriteria. De geselecteerde artikelen werden gebruikt om de uitgangsvraag te beantwoorden. De databases waarin is gezocht, de zoekactie of gebruikte trefwoorden van de zoekactie en de gehanteerde selectiecriteria zijn te vinden in het hoofdstuk van desbetreffende uitgangsvraag.
Kwaliteitsbeoordeling individuele studies
Individuele studies werden systematisch beoordeeld, op basis van op voorhand opgestelde methodologische kwaliteitscriteria, om zo het risico op vertekende studieresultaten (risk of bias) te kunnen schatten. Deze beoordelingen kunt u vinden in de Risk of bias tabellen.
Samenvatten van de literatuur
De relevante onderzoeksgegevens van alle geselecteerde artikelen werden overzichtelijk weergegeven in evidence tabellen. De belangrijkste bevindingen uit de literatuur werden beschreven in de samenvatting van de literatuur. Bij een voldoende aantal studies en overeenkomstigheid (homogeniteit) tussen de studies werden de gegevens ook kwantitatief samengevat (meta-analyse) met behulp van Review Manager 5.
Beoordelen van de kracht van het wetenschappelijke bewijs
A) Voor interventievragen
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor ‘Grading Recommendations Assessment, Development and Evaluation’ (zie http://www.gradeworkinggroup.org) (Schünemann H, 2013).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, matig, laag en zeer laag. Deze gradaties verwijzen naar de mate van vertrouwen in de literatuurconclusie.
|
GRADE |
Definitie |
|
Hoog |
|
|
Matig |
|
|
Laag |
|
|
Zeer laag |
|
B) Voor vragen over waarde diagnostische tests, schade of bijwerkingen, etiologie en prognose
De GRADE methodiek is door de Nederlandse werkgroep GRADE-NL (nog) niet vastgesteld voor dit type vraagstelling. De bewijskracht van de conclusie is bepaald volgens de EBRO-methode (Van Everdingen, 2004).
Belangrijkste verschillen tussen de GRADE- en ACCP-indeling
- Met de ACCP-indeling worden aanbevelingen gegradeerd, met de GRADE methodiek worden conclusies gegradeerd. In de ACCP-aanbevelingen wordt wel rekening gehouden met overige (meer subjectieve) overwegingen (bijwerkingen, kosten, gemak voor patiënt), maar dit is niet expliciet terug te vinden; dit komt terug in grootte van het effect (zie punt 2). In de GRADE methodiek worden de overige overwegingen (bijwerkingen, kosten, patiëntenperspectief, expert opinion) gewogen en transparant beschreven, deze overwegingen samen met de wetenschappelijke conclusies leiden tot de aanbevelingen;
- In de ACCP-indeling wordt onderscheid gemaakt tussen een duidelijk klinisch effect (1) en een klein of onduidelijk effect (2), volgens de GRADE-methodiek wordt vooraf benoemde klinische relevantie meegewogen in de gradering van de conclusies.
Formuleren van de conclusies
Voor vragen over de waarde van diagnostische testen, over schade of bijwerkingen, etiologie en prognose is het wetenschappelijke bewijs samengevat in één of meerdere conclusie(s), waarbij het niveau van het meest relevante bewijs is weergegeven.
Bij interventievragen verwijst de conclusie niet naar één of meer artikelen, maar wordt getrokken op basis van alle studies samen (body of evidence). Hierbij maakten de werkgroepleden de balans op van elke interventie (overall conclusie). Bij het opmaken van de balans werden de gunstige en ongunstige effecten voor de patiënt afgewogen. De overall bewijskracht wordt bepaald door de laagste bewijskracht gevonden bij een van de kritieke uitkomstmaten. Bij complexe besluitvorming waarin naast de conclusies uit de systematische literatuuranalyse vele aanvullende argumenten (overwegingen) een rol spelen, werd afgezien van een overall conclusie. In dat geval werden de gunstige en ongunstige effecten van de interventies samen met alle aanvullende argumenten gewogen onder het kopje 'Overwegingen'.
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals criteria die van invloed zijn op de aanbeveling, de expertise van de werkgroepleden, de waarden en voorkeuren van de patiënt (patient values and preferences), kosten, beschikbaarheid van voorzieningen of organisatorische zaken. Deze aspecten worden, voor zover geen onderdeel van de literatuursamenvatting, vermeld en beoordeeld (gewogen) onder het kopje ‘Overwegingen’.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Conform de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk. De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen.
Randvoorwaarden (Organisatie van zorg)
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijn is expliciet rekening gehouden met de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van een specifieke uitgangsvraag maken onderdeel uit van de overwegingen bij de bewuste uitgangsvraag. De richtlijn bevat geen organisatie van zorg hoofdstuk, omdat er over organisatie van zorg en samenwerking binnen de keten reeds documenten bestaan (bijvoorbeeld LSKA 2.0).
Indicatorontwikkeling
Gelijktijdig met het ontwikkelen van de richtlijn werden er interne kwaliteitsindicatoren ontwikkeld om het toepassen van de richtlijn in de praktijk te volgen en te versterken (de indicatoren zijn te vinden in de aanverwante producten). Meer informatie over de methode van indicatorontwikkeling is op te vragen bij het Kennisinstituut van Medisch Specialisten (secretariaat@kennisinstituut.nl).
Kennislacunes
Tijdens de ontwikkeling van deze richtlijn is systematisch gezocht naar onderzoek waarvan de resultaten bijdragen aan een antwoord op de uitgangsvragen. Bij elke uitgangsvraag is door de werkgroep nagegaan of er (aanvullend) wetenschappelijk onderzoek gewenst is. Een overzicht van aanbevelingen voor nader/vervolg onderzoek worden toegevoegd na de commentaarfase.
Commentaar- en autorisatiefase
De conceptrichtlijn wordt aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor commentaar. De commentaren worden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren wordt de conceptrichtlijn aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijn wordt aan de betrokken (wetenschappelijke) verenigingen voorgelegd voor autorisatie en door hen geautoriseerd.
Zoekverantwoording
|
Database |
Zoektermen |
Totaal |
|
Medline (OVID)
2014 – juni 2018
|
1 ("Venous thromboembolism" or ("venous thrombo-embolism" or VTE) or "deep vein thrombosis").ti,ab,kw. or exp Venous Thrombosis/ or DVT.ti,ab,kw. or ("thrombo-embolic" or thromboembolic).ti,ab,kw. or exp VENOUS THROMBOEMBOLISM/ or exp THROMBOEMBOLISM/ or (thromboembolism or thromboembolism*).ti,ab,kw. or "pulmonary embolism".ti,ab,kw. or exp Pulmonary Embolism/ or ("blood clot*" or "blood coagulation").ti,ab,kw. or exp Blood Coagulation/ or thrombus.ti,ab,kw. or exp THROMBUS/ or exp THROMBOSIS/ or thrombosis.ti,ab,kw. or "post-thrombotic".ti,ab,kw. or ("postthrombotic syndrome*" or "post-thrombotic syndrom*").ti,ab,kw. or Thrombophlebitis/ (331760) 2 exp Thrombolytic Therapy/ or (thrombolysis or "Thrombolytic Therap*").ti,ab. or exp Fibrinolytic Agents/ or Fibrinolysis/ or Fibrinol*.ti,ab. or Plasminogen Activators/ or (plasminogen adj2 activator*).ti,ab. or (rt-pa or tPA or urokinase or alteplase or reteplase or tenecteplase or saruplase or anistreplase or monteplase or streptokinase or staphylokinase or avelizin or awelysin or celiase or distreptase or Kabikinase or "kabivitrum 22" or Streptase or streptodecase or apsac or Abbokinase or renokinase orActilyse or Activase or Eminase or Retavase or Rapilysin or desmopletase or u-pa or alfimeprase or thromboly* or fibrinoly* or antithrombotic or antithrombic).ti,ab. (246726) 3 Acute Disease/ or acute*.ti,ab. (1122547) 4 1 and 2 and 3 (14130) 5 limit 4 to (english language and yr="2014 -Current") (2285) 6 (meta-analysis/ or meta-analysis as topic/ or (meta adj analy$).tw. or ((systematic* or literature) adj2 review$1).tw. or (systematic adj overview$1).tw. or exp "Review Literature as Topic"/ or cochrane.ab. or cochrane.jw. or embase.ab. or medline.ab. or (psychlit or psyclit).ab. or (cinahl or cinhal).ab. or cancerlit.ab. or ((selection criteria or data extraction).ab. and "review"/)) not (Comment/ or Editorial/ or Letter/ or (animals/ not humans/)) (358007) 7 (exp clinical trial/ or randomized controlled trial/ or exp clinical trials as topic/ or randomized controlled trials as topic/ or Random Allocation/ or Double-Blind Method/ or Single-Blind Method/ or (clinical trial, phase i or clinical trial, phase ii or clinical trial, phase iii or clinical trial, phase iv or controlled clinical trial or randomized controlled trial or multicenter study or clinical trial).pt. or random*.ti,ab. or (clinic* adj trial*).tw. or ((singl* or doubl* or treb* or tripl*) adj (blind$3 or mask$3)).tw. or Placebos/ or placebo*.tw.) not (animals/ not humans/) (1764590) 8 5 and 6 (186) = 186 SR’s 9 5 and 7 (581) 10 8 or 9 (643) 11 9 not 8 (457) = 457 RCT’s
= 643 |
789 |
|
Embase (Elsevier) |
((('venous thromboembolism':ab,ti OR ((venous NEAR/1 'thrombo embolism'):ab,ti) OR vte:ab,ti OR 'deep vein thrombosis':ab,ti OR dvt:ab,ti OR 'thrombo-embolic':ab,ti OR thromboembolic:ab,ti OR thromboembolism:ab,ti OR thromboembolism*:ab,ti OR 'pulmonary embolism':ab,ti OR 'blood clot':ab,ti OR 'blood coagulation':ab,ti OR thrombus:ab,ti OR thrombosis:ab,ti OR 'post-thrombotic':ab,ti OR postthrombotic:ab,ti OR 'post thrombotic':ab,ti OR 'thromboembolism'/exp/mj) AND ('fibrinolytic therapy'/exp/mj OR 'fibrinolytic agent'/exp/mj OR 'plasminogen activator'/exp/mj OR thrombolysis:ab,ti OR 'thrombolytic therapy':ab,ti OR (('rt pa':ab,ti OR tpa:ab,ti OR urokinase:ab,ti OR alteplase:ab,ti OR reteplase:ab,ti OR tenecteplase:ab,ti OR saruplase:ab,ti OR anistreplase:ab,ti OR monteplase:ab,ti OR streptokinase:ab,ti OR staphylokinase:ab,ti OR avelizin:ab,ti OR awelysin:ab,ti OR celiase:ab,ti OR distreptase:ab,ti OR kabikinase:ab,ti OR 'kabivitrum 22':ab,ti OR streptase:ab,ti OR streptodecase:ab,ti OR apsac:ab,ti OR abbokinase:ab,ti OR renokinase:ab,ti) AND oractilyse:ab,ti) OR activase:ab,ti OR eminase:ab,ti OR retavase:ab,ti OR rapilysin:ab,ti OR desmopletase:ab,ti OR 'u pa':ab,ti OR alfimeprase:ab,ti OR thromboly*:ab,ti OR fibrinoly*:ab,ti OR antithrombotic:ab,ti OR antithrombic:ab,ti) AND ('acute disease'/exp OR acute*:ab,ti) AND (2014-2018)/py AND (english)/lim NOT 'conference abstract':it) = 1493
Gebruikte filters: Systematic Reviews (('meta analysis'/de OR cochrane:ab OR embase:ab OR psycinfo:ab OR cinahl:ab OR medline:ab OR ((systematic NEAR/1 (review OR overview)):ab,ti) OR ((meta NEAR/1 analy*):ab,ti) OR metaanalys*:ab,ti OR 'data extraction':ab OR cochrane:jt OR 'systematic review'/de) NOT (('animal experiment'/exp OR 'animal model'/exp OR 'nonhuman'/exp) NOT 'human'/exp))) = 98
Randomized Controlled Trials (('clinical trial'/exp OR 'randomization'/exp OR 'single blind procedure'/exp OR 'double blind procedure'/exp OR 'crossover procedure'/exp OR 'placebo'/exp OR 'prospective study'/exp OR rct:ab,ti OR random*:ab,ti OR 'single blind':ab,ti OR 'randomised controlled trial':ab,ti OR 'randomized controlled trial'/exp OR placebo*:ab,ti) NOT 'conference abstract':it)) = 302
= 400 |

